Buspar 5mg, 10mg Buspirone Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Buspar i jak jest używany?
Buspar 5mg to lek na receptę stosowany w leczeniu objawów zaburzeń lękowych. Buspar 5 mg może być stosowany samodzielnie lub z innymi lekami.
Buspar należy do klasy leków zwanych środkami przeciwlękowymi, anksjolitycznymi, niebenzodiazepinami.
Jakie są możliwe skutki uboczne Buspar?
Jakie są możliwe skutki uboczne Buspar 5mg?
Buspar może powodować poważne skutki uboczne, w tym:
- ból w klatce piersiowej,
- duszność i
- zawroty
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Buspar to:
- ból głowy,
- zawroty głowy,
- senność,
- problem ze snem (bezsenność),
- mdłości,
- rozstrój żołądka i
- uczucie zdenerwowania lub podekscytowania
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Buspar. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
Tabletki chlorowodorku buspironu, USP są środkiem przeciwlękowym, który nie jest chemicznie ani farmakologicznie związany z benzodiazepinami, barbituranami lub innymi lekami uspokajającymi/lękowymi.
Chlorowodorek buspironu, USP to biały krystaliczny proszek. Jest bardzo dobrze rozpuszczalny w wodzie; dobrze rozpuszczalny w metanolu i chlorku metylenu; słabo rozpuszczalny w etanolu i acetonitrylu; bardzo słabo rozpuszczalny w octanie etylu i praktycznie nierozpuszczalny w heksanach. Jego masa cząsteczkowa wynosi 422. Chemicznie chlorowodorek buspironu jest monochlorowodorkiem 8-[4-[4-(2-pirymidynylo)-1-piperazynylo]butylo]-8-azaspiro[4.5]dekano-7,9-dionu. Wzór cząsteczkowy C21H31N5O2•HCl jest reprezentowany przez następujący wzór strukturalny:
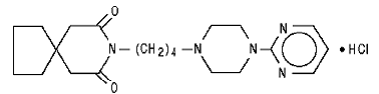
Każda tabletka buspironu chlorowodorku przeznaczona do podawania doustnego zawiera 5 mg lub 10 mg lub 15 mg lub 30 mg buspironu chlorowodorku (co odpowiada odpowiednio 4,6 mg, 9,1 mg, 13,7 mg i 27,4 mg buspironu w postaci wolnej zasady). Ponadto każda tabletka zawiera następujące składniki nieaktywne: koloidalny dwutlenek krzemu, monohydrat laktozy, stearynian magnezu, celulozę mikrokrystaliczną oraz glikolan sodowy skrobi. Tabletki 5 mg i 10 mg są podzielone na dwie części. Tak więc tabletka 5 mg może również zapewnić dawkę 2,5 mg, a tabletka 10 mg może zapewnić dawkę 5 mg. Tabletki 15 mg i 30 mg są podzielone tak, aby można je było podzielić na dwie części lub na trzy części. Tak więc pojedyncza tabletka 15 mg może zapewnić następujące dawki: 15 mg (cała tabletka), 10 mg (dwie trzecie tabletki), 7,5 mg (pół tabletki) lub 5 mg (jedna trzecia tabletki) . Jedna tabletka 30 mg może zapewnić następujące dawki: 30 mg (cała tabletka), 20 mg (dwie trzecie tabletki), 15 mg (pół tabletki) lub 10 mg (jedna trzecia tabletki).
WSKAZANIA
Tabletki chlorowodorku buspironu są wskazane do leczenia zaburzeń lękowych lub krótkotrwałego łagodzenia objawów lęku. Lęk lub napięcie związane ze stresem dnia codziennego zwykle nie wymaga leczenia lekiem przeciwlękowym.
Skuteczność tabletek chlorowodorku buspironu została wykazana w kontrolowanych badaniach klinicznych u pacjentów ambulatoryjnych, u których rozpoznanie w przybliżeniu odpowiada uogólnionemu zaburzeniu lękowemu (GAD). Wielu pacjentów włączonych do tych badań miało również współistniejące objawy depresyjne, a tabletki chlorowodorku buspironu łagodziły stany lękowe w obecności tych współistniejących objawów depresyjnych. Pacjenci oceniani w tych badaniach doświadczali objawów przez okres od 1 miesiąca do ponad 1 roku przed badaniem, ze średnim czasem trwania objawów wynoszącym 6 miesięcy. Uogólnione zaburzenie lękowe (300.02) opisano w Podręczniku diagnostycznym i statystycznym Amerykańskiego Towarzystwa Psychiatrycznego, III1 w następujący sposób:
Uogólniony, uporczywy lęk (trwający co najmniej 1 miesiąc ciągłego trwania), objawiający się objawami z trzech z czterech następujących kategorii:
Napięcie silnika
Drżenie, drżenie, nerwowość, drżenie, napięcie, bóle mięśni, męczliwość, niemożność odprężenia się, drganie powiek, zmarszczone brwi, napięta twarz, wiercenie się, niepokój, lekkie przerażenie.
Nadpobudliwość autonomiczna
Pocenie się, kołatanie lub przyspieszone bicie serca, zimne, wilgotne dłonie, suchość w ustach, zawroty głowy, zawroty głowy, parestezje (mrowienie w dłoniach lub stopach), rozstrój żołądka, okresy gorąca lub zimna, częste oddawanie moczu, biegunka, dyskomfort w jamie brzusznej, guzek w gardle, uderzenia gorąca, bladość, wysokie tętno spoczynkowe i częstość oddechów.
Pełne Oczekiwania
Niepokój, zmartwienie, strach, przeżuwanie i oczekiwanie nieszczęścia dla siebie lub innych.
Czujność i skanowanie
Nadmierna uwaga skutkująca rozpraszaniem uwagi, trudnościami w koncentracji, bezsennością, uczuciem "podenerwowania", drażliwością, zniecierpliwieniem.
Powyższe objawy nie byłyby spowodowane innym zaburzeniem psychicznym, takim jak zaburzenie depresyjne czy schizofrenia. Jednak w GAD często występują łagodne objawy depresyjne.
Skuteczność tabletek chlorowodorku buspironu przy długotrwałym stosowaniu, to jest przez ponad 3 do 4 tygodni, nie została wykazana w kontrolowanych badaniach. Nie ma dostępnego materiału dowodowego, który systematycznie odnosiłby się do odpowiedniego czasu trwania leczenia GAD. Jednak w badaniu dotyczącym długotrwałego stosowania 264 pacjentów leczono tabletkami chlorowodorku buspironu przez 1 rok bez złego wpływu. Dlatego lekarz, który zdecyduje się na stosowanie tabletek chlorowodorku buspironu przez dłuższy czas, powinien okresowo dokonywać ponownej oceny przydatności leku dla indywidualnego pacjenta.
DAWKOWANIE I SPOSÓB PODAWANIA
Zalecana dawka początkowa to 15 mg na dobę (7,5 mg dwa razy na dobę). Aby uzyskać optymalną odpowiedź terapeutyczną, w odstępach 2 do 3 dni, dawkę można zwiększać o 5 mg na dobę, w razie potrzeby. Maksymalna dzienna dawka nie powinna przekraczać 60 mg na dobę. W badaniach klinicznych umożliwiających dostosowanie dawki, powszechnie stosowano dawki podzielone od 20 mg do 30 mg na dobę.
Biodostępność buspironu jest zwiększona po podaniu z pokarmem w porównaniu ze stanem na czczo (patrz FARMAKOLOGIA KLINICZNA ). W związku z tym pacjenci powinni przyjmować buspiron w spójny sposób, uwzględniając czas dawkowania; zawsze z jedzeniem lub zawsze bez jedzenia.
Gdy buspiron ma być podawany z silnym inhibitorem CYP3A4, zalecenia dotyczące dawkowania opisane w INTERAKCJE Z LEKAMI należy postępować zgodnie z sekcją.
JAK DOSTARCZONE
Tabletki Buspiron Hydrochloride USP, 5 mg, są białe lub prawie białe, w kształcie kapsułki, płaskie, ze ściętymi krawędziami, z wytłoczonym na jednej stronie przecięciem; jedna strona bisect jest wytłoczona 'ZE' a druga '36', a druga strona jest gładka
Dane producenta: nie dotyczy. Poprawiono: maj 2016
SKUTKI UBOCZNE
Brak informacji.
INTERAKCJE Z LEKAMI
Środki psychotropowe
Inhibitory MAO
Zaleca się, aby tabletki chlorowodorku buspironu nie były stosowane jednocześnie z inhibitorami MAO (patrz OSTRZEŻENIA ).
Amitryptylina
Po dodaniu buspironu do schematu dawkowania amitryptyliny nie zaobserwowano statystycznie istotnych różnic parametrów farmakokinetycznych w stanie stacjonarnym (Cmax, AUC i Cmin) amitryptyliny lub jej metabolitu nortryptyliny.
Diazepam
Po dodaniu buspironu do schematu dawkowania diazepamu nie zaobserwowano statystycznie istotnych różnic parametrów farmakokinetycznych w stanie stacjonarnym (Cmax, AUC i Cmin) dla diazepamu, ale zaobserwowano wzrost o około 15% dla nordiazepamu i niewielkie działania niepożądane kliniczne (zawroty głowy, ból głowy i nudności).
Haloperidol
W badaniu z udziałem zdrowych ochotników jednoczesne podawanie buspironu i haloperydolu powodowało zwiększenie stężenia haloperydolu w surowicy. Kliniczne znaczenie tego odkrycia nie jest jasne.
Nefazodon
[Widzieć Inhibitory i induktory cytochromu P450 3A4 (CYP3A4) ].
Trazodon
Istnieje jeden raport sugerujący, że jednoczesne stosowanie Desyrel®# (chlorowodorek trazodonu) i buspironu mogło spowodować 3-6-krotne podwyższenie SGPT (ALT) u kilku pacjentów. W podobnym badaniu, w którym próbowano powtórzyć to odkrycie, nie zidentyfikowano żadnego interaktywnego wpływu na transaminazy wątrobowe.
Triazolam/Flurazepam
Jednoczesne podawanie buspironu z triazolamem lub flurazepamem nie wydawało się przedłużać ani nasilać uspokajającego działania benzodiazepiny.
Inne psychotropy
Ponieważ nie badano skutków jednoczesnego podawania buspironu z większością innych leków psychotropowych, należy zachować ostrożność podczas jednoczesnego stosowania buspironu z innymi lekami działającymi na OUN.
Inhibitory i induktory cytochromu P450 3A4 (CYP3A4)
Wykazano in vitro, że buspiron jest metabolizowany przez CYP3A4. To odkrycie jest zgodne z interakcjami in vivo obserwowanymi między buspironem a następującymi:
diltiazem i werapamil
badaniu z udziałem dziewięciu zdrowych ochotników, jednoczesne podawanie buspironu (10 mg w dawce pojedynczej) z werapamilem (80 mg trzy razy na dobę) lub diltiazemem (60 mg trzy razy na dobę) zwiększało stężenie buspironu w osoczu (werapamil zwiększał AUC i Cmax buspironu 3,4-krotnie, podczas gdy diltiazem zwiększenie AUC i Cmax odpowiednio 5,5-krotne i 4-krotne). Konieczna może być późniejsza modyfikacja dawki, która powinna opierać się na ocenie klinicznej.
Erytromycyna
badaniu z udziałem zdrowych ochotników jednoczesne podawanie buspironu (10 mg w pojedynczej dawce) z erytromycyną (1,5 g/dobę przez 4 dni) zwiększyło stężenie buspironu w osoczu (5-krotny wzrost Cmax i 6-krotny wzrost AUC). Tym interakcjom farmakokinetycznym towarzyszyła zwiększona częstość występowania działań niepożądanych przypisywanych buspironowi. Jeśli oba leki mają być stosowane w skojarzeniu, zaleca się małą dawkę buspironu (np. 2,5 mg dwa razy na dobę). Późniejsza modyfikacja dawki każdego leku powinna opierać się na ocenie klinicznej.
Sok grejpfrutowy
W badaniu z udziałem zdrowych ochotników, jednoczesne podawanie buspironu (10 mg w pojedynczej dawce) z sokiem grejpfrutowym (200 ml podwójnej mocy tid przez 2 dni) zwiększyło stężenie buspironu w osoczu (4,3-krotny wzrost Cmax; 9,2-krotny wzrost AUC ). Pacjentom otrzymującym buspiron należy zalecić unikanie picia tak dużych ilości soku grejpfrutowego.
Itrakonazol
badaniu z udziałem zdrowych ochotników jednoczesne podawanie buspironu (10 mg w pojedynczej dawce) z itrakonazolem (200 mg/dobę przez 4 dni) zwiększyło stężenie buspironu w osoczu (13-krotny wzrost Cmax i 19-krotny wzrost AUC). Tym interakcjom farmakokinetycznym towarzyszyła zwiększona częstość występowania działań niepożądanych przypisywanych buspironowi. Jeśli oba leki mają być stosowane w skojarzeniu, zaleca się małą dawkę buspironu (np. 2,5 mg raz na dobę). Późniejsza modyfikacja dawki każdego leku powinna opierać się na ocenie klinicznej.
Nefazodon
badaniu farmakokinetyki w stanie stacjonarnym u zdrowych ochotników jednoczesne podawanie buspironu (2,5 lub 5 mg dwa razy na dobę) z nefazodonem (250 mg dwa razy na dobę) powodowało znaczne zwiększenie stężenia buspironu w osoczu (do 20-krotne zwiększenie Cmax i do 50 -krotność AUC) i statystycznie istotne zmniejszenie (około 50%) stężeń metabolitu buspironu 1-PP w osoczu. Po podaniu buspironu w dawce 5 mg dwa razy na dobę zaobserwowano nieznaczny wzrost AUC dla nefazodonu (23%) i jego metabolitów hydroksynefazodonu (HO-NEF) (17%) i meta-chlorofenylopiperazyny (9%). Nieznaczny wzrost Cmax zaobserwowano dla nefazodonu (8%) i jego metabolitu HO-NEF (11%).
Osoby otrzymujące buspiron 5 mg dwa razy na dobę i nefazodon 250 mg dwa razy na dobę doświadczyły zawrotów głowy, osłabienia, zawrotów głowy i senności, zdarzenia niepożądane obserwowane również w przypadku każdego leku osobno. Jeśli oba leki mają być stosowane w skojarzeniu, zaleca się małą dawkę buspironu (np. 2,5 mg raz na dobę). Późniejsza modyfikacja dawki każdego leku powinna opierać się na ocenie klinicznej.
ryfampicyna
W badaniu z udziałem zdrowych ochotników jednoczesne podawanie buspironu (30 mg w pojedynczej dawce) z ryfampicyną (600 mg/dobę przez 5 dni) zmniejszyło stężenia w osoczu (83,7% zmniejszenie Cmax; 89,6% zmniejszenie AUC) i działanie farmakodynamiczne buspiron. Jeśli oba leki mają być stosowane w połączeniu, dawka buspironu może wymagać dostosowania, aby utrzymać działanie przeciwlękowe.
Inne inhibitory i induktory CYP3A4
Substancje hamujące CYP3A4, takie jak ketokonazol lub rytonawir, mogą hamować metabolizm buspironu i zwiększać stężenie buspironu w osoczu, natomiast substancje indukujące CYP3A4, takie jak deksametazon, lub niektóre leki przeciwdrgawkowe (fenytoina, fenobarbital, karbamazepina) mogą zwiększać tempo metabolizmu buspironu. Jeśli pacjentowi ustalono stałą dawkę buspironu, może być konieczne dostosowanie dawki buspironu, aby uniknąć działań niepożądanych, które można przypisać buspironowi lub zmniejszonej aktywności przeciwlękowej. W związku z tym, przy podawaniu z silnym inhibitorem CYP3A4, zaleca się ostrożne stosowanie małej dawki buspironu. W przypadku stosowania w połączeniu z silnym induktorem CYP3A4 może być konieczne dostosowanie dawki buspironu w celu utrzymania działania przeciwlękowego.
Inne leki
Cymetydyna
Stwierdzono, że równoczesne podawanie buspironu z cymetydyną zwiększało Cmax (40%) i Tmax (2-krotnie), ale miało minimalny wpływ na AUC buspironu.
Wiązanie białek
In vitro buspiron nie wypiera ściśle związanych leków, takich jak fenytoina, propranolol i warfaryna, z białek surowicy. Jednak odnotowano jeden przypadek wydłużenia czasu protrombinowego, gdy buspiron został dodany do schematu leczenia pacjenta leczonego warfaryną. Pacjent otrzymywał również przewlekle fenytoinę, fenobarbital, digoksynę i Synthroid®*. In vitro buspiron może wypierać mniej silnie związane leki, takie jak digoksyna. Kliniczne znaczenie tej właściwości nie jest znane.
Terapeutyczne stężenia aspiryny, dezypraminy, diazepamu, flurazepamu, ibuprofenu, propranololu, tiorydazyny i tolbutamidu miały jedynie ograniczony wpływ na stopień wiązania buspironu z białkami osocza (patrz FARMAKOLOGIA KLINICZNA ).
Interakcje leków/testów laboratoryjnych
Chlorowodorek buspironu może zaburzać wyniki testu metanefryny/katecholamin w moczu. Został on błędnie odczytany jako metanefryna podczas rutynowych testów w kierunku guza chromochłonnego, co skutkowało fałszywie dodatnim wynikiem laboratoryjnym. W związku z tym należy odstawić buspiron chlorowodorek na co najmniej 48 godzin przed oddaniem moczu do katecholamin.
Nadużywanie i uzależnienie od narkotyków
Klasa substancji kontrolowanych
Chlorowodorek buspironu nie jest substancją kontrolowaną.
Uzależnienie fizyczne i psychologiczne
badaniach na ludziach i zwierzętach buspiron nie wykazał możliwości nadużywania lub przekierowania i nie ma dowodów na to, że powoduje tolerancję lub uzależnienie fizyczne lub psychiczne. Ludzi ochotników z historią używania narkotyków rekreacyjnych lub alkoholu przebadano w dwóch badaniach klinicznych z podwójnie ślepą próbą. Żaden z badanych nie był w stanie odróżnić tabletek chlorowodorku buspironu od placebo. Natomiast badani wykazywali statystycznie istotną preferencję dla metakwalonu i diazepamu. Badania na małpach, myszach i szczurach wykazały, że buspiron nie ma możliwości nadużywania. Po długotrwałym podawaniu szczurom nagłe odstawienie buspironu nie powodowało utraty masy ciała często obserwowanej w przypadku substancji powodujących uzależnienie fizyczne.
Chociaż nie ma bezpośrednich dowodów na to, że tabletki chlorowodorku buspironu powodują uzależnienie fizyczne lub zachowania związane z poszukiwaniem leku, trudno jest przewidzieć na podstawie eksperymentów stopień, w jakim lek działający na OUN będzie niewłaściwie używany, przekierowywany i/lub nadużywany po wprowadzeniu do obrotu. W związku z tym lekarze powinni uważnie oceniać pacjentów pod kątem historii nadużywania leków i uważnie obserwować takich pacjentów, obserwując ich pod kątem oznak niewłaściwego stosowania lub nadużywania tabletek chlorowodorku buspironu (np. rozwój tolerancji, zwiększanie dawki, poszukiwanie leku).
Klasa substancji kontrolowanych
Chlorowodorek buspironu nie jest substancją kontrolowaną.
Uzależnienie fizyczne i psychologiczne
badaniach na ludziach i zwierzętach buspiron nie wykazał możliwości nadużywania lub przekierowania i nie ma dowodów na to, że powoduje tolerancję lub uzależnienie fizyczne lub psychiczne. Ludzi ochotników z historią używania narkotyków rekreacyjnych lub alkoholu przebadano w dwóch badaniach klinicznych z podwójnie ślepą próbą. Żaden z badanych nie był w stanie odróżnić tabletek chlorowodorku buspironu od placebo. Natomiast badani wykazywali statystycznie istotną preferencję dla metakwalonu i diazepamu. Badania na małpach, myszach i szczurach wykazały, że buspiron nie ma możliwości nadużywania. Po długotrwałym podawaniu szczurom nagłe odstawienie buspironu nie powodowało utraty masy ciała często obserwowanej w przypadku substancji powodujących uzależnienie fizyczne.
Chociaż nie ma bezpośrednich dowodów na to, że tabletki chlorowodorku buspironu powodują uzależnienie fizyczne lub zachowania związane z poszukiwaniem leku, trudno jest przewidzieć na podstawie eksperymentów stopień, w jakim lek działający na OUN będzie niewłaściwie używany, przekierowywany i/lub nadużywany po wprowadzeniu do obrotu. W związku z tym lekarze powinni uważnie oceniać pacjentów pod kątem historii nadużywania leków i uważnie obserwować takich pacjentów, obserwując ich pod kątem oznak niewłaściwego stosowania lub nadużywania tabletek chlorowodorku buspironu (np. rozwój tolerancji, zwiększanie dawki, poszukiwanie leku).
OSTRZEŻENIA
Podawanie tabletek buspironu chlorowodorku pacjentowi przyjmującemu inhibitor monoaminooksydazy (IMAO) może stanowić zagrożenie. Istnieją doniesienia o występowaniu podwyższonego ciśnienia krwi po dodaniu tabletek chlorowodorku buspironu do schematu leczenia zawierającego MAOI. Dlatego nie zaleca się stosowania tabletek chlorowodorku buspironu jednocześnie z IMAO.
Ponieważ tabletki chlorowodorku buspironu nie mają ustalonego działania przeciwpsychotycznego, nie należy ich stosować zamiast odpowiedniego leczenia przeciwpsychotycznego.
ŚRODKI OSTROŻNOŚCI
Ogólny
Zakłócenia sprawności poznawczej i motorycznej
Badania wskazują, że tabletki chlorowodorku buspironu działają mniej uspokajająco niż inne leki przeciwlękowe i nie powodują znaczącego upośledzenia funkcji. Jednak jego wpływ na OUN u każdego indywidualnego pacjenta może nie być przewidywalny. Dlatego pacjentów należy ostrzec przed prowadzeniem samochodu lub obsługą skomplikowanych maszyn, dopóki nie upewnią się, że leczenie buspironem nie wpływa na nich niekorzystnie.
Chociaż formalne badania interakcji buspironu chlorowodorku z alkoholem wskazują, że buspiron nie zwiększa wywołanych alkoholem zaburzeń sprawności motorycznej i umysłowej, rozsądnie jest unikać jednoczesnego stosowania alkoholu i buspironu.
Możliwość wystąpienia reakcji odstawiennych u pacjentów uzależnionych od leków uspokajających, nasennych lub przeciwlękowych
Ponieważ tabletki chlorowodorku buspironu nie wykazują tolerancji krzyżowej z benzodiazepinami i innymi powszechnie stosowanymi lekami uspokajającymi/nasennymi, nie zablokują zespołu odstawienia często obserwowanego po zaprzestaniu leczenia tymi lekami. Dlatego przed rozpoczęciem leczenia chlorowodorkiem buspironu w tabletkach zaleca się stopniowe wycofywanie pacjentów z wcześniejszego leczenia, zwłaszcza pacjentów, którzy przewlekle stosowali leki działające hamująco na ośrodkowy układ nerwowy. Objawy z odbicia lub odstawienia mogą pojawiać się w różnych okresach czasu, częściowo w zależności od rodzaju leku i jego efektywnego okresu półtrwania w fazie eliminacji.
Zespół odstawienia leków uspokajających/nasennych/lękowych może objawiać się dowolną kombinacją drażliwości, lęku, pobudzenia, bezsenności, drżenia, skurczów brzucha, skurczów mięśni, wymiotów, pocenia się, objawów grypopodobnych bez gorączki, a czasami nawet drgawek .
Możliwe obawy związane z wiązaniem buspironu z receptorami dopaminy
Ponieważ buspiron może wiązać się z centralnymi receptorami dopaminy, pojawiło się pytanie o jego potencjał powodowania ostrych i przewlekłych zmian funkcji neurologicznych, w których pośredniczy dopamina (np. dystonia, pseudoparkinsonizm, akatyzja i późna dyskineza). Doświadczenie kliniczne w kontrolowanych badaniach nie wykazało żadnej znaczącej aktywności podobnej do neuroleptyków; jednak u niewielkiej części pacjentów leczonych buspironem zgłoszono zespół niepokoju, pojawiający się wkrótce po rozpoczęciu leczenia. Zespół można wyjaśnić na kilka sposobów. Na przykład buspiron może zwiększać centralną aktywność noradrenergiczną; alternatywnie, efekt może być przypisany efektom dopaminergicznym (tj. reprezentuje akatyzję). Widzieć DZIAŁANIA NIEPOŻĄDANE : Doświadczenie postmarketingowe .
Informacje dla pacjentów
Aby zapewnić bezpieczne i skuteczne stosowanie tabletek chlorowodorku buspironu, pacjentom należy przekazać następujące informacje i instrukcje:
Poinformuj swojego lekarza o wszelkich lekach, lekach wydawanych na receptę lub bez recepty, alkoholu lub lekach, które obecnie przyjmujesz lub planujesz przyjmować podczas leczenia tabletkami chlorowodorku buspironu.
Należy poinformować lekarza, jeśli pacjentka jest w ciąży, planuje zajść w ciążę lub zajdzie w ciążę podczas przyjmowania tabletek buspironu chlorowodorku.
Poinformuj swojego lekarza, jeśli karmisz piersią niemowlę.
Dopóki nie doświadczysz, jak ten lek wpływa na ciebie, nie prowadź samochodu ani nie obsługuj potencjalnie niebezpiecznych maszyn.
Należy konsekwentnie przyjmować chlorowodorek buspironu, zawsze z jedzeniem lub zawsze bez jedzenia.
Podczas leczenia tabletkami chlorowodorku buspironu należy unikać picia dużych ilości soku grejpfrutowego.
Testy laboratoryjne
Nie są zalecane żadne specjalne testy laboratoryjne.
rakotwórczość, mutageneza, upośledzenie płodności
Nie zaobserwowano dowodów na potencjalne działanie rakotwórcze u szczurów podczas 24-miesięcznego badania przy około 133-krotności maksymalnej zalecanej dawki doustnej dla ludzi; lub u myszy, podczas 18-miesięcznego badania przy około 167-krotności maksymalnej zalecanej dawki doustnej dla ludzi.
Z aktywacją metaboliczną lub bez niej, buspiron nie indukował mutacji punktowych w pięciu szczepach Salmonella typhimurium (test Amesa) ani w hodowlach komórek mysiego chłoniaka L5178YTK+, nie zaobserwowano również uszkodzeń DNA w przypadku buspironu w ludzkich komórkach Wi-38. Aberracje chromosomowe lub nieprawidłowości nie występowały w komórkach szpiku kostnego myszy, którym podawano jedną lub pięć dziennych dawek buspironu.
Ciąża
Efekty teratogenne
Ciąża Kategoria B
badaniach rozrodczości przeprowadzonych na szczurach i królikach, którym podawano dawki buspironu około 30 razy większe od maksymalnej zalecanej dawki u ludzi, nie zaobserwowano zaburzeń płodności ani uszkodzenia płodu. Jednak u ludzi nie przeprowadzono odpowiednich i dobrze kontrolowanych badań w czasie ciąży. Ponieważ badania reprodukcji na zwierzętach nie zawsze pozwalają przewidzieć reakcję człowieka, lek ten powinien być stosowany w czasie ciąży tylko wtedy, gdy jest to bezwzględnie konieczne.
Praca i dostawa
Wpływ chlorowodorku buspironu na poród i poród u kobiet nie jest znany. W badaniach rozrodczości u szczurów nie odnotowano żadnych działań niepożądanych.
Matki karmiące
Stopień przenikania buspironu lub jego metabolitów do mleka ludzkiego nie jest znany. Jednak u szczurów buspiron i jego metabolity przenikają do mleka. Jeśli jest to klinicznie możliwe, należy unikać podawania tabletek chlorowodorku buspironu kobietom karmiącym.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność buspironu oceniano w dwóch 6-tygodniowych badaniach kontrolowanych placebo z udziałem łącznie 559 pacjentów pediatrycznych (w wieku od 6 do 17 lat) z GAD. Badane dawki wynosiły 7,5 mg do 30 mg dwa razy na dobę (15 do 60 mg/dobę). Nie było istotnych różnic między buspironem a placebo w odniesieniu do objawów GAD po dawkach zalecanych w leczeniu GAD u dorosłych. Badania farmakokinetyczne wykazały, że dla identycznych dawek, ekspozycja osocza na buspiron i jego aktywny metabolit 1-PP jest równa lub większa u pacjentów pediatrycznych niż u dorosłych. W badaniach tych nie powiązano żadnych nieoczekiwanych wyników dotyczących bezpieczeństwa z buspironem. Brak danych dotyczących długoterminowego bezpieczeństwa i skuteczności w tej populacji.
Zastosowanie geriatryczne
jednym badaniu obejmującym 6632 pacjentów, którzy otrzymywali buspiron w leczeniu lęku, 605 pacjentów miało ≥ 65 lat, a 41 ≥ 75 lat; profile bezpieczeństwa i skuteczności dla tych 605 pacjentów w podeszłym wieku (średnia wieku = 70,8 lat) były podobne do tych w młodszej populacji (średnia wieku = 43,3 lat). Przegląd spontanicznie zgłaszanych niepożądanych zdarzeń klinicznych nie wykazał różnic między pacjentami w podeszłym wieku i młodszymi, ale nie można wykluczyć większej wrażliwości niektórych starszych pacjentów.
Wiek nie miał wpływu na farmakokinetykę buspironu (patrz FARMAKOLOGIA KLINICZNA , Specjalne populacje ).
Stosowanie u pacjentów z zaburzeniami czynności wątroby lub nerek
Buspiron jest metabolizowany przez wątrobę i wydalany przez nerki. Badanie farmakokinetyczne u pacjentów z zaburzeniami czynności wątroby lub nerek wykazało zwiększone stężenie buspironu w osoczu i wydłużony okres półtrwania. Dlatego nie zaleca się podawania tabletek buspironu chlorowodorku pacjentom z ciężkimi zaburzeniami czynności wątroby lub nerek (patrz FARMAKOLOGIA KLINICZNA ).
PRZEDAWKOWAĆ
Brak informacji.
PRZECIWWSKAZANIA
Tabletki chlorowodorku buspironu są przeciwwskazane u pacjentów z nadwrażliwością na chlorowodorek buspironu.
FARMAKOLOGIA KLINICZNA
Mechanizm działania buspironu jest nieznany. Buspiron różni się od typowych benzodiazepinowych środków przeciwlękowych tym, że nie wykazuje działania przeciwdrgawkowego ani zwiotczającego mięśnie. Brakuje również wyraźnego działania uspokajającego, które jest związane z bardziej typowymi lekami przeciwlękowymi. Badania przedkliniczne in vitro wykazały, że buspiron ma wysokie powinowactwo do receptorów serotoninowych (5-HT1A). Buspiron nie wykazuje znaczącego powinowactwa do receptorów benzodiazepinowych i nie wpływa na wiązanie GABA in vitro lub in vivo w badaniach na modelach przedklinicznych.
Buspiron ma umiarkowane powinowactwo do mózgowych receptorów dopaminy D2. Niektóre badania sugerują, że buspiron może mieć pośredni wpływ na inne układy neuroprzekaźników.
Chlorowodorek buspironu jest szybko wchłaniany przez człowieka i podlega intensywnemu metabolizmowi pierwszego przejścia. W badaniu radioznakowanym niezmieniony buspiron w osoczu stanowił tylko około 1% radioaktywności w osoczu. Po podaniu doustnym stężenia niezmienionego buspironu w osoczu są bardzo małe i zmienne u poszczególnych pacjentów. Maksymalne stężenia w osoczu od 1 ng/ml do 6 ng/ml obserwowano po 40 do 90 minutach po podaniu pojedynczej dawki doustnej 20 mg. Biodostępność po podaniu pojedynczej dawki niezmienionego buspironu przyjmowanego w postaci tabletki wynosi średnio około 90% równoważnej dawki roztworu, ale istnieje duża zmienność.
Wpływ pokarmu na biodostępność tabletek chlorowodorku buspironu badano u ośmiu osób. Otrzymali dawkę 20 mg z jedzeniem i bez jedzenia; pole pod krzywą zależności stężenia od czasu (AUC) i szczytowego stężenia w osoczu (Cmax) niezmienionego buspironu zwiększyło się odpowiednio o 84% i 116%, ale całkowita ilość materiału immunoreaktywnego na buspiron nie uległa zmianie. Sugeruje to, że jedzenie może zmniejszać stopień przedukładowego klirensu buspironu (patrz DAWKOWANIE I SPOSÓB PODAWANIA ).
Badanie z wielokrotnymi dawkami przeprowadzone na 15 osobach sugeruje, że buspiron ma nieliniową farmakokinetykę. W związku z tym zwiększenie dawki i wielokrotne dawkowanie może prowadzić do nieco wyższych poziomów we krwi niezmienionego buspironu, niż można by oczekiwać na podstawie wyników badań z pojedynczą dawką.
Badanie wiązania z białkami in vitro wykazało, że około 86% buspironu wiąże się z białkami osocza. Zaobserwowano również, że aspiryna zwiększała stężenie wolnego buspironu w osoczu o 23%, podczas gdy flurazepam obniżał stężenie wolnego buspironu w osoczu o 20%. Nie wiadomo jednak, czy leki te wywierają podobny wpływ na stężenie wolnego buspironu w osoczu in vivo, ani czy takie zmiany, jeśli wystąpią, powodują klinicznie istotne różnice w wynikach leczenia. Badanie in vitro wykazało, że buspiron nie wypiera z białek osocza leków silnie wiążących się z białkami, takich jak fenytoina, warfaryna i propranolol, oraz że buspiron może wypierać digoksynę.
Buspiron jest metabolizowany głównie przez utlenianie, w którym in vitro, jak wykazano, pośredniczy cytochrom P450 3A4 (CYP3A4) (patrz INTERAKCJE Z LEKAMI ). Powstaje kilka hydroksylowanych pochodnych i farmakologicznie czynny metabolit 1-pirymidynylopiperazyna (1-PP). W modelach zwierzęcych przewidujących potencjał przeciwlękowy, 1-PP ma około jedną czwartą aktywności buspironu, ale jest obecny w 20-krotnie większych ilościach. Jednak prawdopodobnie nie ma to znaczenia u ludzi: próbki krwi od ludzi przewlekle narażonych na działanie chlorowodorku buspironu nie wykazują wysokiego poziomu 1-PP; średnie wartości wynoszą około 3 ng/ml, a najwyższy poziom we krwi ludzkiej odnotowany wśród 108 przewlekle leczonych pacjentów wynosił 17 ng/ml, mniej niż 1/200 poziomu 1-PP stwierdzonego u zwierząt otrzymujących duże dawki buspironu bez oznak toksyczności.
W badaniu pojedynczej dawki buspironu znakowanego węglem 14C, 29% do 63% dawki było wydalane z moczem w ciągu 24 godzin, głównie w postaci metabolitów; wydalanie z kałem stanowiło 18% do 38% dawki. Średni okres półtrwania w fazie eliminacji niezmienionego buspironu po podaniu pojedynczych dawek od 10 mg do 40 mg wynosi około 2 do 3 godzin.
Specjalne populacje
Wpływ wieku i płci
Po podaniu pojedynczej lub wielokrotnej dawki u dorosłych nie zaobserwowano istotnych różnic w farmakokinetyce buspironu (AUC i Cmax) między osobami w podeszłym wieku i młodszymi oraz między mężczyznami i kobietami.
Niewydolność wątroby
Po wielokrotnym podaniu buspironu pacjentom z zaburzeniami czynności wątroby, AUC buspironu w stanie stacjonarnym zwiększyło się 13-krotnie w porównaniu z osobami zdrowymi (patrz ŚRODKI OSTROŻNOŚCI ).
Zaburzenia czynności nerek
Po wielokrotnym podaniu buspironu pacjentom z zaburzeniami czynności nerek (Clcr = 10 do 70 ml/min/1,73 m2) AUC buspironu w stanie stacjonarnym zwiększyło się 4-krotnie w porównaniu ze zdrowymi (Clcr ≥ 80 ml/min/1,73 m2) (Widzieć ŚRODKI OSTROŻNOŚCI ).
Efekty wyścigu
Nie badano wpływu rasy na farmakokinetykę buspironu.
INFORMACJA O PACJENCIE
chlorowodorek buspironu Tabletki, USP Dla tabletek 15 mg i 30 mg
JAK UŻYWAĆ
Reakcja na buspiron jest różna u poszczególnych osób. Lekarz może uznać za konieczne dostosowanie dawki w celu uzyskania właściwej odpowiedzi.
Każda tabletka jest podzielona i można ją dokładnie przełamać.
Aby dokładnie i łatwo przełamać tabletkę, należy ją trzymać kciukami i palcami wskazującymi, blisko odpowiedniego nacięcia (rowka). Następnie, z nacięciem tabletki skierowanym do siebie, naciśnij i oddziel segmenty tabletki (nie należy używać segmentów uszkodzonych nieprawidłowo).
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
