Catapres 100mcg Clonidine Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Catapres i jak się go stosuje?
Catapres to lek na receptę stosowany w leczeniu objawów nadciśnienia tętniczego, zespołu nadpobudliwości psychoruchowej z deficytem uwagi (ADHD) i bólu nowotworowego. Catapres 100mcg może być stosowany samodzielnie lub z innymi lekami.
Catapres 100mcg należy do klasy leków zwanych agonistami alfa2, działającymi centralnie, środkami ADHD.
Nie wiadomo, czy Catapres 100mcg jest bezpieczny i skuteczny u dzieci w wieku poniżej 12 lat.
Jakie są możliwe skutki uboczne Catapres?
Catapres może powodować poważne skutki uboczne, w tym:
- objawy odstawienia,
- nerwowość,
- podniecenie,
- ból głowy,
- drżenie i
- szybki wzrost ciśnienia krwi
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Catapres 100mcg to:
- suchość w ustach,
- zawroty głowy,
- senność,
- zmęczenie,
- zaparcie,
- ból głowy,
- nudności i
- kłopoty ze snem (bezsenność)
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne stosowania leku Catapres. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
Catapres® (chlorowodorek klonidyny, USP) to działający ośrodkowo alfa-agonista hipotensyjny, dostępny w postaci tabletek do podawania doustnego w trzech mocach dawkowania: 0,1 mg, 0,2 mg i 0,3 mg. Tabletka 0,1 mg odpowiada 0,087 mg wolnej zasady.
Nieaktywnymi składnikami są koloidalny dwutlenek krzemu, skrobia kukurydziana, dwuzasadowy fosforan wapnia, FD&C Yellow No. 6, żelatyna, gliceryna, laktoza i stearynian magnezu. Tabletka Catapres 0,1 mg zawiera również FD&C Blue No.1 i FD&C Red No.3.
Chlorowodorek klonidyny jest pochodną imidazoliny i występuje jako związek mezomeryczny. Nazwa chemiczna to chlorowodorek 2-(2,6-dichlorofenyloamino)-2-imidazoliny. Poniżej znajduje się wzór strukturalny:
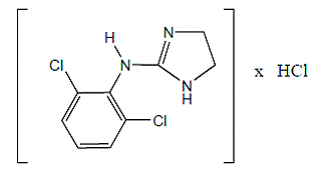 C9H9Cl2N3 · HCl Mol. wag. 266,56
C9H9Cl2N3 · HCl Mol. wag. 266,56 Chlorowodorek klonidyny to bezwonna, gorzka, biała, krystaliczna substancja rozpuszczalna w wodzie i alkoholu.
WSKAZANIA
Tabletki Catapres są wskazane w leczeniu nadciśnienia tętniczego. Tabletki CATAPRES można stosować samodzielnie lub jednocześnie z innymi środkami przeciwnadciśnieniowymi.
DAWKOWANIE I SPOSÓB PODAWANIA
Dorośli ludzie
Dawka tabletek Catapres® (chlorowodorek klonidyny, USP) musi być dostosowana do indywidualnej odpowiedzi ciśnienia krwi pacjenta. Poniżej znajduje się ogólny przewodnik po jego administracji.
Dawka początkowa
Tabletka 0,1 mg dwa razy na dobę (rano i przed snem). Pacjenci w podeszłym wieku mogą odnieść korzyść z mniejszej dawki początkowej.
Dawka podtrzymująca
Dalsze zwiększanie dawki o 0,1 mg na dobę można w razie potrzeby wykonywać w odstępach tygodniowych, aż do uzyskania pożądanej odpowiedzi. Przyjmowanie większej porcji doustnej dawki dobowej przed snem może zminimalizować przemijające skutki dostosowania w postaci suchości w jamie ustnej i senności. Najczęściej stosowane dawki terapeutyczne mieszczą się w zakresie od 0,2 mg do 0,6 mg dziennie, podawane w dawkach podzielonych. Badania wykazały, że 2,4 mg to maksymalna skuteczna dawka dzienna, ale dawki tak wysokie jak ta są rzadko stosowane.
Zaburzenia czynności nerek
Pacjenci z zaburzeniami czynności nerek mogą odnieść korzyść z mniejszej dawki początkowej. Pacjenci powinni być uważnie monitorowani. Ponieważ tylko minimalna ilość klonidyny jest usuwana podczas rutynowej hemodializy, nie ma potrzeby dodatkowego podawania klonidyny po dializie.
JAK DOSTARCZONE
Tabletki Catapres® (chlorowodorek klonidyny, USP) są dostarczane w następujący sposób:
Przechowywać w 25°C (77°F); dozwolone wycieczki do 15°-30°C (59°-86°F) [Widzieć Temperatura pokojowa kontrolowana przez USP ].
Dozować w szczelnym, odpornym na światło pojemniku.
Dystrybutor: Boehringer Ingelheim Pharmaceuticals, Inc., Ridgefield, CT 06877 USA. Producent: Boehringer Ingelheim Promeco SA de CV, Mexico City, Meksyk. Licencjonowany od: Boehringer Ingelheim, International GmbH, z zapytaniami medycznymi należy kierować na adres: (800) 542-6257 lub (800) 459-9906. Poprawiono: maj 2012
SKUTKI UBOCZNE
Większość działań niepożądanych jest łagodna i ma tendencję do zmniejszania się wraz z kontynuacją leczenia. Najczęstsze (które wydają się być zależne od dawki) to suchość w ustach, występująca u około 40 na 100 pacjentów; senność, około 33 na 100; zawroty głowy, około 16 na 100; zaparcia i uspokojenie, każde około 10 na 100.
pacjentów otrzymujących tabletki CATAPRES 100mcg tabletki zgłaszano również następujące rzadsze działania niepożądane, ale w wielu przypadkach pacjenci otrzymywali jednocześnie leki i związek przyczynowy nie został ustalony.
Ciało jako całość: Zmęczenie, gorączka, ból głowy, bladość, osłabienie i zespół odstawienia. Odnotowano również słabo dodatni test Coombsa i zwiększoną wrażliwość na alkohol.
Układ sercowo-naczyniowy: Bradykardia, zastoinowa niewydolność serca, nieprawidłowości elektrokardiograficzne (tj. zatrzymanie węzła zatokowego, bradykardia złączowa, blok przedsionkowo-komorowy wysokiego stopnia i arytmie), objawy ortostatyczne, kołatanie serca, objaw Raynauda, omdlenie i tachykardia. Zgłaszano przypadki bradykardii zatokowej i bloku przedsionkowo-komorowego, zarówno przy jednoczesnym zastosowaniu naparstnicy, jak i bez niej.
Ośrodkowy układ nerwowy: Pobudzenie, lęk, majaczenie, urojenia, omamy (w tym wzrokowe i słuchowe), bezsenność, depresja psychiczna, nerwowość, inne zmiany behawioralne, parestezje, niepokój, zaburzenia snu i żywe sny lub koszmary.
Dermatologiczny: Łysienie, obrzęk naczynioruchowy, pokrzywka, świąd, wysypka i pokrzywka.
Przewód pokarmowy: Ból brzucha, jadłowstręt, zaparcia, zapalenie wątroby, złe samopoczucie, łagodne przemijające nieprawidłowości w testach czynności wątroby, nudności, zapalenie ślinianek przyusznych, niedrożność rzekoma (w tym niedrożność rzekoma okrężnicy), ból ślinianek i wymioty.
Układ moczowo-płciowy: Zmniejszona aktywność seksualna, trudności w oddawaniu moczu, zaburzenia erekcji, utrata libido, nokturia i zatrzymanie moczu.
Hematologiczny: Małopłytkowość.
Metaboliczny: Ginekomastia, przemijające podwyższenie stężenia glukozy we krwi lub fosfokinazy kreatynowej w surowicy oraz przyrost masy ciała.
Układ mięśniowo-szkieletowy: Skurcze nóg i bóle mięśni lub stawów.
Oro-otlaryngologia: Suchość błony śluzowej nosa.
Okulistyczne: Zaburzenia akomodacji, niewyraźne widzenie, pieczenie oczu, zmniejszone łzawienie i suchość oczu.
INTERAKCJE Z LEKAMI
Klonidyna może nasilać depresyjne działanie alkoholu, barbituranów lub innych leków uspokajających na ośrodkowy układ nerwowy. Jeśli pacjent otrzymujący chlorowodorek klonidyny przyjmuje również trójpierścieniowe leki przeciwdepresyjne, hipotensyjne działanie klonidyny może być zmniejszone, co wymaga zwiększenia dawki klonidyny. Jeśli pacjent otrzymujący klonidynę przyjmuje również neuroleptyki, mogą wystąpić lub nasilić zaburzenia regulacji ortostatycznej (np. niedociśnienie ortostatyczne, zawroty głowy, zmęczenie).
Monitorować częstość akcji serca u pacjentów otrzymujących klonidynę jednocześnie z lekami, o których wiadomo, że wpływają na czynność węzła zatokowego lub przewodzenie w węźle pk, np. naparstnica, blokery kanału wapniowego i beta-blokery. W związku ze stosowaniem klonidyny jednocześnie z diltiazemem lub werapamilem zgłaszano bradykardię zatokową skutkującą hospitalizacją i wstawieniem stymulatora serca.
Amitryptylina w połączeniu z klonidyną nasila objawy zmian rogówki u szczurów (patrz Toksykologia ).
Na podstawie obserwacji pacjentów w stanie majaczenia alkoholowego sugerowano, że duże dożylne dawki klonidyny mogą zwiększać potencjał arytmogenny (wydłużenie odstępu QT, migotanie komór) dużych dawek dożylnych haloperidolu. Nie ustalono związku przyczynowego i znaczenia dla tabletek doustnych zawierających klonidynę.
OSTRZEŻENIA
Wycofanie
Pacjentów należy pouczyć, aby nie przerywali leczenia bez konsultacji z lekarzem. Nagłe zaprzestanie leczenia klonidyną w niektórych przypadkach powodowało objawy takie jak nerwowość, pobudzenie, ból głowy i drżenie, którym towarzyszył lub po którym następował gwałtowny wzrost ciśnienia krwi i podwyższone stężenie katecholamin w osoczu. Wydaje się, że prawdopodobieństwo wystąpienia takich reakcji w przypadku przerwania leczenia klonidyną jest większe po podaniu większych dawek lub kontynuacji jednoczesnego leczenia beta-adrenolitykami i dlatego zaleca się szczególną ostrożność w takich sytuacjach. Po odstawieniu klonidyny zgłaszano rzadkie przypadki encefalopatii nadciśnieniowej, incydentów naczyniowo-mózgowych i zgonów. W przypadku przerwania leczenia tabletkami CATAPRES, lekarz powinien stopniowo zmniejszać dawkę w ciągu 2 do 4 dni, aby uniknąć objawów odstawienia.
Nadmierny wzrost ciśnienia krwi po odstawieniu tabletek CATAPRES 100mcg można odwrócić podając doustnie chlorowodorek klonidyny lub dożylnie fentolaminę. Jeśli leczenie ma zostać przerwane u pacjentów otrzymujących jednocześnie beta-bloker i klonidynę, beta-bloker należy odstawić na kilka dni przed stopniowym odstawieniem tabletek CATAPRES 100mcg.
Ponieważ dzieci często cierpią na choroby przewodu pokarmowego, które prowadzą do wymiotów, mogą być szczególnie podatne na epizody nadciśnienia wynikające z nagłej niemożności przyjmowania leków.
ŚRODKI OSTROŻNOŚCI
Ogólny
U pacjentów, u których rozwinęło się miejscowe uczulenie kontaktowe na Catapres-TTS® (klonidyna), kontynuacja leczenia Catapres-TTS lub zastąpienie doustnego leczenia chlorowodorkiem klonidyny może wiązać się z rozwojem uogólnionej wysypki skórnej.
pacjentów, u których wystąpi reakcja alergiczna na Catapres-TTS, zastąpienie doustnego chlorowodorku klonidyny może również wywołać reakcję alergiczną (w tym uogólnioną wysypkę, pokrzywkę lub obrzęk naczynioruchowy).
Sympatykolityczne działanie klonidyny może nasilać dysfunkcję węzła zatokowego i blok przedsionkowo-komorowy (AV), zwłaszcza u pacjentów przyjmujących inne leki sympatykolityczne. Istnieją doniesienia po wprowadzeniu do obrotu dotyczące pacjentów z zaburzeniami przewodzenia i (lub) przyjmujących inne leki sympatykolityczne, u których wystąpiła ciężka bradykardia wymagająca dożylnego podania atropiny, dożylnego izoproterenolu i tymczasowej stymulacji serca podczas przyjmowania klonidyny.
W nadciśnieniu tętniczym wywołanym przez guz chromochłonny nie należy spodziewać się efektu terapeutycznego tabletek CATAPRES 100mcg.
Zastosowanie okołooperacyjne
Podawanie tabletek Catapres® (chlorowodorek klonidyny, USP) powinno być kontynuowane w ciągu 4 godzin po zabiegu i wznowione tak szybko, jak to możliwe. Ciśnienie krwi powinno być dokładnie monitorowane podczas zabiegu chirurgicznego, aw razie potrzeby powinny być dostępne dodatkowe środki kontroli ciśnienia krwi.
rakotwórczość, mutageneza, upośledzenie płodności
Przewlekłe podawanie klonidyny w diecie nie miało działania rakotwórczego u szczurów (132 tygodnie) lub myszy (78 tygodni) otrzymujących odpowiednio do 46 lub 70-krotność maksymalnej zalecanej dziennej dawki u ludzi wyrażonych w mg/kg (9- lub 6-krotność MRDHD na mg/m² podstawy). Nie było dowodów na genotoksyczność w teście Amesa na mutagenność lub teście mikrojądrowym myszy na klastogenność.
Dawki klonidyny do 150 μg/kg (około 3 razy MRDHD) nie miały wpływu na płodność samców i samic szczurów. W oddzielnym eksperymencie, płodność samic szczurów wydawała się być zaburzona przy poziomach dawek od 500 do 2000 μg/kg (10 do 40 razy MRDHD doustnie w przeliczeniu na mg/kg; 2 do 8 razy MRDHD w przeliczeniu na mg/m² ).
Ciąża
Efekty teratogenne
Ciąża Kategoria C
Badania nad reprodukcją przeprowadzone na królikach przy dawkach do około 3 razy większych od maksymalnej zalecanej dziennej dawki dla ludzi (MRDHD) tabletek Catapres® (chlorowodorek klonidyny, USP) nie wykazały działania teratogennego lub embriotoksycznego u królików. Jednak u szczurów dawki tak niskie jak 1/3 MRDHD doustnie (1/15 MRDHD w przeliczeniu na mg/m²) klonidyny wiązały się ze zwiększoną resorpcją w badaniu, w którym matki były leczone w sposób ciągły od 2 miesięcy przed kryciem . Zwiększona resorpcja nie była związana z leczeniem w tym samym czasie lub przy wyższych poziomach dawek (do 3-krotności doustnej MRDHD), gdy samice leczono w 6. do 15. dniu ciąży. Wzrost resorpcji obserwowano przy znacznie wyższych poziomach dawek (40-krotnie doustny MRDHD w przeliczeniu na mg/kg; 4 do 8-krotność MRDHD w przeliczeniu na mg/m²) u myszy i szczurów leczonych w dniach ciąży od 1 do 14 (najniższa stosowana w badaniu dawka wynosiła 500 μg/kg).
Nie przeprowadzono odpowiednich, dobrze kontrolowanych badań u kobiet w ciąży. Klonidyna przenika przez barierę łożyskową (patrz FARMAKOLOGIA KLINICZNA , Farmakokinetyka ). Ponieważ badania reprodukcji na zwierzętach nie zawsze pozwalają przewidzieć reakcję człowieka, lek ten powinien być stosowany w czasie ciąży tylko wtedy, gdy jest to bezwzględnie konieczne.
Matki karmiące
Ponieważ chlorowodorek klonidyny przenika do mleka ludzkiego, należy zachować ostrożność podając tabletki CATAPRES 100mcg kobiecie karmiącej.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność u pacjentów pediatrycznych nie zostały ustalone w odpowiednich i dobrze kontrolowanych badaniach (patrz OSTRZEŻENIA , Wycofanie ).
PRZEDAWKOWAĆ
Nadciśnienie może rozwinąć się wcześnie, a następnie może wystąpić niedociśnienie, bradykardia, depresja oddechowa, hipotermia, senność, osłabienie lub brak odruchów, osłabienie, drażliwość i zwężenie źrenic. Częstość występowania depresji OUN może być wyższa u dzieci niż u dorosłych. Duże przedawkowanie może spowodować odwracalne zaburzenia przewodzenia w sercu lub zaburzenia rytmu serca, bezdech, śpiączkę i drgawki. Oznaki i objawy przedawkowania zwykle pojawiają się w ciągu 30 minut do dwóch godzin po ekspozycji. Już 0,1 mg klonidyny powodowało objawy toksyczności u dzieci.
Nie ma swoistego antidotum na przedawkowanie klonidyny. Przedawkowanie klonidyny może spowodować szybki rozwój depresji OUN; dlatego nie zaleca się wywoływania wymiotów syropem z ipekaku. Płukanie żołądka może być wskazane po niedawnym i/lub dużym spożyciu. Korzystne może być podanie węgla aktywowanego i/lub środka przeczyszczającego. Leczenie wspomagające może obejmować siarczan atropiny w przypadku bradykardii, płyny dożylne i/lub leki wazopresyjne w przypadku niedociśnienia oraz leki rozszerzające naczynia w przypadku nadciśnienia. Nalokson może być użytecznym środkiem pomocniczym w leczeniu depresji oddechowej, niedociśnienia i/lub śpiączki wywołanej przez klonidynę; Należy monitorować ciśnienie krwi, ponieważ podawanie naloksonu czasami powodowało paradoksalne nadciśnienie. Dializa prawdopodobnie nie wpłynie znacząco na eliminację klonidyny.
Największe zgłoszone do tej pory przedawkowanie dotyczyło 28-letniego mężczyzny, który połknął 100 mg chlorowodorku klonidyny w proszku. U tego pacjenta rozwinęło się nadciśnienie, a następnie niedociśnienie, bradykardia, bezdech, halucynacje, półśpiączka i przedwczesne skurcze komorowe. Pacjentka całkowicie wyzdrowiała po intensywnym leczeniu. Stężenia klonidyny w osoczu wynosiły 60 ng/ml po 1 godzinie, 190 ng/ml po 1,5 godziny, 370 ng/ml po 2 godzinach i 120 ng/ml po 5,5 i 6,5 godziny. U myszy i szczurów doustna dawka LD50 klonidyny wynosi odpowiednio 206 i 465 mg/kg.
PRZECIWWSKAZANIA
Tabletek Catapres® (chlorowodorek klonidyny, USP) nie należy stosować u pacjentów ze stwierdzoną nadwrażliwością na klonidynę (patrz ŚRODKI OSTROŻNOŚCI ).
FARMAKOLOGIA KLINICZNA
Klonidyna stymuluje alfa-adrenoreceptory w pniu mózgu. Działanie to powoduje zmniejszenie odpływu współczulnego z ośrodkowego układu nerwowego oraz zmniejszenie oporu obwodowego, oporu naczyniowego nerek, częstości akcji serca i ciśnienia krwi. Tabletki CATAPRES 100mcg działają stosunkowo szybko. Ciśnienie krwi pacjenta spada w ciągu 30 do 60 minut po podaniu doustnym, maksymalny spadek następuje w ciągu 2 do 4 godzin. Przepływ krwi przez nerki i szybkość filtracji kłębuszkowej pozostają zasadniczo niezmienione. Normalne odruchy postawy są nienaruszone; dlatego objawy ortostatyczne są łagodne i rzadkie.
Ostre badania z użyciem chlorowodorku klonidyny u ludzi wykazały umiarkowane zmniejszenie (15% do 20%) pojemności minutowej serca w pozycji leżącej bez zmiany oporu obwodowego: przy pochyleniu o 45° następuje mniejsze zmniejszenie pojemności minutowej serca i zmniejszenie oporu obwodowego. Podczas długotrwałej terapii rzut serca ma tendencję do powrotu do wartości kontrolnych, podczas gdy opór obwodowy pozostaje zmniejszony. U większości pacjentów, którym podawano klonidynę, zaobserwowano spowolnienie tętna, ale lek nie zmienia prawidłowej odpowiedzi hemodynamicznej na wysiłek.
U niektórych pacjentów może rozwinąć się tolerancja na działanie hipotensyjne, co wymaga ponownej oceny leczenia.
Inne badania na pacjentach dostarczyły dowodów na zmniejszenie aktywności reninowej osocza oraz wydalania aldosteronu i katecholamin. Dokładny związek tych działań farmakologicznych z przeciwnadciśnieniowym działaniem klonidyny nie został w pełni wyjaśniony.
Klonidyna silnie stymuluje uwalnianie hormonu wzrostu zarówno u dzieci, jak iu dorosłych, ale przy długotrwałym stosowaniu nie powoduje przewlekłego podwyższenia poziomu hormonu wzrostu.
Farmakokinetyka
Farmakokinetyka klonidyny jest proporcjonalna do dawki w zakresie od 100 do 600 μg. Całkowita biodostępność klonidyny po podaniu doustnym wynosi od 70% do 80%. Maksymalne stężenie klonidyny w osoczu osiągane jest w ciągu około 1 do 3 godzin.
Po podaniu dożylnym klonidyna wykazuje dwufazową dyspozycję z okresem półtrwania dystrybucji wynoszącym około 20 minut i okresem półtrwania w fazie eliminacji od 12 do 16 godzin. Okres półtrwania wydłuża się do 41 godzin u pacjentów z ciężkimi zaburzeniami czynności nerek. Klonidyna przenika przez barierę łożyskową. Wykazano, że przenika przez barierę krew-mózg u szczurów.
Po podaniu doustnym około 40% do 60% wchłoniętej dawki jest wydalane z moczem w postaci niezmienionej w ciągu 24 godzin. Około 50% wchłoniętej dawki jest metabolizowane w wątrobie. Ani pokarm, ani rasa pacjenta nie wpływają na farmakokinetykę klonidyny.
Działanie przeciwnadciśnieniowe osiąga się przy stężeniach w osoczu od około 0,2 do 2,0 ng/ml u pacjentów z prawidłową czynnością wydalniczą. Dalszy wzrost stężeń w osoczu nie wzmocni działania przeciwnadciśnieniowego.
Toksykologia
W kilku badaniach z doustnym chlorowodorkiem klonidyny u szczurów albinosów leczonych przez sześć miesięcy lub dłużej obserwowano zależne od dawki zwiększenie częstości występowania i nasilenia spontanicznego zwyrodnienia siatkówki. Badania dystrybucji w tkankach u psów i małp wykazały stężenie klonidyny w naczyniówce.
Ze względu na zwyrodnienie siatkówki obserwowane u szczurów, podczas badań klinicznych u 908 pacjentów przeprowadzono badania oczu przed i okresowo po rozpoczęciu leczenia klonidyną. U 353 z tych 908 pacjentów badania wzroku prowadzono przez okres 24 miesięcy lub dłuższy. Z wyjątkiem pewnej suchości oczu, nie odnotowano żadnych nieprawidłowych zmian okulistycznych związanych z lekiem, a według specjalistycznych testów, takich jak elektroretinografia i olśnienie plamki, czynność siatkówki pozostała niezmieniona.
W połączeniu z amitryptyliną podanie chlorowodorku klonidyny doprowadziło do rozwoju zmian rogówkowych u szczurów w ciągu 5 dni.
INFORMACJA O PACJENCIE
Należy ostrzec pacjentów, aby nie przerywali leczenia tabletkami CATAPRES 100mcg bez porady lekarza.
Ponieważ pacjenci mogą odczuwać działanie uspokajające, zawroty głowy lub zaburzenia akomodacji podczas stosowania klonidyny, należy ich ostrzec przed wykonywaniem czynności, takich jak prowadzenie pojazdu lub obsługiwanie urządzeń lub maszyn. Należy również poinformować pacjentów, że to działanie uspokajające może być nasilone przez jednoczesne stosowanie alkoholu, barbituranów lub innych leków uspokajających.
Należy ostrzec pacjentów noszących soczewki kontaktowe, że leczenie tabletkami CATAPRES może powodować suchość oczu.
