Coreg 3.12mg, 6.25mg, 12.5mg, 25mg Carvedilol Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Coreg 25mg i jak się go stosuje?
Coreg to lek na receptę stosowany w leczeniu objawów niewydolności serca i wysokiego ciśnienia krwi (nadciśnienia). Coreg 25mg może być stosowany samodzielnie lub z innymi lekami.
Coreg należy do klasy leków o nazwie Beta-Blockers, Alpha Activity.
Nie wiadomo, czy Coreg 25mg jest bezpieczny i skuteczny u dzieci.
Jakie są możliwe skutki uboczne Coreg?
Coreg może powodować poważne skutki uboczne, w tym:
- zawroty,
- powolne lub nierówne bicie serca,
- uczucie zimna lub drętwienie palców rąk i nóg,
- ból w klatce piersiowej,
- suchy kaszel,
- świszczący oddech,
- ucisk w klatce piersiowej,
- obrzęk,
- szybki przyrost masy ciała,
- uczucie duszności,
- zwiększone pragnienie,
- zwiększone oddawanie moczu,
- suchość w ustach i
- owocowy zapach oddechu
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Coreg 6,25 mg to:
- zawroty głowy,
- wolne bicie serca,
- biegunka,
- przybranie na wadze,
- suche oczy i
- trudności w używaniu soczewek kontaktowych
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Coreg. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
Karwedylol jest nieselektywnym lekiem blokującym receptory β-adrenergiczne o działaniu blokującym receptory α1. Jest to (±)-1(karbazol-4-iloksy)-3-[[2-(o-metoksyfenoksy)etylo]amino]-2-propanol. Karwedilol jest mieszaniną racemiczną o następującej budowie:
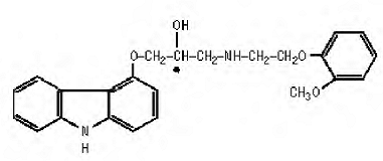
COREG 6,25 mg to biała, owalna tabletka powlekana zawierająca 3,125 mg, 6,25 mg, 12,5 mg lub 25 mg karwedylolu. Tabletki 6,25 mg, 12,5 mg i 25 mg to tabletki TILTAB. Składniki nieaktywne to koloidalny dwutlenek krzemu, krospowidon, hypromeloza, laktoza, stearynian magnezu, glikol polietylenowy, polisorbat 80, powidon, sacharoza i dwutlenek tytanu.
Karwedilol jest proszkiem o barwie od białej do białawej o masie cząsteczkowej 406,5 i wzorze cząsteczkowym C24H26N2O4. Jest swobodnie rozpuszczalny w dimetylosulfotlenku; rozpuszczalny w chlorku metylenu i metanolu; słabo rozpuszczalny w 95% etanolu i izopropanolu; słabo rozpuszczalny w eterze etylowym; i praktycznie nierozpuszczalny w wodzie, płynie żołądkowym (symulowany, TS, pH 1,1) i płynie jelitowym (symulowany, TS bez pankreatyny, pH 7,5).
WSKAZANIA
Niewydolność serca
COREG jest wskazany w leczeniu łagodnej do ciężkiej przewlekłej niewydolności serca pochodzenia niedokrwiennego lub kardiomiopatii, zwykle jako dodatek do leków moczopędnych, inhibitorów ACE i naparstnicy, w celu wydłużenia przeżycia, a także zmniejszenia ryzyka hospitalizacji [patrz INTERAKCJE Z LEKAMI , Studia kliniczne ].
Dysfunkcja lewej komory po zawale mięśnia sercowego
COREG jest wskazany w celu zmniejszenia śmiertelności sercowo-naczyniowej u pacjentów w stanie klinicznym stabilnych, którzy przeżyli ostrą fazę zawału mięśnia sercowego i mają frakcję wyrzutową lewej komory mniejszą lub równą 40% (z objawową niewydolnością serca lub bez) [patrz Studia kliniczne ].
Nadciśnienie
COREG 25 mg jest wskazany w leczeniu nadciśnienia pierwotnego [patrz Studia kliniczne ]. Może być stosowany samodzielnie lub w połączeniu z innymi lekami przeciwnadciśnieniowymi, zwłaszcza diuretykami typu tiazydowego [patrz INTERAKCJE Z LEKAMI ].
DAWKOWANIE I SPOSÓB PODAWANIA
COREG należy przyjmować z jedzeniem, aby spowolnić tempo wchłaniania i zmniejszyć częstość występowania efektów ortostatycznych.
Niewydolność serca
DAWKOWANIE MUSI BYĆ INDYWIDUALIZOWANE I ŚCIŚLE MONITOROWANE PRZEZ LEKARZA PODCZAS UP-MIARECZKOWANIA. Przed rozpoczęciem podawania 12,5 mg COREG zaleca się zminimalizowanie retencji płynów. Zalecana dawka początkowa COREG wynosi 3,125 mg dwa razy na dobę przez 2 tygodnie. Jeśli jest tolerowana, pacjentom można zwiększyć dawkę do 6,25, 12,5 i 25 mg dwa razy na dobę w kolejnych odstępach co najmniej 2 tygodni. Pacjenci powinni otrzymywać niższe dawki, jeśli większe dawki nie są tolerowane. Pacjentom z łagodną do umiarkowanej niewydolnością serca o masie ciała powyżej 85 kg (187 funtów) podawano maksymalną dawkę 50 mg dwa razy na dobę.
Należy pouczyć pacjentów, że rozpoczęcie leczenia i (w mniejszym stopniu) zwiększenie dawki może wiązać się z przemijającymi objawami zawrotów głowy lub oszołomienia (i rzadko omdlenia) w ciągu pierwszej godziny po podaniu. W tych okresach pacjenci powinni unikać takich sytuacji, jak prowadzenie pojazdu lub niebezpieczne czynności, w przypadku których objawy mogą spowodować obrażenia. Objawy rozszerzające naczynia często nie wymagają leczenia, ale przydatne może być oddzielenie czasu podawania 6,25 mg COREG od dawki inhibitora ACE lub czasowe zmniejszenie dawki inhibitora ACE. Dawki COREG 12,5 mg nie należy zwiększać do czasu ustabilizowania objawów zaostrzenia niewydolności serca lub rozszerzenia naczyń krwionośnych.
Zatrzymanie płynów (z przemijającymi objawami niewydolności serca lub bez nich) należy leczyć poprzez zwiększenie dawki leków moczopędnych.
Dawkę COREG należy zmniejszyć, jeśli u pacjentów wystąpi bradykardia (częstość akcji serca poniżej 55 uderzeń na minutę).
Epizody zawrotów głowy lub zatrzymanie płynów podczas rozpoczynania leczenia COREG 3,12 mg można na ogół opanować bez przerywania leczenia i nie wykluczają one późniejszego pomyślnego dostosowania dawki lub korzystnej odpowiedzi na karwedilol.
Dysfunkcja lewej komory po zawale mięśnia sercowego
DAWKOWANIE MUSI BYĆ INDYWIDUALNE I MONITOROWANE PODCZAS WZMACNIAJĄCEGO MIARECZKOWANIA. Leczenie preparatem COREG można rozpocząć w trybie szpitalnym lub ambulatoryjnym i należy je rozpocząć po osiągnięciu przez pacjenta stabilności hemodynamicznej i zminimalizowaniu retencji płynów. Zaleca się, aby COREG 3,12 mg rozpocząć od 6,25 mg dwa razy na dobę i zwiększyć po 3 do 10 dniach, w zależności od tolerancji, do 12,5 mg dwa razy na dobę, a następnie ponownie do docelowej dawki 25 mg dwa razy na dobę. Można zastosować niższą dawkę początkową (3,125 mg dwa razy na dobę) i/lub tempo zwiększania dawki może być spowolnione, jeśli jest to klinicznie wskazane (np. z powodu niskiego ciśnienia krwi lub częstości akcji serca lub zatrzymania płynów). Pacjenci powinni otrzymywać niższe dawki, jeśli większe dawki nie są tolerowane. Zalecany schemat dawkowania nie musi być zmieniany u pacjentów, którzy otrzymywali β-adrenolityk dożylny lub doustny w ostrej fazie zawału mięśnia sercowego.
Nadciśnienie
DAWKOWANIE MUSI BYĆ Zindywidualizowane. Zalecana dawka początkowa leku COREG 6,25 mg wynosi 6,25 mg dwa razy na dobę. Jeśli ta dawka jest tolerowana, stosując jako wytyczne ciśnienie skurczowe w pozycji stojącej mierzone około 1 godziny po podaniu, dawkę należy utrzymywać przez 7 do 14 dni, a następnie w razie potrzeby zwiększyć do 12,5 mg dwa razy na dobę, w oparciu o minimalne ciśnienie krwi, ponownie stosując stojące ciśnienie skurczowe 1 godzinę po podaniu jako wskazówka tolerancji. Tę dawkę należy również utrzymywać przez 7 do 14 dni, a następnie można ją zwiększyć do 25 mg dwa razy na dobę, jeśli jest tolerowana i konieczna. Pełne działanie przeciwnadciśnieniowe COREG 6,25 mg jest widoczne w ciągu 7 do 14 dni. Całkowita dzienna dawka nie powinna przekraczać 50 mg.
Można oczekiwać, że równoczesne podawanie z lekiem moczopędnym spowoduje addytywne działanie i nasilenie ortostatycznego składnika działania karwedylolu.
Niewydolność wątroby
Preparatu COREG 25 mg nie należy podawać pacjentom z ciężkimi zaburzeniami czynności wątroby [patrz PRZECIWWSKAZANIA ].
JAK DOSTARCZONE
Dawkowanie i mocne strony
Białe, owalne tabletki powlekane są dostępne w następujących mocach:
- 3,125 mg – wygrawerowane „39” i „SB”
- 6,25 mg – grawerowane „4140” i „SB”
- 12,5 mg – grawerowane „4141” i „SB”
- 25 mg – grawerowane „4142” i „SB”
Składowania i stosowania
Białe, owalne tabletki powlekane są dostępne w następujących mocach:
- 3,125 mg – wygrawerowane „39” i „SB”
- 6,25 mg – grawerowane „4140” i „SB”
- 12,5 mg – grawerowane „4141” i „SB”
- 25 mg – grawerowane „4142” i „SB”
Tabletki 6,25 mg, 12,5 mg i 25 mg to tabletki TILTAB.
- Butelki 3,125 mg po 100 sztuk: NDC 0007-4139-20
- Butelki 6,25 mg po 100 sztuk: NDC 0007-4140-20
- Butelki 12,5 mg po 100 sztuk: NDC 0007-4141-20
- Butelki 25 mg po 100 sztuk: NDC 0007-4142-20
Przechowywać w temperaturze poniżej 30°C (86°F). Chronić przed wilgocią. Dozuj w szczelnym, odpornym na światło pojemniku.
Wyprodukowano dla: GlaxoSmithKline Research Triangle Park, NC 27709. Aktualizacja: wrzesień 2017.
SKUTKI UBOCZNE
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
COREG 25 mg został oceniony pod kątem bezpieczeństwa u pacjentów z niewydolnością serca (łagodna, umiarkowana i ciężka), u pacjentów z dysfunkcją lewej komory serca po zawale mięśnia sercowego oraz u pacjentów z nadciśnieniem. Obserwowany profil zdarzeń niepożądanych był zgodny z farmakologią leku i stanem zdrowia uczestników badań klinicznych. Zdarzenia niepożądane zgłoszone dla każdej z tych populacji pacjentów przedstawiono poniżej. Wykluczone są zdarzenia niepożądane uważane za zbyt ogólne, aby miały charakter informacyjny, oraz te, które nie są racjonalnie związane ze stosowaniem leku, ponieważ były związane z leczonym stanem lub są bardzo częste w leczonej populacji. Częstość występowania zdarzeń niepożądanych była zasadniczo podobna we wszystkich podgrupach demograficznych (mężczyźni i kobiety, osoby starsze i inne niż osoby starsze, osoby czarne i inne).
Niewydolność serca
COREG 12,5 mg został oceniony pod kątem bezpieczeństwa w niewydolności serca u ponad 4500 pacjentów na całym świecie, z których ponad 2100 uczestniczyło w badaniach klinicznych kontrolowanych placebo. Około 60% całej leczonej populacji w badaniach klinicznych kontrolowanych placebo otrzymywało COREG 3,12 mg przez co najmniej 6 miesięcy, a 30% otrzymywało COREG przez co najmniej 12 miesięcy. W badaniu COMET 1511 pacjentów z łagodną lub umiarkowaną niewydolnością serca było leczonych COREG przez okres do 5,9 roku (średnia: 4,8 roku). Zarówno w amerykańskich badaniach klinicznych dotyczących łagodnej do umiarkowanej niewydolności serca, w których porównywano COREG 3,12 mg w dawkach dobowych do 100 mg (n = 765) z placebo (n = 437), jak i w międzynarodowym badaniu klinicznym dotyczącym ciężkiej niewydolności serca (COPERNICUS ), w którym porównano COREG w dawkach dobowych do 50 mg (n=1156) z placebo (n=1133), wskaźniki przerwania leczenia z powodu działań niepożądanych były podobne u pacjentów z karwedylolem i placebo. W badaniach klinicznych kontrolowanych placebo, jedyną przyczyną przerwania leczenia większą niż 1% i występującą częściej w przypadku karwedylolu były zawroty głowy (1,3% w przypadku karwedylolu, 0,6% w przypadku placebo w badaniu COPERNICUS).
tabeli 1 przedstawiono zdarzenia niepożądane zgłaszane u pacjentów z łagodną lub umiarkowaną niewydolnością serca włączonych do amerykańskich badań klinicznych kontrolowanych placebo oraz z ciężką niewydolnością serca włączonych do badania COPERNICUS. Przedstawiono zdarzenia niepożądane, które występowały częściej u osób leczonych lekiem niż u osób otrzymujących placebo, z częstością większą niż 3% u osób leczonych karwedylolem, niezależnie od związku przyczynowego. Mediana ekspozycji na lek w badaniu wyniosła 6,3 miesiąca zarówno dla karwedylolu, jak i placebo w badaniach z łagodną lub umiarkowaną niewydolnością serca oraz 10,4 miesiąca w badaniu z udziałem pacjentów z ciężką niewydolnością serca. Profil zdarzeń niepożądanych COREG 3,12 mg obserwowany w długoterminowym badaniu COMET był zasadniczo podobny do tego obserwowanego w amerykańskich badaniach niewydolności serca.
W badaniach tych zgłaszano również niewydolność serca i duszność, ale wskaźniki te były równe lub większe u osób, które otrzymywały placebo.
Następujące działania niepożądane zgłaszano z częstością większą niż 1%, ale mniejszą lub równą 3% i częściej podczas stosowania leku COREG 3,12 mg w badaniach kontrolowanych placebo w Stanach Zjednoczonych u pacjentów z łagodną lub umiarkowaną niewydolnością serca lub u pacjentów z ciężką niewydolnością serca w badaniu COPERNICUS.
Częstość występowania większa niż 1% do mniej niż lub równa 3%
Ciało jako całość: Alergia, złe samopoczucie, hipowolemia, gorączka, obrzęk nóg.
Układ sercowo-naczyniowy: Przeciążenie płynami, niedociśnienie ortostatyczne, zaostrzenie dławicy piersiowej, blok przedsionkowo-komorowy, kołatanie serca, nadciśnienie.
Centralny i obwodowy układ nerwowy: Hipestezja, zawroty głowy, parestezje.
Przewód pokarmowy: Melena, zapalenie przyzębia.
Wątroba i układ żółciowy: Zwiększony SGPT, zwiększony SGOT.
Metaboliczne i odżywcze: Hiperurykemia, hipoglikemia, hiponatremia, zwiększenie aktywności fosfatazy zasadowej, cukromocz, hiperwolemia, cukrzyca, zwiększenie GGT, utrata masy ciała, hiperkaliemia, zwiększenie stężenia kreatyniny.
Układ mięśniowo-szkieletowy: Skurcze mięśni.
Płytki krwi, krwawienie i krzepnięcie: Zmniejszenie protrombiny, plamica, małopłytkowość.
Psychiatryczny: Senność.
Rozrodczy, samiec: Impotencja.
Zmysły specjalne: Rozmazany obraz.
Układ moczowy: Niewydolność nerek, albuminuria, krwiomocz.
Dysfunkcja lewej komory po zawale mięśnia sercowego
COREG oceniano pod kątem bezpieczeństwa u osób, które przeżyły ostry zawał mięśnia sercowego z dysfunkcją lewej komory w badaniu CAPRICORN, w którym wzięło udział 969 osób, które otrzymały COREG 6,25 mg i 980 osób, które otrzymały placebo. Około 75% pacjentów otrzymywało COREG 25 mg przez co najmniej 6 miesięcy, a 53% otrzymywało COREG 12,5 mg przez co najmniej 12 miesięcy. Badani byli leczeni przez średnio 12,9 miesiąca i 12,8 miesiąca odpowiednio 12,5 mg COREG i placebo.
Najczęstsze zdarzenia niepożądane zgłaszane po podaniu COREG 25 mg w badaniu CAPRICORN były zgodne z profilem leku w amerykańskich badaniach niewydolności serca i badaniu COPERNICUS. Jedynymi dodatkowymi zdarzeniami niepożądanymi zgłaszanymi w badaniu CAPRICORN u ponad 3% pacjentów i częściej leczonych karwedylolem były duszność, niedokrwistość i obrzęk płuc. Następujące działania niepożądane zgłaszano z częstością większą niż 1%, ale mniejszą lub równą 3% i częściej w przypadku COREG: zespół grypy, udar naczyniowy mózgu, zaburzenia naczyń obwodowych, hipotonia, depresja, ból żołądkowo-jelitowy, zapalenie stawów i dna moczanowa. Całkowity odsetek przerwań z powodu zdarzeń niepożądanych był podobny w obu grupach badanych. W tej bazie danych jedyną przyczyną przerwania leczenia większą niż 1% i występującą częściej w przypadku karwedylolu było niedociśnienie (1,5% w przypadku karwedylolu, 0,2% w przypadku placebo).
Nadciśnienie
COREG oceniano pod kątem bezpieczeństwa w nadciśnieniu u ponad 2193 osób w badaniach klinicznych w USA i 2976 osób w międzynarodowych badaniach klinicznych. Około 36% całej leczonej populacji otrzymywało COREG przez co najmniej 6 miesięcy. Większość zdarzeń niepożądanych zgłaszanych podczas leczenia COREG 25 mg miała nasilenie łagodne do umiarkowanego. W kontrolowanych badaniach klinicznych w USA bezpośrednio porównujących COREG 12,5 mg w dawkach do 50 mg (n = 1142) z placebo (n = 462), 4,9% pacjentów otrzymujących COREG 6,25 mg przerwało leczenie z powodu zdarzeń niepożądanych w porównaniu z 5,2% pacjentów otrzymujących placebo. Chociaż nie było ogólnej różnicy w częstości przerwania leczenia, przerwanie leczenia było częstsze w grupie leczonej karwedylolem z powodu niedociśnienia ortostatycznego (1% w porównaniu z 0). Ogólna częstość występowania zdarzeń niepożądanych w amerykańskich badaniach kontrolowanych placebo wzrosła wraz ze wzrostem dawki COREG. W przypadku pojedynczych zdarzeń niepożądanych można to odróżnić jedynie od zawrotów głowy, których częstość wzrosła z 2% do 5%, gdy całkowita dawka dobowa wzrosła z 6,25 mg do 50 mg.
Tabela 2 przedstawia zdarzenia niepożądane w badaniach klinicznych kontrolowanych placebo w Stanach Zjednoczonych dotyczące nadciśnienia tętniczego, które wystąpiły z częstością większą lub równą 1% niezależnie od przyczynowości i które występowały częściej u osób leczonych lekami niż u osób otrzymujących placebo.
W badaniach tych zgłaszano również duszność i zmęczenie, ale wskaźniki te były równe lub większe u osób, które otrzymywały placebo.
Następujące działania niepożądane, które nie zostały opisane powyżej, zostały zgłoszone jako prawdopodobnie lub prawdopodobnie związane z 25 mg COREG w ogólnoświatowych otwartych lub kontrolowanych badaniach klinicznych z zastosowaniem COREG w dawce 12,5 mg u pacjentów z nadciśnieniem lub niewydolnością serca.
Częstość występowania większa niż 0,1% do mniej niż lub równa 1%
Układ sercowo-naczyniowy: Niedokrwienie obwodowe, tachykardia.
Centralny i obwodowy układ nerwowy m: Hipokinezja.
Przewód pokarmowy: Bilirubinemia, zwiększenie aktywności enzymów wątrobowych (0,2% pacjentów z nadciśnieniem tętniczym i 0,4% pacjentów z niewydolnością serca zostało przerwanych z leczenia z powodu zwiększenia aktywności enzymów wątrobowych) [patrz Doświadczenie postmarketingowe ].
Psychiatryczny: Nerwowość, zaburzenia snu, zaostrzona depresja, zaburzenia koncentracji, nieprawidłowe myślenie, paroniria, labilność emocjonalna.
Układ oddechowy: Astma [patrz PRZECIWWSKAZANIA ].
Rozrodczy, samiec: Zmniejszone libido.
Skóra i przydatki: Świąd, wysypka rumieniowa, wysypka plamisto-grudkowa, wysypka łuszczycopodobna, reakcja nadwrażliwości na światło.
Zmysły specjalne: Szum w uszach.
Układ moczowy: Zwiększona częstotliwość mikcji.
Autonomiczny układ nerwowy: Suchość w ustach, zwiększona potliwość.
Metaboliczne i odżywcze: Hipokaliemia, hipertriglicerydemia.
Hematologiczny: Niedokrwistość, leukopenia.
Następujące zdarzenia zgłoszono u mniej niż 0,1% pacjentów i są potencjalnie ważne: całkowity blok przedsionkowo-komorowy, blok odnogi pęczka Hisa, niedokrwienie mięśnia sercowego, zaburzenia naczyniowo-mózgowe, drgawki, migrena, nerwobóle, niedowład, reakcja rzekomoanafilaktyczna, łysienie, złuszczające zapalenie skóry, amnezja, krwotok z przewodu pokarmowego, skurcz oskrzeli, obrzęk płuc, osłabienie słuchu, zasadowica oddechowa, podwyższony BUN, obniżony HDL, pancytopenia i atypowe limfocyty.
Nieprawidłowości laboratoryjne
Podczas leczenia COREG obserwowano odwracalne zwiększenie aktywności aminotransferaz w surowicy (AlAT lub AspAT). Częstość zwiększenia aktywności aminotransferaz (2 do 3 razy powyżej górnej granicy normy) obserwowana podczas kontrolowanych badań klinicznych była na ogół podobna u pacjentów leczonych COREG i otrzymujących placebo. Jednak w przypadku COREG zaobserwowano podwyższenie poziomu transaminaz, potwierdzone przez ponowne prowokację. W długoterminowym, kontrolowanym placebo badaniu z ciężką niewydolnością serca, pacjenci leczeni COREG 25 mg mieli niższe wartości transaminaz wątrobowych niż pacjenci otrzymujący placebo, prawdopodobnie dlatego, że poprawa czynności serca wywołana przez COREG 6,25 mg prowadziła do mniejszego przekrwienia wątroby i/ lub poprawiony przepływ krwi przez wątrobę.
COREG 25 mg nie był związany z klinicznie istotnymi zmianami stężenia potasu w surowicy, całkowitych triglicerydów, całkowitego cholesterolu, cholesterolu HDL, kwasu moczowego, azotu mocznikowego we krwi lub kreatyniny. Nie odnotowano klinicznie istotnych zmian stężenia glukozy w surowicy na czczo u pacjentów z nadciśnieniem; Stężenie glukozy w surowicy na czczo nie było oceniane w badaniach klinicznych dotyczących niewydolności serca.
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania COREG po dopuszczeniu do obrotu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Zaburzenia krwi i układu chłonnego
Anemia aplastyczna.
Zaburzenia układu immunologicznego
Nadwrażliwość (np. reakcje anafilaktyczne, obrzęk naczynioruchowy, pokrzywka).
Zaburzenia nerek i dróg moczowych
Niemożność utrzymania moczu.
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia
Śródmiąższowe zapalenie płuc.
Zaburzenia skóry i tkanki podskórnej
Zespół Stevensa-Johnsona, martwica toksyczno-rozpływna naskórka, rumień wielopostaciowy.
INTERAKCJE Z LEKAMI
Inhibitory CYP2D6 i słabe metabolizmy
Nie badano interakcji karwedylolu z silnymi inhibitorami izoenzymu CYP2D6 (takimi jak chinidyna, fluoksetyna, paroksetyna i propafenon), ale można się spodziewać, że leki te będą zwiększać stężenie enancjomeru R(+) karwedylolu we krwi [patrz FARMAKOLOGIA KLINICZNA ]. Retrospektywna analiza skutków ubocznych w badaniach klinicznych wykazała, że osoby słabo metabolizujące 2D6 miały wyższy wskaźnik zawrotów głowy podczas zwiększania dawki, prawdopodobnie w wyniku rozszerzającego naczynia działania wyższych stężeń enancjomeru R(+) blokującego receptory alfa.
Środki hipotensyjne
Pacjenci przyjmujący beta-adrenolityki i leki mogące zmniejszać ilość katecholamin (np. inhibitory rezerpiny i monoaminooksydazy) powinni być uważnie obserwowani pod kątem objawów niedociśnienia i/lub ciężkiej bradykardii.
Jednoczesne podawanie klonidyny z beta-adrenolitykiem może powodować niedociśnienie i bradykardię. W przypadku zakończenia jednoczesnego leczenia β-adrenolitykiem i klonidyną, należy najpierw odstawić β-adrenolityk. Leczenie klonidyną można następnie przerwać kilka dni później poprzez stopniowe zmniejszanie dawki.
Cyklosporyna
Po rozpoczęciu leczenia karwedylolem u 21 pacjentów po przeszczepieniu nerki, cierpiących na przewlekłe odrzucanie naczyniowe, obserwowano niewielkie zwiększenie średniego minimalnego stężenia cyklosporyny. U około 30% badanych dawka cyklosporyny musiała zostać zmniejszona w celu utrzymania stężeń cyklosporyny w zakresie terapeutycznym, podczas gdy u pozostałych nie było potrzeby dostosowania. Średnio dla grupy dawka cyklosporyny została zmniejszona u tych osób o około 20%. Ze względu na duże różnice międzyosobnicze w zakresie wymaganego dostosowania dawki zaleca się ścisłe monitorowanie stężenia cyklosporyny po rozpoczęciu leczenia karwedylolem i odpowiednie dostosowanie dawki cyklosporyny.
Glikozydy naparstnicy
Zarówno glikozydy naparstnicy, jak i β-adrenolityki spowalniają przewodzenie przedsionkowo-komorowe i zmniejszają częstość akcji serca. Jednoczesne stosowanie może zwiększać ryzyko bradykardii. Stężenie digoksyny zwiększa się o około 15% w przypadku jednoczesnego podawania digoksyny i karwedylolu. Dlatego zaleca się wzmożone monitorowanie digoksyny podczas rozpoczynania, dostosowywania lub przerywania COREG [patrz FARMAKOLOGIA KLINICZNA ].
Induktory/inhibitory metabolizmu wątrobowego
Ryfampicyna zmniejszała stężenie karwedylolu w osoczu o około 70% [patrz FARMAKOLOGIA KLINICZNA ]. Cymetydyna zwiększała AUC o około 30%, ale nie powodowała zmiany Cmax [patrz FARMAKOLOGIA KLINICZNA ].
Amiodaron
Amiodaron i jego metabolit deetyloamiodaron, inhibitory CYP2C9 i glikoproteiny P, co najmniej dwukrotnie zwiększyły stężenie S(-)-enancjomeru karwedylolu [patrz FARMAKOLOGIA KLINICZNA ]. Jednoczesne podawanie amiodaronu lub innych inhibitorów CYP2C9, takich jak flukonazol, z COREG może nasilać działanie β-adrenolityczne, powodując dalsze spowolnienie częstości akcji serca lub przewodzenia w sercu. Pacjenci powinni być obserwowani pod kątem objawów bradykardii lub bloku serca, szczególnie gdy jeden lek jest dodawany do wcześniej stosowanego leczenia drugim.
Blokery kanału wapniowego
Podczas jednoczesnego podawania COREG 25 mg z diltiazemem obserwowano zaburzenia przewodzenia (rzadko z zaburzeniami hemodynamicznymi). Podobnie jak w przypadku innych beta-adrenolityków, jeśli COREG 25 mg podawany jest z blokerami kanału wapniowego typu werapamil lub diltiazem, zaleca się monitorowanie EKG i ciśnienia tętniczego.
Insulina lub hipoglikemia doustna
β-blokery mogą nasilać obniżające poziom cukru we krwi działanie insuliny i doustnych leków hipoglikemizujących. Dlatego u pacjentów przyjmujących insulinę lub doustne leki hipoglikemizujące zaleca się regularne monitorowanie stężenia glukozy we krwi [patrz OSTRZEŻENIA I ŚRODKI ].
Znieczulenie
Jeśli leczenie COREG ma być kontynuowane okołooperacyjnie, należy zachować szczególną ostrożność przy stosowaniu środków znieczulających obniżających czynność mięśnia sercowego, takich jak eter, cyklopropan i trichloroetylen [patrz PRZEDAWKOWAĆ ].
OSTRZEŻENIA
Zawarte jako część "ŚRODKI OSTROŻNOŚCI" Sekcja
ŚRODKI OSTROŻNOŚCI
Zaprzestanie terapii
Pacjentom z chorobą wieńcową leczonych preparatem COREG należy odradzać nagłe przerwanie leczenia. U pacjentów z dusznicą bolesną po nagłym przerwaniu leczenia β-adrenolitykami zgłaszano ciężkie zaostrzenie dławicy piersiowej i wystąpienie zawału mięśnia sercowego oraz komorowych zaburzeń rytmu serca. Ostatnie 2 powikłania mogą wystąpić z lub bez wcześniejszego zaostrzenia dławicy piersiowej. Podobnie jak w przypadku innych beta-adrenolityków, gdy planowane jest odstawienie COREG, należy uważnie obserwować pacjentów i zalecić im ograniczenie aktywności fizycznej do minimum. O ile to możliwe, COREG należy odstawić na 1 do 2 tygodni. Jeśli dławica piersiowa nasili się lub rozwinie się ostra niewydolność wieńcowa, zaleca się niezwłoczne wznowienie leczenia COREG, przynajmniej tymczasowo. Ponieważ choroba wieńcowa jest powszechna i może być nierozpoznana, rozsądne może być nie przerywanie nagle leczenia COREG 3,12 mg, nawet u pacjentów leczonych tylko z powodu nadciśnienia tętniczego lub niewydolności serca.
Bradykardia
badaniach klinicznych COREG 25 mg powodował bradykardię u około 2% osób z nadciśnieniem, 9% osób z niewydolnością serca i 6,5% osób z zawałem mięśnia sercowego i dysfunkcją lewej komory. Jeśli częstość tętna spadnie poniżej 55 uderzeń na minutę, dawkę należy zmniejszyć.
Niedociśnienie
badaniach klinicznych dotyczących głównie łagodnej do umiarkowanej niewydolności serca, niedociśnienie i niedociśnienie ortostatyczne wystąpiły u 9,7%, a omdlenia u 3,4% pacjentów otrzymujących COREG w porównaniu z odpowiednio 3,6% i 2,5% pacjentów otrzymujących placebo. Ryzyko wystąpienia tych zdarzeń było największe w ciągu pierwszych 30 dni dawkowania, co odpowiada okresowi zwiększania dawki i było przyczyną przerwania leczenia u 0,7% pacjentów otrzymujących COREG 12,5 mg w porównaniu z 0,4% pacjentów otrzymujących placebo. W długotrwałym, kontrolowanym placebo badaniu dotyczącym ciężkiej niewydolności serca (COPERNICUS), niedociśnienie i niedociśnienie ortostatyczne wystąpiły u 15,1%, a omdlenia u 2,9% pacjentów z niewydolnością serca otrzymujących COREG w porównaniu z odpowiednio 8,7% i 2,3% pacjentów otrzymujących placebo. Zdarzenia te były przyczyną przerwania leczenia u 1,1% pacjentów otrzymujących COREG w porównaniu z 0,8% pacjentów otrzymujących placebo.
Niedociśnienie ortostatyczne wystąpiło u 1,8%, a omdlenia u 0,1% pacjentów z nadciśnieniem, głównie po podaniu dawki początkowej lub w momencie zwiększania dawki i było przyczyną przerwania leczenia u 1% pacjentów.
W badaniu CAPRICORN u osób, które przeżyły ostry zawał mięśnia sercowego, niedociśnienie lub niedociśnienie ortostatyczne wystąpiły u 20,2% pacjentów otrzymujących COREG w porównaniu z 12,6% pacjentów otrzymujących placebo. Omdlenie zgłoszono odpowiednio u 3,9% i 1,9% badanych. Zdarzenia te były przyczyną przerwania leczenia u 2,5% pacjentów otrzymujących COREG w porównaniu z 0,2% pacjentów otrzymujących placebo.
Rozpoczęcie od małej dawki, podawanie z pokarmem i stopniowe zwiększanie dawki powinno zmniejszyć prawdopodobieństwo omdleń lub nadmiernego niedociśnienia [patrz DAWKOWANIE I SPOSÓB PODAWANIA ]. Podczas rozpoczynania leczenia należy ostrzec pacjenta, aby unikał sytuacji, takich jak prowadzenie pojazdu lub wykonywanie niebezpiecznych czynności, które mogą spowodować obrażenia w przypadku omdlenia.
Niewydolność serca/zatrzymanie płynów
Podczas zwiększania dawki karwedylolu może wystąpić pogorszenie niewydolności serca lub zatrzymanie płynów. Jeśli takie objawy wystąpią, należy zwiększyć leki moczopędne, a dawki karwedylolu nie należy zwiększać do czasu przywrócenia stabilności klinicznej [patrz DAWKOWANIE I SPOSÓB PODAWANIA ]. Czasami konieczne jest zmniejszenie dawki karwedylolu lub czasowe jej odstawienie. Takie epizody nie wykluczają późniejszego pomyślnego miareczkowania karwedylolu lub pozytywnej odpowiedzi na karwedilol. W badaniu kontrolowanym placebo z udziałem pacjentów z ciężką niewydolnością serca, nasilenie niewydolności serca w ciągu pierwszych 3 miesięcy zgłaszano w podobnym stopniu w przypadku karwedylolu i placebo. Gdy leczenie utrzymywano dłużej niż 3 miesiące, nasilenie niewydolności serca zgłaszano rzadziej u pacjentów leczonych karwedylolem niż otrzymujących placebo. Nasilenie niewydolności serca obserwowane podczas długotrwałego leczenia jest bardziej prawdopodobnie związane z chorobą podstawową pacjenta niż z leczeniem karwedylolem.
Niealergiczny skurcz oskrzeli
Pacjenci ze skurczem oskrzeli (np. przewlekłym zapaleniem oskrzeli, rozedmą) zasadniczo nie powinni otrzymywać β-adrenolityków. COREG można jednak stosować ostrożnie u pacjentów, którzy nie reagują lub nie tolerują innych leków przeciwnadciśnieniowych. Rozsądnie jest, jeśli stosuje się COREG, stosować najmniejszą skuteczną dawkę, aby zminimalizować hamowanie endogennych lub egzogennych β-agonistów.
Do badań klinicznych z udziałem pacjentów z niewydolnością serca włączano pacjentów ze skurczem oskrzeli, jeśli nie wymagali oni leków doustnych lub wziewnych w celu leczenia skurczu oskrzeli. U takich pacjentów zaleca się ostrożne stosowanie karwedylolu. Zalecenia dotyczące dawkowania należy ściśle przestrzegać, a dawkę należy zmniejszyć, jeśli podczas zwiększania dawki zaobserwuje się jakiekolwiek objawy skurczu oskrzeli.
Kontrola glikemii w cukrzycy typu 2
Ogólnie rzecz biorąc, β-adrenolityki mogą maskować niektóre objawy hipoglikemii, zwłaszcza tachykardię. Nieselektywne beta-adrenolityki mogą nasilać hipoglikemię indukowaną przez insulinę i opóźniać powrót stężenia glukozy w surowicy. Należy ostrzec pacjentów z samoistną hipoglikemią lub pacjentów z cukrzycą otrzymujących insulinę lub doustne leki hipoglikemizujące.
U pacjentów z niewydolnością serca i cukrzycą leczenie karwedylolem może prowadzić do nasilenia hiperglikemii, co odpowiada intensyfikacji leczenia hipoglikemizującego. Zaleca się monitorowanie stężenia glukozy we krwi podczas rozpoczynania, dostosowywania lub zaprzestania podawania karwedylolu. Nie przeprowadzono badań mających na celu zbadanie wpływu karwedylolu na kontrolę glikemii u pacjentów z cukrzycą i niewydolnością serca.
badaniu zaprojektowanym w celu zbadania wpływu karwedylolu na kontrolę glikemii w populacji z łagodnym do umiarkowanego nadciśnieniem i dobrze kontrolowaną cukrzycą typu 2, karwedylol nie miał niekorzystnego wpływu na kontrolę glikemii, na podstawie pomiarów HbA1c [patrz Studia kliniczne ].
Choroba naczyń obwodowych
β-adrenolityki mogą przyspieszać lub nasilać objawy niewydolności tętniczej u pacjentów z chorobą naczyń obwodowych. U takich osób należy zachować ostrożność.
Pogorszenie funkcji nerek
Rzadko stosowanie karwedylolu u pacjentów z niewydolnością serca powodowało pogorszenie czynności nerek. Wydaje się, że pacjenci z grupy ryzyka to pacjenci z niskim ciśnieniem krwi (skurczowe ciśnienie krwi poniżej 100 mm Hg), chorobą niedokrwienną serca i rozlaną chorobą naczyń i/lub współistniejącą niewydolnością nerek. Czynność nerek powróciła do stanu wyjściowego po odstawieniu karwedylolu. U pacjentów z tymi czynnikami ryzyka zaleca się monitorowanie czynności nerek podczas zwiększania dawki karwedylolu i odstawienie leku lub zmniejszenie dawki w przypadku pogorszenia czynności nerek.
Główna operacja
Nie należy rutynowo odstawiać β-adrenolityków przewlekle podawanych przed poważnym zabiegiem chirurgicznym; jednak upośledzona zdolność serca do reagowania na odruchowe bodźce adrenergiczne może zwiększać ryzyko znieczulenia ogólnego i zabiegów chirurgicznych.
Tyreotoksykoza
Blokada beta-adrenergiczna może maskować kliniczne objawy nadczynności tarczycy, takie jak tachykardia. Nagłe odstawienie β-blokady może prowadzić do nasilenia objawów nadczynności tarczycy lub wywołać burzę tarczycową.
Guz chromochłonny
U pacjentów z guzem chromochłonnym nadnerczy przed zastosowaniem jakiegokolwiek leku β-adrenolitycznego należy zastosować α-adrenolityk. Chociaż karwedylol ma działanie farmakologiczne blokujące zarówno receptory α, jak i β, nie ma doświadczeń dotyczących jego stosowania w tej chorobie. Dlatego należy zachować ostrożność podczas podawania karwedylolu pacjentom z podejrzeniem guza chromochłonnego.
Wariant Prinzmetala Angina
Leki o nieselektywnym działaniu β-adrenolitycznym mogą wywoływać ból w klatce piersiowej u pacjentów z dusznicą bolesną typu Prinzmetala. Nie ma doświadczenia klinicznego ze stosowaniem karwedylolu u tych pacjentów, chociaż działanie a-adrenolityczne może zapobiegać takim objawom. Należy jednak zachować ostrożność podczas podawania karwedylolu pacjentom z podejrzeniem dławicy piersiowej typu Prinzmetala.
Ryzyko reakcji anafilaktycznej
Podczas przyjmowania beta-adrenolityków pacjenci z ciężką reakcją anafilaktyczną w wywiadzie na różne alergeny mogą być bardziej reaktywni na powtarzane prowokacje, przypadkowe, diagnostyczne lub terapeutyczne. Tacy pacjenci mogą nie reagować na zwykłe dawki epinefryny stosowane w leczeniu reakcji alergicznej.
Śródoperacyjny zespół wiotkiej tęczówki
Intraoperative Floppy Iris Syndrome (IFIS) obserwowano podczas operacji zaćmy u niektórych pacjentów leczonych alfa-1-blokerami (COREG jest alfa/beta-blokerem). Ten wariant zespołu małej źrenicy charakteryzuje się połączeniem wiotkiej tęczówki, która faluje w odpowiedzi na śródoperacyjne prądy irygacyjne, postępującej śródoperacyjnej zwężenia źrenicy pomimo przedoperacyjnego rozszerzenia za pomocą standardowych leków rozszerzających źrenice oraz potencjalnego wypadania tęczówki w kierunku nacięć fakoemulsyfikacyjnych. Okulista pacjenta powinien być przygotowany na ewentualne modyfikacje techniki chirurgicznej, takie jak wykorzystanie haczyków tęczówki, pierścieni rozszerzających tęczówkę lub substancji lepkosprężystych. Wydaje się, że przerwanie terapii blokerami alfa-1 przed operacją zaćmy nie przynosi korzyści.
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( INFORMACJA O PACJENCIE ).
Pacjentów przyjmujących COREG należy poinformować o następujących kwestiach:
- Pacjenci powinni przyjmować COREG z jedzeniem.
- Pacjenci nie powinni przerywać ani przerywać stosowania COREG 25 mg bez porady lekarza.
- Pacjenci z niewydolnością serca powinni skonsultować się z lekarzem, jeśli wystąpią oznaki lub objawy pogorszenia niewydolności serca, takie jak przyrost masy ciała lub narastająca duszność.
- W pozycji stojącej pacjenci mogą odczuwać spadek ciśnienia krwi, co powoduje zawroty głowy i, rzadko, omdlenia. Pacjenci powinni siedzieć lub leżeć, gdy wystąpią objawy obniżonego ciśnienia krwi.
- W przypadku wystąpienia zawrotów głowy lub zmęczenia pacjenci powinni unikać prowadzenia pojazdów lub wykonywania niebezpiecznych zadań.
- Pacjenci powinni skonsultować się z lekarzem w przypadku wystąpienia zawrotów głowy lub omdlenia, w przypadku konieczności dostosowania dawki.
- Pacjenci z cukrzycą powinni zgłaszać lekarzowi wszelkie zmiany poziomu cukru we krwi.
- Osoby noszące soczewki kontaktowe mogą odczuwać zmniejszone łzawienie.
COREG 25 mg, COREG 3,12 mg CR i TILTAB są znakami towarowymi należącymi do lub licencjonowanymi przez grupę spółek GSK.
Druga wymieniona marka jest znakiem towarowym należącym do lub licencjonowanym przez jego właściciela i nie jest własnością ani nie jest licencjonowana przez grupę spółek GSK. Producent tej marki nie jest powiązany i nie wspiera grupy firm GSK ani jej produktów.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
W 2-letnich badaniach przeprowadzonych na szczurach, którym podawano karwedilol w dawkach do 75 mg na kg na dobę (12-krotność MRHD w mg na m2) lub na myszach podawano do 200 mg na kg na dobę (16-krotność MRHD na mg na m2). m2), karwedilol nie miał działania rakotwórczego.
Karwedylol dał wynik ujemny w szeregu testów genotoksyczności, w tym w testach Amesa i CHO/HGPRT pod kątem mutagenności oraz w testach na klastogenność in vitro mikrojąder u chomików i in vivo na ludzkich limfocytach.
połączonym badaniu toksyczności płodności/rozwoju/pourodzenia szczurom podawano doustnie karwedylol (12, 60, 300 mg na kg na dobę) przez zgłębnik przez 2 tygodnie przed kryciem oraz przez krycie, ciążę i odstawienie od matki dla samic i przez 62 lata. dni przed i po kryciu dla samców. W dawce 300 mg na kg na dobę (większej lub równej 50-krotności MRHD wyrażonej w mg na m2) karwedylol był toksyczny dla dorosłych szczurów (sedacja, zmniejszony przyrost masy ciała) i wiązał się ze zmniejszoną liczbą udanych kojarzeń, długotrwałym czas godowy, mniej ciałek żółtych i implantów na matkę, mniej żywych młodych w miocie i opóźnienia w fizycznym wzroście/rozwoju. Poziom bez wpływu na jawną toksyczność i upośledzenie płodności wynosił 60 mg na kg dziennie (10-krotność MRHD w mg na m2).
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
Dostępne dane dotyczące stosowania COREG 12,5 mg u kobiet w ciąży są niewystarczające do ustalenia, czy istnieje związane z lekiem ryzyko wystąpienia niekorzystnych wyników rozwojowych. Istnieje ryzyko dla matki i płodu związane ze źle kontrolowanym nadciśnieniem w ciąży. Stosowanie beta-adrenolityków w trzecim trymestrze ciąży może zwiększać ryzyko niedociśnienia, bradykardii, hipoglikemii i depresji oddechowej u noworodka [ patrz Rozważania kliniczne ]. W badaniach na zwierzętach dotyczących reprodukcji nie było dowodów na niekorzystne skutki rozwojowe przy klinicznie istotnych dawkach [ patrz Dane ]. Doustne podawanie karwedylolu ciężarnym samicom szczurów podczas organogenezy powodowało utratę po implantacji, zmniejszenie masy ciała płodu i zwiększoną częstość opóźnionego rozwoju szkieletu płodu w dawkach toksycznych dla matki, które były 50 razy większe od maksymalnej zalecanej dawki u ludzi (MRHD). Ponadto doustne podawanie karwedylolu ciężarnym królikom podczas organogenezy skutkowało zwiększoną utratą po implantacji w dawkach 25-krotnie większych niż MRHD [ patrz Dane ].
Szacowane ryzyko tła poważnych wad wrodzonych i poronienia dla wskazanych populacji jest nieznane. Wszystkie ciąże wiążą się z ryzykiem wady wrodzonej, utraty lub innych niekorzystnych skutków. W ogólnej populacji Stanów Zjednoczonych szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2% do 4% i 15% do 20%.
Rozważania kliniczne
Związane z chorobą ryzyko matki i/lub zarodka/płodu
Nadciśnienie w ciąży zwiększa ryzyko wystąpienia u matki stanu przedrzucawkowego, cukrzycy ciążowej, przedwczesnego porodu i powikłań porodowych (np. konieczności cięcia cesarskiego i krwotoku poporodowego). Nadciśnienie zwiększa ryzyko zahamowania wzrostu płodu i zgonu wewnątrzmacicznego u płodu. Kobiety w ciąży z nadciśnieniem powinny być dokładnie monitorowane i odpowiednio leczone.
Działania niepożądane u płodu/noworodka
Noworodki kobiet z nadciśnieniem leczonych beta-blokerami w trzecim trymestrze ciąży mogą być narażone na zwiększone ryzyko niedociśnienia, bradykardii, hipoglikemii i depresji oddechowej. Obserwować noworodki pod kątem objawów niedociśnienia, bradykardii, hipoglikemii i depresji oddechowej i odpowiednio postępować.
Dane
Dane zwierząt
Badania przeprowadzone na szczurach i królikach, którym podawano karwedylol podczas organogenezy płodów, wykazały zwiększoną utratę poimplantacyjną u szczurów po toksycznej dla matki dawce 300 mg na kg na dobę (50-krotność MRHD w mg na m2) i u królików (przy braku matki toksyczność) w dawkach 75 mg na kg na dzień (25-krotność MRHD w mg na m2). U szczurów zaobserwowano również zmniejszenie masy ciała płodu przy 300 mg na kg na dobę (50-krotność MRHD wyrażonej w mg na m2), któremu towarzyszyło zwiększone występowanie płodów z opóźnionym rozwojem szkieletu. U szczurów poziom bez wpływu na zarodek i płód wynosił 60 mg na kg dziennie (10-krotność MRHD w mg na m2); u królików wynosiła 15 mg na kg dziennie (5-krotność MRHD w mg na m2). W badaniu rozwoju przed- i pourodzeniowego szczurów, którym podawano karwedylol od późnej ciąży do laktacji, zaobserwowano zwiększoną śmiertelność zarodków po toksycznej dla matki dawce 200 mg na kg na dobę (około 32-krotność MRHD w mg na m2). a śmiertelność młodych i opóźnienia w fizycznym wzroście/rozwoju zaobserwowano przy 60 mg na kg dziennie (10-krotność MRHD w mg na m2) przy braku toksyczności matczynej. Poziom bez efektu wynosił 12 mg na kg dziennie (2-krotność MRHD jako mg na m2). Karwedylol był obecny w tkance płodowej szczura.
Laktacja
Podsumowanie ryzyka
Brak danych dotyczących obecności karwedylolu w mleku ludzkim, wpływu na niemowlę karmione piersią ani wpływu na produkcję mleka. Karwedylol jest obecny w mleku karmiących szczurów. Należy brać pod uwagę korzyści rozwojowe i zdrowotne wynikające z karmienia piersią, a także kliniczne zapotrzebowanie matki na COREG oraz wszelkie potencjalne niekorzystne skutki stosowania COREG 3,12 mg lub choroby podstawowej u matki karmionego piersią na niemowlę karmione piersią.
Zastosowanie pediatryczne
Skuteczność COREG 3,12 mg u pacjentów w wieku poniżej 18 lat nie została ustalona.
badaniu z podwójnie ślepą próbą 161 dzieci (średni wiek: 6 lat; zakres: od 2 miesięcy do 17 lat; 45% w wieku poniżej 2 lat) z przewlekłą niewydolnością serca [II-IV klasa NYHA, frakcja wyrzutowa lewej komory poniżej 40% u dzieci z układową lewą komorą (LV) i umiarkowaną-ciężką dysfunkcją komory jakościowo metodą echo u dzieci z układową komorą, która nie była LV], które otrzymywały standardowe leczenie podstawowe, przydzielono losowo do grupy placebo lub 2 dawek karwedylolu. Te poziomy dawek powodowały zmniejszenie częstości akcji serca skorygowane względem placebo o 4 do 6 uderzeń serca na minutę, co wskazuje na aktywność β-blokady. Ekspozycja wydawała się być mniejsza u pacjentów pediatrycznych niż u dorosłych. Po 8 miesiącach obserwacji nie stwierdzono istotnego wpływu leczenia na wyniki kliniczne. Działania niepożądane w tym badaniu, które wystąpiły u ponad 10% pacjentów leczonych COREG i dwukrotnie częściej niż w grupie placebo obejmowały ból w klatce piersiowej (17% wobec 6%), zawroty głowy (13% wobec 2%) i duszność ( 11% w porównaniu z 0%).
Zastosowanie geriatryczne
Spośród 765 pacjentów z niewydolnością serca przydzielonych losowo do grupy COREG 6,25 mg w amerykańskich badaniach klinicznych, 31% (235) było w wieku 65 lat lub starszych, a 7,3% (56) było w wieku 75 lat lub starszych. Spośród 1156 pacjentów przydzielonych losowo do grupy otrzymującej COREG 3,12 mg w długoterminowym, kontrolowanym placebo badaniu z ciężką niewydolnością serca, 47% (547) było w wieku 65 lat lub starszych, a 15% (174) było w wieku 75 lat lub starszych. Spośród 3025 osób otrzymujących COREG 6,25 mg w badaniach dotyczących niewydolności serca na całym świecie, 42% było w wieku 65 lat lub starszych.
Spośród 975 pacjentów z zawałem mięśnia sercowego przydzielonych losowo do grupy COREG w badaniu CAPRICORN, 48% (468) było w wieku 65 lat lub starszych, a 11% (111) było w wieku 75 lat lub starszych.
Spośród 2065 pacjentów z nadciśnieniem w amerykańskich badaniach klinicznych dotyczących skuteczności lub bezpieczeństwa, którzy byli leczeni COREG 25 mg, 21% (436) było w wieku 65 lat lub starszych. Spośród 3722 pacjentów otrzymujących COREG w badaniach klinicznych nadciśnienia tętniczego prowadzonych na całym świecie, 24% było w wieku 65 lat lub starszych.
wyjątkiem zawrotów głowy u osób z nadciśnieniem (częstość występowania 8,8% u osób starszych w porównaniu z 6% u osób młodszych), nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności (patrz Ryciny 2 i 4) między osobami starszymi i młodszymi u każdego z te populacje. Podobnie, inne zgłoszone doświadczenia kliniczne nie wykazały różnic w odpowiedziach między osobami starszymi i młodszymi, ale nie można wykluczyć większej wrażliwości niektórych osób starszych.
PRZEDAWKOWAĆ
Przedawkowanie może spowodować ciężkie niedociśnienie, bradykardię, niewydolność serca, wstrząs kardiogenny i zatrzymanie akcji serca. Mogą również wystąpić problemy z oddychaniem, skurcze oskrzeli, wymioty, utrata przytomności i uogólnione drgawki.
Pacjenta należy ułożyć w pozycji leżącej i, jeśli to konieczne, obserwować i leczyć w warunkach intensywnej terapii. Można podawać następujące środki:
W przypadku nadmiernej bradykardii : Atropina, 2 mg IV.
Aby wspierać funkcję sercowo-naczyniową Glukagon, 5 do 10 mg dożylnie szybko przez 30 sekund, a następnie ciągły wlew 5 mg na godzinę; sympatykomimetyki (dobutamina, izoprenalina, adrenalina) w dawkach zależnych od masy ciała i działania.
Jeśli dominuje rozszerzenie naczyń obwodowych, może być konieczne podawanie adrenaliny lub noradrenaliny z ciągłym monitorowaniem stanu krążenia. W przypadku bradykardii opornej na leczenie należy zastosować stymulator. W przypadku skurczu oskrzeli należy podać β-sympatykomimetyki (w postaci aerozolu lub IV) lub aminofilinę IV. W przypadku drgawek zaleca się powolne dożylne wstrzyknięcie diazepamu lub klonazepamu.
UWAGA: W przypadku ciężkiego zatrucia, z objawami wstrząsu, leczenie odtrutkami należy kontynuować przez wystarczająco długi czas, odpowiadający 7-10 godzinnemu okresowi półtrwania karwedylolu.
Zgłaszano przypadki przedawkowania preparatu COREG 3,12 mg w monoterapii lub w skojarzeniu z innymi lekami. W niektórych przypadkach spożyte ilości przekroczyły 1000 miligramów. Występujące objawy obejmowały niskie ciśnienie krwi i tętno. Zapewniono standardowe leczenie podtrzymujące i osoby wyzdrowiały.
PRZECIWWSKAZANIA
COREG 25mg jest przeciwwskazany w następujących stanach:
- Astma oskrzelowa lub pokrewne stany skurczowe oskrzeli. Zgony ze stanu astmatycznego zgłaszano po podaniu pojedynczych dawek COREG.
- Blok AV II lub III stopnia.
- Zespół chorej zatoki.
- Ciężka bradykardia (o ile nie ma stałego rozrusznika serca).
- Pacjenci we wstrząsie kardiogennym lub z niewyrównaną niewydolnością serca, wymagający dożylnego leczenia inotropowego. Takich pacjentów należy najpierw odstawić od terapii dożylnej przed rozpoczęciem COREG.
- Pacjenci z ciężkimi zaburzeniami czynności wątroby.
- Pacjenci z ciężką reakcją nadwrażliwości w wywiadzie (np. zespół Stevensa-Johnsona, reakcja anafilaktyczna, obrzęk naczynioruchowy) na którykolwiek składnik tego leku lub inne leki zawierające karwedylol.
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
COREG 3,12 mg jest mieszaniną racemiczną, w której nieselektywne działanie blokujące receptory β-adrenergiczne występuje w enancjomerze S(-), a aktywność blokująca receptory α1-adrenergiczne występuje w równym stopniu w enancjomerach R(+) i S(-). COREG 6,25 mg nie ma wewnętrznej aktywności sympatykomimetycznej.
Farmakodynamika
Niewydolność serca
Nie ustalono podstaw korzystnego działania COREG w niewydolności serca.
dwóch badaniach kontrolowanych placebo porównywano ostre działanie hemodynamiczne COREG z pomiarami wyjściowymi u 59 i 49 pacjentów z niewydolnością serca klasy II-IV wg NYHA, otrzymujących leki moczopędne, inhibitory ACE i naparstnicę. Wystąpiły znaczne obniżenie ogólnoustrojowego ciśnienia krwi, ciśnienia w tętnicy płucnej, ciśnienia zaklinowania w kapilarach płucnych i częstości akcji serca. Początkowy wpływ na pojemność minutową serca, wskaźnik objętości wyrzutowej i systemowy opór naczyniowy był niewielki i zmienny.
W badaniach tych ponownie mierzono efekty hemodynamiczne po 12 do 14 tygodniach. COREG w dawce 25 mg istotnie obniżył ciśnienie krwi systemowej, ciśnienie w tętnicy płucnej, ciśnienie w prawym przedsionku, systemowy opór naczyniowy i częstość akcji serca, przy jednoczesnym zwiększeniu wskaźnika objętości wyrzutowej.
Wśród 839 pacjentów z niewydolnością serca klasy II-III NYHA leczonych przez 26 do 52 tygodni w 4 amerykańskich badaniach kontrolowanych placebo, średnia frakcja wyrzutowa lewej komory (EF) mierzona za pomocą wentrykulografii z użyciem radionuklidów wzrosła o 9 jednostek EF (%) u osób otrzymujących COREG 6,25 mg i o 2 jednostki EF u pacjentów otrzymujących placebo w dawce docelowej 25 do 50 mg dwa razy dziennie. Wpływ karwedylolu na frakcję wyrzutową był związany z dawką. Dawki 6,25 mg dwa razy na dobę, 12,5 mg dwa razy na dobę i 25 mg dwa razy na dobę wiązały się ze wzrostem EF skorygowanym względem placebo odpowiednio o 5 jednostek EF, 6 jednostek EF i 8 jednostek EF; każdy z tych efektów był nominalnie istotny statystycznie.
Dysfunkcja lewej komory po zawale mięśnia sercowego
Nie ustalono podstaw korzystnego działania COREG 25 mg u pacjentów z dysfunkcją lewej komory serca po ostrym zawale mięśnia sercowego.
Nadciśnienie
Mechanizm działania β-blokady nie został poznany.
Działanie blokujące receptory β-adrenergiczne wykazano w badaniach na zwierzętach i ludziach, wykazując, że karwedylol (1) zmniejsza pojemność minutową serca u zdrowych osób, (2) zmniejsza częstoskurcz wywołany wysiłkiem fizycznym i/lub izoproterenolem oraz (3) zmniejsza odruchowy częstoskurcz ortostatyczny. Znaczące działanie blokujące receptory β-adrenergiczne obserwuje się zwykle w ciągu 1 godziny od podania leku.
Działanie blokujące receptory α1-adrenergiczne wykazano w badaniach na ludziach i zwierzętach, wykazując, że karwedilol (1) osłabia działanie presyjne fenylefryny, (2) powoduje rozszerzenie naczyń i (3) zmniejsza obwodowy opór naczyniowy. Efekty te przyczyniają się do obniżenia ciśnienia krwi i zwykle są widoczne w ciągu 30 minut od podania leku.
Ze względu na blokowanie receptorów α1 przez karwedilol, ciśnienie tętnicze jest bardziej obniżone w pozycji stojącej niż w pozycji leżącej i mogą wystąpić objawy niedociśnienia ortostatycznego (1,8%), w tym rzadkie przypadki omdleń. Po podaniu doustnym, gdy wystąpiło niedociśnienie ortostatyczne, było ono przemijające i występuje niezbyt często, gdy COREG podawany jest z pokarmem w zalecanej dawce początkowej, a zwiększanie dawki jest ściśle monitorowane [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
U pacjentów z nadciśnieniem i prawidłową czynnością nerek dawki terapeutyczne COREG zmniejszały nerkowy opór naczyniowy bez zmiany szybkości przesączania kłębuszkowego lub przepływu osocza przez nerki. Zmiany w wydalaniu sodu, potasu, kwasu moczowego i fosforu u pacjentów z nadciśnieniem i prawidłową czynnością nerek były podobne po zastosowaniu COREG i placebo.
COREG 3,12 mg ma niewielki wpływ na poziom katecholamin w osoczu, aldosteronu lub elektrolitów w osoczu, ale znacznie zmniejsza aktywność reninową osocza, gdy jest podawany przez co najmniej 4 tygodnie. Zwiększa również poziom przedsionkowego peptydu natriuretycznego.
Farmakokinetyka
COREG jest szybko i intensywnie wchłaniany po podaniu doustnym, przy bezwzględnej biodostępności wynoszącej około 25% do 35% ze względu na znaczny stopień metabolizmu pierwszego przejścia. Po podaniu doustnym pozorny średni okres półtrwania karwedylolu w końcowej fazie eliminacji wynosi na ogół od 7 do 10 godzin. Osiągane stężenia w osoczu są proporcjonalne do podanej dawki doustnej. Przy podawaniu z pokarmem szybkość wchłaniania jest spowolniona, o czym świadczy opóźnienie w osiągnięciu maksymalnego stężenia w osoczu, bez znaczącej różnicy w zakresie biodostępności. Przyjmowanie COREG z jedzeniem powinno minimalizować ryzyko hipotonii ortostatycznej.
Karwedylol jest intensywnie metabolizowany. Po podaniu doustnym znakowanego radioaktywnie karwedylolu zdrowym ochotnikom, karwedylol stanowił jedynie około 7% całkowitej radioaktywności w osoczu, mierzonej polem pod krzywą (AUC). Mniej niż 2% dawki było wydalane w postaci niezmienionej z moczem. Karwedilol jest metabolizowany głównie przez utlenianie pierścieni aromatycznych i glukuronidację.
Metabolity oksydacyjne są dalej metabolizowane przez sprzęganie poprzez glukuronidację i siarczanowanie. Metabolity karwedylolu są wydalane głównie z żółcią z kałem. Demetylacja i hydroksylacja w pierścieniu fenolowym wytwarzają 3 aktywne metabolity o działaniu blokującym receptory β. Z badań przedklinicznych wynika, że metabolit 4'-hydroksyfenylowy jest około 13 razy silniejszy niż karwedilol w blokowaniu receptorów β.
porównaniu z karwedylolem, 3 aktywne metabolity wykazują słabe działanie rozszerzające naczynia krwionośne. Stężenie aktywnych metabolitów w osoczu wynosi około jednej dziesiątej wartości obserwowanych dla karwedylolu i ma właściwości farmakokinetyczne podobne do macierzystego.
Po podaniu doustnym zdrowym osobom karwedylol podlega stereoselektywnemu metabolizmowi pierwszego przejścia, przy czym stężenie R(+)-karwedylolu w osoczu jest około 2 do 3 razy wyższe niż S(-)-karwedylolu. Średnie pozorne okresy półtrwania w końcowej fazie eliminacji dla R(+)-karwedylolu wynoszą od 5 do 9 godzin w porównaniu z 7 do 11 godzin dla enancjomeru S(-).
Głównymi enzymami P450 odpowiedzialnymi za metabolizm R(+) i S(-)-karwedylolu w mikrosomach wątroby ludzkiej były CYP2D6 i CYP2C9 oraz w mniejszym stopniu CYP3A4, 2C19, 1A2 i 2E1. Uważa się, że CYP2D6 jest głównym enzymem w 4'- i 5'-hydroksylacji karwedylolu, z potencjalnym udziałem 3A4. Uważa się, że CYP2C9 ma pierwszorzędne znaczenie w szlaku O-metylacji S(-)-karwedylolu.
Karwedilol podlega skutkom polimorfizmu genetycznego, ponieważ osoby słabo metabolizujące gruzezochinę (marker cytochromu P450 2D6) wykazują od 2 do 3 razy wyższe stężenie R(+)-karwedylolu w osoczu w porównaniu z osobami intensywnie metabolizującymi. W przeciwieństwie do tego, poziomy S(-)-karwedylolu w osoczu są podwyższone tylko o około 20% do 25% u osób słabo metabolizujących, co wskazuje, że ten enancjomer jest metabolizowany w mniejszym stopniu przez cytochrom P450 2D6 niż R(+)-karwedilol. Wydaje się, że farmakokinetyka karwedylolu nie różni się u osób słabo metabolizujących S-mefenytoinę (pacjenci z niedoborem cytochromu P450 2C19).
Karwedylol wiąże się w ponad 98% z białkami osocza, głównie z albuminą. Wiązanie z białkami osocza jest niezależne od stężenia w zakresie terapeutycznym. Karwedylol jest podstawowym, lipofilowym związkiem o objętości dystrybucji w stanie stacjonarnym około 115 l, co wskazuje na znaczną dystrybucję do tkanek pozanaczyniowych. Klirens osocza waha się od 500 do 700 ml/min.
Określone populacje
Niewydolność serca
Stężenia karwedylolu i jego enancjomerów w osoczu w stanie stacjonarnym wzrastały proporcjonalnie w zakresie dawek od 6,25 do 50 mg u pacjentów z niewydolnością serca. W porównaniu ze zdrowymi ochotnikami, u osób z niewydolnością serca średnie wartości AUC i Cmax dla karwedylolu i jego enancjomerów były wyższe, przy czym u 6 osób z niewydolnością serca IV klasy NYHA zaobserwowano nawet o 50% do 100% wyższe wartości. Średni pozorny okres półtrwania w końcowej fazie eliminacji karwedylolu był podobny do obserwowanego u zdrowych osób.
Geriatryczny
Poziomy karwedylolu w osoczu są średnio o około 50% wyższe u osób starszych w porównaniu z osobami młodymi. Zaburzenia czynności wątroby W porównaniu ze zdrowymi osobami, u pacjentów z ciężką niewydolnością wątroby (marskość) stężenie karwedylolu wzrasta od 4 do 7 razy. Karwedylol jest przeciwwskazany u pacjentów z ciężkimi zaburzeniami czynności wątroby.
Zaburzenia czynności nerek
Chociaż karwedylol jest metabolizowany głównie w wątrobie, donoszono, że stężenia karwedylolu w osoczu są zwiększone u pacjentów z zaburzeniami czynności nerek. Na podstawie średnich danych AUC, u pacjentów z nadciśnieniem i umiarkowanymi do ciężkich zaburzeniami czynności nerek obserwowano o około 40% do 50% wyższe stężenia karwedylolu w osoczu w porównaniu z grupą kontrolną pacjentów z nadciśnieniem i prawidłową czynnością nerek. Jednak zakresy wartości AUC były podobne w obu grupach. Zmiany średnich maksymalnych stężeń w osoczu były mniej wyraźne, około 12% do 26% większe u osób z zaburzeniami czynności nerek.
Ze względu na wysoki stopień wiązania białek osocza karwedylol nie wydaje się być znacząco usuwany przez hemodializę.
Interakcje między lekami
Ponieważ karwedylol podlega znacznemu metabolizmowi oksydacyjnemu, na metabolizm i farmakokinetykę karwedylolu może wpływać indukcja lub hamowanie enzymów cytochromu P450.
Amiodaron
badaniu farmakokinetycznym przeprowadzonym na 106 japońskich pacjentach z niewydolnością serca, jednoczesne podawanie małych dawek nasycających i podtrzymujących amiodaronu z karwedylolem powodowało co najmniej 2-krotne zwiększenie stężenia minimalnego S(-)-karwedylolu w stanie stacjonarnym [patrz INTERAKCJE Z LEKAMI ].
Cymetydyna
W badaniu farmakokinetycznym przeprowadzonym z udziałem 10 zdrowych mężczyzn, cymetydyna (1000 mg na dobę) zwiększała AUC karwedylolu w stanie stacjonarnym o 30% bez zmiany Cmax [patrz INTERAKCJE Z LEKAMI ].
Digoksyna
Po jednoczesnym podawaniu karwedylolu (25 mg raz na dobę) i digoksyny (0,25 mg raz na dobę) przez 14 dni, AUC w stanie stacjonarnym i minimalne stężenia digoksyny wzrosły odpowiednio o 14% i 16% u 12 pacjentów z nadciśnieniem [patrz INTERAKCJE Z LEKAMI ].
Glyburyd
U 12 zdrowych ochotników skojarzone podawanie karwedylolu (25 mg raz na dobę) i pojedynczej dawki gliburydu nie spowodowało klinicznie istotnej interakcji farmakokinetycznej dla żadnego ze związków.
Hydrochlorotiazyd
Pojedyncza doustna dawka 25 mg karwedylolu nie zmieniła farmakokinetyki pojedynczej doustnej dawki 25 mg hydrochlorotiazydu u 12 pacjentów z nadciśnieniem. Podobnie hydrochlorotiazyd nie miał wpływu na farmakokinetykę karwedylolu.
ryfampicyna
W badaniu farmakokinetycznym przeprowadzonym na 8 zdrowych mężczyznach ryfampicyna (600 mg na dobę przez 12 dni) zmniejszyła AUC i Cmax karwedylolu o około 70% [patrz INTERAKCJE Z LEKAMI ].
Torsemid
W badaniu z udziałem 12 zdrowych osób, skojarzone doustne podawanie karwedylolu 25 mg raz na dobę i torsemidu 5 mg raz na dobę przez 5 dni nie spowodowało żadnych istotnych różnic w ich farmakokinetyce w porównaniu z podawaniem samych leków.
Warfaryna
Karwedylol (12,5 mg dwa razy na dobę) nie miał wpływu na wskaźniki czasu protrombinowego w stanie stacjonarnym i nie zmieniał farmakokinetyki R(+)- i S(-)-warfaryny po jednoczesnym podaniu z warfaryną u 9 zdrowych ochotników.
Studia kliniczne
Niewydolność serca
Łącznie 6975 pacjentów z łagodną do ciężkiej niewydolnością serca oceniano w kontrolowanych placebo badaniach karwedylolu.
Łagodna do umiarkowanej niewydolność serca
Karwedylol badano w 5 wieloośrodkowych badaniach kontrolowanych placebo oraz w 1 badaniu z aktywną kontrolą (badanie COMET) z udziałem pacjentów z łagodną lub umiarkowaną niewydolnością serca.
czterech wieloośrodkowych badaniach z podwójnie ślepą próbą, kontrolowanych placebo w Stanach Zjednoczonych wzięło udział 1094 pacjentów (696 przydzielonych losowo do grupy leczonej karwedylolem) z niewydolnością serca klasy II-III wg NYHA i frakcją wyrzutową mniejszą lub równą 0,35. Zdecydowana większość przyjmowała naparstnicę, leki moczopędne i inhibitor ACE w momencie rozpoczęcia badania. Pacjenci zostali przydzieleni do badań na podstawie zdolności wysiłkowych. W australijsko-nowozelandzkim badaniu kontrolowanym placebo z podwójnie ślepą próbą wzięło udział 415 pacjentów (w połowie przydzielonych losowo do karwedylolu) z mniej ciężką niewydolnością serca. Wszystkie protokoły wykluczały pacjentów, u których spodziewano się przeszczepu serca podczas 7,5 do 15 miesięcy obserwacji z podwójnie ślepą próbą. Wszyscy zrandomizowani pacjenci tolerowali dwutygodniowy kurs karwedylolu 6,25 mg dwa razy na dobę.
każdym badaniu występował pierwszorzędowy punkt końcowy, albo progresja niewydolności serca (1 badanie w USA) albo tolerancja wysiłku (2 badania w USA spełniające cele rekrutacyjne i badanie Australia-Nowa Zelandia). W badaniach tych określono wiele drugorzędowych punktów końcowych, w tym klasyfikację NYHA, ogólną ocenę pacjenta i lekarza oraz hospitalizację z przyczyn sercowo-naczyniowych. Inne analizy, które nie były planowane prospektywnie, obejmowały sumę zgonów i łącznej liczby hospitalizacji z przyczyn sercowo-naczyniowych. W sytuacjach, w których pierwszorzędowe punkty końcowe badania nie wykazują znaczącej korzyści z leczenia, przypisanie wartości istotności do innych wyników jest złożone i takie wartości należy interpretować ostrożnie.
Wyniki prób w USA i Australii i Nowej Zelandii były następujące:
Spowolnienie postępu niewydolności serca
Jedno z wieloośrodkowych badań w USA (366 uczestników) miało jako główny punkt końcowy sumę śmiertelności z przyczyn sercowo-naczyniowych, hospitalizacji z przyczyn sercowo-naczyniowych i utrzymującego się wzrostu liczby leków na niewydolność serca. Progresja niewydolności serca zmniejszyła się w okresie obserwacji trwającej średnio 7 miesięcy o 48% (p = 0,008).
W badaniu australijsko-nowozelandzkim śmiertelność i całkowita liczba hospitalizacji zmniejszyła się o około 25% w okresie od 18 do 24 miesięcy. W 3 największych badaniach w USA śmiertelność i całkowita liczba hospitalizacji zmniejszyły się o 19%, 39% i 49%, przy czym w ostatnich 2 badaniach statystycznie znamienne. Wyniki dla Australii i Nowej Zelandii były statystycznie na pograniczu.
Środki funkcjonalne
Żadne z wieloośrodkowych badań nie miało klasyfikacji NYHA jako pierwszorzędowego punktu końcowego, ale wszystkie takie badania miały ją jako drugorzędowy punkt końcowy. We wszystkich badaniach zaobserwowano przynajmniej tendencję do poprawy w klasie NYHA. Tolerancja wysiłku była głównym punktem końcowym w 3 próbach; w żadnym nie stwierdzono statystycznie istotnego efektu.
Miary subiektywne
Karwedilol nie wpływał na jakość życia związaną ze zdrowiem, mierzoną standardowym kwestionariuszem (pierwszorzędowy punkt końcowy w 1 badaniu). Jednak globalne oceny pacjentów i badaczy wykazały znaczną poprawę w większości badań.
Śmiertelność
Śmierć nie była z góry określonym punktem końcowym w żadnej próbie, ale była analizowana we wszystkich próbach. Ogółem w tych 4 badaniach w USA śmiertelność była zmniejszona, nominalnie istotnie, podobnie jak w 2 badaniach.
Próba KOMET
tym badaniu z podwójnie ślepą próbą 3029 pacjentów z niewydolnością serca klasy II-IV wg NYHA (frakcja wyrzutowa lewej komory mniejsza lub równa 35%) przydzielono losowo do grupy otrzymującej karwedilol (dawka docelowa: 25 mg dwa razy na dobę) lub metoprolol o natychmiastowym uwalnianiu. winian (dawka docelowa: 50 mg dwa razy na dobę). Średni wiek badanych wynosił około 62 lata, 80% stanowili mężczyźni, a średnia frakcja wyrzutowa lewej komory na początku badania wynosiła 26%. Około 96% badanych miało niewydolność serca w II lub III klasie wg NYHA. Jednoczesne leczenie obejmowało leki moczopędne (99%), inhibitory ACE (91%), naparstnicę (59%), antagoniści aldosteronu (11%) oraz „statyny” obniżające poziom lipidów (21%). Średni czas obserwacji wyniósł 4,8 roku. Średnia dawka karwedylolu wynosiła 42 mg na dobę.
Badanie miało 2 pierwszorzędowe punkty końcowe: śmiertelność z jakiejkolwiek przyczyny oraz połączenie zgonu i hospitalizacji z dowolnego powodu. Wyniki COMET przedstawiono w tabeli 3 poniżej. Śmiertelność z jakiejkolwiek przyczyny miała większość wagi statystycznej i była głównym wyznacznikiem wielkości próby. Śmiertelność ogólna wyniosła 34% u osób leczonych karwedylolem i 40% w grupie metoprololu o natychmiastowym uwalnianiu (p = 0,0017; współczynnik ryzyka = 0,83, 95% CI: 0,74 do 0,93). Wpływ na śmiertelność wynikał przede wszystkim ze zmniejszenia zgonów z przyczyn sercowo-naczyniowych. Różnica między dwiema grupami w odniesieniu do złożonego punktu końcowego nie była istotna (p = 0,122). Szacowane średnie przeżycie wynosiło 8,0 lat dla karwedylolu i 6,6 lat dla metoprololu o natychmiastowym uwalnianiu.
Nie wiadomo, czy ta postać metoprololu w dowolnej dawce lub ta niska dawka metoprololu w jakiejkolwiek postaci ma jakikolwiek wpływ na przeżycie lub hospitalizację pacjentów z niewydolnością serca. Zatem badanie to wydłuża czas, w którym karwedilol wykazuje korzyści w zakresie przeżycia w niewydolności serca, ale nie jest dowodem, że karwedilol poprawia rokowanie w porównaniu z preparatem metoprololu (TOPROL-XL) z korzyścią w niewydolności serca.
Ciężka niewydolność serca (KOPERNIK)
badaniu COPERNICUS z podwójnie ślepą próbą 2289 osób z niewydolnością serca w spoczynku lub z minimalnym wysiłkiem i frakcją wyrzutową lewej komory mniejszą niż 25% (średnio 20%), pomimo naparstnicy (66%), leków moczopędnych (99%) i Inhibitory ACE (89%) przydzielono losowo do grupy placebo lub karwedylolu. Karwedylol miareczkowano od dawki początkowej 3,125 mg dwa razy na dobę do maksymalnej tolerowanej dawki lub do 25 mg dwa razy na dobę przez co najmniej 6 tygodni. Większość badanych osiągnęła docelową dawkę 25 mg. Badanie przeprowadzono w Europie Wschodniej i Zachodniej, Stanach Zjednoczonych, Izraelu i Kanadzie. Podobna liczba pacjentów w grupie (około 100) wycofała się w okresie miareczkowania.
Pierwszorzędowym punktem końcowym badania była śmiertelność ogólna, ale zbadano również śmiertelność przyczynową oraz ryzyko zgonu lub hospitalizacji (całkowita, sercowo-naczyniowa [CV] lub niewydolność serca [HF]). Opracowujące dane z badań były śledzone przez komitet monitorujący dane, a analizy śmiertelności zostały dostosowane do tych wielu spojrzeń. Badanie zostało przerwane po medianie obserwacji wynoszącej 10 miesięcy z powodu obserwowanego 35% zmniejszenia śmiertelności (z 19,7% na pacjentorok w grupie placebo do 12,8% w grupie karwedylolu; współczynnik ryzyka 0,65, 95% CI: 0,52 do 0,81, P = 0,0014, skorygowane) (patrz Rysunek 1). Wyniki programu COPERNICUS przedstawiono w tabeli 4.
Rycina 1. Analiza przeżycia dla programu COPERNICUS (intent-to-treat) 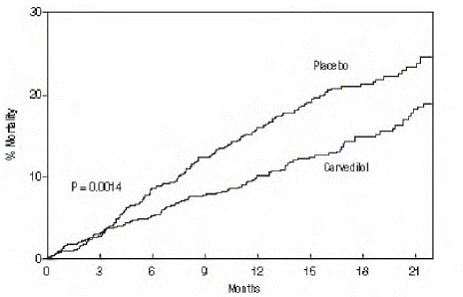
Wpływ na śmiertelność był głównie wynikiem zmniejszenia częstości nagłych zgonów wśród badanych bez pogorszenia niewydolności serca.
Ogólne oceny pacjentów, w których pacjentów leczonych karwedylolem porównywano z placebo, opierały się na wcześniej określonych, okresowych samoocenach pacjentów dotyczących tego, czy stan kliniczny po leczeniu wykazywał poprawę, pogorszenie lub brak zmian w porównaniu z wartościami wyjściowymi. Osoby leczone karwedylolem wykazały znaczną poprawę w ogólnych ocenach w porównaniu z osobami, którym podawano placebo w badaniu COPERNICUS.
W protokole określono również, że będą oceniane hospitalizacje. Mniej pacjentów otrzymujących 6,25 mg COREG niż otrzymujących placebo było hospitalizowanych z jakiegokolwiek powodu (372 wobec 432, p = 0,0029), z przyczyn sercowo-naczyniowych (246 wobec 314, p = 0,0003) lub z powodu nasilenia niewydolności serca (198 wobec 268, p = 0,0001). ).
COREG 6,25 mg miał stały i korzystny wpływ na śmiertelność z jakiejkolwiek przyczyny, jak również na łączne punkty końcowe śmiertelności z jakiejkolwiek przyczyny i hospitalizacji (całkowita, CV lub z powodu niewydolności serca) w ogólnej populacji badania i we wszystkich przebadanych podgrupach, w tym mężczyźni i kobiety, osoby starsze i inne niż w podeszłym wieku, osoby czarne i inne niż czarne oraz chorzy na cukrzycę i osoby bez cukrzycy (zob. ryc. 2).
Rysunek 2. Wpływ na śmiertelność podgrup w programie COPERNICUS 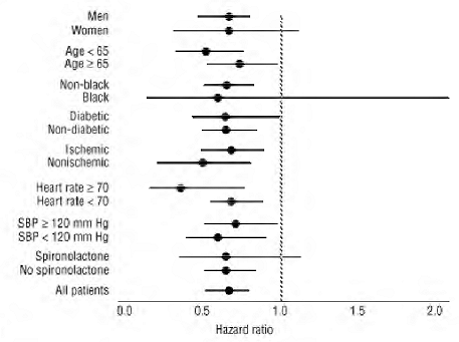
Dysfunkcja lewej komory po zawale mięśnia sercowego
CAPRICORN było badaniem z podwójnie ślepą próbą porównującym karwedilol i placebo u 1959 pacjentów z niedawno przebytym zawałem mięśnia sercowego (w ciągu 21 dni) i frakcją wyrzutową lewej komory mniejszą lub równą 40%, z (47%) lub bez objawów niewydolności serca. Osoby, którym podawano karwedilol, otrzymywały 6,25 mg dwa razy dziennie, miareczkowane jako tolerowane do 25 mg dwa razy dziennie. Badani musieli mieć skurczowe ciśnienie krwi większe niż 90 mm Hg, tętno w pozycji siedzącej większe niż 60 uderzeń na minutę i brak przeciwwskazań do stosowania β-blokerów. Leczenie zawału indeksowego obejmowało aspirynę (85%), β-adrenolityki dożylne lub doustne (37%), azotany (73%), heparynę (64%), trombolityki (40%) i ostrą angioplastykę (12%). Leczenie podstawowe obejmowało inhibitory ACE lub blokery receptora angiotensyny (97%), antykoagulanty (20%), leki hipolipemizujące (23%) i diuretyki (34%). Wyjściowa charakterystyka populacji obejmowała średni wiek 63 lata, 74% mężczyzn, 95% rasy białej, średnie ciśnienie krwi 121/74 mm Hg, 22% z cukrzycą i 54% z nadciśnieniem w wywiadzie. Średnia osiągnięta dawka karwedylolu wynosiła 20 mg dwa razy na dobę; średni czas obserwacji wynosił 15 miesięcy.
Śmiertelność ogólna wyniosła 15% w grupie placebo i 12% w grupie karwedylolu, co wskazuje na 23% zmniejszenie ryzyka u pacjentów leczonych karwedylolem (95% CI: 2% do 40%, p = 0,03), jak pokazano na rycinie 3. Wpływ na śmiertelność w różnych podgrupach przedstawiono na rycinie 4. Prawie wszystkie zgony dotyczyły układu sercowo-naczyniowego (które zostały zmniejszone o 25% przez karwedilol), a większość tych zgonów była nagła lub związana z awarią pompy (oba rodzaje zgonów uległy zmniejszeniu przez karwedilol). Inny punkt końcowy badania, całkowita śmiertelność i hospitalizacja z jakiejkolwiek przyczyny, nie wykazały znaczącej poprawy.
W grupie leczonej karwedylolem zaobserwowano również istotne 40% zmniejszenie częstości występowania zawału mięśnia sercowego zakończonego zgonem lub niezakończonego zgonem (95% CI: 11% do 60%, p = 0,01). Podobne zmniejszenie ryzyka zawału mięśnia sercowego zaobserwowano również w metaanalizie kontrolowanych placebo badań klinicznych karwedylolu w niewydolności serca.
Rycina 3. Analiza przeżycia dla CAPRICORN (intent-to-treat) 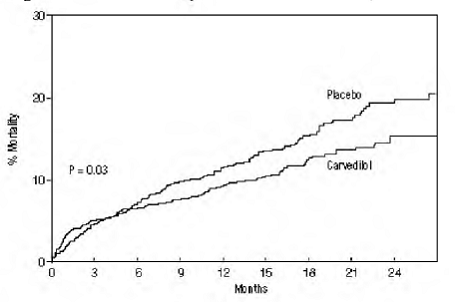
Rysunek 4. Wpływ na śmiertelność w podgrupach w CAPRICORN 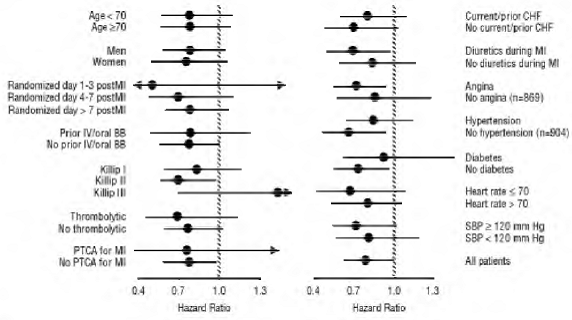
Nadciśnienie
COREG 25 mg badano w 2 badaniach kontrolowanych placebo, w których stosowano dawkowanie dwa razy na dobę w całkowitych dawkach dobowych od 12,5 do 50 mg. W tych i innych badaniach dawka początkowa nie przekraczała 12,5 mg. Przy dawce 50 mg na dobę COREG obniżał ciśnienie krwi w pozycji siedzącej (12-godzinnej) o około 9/5,5 mm Hg; przy 25 mg dziennie efekt wynosił około 7,5/3,5 mm Hg. Porównania dolnego do szczytowego ciśnienia krwi wykazały stosunek dołka do szczytu dla odpowiedzi ciśnienia krwi około 65%. Tętno spadło o około 7,5 uderzeń na minutę przy 50 mg dziennie. Ogólnie, podobnie jak w przypadku innych beta-adrenolityków, odpowiedzi były mniejsze u osób rasy czarnej niż u osób innych ras. W odpowiedzi nie było różnic związanych z wiekiem lub płcią.
Szczytowe działanie przeciwnadciśnieniowe wystąpiło 1 do 2 godzin po podaniu dawki. Zależnej od dawki odpowiedzi na ciśnienie krwi towarzyszyło zależne od dawki zwiększenie działań niepożądanych [patrz DZIAŁANIA NIEPOŻĄDANE ].
Nadciśnienie z cukrzycą typu 2
badaniu z podwójnie ślepą próbą (GEMINI) oceniano COREG 25 mg w połączeniu z inhibitorem ACE lub blokerem receptora angiotensyny w populacji z łagodnym do umiarkowanego nadciśnieniem i dobrze kontrolowaną cukrzycą typu 2. Średnia wyjściowa HbA1c wynosiła 7,2%. COREG miareczkowano do średniej dawki 17,5 mg dwa razy na dobę i utrzymywano przez 5 miesięcy. COREG nie miał niekorzystnego wpływu na kontrolę glikemii, na podstawie pomiarów HbA1c (średnia zmiana od wartości wyjściowej 0,02%, 95% CI: -0,06 do 0,10, P = NS) [patrz OSTRZEŻENIA I ŚRODKI ].
INFORMACJA O PACJENCIE
COREG (Co-REG) (karwedilol) Tabletki
Przeczytaj informacje dla pacjenta dołączone do produktu COREG, zanim zaczniesz go zażywać i za każdym razem, gdy otrzymasz uzupełnienie. Mogą pojawić się nowe informacje. Ta informacja nie zastępuje rozmowy z lekarzem na temat swojego stanu zdrowia lub leczenia. W przypadku jakichkolwiek pytań dotyczących leku COREG 3,12 mg należy zwrócić się do lekarza lub farmaceuty.
Co to jest COREG 3,12 mg?
COREG to lek na receptę należący do grupy leków zwanych „beta-blokerami”. COREG 6,25 mg jest stosowany, często z innymi lekami, w następujących stanach:
- w leczeniu pacjentów z niektórymi rodzajami niewydolności serca
- w leczeniu pacjentów po zawale serca, który pogorszył pompowanie serca
- w leczeniu pacjentów z wysokim ciśnieniem krwi (nadciśnieniem)
COREG nie jest dopuszczony do stosowania u dzieci poniżej 18 roku życia.
Kto nie powinien brać COREG?
Nie należy przyjmować leku COREG 6,25 mg, jeśli:
- mają ciężką niewydolność serca i są hospitalizowani na oddziale intensywnej terapii lub wymagają pewnych leków dożylnych, które wspomagają krążenie (leki inotropowe).
- mają skłonność do astmy lub innych problemów z oddychaniem.
- mieć wolne bicie serca lub serce przerywające bicie (nieregularne bicie serca).
- masz problemy z wątrobą.
- jesteś uczulony na którykolwiek ze składników preparatu COREG. Substancją czynną jest karwedylol. Na końcu tej ulotki znajduje się lista wszystkich składników COREG.
czym powinienem powiedzieć lekarzowi przed przyjęciem COREG?
Poinformuj swojego lekarza o wszystkich swoich schorzeniach, w tym jeśli:
- masz astmę lub inne problemy z płucami (takie jak zapalenie oskrzeli lub rozedma płuc).
- mieć problemy z przepływem krwi w stopach i nogach (choroba naczyń obwodowych). COREG 3,12 mg może pogorszyć niektóre objawy.
- mieć cukrzycę.
- masz problemy z tarczycą.
- mają stan zwany guzem chromochłonnym.
- miał ciężkie reakcje alergiczne.
- jesteś w ciąży lub próbuje zajść w ciążę. Nie wiadomo, czy COREG jest bezpieczny dla nienarodzonego dziecka. Ty i Twój lekarz powinniście porozmawiać o najlepszym sposobie kontrolowania wysokiego ciśnienia krwi podczas ciąży.
- karmią piersią. Nie wiadomo, czy COREG przenika do mleka matki. Porozmawiaj z lekarzem o najlepszym sposobie karmienia dziecka, jeśli przyjmujesz COREG.
- są zaplanowani na operację i otrzymają środki znieczulające.
- są zaplanowani do operacji zaćmy i przyjęli lub obecnie przyjmują COREG.
- przyjmujesz leki na receptę lub bez recepty, witaminy i suplementy ziołowe. COREG i niektóre inne leki mogą wzajemnie na siebie wpływać i powodować poważne działania niepożądane. COREG 3,12 mg może wpływać na działanie innych leków. Również inne leki mogą wpływać na skuteczność działania leku COREG 25 mg.
Zachowaj listę wszystkich przyjmowanych leków. Pokaż tę listę swojemu lekarzowi i farmaceucie przed rozpoczęciem przyjmowania nowego leku.
Jak powinienem przyjmować COREG?
Ważne jest, aby lek przyjmować codziennie, zgodnie z zaleceniami lekarza. Nagłe przerwanie stosowania leku COREG może spowodować ból w klatce piersiowej i (lub) zawał serca. Jeśli lekarz zdecyduje, że należy przerwać przyjmowanie leku COREG 6,25 mg, może powoli zmniejszać dawkę przez pewien czas, zanim całkowicie zaprzestanie leczenia.
- Weź COREG dokładnie zgodnie z zaleceniami. Lekarz poinformuje, ile tabletek należy przyjmować i jak często. Aby zminimalizować możliwe działania niepożądane, lekarz może rozpocząć od małej dawki, a następnie powoli ją zwiększać.
- Nie należy przerywać stosowania leku COREG ani zmieniać ilości przyjmowanego leku COREG bez konsultacji z lekarzem.
- Należy poinformować lekarza, jeśli podczas stosowania leku COREG przytyje się lub ma problemy z oddychaniem.
- Weź COREG z jedzeniem.
- W przypadku pominięcia dawki leku COREG 3,12 mg, należy ją przyjąć, gdy tylko sobie o tym przypomni, chyba że nadszedł czas przyjęcia kolejnej dawki. Następną dawkę należy przyjąć o zwykłej porze. Nie należy przyjmować 2 dawek jednocześnie.
- Jeśli zażyjesz za dużo COREG 25mg, natychmiast skontaktuj się z lekarzem lub ośrodkiem kontroli zatruć.
Czego powinienem unikać podczas przyjmowania COREG 3,12 mg?
- COREG może powodować zawroty głowy, zmęczenie lub omdlenia. Nie prowadź samochodu, nie używaj maszyn ani nie rób niczego, co wymaga czujności, jeśli masz te objawy.
Jakie są możliwe skutki uboczne COREG?
- Niskie ciśnienie krwi (które może powodować zawroty głowy lub omdlenia podczas wstawania). Jeśli tak się stanie, natychmiast usiądź lub połóż się i powiedz o tym swojemu lekarzowi.
- Zmęczenie. Jeśli czujesz się zmęczony lub masz zawroty głowy, nie powinieneś prowadzić pojazdów, obsługiwać maszyn ani robić niczego, co wymaga czujności.
- Wolne bicie serca.
- Zmiany poziomu cukru we krwi. Jeśli masz cukrzycę, poinformuj lekarza o jakichkolwiek zmianach poziomu cukru we krwi.
- COREG może ukrywać niektóre objawy niskiego poziomu cukru we krwi, zwłaszcza szybkie bicie serca.
- COREG może maskować objawy nadczynności tarczycy (nadczynność tarczycy).
- Pogorszenie ciężkich reakcji alergicznych.
- U pacjentów przyjmujących COREG występowały rzadkie, ale poważne reakcje alergiczne (w tym pokrzywka lub obrzęk twarzy, warg, języka i (lub) gardła, które mogą powodować trudności w oddychaniu lub połykaniu). Te reakcje mogą zagrażać życiu.
Inne skutki uboczne COREG to duszność, przyrost masy ciała, biegunka i mniej łez lub suchych oczu, które stają się uciążliwe, jeśli nosisz soczewki kontaktowe.
Zadzwoń do lekarza, jeśli masz jakiekolwiek objawy niepożądane, które Cię niepokoją lub nie odchodzą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA1088.
Jak przechowywać COREG 6,25 mg?
- Przechowywać COREG w temperaturze poniżej 86 ° F (30 ° C). Utrzymuj tabletki w stanie suchym.
- Bezpiecznie wyrzuć COREG, który jest nieaktualny lub nie jest już potrzebny.
- Lek COREG 6,25 mg i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Ogólne informacje o COREG
Czasami przepisuje się leki na inne schorzenia niż te opisane w ulotkach informacyjnych dla pacjentów. Nie należy stosować leku COREG 3,12 mg w przypadku schorzenia, na które nie został przepisany. Nie należy podawać leku COREG innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić.
Niniejsza ulotka podsumowuje najważniejsze informacje o COREG. Jeśli chcesz uzyskać więcej informacji, porozmawiaj ze swoim lekarzem. Możesz poprosić swojego lekarza lub farmaceutę o informacje na temat leku COREG 6,25 mg przeznaczonego dla pracowników służby zdrowia.
Jakie są składniki COREG?
Składnik aktywny: karwedilol.
Składniki nieaktywne: koloidalny dwutlenek krzemu, krospowidon, hypromeloza, laktoza, stearynian magnezu, glikol polietylenowy, polisorbat 80, powidon, sacharoza i dwutlenek tytanu.
Tabletki karwedylolu są dostępne w następujących mocach: 3,125 mg, 6,25 mg, 12,5 mg, 25 mg.
Co to jest wysokie ciśnienie krwi (nadciśnienie)?
Ciśnienie krwi to siła krwi w naczyniach krwionośnych, kiedy serce bije i kiedy serce odpoczywa. Masz wysokie ciśnienie krwi, gdy siła jest zbyt duża. Wysokie ciśnienie krwi sprawia, że serce pracuje ciężej, pompując krew przez organizm i powoduje uszkodzenie naczyń krwionośnych. COREG może pomóc w rozluźnieniu naczyń krwionośnych, dzięki czemu ciśnienie krwi jest niższe. Leki obniżające ciśnienie krwi mogą zmniejszać ryzyko udaru lub zawału serca.
