Effexor 37.5mg, 75mg Venlafaxine Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
INFORMACJA O PACJENCIE
Effexor (wenlafaksyna) (ven-la-fax-een) Tabletki, USP
Przeczytaj Przewodnik po lekach, który jest dostarczany z tabletkami wenlafaksyny, USP, zanim zaczniesz je zażywać i za każdym razem, gdy otrzymasz uzupełnienie. Mogą pojawić się nowe informacje. Ten przewodnik po lekach nie zastępuje rozmowy z lekarzem o stanie zdrowia lub leczeniu. Porozmawiaj ze swoim lekarzem, jeśli jest coś, czego nie rozumiesz lub chcesz dowiedzieć się więcej.
Jakie są najważniejsze informacje, które powinienem wiedzieć na temat tabletek wenlafaksyny, USP?
Tabletki wenlafaksyny, USP i inne leki przeciwdepresyjne mogą powodować poważne działania niepożądane, w tym:
1. Myśli lub działania samobójcze:
- Tabletki wenlafaksyny, USP i inne leki przeciwdepresyjne mogą nasilać myśli lub działania samobójcze u niektórych dzieci, nastolatków lub młodych dorosłych w ciągu pierwszych kilku miesięcy leczenia lub po zmianie dawki.
- Depresja lub inne poważne choroby psychiczne są najważniejszymi przyczynami myśli lub działań samobójczych.
- Zwróć uwagę na te zmiany i natychmiast skontaktuj się z lekarzem, jeśli zauważysz:
- Nowe lub nagłe zmiany nastroju, zachowania, działań, myśli lub uczuć, zwłaszcza jeśli są poważne.
- Należy zwrócić szczególną uwagę na takie zmiany w przypadku rozpoczęcia stosowania tabletek wenlafaksyny, USP lub zmiany dawki.
Zachowaj wszystkie wizyty kontrolne u swojego lekarza i dzwoń między wizytami, jeśli obawiasz się objawów.
Zadzwoń do swojego lekarza natychmiast, jeśli masz którykolwiek z poniższych objawów, lub zadzwoń pod numer 911 w nagłych wypadkach, zwłaszcza jeśli są nowe, gorsze lub martwią Cię:
- próby popełnienia samobójstwa
- działając na niebezpieczne impulsy
- zachowywanie się agresywnie lub agresywnie
- myśli o samobójstwie lub śmierci
- nowa lub gorsza depresja
- nowy lub gorszy lęk lub ataki paniki
- uczucie pobudzenia, niepokoju, złości lub poirytowania
- problemy ze snem
- wzrost aktywności lub mówienie więcej niż to, co jest dla Ciebie normalne
- inne nietypowe zmiany w zachowaniu lub nastroju
Zadzwoń do swojego lekarza natychmiast, jeśli wystąpi którykolwiek z poniższych objawów, lub zadzwoń pod numer 911 w nagłych wypadkach. Tabletki wenlafaksyny, USP mogą być związane z następującymi poważnymi skutkami ubocznymi:
2. Zespół serotoninowy
Ten stan może zagrażać życiu i może obejmować:
- pobudzenie, halucynacje, śpiączka lub inne zmiany stanu psychicznego
- problemy z koordynacją lub drgania mięśni (nadmierne odruchy)
- przyspieszone bicie serca, wysokie lub niskie ciśnienie krwi
- pocenie się lub gorączka
- nudności, wymioty lub biegunka
- sztywność mięśni
3. Zmiany ciśnienia krwi. Tabletki wenlafaksyny, USP mogą:
- zwiększyć ciśnienie krwi. Kontroluj wysokie ciśnienie krwi przed rozpoczęciem leczenia i regularnie monitoruj ciśnienie krwi
4. Powiększone źrenice (rozszerzenie źrenic).
5. Lęk i bezsenność.
6. Zmiany apetytu lub wagi.
- podczas leczenia dzieci i młodzież należy monitorować wzrost i wagę
7. Epizody maniakalne/hipomaniczne:
- znacznie zwiększona energia
- poważne problemy ze snem
- wyścigi myśli
- lekkomyślne zachowanie
- niezwykle wielkie pomysły
- nadmierne szczęście lub drażliwość
- mówisz więcej lub szybciej niż zwykle
8. Niski poziom soli (sodu) we krwi.
Osoby starsze mogą być na to bardziej narażone. Objawy mogą obejmować:
- ból głowy
- słabość lub niepewność
- splątanie, problemy z koncentracją, myślenie lub problemy z pamięcią
9. Drgawki lub konwulsje.
10. Nieprawidłowe krwawienie: tabletki wenlafaksyny, USP i inne leki przeciwdepresyjne mogą zwiększać ryzyko krwawienia lub siniaków, zwłaszcza jeśli przyjmujesz warfarynę rozrzedzającą krew (Coumadin®, Jantoven®), niesteroidowy lek przeciwzapalny (NLPZ, np. ibuprofen lub naproksen) lub aspiryna.
11. Podwyższony poziom cholesterolu.
12. Choroba płuc i zapalenie płuc: tabletki wenlafaksyny, USP mogą powodować rzadkie problemy z płucami. Objawy obejmują:
- nasilająca się duszność
- kaszel
- dyskomfort w klatce piersiowej
13. Ciężkie reakcje alergiczne:
- problemy z oddychaniem
- obrzęk twarzy, języka, oczu lub ust
- wysypka, swędzące pręgi (pokrzywka) lub pęcherze, samodzielnie lub z gorączką lub bólem stawów
14. Problemy wizualne:
- ból oka
- zmiany w wizji
- obrzęk lub zaczerwienienie w oku lub wokół niego
Tylko niektórzy ludzie są narażeni na te problemy. Możesz chcieć przejść badanie wzroku, aby sprawdzić, czy jesteś zagrożony i otrzymać leczenie zapobiegawcze, jeśli tak.
Nie należy przerywać stosowania leku Venlafaxine Tablets, USP bez uprzedniej konsultacji z lekarzem. Zbyt szybkie odstawienie tabletek wenlafaksyny, USP lub zbyt szybka zmiana z innego leku przeciwdepresyjnego może spowodować poważne objawy, w tym:
- niepokój, drażliwość
- uczucie zmęczenia, niepokoju lub problemy ze snem
- ból głowy, pocenie się, zawroty głowy
- odczucia podobne do porażenia prądem, drżenie, dezorientacja, koszmary senne
- wymioty, nudności, biegunka
Co to są tabletki wenlafaksyny, USP?
Tabletki Venlafaxine, USP to lek na receptę stosowany w leczeniu depresji. Ważne jest, aby porozmawiać z lekarzem o ryzyku związanym z leczeniem depresji, a także o ryzyku nieleczenia jej. Powinieneś omówić wszystkie opcje leczenia z lekarzem.
Porozmawiaj ze swoim lekarzem, jeśli uważasz, że twój stan nie poprawia się dzięki tabletkom wenlafaksyny, leczeniu USP.
Kto nie powinien przyjmować tabletek wenlafaksyny, USP?
- Nie należy przyjmować tabletek wenlafaksyny, USP, jeśli:
- jesteś uczulony na tabletki wenlafaksyny, USP lub którykolwiek ze składników tabletek wenlafaksyny, USP. Pełna lista składników tabletek wenlafaksyny znajduje się na końcu niniejszego Przewodnika po lekach, USP.
- mieć niekontrolowaną jaskrę z wąskim kątem;
- weź inhibitor monoaminooksydazy (MAOI). Zapytaj swojego lekarza lub farmaceutę, jeśli nie jesteś pewien, czy przyjmujesz IMAO, w tym antybiotyk linezolid.
- Nie należy przyjmować IMAO w ciągu 7 dni od odstawienia tabletek wenlafaksyny, USP, chyba że zaleci to lekarz.
- Nie należy rozpoczynać przyjmowania tabletek wenlafaksyny, USP, jeśli zaprzestano przyjmowania MAOI w ciągu ostatnich 2 tygodni, chyba że zaleci to lekarz.
Osoby, które przyjmują tabletki wenlafaksyny, USP zbliżają się w czasie do MAOI, mogą mieć poważne, a nawet zagrażające życiu skutki uboczne. Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z tych objawów:
- wysoka gorączka
- niekontrolowane skurcze mięśni
- sztywne mięśnie
- gwałtowne zmiany częstości akcji serca lub ciśnienia krwi
- dezorientacja
- utrata przytomności (omdlenie)
czym powinienem powiedzieć lekarzowi przed zażyciem tabletek wenlafaksyny, USP? Zapytaj, jeśli nie jesteś pewien.
Przed rozpoczęciem przyjmowania tabletek wenlafaksyny, USP, poinformuj swojego lekarza, jeśli:
- Przyjmują niektóre leki, takie jak:
- Leki stosowane w leczeniu migrenowych bólów głowy, takie jak:
- tryptany
- Leki stosowane w leczeniu zaburzeń nastroju, lęku, psychozy lub zaburzeń myślenia, takie jak:
- trójpierścieniowe leki przeciwdepresyjne
- lit
- SSRI
- SNRI
- leki przeciwpsychotyczne
- Leki stosowane w leczeniu bólu, takie jak:
- tramadol
- Leki stosowane w celu rozrzedzenia krwi, takie jak:
- warfaryna
- Leki stosowane w leczeniu zgagi, takie jak:
- Cymetydyna
- Leki lub suplementy dostępne bez recepty, takie jak:
- Aspiryna lub inne NLPZ
- Tryptofan
- ziele dziurawca zwyczajnego
- masz problemy z sercem
- mieć cukrzycę
- masz problemy z wątrobą
- masz problemy z nerkami
- masz problemy z tarczycą
- mieć jaskrę?
- masz lub miałeś drgawki lub konwulsje
- masz chorobę afektywną dwubiegunową lub manię
- masz niski poziom sodu we krwi
- mieć wysokie ciśnienie krwi
- mieć wysoki poziom cholesterolu
- masz lub miałeś problemy z krwawieniem
- są w ciąży lub planują zajść w ciążę. Nie wiadomo, czy tabletki wenlafaksyny, USP zaszkodzą nienarodzonemu dziecku. Porozmawiaj ze swoim lekarzem o korzyściach i zagrożeniach związanych z leczeniem depresji podczas ciąży
- karmisz piersią lub planujesz karmić piersią. Niektóre tabletki wenlafaksyny, USP, mogą przenikać do mleka matki. Porozmawiaj ze swoim lekarzem o najlepszym sposobie karmienia dziecka podczas przyjmowania tabletek wenlafaksyny, USP.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym o lekach na receptę i bez recepty, witaminach i suplementach ziołowych. Tabletki wenlafaksyny, USP i niektóre leki mogą wchodzić ze sobą w interakcje, mogą nie działać tak dobrze lub mogą powodować poważne działania niepożądane.
Twój lekarz lub farmaceuta może powiedzieć Ci, czy można bezpiecznie przyjmować tabletki wenlafaksyny, USP z innymi lekami. Nie należy rozpoczynać ani przerywać przyjmowania jakichkolwiek leków podczas przyjmowania tabletek wenlafaksyny, USP bez uprzedniej konsultacji z lekarzem.
Jeśli pacjent przyjmuje tabletki wenlafaksyny, USP, nie powinien przyjmować żadnych innych leków zawierających (wenlafaksynę), w tym: chlorowodorek wenlafaksyny.
Jak powinienem przyjmować tabletki wenlafaksyny, USP?
- Weź tabletki wenlafaksyny, USP dokładnie zgodnie z zaleceniami. Twój lekarz może potrzebować zmienić dawkę tabletek wenlafaksyny, USP, dopóki nie będzie to właściwa dawka dla Ciebie.
- Tabletki wenlafaksyny, USP należy przyjmować z jedzeniem.
- W przypadku pominięcia dawki tabletek wenlafaksyny, USP, należy przyjąć pominiętą dawkę, gdy tylko sobie o tym przypomni. Jeśli zbliża się pora przyjęcia następnej dawki, pomiń pominiętą dawkę i weź kolejną dawkę o zwykłej porze. Nie należy przyjmować dwóch dawek tabletek wenlafaksyny, USP w tym samym czasie.
- Jeśli zażyjesz zbyt dużo tabletek wenlafaksyny, USP, natychmiast skontaktuj się z lekarzem lub ośrodkiem kontroli zatruć lub skorzystaj z pomocy w nagłych wypadkach.
- W przypadku zmiany z innego leku przeciwdepresyjnego na tabletki wenlafaksyny, lekarz USP może chcieć najpierw obniżyć dawkę początkowego leku przeciwdepresyjnego, aby uniknąć skutków ubocznych
Czego powinienem unikać podczas przyjmowania tabletek wenlafaksyny, USP?
Tabletki wenlafaksyny, USP mogą powodować senność lub mogą wpływać na zdolność podejmowania decyzji, jasnego myślenia lub szybkiego reagowania.
Nie powinieneś prowadzić pojazdów, obsługiwać ciężkich maszyn ani wykonywać innych niebezpiecznych czynności, dopóki nie dowiesz się, jak wpływają na Ciebie tabletki wenlafaksyny, USP. Nie należy pić alkoholu podczas stosowania tabletek wenlafaksyny, USP.
Jakie są możliwe skutki uboczne tabletek wenlafaksyny, USP?
Tabletki wenlafaksyny, USP mogą powodować poważne skutki uboczne, w tym:
- Patrz „Jakie są najważniejsze informacje, które powinienem wiedzieć na temat tabletek wenlafaksyny, USP?”
- Podwyższony poziom cholesterolu - regularnie sprawdzaj poziom cholesterolu
- Noworodki, których matki przyjmują tabletki wenlafaksyny, USP w trzecim trymestrze mogą mieć problemy zaraz po urodzeniu, w tym:
- problemy z karmieniem i oddychaniem
- drgawki
- drżenie, roztrzęsienie lub ciągły płacz
- Jaskra z wąskim kątem przesączania/powiększone źrenice.
Regularnie sprawdzaj ciśnienie w oku, jeśli:
- masz historię podwyższonego ciśnienia w oku
- są zagrożone niektórymi rodzajami jaskry
Częste możliwe działania niepożądane u osób przyjmujących tabletki wenlafaksyny, USP obejmują:
niezwykłe sny
- problemy seksualne
- utrata apetytu, zaparcia, biegunka, nudności lub wymioty lub suchość w ustach
- uczucie zmęczenia, zmęczenia lub nadmiernej senności
- zmiana nawyków snu, problemy ze snem
- ziewanie
- drżenie lub drżenie
- zawroty głowy, niewyraźne widzenie
- wyzysk
- uczucie niepokoju, nerwowości lub roztrzęsienia
- ból głowy
- wzrost tętna
Poinformuj swojego lekarza, jeśli masz jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne tabletek wenlafaksyny, USP.
Aby uzyskać więcej informacji, zapytaj swojego lekarza lub farmaceutę.
ZADZWOŃ DO LEKARZA, ABY UZYSKAĆ PORADĘ MEDYCZNĄ DOTYCZĄCĄ SKUTKÓW UBOCZNYCH. SKUTKI UBOCZNE MOŻNA ZGŁASZAĆ FDA POD numerem 1-800-FDA-1088.
Jak przechowywać tabletki wenlafaksyny, USP?
- Przechowywać w temperaturze 20 ° do 25 ° C (68 ° do 77 ° F) dopuszczalne odchylenia od 15 ° do 30 ° C (59 ° do 86 ° F) [Patrz Temperatura pokojowa kontrolowana przez USP ].
- Przechowuj tabletki welafaksyny, USP w suchym miejscu.
Tabletki wenlafaksyny, USP i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Ogólne informacje na temat tabletek wenlafaksyny, leków USP są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Nie należy stosować tabletek wenlafaksyny, USP w przypadku schorzenia, na które nie została przepisana. Nie podawaj tabletek wenlafaksyny, USP innym osobom, nawet jeśli mają ten sam stan. Może im to zaszkodzić.
Niniejszy Przewodnik po lekach podsumowuje najważniejsze informacje dotyczące tabletek wenlafaksyny, USP. Jeśli chcesz uzyskać więcej informacji, porozmawiaj ze swoim lekarzem. Możesz poprosić swojego lekarza lub farmaceutę o informacje na temat tabletek wenlafaksyny, USP, które są przeznaczone dla pracowników służby zdrowia.
Aby zgłosić PODEJRZEWANE DZIAŁANIA NIEPOŻĄDANE, należy skontaktować się z Sun Pharmaceutical Industries, Inc. pod numerem 1-800-818-4555.
Jakie są składniki tabletek wenlafaksyny, USP?
Składnik aktywny: (wenlafaksyna)
Nieaktywne składniki:
- Tabletki: celuloza mikrokrystaliczna, laktoza jednowodna, skrobia żelowana, glikolan sodowy skrobi, czerwony tlenek żelaza, żółty tlenek żelaza, koloidalny dwutlenek krzemu i stearynian magnezu
Niniejszy przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków dla wszystkich leków przeciwdepresyjnych.
WSKAZANIA
Ciężkie zaburzenie depresyjne
Kapsułki o przedłużonym uwalnianiu Effexor XR (chlorowodorek wenlafaksyny) są wskazane w leczeniu dużego zaburzenia depresyjnego (MDD). Skuteczność ustalono w trzech krótkoterminowych (4, 8 i 12 tygodni) i dwóch długoterminowych badaniach podtrzymujących.
Uogólnione zaburzenie lękowe
Effexor XR jest wskazany w leczeniu zespołu lęku uogólnionego (GAD). Skuteczność ustalono w dwóch 8-tygodniowych i dwóch 26-tygodniowych badaniach kontrolowanych placebo.
Fobia społeczna
Effexor XR jest wskazany w leczeniu zespołu lęku społecznego (SAD), znanego również jako fobia społeczna. Skuteczność ustalono w czterech 12-tygodniowych i jednym 26-tygodniowym badaniu kontrolowanym placebo.
Zaburzenie lękowe
Effexor XR jest wskazany w leczeniu zespołu lęku napadowego (PD), z agorafobią lub bez agorafobii. Skuteczność ustalono w dwóch 12-tygodniowych badaniach kontrolowanych placebo.
DAWKOWANIE I SPOSÓB PODAWANIA
Effexor 37,5 mg XR należy podawać w pojedynczej dawce z posiłkiem, rano lub wieczorem, mniej więcej o tej samej porze każdego dnia [patrz FARMAKOLOGIA KLINICZNA ]. Każdą kapsułkę należy połykać w całości, popijając płynem, a nie dzielić, kruszyć, żuć ani umieszczać w wodzie lub można ją podawać ostrożnie otwierając kapsułkę i posypując całą zawartość łyżką musu jabłkowego. Tę mieszaninę leku/pokarmu należy natychmiast połknąć bez rozgryzania i popić szklanką wody, aby zapewnić całkowite połknięcie peletek (sferoidów).
Ciężkie zaburzenie depresyjne
Dla większości pacjentów zalecana dawka początkowa produktu Effexor 37,5 mg XR wynosi 75 mg na dobę, podawana w pojedynczej dawce. U niektórych pacjentów może być pożądane rozpoczęcie od 37,5 mg dziennie przez 4 do 7 dni, aby umożliwić nowym pacjentom przystosowanie się do leczenia przed zwiększeniem dawki do 75 mg dziennie. Pacjenci, którzy nie reagują na początkową dawkę 75 mg na dobę, mogą odnieść korzyść ze zwiększenia dawki do maksymalnie 225 mg na dobę. Dawki należy zwiększać w razie potrzeby o maksymalnie 75 mg na dobę i należy je wykonywać w odstępach nie krótszych niż 4 dni, ponieważ stężenia wenlafaksyny i jej głównych metabolitów w osoczu w stanie stacjonarnym są osiągane u większości pacjentów do 4. dnia. [Widzieć FARMAKOLOGIA KLINICZNA ]. W badaniach klinicznych ustalających skuteczność, zwiększanie dawki było dozwolone w odstępach co 2 tygodnie.
Należy zauważyć, że podczas gdy maksymalna zalecana dawka dla pacjentów ambulatoryjnych z umiarkowaną depresją wynosi również 225 mg dziennie dla produktu Effexor (o natychmiastowym uwalnianiu), pacjenci hospitalizowani z cięższą depresją w jednym badaniu programu rozwoju tego produktu odpowiedzieli na średnią dawkę 350 mg na dzień (zakres od 150 do 375 mg na dzień). Nie wiadomo, czy większe dawki leku Effexor 37,5 mg XR są potrzebne pacjentom z cięższą depresją; jednak doświadczenie z dawkami Effexor 75 mg XR większymi niż 225 mg dziennie jest bardzo ograniczone.
Uogólnione zaburzenie lękowe
Dla większości pacjentów zalecana dawka początkowa produktu Effexor XR wynosi 75 mg na dobę, podawana w pojedynczej dawce. U niektórych pacjentów może być pożądane rozpoczęcie od 37,5 mg dziennie przez 4 do 7 dni, aby umożliwić nowym pacjentom przystosowanie się do leczenia przed zwiększeniem dawki do 75 mg dziennie. Pacjenci, którzy nie reagują na początkową dawkę 75 mg na dobę, mogą odnieść korzyść ze zwiększenia dawki do maksymalnie 225 mg na dobę. Dawki należy zwiększać w razie potrzeby o maksymalnie 75 mg na dobę i należy je wykonywać w odstępach nie krótszych niż 4 dni, ponieważ stężenia wenlafaksyny i jej głównych metabolitów w osoczu w stanie stacjonarnym są osiągane u większości pacjentów do 4. dnia. [Widzieć FARMAKOLOGIA KLINICZNA ].
Zaburzenie lęku społecznego (fobia społeczna)
Zalecana dawka to 75 mg na dobę, podawana w pojedynczej dawce. Nie było dowodów na to, że wyższe dawki przynoszą dodatkowe korzyści.
Zaburzenie lękowe
Zalecana dawka początkowa leku Effexor 75 mg XR wynosi 37,5 mg na dobę przez 7 dni. Pacjenci, którzy nie reagują na 75 mg na dobę, mogą odnieść korzyść ze zwiększenia dawki do maksymalnie około 225 mg na dobę. W razie potrzeby zwiększanie dawki powinno następować o maksymalnie 75 mg na dobę i powinno odbywać się w odstępach nie krótszych niż 7 dni.
Zmiana pacjentów z tabletek Effexor 37,5 mg
Pacjenci z depresją, którzy są obecnie leczeni dawką terapeutyczną produktem Effexor (o natychmiastowym uwalnianiu) mogą zostać przestawieni na Effexor 37,5 mg XR w najbliższej równoważnej dawce (mg na dobę), np. 37,5 mg wenlafaksyny dwa razy dziennie na 75 mg Effexor 75 mg XR raz dziennie. Jednak może być konieczne indywidualne dostosowanie dawki.
Określone populacje
Pacjenci z niewydolnością wątroby
Całkowitą dawkę dobową należy zmniejszyć o 50% u pacjentów z łagodnymi (Child-Pugh=5-6) do umiarkowanych (Child-Pugh=7-9) zaburzeniami czynności wątroby. U pacjentów z ciężkimi zaburzeniami czynności wątroby (Child-Pugh=10-15) lub marskością wątroby może być konieczne zmniejszenie dawki o 50% lub więcej [patrz Używaj w określonych populacjach ].
Pacjenci z niewydolnością nerek
Całkowitą dawkę dobową należy zmniejszyć o 25% do 50% u pacjentów z łagodnymi (CLkr=60-89 ml/min) lub umiarkowanymi (CLkr=30-59 ml/min) zaburzeniami czynności nerek. U pacjentów poddawanych hemodializie lub z ciężkimi zaburzeniami czynności nerek (CLcr Używaj w określonych populacjach ].
Leczenie podtrzymujące
Nie ma dostępnych dowodów z kontrolowanych badań wskazujących, jak długo pacjenci z MDD, GAD, SAD lub PD powinni być leczeni produktem Effexor 75 mg XR.
Powszechnie uważa się, że ostre epizody MDD wymagają kilku miesięcy lub dłużej długotrwałego leczenia farmakologicznego wykraczającego poza odpowiedź na ostry epizod. Effexor XR/Effexor wykazały kontynuację odpowiedzi w badaniach klinicznych do 52 tygodni, przy tej samej dawce, na którą pacjenci odpowiadali podczas początkowego leczenia [patrz Studia kliniczne ]. Nie wiadomo, czy dawka produktu Effexor XR potrzebna do leczenia podtrzymującego jest taka sama jak dawka potrzebna do uzyskania początkowej odpowiedzi. Pacjenci powinni być okresowo poddawani ponownej ocenie w celu określenia potrzeby leczenia podtrzymującego i odpowiedniej dawki do takiego leczenia.
U pacjentów z GAD i SAD wykazano, że Effexor 37,5 mg XR jest skuteczny w 6-miesięcznych badaniach klinicznych. Konieczność kontynuowania leczenia u pacjentów z GAD i SAD, u których nastąpiła poprawa po leczeniu produktem Effexor XR, powinna być okresowo poddawana ponownej ocenie.
W badaniu klinicznym dotyczącym PD pacjenci kontynuujący leczenie produktem Effexor 75 mg XR w tej samej dawce, na którą uzyskali odpowiedź w ciągu pierwszych 12 tygodni leczenia, doświadczyli statystycznie istotnie dłuższego czasu do nawrotu niż pacjenci przydzieleni losowo do grupy placebo [patrz Studia kliniczne ]. Konieczność kontynuowania leczenia u pacjentów z chP, u których nastąpiła poprawa po leczeniu produktem Effexor XR, powinna być okresowo poddawana ponownej ocenie.
Wycofanie Effexor XR
przypadku przerwania leczenia produktem Effexor 37,5 mg XR zaleca się stopniowe zmniejszanie dawki, a nie nagłe jej zaprzestanie. W badaniach klinicznych produktu Effexor 37,5 mg XR zmniejszanie dawki osiągnięto poprzez zmniejszenie dawki dobowej o 75 mg w odstępach tygodniowych. Może być konieczna indywidualizacja zwężania [patrz OSTRZEŻENIA I ŚRODKI ]. U niektórych pacjentów może być konieczne przerwanie leczenia w ciągu kilku miesięcy.
Przełączanie pacjentów na lub z inhibitora monoaminooksydazy (MAOI) przeznaczonego do leczenia zaburzeń psychicznych
Pomiędzy odstawieniem MAOI (przeznaczonego do leczenia zaburzeń psychicznych) a rozpoczęciem leczenia produktem Effexor XR powinno upłynąć co najmniej 14 dni. Ponadto należy odczekać co najmniej 7 dni po odstawieniu leku Effexor XR przed rozpoczęciem stosowania MAOI przeznaczonego do leczenia zaburzeń psychicznych [patrz PRZECIWWSKAZANIA , OSTRZEŻENIA I ŚRODKI , oraz INTERAKCJE Z LEKAMI ].
Stosowanie Effexor XR z innymi MAOI, takimi jak linezolid lub dożylny błękit metylenowy
Nie należy rozpoczynać stosowania leku Effexor 75 mg XR u pacjenta leczonego linezolidem lub dożylnie błękitem metylenowym, ponieważ istnieje zwiększone ryzyko wystąpienia zespołu serotoninowego. U pacjenta wymagającego pilniejszego leczenia schorzenia psychicznego należy rozważyć inne interwencje, w tym hospitalizację [patrz PRZECIWWSKAZANIA ].
niektórych przypadkach pacjent już otrzymujący terapię Effexor 37,5 mg XR może wymagać pilnego leczenia linezolidem lub dożylnym błękitem metylenowym. Jeśli akceptowalne alternatywy dla linezolidu lub błękitu metylenowego podawanego dożylnie nie są dostępne, a potencjalne korzyści z leczenia linezolidem lub błękitem metylenowym podawanym dożylnie są oceniane jako przewyższające ryzyko wystąpienia zespołu serotoninowego u konkretnego pacjenta, należy niezwłocznie przerwać stosowanie produktu Effexor XR i podać linezolid lub błękit metylenowy podawany dożylnie. można podawać. Obserwować pacjenta pod kątem objawów zespołu serotoninowego przez 7 dni lub do 24 godzin po podaniu ostatniej dawki linezolidu lub dożylnego błękitu metylenowego, w zależności od tego, co nastąpi wcześniej. Leczenie preparatem Effexor 75 mg XR można wznowić 24 godziny po podaniu ostatniej dawki linezolidu lub dożylnie błękitu metylenowego [patrz OSTRZEŻENIA I ŚRODKI ].
Ryzyko podawania błękitu metylenowego drogą nie dożylną (taką jak tabletki doustne lub miejscowe wstrzyknięcie) lub w dawkach dożylnych znacznie mniejszych niż 1 mg/kg jednocześnie z produktem Effexor XR jest niejasne. Klinicysta powinien jednak mieć świadomość, że przy takim stosowaniu mogą pojawić się objawy zespołu serotoninowego [patrz OSTRZEŻENIA I ŚRODKI ].
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Effexor 37,5 mg XR® (chlorowodorek wenlafaksyny) kapsułki o przedłużonym uwalnianiu są dostępne w następujących mocach:
- Kapsułki 37,5 mg (szare wieczko/brzoskwiniowy korpus z „W” i „Effexor 75mg XR” na wieczku i „37,5” na korpusie)
- Kapsułki 75 mg (brzoskwiniowe wieczko i korpus z literami „W” i „Effexor 37,5 mg XR” na wieczku i „75” na korpusie)
- Kapsułki 150 mg (ciemnopomarańczowe wieczko i korpus z literami „W” i „Effexor 75mg XR” na wieczku i „150” na korpusie)
Składowania i stosowania
Effexor XR® (chlorowodorek wenlafaksyny) kapsułki o przedłużonym uwalnianiu są dostępne w następujący sposób:
NDC 0008-0837-20, butelka 15 kapsułek w opakowaniu jednostkowym. NDC 0008-0837-21, butelka 30 kapsułek w opakowaniu jednostkowym. NDC 0008-0837-22, butelka 90 kapsułek w opakowaniu jednostkowym. NDC 0008-0837-03, karton 10 blistrów Redipak® po 10 kapsułek każdy.
NDC 0008-0833-20, butelka 15 kapsułek w opakowaniu jednostkowym. NDC 0008-0833-21, butelka 30 kapsułek w opakowaniu jednostkowym. NDC 0008-0833-22, butelka 90 kapsułek w opakowaniu jednostkowym. NDC 0008-0833-03, karton 10 blistrów Redipak® po 10 kapsułek każdy.
NDC 0008-0836-20, butelka 15 kapsułek w opakowaniu jednostkowym. NDC 0008-0836-21, butelka 30 kapsułek w opakowaniu jednostkowym. NDC 0008-0836-22, butelka 90 kapsułek w opakowaniu jednostkowym. NDC 0008-0836-03, karton 10 blistrów Redipak® po 10 kapsułek każdy.
- 37,5 mg , szare wieczko/brzoskwiniowy korpus z literami „W” i „Effexor XR” na wieczku oraz „37,5” na korpusie.
- 75 mg , brzoskwiniowe wieczko i korpus z literami „W” i „Effexor 37,5 mg XR” na wieczku oraz „75” na korpusie.
- 150 mg ciemnopomarańczowa wieczko i korpus z literami „W” i „Effexor XR” na wieczku i „150” na korpusie.
Przechowywać w kontrolowanej temperaturze pokojowej, od 20° do 25°C (68° do 77°F).
Opakowanie jednostkowe przeznaczone jest do dozowania jako jednostka.
Dystrybutor: Wyeth Pharmaceuticals LLC, spółka zależna Pfizer Inc, Philadelpia, PA 19101. Aktualizacja: listopad 2021
SKUTKI UBOCZNE
Następujące działania niepożądane omówiono bardziej szczegółowo w innych sekcjach etykiety:
- Nadwrażliwość [patrz PRZECIWWSKAZANIA ]
- Myśli i zachowania samobójcze u dzieci, młodzieży i dorosłych [patrz OSTRZEŻENIA I ŚRODKI ]
- Zespół serotoninowy [patrz OSTRZEŻENIA I ŚRODKI ]
- Wzrost ciśnienia krwi [patrz OSTRZEŻENIA I ŚRODKI ]
- Nieprawidłowe krwawienie [patrz OSTRZEŻENIA I ŚRODKI ]
- Jaskra zamykającego się kąta [patrz OSTRZEŻENIA I ŚRODKI ]
- Aktywacja manii/hipomanii [patrz OSTRZEŻENIA I ŚRODKI ]
- Syndrom odstawienia [patrz OSTRZEŻENIA I ŚRODKI ]
- Napad [patrz OSTRZEŻENIA I ŚRODKI ]
- Hiponatremia [patrz OSTRZEŻENIA I ŚRODKI ]
- Zmiany masy ciała i wzrostu u pacjentów pediatrycznych [patrz OSTRZEŻENIA I ŚRODKI ]
- Zmiany apetytu u pacjentów pediatrycznych [patrz OSTRZEŻENIA I ŚRODKI ]
- Śródmiąższowa choroba płuc i eozynofilowe zapalenie płuc [patrz OSTRZEŻENIA I ŚRODKI ]
- Dysfunkcje seksualne [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Najczęstsze działania niepożądane
Najczęściej obserwowanymi działaniami niepożądanymi w bazie danych badań klinicznych u pacjentów z MDD, GAD, SAD i PD leczonych produktem Effexor XR (częstość występowania ≥ 5% i co najmniej dwukrotnie większa niż w przypadku placebo) były: nudności (30,0%), senność (15,3 %), suchość w ustach (14,8%), pocenie się (11,4%), nieprawidłowy wytrysk (9,9%), anoreksja (9,8%), zaparcia (9,3%), impotencja (5,3%) i obniżone libido (5,1%).
Działania niepożądane zgłaszane jako przyczyny przerwania leczenia
Łącznie w krótkoterminowych, kontrolowanych placebo badaniach przed wprowadzeniem do obrotu we wszystkich wskazaniach, 12% z 3558 pacjentów, którzy otrzymywali Effexor XR (37,5-225 mg) przerwało leczenie z powodu działań niepożądanych, w porównaniu z 4% z 2197 pacjentów otrzymujących placebo w tych badaniach.W Tabeli 7 przedstawiono najczęstsze działania niepożądane prowadzące do przerwania leczenia u ≥ 1% pacjentów leczonych produktem Effexor XR w badaniach krótkoterminowych (do 12 tygodni) we wszystkich wskazaniach.
Częste działania niepożądane w badaniach kontrolowanych placebo
Liczbę pacjentów otrzymujących wielokrotne dawki produktu Effexor XR podczas oceny przed wprowadzeniem do obrotu dla każdego zatwierdzonego wskazania przedstawiono w Tabeli 8. Warunki i czas trwania ekspozycji na wenlafaksynę we wszystkich programach rozwojowych były bardzo zróżnicowane i obejmowały (w nakładających się kategoriach) otwarte i podwójne badania ślepe, badania niekontrolowane i kontrolowane, badania szpitalne (wyłącznie Effexor) i badania ambulatoryjne, badania z ustaloną dawką i miareczkowaniem.
Częstość występowania częstych działań niepożądanych (które wystąpiły u ≥ 2% pacjentów leczonych produktem Effexor XR [357 pacjentów z MDD, 1381 pacjentów z GAD, 819 pacjentów z SAD i 1001 pacjentów z PD] i częściej niż placebo) u pacjentów leczonych produktem Effexor XR w skrócie -określone, kontrolowane placebo badania kliniczne ze stałą i zmienną dawką (dawki od 37,5 do 225 mg na dobę) przedstawiono w Tabeli 9.
Profil działań niepożądanych nie różnił się istotnie w różnych populacjach pacjentów.
Inne działania niepożądane obserwowane w badaniach klinicznych
Ciało jako całość: Reakcja nadwrażliwości na światło, dreszcze
Układu sercowo-naczyniowego: Niedociśnienie ortostatyczne, omdlenie, niedociśnienie, tachykardia
Układ trawienny: Krwotok z przewodu pokarmowego [patrz OSTRZEŻENIA I ŚRODKI ],
bruksizm Układ hemiczny/limfatyczny: Wybroczyny [patrz OSTRZEŻENIA I ŚRODKI ]
Metaboliczne/odżywcze: Hipercholesterolemia, przyrost masy ciała [patrz OSTRZEŻENIA I ŚRODKI ], utrata masy ciała [patrz OSTRZEŻENIA I ŚRODKI ]
System nerwowy: Napady [patrz OSTRZEŻENIA I ŚRODKI ], reakcja maniakalna [patrz OSTRZEŻENIA I ŚRODKI ], pobudzenie, splątanie, akatyzja, halucynacje, hipertonia, mioklonie, depersonalizacja, apatia
Skóra i przydatki: Pokrzywka, świąd, wysypka, łysienie
Specjalne zmysły: Rozszerzenie źrenic, zaburzenia akomodacji, szum w uszach, perwersja smaku
Układ moczowo-płciowy: Zatrzymanie moczu, zaburzenia oddawania moczu, nietrzymanie moczu, zwiększona częstość oddawania moczu, zaburzenia miesiączkowania związane ze zwiększonym krwawieniem lub zwiększonym nieregularnym krwawieniem (np. krwotok miesiączkowy, krwotok maciczny)
Zmiany Znaków Życiowych
badaniach poprzedzających wprowadzenie do obrotu kontrolowanych placebo stwierdzono wzrost średniego ciśnienia krwi (patrz Tabela 10). W większości wskazań u pacjentów leczonych produktem Effexor w dawce 37,5 mg XR widoczny był zależny od dawki wzrost średniego skurczowego i rozkurczowego ciśnienia krwi w pozycji leżącej. We wszystkich badaniach klinicznych dotyczących MDD, GAD, SAD i PD, 1,4% pacjentów w grupach Effexor XR doświadczyło wzrostu SDBP o ≥15 mm Hg wraz z ciśnieniem krwi ≥ 105 mm Hg, w porównaniu z 0,9% pacjentów w grupie grupy placebo. Podobnie, 1% pacjentów w grupach Effexor 37,5 mg XR doświadczyło wzrostu SSBP o ≥ 20 mm Hg przy ciśnieniu krwi ≥ 180 mm Hg, w porównaniu z 0,3% pacjentów w grupach placebo.
Leczenie produktem Effexor 37,5 mg XR wiązało się z utrzymującym się nadciśnieniem tętniczym (zdefiniowanym jako pojawiające się w trakcie leczenia rozkurczowe ciśnienie krwi [SDBP] ≥ 90 mm Hg i ≥ 10 mm Hg powyżej wartości wyjściowej w trzech kolejnych wizytach w trakcie terapii (patrz Tabela 11). pacjentów otrzymywało średnie dawki produktu Effexor XR powyżej 300 mg na dobę w badaniach klinicznych w celu pełnej oceny częstości występowania utrzymującego się wzrostu ciśnienia krwi po tych większych dawkach.
Effexor 37,5 mg XR wiązał się ze średnim wzrostem częstości tętna w porównaniu z placebo w badaniach kontrolowanych placebo przed wprowadzeniem do obrotu (patrz Tabela 12) [patrz OSTRZEŻENIA I ŚRODKI ].
Zmiany laboratoryjne
Cholesterol w surowicy
Effexor XR wiązał się ze średnim końcowym wzrostem stężenia cholesterolu w surowicy w porównaniu ze średnim końcowym spadkiem dla placebo w badaniach klinicznych przed wprowadzeniem do obrotu MDD, GAD, SAD i PD (Tabela 13).
Leczenie produktem Effexor 75 mg XR (chlorowodorek wenlafaksyny) w postaci kapsułek o przedłużonym uwalnianiu przez okres do 12 tygodni w badaniach klinicznych przed wprowadzeniem do obrotu, kontrolowanych placebo, dotyczących ciężkiej depresji wiązało się ze średnim wzrostem stężenia cholesterolu w surowicy w trakcie leczenia o około 1,5 mg/dl w porównaniu z średnie końcowe zmniejszenie o 7,4 mg/dl dla placebo. Leczenie produktem Effexor XR przez okres do 8 tygodni i do 6 miesięcy w badaniach GAD kontrolowanych placebo przed wprowadzeniem do obrotu wiązało się ze średnim końcowym wzrostem stężenia cholesterolu w surowicy o około 1,0 mg/dl i 2,3 mg/dl, podczas gdy u pacjentów otrzymujących placebo średnie końcowe spadki odpowiednio o 4,9 mg/dl i 7,7 mg/dl. Leczenie produktem Effexor XR przez okres do 12 tygodni i do 6 miesięcy w kontrolowanych placebo badaniach dotyczących zaburzeń lękowych przed wprowadzeniem do obrotu wiązało się ze średnim końcowym wzrostem stężenia cholesterolu w surowicy w trakcie terapii o odpowiednio około 7,9 mg/dl i 5,6 mg/dl. ze średnimi końcowymi spadkami odpowiednio o 2,9 i 4,2 mg/dl dla placebo. Leczenie produktem Effexor XR przez okres do 12 tygodni w badaniach klinicznych kontrolowanych placebo dotyczących lęku napadowego przed wprowadzeniem do obrotu wiązało się ze średnim końcowym wzrostem stężenia cholesterolu w surowicy podczas terapii o około 5,8 mg/dl w porównaniu ze średnim końcowym zmniejszeniem o 3,7 mg/dl w przypadku placebo.
pacjentów leczonych produktem Effexor (o natychmiastowym uwalnianiu) przez co najmniej 3 miesiące w 12-miesięcznych badaniach kontynuacyjnych kontrolowanych placebo, średni końcowy wzrost stężenia cholesterolu całkowitego w trakcie leczenia wyniósł 9,1 mg/dl w porównaniu ze spadkiem o 7,1 mg/dl w grupie placebo- leczonych pacjentów. Ten wzrost był zależny od czasu trwania badania i zwykle był większy przy wyższych dawkach. Klinicznie istotne zwiększenie stężenia cholesterolu w surowicy, zdefiniowane jako 1) końcowy wzrost stężenia cholesterolu w surowicy w trakcie terapii ≥50 mg/dl od wartości początkowej do wartości ≥261 mg/dl lub 2) średni wzrost stężenia cholesterolu w surowicy podczas terapii ≥ 50 mg/dl od wartości wyjściowej do wartości ≥261 mg/dl odnotowano u 5,3% pacjentów leczonych wenlafaksyną i 0,0% pacjentów otrzymujących placebo.
Triglicerydy w surowicy
Effexor 75 mg XR wiązał się ze średnim końcowym wzrostem stężenia triglicerydów w surowicy na czczo w porównaniu z placebo w badaniach klinicznych przed wprowadzeniem do obrotu SAD i PD trwających do 12 tygodni (dane zbiorcze) i przez 6 miesięcy (Tabela 14).
Pacjenci pediatryczni
Ogólnie profil działań niepożądanych wenlafaksyny (w badaniach klinicznych kontrolowanych placebo) u dzieci i młodzieży (w wieku od 6 do 17 lat) był podobny do obserwowanego u dorosłych. Podobnie jak u dorosłych zaobserwowano zmniejszony apetyt, utratę masy ciała, podwyższone ciśnienie krwi i podwyższony poziom cholesterolu w surowicy [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
W pediatrycznych badaniach klinicznych zaobserwowano działanie niepożądane, myśli samobójcze.
W szczególności u dzieci i młodzieży obserwowano następujące działania niepożądane: ból brzucha, pobudzenie, niestrawność, wybroczyny, krwawienie z nosa i bóle mięśni.
Działania niepożądane zidentyfikowane podczas stosowania po zatwierdzeniu
Następujące działania niepożądane zostały zidentyfikowane po zatwierdzeniu produktu Effexor XR. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z narażeniem na lek:
Ciało jako całość: Anafilaksja, obrzęk naczynioruchowy
Układu sercowo-naczyniowego: Wydłużenie odstępu QT, migotanie komór, częstoskurcz komorowy (w tym torsade de pointes), kardiomiopatia takotsubo
Układ trawienny: Zapalenie trzustki
Układ hemiczny/limfatyczny: Krwawienie z błony śluzowej [patrz OSTRZEŻENIA I ŚRODKI ], zaburzenia krwi (w tym agranulocytoza, niedokrwistość aplastyczna, neutropenia i pancytopenia), wydłużony czas krwawienia, małopłytkowość
Metaboliczne/odżywcze: Hiponatremia [patrz OSTRZEŻENIA I ŚRODKI ], zespół nieprawidłowego wydzielania hormonu antydiuretycznego (SIADH) [patrz OSTRZEŻENIA I ŚRODKI ], nieprawidłowe wyniki testów czynnościowych wątroby, zapalenie wątroby, zwiększone stężenie prolaktyny
Układ mięśniowo-szkieletowy: Rabdomioliza
System nerwowy: Złośliwy Zespół Neuroleptyczny (NMS) [patrz OSTRZEŻENIA I ŚRODKI ], zespół serotoninergiczny [patrz OSTRZEŻENIA I ŚRODKI ], majaczenie, reakcje pozapiramidowe (w tym dystonia i dyskineza), zaburzenia koordynacji i równowagi, dyskinezy późne
Układ oddechowy: Duszność, śródmiąższowa choroba płuc, eozynofilia płucna [patrz OSTRZEŻENIA I ŚRODKI ]
Skóra i przydatki: Zespół Stevensa-Johnsona, toksyczna nekroliza naskórka, rumień wielopostaciowy
Specjalne zmysły: Jaskra zamykającego się kąta [patrz OSTRZEŻENIA I ŚRODKI ]
INTERAKCJE Z LEKAMI
Leki działające na ośrodkowy układ nerwowy (OUN)
Ryzyko stosowania wenlafaksyny w połączeniu z innymi lekami działającymi na OUN nie było systematycznie oceniane. W związku z tym zaleca się ostrożność, gdy Effexor XR jest stosowany w skojarzeniu z innymi lekami działającymi na OUN.
Inhibitory monoaminooksydazy
Działania niepożądane, z których niektóre były poważne, zgłaszano u pacjentów, którzy niedawno odstawili IMAO i rozpoczęli leczenie lekami przeciwdepresyjnymi o właściwościach farmakologicznych podobnych do Effexor XR (SNRI lub SSRI) lub u których niedawno przerwano leczenie SNRI lub SSRI. do inicjacji MAOI [patrz DAWKOWANIE I SPOSÓB PODAWANIA , PRZECIWWSKAZANIA oraz OSTRZEŻENIA I ŚRODKI ].
Leki serotoninergiczne
Biorąc pod uwagę mechanizm działania produktu Effexor XR i możliwość wystąpienia zespołu serotoninowego, zaleca się ostrożność podczas jednoczesnego podawania produktu Effexor XR z innymi lekami, które mogą wpływać na układy neuroprzekaźników serotoninergicznych, takimi jak tryptany, leki z grupy SSRI, inne leki z grupy SNRI, linezolid (antybiotyk, który odwracalny nieselektywny MAOI), lit, tramadol lub ziele dziurawca. Jeśli jednoczesne leczenie produktem Effexor XR i tymi lekami jest klinicznie uzasadnione, zaleca się uważną obserwację pacjenta, szczególnie podczas rozpoczynania leczenia i zwiększania dawki. Nie zaleca się jednoczesnego stosowania produktu Effexor 75 mg XR z suplementami tryptofanu [patrz DAWKOWANIE I SPOSÓB PODAWANIA , PRZECIWWSKAZANIA , oraz OSTRZEŻENIA I ŚRODKI ].
Leki, które zakłócają hemostazę (np. NLPZ, aspiryna i warfaryna)
Uwalnianie serotoniny przez płytki krwi odgrywa ważną rolę w hemostazie. Stosowanie leków psychotropowych, które zaburzają wychwyt zwrotny serotoniny, wiąże się z występowaniem krwawienia z górnego odcinka przewodu pokarmowego, a jednoczesne stosowanie NLPZ lub aspiryny może nasilać to ryzyko krwawienia [patrz OSTRZEŻENIA I ŚRODKI ]. Zgłaszano zmiany w działaniu przeciwzakrzepowym, w tym zwiększone krwawienie, gdy SSRI i SNRI są podawane jednocześnie z warfaryną. Pacjenci otrzymujący leczenie warfaryną powinni być uważnie obserwowani podczas rozpoczynania lub kończenia leczenia produktem Effexor 37,5 mg XR.
Środki odchudzające
Nie ustalono bezpieczeństwa i skuteczności terapii wenlafaksyną w połączeniu z lekami odchudzającymi, w tym fenterminą. Nie zaleca się jednoczesnego podawania produktu Effexor XR i środków odchudzających. Effexor XR nie jest wskazany do odchudzania samodzielnie lub w połączeniu z innymi produktami.
Wpływ innych leków na Effexor XR
Rycina 1: Wpływ leków wchodzących w interakcje na farmakokinetykę wenlafaksyny i aktywnego metabolitu O-desmetylowenlafaksyny (ODV).
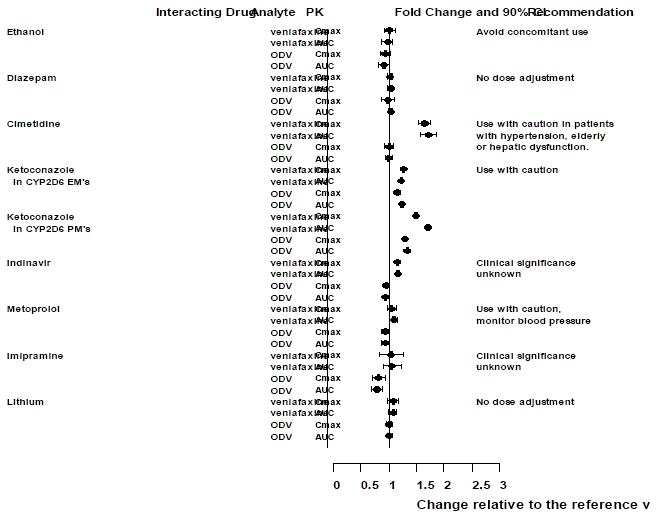
Wpływ Effexor XR na inne leki
Rysunek 2: Wpływ wenlafaksyny na farmakokinetykę leków wchodzących w interakcje i ich aktywnych metabolitów.
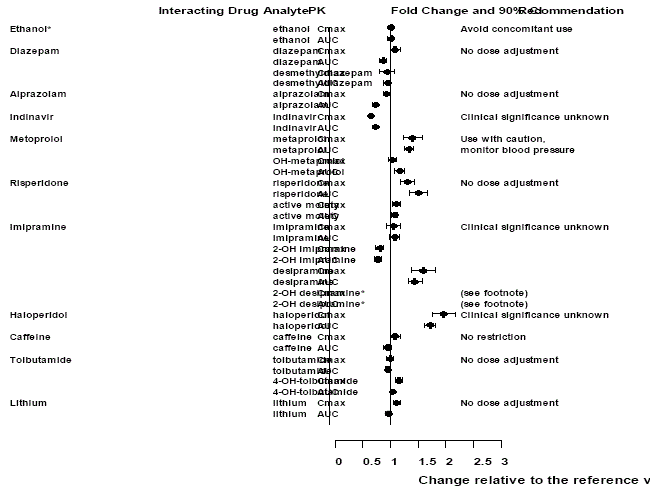
Notatka
Podawanie wenlafaksyny w schemacie stabilnym nie wyolbrzymiało efektów psychomotorycznych i psychometrycznych wywoływanych przez etanol u tych samych osób, które nie otrzymywały wenlafaksyny.
Interakcje lekowo-laboratoryjne
Fałszywie dodatnie testy przesiewowe moczu na obecność fencyklidyny (PCP) i amfetaminy zgłaszano u pacjentów przyjmujących wenlafaksynę. Wynika to z braku specyficzności badań przesiewowych. Fałszywie dodatnie wyniki testu można spodziewać się przez kilka dni po zaprzestaniu leczenia wenlafaksyną. Testy potwierdzające, takie jak chromatografia gazowa/spektrometria mas, pozwolą odróżnić wenlafaksynę od PCP i amfetaminy.
Nadużywanie i uzależnienie od narkotyków
Substancja kontrolowana
Effexor 75mg XR nie jest substancją kontrolowaną.
Nadużywać
Chociaż wenlafaksyna nie była systematycznie badana w badaniach klinicznych pod kątem jej potencjalnego nadużywania, w badaniach klinicznych nie stwierdzono zachowań związanych z poszukiwaniem leku. Nie można jednak przewidzieć na podstawie doświadczeń przed wprowadzeniem do obrotu, w jakim stopniu lek działający na OUN będzie niewłaściwie używany, przekierowywany i/lub nadużywany po wprowadzeniu do obrotu. W związku z tym lekarze powinni uważnie oceniać pacjentów pod kątem historii nadużywania leków i uważnie obserwować takich pacjentów, obserwując ich pod kątem oznak niewłaściwego lub nadużywania wenlafaksyny (np. rozwój tolerancji, zwiększenie dawki, zachowanie związane z poszukiwaniem leku).
Zależność
Badania in vitro wykazały, że wenlafaksyna praktycznie nie wykazuje powinowactwa do receptorów opiatów, benzodiazepin, fencyklidyny (PCP) ani kwasu N-metylo-D-asparaginowego (NMDA).
Nie stwierdzono, aby wenlafaksyna wywierała jakiekolwiek znaczące działanie pobudzające ośrodkowy układ nerwowy u gryzoni. W badaniach dotyczących dyskryminacji leków naczelnych, wenlafaksyna nie wykazała znaczącej podatności na nadużywanie środków pobudzających lub depresyjnych.
pacjentów otrzymujących wenlafaksynę zgłaszano skutki odstawienia [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
OSTRZEŻENIA
Zawarte jako część "ŚRODKI OSTROŻNOŚCI" Sekcja
ŚRODKI OSTROŻNOŚCI
Myśli i zachowania samobójcze u dzieci, młodzieży i młodych dorosłych
Pacjenci z ciężkimi zaburzeniami depresyjnymi (MDD), zarówno dorośli, jak i pediatryczni, mogą doświadczać nasilenia depresji i/lub pojawienia się myśli i zachowań samobójczych (samobójstwa) lub nietypowych zmian w zachowaniu, niezależnie od tego, czy przyjmują leki przeciwdepresyjne, a to ryzyko może utrzymywać się aż do wystąpienia znacznej remisji. Samobójstwo jest znanym ryzykiem depresji i niektórych innych zaburzeń psychicznych, a same te zaburzenia są najsilniejszymi predyktorami samobójstwa. Od dawna istnieje jednak obawa, że leki przeciwdepresyjne mogą odgrywać rolę w wywoływaniu nasilenia depresji i pojawianiu się myśli samobójczych u niektórych pacjentów we wczesnych fazach leczenia. Zbiorcze analizy krótkoterminowych, kontrolowanych placebo badań leków przeciwdepresyjnych (SSRI i inne) wykazały, że leki te zwiększają ryzyko myśli i zachowań samobójczych (samobójstwa) u dzieci, młodzieży i młodych dorosłych (w wieku 18-24 lat) z MDD i inne zaburzenia psychiczne. Badania krótkoterminowe nie wykazały wzrostu ryzyka samobójstw w przypadku stosowania leków przeciwdepresyjnych w porównaniu z placebo u osób dorosłych w wieku powyżej 24 lat; u osób dorosłych w wieku 65 lat i starszych odnotowano zmniejszenie liczby przyjmowanych leków przeciwdepresyjnych w porównaniu z placebo.
Połączone analizy badań kontrolowanych placebo u dzieci i młodzieży z MDD, zaburzeniami obsesyjno-kompulsywnymi (OCD) lub innymi zaburzeniami psychicznymi obejmowały łącznie 24 krótkoterminowe badania 9 leków przeciwdepresyjnych z udziałem ponad 4400 pacjentów. Zbiorcze analizy badań kontrolowanych placebo u dorosłych z MDD lub innymi zaburzeniami psychicznymi obejmowały łącznie 295 badań krótkoterminowych (mediana czasu trwania wynosząca 2 miesiące) 11 leków przeciwdepresyjnych u ponad 77 000 pacjentów. Istniało znaczne zróżnicowanie ryzyka samobójstwa wśród leków, ale tendencja do wzrostu u młodszych pacjentów w przypadku prawie wszystkich badanych leków. Istniały różnice w bezwzględnym ryzyku samobójstwa w różnych wskazaniach, z największą częstością występowania MDD. Różnice ryzyka (lek w porównaniu z placebo) były jednak stosunkowo stabilne w obrębie warstw wiekowych i we wskazaniach. Te różnice ryzyka (różnica między lekami a placebo w liczbie przypadków samobójstw na 1000 leczonych pacjentów) przedstawiono w Tabeli 1.
żadnym z badań pediatrycznych nie wystąpiły samobójstwa. W badaniach z udziałem dorosłych zdarzały się samobójstwa, ale liczba ta nie była wystarczająca, aby wyciągnąć jakiekolwiek wnioski na temat wpływu leku na samobójstwo.
Nie wiadomo, czy ryzyko samobójstwa rozciąga się na dłuższe używanie, tj. dłużej niż kilka miesięcy. Jednak istnieją dowody z kontrolowanych placebo badań podtrzymujących u dorosłych z depresją, że stosowanie leków przeciwdepresyjnych może opóźnić nawrót depresji.
Wszyscy pacjenci leczeni lekami przeciwdepresyjnymi w jakimkolwiek wskazaniu powinni być odpowiednio monitorowani i obserwowani pod kątem pogorszenia stanu klinicznego, skłonności samobójczych i nietypowych zmian w zachowaniu, szczególnie w ciągu pierwszych kilku miesięcy terapii lekowej lub w czasie zmiany dawki, albo zwiększa się lub maleje.
dorosłych i dzieci leczonych lekami przeciwdepresyjnymi z powodu MDD zgłaszano następujące objawy: lęk, pobudzenie, napady paniki, bezsenność, drażliwość, wrogość, agresywność, impulsywność, akatyzję (niepokój psychoruchowy), hipomanię i manię. dla innych wskazań, zarówno psychiatrycznych, jak i niepsychiatrycznych. Chociaż nie ustalono związku przyczynowo-skutkowego między pojawieniem się takich objawów a nasileniem depresji i/lub pojawieniem się impulsów samobójczych, istnieje obawa, że takie objawy mogą być prekursorem pojawiania się samobójstw.
Należy rozważyć zmianę schematu leczenia, w tym ewentualnie odstawienie leku, u pacjentów, u których depresja jest stale nasilona lub u których pojawiają się myśli samobójcze lub objawy, które mogą być prekursorami nasilenia depresji lub myśli samobójczych, zwłaszcza jeśli objawy te są ciężkie, nagłe na początku lub nie były częścią objawów prezentowanych przez pacjenta.
Jeśli podjęto decyzję o przerwaniu leczenia, należy zmniejszyć dawkę leków tak szybko, jak to możliwe, ale z uwzględnieniem, że nagłe odstawienie może wiązać się z pewnymi objawami [patrz Zespół odstawienia oraz DAWKOWANIE I SPOSÓB PODAWANIA ].
Rodziny i opiekunowie pacjentów leczonych lekami przeciwdepresyjnymi z powodu MDD lub innych wskazań, zarówno psychiatrycznych, jak i niepsychiatrycznych, powinni być ostrzeżeni o konieczności monitorowania pacjentów pod kątem pojawienia się pobudzenia, drażliwości, nietypowych zmian w zachowaniu i innych objawów opisanych powyżej, ponieważ a także pojawienia się samobójstw i natychmiastowego zgłaszania takich objawów świadczeniodawcom. Taki monitoring powinien obejmować codzienną obserwację rodzin i opiekunów. Recepty na Effexor XR należy wypisać na najmniejszą ilość kapsułek zgodnie z dobrym postępowaniem z pacjentem, aby zmniejszyć ryzyko przedawkowania.
Badanie przesiewowe pacjentów pod kątem choroby afektywnej dwubiegunowej
Poważny epizod depresyjny może być początkowym objawem choroby afektywnej dwubiegunowej. Powszechnie uważa się (chociaż nie zostało to potwierdzone w badaniach kontrolowanych), że leczenie takiego epizodu samym lekiem przeciwdepresyjnym może zwiększyć prawdopodobieństwo wystąpienia epizodu mieszanego/maniakalnego u pacjentów z ryzykiem choroby afektywnej dwubiegunowej. Nie wiadomo, czy którykolwiek z objawów opisanych powyżej reprezentuje taką konwersję. Jednak przed rozpoczęciem leczenia lekiem przeciwdepresyjnym pacjenci z objawami depresji powinni zostać odpowiednio przebadani w celu ustalenia, czy są oni zagrożeni chorobą afektywną dwubiegunową; takie badania przesiewowe powinny obejmować szczegółowy wywiad psychiatryczny, w tym wywiad rodzinny dotyczący samobójstw, choroby afektywnej dwubiegunowej i depresji. Należy zauważyć, że Effexor XR nie jest zatwierdzony do stosowania w leczeniu depresji dwubiegunowej.
Zespół serotoninowy
Zgłaszano rozwój potencjalnie zagrażającego życiu zespołu serotoninowego podczas stosowania inhibitorów wychwytu zwrotnego serotoniny i noradrenaliny (SNRI) i SSRI, w tym samego produktu Effexor XR, ale szczególnie podczas jednoczesnego stosowania innych leków serotoninergicznych (w tym tryptanów, trójpierścieniowych leków przeciwdepresyjnych, fentanylu, litu, tramadol, tryptofan, buspiron, amfetaminy, ziele dziurawca) oraz z lekami zaburzającymi metabolizm serotoniny, w szczególności MAOI, zarówno przeznaczonymi do leczenia zaburzeń psychicznych, jak i innymi, takimi jak linezolid czy dożylny błękit metylenowy).
Objawy zespołu serotoninowego mogą obejmować zmiany stanu psychicznego (np. pobudzenie, halucynacje, majaczenie, śpiączka) niestabilność autonomiczną (np. tachykardia, niestabilne ciśnienie krwi, hipertermia, pocenie się, uderzenia gorąca i zawroty głowy), objawy nerwowo-mięśniowe (np. drżenie, sztywność, mioklonie hiperrefleksja, brak koordynacji); drgawki i objawy żołądkowo-jelitowe (np. nudności, wymioty, biegunka). Pacjenci powinni być monitorowani pod kątem wystąpienia zespołu serotoninowego.
Jednoczesne stosowanie leku Effexor XR z inhibitorami MAO (przeznaczonymi do leczenia zaburzeń psychicznych) jest przeciwwskazane. Nie należy również rozpoczynać leczenia produktem Effexor XR u pacjentów leczonych inhibitorami MAO, takimi jak linezolid lub dożylnie błękit metylenowy. Wszystkie raporty z błękitem metylenowym, które dostarczały informacji na temat drogi podania, dotyczyły podawania dożylnego w zakresie dawek od 1 mg/kg do 8 mg/kg. Żadne doniesienia nie dotyczyły podawania błękitu metylenowego innymi drogami (takimi jak tabletki doustne lub miejscowe wstrzyknięcie do tkanek) lub w niższych dawkach. Mogą zaistnieć okoliczności, w których konieczne jest rozpoczęcie leczenia MAOI, takim jak linezolid lub dożylnie błękit metylenowy, u pacjenta przyjmującego Effexor 37,5 mg XR. Effexor XR należy odstawić przed rozpoczęciem leczenia IMAO [patrz PRZECIWWSKAZANIA , DAWKOWANIE I SPOSÓB PODAWANIA , oraz INTERAKCJE Z LEKAMI ].
Jeśli jednoczesne stosowanie produktu Effexor 37,5 mg XR z innymi lekami serotoninergicznymi (np. tryptany, trójpierścieniowe leki przeciwdepresyjne, mirtazapina, fentanyl, lit, tramadol, buspiron, amfetamina, tryptofan lub ziele dziurawca) jest uzasadnione klinicznie, uważna obserwacja pacjentów, szczególnie podczas rozpoczynania leczenia i zwiększania dawki [patrz INTERAKCJE Z LEKAMI ]. Pacjenci powinni być świadomi potencjalnego ryzyka wystąpienia zespołu serotoninowego. W przypadku wystąpienia powyższych zdarzeń należy natychmiast przerwać leczenie produktem Effexor XR i innymi jednocześnie stosowanymi środkami serotoninergicznymi i rozpocząć wspomagające leczenie objawowe.
Wzrost ciśnienia krwi
W kontrolowanych badaniach zaobserwowano zależne od dawki wzrosty skurczowego i rozkurczowego ciśnienia krwi, a także przypadki utrzymującego się nadciśnienia [patrz DZIAŁANIA NIEPOŻĄDANE ].
Monitoruj ciśnienie krwi przed rozpoczęciem leczenia lekiem Effexor 37,5 mg XR i regularnie w trakcie leczenia. Przed rozpoczęciem leczenia preparatem Effexor 75 mg XR należy kontrolować istniejące nadciśnienie. Należy zachować ostrożność podczas leczenia pacjentów z istniejącym wcześniej nadciśnieniem lub chorobami sercowo-naczyniowymi lub mózgowo-naczyniowymi, które mogą być osłabione przez wzrost ciśnienia krwi. Długotrwały wzrost ciśnienia krwi może prowadzić do niekorzystnych wyników. Zgłaszano przypadki podwyższonego ciśnienia krwi wymagające natychmiastowego leczenia po zastosowaniu leku Effexor XR. Rozważyć zmniejszenie dawki lub przerwanie leczenia u pacjentów, u których występuje utrzymujący się wzrost ciśnienia krwi.
We wszystkich badaniach klinicznych produktu Effexor 37,5 mg u 1,4% pacjentów w grupach leczonych produktem Effexor XR wystąpił wzrost rozkurczowego ciśnienia krwi (SDBP) o ≥15 mm Hg o ≥ 105 mm Hg w porównaniu z 0,9% pacjentów w grupach otrzymujących placebo. Podobnie, 1% pacjentów w grupach leczonych produktem Effexor 75 mg XR doświadczyło wzrostu skurczowego ciśnienia krwi o ≥ 20 mm Hg (SSBP) przy ciśnieniu krwi ≥ 180 mm Hg, w porównaniu z 0,3% pacjentów w grupach placebo [patrz Tabela 10. w DZIAŁANIA NIEPOŻĄDANE ]. Leczenie produktem Effexor 75 mg XR wiązało się z utrzymującym się nadciśnieniem tętniczym (zdefiniowanym jako SDBP pojawiające się w trakcie leczenia ≥ 90 mm Hg i ≥ 10 mm Hg powyżej wartości wyjściowej dla trzech kolejnych wizyt w trakcie terapii [patrz Tabela 11 w DZIAŁANIA NIEPOŻĄDANE ]. W badaniach klinicznych niewystarczająca liczba pacjentów otrzymywała średnie dawki produktu Effexor 37,5 mg XR powyżej 300 mg na dobę, aby w pełni ocenić częstość występowania utrzymującego się wzrostu ciśnienia krwi przy tych większych dawkach.
Nieprawidłowe krwawienie
SSRI i SNRI, w tym Effexor 37,5 mg XR, mogą zwiększać ryzyko krwawień, od wybroczyn, krwiaków, krwawienia z nosa, wybroczyn i krwotoków z przewodu pokarmowego do krwotoków zagrażających życiu. Jednoczesne stosowanie aspiryny, niesteroidowych leków przeciwzapalnych (NLPZ), warfaryny i innych leków przeciwzakrzepowych lub innych leków, o których wiadomo, że wpływają na czynność płytek krwi, może zwiększać to ryzyko. Opisy przypadków i badania epidemiologiczne (kontrola przypadków i projekt kohortowy) wykazały związek między stosowaniem leków zakłócających wychwyt zwrotny serotoniny a występowaniem krwawienia z przewodu pokarmowego. Należy zwrócić uwagę pacjentów na ryzyko krwawienia związane z jednoczesnym stosowaniem produktu Effexor 75 mg XR i NLPZ, aspiryny lub innych leków wpływających na krzepnięcie.
Jaskra zamykającego się kąta
Rozszerzenie źrenicy, które występuje po zastosowaniu wielu leków przeciwdepresyjnych, w tym Effexor XR, może wywołać atak zamykania kąta u pacjenta z anatomicznie wąskim kątem, który nie ma drożnej tęczówki.
Aktywacja manii/hipomanii
badaniach przed wprowadzeniem do obrotu dotyczących MDD, SAD i PD pacjentów leczonych produktem Effexor w dawce 37,5 mg XR zgłaszano manię lub hipomanię (patrz Tabela 2). Manię/hipomanię zgłaszano również u niewielkiego odsetka pacjentów z zaburzeniami nastroju, którzy byli leczeni innymi dostępnymi na rynku lekami w leczeniu MDD. Effexor 37,5 mg XR należy stosować ostrożnie u pacjentów z manią lub hipomanią w wywiadzie.
Zespół odstawienia
Objawy odstawienne były systematycznie oceniane u pacjentów przyjmujących wenlafaksynę, włączając w to prospektywne analizy badań klinicznych dotyczących GAD oraz retrospektywne przeglądy badań dotyczących MDD i SAD. Stwierdzono, że nagłe odstawienie lub zmniejszenie dawki wenlafaksyny w różnych dawkach wiąże się z pojawieniem się nowych objawów, których częstość wzrasta wraz ze wzrostem dawki i dłuższym czasem trwania leczenia. Zgłaszane objawy obejmują pobudzenie, anoreksję, lęk, splątanie, zaburzenia koordynacji i równowagi, biegunkę, zawroty głowy, suchość w ustach, nastrój dysforyczny, drętwienie, zmęczenie, objawy grypopodobne, bóle głowy, hipomanię, bezsenność, nudności, nerwowość, koszmary senne, zaburzenia czucia ( w tym odczucia elektryczne podobne do wstrząsu), senność, pocenie się, drżenie, zawroty głowy i wymioty.
Istnieją doniesienia po wprowadzeniu do obrotu o poważnych objawach odstawienia, które mogą być przewlekłe i ciężkie. U pacjentów po zmniejszeniu dawki produktu Effexor 75 mg XR, w tym podczas odstawienia, u pacjentów obserwowano całkowite samobójstwo, myśli samobójcze, agresję i zachowania agresywne. Inne doniesienia po wprowadzeniu do obrotu opisują zmiany widzenia (takie jak niewyraźne widzenie lub problemy z koncentracją) i podwyższone ciśnienie krwi po odstawieniu lub zmniejszeniu dawki leku Effexor XR.
Podczas wprowadzania do obrotu produktu Effexor XR, innych leków SNRI i SSRI pojawiły się spontaniczne doniesienia o innych zdarzeniach niepożądanych występujących po odstawieniu tych leków, zwłaszcza nagłych, w tym: drażliwość, letarg, chwiejność emocjonalna, szum w uszach i drgawki.
Pacjentów należy monitorować pod kątem tych objawów po przerwaniu leczenia produktem Effexor XR. Zaleca się stopniowe zmniejszanie dawki, a nie nagłe zaprzestanie. Jeśli po zmniejszeniu dawki lub po przerwaniu leczenia wystąpią objawy nie do zniesienia, można rozważyć wznowienie wcześniej przepisanej dawki. Następnie lekarz może kontynuować zmniejszanie dawki, ale w bardziej stopniowym tempie. U niektórych pacjentów może być konieczne przerwanie leczenia w ciągu kilku miesięcy [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Napady padaczkowe
Podczas leczenia wenlafaksyną wystąpiły napady drgawkowe. Effexor 75 mg XR, podobnie jak wiele leków przeciwdepresyjnych, należy stosować ostrożnie u pacjentów z drgawkami w wywiadzie i należy go odstawić u każdego pacjenta, u którego wystąpią drgawki. [Musi złagodzić ryzyko: czynniki ryzyka, towarzyszące leki, które obniżają próg drgawkowy.]
Hiponatremia
Hiponatremia może wystąpić w wyniku leczenia SSRI i SNRI, w tym Effexor 37,5 mg XR. W wielu przypadkach hiponatremia wydaje się być wynikiem zespołu nieprawidłowego wydzielania hormonu antydiuretycznego (SIADH). Zgłaszano przypadki ze stężeniem sodu w surowicy poniżej 110 mmol/l. Pacjenci w podeszłym wieku mogą być bardziej narażeni na rozwój hiponatremii w przypadku SSRI i SNRI [patrz Używaj w określonych populacjach ]. Również pacjenci przyjmujący leki moczopędne lub ci, którzy w inny sposób są odwodnieni, mogą być narażeni na większe ryzyko. Należy rozważyć przerwanie leczenia produktem Effexor 37,5 mg XR u pacjentów z objawową hiponatremią i zastosować odpowiednią interwencję medyczną.
Oznaki i objawy hiponatremii obejmują ból głowy, trudności z koncentracją, zaburzenia pamięci, splątanie, osłabienie i chwiejność, które mogą prowadzić do upadków. Oznaki i objawy związane z cięższymi i/lub ostrymi przypadkami obejmowały halucynacje, omdlenia, drgawki, śpiączkę, zatrzymanie oddechu i śmierć.
Zmiany masy ciała i wzrostu u pacjentów pediatrycznych
Zmiany wagi
Średnia zmiana masy ciała i częstość utraty masy ciała (odsetek pacjentów, którzy stracili 3,5% lub więcej) w kontrolowanych placebo badaniach pediatrycznych dotyczących MDD, GAD i SAD przedstawiono w tabelach 3 i 4.
Utrata masy ciała nie ograniczała się do pacjentów z anoreksją związaną z leczeniem [patrz Zmiany apetytu u pacjentów pediatrycznych ].
Ryzyko związane z długotrwałym stosowaniem leku Effexor 75 mg XR oceniono w otwartym badaniu MDD u dzieci i młodzieży, które otrzymywały lek Effexor XR przez okres do sześciu miesięcy. U dzieci i młodzieży biorących udział w badaniu przyrost masy ciała był mniejszy niż oczekiwano, na podstawie danych uzyskanych od rówieśników dobranych pod względem wieku i płci. Różnica między zaobserwowanym przyrostem masy ciała a oczekiwanym przyrostem masy ciała była większa u dzieci (
Zmiany wysokości
Tabela 5 przedstawia średni wzrost wzrostu u pacjentów pediatrycznych w krótkoterminowych, kontrolowanych placebo badaniach MDD, GAD i SAD. Różnice we wzroście w badaniach GAD i MDD były najbardziej zauważalne u pacjentów w wieku poniżej 12 lat.
W sześciomiesięcznym, otwartym badaniu MDD, wzrost wzrostu dzieci i młodzieży był mniejszy niż oczekiwano, na podstawie danych uzyskanych od rówieśników dobranych pod względem wieku i płci. Różnica między obserwowanym a oczekiwanym tempem wzrostu była większa u dzieci (
Zmiany apetytu u pacjentów pediatrycznych
Zmniejszony apetyt (zgłaszany jako jadłowstręt związany z leczeniem) był częściej obserwowany u pacjentów leczonych produktem Effexor XR w porównaniu z pacjentami otrzymującymi placebo w ocenie produktu Effexor XR przed wprowadzeniem do obrotu pod kątem MDD, GAD i SAD (patrz Tabela 6).
Śródmiąższowa choroba płuc i eozynofilowe zapalenie płuc
Rzadko zgłaszano śródmiąższową chorobę płuc i eozynofilowe zapalenie płuc związane z leczeniem wenlafaksyną. Możliwość wystąpienia tych działań niepożądanych należy rozważyć u pacjentów leczonych wenlafaksyną, u których występuje postępująca duszność, kaszel lub dyskomfort w klatce piersiowej. Tacy pacjenci powinni zostać niezwłocznie poddani ocenie lekarskiej i należy rozważyć przerwanie leczenia wenlafaksyną.
Seksualna dysfunkcja
Stosowanie SNRI, w tym Effexor XR, może powodować objawy dysfunkcji seksualnych [patrz DZIAŁANIA NIEPOŻĄDANE ]. U pacjentów płci męskiej stosowanie SNRI może skutkować opóźnieniem lub niepowodzeniem wytrysku, zmniejszeniem libido i zaburzeniami erekcji. U pacjentek stosowanie SNRI może skutkować obniżeniem libido i opóźnieniem lub brakiem orgazmu.
Ważne jest, aby lekarze przepisujący lek pytali o funkcje seksualne przed rozpoczęciem leczenia produktem Effexor 37,5 mg XR i pytali konkretnie o zmiany funkcji seksualnych podczas leczenia, ponieważ funkcje seksualne mogą nie być zgłaszane spontanicznie. Podczas oceny zmian funkcji seksualnych ważne jest zebranie szczegółowej historii (w tym czasu wystąpienia objawów), ponieważ objawy seksualne mogą mieć inne przyczyny, w tym leżące u ich podstaw zaburzenia psychiczne. Omów potencjalne strategie postępowania, aby wspierać pacjentów w podejmowaniu świadomych decyzji dotyczących leczenia.
Informacje dotyczące poradnictwa dla pacjentów
Zobacz zatwierdzone przez FDA INFORMACJA O PACJENCIE ( Przewodnik po lekach ).
Lekarze przepisujący lek lub inni pracownicy służby zdrowia powinni informować pacjentów, ich rodziny i ich opiekunów o korzyściach i zagrożeniach związanych z leczeniem produktem Effexor 37,5 mg XR oraz powinni doradzić im właściwe stosowanie. Dla Effexor 75 mg XR dostępny jest przewodnik po lekach dla pacjentów na temat „Leków przeciwdepresyjnych, depresji i innych poważnych chorób psychicznych oraz myśli lub działań samobójczych”. Lekarz przepisujący lek lub pracownik służby zdrowia powinien poinstruować pacjentów, ich rodziny i ich opiekunów, aby przeczytali Przewodnik dotyczący leków i powinni pomóc im w zrozumieniu jego treści. Pacjenci powinni mieć możliwość omówienia treści Przewodnika po lekach i uzyskania odpowiedzi na wszelkie pytania, jakie mogą mieć. Pełny tekst Przewodnika po lekach jest przedrukowany na końcu tego dokumentu. Pacjentów należy poinformować o następujących kwestiach i poprosić ich o powiadomienie lekarza przepisującego lek, jeśli wystąpią one podczas przyjmowania leku Effexor XR.
Myśli i zachowania samobójcze
Doradź pacjentom, ich rodzinom i opiekunom, aby zwracali uwagę na pojawienie się myśli samobójczych, nasilenia depresji i innych objawów psychicznych (lęk, pobudzenie, napady paniki, bezsenność, drażliwość, wrogość, agresywność, impulsywność, akatyzja, niepokój psychoruchowy, hipomania, mania, inne nietypowe zmiany w zachowaniu), zwłaszcza na początku leczenia i gdy dawka jest zwiększana lub zmniejszana. Takie objawy należy zgłaszać lekarzowi przepisującemu pacjentowi lub pracownikowi służby zdrowia, zwłaszcza jeśli są one ciężkie, mają nagły początek lub nie były częścią objawów występujących u pacjenta. Takie objawy mogą wiązać się ze zwiększonym ryzykiem myśli i zachowań samobójczych i wskazują na potrzebę bardzo ścisłego monitorowania [patrz PUDEŁKO OSTRZEŻENIE oraz OSTRZEŻENIA I ŚRODKI ].
Leki towarzyszące
Należy doradzić pacjentom przyjmującym Effexor XR, aby nie stosowali jednocześnie innych produktów zawierających wenlafaksynę lub deswenlafaksynę. Pracownicy służby zdrowia powinni poinstruować pacjentów, aby nie przyjmowali leku Effexor XR z IMAO lub w ciągu 14 dni od odstawienia IMAO oraz 7 dni po odstawieniu leku Effexor XR przed rozpoczęciem stosowania IMAO [patrz PRZECIWWSKAZANIA ].
Zespół serotoninowy
Należy ostrzec pacjentów o ryzyku wystąpienia zespołu serotoninowego przy jednoczesnym stosowaniu produktu Effexor 75 mg XR i tryptanów, tramadolu, amfetaminy, suplementów tryptofanu, z lekami przeciwpsychotycznymi lub innymi antagonistami dopaminy lub innymi środkami serotoninergicznymi [patrz OSTRZEŻENIA I ŚRODKI oraz INTERAKCJE Z LEKAMI ].
Podwyższone ciśnienie krwi
Poinformuj pacjentów, że powinni regularnie monitorować ciśnienie krwi podczas przyjmowania leku Effexor XR [patrz OSTRZEŻENIA I ŚRODKI ].
Nieprawidłowe krwawienie
Należy ostrzec pacjentów przed jednoczesnym stosowaniem produktu Effexor 75 mg XR i NLPZ, aspiryny, warfaryny lub innych leków wpływających na krzepnięcie, ponieważ łączne stosowanie leków psychotropowych zaburzających wychwyt zwrotny serotoniny i tych środków wiąże się ze zwiększonym ryzykiem krwawienia [patrz OSTRZEŻENIA I ŚRODKI ].
Jaskra zamykającego się kąta
Należy poinformować pacjentów, że przyjmowanie leku Effexor XR może powodować łagodne rozszerzenie źrenic, które u osób podatnych może prowadzić do epizodu jaskry zamykającego się kąta. Wcześniej istniejąca jaskra jest prawie zawsze jaskrą otwartego kąta, ponieważ jaskra zamkniętego kąta, po zdiagnozowaniu, może być ostatecznie leczona za pomocą irydektomii. Jaskra otwartego kąta nie jest czynnikiem ryzyka jaskry zamykającego się kąta. Pacjenci mogą chcieć zostać przebadani w celu ustalenia, czy są podatni na zamknięcie kąta i przejść zabieg profilaktyczny (np. irydektomia), jeśli są podatni [patrz OSTRZEŻENIA I ŚRODKI ].
Aktywacja manii/hipomanii
Doradź pacjentom, ich rodzinom i opiekunom, aby obserwowali oznaki aktywacji manii/hipomanii [patrz OSTRZEŻENIA I ŚRODKI ].
Choroba sercowo-naczyniowa/mózgowo-naczyniowa
Zaleca się ostrożność podczas podawania produktu Effexor XR pacjentom z zaburzeniami krążenia, naczyń mózgowych lub metabolizmu lipidów [patrz DZIAŁANIA NIEPOŻĄDANE ].
Podwyższenie poziomu cholesterolu i trójglicerydów w surowicy
Poinformuj pacjentów, że może wystąpić podwyższenie poziomu cholesterolu całkowitego, LDL i triglicerydów oraz że można rozważyć pomiar stężenia lipidów w surowicy [patrz OSTRZEŻENIA I ŚRODKI ].
Zespół odstawienia
Poradź pacjentom, aby nie przerywali przyjmowania leku Effexor 75 mg XR bez uprzedniej rozmowy z lekarzem. Pacjenci powinni być świadomi, że przerwanie leczenia może wystąpić podczas odstawiania leku Effexor XR [patrz OSTRZEŻENIA I ŚRODKI oraz DZIAŁANIA NIEPOŻĄDANE ].
Seksualna dysfunkcja
Poinformuj pacjentów, że stosowanie Effexor XR może powodować objawy dysfunkcji seksualnej zarówno u pacjentów płci męskiej, jak i żeńskiej. Poinformuj pacjentów, że powinni omówić wszelkie zmiany funkcji seksualnych i potencjalne strategie postępowania ze swoim lekarzem [patrz OSTRZEŻENIA I ŚRODKI ].
Zakłócenia sprawności poznawczej i motorycznej
Przestrzegaj pacjentów przed obsługą niebezpiecznych maszyn, w tym samochodów, dopóki nie upewnią się, że terapia Effexor 37,5 mg XR nie wpływa negatywnie na ich zdolność do wykonywania takich czynności.
Alkohol
Poradzić pacjentom, aby unikali alkoholu podczas przyjmowania leku Effexor 37,5 mg XR [patrz INTERAKCJE Z LEKAMI ].
Reakcje alergiczne
Poradź pacjentom, aby powiadomili swojego lekarza, jeśli wystąpią objawy alergiczne, takie jak wysypka, pokrzywka, obrzęk lub trudności w oddychaniu.
Ciąża
Poradzić pacjentkom, aby powiadomiły lekarza, jeśli zajdą w ciążę lub zamierzają zajść w ciążę podczas leczenia [patrz Używaj w określonych populacjach ].
Pielęgniarstwo
Doradź pacjentom, aby powiadomili swojego lekarza, jeśli karmią piersią niemowlę [patrz Używaj w określonych populacjach ].
Resztkowe sferoidy
Effexor XR zawiera sferoidy, które powoli uwalniają lek do przewodu pokarmowego. Nierozpuszczalna część tych sferoidów jest eliminowana, a pacjenci mogą zauważyć sferoidy przechodzące w kale lub przez kolostomię. Pacjentów należy poinformować, że aktywny lek został już wchłonięty, zanim pacjent zobaczy sferoidy.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Karcynogeneza
Nowotwory nie zwiększały się po leczeniu wenlafaksyną u myszy lub szczurów. Wenlafaksynę podawano myszom przez zgłębnik doustny przez 18 miesięcy w dawkach do 120 mg/kg na dobę, co stanowiło 1,7-krotność maksymalnej zalecanej dawki u ludzi w przeliczeniu na mg/m2. Wenlafaksynę podawano również szczurom przez zgłębnik doustny przez 24 miesiące w dawkach do 120 mg/kg na dobę. U szczurów otrzymujących dawkę 120 mg/kg stężenie wenlafaksyny w osoczu podczas sekcji zwłok było 1-krotne (samce szczurów) i 6-krotne (samice szczurów) od stężenia w osoczu pacjentów otrzymujących maksymalną zalecaną dawkę u ludzi. Poziomy O-demetylowego metabolitu (ODV) w osoczu były niższe u szczurów niż u pacjentów otrzymujących maksymalną zalecaną dawkę. O-demetylowenlafaksyna (ODV), główny ludzki metabolit wenlafaksyny, podawana przez zgłębnik doustny myszom i szczurom przez 2 lata nie zwiększała częstości występowania nowotworów w żadnym z badań. Myszy otrzymywały ODV w dawkach do 500/300 mg/kg/dzień (dawka obniżona po 45 tygodniach dawkowania). Ekspozycja przy dawce 300 mg/kg/dobę jest 9 razy większa od dawki 225 mg/dobę stosowanej u ludzi. Szczury otrzymywały ODV w dawkach do 300 mg/kg/dzień (samce) lub 500 mg/kg/dzień (samice). Ekspozycja przy najwyższej dawce jest około 8 (mężczyźni) lub 11 (kobiety) razy większa od dawki 225 mg/dobę stosowanej u ludzi.
Mutageneza
Wenlafaksyna i główny metabolit ludzki, ODV, nie wykazywały działania mutagennego w teście powrotnej mutacji Amesa w bakteriach Salmonella lub teście mutacji genowej do przodu w komórkach jajnika chomika chińskiego/HGPRT ssaków. Wenlafaksyna nie wykazywała również działania mutagennego ani klastogennego w teście transformacji komórek myszy BALB/c-3T3 in vitro, teście wymiany chromatyd siostrzanych w hodowanych komórkach jajnika chomika chińskiego ani w teście aberracji chromosomowych in vivo w szpiku kostnym szczura. ODV nie wykazywał działania klastogennego w teście aberracji chromosomowych komórek jajnika chomika chińskiego in vitro ani w teście aberracji chromosomowych in vivo u szczurów.
Upośledzenie płodności
Badania rozrodczości i płodności wenlafaksyny u szczurów nie wykazały niepożądanego wpływu wenlafaksyny na płodność samców i samic po podaniu doustnych dawek do 2 razy większych od maksymalnej zalecanej dawki u ludzi, wynoszącej 225 mg/dobę w przeliczeniu na mg/m2. Jednak w badaniu, w którym samce i samice szczurów leczono O-demetylowenlafaksyną (ODV), głównym ludzkim metabolitem wenlafaksyny, przed oraz podczas kojarzenia i ciąży, zaobserwowano zmniejszoną płodność. Miało to miejsce przy ekspozycji ODV (AUC) około 2 do 3 razy większej niż w przypadku dawki ludzkiej wenlafaksyny 225 mg/dobę.
Używaj w określonych populacjach
Ciąża
Efekty teratogenne
Ciąża Kategoria C
Wenlafaksyna nie powodowała wad rozwojowych u potomstwa szczurów lub królików, którym podawano dawki do 2,5-krotności (szczury) lub 4-krotności (królik) maksymalnej zalecanej dawki dobowej u ludzi w przeliczeniu na mg/m2. Jednak u szczurów zaobserwowano zmniejszenie masy potomstwa, wzrost potomstwa martwo urodzonych oraz wzrost śmiertelności młodych w ciągu pierwszych 5 dni laktacji, gdy dawkowanie rozpoczęto w czasie ciąży i kontynuowano aż do odsadzenia. Przyczyna tych zgonów nie jest znana. Efekty te wystąpiły przy 2,5-krotności (mg/m2) maksymalnej dawki dobowej dla człowieka. Dawka niepowodująca efektu w przypadku śmiertelności młodych szczurów była 0,25 razy większa od dawki dla ludzi w przeliczeniu na mg/m2. W badaniach dotyczących rozwoju rozrodczego szczurów i królików z O-demetylowenlafaksyną (ODV), głównym ludzkim metabolitem wenlafaksyny, nie obserwowano dowodów działania teratogennego przy marginesach ekspozycji wynoszących 13 u szczurów i 0,3 u królików. Nie ma odpowiednich i dobrze kontrolowanych badań u kobiet w ciąży. Effexor XR powinien być stosowany w okresie ciąży tylko wtedy, gdy potencjalna korzyść uzasadnia potencjalne ryzyko dla płodu. Ponieważ badania reprodukcji na zwierzętach nie zawsze pozwalają przewidzieć reakcję człowieka, lek ten powinien być stosowany w czasie ciąży tylko wtedy, gdy jest to bezwzględnie konieczne.
Efekty nieteratogenne
U noworodków narażonych na działanie produktu Effexor 37,5 mg XR, innych leków SNRI lub SSRI pod koniec trzeciego trymestru wystąpiły powikłania wymagające przedłużonej hospitalizacji, wspomagania oddychania i karmienia przez sondę. Takie komplikacje mogą pojawić się natychmiast po porodzie. Zgłaszane objawy kliniczne obejmowały niewydolność oddechową, sinicę, bezdech, drgawki, niestabilność temperatury, trudności w karmieniu, wymioty, hipoglikemię, hipotonię, hipertonię, hiperrefleksję, drżenie, drżenie, drażliwość i ciągły płacz. Cechy te są zgodne albo z bezpośrednim toksycznym działaniem SSRI i SNRI, albo z zespołem odstawienia leku. Należy zauważyć, że w niektórych przypadkach obraz kliniczny jest zgodny z zespołem serotoninowym [patrz OSTRZEŻENIA I ŚRODKI oraz INTERAKCJE Z LEKAMI ]. Podczas leczenia kobiety w ciąży produktem Effexor XR w trzecim trymestrze lekarz powinien dokładnie rozważyć potencjalne ryzyko i korzyści leczenia.
Praca i dostawa
Wpływ wenlafaksyny na poród i poród u ludzi jest nieznany.
Matki karmiące
Zgłaszano, że wenlafaksyna i ODV przenikają do mleka ludzkiego. Ze względu na możliwość wystąpienia poważnych działań niepożądanych u karmionych niemowląt produktem Effexor XR należy podjąć decyzję, czy przerwać karmienie piersią, czy przerwać stosowanie leku, biorąc pod uwagę znaczenie leku dla matki.
Zastosowanie pediatryczne
Przeprowadzono dwa kontrolowane placebo badania z udziałem 766 pacjentów pediatrycznych z MDD i dwa kontrolowane placebo badania z udziałem 793 pacjentów pediatrycznych z GAD z użyciem preparatu Effexor XR, a dane nie były wystarczające, aby uzasadnić twierdzenie o stosowaniu u dzieci.
Każdy, kto rozważa zastosowanie leku Effexor XR u dzieci lub młodzieży, musi zrównoważyć potencjalne ryzyko z potrzebą kliniczną [patrz PUDEŁKO OSTRZEŻENIE , OSTRZEŻENIA I ŚRODKI oraz DZIAŁANIA NIEPOŻĄDANE ].
Chociaż żadne badania nie zostały zaprojektowane w celu oceny przede wszystkim wpływu leku Effexor 37,5 mg XR na wzrost, rozwój i dojrzewanie dzieci i młodzieży, przeprowadzone badania sugerują, że Effexor XR może niekorzystnie wpływać na wagę i wzrost [patrz OSTRZEŻENIA I ŚRODKI ]. W przypadku podjęcia decyzji o leczeniu pacjenta pediatrycznego produktem Effexor XR zaleca się regularne monitorowanie masy ciała i wzrostu podczas leczenia, zwłaszcza jeśli leczenie ma być kontynuowane przez długi czas [patrz OSTRZEŻENIA I ŚRODKI ]. Bezpieczeństwo leczenia produktem Effexor 75 mg XR u dzieci nie było systematycznie oceniane w przypadku leczenia przewlekłego trwającego dłużej niż sześć miesięcy. W badaniach przeprowadzonych u dzieci (w wieku 6-17 lat) występowanie wzrostu ciśnienia krwi i cholesterolu, które uznano za klinicznie istotne u dzieci, było podobne do obserwowanego u dorosłych pacjentów. W związku z tym środki ostrożności dla dorosłych dotyczą pacjentów pediatrycznych [patrz OSTRZEŻENIA I ŚRODKI ].
Zastosowanie geriatryczne
W Tabeli 15 przedstawiono odsetek pacjentów w wieku 65 lat lub starszych biorących udział w badaniach klinicznych produktu Effexor 37,5 mg XR na MDD, GAD, SAD i PD.
Nie zaobserwowano ogólnych różnic w skuteczności lub bezpieczeństwie między pacjentami w podeszłym wieku a młodszymi pacjentami, a inne doniesienia kliniczne na ogół nie wykazały różnic w odpowiedzi między pacjentami w podeszłym wieku i młodszymi. Nie można jednak wykluczyć większej wrażliwości niektórych osób starszych. SSRI i SNRI, w tym Effexor XR, były związane z przypadkami klinicznie istotnej hiponatremii u pacjentów w podeszłym wieku, którzy mogą być bardziej narażeni na to zdarzenie niepożądane [patrz OSTRZEŻENIA I ŚRODKI ].
Farmakokinetyka wenlafaksyny i ODV nie jest istotnie zmieniona u osób w podeszłym wieku [patrz FARMAKOLOGIA KLINICZNA ] (patrz rysunek 3). Nie zaleca się dostosowywania dawki u osób w podeszłym wieku wyłącznie na podstawie wieku, chociaż inne okoliczności kliniczne, z których niektóre mogą występować częściej u osób w podeszłym wieku, takie jak zaburzenia czynności nerek lub wątroby, mogą uzasadniać zmniejszenie dawki [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Wiek i płeć
Analiza farmakokinetyki populacyjnej 404 pacjentów leczonych produktem Effexor z dwóch badań obejmujących schematy leczenia zarówno dwa razy na dobę, jak i trzy razy na dobę wykazała, że znormalizowane dawki minimalne wenlafaksyny lub ODV w osoczu nie ulegały zmianie w zależności od wieku lub płci. Dostosowanie dawki w zależności od wieku lub płci pacjenta na ogół nie jest konieczne [patrz DAWKOWANIE I SPOSÓB PODAWANIA ] (patrz Tabela 15).
Stosowanie w podgrupach pacjentów
Rycina 3: Farmakokinetyka wenlafaksyny i jej metabolitu O-desmetylowenlafaksyny (ODV) w szczególnych populacjach.
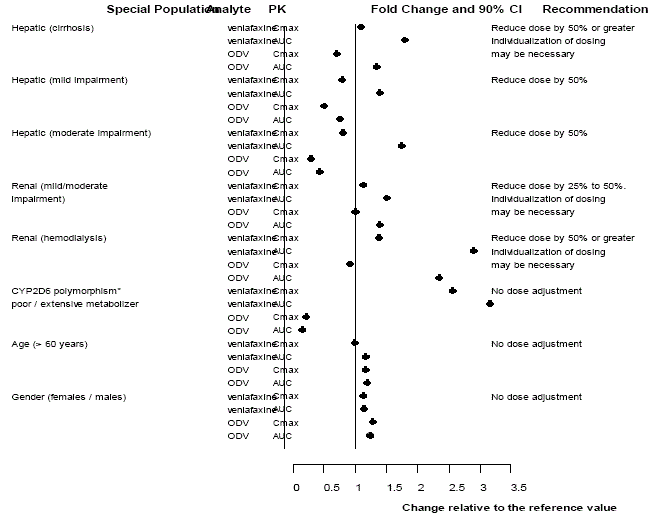
PRZEDAWKOWAĆ
Ludzkie doświadczenie
Podczas ocen przed wprowadzeniem do obrotu produktu Effexor 75 mg XR (dla MDD, GAD, SAD i PD) i Effexor (dla MDD) odnotowano dwadzieścia zgłoszeń ostrego przedawkowania produktu Effexor (odpowiednio 6 i 14 zgłoszeń u pacjentów z produktem Effexor XR i Effexor 75 mg). , samodzielnie lub w połączeniu z innymi narkotykami i/lub alkoholem.
Najczęściej zgłaszanym objawem była senność. Wśród innych zgłaszanych objawów były parestezje wszystkich czterech kończyn, umiarkowane zawroty głowy, nudności, drętwienie rąk i stóp oraz okresy gorąca i przeziębienia 5 dni po przedawkowaniu. W większości przypadków z przedawkowaniem nie wiązały się żadne oznaki ani objawy. Większość zgłoszeń dotyczyła połknięcia, w którym całkowita pobrana dawka wenlafaksyny była oszacowana na nie więcej niż kilkakrotnie wyższa niż zwykła dawka terapeutyczna. U jednego pacjenta, który przyjął 2,75 g wenlafaksyny zaobserwowano dwa uogólnione drgawki i wydłużenie odstępu QTc do 500 ms, w porównaniu z 405 ms na początku. U dwóch pozostałych pacjentów zgłoszono łagodną częstoskurcz zatokowy.
Działania podjęte w celu leczenia przedawkowania obejmowały brak leczenia, hospitalizację i leczenie objawowe oraz hospitalizację z leczeniem węglem aktywowanym. Wszyscy pacjenci wyzdrowieli.
doświadczenia po wprowadzeniu produktu do obrotu wynika, że przedawkowanie wenlafaksyny występowało głównie w połączeniu z alkoholem i (lub) innymi lekami. Najczęściej zgłaszanymi zdarzeniami przedawkowania są częstoskurcz, zmiany w stanie świadomości (od senności do śpiączki), rozszerzenie źrenic, drgawki i wymioty.
Zgłaszano zmiany w elektrokardiogramie (np. wydłużenie odstępu QT, blok odnogi pęczka Hisa, wydłużenie zespołu QRS), częstoskurcz komorowy, bradykardię, niedociśnienie, rabdomiolizę, zawroty głowy, martwicę wątroby, zespół serotoninowy i zgon.
Opublikowane badania retrospektywne wskazują, że przedawkowanie wenlafaksyny może wiązać się ze zwiększonym ryzykiem zgonu w porównaniu z obserwowanym w przypadku leków przeciwdepresyjnych SSRI, ale niższym niż w przypadku trójpierścieniowych leków przeciwdepresyjnych. Badania epidemiologiczne wykazały, że pacjenci leczeni wenlafaksyną są bardziej obciążeni czynnikami ryzyka samobójstwa niż pacjenci leczeni SSRI. Nie jest jasne, w jakim stopniu stwierdzenie zwiększonego ryzyka zgonu można przypisać toksyczności wenlafaksyny po przedawkowaniu, w przeciwieństwie do niektórych cech charakterystycznych pacjentów leczonych wenlafaksyną. Recepty na Effexor 75mg XR należy wypisać na najmniejszą ilość kapsułek zgodnie z dobrym postępowaniem z pacjentem, aby zmniejszyć ryzyko przedawkowania.
Zarządzanie przedawkowaniem
Skonsultuj się z Certyfikowanym Centrum Kontroli Zatruć w celu uzyskania aktualnych wskazówek i porad (1-800-222-1222 lub www.poison.org). W przypadku przedawkowania należy zapewnić opiekę podtrzymującą, w tym ścisły nadzór i monitorowanie lekarskie. Leczenie powinno polegać na zastosowaniu ogólnych środków stosowanych w przypadku przedawkowania jakiegokolwiek leku. Rozważ możliwość wielokrotnego przedawkowania leków. Zapewnić odpowiednie drogi oddechowe, natlenienie i wentylację. Monitoruj rytm serca i parametry życiowe. Zapewnij środki wspomagające i objawowe.
PRZECIWWSKAZANIA
Nadwrażliwość
Nadwrażliwość na chlorowodorek wenlafaksyny, bursztynian deswenlafaksyny lub na którąkolwiek substancję pomocniczą preparatu
Jednoczesne stosowanie z inhibitorami monoaminooksydazy (MAOI)
Stosowanie inhibitorów MAO (przeznaczonych do leczenia zaburzeń psychicznych) jednocześnie z preparatem Effexor 75 mg XR lub w ciągu 7 dni od przerwania leczenia preparatem Effexor XR jest przeciwwskazane ze względu na zwiększone ryzyko wystąpienia zespołu serotoninowego. Przeciwwskazane jest również stosowanie produktu Effexor 37,5 mg XR w ciągu 14 dni od zaprzestania leczenia IMAO (przeznaczonym do leczenia zaburzeń psychicznych) [patrz DAWKOWANIE I SPOSÓB PODAWANIA , OSTRZEŻENIA I ŚRODKI , oraz INTERAKCJE Z LEKAMI ].
Rozpoczęcie stosowania preparatu Effexor XR u pacjenta leczonego MAOI, takim jak linezolid lub dożylnie błękit metylenowy, jest również przeciwwskazane ze względu na zwiększone ryzyko wystąpienia zespołu serotoninowego [patrz DAWKOWANIE I SPOSÓB PODAWANIA , OSTRZEŻENIA I ŚRODKI , oraz INTERAKCJE Z LEKAMI ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Dokładny mechanizm przeciwdepresyjnego działania wenlafaksyny u ludzi nie jest znany, ale uważa się, że jest on związany z nasileniem serotoniny i noradrenaliny w ośrodkowym układzie nerwowym poprzez hamowanie ich wychwytu zwrotnego. Badania niekliniczne wykazały, że wenlafaksyna i jej aktywny metabolit ODV są silnymi i selektywnymi inhibitorami wychwytu zwrotnego serotoniny i noradrenaliny w neuronach oraz słabymi inhibitorami wychwytu zwrotnego dopaminy.
Farmakodynamika
Wenlafaksyna i ODV nie wykazują znaczącego powinowactwa do receptorów muskarynowo-cholinergicznych, H1-histaminergicznych lub α1 adrenergicznych in vitro. Przypuszcza się, że aktywność farmakologiczna na tych receptorach jest związana z różnymi efektami antycholinergicznymi, uspokajającymi i sercowo-naczyniowymi obserwowanymi w przypadku innych leków psychotropowych. Wenlafaksyna i ODV nie wykazują aktywności hamującej monoaminooksydazę (MAO).
Elektrofizjologia serca
Wpływ wenlafaksyny na odstęp QT oceniano w randomizowanym, podwójnie zaślepionym, kontrolowanym placebo i dodatnim, trzyokresowym, dokładnym badaniu odstępu QT z udziałem 54 zdrowych osób dorosłych. Nie wykryto znaczącego wpływu wenlafaksyny 450 mg na wydłużenie odstępu QT.
Farmakokinetyka
Stężenia wenlafaksyny i ODV w osoczu w stanie stacjonarnym są osiągane w ciągu 3 dni po doustnym podaniu wielokrotnych dawek. Wenlafaksyna i ODV wykazywały kinetykę liniową w zakresie dawek od 75 do 450 mg na dobę. Średni±SD klirens osoczowy wenlafaksyny i ODV w stanie stacjonarnym wynosi odpowiednio 1,3±0,6 i 0,4±0,2 l/h/kg; pozorny okres półtrwania w fazie eliminacji wynosi odpowiednio 5±2 i 11±2 godziny; a pozorna (w stanie stacjonarnym) objętość dystrybucji wynosi odpowiednio 7,5±3,7 i 5,7±1,8 l/kg. Wenlafaksyna i ODV w minimalnym stopniu wiążą się z białkami osocza w stężeniach terapeutycznych (odpowiednio 27% i 30%).
Absorpcja i dystrybucja
Wenlafaksyna jest dobrze wchłaniana i intensywnie metabolizowana w wątrobie. ODV jest głównym aktywnym metabolitem. Na podstawie badań bilansu masy wchłania się co najmniej 92% pojedynczej doustnej dawki wenlafaksyny. Całkowita biodostępność wenlafaksyny wynosi około 45%.
Podawanie produktu Effexor 37,5 mg XR (150 mg raz na dobę) na ogół skutkowało niższymi wartościami Cmax i późniejszymi Tmax niż w przypadku produktu Effexor (o natychmiastowym uwalnianiu) podawanego dwa razy na dobę (Tabela 16). Gdy równe dawki dobowe wenlafaksyny podawano w postaci tabletki o natychmiastowym uwalnianiu lub kapsułki o przedłużonym uwalnianiu, ekspozycja zarówno na wenlafaksynę, jak i na ODV była podobna dla obu terapii, a fluktuacja stężeń w osoczu była nieco mniejsza w przypadku produktu Effexor 37,5 mg. Kapsuła XR. Dlatego Effexor XR zapewnia wolniejsze tempo wchłaniania, ale taki sam stopień wchłaniania w porównaniu z tabletką o natychmiastowym uwalnianiu.
Pokarm nie wpływał na biodostępność wenlafaksyny ani jej aktywnego metabolitu ODV. Czas podania (przed południem lub wieczorem) nie wpływał na farmakokinetykę wenlafaksyny i ODV z kapsułki 75 mg Effexor 75 mg XR.
Wenlafaksyna nie wiąże się silnie z białkami osocza; dlatego podanie produktu Effexor 37,5 mg XR pacjentowi przyjmującemu inny lek silnie związany z białkami nie powinno powodować zwiększenia wolnych stężeń innego leku.
Metabolizm i eliminacja
Po wchłonięciu wenlafaksyna podlega intensywnemu metabolizmowi przedukładowemu w wątrobie, głównie do ODV, ale także do N-demetylowenlafaksyny, N,O-didesmetylowenlafaksyny i innych mniejszych metabolitów. Badania in vitro wskazują, że tworzenie ODV jest katalizowane przez CYP2D6; zostało to potwierdzone w badaniu klinicznym wykazującym, że pacjenci z niskim poziomem CYP2D6 (słabi metabolizujący) mieli podwyższony poziom wenlafaksyny i obniżony poziom ODV w porównaniu do osób z normalnym poziomem CYP2D6 (osoby intensywnie metabolizujące) [patrz Używaj w określonych populacjach ].
Około 87% dawki wenlafaksyny jest odzyskiwane w moczu w ciągu 48 godzin w postaci niezmienionej wenlafaksyny (5%), niesprzężonej ODV (29%), sprzężonej ODV (26%) lub innych mniejszych nieaktywnych metabolitów (27%). Eliminacja nerkowa wenlafaksyny i jej metabolitów jest zatem główną drogą wydalania.
Studia kliniczne
Ciężkie zaburzenie depresyjne
Skuteczność produktu Effexor 75 mg XR (chlorowodorek wenlafaksyny) w postaci kapsułek o przedłużonym uwalnianiu w leczeniu dużych zaburzeń depresyjnych (MDD) ustalono w dwóch kontrolowanych placebo, krótkoterminowych (8 tygodni w badaniu 1; 12 tygodni w badaniu 2), elastycznych -badania dawek, z dawkami rozpoczynającymi się od 75 mg na dobę do 225 mg na dobę u dorosłych pacjentów ambulatoryjnych spełniających kryteria MDD DSM-III-R lub DSM-IV. U pacjentów ambulatoryjnych z umiarkowaną depresją początkowa dawka wenlafaksyny wynosiła 75 mg na dobę. W obu badaniach preparat Effexor XR wykazał wyższość nad placebo w podstawowym pomiarze skuteczności zdefiniowanym jako zmiana od wartości wyjściowej w całkowitym wyniku HAM-D-21 do wizyty w punkcie końcowym, Effexor XR wykazał również wyższość nad placebo w kluczowym drugorzędowym punkcie końcowym skuteczności, klinicznym Globalne wrażenia (CGI) Skala ciężkości choroby. Badanie podzbiorów płci w badanej populacji nie wykazało żadnej zróżnicowanej reaktywności ze względu na płeć.
4-tygodniowe badanie pacjentów hospitalizowanych spełniających kryteria MDD z melancholią DSM-III-R stosujących Effexor 37,5 mg w zakresie od 150 do 375 mg na dobę (podzielonych według schematu 3 razy dziennie) wykazało przewagę produktu Effexor nad placebo na podstawie całkowitego wyniku HAM-D-21. Średnia dawka u osób, które ukończyły leczenie wynosiła 350 mg na dobę (badanie 3).
długoterminowym badaniu dorośli pacjenci ambulatoryjny z MDD, u których wystąpiła odpowiedź podczas 8-tygodniowego otwartego badania Effexor 37,5 mg XR (75, 150 lub 225 mg raz na dobę każdego ranka) zostali losowo przydzieleni do kontynuacji leczenia produktem Effexor. Dawka XR lub placebo przez okres do 26 tygodni obserwacji pod kątem nawrotu. Odpowiedź podczas fazy otwartej zdefiniowano jako wynik CGI ciężkości choroby wynoszący ≤3 i całkowity wynik w skali HAM-D-21 wynoszący ≤10 w 56. dniu oceny. Nawrót podczas fazy podwójnie ślepej próby zdefiniowano w następujący sposób: (1) ponowne pojawienie się dużej depresji zdefiniowanej według kryteriów DSM-IV i punktacja Ciężkości choroby w skali CGI ≥4 (umiarkowanie chory), (2) 2 kolejne CGI Punktacja ciężkości choroby ≥4 lub (3) końcowa punktacja ciężka choroby w skali CGI ≥4 dla każdego pacjenta, który z jakiegokolwiek powodu wycofał się z badania. Pacjenci otrzymujący dalsze leczenie produktem Effexor 37,5 mg XR doświadczyli statystycznie istotnie niższych wskaźników nawrotów w ciągu kolejnych 26 tygodni w porównaniu z pacjentami otrzymującymi placebo (badanie 4).
drugim dłuższym badaniu dorośli pacjenci ambulatoryjny z MDD, typ nawrotowy, u których wystąpiła odpowiedź (całkowity wynik w skali HAM-D21 ≤ 12 w 56. dniu oceny) i nadal odczuwali poprawę [zdefiniowano jako spełnienie następujących kryteriów od 56. do 180. dnia : (1) brak całkowitego wyniku w HAM-D-21 ≥ 20; (2) nie więcej niż 2 całkowite wyniki w skali HAM39 D-21 > 10 oraz (3) brak pojedynczego wyniku CGI w skali ciężkości choroby ≥ 4 (umiarkowanie chory)] w ciągu pierwszych 26 tygodni leczenia produktem Effexor [100 do 200 mg na dzień, w schemacie dwa razy dziennie] zostali losowo przydzieleni do kontynuacji tej samej dawki produktu Effexor lub do placebo. Okres obserwacji pacjentów pod kątem nawrotu, zdefiniowany jako punkt ciężkości choroby ≥ 4 w skali CGI, trwał do 52 tygodni. Pacjenci otrzymujący kontynuację leczenia produktem Effexor doświadczyli statystycznie istotnie niższych wskaźników nawrotów w ciągu kolejnych 52 tygodni w porównaniu z pacjentami otrzymującymi placebo (badanie 5).
Uogólnione zaburzenie lękowe
Skuteczność produktu Effexor XR w leczeniu zespołu lęku uogólnionego (GAD) została potwierdzona w dwóch 8-tygodniowych, kontrolowanych placebo badaniach ze stałą dawką (75 do 225 mg na dobę), jednym 6-miesięcznym, kontrolowanym placebo, elastycznym -badanie dawki (75 do 225 mg na dobę) oraz jedno 6-miesięczne, kontrolowane placebo badanie z zastosowaniem stałej dawki (37,5, 75 i 150 mg na dobę) z udziałem dorosłych pacjentów ambulatoryjnych spełniających kryteria DSM-IV dla GAD.
jednym 8-tygodniowym badaniu, Effexor XR wykazał wyższość nad placebo dla dawek 75, 150 i 225 mg na dobę, mierzoną za pomocą całkowitego wyniku Skali Oceny Lęku Hamiltona (HAM-A), zarówno lęku, jak i napięcia HAM-A. pozycje oraz skala Clinical Global Impressions (CGI). Jednak dawki 75 i 150 mg na dobę nie były tak konsekwentnie skuteczne jak najwyższa dawka (badanie 1). Drugie 8-tygodniowe badanie oceniające dawki 75 i 150 mg na dobę oraz placebo wykazało, że obie dawki były bardziej skuteczne niż placebo w przypadku niektórych z tych samych wyników; jednakże dawka 75 mg na dzień była bardziej konsekwentnie skuteczna niż dawka 150 mg na dzień (badanie 2). Zależność dawka-odpowiedź dla skuteczności w GAD nie została jasno ustalona w badanym zakresie dawek od 75 do 225 mg na dobę.
Dwa 6-miesięczne badania, z których jedno oceniało dawki produktu Effexor 75 mg XR wynoszące 37,5, 75 i 150 mg na dobę (badanie 3), a drugie oceniało dawki produktu Effexor XR od 75 do 225 mg na dobę (badanie 4), wykazały, że dawki dobowe wynoszące 75 mg lub więcej było skuteczniejsze niż placebo w całości HAM-A, zarówno w elementach lęku i napięcia HAM-A, jak i w skali CGI w ciągu 6 miesięcy leczenia. Chociaż istniały również dowody na wyższość nad placebo dla dawki 37,5 mg na dobę, dawka ta nie była tak konsekwentnie skuteczna jak dawki wyższe.
Badanie podzbiorów płci w badanej populacji nie wykazało żadnej zróżnicowanej reaktywności ze względu na płeć.
Zaburzenie lęku społecznego (znane również jako fobia społeczna)
Skuteczność produktu Effexor 37,5 mg XR w leczeniu zespołu lęku społecznego (ang. Social Anxiety Disorder – SAD) została potwierdzona w czterech 12-tygodniowych, wieloośrodkowych, kontrolowanych placebo badaniach z zastosowaniem elastycznej dawki, prowadzonych metodą podwójnie ślepej próby w grupach równoległych (badania 1-4) i jedno 6-miesięczne badanie z podwójnie ślepą próbą w grupach równoległych, kontrolowane placebo, z zastosowaniem stałej/elastycznej dawki, które obejmowało dawki w zakresie od 75 do 225 mg na dobę u dorosłych pacjentów ambulatoryjnych spełniających kryteria SAD DSM-IV (badanie 5 ).
W tych pięciu badaniach preparat Effexor 75 mg XR był statystycznie istotnie skuteczniejszy niż placebo pod względem zmiany od punktu początkowego do punktu końcowego w całkowitej punktacji Skali Lęku Społecznego Liebowitza (LSAS). Nie było dowodów na jakąkolwiek większą skuteczność w grupie 150 do 225 mg dziennie w porównaniu z grupą 75 mg dziennie w badaniu 6-miesięcznym.
Badanie podzbiorów badanej populacji nie wykazało żadnej zróżnicowanej reaktywności ze względu na płeć. Nie było wystarczających informacji, aby określić wpływ wieku lub rasy na wyniki tych badań.
Zaburzenie lękowe
Skuteczność produktu Effexor XR w leczeniu zespołu lęku napadowego (PD) została potwierdzona w dwóch 12-tygodniowych, wieloośrodkowych, kontrolowanych placebo badaniach z podwójnie ślepą próbą u dorosłych pacjentów ambulatoryjnych spełniających kryteria DSM-IV dla PD, z agorafobią lub bez. Pacjenci otrzymywali stałe dawki 75 lub 150 mg na dobę w jednym badaniu (badanie 1) i 75 lub 225 mg na dobę w drugim badaniu (badanie 2).
Skuteczność oceniano na podstawie wyników w trzech zmiennych: (1) odsetek pacjentów bez napadów paniki z pełnymi objawami w skali Panic and Anticipatory Anxiety Scale (PAAS); (2) średnia zmiana od punktu początkowego do punktu końcowego w łącznym wyniku w skali PDSS (Panic Disorder Severity Scale); oraz (3) odsetek pacjentów ocenionych jako reagujący (znaczna poprawa lub bardzo duża poprawa) w skali poprawy CGI (Clinical Global Impressions). W tych dwóch badaniach preparat Effexor XR był statystycznie istotnie skuteczniejszy niż placebo (dla każdej ustalonej dawki) we wszystkich trzech punktach końcowych, ale nie ustalono wyraźnie zależności dawka-odpowiedź.
Badanie podzbiorów badanej populacji nie wykazało żadnej zróżnicowanej reaktywności ze względu na płeć. Nie było wystarczających informacji, aby określić wpływ wieku lub rasy na wyniki tych badań.
długoterminowym badaniu (badanie 3) dorośli pacjenci ambulatoryjny spełniający kryteria DSM-IV dla PD, którzy odpowiedzieli podczas 12-tygodniowej fazy otwartej za pomocą produktu Effexor 75 mg XR (75 do 225 mg na dobę), zostali losowo przydzieleni do kontynuowania tego samego leku Effexor 75 mg Dawka XR (75, 150 lub 225 mg) lub zmiana na placebo w celu obserwacji nawrotu w warunkach podwójnie ślepej próby. Odpowiedź w fazie otwartej zdefiniowano jako ≤ 1 pełny napad paniki na tydzień w ciągu ostatnich 2 tygodni fazy otwartej oraz wynik poprawy w skali CGI równy 1 (bardzo duża poprawa) lub 2 (znaczna poprawa). Nawrót podczas fazy podwójnie ślepej próby zdefiniowano jako wystąpienie 2 lub więcej ataków paniki z pełnymi objawami tygodniowo przez 2 kolejne tygodnie lub przerwanie leczenia z powodu utraty skuteczności określonej przez badaczy podczas badania. Randomizowani pacjenci byli w stanie odpowiedzi przez średni czas 34 dni przed randomizacją. W fazie randomizowanej następującej po 12-tygodniowym okresie otwartej próby pacjenci otrzymujący nadal produkt Effexor 75 mg XR doświadczyli statystycznie istotnie dłuższego czasu do nawrotu.
Pacjenci pediatryczni
Przeprowadzono dwa badania kontrolowane placebo z udziałem 766 pacjentów pediatrycznych z MDD i dwa badania kontrolowane placebo z udziałem 793 pacjentów pediatrycznych z GAD, a dane nie były wystarczające, aby uzasadnić twierdzenie o stosowaniu u dzieci.
Co to jest Effexor i jak się go stosuje?
Effexor to lek na receptę stosowany w leczeniu objawów depresji, uogólnionego lęku, lęku społecznego i lęku napadowego. Effexor można stosować samodzielnie lub z innymi lekami.
Effexor należy do klasy leków zwanych antydepresantami, selektywnymi inhibitorami wychwytu zwrotnego serotoniny i noradrenaliny (SNRI).
Jakie są możliwe skutki uboczne Effexor 37,5 mg?
Effexor może powodować poważne skutki uboczne, w tym:
- rozmazany obraz,
- widzenie tunelowe,
- ból lub obrzęk oka,
- widząc aureole okrągłe światła,
- łatwe powstawanie siniaków lub krwawień (krwawienia z nosa, krwawiące dziąsła),
- krew w moczu lub stolcu,
- kaszel krwią,
- kaszel,
- ucisk w klatce piersiowej,
- problemy z oddychaniem,
- drgawki (drgawki),
- ból głowy,
- dezorientacja,
- bełkotliwa wymowa,
- silne osłabienie,
- wymioty,
- utrata koordynacji,
- czuć się niepewnie,
- bardzo sztywny (sztywny) mięsień,
- wysoka gorączka,
- wyzysk,
- dezorientacja,
- szybkie lub nierówne bicie serca,
- drżenia i
- zawroty
- Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
- Najczęstsze skutki uboczne Effexor to:
- zawroty głowy,
- senność,
- lęk,
- czuć się zdenerwowanym,
- problemy ze snem (bezsenność),
- zmiany widzenia,
- mdłości,
- wymioty,
- biegunka,
- zmiany wagi lub apetytu,
- suchość w ustach,
- ziewanie,
- zwiększona potliwość,
- zmniejszony popęd płciowy,
- impotencja,
- nieprawidłowy wytrysk i
- trudności z orgazmem
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Effexor. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OSTRZEŻENIE
Samobójstwa i leki przeciwdepresyjne
Leki przeciwdepresyjne zwiększały w porównaniu z placebo ryzyko myśli i zachowań samobójczych (samobójstwa) u dzieci, młodzieży i młodych dorosłych w krótkoterminowych badaniach nad ciężkimi zaburzeniami depresyjnymi (MDD) i innymi zaburzeniami psychicznymi. Każdy, kto rozważa stosowanie tabletek wenlafaksyny, USP lub jakiegokolwiek innego leku przeciwdepresyjnego u dzieci, młodzieży lub młodych dorosłych, musi zrównoważyć to ryzyko z potrzebą kliniczną. Badania krótkoterminowe nie wykazały wzrostu ryzyka samobójstw w przypadku stosowania leków przeciwdepresyjnych w porównaniu z placebo u osób dorosłych w wieku powyżej 24 lat; wystąpiło zmniejszenie ryzyka w przypadku stosowania leków przeciwdepresyjnych w porównaniu z placebo u osób dorosłych w wieku 65 lat i starszych. Depresja i niektóre inne zaburzenia psychiczne same w sobie wiążą się ze wzrostem ryzyka samobójstwa. Pacjenci w każdym wieku, którzy rozpoczynają leczenie lekami przeciwdepresyjnymi, powinni być odpowiednio monitorowani i ściśle obserwowani pod kątem pogorszenia stanu klinicznego, skłonności samobójczych lub nietypowych zmian w zachowaniu. Rodziny i opiekunowie powinni być poinformowani o potrzebie ścisłej obserwacji i komunikacji z lekarzem. Tabletki wenlafaksyny, USP nie są zatwierdzone do stosowania u pacjentów pediatrycznych. (Widzieć OSTRZEŻENIA : Pogorszenie stanu klinicznego i ryzyko samobójstwa , INFORMACJA O PACJENCIE , oraz ŚRODKI OSTROŻNOŚCI : Zastosowanie pediatryczne ).
OPIS
Tabletki wenlafaksyny USP to strukturalnie nowy lek przeciwdepresyjny do podawania doustnego. Jest on oznaczony jako chlorowodorek (R/S)-1-[2-(dimetyloamino)-1-(4-metoksyfenylo)etylo]cykloheksanolu lub (±)-1-[α-[(dimetyloamino)metylo]-p- chlorowodorek metoksybenzylo]cykloheksanolu i ma wzór empiryczny C17H27NO2 HCl. Jego masa cząsteczkowa wynosi 313,87. Wzór strukturalny pokazano poniżej.
Chlorowodorek wenlafaksyny jest białym lub prawie białym krystalicznym ciałem stałym o rozpuszczalności 572 mg/ml w wodzie (dostosowanej do siły jonowej 0,2 M chlorkiem sodu). Jego współczynnik podziału oktanol:woda (0,2 M chlorek sodu) wynosi 0,43.
Tabletki prasowane zawierają chlorowodorek wenlafaksyny, odpowiadający USP 25 mg, 37,5 mg, 50 mg, 75 mg lub 100 mg zasady wenlafaksyny oraz następujące składniki nieaktywne: celuloza mikrokrystaliczna, laktoza jednowodna, wstępnie żelatynizowana skrobia, glikolan sodowy skrobi, czerwony tlenek żelaza, żółty tlenek żelaza, koloidalny dwutlenek krzemu i stearynian magnezu.
