Fosamax 35mg, 70mg Alendronate Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Fosamax 70mg i jak się go stosuje?
Fosamax 35mg to lek na receptę stosowany w zapobieganiu i leczeniu niektórych rodzajów utraty masy kostnej (osteoporozy) u osób dorosłych. Fosamax 70mg może być stosowany samodzielnie lub z innymi lekami.
Fosamax jest modyfikatorem metabolizmu wapnia, pochodnymi bisfosfonianu.
Nie wiadomo, czy Fosamax jest bezpieczny i skuteczny u dzieci.
Jakie są możliwe skutki uboczne Fosamaxu?
Fosamax może powodować poważne skutki uboczne, w tym:
- ból w klatce piersiowej
- nowa lub pogarszająca się zgaga
- ból lub pieczenie pod żebrami lub w plecach
- ciężka zgaga
- piekący ból w górnej części żołądka lub odkrztuszanie krwi
- nowy lub nietypowy ból w udzie lub biodrze
- ból szczęki
- drętwienie
- obrzęk
- silny ból stawów, kości lub mięśni
- skurcze lub skurcze mięśni
- drętwienie lub mrowienie uczucie wokół ust lub w palcach rąk lub nóg
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Fosamax to:
- zgaga
- rozstrój żołądka
- ból brzucha
- mdłości
- biegunka
- zaparcie
- ból kości
- ból w mięśniach
- ból stawu
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Fosamax. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
FOSAMAX (alendronian sodu) jest bisfosfonianem, który działa jako swoisty inhibitor resorpcji kości za pośrednictwem osteoklastów. Bisfosfoniany to syntetyczne analogi pirofosforanu, które wiążą się z hydroksyapatytem znajdującym się w kości.
Alendronian sodu jest chemicznie opisany jako trihydrat soli monosodowej kwasu (4-amino-1-hydroksybutylideno)bisfosfonowego.
Empiryczny wzór alendronianu sodu to C4H12NNaO7P2 •3H2O, a jego waga wynosi 325,12. Wzór strukturalny to:
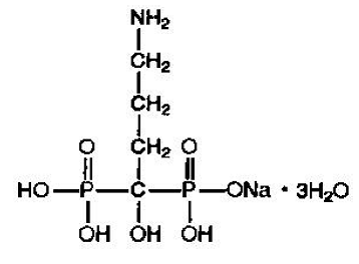
Alendronian sodu jest białym, krystalicznym, niehigroskopijnym proszkiem. Jest rozpuszczalny w wodzie, bardzo słabo rozpuszczalny w alkoholu i praktycznie nierozpuszczalny w chloroformie.
Tabletki FOSAMAX 70 mg do podawania doustnego zawierają 91,37 mg trójwodzianu soli monosodowej alendronianu, co odpowiada molowo 70 mg wolnego kwasu, oraz następujące składniki nieaktywne: celuloza mikrokrystaliczna, bezwodna laktoza, kroskarmeloza sodowa i stearynian magnezu.
WSKAZANIA
Leczenie® osteoporozy u kobiet po menopauzie
FOSAMAX jest wskazany w leczeniu osteoporozy u kobiet po menopauzie. U kobiet po menopauzie FOSAMAX 70 mg zwiększa masę kostną i zmniejsza częstość występowania złamań, w tym biodra i kręgosłupa (złamania kompresyjne kręgów). [Widzieć Studia kliniczne ]
Zapobieganie osteoporozie u kobiet po menopauzie
FOSAMAX 70 mg jest wskazany w zapobieganiu osteoporozie pomenopauzalnej [patrz Studia kliniczne ].
Leczenie zwiększające masę kostną u mężczyzn z osteoporozą
FOSAMAX jest wskazany do leczenia w celu zwiększenia masy kostnej u mężczyzn z osteoporozą [patrz Studia kliniczne ].
Leczenie osteoporozy wywołanej glukokortykoidami
FOSAMAX jest wskazany w leczeniu osteoporozy wywołanej przez glikokortykosteroidy u mężczyzn i kobiet otrzymujących glikokortykosteroidy w dziennej dawce odpowiadającej 7,5 mg lub większej prednizonu i mających niską gęstość mineralną kości [patrz Studia kliniczne ].
Leczenie choroby Pageta kości
FOSAMAX 35mg jest wskazany w leczeniu choroby Pageta kości u mężczyzn i kobiet. Leczenie jest wskazane u pacjentów z chorobą Pageta kości, u których fosfataza alkaliczna jest co najmniej dwukrotnie wyższa od górnej granicy normy, lub u pacjentów z objawami lub u których występuje ryzyko przyszłych powikłań choroby. [Widzieć Studia kliniczne ]
Ważne ograniczenia użytkowania
Nie określono optymalnego czasu użytkowania. Bezpieczeństwo i skuteczność preparatu FOSAMAX w leczeniu osteoporozy opierają się na danych klinicznych z okresu czterech lat. U wszystkich pacjentów leczonych bisfosfonianami należy okresowo poddawać ponownej ocenie potrzebę kontynuacji leczenia. U pacjentów z niskim ryzykiem złamań należy rozważyć odstawienie leku po 3 do 5 latach stosowania. U pacjentów, którzy przerywają terapię, należy okresowo poddawać ponownej ocenie ryzyko złamań.
DAWKOWANIE I SPOSÓB PODAWANIA
Chociaż tabletki alendronianu 5 mg, 10 mg, 35 mg i 40 mg są dostępne na rynku, FOSAMAX 35 mg nie jest już sprzedawany w mocach 5 mg, 10 mg, 35 mg i 40 mg.
Chociaż na rynku może być dostępny roztwór doustny alendronianu, FOSAMAX 35 mg roztwór doustny nie jest już dostępny w obrocie.
Leczenie osteoporozy u kobiet po menopauzie
Zalecana dawka to:
- jedna tabletka 70 mg raz w tygodniu lub
- jedna butelka 70 mg roztworu doustnego raz w tygodniu lub
- jedna tabletka 10 mg raz na dobę
Zapobieganie osteoporozie u kobiet po menopauzie
Zalecana dawka to:
- jedna tabletka 35 mg raz w tygodniu lub
- jedna tabletka 5 mg raz na dobę
Leczenie zwiększające masę kostną u mężczyzn z osteoporozą
Zalecana dawka to:
- jedna tabletka 70 mg raz w tygodniu lub
- jedna butelka 70 mg roztworu doustnego raz w tygodniu lub
- jedna tabletka 10 mg raz na dobę
Leczenie osteoporozy wywołanej glukokortykoidami
Zalecana dawka to jedna tabletka 5 mg raz na dobę, z wyjątkiem kobiet po menopauzie nieotrzymujących estrogenów, dla których zalecana dawka to jedna tabletka 10 mg raz na dobę.
Leczenie choroby Pageta kości
Zalecany schemat leczenia to 40 mg raz dziennie przez sześć miesięcy.
Ponowne leczenie choroby Pageta
Można rozważyć ponowne leczenie FOSAMAX 35 mg po sześciomiesięcznym okresie oceny po leczeniu u pacjentów z nawrotem, w oparciu o zwiększenie stężenia fosfatazy zasadowej w surowicy, które należy okresowo mierzyć. Ponowne leczenie można również rozważyć u osób, u których nie udało się znormalizować fosfatazy alkalicznej w surowicy.
Ważne instrukcje administracyjne
Poinstruuj pacjentów, aby wykonali następujące czynności:
- Lek FOSAMAX należy przyjmować co najmniej pół godziny przed pierwszym posiłkiem, napojem lub lekiem, popijając tylko czystą wodą [patrz Informacje dotyczące poradnictwa dla pacjentów ]. Inne napoje (w tym woda mineralna), jedzenie i niektóre leki prawdopodobnie zmniejszają wchłanianie FOSAMAX [patrz INTERAKCJE Z LEKAMI ]. Odczekanie mniej niż 30 minut lub przyjmowanie leku FOSAMAX 70 mg z jedzeniem, napojami (innymi niż zwykła woda) lub innymi lekami zmniejszy działanie leku FOSAMAX 70 mg poprzez zmniejszenie jego wchłaniania do organizmu.
- Weź FOSAMAX po wstaniu na cały dzień. Aby ułatwić dostarczanie do żołądka, a tym samym zmniejszyć ryzyko podrażnienia przełyku, tabletkę FOSAMAX 35 mg należy połykać popijając pełną szklanką wody (6-8 uncji). Aby ułatwić opróżnianie żołądka, po FOSAMAX 70 mg roztwór doustny należy wypić co najmniej 2 uncje (ćwierć szklanki) wody. Pacjenci nie powinni kłaść się przez co najmniej 30 minut i do czasu po pierwszym posiłku w ciągu dnia. FOSAMAX nie powinien być przyjmowany przed snem ani przed wstaniem z łóżka. Niezastosowanie się do tych instrukcji może zwiększyć ryzyko wystąpienia niepożądanych doświadczeń ze strony przełyku [patrz OSTRZEŻENIA I ŚRODKI oraz Informacje dotyczące poradnictwa dla pacjentów ].
Zalecenia dotyczące suplementacji wapnia i witaminy D
Poinstruuj pacjentów, aby przyjmowali suplementy wapnia, jeśli spożycie w diecie jest niewystarczające [patrz OSTRZEŻENIA I ŚRODKI ]. Pacjenci ze zwiększonym ryzykiem niedoboru witaminy D (np. w wieku powyżej 70 lat, przebywający w domu opieki lub przewlekle chorzy) mogą potrzebować suplementacji witaminą D. Pacjenci z zespołami złego wchłaniania żołądkowo-jelitowego mogą wymagać wyższych dawek suplementacji witaminy D i należy rozważyć oznaczenie 25-hydroksywitaminy D.
Pacjenci leczeni glikokortykosteroidami powinni otrzymywać odpowiednią ilość wapnia i witaminy D.
Instrukcje dotyczące podawania pominiętych dawek
W przypadku pominięcia dawki FOSAMAX podawanej raz w tygodniu należy poinstruować pacjentów, aby przyjmowali jedną dawkę rano po przypomnieniu sobie. Nie powinni przyjmować dwóch dawek tego samego dnia, ale powinni powrócić do przyjmowania jednej dawki raz w tygodniu, jak pierwotnie zaplanowano na wybrany dzień.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
- Tabletki 70 mg to białe, owalne, niepowlekane tabletki z kodem 31 po jednej stronie i obrysem kości po drugiej.
Składowania i stosowania
Nr 3814 – Tabletki FOSAMAX, 70 mg, to białe, owalne, niepowlekane tabletki z kodem 31 po jednej stronie i obrysem kości po drugiej:
NDC 0006-0031-44 blister jednostkowy po 4 szt.
Magazynowanie
Tabletki FOSAMAX
Przechowywać w dobrze zamkniętym pojemniku w temperaturze pokojowej 15-30°C (59-86°F).
Dystrybutor: Merck Sharp & Dohme Corp., spółka zależna MERCK & CO., INC., Whitehouse Station, NJ 08889, USA. Poprawiono: sierpień 2019 r.
SKUTKI UBOCZNE
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce klinicznej.
Leczenie osteoporozy u kobiet po menopauzie
Dzienne dozowanie
Bezpieczeństwo preparatu FOSAMAX 35 mg w leczeniu osteoporozy pomenopauzalnej oceniano w czterech badaniach klinicznych, w których wzięło udział 7453 kobiet w wieku 44-84 lat. Badanie 1 i badanie 2 były identycznie zaprojektowanymi, trzyletnimi, kontrolowanymi placebo, wieloośrodkowymi badaniami z podwójnie ślepą próbą (Stany Zjednoczone i międzynarodowe n=994); Badanie 3 obejmowało trzyletnią kohortę złamań kręgów w ramach Fracture Intervention Trial [FIT] (n=2027), a badanie 4 — czteroletnią kohortę kliniczną złamań kręgów FIT (n=4432). Ogółem 3620 pacjentów otrzymywało placebo, a 3432 pacjentów otrzymywało FOSAMAX. Do tych badań klinicznych włączono pacjentów z istniejącą wcześniej chorobą przewodu pokarmowego i jednocześnie stosujących niesteroidowe leki przeciwzapalne. W badaniu 1 i badaniu 2 wszystkie kobiety otrzymywały 500 mg wapnia pierwiastkowego w postaci węglanu. W badaniu 3 i badaniu 4 wszystkie kobiety, które spożywały w diecie mniej niż 1000 mg wapnia dziennie otrzymywały 500 mg wapnia i 250 jednostek międzynarodowych witaminy D dziennie.
Wśród pacjentów leczonych alendronianem w dawce 10 mg lub placebo w Badaniu 1 i Badaniu 2 oraz u wszystkich pacjentów w Badaniu 3 i Badaniu 4 częstość występowania śmiertelności z jakiejkolwiek przyczyny wynosiła 1,8% w grupie placebo i 1,8% w grupie FOSAMAX 35 mg. Częstość występowania poważnych zdarzeń niepożądanych wynosiła 30,7% w grupie placebo i 30,9% w grupie FOSAMAX. Odsetek pacjentów, którzy przerwali badanie z powodu jakiegokolwiek klinicznego zdarzenia niepożądanego, wyniósł 9,5% w grupie placebo i 8,9% w grupie FOSAMAX 70 mg. Działania niepożądane z tych badań uznane przez badaczy za prawdopodobnie, prawdopodobnie lub zdecydowanie związane z lekiem u co najmniej 1% pacjentów leczonych FOSAMAX 35 mg lub placebo przedstawiono w Tabeli 1.
Wystąpiła wysypka i rumień.
Działania niepożądane ze strony przewodu pokarmowego
jednego pacjenta leczonego FOSAMAX (10 mg/dobę), który miał w wywiadzie chorobę wrzodową żołądka i gastrektomię i który jednocześnie przyjmował aspirynę, rozwinął się wrzód zespolenia z łagodnym krwotokiem, który uznano za związany z przyjmowaniem leku. Aspiryna i FOSAMAX zostały odstawione, a pacjent wyzdrowiał. W populacjach z badania 1 i badania 2 49-54% miało w wywiadzie zaburzenia żołądkowo-jelitowe na początku badania, a 54-89% stosowało niesteroidowe leki przeciwzapalne lub aspirynę w pewnym okresie trwania badań. [Widzieć OSTRZEŻENIA I ŚRODKI ]
Wyniki badań laboratoryjnych
W wieloośrodkowych, kontrolowanych badaniach z podwójnie ślepą próbą, bezobjawowe, łagodne i przemijające zmniejszenie stężenia wapnia i fosforanów w surowicy obserwowano odpowiednio u około 18% i 10% pacjentów przyjmujących FOSAMAX w porównaniu z około 12% i 3% pacjentów przyjmujących placebo. Jednak częstość występowania zmniejszenia stężenia wapnia w surowicy do mniej niż 8,0 mg/dl (2,0 mM) i fosforanów w surowicy do mniej niż lub równego 2,0 mg/dl (0,65 mM) była podobna w obu leczonych grupach.
Dozowanie tygodniowe
Bezpieczeństwo FOSAMAX 70 mg raz w tygodniu w leczeniu osteoporozy pomenopauzalnej oceniano w rocznym, podwójnie zaślepionym, wieloośrodkowym badaniu porównującym FOSAMAX 70 mg raz w tygodniu i FOSAMAX 10 mg raz na dobę. Ogólne profile bezpieczeństwa i tolerancji FOSAMAX 70 mg raz w tygodniu i FOSAMAX 10 mg na dobę były podobne. Działania niepożądane uznane przez badaczy za prawdopodobnie, prawdopodobnie lub zdecydowanie związane z lekiem u co najmniej 1% pacjentów w obu grupach przedstawiono w Tabeli 2.
Zapobieganie osteoporozie u kobiet po menopauzie
Dzienne dozowanie
Bezpieczeństwo stosowania produktu FOSAMAX w dawce 5 mg/dobę u kobiet w wieku 40-60 lat po menopauzie oceniano w trzech badaniach z podwójnie ślepą próbą, kontrolowanych placebo, z udziałem ponad 1400 pacjentów przydzielonych losowo do grupy otrzymującej FOSAMAX przez dwa lub trzy lata. W tych badaniach ogólne profile bezpieczeństwa FOSAMAX 5 mg/dobę i placebo były podobne. Przerwanie leczenia z powodu jakiegokolwiek klinicznego zdarzenia niepożądanego wystąpiło u 7,5% z 642 pacjentów leczonych FOSAMAX 5 mg/dobę i 5,7% z 648 pacjentów otrzymujących placebo.
Dozowanie tygodniowe
Bezpieczeństwo FOSAMAX 35 mg raz w tygodniu w porównaniu z FOSAMAX 5 mg na dobę oceniano w rocznym, podwójnie zaślepionym, wieloośrodkowym badaniu z udziałem 723 pacjentów. Ogólne profile bezpieczeństwa i tolerancji FOSAMAX 35 mg raz w tygodniu i FOSAMAX 5 mg na dobę były podobne.
Działania niepożądane z tych badań uznane przez badaczy za prawdopodobnie, prawdopodobnie lub zdecydowanie związane z lekiem u co najmniej 1% pacjentów leczonych albo raz w tygodniu FOSAMAX 35 mg, FOSAMAX 5 mg/dobę albo placebo przedstawiono w Tabeli 3. .
Jednoczesne stosowanie z estrogenową/hormonową terapią zastępczą
W dwóch badaniach (trwających rok i dwa lata) z udziałem kobiet po menopauzie z osteoporozą (ogółem: n=853), profil bezpieczeństwa i tolerancji skojarzonego leczenia FOSAMAX 10 mg raz na dobę i estrogenem ± progestyna (n=354) był zgodne z indywidualnymi zabiegami.
Osteoporoza u mężczyzn
dwóch kontrolowanych placebo, podwójnie zaślepionych, wieloośrodkowych badaniach u mężczyzn (dwuletnie badanie FOSAMAX 10 mg/dobę i roczne badanie FOSAMAX 70 mg raz w tygodniu) częstość przerywania leczenia z powodu jakichkolwiek niepożądanych objawów klinicznych zdarzenia wyniosły 2,7% w przypadku FOSAMAX 10 mg/dobę w porównaniu z 10,5% w przypadku placebo i 6,4% w przypadku FOSAMAX 70 mg raz w tygodniu w porównaniu z 8,6% w przypadku placebo. Działania niepożądane uznane przez badaczy za prawdopodobnie, prawdopodobnie lub zdecydowanie związane z lekiem u co najmniej 2% pacjentów leczonych FOSAMAX 70 mg lub placebo przedstawiono w Tabeli 4.
Osteoporoza indukowana glukokortykoidami
dwóch trwających rok, kontrolowanych placebo, wieloośrodkowych badaniach z podwójnie ślepą próbą u pacjentów otrzymujących glikokortykosteroidy, ogólne profile bezpieczeństwa i tolerancji FOSAMAX 5 i 10 mg/dobę były zasadniczo podobne do profili placebo. Działania niepożądane uznane przez badaczy za prawdopodobnie, prawdopodobnie lub zdecydowanie związane z lekiem u co najmniej 1% pacjentów leczonych FOSAMAX 5 lub 10 mg/dobę lub placebo przedstawiono w Tabeli 5.
Ogólny profil bezpieczeństwa i tolerancji w populacji osteoporozy indukowanej glikokortykosteroidami, która kontynuowała leczenie przez drugi rok badań (FOSAMAX: n=147) był zgodny z profilem obserwowanym w pierwszym roku.
Choroba Pageta kości
badaniach klinicznych (osteoporoza i choroba Pageta) zdarzenia niepożądane zgłoszone u 175 pacjentów przyjmujących FOSAMAX 40 mg/dobę przez 3-12 miesięcy były podobne do tych u kobiet po menopauzie leczonych FOSAMAX 10 mg/dobę. U pacjentów przyjmujących FOSAMAX w dawce 40 mg/dobę zaobserwowano jednak wyraźną zwiększoną częstość występowania działań niepożądanych dotyczących górnego odcinka przewodu pokarmowego (17,7% FOSAMAX w porównaniu z 10,2% placebo). Jeden przypadek zapalenia przełyku i dwa przypadki zapalenia żołądka spowodowały przerwanie leczenia.
Dodatkowo ból mięśniowo-szkieletowy (kości, mięśni lub stawów), który został opisany u pacjentów z chorobą Pageta leczonych innymi bisfosfonianami, został uznany przez badaczy za prawdopodobnie, prawdopodobnie lub zdecydowanie związany z lekiem u około 6% pacjentów leczeni FOSAMAX 40 mg/dobę w porównaniu z około 1% pacjentów otrzymujących placebo, ale rzadko prowadzili do przerwania leczenia. Przerwanie leczenia z powodu jakichkolwiek klinicznych zdarzeń niepożądanych wystąpiło u 6,4% pacjentów z chorobą Pageta leczonych FOSAMAX 40 mg/dzień i 2,4% pacjentów leczonych placebo.
Doświadczenie pomarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania produktu FOSAMAX po dopuszczeniu do obrotu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Ciało jako całość: reakcje nadwrażliwości, w tym pokrzywka i obrzęk naczynioruchowy. Po zastosowaniu produktu FOSAMAX zgłaszano przemijające objawy bólu mięśni, złego samopoczucia, osłabienia i gorączki, zazwyczaj w związku z rozpoczęciem leczenia. Wystąpiła objawowa hipokalcemia, zwykle związana ze stanami predysponującymi. Obrzęki obwodowe.
Przewód pokarmowy: zapalenie przełyku, nadżerki przełyku, owrzodzenia przełyku, zwężenie lub perforacja przełyku oraz owrzodzenie części ustnej gardła. Zgłaszano również przypadki wrzodów żołądka lub dwunastnicy, niektóre ciężkie i z powikłaniami [patrz DAWKOWANIE I SPOSÓB PODAWANIA ; OSTRZEŻENIA I ŚRODKI ].
Zgłaszano miejscową martwicę kości szczęki, zwykle związaną z ekstrakcją zęba i/lub miejscową infekcją z opóźnionym gojeniem [patrz OSTRZEŻENIA I ŚRODKI ].
Układ mięśniowo-szkieletowy: ból kości, stawów i (lub) mięśni, czasami silny i obezwładniający [patrz OSTRZEŻENIA I ŚRODKI ]; obrzęk stawów; niskoenergetyczne złamania trzonu kości udowej i złamania podkrętarzowe [patrz OSTRZEŻENIA I ŚRODKI ].
System nerwowy: zawroty głowy i zawroty głowy.
Płucny: ostre zaostrzenia astmy.
Skóra: wysypka (sporadycznie z nadwrażliwością na światło), świąd, łysienie, ciężkie reakcje skórne, w tym zespół Stevensa-Johnsona i martwica toksyczno-rozpływna naskórka.
Zmysły specjalne: zapalenie błony naczyniowej oka, zapalenie twardówki lub zapalenie nadtwardówki. Perlak przewodu słuchowego zewnętrznego (ogniskowa martwica kości).
INTERAKCJE Z LEKAMI
Suplementy wapnia/środki zobojętniające kwasy
Jednoczesne podawanie FOSAMAX i wapnia, środków zobojętniających lub doustnych leków zawierających kationy wielowartościowe będzie zakłócać wchłanianie FOSAMAX. Dlatego należy poinstruować pacjentów, aby odczekali co najmniej pół godziny po przyjęciu leku FOSAMAX 35 mg przed przyjęciem jakichkolwiek innych leków doustnych.
Aspiryna
W badaniach klinicznych częstość występowania działań niepożądanych dotyczących górnego odcinka przewodu pokarmowego była zwiększona u pacjentów otrzymujących jednocześnie terapię dobowymi dawkami produktu FOSAMAX 35 mg powyżej 10 mg i produktami zawierającymi aspirynę.
Niesteroidowe leki przeciwzapalne
FOSAMAX 35 mg może być podawany pacjentom przyjmującym niesteroidowe leki przeciwzapalne (NLPZ). W 3-letnim kontrolowanym badaniu klinicznym (n=2027), podczas którego większość pacjentów otrzymywała jednocześnie NLPZ, częstość występowania działań niepożądanych dotyczących górnego odcinka przewodu pokarmowego była podobna u pacjentów przyjmujących FOSAMAX w dawce 5 lub 10 mg/dobę w porównaniu z pacjentami przyjmującymi placebo. Jednakże, ponieważ stosowanie NLPZ wiąże się z podrażnieniem przewodu pokarmowego, należy zachować ostrożność podczas jednoczesnego stosowania z FOSAMAX.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Reakcje niepożądane dotyczące górnego odcinka przewodu pokarmowego
FOSAMAX 35mg, podobnie jak inne bisfosfoniany podawane doustnie, może powodować miejscowe podrażnienie błony śluzowej górnego odcinka przewodu pokarmowego. Ze względu na te możliwe działania drażniące i możliwość pogorszenia choroby podstawowej, należy zachować ostrożność podając FOSAMAX pacjentom z aktywnymi problemami górnego odcinka przewodu pokarmowego (takimi jak znany przełyk Barretta, dysfagia, inne choroby przełyku, zapalenie żołądka, dwunastnicy lub wrzody).
pacjentów otrzymujących doustne bisfosfoniany, w tym FOSAMAX, zgłaszano działania niepożądane dotyczące przełyku, takie jak zapalenie przełyku, owrzodzenie przełyku i nadżerki przełyku, czasami z krwawieniem, a rzadko z następowym zwężeniem lub perforacją przełyku. W niektórych przypadkach były one ciężkie i wymagały hospitalizacji. Dlatego lekarze powinni zwracać uwagę na wszelkie oznaki lub objawy wskazujące na możliwą reakcję przełyku, a pacjentów należy poinstruować, aby przerwali stosowanie produktu FOSAMAX 70 mg i zwrócili się o pomoc medyczną w przypadku wystąpienia u nich dysfagii, odynofagii, bólu zamostkowego lub zgagi lub jej nasilenia.
Ryzyko ciężkich działań niepożądanych ze strony przełyku wydaje się być większe u pacjentów, którzy kładą się po przyjęciu doustnych bisfosfonianów, w tym FOSAMAX 70 mg i (lub) nie połykają doustnych bisfosfonianów, w tym FOSAMAX 35 mg, popijając zalecaną pełną szklanką (6-8 uncji) wody oraz /lub którzy nadal przyjmują doustne bisfosfoniany, w tym FOSAMAX 70 mg, po wystąpieniu objawów sugerujących podrażnienie przełyku. Dlatego bardzo ważne jest przekazanie pacjentowi pełnej instrukcji dawkowania i zrozumienie przez nią [patrz DAWKOWANIE I SPOSÓB PODAWANIA ]. U pacjentów, którzy z powodu upośledzenia umysłowego nie mogą przestrzegać zaleceń dotyczących dawkowania, leczenie preparatem FOSAMAX należy stosować pod odpowiednim nadzorem.
Po wprowadzeniu do obrotu zgłaszano przypadki wrzodów żołądka i dwunastnicy po doustnym stosowaniu bisfosfonianów, niektóre ciężkie i z powikłaniami, chociaż w kontrolowanych badaniach klinicznych nie zaobserwowano zwiększonego ryzyka [patrz DZIAŁANIA NIEPOŻĄDANE ].
Metabolizm mineralny
Hipokalcemię należy skorygować przed rozpoczęciem leczenia preparatem FOSAMAX [patrz PRZECIWWSKAZANIA ]. Inne zaburzenia wpływające na metabolizm minerałów (takie jak niedobór witaminy D) również powinny być skutecznie leczone. U pacjentów z tymi schorzeniami należy monitorować stężenie wapnia w surowicy i objawy hipokalcemii podczas leczenia preparatem FOSAMAX.
Przypuszczalnie ze względu na wpływ preparatu FOSAMAX na zwiększenie mineralizacji kości, mogą wystąpić niewielkie, bezobjawowe spadki poziomu wapnia i fosforanów w surowicy, szczególnie u pacjentów z chorobą Pageta, u których tempo obrotu kostnego przed leczeniem może być znacznie podwyższone, a pacjentów otrzymujących glikokortykosteroidy, u których wchłanianie wapnia może być zmniejszone.
Zapewnienie odpowiedniego spożycia wapnia i witaminy D jest szczególnie ważne u pacjentów z chorobą Pageta kości iu pacjentów otrzymujących glukokortykoidy.
Ból mięśniowo-szkieletowy
Po wprowadzeniu produktu do obrotu zgłaszano ciężkie i sporadycznie powodujące niesprawność bóle kości, stawów i (lub) mięśni u pacjentów przyjmujących bisfosfoniany zatwierdzone do zapobiegania i leczenia osteoporozy [patrz DZIAŁANIA NIEPOŻĄDANE ]. Ta kategoria leków obejmuje FOSAMAX (alendronian). Większość pacjentek stanowiły kobiety po menopauzie. Czas do wystąpienia objawów wahał się od jednego dnia do kilku miesięcy po rozpoczęciu leczenia. Przerwać stosowanie, jeśli wystąpią poważne objawy. Większość pacjentów złagodziła objawy po odstawieniu. Podgrupa miała nawrót objawów po ponownym podaniu tego samego leku lub innego bisfosfonianu.
W kontrolowanych placebo badaniach klinicznych FOSAMAX odsetek pacjentów z tymi objawami był podobny w grupach otrzymujących FOSAMAX 35 mg i placebo.
Martwica kości szczęki
Martwica kości szczęki (ONJ), która może wystąpić samoistnie, jest zwykle związana z ekstrakcją zęba i (lub) miejscowym zakażeniem z opóźnionym gojeniem i była zgłaszana u pacjentów przyjmujących bisfosfoniany, w tym FOSAMAX. Znane czynniki ryzyka martwicy kości szczęki obejmują inwazyjne procedury stomatologiczne (np. ekstrakcja zęba, implanty dentystyczne, chirurgia kości), rozpoznanie raka, jednoczesne terapie (np. chemioterapia, kortykosteroidy, inhibitory angiogenezy), zła higiena jamy ustnej i choroby współistniejące zaburzenia (np. przyzębia i/lub inne istniejące wcześniej choroby zębów, anemia, koagulopatia, infekcja, źle dopasowane protezy). Ryzyko wystąpienia ONJ może wzrastać wraz z czasem ekspozycji na bisfosfoniany.
W przypadku pacjentów wymagających inwazyjnych zabiegów stomatologicznych przerwanie leczenia bisfosfonianami może zmniejszyć ryzyko wystąpienia ONJ. Ocena kliniczna lekarza prowadzącego i/lub chirurga jamy ustnej powinna kierować planem postępowania dla każdego pacjenta w oparciu o indywidualną ocenę korzyści/ryzyka.
Pacjenci, u których podczas leczenia bisfosfonianami rozwinie się martwica kości szczęki, powinni być objęci opieką chirurga jamy ustnej. U tych pacjentów rozległa chirurgia stomatologiczna w celu leczenia ONJ może zaostrzyć stan. Należy rozważyć przerwanie leczenia bisfosfonianami na podstawie indywidualnej oceny korzyści/ryzyka.
Nietypowe złamania podkrętarzowe i trzonu kości udowej
U pacjentów leczonych bisfosfonianami zgłaszano złamania atypowe, niskoenergetyczne lub niskourazowe trzonu kości udowej. Te złamania mogą wystąpić w dowolnym miejscu trzonu kości udowej od miejsca tuż poniżej krętarza mniejszego do nadkłykcia nadkłykciowego i mają orientację poprzeczną lub krótką, ukośną, bez oznak rozdrobnienia. Przyczynowość nie została ustalona, ponieważ te złamania występują również u pacjentów z osteoporozą, którzy nie byli leczeni bisfosfonianami.
Atypowe złamania kości udowej najczęściej występują z minimalnym urazem lub bez urazu dotkniętego obszaru. Mogą być obustronne, a wielu pacjentów zgłasza ból prodromalny w dotkniętym obszarze, zwykle objawiający się tępym bólem uda, na kilka tygodni lub miesięcy przed wystąpieniem całkowitego złamania. Szereg raportów wskazuje, że pacjenci otrzymywali również leczenie glikokortykosteroidami (np. prednizonem) w momencie złamania.
Każdy pacjent z historią ekspozycji na bisfosfoniany, u którego występuje ból uda lub pachwiny, powinien być podejrzewany o nietypowe złamanie i powinien zostać poddany ocenie w celu wykluczenia niecałkowitego złamania kości udowej. Pacjenci zgłaszający się z nietypowym złamaniem powinni być również oceniani pod kątem objawów i oznak złamania w przeciwległej kończynie. Należy rozważyć przerwanie leczenia bisfosfonianami do czasu oceny ryzyka/korzyści indywidualnie.
Zaburzenia czynności nerek
FOSAMAX 35 mg nie jest zalecany u pacjentów z klirensem kreatyniny mniejszym niż 35 ml/min.
Osteoporoza indukowana glukokortykoidami
Nie ustalono stosunku ryzyka do korzyści związanych ze stosowaniem preparatu FOSAMAX przy dziennych dawkach glikokortykosteroidów mniejszych niż 7,5 mg prednizonu lub odpowiednika [patrz WSKAZANIA I ZASTOSOWANIE ]. Przed rozpoczęciem leczenia należy ustalić stan hormonalny gonad zarówno u mężczyzn, jak iu kobiet i rozważyć odpowiednią wymianę.
Pomiar gęstości mineralnej kości należy wykonać na początku leczenia i powtórzyć po 6 do 12 miesiącach leczenia skojarzonego FOSAMAX i glikokortykosteroidami.
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( Przewodnik po lekach ).
Należy poinstruować pacjentów, aby przed rozpoczęciem leczenia preparatem FOSAMAX zapoznali się z Przewodnikiem po lekach i ponownie zapoznawali się z nim za każdym razem, gdy recepta jest odnawiana.
Zalecenia dotyczące osteoporozy, w tym suplementacja wapnia i witaminy D
Poinstruuj pacjentów, aby przyjmowali suplementy wapnia i witaminy D, jeśli dzienna podaż w diecie jest niewystarczająca. Należy rozważyć ćwiczenia z obciążeniem wraz z modyfikacją pewnych czynników behawioralnych, takich jak palenie papierosów i/lub nadmierne spożycie alkoholu, jeśli te czynniki istnieją.
Instrukcje dotyczące dawkowania
Poinstruuj pacjentów, że oczekiwane korzyści ze stosowania leku FOSAMAX 70 mg można osiągnąć tylko wtedy, gdy zostanie on zażyty z czystą wodą jako pierwszy po wstaniu na co najmniej 30 minut przed pierwszym posiłkiem, napojem lub lekiem danego dnia. Wykazano, że nawet dozowanie soku pomarańczowego lub kawy znacznie zmniejsza wchłanianie FOSAMAX [patrz FARMAKOLOGIA KLINICZNA ].
Należy poinstruować pacjentów, aby nie żuli ani nie ssali tabletki ze względu na możliwość wystąpienia owrzodzenia jamy ustnej i gardła.
Należy poinstruować pacjentów, aby połknęli każdą tabletkę FOSAMAX popijając pełną szklanką wody (6-8 uncji), aby ułatwić dostarczenie do żołądka, a tym samym zmniejszyć ryzyko podrażnienia przełyku. Należy poinstruować pacjentów, aby po przyjęciu FOSAMAX 70 mg roztwór doustny wypili co najmniej 2 uncje (ćwierć szklanki) wody w celu ułatwienia opróżniania żołądka.
Poinstruuj pacjentów, aby nie kładli się przez co najmniej 30 minut i po pierwszym posiłku w ciągu dnia.
Należy poinstruować pacjentów, aby nie przyjmowali leku FOSAMAX przed snem lub przed wstaniem z łóżka w ciągu dnia. Należy poinformować pacjentów, że nieprzestrzeganie tych instrukcji może zwiększyć ryzyko wystąpienia problemów przełyku.
Należy poinstruować pacjentów, że jeśli wystąpią u nich objawy choroby przełyku (takie jak trudności lub ból podczas przełykania, ból zamostkowy lub nowa lub nasilenie zgagi), powinni przerwać stosowanie leku FOSAMAX i skonsultować się z lekarzem.
W przypadku pominięcia dawki FOSAMAX 70 mg raz w tygodniu należy poinstruować pacjentów, aby przyjmowali jedną dawkę rano po przypomnieniu sobie. Nie powinni przyjmować dwóch dawek tego samego dnia, ale powinni powrócić do przyjmowania jednej dawki raz w tygodniu, jak pierwotnie zaplanowano na wybrany dzień.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
92-tygodniowym badaniu rakotwórczości po podaniu doustnym alendronianu w dawkach 1, 3 i 10 mg/kg mc./ dzień (mężczyźni) lub 1, 2 i 5 mg/kg/dzień (kobiety). Dawki te są równoważne około 0,1 do 1 razy najwyższej zalecanej klinicznej dawki dobowej wynoszącej 40 mg w przeliczeniu na powierzchnię, mg/m². Znaczenie tego odkrycia dla ludzi nie jest znane.
W dwuletnim badaniu rakotwórczości po podaniu doustnym dawek 1 i 3,75 mg/kg masy ciała u samców szczurów otrzymujących dużą dawkę (p=0,003) stwierdzono wzrost gruczolaków komórek okołopęcherzykowych (tarczycy). Dawki te odpowiadają w przybliżeniu 0,3 i 1 razy klinicznej dawce dobowej 40 mg w przeliczeniu na powierzchnię, mg/m². Znaczenie tego odkrycia dla ludzi nie jest znane.
Alendronian nie był genotoksyczny w teście mutagenezy mikrobiologicznej in vitro z aktywacją metaboliczną i bez aktywacji metabolicznej, w teście mutagenezy komórek ssaków in vitro, w teście elucji alkalicznej in vitro w hepatocytach szczura oraz w teście aberracji chromosomowych in vivo u myszy. Jednak w teście aberracji chromosomowych in vitro w komórkach jajnika chomika chińskiego alendronian dał niejednoznaczne wyniki.
Alendronian nie miał wpływu na płodność (samce i samice) szczurów w dawkach doustnych do 5 mg/kg/dobę (około 1-krotność klinicznej dawki dobowej 40 mg w przeliczeniu na powierzchnię, mg/m²).
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
Dostępne dane dotyczące stosowania preparatu FOSAMAX u kobiet w ciąży są niewystarczające, aby poinformować o związanym z lekiem ryzyku niekorzystnych wyników dla matki lub płodu. Odstawić FOSAMAX 35 mg po stwierdzeniu ciąży.
badaniach na zwierzętach dotyczących reprodukcji, codzienne doustne podawanie alendronianu szczurom przed kryciem aż do końca ciąży lub laktacji wykazało skrócenie przeżycia po implantacji i zmniejszenie przyrostu masy ciała u młodych, począwszy od dawek odpowiadających mniej niż połowie najwyższej zalecanej klinicznej dawki dobowej 40 mg ( w oparciu o powierzchnię ciała, mg/m²). Doustne podawanie alendronianu szczurom w trakcie organogenezy powodowało zmniejszenie kostnienia płodu, począwszy od dawek trzykrotnie większych niż kliniczna dawka dobowa 40 mg. Nie zaobserwowano podobnych działań na płód u ciężarnych królików, którym podawano doustnie podczas organogenezy dawki odpowiadające około 10-krotności klinicznej dawki dobowej 40 mg.
Opóźnione lub nieudane porody, przedłużający się poród oraz zgony matek i płodów w późnej ciąży z powodu hipokalcemii matki występowały u szczurów po podaniu doustnych dawek tak niskich, jak jedna dziesiąta klinicznej dawki dobowej 40 mg (patrz Dane ).
Bisfosfoniany są wbudowywane w macierz kostną, z której są stopniowo uwalniane na przestrzeni lat. Ilość bisfosfonianu wprowadzonego do kości dorosłego człowieka i dostępnego do uwolnienia do krążenia ogólnego jest bezpośrednio związana z dawką i czasem stosowania bisfosfonianu. W związku z tym, w oparciu o mechanizm działania bisfosfonianów, istnieje potencjalne ryzyko uszkodzenia płodu, głównie kośćca, jeśli kobieta zajdzie w ciążę po zakończeniu leczenia bisfosfonianami. Nie badano wpływu zmiennych, takich jak czas od przerwania leczenia bisfosfonianami do poczęcia, konkretny zastosowany bisfosfonian oraz droga podania (dożylna lub doustna) na ryzyko.
Szacowane ryzyko tła poważnych wad wrodzonych i poronienia dla wskazanej populacji jest nieznane. Wszystkie ciąże niosą ze sobą ryzyko wad wrodzonych, utraty lub innych niekorzystnych skutków. W ogólnej populacji USA szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2-4% i 15-20%.
Dane
Dane zwierząt
Badania rozrodu u szczurów, którym podawano doustnie od okresu przed kryciem do końca ciąży lub laktacji, wykazały zmniejszoną przeżywalność po implantacji, zaczynając od 2 mg/kg/dobę i zmniejszony przyrost masy ciała, począwszy od 1 mg/kg/dobę, dawki odpowiadające mniej niż połowie 40 mg kliniczna dawka dobowa w zależności od powierzchni ciała, mg/m². Częstość występowania niepełnego kostnienia płodu w kościach kręgów, czaszki i mostka była zwiększona u szczurów, którym podawano doustnie podczas organogenezy, począwszy od dawki 10 mg/kg mc./dobę (około 3-krotność klinicznej dawki dobowej 40 mg). Nie zaobserwowano podobnych działań na płód u ciężarnych królików, którym podawano doustnie podczas organogenezy dawkę do 35 mg/kg/dobę (co odpowiada około 10-krotności klinicznej dawki dobowej 40 mg).
Zarówno całkowity, jak i zjonizowany wapń zmniejszył się u ciężarnych szczurów, którym podawano doustnie alendronian w dawce 15 mg/kg/dobę (około 4-krotność klinicznej dawki dobowej 40 mg), powodując opóźnienia i niepowodzenia porodu. Obserwowano przedłużający się poród spowodowany hipokalcemią matki, gdy szczury były leczone od okresu przed kryciem aż do ciąży, zaczynając od dawki 0,5 mg/kg/dobę (około jedna dziesiąta klinicznej dawki dobowej 40 mg). Toksyczność dla matki (zgony w późnej ciąży) wystąpiły również u samic szczurów, którym podawano doustnie 15 mg/kg/dobę (około 4-krotność klinicznej dawki dobowej 40 mg) w różnych okresach ciąży. Te zgony matek zostały zmniejszone, ale nie wyeliminowane przez zaprzestanie leczenia. Suplementacja wapnia w wodzie pitnej lub podskórnej minipompce szczurom, którym podawano doustnie alendronian w dawce 15 mg/kg/dobę, nie mogła złagodzić hipokalcemii ani zapobiec zgonom matek i noworodków związanych z dystocją. Jednak dożylna suplementacja wapnia zapobiegała zgonom matek, ale nie noworodków.
Laktacja
Podsumowanie ryzyka
Nie wiadomo, czy alendronian jest obecny w mleku kobiecym, wpływa na produkcję mleka kobiecego lub ma wpływ na niemowlę karmione piersią. Należy wziąć pod uwagę korzyści rozwojowe i zdrowotne wynikające z karmienia piersią, a także kliniczne zapotrzebowanie matki na FOSAMAX 70 mg oraz wszelkie potencjalne niekorzystne skutki stosowania FOSAMAX na dziecko karmione piersią lub wynikające z tego schorzenia.
Zastosowanie pediatryczne
FOSAMAX 70mg nie jest wskazany do stosowania u dzieci.
Bezpieczeństwo i skuteczność preparatu FOSAMAX badano w randomizowanym, podwójnie zaślepionym, kontrolowanym placebo dwuletnim badaniu z udziałem 139 pacjentów pediatrycznych w wieku 4-18 lat z ciężką wrodzoną łamliwością kości (OI). Stu dziewięciu pacjentów zostało losowo przydzielonych do grupy otrzymującej 5 mg FOSAMAX 35 mg na dobę (masa ciała poniżej 40 kg) lub 10 mg FOSAMAX 70 mg na dobę (masa ciała większa lub równa 40 kg), a 30 pacjentów do grupy placebo. Średnia wyjściowa wartość Z-score BMD kręgosłupa lędźwiowego pacjentów wynosiła -4,5. Średnia zmiana wskaźnika Z-score BMD kręgosłupa lędźwiowego od wartości początkowej do miesiąca 24 wyniosła 1,3 u pacjentów leczonych FOSAMAX 35 mg i 0,1 u pacjentów otrzymujących placebo. Leczenie FOSAMAX 35 mg nie zmniejszyło ryzyka złamań. Szesnaście procent pacjentów FOSAMAX, którzy doznali złamania potwierdzonego radiologicznie do 12. miesiąca badania, miało opóźnione gojenie złamań (przebudowa modzeli) lub brak zrostu złamania w ocenie radiologicznej w 24. miesiącu w porównaniu z 9% pacjentów otrzymujących placebo. U pacjentów leczonych preparatem FOSAMAX dane z histomorfometrii kości uzyskane w miesiącu 24 wykazały zmniejszony obrót kostny i opóźniony czas mineralizacji; nie było jednak defektów mineralizacji. Nie było statystycznie istotnych różnic pomiędzy grupami otrzymującymi FOSAMAX 35 mg i placebo w zmniejszaniu bólu kości. Biodostępność po podaniu doustnym u dzieci była podobna do obserwowanej u dorosłych.
Ogólny profil bezpieczeństwa preparatu FOSAMAX u pacjentów z wrodzoną łamliwością kości leczonych przez okres do 24 miesięcy był zasadniczo podobny do tego u dorosłych z osteoporozą leczonych preparatem FOSAMAX. Jednak u pacjentów z wrodzoną łamliwością kości leczonych preparatem FOSAMAX występowało częstsze występowanie wymiotów w porównaniu z placebo. Podczas 24-miesięcznego okresu leczenia wymioty obserwowano u 32 z 109 (29,4%) pacjentów leczonych FOSAMAX 70 mg i 3 z 30 (10%) pacjentów otrzymujących placebo.
W badaniu farmakokinetycznym u 6 z 24 dzieci z wrodzoną wadą osteogenezy, które otrzymały pojedynczą doustną dawkę produktu FOSAMAX 35 lub 70 mg, wystąpiła gorączka, objawy grypopodobne i (lub) łagodna limfocytopenia w ciągu 24 do 48 godzin po podaniu. Zdarzenia te, trwające nie dłużej niż 2 do 3 dni i odpowiadające na paracetamol, są zgodne z odpowiedzią ostrej fazy obserwowaną u pacjentów otrzymujących bisfosfoniany, w tym FOSAMAX. [Widzieć DZIAŁANIA NIEPOŻĄDANE ]
Zastosowanie geriatryczne
Spośród pacjentów otrzymujących FOSAMAX w badaniu Fracture Intervention Trial (FIT), 71% (n=2302) miało co najmniej 65 lat, a 17% (n=550) było co najmniej 75 lat. Spośród pacjentów otrzymujących FOSAMAX 70 mg w Stanach Zjednoczonych i międzynarodowe badania leczenia osteoporozy u kobiet, badania nad osteoporozą u mężczyzn, badania nad osteoporozą indukowaną glikokortykosteroidami oraz badania nad chorobą Pageta [patrz Studia kliniczne ], odpowiednio 45%, 54%, 37% i 70% miało 65 lat lub więcej. Nie zaobserwowano ogólnych różnic w skuteczności lub bezpieczeństwie między tymi pacjentami a młodszymi pacjentami, ale nie można wykluczyć większej wrażliwości niektórych starszych osób.
Zaburzenia czynności nerek
FOSAMAX 70 mg nie jest zalecany u pacjentów z klirensem kreatyniny mniejszym niż 35 ml/min. Nie ma konieczności dostosowania dawkowania u pacjentów z wartościami klirensu kreatyniny w zakresie 35-60 ml/min [patrz FARMAKOLOGIA KLINICZNA ].
Niewydolność wątroby
Ponieważ istnieją dowody, że alendronian nie jest metabolizowany ani wydalany z żółcią, nie przeprowadzono badań u pacjentów z zaburzeniami czynności wątroby. Nie jest konieczne dostosowanie dawki [patrz FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
Znaczącą śmiertelność po pojedynczych dawkach doustnych zaobserwowano u samic szczurów i myszy przy odpowiednio 552 mg/kg (3256 mg/m²) i 966 mg/kg (2898 mg/m²). U mężczyzn wartości te były nieco wyższe, odpowiednio 626 i 1280 mg/kg. Nie stwierdzono śmiertelności u psów przy dawkach doustnych do 200 mg/kg (4000 mg/m²).
Brak szczegółowych informacji dotyczących leczenia przedawkowania FOSAMAX. Hipokalcemia, hipofosfatemia i działania niepożądane dotyczące górnego odcinka przewodu pokarmowego, takie jak rozstrój żołądka, zgaga, zapalenie przełyku, zapalenie żołądka lub wrzód, mogą wynikać z przedawkowania doustnego. W celu związania alendronianu należy podawać mleko lub leki zobojętniające. Ze względu na ryzyko podrażnienia przełyku nie należy wywoływać wymiotów, a pacjent powinien pozostać w pełnej pozycji pionowej.
Dializa nie byłaby korzystna.
PRZECIWWSKAZANIA
FOSAMAX 35mg jest przeciwwskazany u pacjentów z następującymi schorzeniami:
- Nieprawidłowości przełyku, które opóźniają opróżnianie przełyku, takie jak zwężenie lub achalazja [patrz OSTRZEŻENIA I ŚRODKI ]
- Niezdolność do stania lub siedzenia prosto przez co najmniej 30 minut [patrz DAWKOWANIE I SPOSÓB PODAWANIA ; OSTRZEŻENIA I ŚRODKI ]
- Nie podawać leku FOSAMAX 35 mg roztwór doustny pacjentom ze zwiększonym ryzykiem zachłyśnięcia.
- Hipokalcemia [patrz OSTRZEŻENIA I ŚRODKI ]
- Nadwrażliwość na którykolwiek składnik tego produktu. Zgłaszano reakcje nadwrażliwości, w tym pokrzywkę i obrzęk naczynioruchowy [patrz DZIAŁANIA NIEPOŻĄDANE ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Badania na zwierzętach wykazały następujący sposób działania. Na poziomie komórkowym alendronian wykazuje preferencyjną lokalizację w miejscach resorpcji kości, szczególnie pod osteoklastami. Osteoklasty normalnie przylegają do powierzchni kości, ale nie mają pofałdowanej granicy, która wskazuje na aktywną resorpcję. Alendronian nie zaburza rekrutacji lub przyłączania osteoklastów, ale hamuje aktywność osteoklastów. Badania na myszach dotyczące lokalizacji radioaktywnego [3H]alendronianu w kościach wykazały około 10-krotnie wyższy wychwyt na powierzchni osteoklastów niż na powierzchni osteoblastów. Kości badane 6 i 49 dni po podaniu [3H]alendronianu odpowiednio szczurom i myszom wykazały, że normalna kość utworzyła się na wierzchu alendronianu, który został włączony do macierzy. Alendronian, włączony do macierzy kostnej, nie jest aktywny farmakologicznie. Dlatego alendronian musi być podawany w sposób ciągły w celu zahamowania osteoklastów na nowo utworzonych powierzchniach resorpcyjnych. Histomorfometria u pawianów i szczurów wykazała, że leczenie alendronianem zmniejsza obrót kostny (tj. liczbę miejsc, w których następuje przebudowa kości). Ponadto tworzenie kości przekracza resorpcję kości w tych miejscach przebudowy, co prowadzi do postępującego przyrostu masy kostnej.

Farmakodynamika
Alendronian jest bisfosfonianem, który wiąże się z hydroksyapatytem kości i specyficznie hamuje aktywność osteoklastów, komórek resorbujących kości. Alendronian zmniejsza resorpcję kości bez bezpośredniego wpływu na tworzenie kości, chociaż ten ostatni proces jest ostatecznie zmniejszony, ponieważ resorpcja i tworzenie kości są sprzężone podczas obrotu kostnego.
Osteoporoza u kobiet po menopauzie
Osteoporoza charakteryzuje się niską masą kostną, co prowadzi do zwiększonego ryzyka złamań. Rozpoznanie może potwierdzić stwierdzenie małej masy kostnej, złamanie na zdjęciu rentgenowskim, złamanie osteoporotyczne w wywiadzie lub utrata wzrostu lub kifoza wskazująca na złamanie kręgu (kręgosłupa). Osteoporoza występuje zarówno u mężczyzn, jak iu kobiet, ale najczęściej występuje u kobiet po menopauzie, kiedy zwiększa się obrót kostny, a szybkość resorpcji kości przekracza tempo tworzenia kości. Zmiany te powodują postępującą utratę masy kostnej i prowadzą do osteoporozy u znacznej części kobiet po 50 roku życia. Częstymi konsekwencjami są złamania, zwykle kręgosłupa, biodra i nadgarstka. Od 50 do 90 lat ryzyko złamania szyjki kości udowej u białych kobiet wzrasta 50-krotnie, a ryzyko złamań kręgów 15- do 30-krotnie. Szacuje się, że około 40% 50-letnich kobiet dozna jednego lub więcej złamań kręgosłupa, biodra lub nadgarstka związanych z osteoporozą w ciągu pozostałych ich życia. W szczególności złamania biodra wiążą się ze znaczną zachorowalnością, niepełnosprawnością i śmiertelnością.
Codzienne doustne dawki alendronianu (5, 20 i 40 mg przez sześć tygodni) u kobiet po menopauzie powodowały zmiany biochemiczne wskazujące na zależne od dawki hamowanie resorpcji kości, w tym zmniejszenie stężenia wapnia w moczu i markerów degradacji kolagenu kostnego w moczu (takich jak deoksypirydynolina i połączone N-telopeptydy kolagenu typu I). Te zmiany biochemiczne miały tendencję do powrotu do wartości wyjściowych już po 3 tygodniach od przerwania terapii alendronianem i nie różniły się od placebo po 7 miesiącach.
Długotrwałe leczenie osteoporozy preparatem FOSAMAX 10 mg/dobę (do pięciu lat) zmniejszyło wydalanie z moczem markerów resorpcji kości, deoksypirydynoliny i usieciowanych N-telopeptydów kolagenu typu I odpowiednio o około 50% i 70% , aby osiągnąć poziom podobny do obserwowanego u zdrowych kobiet przed menopauzą. Podobne spadki zaobserwowano u pacjentów w badaniach dotyczących zapobiegania osteoporozie, którzy otrzymywali FOSAMAX 5 mg/dobę. Spadek tempa resorpcji kości wskazywany przez te markery był widoczny już po jednym miesiącu, a po trzech do sześciu miesiącach osiągnął plateau, które utrzymywało się przez cały czas leczenia FOSAMAX. W badaniach dotyczących leczenia osteoporozy FOSAMAX w dawce 10 mg/dobę zmniejszał markery kościotworzenia, osteokalcyny i fosfatazy alkalicznej swoistej dla kości o około 50% oraz całkowitą fosfatazę alkaliczną w surowicy o około 25 do 30%, aby osiągnąć plateau po 6 do 12 miesiącach. W badaniach dotyczących zapobiegania osteoporozie, FOSAMAX 5 mg/dobę zmniejszał poziom osteokalcyny i całkowitej fosfatazy zasadowej w surowicy odpowiednio o około 40% i 15%. Podobne zmniejszenie tempa obrotu kostnego obserwowano u kobiet po menopauzie podczas rocznych badań, w których FOSAMAX 70 mg raz w tygodniu był stosowany w leczeniu osteoporozy, a raz w tygodniu 35 mg FOSAMAX w zapobieganiu osteoporozie. Dane te wskazują, że tempo obrotu kostnego osiągnęło nowy stan stacjonarny, pomimo postępującego wzrostu całkowitej ilości alendronianu odkładającego się w kości.
wyniku zahamowania resorpcji kości po leczeniu preparatem FOSAMAX obserwowano również bezobjawowe zmniejszenie stężenia wapnia i fosforanów w surowicy. W badaniach długoterminowych, zmniejszenie stężenia wapnia w surowicy (około 2%) i fosforanów (około 4 do 6%) w stosunku do wartości początkowej było widoczne w pierwszym miesiącu po rozpoczęciu podawania FOSAMAX 10 mg. Nie zaobserwowano dalszego spadku stężenia wapnia w surowicy w ciągu pięciu lat leczenia; jednak poziom fosforanów w surowicy powrócił do poziomu sprzed badania w ciągu lat od trzeciego do piątego. Podobne redukcje obserwowano po podaniu FOSAMAX 5 mg/dobę. W rocznych badaniach z FOSAMAX 35 i 70 mg raz w tygodniu podobne zmniejszenie obserwowano po 6 i 12 miesiącach. Zmniejszenie stężenia fosforanów w surowicy może odzwierciedlać nie tylko dodatni bilans mineralny kości dzięki FOSAMAX 70 mg, ale także zmniejszenie zwrotnego wchłaniania fosforanów przez nerki.
Osteoporoza u mężczyzn
Leczenie mężczyzn z osteoporozą preparatem FOSAMAX 10 mg/dobę przez dwa lata zmniejszyło wydalanie z moczem usieciowanych N-telopeptydów kolagenu typu I o około 60% i fosfatazy alkalicznej swoistej dla kości o około 40%. Podobne zmniejszenie zaobserwowano w rocznym badaniu u mężczyzn z osteoporozą otrzymujących raz w tygodniu FOSAMAX 70 mg.
Osteoporoza indukowana glukokortykoidami
Długotrwałe stosowanie glikokortykosteroidów jest często związane z rozwojem osteoporozy i wynikającymi z niej złamaniami (zwłaszcza kręgów, biodra i żeber). Występuje zarówno u mężczyzn, jak iu kobiet w każdym wieku. Osteoporoza występuje w wyniku zahamowania tworzenia się kości i zwiększonej resorpcji kości, co skutkuje utratą masy kostnej netto. Alendronian zmniejsza resorpcję kości bez bezpośredniego hamowania tworzenia kości.
badaniach klinicznych trwających do dwóch lat' czas trwania, FOSAMAX 5 i 10 mg/dobę redukował usieciowane N-telopeptydy kolagenu typu I (marker resorpcji kości) o około 60% oraz redukował swoistą dla kości fosfatazę alkaliczną i całkowitą fosfatazę alkaliczną w surowicy (markery tworzenia kości) przez odpowiednio około 15 do 30% i 8 do 18%. W wyniku zahamowania resorpcji kości, FOSAMAX 5 i 10 mg/dobę wywoływały bezobjawowe zmniejszenie stężenia wapnia w surowicy (około 1 do 2%) i fosforanów w surowicy (około 1 do 8%).
Choroba Pageta kości
Choroba Pageta kości jest przewlekłą, ogniskową chorobą szkieletową charakteryzującą się znacznie nasiloną i nieuporządkowaną przebudową kości. Po nadmiernej osteoklastycznej resorpcji kości następuje osteoblastyczne tworzenie nowej kości, co prowadzi do zastąpienia normalnej architektury kości przez zdezorganizowaną, powiększoną i osłabioną strukturę kości.
Objawy kliniczne choroby Pageta wahają się od braku objawów do ciężkiej chorobowości spowodowanej bólem kości, deformacją kości, złamaniami patologicznymi oraz powikłaniami neurologicznymi i innymi. Fosfataza zasadowa w surowicy, najczęściej stosowany biochemiczny wskaźnik aktywności choroby, stanowi obiektywną miarę ciężkości choroby i odpowiedzi na terapię.
FOSAMAX 70mg bezpośrednio zmniejsza szybkość resorpcji kości, co prowadzi do pośredniego zmniejszenia kościotworzenia. W badaniach klinicznych FOSAMAX w dawce 40 mg raz na dobę przez sześć miesięcy powodował znaczne zmniejszenie stężenia fosfatazy zasadowej w surowicy oraz markerów degradacji kolagenu kostnego w moczu. W wyniku zahamowania resorpcji kości, FOSAMAX wywoływał na ogół łagodne, przemijające i bezobjawowe zmniejszenie stężenia wapnia i fosforanów w surowicy.
Farmakokinetyka
Wchłanianie
porównaniu z referencyjną dawką dożylną, średnia biodostępność alendronianu po podaniu doustnym u kobiet wynosiła 0,64% dla dawek w zakresie od 5 do 70 mg przy podawaniu po całonocnym poszczeniu i na dwie godziny przed standardowym śniadaniem. Biodostępność po podaniu doustnym tabletki 10 mg u mężczyzn (0,59%) była podobna do tej u kobiet po całonocnym poszczeniu i 2 godziny przed śniadaniem.
FOSAMAX 70 mg roztwór doustny i FOSAMAX 70 mg tabletka są równie biodostępne.
Badanie oceniające wpływ pory posiłku na biodostępność alendronianu przeprowadzono u 49 kobiet po menopauzie. Biodostępność była zmniejszona (o około 40%), gdy 10 mg alendronianu podano 0,5 lub 1 godzinę przed standardowym śniadaniem, w porównaniu z dawką 2 godziny przed jedzeniem. W badaniach dotyczących leczenia i zapobiegania osteoporozie alendronian był skuteczny, gdy był podawany co najmniej 30 minut przed śniadaniem.
Dostępność biologiczna była nieistotna, niezależnie od tego, czy alendronian był podawany z lub do dwóch godzin po standardowym śniadaniu. Jednoczesne podawanie alendronianu z kawą lub sokiem pomarańczowym zmniejszało biodostępność o około 60%.
Dystrybucja
Badania przedkliniczne (na samcach szczurów) wykazały, że alendronian przejściowo przenika do tkanek miękkich po podaniu dożylnym w dawce 1 mg/kg, ale następnie jest szybko redystrybuowany do kości lub wydalany z moczem. Średnia objętość dystrybucji w stanie stacjonarnym, z wyłączeniem kości, wynosi u ludzi co najmniej 28 l. Stężenia leku w osoczu po terapeutycznych dawkach doustnych są zbyt niskie (poniżej 5 ng/ml) do wykrywania analitycznego. Wiązanie z białkami w ludzkim osoczu wynosi około 78%.
Metabolizm
Nie ma dowodów na to, że alendronian jest metabolizowany u zwierząt lub ludzi.
Wydalanie
Po podaniu pojedynczej dawki dożylnej [14C]alendronianu, około 50% radioaktywności zostało wydalone z moczem w ciągu 72 godzin, aw kale odzyskano niewielką lub wcale radioaktywność. Po podaniu pojedynczej dawki dożylnej 10 mg klirens nerkowy alendronianu wynosił 71 ml/min (64, 78; 90% przedział ufności [CI]), a klirens ogólnoustrojowy nie przekraczał 200 ml/min. Stężenia w osoczu spadły o ponad 95% w ciągu 6 godzin po podaniu dożylnym. Szacuje się, że końcowy okres półtrwania u ludzi przekracza 10 lat, prawdopodobnie odzwierciedlając uwalnianie alendronianu ze szkieletu. Na podstawie powyższego szacuje się, że po 10 latach doustnego leczenia FOSAMAX (10 mg dziennie) ilość alendronianu uwalnianego codziennie ze szkieletu wynosi około 25% ilości wchłanianej z przewodu pokarmowego.
Określone populacje
Płeć
Biodostępność i frakcja dawki dożylnej wydalana z moczem były podobne u mężczyzn i kobiet.
Geriatryczny
Biodostępność i rozmieszczenie (wydalanie z moczem) były podobne u pacjentów w podeszłym wieku i młodszych. Nie ma konieczności dostosowania dawkowania u pacjentów w podeszłym wieku.
Wyścig
Nie badano różnic farmakokinetycznych ze względu na rasę.
Zaburzenia czynności nerek
Badania przedkliniczne pokazują, że u szczurów z niewydolnością nerek wzrastające ilości leku są obecne w osoczu, nerkach, śledzionie i piszczeli. U zdrowych osób lek, który nie odkłada się w kościach, jest szybko wydalany z moczem. Nie znaleziono dowodów na wysycenie wychwytu kostnego po 3 tygodniach podawania skumulowanych dożylnych dawek 35 mg/kg młodym samcom szczurów. Chociaż nie przeprowadzono żadnych formalnych badań farmakokinetycznych dotyczących zaburzeń czynności nerek u pacjentów, prawdopodobne jest, że podobnie jak u zwierząt, eliminacja alendronianu przez nerki będzie zmniejszona u pacjentów z zaburzeniami czynności nerek. Dlatego też można oczekiwać nieco większej akumulacji alendronianu w kościach u pacjentów z zaburzeniami czynności nerek.
Nie ma konieczności dostosowania dawkowania u pacjentów z klirensem kreatyniny 35 do 60 ml/min. FOSAMAX 35 mg nie jest zalecany u pacjentów z klirensem kreatyniny mniejszym niż 35 ml/min ze względu na brak doświadczenia z alendronianem w niewydolności nerek.
Niewydolność wątroby
Ponieważ istnieją dowody, że alendronian nie jest metabolizowany ani wydalany z żółcią, nie przeprowadzono badań u pacjentów z zaburzeniami czynności wątroby. Nie jest konieczne dostosowanie dawki.
Interakcje leków
Wykazano, że dożylna ranitydyna podwaja biodostępność alendronianu podawanego doustnie. Kliniczne znaczenie tej zwiększonej biodostępności oraz to, czy podobny wzrost wystąpi u pacjentów otrzymujących doustnie antagonistów receptora H2, nie jest znane.
U zdrowych osób prednizon podawany doustnie (20 mg trzy razy na dobę przez pięć dni) nie powodował klinicznie znaczącej zmiany biodostępności alendronianu po podaniu doustnym (średni wzrost w zakresie od 20 do 44%).
Produkty zawierające wapń i inne kationy wielowartościowe mogą zakłócać wchłanianie alendronianu.
Toksykologia i/lub farmakologia zwierząt
Względne działanie hamujące na resorpcję kości i mineralizację alendronianu i etidronianu porównano w teście Schenka, który opiera się na badaniu histologicznym nasad kości rosnących szczurów. W tym teście najniższa dawka alendronianu, która zakłócała mineralizację kości (prowadząc do osteomalacji) była 6000-krotnie większa od dawki antyresorpcyjnej. Odpowiedni stosunek dla etidronianu wynosił jeden do jednego. Dane te sugerują, że alendronian podawany w dawkach terapeutycznych prawdopodobnie nie wywoła osteomalacji.
Studia kliniczne
Leczenie osteoporozy u kobiet po menopauzie
Dzienne dozowanie
Skuteczność FOSAMAX 10 mg na dobę oceniano w czterech badaniach klinicznych. Do badania 1, trzyletniego, wieloośrodkowego, podwójnie zaślepionego, kontrolowanego placebo badania klinicznego w Stanach Zjednoczonych włączono 478 pacjentów z BMD T-score na poziomie lub poniżej minus 2,5 z lub bez wcześniejszego złamania kręgów; Badanie 2, trzyletnie, wieloośrodkowe, prowadzone metodą podwójnie ślepej próby, kontrolowane placebo Wielonarodowe badanie kliniczne obejmowało 516 pacjentów z BMD T-score na poziomie minus 2,5 lub poniżej, z lub bez wcześniejszego złamania kręgów; Badanie 3, trzyletnie badanie Fracture Intervention Trial (FIT), badanie, do którego włączono 2027 pacjentów po menopauzie z co najmniej jednym wyjściowym złamaniem kręgu; oraz badanie 4, czteroletnie badanie FIT: badanie, do którego włączono 4432 pacjentki po menopauzie z niską masą kostną, ale bez wyjściowego złamania kręgów.
Wpływ na częstość występowania złamań
Aby ocenić wpływ preparatu FOSAMAX na częstość występowania złamań kręgów (wykrywanych za pomocą radiografii cyfrowej; około jedna trzecia z nich miała objawy kliniczne), badania amerykańskie i międzynarodowe połączono w analizie porównującej placebo z grupami dawek zbiorczych preparatu FOSAMAX (5 lub 10 mg przez trzy lata lub 20 mg przez dwa lata, a następnie 5 mg przez rok). Wystąpiło statystycznie istotne zmniejszenie odsetka pacjentów leczonych preparatem FOSAMAX 70 mg, u których wystąpiło jedno lub więcej nowych złamań kręgów w porównaniu z pacjentami otrzymującymi placebo (3,2% w porównaniu z 6,2%; względne zmniejszenie ryzyka o 48%). Zaobserwowano również zmniejszenie całkowitej liczby nowych złamań kręgów (4,2 vs 11,3 na 100 pacjentów). W analizie zbiorczej pacjenci, którzy otrzymywali FOSAMAX, mieli statystycznie istotnie mniejszą utratę wzrostu niż obserwowana u pacjentów otrzymujących placebo (-3,0 mm w porównaniu z -4,6 mm).
Badanie Fracture Intervention Trial (FIT) składało się z dwóch badań u kobiet po menopauzie: trzyletniego badania pacjentów, u których wystąpiło co najmniej jedno wyjściowe radiologiczne złamanie kręgów oraz czteroletniego badania pacjentów z niską masą kostną, ale bez wyjściowego złamania kręgów. W obu badaniach FIT 96% zrandomizowanych pacjentów ukończyło badania (tj. odbyło wizytę zamykającą przed planowanym zakończeniem badania); około 80% pacjentów po zakończeniu nadal przyjmowało badany lek.
Fracture Intervention Trial: Badanie trzyletnie (pacjenci z co najmniej jednym wyjściowym radiograficznym złamaniem kręgu)
To randomizowane, podwójnie zaślepione, kontrolowane placebo badanie z udziałem 2027 pacjentów (FOSAMAX 70 mg, n=1022; placebo, n=1005) wykazało, że leczenie preparatem FOSAMAX spowodowało statystycznie istotne zmniejszenie częstości złamań po trzech latach, jak pokazano w Tabeli 6. .
Ponadto w tej populacji pacjentów z wyjściowym złamaniem kręgów leczenie preparatem FOSAMAX istotnie zmniejszyło częstość hospitalizacji (25,0% vs. 30,7%).
W trzyletnim badaniu FIT złamania biodra wystąpiły u 22 (2,2%) ze 1005 pacjentów otrzymujących placebo i 11 (1,1%) z 1022 pacjentów otrzymujących FOSAMAX, p=0,047. Rycina 1 przedstawia skumulowaną częstość złamań szyjki kości udowej w tym badaniu.
Rycina 1: Skumulowany częstość występowania złamań biodra w trzyletnim badaniu FIT (pacjenci z radiograficznym złamaniem kręgów na początku badania)
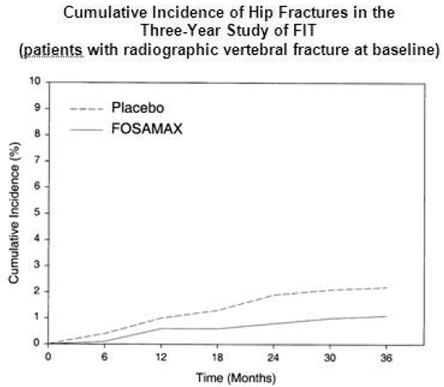
Badanie interwencyjne złamań: badanie czteroletnie (pacjenci z niską masą kostną, ale bez wyjściowego radiograficznego złamania kręgu)
tym randomizowanym, podwójnie zaślepionym, kontrolowanym placebo badaniu obejmującym 4432 pacjentów (FOSAMAX 70 mg, n=2214; placebo, n=2218) dalej badano zmniejszenie częstości złamań w wyniku stosowania FOSAMAX. Celem badania była rekrutacja kobiet z osteoporozą, zdefiniowaną jako wyjściowa BMD szyjki kości udowej z co najmniej dwoma odchyleniami standardowymi poniżej średniej dla młodych dorosłych kobiet. Jednak ze względu na kolejne rewizje wartości normatywnych BMD szyjki kości udowej stwierdzono, że 31% pacjentów nie spełnia tego kryterium włączenia, a zatem do badania włączono zarówno kobiety z osteoporozą, jak i bez osteoporozy. Wyniki przedstawiono w tabeli 7 dla pacjentów z osteoporozą.
Wyniki dotyczące złamań w różnych badaniach
trzyletnim badaniu FIT FOSAMAX 35 mg zmniejszył odsetek kobiet, u których wystąpiło co najmniej jedno nowe złamanie kręgu w radiografii z 15,0% do 7,9% (47% względne zmniejszenie ryzyka, p
FOSAMAX zmniejszył odsetek kobiet doświadczających wielu (dwóch lub więcej) nowych złamań kręgów z 4,2% do 0,6% (87% względne zmniejszenie ryzyka, p
związku z tym FOSAMAX 35 mg zmniejszył częstość występowania radiograficznych złamań kręgów u kobiet z osteoporozą, niezależnie od tego, czy miały one wcześniejsze radiologiczne złamania kręgów.
Wpływ na gęstość mineralną kości
Skuteczność gęstości mineralnej kości FOSAMAX 10 mg raz na dobę u kobiet po menopauzie w wieku od 44 do 84 lat z osteoporozą (gęstość mineralna kości kręgosłupa lędźwiowego [BMD] o co najmniej 2 odchylenia standardowe poniżej średniej przedmenopauzalnej) wykazano w czterech ślepe, kontrolowane placebo badania kliniczne trwające dwa lub trzy lata Trwanie.
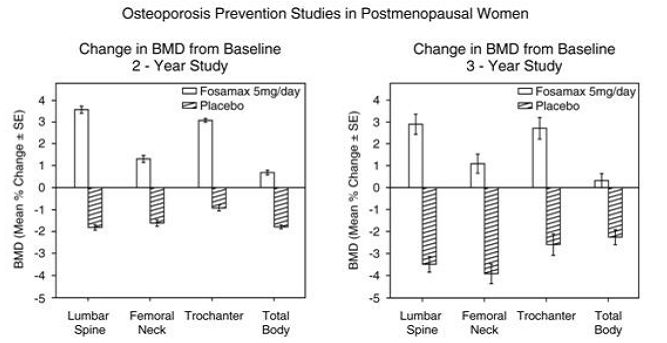
Rysunek 2 przedstawia średnie zwiększenie BMD kręgosłupa lędźwiowego, szyjki kości udowej i krętarza u pacjentów otrzymujących FOSAMAX w dawce 10 mg/dobę w porównaniu z pacjentami otrzymującymi placebo po trzech latach dla każdego z tych badań.
Rycina 2: Badania leczenia osteoporozy u kobiet po menopauzie Wzrost BMD FOSAMAX 10 mg/dzień po trzech latach
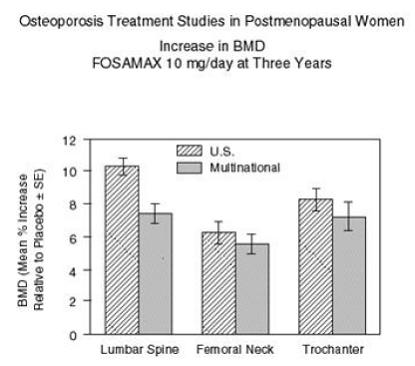
Po trzech latach w każdym miejscu pomiaru w każdym badaniu u pacjentów, którzy otrzymywali FOSAMAX w dawce 10 mg/dobę, obserwowano znaczący wzrost BMD, zarówno w stosunku do wartości wyjściowych, jak i placebo. BMD całego ciała również znacznie wzrosło w każdym badaniu, co sugeruje, że wzrost masy kostnej kręgosłupa i biodra nie nastąpił kosztem innych miejsc szkieletowych. Wzrost BMD był widoczny już po trzech miesiącach i trwał przez trzy lata leczenia. (Patrz Rycina 3 dla wyników dotyczących kręgosłupa lędźwiowego). W dwuletnim przedłużeniu tych badań leczenie 147 pacjentów FOSAMAX w dawce 10 mg/dobę spowodowało ciągły wzrost BMD w odcinku lędźwiowym kręgosłupa i krętarzu (bezwzględny dodatkowy wzrost między 3 a 5: kręgosłup lędźwiowy 0,94%; krętarz 0,88%). Utrzymano BMD szyjki kości udowej, przedramienia i całego ciała. FOSAMAX był podobnie skuteczny niezależnie od wieku, rasy, wyjściowego wskaźnika obrotu kostnego i wyjściowego BMD w badanym zakresie (co najmniej 2 odchylenia standardowe poniżej średniej przedmenopauzalnej).
Rycina 3: Badania leczenia osteoporozy u kobiet po menopauzie Przebieg czasowy działania FOSAMAX 10 mg/dobę w porównaniu z placebo: Procentowa zmiana BMD kręgosłupa lędźwiowego w stosunku do wartości wyjściowych
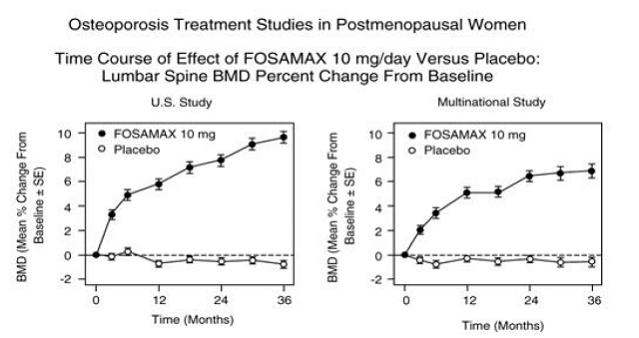
U pacjentek z osteoporozą pomenopauzalną leczonych FOSAMAX 10 mg/dobę przez rok lub dwa lata oceniano skutki przerwania leczenia. Po odstawieniu nie było dalszego wzrostu masy kostnej, a wskaźniki utraty masy kostnej były podobne do tych w grupach placebo.
Histologia kości
Badanie histologiczne kości u 270 pacjentek po menopauzie z osteoporozą leczonych preparatem FOSAMAX w dawkach od 1 do 20 mg/dobę przez rok, dwa lub trzy lata ujawniło prawidłową mineralizację i strukturę, jak również spodziewane zmniejszenie obrotu kostnego w porównaniu z placebo. Dane te, wraz z prawidłową histologią kości i zwiększoną wytrzymałością kości obserwowaną u szczurów i pawianów narażonych na długotrwałe leczenie alendronianem, potwierdzają wniosek, że kość powstająca podczas leczenia FOSAMAX 35 mg ma normalną jakość.
Wpływ na wysokość
FOSAMAX w okresie trzech lub czterech lat wiązał się ze statystycznie istotnym zmniejszeniem utraty wzrostu w porównaniu z placebo u pacjentów ze złamaniami kręgów w punkcie wyjściowym i bez nich. Pod koniec badań FIT różnice między grupami leczenia wynosiły 3,2 mm w badaniu trzyletnim i 1,3 mm w badaniu czteroletnim.
Dozowanie tygodniowe
Równoważność terapeutyczna FOSAMAX 70 mg raz w tygodniu (n=519) i FOSAMAX 10 mg na dobę (n=370) została wykazana w rocznym, podwójnie zaślepionym, wieloośrodkowym badaniu kobiet po menopauzie z osteoporozą. W pierwotnej analizie osób, które ukończyły badanie, średni wzrost BMD w odcinku lędźwiowym kręgosłupa w porównaniu z wartościami wyjściowymi po roku wyniósł 5,1% (4,8, 5,4%; 95% CI) w grupie otrzymującej 70 mg raz w tygodniu (n=440) i 5,4% ( 5,0, 5,8%; 95% CI) w grupie 10 mg na dobę (n=330). Obie grupy leczenia były również podobne pod względem wzrostu BMD w innych miejscach szkieletu. Wyniki analizy zamiaru leczenia były zgodne z pierwotną analizą osób, które ukończyły leczenie.
Jednoczesne stosowanie z estrogenową/hormonową terapią zastępczą (HTZ)
Wpływ na BMD leczenia FOSAMAX 10 mg raz na dobę i skoniugowanym estrogenem (0,625 mg/dobę) w monoterapii lub w skojarzeniu oceniano w dwuletnim, podwójnie zaślepionym, kontrolowanym placebo badaniu z histerektomią kobiet po menopauzie z osteoporozą (n= 425). Po dwóch latach wzrost BMD kręgosłupa lędźwiowego w stosunku do wartości wyjściowej był znacznie większy w przypadku kombinacji (8,3%) niż w przypadku samego estrogenu lub samego FOSAMAX (oba 6,0%).
Wpływ na BMD po dodaniu FOSAMAX 35 mg do stałych dawek (przez co najmniej jeden rok) HTZ (estrogen ± progestyna) oceniano w rocznym, podwójnie zaślepionym, kontrolowanym placebo badaniu u kobiet po menopauzie z osteoporozą (n=428). Dodanie FOSAMAX 10 mg raz na dobę do HTZ spowodowało, po roku, znacznie większy wzrost BMD kręgosłupa lędźwiowego (3,7%) w porównaniu z samą HTZ (1,1%).
badaniach tych znaczące wzrosty lub korzystne tendencje w BMD dla terapii skojarzonej w porównaniu z samą HTZ zaobserwowano w całym biodrze, szyjce kości udowej i krętarzu. Nie zaobserwowano znaczącego wpływu na BMD całego ciała.
Badania histomorfometryczne biopsji transbiodrowych u 92 pacjentów wykazały prawidłową architekturę kości. W porównaniu z placebo, po 18 miesiącach leczenia skojarzonego FOSAMAX 35 mg i HTZ wystąpiło 98% zahamowanie obrotu kostnego (ocenione na podstawie mineralizacji powierzchni), 94% przy samym FOSAMAX 35 mg i 78% przy samej HTZ. Nie badano długoterminowego wpływu skojarzonego FOSAMAX 35 mg i HTZ na występowanie złamań i gojenie złamań.
Zapobieganie osteoporozie u kobiet po menopauzie
Dzienne dozowanie
Zapobieganie utracie masy kostnej wykazano w dwóch podwójnie ślepych, kontrolowanych placebo badaniach kobiet po menopauzie w wieku 40-60 lat. Tysiąc sześćset dziewięć pacjentek (FOSAMAX 5 mg/dobę; n=498), które były co najmniej sześć miesięcy po menopauzie, zostało włączonych do dwuletniego badania bez względu na ich wyjściową BMD. W drugim badaniu 447 pacjentek (FOSAMAX 5 mg/dobę; n=88), w wieku od sześciu miesięcy do trzech lat po menopauzie, było leczonych przez okres do trzech lat. U pacjentów otrzymujących placebo obserwowano utratę BMD o około 1% rocznie w kręgosłupie, biodrze (szyjka kości udowej i krętarzu) i całym ciele. W przeciwieństwie do tego, FOSAMAX 5 mg/dzień zapobiegał utracie masy kostnej u większości pacjentów i wywoływał znaczny wzrost średniej masy kostnej w każdym z tych miejsc (patrz Rysunek 4). Ponadto FOSAMAX w dawce 5 mg/dobę zmniejszył szybkość utraty masy kostnej przedramienia o około połowę w porównaniu z placebo. FOSAMAX 5 mg/dobę był podobnie skuteczny w tej populacji, niezależnie od wieku, czasu od menopauzy, rasy i wyjściowego tempa obrotu kostnego.
Rycina 4: Badania profilaktyki osteoporozy u kobiet po menopauzie
Histologia kości
Histologia kości była prawidłowa u 28 pacjentów poddanych biopsji pod koniec trzech lat, którzy otrzymywali FOSAMAX w dawkach do 10 mg/dobę.
Dozowanie tygodniowe
Równoważność terapeutyczna FOSAMAX 35 mg raz w tygodniu (n=362) i FOSAMAX 5 mg na dobę (n=361) została wykazana w rocznym, podwójnie zaślepionym, wieloośrodkowym badaniu kobiet po menopauzie bez osteoporozy. W pierwotnej analizie osób, które ukończyły badanie, średni wzrost BMD w odcinku lędźwiowym kręgosłupa w porównaniu z wartościami wyjściowymi po roku wyniósł 2,9% (2,6, 3,2%; 95% CI) w grupie otrzymującej 35 mg raz w tygodniu (n=307) i 3,2% ( 2,9, 3,5%; 95% CI) w grupie 5 mg na dobę (n=298). Obie grupy leczenia były również podobne pod względem wzrostu BMD w innych miejscach szkieletu. Wyniki analizy zamiaru leczenia były zgodne z pierwotną analizą osób, które ukończyły leczenie.
Leczenie zwiększające masę kostną u mężczyzn z osteoporozą
Skuteczność preparatu FOSAMAX 35 mg u mężczyzn z osteoporozą hipogonadalną lub idiopatyczną wykazano w dwóch badaniach klinicznych.
Dzienne dozowanie
Do dwuletniego, podwójnie zaślepionego, kontrolowanego placebo, wieloośrodkowego badania FOSAMAX 10 mg raz na dobę włączono w sumie 241 mężczyzn w wieku od 31 do 87 lat (średnia 63). Wszyscy pacjenci biorący udział w badaniu mieli albo BMD T-score mniejsze lub równe -2 w obrębie szyjki kości udowej i mniejsze lub równe -1 w odcinku lędźwiowym kręgosłupa, albo początkowe złamanie osteoporotyczne i BMD T-score mniejsze niż lub równy -1 na szyjce kości udowej. Po dwóch latach średni wzrost BMD w porównaniu z placebo u mężczyzn otrzymujących FOSAMAX 10 mg/dobę był znaczący w następujących miejscach: kręgosłup lędźwiowy, 5,3%; szyjka udowa 2,6%; krętarz, 3,1%; i całego ciała 1,6%. Leczenie FOSAMAX 70 mg również zmniejszyło utratę wzrostu (FOSAMAX, -0,6 mm w porównaniu z placebo, -2,4 mm).
Dozowanie tygodniowe
Do rocznego, podwójnie zaślepionego, kontrolowanego placebo, wieloośrodkowego badania FOSAMAX 70 mg raz w tygodniu włączono łącznie 167 mężczyzn w wieku od 38 do 91 lat (średnia 66). Pacjenci biorący udział w badaniu mieli albo BMD T-score mniejsze lub równe -2 w okolicy szyjki kości udowej i mniejsze lub równe -1 w odcinku lędźwiowym kręgosłupa, albo BMD T-score mniejsze lub równe -2 w kręgosłupa lędźwiowego i mniejsze lub równe -1 w szyjce kości udowej lub początkowe złamanie osteoporotyczne i BMD T-score mniejsze lub równe -1 w szyjce kości udowej. Po roku średni wzrost BMD w porównaniu z placebo u mężczyzn otrzymujących FOSAMAX 70 mg raz w tygodniu był znaczący w następujących miejscach: kręgosłup lędźwiowy, 2,8%; szyja udowa 1,9%; krętarz, 2,0%; i całego ciała 1,2%. Te wzrosty BMD były podobne do obserwowanych po roku w badaniu 10 mg raz na dobę.
obu badaniach odpowiedzi BMD były podobne bez względu na wiek (większe lub równe 65 lat vs. mniej niż 65 lat), czynność gonad (początkowy testosteron poniżej 9 ng/dl vs. większy lub równy 9 ng/dl) lub wyjściową wartość BMD (T-score szyjki kości udowej i kręgosłupa lędźwiowego mniejszy lub równy -2,5 vs. większy niż -2,5).
Leczenie osteoporozy wywołanej glukokortykoidami
Skuteczność produktu FOSAMAX 5 i 10 mg raz na dobę u mężczyzn i kobiet otrzymujących glikokortykosteroidy (co najmniej 7,5 mg/dobę prednizonu lub odpowiednika) wykazano w dwóch jednorocznych, podwójnie zaślepionych, randomizowanych, kontrolowanych placebo, wieloośrodkowych badaniach praktycznie identyczny projekt, jeden wykonywany w Stanach Zjednoczonych, a drugi w 15 różnych krajach (wielonarodowy [który obejmował również FOSAMAX 2,5 mg/dzień]). Do badań tych włączono odpowiednio 232 i 328 pacjentów w wieku od 17 do 83 lat z różnymi chorobami wymagającymi glikokortykoidów. Pacjenci otrzymywali suplementację wapnia i witaminę D. Rycina 5 przedstawia średni wzrost w porównaniu z placebo BMD kręgosłupa lędźwiowego, szyjki kości udowej i krętarza u pacjentów otrzymujących FOSAMAX w dawce 5 mg/dobę w każdym badaniu.
Rycina 5: Badania u pacjentów leczonych glikokortykosteroidami Wzrost BMD FOSAMAX 5 mg/dobę po roku
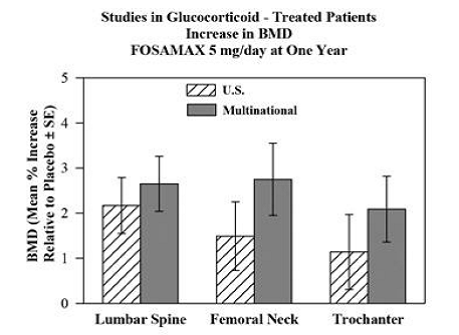
Po roku, w połączonych badaniach, w każdym z tych ośrodków, u pacjentów otrzymujących FOSAMAX w dawce 5 mg/dobę zaobserwowano znaczący wzrost BMD w porównaniu z placebo. U pacjentów otrzymujących placebo istotne zmniejszenie BMD wystąpiło w szyjce kości udowej (-1,2%), a mniejsze w odcinku lędźwiowym kręgosłupa i krętarzu. BMD całego ciała utrzymywano stosując FOSAMAX 5 mg/dobę. Wzrost BMD po podaniu FOSAMAX 10 mg/dobę był podobny do wzrostu po podaniu FOSAMAX 5 mg/dobę u wszystkich pacjentek z wyjątkiem kobiet po menopauzie nieotrzymujących terapii estrogenowej. U tych kobiet wzrost (w porównaniu do placebo) podczas stosowania FOSAMAX 10 mg/dobę był większy niż podczas stosowania FOSAMAX 5 mg/dobę w odcinku lędźwiowym kręgosłupa (4,1% w porównaniu z 1,6%) i krętarzu (2,8% w porównaniu z 1,7%), ale nie w innych witrynach. FOSAMAX 35 mg był skuteczny niezależnie od dawki i czasu trwania stosowania glikokortykosteroidów. Ponadto FOSAMAX był podobnie skuteczny niezależnie od wieku (poniżej 65 lat w porównaniu z wiekami powyżej lub równymi 65), rasy (kaukaska w porównaniu z innymi rasami), płci, choroby podstawowej, wyjściowego BMD, wyjściowego obrotu kostnego i stosowania z różnorodność popularnych leków.
Histologia kości była prawidłowa u 49 pacjentów poddanych biopsji pod koniec jednego roku, którzy otrzymywali FOSAMAX w dawkach do 10 mg/dobę.
Spośród pierwotnych 560 pacjentów w tych badaniach, 208 pacjentów, którzy nadal otrzymywali prednizon w dawce co najmniej 7,5 mg/dobę lub odpowiednik, kontynuowało roczne badanie z podwójnie ślepą próbą. Po dwóch latach leczenia BMD kręgosłupa wzrosło o 3,7% i 5,0% w porównaniu z placebo odpowiednio w przypadku FOSAMAX 5 i 10 mg/dobę. Znaczący wzrost BMD (w porównaniu z placebo) zaobserwowano również w obrębie szyjki kości udowej, krętarza i całego ciała.
Po roku u 2,3% pacjentów leczonych preparatem FOSAMAX 5 lub 10 mg/dobę (łącznie) w porównaniu z 3,7% pacjentów otrzymujących placebo doszło do nowego złamania kręgu (nieistotne). Jednak w populacji badanej przez dwa lata leczenie preparatem FOSAMAX (grupy dawek zbiorczych: 5 lub 10 mg przez dwa lata lub 2,5 mg przez rok, a następnie 10 mg przez rok) znacząco zmniejszyło częstość występowania nowych złamań kręgów. (FOSAMAX 0,7% w porównaniu z placebo 6,8%).
Leczenie choroby Pageta kości
Skuteczność preparatu FOSAMAX 40 mg raz na dobę przez sześć miesięcy wykazano w dwóch badaniach klinicznych z podwójnie ślepą próbą u pacjentów płci męskiej i żeńskiej z chorobą Pageta o nasileniu umiarkowanym do ciężkiego (fosfataza alkaliczna co najmniej dwukrotnie większa od górnej granicy normy): placebo kontrolowane, międzynarodowe badanie oraz badanie porównawcze w USA z użyciem etidronianu disodu 400 mg/dobę. Rycina 6 przedstawia średnie procentowe zmiany w stosunku do wartości wyjściowych w fosfatazie alkalicznej w surowicy przez okres do sześciu miesięcy randomizowanego leczenia.
Rysunek 6: Badania nad wpływem choroby Pageta na kości na fosfatazę alkaliczną FOSAMAX 40 mg/dobę w porównaniu z placebo lub etydronianem 400 mg/dobę
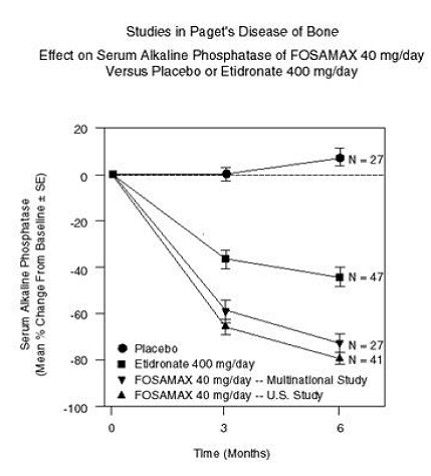
Po sześciu miesiącach supresja fosfatazy alkalicznej u pacjentów leczonych FOSAMAX była znacznie większa niż uzyskana z etidronianem i kontrastowała z całkowitym brakiem odpowiedzi u pacjentów otrzymujących placebo. Odpowiedź (definiowana jako normalizacja poziomu fosfatazy alkalicznej w surowicy lub spadek od wartości wyjściowej większy lub równy 60%) wystąpiła u około 85% pacjentów leczonych preparatem FOSAMAX w połączonych badaniach w porównaniu z 30% w grupie etidronianu i 0% w grupie placebo Grupa. FOSAMAX 70 mg był podobnie skuteczny bez względu na wiek, płeć, rasę, wcześniejsze stosowanie innych bisfosfonianów lub wyjściową fosfatazę alkaliczną w badanym zakresie (co najmniej dwukrotność górnej granicy normy).
Histologię kości oceniano u 33 pacjentów z chorobą Pageta leczonych FOSAMAX 40 mg/dzień przez 6 miesięcy. Jak u pacjentów leczonych z powodu osteoporozy [patrz Studia kliniczne ], FOSAMAX nie zaburzał mineralizacji i zaobserwowano oczekiwany spadek tempa obrotu kostnego. Podczas leczenia preparatem FOSAMAX powstała normalna kość blaszkowata, nawet tam, gdzie wcześniej istniejąca kość była spleciona i zdezorganizowana. Ogólnie rzecz biorąc, dane histologiczne kości potwierdzają wniosek, że kość wytworzona podczas leczenia FOSAMAX 35 mg jest normalnej jakości.
INFORMACJA O PACJENCIE
FOSAMAX® (FOSS-ah-max) (alendronian sodu) Tabletki
Przeczytaj Przewodnik po lekach dołączony do FOSAMAX 70 mg przed rozpoczęciem jego przyjmowania i za każdym razem, gdy otrzymujesz uzupełnienie. Mogą pojawić się nowe informacje. Niniejszy Przewodnik po lekach nie zastępuje rozmowy z lekarzem na temat stanu zdrowia lub leczenia. Porozmawiaj z lekarzem, jeśli masz jakiekolwiek pytania dotyczące leku FOSAMAX.
Jakie są najważniejsze informacje, które powinienem wiedzieć o FOSAMAX 70mg?
FOSAMAX 70mg może powodować poważne skutki uboczne, w tym:
1. Problemy z przełykiem.
U niektórych osób przyjmujących FOSAMAX 35 mg mogą wystąpić problemy w przełyku (przewód łączący jamę ustną i żołądek).
Problemy te obejmują podrażnienie, stan zapalny lub wrzody przełyku, które czasami mogą krwawić.
- Ważne jest, aby przyjmować FOSAMAX 70 mg dokładnie zgodnie z zaleceniami, aby zmniejszyć ryzyko wystąpienia problemów z przełykiem. (Patrz rozdział „Jak powinienem przyjmować FOSAMAX?”)
- Należy przerwać przyjmowanie leku FOSAMAX i natychmiast skontaktować się z lekarzem w przypadku wystąpienia bólu w klatce piersiowej, pojawienia się nowej lub nasilenia zgagi lub problemów lub bólu podczas przełykania.
2. Niski poziom wapnia we krwi (hipokalcemia).
FOSAMAX może obniżać stężenie wapnia we krwi. Jeśli masz niski poziom wapnia we krwi przed rozpoczęciem stosowania leku FOSAMAX, może się to pogorszyć podczas leczenia. Niskie stężenie wapnia we krwi należy leczyć przed przyjęciem leku FOSAMAX. Większość osób z niskim poziomem wapnia we krwi nie ma objawów, ale niektóre osoby mogą mieć objawy. Zadzwoń do lekarza natychmiast, jeśli masz objawy niskiego stężenia wapnia we krwi, takie jak:
- Skurcze, drgania lub skurcze mięśni
- Drętwienie lub mrowienie w palcach rąk i nóg lub wokół ust
Lekarz może przepisać wapń i witaminę D, aby zapobiec niskiemu poziomowi wapnia we krwi podczas przyjmowania leku FOSAMAX. Przyjmuj wapń i witaminę D zgodnie z zaleceniami lekarza.
3. Ból kości, stawów lub mięśni.
Niektóre osoby przyjmujące FOSAMAX rozwijają silny ból kości, stawów lub mięśni.
4. Ciężkie problemy z kością szczęki (martwica kości).
Podczas przyjmowania leku FOSAMAX mogą wystąpić poważne problemy z kością szczęki. Lekarz powinien zbadać jamę ustną przed rozpoczęciem stosowania leku FOSAMAX. Lekarz może zalecić wizytę u dentysty przed rozpoczęciem stosowania leku FOSAMAX. Podczas leczenia lekiem FOSAMAX ważne jest, aby dbać o dobrą pielęgnację jamy ustnej.
5. Nietypowe złamania kości udowej.
U niektórych osób doszło do nietypowych złamań kości udowej. Objawy złamania mogą obejmować nowy lub nietypowy ból w biodrze, pachwinie lub udzie.
Zadzwoń do lekarza natychmiast, jeśli wystąpi którykolwiek z tych działań niepożądanych.
Co to jest FOSAMAX 70mg?
- FOSAMAX 70mg to lek na receptę stosowany do:
- Leczenie lub zapobieganie osteoporozie u kobiet po menopauzie. Pomaga zmniejszyć ryzyko złamania (złamania) biodra lub kręgosłupa.
- Zwiększenie masy kostnej u mężczyzn z osteoporozą.
- Leczenie osteoporozy u mężczyzn lub kobiet przyjmujących kortykosteroidy.
Leczyć niektórych mężczyzn i kobiety z chorobą Pageta kości.
Nie wiadomo, jak długo FOSAMAX 70mg działa w leczeniu i profilaktyce osteoporozy. Należy regularnie odwiedzać lekarza, aby ustalić, czy FOSAMAX 70 mg jest nadal odpowiedni dla Ciebie.
FOSAMAX nie jest przeznaczony do stosowania u dzieci.
Kto nie powinien brać FOSAMAX 70mg?
Nie należy przyjmować leku FOSAMAX, jeśli:
- Masz pewne problemy z przełykiem, rurką łączącą usta z żołądkiem
- Nie może stać ani siedzieć prosto przez co najmniej 30 minut
- Masz niski poziom wapnia we krwi
- Jesteś uczulony na FOSAMAX 70mg lub którykolwiek z jego składników. Lista składników znajduje się na końcu tej ulotki.
O czym powinienem powiedzieć lekarzowi przed przyjęciem leku FOSAMAX 35mg?
Przed rozpoczęciem stosowania leku FOSAMAX należy porozmawiać z lekarzem, jeśli:
- Masz problemy z połykaniem
- Masz problemy z żołądkiem lub trawieniem
- Masz niski poziom wapnia we krwi
- Zaplanuj operację dentystyczną lub usunięcie zębów
- Masz problemy z nerkami
- Powiedziano mi, że masz problemy z wchłanianiem minerałów w żołądku lub jelitach (zespół złego wchłaniania)
- Jesteś w ciąży, próbujesz zajść w ciążę lub podejrzewasz, że jesteś w ciąży. W przypadku zajścia w ciążę podczas przyjmowania leku FOSAMAX należy przerwać jego stosowanie i skontaktować się z lekarzem. Nie wiadomo, czy FOSAMAX może zaszkodzić nienarodzonemu dziecku.
- Karmią piersią lub planują karmić piersią. Nie wiadomo, czy FOSAMAX przenika do mleka i może zaszkodzić dziecku.
Szczególnie powiedz swojemu lekarzowi, jeśli przyjmujesz:
- leki zobojętniające kwasy
- aspiryna
- Niesteroidowe leki przeciwzapalne (NLPZ)
Poinformuj lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe. Niektóre leki mogą wpływać na działanie leku FOSAMAX 70mg.
Poznaj leki, które przyjmujesz. Zachowaj ich listę i pokazuj ją swojemu lekarzowi i farmaceucie za każdym razem, gdy otrzymasz nowy lek.
Jak powinienem przyjmować FOSAMAX 35mg?
- Lek FOSAMAX 35 mg należy przyjmować zgodnie z zaleceniami lekarza.
- FOSAMAX działa tylko wtedy, gdy jest przyjmowany na pusty żołądek.
- Lek FOSAMAX 35 mg należy przyjmować rano po wstaniu z łóżka i przed przyjęciem pierwszego posiłku, napoju lub innego leku.
- Weź FOSAMAX, gdy siedzisz lub stoisz.
- Nie żuć ani nie ssać tabletki FOSAMAX.
- Tabletkę FOSAMAX należy połykać wyłącznie popijając pełną szklanką (6-8 uncji) czystej wody.
- Nie rób weź FOSAMAX z wodą mineralną, kawą, herbatą, napojem gazowanym lub sokiem.
- W przypadku stosowania leku Alendronate Daily:
- Należy przyjmować 1 tabletkę alendronianu raz dziennie, codziennie rano po wstaniu z łóżka i przed przyjęciem pierwszego posiłku, napoju lub innego leku.
- Jeśli przyjmujesz FOSAMAX raz w tygodniu:
- Wybierz dzień tygodnia, który najlepiej pasuje do Twojego harmonogramu.
- Przyjmować 1 dawkę leku FOSAMAX co tydzień w wybrany dzień po wstaniu z łóżka i przed przyjęciem pierwszego posiłku, napoju lub innego leku.
- W przypadku stosowania leku Alendronate Daily:
Po połknięciu tabletki FOSAMAX 35 mg odczekać co najmniej 30 minut:
- Zanim się położysz. Możesz siedzieć, stać lub chodzić i wykonywać normalne czynności, takie jak czytanie.
- Przed przyjęciem pierwszego posiłku lub napoju, z wyjątkiem zwykłej wody.
- Przed przyjęciem innych leków, w tym leków zobojętniających, wapnia i innych suplementów i witamin.
Nie należy kłaść się przez co najmniej 30 minut po przyjęciu leku FOSAMAX i po zjedzeniu pierwszego posiłku w ciągu dnia.
W przypadku pominięcia dawki FOSAMAX 70mg nie należy przyjmować jej później w ciągu dnia. Przyjmij pominiętą dawkę następnego ranka po przypomnieniu sobie, a następnie wróć do normalnego harmonogramu. Nie należy przyjmować 2 dawek tego samego dnia.
W przypadku zażycia zbyt dużej dawki leku FOSAMAX 70 mg należy skontaktować się z lekarzem. Nie próbuj wymiotować. Nie kładź się.
Jakie są możliwe skutki uboczne FOSAMAX 70mg?
FOSAMAX może powodować poważne skutki uboczne.
- Zobacz „Jakie są najważniejsze informacje, które powinienem wiedzieć o FOSAMAX?”
Najczęstsze działania niepożądane FOSAMAX 70mg to:
- Ból brzucha (brzucha)
- Zgaga
- Zaparcie
- Biegunka
- Rozstrój żołądka
- Ból w kościach, stawach lub mięśniach
- Mdłości
Mogą wystąpić reakcje alergiczne, takie jak pokrzywka lub obrzęk twarzy, warg, języka lub gardła.
Zgłaszano pogorszenie astmy.
Należy poinformować lekarza, jeśli wystąpią jakiekolwiek objawy niepożądane, które Cię niepokoją lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne FOSAMAX. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać FOSAMAX?
- Przechowywać FOSAMAX 35mg w temperaturze pokojowej, 59°F do 86°F (15°C do 30°C).
- Przechowywać FOSAMAX w szczelnie zamkniętym pojemniku.
Przechowywać FOSAMAX i wszystkie leki w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu FOSAMAX.
Leki są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Nie należy stosować leku FOSAMAX 35 mg na stan, na który nie został przepisany. Nie należy podawać leku FOSAMAX 35mg innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić.
Ten przewodnik po lekach podsumowuje najważniejsze informacje o FOSAMAX. Jeśli chcesz uzyskać więcej informacji, porozmawiaj ze swoim lekarzem. Możesz poprosić swojego lekarza lub farmaceutę o informacje o FOSAMAX, które są przeznaczone dla pracowników służby zdrowia. Aby uzyskać więcej informacji, przejdź do: www.FOSAMAX.com lub zadzwoń pod numer 1-800-622-4477 (bezpłatny).
Jakie są składniki FOSAMAX?
Składnik aktywny: sól sodowa alendronianu
Składniki nieaktywne: celuloza mikrokrystaliczna, laktoza bezwodna, kroskarmeloza sodowa, stearynian magnezu.
Ten przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków.
