Leczenie raka: Nolvadex 10mg, 20mg Tamoxifen Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Nolvadex i jak się go stosuje?
Nolvadex 10mg to lek na receptę stosowany w leczeniu objawów raka piersi. Nolvadex może być stosowany samodzielnie lub z innymi lekami.
Nolvadex 20mg należy do klasy leków zwanych antyneoplastycznymi, antagonistami receptora estrogenowego.
Nie wiadomo, czy Nolvadex 20mg jest bezpieczny i skuteczny u dzieci.
Jakie są możliwe skutki uboczne Nolvadexu 20mg?
Nolvadex może powodować poważne skutki uboczne, w tym:
- zmiany widzenia,
- ból oka,
- łatwe siniaczenie lub krwawienie,
- zmiany nastroju,
- obrzęk kostek lub stóp oraz
- niezwykłe zmęczenie
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Nolvadexu to:
- uderzenia gorąca,
- płukanie,
- zmiany w okresach menstruacyjnych,
- mdłości,
- kurcze nóg,
- skurcze brzucha,
- ból kości,
- ból w mięśniach,
- kaszel,
- obrzęk,
- zmęczenie,
- przerzedzenie włosów,
- ból głowy,
- depresja i
- utrata zdolności/zainteresowania seksualnego (u mężczyzn)
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Nolvadexu. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
OSTRZEŻENIE
Dla kobiet z rakiem przewodowym in situ (DCIS) i kobiet z wysokim ryzykiem raka piersi: Poważne i zagrażające życiu zdarzenia związane ze stosowaniem preparatu NOLVADEX (cytrynian tamoksyfenu) w warunkach redukcji ryzyka (kobiety z grupy wysokiego ryzyka zachorowania na raka i kobiety z DCIS) obejmują nowotwory macicy, udar i zatorowość płucną. Częstość występowania tych zdarzeń oszacowano na podstawie badania NSABP P-1 (patrz FARMAKOLOGIA KLINICZNA-Badania kliniczne - Zmniejszenie zachorowalności na raka piersi u kobiet wysokiego ryzyka ). Nowotwory złośliwe macicy składają się zarówno z gruczolakoraka endometrium (zapadalność na 1000 kobietolat wynosi 2,20 dla NOLVADEX (cytrynian tamoksyfenu) vs 0,71 dla placebo) oraz mięsaka macicy (zapadalność na 1000 kobietolat wynosi 0,17 dla NOLVADEX (cytrynian tamoksyfenu) vs. placebo)*. W przypadku udaru częstość występowania na 1000 kobietolat wynosiła 1,43 dla NOLVADEX (cytrynian tamoksyfenu) w porównaniu z 1,00 dla placebo**. W przypadku zatorowości płucnej częstość występowania na 1000 kobieto-lat wynosiła 0,75 dla NOLVADEX (cytrynian tamoksyfenu) w porównaniu z 0,25 dla placebo**.
Niektóre udary, zatory płucne i nowotwory macicy były śmiertelne.
Pracownicy służby zdrowia powinni omówić potencjalne korzyści w porównaniu z potencjalnym ryzykiem tych poważnych zdarzeń z kobietami z grupy wysokiego ryzyka zachorowania na raka piersi i kobietami z DCIS, biorąc pod uwagę NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia ryzyka zachorowania na raka piersi.
Korzyści płynące ze stosowania NOLVADEX (cytrynian tamoksyfenu) przewyższają ryzyko u kobiet, u których zdiagnozowano już raka piersi.
BIBLIOGRAFIA
*Zaktualizowane dane z obserwacji długoterminowej (mediana czasu obserwacji wynosi 6,9 roku) z badania NSABP P-1. Widzieć OSTRZEŻENIA: Wpływ na raka macicy i endometrium i mięsaka macicy .
**Patrz Tabela 3 poniżej FARMAKOLOGIA KLINICZNA-Badania kliniczne .
OPIS
Tabletki NOLVADEX® (cytrynian tamoksyfenu), niesteroidowy antyestrogen, są przeznaczone do podawania doustnego. Tabletki NOLVADEX (tamoksyfen cytrynian) są dostępne jako:
Tabletki 10 mg
Każda tabletka zawiera 15,2 mg cytrynianu tamoksyfenu, co odpowiada 10 mg tamoksyfenu.
Tabletki 20 mg
Każda tabletka zawiera 30,4 mg cytrynianu tamoksyfenu, co odpowiada 20 mg tamoksyfenu.
Składniki Nieaktywne: wapń karboksymetylocelulozy, stearynian magnezu, mannitol i skrobia.
Chemicznie NOLVADEX (cytrynian tamoksyfenu) jest izomerem trans pochodnej trifenyloetylenu. Nazwa chemiczna to (Z)2-[4-(1,2-difenylo-1-butenylo)fenoksy]-N,N-dimetyloetanoamina 2hydroksy-1,2,3-propanotrikarboksylan (1:1). Wzory strukturalne i empiryczne to:
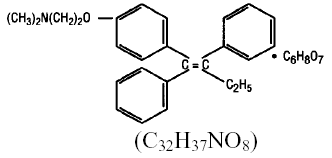
Cytrynian tamoksyfenu ma masę cząsteczkową 563,62, pKa' wynosi 8,85, rozpuszczalność równowagowa w wodzie w 37°C wynosi 0,5 mg/ml, aw 0,02 N HCl w 37°C wynosi 0,2 mg/ml.
WSKAZANIA
Rak piersi z przerzutami
NOLVADEX (cytrynian tamoksyfenu) jest skuteczny w leczeniu przerzutowego raka piersi u kobiet i mężczyzn. U kobiet przed menopauzą z przerzutowym rakiem piersi NOLVADEX (cytrynian tamoksyfenu) jest alternatywą dla wycięcia jajników lub napromieniania jajników. Dostępne dowody wskazują, że pacjenci, u których guzy wykazują obecność receptorów estrogenowych, mają większe szanse na skorzystanie z terapii NOLVADEX (cytrynian tamoksyfenu).
Leczenie uzupełniające raka piersi
NOLVADEX (cytrynian tamoksyfenu) jest wskazany w leczeniu raka piersi z przerzutami do węzłów chłonnych u kobiet po całkowitej mastektomii lub mastektomii odcinkowej, rozwarstwieniu pach i napromienianiu piersi. W niektórych badaniach preparatu NOLVADEX (cytrynian tamoksyfenu) z adiuwantem, większość dotychczasowych korzyści odnosiła podgrupa z co najmniej czterema zajętymi węzłami pachowymi.
NOLVADEX (cytrynian tamoksyfenu) jest wskazany w leczeniu raka piersi bez przerzutów do węzłów chłonnych pachowych u kobiet po całkowitej mastektomii lub mastektomii odcinkowej, rozwarstwieniu pach i napromienianiu piersi.
Wartości receptorów estrogenowych i progesteronowych mogą pomóc w przewidywaniu, czy adiuwantowa terapia NOLVADEX (cytrynian tamoksyfenu) może być korzystna.
NOLVADEX (tamoksyfen cytrynian) zmniejsza występowanie kontralateralnego raka piersi u pacjentek otrzymujących uzupełniającą terapię NOLVADEX (tamoksyfen cytrynian) z powodu raka piersi.
Rak przewodowy in situ (DCIS)
kobiet z DCIS po operacji piersi i radioterapii, NOLVADEX (cytrynian tamoksyfenu) jest wskazany w celu zmniejszenia ryzyka inwazyjnego raka piersi (patrz OSTRZEŻENIE W PUDEŁKU na początku etykiety). Decyzja o leczeniu NOLVADEXEM (tamoksyfen cytrynian) w celu zmniejszenia zachorowalności na raka piersi powinna być oparta na indywidualnej ocenie korzyści i ryzyka leczenia NOLVADEXEM (tamoksyfen cytrynian).
Aktualne dane z badań klinicznych potwierdzają pięcioletnią terapię uzupełniającą NOLVADEX (cytrynian tamoksyfenu) u pacjentek z rakiem piersi.
Zmniejszenie zachorowalności na raka piersi u kobiet wysokiego ryzyka
NOLVADEX (cytrynian tamoksyfenu) jest wskazany w celu zmniejszenia zachorowalności na raka piersi u kobiet z grupy wysokiego ryzyka raka piersi. Efekt ten wykazano w badaniu planowanym na 5 lat z medianą okresu obserwacji 4,2 roku. Dwadzieścia pięć procent uczestników otrzymywało lek przez 5 lat. Skutki długoterminowe nie są znane. W tym badaniu nie stwierdzono wpływu tamoksyfenu na całkowitą śmiertelność związaną z rakiem piersi (patrz OSTRZEŻENIE W PUDEŁKU na początku etykiety).
NOLVADEX (cytrynian tamoksyfenu) jest wskazany tylko dla kobiet wysokiego ryzyka. „Wysokie ryzyko” definiuje się jako kobiety w wieku co najmniej 35 lat z 5-letnim przewidywanym ryzykiem raka piersi ≥ 1,67%, obliczonym za pomocą modelu Gail.
Przykładami kombinacji czynników przewidujących 5-letnie ryzyko ≥ 1,67% są:
Wiek 35 lat lub starszy i dowolna z następujących kombinacji czynników:
- Jeden krewny pierwszego stopnia z historią raka piersi, 2 lub więcej łagodnych biopsji oraz historia biopsji piersi wykazującej atypowy rozrost; lub
- Co najmniej 2 krewnych pierwszego stopnia z historią raka piersi i osobistą historią co najmniej jednej biopsji piersi; lub
- LCIS
Wiek co najmniej 40 lat i dowolna z następujących kombinacji czynników:
- Jeden krewny pierwszego stopnia z historią raka piersi, 2 lub więcej łagodnych biopsji, wiek przy pierwszym urodzeniu co najmniej 25 lat i wiek pierwszej miesiączki 11 lat lub młodszy; lub
- Co najmniej 2 krewnych pierwszego stopnia z historią raka piersi w wieku przy pierwszym urodzeniu 19 lat lub młodszym; lub
- Jeden krewny pierwszego stopnia z historią raka piersi i osobistą historią biopsji piersi wykazującej atypowy rozrost.
Wiek co najmniej 45 lat i dowolna z następujących kombinacji czynników:
- Przynajmniej 2 krewnych pierwszego stopnia z historią raka piersi w wieku przy pierwszym urodzeniu 24 lub młodszym; lub
- Jedna krewna pierwszego stopnia z rakiem piersi w wywiadzie z osobistą historią łagodnej biopsji piersi, wiek w momencie pierwszej pierwszej miesiączki lub mniej i wiek przy pierwszym urodzeniu 20 lub więcej.
Wiek co najmniej 50 lat oraz dowolna z następujących kombinacji czynników:
- Co najmniej 2 krewnych pierwszego stopnia z historią raka piersi; lub
- Historia jednej biopsji piersi wykazującej hiperplazję atypową, wiek przy pierwszym urodzeniu 30 lub więcej lat i wiek pierwszej miesiączki 11 lub mniej; lub
- Historia co najmniej dwóch biopsji piersi z atypowym przerostem piersi w wywiadzie i wiekiem przy pierwszym urodzeniu 30 lub więcej.
Wiek co najmniej 55 lat i dowolna z następujących kombinacji czynników:
- Jeden krewny pierwszego stopnia z historią raka piersi z wywiadem łagodnej biopsji piersi, w wieku 11 miesięcy lub młodszym; lub
- Historia co najmniej 2 biopsji piersi z historią atypowego przerostu piersi i wiekiem przy pierwszym urodzeniu na żywo 20 lat lub więcej.
w wieku 60 lat lub starszym oraz:
- Przewidywane 5-letnie ryzyko raka piersi ≥ 1,67%, obliczone za pomocą modelu Gail.
W przypadku kobiet, których czynniki ryzyka nie zostały opisane w powyższych przykładach, model Gail jest niezbędny do oszacowania bezwzględnego ryzyka raka piersi. Pracownicy służby zdrowia mogą uzyskać narzędzie oceny ryzyka modelu Gail, dzwoniąc pod numer 1-800-544-2007.
Nie ma wystarczających danych dotyczących wpływu NOLVADEX (cytrynian tamoksyfenu) na zachorowalność na raka piersi u kobiet z dziedzicznymi mutacjami (BRCA1, BRCA2), aby móc sformułować szczegółowe zalecenia dotyczące skuteczności NOLVADEXU (cytrynian tamoksyfenu) u tych pacjentów.
Po dokonaniu oceny ryzyka zachorowania na raka piersi, decyzja dotycząca leczenia preparatem NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia zachorowalności na raka piersi powinna być oparta na indywidualnej ocenie korzyści i ryzyka leczenia preparatem NOLVADEX (cytrynian tamoksyfenu). W badaniu NSABP P-1 leczenie NOLVADEX (cytrynian tamoksyfenu) obniżyło ryzyko zachorowania na raka piersi w okresie obserwacji badania, ale nie wyeliminowało ryzyka raka piersi (patrz Tabela 3 w FARMAKOLOGIA KLINICZNA ).
DAWKOWANIE I SPOSÓB PODAWANIA
Dla pacjentek z rakiem piersi zalecana dzienna dawka wynosi 20-40 mg. Dawki większe niż 20 mg na dobę należy podawać w dawkach podzielonych (rano i wieczorem).
trzech badaniach dotyczących pojedynczego środka wspomagającego u kobiet, jedną tabletkę 10 mg NOLVADEX (cytrynian tamoksyfenu) podawano dwa (ECOG i NATO) lub trzy (Toronto) razy dziennie przez dwa lata. W badaniu uzupełniającym NSABP B-14 u kobiet z rakiem piersi bez przerzutów do węzłów chłonnych, jedną tabletkę 10 mg NOLVADEX (cytrynian tamoksyfenu) podawano dwa razy dziennie przez co najmniej 5 lat. Wyniki badania B-14 sugerują, że kontynuacja terapii przez ponad pięć lat nie zapewnia dodatkowych korzyści (patrz FARMAKOLOGIA KLINICZNA ). W przeglądzie EBCTCG z 1995 r. zmniejszenie nawrotów i śmiertelności było większe w tych badaniach, w których stosowano tamoksyfen przez około 5 lat, niż w tych, w których stosowano tamoksyfen przez krótszy okres leczenia. Nic nie wskazywało na to, że dawki większe niż 20 mg na dobę były bardziej skuteczne. Aktualne dane z badań klinicznych potwierdzają 5-letnią terapię uzupełniającą NOLVADEX (cytrynian tamoksyfenu) u pacjentek z rakiem piersi.
Rak przewodowy in situ (DCIS)
Zalecana dawka to NOLVADEX (cytrynian tamoksyfenu) 20 mg na dobę przez 5 lat.
Zmniejszenie zachorowalności na raka piersi u kobiet wysokiego ryzyka
Zalecana dawka to NOLVADEX (cytrynian tamoksyfenu) 20 mg na dobę przez 5 lat. Nie ma danych uzasadniających stosowanie leku NOLVADEX (cytrynian tamoksyfenu) poza okresem 5 lat (patrz FARMAKOLOGIA KLINICZNA-Badania kliniczne - Zmniejszenie zachorowalności na raka piersi u kobiet wysokiego ryzyka ).
JAK DOSTARCZONE
Tabletki 10 mg zawierające tamoksyfen w postaci cytrynianu w ilości odpowiadającej 10 mg tamoksyfenu (okrągła, dwuwypukła, niepowlekana, biała tabletka z oznaczeniem NOLVADEX (cytrynian tamoksyfenu) 600 wytłoczonym po jednej stronie i kameą wytłoczonym po drugiej stronie) są dostarczane w butelkach po 60 sztuk tabletki. NDC 0310-0600-60.
Tabletki 20 mg zawierające tamoksyfen w postaci cytrynianu w ilości odpowiadającej 20 mg tamoksyfenu (okrągła, dwuwypukła, niepowlekana, biała tabletka z oznaczeniem NOLVADEX (cytrynian tamoksyfenu) 604 wytłoczonym po jednej stronie i kameą wytłoczonym po drugiej stronie) są dostarczane w butelkach po 30 sztuk tabletki. NDC 0310-0604-30.
Przechowywać w kontrolowanej temperaturze pokojowej, 20-25°C (68-77°F) [patrz USP]. Dozować w dobrze zamkniętym pojemniku odpornym na światło.
*Coumadin® jest zarejestrowanym znakiem towarowym firmy Bristol-Myers Squibb Pharmaceuticals. Wszystkie inne znaki towarowe są własnością grupy AstraZeneca, AstraZeneca Pharmaceuticals LP Wilmington, Delaware 19850-5437. Rev 09-27-05. Data aktualizacji FDA: 3/9/2006
SKUTKI UBOCZNE
Działania niepożądane leku NOLVADEX (cytrynian tamoksyfenu) są stosunkowo łagodne i rzadko na tyle ciężkie, że wymagają przerwania leczenia u pacjentek z rakiem piersi.
Dalsze badania kliniczne przyniosły dalsze informacje, które lepiej wskazują na częstość występowania działań niepożądanych po zastosowaniu preparatu NOLVADEX (cytrynian tamoksyfenu) w porównaniu z placebo.
Rak piersi z przerzutami
Wystąpił nasilający się ból kości i guza, a także miejscowe zaostrzenie choroby, które czasami są związane z dobrą reakcją guza. Pacjenci ze zwiększonym bólem kości mogą wymagać dodatkowych środków przeciwbólowych. Pacjenci z chorobami tkanek miękkich mogą mieć nagły wzrost wielkości wcześniej istniejących zmian, czasami związany z wyraźnym rumieniem w obrębie i wokół zmian i/lub rozwojem nowych zmian. Gdy wystąpią, ból kości lub zaostrzenie choroby są widoczne wkrótce po rozpoczęciu stosowania leku NOLVADEX (cytrynian tamoksyfenu) i zwykle szybko ustępują.
U pacjentek leczonych lekiem NOLVADEX (cytrynian tamoksyfenu) z powodu raka piersi z przerzutami, najczęstszym działaniem niepożądanym leku NOLVADEX (cytrynian tamoksyfenu) są uderzenia gorąca.
Inne działania niepożądane, które występują rzadko, to hiperkalcemia, obrzęki obwodowe, niesmak pokarmowy, świąd sromu, depresja, zawroty głowy, uczucie pustki w głowie, ból głowy, przerzedzenie włosów i/lub częściowa utrata włosów oraz suchość pochwy.
Kobiety przed menopauzą
Poniższa tabela podsumowuje częstość występowania działań niepożądanych zgłaszanych z częstością 2% lub większą w badaniach klinicznych (Ingle, Pritchard, Buchanan), w których porównywano terapię NOLVADEX (cytrynian tamoksyfenu) z ablacją jajników u pacjentek przed menopauzą z przerzutowym rakiem piersi.
Męski rak piersi
NOLVADEX (cytrynian tamoksyfenu) jest dobrze tolerowany przez mężczyzn z rakiem piersi. Doniesienia z literatury i opisy przypadków sugerują, że profil bezpieczeństwa NOLVADEX (cytrynian tamoksyfenu) u mężczyzn jest podobny do obserwowanego u kobiet. Utrata libido i impotencja spowodowały przerwanie terapii tamoksyfenem u mężczyzn. Również u mężczyzn oligospermicznych leczonych tamoksyfenem, poziom LH, FSH, testosteronu i estrogenu był podwyższony. Nie zgłoszono żadnych istotnych zmian klinicznych.
Adiuwantowy rak piersi
badaniu NSABP B-14 kobiety z rakiem piersi bez przerzutów do pach zostały losowo przydzielone do grupy otrzymującej przez 5 lat NOLVADEX (cytrynian tamoksyfenu) 20 mg/dobę lub placebo po pierwotnym zabiegu chirurgicznym. Zgłoszone działania niepożądane zestawiono poniżej (średni okres obserwacji około 6,8 lat) wykazując, że zdarzenia niepożądane występują częściej w przypadku stosowania leku NOLVADEX (cytrynian tamoksyfenu) niż w przypadku placebo. Częstość występowania uderzeń gorąca (64% vs 48%), upławów (30% vs 15%) i nieregularnych miesiączek (25% vs 19%) była wyższa w grupie NOLVADEX (cytrynian tamoksyfenu) w porównaniu z placebo. Wszystkie inne działania niepożądane wystąpiły z podobną częstością w 2 leczonych grupach, z wyjątkiem zdarzeń zakrzepowych; większą częstość występowania obserwowano u pacjentów leczonych preparatem NOLVADEX (cytrynian tamoksyfenu) (w ciągu 5 lat, 1,7% w porównaniu do 0,4%). Dwóch pacjentów leczonych NOLVADEX (cytrynian tamoksyfenu), u których wystąpiły zdarzenia zakrzepowe, zmarło.
badaniu uzupełniającym raka piersi Eastern Cooperative Oncology Group (ECOG) kobietom po mastektomii przez 2 lata podawano NOLVADEX (cytrynian tamoksyfenu) lub placebo. W porównaniu z placebo, NOLVADEX (cytrynian tamoksyfenu) wykazał znacznie większą częstość występowania uderzeń gorąca (19% vs. 8% dla placebo). Częstość występowania wszystkich innych działań niepożądanych była podobna w 2 grupach terapeutycznych, z wyjątkiem małopłytkowości, w której częstość występowania NOLVADEX (cytrynian tamoksyfenu) wynosiła 10% w porównaniu z 3% w przypadku placebo, co stanowi graniczną istotność statystyczną.
innych badaniach adjuwantowych, Toronto i NOLVADEX (cytrynian tamoksyfenu) Adjuvant Trial Organization (NATO), kobiety otrzymywały NOLVADEX (cytrynian tamoksyfenu) lub nie otrzymywały żadnej terapii. W badaniu Toronto uderzenia gorąca zaobserwowano u 29% pacjentów otrzymujących NOLVADEX (cytrynian tamoksyfenu) w porównaniu z 1% w grupie nieleczonej. W badaniu NATO uderzenia gorąca i krwawienia z pochwy zgłoszono odpowiednio u 2,8% i 2,0% kobiet w grupie NOLVADEX (cytrynian tamoksyfenu) w porównaniu z 0,2% w przypadku każdej z nich w grupie nieleczonej.
Anastrozole Adjuvant Trial - Badanie Anastrozole w porównaniu z NOLVADEX (cytrynian tamoksyfenu) w leczeniu adjuwantowym wczesnego raka piersi (Widzieć FARMAKOLOGIA KLINICZNA - Studia kliniczne).
Przy medianie obserwacji wynoszącej 33 miesiące, skojarzenie anastrozolu i NOLVADEX (cytrynian tamoksyfenu) nie wykazało żadnej korzyści pod względem skuteczności w porównaniu z terapią NOLVADEX (cytrynian tamoksyfenu) podawanym w monoterapii u wszystkich pacjentów, jak również w subpopulacji z dodatnim receptorem hormonalnym. To ramię leczenia zostało przerwane z badania. Mediana czasu trwania leczenia uzupełniającego w celu oceny bezpieczeństwa wyniosła 59,8 miesiąca i 59,6 miesiąca odpowiednio dla pacjentów otrzymujących anastrozol 1 mg i NOLVADEX (cytrynian tamoksyfenu) 20 mg.
W poniższej tabeli przedstawiono działania niepożądane występujące z częstością co najmniej 5% w każdej z leczonych grup podczas leczenia lub w ciągu 14 dni od zakończenia leczenia.
Zdarzenia niepożądane występujące z częstością co najmniej 5% w każdej grupie leczenia podczas leczenia lub w ciągu 14 dni od zakończenia leczenia
Pewne zdarzenia niepożądane i kombinacje zdarzeń niepożądanych zostały określone prospektywnie do analizy, w oparciu o znane właściwości farmakologiczne i profile skutków ubocznych tych dwóch leków (patrz poniższa tabela).
Liczba (%) pacjentów z wcześniej określonym zdarzeniem niepożądanym w badaniu Anastrozol Adiuwant1
Pacjenci otrzymujący anastrozol mieli nasilenie chorób stawów (w tym zapalenia stawów, artrozy i bólu stawów) w porównaniu z pacjentami otrzymującymi NOLVADEX (cytrynian tamoksyfenu). Pacjenci otrzymujący anastrozol mieli zwiększoną częstość wszystkich złamań (szczególnie złamań kręgosłupa, biodra i nadgarstka) [315 (10%)] w porównaniu z pacjentami otrzymującymi NOLVADEX (cytrynian tamoksyfenu) [209 (7%)]. U pacjentek otrzymujących anastrozol zmniejszyło się występowanie uderzeń gorąca, krwawień z pochwy, upławów, raka endometrium, żylnych epizodów zakrzepowo-zatorowych i niedokrwiennych epizodów naczyniowo-mózgowych w porównaniu z pacjentami otrzymującymi NOLVADEX (cytrynian tamoksyfenu).
Pacjenci otrzymujący NOLVADEX (cytrynian tamoksyfenu) mieli zmniejszenie hipercholesterolemii (108 [3,5%)] w porównaniu do pacjentów otrzymujących anastrozol (278 [9%]). Dławicę piersiową zgłoszono u 71 [2,3%] pacjentów w ramieniu anastrozolu i 51 [1,6%] pacjentów w ramieniu NOLVADEX (cytrynian tamoksyfenu); Zawał mięśnia sercowego zgłoszono u 37 [1,2%] pacjentów w ramieniu anastrozol i u 34 [1,1%] pacjentów w ramieniu NOLVADEX (tamoksyfen cytrynian).
Wyniki badania uzupełniającego kości po 12 i 24 miesiącach wykazały, że u pacjentów otrzymujących anastrozol wystąpiło średnie zmniejszenie zarówno w odcinku lędźwiowym kręgosłupa, jak i całkowitej gęstości mineralnej kości biodrowej (BMD) w porównaniu z wartością wyjściową. Pacjenci otrzymujący NOLVADEX (cytrynian tamoksyfenu) mieli średni wzrost zarówno odcinka lędźwiowego kręgosłupa, jak i całkowitego BMD biodra w porównaniu z wartościami wyjściowymi.
Rak przewodowy in situ (DCIS)
Rodzaj i częstość działań niepożądanych w badaniu NSABP B-24 były zgodne z tymi obserwowanymi w innych badaniach z adiuwantami przeprowadzonych z preparatem NOLVADEX (cytrynian tamoksyfenu).
Zmniejszenie zachorowalności na raka piersi u kobiet wysokiego ryzyka
badaniu NSABP P-1 odnotowano wzrost pięciu poważnych działań niepożądanych w grupie NOLVADEX (cytrynian tamoksyfenu): rak endometrium (33 przypadki w grupie NOLVADEX (cytrynian tamoksyfenu) w porównaniu do 14 w grupie placebo); zatorowość płucna (18 przypadków w grupie NOLVADEX (cytrynian tamoksyfenu) vs. 6 w grupie placebo); zakrzepica żył głębokich (30 przypadków w grupie NOLVADEX (cytrynian tamoksyfenu) vs. 19 w grupie placebo); udar (34 przypadki w grupie NOLVADEX (cytrynian tamoksyfenu) vs. 24 w grupie placebo); powstawanie zaćmy (540 przypadków w grupie NOLVADEX (tamoksyfen cytrynian) vs. 483 w grupie placebo) i operacja zaćmy (101 przypadków w grupie NOLVADEX (tamoksyfen cytrynian) vs. 63 w grupie placebo) (patrz OSTRZEŻENIA oraz Tabela 3 w calach FARMAKOLOGIA KLINICZNA ).
W poniższej tabeli przedstawiono zdarzenia niepożądane obserwowane w badaniu NSABP P-1 według ramienia leczenia. Przedstawiono tylko zdarzenia niepożądane częstsze w przypadku NOLVADEX (cytrynian tamoksyfenu) niż placebo.
badaniu NSABP P-1, odpowiednio 15,0% i 9,7% uczestników otrzymujących NOLVADEX (cytrynian tamoksyfenu) i placebo wycofało się z badania z powodów medycznych. Poniżej przedstawiono medyczne powody rezygnacji z terapii NOLVADEX (cytrynian tamoksyfenu) i placebo, odpowiednio: uderzenia gorąca (3,1% vs 1,5%) i wydzielina z pochwy (0,5% vs 0,1%).
W badaniu NSABP P-1 8,7% i 9,6% uczestników otrzymujących NOLVADEX (cytrynian tamoksyfenu) i placebo, odpowiednio, wycofało się z powodów niemedycznych.
badaniu NSABP P-1 uderzenia gorąca o dowolnym nasileniu wystąpiły u 68% kobiet otrzymujących placebo i u 80% kobiet otrzymujących NOLVADEX (cytrynian tamoksyfenu). Ciężkie uderzenia gorąca wystąpiły u 28% kobiet przyjmujących placebo i 45% kobiet przyjmujących NOLVADEX (cytrynian tamoksyfenu). Wydzielina z pochwy wystąpiła odpowiednio u 35% i 55% kobiet otrzymujących placebo i NOLVADEX (cytrynian tamoksyfenu); i był ciężki odpowiednio w 4,5% i 12,3%. Nie było różnicy w częstości występowania krwawień z pochwy między ramionami leczenia.
Pacjenci pediatryczni – zespół McCune-Albrighta
Średnia objętość macicy wzrosła po 6 miesiącach leczenia i podwoiła się pod koniec rocznego badania. Związek przyczynowy nie został ustalony; jednak ze względu na wzrost częstości występowania gruczolakoraka endometrium i mięsaka macicy u dorosłych leczonych produktem NOLVADEX (patrz OSTRZEŻENIE W PUDEŁKU ), zalecane jest ciągłe monitorowanie pacjentów McCune-Albright leczonych preparatem NOLVADEX (cytrynian tamoksyfenu) pod kątem długotrwałych skutków. Bezpieczeństwo i skuteczność preparatu NOLVADEX (cytrynian tamoksyfenu) u dziewcząt w wieku od 2 do 10 lat z zespołem McCune-Albrighta i przedwczesnym dojrzewaniem nie były badane po upływie jednego roku leczenia. Nie ustalono długoterminowych skutków terapii NOLVADEX (cytrynian tamoksyfenu) u dziewcząt.
Doświadczenie postmarketingowe
Rzadziej zgłaszanymi działaniami niepożądanymi są krwawienia z pochwy, upławy, nieregularne miesiączki, wysypka skórna i bóle głowy. Zwykle nie były one na tyle nasilone, aby wymagały zmniejszenia dawki lub przerwania leczenia. Podczas leczenia preparatem NOLVADEX (cytrynian tamoksyfenu) zgłaszano bardzo rzadkie przypadki rumienia wielopostaciowego, zespołu Stevensa-Johnsona, pemfigoidu pęcherzowego, śródmiąższowego zapalenia płuc i rzadkich przypadków reakcji nadwrażliwości, w tym obrzęku naczynioruchowego. W niektórych przypadkach czas do zachorowania wynosił ponad rok. Rzadko zwiększenie stężenia triglicerydów w surowicy, w niektórych przypadkach z zapaleniem trzustki, może być związane ze stosowaniem NOLVADEX (cytrynian tamoksyfenu) (patrz ŚRODKI OSTROŻNOŚCI – Interakcje leków/testów laboratoryjnych Sekcja).
INTERAKCJE Z LEKAMI
Gdy NOLVADEX (cytrynian tamoksyfenu) jest stosowany w skojarzeniu z antykoagulantami typu kumaryny, może wystąpić znaczne nasilenie działania przeciwzakrzepowego. Jeśli istnieje takie jednoczesne podawanie, zaleca się dokładne monitorowanie czasu protrombinowego pacjenta.
W badaniu NSABP P-1 kobiety, które z jakiegokolwiek powodu wymagały antykoagulantów typu kumaryny, nie kwalifikowały się do udziału w badaniu (zob. PRZECIWWSKAZANIA ).
Istnieje zwiększone ryzyko wystąpienia zdarzeń zakrzepowo-zatorowych, gdy leki cytotoksyczne są stosowane w połączeniu z NOLVADEX (cytrynian tamoksyfenu).
Tamoksyfen zmniejszał stężenie letrozolu w osoczu o 37%. Wpływ tamoksyfenu na metabolizm i wydalanie innych leków przeciwnowotworowych, takich jak cyklofosfamid i inne leki wymagające aktywacji oksydaz o mieszanej funkcji, nie jest znany. Wykazano, że stężenia tamoksyfenu i N-demetylotamoksyfenu w osoczu zmniejszają się podczas jednoczesnego podawania z ryfampiną lub aminoglutetymidem. Uważa się, że indukcja metabolizmu, w którym pośredniczy CYP3A4, jest mechanizmem, za pomocą którego dochodzi do tych redukcji; inne czynniki indukujące CYP3A4 nie były badane w celu potwierdzenia tego efektu.
Jeden pacjent otrzymujący NOLVADEX (cytrynian tamoksyfenu) z fenobarbitalem wykazywał w stanie stacjonarnym stężenie tamoksyfenu niższe niż obserwowane u innych pacjentów (tj. 26 ng/ml w porównaniu ze średnią wartością 122 ng/ml). Jednak kliniczne znaczenie tego odkrycia nie jest znane. Ryfampicyna indukowała metabolizm tamoksyfenu i znacząco obniżała stężenie tamoksyfenu w osoczu u 10 pacjentów. Aminoglutetymid zmniejsza stężenie tamoksyfenu i N-desmetylotamoksyfenu w osoczu. Medroksyprogesteron zmniejsza stężenie N-desmetylu w osoczu, ale nie tamoksyfenu.
Wykazano, że równoczesne leczenie bromokryptyną podnosi poziom tamoksyfenu i N-demetylotamoksyfenu w surowicy.
W oparciu o wyniki kliniczne i farmakokinetyczne z badania adiuwantowego anastrozolu, NOLVADEX (cytrynian tamoksyfenu) nie powinien być podawany z anastrozolem (patrz FARMAKOLOGIA KLINICZNA - Interakcje między lekami Sekcja).
Interakcje lekowe/testy laboratoryjne
Podczas obserwacji po wprowadzeniu produktu do obrotu zgłoszono podwyższenie T4 u kilku pacjentek po menopauzie, co można wyjaśnić wzrostem stężenia globuliny wiążącej tarczycę. Wzrostom tym nie towarzyszyła kliniczna nadczynność tarczycy.
U pacjentek po menopauzie otrzymujących NOLVADEX (cytrynian tamoksyfenu) rzadko obserwowano zmiany wskaźnika kariopiknotycznego w rozmazach z pochwy i różne stopnie wpływu estrogenów na rozmazy Pap.
Po wprowadzeniu do obrotu produktu NOLVADEX (cytrynian tamoksyfenu) zgłaszano rzadkie przypadki hiperlipidemii. Okresowe monitorowanie stężenia triglicerydów i cholesterolu w osoczu może być wskazane u pacjentów z istniejącą wcześniej hiperlipidemią (patrz REAKCJE NIEPOŻĄDANE-Doświadczenie postmarketingowe Sekcja).
OSTRZEŻENIA
Skutki u pacjentów z rakiem piersi z przerzutami
Podobnie jak w przypadku innych addytywnych terapii hormonalnych (estrogeny i androgeny), hiperkalcemia była zgłaszana u niektórych pacjentów z rakiem piersi z przerzutami do kości w ciągu kilku tygodni od rozpoczęcia leczenia preparatem NOLVADEX (cytrynian tamoksyfenu). W przypadku wystąpienia hiperkalcemii należy podjąć odpowiednie środki, a jeśli jest ciężka, należy odstawić NOLVADEX (cytrynian tamoksyfenu).
Wpływ na raka macicy i endometrium i mięsaka macicy
związku z leczeniem preparatem NOLVADEX (cytrynian tamoksyfenu) zgłaszano zwiększoną częstość występowania nowotworów macicy. Mechanizm leżący u podstaw jest nieznany, ale może być związany z estrogenopodobnym działaniem preparatu NOLVADEX (cytrynian tamoksyfenu). Większość nowotworów macicy obserwowanych w związku z lekiem NOLVADEX (cytrynian tamoksyfenu) jest klasyfikowana jako gruczolakorak endometrium. Zgłaszano jednak również rzadkie mięsaki macicy, w tym złośliwe mieszane guzy Mulleriana (MMMT). Mięsak macicy zwykle wiąże się z wyższym stopniem FIGO (III/IV) w momencie rozpoznania, gorszym rokowaniem i krótszym czasem przeżycia. Zgłaszano, że mięsak macicy występuje częściej u osób długotrwale stosujących (≥ 2 lata) NOLVADEX (cytrynian tamoksyfenu) niż u osób niestosujących. Niektóre nowotwory macicy (rak endometrium lub mięsak macicy) zakończyły się zgonem.
badaniu NSABP P-1 wśród uczestników randomizowanych do grupy NOLVADEX (cytrynian tamoksyfenu) wystąpił statystycznie istotny wzrost częstości występowania raka endometrium (33 przypadki inwazyjnego raka endometrium w porównaniu z 14 przypadkami wśród uczestników randomizowanych do grupy placebo (RR=2,48) , 95% CI: 1,27-4,92. 33 przypadki u uczestniczek otrzymujących NOLVADEX (cytrynian tamoksyfenu) były w stadium I FIGO, w tym 20 IA, 12 IB i 1 IC gruczolakorak endometrium. (8 IA i 5 IB), a 1 to stopień IV wg FIGO. Pięć kobiet otrzymujących NOLVADEX (cytrynian tamoksyfenu) i 1 otrzymująca placebo oprócz zabiegu chirurgicznego otrzymało radioterapię pooperacyjną. czas randomizacji (26 przypadków inwazyjnego raka endometrium, w porównaniu do 6 przypadków wśród uczestniczek randomizowanych do grupy placebo (RR=4,50, 95% CI: 1,78-13,16) Wśród kobiet ≤ 49 lat w momencie randomizacji było 7 przypadków z ja inwazyjny rak endometrium, w porównaniu z 8 przypadkami wśród uczestników randomizowanych do grupy placebo (RR=0,94, 95% CI: 0,28-2,89). Jeśli wziąć pod uwagę wiek w momencie rozpoznania, wystąpiły 4 przypadki raka endometrium wśród uczestniczek ≤49 przydzielonych losowo do grupy NOLVADEX (cytrynian tamoksyfenu) w porównaniu do 2 wśród uczestniczek przydzielonych losowo do grupy placebo (RR=2,21, 95% CI: 0,4-12,0). W przypadku kobiet ≥ 50 w momencie rozpoznania, było 29 przypadków wśród uczestników randomizowanych do grupy NOLVADEX (cytrynian tamoksyfenu) w porównaniu do 12 wśród kobiet otrzymujących placebo (RR=2,5, 95% CI: 1,3-4,9). Wskaźniki ryzyka były podobne w obu grupach, chociaż mniej zdarzeń wystąpiło u młodszych kobiet. Większość (29 z 33 przypadków w grupie NOLVADEX (tamoksyfen cytrynian)) raków endometrium rozpoznano u kobiet z objawami, chociaż 5 z 33 przypadków w grupie NOLVADEX (tamoksyfen cytrynian) wystąpiło u kobiet bez objawów. Wśród kobiet otrzymujących NOLVADEX (cytrynian tamoksyfenu) zdarzenia wystąpiły między 1 a 61 miesiącem (średnia=32 miesiące) od rozpoczęcia leczenia.
zaktualizowanym przeglądzie danych długoterminowych (mediana całkowitego okresu obserwacji wynosi 6,9 roku, w tym obserwacji zaślepionej) u 8306 kobiet z nienaruszoną macicą podczas randomizacji w badaniu zmniejszania ryzyka NSABP P-1, częstość występowania obu gruczolakoraków i rzadkich mięsaków macicy obserwowano u kobiet przyjmujących NOLVADEX (cytrynian tamoksyfenu). Podczas zaślepionej obserwacji stwierdzono 36 przypadków gruczolakoraka endometrium w stopniu FIGO (22 w stopniu FIGO IA, 13 IB i 1 IC) u kobiet otrzymujących NOLVADEX (cytrynian tamoksyfenu) i 15 przypadków u kobiet otrzymujących placebo [14 było w stopniu FIGO I (9 IA i 5 IB), a 1 przypadek to FIGO stopień IV]. Spośród pacjentek otrzymujących NOLVADEX (cytrynian tamoksyfenu), u których rozwinął się rak endometrium, jeden z rakiem w stadium IA i 4 z rakiem w stadium IB otrzymały radioterapię. W grupie placebo jeden pacjent z rakiem FIGO w stadium 1B otrzymał radioterapię, a pacjent z rakiem FIGO w stadium IVB otrzymał chemioterapię i terapię hormonalną. Podczas całkowitej obserwacji gruczolakorak endometrium stwierdzono u 53 kobiet przydzielonych losowo do grupy NOLVADEX (cytrynian tamoksyfenu) (30 przypadków w stopniu FIGO IA, 20 w stopniu IB, 1 w stopniu IC i 2 w stopniu IIIC) i 17 kobiet placebo (9 przypadków to Stopień FIGO IA, 6 to Stopień IB, 1 to Stopień IIIC, a 1 to Stopień IVB) (przypadki na 1000 kobietolat odpowiednio 2,20 i 0,71). Niektórzy pacjenci oprócz zabiegu chirurgicznego otrzymywali radioterapię pooperacyjną. Mięsaki macicy zgłoszono u 4 kobiet przydzielonych losowo do grupy NOLVADEX (cytrynian tamoksyfenu) (1 była FIGO IA, 1 FIGO IB, 1 FIGO IIA i 1 FIGO IIIC) i jedną pacjentkę przydzieloną losowo do grupy placebo (FIGO 1A); zapadalność na 1000 kobietolat odpowiednio 0,17 i 0,04. Spośród pacjentów przydzielonych losowo do grupy NOLVADEX (cytrynian tamoksyfenu), przypadki FIGO IA i IB były odpowiednio MMMT i mięsakiem; FIGO II był MMMT; a FIGO III był mięsakiem; a jeden pacjent przydzielony losowo do placebo miał MMMT. Podobną zwiększoną częstość występowania gruczolakoraka endometrium i mięsaka macicy zaobserwowano u kobiet otrzymujących NOLVADEX (cytrynian tamoksyfenu) w pięciu innych badaniach klinicznych NSABP.
Każda pacjentka otrzymująca lub która wcześniej otrzymywała NOLVADEX (cytrynian tamoksyfenu), która zgłasza nieprawidłowe krwawienie z pochwy, powinna zostać niezwłocznie zbadana. Pacjenci otrzymujący lub otrzymujący wcześniej NOLVADEX (cytrynian tamoksyfenu) powinni mieć coroczne badania ginekologiczne i powinni niezwłocznie poinformować swoich lekarzy, jeśli wystąpią u nich jakiekolwiek nieprawidłowe objawy ginekologiczne, np. nieregularne miesiączki, nieprawidłowe krwawienie z pochwy, zmiany w wydzielinie z pochwy lub ból w obrębie miednicy lub nacisk.
W badaniu P-1 pobieranie próbek endometrium nie zmieniło wskaźnika wykrywalności raka endometrium w porównaniu z kobietami, które nie pobierały próbek endometrium (0,6% z pobieraniem próbek, 0,5% bez pobierania próbek) u kobiet z nienaruszoną macicą. Nie ma danych sugerujących, że rutynowe pobieranie próbek endometrium u bezobjawowych kobiet przyjmujących NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia zachorowalności na raka piersi byłoby korzystne.
Niezłośliwy wpływ na macicę
związku z leczeniem preparatem NOLVADEX (cytrynian tamoksyfenu) zgłaszano zwiększoną częstość występowania zmian endometrium, w tym rozrostu i polipów. Częstość występowania i wzór tego wzrostu sugerują, że mechanizm leżący u podstaw tego leku jest związany z estrogennymi właściwościami NOLVADEX (cytrynian tamoksyfenu).
Istnieje kilka doniesień o endometriozie i mięśniakach macicy u kobiet otrzymujących NOLVADEX (cytrynian tamoksyfenu). Mechanizm leżący u podstaw może wynikać z częściowego działania estrogenowego NOLVADEX (cytrynian tamoksyfenu). Torbiele jajników obserwowano również u niewielkiej liczby pacjentek przed menopauzą z zaawansowanym rakiem piersi, które były leczone lekiem NOLVADEX (cytrynian tamoksyfenu).
Doniesiono, że NOLVADEX (cytrynian tamoksyfenu) powoduje nieregularne miesiączki lub brak miesiączki.
Działanie zakrzepowo-zatorowe NOLVADEX (cytrynian tamoksyfenu)
Istnieją dowody na zwiększoną częstość występowania zdarzeń zakrzepowo-zatorowych, w tym zakrzepicy żył głębokich i zatorowości płucnej, podczas leczenia preparatem NOLVADEX (cytrynian tamoksyfenu). Gdy NOLVADEX (cytrynian tamoksyfenu) jest podawany jednocześnie z chemioterapią, może wystąpić dalszy wzrost częstości występowania objawów zakrzepowo-zatorowych. W leczeniu raka piersi u kobiet z incydentami zakrzepowo-zatorowymi w wywiadzie należy dokładnie rozważyć ryzyko i korzyści związane ze stosowaniem preparatu NOLVADEX (cytrynian tamoksyfenu). W małym podbadaniu (N=81) badania NSABP P-1 nie wydaje się, aby przeprowadzanie badań przesiewowych u kobiet w kierunku mutacji G20210A czynnika V Leiden i protrombiny jako sposobu identyfikacji tych, którzy mogą nie być odpowiednimi kandydatami do cytrynian).
Dane z badania NSABP P-1 pokazują, że uczestnicy otrzymujący NOLVADEX (cytrynian tamoksyfenu) bez historii zatorowości płucnej (PE) mieli statystycznie istotny wzrost zatorowości płucnej (18-NOLVADEX (cytrynian tamoksyfenu), 6-placebo, RR=3,01 , 95% CI: 1,15-9,27). Trzy z zatorów płucnych, wszystkie w ramieniu NOLVADEX (cytrynian tamoksyfenu), były śmiertelne. Osiemdziesiąt siedem procent przypadków zatorowości płucnej wystąpiło w momencie randomizacji u kobiet w wieku co najmniej 50 lat. Wśród kobiet otrzymujących NOLVADEX (cytrynian tamoksyfenu) zdarzenia wystąpiły między 2 a 60 miesiącem (średnia = 27 miesięcy) od rozpoczęcia leczenia.
tej samej populacji, nieistotny statystycznie wzrost zakrzepicy żył głębokich (ZŻG) zaobserwowano w grupie NOLVADEX (cytrynian tamoksyfenu) (30-NOLVADEX (cytrynian tamoksyfenu), 19-placebo; RR=1,59, 95% CI: 0,86 -2,98). Taki sam wzrost względnego ryzyka zaobserwowano u kobiet ≤ 49 i ≥ 50, chociaż mniej zdarzeń wystąpiło u młodszych kobiet. Kobiety, u których wystąpiły zdarzenia zakrzepowo-zatorowe, były zagrożone drugim zdarzeniem pokrewnym (7 z 25 kobiet otrzymujących placebo, 5 z 48 kobiet przyjmujących NOLVADEX (cytrynian tamoksyfenu)) i były narażone na powikłania zdarzenia i jego leczenia (0/25 w dniu placebo, 4/48 na NOLVADEX (cytrynian tamoksyfenu)). Wśród kobiet otrzymujących NOLVADEX (cytrynian tamoksyfenu) zdarzenia zakrzepicy żył głębokich wystąpiły między 2 a 57 miesiącem (średnia = 19 miesięcy) od rozpoczęcia leczenia.
Wystąpił nieistotny statystycznie wzrost udaru mózgu wśród pacjentów przydzielonych losowo do grupy NOLVADEX (cytrynian tamoksyfenu) (24-Placebo; 34-NOLVADEX (cytrynian tamoksyfenu); RR=1,42; 95% CI 0,82-2,51). Sześć z 24 udarów w grupie placebo uznano za krwotoczne, a 10 z 34 udarów w grupie NOLVADEX (cytrynian tamoksyfenu) zakwalifikowano jako krwotoczne. Siedemnaście z 34 udarów w grupie NOLVADEX (cytrynian tamoksyfenu) uznano za okluzyjne, a 7 uznano za o nieznanej etiologii. Czternaście z 24 udarów w ramieniu placebo było okluzyjnych, a 4 o nieznanej etiologii. Wśród tych udarów 3 udary w grupie placebo i 4 w grupie NOLVADEX (cytrynian tamoksyfenu) były śmiertelne. Osiemdziesiąt osiem procent udarów wystąpiło u kobiet w wieku co najmniej 50 lat w momencie randomizacji. Wśród kobiet otrzymujących NOLVADEX (cytrynian tamoksyfenu) zdarzenia wystąpiły między 1 a 63 miesiącem (średnia = 30 miesięcy) od rozpoczęcia leczenia.
Wpływ na wątrobę: Rak wątroby
W szwedzkim badaniu, w którym stosowano adiuwant NOLVADEX (cytrynian tamoksyfenu) 40 mg/dobę przez 2-5 lat, zgłoszono 3 przypadki raka wątroby w grupie leczonej NOLVADEX (cytrynian tamoksyfenu) w porównaniu z 1 przypadkiem w grupie obserwacyjnej (patrz ŚRODKI OSTROŻNOŚCI- Karcynogeneza ). W innych badaniach klinicznych oceniających NOLVADEX (cytrynian tamoksyfenu) nie zgłoszono do tej pory żadnego przypadku raka wątroby.
Jeden przypadek raka wątroby został zgłoszony w NSABP P-1 u uczestnika randomizowanego do grupy NOLVADEX (cytrynian tamoksyfenu).
Wpływ na wątrobę: skutki niezłośliwe
NOLVADEX (cytrynian tamoksyfenu) był związany ze zmianami poziomu enzymów wątrobowych, a w rzadkich przypadkach z szeregiem poważniejszych nieprawidłowości wątroby, w tym stłuszczeniem wątroby, cholestazą, zapaleniem i martwicą wątroby. Kilka z tych poważnych przypadków obejmowało ofiary śmiertelne. W większości zgłoszonych przypadków związek z preparatem NOLVADEX (cytrynian tamoksyfenu) jest niepewny. Odnotowano jednak pewne pozytywne zmiany i wycofania.
W badaniu NSABP P-1 zaobserwowano kilka zmian funkcji wątroby stopnia 3-4 (SGOT, SGPT, bilirubina, fosfataza alkaliczna) (10 w grupie placebo i 6 w grupie NOLVADEX (cytrynian tamoksyfenu)). Lipidy surowicy nie były systematycznie zbierane.
Inne nowotwory
badaniach klinicznych po leczeniu raka piersi preparatem NOLVADEX (cytrynian tamoksyfenu) zgłaszano szereg wtórnych guzów pierwotnych, występujących w miejscach innych niż endometrium. Dane z badań NSABP B-14 i P-1 nie wykazują wzrostu występowania innych nowotworów (pozamacicznych) wśród pacjentek otrzymujących NOLVADEX (cytrynian tamoksyfenu). To, czy zwiększone ryzyko innych nowotworów (nie macicy) jest związane z NOLVADEX (cytrynian tamoksyfenu) jest nadal niepewne i nadal jest oceniane.
Wpływ na oko
U pacjentów otrzymujących NOLVADEX (cytrynian tamoksyfenu) zgłaszano zaburzenia widzenia, w tym zmiany w rogówce, pogorszenie postrzegania kolorów, zakrzepicę żył siatkówki i retinopatię. U pacjentów otrzymujących NOLVADEX (cytrynian tamoksyfenu) zgłaszano zwiększoną częstość występowania zaćmy i konieczność jej operacji.
badaniu NSABP P-1 zwiększone ryzyko granicznego znaczenia rozwoju zaćmy wśród kobiet bez zaćmy na początku badania (540-NOLVADEX (cytrynian tamoksyfenu) ; 483 placebo; RR = 1,13, 95% CI: 1,00-1,28) było zauważony. Wśród tych samych kobiet NOLVADEX (cytrynian tamoksyfenu) wiązał się ze zwiększonym ryzykiem operacji zaćmy (101-NOLVADEX (cytrynian tamoksyfenu); 63-placebo; RR=1,62, 95% CI 1,18-2,22) (patrz Tabela 3 w FARMAKOLOGIA KLINICZNA ). Wśród wszystkich kobiet biorących udział w badaniu (z zaćmą lub bez zaćmy na początku badania), NOLVADEX (cytrynian tamoksyfenu) wiązał się ze zwiększonym ryzykiem operacji zaćmy (201-NOLVADEX (cytrynian tamoksyfenu); 129-placebo; RR=1,58, 95% CI 1,26-1,97). Podczas badania nie były wymagane badania oczu. Nie można wyciągnąć żadnych innych wniosków dotyczących zdarzeń okulistycznych bez zaćmy.
Kategoria ciąży D
NOLVADEX (cytrynian tamoksyfenu) może powodować uszkodzenie płodu, gdy jest podawany kobiecie w ciąży. Kobietom należy zalecić, aby nie zaszły w ciążę podczas przyjmowania leku NOLVADEX (cytrynian tamoksyfenu) lub w ciągu 2 miesięcy od odstawienia leku NOLVADEX (cytrynian tamoksyfenu) i powinny stosować barierowe lub niehormonalne środki antykoncepcyjne, jeśli są aktywne seksualnie. Tamoxifen nie powoduje niepłodności, nawet przy nieregularnych miesiączkach. Oczekuje się, że antyestrogenowe właściwości leku mają wpływ na funkcje rozrodcze. W badaniach rozrodczości u szczurów przy dawkach równych lub niższych od dawek stosowanych u ludzi zaobserwowano nieteratogenne zmiany rozwojowe szkieletu, które okazały się odwracalne. Ponadto w badaniach płodności na szczurach i badaniach teratologicznych na królikach z zastosowaniem dawek równych lub niższych od stosowanych u ludzi, zaobserwowano mniejszą częstość implantacji zarodków i większą częstość zgonów płodów lub opóźnienie wzrostu płodu, z wolniejszym uczeniem się niektóre szczenięta szczurów w porównaniu z historycznymi kontrolami. Kilku ciężarnym marmozetom podczas organogenezy lub w drugiej połowie ciąży podawano dawkę 10 mg/kg/dobę (około 2-krotność maksymalnej zalecanej dawki dziennej dla człowieka w przeliczeniu na mg/m2). Nie zaobserwowano deformacji i chociaż dawka była wystarczająco wysoka, aby przerwać ciążę u niektórych zwierząt, te, które utrzymały ciążę, nie wykazywały żadnych objawów teratogennych wad rozwojowych.
modelach rozwoju płodowego układu rozrodczego u gryzoni tamoksyfen (w dawkach od 0,002 do 2,4 razy większej od maksymalnej zalecanej dawki dobowej u ludzi w przeliczeniu na mg/m2) powodował zmiany u obu płci podobne do tych, jakie wywołuje estradiol, etynyloestradiol i dietylostilbestrol. Chociaż kliniczne znaczenie tych zmian nie jest znane, niektóre z tych zmian, zwłaszcza gruczolak pochwy, są podobne do zmian obserwowanych u młodych kobiet, które były narażone na dietylostilbestrolu w okresie życia płodowego i u których ryzyko rozwoju gruczolakoraka jasnokomórkowego wynosi 1 na 1000 pochwa lub szyjka macicy. Dotychczas nie wykazano, aby ekspozycja in utero na tamoksyfen powodowała u młodych kobiet gruczolak pochwy lub jasnokomórkowego gruczolakoraka pochwy lub szyjki macicy. Jednak tylko niewielka liczba młodych kobiet była narażona na tamoksyfen in utero, a mniejsza liczba była obserwowana wystarczająco długo (do wieku 15-20 lat), aby ustalić, czy w wyniku tej ekspozycji może wystąpić neoplazja pochwy lub szyjki macicy.
Nie ma odpowiednich i dobrze kontrolowanych badań tamoksyfenu u kobiet w ciąży. Odnotowano niewielką liczbę doniesień o krwawieniach z pochwy, samoistnych aborcjach, wadach wrodzonych i obumarciach płodów u kobiet w ciąży. Jeśli lek ten jest stosowany w okresie ciąży lub pacjentka zajdzie w ciążę w trakcie przyjmowania tego leku lub w ciągu około dwóch miesięcy po zaprzestaniu leczenia, należy pacjentkę poinformować o potencjalnym ryzyku dla płodu, w tym o potencjalnym ryzyku odległym jak syndrom.
Zmniejszenie zachorowalności na raka piersi u kobiet wysokiego ryzyka — kategoria ciąży D
W przypadku aktywnych seksualnie kobiet w wieku rozrodczym leczenie NOLVADEX (cytrynian tamoksyfenu) należy rozpocząć podczas menstruacji. U kobiet z nieregularnymi miesiączkami wystarczający jest ujemny wynik B-HCG bezpośrednio przed rozpoczęciem leczenia (patrz ŚRODKI OSTROŻNOŚCI-INFORMACJE DLA PACJENTÓW - Zmniejszenie zachorowalności na raka piersi u kobiet wysokiego ryzyka ).
ŚRODKI OSTROŻNOŚCI
Ogólny
pacjentek przyjmujących NOLVADEX (cytrynian tamoksyfenu) z powodu raka piersi zgłaszano sporadycznie zmniejszenie liczby płytek krwi, zwykle do 50 000-100 000/mm3, rzadko mniejsze. U pacjentów ze znaczną małopłytkowością wystąpiły rzadkie epizody krwotoczne, ale nie jest pewne, czy epizody te są spowodowane terapią NOLVADEX (cytrynian tamoksyfenu). Obserwowano leukopenię, czasami w połączeniu z niedokrwistością i (lub) małopłytkowością. Odnotowano rzadkie przypadki neutropenii i pancytopenii u pacjentów otrzymujących NOLVADEX (cytrynian tamoksyfenu); czasami może to być poważne.
W badaniu NSABP P-1, 6 kobiet otrzymujących NOLVADEX (cytrynian tamoksyfenu) i 2 kobiety otrzymujące placebo doświadczyły spadku liczby płytek krwi stopnia 3-4 (≤ 50 000/mm³).
Informacje dla pacjentów
Pacjentów należy poinstruować, aby przeczytali Przewodnik po lekach dostarczane zgodnie z wymogami prawa po wydaniu leku NOLVADEX 10 mg. Pełny tekst Przewodnik po lekach jest przedrukowany na końcu tego dokumentu.
Redukcja inwazyjnego raka piersi i DCIS u kobiet z DCIS
Kobiety z DCIS leczone lumpektomią i radioterapią, które rozważają stosowanie preparatu NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia częstości występowania drugiego raka piersi, powinny ocenić ryzyko i korzyści z leczenia, ponieważ leczenie preparatem NOLVADEX (cytrynian tamoksyfenu) zmniejszyło częstość występowania inwazyjnego raka piersi raka, ale nie wykazano wpływu na przeżycie (patrz Tabela 1 w FARMAKOLOGIA KLINICZNA ).
Zmniejszenie zachorowalności na raka piersi u kobiet wysokiego ryzyka
Kobiety z grupy wysokiego ryzyka zachorowania na raka piersi mogą rozważyć zastosowanie terapii NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia zachorowalności na raka piersi. To, czy uważa się, że korzyści z leczenia przewyższają ryzyko, zależy od osobistej historii zdrowia kobiety oraz od tego, jak ocenia ona korzyści i ryzyko. Dlatego też terapia NOLVADEX (tamoksyfen cytrynian) w celu zmniejszenia częstości występowania raka piersi może nie być odpowiednia dla wszystkich kobiet z grupy wysokiego ryzyka zachorowania na raka piersi. Kobiety, które rozważają terapię NOLVADEX (cytrynian tamoksyfenu), powinny skonsultować się z lekarzem w celu oceny potencjalnych korzyści i zagrożeń przed rozpoczęciem leczenia w celu zmniejszenia zachorowalności na raka piersi (patrz Tabela 3 w FARMAKOLOGIA KLINICZNA ). Kobiety powinny zrozumieć, że NOLVADEX (cytrynian tamoksyfenu) zmniejsza zachorowalność na raka piersi, ale może nie eliminować ryzyka. NOLVADEX (cytrynian tamoksyfenu) zmniejszał częstość występowania małych guzów z obecnością receptorów estrogenowych, ale nie zmieniał częstości występowania guzów bez receptorów estrogenowych lub większych guzów. U kobiet z rakiem piersi, u których występuje wysokie ryzyko zachorowania na drugi rak piersi, leczenie około 5-letnim lekiem NOLVADEX (cytrynian tamoksyfenu) zmniejszyło roczną częstość występowania drugiego raka piersi o około 50%.
Kobiety w ciąży lub planujące ciążę nie powinny przyjmować leku NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia ryzyka raka piersi. Skuteczna antykoncepcja niehormonalna musi być stosowana przez wszystkie kobiety przed menopauzą przyjmujące NOLVADEX (cytrynian tamoksyfenu) i przez około dwa miesiące po zakończeniu terapii, jeśli są aktywne seksualnie. Tamoxifen nie powoduje niepłodności, nawet przy nieregularnych miesiączkach. W przypadku aktywnych seksualnie kobiet w wieku rozrodczym leczenie NOLVADEX (cytrynian tamoksyfenu) należy rozpocząć podczas menstruacji. U kobiet z nieregularnymi miesiączkami wystarczający jest ujemny wynik B-HCG bezpośrednio przed rozpoczęciem leczenia (patrz OSTRZEŻENIA — kategoria ciążowa D ).
Przeprowadzono dwa europejskie badania nad tamoksyfenem w celu zmniejszenia ryzyka raka piersi, które nie wykazały różnicy w liczbie przypadków raka piersi między ramionami z tamoksyfenem i placebo. Badania te miały projekty badawcze, które różniły się od NSABP P-1, były mniejsze niż NSABP P-1 i obejmowały kobiety z niższym ryzykiem raka piersi niż te z P-1.
Monitorowanie podczas terapii NOLVADEX (cytrynian tamoksyfenu)
Kobiety przyjmujące lub wcześniej przyjmowane NOLVADEX (cytrynian tamoksyfenu) należy poinstruować, aby niezwłocznie zwróciły się o pomoc lekarską w przypadku pojawienia się nowych guzków piersi, krwawienia z pochwy, objawów ginekologicznych (nieregularności miesiączkowania, zmian w wydzielinie z pochwy lub bólu lub ucisku w miednicy), objawów obrzęku nóg lub tkliwość, niewyjaśniona duszność lub zmiany widzenia. Kobiety powinny poinformować wszystkich opiekunów, niezależnie od powodu oceny, że przyjmują NOLVADEX (cytrynian tamoksyfenu) .
Kobiety przyjmujące NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia zachorowalności na raka piersi powinny mieć przed rozpoczęciem leczenia badanie piersi, mammografię i badanie ginekologiczne. Badania te należy powtarzać w regularnych odstępach czasu podczas terapii, zgodnie z dobrą praktyką medyczną. Kobiety przyjmujące NOLVADEX (tamoksyfen cytrynian) jako adjuwantowe leczenie raka piersi powinny przestrzegać tych samych procedur monitorowania, co kobiety przyjmujące NOLVADEX (tamoksyfen cytrynian) w celu zmniejszenia częstości występowania raka piersi. Kobiety przyjmujące NOLVADEX (cytrynian tamoksyfenu) w leczeniu przerzutowego raka piersi powinny dokonać przeglądu tego planu monitorowania ze swoim opiekunem i wybrać odpowiednie metody i harmonogram oceny.
Testy laboratoryjne
Należy wykonywać okresową pełną morfologię krwi, w tym liczbę płytek krwi, oraz okresowe badania czynności wątroby.
Podczas badania ATAC, więcej pacjentów otrzymujących anastrozol miało podwyższone stężenie cholesterolu w surowicy w porównaniu do pacjentów otrzymujących NOLVADEX (cytrynian tamoksyfenu) (odpowiednio 9% w porównaniu z 3,5%).
Karcynogeneza
Konwencjonalne badanie kancerogenezy u szczurów w dawkach 5, 20 i 35 mg/kg/dobę (około jedno-, trzy- i siedmiokrotna maksymalna zalecana dawka dobowa dla ludzi w przeliczeniu na mg/m²) podawanych przez zgłębnik doustny przez okres do 2 lat ) wykazały znaczny wzrost raka wątrobowokomórkowego we wszystkich dawkach. Częstość występowania tych guzów była znacznie większa wśród szczurów, którym podawano 20 lub 35 mg/kg/dzień (69%) w porównaniu do tych, którym podawano 5 mg/kg/dzień (14%). W oddzielnym badaniu szczurom podawano tamoksyfen w dawce 45 mg/kg/dobę (około dziewięciokrotność maksymalnej dawki dziennej zalecanej dla ludzi w przeliczeniu na mg/m2); neoplazja wątrobowokomórkowa występowała po 3 do 6 miesiącach.
Guzy jajnika z komórek ziarnistych i guzy jąder z komórek śródmiąższowych obserwowano w dwóch oddzielnych badaniach na myszach. Myszom podawano trans i racemiczne formy tamoksyfenu przez 13 do 15 miesięcy w dawkach 5, 20 i 50 mg/kg/dzień (około połowa, dwa i pięć razy więcej niż zalecana dzienna dawka dla ludzi na mg/m²). podstawa).
Mutageneza
Nie stwierdzono potencjału genotoksycznego w konwencjonalnym zestawie testów in vivo i in vitro z pro- i eukariotycznymi systemami testowymi z systemami metabolizującymi leki. Jednak zwiększone poziomy adduktów DNA zaobserwowano po znakowaniu 32P w DNA z wątroby szczura i hodowanych ludzkich limfocytów. Stwierdzono również, że tamoksyfen zwiększa poziom tworzenia mikrojąder in vitro w ludzkiej linii komórek limfoblastoidalnych (MCL-5). W oparciu o te ustalenia, tamoksyfen jest genotoksyczny w komórkach MCL-5 gryzoni i ludzi.
Upośledzenie płodności
Tamoksyfen powodował zaburzenia płodności i poczęcia u samic szczurów w dawkach 0,04 mg/kg/dobę (około 0,01-krotność maksymalnej dawki dobowej zalecanej dla człowieka w przeliczeniu na mg/m2), gdy był podawany przez dwa tygodnie przed kryciem do 7 dnia ciąży . Przy tej dawce wskaźniki płodności i reprodukcji były znacznie zmniejszone wraz z całkowitą śmiertelnością płodów. Śmiertelność płodów była również zwiększona przy dawkach 0,16 mg/kg/dobę (około 0,03-krotność maksymalnej zalecanej dawki dobowej u ludzi w przeliczeniu na mg/m2), gdy samicom szczurów podawano dawki od 7 do 17 dnia ciąży. Tamoksyfen powodował poronienie, przedwczesny poród i śmierć płodów u królików, którym podano dawki równe lub większe niż 0,125 mg/kg/dobę (około 0,05-krotność maksymalnej dawki dziennej zalecanej dla ludzi w przeliczeniu na mg/m2). Nie stwierdzono zmian teratogennych ani u szczurów, ani u królików.
Kategoria ciąży D
Widzieć OSTRZEŻENIA .
Matki karmiące
Istnieją doniesienia, że tamoksyfen hamuje laktację. Dwa badania kontrolowane placebo z udziałem ponad 150 kobiet wykazały, że tamoksyfen znacząco hamuje wczesną poporodową produkcję mleka. W obu badaniach tamoksyfen podawano w ciągu 24 godzin od porodu przez okres od 5 do 18 dni. Wpływ tamoksyfenu na ustaloną produkcję mleka nie jest znany.
Nie ma danych dotyczących przenikania tamoksyfenu do mleka ludzkiego. W przypadku wydalania nie ma danych dotyczących wpływu tamoksyfenu zawartego w mleku matki na niemowlę karmione piersią lub zwierzęta karmione piersią. Jednak bezpośrednia ekspozycja noworodków na tamoksyfen myszy i szczurów (nie poprzez mleko matki) powodowała 1) uszkodzenia układu rozrodczego u samic gryzoni (podobne do tych obserwowanych u ludzi po ekspozycji wewnątrzmacicznej na dietylostilbestrol) i 2) wady czynnościowe układu rozrodczego u samców gryzonie, takie jak zanik jąder i zatrzymanie spermatogenezy.
Nie wiadomo, czy NOLVADEX (cytrynian tamoksyfenu) przenika do mleka ludzkiego. Ze względu na możliwość wystąpienia poważnych działań niepożądanych u niemowląt karmionych NOLVADEX (cytrynian tamoksyfenu), kobiety przyjmujące NOLVADEX (cytrynian tamoksyfenu) nie powinny karmić piersią.
Zmniejszenie zachorowalności na raka piersi u kobiet wysokiego ryzyka z DCIS
Nie wiadomo, czy NOLVADEX (cytrynian tamoksyfenu) przenika do mleka ludzkiego. Ze względu na możliwość wystąpienia poważnych działań niepożądanych u niemowląt karmionych NOLVADEX (cytrynian tamoksyfenu), kobiety przyjmujące NOLVADEX (cytrynian tamoksyfenu) nie powinny karmić piersią.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność preparatu NOLVADEX (cytrynian tamoksyfenu) u dziewcząt w wieku od 2 do 10 lat z zespołem McCune-Albrighta i przedwczesnym dojrzewaniem nie były badane po upływie jednego roku leczenia. Nie ustalono długoterminowych skutków terapii NOLVADEX (cytrynian tamoksyfenu) u dziewcząt. U osób dorosłych leczonych preparatem NOLVADEX (cytrynian tamoksyfenu) zaobserwowano zwiększenie częstości występowania nowotworów macicy, udaru mózgu i zatorowości płucnej (patrz OSTRZEŻENIE W PUDEŁKU , oraz FARMAKOLOGIA KLINICZNA-Badania kliniczne-Zespół McCune-Albright podrozdział).
Zastosowanie geriatryczne
badaniu NSABP P-1 odsetek kobiet w wieku co najmniej 65 lat wyniósł 16%. Kobiety w wieku co najmniej 70 lat stanowiły 6% uczestników. Zmniejszenie zachorowalności na raka piersi zaobserwowano wśród uczestników w każdym z podzbiorów: W sumie 28 i 10 inwazyjnych raków piersi zaobserwowano wśród uczestników 65 i starszych odpowiednio w grupach placebo i NOLVADEX (cytrynian tamoksyfenu). W przypadku wszystkich innych wyników wyniki w tej podgrupie odzwierciedlają wyniki obserwowane w podgrupie kobiet w wieku co najmniej 50 lat. Nie zaobserwowano ogólnych różnic w tolerancji między starszymi i młodszymi pacjentami (patrz FARMAKOLOGIA KLINICZNA - Badania kliniczne - Zmniejszenie zachorowalności na raka piersi u kobiet wysokiego ryzyka Sekcja).
badaniu NSABP B-24 odsetek kobiet w wieku co najmniej 65 lat wyniósł 23%. Kobiety w wieku co najmniej 70 lat stanowiły 10% uczestników. W sumie 14 i 12 inwazyjnych raków piersi zaobserwowano wśród uczestników 65 i starszych odpowiednio w grupach placebo i NOLVADEX (cytrynian tamoksyfenu). Ten podzbiór jest zbyt mały, aby wyciągnąć jakiekolwiek wnioski dotyczące skuteczności. We wszystkich innych punktach końcowych wyniki w tej podgrupie były porównywalne z wynikami młodszych kobiet włączonych do tego badania. Nie zaobserwowano ogólnych różnic w tolerancji między starszymi i młodszymi pacjentami.
PRZEDAWKOWAĆ
Objawami obserwowanymi przy najwyższych dawkach po badaniach mających na celu określenie LD50 u zwierząt były trudności z oddychaniem i drgawki.
Nie zgłoszono ostrego przedawkowania u ludzi. W badaniu z udziałem pacjentów z zaawansowanym rakiem z przerzutami, w którym specyficznie określono maksymalną tolerowaną dawkę preparatu NOLVADEX (cytrynian tamoksyfenu) w ocenie stosowania bardzo dużych dawek w celu odwrócenia oporności wielolekowej, stwierdzono ostrą neurotoksyczność objawiającą się drżeniem, hiperrefleksją, niestabilnym chodem i zawrotami głowy. Objawy te wystąpiły w ciągu 3-5 dni od rozpoczęcia stosowania leku NOLVADEX (cytrynian tamoksyfenu) i ustąpiły w ciągu 2-5 dni po zakończeniu leczenia. Nie stwierdzono trwałej toksyczności neurologicznej. Jeden pacjent doświadczył drgawek kilka dni po odstawieniu leku NOLVADEX (cytrynian tamoksyfenu) i ustąpiły objawy neurotoksyczne. Związek przyczynowy napadu padaczkowego z terapią NOLVADEX (cytrynian tamoksyfenu) jest nieznany. Wszystkie dawki podawane tym pacjentom były większe niż 400 mg/m2 dawki nasycającej, a następnie dawki podtrzymujące 150 mg/m2 NOLVADEX (cytrynian tamoksyfenu) podawane dwa razy dziennie.
tym samym badaniu wydłużenie odstępu QT na elektrokardiogramie odnotowano, gdy pacjentom podawano dawki wyższe niż 250 mg/m2 dawki nasycającej, a następnie dawki podtrzymujące 80 mg/m2 NOLVADEX (cytrynian tamoksyfenu) podawane dwa razy na dobę. W przypadku kobiety o powierzchni ciała 1,5 m² minimalna dawka nasycająca i dawki podtrzymujące podawane, przy których wystąpiły objawy neurologiczne i zmiany odstępu QT, były co najmniej 6-krotnie większe w porównaniu z maksymalną zalecaną dawką.
Nie jest znane żadne specyficzne leczenie przedawkowania; leczenie musi być objawowe.
PRZECIWWSKAZANIA
NOLVADEX (cytrynian tamoksyfenu) jest przeciwwskazany u pacjentów ze stwierdzoną nadwrażliwością na lek lub którykolwiek z jego składników.
Zmniejszenie zachorowalności na raka piersi u kobiet wysokiego ryzyka i kobiet z DCIS
NOLVADEX (tamoksyfen cytrynian) jest przeciwwskazany u kobiet, które wymagają jednoczesnego leczenia przeciwzakrzepowego typu kumaryny lub u kobiet z zakrzepicą żył głębokich lub zatorem płucnym w wywiadzie.
FARMAKOLOGIA KLINICZNA
NOLVADEX (cytrynian tamoksyfenu) jest środkiem niesteroidowym, który wykazał silne właściwości antyestrogenowe w testach na zwierzętach. Efekty antyestrogenowe mogą być związane z jego zdolnością do konkurowania z estrogenem o miejsca wiązania w tkankach docelowych, takich jak piersi. Tamoksyfen hamuje indukcję raka sutka szczura indukowanego przez dimetylobenzantracen (DMBA) i powoduje regresję już ustalonych guzów indukowanych DMBA. W tym modelu szczurzym wydaje się, że tamoksyfen wywiera działanie przeciwnowotworowe poprzez wiązanie receptorów estrogenowych.
W cytozolach pochodzących z ludzkich gruczolakoraków piersi tamoksyfen konkuruje z estradiolem o białko receptora estrogenowego.
Absorpcja i dystrybucja
Po podaniu pojedynczej dawki doustnej 20 mg tamoksyfenu średnie maksymalne stężenie w osoczu wynoszące 40 ng/ml (zakres od 35 do 45 ng/ml) wystąpiło około 5 godzin po podaniu. Spadek stężenia tamoksyfenu w osoczu jest dwufazowy z okresem półtrwania w końcowej fazie eliminacji wynoszącym około 5 do 7 dni. Średnie maksymalne stężenie N-desmetylotamoksyfenu w osoczu wynosi 15 ng/ml (zakres od 10 do 20 ng/ml). Przewlekłe podawanie 10 mg tamoksyfenu dwa razy na dobę przez 3 miesiące pacjentom skutkuje średnimi stężeniami w osoczu w stanie stacjonarnym wynoszącymi 120 ng/ml (zakres 67-183 ng/ml) dla tamoksyfenu i 336 ng/ml (zakres 148-654 ng/ ml) dla N-desmetylotamoksyfenu. Średnie stężenia tamoksyfenu i N-desmetylotamoksyfenu w osoczu w stanie stacjonarnym po podawaniu 20 mg tamoksyfenu raz na dobę przez 3 miesiące wynoszą 122 ng/ml (zakres 71-183 ng/ml) i 353 ng/ml (zakres 152-706 ng /ml). Po rozpoczęciu leczenia stężenie tamoksyfenu w stanie stacjonarnym jest osiągane po około 4 tygodniach, a stężenia w stanie stacjonarnym dla N-desmetylotamoksyfenu po około 8 tygodniach, co sugeruje, że okres półtrwania tego metabolitu wynosi około 14 dni. W badaniu krzyżowym w stanie stacjonarnym, w którym podawano tabletki 10 mg NOLVADEX (cytrynian tamoksyfenu) dwa razy na dobę w porównaniu z tabletkami 20 mg NOLVADEX (cytrynian tamoksyfenu) podawanymi raz na dobę, tabletka 20 mg NOLVADEX (cytrynian tamoksyfenu) była biorównoważna z 10 mg NOLVADEX (cytrynian tamoksyfenu) tabletki.
Metabolizm
Tamoksyfen jest intensywnie metabolizowany po podaniu doustnym. N-desmetylotamoksyfen jest głównym metabolitem występującym w osoczu pacjentów. Aktywność biologiczna N-desmetylotamoksyfenu wydaje się być podobna do aktywności tamoksyfenu. 4-hydroksytamoksyfen i pochodna alkoholu pierwszorzędowego tamoksyfenu w łańcuchu bocznym zostały zidentyfikowane jako metabolity o mniejszym znaczeniu w osoczu. Tamoksyfen jest substratem cytochromu P-450 3A, 2C9 i 2D6 oraz inhibitorem glikoproteiny P.
Wydalanie
Badania z udziałem kobiet otrzymujących 20 mg tamoksyfenu znakowanego 14C wykazały, że około 65% podanej dawki zostało wydalone z organizmu w ciągu 2 tygodni, przy czym główną drogą eliminacji jest wydalanie z kałem. Lek jest wydalany głównie w postaci koniugatów polarnych, przy czym niezmieniony lek i nieskoniugowane metabolity stanowią mniej niż 30% całkowitej radioaktywności kału.
Specjalne populacje
Wpływ wieku, płci i rasy na farmakokinetykę tamoksyfenu nie został określony. Nie określono wpływu zmniejszonej czynności wątroby na metabolizm i farmakokinetykę tamoksyfenu.
Pacjenci pediatryczni
Farmakokinetykę tamoksyfenu i N-desmetylotamoksyfenu scharakteryzowano za pomocą populacyjnej analizy farmakokinetycznej z użyciem nielicznych próbek na pacjenta uzyskanych od 27 dzieci w wieku od 2 do 10 lat włączonych do badania zaprojektowanego w celu oceny bezpieczeństwa, skuteczności i farmakokinetyki preparatu NOLVADEX (tamoksyfen). cytrynian) w leczeniu zespołu McCune-Albright. W celu określenia strukturalnego modelu farmakokinetyki tamoksyfenu do analizy włączono bogate dane z dwóch badań farmakokinetycznych cytrynianu tamoksyfenu, w których 59 kobiet po menopauzie z rakiem piersi ukończyło badania. Model jednoprzedziałowy zapewniał najlepsze dopasowanie do danych.
dzieci i młodzieży średnie maksymalne stężenie w osoczu w stanie stacjonarnym (Css, max) i AUC wyniosły odpowiednio 187 ng/ml i 4110 ng h/ml, a Css, max wystąpiło po około 8 godzinach od podania. Klirens (CL/F) skorygowany o masę ciała u dzieci i młodzieży był około 2,3 razy większy niż u kobiet z rakiem piersi. W najmłodszej kohorcie pacjentek pediatrycznych (2-6 lat) CL/F był 2,6-krotnie wyższy; w najstarszej kohorcie (7-10,9 lat) CL/F był około 1,9-krotnie wyższy. Ekspozycja na N-desmetylotamoksyfen była porównywalna u pacjentów pediatrycznych i dorosłych. Bezpieczeństwo i skuteczność preparatu NOLVADEX (cytrynian tamoksyfenu) u dziewcząt w wieku od 2 do 10 lat z zespołem McCune-Albrighta i przedwczesnym dojrzewaniem nie były badane po upływie jednego roku leczenia. Nie ustalono długoterminowych skutków terapii NOLVADEX (cytrynian tamoksyfenu) u dziewcząt. osób dorosłych leczonych preparatem NOLVADEX (cytrynian tamoksyfenu) zaobserwowano zwiększenie częstości występowania nowotworów macicy, udaru mózgu i zatorowości płucnej (patrz OSTRZEŻENIE W PUDEŁKU ).
Interakcje między lekami
Badania in vitro wykazały, że erytromycyna, cyklosporyna, nifedypina i diltiazem kompetycyjnie hamowały tworzenie N-desmetylotamoksyfenu o wartości K1 wynoszącej odpowiednio 20, 1, 45 i 30 µM. Znaczenie kliniczne tych badań in vitro jest nieznane.
Tamoksyfen zmniejszał stężenie letrozolu w osoczu o 37% podczas jednoczesnego podawania tych leków. Ryfampicyna, induktor cytochromu P-450 3A4 zmniejszała AUC i Cmax tamoksyfenu odpowiednio o 86% i 55%. Aminoglutetymid zmniejsza stężenie tamoksyfenu i N-desmetylotamoksyfenu w osoczu. Medroksyprogesteron zmniejsza stężenie N-desmetylu w osoczu, ale nie tamoksyfenu.
badaniu dotyczącym adiuwantowego anastrozolu jednoczesne podawanie anastrozolu i NOLVADEX (cytrynian tamoksyfenu) u pacjentek z rakiem piersi zmniejszyło stężenie anastrozolu w osoczu o 27% w porównaniu z uzyskanym po zastosowaniu samego anastrozolu; jednak jednoczesne podawanie nie miało wpływu na farmakokinetykę tamoksyfenu lub N-desmetylotamoksyfenu (patrz ŚRODKI OSTROŻNOŚCI - INTERAKCJE Z LEKAMI ). NOLVADEX (cytrynian tamoksyfenu) nie powinien być podawany jednocześnie z anastrozolem.
Studia kliniczne
Rak piersi z przerzutami
Kobiety przed menopauzą (NOLVADEX (cytrynian tamoksyfenu) vs. ablacja)
trzech prospektywnych, randomizowanych badaniach (Ingle, Pritchard, Buchanan) porównano NOLVADEX (cytrynian tamoksyfenu) z ablacją jajników (wycięciem jajników lub napromienianiem jajników) u kobiet przed menopauzą z zaawansowanym rakiem piersi. Chociaż odsetek obiektywnych odpowiedzi, czas do niepowodzenia leczenia i przeżycie były podobne w przypadku obu metod leczenia, ograniczony przyrost liczby pacjentów uniemożliwił wykazanie równoważności. W przeglądowej analizie danych dotyczących przeżycia z 3 badań, współczynnik ryzyka zgonu (NOLVADEX (cytrynian tamoksyfenu)/ablacja jajników) wynosił 1,00 z dwustronnym 95% przedziałem ufności wynoszącym od 0,73 do 1,37. Podwyższone stężenie estrogenów w surowicy i osoczu zaobserwowano u kobiet przed menopauzą otrzymujących NOLVADEX (tamoksyfen cytrynian), ale dane z randomizowanych badań nie sugerują niekorzystnego wpływu tego wzrostu. Ograniczona liczba pacjentek przed menopauzą z progresją choroby podczas leczenia NOLVADEX (cytrynian tamoksyfenu) odpowiedziała na późniejszą ablację jajników.
Męski rak piersi
Opublikowane wyniki od 122 pacjentów (119 możliwych do oceny) i opisy przypadków u 16 pacjentów (13 możliwych do oceny) leczonych preparatem NOLVADEX (cytrynian tamoksyfenu) wykazały, że NOLVADEX (cytrynian tamoksyfenu) jest skuteczny w paliatywnym leczeniu męskiego raka piersi. Sześćdziesięciu sześciu z tych 132 ocenianych pacjentów odpowiedziało na NOLVADEX (cytrynian tamoksyfenu), co stanowi 50% odsetek obiektywnych odpowiedzi.
Adiuwantowy rak piersi
Przegląd
The Early Breast Cancer Trialists' Collaborative Group (EBCTCG) przeprowadziła na całym świecie przeglądy systemowej terapii wspomagającej we wczesnym raku piersi w 1985, 1990 i ponownie w 1995 roku. adiuwant NOLVADEX (cytrynian tamoksyfenu) w dawkach 20-40 mg/dobę przez 1-5+ lat. Dwadzieścia pięć procent pacjentów otrzymało 1 rok lub krócej leczenia próbnego, 52% otrzymało 2 lata, a 23% około 5 lat. Czterdzieści osiem procent guzów miało receptor estrogenowy (ER) dodatni (> 10 fmol/mg), 21% miało ER słaby (
Wśród kobiet z ER-dodatnim lub nieznanym rakiem piersi i dodatnimi węzłami chłonnymi, które otrzymały około 5 lat leczenia, całkowite przeżycie po 10 latach wyniosło 61,4% dla NOLVADEX (cytrynian tamoksyfenu) w porównaniu do 50,5% dla grupy kontrolnej (logrank 2p
Wpływ zaplanowanego czasu trwania tamoksyfenu można opisać następująco. U kobiet z ER-dodatnim lub nieznanym rakiem piersi otrzymujących 1 rok lub mniej, 2 lata lub około 5 lat NOLVADEX (cytrynian tamoksyfenu), proporcjonalne zmniejszenie śmiertelności wyniosło odpowiednio 12%, 17% i 26% (tendencja znamienna przy 2p
Korzyść jest mniej wyraźna w przypadku kobiet z rakiem piersi ze słabym ER, u których proporcjonalne zmniejszenie nawrotów wynosiło 10% (2p = 0,007) dla wszystkich czasów łącznie lub 9% (2p = 0,02), jeśli wykluczono przeciwległe raki piersi. Odpowiednie zmniejszenie śmiertelności wyniosło 6% (NS). Efekty około 5 lat stosowania leku NOLVADEX (cytrynian tamoksyfenu) na nawroty i śmiertelność były podobne niezależnie od wieku i jednoczesnej chemioterapii. Nic nie wskazywało na to, że dawki większe niż 20 mg na dobę były bardziej skuteczne.
Anastrozole Adjuvant ATAC Trial - Badanie Anastrozole w porównaniu z NOLVADEX (cytrynian tamoksyfenu) w leczeniu uzupełniającym wczesnego raka piersi - Badanie adiuwantowe z anastrozolem zostało przeprowadzone u 9366 kobiet po menopauzie z operacyjnym rakiem piersi, które zostały losowo przydzielone do leczenia adiuwantowego anastrozolem 1 mg na dobę, NOLVADEX (cytrynian tamoksyfenu) 20 mg na dobę lub połączeniem tych dwóch metod leczenia przez pięć lat lub do nawrotu. choroby. Przy medianie okresu obserwacji wynoszącej 33 miesiące, skojarzenie anastrozolu i NOLVADEX (cytrynian tamoksyfenu) nie wykazało żadnej korzyści pod względem skuteczności w porównaniu z leczeniem samym NOLVADEXEM (cytrynian tamoksyfenu) u wszystkich pacjentów, jak również w subpopulacji z dodatnimi receptorami hormonalnymi. To ramię leczenia zostało przerwane z badania. Należy zapoznać się FARMAKOLOGIA KLINICZNA-Populacje specjalne-Interakcje między lekami , ŚRODKI OSTROŻNOŚCI-Badania laboratoryjne , ŚRODKI OSTROŻNOŚCI – Interakcje leków oraz DZIAŁANIA NIEPOŻĄDANE sekcje zawierające informacje dotyczące bezpieczeństwa z tego badania. Aby uzyskać dodatkowe informacje dotyczące tego badania, należy zapoznać się z pełną informacją dotyczącą przepisywania leku ARIMIDEX® (anastrozol) w tabletkach 1 mg.
Pacjenci w dwóch ramionach monoterapii w badaniu ATAC byli leczeni przez medianę 60 miesięcy (5 lat) i obserwowani przez medianę 68 miesięcy. Przeżycie wolne od choroby w populacji ITT było statystycznie istotnie lepsze [współczynnik ryzyka (HR) = 0,87, 95% CI: 0,78, 0,97, p=0,0127] w ramieniu anastrazolu w porównaniu z ramieniem NOLVADEX (cytrynian tamoksyfenu) .
Węzeł Pozytywny - Indywidualne Studia
Dwa badania (Hubay i NSABP B-09) wykazały poprawę przeżycia wolnego od choroby po radykalnej lub zmodyfikowanej radykalnej mastektomii u kobiet po menopauzie lub kobiet w wieku 50 lat lub starszych z chirurgicznie wyleczalnym rakiem piersi z dodatnimi węzłami pachowymi, gdy NOLVADEX (cytrynian tamoksyfenu) był dodany do adiuwantowej chemioterapii cytotoksycznej. W badaniu Hubay, NOLVADEX (cytrynian tamoksyfenu) dodano do CMF w „niskiej dawce” (cyklofosfamid, metotreksat i fluorouracyl). W badaniu NSABP B-09 NOLVADEX (cytrynian tamoksyfenu) dodano do melfalanu [Iperyna L-fenyloalaniny (P)] i fluorouracylu (F).
badaniu Hubay pacjenci z dodatnim (powyżej 3 fmol) receptorem estrogenowym mieli większe szanse na odniesienie korzyści. W badaniu NSABP B-09 u kobiet w wieku 50-59 lat, tylko kobiety z poziomem receptorów estrogenowych i progesteronowych 10 fmol lub wyższym wyraźnie odniosły korzyści, podczas gdy zaobserwowano nieistotny statystycznie trend w kierunku działań niepożądanych u kobiet z poziomem receptorów zarówno estrogenowych, jak i progesteronowych mniej niż 10 fmol. U kobiet w wieku 60-70 lat zaobserwowano tendencję do korzystnego działania NOLVADEX (cytrynian tamoksyfenu) bez wyraźnego związku ze statusem receptora estrogenowego lub progesteronowego.
Trzy prospektywne badania (ECOG-1178, Toronto, NATO) z zastosowaniem NOLVADEX (cytrynian tamoksyfenu) jako adiuwant jako pojedynczy środek wykazały poprawę przeżycia wolnego od choroby po całkowitej mastektomii i resekcji pach u kobiet po menopauzie z dodatnimi węzłami pachowymi w porównaniu z grupą kontrolną placebo/brak leczenia . Badanie NATO wykazało również ogólną korzyść w zakresie przeżywalności.
Węzeł negatywny - badania indywidualne
NSABP B-14, prospektywne, podwójnie zaślepione, randomizowane badanie, porównywało NOLVADEX (cytrynian tamoksyfenu) z placebo u kobiet z rakiem piersi z ujemnymi węzłami pachowymi, z dodatnim receptorem estrogenowym (≥ 10 fmol/mg białka cytozolu) (jako leczenie uzupełniające , po całkowitej mastektomii i resekcji pachowej lub resekcji odcinkowej
INFORMACJA O PACJENCIE
PRZEWODNIK LEKÓW
NOLVADEX (cytrynian tamoksyfenu) ® (NOLE-vah-dex) Tabletki Nazwa ogólna: tamoksyfen (ta-MOX-I-fen)
Napisany dla kobiet, które stosują NOLVADEX (cytrynian tamoksyfenu) w celu obniżenia wysokiego ryzyka zachorowania na raka piersi lub które mają raka przewodowego in situ (DCIS)
Niniejszy Przewodnik po lekach omawia jedynie stosowanie NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia ryzyka zachorowania na raka piersi u kobiet wysokiego ryzyka i kobiet leczonych z powodu DCIS.
Osoby przyjmujące NOLVADEX (cytrynian tamoksyfenu) leczyć rak piersi ma inne korzyści i inne decyzje do podjęcia niż kobiety wysokiego ryzyka lub kobiety z rakiem przewodowym in situ (DCIS) przyjmujące NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia ryzyka zachorowania na raka piersi. Jeśli masz już raka piersi, porozmawiaj ze swoim lekarzem o tym, jak korzyści z leczenia raka piersi lekiem NOLVADEX (cytrynian tamoksyfenu) porównują się z ryzykiem opisanym w tym dokumencie.
Dlaczego powinienem przeczytać ten Przewodnik po lekach?
Ten przewodnik zawiera informacje, które pomogą Ci zdecydować, czy użyć NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia ryzyka zachorowania na raka piersi.
Ty i twój lekarz powinniście porozmawiać o tym, czy możliwe korzyści ze stosowania leku NOLVADEX (cytrynian tamoksyfenu) w zmniejszaniu dużego ryzyka zachorowania na raka piersi są większe niż możliwe ryzyko. Twój lekarz ma specjalny program komputerowy lub podręczny kalkulator, aby stwierdzić, czy należysz do grupy wysokiego ryzyka. Jeśli pacjentka ma DCIS i była leczona chirurgicznie i radioterapią, lekarz może przepisać NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia ryzyka zachorowania na inwazyjnego (rozprzestrzeniającego się) raka piersi.
Przeczytaj uważnie ten przewodnik przed rozpoczęciem stosowania NOLVADEX (cytrynian tamoksyfenu) . Ważne jest, aby czytać informacje, które otrzymujesz za każdym razem, gdy otrzymujesz więcej leku. Może być coś nowego. Ten przewodnik nie mówi wszystkiego o NOLVADEX (cytrynian tamoksyfenu) i robi nie zamiast rozmawiać z lekarzem.
Tylko Ty i Twój lekarz możecie ustalić, czy NOLVADEX (cytrynian tamoksyfenu) jest dla Ciebie odpowiedni.
Jakie są najważniejsze informacje, które powinienem wiedzieć o stosowaniu NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia ryzyka zachorowania na raka piersi?
NOLVADEX (cytrynian tamoksyfenu) jest lekiem na receptę, który pod pewnymi względami jest podobny do estrogenu (hormonu żeńskiego), a pod innymi względami różni się od niego. W przypadku piersi NOLVADEX (cytrynian tamoksyfenu) może blokować działanie estrogenu. Ponieważ tak się dzieje, NOLVADEX (cytrynian tamoksyfenu) może blokować wzrost raka piersi, który potrzebuje estrogenu do wzrostu (raki z dodatnim receptorem estrogenowym lub progesteronowym).
NOLVADEX (cytrynian tamoksyfenu) może zmniejszyć ryzyko zachorowania na raka piersi u kobiet z wyższym niż normalnie ryzykiem zachorowania na raka piersi w ciągu najbliższych pięciu lat (kobiety wysokiego ryzyka) oraz kobiet z DCIS.
Ponieważ kobiety wysokiego ryzyka nie mają jeszcze raka, ważne jest, aby dokładnie przemyśleć, czy możliwe korzyści ze stosowania NOLVADEX (cytrynian tamoksyfenu) w zmniejszeniu ryzyka zachorowania na raka piersi są większe niż możliwe ryzyko.
Niniejszy przewodnik po lekach zawiera przegląd zagrożeń i korzyści związanych ze stosowaniem NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia ryzyka zachorowania na raka piersi u kobiet wysokiego ryzyka i kobiet z DCIS. Ten przewodnik nie nie omówić specjalne korzyści i decyzje dla osób, które już mają raka piersi.
Dlaczego kobiety i mężczyźni stosują NOLVADEX (cytrynian tamoksyfenu)?
NOLVADEX (cytrynian tamoksyfenu) ma więcej niż jedno zastosowanie. NOLVADEX (cytrynian tamoksyfenu) stosuje się:
zmniejszyć szansę zachorowania na raka piersi u kobiet z wyższym niż normalnie ryzykiem zachorowania na raka piersi w ciągu najbliższych 5 lat (kobiety wysokiego ryzyka)
zmniejszyć szansę inwazyjnego (rozprzestrzeniającego się) raka piersi u kobiet, które przeszły operację i radioterapię z powodu raka przewodowego in situ (DCIS). DCIS oznacza, że rak znajduje się tylko wewnątrz przewodów mlecznych.
leczyć raka piersi u kobiet po zakończeniu wczesnego leczenia. Wczesne leczenie może obejmować operację, radioterapię i chemioterapię. NOLVADEX (cytrynian tamoksyfenu) może zapobiegać rozprzestrzenianiu się raka na inne części ciała. Może również zmniejszyć ryzyko zachorowania kobiety na nowego raka piersi. u kobiet i mężczyzn,
leczyć rak piersi, który rozprzestrzenił się na inne części ciała (rak piersi z przerzutami).
Ten przewodnik mówi tylko o stosowaniu NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia ryzyka zachorowania na raka piersi (#1 i #2 powyżej).
Jakie korzyści przynosi NOLVADEX (cytrynian tamoksyfenu) w zmniejszaniu ryzyka zachorowania na raka piersi u kobiet wysokiego ryzyka i kobiet leczonych z powodu DCIS?
Przyjrzano się dużemu badaniu amerykańskiemu kobiety wysokiego ryzyka porównali tych, którzy przyjmowali NOLVADEX (cytrynian tamoksyfenu) przez 5 lat z innymi, którzy brali pigułkę bez NOLVADEXU (cytrynian tamoksyfenu) (placebo). Kobiety wysokiego ryzyka zostały zdefiniowane jako kobiety, u których prawdopodobieństwo zachorowania na raka piersi wynosi 1,7% lub więcej w ciągu najbliższych 5 lat, na podstawie specjalnego programu komputerowego. W tym badaniu:
- Na każde 1000 kobiet wysokiego ryzyka kto wziął placebo? , każdego roku około 7 zachorowało na raka piersi.
- Na każde 1000 kobiet wysokiego ryzyka którzy przyjmowali NOLVADEX (cytrynian tamoksyfenu) , każdego roku około 4 zachorowało na raka piersi.
Badanie wykazało, że średnio kobiety wysokiego ryzyka, które przyjmowały NOLVADEX (cytrynian tamoksyfenu) obniżyły swoje szanse zachorowania na raka piersi o 44%, z 7 na 1000 do 4 na 1000.
Przyjrzano się innym amerykańskim badaniom kobiety z DCIS i porównali tych, którzy przyjmowali NOLVADEX (cytrynian tamoksyfenu) przez 5 lat z innymi, którzy przyjmowali placebo. W tym badaniu:
- Na każde 1000 kobiet z DCIS kto wziął placebo? każdego roku około 17 zachorowało na raka piersi.
- Na każde 1000 kobiet z DCIS którzy przyjmowali NOLVADEX (cytrynian tamoksyfenu) , każdego roku około 10 zachorowało na raka piersi.
Badanie wykazało, że kobiety z DCIS, które przyjmowały NOLVADEX (cytrynian tamoksyfenu) obniżyły swoje szanse na inwazyjny (rozprzestrzeniający się) rak piersi o 43%, z 17 na 1000 do 10 na 1000.
Badania te nie oznaczają, że przyjmowanie NOLVADEX (cytrynian tamoksyfenu) zmniejszy twoją osobistą szansę zachorowania na raka piersi. Nie wiemy, jakie korzyści odniesie jedna kobieta, która zażyje NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia ryzyka zachorowania na raka piersi.
Jakie są zagrożenia związane z NOLVADEX (cytrynian tamoksyfenu)?
W badaniach opisanych w punkcie „Jakie korzyści przynosi NOLVADEX (cytrynian tamoksyfenu)?”, kobiety wysokiego ryzyka, które przyjmowały NOLVADEX (cytrynian tamoksyfenu) częściej wykazywały pewne działania niepożądane niż te, które przyjmowały placebo.
Niektóre z tych skutków ubocznych mogą spowodować śmierć.
W jednym badaniu u kobiet, które nadal miały macicę
- Na każde 1000 kobiet, które przyjmowały placebo, co roku 1 zachorowała na raka endometrium (rak wyściółki macicy) i żadna nie zachorowała na mięsaka macicy (rak trzonu macicy).
- Na każde 1000 kobiet, które przyjmowały NOLVADEX (cytrynian tamoksyfenu), co roku 2 zachorowały na raka endometrium, a mniej niż 1 zachorowała na mięsaka macicy.
Wyniki te pokazują, że średnio u kobiet wysokiego ryzyka który wciąż miał swoją macicę NOLVADEX (cytrynian tamoksyfenu) podwoił ryzyko zachorowania na raka endometrium z 1 na 1000 do 2 na 1000 i zwiększył ryzyko zachorowania na mięsaka macicy. Nie oznacza to, że przyjmowanie leku NOLVADEX (cytrynian tamoksyfenu) podwoi twoją osobistą szansę zachorowania na raka endometrium lub zwiększy ryzyko zachorowania na mięsaka macicy. Nie wiemy, jakie będzie to ryzyko dla jednej kobiety. Ryzyko jest inne w przypadku kobiet, które nie mają już macicy.
wszystkich kobiet biorących udział w tym badaniu przyjmowanie NOLVADEX (cytrynian tamoksyfenu) zwiększało ryzyko wystąpienia zakrzepów krwi w płucach lub żyłach lub udaru. W niektórych przypadkach kobiety umierały z powodu tych efektów.
NOLVADEX (tamoksyfen cytrynian) zwiększał ryzyko wystąpienia zaćmy (zmętnienia soczewki oka) lub konieczności operacji zaćmy. (Zobacz „Jakie są możliwe skutki uboczne NOLVADEX (cytrynian tamoksyfenu)?”, aby uzyskać więcej informacji na temat działań niepożądanych).
Czego nie wiemy o przyjmowaniu NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia ryzyka zachorowania na raka piersi?
Nie wiemy
- jeśli NOLVADEX (cytrynian tamoksyfenu) zmniejsza ryzyko zachorowania na raka piersi u kobiet z nieprawidłowymi genami raka piersi (BRCA1 i BRCA2)
- jeśli przyjmowanie leku NOLVADEX (cytrynian tamoksyfenu) przez 5 lat zmniejsza liczbę nowotworów piersi, które kobieta zachoruje w ciągu swojego życia lub opóźnia tylko niektóre nowotwory piersi
- czy NOLVADEX (cytrynian tamoksyfenu) pomaga kobiecie żyć dłużej
- skutki przyjmowania NOLVADEX (cytrynian tamoksyfenu) z hormonalną terapią zastępczą (HTZ), pigułkami antykoncepcyjnymi lub androgenami (hormonami męskimi)
- korzyści ze stosowania leku NOLVADEX (cytrynian tamoksyfenu) u osób poniżej 35 roku życia
Prowadzone są badania, aby dowiedzieć się więcej na temat długoterminowych korzyści i zagrożeń związanych ze stosowaniem NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia ryzyka zachorowania na raka piersi.
Jakie są możliwe skutki uboczne NOLVADEX (cytrynian tamoksyfenu)?
Najczęstszym działaniem niepożądanym leku NOLVADEX (cytrynian tamoksyfenu) są uderzenia gorąca. To nie jest oznaka poważnego problemu.
Kolejnym najczęstszym działaniem niepożądanym jest upławy. Jeśli wydzielina jest krwawa, może to świadczyć o poważnym problemie. [Patrz „Zmiany w wyściółce (endometrium) lub korpusie macicy” poniżej.]
Mniej powszechne, ale poważne skutki uboczne NOLVADEX (cytrynian tamoksyfenu) są wymienione poniżej. Mogą wystąpić w dowolnym momencie. Należy natychmiast skontaktować się z lekarzem, jeśli wystąpią jakiekolwiek objawy działań niepożądanych wymienionych poniżej:
- Zmiany w wyściółce (endometrium) lub korpusie macicy. Zmiany te mogą oznaczać początek poważnych problemów, w tym raka macicy. Oznaki zmian w macicy to:
- Krwawienie z pochwy lub krwawa wydzielina, która może mieć rdzawy lub brązowy kolor. Powinieneś skontaktować się z lekarzem, nawet jeśli wystąpi tylko niewielkie krwawienie.
- Zmiana miesięcznego krwawienia, taka jak ilość lub czas krwawienia lub zwiększona krzepliwość.
- Ból lub ucisk w miednicy (poniżej pępka).
- Zakrzepy krwi w żyłach lub płucach. Mogą one powodować poważne problemy, w tym śmierć. Zakrzepy mogą wystąpić do 2-3 miesięcy po zaprzestaniu przyjmowania leku NOLVADEX (cytrynian tamoksyfenu). Oznaki zakrzepów krwi to:
- nagły ból w klatce piersiowej, duszność, odkrztuszanie krwi
- ból, tkliwość lub obrzęk jednej lub obu nóg
- Uderzenie. Udar może spowodować poważne problemy zdrowotne, w tym śmierć. Oznaki udaru to:
- nagłe osłabienie, mrowienie lub drętwienie twarzy, ręki lub nogi, zwłaszcza po jednej stronie ciała
- nagłe zamieszanie, trudności w mówieniu lub rozumieniu
- nagłe problemy z widzeniem w jednym lub obu oczach
- nagłe problemy z chodzeniem, zawroty głowy, utrata równowagi lub koordynacji
- nagły silny ból głowy bez znanej przyczyny
- Zaćma lub zwiększone ryzyko konieczności operacji zaćmy. Oznaką tych problemów jest powolne rozmycie widzenia.
- Problemy z wątrobą, w tym żółtaczka. Objawy problemów z wątrobą obejmują brak apetytu i zażółcenie skóry lub białek oczu.
To nie wszystkie możliwe działania niepożądane NOLVADEX (cytrynian tamoksyfenu). Aby uzyskać pełną listę, zapytaj swojego lekarza lub farmaceutę.
Kto nie powinien brać NOLVADEX (cytrynian tamoksyfenu)?
Nie należy przyjmować leku NOLVADEX (cytrynian tamoksyfenu) z jakiegokolwiek powodu, jeśli:
- Jesteś w ciąży lub planujesz zajść w ciążę podczas przyjmowania leku NOLVADEX (cytrynian tamoksyfenu) lub w ciągu 2 miesięcy po zaprzestaniu przyjmowania leku NOLVADEX (cytrynian tamoksyfenu). NOLVADEX (cytrynian tamoksyfenu) może zaszkodzić nienarodzonemu dziecku. Usunięcie NOLVADEX (cytrynian tamoksyfenu) z organizmu zajmuje około 2 miesięcy. Aby upewnić się, że nie jesteś w ciąży, możesz zacząć przyjmować NOLVADEX (cytrynian tamoksyfenu) podczas miesiączki. Możesz też wykonać test ciążowy, aby upewnić się, że nie jesteś w ciąży, zanim zaczniesz.
- Czy karmi piersią. Nie wiemy, czy NOLVADEX (cytrynian tamoksyfenu) może przenikać do mleka i zaszkodzić dziecku.
- Miałeś reakcję alergiczną na NOLVADEX (cytrynian tamoksyfenu) lub tamoksyfen (inna nazwa NOLVADEX (cytrynian tamoksyfenu)) lub na którykolwiek z jego nieaktywnych składników.
W przypadku zajścia w ciążę podczas przyjmowania leku NOLVADEX (cytrynian tamoksyfenu), należy natychmiast przerwać jego stosowanie i skontaktować się z lekarzem. NOLVADEX (cytrynian tamoksyfenu) może zaszkodzić nienarodzonemu dziecku. Nie należy przyjmować leku NOLVADEX (cytrynian tamoksyfenu) w celu zmniejszenia ryzyka zachorowania na raka piersi, jeśli:
- Miałeś kiedyś zakrzep krwi, który wymagał leczenia.
- Zażywasz leki rozrzedzające krew, takie jak warfaryna (zwana również Coumadin®*).
- Twoja zdolność do poruszania się jest ograniczona przez większość godzin na jawie.
- Jesteś zagrożony zakrzepami krwi. Lekarz może powiedzieć, czy istnieje wysokie ryzyko powstania zakrzepów krwi.
- Nie masz większej niż normalnie szansy na zachorowanie na raka piersi. Twój lekarz może ci powiedzieć, czy jesteś kobietą wysokiego ryzyka.
Jak zażywać NOLVADEX (cytrynian tamoksyfenu)?
- Tabletkę(i) należy połknąć w całości, popijając wodą lub innym płynem bezalkoholowym. NOLVADEX (cytrynian tamoksyfenu) można przyjmować z posiłkiem lub bez posiłku. Lek należy przyjmować codziennie. Łatwiej będzie zapamiętać, jeśli zażywasz go codziennie o tej samej porze.
- W przypadku pominięcia dawki należy ją przyjąć, gdy sobie przypomnisz, a następną dawkę przyjąć jak zwykle. Jeśli zbliża się pora przyjęcia następnej dawki lub jeśli przypomnisz sobie o kolejnej dawce, nie należy przyjmować dodatkowych tabletek w celu uzupełnienia pominiętej dawki.
- Lek NOLVADEX (cytrynian tamoksyfenu) należy przyjmować przez 5 lat, chyba że lekarz zaleci inaczej.
Czego powinienem unikać biorąc NOLVADEX (cytrynian tamoksyfenu)?
- Nie należy zachodzić w ciążę podczas przyjmowania leku NOLVADEX (cytrynian tamoksyfenu) lub przez 2 miesiące po jego odstawieniu. NOLVADEX (cytrynian tamoksyfenu) może powstrzymać działanie hormonalnych metod antykoncepcji. Metody hormonalne obejmują pigułki antykoncepcyjne, plastry, zastrzyki, pierścienie i implanty. Dlatego przyjmując NOLVADEX (cytrynian tamoksyfenu), stosować metody kontroli urodzeń, które nie wykorzystują hormonów, takie jak prezerwatywy, membrany ze środkiem plemnikobójczym lub zwykłe wkładki domaciczne. W przypadku zajścia w ciążę należy natychmiast przerwać stosowanie leku NOLVADEX (cytrynian tamoksyfenu) i skontaktować się z lekarzem.
- Nie karmić piersią. Nie wiemy, czy NOLVADEX (cytrynian tamoksyfenu) może przenikać do mleka i czy może zaszkodzić dziecku.
Co powinienem zrobić podczas przyjmowania leku NOLVADEX (cytrynian tamoksyfenu)?
- Mieć regularne kontrole ginekologiczne („egzamin kobiet”), badanie piersi i mammografię. Twój lekarz powie Ci, jak często. Będą one sprawdzać oznaki raka piersi i raka endometrium (wyściółki macicy). Ponieważ NOLVADEX (cytrynian tamoksyfenu) nie zapobiega wszystkim rakom piersi i możesz zachorować na inne rodzaje raka, potrzebujesz tych badań, aby jak najwcześniej wykryć jakiekolwiek nowotwory.
- Ponieważ NOLVADEX (cytrynian tamoksyfenu) może powodować poważne skutki uboczne, zwracaj szczególną uwagę na swój organizm. Objawy, na które należy zwrócić uwagę, są wymienione w części „Jakie są możliwe skutki uboczne stosowania leku NOLVADEX (cytrynian tamoksyfenu)?”
- Poinformuj wszystkich lekarzy, że widzisz, że przyjmujesz NOLVADEX (cytrynian tamoksyfenu).
- Należy natychmiast poinformować lekarza, jeśli pojawią się nowe guzki piersi.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu NOLVADEX (cytrynian tamoksyfenu)
Leki są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Lekarz przepisał NOLVADEX (cytrynian tamoksyfenu) tylko dla Ciebie. Nie podawaj go innym osobom, nawet jeśli mają podobny stan, ponieważ może im to zaszkodzić. Nie używaj go w stanie, na który nie został przepisany.
Niniejszy Przewodnik po lekach jest podsumowaniem informacji o NOLVADEX (cytrynian tamoksyfenu) dla kobiet, które stosują NOLVADEX (cytrynian tamoksyfenu) w celu obniżenia wysokiego ryzyka zachorowania na raka piersi lub z DCIS. Aby uzyskać więcej informacji na temat leku NOLVADEX (cytrynian tamoksyfenu), należy zwrócić się do lekarza lub farmaceuty. Mogą udzielić informacji na temat NOLVADEX (cytrynian tamoksyfenu), które są napisane dla pracowników służby zdrowia. Aby uzyskać więcej informacji na temat NOLVADEX (cytrynian tamoksyfenu) lub raka piersi, odwiedź stronę www.NOLVADEX (cytrynian tamoksyfenu) .com lub zadzwoń pod numer 1-800-236-9933.
Składniki: cytrynian tamoksyfenu, wapń karboksymetylocelulozy, stearynian magnezu, mannitol i skrobia.
Ten przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków
