Procardia 30mg Nifedipine Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Procardia 30mg i jak się go stosuje?
Procardia to lek na receptę stosowany w leczeniu objawów bólu w klatce piersiowej (dławicy piersiowej), wysokiego ciśnienia krwi (nadciśnienia) i nadciśnienia płucnego. Procardia 30mg może być stosowana samodzielnie lub z innymi lekami.
Procardia należy do klasy leków zwanych blokerami kanału wapniowego; Blokery kanału wapniowego, dihydrofirydyna.
Nie wiadomo, czy Procardia jest bezpieczna i skuteczna u dzieci.
Jakie są możliwe skutki uboczne Procardia?
Procardia może powodować poważne skutki uboczne, w tym:
- gorączka,
- ból gardła,
- płonące oczy,
- ból skóry,
- czerwona lub fioletowa wysypka skórna z powstawaniem pęcherzy i łuszczeniem się,
- nasilający się ból w klatce piersiowej,
- bicie serca,
- fruwające w piersi,
- zawroty,
- obrzęk rąk lub nóg,
- ból w górnej części brzucha i
- zażółcenie skóry lub oczu (żółtaczka)
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Procardia 30mg to:
- obrzęk,
- zaczerwienienie (uczucie ciepła, zaczerwienienie lub mrowienie),
- ból głowy,
- zawroty głowy,
- mdłości,
- zgaga i
- uczucie osłabienia lub zmęczenia
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Procardia. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
OPIS
PROCARDIA® (nifedypina) jest lekiem przeciwdławicowym należącym do klasy środków farmakologicznych, blokerów kanału wapniowego. Nifedypina to kwas 3,5-pirydynodikarboksylowy, 1,4-dihydro-2,6-dimetylo-4-(2-nitrofenylo)-, ester dimetylowy, C17H18N2O6 i ma wzór strukturalny:
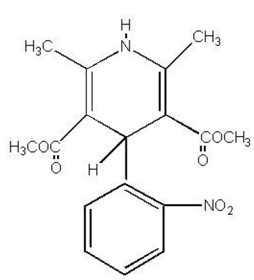
Nifedypina jest żółtą substancją krystaliczną, praktycznie nierozpuszczalną w wodzie, ale rozpuszczalną w etanolu. Ma masę cząsteczkową 346,3. Kapsułki PROCARDIA mają postać miękkich kapsułek żelatynowych do podawania doustnego, z których każda zawiera 10 mg nifedypiny.
Składnikami obojętnymi w preparacie są: gliceryna; olej miętowy; glikol polietylenowy; miękkie kapsułki żelatynowe (zawierające żółty 6 i mogą zawierać czerwony tlenek żelaza i inne składniki obojętne); i woda. Kapsułki 10 mg zawierają również sól sodową sacharyny.
WSKAZANIA
Angina naczynioskurczowa
PROCARDIA (nifedypina) jest wskazana w leczeniu dusznicy bolesnej naczynioskurczowej potwierdzonej jednym z następujących kryteriów: 1) klasyczny typ dusznicy bolesnej w spoczynku z uniesieniem odcinka ST, 2) dusznica bolesna lub skurcz tętnicy wieńcowej wywołany przez ergonowinę lub 3) potwierdzona angiograficznie skurcz tętnicy wieńcowej. U tych pacjentów, u których wykonano angiografię, obecność znacznej utrwalonej choroby obturacyjnej nie jest niezgodna z rozpoznaniem dławicy naczynioskurczowej, pod warunkiem, że spełnione są powyższe kryteria. PROCARDIA 30 mg może być również stosowana, gdy obraz kliniczny sugeruje możliwy komponent naczynioskurczowy, ale gdy skurcz naczyń nie został potwierdzony, np. gdy ból ma zmienny próg podczas wysiłku lub gdy dławica piersiowa jest oporna na azotany i/lub odpowiednie dawki beta-adrenolityków.
Przewlekła stabilna dławica piersiowa (klasyczna dławica piersiowa związana z wysiłkiem)
PROCARDIA 30 mg jest wskazana w leczeniu przewlekłej stabilnej dławicy piersiowej (dławicy wysiłkowej) bez objawów skurczu naczyń u pacjentów, u których objawy utrzymują się pomimo odpowiednich dawek beta-adrenolityków i/lub azotanów organicznych lub którzy nie tolerują tych leków.
W przewlekłej stabilnej dławicy piersiowej (dławica piersiowa związana z wysiłkiem) PROCARDIA okazała się skuteczna w kontrolowanych badaniach trwających do ośmiu tygodni w zmniejszaniu częstości dławicy piersiowej i zwiększaniu tolerancji wysiłku, ale potwierdzenie trwałej skuteczności i oceny długoterminowego bezpieczeństwa u tych pacjentów jest niekompletne. .
Kontrolowane badania przeprowadzone na niewielkiej liczbie pacjentów sugerują, że jednoczesne stosowanie produktu PROCARDIA 30 mg i beta-adrenolityków może być korzystne u pacjentów z przewlekłą stabilną dławicą piersiową, ale dostępne informacje nie są wystarczające, aby z pewnością przewidzieć skutki jednoczesnego leczenia, zwłaszcza u pacjentów z upośledzoną czynnością lewej komory lub zaburzenia przewodzenia w sercu. Przy wprowadzaniu takiej terapii skojarzonej należy uważnie monitorować ciśnienie krwi, ponieważ połączone działanie leków może spowodować ciężkie niedociśnienie. (Widzieć OSTRZEŻENIA .)
DAWKOWANIE I SPOSÓB PODAWANIA
Dawkę produktu PROCARDIA 30 mg potrzebną do zahamowania dusznicy bolesnej, która może być tolerowana przez pacjenta, należy ustalić poprzez dostosowanie dawki. Nadmierne dawki mogą powodować niedociśnienie.
Leczenie należy rozpocząć od kapsułki 10 mg. Dawka początkowa to jedna kapsułka 10 mg, połykana w całości, 3 razy dziennie. Zwykle skuteczny zakres dawek wynosi 10–20 mg trzy razy na dobę. Niektórzy pacjenci, zwłaszcza ci z objawami skurczu tętnicy wieńcowej, reagują tylko na wyższe dawki, częstsze podawanie lub jedno i drugie. U takich pacjentów skuteczne mogą być dawki 20–30 mg trzy lub cztery razy dziennie. Dawki powyżej 120 mg na dobę są rzadko konieczne. Nie zaleca się więcej niż 180 mg dziennie.
W większości przypadków miareczkowanie PROCARDIA powinno trwać 7–14 dni, tak aby lekarz mógł ocenić odpowiedź na każdy poziom dawki i monitorować ciśnienie krwi przed przejściem do wyższych dawek.
Jeżeli objawy to uzasadniają, miareczkowanie może przebiegać szybciej, pod warunkiem częstej oceny pacjenta. W zależności od poziomu aktywności fizycznej pacjenta, częstości napadów i podjęzykowego spożycia nitrogliceryny, dawkę preparatu PROCARDIA 30 mg można zwiększyć z 10 mg 3xdz do 20 mg 3xdz, a następnie do 30 mg 3xdz. przez okres trzech dni.
U hospitalizowanych pacjentów pod ścisłą obserwacją dawkę można zwiększać o 10 mg w okresach od czterech do sześciu godzin, w celu opanowania bólu i arytmii spowodowanych niedokrwieniem. Pojedyncza dawka rzadko powinna przekraczać 30 mg.
Należy unikać jednoczesnego podawania nifedypiny z sokiem grejpfrutowym (patrz FARMAKOLOGIA KLINICZNA oraz INTERAKCJE Z LEKAMI ).
Nie zaobserwowano „efektu z odbicia” po odstawieniu produktu PROCARDIA. Jeśli jednak konieczne jest przerwanie stosowania produktu PROCARDIA, zgodnie z dobrą praktyką kliniczną dawkę należy zmniejszać stopniowo pod ścisłą kontrolą lekarza.
Jednoczesne podawanie z innymi lekami przeciwdławicowymi
Podjęzykową nitroglicerynę można stosować w razie potrzeby w celu opanowania ostrych objawów dusznicy bolesnej, szczególnie podczas miareczkowania produktu PROCARDIA. Widzieć INTERAKCJE Z LEKAMI , w celu uzyskania informacji na temat równoczesnego podawania produktu PROCARDIA 30 mg z beta-adrenolitykami lub długo działającymi azotanami.
JAK DOSTARCZONE
PROCARDIA miękkie kapsułki żelatynowe dostarczane są w:
Butelki po 100: 10 mg ( NDC 0069-2600-66)
Kapsułki należy chronić przed światłem i wilgocią oraz przechowywać w kontrolowanej temperaturze pokojowej, od 15 do 25°C, w oryginalnym opakowaniu producenta.
Dystrybutor: Pfizer Labs, Oddział Pfizer Inc, NY, NY 10017. Aktualizacja: lipiec 2016
SKUTKI UBOCZNE
W amerykańskich i zagranicznych kontrolowanych badaniach z wielokrotnymi dawkami, w których działania niepożądane zgłaszano spontanicznie, działania niepożądane występowały często, ale na ogół nie były poważne i rzadko wymagały przerwania leczenia lub dostosowania dawki. Większość z nich była oczekiwanymi konsekwencjami działań rozszerzających naczynia krwionośne produktu PROCARDIA.
Istnieje również duże niekontrolowane doświadczenie u ponad 2100 pacjentów w Stanach Zjednoczonych. Większość pacjentów cierpiała na naczynioskurczową lub oporną dusznicę bolesną, a około połowa otrzymywała jednocześnie leki blokujące receptory beta-adrenergiczne. Najczęstszymi zdarzeniami niepożądanymi były:
Zapadalność Około 10%
Układ sercowo-naczyniowy: obrzęk obwodowy
Ośrodkowy układ nerwowy: zawroty głowy lub oszołomienie
Przewód pokarmowy: mdłości
Systemowe: ból głowy i uderzenia gorąca, osłabienie
Zapadalność Około 5%
Układ sercowo-naczyniowy: przemijające niedociśnienie
Częstość występowania 2% lub mniej
Układ sercowo-naczyniowy: palpitacja
Oddechowy: przekrwienie nosa i klatki piersiowej, duszność
Przewód pokarmowy: biegunka, zaparcia, skurcze, wzdęcia
Układ mięśniowo-szkieletowy: stany zapalne, sztywność stawów, skurcze mięśni
Ośrodkowy układ nerwowy: drżenie, nerwowość, roztrzęsienie, zaburzenia snu, niewyraźne widzenie, zaburzenia równowagi
Inny: zapalenie skóry, świąd, pokrzywka, gorączka, pocenie się, dreszcze, trudności seksualne
Częstość występowania Około 0,5%
Układ sercowo-naczyniowy: omdlenie (głównie po podaniu dawki początkowej i (lub) zwiększeniu dawki), erytromelalgia
Częstość występowania mniejsza niż 0,5%
Hematologiczny: małopłytkowość, niedokrwistość, leukopenia, plamica
Przewód pokarmowy: alergiczne zapalenie wątroby
Twarz i gardło: obrzęk naczynioruchowy (u kilku pacjentów głównie obrzęk jamy ustnej i gardła z trudnościami w oddychaniu), przerost dziąseł
OUN: depresja, zespół paranoidalny
Zmysły specjalne: przejściowa ślepota na szczycie poziomu w osoczu, szum w uszach
Układ moczowo-płciowy: nokturia, wielomocz
Inny: zapalenie stawów z ANA (+), złuszczające zapalenie skóry, ginekomastia
Układ mięśniowo-szkieletowy: bóle mięśniowe
Kilka z tych działań niepożądanych wydaje się być związanych z dawką. Obrzęki obwodowe wystąpiły u około jednego na 25 pacjentów przy dawkach mniejszych niż 60 mg dziennie iu około jednego pacjenta na ośmiu przy dawce 120 mg dziennie lub większej. Przemijające niedociśnienie, zazwyczaj o nasileniu łagodnym do umiarkowanego i rzadko wymagające przerwania leczenia, wystąpiło u jednego z 50 pacjentów przy dawce mniejszej niż 60 mg na dobę iu jednego z 20 pacjentów przy dawce 120 mg na dobę lub większej.
Bardzo rzadko wprowadzenie produktu PROCARDIA 30 mg wiązało się z nasileniem bólu dławicowego, prawdopodobnie z powodu związanego z tym niedociśnienia. Wystąpiła również przejściowa jednostronna utrata wzroku.
Ponadto zaobserwowano poważniejsze zdarzenia niepożądane, których nie można łatwo odróżnić od naturalnego przebiegu choroby u tych pacjentów. Pozostaje jednak możliwe, że niektóre lub wiele z tych zdarzeń było związanych z narkotykami. Zawał mięśnia sercowego wystąpił u około 4% pacjentów, a zastoinowa niewydolność serca lub obrzęk płuc u około 2%. Arytmie komorowe lub zaburzenia przewodzenia występowały u mniej niż 0,5% pacjentów.
W podgrupie ponad 1000 pacjentów otrzymujących produkt PROCARDIA 30 mg z równoczesnym leczeniem beta-adrenolitykami wzór i częstość występowania działań niepożądanych nie różniły się od tych w całej grupie pacjentów leczonych produktem PROCARDIA (nifedypina). (Widzieć ŚRODKI OSTROŻNOŚCI .)
podgrupie około 250 pacjentów z rozpoznaną zastoinową niewydolnością serca i dusznicą bolesną (około 10% całej populacji pacjentów) zawroty głowy lub oszołomienie, obrzęki obwodowe, bóle głowy lub uderzenia gorąca wystąpiły u jednego na ośmiu pacjentów. Niedociśnienie wystąpiło u około jednego na 20 pacjentów. Omdlenie wystąpiło u około jednego pacjenta na 250. Zawał mięśnia sercowego lub objawy zastoinowej niewydolności serca wystąpiły u około jednego pacjenta na 15. Zaburzenia rytmu przedsionkowego lub komorowego wystąpiły u około jednego pacjenta na 150.
Po wprowadzeniu produktu do obrotu rzadko zgłaszano przypadki złuszczającego zapalenia skóry wywołanego przez nifedypinę. Odnotowano rzadkie przypadki złuszczających lub pęcherzowych działań niepożądanych skóry (takich jak rumień wielopostaciowy, zespół Stevensa-Johnsona i toksyczne martwicze oddzielanie się naskórka) oraz reakcje nadwrażliwości na światło. Zgłaszano również ostrą uogólnioną osutka krostkowa.
INTERAKCJE Z LEKAMI
Beta-adrenergiczne środki blokujące
(Widzieć WSKAZANIA I ZASTOSOWANIE oraz OSTRZEŻENIA .) Doświadczenie u ponad 1400 pacjentów w nieporównawczym badaniu klinicznym wykazało, że jednoczesne podawanie produktu PROCARDIA 30 mg i beta-adrenolityków jest zwykle dobrze tolerowane, ale istnieją sporadyczne doniesienia w piśmiennictwie sugerujące, że połączenie może zwiększać prawdopodobieństwo zastoinowej niewydolności serca, ciężkie niedociśnienie lub zaostrzenie dławicy piersiowej.
Azotany długodziałające
PROCARDIA 30 mg może być bezpiecznie podawana razem z azotanami, ale nie przeprowadzono kontrolowanych badań oceniających skuteczność przeciwdławicową tej kombinacji.
Naparstnica
Ponieważ istnieją pojedyncze doniesienia o pacjentach z podwyższonym poziomem digoksyny i ponieważ istnieje możliwość interakcji między digoksyną i nifedypiną, zaleca się monitorowanie poziomu digoksyny podczas rozpoczynania, dostosowywania i kończenia leczenia nifedypiną, aby uniknąć możliwej nadmiernej lub niedostatecznej digitalizacji .
Chinidyna
Istnieją rzadkie doniesienia o interakcji chinidyny i nifedypiny (ze zmniejszonym stężeniem chinidyny w osoczu).
Antykoagulanty kumaryny
Rzadko zgłaszano przypadki wydłużenia czasu protrombinowego u pacjentów przyjmujących leki przeciwzakrzepowe z grupy kumaryny, którym podawano produkt PROCARDIA. Jednak związek z terapią PROCARDIA jest niepewny.
Cymetydyna
Badanie z udziałem sześciu zdrowych ochotników wykazało znaczny wzrost szczytowych poziomów nifedypiny w osoczu (80%) i powierzchni pod krzywą (74%) po tygodniowym kursie cymetydyny w dawce 1000 mg na dobę i nifedypiny w dawce 40 mg na dobę. dzień. Ranitydyna powodowała mniejsze, nieistotne wzrosty. W działaniu może pośredniczyć znane hamowanie cymetydyny na wątrobowy cytochrom P-450, układ enzymatyczny prawdopodobnie odpowiedzialny za metabolizm pierwszego przejścia nifedypiny. Jeśli leczenie nifedypiną zostanie rozpoczęte u pacjenta aktualnie otrzymującego cymetydynę, zaleca się ostrożne dostosowywanie dawki.
Nifedypina jest metabolizowana przez CYP3A4. Jednoczesne podawanie nifedypiny z fenytoiną, induktorem CYP3A4, zmniejsza ogólnoustrojową ekspozycję na nifedypinę o około 70%. Należy unikać jednoczesnego podawania nifedypiny z fenytoiną lub jakimkolwiek znanym induktorem CYP3A4 lub rozważyć alternatywne leczenie przeciwnadciśnieniowe.
Inhibitory CYP3A, takie jak flukonazol, itrakonazol, klarytromycyna, erytromycyna, nefazodon, fluoksetyna, sakwinawir, indynawir i nelfinawir, podczas jednoczesnego podawania mogą powodować zwiększenie ekspozycji na nifedypinę. Może być konieczne uważne monitorowanie i dostosowanie dawki; rozważyć rozpoczęcie leczenia nifedypiną od najmniejszej dostępnej dawki, jeśli jest podawana jednocześnie z tymi lekami.
Inne interakcje
Sok grejpfrutowy
Jednoczesne podawanie nifedypiny z sokiem grejpfrutowym powodowało w przybliżeniu podwojenie AUC i Cmax nifedypiny bez zmiany okresu półtrwania. Zwiększone stężenia w osoczu najprawdopodobniej wynikają z zahamowania metabolizmu pierwszego przejścia związanego z CYP 3A4. Unikaj spożywania grejpfruta i soku grejpfrutowego podczas przyjmowania nifedypiny.
OSTRZEŻENIA
Nadmierne niedociśnienie
Chociaż u większości pacjentów działanie hipotensyjne produktu PROCARDIA 30 mg jest umiarkowane i dobrze tolerowane, okazjonalni pacjenci mieli nadmierne i źle tolerowane niedociśnienie. Odpowiedzi te występowały zwykle podczas początkowego zwiększania dawki lub podczas późniejszego zwiększania dawki. Chociaż pacjenci rzadko doświadczali nadmiernego niedociśnienia podczas stosowania samego produktu PROCARDIA 30 mg, może ono występować częściej u pacjentów leczonych jednocześnie beta-adrenolitykami. Chociaż produkt PROCARDIA i inne kapsułki nifedypiny o natychmiastowym uwalnianiu nie zostały zatwierdzone do tego celu, były stosowane (doustnie i podjęzykowo) w celu ostrego obniżenia ciśnienia krwi. Kilka dobrze udokumentowanych doniesień opisuje przypadki głębokiego niedociśnienia, zawału mięśnia sercowego i zgonu, gdy stosowano w ten sposób nifedypinę o natychmiastowym uwalnianiu. Kapsułek PROCARDIA nie należy stosować do ostrego obniżenia ciśnienia krwi.
pacjentów otrzymujących produkt PROCARDIA 30 mg w skojarzeniu z beta-adrenolitykiem, którzy przeszli operację pomostowania tętnic wieńcowych z zastosowaniem znieczulenia w dużych dawkach fentanylem, zgłaszano ciężkie niedociśnienie i (lub) zwiększone zapotrzebowanie na płyny. Wydaje się, że interakcja z wysokimi dawkami fentanylu wynika ze skojarzenia leku PROCARDIA i beta-blokera, ale nie można wykluczyć możliwości, że może wystąpić w przypadku samego leku PROCARDIA 30 mg, z małymi dawkami fentanylu, podczas innych zabiegów chirurgicznych lub z innymi narkotycznymi lekami przeciwbólowymi. wykluczone. U pacjentów leczonych produktem PROCARDIA, u których rozważany jest zabieg chirurgiczny z zastosowaniem znieczulenia w dużych dawkach fentanylu, lekarz powinien zdawać sobie sprawę z tych potencjalnych problemów i, jeśli pozwala na to stan pacjenta, należy odczekać (co najmniej 36 godzin) na wypłukanie produktu PROCARDIA 30 mg z produktu PROCARDIA. ciało przed operacją.
Zwiększona dławica piersiowa i/lub zawał mięśnia sercowego
Rzadko u pacjentów, zwłaszcza z ciężką obturacyjną chorobą wieńcową, po rozpoczęciu podawania produktu PROCARDIA w dawce 30 mg lub w momencie zwiększania dawki rozwinęła się dobrze udokumentowana zwiększona częstość, czas trwania i/lub nasilenie dławicy piersiowej lub ostrego zawału mięśnia sercowego. Mechanizm tego efektu nie jest ustalony.
W kilku dobrze kontrolowanych, randomizowanych badaniach oceniano stosowanie nifedypiny o natychmiastowym uwalnianiu u pacjentów, którzy właśnie przebyli utrwalony zawał mięśnia sercowego. W żadnym z tych badań nie wydaje się, aby nifedypina o natychmiastowym uwalnianiu przynosiła jakiekolwiek korzyści. W niektórych badaniach u pacjentów otrzymujących nifedypinę o natychmiastowym uwalnianiu wyniki były znacznie gorsze niż u pacjentów otrzymujących placebo. Kapsułek PROCARDIA 30 mg nie należy podawać w ciągu pierwszego tygodnia lub dwóch po zawale mięśnia sercowego, a także należy ich unikać w przypadku ostrego zespołu wieńcowego (kiedy zawał może być nieuchronny).
Stosowanie w samoistnym nadciśnieniu
PROCARDIA 30 mg i inne kapsułki nifedypiny o natychmiastowym uwalnianiu były również stosowane do długoterminowej kontroli nadciśnienia pierwotnego, chociaż kapsułki PROCARDIA 30 mg nie zostały zatwierdzone do tego celu i nie przeprowadzono odpowiednio kontrolowanych badań w celu określenia odpowiedniej dawki lub odstępu między dawkami do takiego leczenia. Kapsułek PROCARDIA 30 mg nie należy stosować do kontroli nadciśnienia pierwotnego.
Wycofanie beta-blokerów
pacjentów, którzy niedawno odstawili beta-adrenolityki, może rozwinąć się zespół odstawienia z nasiloną dusznicą bolesną, prawdopodobnie związany ze zwiększoną wrażliwością na katecholaminy. Rozpoczęcie leczenia PROCARDIA 30 mg nie zapobiegnie temu zjawisku i można się spodziewać, że zaostrzy je poprzez wywołanie odruchowego uwalniania katecholamin. Istnieją sporadyczne doniesienia o nasileniu dławicy piersiowej w sytuacji odstawienia beta-adrenolityka i rozpoczęcia stosowania produktu PROCARDIA. Jeśli to możliwe, ważne jest zmniejszanie dawki beta-adrenolityków, zamiast ich nagłego odstawiania przed rozpoczęciem stosowania leku PROCARDIA.
Zastoinowa niewydolność serca
Rzadko u pacjentów, zwykle otrzymujących beta-adrenolityki, po rozpoczęciu stosowania produktu PROCARDIA rozwinęła się niewydolność serca. Pacjenci z napiętym zwężeniem aorty mogą być bardziej narażeni na takie zdarzenie, ponieważ można oczekiwać, że efekt odciążający produktu PROCARDIA 30 mg będzie dla nich mniej korzystny ze względu na ich stałą impedancję przepływu przez zastawkę aortalną.
ŚRODKI OSTROŻNOŚCI
Ogólny
Niedociśnienie
Ponieważ PROCARDIA zmniejsza obwodowy opór naczyniowy, zaleca się uważne monitorowanie ciśnienia krwi podczas pierwszego podawania i dostosowywanie dawki produktu PROCARDIA 30 mg. Dokładna obserwacja jest szczególnie zalecana w przypadku pacjentów już przyjmujących leki, o których wiadomo, że obniżają ciśnienie krwi. (Widzieć OSTRZEŻENIA .)
Obrzęki obwodowe
U około jednego na dziesięciu pacjentów leczonych produktem PROCARDIA (nifedypina) występuje łagodny do umiarkowanego obrzęk obwodowy, zwykle związany z rozszerzeniem naczyń tętniczych, a nie z powodu dysfunkcji lewej komory. Ten obrzęk występuje głównie w kończynach dolnych i zwykle reaguje na leczenie moczopędne. W przypadku pacjentów, u których dławica piersiowa jest powikłana zastoinową niewydolnością serca, należy zachować ostrożność, aby odróżnić ten obrzęk obwodowy od skutków narastającej dysfunkcji lewej komory.
Testy laboratoryjne
Odnotowano rzadkie, zwykle przemijające, ale czasami znaczące podwyższenie poziomu enzymów, takich jak fosfataza alkaliczna, CPK, LDH, SGOT i SGPT. Związek z terapią PROCARDIA jest w większości przypadków niepewny, ale w niektórych prawdopodobny. Te nieprawidłowości laboratoryjne rzadko wiązały się z objawami klinicznymi; zgłaszano jednak cholestazę z żółtaczką lub bez. Zgłaszano rzadkie przypadki alergicznego zapalenia wątroby.
PROCARDIA 30mg, podobnie jak inne blokery kanału wapniowego, zmniejsza agregację płytek krwi in vitro. Ograniczone badania kliniczne wykazały umiarkowane, ale statystycznie istotne zmniejszenie agregacji płytek i wydłużenie czasu krwawienia u niektórych pacjentów z produktem PROCARDIA. Uważa się, że jest to funkcja hamowania transportu wapnia przez błonę płytek krwi. Nie wykazano znaczenia klinicznego tych wyników.
Zgłaszano dodatni wynik bezpośredniego testu Coombsa z niedokrwistością hemolityczną lub bez niej, ale nie można było ustalić związku przyczynowego między podaniem produktu PROCARDIA a dodatnim wynikiem tego testu laboratoryjnego, w tym z hemolizą.
Chociaż produkt PROCARDIA 30 mg był bezpiecznie stosowany u pacjentów z zaburzeniami czynności nerek i opisywano, że wywiera korzystny wpływ, w niektórych przypadkach zgłaszano rzadkie, odwracalne zwiększenie stężenia BUN i kreatyniny w surowicy u pacjentów z istniejącą wcześniej przewlekłą niewydolnością nerek. Związek z terapią PROCARDIA jest w większości przypadków niepewny, ale w niektórych prawdopodobny.
rakotwórczość, mutageneza, upośledzenie płodności
Nifedypina była podawana doustnie szczurom przez dwa lata i nie wykazano jej działania rakotwórczego. Podawana szczurom przed kryciem nifedypina powodowała zmniejszenie płodności w dawce około 5-krotnie większej niż maksymalna zalecana dawka u ludzi. W piśmiennictwie istnieje doniesienie o odwracalnym zmniejszeniu zdolności nasienia ludzkiego uzyskanego od ograniczonej liczby niepłodnych mężczyzn przyjmujących zalecane dawki nifedypiny do wiązania się z komórką jajową i zapłodnienia jej in vitro. Badania mutagenności in vivo były negatywne.
Ciąża
Wykazano, że nifedypina powoduje objawy teratogenne u szczurów i królików, w tym anomalie palców podobne do tych zgłaszanych dla fenytoiny. Zgłaszano występowanie anomalii palców u innych przedstawicieli klasy dihydropirydyn i prawdopodobnie są one wynikiem upośledzonego przepływu krwi w macicy. Podawanie nifedypiny wiązało się z różnymi działaniami embriotoksycznymi, łożyskowymi i płodowymi, w tym skarłowaciałymi płodami (szczury, myszy, króliki), deformacjami żeber (myszy), rozszczepem podniebienia (myszy), małymi łożyskami i słabo rozwiniętymi kosmkami kosmówki (małpy), embrionami i zgonów płodów (szczury, myszy, króliki) oraz przedłużoną ciążę/zmniejszoną przeżywalność noworodków (szczury; nie oceniano u innych gatunków). W przeliczeniu na mg/kg, wszystkie dawki związane z teratogennym działaniem embriotoksycznym lub fetotoksycznym u zwierząt były wyższe (5 do 50 razy) niż maksymalna zalecana dawka dla ludzi wynosząca 120 mg/dobę. W przeliczeniu na mg/m² niektóre dawki były wyższe, a inne niższe niż maksymalna zalecana dawka dla ludzi, ale wszystkie mieściły się w zakresie rzędu wielkości. Dawki związane z działaniem toksycznym na łożysko u małp były równoważne lub niższe niż maksymalna zalecana dawka u ludzi wyrażona w mg/m².
Nie ma odpowiednich i dobrze kontrolowanych badań u kobiet w ciąży. PROCARDIA powinna być stosowana w okresie ciąży tylko wtedy, gdy potencjalna korzyść przewyższa potencjalne ryzyko.
Laktacja
Nifedypina przenika do mleka matki. PROCARDIA powinna być stosowana w okresie karmienia piersią tylko wtedy, gdy potencjalna korzyść przewyższa potencjalne ryzyko.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność u pacjentów pediatrycznych nie zostały ustalone. Nie zaleca się stosowania w populacji pediatrycznej.
Zastosowanie geriatryczne
Wydaje się, że wiek ma istotny wpływ na farmakokinetykę nifedypiny. Klirens jest zmniejszony, co skutkuje wyższym AUC u osób w podeszłym wieku. Zmiany te nie są spowodowane zmianami czynności nerek (patrz FARMAKOLOGIA KLINICZNA , Farmakokinetyka ).
PRZEDAWKOWAĆ
Doświadczenie z przedawkowaniem nifedypiny jest ograniczone. Ogólnie rzecz biorąc, przedawkowanie nifedypiny prowadzące do wyraźnego niedociśnienia tętniczego wymaga aktywnego wspomagania układu sercowo-naczyniowego, w tym monitorowania czynności układu krążenia i układu oddechowego, uniesienia kończyn oraz rozsądnego stosowania wlewu wapnia, leków zwiększających ciśnienie i płynów. Oczekuje się, że klirens nifedypiny będzie przedłużony u pacjentów z zaburzeniami czynności wątroby. Ponieważ nifedypina silnie wiąże się z białkami, dializa prawdopodobnie nie przyniesie żadnych korzyści; jednak plazmafereza może być korzystna.
PRZECIWWSKAZANIA
Znana reakcja nadwrażliwości na PROCARDIA.
FARMAKOLOGIA KLINICZNA
PROCARDIA jest inhibitorem napływu jonów wapnia (blokerem wolnego kanału lub antagonistą jonów wapnia) i hamuje przezbłonowy napływ jonów wapnia do mięśnia sercowego i mięśni gładkich. Procesy skurczu mięśnia sercowego i mięśni gładkich naczyń są zależne od przemieszczania się pozakomórkowych jonów wapnia do tych komórek przez określone kanały jonowe. PROCARDIA 30 mg selektywnie hamuje napływ jonów wapnia przez błonę komórkową mięśnia sercowego i mięśni gładkich naczyń bez zmiany stężenia wapnia w surowicy.
Mechanizm akcji
Dokładne środki, za pomocą których to hamowanie łagodzi dusznicę bolesną, nie zostały w pełni określone, ale obejmują co najmniej dwa następujące mechanizmy:
Relaks i zapobieganie skurczowi tętnic wieńcowych
PROCARDIA rozszerza główne tętnice wieńcowe i tętniczki wieńcowe, zarówno w obszarach prawidłowych, jak i niedokrwionych, i jest silnym inhibitorem skurczu tętnic wieńcowych, zarówno samoistnego, jak i wywołanego ergonowiną. Ta właściwość zwiększa dostarczanie tlenu do mięśnia sercowego u pacjentów ze skurczem tętnic wieńcowych i jest odpowiedzialna za skuteczność PROCARDIA 30 mg w dławicy naczynioskurczowej (Prinzmetala lub jej odmiana). Nie jest jasne, czy efekt ten odgrywa jakąkolwiek rolę w klasycznej dławicy piersiowej, ale badania tolerancji wysiłku nie wykazały wzrostu maksymalnego produktu ciśnienia wysiłku, powszechnie akceptowanej miary wykorzystania tlenu. Sugeruje to, że ogólnie złagodzenie skurczu lub rozszerzenie tętnic wieńcowych nie jest ważnym czynnikiem w klasycznej dławicy piersiowej.
Redukcja wykorzystania tlenu
PROCARDIA regularnie obniża ciśnienie tętnicze w spoczynku i na danym poziomie wysiłku, rozszerzając tętniczki obwodowe i zmniejszając całkowity opór obwodowy (obciążenie następcze), na który działa serce. To odciążenie serca zmniejsza zużycie energii przez mięsień sercowy i zapotrzebowanie na tlen i prawdopodobnie odpowiada za skuteczność produktu PROCARDIA w przewlekłej stabilnej dławicy piersiowej.
Farmakokinetyka i metabolizm
PROCARDIA szybko i całkowicie wchłania się po podaniu doustnym. Lek jest wykrywalny w surowicy 10 minut po podaniu doustnym, a maksymalne stężenie we krwi występuje po około 30 minutach. Biodostępność jest proporcjonalna do dawki od 10 do 30 mg; okres półtrwania nie zmienia się znacząco wraz z dawką. Istnieje niewielka różnica we względnej biodostępności, gdy kapsułki PROCARDIA są podawane doustnie i albo połykane w całości, ugryzione i połknięte, albo ugryzione i trzymane podjęzykowo. Jednak przegryzienie kapsułki przed połknięciem powoduje nieco wcześniejsze stężenie w osoczu (27 ng/ml 10 minut po 10 mg) niż w przypadku połknięcia kapsułki w stanie nienaruszonym. PROCARDIA 30mg silnie wiąże się z białkami surowicy. PROCARDIA jest w znacznym stopniu przekształcana do nieaktywnych metabolitów, a około 80% produktu PROCARDIA 30 mg i metabolitów jest wydalane przez nerki. Okres półtrwania w fazie eliminacji nifedypiny wynosi około dwóch godzin. Ponieważ biotransformacja wątrobowa jest główną drogą wydalania nifedypiny, farmakokinetyka może być zmieniona u pacjentów z przewlekłą chorobą wątroby. Pacjenci z zaburzeniami czynności wątroby (marskość wątroby) mają dłuższy okres półtrwania i większą biodostępność nifedypiny niż zdrowi ochotnicy. Stopień wiązania nifedypiny z białkami surowicy jest wysoki (92-98%). Wiązanie z białkami może być znacznie zmniejszone u pacjentów z zaburzeniami czynności nerek lub wątroby.
Po podaniu dożylnym klirens nifedypiny zmniejszył się o 33% u zdrowych osób w podeszłym wieku w porównaniu z młodymi zdrowymi osobami.
Hemodynamika
Podobnie jak inne blokery wolnego kanału, PROCARDIA wywiera ujemny wpływ inotropowy na izolowaną tkankę mięśnia sercowego. Jest to rzadko, jeśli w ogóle, obserwowane u nienaruszonych zwierząt lub ludzi, prawdopodobnie z powodu odruchowych reakcji na jego działanie rozszerzające naczynia krwionośne. U ludzi PROCARDIA 30 mg powoduje zmniejszony opór naczyń obwodowych oraz spadek ciśnienia skurczowego i rozkurczowego, zwykle niewielki (skurczowe 5-10 mm Hg), ale czasami większy. Zwykle występuje niewielki wzrost częstości akcji serca, odruchowa reakcja na rozszerzenie naczyń. Pomiary czynności serca u pacjentów z prawidłową czynnością komór generalnie wykazały niewielki wzrost wskaźnika sercowego bez większego wpływu na frakcję wyrzutową, ciśnienie końcoworozkurczowe lewej komory (LVEDP) lub objętość (LVEDV). U pacjentów z zaburzeniami czynności komór większość ostrych badań wykazała pewien wzrost frakcji wyrzutowej i zmniejszenie ciśnienia napełniania lewej komory.
Efekty elektrofizjologiczne
Chociaż, podobnie jak inne produkty z tej klasy, PROCARDIA zmniejsza czynność węzła zatokowo-przedsionkowego i przewodzenie przedsionkowo-komorowe w izolowanych preparatach mięśnia sercowego, takiego działania nie obserwowano w badaniach na zdrowych zwierzętach ani u ludzi. W oficjalnych badaniach elektrofizjologicznych, głównie u pacjentów z prawidłowym układem przewodzenia, produkt PROCARDIA 30 mg nie wykazywał tendencji do przedłużania przewodzenia przedsionkowo-komorowego, wydłużania czasu powrotu węzła zatokowego ani do spowolnienia rytmu zatokowego.
INFORMACJA O PACJENCIE
Brak informacji. Proszę odnieść się do OSTRZEŻENIA oraz ŚRODKI OSTROŻNOŚCI Sekcje.
