Rhinocort 100mcg Budesonide Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Rhinocort Aqua i jak się go stosuje?
Spray do nosa Rhinocort Aqua (budezonid) to steryd stosowany w leczeniu objawów ze strony nosa, takich jak przekrwienie, kichanie i katar spowodowany sezonowymi lub całorocznymi alergiami. Spray do nosa Rhinocort Aqua jest również stosowany do zapobiegania nawrotom polipów nosa po usunięciu chirurgicznym.
Jakie są skutki uboczne Rhinocort 100mcg Aqua?
Częste działania niepożądane aerozolu do nosa Rhinocort Aqua obejmują:
- suchość lub podrażnienie nosa/gardła,
- ból gardła,
- kaszel,
- kichanie,
- krwotok z nosa,
- nieprzyjemny smak/zapach,
- owrzodzenia lub białe plamy wewnątrz lub wokół nosa, lub
- ból, obrzęk, pieczenie, swędzenie lub podrażnienie wokół nosa.
Należy poinformować lekarza, jeśli wystąpią rzadkie, ale poważne działania niepożądane po zastosowaniu aerozolu do nosa Rhinocort Aqua, w tym:
- utrata smaku lub zapachu, lub
- ból lub rany w nosie.
OPIS
Budesonid, aktywny składnik preparatu RHINOCORT AQUA (budezonid) w aerozolu do nosa, jest syntetycznym kortykosteroidem o działaniu przeciwzapalnym.
Jest oznaczony chemicznie jako (RS)-11-beta,16-alfa,17,21-tetrahydroksypregna-1,4-dieno-3,20-dion cykliczny 16,17-acetal z aldehydem masłowym.
Budezonid jest dostarczany jako mieszanina dwóch epimerów (22R i 22S).
Empiryczny wzór budezonidu to C25H34O6, a jego masa cząsteczkowa wynosi 430,5.
Jego wzór strukturalny to:
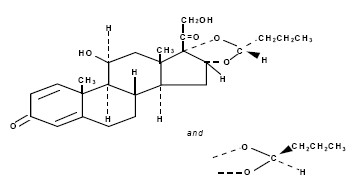
Budezonid jest białym lub prawie białym, bezwonnym proszkiem, który jest praktycznie nierozpuszczalny w wodzie i heptanie, słabo rozpuszczalny w etanolu i swobodnie rozpuszczalny w chloroformie.
Jego współczynnik podziału między oktanol i wodę przy pH 5 wynosi 1,6 x103.
RHINOCORT AQUA (budezonid) aerozol do nosa jest bezzapachowym preparatem do rozpylania z odmierzaną dawką, zawierającym zmikronizowaną zawiesinę budezonidu w środowisku wodnym. Pożywka zawiera celulozę mikrokrystaliczną i sól sodową karboksymetylocelulozy, dekstrozę bezwodną, polisorbat 80, wersenian disodowy, sorbinian potasu i wodę oczyszczoną; dodaje się kwas chlorowodorowy w celu dostosowania pH do docelowej wartości 4,5.
RHINOCORT 100mcg AQUA Nasal Spray dostarcza 32 mcg budezonidu na spray.
Każda butelka RHINOCORT 100 mcg AQUA (budezonid) aerozol do nosa 32 mcg zawiera 120 dozowanych rozpyleń po wstępnym przygotowaniu.
Przed pierwszym użyciem pojemnik należy delikatnie wstrząsnąć, a pompę należy zalać, uruchamiając osiem razy. W przypadku codziennego użytku pompy nie trzeba ponownie przygotowywać. Jeśli nie jest używany przez dwa kolejne dni, ponownie spryskaj jednym rozpyleniem lub do momentu pojawienia się drobnego rozpylenia. W przypadku nieużywania przez ponad 14 dni, spłucz aplikator i wykonaj dwa rozpylenia lub do momentu pojawienia się drobnego mgiełki.
WSKAZANIA
Leczenie sezonowego lub całorocznego alergicznego nieżytu nosa
RHINOCORT AQUA (budezonid) aerozol do nosa jest wskazany w leczeniu objawów ze strony nosa sezonowego lub całorocznego alergicznego nieżytu nosa u dorosłych i dzieci w wieku sześciu lat i starszych.
DAWKOWANIE I SPOSÓB PODAWANIA
Zalecana dawka początkowa dla dorosłych i dzieci w wieku 6 lat i starszych wynosi 64 mikrogramy na dobę podawane jako jedno rozpylenie do nozdrza RHINOCORT AQUA (budezonid) aerozol do nosa 32 mikrogramy raz na dobę. Niektórzy pacjenci, którzy nie osiągają kontroli objawów przy zalecanej dawce początkowej, mogą odnieść korzyść ze zwiększonej dawki. Maksymalna zalecana dawka dla dorosłych (w wieku 12 lat i starszych) wynosi 256 µg na dobę, podawana w postaci czterech rozpyleń do nozdrza raz na dobę RHINOCORT AQUA (budezonid) aerozol do nosa 32 µg, a maksymalna zalecana dawka dla pacjentów pediatrycznych (6 do
Zawsze pożądane jest miareczkowanie indywidualnego pacjenta do minimalnej skutecznej dawki, aby zmniejszyć możliwość wystąpienia działań niepożądanych. Poprawę objawów ze strony nosa można zauważyć u pacjentów w ciągu 10 godzin od pierwszego zastosowania leku RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa, jednak poprawa kliniczna trwa zwykle od 1 do 2 dni, a maksymalne korzyści po około 2 tygodniach. Gdy osiągnięto maksymalne korzyści i opanowano objawy, zmniejszenie dawki może być skuteczne w utrzymaniu kontroli objawów alergicznego nieżytu nosa u pacjentów, których początkowo kontrolowano przy wyższych dawkach.
Przed pierwszym użyciem pojemnik należy delikatnie wstrząsnąć, a pompę należy zalać, uruchamiając osiem razy. W przypadku codziennego użytku pompy nie trzeba ponownie przygotowywać. Jeśli nie jest używany przez dwa kolejne dni, ponownie spryskaj jednym rozpyleniem lub do momentu pojawienia się drobnego rozpylenia. W przypadku nieużywania przez ponad 14 dni, spłucz aplikator i wykonaj dwa rozpylenia lub do momentu pojawienia się drobnego mgiełki. Przed każdym użyciem delikatnie wstrząsnąć pojemnikiem.
Ilustrowany Instrukcja użytkowania dla pacjenta dołączyć do każdego opakowania RHINOCORT AQUA (budezonid) aerozol do nosa 32 mcg.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
RHINOCORT AQUA (budezonid) aerozol do nosa jest zawiesiną aerozolu do nosa. Każdy spray dostarcza 32 mcg budezonidu. Każda butelka RHINOCORT 100 mcg AQUA (budezonid) aerozol do nosa 32 mcg zawiera 120 dozowanych rozpyleń po wstępnym przygotowaniu.
RHINOCORT 100mcg AQUA (budezonid) Aerozol do nosa 32mcg jest dostępny w butelce ze szkła oranżowego z rozpylaczem z dozownikiem i zieloną nasadką ochronną. RHINOCORT 100mcg AQUA (budezonid) Aerozol do nosa 32mcg ( NDC 0186-1070-08) zapewnia 120 dozowanych rozpyleń po wstępnym zagruntowaniu; masa netto wypełnienia 8,6 g. Butelka RHINOCORT 100 mcg AQUA (budezonid) aerozol do nosa 32 mcg została napełniona nadmiarem, aby zapewnić działanie inicjujące. Butelkę należy wyrzucić po 120 rozpyleniach po początkowym przygotowaniu, ponieważ ilość budezonidu dostarczana później na rozpylenie może być znacznie mniejsza niż dawka na etykiecie. Każde rozpylenie dostarcza pacjentowi 32 mcg budezonidu.
RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa należy przechowywać w kontrolowanej temperaturze pokojowej, 20 do 25°C (68 do 77°F) z zaworem do góry. Nie zamrażać. Chronić przed światłem. Delikatnie wstrząsnąć przed użyciem. Nie spryskiwać oczu.
Dystrybucja: AstraZeneca LP, Wilmington, DE 19850. Wersja: 12/2010
SKUTKI UBOCZNE
Stosowanie kortykosteroidów ogólnoustrojowo i donosowo może skutkować:
- Krwawienie z nosa, zakażenie Candida albicans, perforacja przegrody nosowej i zaburzenia gojenia ran [patrz OSTRZEŻENIA I ŚRODKI ].
- Nadwrażliwość, w tym anafilaksja [patrz OSTRZEŻENIA I ŚRODKI ].
- Immunosupresja [patrz OSTRZEŻENIA I ŚRODKI ].
- Hiperkortyka i zahamowanie czynności kory nadnerczy [patrz OSTRZEŻENIA I ŚRODKI ].
- Efekt wzrostu [patrz OSTRZEŻENIA I ŚRODKI oraz Stosowanie w określonych populacjach ].
- Jaskra i zaćma [patrz OSTRZEŻENIA I ŚRODKI ].
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Częstość występowania częstych działań niepożądanych w Tabeli 1 jest oparta na dwóch amerykańskich i pięciu nieamerykańskich kontrolowanych badaniach klinicznych z udziałem 1526 pacjentów z sezonowym lub całorocznym nieżytem nosa u dorosłych i dzieci w wieku ≥ 6 lat leczonych produktem RHINOCORT AQUA (budezonid) w aerozolu do nosa w dawkach do 400 mcg raz dziennie przez 3-6 tygodni. Populacja ta obejmowała 745 kobiet i 781 mężczyzn w średnim wieku 31 lat (zakres 6-85 lat, 349 to 6
Podobny profil działań niepożądanych zaobserwowano w podgrupie dzieci w wieku od 6 do 12 lat. Ci pacjenci są uwzględnieni w Tabeli 1.
Dwa do trzech procent (2-3%) pacjentów biorących udział w badaniach klinicznych przerwało leczenie z powodu działań niepożądanych. Podczas kontrolowanych badań klinicznych produktu RHINOCORT AQUA (budezonid) aerozol do nosa nie zgłaszano ogólnoustrojowych działań niepożądanych kortykosteroidów.
W przypadku przekroczenia zalecanych dawek lub jeśli osoby są szczególnie wrażliwe, mogą wystąpić objawy hiperkortycyzmu, tj. zespół Gushinga i zahamowanie czynności kory nadnerczy.
Doświadczenie postmarketingowe
Następujące działania niepożądane zgłaszano po zatwierdzeniu produktu RHINOCORT AQUA (budezonid) aerozol do nosa. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Zaburzenia układu immunologicznego: natychmiastowe i opóźnione reakcje nadwrażliwości (w tym reakcja anafilaktyczna, pokrzywka, wysypka, zapalenie skóry, obrzęk naczynioruchowy i świąd), [patrz OSTRZEŻENIA I ŚRODKI oraz PRZECIWWSKAZANIA ]
Zaburzenia oka: jaskra, podwyższone ciśnienie śródgałkowe, zaćma [patrz OSTRZEŻENIA I ŚRODKI ]
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia: perforacja przegrody nosowej, anosmia, zaburzenia gardła (podrażnienie gardła, ból gardła, obrzęk gardła, pieczenie i swędzenie gardła) i świszczący oddech
Zaburzenia serca: kołatanie serca
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej: zahamowanie wzrostu [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ]
INTERAKCJE Z LEKAMI
Inhibitory cytochromu P450 3A4
Główną drogą metabolizmu kortykosteroidów, w tym budezonidu, jest izoenzym 3A4 (CYP3A4) cytochromu P450 (CYP). Po podaniu doustnym ketokonazolu, silnego inhibitora CYP3A4, wzrosło średnie stężenie budezonidu podawanego doustnie. Jednoczesne podawanie CYP3A4 może hamować metabolizm i zwiększać ogólnoustrojową ekspozycję na budezonid. Należy zachować ostrożność rozważając jednoczesne podanie preparatu RHINOCORT AQUA (budezonid) aerozol do nosa z długotrwałym ketokonazolem i innymi znanymi silnymi inhibitorami CYP3A4 (np. rytonawir, klarytromycyna atazanawiru, indynawir itrakonazol, nefazodon, nelfinawir-sakwinawir) [patrz OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Lokalne efekty nosowe
Krwawienie z nosa
W badaniach klinicznych trwających od 3 do 52 tygodni krwawienie z nosa obserwowano częściej u pacjentów leczonych produktem RHINOCORT 100 mcg AQUA (budezonid) aerozol do nosa niż u pacjentów otrzymujących placebo [patrz DZIAŁANIA NIEPOŻĄDANE ].
Zakażenie Candida
badaniach klinicznych z budezonidem podawanym donosowo wystąpił rozwój miejscowych zakażeń nosa i gardła wywołanych przez Candida albicans. W przypadku rozwoju takiego zakażenia może być konieczne zastosowanie odpowiedniego leczenia miejscowego lub ogólnoustrojowego oraz przerwanie leczenia preparatem RHINOCORT AQUA (budezonid) w aerozolu do nosa. Pacjenci stosujący RHINOCORT AQUA (budezonid) aerozol do nosa przez kilka miesięcy lub dłużej powinni być okresowo badani pod kątem obecności infekcji Candida lub innych objawów niepożądanych działań na błonę śluzową nosa.
Perforacja przegrody nosowej
Zgłaszano przypadki perforacji przegrody nosowej po donosowym podaniu kortykosteroidów, w tym budezonidu [patrz DZIAŁANIA NIEPOŻĄDANE ].
Upośledzone gojenie się ran
Ze względu na hamujący wpływ kortykosteroidów na gojenie ran, pacjenci, którzy niedawno przeszli owrzodzenie przegrody nosowej, operację nosa lub uraz nosa, nie powinni stosować kortykosteroidów donosowych do czasu zagojenia.
Reakcje nadwrażliwości, w tym anafilaksja
Mogą wystąpić reakcje nadwrażliwości, w tym reakcja anafilaktyczna, pokrzywka, wysypka, zapalenie skóry, obrzęk naczynioruchowy i świąd [patrz PRZECIWWSKAZANIA oraz REAKCJE NIEPOŻĄDANE, Doświadczenie postmarketingowe ].
Immunosupresja
Pacjenci przyjmujący leki hamujące układ odpornościowy są bardziej podatni na infekcje niż osoby zdrowe. Na przykład ospa wietrzna i odra mogą mieć bardziej poważny, a nawet śmiertelny przebieg u podatnych dzieci lub dorosłych stosujących kortykosteroidy. W przypadku takich dzieci lub osób dorosłych, które nie miały tych chorób lub nie zostały odpowiednio zaszczepione, należy zachować szczególną ostrożność, aby uniknąć narażenia. Nie wiadomo, w jaki sposób dawka, droga i czas podawania kortykosteroidów wpływają na ryzyko rozwoju rozsianego zakażenia. Nie jest również znany wpływ choroby podstawowej i/lub wcześniejszego leczenia kortykosteroidami na ryzyko. W przypadku narażenia na ospę wietrzną wskazane może być leczenie immunoglobulinami przeciwko ospie wietrznej i półpaścowi (VZIG) lub połączonymi immunoglobulinami dożylnymi (WIG). W przypadku narażenia na odrę, może być wskazana profilaktyka za pomocą połączonej domięśniowej immunoglobuliny (IG). (Widzieć odpowiednie ulotki informacyjne zawierające pełne informacje dotyczące przepisywania leków VZIG i IG ). Jeśli rozwinie się ospa wietrzna, można rozważyć leczenie środkami przeciwwirusowymi.
Nie badano klinicznego przebiegu ospy wietrznej lub odry u pacjentów leczonych kortykosteroidami donosowymi lub wziewnymi. Chociaż nie ma danych dotyczących donosowych kortykosteroidów, w badaniu klinicznym oceniano odpowiedź immunologiczną na szczepionkę przeciwko ospie wietrznej u pacjentów z astmą w wieku od 12 miesięcy do 8 lat, którzy byli leczeni budezonidem w postaci zawiesiny do inhalacji.
Otwarte, nierandomizowane badanie kliniczne oceniało odpowiedź immunologiczną na szczepionkę przeciwko ospie wietrznej u 243 pacjentów z astmą w wieku od 12 miesięcy do 8 lat, którzy byli leczeni budezonidem w postaci zawiesiny do inhalacji w dawce 0,25 mg do 1 mg na dobę (n=151) lub na astmę bez kortykosteroidów (n=92) (tj. betai-agoniści, antagoniści receptora leukotrienowego lub kromony). Odsetek pacjentów, u których wystąpiło miano przeciwciał seroprotekcyjnych ≥ 5,0 (wartość gpELISA) w odpowiedzi na szczepienie, był podobny u pacjentów leczonych budezonidem w postaci zawiesiny do inhalacji (85%) w porównaniu z pacjentami leczonymi astmą bez kortykosteroidów (90%). U żadnego pacjenta leczonego budezonidem w postaci zawiesiny do inhalacji nie rozwinęła się ospa wietrzna w wyniku szczepienia.
Kortykosteroidy należy stosować ostrożnie, jeśli w ogóle, u pacjentów z czynną lub nieaktywną gruźlicą, nieleczonymi zakażeniami grzybiczymi, bakteryjnymi, ogólnoustrojowymi wirusowymi lub pasożytniczymi; lub opryszczka oczna.
Skutki osi podwzgórze-przysadka-nadnercza
Hiperkortyczność i zahamowanie czynności kory nadnerczy: Gdy donosowe steroidy są stosowane w dawkach większych niż zalecane lub u osób podatnych w zalecanych dawkach, mogą wystąpić ogólnoustrojowe efekty kortykosteroidów, takie jak hiperkortyczność i zahamowanie czynności kory nadnerczy. W przypadku wystąpienia takich zmian, dawkowanie preparatu RHINOCORT 100 mcg AQUA (budezonid) aerozol do nosa należy odstawiać powoli, zgodnie z przyjętymi procedurami przerywania doustnego leczenia kortykosteroidami.
Zastąpieniu kortykosteroidu ogólnoustrojowego kortykosteroidem do stosowania miejscowego mogą towarzyszyć objawy niewydolności nadnerczy, a ponadto u niektórych pacjentów mogą wystąpić objawy odstawienia kortykosteroidu, np. ból stawów i/lub mięśni, zmęczenie, osłabienie, nudności, wymioty, niedociśnienie, zmęczenie i depresja. Pacjenci wcześniej leczeni przez dłuższy czas ogólnoustrojowymi kortykosteroidami powinni być powoli odzwyczajani podczas przechodzenia na miejscowe kortykosteroidy i uważnie monitorowani pod kątem ostrej niewydolności nadnerczy w odpowiedzi na stres. U pacjentów z astmą lub innymi stanami klinicznymi wymagającymi długotrwałego leczenia kortykosteroidami ogólnoustrojowymi zbyt szybkie zmniejszenie stężenia kortykosteroidów ogólnoustrojowych może spowodować poważne nasilenie objawów.
Interakcje z silnymi inhibitorami cytochromu P450 3A4
Należy zachować ostrożność rozważając jednoczesne podawanie preparatu RHINOCORT AQUA aerozol do nosa z ketokonazolem i innymi znanymi silnymi inhibitorami CYP3A4 (np. rytonawirem, atazanawirem, klarytromycyną, indynawirem, itrakonazolem, nefazodonem, nelfinawirem, sakwinawirem, nasileniem działań niepożądanych związanych z telitromycyną) może wystąpić ogólnoustrojowa ekspozycja na budezonid [patrz INTERAKCJE LEKOWE, FARMAKOLOGIA KLINICZNA ].
Wpływ na wzrost
Kortykosteroidy donosowe, w tym budezonid, mogą powodować spowolnienie wzrostu, gdy są podawane pacjentom pediatrycznym. Rutynowo monitorować wzrost pacjentów pediatrycznych otrzymujących długotrwałe leczenie preparatem RHINOCORT 100mcg AQUA (budezonid) w aerozolu do nosa. Aby zminimalizować ogólnoustrojowe skutki donosowych kortykosteroidów, w tym RHINOCORT AQUA (budezonid) w aerozolu do nosa, należy dostosować dawkę każdego pacjenta do najniższej, która skutecznie kontroluje jego objawy [patrz Stosowanie w określonych populacjach, stosowanie u dzieci ].
Jaskra i zaćma
Po donosowym podaniu kortykosteroidów, w tym budezonidu, zgłaszano jaskrę, zwiększone ciśnienie wewnątrzgałkowe i zaćmę. W związku z tym uzasadnione jest ścisłe monitorowanie pacjentów ze zmianami widzenia lub z wywiadem podwyższonego ciśnienia śródgałkowego, jaskry i (lub) zaćmy [patrz DZIAŁANIA NIEPOŻĄDANE ].
Informacje dotyczące poradnictwa dla pacjentów
[Widzieć Oznakowanie pacjenta zatwierdzone przez FDA ]
Pacjenci leczeni preparatem RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa powinni otrzymać następujące informacje i instrukcje. Informacje te mają na celu pomóc pacjentowi w bezpiecznym i skutecznym stosowaniu leku. Nie jest to ujawnienie wszystkich możliwych działań niepożądanych lub zamierzonych. W celu prawidłowego stosowania aerozolu do nosa RHINOCORT 100mcg AQUA (budezonid) i osiągnięcia maksymalnej poprawy pacjent powinien zapoznać się z towarzyszącym mu Oznakowaniem Pacjenta zatwierdzonym przez FDA i przestrzegać go.
Lokalne efekty nosowe
Należy poinformować pacjentów, że u niektórych pacjentów krwawienie z nosa i zlokalizowane zakażenia Candida albicans występowały w nosie i gardle. Jeśli rozwinie się kandydoza, należy ją leczyć odpowiednią terapią miejscową lub ogólnoustrojową i przerwać leczenie preparatem RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa. Ponadto kortykosteroidy donosowe są związane z perforacją przegrody nosowej i upośledzeniem gojenia się ran. Pacjenci, którzy niedawno doświadczyli owrzodzenia nosa, operacji nosa lub urazu nosa, nie powinni stosować RHINOCORT AQUA (budezonid) aerozol do nosa do czasu zagojenia [patrz OSTRZEŻENIA I ŚRODKI ].
Nadwrażliwość, w tym anafilaksja
Należy poinformować pacjentów, że podczas stosowania produktu RHINOCORT AQUA (budezonid) w aerozolu do nosa zgłaszano reakcje nadwrażliwości, w tym reakcje anafilaktyczne, pokrzywkę, wysypkę, zapalenie skóry, obrzęk naczynioruchowy i świąd. Zaprzestać
RHINOCORT AQUA (budezonid) aerozol do nosa, jeśli takie reakcje wystąpią [patrz PRZECIWWSKAZANIA, OSTRZEŻENIA I ŚRODKI oraz DZIAŁANIA NIEPOŻĄDANE ].
Immunosupresja
Pacjentów przyjmujących immunosupresyjne dawki kortykosteroidów należy ostrzec, aby unikali narażenia na ospę wietrzną lub odrę, a w przypadku narażenia niezwłocznie skonsultowali się z lekarzem. Pacjentów należy poinformować o możliwym pogorszeniu istniejącej gruźlicy, zakażenia grzybiczego, bakteryjnego, wirusowego lub pasożytniczego lub opryszczki oka [patrz OSTRZEŻENIA I ŚRODKI ].
Zmniejszona prędkość wzrostu
Należy pouczyć pacjentów, że kortykosteroidy podawane donosowo, w tym budezonid, mogą powodować spowolnienie wzrostu podczas podawania dzieciom. Lekarze powinni uważnie śledzić rozwój dzieci i młodzieży przyjmujących kortykosteroidy dowolną drogą [patrz OSTRZEŻENIA I ŚRODKI ].
Jaskra i zaćma
Należy pouczyć pacjentów, że długotrwałe stosowanie donosowych kortykosteroidów, w tym budezonidu, może zwiększać ryzyko niektórych problemów z oczami (zaćmy i jaskry). Pacjenci powinni poinformować swojego lekarza w przypadku zauważenia zmiany widzenia podczas stosowania leku RHINOCORT AQUA (budezonid) w aerozolu do nosa [patrz OSTRZEŻENIA I ŚRODKI ].
Używaj codziennie
Pacjenci powinni stosować RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa w regularnych odstępach czasu, ponieważ jego skuteczność zależy od regularnego stosowania. Pacjenci mogą zauważyć złagodzenie objawów ze strony nosa w ciągu 10 godzin od pierwszego zastosowania leku RHINOCORT AQUA (budezonid) w aerozolu do nosa. Maksymalne korzyści można osiągnąć dopiero po około 2 tygodniach od rozpoczęcia leczenia [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Pacjenci powinni przyjmować lek zgodnie z zaleceniami i nie przekraczać przepisanej dawki. Pacjent powinien skontaktować się z lekarzem, jeśli objawy nie ustąpią po dwóch tygodniach lub jeśli stan się pogorszy. Pacjenci, którzy doświadczają nawracających epizodów krwawienia z nosa (krwawienia z nosa) lub dyskomfortu w przegrodzie nosowej podczas przyjmowania tego leku, powinni skontaktować się z lekarzem. W celu prawidłowego stosowania aerozolu do nosa RHINOCORT AQUA (budezonid) i uzyskania maksymalnej poprawy pacjent powinien uważnie przeczytać załączone informacje dla pacjenta i przestrzegać ich. Nie należy stosować aerozolu do nosa RHINOCORT 100mcg AQUA (budezonid) po użyciu podanej liczby rozpyleń (nie obejmuje zalewania) lub po upływie daty ważności podanej na opakowaniu lub etykiecie butelki.
Jak stosować RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa
Pacjentów należy dokładnie poinstruować na temat stosowania tego produktu leczniczego, aby zapewnić optymalne dostarczanie dawki [patrz INFORMACJA O PACJENCIE ].
Toksykologia niekliniczna
Karcynogeneza, mutageneza, upośledzenie płodności
104-tygodniowym badaniu doustnym na szczurach Sprague-Dawley zaobserwowano statystycznie istotny wzrost częstości występowania glejaków u samców szczurów otrzymujących doustną dawkę budezonidu 50 μg/kg mc./dobę (około dwukrotność maksymalnej zalecanej dawki donosowej u szczurów). dorosłych i dzieci w mcg/m2). Nie zaobserwowano rakotwórczości u samców szczurów przy dawkach doustnych do 25 mcg/kg (w przybliżeniu równych maksymalnej zalecanej dziennej dawce donosowej u dorosłych i dzieci na podstawie mcg/m2 oraz u samic szczurów przy dawkach doustnych do 50 mcg/kg około dwukrotność maksymalnej zalecanej dobowej dawki donosowej u dorosłych i dzieci w mikrogramach/m2. W dwóch dodatkowych dwuletnich badaniach na samcach szczurów Fischer i Sprague-Dawley budezonid nie powodował glejaków w dawce doustnej 50 μg/kg (około dwukrotność maksymalnej zalecanej dziennej dawki donosowej u dorosłych i dzieci w przeliczeniu na mcg/m2). Jednak u samców szczurów rasy Sprague-Dawley budezonid powodował statystycznie istotny wzrost częstości występowania guzów wątrobowokomórkowych po podaniu doustnym dawki 50 μg/kg (około dwukrotność maksymalnej zalecanej dziennej dawki donosowej u dorosłych i dzieci w przeliczeniu na mcg/m2) ). Jednoczesne referencyjne kortykosteroidy (prednizolon i acetonid triamcynolonu) w tych dwóch badaniach wykazały podobne wyniki.
Nie było dowodów na działanie rakotwórcze, gdy budezonid był podawany doustnie myszom przez 91 tygodni w dawkach do 200 μg/kg/dobę (około 3-krotność maksymalnej zalecanej dziennej dawki donosowej u dorosłych i dzieci w przeliczeniu na μg/m2). .
Budezonid nie wykazywał działania mutagennego ani klastogennego w sześciu różnych testach: test Ames Salmonella/płytka mikrosomowa, test mikrojądrowy u myszy, test chłoniaka u myszy, test aberracji chromosomowych w ludzkich limfocytach, test letalny recesywny sprzężony z płcią u Drosophila melanogaster oraz analiza naprawy DNA u szczura hodowla hepatocytów.
U szczurów budezonid nie miał wpływu na płodność w dawkach podskórnych do 80 mcg/kg (około 3-krotność maksymalnej zalecanej dawki donosowej u dorosłych w mcg/m2).
Przy podskórnej dawce 20 mcg/kg/dobę (mniej niż maksymalna zalecana dzienna dawka donosowa u dorosłych w mcg/m2) zmniejsza przyrost masy ciała matki, żywotność prenatalną i żywotność młodych przy urodzeniu i podczas laktacji byli obserwowani. Nie zaobserwowano takich efektów przy 5 mcg/kg (mniej niż maksymalna zalecana dzienna dawka donosowa u dorosłych na podstawie mcg/m2).
Używaj w określonych populacjach
Ciąża
Efekty teratogenne: Ciąża Kategoria B. Wpływ budezonidu na wyniki w ciąży u ludzi oceniano na podstawie ocen rejestrów urodzeń związanych ze stosowaniem przez matkę wziewnego budezonidu (tj. PULMICORT TURBUHALER) i budezonidu podawanego donosowo (tj. RHINOCORT 100mcg AQUA (budezonid) w aerozolu do nosa). Wyniki populacyjnych prospektywnych kohortowych badań epidemiologicznych analizujących dane z trzech szwedzkich rejestrów obejmujących około 99% ciąż z lat 1995-2001 (tj. Szwedzki Rejestr Urodzeń Medycznych; Rejestr Wad Wrodzonych; Rejestr Kardiologii Dziecięcej) wskazują na brak zwiększonego ryzyka ogólnego wrodzone wady rozwojowe wynikające ze stosowania wziewnego lub donosowego budezonidu we wczesnej ciąży.
Wady wrodzone badano u 2014 niemowląt urodzonych przez matki zgłaszające stosowanie wziewnego budezonidu w leczeniu astmy we wczesnej ciąży (zwykle 10-12 tygodni po ostatniej miesiączce), w okresie, w którym występuje większość poważnych wad rozwojowych narządów.1 Ogólna częstość występowania wad wrodzonych był podobny w porównaniu do wskaźnika populacji ogólnej (odpowiednio 3,8% vs 3,5%). Liczba noworodków urodzonych z rozszczepem twarzoczaszki i wadami serca była zbliżona do oczekiwanej liczby w populacji ogólnej (odpowiednio 4 dzieci vs. 3,3 i 18 dzieci vs. 17-18). W kolejnym badaniu, w którym łączna liczba niemowląt wyniosła 2534, wskaźnik ogólnych wad wrodzonych u niemowląt, których matki były narażone na wziewny budezonid we wczesnej ciąży, nie różnił się od wskaźnika u wszystkich noworodków w tym samym okresie (3,6%). ).2 Trzecie badanie ze Szwedzkiego Medycznego Rejestru Urodzenia obejmujące 2968 ciąż narażonych na wziewny budezonid, z których większość stanowiła ekspozycja w pierwszym trymestrze, podało wiek ciążowy, masę urodzeniową, długość urodzenia, martwe urodzenia i porody mnogie podobne u narażonych niemowląt w porównaniu z nienarażone niemowlęta.3
Wady wrodzone badano u 2113 niemowląt urodzonych przez matki zgłaszające donosowe stosowanie budezonidu we wczesnej ciąży. Częstość występowania wad wrodzonych była podobna w porównaniu z populacją ogólną (odpowiednio 4,5% vs 3,5%). Skorygowany iloraz szans (OR) wyniósł 1,06 (95% CI 0,86-1,31). Liczba niemowląt urodzonych z rozszczepem twarzoczaszki była zbliżona do oczekiwanej liczby w populacji ogólnej (odpowiednio 3 i 3 dzieci). Liczba noworodków urodzonych z wadami serca przekroczyła oczekiwaną w populacji ogólnej (odpowiednio 28 dzieci vs. 17,8). Ekspozycja ogólnoustrojowa na budezonid podawany donosowo jest 6-krotnie mniejsza niż w przypadku budezonidu podawanego wziewnie i nie obserwowano związku wad serca z większą ekspozycją na budezonid.
Pomimo badań na zwierzętach wydaje się, że możliwość uszkodzenia płodu jest znikoma, jeśli lek jest stosowany w czasie ciąży. Niemniej jednak, ponieważ badania na ludziach nie mogą wykluczyć możliwości wystąpienia szkody, RHINOCORT AQUA (budezonid) aerozol do nosa należy stosować w okresie ciąży tylko w przypadku wyraźnej konieczności.
Budezonid powodował utratę płodów, zmniejszenie masy potomstwa i nieprawidłowości szkieletu po podaniu podskórnym u królików dawki około 2 razy większej niż maksymalna zalecana dobowa dawka donosowa u dorosłych na podstawie mcg/m2 oraz dawki podskórnej około 16 razy większej niż dawka podskórna u szczurów. maksymalna zalecana dobowa dawka donosowa u dorosłych w mcg/m2. Nie zaobserwowano działania teratogennego ani embriobójczego u szczurów, gdy budezonid był podawany wziewnie w dawkach do około 8-krotności maksymalnej zalecanej donosowej dawki donosowej u dorosłych w mcg/m2.
Doświadczenie z doustnymi kortykosteroidami od czasu ich wprowadzenia do dawek farmakologicznych, w przeciwieństwie do dawek fizjologicznych, sugeruje, że gryzonie są bardziej podatne na działanie teratogenne kortykosteroidów niż ludzie.
Efekty nieteratogenne: Niedoczynność kory nadnerczy może wystąpić u niemowląt urodzonych przez matki otrzymujące kortykosteroidy w czasie ciąży. Takie niemowlęta należy uważnie obserwować.
Matki karmiące
Budezonid jest wydzielany do mleka ludzkiego. Dane dotyczące budezonidu podawanego za pomocą inhalatora proszkowego wskazują, że całkowita dobowa doustna dawka budezonidu dostępna w mleku matki dla niemowlęcia wynosi około 0,3% do 1% dawki inhalowanej przez matkę [patrz FARMAKOLOGIA KLINICZNA, farmakokinetyka, populacje specjalne, pielęgniarstwo ]. Nie przeprowadzono żadnych badań u kobiet karmiących piersią z zastosowaniem RHINOCORT 100mcg AQUA Nasal Spray; oczekuje się jednak, że dawka budezonidu dostępna dla niemowlęcia w mleku matki, wyrażona jako procent dawki matczynej, będzie podobna. RHINOCORT AQUA (budezonid) aerozol do nosa powinien być stosowany u kobiet karmiących tylko wtedy, gdy jest to uzasadnione klinicznie. Lekarze przepisujący lek powinni porównać znane korzyści z karmienia piersią dla matki i niemowlęcia z potencjalnym ryzykiem minimalnej ekspozycji niemowlęcia na budezonid. Rozważania dotyczące dawkowania obejmują przepisanie lub dostosowanie dawki do najmniejszej klinicznie skutecznej dawki oraz stosowanie RHINOCORT 100 mcg AQUA (budezonid) aerozolu do nosa bezpośrednio po karmieniu piersią w celu maksymalizacji odstępu czasu między dawkowaniem a karmieniem piersią w celu zminimalizowania narażenia niemowlęcia.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność u dzieci w wieku poniżej 6 lat nie zostały ustalone.
Kontrolowane badania kliniczne wykazały, że kortykosteroidy podawane donosowo mogą powodować zmniejszenie szybkości wzrostu u dzieci. Efekt ten zaobserwowano przy braku laboratoryjnych dowodów na zahamowanie osi podwzgórze-przysadka-nadnercza (HPA), co sugeruje, że szybkość wzrostu jest bardziej czułym wskaźnikiem ogólnoustrojowej ekspozycji na kortykosteroidy u dzieci niż niektóre powszechnie stosowane testy czynności osi HPA . Długoterminowe skutki tego zmniejszenia szybkości wzrostu związanego z donosowymi kortykosteroidami, w tym wpływ na ostateczny wzrost osoby dorosłej, są nieznane. Możliwość „nadrobienia” wzrostu po przerwaniu leczenia kortykosteroidami donosowymi nie została odpowiednio zbadana.
Wzrost pacjentów pediatrycznych otrzymujących kortykosteroidy donosowe, w tym RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa, powinien być rutynowo monitorowany (np. za pomocą stadiometrii). Potencjalny wpływ przedłużonego leczenia na wzrost należy porównać z uzyskanymi korzyściami klinicznymi oraz ryzykiem i korzyściami związanymi z terapiami alternatywnymi. Aby zminimalizować ogólnoustrojowe działanie kortykosteroidów donosowych, w tym RHINOCORT AQUA (budezonid) aerozol do nosa, każdemu pacjentowi należy dostosować dawkę do najniższej dawki, która skutecznie kontroluje jego objawy.
Przeprowadzono roczne, kontrolowane placebo badanie kliniczne wzrostu z udziałem 229 pacjentów pediatrycznych (w wieku od 4 do 8 lat) w celu oceny działania produktu RHINOCORT AQUA (budezonid) w aerozolu do nosa (pojedyncza dawka dobowa 64 mikrogramów, zalecana dawka początkowa). dla dzieci w wieku 6 lat i powyżej) na szybkość wzrostu. W populacji 141 pacjentów otrzymujących RHINOCORT AQUA (budezonid) aerozol do nosa 100 mcg i 67 otrzymujących placebo, oszacowanie punktowe szybkości wzrostu po zastosowaniu produktu RHINOCORT AQUA (budezonid) w aerozolu do nosa było o 0,25 cm/rok niższe niż w przypadku placebo (95% przedział ufności). od 0,59 cm/rok mniej niż placebo do 0,08 cm/rok więcej niż placebo).
badaniu dzieci z astmą w wieku 5-12 lat, u dzieci leczonych budezonidem podawanym za pomocą inhalatora suchego proszku 200 mcg dwa razy dziennie (n=311) nastąpiło zmniejszenie wzrostu o 1,1 cm (0,433 cala) w porównaniu z osobami otrzymującymi placebo ( n=418) na koniec roku; różnica między tymi dwiema grupami leczenia nie zwiększyła się dalej w ciągu trzech lat dodatkowego leczenia. Pod koniec czterech lat dzieci leczone inhalatorem budezonidu w postaci suchego proszku i dzieci leczone placebo miały podobne szybkości wzrostu. Wnioski wyciągnięte z tego badania mogą być mylone z powodu nierównego stosowania kortykosteroidów w grupach terapeutycznych i włączenia danych od pacjentów osiągających dojrzałość płciową w trakcie badania.
Ogólnoustrojowe działanie wziewnych kortykosteroidów jest związane z ogólnoustrojową ekspozycją na takie leki. Badania farmakokinetyczne wykazały, że zarówno u dorosłych, jak i dzieci, ogólnoustrojowa ekspozycja na budezonid w najwyższych zalecanych dawkach produktu leczniczego RHINOCORT AQUA (budezonid) aerozol do nosa nie będzie większa niż ekspozycja przy najniższych zalecanych dawkach za pomocą inhalatora suchego proszku. W związku z tym można oczekiwać, że działanie ogólnoustrojowe (oś HPA i wzrost) budezonidu dostarczanego z produktu RHINOCORT AQUA (budezonid) aerozol do nosa nie będzie większe niż zgłaszane dla budezonidu podawanego wziewnie za pomocą inhalatora proszkowego.
Nie można wykluczyć, że RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa może powodować zahamowanie wzrostu u pacjentów podatnych lub gdy jest podawany w dawkach powyżej 64 mikrogramów na dobę. Zalecany zakres dawkowania u pacjentów w wieku od 6 do 11 lat wynosi od 64 do 128 mcg na dobę [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Zastosowanie geriatryczne
Spośród 2461 pacjentów biorących udział w badaniach klinicznych produktu RHINOCORT 100 mcg AQUA (budezonid) aerozol do nosa 5% było w wieku 60 lat i starszych. Nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między tymi osobami a młodszymi pacjentami, z wyjątkiem działań niepożądanych zgłaszanych częstość krwawienia z nosa, która wzrastała wraz z wiekiem. Co więcej, inne zgłoszone doświadczenia kliniczne nie wykazały żadnych innych różnic w odpowiedziach między starszymi i młodszymi pacjentami, ale nie można wykluczyć większej wrażliwości niektórych starszych osób.
Niewydolność wątroby
Nie przeprowadzono formalnych badań farmakokinetycznych z użyciem preparatu RHINOCORT 100 mcg AQUA (budezonid) aerozol do nosa u pacjentów z zaburzeniami czynności wątroby. Jednakże, ponieważ budezonid jest usuwany głównie w wyniku metabolizmu wątrobowego, zaburzenia czynności wątroby mogą prowadzić do kumulacji budezonidu w osoczu. Dlatego pacjenci z chorobą wątroby powinni być ściśle monitorowani.
PRZEDAWKOWAĆ
Ostre przedawkowanie tej postaci dawkowania jest mało prawdopodobne, ponieważ jedna butelka zawierająca 120 dawek preparatu RHINOCORT 100 mcg AQUA (budesonid) aerozol do nosa 32 mcg zawiera tylko około 5,4 mg budezonidu. Przewlekłe przedawkowanie może skutkować oznakami/objawami hiperkortycyzmu [patrz OSTRZEŻENIA I ŚRODKI ].
PRZECIWWSKAZANIA
RHINOCORT AQUA (budezonid) aerozol do nosa jest przeciwwskazany u pacjentów z nadwrażliwością na którykolwiek ze składników [patrz OSTRZEŻENIA I ŚRODKI ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Budezonid jest kortykosteroidem o działaniu przeciwzapalnym, który wykazuje silne działanie glikokortykoidowe i słabe działanie mineralokortykoidowe. W standardowych modelach in vitro i zwierzęcych budezonid ma około 200-krotnie większe powinowactwo do receptora glukokortykoidowego i 1000-krotnie większą siłę działania przeciwzapalnego do stosowania miejscowego niż kortyzol (test obrzęku ucha wywołanego olejem krotonowym u szczurów). Jako miara aktywności ogólnoustrojowej budezonid jest 40 razy silniejszy niż kortyzol przy podawaniu podskórnym i 25 razy silniejszy przy podawaniu doustnym w teście inwolucji grasicy szczura. Kliniczne znaczenie tego nie jest znane.
Aktywność preparatu RHINOCORT 100mcg AQUA Nasal Spray wynika z działania leku macierzystego, budezonidu. W badaniach powinowactwa receptora glukokortykoidowego forma 22R była dwa razy bardziej aktywna niż epimer 22S. Badania in vitro wykazały, że dwie formy budezonidu nie ulegają wzajemnej konwersji.
Dokładny mechanizm działania kortykosteroidów na stan zapalny w sezonowym i całorocznym alergicznym nieżycie nosa nie jest dobrze poznany. Stan zapalny jest ważnym elementem patogenezy sezonowego i całorocznego alergicznego nieżytu nosa. Kortykosteroidy mają szeroki zakres działania hamującego na wiele typów komórek (np. komórki tuczne, eozynofile, neutrofile, makrofagi i limfocyty) i mediatorów (np. histamina, eikozanoidy, leukotrieny i cytokiny) zaangażowanych w reakcje alergiczne i niealergiczne zapalenie. Te przeciwzapalne działania kortykosteroidów mogą przyczyniać się do ich skuteczności w sezonowym i całorocznym alergicznym nieżycie nosa.
Farmakodynamika
W 3-tygodniowym badaniu klinicznym dotyczącym sezonowego nieżytu nosa, porównującym 100 µg inhalatora donosowego RHINOCORT, podawanego doustnie budezonidu i placebo u 98 pacjentów z alergicznym nieżytem nosa wywołanym pyłkiem brzozy, wykazano, że działanie terapeutyczne inhalatora do nosa RHINOCORT można przypisać miejscowemu działaniu budezonid.

Efekty osi HPA
Wpływ preparatu RHINOCORT 100mcg AQUA (budezonid) na czynność nadnerczy oceniano w kilku badaniach klinicznych. W trwającym cztery tygodnie badaniu klinicznym u 61 dorosłych pacjentów, którzy otrzymywali 256 mcg produktu RHINOCORT AQUA (budezonid) nasal spray na dobę, nie stwierdzono istotnych różnic w stężeniach kortyzolu w osoczu mierzonych przed i 60 minut po podaniu domięśniowym 0,25 mg kosyntropiny w porównaniu z pacjentami otrzymującymi placebo. Nie było spójnych różnic w 24-godzinnych pomiarach kortyzolu w moczu u pacjentów otrzymujących do 400 mcg na dobę. Podobne wyniki zaobserwowano w badaniu 150 dzieci i młodzieży w wieku od 6 do 17 lat z całorocznym nieżytem nosa, którym podawano 256 mcg dziennie przez okres do 12 miesięcy.
Po leczeniu zalecaną maksymalną dawką dobową preparatu RHINOCORT AQUA (budezonid) w aerozolu do nosa (256 mcg) przez siedem dni wystąpił niewielki, ale statystycznie istotny spadek powierzchni pod krzywą stężenia kortyzolu w osoczu w ciągu 24 godzin (AUC0-24h). ) u zdrowych dorosłych ochotników.
Po podaniu preparatu RHINOCORT AQUA (budezonid) aerozol do nosa w dawkach od 100 do 800 mcg na dobę przez okres do czterech dni 78 zdrowym dorosłym ochotnikom zaobserwowano zależne od dawki zahamowanie 24-godzinnego wydalania kortyzolu z moczem. Znaczenie kliniczne tych wyników nie jest znane.
Farmakokinetyka
Wchłanianie
Po donosowym podaniu pojedynczej dawki RHINOCORT AQUA (budezonid) aerozol do nosa (128 μg), średnie maksymalne stężenie w osoczu wynoszące około 0,3 nmol/l występuje po około 0,5 godziny po podaniu. W porównaniu z dawką dożylną około 34% dostarczonej dawki donosowej dociera do krążenia ogólnoustrojowego, z czego większość jest wchłaniana przez błonę śluzową nosa. Podczas gdy budezonid jest dobrze wchłaniany z przewodu pokarmowego, biodostępność po podaniu doustnym budezonidu jest niska (~10%) głównie z powodu intensywnego metabolizmu pierwszego przejścia w wątrobie.
Dystrybucja
Objętość dystrybucji budezonidu wynosiła około 2-3 l/kg. Wiązał się w 85-90% z białkami osocza. Objętość dystrybucji epimeru 22R jest prawie dwukrotnie większa niż epimeru 22S. Wiązanie z białkami było stałe w zakresie stężeń (1-100 nmol/l) osiągniętym i przekraczającym zalecane dawki preparatu RHINOCORT 100 µg AQUA Nasal Spray. Budezonid wykazywał niewielkie lub żadne wiązanie z globuliną wiążącą kortykosteroidy. Budezonid szybko równoważył się z czerwonymi krwinkami w sposób niezależny od stężenia, przy stosunku krew/osocze wynoszącym około 0,8.
Metabolizm
Badania in vitro z homogenatami wątroby ludzkiej wykazały, że budezonid jest szybko i intensywnie metabolizowany. Wyizolowano i zidentyfikowano dwa główne metabolity powstające w wyniku biotransformacji katalizowanej izoenzymem 3A4 (CYP3A4) cytochromu P450 (CYP) jako 16α-hydroksyprednizolon i 6p-hydroksybudezonid. Aktywność kortykosteroidowa każdego z tych dwóch metabolitów jest mniejsza niż 1% aktywności związku macierzystego. Nie wykryto jakościowej różnicy między wzorcami metabolicznymi in vitro i in vivo. W preparatach ludzkich płuc i surowicy zaobserwowano znikomą inaktywację metaboliczną.
Wydalanie/Eliminacja
Forma 22R budezonidu była preferencyjnie usuwana przez wątrobę z klirensem ogólnoustrojowym 1,4 l/min wobec 1,0 l/min dla formy 22S. Końcowy okres półtrwania, 2 do 3 godzin, był taki sam dla obu epimerów i niezależny od dawki. Budezonid był wydalany z moczem i kałem w postaci metabolitów. Około 2/3 donosowej radioznakowanej dawki odzyskano w moczu, a pozostałą część w kale. W moczu nie wykryto budezonidu w postaci niezmienionej.
Określone populacje
Geriatryczny
Farmakokinetyka preparatu RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa u pacjentów w podeszłym wieku nie była szczegółowo badana.
Pediatryczny
Po podaniu preparatu RHINOCORT 100 mcg AQUA (budezonid) aerozol do nosa czas do osiągnięcia maksymalnego stężenia leku i okres półtrwania w osoczu były podobne u dzieci i dorosłych. Dzieci miały stężenia w osoczu około dwukrotnie większe niż obserwowane u dorosłych, głównie ze względu na różnice w masie ciała między dziećmi i dorosłymi.
Płeć
Nie przeprowadzono specjalnych badań farmakokinetycznych oceniających wpływ płci na farmakokinetykę budezonidu. Jednak po podaniu 400 µg preparatu RHINOCORT 100 µg AQUA (budezonid) aerozol do nosa 7 mężczyznom i 8 kobietom ochotnikom w badaniu farmakokinetycznym nie stwierdzono większych różnic w parametrach farmakokinetycznych między płciami.
Wyścig
Nie przeprowadzono specjalnych badań oceniających wpływ rasy na farmakokinetykę budezonidu.
Matki karmiące
Dyspozycje budezonidu podawanego drogą inhalacji doustnej z inhalatora proszkowego w dawkach 200 lub 400 mcg dwa razy na dobę przez co najmniej 3 miesiące badano u ośmiu kobiet karmiących piersią z astmą od 1 do 6 miesięcy po porodzie. Ekspozycja ogólnoustrojowa na budezonid u tych kobiet wydaje się być porównywalna z wynikami innych badań, które stwierdzono u kobiet nie karmiących piersią z astmą. Mleko z piersi uzyskane w ciągu ośmiu godzin po podaniu wykazało, że maksymalne stężenie budezonidu dla dawek 400 i 800 mcg wynosiło odpowiednio 0,39 i 0,78 nmol/l i wystąpiło w ciągu 45 minut po podaniu. Szacowana doustna dawka dobowa budezonidu z mleka matki dla niemowlęcia wynosiła około 0,007 i 0,014 mcg/kg/dobę dla dwóch schematów dawkowania stosowanych w tym badaniu, co stanowi około 0,3% do 1% dawki wdychanej przez matkę. Poziomy budezonidu w próbkach osocza pobranych od pięciu niemowląt około 90 minut po karmieniu piersią (i około 140 minut po podaniu leku matce) były poniżej mierzalnych poziomów ( Stosowanie w określonych populacjach, karmiące matki ].
Niewydolność nerek lub wątroby
Nie badano farmakokinetyki budezonidu u pacjentów z zaburzeniami czynności nerek. Zaburzenia czynności wątroby mogą wpływać na eliminację kortykosteroidów. Na farmakokinetykę budezonidu wpływały zaburzenia czynności wątroby, o czym świadczy podwojenie dostępności ogólnoustrojowej po przyjęciu doustnym. Nie ustalono związku tego wyniku z budezonidem podawanym donosowo.
Interakcje między lekami
Inhibitory enzymów cytochromu P450
Ketokonazol: Ketokonazol, silny inhibitor izoenzymu 3A4 (CYP3A4) cytochromu P450 (CYP), głównego enzymu metabolicznego kortykosteroidów, zwiększa stężenie budezonidu przyjmowanego doustnie w osoczu [patrz OSTRZEŻENIA I ŚRODKI oraz INTERAKCJE Z LEKAMI ].
Cymetydyna: W zalecanych dawkach cymetydyna, niespecyficzny inhibitor enzymów CYP, miała niewielki, ale klinicznie nieistotny wpływ na farmakokinetykę budezonidu podawanego doustnie.
Toksykologia i/lub Farmakologia Zwierząt
Budezonid wykazywał działanie teratogenne i embriobójcze u królików i szczurów. Budezonid po podaniu podskórnym dawki 25 μg/kg u królików (w przybliżeniu 2-krotność maksymalnej zalecanej dziennej dawki donosowej u dorosłych w mcg/m2) i w dawce podskórnej 500 mcg powodował utratę płodów, zmniejszenie masy ciała młodych i nieprawidłowości w obrębie układu kostnego. /kg u szczurów (około 16-krotność maksymalnej zalecanej dziennej dawki donosowej u dorosłych w mcg/m2). U szczurów nie zaobserwowano działania teratogennego ani embriobójczego budezonidu w dawkach wziewnych do 250 μg/kg (około 8-krotność maksymalnej zalecanej dawki donosowej u dorosłych w mcg/m2).
Studia kliniczne
Skuteczność terapeutyczna preparatu RHINOCORT AQUA (budezonid) aerozol do nosa została oceniona w kontrolowanych placebo badaniach klinicznych sezonowego i całorocznego alergicznego nieżytu nosa trwających 3-6 tygodni.
Liczba pacjentów leczonych budezonidem w tych badaniach wynosiła 90 mężczyzn i 51 kobiet w wieku 6-12 lat oraz 691 mężczyzn i 694 kobiet w wieku 12 lat i starszych. Pacjenci byli głównie rasy kaukaskiej.
Ogólnie wyniki tych badań klinicznych wykazały, że RHINOCORT AQUA (budezonid) aerozol do nosa podawany raz na dobę zapewnia statystycznie istotne zmniejszenie nasilenia objawów ze strony nosa sezonowego i całorocznego alergicznego nieżytu nosa, w tym kataru, kichania i przekrwienia błony śluzowej nosa.
Poprawę objawów ze strony nosa można zauważyć u pacjentów w ciągu 10 godzin od pierwszego zastosowania leku RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa. Ten czas do wystąpienia jest poparty jednostkowym badaniem środowiskowym u pacjentów z sezonowym alergicznym nieżytem nosa, które wykazało, że RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa prowadził do statystycznie istotnej poprawy objawów ze strony nosa w porównaniu z placebo o 10 godzin. Dalsze wsparcie pochodzi z badania klinicznego pacjentów z całorocznym alergicznym zapaleniem błony śluzowej nosa, które wykazało statystycznie istotną poprawę objawów ze strony nosa zarówno dla produktu RHINOCORT AQUA (budezonid) w aerozolu do nosa, jak i dla aktywnego leku porównawczego (furoinian mometazonu) w porównaniu z placebo o 8 godzin. Początek był również oceniany w tym badaniu przy szczytowym natężeniu przepływu wdechowego przez nos, a ten punkt końcowy nie wykazał skuteczności dla żadnego aktywnego leczenia. Chociaż statystycznie istotne złagodzenie objawów ze strony nosa w porównaniu z placebo odnotowano w ciągu 8-10 godzin w tych badaniach, około połowa do dwóch trzecich ostatecznej poprawy klinicznej po zastosowaniu leku RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa występuje w ciągu pierwszych 1-2 dni. a maksymalne korzyści mogą być osiągnięte dopiero po około 2 tygodniach od rozpoczęcia leczenia.
BIBLIOGRAFIA
Kallen B, Rydhstroem H, Aberg A. Wady wrodzone po zastosowaniu wziewnego budezonidu we wczesnej ciąży. Obstet Gynecol 1999; 93:392-395.
2 Ericson A, Kallen B. Używanie narkotyków w ciąży: unikalna szwedzka metoda rejestracji, którą można ulepszyć. Szwedzka Agencja Produktów Medycznych 1999; 1:8-11.
3 Norjavaara E, Gerhardsson de Verdier M. Prawidłowe wyniki ciąży w badaniu populacyjnym obejmującym 2968 ciężarnych kobiet narażonych na budezonid. J Allergy Clin Immunol 2003;! 11:736-742.
INFORMACJA O PACJENCIE
RHINOCORT 100mcg AQUA (budezonid) ® (RINE-o-cort AH-kwa) (budezonid) Spray do nosa
Do użytku tylko w nosie
Przeczytaj informacje dla pacjenta dołączone do sprayu do nosa RHINOCORT 100mcg AQUA (budezonid) przed rozpoczęciem stosowania i za każdym razem, gdy otrzymasz uzupełnienie. Mogą pojawić się nowe informacje. Informacje te nie zastępują rozmowy z lekarzem o stanie zdrowia lub leczeniu. W przypadku pytań dotyczących leku RHINOCORT AQUA (budezonid) aerozol do nosa, należy zwrócić się do lekarza lub farmaceuty.
Co to jest spray do nosa RHINOCORT 100mcg AQUA (budezonid)?
RHINOCORT AQUA (budezonid) aerozol do nosa jest lekiem na receptę stosowanym w leczeniu sezonowych i całorocznych objawów alergii u dorosłych i dzieci w wieku 6 lat i starszych.
RHINOCORT AQUA Aerozol do nosa zawiera budezonid, który jest sztucznym (syntetycznym) kortykosteroidem. Kortykosteroidy donosowe to naturalne hormony występujące w organizmie, które zmniejszają obrzęk wyściółki nosa. Rozpylanie aerozolu do nosa RHINOCORT 100mcg AQUA (budezonid) pomaga zmniejszyć nosowe objawy alergicznego nieżytu nosa (zapalenie błony śluzowej nosa), takie jak zatkany nos, katar, swędzenie i kichanie.
Nie wykazano bezpieczeństwa i skuteczności preparatu RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa u dzieci w wieku poniżej 6 lat.
Kto nie powinien stosować aerozolu do nosa RHINOCORT AQUA (budezonid)?
Nie należy stosować aerozolu do nosa RHINOCORT 100mcg AQUA (budezonid):
- jeśli pacjent ma uczulenie na budezonid lub którykolwiek ze składników aerozolu do nosa RHINOCORT AQUA. Pełny wykaz składników preparatu RHINOCORT AQUA (budezonid) aerozol do nosa znajduje się na końcu tej ulotki.
czym powinienem powiedzieć lekarzowi przed użyciem RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa?
Przed zastosowaniem leku RHINOCORT AQUA (budezonid) aerozol do nosa należy poinformować lekarza lub farmaceutę, jeśli:
- ostatnio był w pobliżu każdego, kto choruje na ospę wietrzną lub odrę?
- masz problemy z wątrobą
- masz jakieś nieleczone infekcje
- kiedykolwiek miałeś infekcję zwaną gruźlicą
- mieć infekcję oka
- niedawno przeszedł operację lub uraz nosa
- masz jakiekolwiek inne schorzenia
- są w ciąży lub planują zajść w ciążę. Nie wiadomo, czy RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa zaszkodzi nienarodzonemu dziecku. Porozmawiaj z lekarzem, jeśli jesteś w ciąży lub planujesz zajść w ciążę.
- karmisz piersią lub planujesz karmić piersią. RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa może przenikać do mleka matki. Porozmawiaj z lekarzem o najlepszym sposobie karmienia dziecka, jeśli przyjmujesz RHINOCORT AQUA (budezonid) aerozol do nosa.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, tym leki na receptę i bez recepty, witaminy i suplementy ziołowe.
RHINOCORT AQUA (budezonid) aerozol do nosa może wpływać na działanie innych leków, a inne leki mogą wpływać na działanie leku RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa.
Poznaj leki, które przyjmujesz. Miej przy sobie listę swoich leków, aby pokazać swojemu lekarzowi i farmaceucie, kiedy otrzymasz nowy lek.
Jak stosować spray do nosa RHINOCORT 100mcg AQUA (budezonid)?
- RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa jest przeznaczony do stosowania wyłącznie do nosa. Nie rozpylaj go do oczu ani ust.
- Stosuj spray do nosa RHINOCORT AQUA (budezonid) zgodnie z zaleceniami lekarza.
- Bardzo ważne jest regularne stosowanie leku RHINOCORT AQUA (budezonid) aerozol do nosa. Nie należy przerywać stosowania aerozolu do nosa RHINOCORT AQUA (budezonid) ani zmieniać dawki bez konsultacji z lekarzem, nawet jeśli czujesz się lepiej.
- Porozmawiaj z lekarzem, jeśli objawy nie ustąpią po przyjmowaniu leku RHINOCORT AQUA (budezonid) aerozol do nosa przez 2 tygodnie lub jeśli objawy się pogorszą.
- Dorosły powinien pomóc małemu dziecku w stosowaniu tego leku.
- Pełne informacje na temat stosowania leku RHINOCORT AQUA (budezonid) w aerozolu do nosa można znaleźć w Instrukcji stosowania dla pacjenta na końcu tej ulotki.
Jakie są możliwe skutki uboczne RHINOCORT AQUA (budezonid) aerozol do nosa?
RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa może powodować poważne skutki uboczne, w tym:
- dziura w chrząstce wewnątrz nosa (perforacja przegrody nosowej). Poinformuj swojego lekarza, jeśli podczas oddychania dobiegasz z nosa.
- powolne gojenie się ran. Nie należy stosować aerozolu do nosa RHINOCORT 100mcg AQUA (budezonid) do czasu wygojenia nosa, jeśli masz ból w nosie, jeśli przeszłaś operację nosa lub jeśli nos został uszkodzony.
- infekcja grzybicza w nosie.
- reakcje alergiczne. Poinformuj swojego lekarza lub natychmiast uzyskaj pomoc medyczną, jeśli masz:
- wysypka skórna, zaczerwienienie lub obrzęk
- silne swędzenie
- obrzęk twarzy, ust i języka
- problemy z układem odpornościowym, które mogą zwiększać ryzyko infekcji. Bardziej prawdopodobne jest wystąpienie infekcji, jeśli pacjent przyjmuje leki osłabiające zdolność organizmu do zwalczania infekcji. Unikaj kontaktu z osobami cierpiącymi na choroby zakaźne, takie jak ospa wietrzna lub odra, podczas stosowania aerozolu do nosa RHINOCORT AQUA (budezonid). Objawy zakażenia mogą obejmować gorączkę, ból, bóle, dreszcze, uczucie zmęczenia, nudności i wymioty.
- niewydolność nadnerczy, Niewydolność nadnerczy to stan, w którym nadnercza nie wytwarzają wystarczającej ilości hormonów steroidowych. Objawy niewydolności nadnerczy mogą obejmować zmęczenie, osłabienie, nudności, wymioty i niskie ciśnienie krwi.
- spowolniony lub opóźniony wzrost u dzieci. Wzrost dziecka powinien być regularnie kontrolowany podczas stosowania RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa.
- problemy z oczami, takie jak jaskra i zaćma. Poinformuj swojego lekarza, jeśli masz zmianę widzenia lub masz historię zwiększonego ciśnienia śródgałkowego, jaskry i / lub zaćmy.
Zadzwoń do swojego lekarza lub natychmiast uzyskaj pomoc medyczną, jeśli wystąpią objawy któregokolwiek z poważnych działań niepożądanych wymienionych powyżej.
Najczęstsze skutki uboczne RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa to:
- krwotok z nosa
- ból gardła
- trudności z oddychaniem, takie jak świszczący oddech lub ucisk w klatce piersiowej
- kaszel
- podrażnienie nosa
Poinformuj swojego lekarza, jeśli masz jakiekolwiek skutki uboczne, które Ci przeszkadzają lub nie ustępują.
To nie są wszystkie możliwe skutki uboczne RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa. Aby uzyskać więcej informacji, zapytaj swojego lekarza lub farmaceutę.
Zadzwoń do swojego lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088 lub www.fda.gov/medwatch.
Działania niepożądane można zgłaszać firmie AstraZeneca pod numerem 1-800-236-9933.
Co powinienem wiedzieć o alergicznym nieżycie nosa?
„Nieżyt nosa” oznacza zapalenie błony śluzowej nosa. Czasami nazywa się to „katarem siennym”. Alergiczny nieżyt nosa może być spowodowany alergią na pyłki, sierść zwierząt, roztocza kurzu domowego i zarodniki pleśni. Jeśli masz alergiczny nieżyt nosa, twój nos staje się zatkany, cieknie i swędzi. Możesz też dużo kichać. Możesz mieć czerwone, swędzące, łzawiące oczy; swędzące gardło; lub zablokowane, swędzące uszy.
RHINOCORT AQUA (budezonid) aerozol do nosa pomaga złagodzić objawy ze strony nosa.
Jeśli masz również swędzące, łzawiące oczy, powinieneś powiedzieć o tym swojemu lekarzowi. Może przepisać dodatkowe leki w celu leczenia tych objawów.
Jak przechowywać RHINOCORT AQUA (budezonid) aerozol do nosa?
- RHINOCORT AQUA (budezonid) aerozol do nosa należy przechowywać w temperaturze od 20°C do 25°C.
- Nie zamrażać RHINOCORT AQUA (budezonid) aerozol do nosa.
- Chronić przed światłem RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa.
- Nie należy stosować aerozolu do nosa RHINOCORT 100mcg AQUA (budezonid) po użyciu podanej liczby rozpyleń (nie obejmuje zalewania) lub po upływie daty ważności podanej na opakowaniu lub etykiecie butelki.
- Trzymaj zieloną nasadkę ochronną na aerozolu do nosa RHINOCORT AQUA (budezonid), gdy nie jest używany. (Proszę zobaczyć Przed użyciem na odwrotnej stronie ).
- Przechowuj RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa i wszystkie leki poza zasięgiem dzieci.
Ogólne informacje dotyczące bezpiecznego i skutecznego stosowania aerozolu do nosa RHINOCORT AQUA (budezonid):
Nie należy stosować aerozolu do nosa RHINOCORT 100mcg AQUA (budezonid) w stanach, na które nie został przepisany. Nie należy podawać leku RHINOCORT AQUA (budezonid) aerozol do nosa innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić.
Niniejsza ulotka z informacjami dla pacjenta podsumowuje najważniejsze informacje dotyczące preparatu RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa. Jeśli chcesz uzyskać więcej informacji, porozmawiaj ze swoim lekarzem. Możesz poprosić farmaceutę lub pracownika służby zdrowia o informacje na temat RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa, który jest przeznaczony dla pracowników służby zdrowia.
Aby uzyskać więcej informacji, odwiedź stronę www.astrazeneca-us.com lub zadzwoń do AstraZeneca pod numer 1-800-236-9933.
Jakie są składniki sprayu do nosa RHINOCORT AQUA (budezonid)?
Składnik czynny: budezonid
Nieaktywne składniki: Celuloza mikrokrystaliczna i karboksymetyloceluloza sodowa, dekstroza bezwodna, polisorbat 80, wersenian disodowy, sorbinian potasu, woda oczyszczona i kwas solny.
Instrukcja użytkowania dla pacjenta
Do stosowania wyłącznie w nosie. Nie spryskiwać oczu ani ust.
Przed rozpoczęciem stosowania leku RHINOCORT 100mcg AQUA (budezonid) aerozol do nosa należy uważnie przeczytać instrukcję dla pacjenta. Jeśli masz jakieś pytania, zapytaj swojego lekarza
Rysunek A 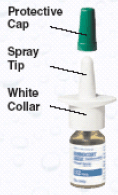
Jak przygotować spray do nosa RHINOCORT AQUA (budezonid)?
Przed zastosowaniem aerozolu do nosa RHINOCORT AQUA (budezonid) należy zagruntować butelkę. Aby przygotować spray do nosa RHINOCORT 100mcg AQUA (budezonid):
1. Pociągnij, aby zdjąć zieloną nasadkę ochronną z aerozolu do nosa.
2. Delikatnie wstrząsnąć butelką przez kilka sekund przed każdym użyciem.
3. Trzymaj butelkę mocno, jak pokazano na Rysunku B, palcem wskazującym i środkowym po obu stronach końcówki rozpylającej i kciukiem pod butelką.
Rysunek B 
4. Uruchom pompkę, szybko i mocno naciskając biały kołnierz, przytrzymując kciukiem podstawę butelki.
5. Przed pierwszym użyciem RHINOCORT AQUA (budezonid) aerozol do nosa delikatnie wstrząsnąć butelką. Pompę należy zagruntować, naciskając 8 razy biały kołnierz. Pompa jest teraz gotowa do użycia. W przypadku codziennego użytku pompa nie wymaga ponownego napełniania. Jeśli nie jest używany przez 2 dni z rzędu, powtórz 1 rozpylenie lub do momentu pojawienia się drobnego rozpylenia. Jeśli nie była używana przez ponad 14 dni, wypłucz końcówkę rozpylającą pompy, wykonując czynności czyszczenia wymienione na końcu tej ulotki. Po oczyszczeniu zagruntować 2 rozpyleniami lub do momentu pojawienia się drobnego rozpylenia.
Każda butelka aerozolu do nosa RHINOCORT AQUA (budezonid) zawiera wystarczającą ilość leku, aby po przygotowaniu butelki 120 razy rozpylić lek z butelki.
Nie należy używać butelki RHINOCORT 100mcg AQUA (budezonid) aerozolu do nosa po 120 rozpyleniach. Dodatkowe rozpylenie po 120 może nie zawierać odpowiedniej ilości leku. Należy rejestrować liczbę rozpyleń z każdej butelki leku RHINOCORT 100mcg AQUA aerozol do nosa i wyrzucić wszelkie pozostałości leku, które mogły pozostać w butelce. Receptę uzupełniaj co miesiąc.
Jak stosować spray do nosa RHINOCORT 100mcg AQUA (budezonid)?
Postępuj zgodnie z poniższymi instrukcjami w celu codziennego stosowania RHINOCORT AQUA (budezonid) aerozol do nosa:
Rysunek C 
4. Włóż końcówkę rozpylającą do nozdrza (końcówka nie powinna sięgać daleko do nosa). Zamknij drugie nozdrze palcem i lekko pochyl głowę do przodu, aby strumień kierował się w tył nosa (patrz Rysunek D ).
Rysunek D 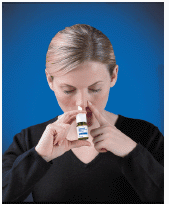
5. Przy każdym rozpyleniu należy aktywować pompkę, szybko i mocno naciskając biały kołnierz, przytrzymując kciukiem podstawę butelki. Oddychaj delikatnie do wewnątrz przez nozdrze.
6. Po rozpyleniu do nozdrza odchyl głowę do tyłu na kilka sekund (patrz Rysunek E ).
Rysunek E 
7. Jeśli potrzebne jest drugie rozpylenie do tego samego nozdrza, powtórz kroki od 3 do 6.
8. Powtórz kroki od 3 do 7 dla drugiego nozdrza.
9. Unikaj wydmuchiwania nosa przez 15 minut po zastosowaniu sprayu do nosa RHINOCORT 100mcg AQUA (budezonid).
10. Wytrzyj końcówkę natryskową czystą chusteczką (patrz Rysunek F ) i załóż zieloną nasadkę ochronną. Przechowuj butelkę w pozycji pionowej.
Rysunek F 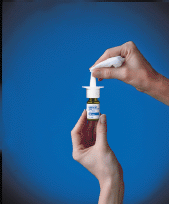
Jak czyścić spray do nosa RHINOCORT 100mcg AQUA (budezonid)?
Rysunek G 
Regularnie płucz zieloną nasadkę ochronną i końcówkę natryskową. Aby to zrobić:
W celu uzyskania dodatkowych informacji na temat aerozolu do nosa RHINOCORT 100mcg AQUA (budezonid) ®, należy zadzwonić do Centrum Informacji AstraZeneca, od poniedziałku do piątku w godzinach 8:00-18:00 czasu wschodniego, z wyjątkiem świąt o godz. 1-800-236-9933.
