Xalatan 2.5ml Latanoprost Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
XALATAN® (latanoprost) roztwór do oczu
OPIS
Latanoprost jest analogiem prostaglandyny F2α. Jego nazwa chemiczna to izopropylo-(Z)-7[(1R,2R,3R,5S)3,5dihydroksy-2-[(3R)-3-hydroksy-5-fenylopentylo]cyklopentylo]-5-heptenian. Jego wzór cząsteczkowy to C26H40O5, a struktura chemiczna to:
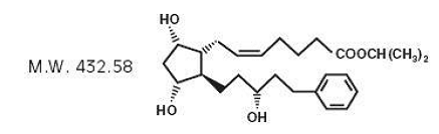
Latanoprost to bezbarwny do lekko żółtego olej, który jest bardzo dobrze rozpuszczalny w acetonitrylu i łatwo rozpuszczalny w acetonie, etanolu, octanie etylu, izopropanolu, metanolu i oktanolu. Jest praktycznie nierozpuszczalny w wodzie.
XALATAN (roztwór do oczu latanoprostu) 0,005% jest dostarczany jako sterylny, izotoniczny, buforowany wodny roztwór latanoprostu o pH około 6,7 i osmolalności około 267 mOsmol/kg. Każdy ml XALATAN zawiera 50 µg latanoprostu. Jako środek konserwujący dodaje się 0,02% chlorek benzalkoniowy. Składniki nieaktywne to: chlorek sodu, jednowodny diwodorofosforan sodu, bezwodny wodorofosforan disodu i woda do wstrzykiwań. Jedna kropla zawiera około 1,5 mcg latanoprostu.
WSKAZANIA
XALATAN 2,5 ml jest wskazany w celu zmniejszenia podwyższonego ciśnienia wewnątrzgałkowego u pacjentów z jaskrą otwartego kąta lub nadciśnieniem ocznym.
DAWKOWANIE I SPOSÓB PODAWANIA
Zalecana dawka to jedna kropla do chorego oka (oczu) raz dziennie wieczorem. W przypadku pominięcia jednej dawki leczenie należy kontynuować, podając następną dawkę jak zwykle.
Dawka XALATAN nie powinna przekraczać raz dziennie; nie zaleca się jednoczesnego stosowania dwóch lub więcej prostaglandyn lub analogów prostaglandyn, w tym XALATAN 2,5 ml. Wykazano, że podawanie tych leków zawierających prostaglandyny częściej niż raz dziennie może zmniejszać działanie obniżające ciśnienie wewnątrzgałkowe (IOP) lub powodować paradoksalne podwyższenie ciśnienia wewnątrzgałkowego.
Zmniejszenie IOP rozpoczyna się około 3 do 4 godzin po podaniu, a maksymalny efekt osiąga się po 8 do 12 godzinach.
XALATAN może być stosowany jednocześnie z innymi produktami leczniczymi do stosowania miejscowego okulistycznych w celu obniżenia IOP. Jeśli stosuje się więcej niż jeden miejscowy lek okulistyczny, leki należy podawać w odstępie co najmniej pięciu (5) minut. Soczewki kontaktowe należy usunąć przed podaniem leku XALATAN 2,5 ml i można je ponownie założyć po 15 minutach od podania
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Sterylny roztwór do oczu zawierający 50 µg/ml latanoprostu.
Składowania i stosowania
XALATAN jest klarownym, izotonicznym, zbuforowanym, zakonserwowanym bezbarwnym roztworem latanoprostu 0,005% (50 mcg/ml). Jest dostarczany w postaci 2,5 ml roztworu w 5 ml przezroczystej butelce z polietylenu o niskiej gęstości z przezroczystą końcówką zakraplającą z polietylenu, turkusową zakrętką z polietylenu o wysokiej gęstości i nasadką z przezroczystego polietylenu o niskiej gęstości z zabezpieczeniem gwarancyjnym.
Napełnienie 2,5 ml, 0,005% (50 mcg/ml): Opakowanie z 1 butelką: NDC 0013-8303-04 Napełnienie 2,5 ml, 0,005% (50 mcg/ml): Opakowanie zbiorcze zawierające 3 butelki: NDC 0013-8303-01
Magazynowanie
Chronić przed światłem. Nieotwarte butelki przechowywać w lodówce w temperaturze od 2° do 8°C (36° do 46°F). Podczas transportu do pacjenta butelka może być utrzymywana w temperaturze do 40°C (104°F) przez okres nieprzekraczający 8 dni. Po otwarciu butelki do użycia można ją przechowywać w temperaturze pokojowej do 25°C (77°F) przez 6 tygodni.
Dystrybutor: Pharmacia & Upjohn Co., Oddział Pfizer Inc., NY, NY 10017. Pfizer Manufacturing Belgium NV Puurs, Belgia. Poprawiony: nie dotyczy
SKUTKI UBOCZNE
Następujące działania niepożądane zostały zgłoszone po wprowadzeniu produktu do obrotu i zostały omówione bardziej szczegółowo w innych punktach etykiety:
- Zmiany pigmentacji tęczówki [patrz OSTRZEŻENIA I ŚRODKI ]
- Ciemnienie skóry powiek [patrz OSTRZEŻENIA I ŚRODKI ]
- Zmiany rzęs (zwiększenie długości, grubości, pigmentacji i liczby rzęs) [patrz OSTRZEŻENIA I ŚRODKI ]
- Zapalenie wewnątrzgałkowe (zapalenie tęczówki/zapalenie błony naczyniowej oka) [patrz OSTRZEŻENIA I ŚRODKI ]
- Obrzęk plamki, w tym torbielowaty obrzęk plamki [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce klinicznej.
XALATAN 2,5 ml badano w trzech wieloośrodkowych, randomizowanych, kontrolowanych badaniach klinicznych. Pacjenci otrzymywali 50 µg/ml XALATAN raz na dobę lub 5 mg/ml aktywnego leku porównawczego (tymolol) dwa razy na dobę. Badana populacja pacjentów miała średni wiek 65±10 lat. Siedem procent pacjentów wycofało się przed upływem 6 miesięcy.
Mniej niż 1% pacjentów leczonych XALATAN 2,5 ml wymagało przerwania leczenia z powodu nietolerancji przekrwienia spojówek.
Zdarzenie oczne/oznaki i objawy zapalenia powiek zostały zidentyfikowane jako „często obserwowane” na podstawie analizy danych z badań klinicznych.
Doświadczenie postmarketingowe
Następujące reakcje zostały zidentyfikowane po wprowadzeniu produktu XALATAN do obrotu w praktyce klinicznej. Ponieważ są one zgłaszane dobrowolnie z populacji o nieznanej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstotliwości lub ustalenie związku przyczynowego z narażeniem na lek. Reakcje, które zostały wybrane do włączenia ze względu na ich powagę, częstotliwość zgłaszania, możliwy związek przyczynowy z XALATAN 2,5 ml lub połączenie tych czynników, obejmują:
Zaburzenia układu nerwowego: Zawroty głowy; ból głowy; Toksyczna martwica naskórka
Zaburzenia oka: Zmiany włosa rzęskowego i meszkowego na powiece (zwiększenie długości, grubości, pigmentacji i liczby rzęs); zapalenie rogówki; obrzęk i nadżerki rogówki; zapalenie wewnątrzgałkowe (zapalenie tęczówki/zapalenie błony naczyniowej oka); obrzęk plamki, w tym torbielowaty obrzęk plamki; trichioza; zmiany okołooczodołowe i powiekowe powodujące pogłębienie bruzdy powiekowej; torbiel tęczówki; ciemnienie skóry powiek; zlokalizowana reakcja skórna na powiekach; zapalenie spojówek; pseudopemfigoid spojówki oka
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia: Astma i zaostrzenie astmy; duszność
Zaburzenia skóry i tkanki podskórnej: świąd
Infekcje i infestacje: opryszczkowe zapalenie rogówki
Zaburzenia serca: Dusznica; kołatanie serca; niestabilna dusznica bolesna
Ogólne Zaburzenia i Warunki Miejsca Administracji: Ból w klatce piersiowej
INTERAKCJE Z LEKAMI
Badania in vitro wykazały, że po zmieszaniu kropli do oczu zawierających timerosal z preparatem XALATAN następuje wytrącanie osadu. Jeśli takie leki są stosowane, należy je podawać w odstępie co najmniej pięciu (5) minut.
Nie zaleca się jednoczesnego stosowania dwóch lub więcej prostaglandyn lub analogów prostaglandyn, w tym XALATAN 2,5 ml. Wykazano, że podawanie tych leków zawierających prostaglandyny częściej niż raz dziennie może zmniejszać działanie obniżające IOP lub powodować paradoksalne podwyższenie IOP.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Pigmentacja
Istnieją doniesienia, że XALATAN powoduje zmiany w tkankach pigmentowanych. Najczęściej zgłaszanymi zmianami była zwiększona pigmentacja tęczówki, tkanki okołooczodołowej (powieki) i rzęs. Oczekuje się, że pigmentacja będzie się nasilać w czasie podawania latanoprostu.
Zmiana pigmentacji wynika raczej ze zwiększonej zawartości melaniny w melanocytach niż ze wzrostu liczby melanocytów. Po odstawieniu latanoprostu, pigmentacja tęczówki prawdopodobnie będzie trwała, podczas gdy pigmentacja tkanki okołooczodołowej i zmiany rzęs są odwracalne u niektórych pacjentów. Pacjenci poddawani leczeniu powinni być poinformowani o możliwości nasilonej pigmentacji. Po 5 latach skutki zwiększonej pigmentacji nie są znane [patrz Studia kliniczne ].
Zmiana koloru tęczówki może nie być zauważalna przez kilka miesięcy, a nawet lat. Zazwyczaj brązowa pigmentacja wokół źrenicy rozprzestrzenia się koncentrycznie w kierunku obwodu tęczówki, a cała tęczówka lub jej części stają się bardziej brązowawe. Wydaje się, że leczenie nie ma wpływu na znamiona ani piegi tęczówki. Chociaż leczenie preparatem XALATAN 2,5 ml może być kontynuowane u pacjentów, u których wystąpi zauważalnie zwiększona pigmentacja tęczówki, pacjenci ci powinni być regularnie badani [patrz INFORMACJA O PACJENCIE ].
Zmiany rzęs
XALATAN 2,5ml może stopniowo zmieniać rzęsy i włosy welusowe leczonego oka; zmiany te obejmują zwiększoną długość, grubość, pigmentację, liczbę rzęs lub włosów oraz niewłaściwie ukierunkowany wzrost rzęs. Zmiany rzęs są zwykle odwracalne po zaprzestaniu leczenia [patrz INFORMACJA O PACJENCIE ].
Zapalenie wewnątrzgałkowe
XALATAN 2,5 ml należy stosować ostrożnie u pacjentów z zapaleniem wewnątrzgałkowym w wywiadzie (zapalenie tęczówki/zapalenie błony naczyniowej oka) i zasadniczo nie należy go stosować u pacjentów z czynnym zapaleniem wewnątrzgałkowym, ponieważ stan zapalny może się nasilić.
Obrzęk plamki żółtej
Podczas leczenia preparatem XALATAN zgłaszano obrzęk plamki, w tym torbielowaty obrzęk plamki. XALATAN 2,5 ml należy stosować ostrożnie u pacjentów z bezsoczewkowością, pacjentów z pseudosoczewką z rozdartą tylną torebką soczewki lub u pacjentów ze znanymi czynnikami ryzyka obrzęku plamki.
Opryszczkowe zapalenie rogówki
Podczas leczenia preparatem XALATAN zgłaszano reaktywację zapalenia rogówki wywołanego przez Herpes simplex. XALATAN 2,5 ml należy stosować ostrożnie u pacjentów z opryszczkowym zapaleniem rogówki w wywiadzie. XALATAN 2,5 ml należy unikać w przypadku aktywnego zapalenia rogówki wywołanego wirusem opryszczki pospolitej, ponieważ stan zapalny może ulec zaostrzeniu.
Bakteryjne zapalenie rogówki
Istnieją doniesienia o bakteryjnym zapaleniu rogówki związanym ze stosowaniem wielodawkowych pojemników produktów okulistycznych do stosowania miejscowego. Pojemniki te zostały nieumyślnie zanieczyszczone przez pacjentów, którzy w większości przypadków mieli współistniejącą chorobę rogówki lub uszkodzenie powierzchni nabłonka oka [patrz INFORMACJA O PACJENCIE ].
Używaj z soczewkami kontaktowymi
Soczewki kontaktowe należy usunąć przed podaniem leku XALATAN i można je ponownie założyć po 15 minutach od podania.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Latanoprost nie wykazywał działania rakotwórczego ani u myszy, ani u szczurów, gdy był podawany przez zgłębnik doustny w dawkach do 170 μg/kg/dobę (około 2800-krotność zalecanej maksymalnej dawki dla ludzi) odpowiednio przez okres do 20 i 24 miesięcy.
Latanoprost nie wykazywał działania mutagennego u bakterii, w chłoniaku myszy ani w testach mikrojądrowych u myszy. Aberracje chromosomowe obserwowano in vitro na ludzkich limfocytach. Dodatkowe badania in vitro i in vivo dotyczące nieplanowanej syntezy DNA u szczurów były negatywne.
W badaniach na zwierzętach nie stwierdzono żadnego wpływu latanoprostu na płodność samców lub samic.
Używaj w określonych populacjach
Ciąża
Efekty teratogenne
Ciąża Kategoria C.
Badania reprodukcji przeprowadzono na szczurach i królikach. U królików, częstość występowania 4 z 16 samic nie miała żywotnych płodów przy dawce, która była około 80-krotnie większa od maksymalnej dawki stosowanej u ludzi, a najwyższa dawka niebędąca zarodkiem u królików była około 15-krotnie większa od maksymalnej dawki stosowanej u ludzi.
Nie ma odpowiednich i dobrze kontrolowanych badań u kobiet w ciąży. XALATAN 2,5 ml należy stosować w okresie ciąży tylko wtedy, gdy potencjalna korzyść uzasadnia potencjalne ryzyko dla płodu.
Matki karmiące
Nie wiadomo, czy ten lek lub jego metabolity przenikają do mleka ludzkiego. Ponieważ wiele leków przenika do mleka ludzkiego, należy zachować ostrożność przy podawaniu preparatu XALATAN 2,5 ml kobiecie karmiącej.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność u pacjentów pediatrycznych nie zostały ustalone.
Zastosowanie geriatryczne
Nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między pacjentami w podeszłym wieku i młodszymi.
PRZEDAWKOWAĆ
Infuzja dożylna do 3 mikrogramów/kg u zdrowych ochotników powodowała średnie stężenia w osoczu 200 razy większe niż podczas leczenia klinicznego i nie obserwowano działań niepożądanych. Dożylne dawki od 5,5 do 10 mcg/kg powodowały ból brzucha, zawroty głowy, zmęczenie, uderzenia gorąca, nudności i pocenie się. W przypadku przedawkowania produktu XALATAN leczenie powinno być objawowe.
PRZECIWWSKAZANIA
Znana nadwrażliwość na latanoprost, chlorek benzalkoniowy lub inne składniki tego produktu.
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Latanoprost jest selektywnym prostanoidowym agonistą receptora FP, który, jak się uważa, obniża ciśnienie wewnątrzgałkowe (IOP) poprzez zwiększenie odpływu cieczy wodnistej. Badania na zwierzętach i ludziach sugerują, że głównym mechanizmem działania jest zwiększony odpływ naczyniówkowo-twardówkowy. Podwyższone IOP stanowi główny czynnik ryzyka utraty pola jaskrowego. Im wyższy poziom IOP, tym większe prawdopodobieństwo uszkodzenia nerwu wzrokowego i utraty pola widzenia.
Farmakodynamika
Zmniejszenie IOP u człowieka rozpoczyna się około 3-4 godzin po podaniu, a maksymalny efekt osiąga się po 8-12 godzinach. Redukcja IOP występuje przez co najmniej 24 godziny.
Farmakokinetyka
Wchłanianie
Latanoprost jest wchłaniany przez rogówkę, gdzie prolek estru izopropylowego jest hydrolizowany do postaci kwasowej, aby stać się biologicznie aktywnym.
Dystrybucja
Objętość dystrybucji u ludzi wynosi 0,16 ± 0,02 l/kg. Kwas latanoprostu można zmierzyć w cieczy wodnistej w ciągu pierwszych 4 godzin, aw osoczu dopiero w ciągu pierwszej godziny po podaniu miejscowym. Badania na ludziach wskazują, że maksymalne stężenie w cieczy wodnistej jest osiągane około dwóch godzin po podaniu miejscowym.
Metabolizm
Latanoprost, prolek estru izopropylowego, jest hydrolizowany przez esterazy w rogówce do biologicznie aktywnego kwasu. Aktywny kwas latanoprostu docierający do krążenia ogólnego jest metabolizowany głównie w wątrobie do metabolitów 1,2-dinoru i 1,2,3,4-tetranoru poprzez β-oksydację kwasu tłuszczowego.
Wydalanie
Eliminacja kwasu latanoprostu z ludzkiego osocza jest szybka (t½ = 17 min) zarówno po podaniu dożylnym, jak i miejscowym. Klirens układowy wynosi około 7 ml/min/kg. W wyniku β-oksydacji w wątrobie metabolity są wydalane głównie przez nerki. Około 88% i 98% podanej dawki jest wydalane w moczu odpowiednio po podaniu miejscowym i dożylnym.
Studia kliniczne
Podwyższone podstawowe IOP
U pacjentów ze średnim początkowym IOP wynoszącym 24-25 mmHg, którzy byli leczeni przez 6 miesięcy w wieloośrodkowych, randomizowanych, kontrolowanych badaniach klinicznych, wykazano zmniejszenie IOP o 6-8 mmHg. To zmniejszenie IOP za pomocą preparatu XALATAN 0,005% podawanego raz na dobę było równoważne działaniu tymololu 0,5% podawanego dwa razy na dobę.
Progresja zwiększonej pigmentacji tęczówki
Przeprowadzono 3-letnie otwarte, prospektywne badanie bezpieczeństwa z 2-letnią fazą przedłużenia w celu oceny progresji nasilonej pigmentacji tęczówki przy ciągłym stosowaniu produktu XALATAN raz na dobę jako terapii wspomagającej u 519 pacjentów z jaskrą otwartego kąta. Analiza została oparta na obserwowanej populacji przypadków 380 pacjentów, którzy kontynuowali fazę przedłużenia.
Wyniki wykazały, że początek zauważalnej zwiększonej pigmentacji tęczówki wystąpił w ciągu pierwszego roku leczenia u większości pacjentów, u których rozwinęła się zauważalnie zwiększona pigmentacja tęczówki. Pacjenci nadal wykazywali oznaki narastającej pigmentacji tęczówki przez pięć lat badania. Obserwacja zwiększonej pigmentacji tęczówki nie wpłynęła na częstość, charakter ani nasilenie zdarzeń niepożądanych (innych niż zwiększona pigmentacja tęczówki) zarejestrowanych w badaniu. Redukcja IOP była podobna niezależnie od rozwoju wzmożonej pigmentacji tęczówki w trakcie badania.
INFORMACJA O PACJENCIE
Potencjał do pigmentacji
Poinformuj pacjentów o możliwości zwiększonej brązowej pigmentacji tęczówki, która może być trwała. Należy poinformować pacjentów o możliwości ściemnienia skóry powiek, które może być odwracalne po odstawieniu leku XALATAN [patrz OSTRZEŻENIA I ŚRODKI ].
Możliwość zmiany rzęs
Poinformować pacjentów o możliwości wystąpienia zmian w zakresie rzęs i włosów meszkowych w leczonym oku podczas leczenia preparatem XALATAN. Zmiany te mogą skutkować dysproporcją między długością, grubością, pigmentacją oczu, liczbą rzęs lub włosków meszkowych i/lub kierunkiem wzrostu rzęs. Zmiany rzęs są zwykle odwracalne po zaprzestaniu leczenia.
Obsługa kontenera
Należy poinstruować pacjentów, aby unikali kontaktu końcówki pojemnika dozującego z okiem lub otaczającymi go strukturami, ponieważ może to spowodować zanieczyszczenie końcówki przez powszechnie znane bakterie wywołujące infekcje oka. Poważne uszkodzenie oka, a następnie utrata wzroku może wynikać ze stosowania zanieczyszczonych roztworów [patrz OSTRZEŻENIA I ŚRODKI ].
Kiedy szukać porady lekarza?
Należy poinformować pacjentów, że jeśli wystąpią u nich współistniejące schorzenia oczu (np. uraz lub infekcja) lub przejdą operację oka lub wystąpią jakiekolwiek reakcje oczne, w szczególności zapalenie spojówek i reakcje powiek, powinni natychmiast zasięgnąć porady lekarza w sprawie dalszego stosowania wielodawkowej dawki pojemnik.
Używaj z soczewkami kontaktowymi
Należy poinformować pacjentów, że XALATAN 2,5 ml zawiera chlorek benzalkoniowy, który może być wchłaniany przez soczewki kontaktowe. Soczewki kontaktowe należy zdjąć przed podaniem roztworu. Soczewki można ponownie założyć 15 minut po podaniu XALATAN.
Stosowanie z innymi lekami okulistycznymi
Jeśli stosuje się więcej niż jeden miejscowy lek okulistyczny, leki należy podawać w odstępie co najmniej pięciu (5) minut.
