Leczenie wypadania włosów: Avodart 0.5mg Dutasteride Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Avodart 0,5 mg i jak się go stosuje?
Avodart 0,5 mg jest lekiem na receptę stosowanym w leczeniu objawów przerostu prostaty (łagodnego przerostu prostaty). Avodart można stosować samodzielnie lub z innymi lekami.
Avodart 0,5 mg należy do klasy leków zwanych inhibitorami 5-alfa-reduktazy.
Nie wiadomo, czy Avodart 0,5 mg jest bezpieczny i skuteczny u dzieci.
Jakie są skutki uboczne Avodart?
Skutki uboczne Avodart 0,5 mg obejmują:
- pokrzywka,
- trudności w oddychaniu,
- obrzęk twarzy lub gardła,
- gorączka,
- ból gardła,
- płonące oczy,
- ból skóry i
- czerwona lub fioletowa wysypka skórna z powstawaniem pęcherzy i łuszczeniem się
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze działania niepożądane leku Avodart 0,5 mg obejmują:
- obniżone libido (popęd seksualny),
- zmniejszona ilość nasienia uwalnianego podczas stosunku,
- impotencja (problemy z uzyskaniem lub utrzymaniem erekcji) oraz
- tkliwość lub powiększenie piersi
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe działania niepożądane leku Avodart. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
AVODART 0,5 mg to syntetyczny związek 4-azasteroidowy, który jest selektywnym inhibitorem izoform 5 alfa-reduktazy steroidowej typu 1 i typu 2, wewnątrzkomórkowego enzymu, który przekształca testosteron w DHT.
Dutasteryd jest chemicznie oznaczony jako (5α,17β)-N-{2,5 bis(trifluorometylo)fenylo}-3-okso-4-azaandrost-1-eno-17-karboksyamid. Empiryczny wzór dutasterydu to C27H30F6N2O2, reprezentujący masę cząsteczkową 528,5 o następującym wzorze strukturalnym:
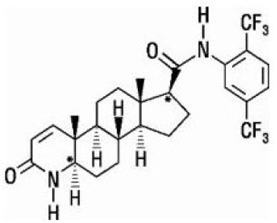
Dutasteryd jest proszkiem o barwie białej do jasnożółtej o temperaturze topnienia od 242° do 250°C. Jest rozpuszczalny w etanolu (44 mg/ml), metanolu (64 mg/ml) i glikolu polietylenowym 400 (3 mg/ml), ale jest nierozpuszczalny w wodzie.
Każda kapsułka miękka żelatynowa AVODART 0,5 mg podawana doustnie zawiera 0,5 mg dutasterydu rozpuszczonego w mieszaninie mono-diglicerydów kwasu kaprylowego/kaprynowego i butylohydroksytoluenu. Nieaktywne substancje pomocnicze w otoczce kapsułki to tlenek żelaza (żółty), żelatyna (z certyfikowanych źródeł bydlęcych wolnych od BSE), gliceryna i dwutlenek tytanu. Miękkie kapsułki żelatynowe są nadrukowane jadalnym czerwonym tuszem.
WSKAZANIA
Monoterapia
AVODART (dutasteryd) miękkie kapsułki żelatynowe są wskazane w leczeniu objawowego łagodnego rozrostu gruczołu krokowego (BPH) u mężczyzn z przerostem gruczołu krokowego w celu:
- poprawić objawy,
- zmniejszyć ryzyko ostrego zatrzymania moczu (AUR) oraz
- zmniejszyć ryzyko konieczności operacji związanej z BPH.
Połączenie z antagonistą alfa-adrenergicznym
AVODART w skojarzeniu z antagonistą receptorów alfa-adrenergicznych, tamsulosyną, jest wskazany w leczeniu objawowego BPH u mężczyzn z przerostem prostaty.
Ograniczenia użytkowania
AVODART 0,5 mg nie jest zatwierdzony do zapobiegania rakowi prostaty.
DAWKOWANIE I SPOSÓB PODAWANIA
Kapsułki należy połykać w całości, nie rozgryzać ani nie otwierać, ponieważ kontakt z zawartością kapsułki może spowodować podrażnienie błony śluzowej jamy ustnej i gardła. AVODART można podawać z jedzeniem lub bez jedzenia.
Monoterapia
Zalecana dawka leku AVODART to 1 kapsułka (0,5 mg) przyjmowana raz na dobę.
Połączenie z antagonistą alfa-adrenergicznym
Zalecana dawka leku AVODART 0,5 mg to 1 kapsułka (0,5 mg) przyjmowana raz na dobę i tamsulosyna 0,4 mg przyjmowana raz na dobę.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
0,5 mg, nieprzezroczyste, ciemnożółte kapsułki żelatynowe z nadrukiem „GX CE2” czerwonym tuszem po jednej stronie.
Składowania i stosowania
AVODART miękkie kapsułki żelatynowe 0,5 mg to podłużne, nieprzezroczyste, ciemnożółte kapsułki żelatynowe z nadrukiem „GX CE2” z czerwonym jadalnym tuszem po jednej stronie, pakowane w butelki po 30 ( NDC 0173-0712-15) i 90 ( NDC 0173-0712-04) z zamknięciem zabezpieczającym przed dziećmi.
Przechowywać w 25°C (77°F); wycieczki dozwolone do 15 ° do 30 ° C (59 ° do 86 ° F) [patrz Temperatura pokojowa kontrolowana przez USP ].
Dutasteryd jest wchłaniany przez skórę. Kapsułki AVODART 0,5 mg nie powinny być obsługiwane przez kobiety w ciąży lub mogące zajść w ciążę ze względu na możliwość wchłaniania dutasterydu i wynikające z tego potencjalne ryzyko dla rozwoju płodu płci męskiej [patrz OSTRZEŻENIA I ŚRODKI ].
Wyprodukowano dla: GlaxoSmithKline Research Triangle Park. Poprawiono: styczeń 2020 r.
SKUTKI UBOCZNE
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniu klinicznym innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Z badań klinicznych produktu AVODART 0,5 mg w monoterapii lub w skojarzeniu z tamsulosyną:
- Najczęstszymi działaniami niepożądanymi zgłaszanymi u osób otrzymujących produkt AVODART 0,5 mg były impotencja, zmniejszenie libido, zaburzenia piersi (w tym powiększenie i tkliwość piersi) oraz zaburzenia wytrysku. Najczęstszymi działaniami niepożądanymi zgłaszanymi u osób otrzymujących leczenie skojarzone (AVODART 0,5 mg plus tamsulosyna) były impotencja, zmniejszenie libido, zaburzenia piersi (w tym powiększenie i tkliwość piersi), zaburzenia wytrysku i zawroty głowy. Zaburzenia wytrysku występowały znacznie częściej u osób otrzymujących terapię skojarzoną (11%) w porównaniu z osobami otrzymującymi AVODART (2%) lub tamsulosynę (4%) w monoterapii.
- Wycofanie z badania z powodu działań niepożądanych wystąpiło u 4% pacjentów otrzymujących AVODART 0,5 mg i 3% pacjentów otrzymujących placebo w badaniach kontrolowanych placebo z AVODART. Najczęstszym działaniem niepożądanym prowadzącym do wycofania się z badania była impotencja (1%).
- badaniu klinicznym oceniającym terapię skojarzoną przerwanie badania z powodu działań niepożądanych wystąpiło u 6% pacjentów otrzymujących terapię skojarzoną (AVODART plus tamsulosyna) i 4% pacjentów otrzymujących AVODART 0,5 mg lub tamsulosin w monoterapii. Najczęstszym działaniem niepożądanym we wszystkich grupach terapeutycznych, prowadzącym do wycofania się z badania, były zaburzenia erekcji (od 1 do 1,5%).
Monoterapia
Ponad 4300 mężczyzn z BPH zostało losowo przydzielonych do grupy otrzymującej placebo lub dawki dobowe produktu AVODART 0,5 mg w 3 identycznych, 2-letnich, kontrolowanych placebo, podwójnie zaślepionych badaniach fazy III dotyczących leczenia, po których następowało 2-letnie badanie otwarte rozbudowa. W okresie leczenia metodą podwójnie ślepej próby 2167 mężczyzn zostało poddanych działaniu preparatu AVODART 0,5 mg, w tym 1772 przez 1 rok i 1510 przez 2 lata. Uwzględniając rozszerzenia otwarte, 1009 mężczyzn było narażonych na lek AVODART 0,5 mg przez 3 lata, a 812 było narażonych na 4 lata. Populacja była w wieku od 47 do 94 lat (średnia wieku 66 lat), a ponad 90% było rasy białej. W Tabeli 1 podsumowano kliniczne działania niepożądane zgłoszone u co najmniej 1% pacjentów otrzymujących AVODART i z większą częstością niż u pacjentów otrzymujących placebo.
Leczenie długoterminowe (do 4 lat)
Rak prostaty o wysokim stopniu złośliwości
Badanie REDUCE było randomizowanym, podwójnie zaślepionym, kontrolowanym placebo badaniem, w którym wzięło udział 8231 mężczyzn w wieku od 50 do 75 lat z PSA w surowicy od 2,5 ng/ml do 10 ng/ml i ujemną biopsją prostaty w ciągu ostatnich 6 miesięcy. Pacjenci zostali losowo przydzieleni do grupy otrzymującej placebo (n = 4126) lub dawki 0,5 mg preparatu AVODART (n = 4 105) przez okres do 4 lat. Średnia wieku wynosiła 63 lata, a 91% było rasy białej. Pacjenci przeszli nakazane przez protokół biopsje gruczołu krokowego zgodnie z harmonogramem po 2 i 4 latach leczenia lub mieli biopsje „z określonej przyczyny” w nieplanowanych terminach, jeśli jest to klinicznie wskazane. Wystąpiła większa częstość występowania raka prostaty w skali 8-10 w skali Gleasona u mężczyzn otrzymujących AVODART (1,0%) w porównaniu z mężczyznami otrzymującymi placebo (0,5%) [patrz WSKAZANIA I ZASTOSOWANIE , OSTRZEŻENIA I ŚRODKI ]. W 7-letnim badaniu klinicznym kontrolowanym placebo z innym inhibitorem 5-alfa-reduktazy (finasteryd 5 mg, PROSCAR) zaobserwowano podobne wyniki dla raka gruczołu krokowego w skali 8-10 w skali Gleasona (finasteryd 1,8% w porównaniu z placebo 1,1%).
Nie wykazano korzyści klinicznych u pacjentów z rakiem prostaty leczonych preparatem AVODART.
Zaburzenia układu rozrodczego i piersi
W 3 kluczowych, kontrolowanych placebo badaniach BPH z zastosowaniem produktu AVODART 0,5 mg, trwających 4 lata, nie było dowodów na nasilenie działań niepożądanych na tle seksualnym (impotencja, zmniejszenie libido i zaburzenia wytrysku) lub zaburzeń piersi związanych z wydłużonym czasem leczenia. Wśród tych 3 badań był 1 przypadek raka piersi w grupie dutasterydu i 1 przypadek w grupie placebo. W 4-letnim badaniu CombAT lub 4-letnim badaniu REDUCE nie zgłoszono żadnego przypadku raka piersi w żadnej grupie terapeutycznej.
Związek między długotrwałym stosowaniem dutasterydu a nowotworami piersi u mężczyzn jest obecnie nieznany.
Połączenie z terapią alfa-blokerami (CombAT)
Ponad 4800 mężczyzn z BPH zostało losowo przydzielonych do grupy otrzymującej 0,5 mg AVODART 0,5 mg, 0,4 mg tamsulosyny lub leczenie skojarzone (0,5 mg AVODART plus 0,4 mg tamsulosyny) podawane raz dziennie w 4-letnim badaniu z podwójnie ślepą próbą. Ogółem 1623 pacjentów otrzymywało monoterapię preparatem AVODART; 1611 osób otrzymało monoterapię tamsulosyną; a 1610 osobników otrzymało terapię skojarzoną. Populacja była w wieku od 49 do 88 lat (średnia wieku 66 lat), a 88% było rasy białej. W Tabeli 2 podsumowano działania niepożądane zgłoszone u co najmniej 1% pacjentów w grupie leczenia skojarzonego i z większą częstością niż u pacjentów otrzymujących monoterapię produktem AVODART 0,5 mg lub tamsulosyną.
Zawał serca
CombAT, po 4 latach leczenia, częstość występowania złożonej niewydolności serca w grupie terapii skojarzonej (12/1610; 0,7%) była wyższa niż w obu grupach monoterapii: AVODART 0,5 mg, 2/1623 (0,1%) i tamsulosyna, 9/1611 (0,6%). Złożona niewydolność serca była również badana w oddzielnym 4-letnim badaniu kontrolowanym placebo oceniającym AVODART u mężczyzn z ryzykiem rozwoju raka prostaty. Częstość występowania niewydolności serca u osób przyjmujących AVODART 0,5 mg wynosiła 0,6% (26/4105) w porównaniu z 0,4% (15/4126) u osób otrzymujących placebo. Większość pacjentów z niewydolnością serca w obu badaniach miała choroby współistniejące związane ze zwiększonym ryzykiem niewydolności serca. Dlatego kliniczne znaczenie nierównowagi liczbowej w niewydolności serca nie jest znane. Nie ustalono związku przyczynowego między produktem AVODART w monoterapii lub w skojarzeniu z tamsulosyną a niewydolnością serca. W żadnym z badań nie zaobserwowano braku równowagi w częstości występowania zdarzeń niepożądanych ze strony układu sercowo-naczyniowego.
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane po dopuszczeniu produktu AVODART do obrotu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek. Reakcje te zostały wybrane do włączenia ze względu na połączenie ich ciężkości, częstości zgłaszania lub potencjalnego związku przyczynowego z produktem AVODART.
Zaburzenia układu immunologicznego
Reakcje nadwrażliwości, w tym wysypka, świąd, pokrzywka, obrzęk miejscowy, ciężkie reakcje skórne i obrzęk naczynioruchowy.
Nowotwory
Męski rak piersi.
Zaburzenia psychiczne
Depresyjny nastrój.
Zaburzenia układu rozrodczego i piersi
Ból jąder i obrzęk jąder.
INTERAKCJE Z LEKAMI
Inhibitory cytochromu P450 3A
Dutasteryd jest intensywnie metabolizowany u ludzi przez izoenzymy cytochromu P450 (CYP)3A4 i CYP3A5. Nie badano wpływu silnych inhibitorów CYP3A4 na dutasteryd. Ze względu na możliwość interakcji lekowych, należy zachować ostrożność przepisując produkt AVODART pacjentom przyjmującym silne, przewlekłe inhibitory enzymu CYP3A4 (np. rytonawir) [patrz FARMAKOLOGIA KLINICZNA ].
Antagoniści alfa-adrenergiczne
Podawanie produktu AVODART w skojarzeniu z tamsulosyną lub terazosyną nie ma wpływu na farmakokinetykę któregokolwiek z antagonistów receptorów alfa-adrenergicznych w stanie stacjonarnym. Nie oceniano wpływu podawania tamsulosyny lub terazosyny na parametry farmakokinetyczne dutasterydu.
Antagoniści kanału wapniowego
Jednoczesne podawanie werapamilu lub diltiazemu zmniejsza klirens dutasterydu i prowadzi do zwiększonej ekspozycji na dutasteryd. Zmiana ekspozycji na dutasteryd nie jest uważana za klinicznie istotną. Nie zaleca się dostosowywania dawki [patrz FARMAKOLOGIA KLINICZNA ].
Cholestyramina
Podanie pojedynczej dawki 5 mg produktu AVODART 0,5 mg, a następnie 1 godzinę później 12 g cholestyraminy nie wpływa na względną biodostępność dutasterydu [patrz FARMAKOLOGIA KLINICZNA ].
Digoksyna
Produkt AVODART 0,5 mg nie zmienia farmakokinetyki digoksyny w stanie stacjonarnym przy jednoczesnym podawaniu w dawce 0,5 mg/dobę przez 3 tygodnie [patrz FARMAKOLOGIA KLINICZNA ].
Warfaryna
Jednoczesne podawanie produktu AVODART 0,5 mg/dobę przez 3 tygodnie z warfaryną nie zmienia farmakokinetyki izomerów S- lub R-warfaryny w stanie stacjonarnym ani nie zmienia wpływu warfaryny na czas protrombinowy [patrz FARMAKOLOGIA KLINICZNA ].
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Wpływ na antygen specyficzny dla prostaty (PSA) i zastosowanie PSA w wykrywaniu raka prostaty
badaniach klinicznych produkt AVODART 0,5 mg zmniejszał stężenie PSA w surowicy o około 50% w ciągu 3 do 6 miesięcy leczenia. Spadek ten był przewidywalny w całym zakresie wartości PSA u osób z objawowym BPH, chociaż może się różnić u poszczególnych osób. AVODART 0,5 mg może również powodować zmniejszenie stężenia PSA w surowicy w przypadku raka prostaty. Aby zinterpretować seryjne PSA u mężczyzn przyjmujących AVODART 0,5 mg, należy ustalić nową wartość wyjściową PSA co najmniej 3 miesiące po rozpoczęciu leczenia, a następnie okresowo monitorować PSA. Każdy potwierdzony wzrost od najniższej wartości PSA podczas stosowania preparatu AVODART może sygnalizować obecność raka prostaty i powinien być oceniany, nawet jeśli poziom PSA nadal mieści się w normalnym zakresie dla mężczyzn nieprzyjmujących inhibitora 5-alphareduktazy. Niezgodność z AVODART może również wpłynąć na wyniki testu PSA.
Aby zinterpretować wyizolowaną wartość PSA u mężczyzny leczonego preparatem AVODART 0,5 mg przez 3 miesiące lub dłużej, wartość PSA należy podwoić w celu porównania z wartościami prawidłowymi u mężczyzn nieleczonych. Stosunek wolnego-całkowitego PSA (procent wolnego PSA) pozostaje stały, nawet pod wpływem preparatu AVODART. Jeśli klinicyści zdecydują się na użycie procentu wolnego PSA jako pomocy w wykrywaniu raka prostaty u mężczyzn otrzymujących AVODART, nie wydaje się konieczne dostosowanie jego wartości.
Jednoczesne podawanie dutasterydu i tamsulosyny powodowało podobne zmiany PSA w surowicy jak w monoterapii dutasterydem.
Zwiększone ryzyko raka prostaty o wysokim stopniu złośliwości
U mężczyzn w wieku od 50 do 75 lat z wcześniejszą negatywną biopsją z powodu raka prostaty i wyjściowym stężeniem PSA pomiędzy 2,5 ng/ml a 10,0 ng/ml przyjmujących preparat AVODART w 4-letnim badaniu Reduction by Dutasteride of Prostate Cancer Events (REDUCE) zwiększona częstość występowania raka prostaty w skali 810 w skali Gleasona w porównaniu z mężczyznami przyjmującymi placebo (AVODART 1,0% w porównaniu z placebo 0,5%) [patrz WSKAZANIA I ZASTOSOWANIE , DZIAŁANIA NIEPOŻĄDANE ]. W 7-letnim badaniu klinicznym kontrolowanym placebo z innym inhibitorem 5-alfa-reduktazy (finasteryd 5 mg, PROSCAR) zaobserwowano podobne wyniki dla raka gruczołu krokowego w skali 8-10 w skali Gleasona (finasteryd 1,8% w porównaniu z placebo 1,1%).
Inhibitory 5-alfa-reduktazy mogą zwiększać ryzyko rozwoju raka prostaty o wysokim stopniu złośliwości. Nie ustalono, czy wpływ inhibitorów 5-alfa-reduktazy na zmniejszenie objętości gruczołu krokowego lub czynniki związane z badaniami miały wpływ na wyniki tych badań.
Ocena pod kątem innych chorób urologicznych
Przed rozpoczęciem leczenia produktem AVODART 0,5 mg należy wziąć pod uwagę inne schorzenia urologiczne, które mogą powodować podobne objawy. Ponadto może współistnieć BPH i rak prostaty.
Transdermalna ekspozycja na AVODART 0,5 mg u kobiet w ciąży – ryzyko dla płodu męskiego
Kapsułki AVODART nie powinny być obsługiwane przez kobiety w ciąży lub mogące być w ciąży. Dutasteryd może być wchłaniany przez skórę i może powodować niezamierzone narażenie płodu i potencjalne ryzyko dla płodu płci męskiej. W przypadku kontaktu kobiety w ciąży z nieszczelnymi kapsułkami dutasterydu, miejsce kontaktu należy natychmiast przemyć wodą z mydłem [patrz Używaj w określonych populacjach ]. Dutasteryd może być wchłaniany przez skórę w oparciu o badania na zwierzętach [patrz Toksykologia niekliniczna ].
Krwiodawstwo
Mężczyźni leczeni preparatem AVODART nie powinni oddawać krwi przed upływem co najmniej 6 miesięcy od przyjęcia ostatniej dawki. Celem tego odroczonego okresu jest zapobieganie podawaniu dutasterydu ciężarnej samicy transfuzji.
Wpływ na charakterystykę nasienia
Wpływ dutasterydu 0,5 mg/dobę na charakterystykę nasienia oceniano u zdrowych mężczyzn przez 52 tygodnie leczenia i 24 tygodnie po zakończeniu leczenia. Po 52 tygodniach, w porównaniu z placebo, leczenie dutasterydem spowodowało średnie zmniejszenie całkowitej liczby plemników, objętości nasienia i ruchliwości plemników; wpływ na całkowitą liczbę plemników nie był odwracalny po 24 tygodniach obserwacji. Stężenie plemników i morfologia plemników nie uległy zmianie, a średnie wartości wszystkich parametrów nasienia pozostawały w normalnym zakresie we wszystkich punktach czasowych. Kliniczne znaczenie wpływu dutasterydu na charakterystykę nasienia dla płodności indywidualnej pacjentki nie jest znane [patrz Używaj w określonych populacjach ].
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( INFORMACJA O PACJENCIE ).
Monitorowanie PSA
Poinformuj pacjentów, że AVODART obniża poziom PSA w surowicy o około 50% w ciągu 3 do 6 miesięcy terapii, chociaż może się to różnić w zależności od osoby. W przypadku pacjentów poddawanych badaniom przesiewowym PSA wzrost stężenia PSA podczas leczenia lekiem AVODART może sygnalizować obecność raka prostaty i powinien zostać oceniony przez lekarza [patrz OSTRZEŻENIA I ŚRODKI ].
Zwiększone ryzyko raka prostaty o wysokim stopniu złośliwości
Poinformuj pacjentów, że u mężczyzn leczonych inhibitorami 5 alfa-reduktazy (wskazanymi w leczeniu BPH), w tym AVODART 0,5 mg, wystąpił wzrost częstości występowania raka prostaty o wysokim stopniu złośliwości, w porównaniu z pacjentami otrzymującymi placebo w badaniach oceniających stosowanie tych leków. leki zmniejszające ryzyko raka prostaty [patrz WSKAZANIA I ZASTOSOWANIE , OSTRZEŻENIA I ŚRODKI , DZIAŁANIA NIEPOŻĄDANE ].
Przezskórna ekspozycja na AVODART u kobiet w ciąży lub potencjalnie w ciąży – ryzyko dla płodu męskiego
Należy poinformować pacjentki, że kapsułki AVODART 0,5 mg nie powinny być obsługiwane przez kobiety w ciąży lub mogące zajść w ciążę ze względu na możliwość wchłaniania dutasterydu i wynikające z tego potencjalne ryzyko dla rozwijającego się płodu płci męskiej. Dutasteryd może być wchłaniany przez skórę i może spowodować niezamierzone narażenie płodu. W przypadku kontaktu kobiety w ciąży lub potencjalnie w ciąży z wyciekającymi kapsułkami produktu AVODART 0,5 mg, miejsce kontaktu należy natychmiast przemyć wodą z mydłem [patrz OSTRZEŻENIA I ŚRODKI , Używaj w określonych populacjach ].
Wpływ na parametry nasienia
Poinformuj mężczyzn, że AVODART 0,5 mg może wpływać na charakterystykę nasienia, ale wpływ na płodność jest nieznany [patrz OSTRZEŻENIA I ŚRODKI , Używaj w określonych populacjach ].
Krwiodawstwo
Poinformuj mężczyzn leczonych preparatem AVODART 0,5 mg, że nie powinni oddawać krwi przez co najmniej 6 miesięcy po przyjęciu ostatniej dawki, aby zapobiec przyjmowaniu dutasterydu przez kobiety w ciąży poprzez transfuzję krwi [patrz OSTRZEŻENIA I ŚRODKI ]. Poziomy dutasterydu w surowicy są wykrywalne przez 4 do 6 miesięcy po zakończeniu leczenia [patrz FARMAKOLOGIA KLINICZNA ].
AVODART jest znakiem towarowym należącym do lub licencjonowanym przez grupę spółek GSK.
Inne wymienione marki są znakami towarowymi należącymi do ich odpowiednich właścicieli lub licencjonowanymi przez nich i nie są własnością ani nie są licencjonowane przez grupę spółek GSK. Twórcy tych marek nie są związani i nie popierają grupy firm GSK ani jej produktów.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Karcynogeneza
Dwuletnie badanie rakotwórczości przeprowadzono na myszach B6C3F1 przy dawkach 3, 35, 250 i 500 mg/kg/dobę dla samców oraz 3, 35 i 250 mg/kg/dobę dla samic; zaobserwowano zwiększoną częstość występowania łagodnych gruczolaków wątrobowokomórkowych przy dawce 250 mg/kg/dzień (290-krotność MRHD przy dawce 0,5 mg dziennie) tylko u samic myszy. Dwa z 3 głównych metabolitów ludzkich wykryto u myszy. Ekspozycja na te metabolity u myszy jest mniejsza niż u ludzi lub nie jest znana.
2-letnim badaniu rakotwórczości na szczurach Han Wistar przy dawkach 1,5, 7,5 i 53 mg/kg/dobę u samców oraz 0,8, 6,3 i 15 mg/kg/dobę u samic zaobserwowano wzrost liczby komórek Leydiga. gruczolaki w jądrach przy 135-krotności MRHD (53 mg/kg/dzień i więcej). Zwiększona częstość występowania hiperplazji komórek Leydiga była obecna przy 52-krotności MRHD (dawki samców szczurów 7,5 mg/kg/dobę i większe). Wykazano dodatnią korelację między zmianami proliferacyjnymi w komórkach Leydiga a wzrostem stężenia krążącego hormonu luteinizującego w przypadku inhibitorów 5-alfa-reduktazy, co jest zgodne z wpływem na oś podwzgórze-przysadka-jądra po zahamowaniu 5-alfa-reduktazy. Przy dawkach rakotwórczych poziom hormonu luteinizującego u szczurów był zwiększony o 167%. W tym badaniu główne metabolity u ludzi były testowane pod kątem rakotwórczości przy około 1 do 3 razy większej od oczekiwanej ekspozycji klinicznej.
Mutageneza
Dutasteryd badano pod kątem genotoksyczności w teście mutagenezy bakteryjnej (test Amesa), teście aberracji chromosomowych w komórkach jajnika chomika chińskiego oraz teście mikrojądrowym u szczurów. Wyniki nie wykazały żadnego potencjału genotoksycznego leku macierzystego. Dwa główne metabolity ludzkie były również ujemne w teście Amesa lub w skróconym teście Amesa.
Upośledzenie płodności
Leczenie dojrzałych płciowo samców szczura dutasterydem w dawce 0,1 razy większej niż MRHD (dawki zwierzęce 0,05 mg/kg/dobę lub większe przez okres do 31 tygodni) na podstawie średniego stężenia w surowicy powodowało zależne od dawki i czasu zmniejszenie płodności we wszystkich dawkach ; zmniejszona liczba plemników w ogonie najądrza (bezwzględna), ale nie stężenie plemników (przy 50 i 500 mg/kg/dzień); zmniejszenie masy najądrza, prostaty i pęcherzyków nasiennych; oraz zmiany mikroskopowe (wakuolizacja cytoplazmatyczna nabłonka kanalików w najądrzach i/lub zmniejszona zawartość cytoplazmatyczna nabłonka, odpowiadająca zmniejszonej aktywności wydzielniczej w prostacie i pęcherzykach nasiennych) w narządach rozrodczych we wszystkich dawkach przy braku toksyczności ojcowskiej. Wpływ na płodność został odwrócony w 6. tygodniu regeneracji we wszystkich dawkach, a liczba plemników była normalna pod koniec 14-tygodniowego okresu regeneracji. Zmiany mikroskopowe nie były już obecne w 14 Tygodniu Rekonwalescencji przy 0,1-krotności MRHD i częściowo ustąpiły w pozostałych grupach terapeutycznych. Niskie poziomy dutasterydu (0,6 do 17 ng/ml) wykryto w surowicy nieleczonych samic szczurów kojarzonych z leczonymi samcami (10 do 500 mg/kg/dobę przez 29 do 30 tygodni), które są 16 do 110 razy większe niż MRHD na podstawie średnie stężenie w surowicy. U samic szczurów nieleczonych samic szczurów kojarzonych z leczonymi samcami szczurów nie wystąpiła feminizacja, mimo że u samic szczurów obserwowano wykrywalne stężenie dutasterydu we krwi.
badaniu płodności u samic szczurów, którym podawano dawki 4 tygodnie przed kryciem przez wczesną ciążę, doustne podawanie dutasterydu w dawkach 0,05, 2,5, 12,5 i 30 mg/kg/dobę powodowało zmniejszenie wielkości miotu z powodu zwiększonej resorpcji i feminizacji. płodów płci męskiej (zmniejszenie odległości odbytowo-płciowej) przy 2 do 10-krotności MRHD (dawki zwierzęce 2,5 mg/kg/dobę lub większe) na podstawie średniego stężenia w surowicy, w obecności toksyczności matczynej (zmniejszony przyrost masy ciała). Masa ciała płodu była również zmniejszona o około 0,02 razy MRHD (dawka szczura 0,05 mg/kg/dobę lub większa) w oparciu o średnie stężenie w surowicy, bez poziomu bez efektu, przy braku toksyczności matczynej.
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
AVODART 0,5 mg jest przeciwwskazany do stosowania w ciąży, ponieważ może zaszkodzić płodowi męskiemu [patrz PRZECIWWSKAZANIA ]. AVODART nie jest wskazany do stosowania u kobiet.
AVODART 0,5 mg to inhibitor 5 alfa-reduktazy, który zapobiega konwersji testosteronu do dihydrotestosteronu (DHT), hormonu niezbędnego do prawidłowego rozwoju męskich narządów płciowych. Oczekiwaną fizjologiczną konsekwencją zahamowania tej przemiany są nieprawidłowości w narządach płciowych płodów płci męskiej. Wyniki te są podobne do obserwacji u niemowląt płci męskiej z genetycznym niedoborem 5 alfa-reduktazy.
W ogólnej populacji Stanów Zjednoczonych szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2% do 4% i 15% do 20%.
badaniach na zwierzętach dotyczących reprodukcji dutasteryd podawany szczurom lub królikom w okresie organogenezy w dawce mniejszej niż maksymalna zalecana dawka u ludzi (MRHD) wynosząca 0,5 mg na dobę, przy braku działania toksycznego na matkę, hamował prawidłowy rozwój zewnętrznych narządów płciowych u potomstwa płci męskiej. Przy 15-krotności MRHD u szczurów obserwowano przedłużającą się ciążę, zmniejszoną masę narządów rozrodczych i opóźnione dojrzewanie płciowe u potomstwa płci męskiej, przy poziomach bez efektów niższych niż MRHD wynoszące 0,5 mg na dobę. Zaobserwowano również zwiększoną masę łożyska u królików, przy czym poziom bez efektu był niższy niż MRHD 0,5 mg na dobę (patrz Dane ).
Chociaż dutasteryd jest wydzielany do nasienia ludzkiego, stężenie leku u partnerki jest około 100 razy mniejsze niż stężenia powodujące nieprawidłowości w męskich narządach płciowych w badaniach na zwierzętach (patrz Dane ). U małp, którym podczas organogenezy podawano dawki we krwi porównywalne lub wyższe, na które według szacunków narażona jest ludzka partnerka, zewnętrzne narządy płciowe potomstwa płci męskiej nie były naruszone. Nie zaobserwowano feminizacji u samców nieleczonych samic szczurów kojarzonych z leczonymi samcami szczurów, mimo że u samic szczurów obserwowano wykrywalny poziom dutasterydu we krwi [patrz Toksykologia niekliniczna ].
Dane
Dane ludzkie
Najwyższe zmierzone stężenie dutasterydu w nasieniu u leczonych mężczyzn wynosiło 14 ng/ml. Chociaż dutasteryd wykrywa się w nasieniu, przy założeniu, że kobieta ważąca 50 kg narażona jest na 5 ml nasienia i 100% wchłanianie, oczekiwane stężenie dutasterydu we krwi kobiety w nasieniu wyniesie około 0,0175 ng/ml. Stężenie to jest około 100 razy mniejsze niż stężenie we krwi powodujące nieprawidłowości w męskich genitaliach w badaniach na zwierzętach. Dutasteryd w wysokim stopniu wiąże się z białkami nasienia ludzkiego (ponad 96%), co może zmniejszać ilość dutasterydu dostępnego do wchłaniania z pochwy.
Dane zwierząt
badaniu dotyczącym rozwoju zarodka i płodu u szczurów, doustne podawanie dutasterydu w dawce 10 razy mniejszej niż MRHD 0,5 mg na dobę (na podstawie średniego stężenia we krwi u mężczyzn) powodowało feminizację męskich narządów płciowych u płodu (zmniejszenie odległości odbytowo-płciowej po 0,05 mg /kg/dzień, przy braku poziomu niepowodującego zmian) przy braku toksyczności matczynej. Ponadto u płodów matek leczonych dawkami 2,5 mg/kg/dobę lub większymi (około 15-krotność MRHD) wystąpił rozwój brodawek sutkowych, spodziectwo i rozdęte gruczoły napletka. Zmniejszoną masę ciała płodu i związane z tym opóźnione kostnienie w obecności toksyczności matczynej (zmniejszony przyrost masy ciała) obserwowano przy ekspozycji matki około 15 razy większej niż MRHD (dawka 2,5 mg/kg/dobę lub większa). Wzrost liczby martwo urodzonych szczeniąt zaobserwowano u matek leczonych dawką 30 mg/kg/dzień (około 111-krotność MRHD), przy poziomie bez efektu 12,5 mg/kg/dzień.
badaniu dotyczącym rozwoju zarodka i płodu królików dawki 28 razy większe niż MRHD (dawki 30 mg/kg/dobę lub większe), w oparciu o średnie stężenie we krwi u mężczyzn, podawano doustnie w dniach od 7 do 29 ciąży (podczas organogenezy i późnej okres rozwoju zewnętrznych narządów płciowych). Ocena histologiczna brodawek narządów płciowych płodów wykazała oznaki feminizacji płodu płci męskiej oraz zrośnięte kości czaszki i zwiększoną masę łożyska przy wszystkich dawkach przy braku toksyczności matczynej. Drugie badanie rozwoju zarodkowo-płodowego u królików, którym podawano przez całą ciążę (organogenezę i późniejszy okres rozwoju zewnętrznych narządów płciowych [od 6 do 29 dni ciąży]) dawkę 0,3-krotności MRHD (dawki 0,05 mg/kg/dobę lub większe, bez poziom efektu), również dostarczyły dowodów na feminizację narządów płciowych u płodów płci męskiej i zwiększenie masy łożyska przy wszystkich dawkach przy braku toksyczności matczynej.
badaniu dotyczącym rozwoju zarodkowo-płodowego ciężarne małpy rezus otrzymywały dożylnie podczas organogenezy (dni ciąży od 20 do 100) poziom dutasterydu we krwi porównywalny lub wyższy od szacowanej ekspozycji na dutasteryd ludzkiej partnerki. Dutasteryd podawano w dniach ciąży od 20 do 100 (podczas organogenezy) w dawkach 400, 780, 1325 lub 2010 ng/dobę (12 małp/grupę). Nie zaobserwowano feminizacji zewnętrznych narządów płciowych samców potomstwa małp. Przy największej badanej dawce obserwowano zmniejszenie masy nadnerczy u płodu, zmniejszenie masy gruczołu krokowego u płodu oraz zwiększenie masy jajników i jąder u płodu. W oparciu o najwyższe zmierzone stężenie dutasterydu w nasieniu u leczonych mężczyzn (14 ng/ml), dawki te u małpy stanowią do 16-krotności potencjalnej maksymalnej ekspozycji kobiety o wadze 50 kg na 5 ml nasienia dziennie z dutasterydu- leczonego mężczyzny, przy założeniu 100% wchłaniania. Poziomy dawek (na podstawie ng/kg) podawane małpom w tym badaniu są od 32 do 186 razy większe od dawki nominalnej (ng/kg), na którą samica byłaby potencjalnie narażona poprzez nasienie. Nie wiadomo, czy króliki lub małpy rezus wytwarzają którykolwiek z głównych metabolitów u ludzi.
badaniu rozwoju przed- i pourodzeniowego jamy ustnej u szczurów zaobserwowano feminizację męskich narządów płciowych. Zmniejszenie odległości odbytowo-płciowej zaobserwowano przy 0,05-krotności MRHD i większej (0,05 mg/kg/dobę i więcej), przy braku poziomu bez efektu, w oparciu o średnie poziomy we krwi u mężczyzn jako oszacowanie AUC. Spodziectwo i rozwój brodawek sutkowych obserwowano przy dawce 2,5 mg/kg/dobę lub większej (14-krotność MRHD lub większej, z poziomem bez efektu przy 0,05 mg/kg/dobę). Dawki 2,5 mg/kg/dobę i większe powodowały również wydłużenie ciąży u samic będących rodzicami, wydłużenie czasu do oddzielenia balano-napletka u potomstwa płci męskiej, skrócenie czasu do drożności pochwy u potomstwa płci żeńskiej oraz zmniejszenie gruczołu krokowego i masy pęcherzyków nasiennych u samców potomstwa. Zwiększona liczba martwych urodzeń i zmniejszona żywotność noworodków u potomstwa odnotowano przy dawce 30 mg/kg/dobę (102-krotność MRHD w obecności toksyczności matczynej [zmniejszona masa ciała]).
Laktacja
Podsumowanie ryzyka
AVODART nie jest wskazany do stosowania u kobiet. Brak dostępnych informacji na temat obecności dutasterydu w mleku kobiecym, wpływu na dziecko karmione piersią lub wpływu na produkcję mleka.
Kobiety i mężczyźni o potencjale rozrodczym
Bezpłodność
Mężczyźni
Wpływ dutasterydu 0,5 mg/dobę na charakterystykę nasienia oceniano u zdrowych ochotników w wieku od 18 do 52 lat (n = 27 dutasteryd, n = 23 placebo) przez 52 tygodnie leczenia i 24 tygodnie po zakończeniu leczenia. Po 52 tygodniach średnie procentowe zmniejszenie w stosunku do wartości wyjściowej całkowitej liczby plemników, objętości nasienia i ruchliwości plemników wyniosło odpowiednio 23%, 26% i 18% w grupie dutasterydu po uwzględnieniu zmian w stosunku do wartości wyjściowych w grupie placebo. Stężenie plemników i morfologia plemników nie uległy zmianie. Po 24 tygodniach obserwacji średnia procentowa zmiana w całkowitej liczbie plemników w grupie dutasterydu pozostała o 23% niższa niż wartość wyjściowa. Podczas gdy średnie wartości dla wszystkich parametrów nasienia we wszystkich punktach czasowych pozostawały w normalnych zakresach i nie spełniały wcześniej zdefiniowanych kryteriów dla klinicznie istotnej zmiany (30%), u 2 pacjentów w grupie dutasterydu zaobserwowano zmniejszenie liczby plemników o ponad 90% w stosunku do wartości wyjściowej w 52 tygodnie, z częściową rekonwalescencją po 24-tygodniowej obserwacji. Kliniczne znaczenie wpływu dutasterydu na charakterystykę nasienia dla płodności poszczególnych pacjentek nie jest znane [patrz OSTRZEŻENIA I ŚRODKI ].
Zastosowanie pediatryczne
AVODART 0,5 mg nie jest wskazany do stosowania u dzieci. Bezpieczeństwo i skuteczność u pacjentów pediatrycznych nie zostały ustalone.
Zastosowanie geriatryczne
Spośród 2167 mężczyzn leczonych produktem AVODART 0,5 mg w 3 badaniach klinicznych 60% było w wieku 65 lat i starszych, a 15% było w wieku 75 lat i starszych. Nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między tymi osobami a młodszymi osobami. Inne zgłoszone doświadczenia kliniczne nie wykazały różnic w odpowiedziach między pacjentami starszymi i młodszymi, ale nie można wykluczyć większej wrażliwości niektórych osób starszych [patrz FARMAKOLOGIA KLINICZNA ].
Zaburzenia czynności nerek
Nie ma konieczności dostosowania dawki produktu AVODART 0,5 mg u pacjentów z zaburzeniami czynności nerek [patrz FARMAKOLOGIA KLINICZNA ].
Niewydolność wątroby
Nie badano wpływu zaburzeń czynności wątroby na farmakokinetykę dutasterydu. Ponieważ dutasteryd jest intensywnie metabolizowany, ekspozycja może być większa u pacjentów z zaburzeniami czynności wątroby. Jednak w badaniu klinicznym, w którym 60 pacjentów otrzymywało 5 mg (10-krotność dawki terapeutycznej) dziennie przez 24 tygodnie, nie zaobserwowano dodatkowych działań niepożądanych w porównaniu z tymi obserwowanymi po dawce terapeutycznej 0,5 mg [patrz FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
W badaniach na ochotnikach pojedyncze dawki dutasterydu do 40 mg (80-krotność dawki terapeutycznej) podawane przez 7 dni nie budziły istotnych obaw dotyczących bezpieczeństwa. W badaniu klinicznym dawki dobowe 5 mg (10-krotność dawki terapeutycznej) podawano 60 pacjentom przez 6 miesięcy bez dodatkowych działań niepożądanych poza tymi obserwowanymi przy dawkach terapeutycznych 0,5 mg.
Nie ma swoistego antidotum na dutasteryd. Dlatego w przypadku podejrzenia przedawkowania należy zastosować leczenie objawowe i wspomagające, biorąc pod uwagę długi okres półtrwania dutasterydu.
PRZECIWWSKAZANIA
AVODART 0,5 mg jest przeciwwskazany do stosowania w:

- Ciąża. Stosowanie dutasterydu jest przeciwwskazane u kobiet w ciąży. W badaniach toksycznego wpływu na reprodukcję i rozwój zwierząt, dutasteryd hamował rozwój zewnętrznych narządów płciowych męskich płodów. Dlatego AVODART 0,5 mg może powodować uszkodzenie płodu, gdy jest podawany kobiecie w ciąży [patrz OSTRZEŻENIA I ŚRODKI , Używaj w określonych populacjach ].
- Pacjenci z wcześniej wykazaną klinicznie istotną nadwrażliwością (np. ciężkie reakcje skórne, obrzęk naczynioruchowy) na AVODART lub inne inhibitory 5 alfa-reduktazy [patrz DZIAŁANIA NIEPOŻĄDANE ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Dutasteryd hamuje konwersję testosteronu do DHT. DHT jest androgenem odpowiedzialnym przede wszystkim za początkowy rozwój i późniejsze powiększenie gruczołu krokowego. Testosteron jest przekształcany w DHT przez enzym 5 alfa-reduktazę, który występuje w postaci 2 izoform, typu 1 i typu 2. Izoenzym typu 2 jest głównie aktywny w tkankach rozrodczych, podczas gdy izoenzym typu 1 jest również odpowiedzialny za konwersję testosteronu w skóra i wątroba.
Dutasteryd jest konkurencyjnym i swoistym inhibitorem izoenzymów alfa-reduktazy typu 1 i typu 2, z którymi tworzy stabilny kompleks enzymatyczny. Dysocjacja z tego kompleksu została oceniona w warunkach in vitro i in vivo i jest niezwykle powolna. Dutasteryd nie wiąże się z ludzkim receptorem androgenowym.
Farmakodynamika
Wpływ na 5 alfa-dihydrotestosteron i testosteron
Maksymalny wpływ dobowych dawek dutasterydu na redukcję DHT jest zależny od dawki i obserwowany w ciągu 1 do 2 tygodni. Po 1 i 2 tygodniach codziennego podawania 0,5 mg dutasterydu mediana stężenia DHT w surowicy zmniejszyła się odpowiednio o 85% i 90%. U pacjentów z BPH leczonych dutasterydem 0,5 mg/dobę przez 4 lata, mediana zmniejszenia DHT w surowicy wyniosła 94% po 1 roku, 93% po 2 latach i 95% zarówno po 3, jak i 4 latach. Mediana wzrostu testosteronu w surowicy wyniosła 19% zarówno po roku, jak i po 2 latach, 26% po 3 latach i 22% po 4 latach, ale średnie i mediany pozostały w zakresie fizjologicznym.
pacjentów z BPH leczonych dutasterydem w dawce 5 mg/dobę lub placebo przez okres do 12 tygodni przed przezcewkową resekcją gruczołu krokowego średnie stężenia DHT w tkance gruczołu krokowego były znacząco niższe w grupie otrzymującej dutasteryd w porównaniu z placebo (784 i 5793 pg/g). odpowiednio, P
Dorośli mężczyźni z genetycznie dziedziczonym niedoborem alfa-reduktazy typu 2 również mają obniżone poziomy DHT. Te samce z niedoborem 5 alfa-reduktazy mają przez całe życie mały gruczoł krokowy i nie rozwijają BPH. Z wyjątkiem towarzyszących wad układu moczowo-płciowego obecnych przy urodzeniu, u tych osób nie zaobserwowano innych nieprawidłowości klinicznych związanych z niedoborem 5 alfa-reduktazy.
Wpływ na inne hormony
zdrowych ochotników 52 tygodnie leczenia dutasterydem 0,5 mg/dobę (n = 26) nie spowodowało klinicznie istotnych zmian w porównaniu z placebo (n = 23) w zakresie globuliny wiążącej hormony płciowe, estradiolu, hormonu luteinizującego, hormonu folikulotropowego, tyroksyna (wolna T4) i dehydroepiandrosteron. Statystycznie istotne, skorygowane do wartości wyjściowych średnie wzrosty w porównaniu z placebo zaobserwowano dla całkowitego testosteronu po 8 tygodniach (97,1 ng/dl, p
Inne efekty
Panel lipidowy w osoczu i gęstość mineralną kości oceniano po 52 tygodniach podawania dutasterydu w dawce 0,5 mg raz na dobę zdrowym ochotnikom. Nie było zmian w gęstości mineralnej kości mierzonej za pomocą absorpcjometrii rentgenowskiej o podwójnej energii w porównaniu z placebo lub wartością podstawową. Ponadto dutasteryd nie wpływał na profil lipidowy osocza (tj. całkowity cholesterol, lipoproteiny o małej gęstości, lipoproteiny o dużej gęstości, triglicerydy). Nie zaobserwowano klinicznie istotnych zmian w odpowiedzi hormonów nadnerczy na stymulację hormonem adrenokortykotropowym (ACTH) w podgrupie populacji (n = 13) w rocznym badaniu zdrowych ochotników.
Farmakokinetyka
Wchłanianie
Po podaniu pojedynczej dawki 0,5 mg w miękkiej kapsułce żelatynowej czas do osiągnięcia maksymalnego stężenia dutasterydu w surowicy (Tmax) występuje w ciągu 2 do 3 godzin. Całkowita biodostępność u 5 zdrowych osób wynosi około 60% (zakres: 40% do 94%). Gdy lek podaje się z pokarmem, maksymalne stężenie w surowicy zmniejszyło się o 10% do 15%. To zmniejszenie nie ma znaczenia klinicznego.
Dystrybucja
Dane farmakokinetyczne po podaniu pojedynczej i wielokrotnej dawki doustnej wskazują, że dutasteryd ma dużą objętość dystrybucji (300 do 500 l). Dutasteryd w dużym stopniu wiąże się z albuminami osocza (99,0%) i kwaśną glikoproteiną alfa-1 (96,6%).
W badaniu zdrowym ochotnikom (n = 26) otrzymującym 0,5 mg/dobę dutasterydu przez 12 miesięcy, stężenie dutasterydu w nasieniu wynosiło średnio 3,4 ng/ml (zakres: 0,4 do 14 ng/ml) po 12 miesiącach i podobnie jak w surowicy osiągnęło -stan stężenia po 6 miesiącach. Średnio po 12 miesiącach 11,5% stężenia dutasterydu w surowicy zostało przeniesione do nasienia.
Metabolizm i eliminacja
Dutasteryd jest intensywnie metabolizowany u ludzi. Badania in vitro wykazały, że dutasteryd jest metabolizowany przez izoenzymy CYP3A4 i CYP3A5. Oba te izoenzymy wytwarzały metabolity 4'-hydroksydutasterydu, 6-hydroksydutasterydu i 6,4'-dihydroksydutasterydu. Ponadto metabolit 15-hydroksydutasterydu był tworzony przez CYP3A4. Dutasteryd nie jest metabolizowany in vitro przez izoenzymy CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 i CYP2E1 ludzkiego cytochromu P450. W surowicy ludzkiej po podaniu do stanu stacjonarnego niezmieniony dutasteryd, 3 główne metabolity (4'-hydroksydutasteryd, 1,2-dihydrodutasteryd i 6-hydroksydutasteryd) oraz 2 mniejsze metabolity (6,4'-dihydroksydutasteryd i 15 -hydroksydutasteryd), jak oceniono na podstawie odpowiedzi spektrometrii masowej. Absolutna stereochemia addycji hydroksylowych w pozycjach 6 i 15 nie jest znana. In vitro, metabolity 4'-hydroksydutasterydu i 1,2-dihydrodutasterydu są znacznie słabsze niż dutasteryd przeciwko obu izoformom ludzkiej 5-alfa-reduktazy. Aktywność 6β-hydroksydutasterydu jest porównywalna z aktywnością dutasterydu.
Dutasteryd i jego metabolity były wydalane głównie z kałem. W procentach dawki było około 5% niezmienionego dutasterydu (~1% do ~15%) i 40% jako metabolity związane z dutasterydem (~2% do ~90%). W moczu wykryto jedynie śladowe ilości niezmienionego dutasterydu (
Okres półtrwania dutasterydu w końcowej fazie eliminacji wynosi około 5 tygodni w stanie stacjonarnym. Średnie stężenie dutasterydu w surowicy w stanie stacjonarnym wynosiło 40 ng/ml po podaniu 0,5 mg/dobę przez 1 rok. Po codziennym dawkowaniu stężenia dutasterydu w surowicy osiągają 65% stężenia w stanie stacjonarnym po 1 miesiącu i około 90% po 3 miesiącach. Ze względu na długi okres półtrwania dutasterydu stężenia w surowicy pozostają wykrywalne (powyżej 0,1 ng/ml) przez okres do 4 do 6 miesięcy po zakończeniu leczenia.
Określone populacje
Pacjenci pediatryczni
Farmakokinetyka dutasterydu nie była badana u osób w wieku poniżej 18 lat.
Pacjenci geriatryczni
Nie ma konieczności dostosowania dawki u osób w podeszłym wieku. Farmakokinetykę i farmakodynamikę dutasterydu oceniano u 36 zdrowych mężczyzn w wieku od 24 do 87 lat po podaniu pojedynczej dawki 5 mg dutasterydu. W tym badaniu po podaniu pojedynczej dawki okres półtrwania dutasterydu wydłużał się wraz z wiekiem (około 170 godzin u mężczyzn w wieku od 20 do 49 lat, około 260 godzin u mężczyzn w wieku od 50 do 69 lat i około 300 godzin u mężczyzn w wieku powyżej 70 lat). Spośród 2167 mężczyzn leczonych dutasterydem w 3 kluczowych badaniach, 60% było w wieku 65 lat i więcej, a 15% było w wieku 75 lat i więcej. Nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między tymi pacjentami a młodszymi pacjentami.
Pacjenci płci męskiej i żeńskiej
AVODART jest przeciwwskazany w ciąży i nie jest wskazany do stosowania u kobiet [patrz PRZECIWWSKAZANIA , OSTRZEŻENIA I ŚRODKI ]. Nie badano farmakokinetyki dutasterydu u kobiet.
Grupy rasowe i etniczne
Nie badano wpływu rasy na farmakokinetykę dutasterydu.
Pacjenci z niewydolnością nerek
Nie badano wpływu zaburzeń czynności nerek na farmakokinetykę dutasterydu. Jednak mniej niż 0,1% dawki 0,5 mg dutasterydu w stanie stacjonarnym jest wykrywane w moczu ludzkim, dlatego nie przewiduje się dostosowania dawki u pacjentów z zaburzeniami czynności nerek.
Pacjenci z niewydolnością wątroby
Nie badano wpływu zaburzeń czynności wątroby na farmakokinetykę dutasterydu. Ponieważ dutasteryd jest intensywnie metabolizowany, ekspozycja może być większa u pacjentów z zaburzeniami czynności wątroby.
Badania interakcji leków
Inhibitory cytochromu P450
Nie przeprowadzono klinicznych badań interakcji leków oceniających wpływ inhibitorów enzymu CYP3A na farmakokinetykę dutasterydu. Jednak na podstawie danych in vitro, stężenie dutasterydu we krwi może się zwiększać w obecności inhibitorów CYP3A4/5, takich jak rytonawir, ketokonazol, werapamil, diltiazem, cymetydyna, troleandomycyna i cyprofloksacyna.
Dutasteryd nie hamuje metabolizmu in vitro modelowych substratów głównych izoenzymów ludzkiego cytochromu P450 (CYP1A2, CYP2C9, CYP2C19, CYP2D6 i CYP3A4) w stężeniu 1000 ng/ml, 25 razy większym niż stężenia w surowicy w stanie stacjonarnym u ludzi .
Antagoniści alfa-adrenergiczne
W jednosekwencyjnym, krzyżowym badaniu u zdrowych ochotników podawanie tamsulosyny lub terazosyny w skojarzeniu z preparatem AVODART nie miało wpływu na farmakokinetykę w stanie stacjonarnym żadnego z antagonistów receptorów alfa-adrenergicznych. Chociaż nie oceniano wpływu podawania tamsulosyny lub terazosyny na parametry farmakokinetyczne dutasterydu, procentowa zmiana stężenia DHT była podobna w przypadku samego preparatu AVODART 0,5 mg w porównaniu z leczeniem skojarzonym.
Antagoniści kanału wapniowego
analizie farmakokinetyki populacyjnej zaobserwowano zmniejszenie klirensu dutasterydu podczas jednoczesnego podawania z inhibitorami CYP3A4 werapamilem (-37%, n = 6) i diltiazemem (-44%, n = 5). W przeciwieństwie do tego, nie zaobserwowano zmniejszenia klirensu, gdy amlodypinę, innego antagonistę kanału wapniowego, który nie jest inhibitorem CYP3A4, podawano jednocześnie z dutasterydem (+7%, n = 4).
Zmniejszenie klirensu, a następnie zwiększenie ekspozycji na dutasteryd w obecności werapamilu i diltiazemu nie jest uważane za istotne klinicznie. Nie zaleca się dostosowywania dawki.
Cholestyramina
Podanie pojedynczej dawki 5 mg produktu AVODART 0,5 mg, a następnie 1 godzinę później 12 g cholestyraminy nie miało wpływu na względną biodostępność dutasterydu u 12 zdrowych ochotników.
Digoksyna
W badaniu z udziałem 20 zdrowych ochotników produkt AVODART 0,5 mg nie zmieniał farmakokinetyki digoksyny w stanie stacjonarnym, gdy był podawany jednocześnie w dawce 0,5 mg/dobę przez 3 tygodnie.
Warfaryna
badaniu z udziałem 23 zdrowych ochotników 3-tygodniowe leczenie produktem AVODART 0,5 mg/dobę nie zmieniło farmakokinetyki izomerów S- lub R-warfaryny w stanie stacjonarnym ani nie zmieniło wpływu warfaryny na czas protrombinowy w przypadku podawania z warfaryną.
Inne terapie towarzyszące
Chociaż nie przeprowadzono specyficznych badań interakcji z innymi związkami, około 90% pacjentów w 3 randomizowanych, podwójnie zaślepionych, kontrolowanych placebo badaniach dotyczących bezpieczeństwa i skuteczności, otrzymujących AVODART przyjmowało jednocześnie inne leki. Nie można było przypisać klinicznie istotnych działań niepożądanych skojarzeniu preparatu AVODART z jednoczesnym leczeniem, gdy preparat AVODART podawano jednocześnie z lekami przeciwhiperlipidemicznymi, inhibitorami konwertazy angiotensyny (ACE), lekami blokującymi receptory beta-adrenergiczne, blokerami kanału wapniowego, kortykosteroidami, lekami moczopędnymi, niesteroidowymi lekami leki przeciwzapalne (NLPZ), inhibitory fosfodiesterazy typu V i antybiotyki chinolonowe.
Toksykologia i/lub farmakologia zwierząt
Badania toksykologiczne ośrodkowego układu nerwowego
szczurów i psów wielokrotne doustne podawanie dutasterydu powodowało u niektórych zwierząt objawy nieswoistej, odwracalnej, ośrodkowej toksyczności bez towarzyszących zmian histopatologicznych przy ekspozycji odpowiednio 425- i 315-krotnie większej niż oczekiwana ekspozycja kliniczna (dla leku macierzystego). .
Absorpcja skórna królika
W badaniu farmakokinetyki skórnej na królikach, wchłanianie przez skórę dutasterydu w CAPMUL (oleinian glicerolu) u królików skutkowało stężeniem w surowicy od 2,7 do 40,5 mcg/h/ml dla dawek odpowiednio 1 do 20 mg/ml lub 56% do 100% zastosowanego dutasterydu do wchłonięcia w warunkach okluzji i długotrwałego działania. Miękkie kapsułki żelatynowe AVODART podawane doustnie zawierają 0,5 mg dutasterydu rozpuszczonego w mieszaninie mono-diglicerydów kwasu kaprylowego/kaprynowego i butylohydroksytoluenu. Dutasteryd w wodzie był minimalnie wchłaniany u królików (2000 mg/kg).
Studia kliniczne
Monoterapia
AVODART 0,5 mg/dobę (n = 2167) lub placebo (n = 2158) oceniano u mężczyzn z BPH w trzech 2-letnich wieloośrodkowych badaniach kontrolowanych placebo, z podwójnie ślepą próbą, z których każde było 2-letnie n = 2340). Ponad 90% badanej populacji było rasy białej. Badani byli w wieku co najmniej 50 lat z PSA w surowicy ≥1,5 ng/ml i
Wpływ na wyniki objawów
Objawy oceniano ilościowo za pomocą AUA-SI, kwestionariusza, który ocenia objawy ze strony układu moczowego (niepełne opróżnianie, częstotliwość, nieciągłość, parcia naglące, słaby strumień, naprężenie i nokturia) poprzez ocenę w skali od 0 do 5, co daje łączny możliwy wynik 35, z wyższe wartości liczbowe całkowitych objawów reprezentujące większe nasilenie objawów. Wyjściowy wynik AUA-SI w 3 badaniach wynosił około 17 jednostek w obu leczonych grupach.
Pacjenci otrzymujący dutasteryd osiągnęli statystycznie istotną poprawę objawów w porównaniu z placebo do 3. miesiąca w 1 badaniu i do 12. miesiąca w pozostałych 2 głównych badaniach. W miesiącu 12. średni spadek w stosunku do wartości wyjściowej w całkowitej punktacji objawów AUA-SI w 3 badaniach zbiorczych wyniósł -3,3 jednostki dla dutasterydu i -2,0 jednostki dla placebo, przy średniej różnicy między 2 grupami leczenia wynoszącej -1,3 (zakres: -1,1 do -1,5 jednostki w każdej z 3 prób, P
Badania te zostały zaprojektowane prospektywnie w celu oceny wpływu na objawy w oparciu o wielkość prostaty na początku badania. U mężczyzn z objętością gruczołu krokowego ≥40 cm3 średnie zmniejszenie wyniosło -3,8 jednostki dla dutasterydu i -1,6 jednostki dla placebo, przy średniej różnicy między 2 grupami leczenia wynoszącej -2,2 w miesiącu 24. U mężczyzn z objętością gruczołu krokowego
Rycina 1: Zmiana punktacji AUA-SI od wartości początkowej (zbiorcze badania randomizowane, podwójnie zaślepione, kontrolowane placebo)
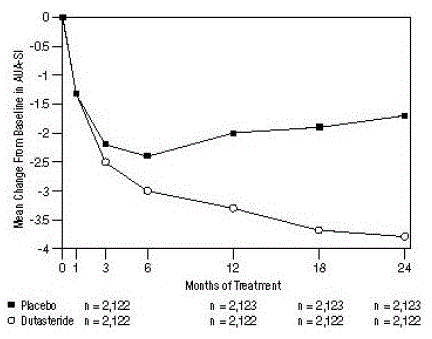
wynik AUA-SI waha się od 0 do 35.
Wpływ na ostre zatrzymanie moczu i potrzebę operacji związanych z BPH
Skuteczność oceniano również po 2 latach leczenia na podstawie częstości występowania AUR wymagającego cewnikowania oraz urologicznej interwencji chirurgicznej związanej z BPH. W porównaniu z placebo, AVODART wiązał się ze statystycznie znamiennie niższą częstością występowania AUR (1,8% dla AVODART w porównaniu z 4,2% dla placebo, p
Rycina 2: Odsetek pacjentów, u których wystąpiło ostre zatrzymanie moczu w okresie 24 miesięcy (zbiorcze badania randomizowane, podwójnie zaślepione, kontrolowane placebo)
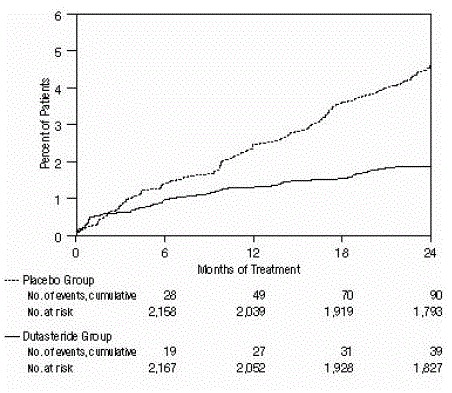
Rycina 3: Odsetek pacjentów poddanych operacji łagodnego rozrostu gruczołu krokowego w okresie 24 miesięcy (łącznie randomizowane, podwójnie zaślepione, kontrolowane placebo)
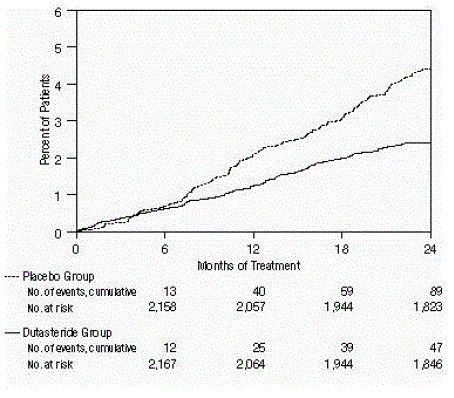
Wpływ na objętość prostaty
Do rozpoczęcia badania wymagana była objętość prostaty co najmniej 30 cm3 mierzona za pomocą ultrasonografii przezodbytniczej. Średnia objętość prostaty w chwili rozpoczęcia badania wynosiła około 54 cm3.
Statystycznie istotne różnice (AVODART 0,5 mg w porównaniu z placebo) odnotowano przy najwcześniejszym pomiarze objętości gruczołu krokowego po leczeniu w każdym badaniu (miesiąc 1, miesiąc 3 lub miesiąc 6) i utrzymywały się one do miesiąca 24. W miesiącu 12 średnia procentowa zmiana objętość prostaty w 3 badaniach zbiorczych wyniosła -24,7% dla dutasterydu i -3,4% dla placebo; średnia różnica (dutasteryd minus placebo) wyniosła -21,3% (zakres: -21,0% do -21,6% w każdym z 3 badań, p
Rycina 4: Procentowa zmiana objętości gruczołu krokowego od wartości początkowej (zbiorcze badania randomizowane, podwójnie zaślepione, kontrolowane placebo)
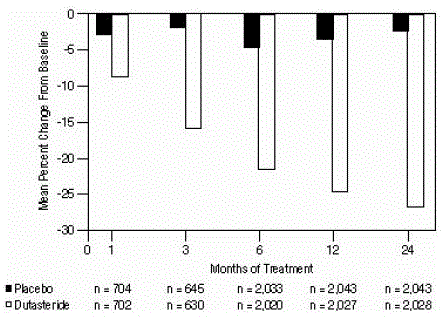
Wpływ na maksymalny przepływ moczu
Do włączenia do badania wymagane było średnie szczytowe natężenie przepływu moczu (Qmax) wynoszące ≤15 ml/s. Qmax wynosił około 10 ml/s na początku badania w 3 kluczowych badaniach.
Różnice między 2 grupami były statystycznie istotne w porównaniu z wartościami wyjściowymi w miesiącu 3 we wszystkich 3 badaniach i utrzymywały się do miesiąca 12. W miesiącu 12 średni wzrost Qmax w 3 połączonych badaniach wyniósł 1,6 ml/s dla produktu AVODART 0,5 mg i 0,7 ml /sek dla placebo; średnia różnica (dutasteryd minus placebo) wyniosła 0,8 ml/s (zakres: 0,7 do 1,0 ml/s w każdym z 3 badań, p
Rycina 5: Zmiana Qmax w stosunku do wartości początkowej (zbiorcze badania randomizowane, podwójnie zaślepione, kontrolowane placebo)
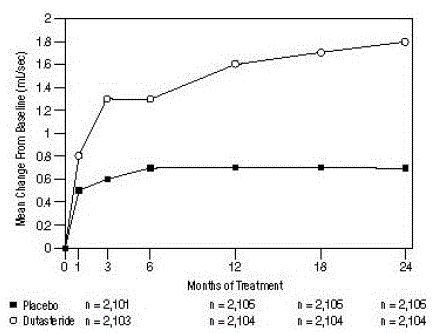
Podsumowanie badań klinicznych
Dane z 3 dużych, dobrze kontrolowanych badań skuteczności wykazują, że leczenie preparatem AVODART (0,5 mg raz na dobę) zmniejsza ryzyko interwencji chirurgicznej zarówno związanej z AUR, jak i BPH w porównaniu z placebo, łagodzi objawy związane z BPH, zmniejsza objętość prostaty i zwiększa maksymalny szybkości przepływu moczu. Dane te sugerują, że AVODART 0,5 mg hamuje proces chorobowy BPH u mężczyzn z powiększoną prostatą.
Połączenie z terapią alfa-blokerami (CombAT)
Skuteczność terapii skojarzonej (AVODART 0,5 mg/dobę plus tamsulosyna 0,4 mg/dobę, n = 1610) porównano z samym AVODART 0,5 mg (n = 1623) lub samą tamsulosyną (n = 1611) w 4-letnim, wieloośrodkowym, randomizowanym , podwójnie ślepa próba. Kryteria włączenia do badania były podobne do podwójnie ślepych, kontrolowanych placebo badań skuteczności monoterapii opisanych w punkcie 14.1. Osiemdziesiąt osiem procent (88%) włączonej do badania populacji było rasy białej. Około 52% badanych było wcześniej narażonych na leczenie 5-alfa-reduktazy – inhibitorem lub antagonistą alfa-adrenergicznym. Spośród 4844 pacjentów losowo przydzielonych do leczenia, 69% pacjentów w grupie skojarzonej, 67% w grupie otrzymującej AVODART 0,5 mg i 61% w grupie tamsulosyny ukończyło 4-letnie leczenie metodą podwójnie ślepej próby.
Wpływ na wynik objawów
Objawy oceniano ilościowo za pomocą pierwszych 7 pytań międzynarodowego wskaźnika objawów prostaty (IPSS) (identycznego z AUA-SI). Punktacja wyjściowa wynosiła około 16,4 jednostek dla każdej grupy leczenia. Terapia skojarzona była statystycznie lepsza od każdej z terapii w monoterapii pod względem zmniejszającej się punktacji objawów w 24. miesiącu, głównym punkcie czasowym dla tego punktu końcowego. W 24. miesiącu średnie zmiany w stosunku do wartości początkowych (±SD) w całkowitej punktacji objawów IPSS wynosiły -6,2 (±7,14) dla kombinacji, -4,9 (±6,81) dla AVODART i -4,3 (±7,01) dla tamsulosyny, ze średnią różnicą pomiędzy skojarzeniem a AVODART 0,5 mg -1,3 jednostki (P
Rysunek 6: Zmiana międzynarodowego wskaźnika objawów prostaty w stosunku do wartości wyjściowej w okresie 48 miesięcy (badanie randomizowane, podwójnie zaślepione, w grupach równoległych [badanie CombAT])
![International Prostate Symptom Score Change from Baseline over a 48Month Period (Randomized, Double-blind, Parallel-Group Trial [CombAT Trial]) - Illustration](/pics/4bcfcb802ee95960e9a1ee78c2411b43.jpg)
Wpływ na ostre zatrzymanie moczu lub potrzebę operacji związanej z BPH
Po 4 latach leczenia terapia skojarzona produktem AVODART 0,5 mg i tamsulosyną nie przyniosła korzyści w porównaniu z monoterapią preparatem AVODART pod względem zmniejszenia częstości występowania AUR lub operacji związanych z BPH.
Wpływ na maksymalny przepływ moczu
Wartość wyjściowa Qmax wynosiła około 10,7 ml/s dla każdej grupy leczenia. Terapia skojarzona była statystycznie lepsza niż każda z metod monoterapii pod względem zwiększania Qmax w 24. miesiącu, głównym punkcie czasowym dla tego punktu końcowego. W miesiącu 24 średni wzrost Qmax od wartości początkowej (±SD) wyniósł 2,4 (±5,26) ml/s dla kombinacji, 1,9 (±5,10) ml/s dla produktu AVODART 0,5 mg i 0,9 (±4,57) ml/s dla tamsulosyną, przy czym średnia różnica między leczeniem skojarzonym a produktem AVODART wynosi 0,5 ml/s (p = 0,003; [95% CI: 0,17; 0,84]), a między leczeniem skojarzonym a tamsulosyną wynosi 1,5 ml/s (p
Dodatkowa poprawa Qmax terapii skojarzonej w porównaniu z monoterapią produktem AVODART 0,5 mg nie była już statystycznie istotna w miesiącu 48.
Rysunek 7: Zmiana Qmax od wartości wyjściowej w okresie 24 miesięcy (randomizowana, podwójnie zaślepiona, w grupach równoległych [badanie CombAT])
![Qmax Change from Baseline over a 24-Month Period (Randomized, Double-blind, Parallel-Group Trial [CombAT Trial]) - Illustration](/pics/9d0401d150227885f5ff562b375f3e80.jpg)
Wpływ na objętość prostaty
Średnia objętość prostaty w momencie rozpoczęcia badania wynosiła około 55 cm3. W miesiącu 24, głównym punkcie czasowym dla tego punktu końcowego, średnie procentowe zmiany objętości gruczołu krokowego względem wartości wyjściowych (±SD) wynosiły -26,9% (±22,57) dla terapii skojarzonej, -28,0% (±24,88) dla produktu AVODART 0,5 mg i 0% (±31,14) dla tamsulosyny, przy średniej różnicy między leczeniem skojarzonym a produktem AVODART 0,5 mg wynoszącą 1,1% (p = NS; [95% CI: -0,6; 2,8]), a między leczeniem skojarzonym a tamsulosyną wynoszącą -26,9% (p
INFORMACJA O PACJENCIE
AVODART (av o dart) (dutasteryd) kapsułki
AVODART 0,5 mg jest przeznaczony do stosowania wyłącznie przez mężczyzn.
Przeczytaj te informacje dla pacjenta przed rozpoczęciem przyjmowania leku AVODART 0,5 mg i za każdym razem, gdy otrzymujesz uzupełnienie. Mogą pojawić się nowe informacje. Informacje te nie zastępują rozmowy z lekarzem na temat Twojego stanu zdrowia lub leczenia.
Co to jest AVODART 0,5 mg?
AVODART 0,5 mg jest lekiem na receptę zawierającym dutasteryd. Preparat AVODART 0,5 mg stosuje się w leczeniu objawów łagodnego rozrostu gruczołu krokowego (BPH) u mężczyzn z przerostem gruczołu krokowego w celu:
- poprawić objawy,
- zmniejszyć ryzyko ostrego zatrzymania moczu (całkowite zablokowanie przepływu moczu),
- zmniejszyć ryzyko konieczności operacji związanej z BPH.
Kto NIE powinien przyjmować leku AVODART?
Nie stosować leku AVODART, jeśli:
- w ciąży lub może zajść w ciążę. AVODART 0,5 mg może zaszkodzić nienarodzonemu dziecku. Kobiety w ciąży nie powinny dotykać kapsułek AVODART. Jeśli kobieta w ciąży z dzieckiem płci męskiej dostanie do organizmu wystarczającą ilość produktu AVODART 0,5 mg przez połknięcie lub dotknięcie produktu AVODART, dziecko płci męskiej może urodzić się z nieprawidłowymi narządami płciowymi. W przypadku kontaktu kobiety w ciąży lub kobiety w wieku rozrodczym z wyciekającymi kapsułkami produktu AVODART 0,5 mg, miejsce kontaktu należy natychmiast przemyć wodą z mydłem.
- dziecko lub nastolatek.
- uczulony na dutasteryd lub którykolwiek ze składników leku AVODART. Pełny wykaz składników leku AVODART znajduje się na końcu tej ulotki.
- uczulony na inne inhibitory 5 alfa-reduktazy, na przykład tabletki PROSCAR (finasteryd) ®.
O czym powinienem powiedzieć lekarzowi przed przyjęciem leku AVODART 0,5 mg?
Przed przyjęciem leku AVODART 0,5 mg należy poinformować lekarza, jeśli:
- masz problemy z wątrobą
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym o lekach na receptę i bez recepty, witaminach i suplementach ziołowych. AVODART i inne leki mogą wzajemnie na siebie oddziaływać, powodując działania niepożądane. Lek AVODART 0,5 mg może wpływać na działanie innych leków, a inne leki mogą wpływać na działanie leku AVODART 0,5 mg.
Poznaj leki, które przyjmujesz. Zachowaj ich listę, aby pokazać swojemu lekarzowi i farmaceucie, kiedy otrzymasz nowy lek.
Jak powinienem przyjmować lek AVODART?
- Przyjmować 1 kapsułkę AVODART raz dziennie.
- Kapsułki AVODART 0,5 mg należy połknąć w całości. Nie należy kruszyć, żuć ani otwierać kapsułek leku AVODART 0,5 mg, ponieważ zawartość kapsułki może podrażniać usta, usta lub gardło.
- Lek AVODART 0,5 mg można przyjmować z posiłkiem lub bez posiłku.
- Jeśli pominiesz dawkę, możesz ją przyjąć później tego samego dnia. Nie należy uzupełniać pominiętej dawki, przyjmując 2 dawki następnego dnia.
Czego powinienem unikać podczas przyjmowania leku AVODART 0,5 mg?
- Nie należy oddawać krwi podczas przyjmowania leku AVODART lub przez 6 miesięcy po jego odstawieniu. Jest to ważne, aby zapobiec przyjmowaniu preparatu AVODART przez kobiety w ciąży poprzez transfuzję krwi.
Jakie są możliwe skutki uboczne leku AVODART?
AVODART może powodować poważne działania niepożądane, w tym:
- Rzadkie i poważne reakcje alergiczne, w tym:
- obrzęk twarzy, języka lub gardła
- poważne reakcje skórne, takie jak złuszczanie skóry
Natychmiast uzyskaj pomoc medyczną, jeśli masz te poważne reakcje alergiczne.
- Większa szansa na poważniejszą postać raka prostaty.
Najczęstsze działania niepożądane leku AVODART to:
- kłopoty z uzyskaniem lub utrzymaniem erekcji (impotencja)*
- zmniejszenie popędu płciowego (libido)*
- problemy z wytryskiem*
- powiększone lub bolesne piersi. Jeśli zauważysz guzki piersi lub wydzielinę z brodawki sutkowej, porozmawiaj ze swoim lekarzem.
*Niektóre z tych zdarzeń mogą się utrzymywać po zaprzestaniu przyjmowania leku AVODART.
Obniżony nastrój zgłaszano u pacjentów otrzymujących AVODART.
Wykazano, że AVODART 0,5 mg zmniejsza liczbę plemników, objętość nasienia i ruchliwość plemników. Jednak wpływ preparatu AVODART 0,5 mg na płodność mężczyzn nie jest znany.
Test antygenu swoistego dla prostaty (PSA): Twój lekarz może sprawdzić, czy nie występują inne problemy z prostatą, w tym rak prostaty, przed rozpoczęciem i podczas przyjmowania leku AVODART. Badanie krwi zwane PSA (antygen specyficzny dla prostaty) jest czasami używane w celu sprawdzenia, czy możesz mieć raka prostaty. AVODART zmniejszy ilość PSA mierzoną we krwi. Twój lekarz jest świadomy tego efektu i nadal może użyć PSA, aby sprawdzić, czy możesz mieć raka prostaty. Podwyższony poziom PSA podczas leczenia lekiem AVODART (nawet jeśli poziom PSA mieści się w normalnym zakresie) powinien zostać oceniony przez lekarza.
Poinformuj swojego lekarza, jeśli masz jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe działania niepożądane związane ze stosowaniem preparatu AVODART. Aby uzyskać więcej informacji, zapytaj swojego lekarza lub farmaceutę.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać lek AVODART 0,5 mg?
- Przechowywać kapsułki AVODART 0,5 mg w temperaturze pokojowej (59°F do 86°F lub 15°C do 30°C).
- Kapsułki leku AVODART 0,5 mg mogą ulec deformacji i (lub) przebarwieniu, jeśli będą przechowywane w wysokiej temperaturze.
- Nie należy stosować leku AVODART 0,5 mg, jeśli kapsułki są zdeformowane, przebarwione lub przeciekają.
- Bezpiecznie wyrzuć lekarstwa, które nie są już potrzebne.
Lek AVODART 0,5 mg i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Czasami leki są przepisywane do celów innych niż wymienione w ulotce dla pacjenta. Nie należy stosować leku AVODART 0,5 mg w stanach, na które nie został przepisany. Nie należy podawać leku AVODART innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić.
Niniejsza ulotka informacyjna dla pacjenta zawiera podsumowanie najważniejszych informacji o produkcie AVODART. Jeśli chcesz uzyskać więcej informacji, porozmawiaj ze swoim lekarzem. Możesz poprosić farmaceutę lub pracownika służby zdrowia o informacje na temat produktu AVODART 0,5 mg, który jest przeznaczony dla pracowników służby zdrowia.
Aby uzyskać więcej informacji, odwiedź stronę www.AVODART.com lub zadzwoń pod numer 1-888-825-5249.
Jakie są składniki leku AVODART 0,5 mg?
Składnik czynny: dutasteryd.
Nieaktywne składniki : butylohydroksytoluen, tlenek żelaza (żółty), żelatyna (z certyfikowanych źródeł bydlęcych wolnych od BSE), gliceryna, mono-diglicerydy kwasu kaprylowego/kaprynowego, dwutlenek tytanu i jadalny czerwony tusz.
Jak działa AVODART?
Wzrost prostaty jest spowodowany przez hormon we krwi zwany dihydrotestosteronem (DHT). AVODART obniża produkcję DHT w organizmie, co u większości mężczyzn prowadzi do obkurczenia powiększonej prostaty. Chociaż niektórzy mężczyźni mają mniej problemów i objawów po 3 miesiącach leczenia lekiem AVODART, zwykle konieczne jest odbycie leczenia trwającego co najmniej 6 miesięcy, aby sprawdzić, czy lek AVODART 0,5 mg będzie dla nich skuteczny.
Niniejsza informacja dla pacjenta została zatwierdzona przez amerykańską Agencję ds. Żywności i Leków.
