Propecia 1mg, 5mg Finasteride Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Propecia 1mg i jak się go stosuje?
Propecia to lek na receptę stosowany w leczeniu objawów łagodnego przerostu gruczołu krokowego (BPH), wypadania włosów typu męskiego (łysienie androgenowe). Propecia może być stosowana samodzielnie lub z innymi lekami.
Propecia 1mg należy do klasy leków zwanych inhibitorami 5-alfa-reduktazy.
Nie wiadomo, czy Propecia 1mg jest bezpieczna i skuteczna u dzieci.
Jakie są możliwe skutki uboczne Propecia 5mg?
Propecia 1mg może powodować poważne skutki uboczne, w tym:
- guzki piersi,
- ból lub tkliwość piersi,
- wydzielina z brodawki i
- wszelkie inne zmiany piersi
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Propecia 5mg to:
- utrata zainteresowania seksem,
- impotencja,
- kłopoty z orgazmem i
- nieprawidłowy wytrysk
Należy poinformować lekarza, jeśli wystąpią jakiekolwiek objawy niepożądane, które Cię niepokoją lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Propecii. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
Tabletki PROPECIA (finasteryd) zawierają finasteryd jako substancję czynną. Finasteryd, syntetyczny związek 4-azasteroidowy, jest specyficznym inhibitorem 5α-reduktazy steroidowej typu II, wewnątrzkomórkowego enzymu, który przekształca androgen testosteron w 5α-dihydrotestosteron (DHT).
Nazwa chemiczna finasterydu to N-tert-Butylo-3-okso-4-aza-5α-androst-1-eno-17β-karboksyamid. Empiryczny wzór finasterydu to C23H36N2O2, a jego masa cząsteczkowa wynosi 372,55. Jego wzór strukturalny to:
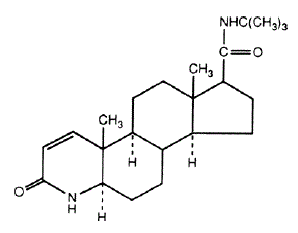
Finasteryd to biały krystaliczny proszek o temperaturze topnienia bliskiej 250 °C. Jest swobodnie rozpuszczalny w chloroformie i rozpuszczalnikach z niższymi alkoholami, ale jest praktycznie nierozpuszczalny w wodzie.
Tabletki PROPECIA (finasteryd) to tabletki powlekane do podawania doustnego. Każda tabletka zawiera 1 mg finasterydu i następujące składniki nieaktywne: monohydrat laktozy, celuloza mikrokrystaliczna, wstępnie żelowana skrobia, sól sodowa glikolanu skrobi, hydroksypropylometyloceluloza, hydroksypropyloceluloza, dwutlenek tytanu, stearynian magnezu, talk, dokuzan sodu, żółty tlenek żelaza i czerwony żelazo tlenek.
WSKAZANIA
PROPECIA® jest wskazany do leczenia łysienia typu męskiego (łysienie androgenowe) TYLKO U MĘŻCZYZN.
Skuteczność w recesji dwuskroniowej nie została ustalona.
PROPECIA nie jest wskazany do stosowania u kobiet.
DAWKOWANIE I SPOSÓB PODAWANIA
PROPECIA może być podawana z posiłkami lub bez posiłków.
Zalecana dawka leku PROPECIA to jedna tabletka (1 mg) przyjmowana raz na dobę.
Ogólnie rzecz biorąc, konieczne jest codzienne stosowanie przez trzy miesiące lub dłużej, zanim zaobserwuje się korzyści. Zaleca się dalsze stosowanie w celu utrzymania korzyści, które należy okresowo oceniać. Przerwanie leczenia prowadzi do odwrócenia efektu w ciągu 12 miesięcy.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Tabletki PROPECIA 5 mg (1 mg) to beżowe, ośmiokątne, powlekane, wypukłe tabletki ze stylizowanym logo P po jednej stronie i preparatem PROPECIA 5 mg po drugiej.
PROPECIA Tabletki, 1 mg, to beżowe, ośmiokątne, powlekane, wypukłe tabletki ze stylizowanym logo P po jednej stronie i PROPECIA po drugiej. Dostarczane są w następujący sposób:
NDC 78206-152-01 butelek po 30 (ze środkiem osuszającym) NDC 78206-152-02 Butelki PROPAK po 90 ® (ze środkiem osuszającym).
Składowania i stosowania
Przechowywać w temperaturze pokojowej, 15-30°C (59-86°F). Przechowywać pojemnik zamknięty i chronić przed wilgocią.
Kobiety w ciąży lub mogące zajść w ciążę nie powinny dotykać pokruszonych lub przełamanych tabletek PROPECIA ze względu na możliwość wchłonięcia finasterydu i wynikające z tego potencjalne ryzyko dla płodu płci męskiej. Tabletki PROPECIA 5 mg są powlekane i zapobiegają kontaktowi z substancją czynną podczas normalnego użytkowania, pod warunkiem, że tabletki nie zostaną przełamane ani zmiażdżone [patrz OSTRZEŻENIA I ŚRODKI , Używaj w określonych populacjach oraz Informacje dotyczące poradnictwa dla pacjentów ].
Dystans. przez: Organon LLC, filię ORGANON & Co., Jersey City, NJ 07302, USA. Aktualizacja: czerwiec 2021
SKUTKI UBOCZNE
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce klinicznej.
Badania kliniczne dla preparatu PROPECIA (finasteryd 1 mg) w leczeniu łysienia typu męskiego
W trzech kontrolowanych badaniach klinicznych preparatu PROPECIA w dawce 5 mg trwających 12 miesięcy, 1,4% pacjentów przyjmujących preparat PROPECIA (n=945) zostało przerwanych z powodu działań niepożądanych, które uznano za prawdopodobnie, prawdopodobnie lub zdecydowanie związane z lekiem (1,6% w przypadku placebo; n=934).
Kliniczne zdarzenia niepożądane, które zostały zgłoszone jako prawdopodobnie, prawdopodobnie lub zdecydowanie związane z lekiem u ≥1% pacjentów leczonych preparatem PROPECIA lub placebo, przedstawiono w Tabeli 1.
TABELA 1: Działania niepożądane związane z lekiem PROPECIA (finasteryd 1 mg) w 1. roku (%) WYPADANIE WŁOSÓW U MĘŻCZYZN
Zintegrowana analiza klinicznych doświadczeń niepożądanych wykazała, że podczas leczenia preparatem PROPECIA 1 mg 36 (3,8%) z 945 mężczyzn zgłosiło jedno lub więcej z tych działań niepożądanych w porównaniu z 20 (2,1%) z 934 mężczyzn otrzymujących placebo (p=0,04) . Ustąpienie nastąpiło u mężczyzn, którzy przerwali terapię preparatem PROPECIA z powodu tych działań niepożądanych oraz u większości tych, którzy kontynuowali terapię. Częstość występowania każdego z powyższych działań niepożądanych zmniejszyła się do ≤0,3% do piątego roku leczenia preparatem PROPECIA.
badaniu finasterydu w dawce 1 mg na dobę zdrowym mężczyznom po 48 tygodniach leczenia zaobserwowano medianę zmniejszenia objętości ejakulatu o 0,3 ml (-11%) w porównaniu z 0,2 ml (-8%) w przypadku placebo. W dwóch innych badaniach wykazano, że finasteryd w dawce 5 razy większej niż dawka preparatu PROPECIA (5 mg na dobę) powodował znaczące zmniejszenie objętości ejakulatu o około 0,5 ml (-25%) w porównaniu z placebo, ale było to odwracalne po przerwaniu leczenia.
W badaniach klinicznych preparatu PROPECIA częstość występowania tkliwości i powiększenia piersi, reakcji nadwrażliwości i bólu jąder u pacjentów leczonych finasterydem nie różniła się od częstości występowania u pacjentów otrzymujących placebo.
Kontrolowane badania kliniczne i długoterminowe otwarte badania rozszerzone dla PROSCAR® (finasteryd 5 mg) i AVODART (dutasteryd) w leczeniu łagodnego rozrostu gruczołu krokowego
badaniu klinicznym PROSCAR Long-Term Efficacy and Safety Study (PLESS), 4-letnim kontrolowanym badaniu klinicznym, oceniano 3040 pacjentów w wieku od 45 do 78 lat z objawowym BPH i przerostem prostaty pod kątem bezpieczeństwa przez okres 4 lat (1524). na PROSCAR 5 mg/dobę i 1516 na placebo). 3,7% (57 pacjentów) leczonych produktem PROSCAR 5 mg i 2,1% (32 pacjentów) leczonych placebo przerwało leczenie z powodu działań niepożądanych związanych z funkcjami seksualnymi, które są najczęściej zgłaszanymi działaniami niepożądanymi.
W Tabeli 2 przedstawiono jedyne kliniczne działania niepożądane, które badacz uznał za prawdopodobnie, prawdopodobnie lub zdecydowanie związane z lekiem, których częstość występowania podczas leczenia produktem PROSCAR wynosiła ≥1% i była większa niż w przypadku placebo w ciągu 4 lat trwania badania. W latach 2-4 badania nie było istotnej różnicy między grupami terapeutycznymi w częstości występowania impotencji, spadku libido i zaburzeń wytrysku.
TABELA 2: Działania niepożądane związane ze stosowaniem leku PROSCAR (finasteryd 5 mg) ŁAGODNY ROZWÓJ PROSTATYCZNY
Profile działań niepożądanych w rocznych, kontrolowanych placebo badaniach III fazy BPH oraz w 5-letnich otwartych badaniach rozszerzonych z zastosowaniem PROSCAR 5 mg i PLESS były podobne.
Nie ma dowodów na nasilenie się niepożądanych doświadczeń seksualnych wraz z wydłużeniem czasu leczenia preparatem PROSCAR 5 mg. Nowe doniesienia o niepożądanych doświadczeniach seksualnych związanych z lekiem zmniejszały się wraz z czasem trwania terapii.
Podczas trwającego od 4 do 6 lat kontrolowanego placebo i lekiem porównawczym badania Medical Therapy of Prostatic Symptoms (MTOPS), do którego włączono 3047 mężczyzn, wystąpiły 4 przypadki raka piersi u mężczyzn leczonych preparatem PROSCAR, ale żadnych przypadków u mężczyzn nieleczonych preparatem PROSCAR. Podczas 4-letniego kontrolowanego placebo badania PLESS, w którym wzięło udział 3040 mężczyzn, wystąpiły 2 przypadki raka piersi u mężczyzn otrzymujących placebo, ale nie zgłoszono żadnego przypadku u mężczyzn leczonych preparatem PROSCAR.
Podczas 7-letniego kontrolowanego placebo badania profilaktyki raka prostaty (PCPT), w którym wzięło udział 18 882 mężczyzn, wystąpił 1 przypadek raka piersi u mężczyzn leczonych preparatem PROSCAR i 1 przypadek raka piersi u mężczyzn otrzymujących placebo. Związek między długotrwałym stosowaniem finasterydu a nowotworem piersi u mężczyzn jest obecnie nieznany.
Badanie PCPT było 7-letnim, randomizowanym, podwójnie zaślepionym, kontrolowanym placebo badaniem, w którym wzięło udział 18 882 zdrowych mężczyzn w wieku ≥55 lat z prawidłowym badaniem palcowym odbytnicy i PSA ≤3,0 ng/ml. Mężczyźni otrzymywali codziennie PROSCAR (finasteryd 5 mg) lub placebo. Pacjenci byli oceniani corocznie za pomocą badania PSA i palcowego odbytnicy. Wykonywano biopsje pod kątem podwyższonego PSA, nieprawidłowego badania palcowego przez odbyt lub zakończenia badania. Częstość występowania raka prostaty w skali 8-10 w skali Gleasona była wyższa u mężczyzn leczonych finasterydem (1,8%) niż u mężczyzn otrzymujących placebo (1,1%). W 4-letnim kontrolowanym placebo badaniu klinicznym z innym inhibitorem 5α-reduktazy [AVODART (dutasteryd)] zaobserwowano podobne wyniki dla raka prostaty w skali 8-10 w skali Gleasona (1% dutasteryd vs 0,5% placebo). Znaczenie kliniczne tych wyników w odniesieniu do stosowania preparatu PROPECIA przez mężczyzn jest nieznane.
Nie wykazano korzyści klinicznych u pacjentów z rakiem prostaty leczonych preparatem PROSCAR. PROSCAR nie jest zatwierdzony do zmniejszania ryzyka zachorowania na raka prostaty.
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania produktu PROPECIA po dopuszczeniu do obrotu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z narażeniem na lek:
Reakcja nadwrażliwości: reakcje nadwrażliwości, takie jak wysypka, świąd, pokrzywka i obrzęk naczynioruchowy (w tym obrzęk warg, języka, gardła i twarzy);
Układ rozrodczy: zaburzenia seksualne, które utrzymywały się po przerwaniu leczenia, w tym zaburzenia erekcji, zaburzenia libido, zaburzenia wytrysku i zaburzenia orgazmu; niepłodność męska i (lub) słaba jakość nasienia (notowano normalizację lub poprawę jakości nasienia po odstawieniu finasterydu); ból jąder; hematospermia.
Nowotwory: męski rak piersi;
Zaburzenia piersi: tkliwość i powiększenie piersi;
Układ nerwowy/psychiatryczny: depresja
INTERAKCJE Z LEKAMI
System enzymatyczny metabolizujący leki sprzężony z cytochromem P450
Nie zidentyfikowano interakcji leków o znaczeniu klinicznym. Wydaje się, że finasteryd nie wpływa na układ enzymatyczny metabolizujący lek związany z cytochromem P450. Związki testowane na ludziach obejmują antypirynę, digoksynę, propranolol, teofilinę i warfarynę i nie znaleziono klinicznie znaczących interakcji.
Inne terapie towarzyszące
Chociaż nie przeprowadzono specyficznych badań interakcji, finasteryd w dawkach 1 mg lub większych był jednocześnie stosowany w badaniach klinicznych z paracetamolem, kwasem acetylosalicylowym, α-blokerami, lekami przeciwbólowymi, inhibitorami konwertazy angiotensyny (ACE), lekami przeciwdrgawkowymi, benzodiazepinami, beta-blokerami, wapniem blokery kanałów, azotany serca, diuretyki, antagoniści H2, inhibitory reduktazy HMG-CoA, inhibitory syntetazy prostaglandyn (określane również jako NLPZ) i chinolonowe leki przeciwzakaźne bez dowodów na klinicznie istotne niepożądane interakcje.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Ekspozycja kobiet – ryzyko dla płodu płci męskiej
PROPECIA nie jest wskazany do stosowania u kobiet. Kobiety w ciąży lub mogące zajść w ciążę nie powinny dotykać pokruszonych lub przełamanych tabletek PROPECIA ze względu na możliwość wchłonięcia finasterydu i wynikające z tego potencjalne ryzyko dla płodu płci męskiej. Tabletki PROPECIA są powlekane i zapobiegają kontaktowi z substancją czynną podczas normalnego użytkowania, pod warunkiem, że tabletki nie zostały przełamane lub pokruszone. [Widzieć WSKAZANIA I ZASTOSOWANIE , PRZECIWWSKAZANIA , Używaj w określonych populacjach , JAK DOSTARCZONE / Składowania i stosowania oraz Informacje dotyczące poradnictwa dla pacjentów ]
Wpływ na antygen specyficzny dla prostaty (PSA)
badaniach klinicznych preparatu PROPECIA (finasteryd, 1 mg) u mężczyzn w wieku 18-41 lat średnia wartość antygenu swoistego dla prostaty (PSA) w surowicy zmniejszyła się z 0,7 ng/ml na początku badania do 0,5 ng/ml w 12. miesiącu. w badaniach klinicznych preparatu PROSCAR (finasteryd, 5 mg) stosowanego u starszych mężczyzn z łagodnym rozrostem gruczołu krokowego (BPH), stężenie PSA jest zmniejszone o około 50%. Inne badania z PROSCAR wykazały, że może on również powodować zmniejszenie stężenia PSA w surowicy w obecności raka prostaty. Te wyniki powinny być brane pod uwagę przy prawidłowej interpretacji PSA w surowicy podczas oceny mężczyzn leczonych finasterydem. Każdy potwierdzony wzrost od najniższej wartości PSA podczas stosowania leku PROPECIA może sygnalizować obecność raka prostaty i powinien być oceniany, nawet jeśli poziom PSA nadal mieści się w normalnym zakresie dla mężczyzn nieprzyjmujących inhibitora 5α-reduktazy. Niezastosowanie się do leczenia preparatem PROPECIA 5 mg może również wpływać na wyniki testu PSA.
Zwiększone ryzyko raka prostaty o wysokim stopniu złośliwości dzięki inhibitorom 5α-reduktazy
Mężczyźni w wieku 55 lat i starsi z prawidłowym badaniem per rectum i PSA ≤3,0 ng/ml na początku leczenia, przyjmujący finasteryd w dawce 5 mg/dobę (5-krotność dawki leku PROPECIA) w 7-letnim badaniu profilaktyki raka prostaty (PCPT) mieli zwiększone ryzyko Gleason uzyskał wynik 8-10 raka prostaty (finasteryd 1,8% vs placebo 1,1%). [Widzieć DZIAŁANIA NIEPOŻĄDANE ] Podobne wyniki zaobserwowano w 4-letnim badaniu klinicznym kontrolowanym placebo z innym inhibitorem 5α-reduktazy (dutasterydem, AVODART) (1% dutasteryd vs 0,5% placebo). Inhibitory 5α-reduktazy mogą zwiększać ryzyko rozwoju raka prostaty o wysokim stopniu złośliwości. Nie ustalono, czy wpływ inhibitorów 5α-reduktazy na zmniejszenie objętości gruczołu krokowego lub czynniki związane z badaniem miały wpływ na wyniki tych badań.
Pacjenci pediatryczni
PROPECIA nie jest wskazany do stosowania u dzieci [patrz Używaj w określonych populacjach ].
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( INFORMACJA O PACJENCIE ).
Ekspozycja kobiet – ryzyko dla płodu płci męskiej
Lekarze powinni poinformować pacjentki, że kobiety w ciąży lub mogące zajść w ciążę nie powinny dotykać pokruszonych lub przełamanych tabletek PROPECIA ze względu na możliwość wchłonięcia finasterydu i wynikające z tego potencjalne ryzyko dla płodu płci męskiej. Tabletki PROPECIA 5 mg są powlekane i zapobiegają kontaktowi z substancją czynną podczas normalnego użytkowania, pod warunkiem, że tabletki nie zostały przełamane lub pokruszone. W przypadku kontaktu kobiety w ciąży lub potencjalnie w ciąży ze zmiażdżonymi lub przełamanymi tabletkami PROPECIA 1 mg, miejsce kontaktu należy natychmiast przemyć wodą z mydłem [patrz PRZECIWWSKAZANIA , OSTRZEŻENIA I ŚRODKI , Używaj w określonych populacjach  i JAK DOSTARCZONE / Składowania i stosowania ].
Zwiększone ryzyko raka prostaty o wysokim stopniu złośliwości
Należy poinformować pacjentów, że w badaniach oceniających stosowanie tych leków w zapobieganiu rakowi prostaty u mężczyzn leczonych inhibitorami 5α-reduktazy wskazanymi do leczenia BPH wystąpił wzrost częstości występowania raka prostaty o wysokim stopniu złośliwości w porównaniu z grupą otrzymującą placebo [patrz OSTRZEŻENIA I ŚRODKI oraz DZIAŁANIA NIEPOŻĄDANE ].
dodatkowe instrukcje
Lekarze powinni poinstruować swoje pacjentki, aby niezwłocznie zgłaszały wszelkie zmiany w piersiach, takie jak guzki, ból lub wydzielina z brodawek sutkowych. Zgłaszano zmiany w piersiach, w tym powiększenie piersi, tkliwość i nowotwór [patrz DZIAŁANIA NIEPOŻĄDANE ].
Lekarze powinni poinstruować swoich pacjentów, aby przed rozpoczęciem leczenia preparatem PROPECIA przeczytali ulotkę dla pacjenta i przeczytali ją ponownie za każdym razem, gdy recepta jest odnawiana, aby byli świadomi aktualnych informacji dla pacjentów dotyczących preparatu PROPECIA.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
W 24-miesięcznym badaniu na szczurach rasy Sprague-Dawley, którym podawano finasteryd w dawkach do 160 mg/kg/dobę u samców i 320 mg/kg/dobę u samic, nie zaobserwowano dowodów na działanie rakotwórcze. Dawki te powodowały u szczurów odpowiednią ekspozycję ogólnoustrojową 888 i 2192 razy większą niż obserwowana u ludzi otrzymujących zalecaną dawkę 1 mg/dobę dla ludzi. Wszystkie obliczenia ekspozycji oparto na obliczonym AUC(0-24godz.) dla zwierząt i średnim AUC(0-24godz.) dla człowieka (0,05 μg•godz./ml).
19-miesięcznym badaniu rakotwórczości u myszy CD-1 zaobserwowano statystycznie istotny (p≤0,05) wzrost częstości występowania gruczolaków jąder z komórek Leydiga przy ekspozycji 1824 razy większej niż ekspozycja u ludzi (250 mg/kg/dobę). U myszy przy 184-krotnej ekspozycji u ludzi szacowanej (25 mg/kg/dobę) iu szczurów przy 312-krotnej ekspozycji u ludzi (≥40 mg/kg/dobę) zaobserwowano zwiększenie częstości występowania rozrostu komórek Leydiga. U obu gatunków gryzoni leczonych dużymi dawkami finasterydu wykazano dodatnią korelację między zmianami proliferacyjnymi w komórkach Leydiga a wzrostem poziomu LH w surowicy (2- do 3-krotnie powyżej kontroli). Nie zaobserwowano zmian w komórkach Leydiga związanych z lekiem ani u szczurów, ani u psów leczonych finasterydem przez 1 rok w dawce 240 i 2800 razy (odpowiednio 20 mg/kg/dobę i 45 mg/kg/dobę) ani u myszy leczonych przez 19 miesięcy przy 18,4-krotnym narażeniu człowieka, szacowane (2,5 mg/kg/dzień).
Nie zaobserwowano dowodów na mutagenność w teście mutagenezy bakteryjnej in vitro, teście mutagenezy na komórkach ssaków ani w teście elucji alkalicznej in vitro. W teście aberracji chromosomowych in vitro, przy użyciu komórek jajnika chomika chińskiego, zaobserwowano nieznaczny wzrost aberracji chromosomowych. W teście aberracji chromosomowych in vivo u myszy, nie zaobserwowano związanego z leczeniem zwiększenia aberracji chromosomowej po zastosowaniu finasterydu w maksymalnej tolerowanej dawce 250 mg/kg/dobę (1824 razy większej od ekspozycji u ludzi), co określono w badaniach rakotwórczości.
dojrzałych płciowo samców królików, którym podawano finasteryd w dawce 4344 razy większej niż ekspozycja u ludzi (80 mg/kg/dobę) przez okres do 12 tygodni, nie zaobserwowano wpływu na płodność, liczbę plemników ani objętość ejakulatu. U dojrzałych płciowo samców szczurów, którym podawano 488-krotną ekspozycję u ludzi (80 mg/kg/dobę), nie stwierdzono znaczącego wpływu na płodność po 6 lub 12 tygodniach leczenia; jednakże, gdy leczenie kontynuowano do 24 lub 30 tygodni, wystąpił wyraźny spadek płodności, płodności i związany z tym istotny spadek masy pęcherzyków nasiennych i prostaty. Wszystkie te działania ustępowały w ciągu 6 tygodni od przerwania leczenia. U szczurów i królików nie zaobserwowano wpływu leku na jądra lub na zdolność kojarzenia się. To zmniejszenie płodności u szczurów leczonych finasterydem jest wtórne do jego wpływu na dodatkowe narządy płciowe (prostata i pęcherzyki nasienne), co skutkuje brakiem tworzenia czopka nasiennego. Czop nasienny jest niezbędny dla prawidłowej płodności u szczurów, ale nie ma znaczenia u człowieka.
Używaj w określonych populacjach
Ciąża
Ciąża Kategoria X [patrz PRZECIWWSKAZANIA ]. PROPECIA 5 mg jest przeciwwskazany do stosowania u kobiet w ciąży lub mogących zajść w ciążę. PROPECIA 5mg to inhibitor 5α-reduktazy typu II, który zapobiega konwersji testosteronu do 5α-dihydrotestosteronu (DHT), hormonu niezbędnego do prawidłowego rozwoju męskich narządów płciowych. W badaniach na zwierzętach finasteryd powodował nieprawidłowy rozwój zewnętrznych narządów płciowych u płodów płci męskiej. Jeśli lek ten jest stosowany w okresie ciąży lub jeśli pacjentka zajdzie w ciążę podczas przyjmowania tego leku, pacjentkę należy poinformować o potencjalnym zagrożeniu dla płodu płci męskiej.
Nieprawidłowy rozwój męskich narządów płciowych jest oczekiwaną konsekwencją, gdy konwersja testosteronu do 5α-dihydrotestosteronu (DHT) jest hamowana przez inhibitory 5α-reduktazy. Wyniki te są podobne do wyników odnotowanych u niemowląt płci męskiej z genetycznym niedoborem 5α-reduktazy. Kobiety mogą być narażone na działanie finasterydu poprzez kontakt z pokruszonymi lub przełamanymi tabletkami PROPECIA 5 mg lub nasieniem partnera przyjmującego lek PROPECIA. W odniesieniu do ekspozycji na finasteryd przez skórę, tabletki PROPECIA są powlekane i zapobiegają kontaktowi skóry z finasterydem podczas normalnego użytkowania, jeśli tabletki nie zostały pokruszone lub przełamane. Kobiety w ciąży lub mogące zajść w ciążę nie powinny dotykać pokruszonych lub przełamanych tabletek PROPECIA 5 mg ze względu na możliwość narażenia płodu płci męskiej. W przypadku kontaktu kobiety w ciąży ze zmiażdżonymi lub przełamanymi tabletkami PROPECIA 1 mg, miejsce kontaktu należy natychmiast przemyć wodą z mydłem. W odniesieniu do potencjalnego narażenia na finasteryd poprzez nasienie przeprowadzono badanie u mężczyzn otrzymujących preparat PROPECIA w dawce 1 mg/dobę, w którym mierzono stężenia finasterydu w nasieniu [patrz FARMAKOLOGIA KLINICZNA ].
badaniu dotyczącym rozwoju zarodka i płodu ciężarne szczury otrzymywały finasteryd w okresie głównej organogenezy (od 6. do 17. dnia ciąży). Przy dawkach podawanych matce doustnie około 1 do 684 razy większej od zalecanej dawki u ludzi (RHD) wynoszącej 1 mg/dobę (na podstawie AUC przy dawkach zwierzęcych od 0,1 do 100 mg/kg/dobę) obserwowano zależne od dawki nasilenie spodziectwa, które wystąpiło u 3,6 do 100% męskiego potomstwa. Mnożniki ekspozycji oszacowano na podstawie danych pochodzących od nieciężarnych szczurów. Od 16 do 17 dnia ciąży u samców płodów szczurów okres krytyczny dla różnicowania zewnętrznych narządów płciowych. Przy dawkach doustnych stosowanych przez matkę około 0,2 razy wyższych od RHD (na podstawie AUC przy dawce zwierzęcej 0,03 mg/kg/dobę) potomstwo płci męskiej miało zmniejszoną masę gruczołu krokowego i pęcherzyków nasiennych, opóźnione oddzielenie napletka i przemijający rozwój brodawek sutkowych. Zmniejszenie odległości odbytowo-płciowej wystąpiło u potomstwa samców ciężarnych szczurów, które otrzymywało około 0,02 razy RHD (na podstawie AUC przy dawce 0,003 mg/kg/dobę zwierzęcia). Nie zaobserwowano nieprawidłowości u potomstwa płci żeńskiej narażonej na jakąkolwiek dawkę finasterydu in utero.
Nie zaobserwowano żadnych nieprawidłowości rozwojowych u potomstwa nieleczonych samic kojarzonych z samcami szczurów, którym podawano finasteryd, które otrzymywały około 488 razy RHD (na podstawie AUC przy dawce zwierzęcej 80 mg/kg/dobę). Nieznacznie zmniejszoną płodność zaobserwowano u potomstwa płci męskiej po podaniu około 20-krotności RHD (w oparciu o AUC przy dawce zwierzęcej 3 mg/kg/dobę) samicom szczurów w późnym okresie ciąży i laktacji. W tych warunkach nie zaobserwowano wpływu na płodność u potomstwa płci żeńskiej.
U płodów królików narażonych na działanie finasterydu w okresie poważnej organogenezy (6-18 dni ciąży) w dawkach do 100 mg/kg mc. króliki). Jednak badanie to mogło nie obejmować okresu krytycznego dla wpływu finasterydu na rozwój zewnętrznych narządów płciowych samców królika.
Wpływ na płód ekspozycji matki na finasteryd w okresie rozwoju embrionalnego i płodowego oceniano na małpach rezus (od 20 do 100 dni ciąży), w gatunku i okresie rozwoju, który pozwala na bardziej przewidywalne specyficzne działania u ludzi niż badania na szczurach i królikach. Dożylne podawanie finasterydu ciężarnym małpom w dawkach do 800 ng/dobę (szacunkowe maksymalne stężenie we krwi wynoszące 1,86 ng/ml lub około 930 razy większe szacowane narażenie kobiet w ciąży na finasteryd z nasienia mężczyzn przyjmujących 1 mg/dobę) spowodowało bez nieprawidłowości u płodów płci męskiej. W celu potwierdzenia znaczenia modelu rezus dla rozwoju płodu ludzkiego, doustne podanie dawki finasterydu (2 mg/kg/dobę lub około 120 000 razy większe od najwyższych szacowanych poziomów finasterydu we krwi z nasienia mężczyzn przyjmujących 1 mg/dobę) do ciężarne małpy powodowały nieprawidłowości zewnętrznych narządów płciowych u płodów płci męskiej. Nie zaobserwowano żadnych innych nieprawidłowości u płodów płci męskiej i nie zaobserwowano nieprawidłowości związanych z finasterydem u płodów żeńskich po żadnej dawce.
Matki karmiące
PROPECIA nie jest wskazany do stosowania u kobiet.
Nie wiadomo, czy finasteryd przenika do mleka ludzkiego.
Zastosowanie pediatryczne
PROPECIA 1 mg nie jest wskazany do stosowania u dzieci.
Bezpieczeństwo i skuteczność u pacjentów pediatrycznych nie zostały ustalone.
Zastosowanie geriatryczne
Badania skuteczności klinicznej preparatu PROPECIA nie obejmowały osób w wieku 65 lat i starszych. Na podstawie farmakokinetyki finasterydu w dawce 5 mg nie jest konieczne dostosowanie dawki preparatu PROPECIA u osób w podeszłym wieku [patrz FARMAKOLOGIA KLINICZNA ]. Jednak skuteczność preparatu PROPECIA 1 mg u osób w podeszłym wieku nie została ustalona.
Niewydolność wątroby
Należy zachować ostrożność podczas podawania produktu PROPECIA 5 mg pacjentom z zaburzeniami czynności wątroby, ponieważ finasteryd jest intensywnie metabolizowany w wątrobie [patrz FARMAKOLOGIA KLINICZNA ].
Zaburzenia czynności nerek
Nie ma konieczności dostosowania dawkowania u pacjentów z zaburzeniami czynności nerek [patrz FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
W badaniach klinicznych pojedyncze dawki finasterydu do 400 mg i wielokrotne dawki finasterydu do 80 mg/dobę przez trzy miesiące nie powodowały działań niepożądanych. Do czasu uzyskania dalszych doświadczeń nie można zalecić żadnego konkretnego leczenia przedawkowania finasterydu.
Istotną śmiertelność zaobserwowano u samców i samic myszy po pojedynczych doustnych dawkach 1500 mg/m2 (500 mg/kg) oraz u samic i samców szczurów po pojedynczych doustnych dawkach 2360 mg/m2 (400 mg/kg) i 5900 mg/m2 (1000 mg/kg).
PRZECIWWSKAZANIA
PROPECIA 5 mg jest przeciwwskazany w następujących przypadkach:
- Ciąża. Stosowanie finasterydu jest przeciwwskazane u kobiet w ciąży lub mogących zajść w ciążę. Ze względu na zdolność inhibitorów 5α-reduktazy typu II do hamowania konwersji testosteronu do 5α-dihydrotestosteronu (DHT), finasteryd może powodować nieprawidłowości zewnętrznych narządów płciowych u płodu płci męskiej kobiety w ciąży otrzymującej finasteryd. W przypadku stosowania tego leku w okresie ciąży lub w przypadku zajścia w ciążę podczas przyjmowania tego leku, ciężarna powinna zostać poinformowana o potencjalnym zagrożeniu dla płodu płci męskiej. [Widzieć OSTRZEŻENIA I ŚRODKI , Używaj w określonych populacjach , JAK DOSTARCZONE / Składowania i stosowania oraz Informacje dotyczące poradnictwa dla pacjentów ] U samic szczurów małe dawki finasterydu podawane w czasie ciąży powodowały nieprawidłowości w zewnętrznych narządach płciowych u potomstwa płci męskiej.
- Nadwrażliwość na którykolwiek składnik tego leku.
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Finasteryd jest konkurencyjnym i swoistym inhibitorem 5α-reduktazy typu II, enzymu wewnątrzkomórkowego, który przekształca androgen testosteron w DHT. U myszy, szczurów, małp i ludzi znajdują się dwa różne izozymy: typ I i II. Każdy z tych izoenzymów ulega zróżnicowanej ekspresji w tkankach i stadiach rozwojowych. U ludzi 5α-reduktaza typu I dominuje w gruczołach łojowych większości obszarów skóry, w tym skóry głowy i wątroby. 5α-reduktaza typu I odpowiada za około jedną trzecią krążącego DHT. Izozym 5α-reduktazy typu II znajduje się głównie w prostacie, pęcherzykach nasiennych, najądrzach i mieszkach włosowych, a także w wątrobie i jest odpowiedzialny za dwie trzecie krążącego DHT.
ludzi mechanizm działania finasterydu opiera się na preferencyjnym hamowaniu izoenzymu typu II. Przy użyciu natywnych tkanek (skóry głowy i prostaty) badania wiązania in vitro badające potencjał finasterydu do hamowania obu izoenzymów wykazały 100-krotną selektywność wobec ludzkiej 5α-reduktazy typu II w stosunku do izoenzymu typu I (IC50 = 500 i 4,2 nM dla typu I i II). W przypadku obu izoenzymów hamowaniu przez finasteryd towarzyszy redukcja inhibitora do dihydrofinasterydu i tworzenie adduktu z NADP+. Obrót kompleksu enzymatycznego jest powolny (t½ około 30 dni dla kompleksu enzymatycznego typu II i 14 dni dla kompleksu typu I). Hamowanie 5α-reduktazy typu II blokuje obwodową konwersję testosteronu do DHT, powodując znaczne zmniejszenie stężenia DHT w surowicy i tkankach.
mężczyzn z wypadaniem włosów typu męskiego (łysienie androgenowe) łysiejąca skóra głowy zawiera zminiaturyzowane mieszki włosowe i zwiększone ilości DHT w porównaniu z owłosioną skórą głowy. U tych mężczyzn podawanie finasterydu zmniejsza stężenie DHT w skórze głowy i surowicy. Względny udział tych redukcji w działaniu leczniczym finasterydu nie został określony. Dzięki temu mechanizmowi finasteryd wydaje się przerywać kluczowy czynnik rozwoju łysienia androgenowego u pacjentów predysponowanych genetycznie.
Farmakodynamika
Finasteryd powoduje szybkie zmniejszenie stężenia DHT w surowicy, osiągając 65% zahamowanie w ciągu 24 godzin od doustnego podania tabletki 1 mg. Średnie poziomy krążącego testosteronu i estradiolu wzrosły o około 15% w porównaniu z wartościami wyjściowymi, ale pozostawały one w zakresie fizjologicznym.
Finasteryd nie wykazuje powinowactwa do receptora androgenowego i nie ma działania androgennego, antyandrogennego, estrogennego, antyestrogenowego ani progestagenowego. W badaniach z finasterydem nie wykryto klinicznie istotnych zmian hormonu luteinizującego (LH), hormonu folikulostymulującego (FSH) ani prolaktyny. U zdrowych ochotników leczenie finasterydem nie zmieniało odpowiedzi LH i FSH na hormon uwalniający gonadotropiny, co wskazuje na brak wpływu na oś podwzgórze-przysadka-jądra.
Finasteryd nie wpływał na poziom krążącego kortyzolu, hormonu tyreotropowego ani tyroksyny, ani nie wpływał na profil lipidowy osocza (np. cholesterol całkowity, lipoproteiny o małej gęstości, lipoproteiny o dużej gęstości i triglicerydy) ani na gęstość mineralną kości.
Farmakokinetyka
Wchłanianie
badaniu z udziałem 15 zdrowych młodych mężczyzn, średnia biodostępność tabletek 1 mg finasterydu wyniosła 65% (zakres 26-170%), w oparciu o stosunek pola pod krzywą (AUC) do wartości odniesienia dożylnego (IV). dawka. W stanie stacjonarnym po podaniu 1 mg/dobę (n=12) maksymalne stężenie finasterydu w osoczu wynosiło średnio 9,2 ng/ml (zakres 4,9-13,7 ng/ml) i było osiągane 1 do 2 godzin po podaniu; AUC wynosiło 53 ng•h/ml (zakres 20-154 ng•h/ml). Pokarm nie wpływał na biodostępność finasterydu.
Dystrybucja
Średnia objętość dystrybucji w stanie stacjonarnym wynosiła 76 litrów (zakres 44-96 litrów; n=15). Około 90% krążącego finasterydu wiąże się z białkami osocza. Po wielokrotnym podaniu finasterydu następuje faza powolnej akumulacji.
Stwierdzono, że finasteryd przekracza barierę krew-mózg.
Poziom nasienia został zmierzony u 35 mężczyzn przyjmujących finasteryd 1 mg/dzień przez 6 tygodni. W 60% (21 z 35) próbek poziomy finasterydu były niewykrywalne ( Używaj w określonych populacjach ]
Metabolizm
Finasteryd jest intensywnie metabolizowany w wątrobie, głównie za pośrednictwem podrodziny enzymów cytochromu P450 3A4. Zidentyfikowano dwa metabolity, monohydroksylowany i monokarboksylowy łańcuch boczny t-butylu, które wykazują nie więcej niż 20% aktywności finasterydu hamującej 5α-reduktazę.
Wydalanie
Po wlewie dożylnym zdrowym młodym ochotnikom (n=15) średni klirens osoczowy finasterydu wynosił 165 ml/min (zakres 70-279 ml/min). Średni końcowy okres półtrwania w osoczu wynosił 4,5 godziny (zakres 3,3-13,4 godziny; n=12). Po podaniu doustnym 14C-finasterydu u ludzi (n=6), średnio 39% (zakres 32-46%) dawki było wydalane z moczem w postaci metabolitów; 57% (zakres 51-64%) zostało wydalone z kałem.
Średni końcowy okres półtrwania wynosi około 5-6 godzin u mężczyzn w wieku 18-60 lat i 8 godzin u mężczyzn w wieku powyżej 70 lat.
TABELA 3: Średnie (SD) parametry farmakokinetyczne u zdrowych mężczyzn (w wieku 18–26 lat)
TABELA 4: Średnie (SD) niekompartmentowe parametry farmakokinetyczne po wielokrotnych dawkach 1 mg/dobę u zdrowych mężczyzn (19-42)
Zaburzenia czynności nerek
Nie ma konieczności dostosowania dawkowania u pacjentów z zaburzeniami czynności nerek. U pacjentów z przewlekłą niewydolnością nerek, z klirensem kreatyniny w zakresie od 9,0 do 55 ml/min, AUC, maksymalne stężenie w osoczu, okres półtrwania i wiązanie z białkami po podaniu pojedynczej dawki 14C-finasterydu były podobne do wartości uzyskiwanych u zdrowych ochotników. Wydalanie metabolitów z moczem było zmniejszone u pacjentów z zaburzeniami czynności nerek. Ten spadek był związany ze wzrostem wydalania metabolitów z kałem. Stężenia metabolitów w osoczu były znacząco wyższe u pacjentów z zaburzeniami czynności nerek (w oparciu o 60% wzrost całkowitej radioaktywności AUC). Jednak finasteryd był tolerowany u mężczyzn z prawidłową czynnością nerek otrzymujących do 80 mg/dobę przez 12 tygodni, gdzie ekspozycja tych pacjentów na metabolity byłaby przypuszczalnie znacznie większa.
Niewydolność wątroby
Nie badano wpływu zaburzeń czynności wątroby na farmakokinetykę finasterydu. Należy zachować ostrożność podczas podawania produktu PROPECIA 1 mg pacjentom z zaburzeniami czynności wątroby, ponieważ finasteryd jest intensywnie metabolizowany w wątrobie.
Studia kliniczne
Studia u mężczyzn
Skuteczność preparatu PROPECIA 1 mg wykazano u mężczyzn (88% rasy kaukaskiej) z łagodnym do umiarkowanego łysieniem androgenowym (łysienie typu męskiego) w wieku od 18 do 41 lat. W celu zapobiegania łojotokowemu zapaleniu skóry, które może zakłócać ocenę wzrostu włosów w tych badaniach, wszyscy mężczyźni, niezależnie od tego, czy byli leczeni finasterydem, czy placebo, zostali poinstruowani, aby podczas pierwsze 2 lata studiów.
Przeprowadzono trzy podwójnie ślepe, randomizowane, kontrolowane placebo badania trwające 12 miesięcy. Dwa główne punkty końcowe to liczba włosów i samoocena pacjenta; dwa drugorzędowe punkty końcowe to ocena badacza i ocena zdjęć. Ponadto zebrano informacje dotyczące funkcji seksualnych (na podstawie kwestionariusza samodzielnego) oraz owłosienia poza skórą głowy. Trzy badania przeprowadzono na 1879 mężczyznach z łagodną lub umiarkowaną, ale nie całkowitą utratą włosów. Do dwóch badań włączono mężczyzn z przeważnie łagodną lub umiarkowaną utratą włosów w okolicy wierzchołkowej (n=1553). Do trzeciego włączono mężczyzn z łagodną lub umiarkowaną utratą włosów w przedniej części środkowej skóry głowy z łysieniem lub bez łysienia wierzchołków (n=326).
Badania u mężczyzn z łysieniem wierzchołkowym
Spośród mężczyzn, którzy ukończyli pierwsze 12 miesięcy z dwóch badań dotyczących łysienia wierzchołkowego, 1215 zdecydowało się kontynuować 12-miesięczne badania z podwójnie ślepą próbą, kontrolowane placebo. 547 mężczyzn otrzymywało preparat PROPECIA 5 mg zarówno w początkowym badaniu, jak i w pierwszym okresie przedłużenia (do 2 lat leczenia) i 60 mężczyzn otrzymywało placebo w tych samych okresach. Rozszerzone badania kontynuowano przez 3 dodatkowe lata, przy czym 323 mężczyzn otrzymujących preparat PROPECIA 5 mg i 23 mężczyzn otrzymujących placebo rozpoczęło piąty rok badania.
celu oceny skutków przerwania leczenia 65 mężczyzn otrzymywało preparat PROPECIA 5 mg przez pierwsze 12 miesięcy, a następnie placebo w pierwszym 12-miesięcznym okresie przedłużenia. Niektórzy z tych mężczyzn kontynuowali dodatkowe badania uzupełniające i zostali ponownie przeniesieni do leczenia preparatem PROPECIA 5 mg, przy czym 32 mężczyzn rozpoczęło piąty rok badania. Wreszcie 543 mężczyzn otrzymywało placebo przez pierwsze 12 miesięcy, a następnie preparat PROPECIA w pierwszym 12-miesięcznym okresie przedłużenia. Niektórzy z tych mężczyzn kontynuowali dodatkowe badania uzupełniające otrzymując produkt PROPECIA 5 mg, przy czym 290 mężczyzn rozpoczęło piąty rok badania (patrz Rycina 1 poniżej).
Liczbę włosów oceniano na podstawie powiększeń fotograficznych reprezentatywnego obszaru aktywnego wypadania włosów. W tych dwóch badaniach u mężczyzn z łysieniem wierzchołkowym, znaczny wzrost liczby włosów wykazano po 6 i 12 miesiącach u mężczyzn leczonych preparatem PROPECIA 5 mg, podczas gdy znaczna utrata włosów w stosunku do wartości wyjściowych została wykazana u osób otrzymujących placebo. Po 12 miesiącach wystąpiła różnica 107 włosów w porównaniu z placebo (p
pacjentów, którzy zmienili placebo na PROPECIA (n=425), liczba włosów zmniejszyła się pod koniec początkowego 12-miesięcznego okresu placebo, a następnie wzrosła liczba włosów po 1 roku leczenia preparatem PROPECIA. Ten wzrost liczby włosów był mniejszy (56 włosów powyżej początkowej wartości wyjściowej) niż wzrost (91 włosów powyżej początkowej wartości wyjściowej) obserwowany po 1 roku leczenia u mężczyzn początkowo przydzielonych losowo do grupy PROPECIA. Chociaż wzrost liczby włosów w porównaniu z początkiem leczenia był porównywalny między tymi dwiema grupami, wyższą bezwzględną liczbę włosów uzyskano u pacjentów, którzy rozpoczęli leczenie preparatem PROPECIA w początkowym badaniu. Przewaga ta utrzymywała się przez pozostałe 3 lata studiów. Zmiana leczenia z preparatu PROPECIA 5 mg na placebo (n=48) pod koniec pierwszych 12 miesięcy spowodowała odwrócenie wzrostu liczby włosów 12 miesięcy później, po 24 miesiącach (patrz Rysunek 1 poniżej).
Po 12 miesiącach u 58% mężczyzn w grupie placebo wystąpiło dalsze wypadanie włosów (definiowane jako zmniejszenie liczby włosów w stosunku do wartości wyjściowych), w porównaniu z 14% mężczyzn leczonych preparatem PROPECIA. U mężczyzn leczonych przez okres do 2 lat 72% mężczyzn w grupie placebo wykazywało utratę włosów, w porównaniu z 17% mężczyzn leczonych preparatem PROPECIA. Po 5 latach 100% mężczyzn w grupie placebo wykazywało utratę włosów, w porównaniu z 35% mężczyzn leczonych preparatem PROPECIA.
Rysunek 1
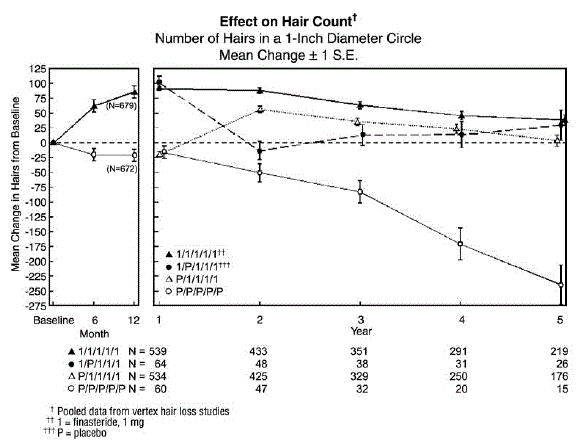
Samoocena pacjenta była uzyskiwana podczas każdej wizyty w klinice na podstawie samodzielnego kwestionariusza, który zawierał pytania dotyczące ich postrzegania wzrostu włosów, wypadania włosów i wyglądu. Ta samoocena wykazała wzrost ilości włosów, zmniejszenie wypadania włosów i poprawę wyglądu u mężczyzn leczonych preparatem PROPECIA. Ogólną poprawę w porównaniu z placebo zaobserwowano już po 3 miesiącach (p
Ocena badacza opierała się na 7-punktowej skali oceniającej wzrost lub spadek włosów na skórze głowy podczas każdej wizyty pacjenta. Ta ocena wykazała znacznie większy wzrost wzrostu włosów u mężczyzn leczonych preparatem PROPECIA w porównaniu z placebo już po 3 miesiącach (p
Niezależny panel ocenił znormalizowane zdjęcia głowy w sposób zaślepiony na podstawie wzrostu lub spadku włosów na skórze głowy przy użyciu tej samej 7-punktowej skali, co ocena badacza. Po 12 miesiącach 48% mężczyzn leczonych preparatem PROPECIA odnotowało wzrost w porównaniu z 7% mężczyzn otrzymujących placebo. Po 2 latach wzrost włosów wykazano u 66% mężczyzn leczonych preparatem PROPECIA 5 mg, w porównaniu z 7% mężczyzn otrzymujących placebo. Po 5 latach 48% mężczyzn leczonych preparatem PROPECIA 5 mg wykazało wzrost włosów, 42% zostało ocenionych jako brak zmian (brak dalszej widocznej progresji wypadania włosów w stosunku do wartości wyjściowych), a 10% zostało ocenionych jako utrata włosów w porównaniu z linia bazowa. Dla porównania, 6% mężczyzn leczonych placebo wykazało wzrost wzrostu włosów, 19% zostało ocenionych jako brak zmian, a 75% zostało ocenionych jako utrata włosów w porównaniu ze stanem wyjściowym.
Do 48-tygodniowego, kontrolowanego placebo badania, zaprojektowanego w celu oceny za pomocą fototrichogramu, wpływu preparatu PROPECIA na całkowite i aktywnie rosnące (anagenowe) włosy na skórze głowy w przypadku łysienia wierzchołkowego wzięło udział 212 mężczyzn z łysieniem androgenowym. Wyjściowo i po 48 tygodniach uzyskano liczbę włosów całkowitych i anagenowych na docelowym obszarze skóry głowy o powierzchni 1 cm². Mężczyźni leczeni preparatem PROPECIA wykazywali wzrost całkowitej liczby włosów ogółem i anagenowych odpowiednio o 7 i 18 włosów w stosunku do wartości wyjściowej, podczas gdy mężczyźni leczeni placebo mieli spadek odpowiednio o 10 i 9 włosów. Te zmiany w liczbie włosów spowodowały różnicę między grupami wynoszącą 17 włosów w całkowitej liczbie włosów (p
Inne wyniki w badaniach łysienia wierzchołkowego
Kwestionariusz funkcji seksualnych został wdrożony samodzielnie przez pacjentów uczestniczących w dwóch próbach łysienia wierzchołków, aby wykryć bardziej subtelne zmiany funkcji seksualnych. W miesiącu 12 statystycznie istotne różnice na korzyść placebo stwierdzono w 3 z 4 domen (zainteresowanie seksualne, erekcje i postrzeganie problemów seksualnych). Nie zaobserwowano jednak istotnej różnicy w pytaniu o ogólną satysfakcję z życia seksualnego.
W jednym z dwóch badań dotyczących łysienia wierzchołków, pacjenci byli pytani o porost włosów poza skórą głowy. PROPECIA nie wpływał na owłosienie na ciele.
Badanie u mężczyzn z wypadaniem włosów w przedniej części skóry głowy
Badanie trwające 12 miesięcy, zaprojektowane w celu oceny skuteczności preparatu PROPECIA 5 mg u mężczyzn z utratą włosów w przedniej części środkowej skóry głowy, również wykazało znaczny wzrost liczby włosów w porównaniu z placebo. Wzrostowi liczby włosów towarzyszyła poprawa samooceny pacjentów, oceny badacza i ocen opartych na standardowych fotografiach. Liczba włosów została uzyskana w przedniej środkowej części skóry głowy i nie obejmowała obszaru dwuskroniowej recesji ani przedniej linii włosów.
Podsumowanie badań klinicznych u mężczyzn
Badania kliniczne przeprowadzono u mężczyzn w wieku od 18 do 41 lat z łagodnym lub umiarkowanym stopniem łysienia androgenowego. Wszyscy mężczyźni leczeni preparatem PROPECIA 5 mg lub placebo otrzymywali szampon na bazie smoły (Szampon Neutrogena T/Gel®) w ciągu pierwszych 2 lat badań. Poprawę kliniczną zaobserwowano już po 3 miesiącach u pacjentów leczonych preparatem PROPECIA 5 mg i doprowadziła ona do zwiększenia liczby włosów na skórze głowy i odrastania włosów. W badaniach klinicznych trwających do 5 lat leczenie preparatem PROPECIA 5 mg spowalniało dalszy postęp wypadania włosów obserwowany w grupie placebo. Ogólnie rzecz biorąc, różnica między grupami leczenia nadal wzrastała w ciągu 5 lat badań.
Analiza etniczna danych klinicznych od mężczyzn
połączonej analizie dwóch badań dotyczących łysienia wierzchołków, średnia zmiana liczby włosów w stosunku do wartości wyjściowej wyniosła 91 vs -19 włosów (PROPECIA 5 mg vs placebo) wśród rasy białej (n=1185), 49 vs -27 włosów wśród osób rasy czarnej (n=84) , 53 do -38 włosów wśród Azjatów (n=17), 67 do 5 włosów wśród Latynosów (n=45) i 67 do -15 włosów wśród innych grup etnicznych (n=20). Samoocena pacjentów wykazała poprawę w grupach rasowych leczonych preparatem PROPECIA, z wyjątkiem zadowolenia z przedniej linii włosów i wierzchołków u czarnoskórych mężczyzn, którzy byli ogólnie usatysfakcjonowani.
Studia u kobiet
W badaniu z udziałem 137 kobiet po menopauzie z łysieniem androgenowym, które były leczone preparatem PROPECIA (n=67) lub placebo (n=70) przez 12 miesięcy, nie można było wykazać skuteczności. Nie stwierdzono poprawy liczby włosów, samooceny pacjenta, oceny badacza ani ocen standaryzowanych zdjęć u kobiet leczonych preparatem PROPECIA w porównaniu z grupą placebo [patrz WSKAZANIA I ZASTOSOWANIE ].
INFORMACJA O PACJENCIE
PROPECIA (Pro-pee-sha) (finasteryd) Tabletki
PROPECIA® jest przeznaczony do użytku WYŁĄCZNIE przez MĘŻCZYZN i NIE powinien być stosowany przez kobiety i dzieci.
Przeczytaj tę Informację dla Pacjenta przed rozpoczęciem przyjmowania leku PROPECIA 5 mg i za każdym razem, gdy otrzymujesz uzupełnienie. Mogą pojawić się nowe informacje. Informacje te nie zastępują rozmowy z lekarzem o stanie zdrowia lub leczeniu.
Co to jest PROPECIA 5mg?
PROPECIA 5mg to lek na receptę stosowany w leczeniu łysienia typu męskiego (łysienie androgenowe).
Nie wiadomo, czy PROPECIA 5 mg działa na cofającą się linię włosów po obu stronach i nad czołem (obszar skroniowy).
PROPECIA 5mg nie jest przeznaczony do stosowania przez kobiety i dzieci.
Kto nie powinien brać PROPECIA 5mg?
Nie należy przyjmować leku PROPECIA 1 mg, jeśli:
- są w ciąży lub mogą zajść w ciążę. PROPECIA może zaszkodzić nienarodzonemu dziecku.
- Tabletki PROPECIA 1 mg są powlekane i zapobiegają kontaktowi z lekiem podczas obsługi, o ile tabletki nie zostaną przełamane lub zmiażdżone. Kobiety w ciąży lub mogące zajść w ciążę nie powinny mieć kontaktu z przełamanymi lub pokruszonymi tabletkami PROPECIA. Jeśli kobieta w ciąży wejdzie w kontakt z pokruszonymi lub złamanymi tabletkami PROPECIA 5 mg, należy natychmiast przemyć miejsce kontaktu mydłem i wodą. W przypadku kontaktu kobiety w ciąży z substancją czynną preparatu PROPECIA 5 mg należy skonsultować się z lekarzem.
- Jeśli kobieta w ciąży z dzieckiem płci męskiej połknie lub wejdzie w kontakt z lekiem zawartym w leku PROPECIA, dziecko płci męskiej może urodzić się z nieprawidłowymi narządami płciowymi.
- jesteś uczulony na którykolwiek ze składników preparatu PROPECIA. Pełny wykaz składników leku PROPECIA znajduje się na końcu tej ulotki.
O czym powinienem powiedzieć lekarzowi przed przyjęciem leku PROPECIA 5 mg?
Przed przyjęciem leku PROPECIA 5 mg, poinformuj swojego lekarza, jeśli:
- masz jakiekolwiek inne schorzenia, w tym problemy z prostatą lub wątrobą
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe.
Poznaj leki, które przyjmujesz. Zachowaj ich listę, aby pokazać swojemu lekarzowi i farmaceucie, kiedy otrzymasz nowy lek.
Jak powinienem zażywać PROPECIA 5mg?
- Weź PROPECIA 5 mg dokładnie tak, jak zalecił Ci lekarz.
- Lek PROPECIA 5 mg można przyjmować z posiłkiem lub bez posiłku.
- W przypadku pominięcia dawki leku PROPECIA 1 mg nie należy przyjmować dodatkowej tabletki. Po prostu weź następną tabletkę jak zwykle.
PROPECIA nie będzie działać szybciej ani lepiej, jeśli będziesz go przyjmować częściej niż raz dziennie.
Jakie są możliwe skutki uboczne preparatu PROPECIA?
- zmniejszenie stężenia antygenu swoistego dla prostaty (PSA) we krwi. PROPECIA może wpływać na badanie krwi zwane PSA (antygen specyficzny dla prostaty) do badań przesiewowych w kierunku raka prostaty. Jeśli masz zrobione badanie PSA, powinieneś powiedzieć swojemu lekarzowi, że przyjmujesz PROPECIA, ponieważ PROPECIA 1 mg obniża poziom PSA. Zmiany w poziomach PSA będą musiały zostać ocenione przez lekarza. Jakikolwiek wzrost poziomu PSA w okresie obserwacji od najniższego punktu może sygnalizować obecność raka prostaty i powinien być oceniany, nawet jeśli wyniki testu nadal mieszczą się w normalnym zakresie dla mężczyzn nieprzyjmujących preparatu PROPECIA. Powinieneś również poinformować swojego lekarza, jeśli nie przyjmowałeś leku PROPECIA 1 mg zgodnie z zaleceniami, ponieważ może to wpłynąć na wyniki testu PSA. Aby uzyskać więcej informacji, porozmawiaj ze swoim lekarzem.
- U mężczyzn przyjmujących finasteryd w dawce 5 razy większej od dawki leku PROPECIA może wystąpić zwiększone ryzyko wystąpienia poważniejszej postaci raka prostaty.
Do najczęstszych skutków ubocznych preparatu PROPECIA należą:
- spadek popędu seksualnego
- kłopoty z uzyskaniem lub utrzymaniem erekcji
- zmniejszenie ilości nasienia
Następujące informacje zostały zgłoszone podczas ogólnego stosowania leku PROPECIA:
- tkliwość i powiększenie piersi. Poinformuj swojego lekarza o wszelkich zmianach w piersiach, takich jak guzki, ból lub wydzielina z brodawki sutkowej.
- depresja;
- spadek popędu płciowego, który utrzymywał się po odstawieniu leku;
- reakcje alergiczne, w tym wysypka, swędzenie, pokrzywka i obrzęk warg, języka, gardła i twarzy;
- problemy z wytryskiem, które utrzymywały się po odstawieniu leków;
- ból jąder;
- krew w nasieniu;
- trudności w osiągnięciu erekcji, która utrzymywała się po odstawieniu leku;
- niepłodność męska i/lub niska jakość nasienia.
- w rzadkich przypadkach męski rak piersi.
Poinformuj swojego lekarza, jeśli masz jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne preparatu PROPECIA. Aby uzyskać więcej informacji, zapytaj swojego lekarza lub farmaceutę.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać PROPECIA 1mg?
- Przechowywać PROPECIA 5 mg w temperaturze pokojowej między 59 ° F do 86 ° F (15 ° C do 30 ° C).
- Przechowywać PROPECIA w zamkniętym pojemniku i przechowywać tabletki PROPECIA 5 mg suche (chronić przed wilgocią).
PROPECIA i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu preparatu PROPECIA.
Czasami leki są przepisywane do celów innych niż te wymienione w tej ulotce informacyjnej dla pacjenta. Nie należy stosować leku PROPECIA 5 mg w przypadku schorzenia, na które nie został przepisany. Nie należy podawać leku PROPECIA innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić.
Niniejsza ulotka dla pacjenta zawiera podsumowanie najważniejszych informacji o produkcie PROPECIA. Jeśli chcesz uzyskać więcej informacji, porozmawiaj ze swoim lekarzem. Możesz poprosić swojego farmaceutę lub pracownika służby zdrowia o informacje o PROPECIA, które są napisane dla pracowników służby zdrowia. Aby uzyskać więcej informacji, zadzwoń pod numer 1-844-674-3200.
Jakie są składniki preparatu PROPECIA 1mg?
Składnik aktywny: finasteryd.
Składniki nieaktywne: monohydrat laktozy, celuloza mikrokrystaliczna, wstępnie żelowana skrobia, glikolan sodowy skrobi, hydroksypropylometyloceluloza, hydroksypropyloceluloza, dwutlenek tytanu, stearynian magnezu, talk, dokuzan sodu, żółty tlenek żelaza i czerwony tlenek żelaza.
Niniejsza informacja dla pacjenta została zatwierdzona przez amerykańską Agencję ds. Żywności i Leków.
