Zanaflex 2mg, 4mg Tizanidine Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Zanaflex 2mg i jak się go stosuje?
Zanaflex 2mg jest lekiem na receptę stosowanym w leczeniu objawów sztywności mięśni (spastyczności) związanych z takimi stanami jak porażenie mózgowe lub inne zaburzenia neurologiczne. Zanaflex 2mg może być stosowany samodzielnie lub z innymi lekami.
Zanaflex 2mg należy do klasy leków o nazwie Centralny Agonista Alfa-2-adrenergiczny.
Nie wiadomo, czy Zanaflex jest bezpieczny i skuteczny u dzieci.
Jakie są możliwe skutki uboczne Zanaflex?
Zanaflex 2mg może powodować poważne skutki uboczne, w tym:
- niskie ciśnienie krwi,
- nieprawidłowe wyniki testów czynności wątroby,
- senność,
- halucynacje,
- nadmierna senność,
- wolne tętno,
- suchość w ustach,
- zmęczenie i
- słabość
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Zanaflex obejmują:
- suchość w ustach,
- zmęczenie,
- słabość,
- zmęczenie,
- zmęczenie,
- zawroty głowy,
- zakażenie dróg moczowych,
- zaparcie,
- nieprawidłowe wyniki testów czynności wątroby,
- wymioty,
- zaburzenia mowy,
- leniwe oko (niedowidzenie),
- częstotliwość oddawania moczu,
- Objawy grypy,
- niekontrolowane ruchy mięśni,
- nerwowość,
- ból gardła i
- katar
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Zanaflex. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
Zanaflex® (chlorowodorek tyzanidyny) jest centralnym agonistą alfa2-adrenergicznym. Chlorowodorek tyzanidyny jest drobnokrystalicznym proszkiem o barwie od białej do białawej, który jest bezwonny lub o słabym charakterystycznym zapachu. Tyzanidyna jest słabo rozpuszczalna w wodzie i metanolu; rozpuszczalność w wodzie zmniejsza się wraz ze wzrostem pH. Jego nazwa chemiczna to monochlorowodorek 5-chloro-4-(2-imidazolin-2-ylamino)-2,1,3-benzotiadiazolu. Wzór cząsteczkowy tyzanidyny to C9H8ClN5S-HCl, jej masa cząsteczkowa to 290,2, a jej wzór strukturalny to:
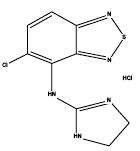
Zanaflex 4mg Capsules® są dostarczane w postaci kapsułek 2, 4 i 6 mg do podawania doustnego. Kapsułki Zanaflex® zawierają substancję czynną, chlorowodorek tyzanidyny (2,29 mg co odpowiada 2 mg zasady tyzanidyny, 4,58 mg co odpowiada 4 mg zasady tyzanidyny i 6,87 mg co odpowiada 6 mg zasady tyzanidyny) oraz składniki nieaktywne, hypromelozę, dwutlenek krzemu, kulki cukru, dwutlenek tytanu, żelatyna i barwniki.
Tabletki Zanaflex® są dostarczane w postaci tabletek 4 mg do podawania doustnego. Tabletki Zanaflex® zawierają składnik aktywny, chlorowodorek tyzanidyny (4,58 mg, co odpowiada 4 mg zasady tyzanidyny) oraz składniki nieaktywne, koloidalny dwutlenek krzemu, kwas stearynowy, celulozę mikrokrystaliczną i bezwodną laktozę.
WSKAZANIA
Zanaflex jest wskazany w leczeniu spastyczności. Ze względu na krótki czas trwania efektu terapeutycznego, leczenie preparatem Zanaflex powinno być zarezerwowane dla tych codziennych czynności i okresów, w których najważniejsze jest złagodzenie spastyczności [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
DAWKOWANIE I SPOSÓB PODAWANIA
Informacje o dawkowaniu
Zanaflex 2mg Capsules® lub Zanaflex® tabletki mogą być przepisywane z jedzeniem lub bez jedzenia. Po wybraniu preparatu i podjęciu decyzji o przyjmowaniu z jedzeniem lub bez, tego schematu nie należy zmieniać.
Pokarm ma złożony wpływ na farmakokinetykę tyzanidyny, która różni się w zależności od różnych preparatów. Kapsułki Zanaflex i tabletki Zanaflex są biorównoważne w warunkach na czczo (ponad 3 godziny po posiłku), ale nie w warunkach po posiłku (w ciągu 30 minut po posiłku). Te różnice farmakokinetyczne mogą skutkować klinicznie istotnymi różnicami w przypadku zmiany podawania tabletki i kapsułek oraz zmiany podawania między stanem po posiłku lub na czczo. Zmiany te mogą skutkować zwiększoną liczbą zdarzeń niepożądanych lub opóźnionym lub szybszym początkiem aktywności, w zależności od charakteru przełącznika. Z tego powodu lekarz przepisujący powinien być dokładnie zaznajomiony ze zmianami kinetyki związanymi z tymi różnymi stanami [patrz FARMAKOLOGIA KLINICZNA ].
Zalecana dawka początkowa to 2 mg. Ponieważ działanie preparatu Zanaflex osiąga szczyt w około 1 do 2 godzin po podaniu i zanika w ciągu 3 do 6 godzin po podaniu, leczenie można powtarzać w odstępach 6 do 8 godzin, w razie potrzeby, do maksymalnie trzech dawek w ciągu 24 godzin.
Dawkę można stopniowo zwiększać o 2 mg do 4 mg na każdą dawkę, z zachowaniem odstępu od 1 do 4 dni, aż do osiągnięcia zadowalającego zmniejszenia napięcia mięśniowego. Całkowita dawka dobowa nie powinna przekraczać 36 mg. Nie badano pojedynczych dawek większych niż 16 mg.
Dawkowanie u pacjentów z niewydolnością nerek
Zanaflex należy stosować ostrożnie u pacjentów z niewydolnością nerek (klirens kreatyniny OSTRZEŻENIA I ŚRODKI ].
Dawkowanie u pacjentów z niewydolnością wątroby
Zanaflex 4 mg należy stosować ostrożnie u pacjentów z zaburzeniami czynności wątroby. U tych pacjentów podczas dostosowywania dawki należy zmniejszyć poszczególne dawki. Jeśli wymagane są wyższe dawki, należy zwiększać dawki indywidualne, a nie częstotliwość dawkowania. Zaleca się monitorowanie aktywności aminotransferaz w punkcie wyjściowym i 1 miesiąc po osiągnięciu maksymalnej dawki lub w przypadku podejrzenia uszkodzenia wątroby [patrz Używaj w określonych populacjach ].
Odstawienie leku
Jeśli leczenie musi zostać przerwane, szczególnie u pacjentów, którzy otrzymywali duże dawki (20 mg do 36 mg na dobę) przez długi czas (9 tygodni lub dłużej) lub którzy mogą jednocześnie przyjmować narkotyki, dawkę należy zmniejszać powoli ( 2 mg do 4 mg na dobę), aby zminimalizować ryzyko odstawienia i nadciśnienia z odbicia, tachykardii i hipertonii [patrz Nadużywanie i uzależnienie od narkotyków ].
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Kapsułki
mg: jasnoniebieski nieprzezroczysty korpus z jasnoniebieskim nieprzezroczystym wieczkiem z nadrukiem „2 MG” na wieczku 4 mg: biały nieprzezroczysty korpus z niebieskim nieprzezroczystym wieczkiem z nadrukiem „4 MG” na wieczku 6 mg: niebieski nieprzezroczysty korpus z niebieskim nieprzezroczystym wieczkiem biały pasek i niebieska nieprzezroczysta czapka z nadrukiem „6 MG” na czapce
Tablety
4 mg białe, niepowlekane tabletki z kwadratową linią podziału po jednej stronie i wytłoczonym napisem „A594” po drugiej stronie
Składowania i stosowania
Kapsułki Zanaflex®
Zanaflex Capsules® (chlorowodorek tyzanidyny) kapsułki są dostępne w trzech mocach jako dwuczęściowe twarde kapsułki żelatynowe zawierające 2,29 mg, 4,58 mg i 6,87 mg chlorowodorku tyzanidyny, co odpowiada 2 mg, 4 mg i 6 mg zasady tyzanidyny.
Kapsułki 2 mg mają jasnoniebieski nieprzezroczysty korpus z jasnoniebieskim nieprzezroczystym wieczkiem z nadrukiem „2 MG” na wieczku: butelki zawierające 150 kapsułek ( NDC 70515-602-15)
Kapsułki 4 mg mają biały nieprzezroczysty korpus z niebieskim nieprzezroczystym wieczkiem z nadrukiem „4 MG” na wieczku: butelki zawierające 150 kapsułek ( NDC 70515-604-15)
Kapsułki 6 mg mają niebieski nieprzezroczysty korpus z białym paskiem i niebieskim nieprzezroczystym wieczkiem z nadrukiem „6 MG” na kapsułkach: butelki zawierające 150 kapsułek ( NDC 70515-606-15)
Przechowywać w 25°C (77°F); dopuszczalne odchylenia od 15°C do 30°C (59°F do 86°F) [patrz Temperatura pokojowa kontrolowana przez USP ]. Dozować w pojemnikach z zamknięciem zabezpieczającym przed dziećmi.
Tabletki Zanaflex®
Tabletki Zanaflex® (chlorowodorek tyzanidyny) są dostępne jako 4 mg białe, niepowlekane tabletki zawierające 4,58 mg chlorowodorku tyzanidyny, co odpowiada 4 mg zasady tyzanidyny. Tabletki mają po jednej stronie kwadratową kreskę, a po drugiej stronie wytłoczony jest napis „A594”. Tabletki są dostarczane w następujący sposób: butelki po 150 tabletek (NDC 70515-594-15).
Przechowywać w 25°C (77°F); dopuszczalne odchylenia od 15°C do 30°C (59°F do 86°F) [patrz Temperatura pokojowa kontrolowana przez USP ].
Dozować w pojemnikach z zamknięciem zabezpieczającym przed dziećmi.
Wyprodukowano dla: Covis Pharma Zug, 6300 Szwajcaria. Poprawiono: grudzień 2020 r.
SKUTKI UBOCZNE
Następujące działania niepożądane opisano w innych punktach informacji o przepisaniu leku:
- Niedociśnienie [patrz OSTRZEŻENIA I ŚRODKI ]
- Uraz wątroby [patrz OSTRZEŻENIA I ŚRODKI ]
- Sedacja [patrz OSTRZEŻENIA I ŚRODKI ]
- Halucynoza / Objawy psychotyczne [patrz OSTRZEŻENIA I ŚRODKI ]
- Reakcje nadwrażliwości [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce klinicznej.
Przeprowadzono trzy podwójnie ślepe, randomizowane, kontrolowane placebo badania kliniczne w celu oceny wpływu tyzanidyny na kontrolę spastyczności. Przeprowadzono dwa badania u pacjentów ze stwardnieniem rozsianym i jedno u pacjentów z urazem rdzenia kręgowego. Każde badanie miało 13-tygodniowy okres aktywnego leczenia, który obejmował 3-tygodniową fazę zwiększania dawki do maksymalnej tolerowanej dawki do 36 mg/dobę w trzech dawkach podzielonych, 9-tygodniową fazę plateau, w której dawka tyzanidyny była utrzymywana na stałym poziomie oraz Zmniejszanie dawki o 1 tydzień. W sumie 264 pacjentów otrzymywało tyzanidynę, a 261 pacjentów otrzymywało placebo. We wszystkich trzech badaniach wiek pacjentów wahał się od 15 do 69 lat, a 51,4 procent stanowiły kobiety. Mediana dawki w fazie plateau wahała się od 20-28 mg/dobę.
Najczęstszymi działaniami niepożądanymi zgłaszanymi w badaniach klinicznych z zastosowaniem wielokrotnych dawek, kontrolowanych placebo, obejmujących 264 pacjentów ze spastycznością, były suchość w ustach, senność/uspokojenie, astenia (osłabienie, zmęczenie i (lub) zmęczenie) oraz zawroty głowy. Trzy czwarte pacjentów oceniło zdarzenia jako łagodne do umiarkowanych, a jedna czwarta pacjentów oceniła zdarzenia jako ciężkie. Zdarzenia te wydawały się być związane z dawką.
W tabeli 1 wymieniono oznaki i objawy, które zgłoszono u ponad 2% pacjentów w trzech badaniach z wielokrotnymi dawkami kontrolowanymi placebo, którzy otrzymywali Zanaflex, gdzie częstość w grupie Zanaflex była większa niż w grupie placebo. Dla celów porównawczych podano również odpowiednią częstotliwość zdarzenia (na 100 pacjentów) wśród pacjentów leczonych placebo.
W badaniu z pojedynczą dawką, kontrolowanym placebo, obejmującym 142 pacjentów ze spastycznością spowodowaną stwardnieniem rozsianym (Badanie 1) [patrz Studia kliniczne ], pacjentów zapytano konkretnie, czy wystąpiły u nich cztery najczęstsze działania niepożądane: suchość w ustach, senność (senność), osłabienie (osłabienie, zmęczenie i/lub zmęczenie) i zawroty głowy. Ponadto obserwowano niedociśnienie i bradykardię. Występowanie tych reakcji podsumowano w Tabeli 2. Inne zdarzenia były na ogół zgłaszane z częstością 2% lub mniejszą.
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania preparatu Zanaflex po zatwierdzeniu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Niektóre zdarzenia, takie jak senność, suchość w ustach, niedociśnienie, obniżone ciśnienie krwi, bradykardia, zawroty głowy, osłabienie lub osłabienie, skurcze mięśni, omamy, zmęczenie, nieprawidłowe wyniki testów czynnościowych wątroby i hepatotoksyczność, były obserwowane w badaniach po wprowadzeniu do obrotu i badaniach klinicznych. w poprzednich rozdziałach tego dokumentu.
Następujące działania niepożądane zostały zidentyfikowane jako występujące po wprowadzeniu preparatu Zanaflex do obrotu. Na podstawie dostarczonych informacji dotyczących tych reakcji nie można całkowicie wykluczyć związku przyczynowego z produktem Zanaflex. Zdarzenia są wymienione w kolejności malejącego znaczenia klinicznego; dotkliwość w warunkach postmarketingowych nie jest zgłaszana.
- Zespół Stevensa Johnsona
- Reakcja anafilaktyczna
- Złuszczające zapalenie skóry
- Częstoskurcz komorowy
- Zapalenie wątroby
- Konwulsja
- Depresja
- Ból stawów
- Parestezje
- Wysypka
- Drżenie
INTERAKCJE Z LEKAMI
Fluwoksamina
Jednoczesne stosowanie fluwoksaminy i Zanaflex 4 mg jest przeciwwskazane. Zmiany farmakokinetyki tyzanidyny podawanej z fluwoksaminą powodowały znaczne obniżenie ciśnienia krwi, zwiększoną senność i nasilenie zaburzeń psychomotorycznych [patrz PRZECIWWSKAZANIA oraz FARMAKOLOGIA KLINICZNA ].
Ciprofloksacyna
Jednoczesne stosowanie cyprofloksacyny i preparatu Zanaflex jest przeciwwskazane. Zmiany farmakokinetyki tyzanidyny podawanej z cyprofloksacyną powodowały znaczne obniżenie ciśnienia krwi, nasilenie senności i nasilenie zaburzeń psychomotorycznych [patrz PRZECIWWSKAZANIA oraz FARMAKOLOGIA KLINICZNA ].
Inhibitory CYP1A2 inne niż fluwoksamina i cyprofloksacyna
Ze względu na potencjalne interakcje, jednoczesne stosowanie preparatu Zanaflex z innymi inhibitorami CYP1A2, takimi jak zileuton, fluorochinolony inne niż silne inhibitory CYP1A2 (które są przeciwwskazane), leki przeciwarytmiczne (amiodaron, meksyletyna, propafenon i werapamil), cymetydyna, famotydyna, doustne środki antykoncepcyjne acyklowiru i tyklopidyny). Jeśli ich stosowanie jest klinicznie konieczne, leczenie należy rozpocząć od dawki 2 mg i zwiększać ją o 2-4 mg na dobę w zależności od odpowiedzi pacjenta na leczenie. W przypadku wystąpienia działań niepożądanych, takich jak niedociśnienie, bradykardia lub nadmierna senność, należy zmniejszyć lub przerwać leczenie produktem Zanaflex [patrz OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
Doustne środki antykoncepcyjne
Nie zaleca się jednoczesnego stosowania produktu Zanaflex 2 mg z doustnymi środkami antykoncepcyjnymi. Jeśli jednak jednoczesne stosowanie jest klinicznie konieczne, należy rozpocząć podawanie preparatu Zanaflex 4 mg pojedynczą dawką 2 mg i zwiększać dawkę o 2-4 mg na dobę w zależności od odpowiedzi pacjenta na leczenie. W przypadku wystąpienia działań niepożądanych, takich jak niedociśnienie, bradykardia lub nadmierna senność, należy zmniejszyć lub przerwać leczenie produktem Zanaflex [patrz FARMAKOLOGIA KLINICZNA ].
Alkohol
Alkohol zwiększa całkowitą ilość leku w krwiobiegu po dawce Zanaflex. Wiązało się to ze wzrostem działań niepożądanych leku Zanaflex. Działanie depresyjne na ośrodkowy układ nerwowy Zanaflexu i alkoholu sumuje się [patrz FARMAKOLOGIA KLINICZNA ].
Inne leki działające hamująco na ośrodkowy układ nerwowy
Uspokajające działanie preparatu Zanaflex z lekami działającymi depresyjnie na ośrodkowy układ nerwowy (np. benzodiazepiny, opioidy, trójpierścieniowe leki przeciwdepresyjne) może się sumować. Monitoruj pacjentów, którzy przyjmują Zanaflex 2 mg z innym lekiem hamującym czynność ośrodkowego układu nerwowego, pod kątem objawów nadmiernej sedacji [patrz FARMAKOLOGIA KLINICZNA ].
Agoniści receptorów α2-adrenergicznych
Ponieważ działanie hipotensyjne może się kumulować, nie zaleca się stosowania preparatu Zanaflex 4 mg z innymi agonistami receptorów α2-adrenergicznych [patrz OSTRZEŻENIA I ŚRODKI ].
Nadużywanie i uzależnienie od narkotyków
Nadużywać
Potencjał nadużyć nie był oceniany w badaniach na ludziach. Po treningu szczury były w stanie odróżnić tyzanidynę od soli fizjologicznej w standardowym paradygmacie rozróżniania, ale nie uogólniły wpływu morfiny, kokainy, diazepamu lub fenobarbitalu na tyzanidynę.
Zależność
Tyzanidyna jest blisko spokrewniona z klonidyną, która jest często nadużywana w połączeniu z narkotykami i wiadomo, że powoduje objawy z odbicia po nagłym odstawieniu. Zgłoszono trzy przypadki objawów z odbicia po nagłym odstawieniu tyzanidyny. Opisy przypadków sugerują, że ci pacjenci również nadużywali narkotyków. Objawy odstawienia obejmowały nadciśnienie, tachykardię, hipertonię, drżenie i lęk. Objawy odstawienia są bardziej prawdopodobne w przypadkach, gdy stosuje się duże dawki, zwłaszcza przez dłuższy czas lub przy jednoczesnym stosowaniu narkotyków. Jeśli leczenie wymaga przerwania, dawkę należy zmniejszać powoli, aby zminimalizować ryzyko wystąpienia objawów odstawiennych [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Wykazano, że małpy samodzielnie podawały tyzanidynę w sposób zależny od dawki, a nagłe zaprzestanie podawania tyzanidyny powodowało przejściowe objawy odstawienia po dawkach >35-krotnie większych niż maksymalna zalecana dawka u ludzi w przeliczeniu na mg/m2. Te przejściowe objawy odstawienia (zwiększona lokomocja, drgania ciała i awersyjne zachowanie wobec obserwatora) nie zostały odwrócone po podaniu naloksonu.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Niedociśnienie
Tyzanidyna jest agonistą receptorów α2-adrenergicznych, który może powodować niedociśnienie. Omdlenie zostało zgłoszone po wprowadzeniu do obrotu. Prawdopodobieństwo znacznego niedociśnienia można zminimalizować poprzez dostosowanie dawki i zwrócenie uwagi na oznaki i objawy niedociśnienia przed zwiększeniem dawki. Ponadto pacjenci przechodzący z pozycji leżącej na sztywno wyprostowanej mogą być narażeni na zwiększone ryzyko niedociśnienia i efektów ortostatycznych.
Monitorować niedociśnienie, gdy Zanaflex jest stosowany u pacjentów otrzymujących jednocześnie terapię przeciwnadciśnieniową. Nie zaleca się stosowania preparatu Zanaflex 2mg z innymi agonistami receptora α2-adrenergicznego. Podczas jednoczesnego podawania fluwoksaminy lub cyprofloksacyny i pojedynczych dawek 4 mg preparatu Zanaflex zgłaszano klinicznie istotne niedociśnienie (spadek ciśnienia skurczowego i rozkurczowego). Dlatego jednoczesne stosowanie preparatu Zanaflex z fluwoksaminą lub cyprofloksacyną, silnymi inhibitorami CYP1A2, jest przeciwwskazane [patrz PRZECIWWSKAZANIA oraz INTERAKCJE Z LEKAMI ].
Ryzyko uszkodzenia wątroby
Zanaflex może powodować uszkodzenie wątroby wątrobowokomórkowej. Zanaflex 4 mg należy stosować ostrożnie u pacjentów z zaburzeniami czynności wątroby. Zaleca się monitorowanie aktywności aminotransferaz w punkcie wyjściowym i 1 miesiąc po osiągnięciu maksymalnej dawki lub w przypadku podejrzenia uszkodzenia wątroby [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz Używaj w określonych populacjach ].
Opanowanie
Zanaflex może powodować sedację, która może zakłócać codzienną aktywność. W badaniach z dawką wielokrotną częstość występowania sedacji u pacjentów osiągnęła najwyższy poziom po pierwszym tygodniu dostosowywania dawki, a następnie pozostawała stabilna przez czas trwania fazy podtrzymującej badania. Działanie depresyjne na OUN produktu Zanaflex z alkoholem i innymi lekami depresyjnymi na OUN (np. benzodiazepinami, opioidami, trójpierścieniowymi lekami przeciwdepresyjnymi) może się sumować. Monitoruj pacjentów przyjmujących Zanaflex 4 mg z innym lekiem hamującym czynność ośrodkowego układu nerwowego pod kątem objawów nadmiernej sedacji [patrz INTERAKCJE Z LEKAMI ].

Halucynoza/Objawy podobne do psychotycznych
Stosowanie leku Zanaflex 4 mg wiązało się z omamami. Powstałe halucynacje wzrokowe lub urojenia zgłoszono u 5 ze 170 pacjentów (3%) w dwóch kontrolowanych badaniach klinicznych w Ameryce Północnej. Większość pacjentów miała świadomość, że wydarzenia były nierealne. Jeden pacjent rozwinął psychozę w związku z halucynacjami. Jeden z tych 5 pacjentów nadal miał problemy przez co najmniej 2 tygodnie po odstawieniu tyzanidyny. Rozważ przerwanie stosowania preparatu Zanaflex u pacjentów, u których wystąpią halucynacje.
Interakcja z inhibitorami CYP1A2
Ze względu na potencjalne interakcje lekowe, Zanaflex 4 mg jest przeciwwskazany u pacjentów przyjmujących silne inhibitory CYP1A2, takie jak fluwoksamina lub cyprofloksacyna. Działania niepożądane, takie jak niedociśnienie, bradykardia lub nadmierna senność mogą wystąpić, gdy Zanaflex jest przyjmowany z innymi inhibitorami CYP1A2, takimi jak zileuton, fluorochinolony inne niż cyprofloksacyna (co jest przeciwwskazane), leki przeciwarytmiczne (amiodaron, meksyletyna, propafenon), cymetydyna, famotydyna, środki antykoncepcyjne, acyklowir i tiklopidyna). Należy unikać jednoczesnego stosowania, chyba że konieczność leczenia preparatem Zanaflex 2 mg jest klinicznie ewidentna. W takim przypadku należy zachować ostrożność [patrz INTERAKCJE Z LEKAMI oraz FARMAKOLOGIA KLINICZNA ].
Reakcje nadwrażliwości
Zanaflex może powodować anafilaksję. Zgłaszano objawy przedmiotowe i podmiotowe, w tym upośledzenie oddychania, pokrzywkę i obrzęk naczynioruchowy gardła i języka. Pacjentów należy poinformować o przedmiotowych i podmiotowych objawach ciężkich reakcji alergicznych oraz poinstruować, aby w przypadku wystąpienia takich objawów i objawów przerwali stosowanie preparatu Zanaflex i natychmiast udali się do lekarza [patrz PRZECIWWSKAZANIA ].
Zwiększone ryzyko działań niepożądanych u pacjentów z niewydolnością nerek
Zanaflex należy stosować ostrożnie u pacjentów z niewydolnością nerek (klirens kreatyniny DAWKOWANIE I SPOSÓB PODAWANIA oraz Używaj w określonych populacjach ].
Wycofanie działań niepożądanych
Działania niepożądane związane z odstawieniem obejmują nadciśnienie z odbicia, tachykardię i hipertonię. Aby zminimalizować ryzyko wystąpienia tych reakcji, szczególnie u pacjentów, którzy otrzymywali duże dawki (20 do 28 mg na dobę) przez długi czas (9 tygodni lub dłużej) lub którzy mogą być jednocześnie leczeni narkotykami, dawkę należy zmniejszyć powoli (2 do 4 mg dziennie) [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Karcynogeneza
Tyzanidynę podawano myszom przez 78 tygodni w dawkach doustnych do 16 mg/kg/dobę, co stanowi dwukrotność maksymalnej zalecanej dawki u ludzi (MRHD) wynoszącej 36 mg/dobę na podstawie powierzchni ciała (mg/m²). Tyzanidynę podawano szczurom przez 104 tygodnie w dawkach doustnych do 9 mg/kg/dobę, co stanowi 2,5-krotność MRHD w przeliczeniu na mg/m². Nie było wzrostu guzów u żadnego z gatunków.
Mutageneza
Tyzanidyna dała wynik negatywny in vitro (mutacja powrotna bakterii [Ames], mutacja genów ssaków i test aberracji chromosomowych w komórkach ssaków) oraz in vivo (mikrojąderka szpiku kostnego i cytogenetyka).
Upośledzenie płodności
Doustne podawanie tyzanidyny szczurom przed i podczas krycia oraz kontynuowanie u samic we wczesnej ciąży powodowało zmniejszenie płodności u samców i samic szczurów w dawkach odpowiednio 30 i 10 mg/kg/dobę. Nie zaobserwowano wpływu na płodność przy dawkach 10 (mężczyźni) i 3 (kobiety) mg/kg/dobę, które są odpowiednio około 3 razy i podobne do MRHD w przeliczeniu na mg/m2.
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
Brak odpowiednich danych dotyczących ryzyka rozwoju związanego ze stosowaniem preparatu Zanaflex 2 mg u kobiet w ciąży. W badaniach na zwierzętach podawanie tyzanidyny w czasie ciąży powodowało toksyczność rozwojową (śmiertelność zarodków i potomstwa oraz niedobory wzrostu) w dawkach mniejszych niż stosowane klinicznie, które nie były związane z toksycznością matczyną (patrz Dane zwierząt ).
W ogólnej populacji USA szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2% - 4% i 15% - 20%. Podstawowe ryzyko poważnych wad wrodzonych i poronienia dla wskazanej populacji jest nieznane.
Dane
Dane zwierząt
Doustne podawanie tyzanidyny (0,3 do 100 mg/kg/dobę) ciężarnym samicom szczurów w okresie organogenezy powodowało śmiertelność zarodków i potomstwa oraz zmniejszenie masy ciała przy dawkach 30 mg/kg/dobę i większych. Toksyczność matczyną obserwowano przy najwyższej badanej dawce. Dawka niepowodująca toksycznego wpływu na rozwój zarodka i płodu u szczurów (3 mg/kg/dobę) jest podobna do maksymalnej zalecanej dawki u ludzi (MRHD) wynoszącej 36 mg/dobę na podstawie powierzchni ciała (mg/m²).
Doustne podawanie tyzanidyny (1 do 100 mg/kg/dobę) ciężarnym królikom w okresie organogenezy powodowało śmiertelność zarodków i potomstwa we wszystkich dawkach. Toksyczność matczyną obserwowano przy najwyższej badanej dawce. Doustne podawanie tyzanidyny (10 i 30 mg/kg/dobę) w okresie okołoporodowym ciąży (2-6 dni przed porodem) powodowało zwiększoną śmiertelność potomstwa po urodzeniu w obu dawkach. Nie zidentyfikowano dawki niepowodującej toksycznego wpływu na rozwój zarodka i płodu u królików. Najniższa testowana dawka (1 mg/kg/dzień) jest mniejsza niż MRHD w przeliczeniu na mg/m².
W badaniu rozwoju przed- i pourodzeniowego u szczurów, doustne podawanie tyzanidyny (3 do 30 mg/kg/dobę) powodowało zwiększoną śmiertelność potomstwa po urodzeniu. Nie zidentyfikowano dawki niepowodującej wpływu na przed- i pourodzeniową toksyczność rozwojową. Najniższa badana dawka (3 mg/kg/dzień) jest podobna do MRHD odpowiednio w mg/m².
Laktacja
Podsumowanie ryzyka
Brak danych dotyczących obecności tyzanidyny w mleku ludzkim, wpływu na niemowlę karmione piersią lub wpływu na wytwarzanie mleka ludzkiego. Badania na zwierzętach wykazały obecność tyzanidyny w mleku zwierząt w okresie laktacji.
Korzyści rozwojowe i zdrowotne wynikające z karmienia piersią powinny być brane pod uwagę wraz z klinicznym zapotrzebowaniem matki na Zanaflex 4 mg oraz wszelkimi potencjalnymi niekorzystnymi skutkami dla karmionego piersią dziecka przez Zanaflex lub z powodu schorzenia matki.
Kobiety i mężczyźni o potencjale rozrodczym
Nie ma odpowiednich i dobrze kontrolowanych badań u ludzi dotyczących wpływu leku Zanaflex 4 mg na potencjał rozrodczy kobiet lub mężczyzn. Doustne podawanie tyzanidyny samcom i samicom szczurów powodowało niekorzystny wpływ na płodność [patrz Toksykologia niekliniczna ].
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność u pacjentów pediatrycznych nie zostały ustalone.
Zastosowanie geriatryczne
Wiadomo, że Zanaflex 2 mg jest w znacznym stopniu wydalany przez nerki, a ryzyko działań niepożądanych tego leku może być większe u pacjentów z zaburzeniami czynności nerek. Ponieważ u pacjentów w podeszłym wieku istnieje większe prawdopodobieństwo upośledzenia czynności nerek, należy zachować ostrożność przy doborze dawki i może być przydatne monitorowanie czynności nerek.
Badania kliniczne preparatu Zanaflex 2 mg nie obejmowały wystarczającej liczby osób w wieku 65 lat i starszych, aby określić, czy reagują oni inaczej niż osoby młodsze. Porównanie krzyżowe danych farmakokinetycznych po podaniu pojedynczej dawki 6 mg Zanaflex 2 mg wykazało, że młodsi pacjenci usuwali lek cztery razy szybciej niż osoby starsze. U pacjentów w podeszłym wieku z niewydolnością nerek (klirens kreatyniny
Upośledzona funkcja nerek
Wiadomo, że zanaflex jest w znacznym stopniu wydalany przez nerki, a ryzyko wystąpienia działań niepożądanych tego leku może być większe u pacjentów z zaburzeniami czynności nerek. U pacjentów z niewydolnością nerek (klirens kreatyniny DAWKOWANIE I SPOSÓB PODAWANIA , OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
Upośledzona funkcja wątroby
Nie oceniano wpływu zaburzeń czynności wątroby na farmakokinetykę tyzanidyny. Ponieważ tyzanidyna jest intensywnie metabolizowana w wątrobie, można się spodziewać, że zaburzenia czynności wątroby będą miały istotny wpływ na farmakokinetykę tyzanidyny [patrz DAWKOWANIE I PODAWANIE , OSTRZEŻENIA I ŚRODKI , oraz FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
Przegląd bazy danych nadzoru bezpieczeństwa ujawnił przypadki celowego i przypadkowego przedawkowania preparatu Zanaflex. Niektóre przypadki zakończyły się śmiercią, a wiele celowych przedawkowań dotyczyło wielu leków, w tym leków hamujących ośrodkowy układ nerwowy. Objawy kliniczne przedawkowania tyzanidyny były zgodne z jej znaną farmakologią. W większości przypadków zaobserwowano zmniejszenie czucia, w tym letarg, senność, splątanie i śpiączkę. Obserwuje się również obniżoną czynność serca, w tym najczęściej bradykardię i niedociśnienie. Inną powszechną cechą przedawkowania tyzanidyny jest depresja oddechowa.
przypadku przedawkowania należy podjąć podstawowe kroki w celu zapewnienia odpowiedniej drożności dróg oddechowych oraz monitorowania układu sercowo-naczyniowego i oddechowego. Tyzanidyna jest lekiem rozpuszczalnym w tłuszczach, który jest tylko słabo rozpuszczalny w wodzie i metanolu. Dlatego dializa prawdopodobnie nie będzie skuteczną metodą usuwania leku z organizmu. Na ogół objawy ustępują w ciągu jednego do trzech dni po odstawieniu tyzanidyny i zastosowaniu odpowiedniej terapii. Ze względu na podobny mechanizm działania objawy i postępowanie w przypadku przedawkowania tyzanidyny są podobne do występujących po przedawkowaniu klonidyny. Aby uzyskać najnowsze informacje dotyczące postępowania w przypadku przedawkowania, skontaktuj się z centrum kontroli zatruć.
PRZECIWWSKAZANIA
Zanaflex jest przeciwwskazany u pacjentów przyjmujących silne inhibitory CYP1A2, takie jak fluwoksamina lub cyprofloksacyna [patrz INTERAKCJE Z LEKAMI ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Tyzanidyna jest centralnym agonistą receptora alfa-2-adrenergicznego i przypuszczalnie zmniejsza spastyczność poprzez zwiększenie presynaptycznego hamowania neuronów ruchowych. Wpływ tyzanidyny jest największy na szlaki polisynaptyczne. Uważa się, że ogólny efekt tych działań zmniejsza facylitację neuronów ruchowych kręgosłupa.
Farmakokinetyka
Absorpcja i dystrybucja
Po podaniu doustnym tyzanidyna jest zasadniczo całkowicie wchłaniana. Całkowita biodostępność tyzanidyny po podaniu doustnym wynosi około 40% (CV = 24%), z powodu intensywnego metabolizmu pierwszego przejścia przez wątrobę. Tyzanidyna ulega znacznej dystrybucji w organizmie, a średnia objętość dystrybucji w stanie stacjonarnym wynosi 2,4 l/kg (CV = 21%) po podaniu dożylnym zdrowym dorosłym ochotnikom. Tyzanidyna wiąże się z białkami osocza w około 30%.
Różnice między kapsułkami 4 mg Zanaflex® a tabletkami Zanaflex®
Zanaflex 2mg Capsules® i Zanaflex® tabletki są biorównoważne w warunkach na czczo, ale nie po posiłku. Pojedynczą dawkę dwóch tabletek 4 mg lub dwóch kapsułek 4 mg podawano w warunkach po posiłku i na czczo w otwartym, czterookresowym, randomizowanym badaniu krzyżowym u 96 ochotników, z których 81 kwalifikowało się do analizy statystycznej. Po podaniu doustnym tabletki lub kapsułki (na czczo) maksymalne stężenie tyzanidyny w osoczu występowało po 1 godzinie po podaniu z okresem półtrwania wynoszącym około 2 godziny. Gdy dwie tabletki 4 mg podawano z jedzeniem, średnie maksymalne stężenie w osoczu zwiększało się o około 30%, a mediana czasu do osiągnięcia maksymalnego stężenia w osoczu wzrosła o 25 minut do 1 godziny i 25 minut. W przeciwieństwie do tego, gdy dwie kapsułki 4 mg podawano z jedzeniem, średnie maksymalne stężenie w osoczu zmniejszyło się o 20%, mediana czasu do maksymalnego stężenia w osoczu wzrosła o 2 do 3 godzin. W konsekwencji średnie Cmax dla kapsułki podawanej z pokarmem wynosi około 66% Cmax dla tabletki podawanej z pokarmem. Pokarm zwiększył również stopień wchłaniania zarówno tabletek, jak i kapsułek. Wzrost w przypadku tabletki (~30%) był znacznie większy niż w przypadku kapsułki (~10%). W konsekwencji, gdy każdy był podawany z pokarmem, ilość wchłonięta z kapsułki stanowiła około 80% ilości wchłoniętej z tabletki. Podawanie zawartości kapsułki posypanej musem jabłkowym nie było biorównoważne z podawaniem nienaruszonej kapsułki na czczo. Podawanie zawartości kapsułki z musem jabłkowym spowodowało 15%-20% wzrost Cmax i AUC tyzanidyny oraz 15-minutowe zmniejszenie mediany czasu opóźnienia i czasu do maksymalnego stężenia w porównaniu z podaniem nienaruszonej kapsułki na czczo.
Rycina 1: Średnie stężenie tyzanidyny w zależności od czasu dla tabletek i kapsułek Zanaflex (2 × 4 mg) w warunkach na czczo i po posiłku
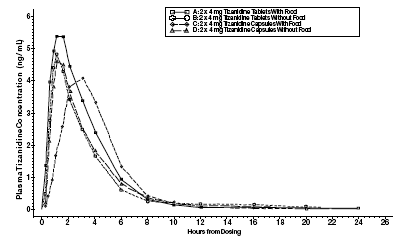
Metabolizm i wydalanie
Tyzanidyna ma farmakokinetykę liniową w stosunku do dawek badanych w badaniach klinicznych (1-20 mg). Okres półtrwania tyzanidyny wynosi około 2,5 godziny (CV=33%). Około 95% podanej dawki jest metabolizowane. Głównym izoenzymem cytochromu P450 biorącym udział w metabolizmie tyzanidyny jest CYP1A2. Nie wiadomo, czy metabolity tyzanidyny są aktywne; ich okresy półtrwania wahają się od 20 do 40 godzin.
Po jednorazowym i wielokrotnym podaniu doustnym 14C-tyzanidyny średnio 60% i 20% całkowitej radioaktywności odzyskano odpowiednio w moczu i kale.
Określone populacje
Efekty wieku
Nie przeprowadzono żadnego specyficznego badania farmakokinetycznego w celu zbadania wpływu wieku. Porównanie między badaniami danych farmakokinetycznych po podaniu pojedynczej dawki 6 mg Zanaflex 2 mg wykazało, że młodsi pacjenci usuwali lek cztery razy szybciej niż osoby starsze. Zanaflex 4 mg nie był badany u dzieci [patrz Używaj w określonych populacjach ].
Niewydolność wątroby
Nie oceniano wpływu zaburzeń czynności wątroby na farmakokinetykę tyzanidyny. Ponieważ tyzanidyna jest w znacznym stopniu metabolizowana w wątrobie, można oczekiwać, że zaburzenia czynności wątroby będą miały istotny wpływ na farmakokinetykę tyzanidyny. Zanaflex nie jest zalecany w tej populacji pacjentów [patrz Używaj w określonych populacjach ].
Zaburzenia czynności nerek
Klirens tyzanidyny jest zmniejszony o ponad 50% u pacjentów w podeszłym wieku z niewydolnością nerek (klirens kreatyniny OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
Wpływ płci
Nie przeprowadzono żadnego specyficznego badania farmakokinetycznego w celu zbadania wpływu płci. Jednak retrospektywna analiza danych farmakokinetycznych po podaniu pojedynczej i wielokrotnej dawki 4 mg Zanaflex 2 mg wykazała, że płeć nie miała wpływu na farmakokinetykę tyzanidyny.
Efekty wyścigu
Nie badano różnic farmakokinetycznych ze względu na rasę.
Interakcje leków
Inhibitory CYP1A2
Interakcja pomiędzy produktem Zanaflex a fluwoksaminą lub cyprofloksacyną jest najprawdopodobniej spowodowana hamowaniem CYP1A2 przez fluwoksaminę lub cyprofloksacynę. Wpływ fluwoksaminy na farmakokinetykę pojedynczej dawki 4 mg preparatu Zanaflex zbadano u 10 zdrowych osób. Cmax, AUC i okres półtrwania tyzanidyny zwiększyły się odpowiednio 12-krotnie, 33-krotnie i 3-krotnie. Wpływ cyprofloksacyny na farmakokinetykę pojedynczej dawki 4 mg produktu Zanaflex 4 mg badano u 10 zdrowych osób. Cmax i AUC tyzanidyny zwiększyły się odpowiednio 7-krotnie i 10-krotnie [patrz PRZECIWWSKAZANIA ].
Chociaż nie przeprowadzono badań klinicznych oceniających wpływ innych inhibitorów CYP1A2 na tyzanidynę, inne inhibitory CYP1A2, takie jak zileuton, inne fluorochinolony, leki przeciwarytmiczne (amiodaron, meksyletyna, propafenon i werapamil), cymetydyna, famotydyna, doustne środki antykoncepcyjne, acyklowir i tiklopi może również prowadzić do znacznego wzrostu stężenia tyzanidyny we krwi [patrz OSTRZEŻENIA I ŚRODKI ].
Badania in vitro izoenzymów cytochromu P450 z użyciem mikrosomów ludzkiej wątroby wskazują, że ani tyzanidyna, ani jej główne metabolity prawdopodobnie nie wpływają na metabolizm innych leków metabolizowanych przez izoenzymy cytochromu P450.
Doustne środki antykoncepcyjne
Nie przeprowadzono żadnego specyficznego badania farmakokinetycznego w celu zbadania interakcji między doustnymi środkami antykoncepcyjnymi a Zanaflex. Retrospektywna analiza populacyjnych danych farmakokinetycznych po podaniu pojedynczej i wielokrotnej dawki 4 mg Zanaflex wykazała jednak, że kobiety przyjmujące jednocześnie doustne środki antykoncepcyjne miały o 50% mniejszy klirens tyzanidyny w porównaniu z kobietami niestosującymi doustnych środków antykoncepcyjnych [patrz OSTRZEŻENIA I ŚRODKI ].
Paracetamol
Tyzanidyna opóźniała Tmax acetaminofenu o 16 minut. Paracetamol nie wpływał na farmakokinetykę tyzanidyny.
Alkohol
Alkohol zwiększał AUC tyzanidyny o około 20%, jednocześnie zwiększając jej Cmax o około 15%. Wiązało się to ze zwiększeniem działań niepożądanych tyzanidyny. Działanie tyzanidyny i alkoholu na ośrodkowy układ nerwowy sumuje się.
Studia kliniczne
Zdolność tyzanidyny do zmniejszania zwiększonego napięcia mięśniowego związanego ze spastycznością wykazano w dwóch odpowiednich i dobrze kontrolowanych badaniach u pacjentów ze stwardnieniem rozsianym lub urazem rdzenia kręgowego (Badania 1 i 2).
Badanie pojedynczej dawki u pacjentów ze stwardnieniem rozsianym ze spastycznością
W badaniu 1 pacjenci ze stwardnieniem rozsianym zostali losowo przydzieleni do otrzymywania pojedynczych dawek doustnych leku lub placebo. Pacjenci i oceniający byli ślepi na przydział leczenia i podjęto wysiłki w celu zmniejszenia prawdopodobieństwa, że oceniający dowiadują się pośrednio o przydziale leczenia (np. nie zapewniali pacjentom bezpośredniej opieki i zabroniono im zadawania pytań dotyczących skutków ubocznych). W sumie 140 pacjentów otrzymywało placebo, 8 mg lub 16 mg Zanaflexu.
Odpowiedź oceniano na podstawie badania fizykalnego; napięcie mięśniowe oceniano w 5-punktowej skali (wynik Ashwortha), z wynikiem 0 używanym do opisania prawidłowego napięcia mięśniowego. Wynik 1 wskazywał na lekkie spastyczne złapanie, podczas gdy wynik 2 wskazywał na wyraźniejszy opór mięśni. Ocena 3 została użyta do opisania znacznego wzrostu tonu, utrudniającego ruch bierny. Mięsień unieruchomiony przez spastyczność otrzymał wynik 4. Zebrano również liczbę spazmów.
Oceny dokonywano po 1, 2, 3 i 6 godzinach po zabiegu. Statystycznie istotne zmniejszenie wyniku Ashwortha dla preparatu Zanaflex 2 mg w porównaniu z placebo wykryto po 1, 2 i 3 godzinach po leczeniu. Rysunek 2 poniżej przedstawia porównanie średniej zmiany napięcia mięśniowego od wartości wyjściowej, mierzonej skalą Ashwortha. Największe zmniejszenie napięcia mięśniowego nastąpiło od 1 do 2 godzin po leczeniu. Po 6 godzinach po leczeniu napięcie mięśniowe w grupach otrzymujących 8 i 16 mg preparatu Zanaflex 2 mg było nie do odróżnienia od napięcia mięśniowego u pacjentów otrzymujących placebo. U danego pacjenta poprawa napięcia mięśniowego była skorelowana ze stężeniem w osoczu. Stężenia w osoczu różniły się w zależności od pacjenta przy danej dawce. Chociaż 16 mg powodowało większy efekt, zdarzenia niepożądane, w tym niedociśnienie, były częstsze i cięższe niż w grupie 8 mg. Nie było różnic w liczbie skurczów występujących w każdej grupie.
Rycina 2: Badanie z pojedynczą dawką — średnia zmiana napięcia mięśniowego w stosunku do wartości wyjściowej mierzona skalą Ashworth ± 95% przedział ufności (ujemny wynik Ashwortha oznacza poprawę napięcia mięśniowego w stosunku do wartości wyjściowej)
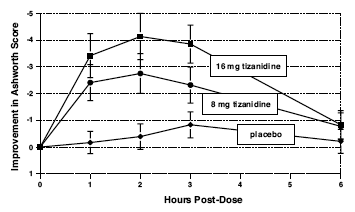
Siedmiotygodniowe badanie u pacjentów z urazem rdzenia kręgowego ze spastycznością
W 7-tygodniowym badaniu (Badanie 2) 118 pacjentów ze spastycznością wtórną do urazu rdzenia kręgowego zostało losowo przydzielonych do grupy placebo lub Zanaflex. Zastosowano kroki podobne do tych, które wykonano w pierwszym badaniu, aby zapewnić integralność zaślepienia.
Pacjenci byli miareczkowani przez 3 tygodnie do maksymalnej tolerowanej dawki lub 36 mg na dobę podawanej w trzech nierównych dawkach (np. 10 mg podawane rano i po południu oraz 16 mg podawane wieczorem). Pacjentom następnie utrzymywano maksymalną tolerowaną dawkę przez 4 dodatkowe tygodnie (tj. faza podtrzymywania). W fazie podtrzymywania napięcie mięśni oceniano w skali Ashwortha w okresie 2,5 godziny po dawce porannej lub popołudniowej. Liczba skurczów w ciągu dnia była codziennie rejestrowana przez pacjentów.
punkcie końcowym (określony w protokole czas oceny wyniku) wystąpiło statystycznie istotne zmniejszenie napięcia mięśniowego i częstotliwości skurczów w grupie leczonej preparatem Zanaflex w porównaniu z placebo. Zmniejszenie napięcia mięśniowego nie wiązało się ze zmniejszeniem siły mięśni (pożądany wynik), ale nie prowadziło również do żadnej stałej przewagi pacjentów leczonych Zanaflexem w zakresie czynności życia codziennego. Rycina 3 poniżej przedstawia porównanie średniej zmiany napięcia mięśniowego od wartości wyjściowej mierzonej skalą Ashwortha.
Rysunek 3: Badanie siedmiotygodniowe — średnia zmiana napięcia mięśniowego 0,5–2,5 godziny po podaniu, mierzona skalą Ashwortha ± 95% przedział ufności (ujemny wynik Ashwortha oznacza poprawę napięcia mięśniowego w stosunku do wartości początkowej)
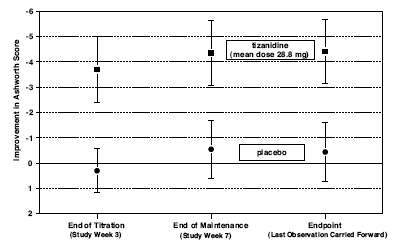
INFORMACJA O PACJENCIE
Poważne interakcje leków
Należy poinformować pacjentów, że nie powinni przyjmować leku Zanaflex, jeśli przyjmują fluwoksaminę lub cyprofloksacynę, ze względu na zwiększone ryzyko poważnych działań niepożądanych, w tym znacznego obniżenia ciśnienia krwi i sedacji. Należy poinstruować pacjentów, aby informowali swoich lekarzy lub farmaceutów o rozpoczęciu lub zaprzestaniu przyjmowania jakichkolwiek leków ze względu na ryzyko związane z interakcją między Zanaflex a innymi lekami.
Dozowanie Zanaflex
Należy poinformować pacjentów, aby przyjmowali Zanaflex 2 mg dokładnie zgodnie z zaleceniami (konsekwentnie z jedzeniem lub bez) i aby nie zmieniali tabletek na kapsułki. Należy poinformować pacjentów, że nie powinni przyjmować większej dawki leku Zanaflex 2 mg niż przepisana ze względu na ryzyko wystąpienia działań niepożądanych przy pojedynczych dawkach większych niż 8 mg lub całkowitych dawkach dobowych większych niż 36 mg. Należy poinformować pacjentów, że nie powinni nagle odstawiać leku Zanaflex 4 mg, ponieważ może wystąpić nadciśnienie z odbicia i tachykardia.
Efekty Zanaflex
Ostrzeż pacjentów, że mogą wystąpić niedociśnienie i zachowaj ostrożność przy zmianie z pozycji leżącej lub siedzącej na stojącą. Należy poinformować pacjentów, że Zanaflex może powodować ich uspokojenie lub senność i powinni zachować ostrożność podczas wykonywania czynności wymagających czujności, takich jak prowadzenie pojazdu lub obsługa maszyn. Należy poinformować pacjentów, że sedacja może być addytywna, gdy Zanaflex 4 mg jest przyjmowany w połączeniu z lekami (baklofen, benzodiazepiny) lub substancjami (np. alkohol), które działają depresyjnie na ośrodkowy układ nerwowy. Przypomnij pacjentom, że jeśli polegają na swojej spastyczności, aby utrzymać postawę i równowagę w poruszaniu się, lub gdy spastyczność jest wykorzystywana do poprawy funkcji, należy stosować Zanaflex, aby zmniejszyć spastyczność i zachować ostrożność.
