Brand Temovate 15g Clobetasol Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Temovate i jak jest używany?
Temovate to lek na receptę stosowany w leczeniu objawów łuszczycy plackowatej i skóry głowy oraz dermatoz reagujących na kortykosteroidy. Temovate można stosować samodzielnie lub z innymi lekami.
Temovate należy do klasy leków zwanych kortykosteroidami do stosowania miejscowego.
Nie wiadomo, czy Temovate jest bezpieczny i skuteczny u dzieci w wieku poniżej 12 lat.
Jakie są możliwe skutki uboczne Temovate?
Temovate może powodować poważne skutki uboczne, w tym:
- pogorszenie stanu Twojej skóry,
- zaczerwienienie, ciepło, obrzęk, sączenie lub silne podrażnienie leczonej skóry,
- rozmazany obraz,
- widzenie tunelowe,
- ból oka,
- widząc aureole wokół świateł,
- zwiększone pragnienie,
- suchość w ustach,
- owocowy zapach oddechu,
- przyrost masy twarzy i ramion,
- powolne gojenie się ran,
- przebarwienia skóry,
- ścieńczenie skóry,
- zwiększone owłosienie ciała,
- zmęczenie,
- zmiany nastroju,
- zmiany menstruacyjne i
- zmiany płciowe
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Temovate to:
- pieczenie, swędzenie, obrzęk lub podrażnienie leczonej skóry,
- sucha lub pękająca skóra,
- zaczerwienienie lub strupowanie wokół mieszków włosowych,
- pajączki,
- rozstępy,
- ścieńczenie skóry,
- wysypka lub pokrzywka,
- trądzik i
- tymczasowa utrata włosów
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Temovate. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
TEMOVATE® (krem i maść z propionianem klobetazolu) Krem i maść 0,05% zawiera substancję czynną propionian klobetazolu, syntetyczny kortykosteroid do miejscowego stosowania dermatologicznego. Clobetasol, analog prednizolonu, ma wysoki stopień aktywności glikokortykoidowej i niewielki stopień aktywności mineralokortykoidowej.
Chemicznie propionian klobetazolu to (11ß,16ß)-21-chloro-9-fluoro-11-hydroksy-16-metylo-17-(1-oksopropoksy)-pregna-1,4-dieno-3,20-dion i ma następujący wzór strukturalny:
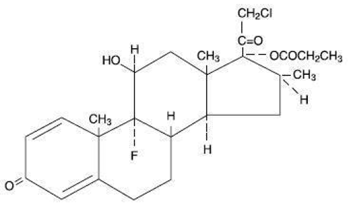
Propionian klobetazolu ma wzór cząsteczkowy C25H32CIFO5 i masę cząsteczkową 467. Jest to nierozpuszczalny w wodzie krystaliczny proszek o barwie białej do kremowej.
TEMOVATE® Krem zawiera propionian klobetazolu 0,5 mg/g w kremowej bazie glikolu propylenowego, monostearynianu gliceryny, alkoholu cetostearylowego, stearynianu gliceryny, stearynianu PEG 100, białego wosku, chlorokrezolu, cytrynianu sodu, monohydratu kwasu cytrynowego i wody oczyszczonej.
TEMOVATE® Maść zawiera 0,5 mg/g propionianu klobetazolu na bazie glikolu propylenowego, półtoraoleinianu sorbitanu i białej wazeliny.
WSKAZANIA
Krem i maść TEMOVATE® to preparaty kortykosteroidowe o bardzo wysokiej sile działania, wskazane do łagodzenia zapalnych i świądowych objawów dermatoz reagujących na kortykosteroidy. Nie zaleca się leczenia trwającego dłużej niż 2 kolejne tygodnie, a całkowita dawka nie powinna przekraczać 50 g/tydzień ze względu na możliwość hamowania osi podwzgórze-przysadka-nadnercza (HPA). Nie zaleca się stosowania u dzieci w wieku poniżej 12 lat.
Podobnie jak w przypadku innych wysoce aktywnych kortykosteroidów, leczenie należy przerwać po osiągnięciu kontroli. Jeśli w ciągu 2 tygodni nie nastąpi poprawa, może być konieczna ponowna ocena diagnozy.
DAWKOWANIE I SPOSÓB PODAWANIA
Nałożyć cienką warstwę kremu lub maści TEMOVATE® na dotknięte obszary skóry dwa razy dziennie i delikatnie i całkowicie wmasować (patrz WSKAZANIA I ZASTOSOWANIE ).
Krem i maść TEMOVATE® to kortykosteroidy o bardzo dużej sile działania; dlatego, leczenie należy ograniczyć do 2 kolejnych tygodni i nie należy stosować ilości większych niż 50 g/tydzień.
Podobnie jak w przypadku innych wysoce aktywnych kortykosteroidów, leczenie należy przerwać po osiągnięciu kontroli. Jeśli w ciągu 2 tygodni nie nastąpi poprawa, może być konieczna ponowna ocena diagnozy.
Kremu i maści TEMOVATE® nie należy stosować z opatrunkami okluzyjnymi.
Zastosowanie geriatryczne
W badaniach, w których pacjenci geriatryczni (65 lat lub starsi, patrz ŚRODKI OSTROŻNOŚCI byli leczeni kremem lub maścią TEMOVATE®, bezpieczeństwo nie różniło się od bezpieczeństwa u młodszych pacjentów; dlatego nie zaleca się dostosowywania dawki.
JAK DOSTARCZONE
TEMOVATE® (krem z propionianem klobetazolu) 0,05% dostarczany jest w:
tuby 30g ( NDC 10337-163-30) oraz probówki 60 g ( NDC 10337-163-60).
TEMOVATE® (maść propionian klobetazolu) 0,05% maść dostarczana jest w:
15-g tuby ( NDC 10337-162-15) i tuby 30 g ( NDC 10337-162-30).
Przechowywać w temperaturze od 15° do 30°C (59° do 86°F). Kremu TEMOVATE® nie należy przechowywać w lodówce. PharmaDerm
Oddział Fougera Pharmaceuticals Inc., Melville, NY 11747 USA. Aktualizacja: styczeń 2012
SKUTKI UBOCZNE
W kontrolowanych badaniach klinicznych najczęstszymi działaniami niepożądanymi zgłaszanymi dla kremu TEMOVATE® były uczucie pieczenia i kłucia u 1% leczonych pacjentów. Rzadziej występującymi działaniami niepożądanymi były świąd, zanik skóry oraz pękanie i szczelinowanie skóry.
kontrolowanych badaniach klinicznych najczęstszymi zdarzeniami niepożądanymi zgłaszanymi dla maści TEMOVATE® były pieczenie, podrażnienie i swędzenie u 0,5% leczonych pacjentów. Rzadziej występującymi działaniami niepożądanymi były kłucie, pękanie, rumień, zapalenie mieszków włosowych, drętwienie palców, zanik skóry i teleangiektazje.
Zespół Cushinga zgłaszano u niemowląt i dorosłych w wyniku przedłużonego stosowania miejscowych preparatów propionianu klobetazolu.
Następujące dodatkowe miejscowe działania niepożądane zgłaszano po miejscowym stosowaniu kortykosteroidów, które mogą występować częściej podczas stosowania opatrunków okluzyjnych i kortykosteroidów o większej sile działania. Reakcje te wymieniono w kolejności występowania w przybliżeniu malejącej: suchość, wykwity trądzikopodobne, hipopigmentacja, okołoustne zapalenie skóry, alergiczne kontaktowe zapalenie skóry, wtórne zakażenie, podrażnienie, rozstępy i prosówki.

INTERAKCJE Z LEKAMI
Brak informacji.
OSTRZEŻENIA
Brak informacji. Proszę zobaczyć PREKACJE poniżej.
ŚRODKI OSTROŻNOŚCI
Ogólny
Kremu i maści TEMOVATE® nie należy stosować w leczeniu trądziku różowatego lub okołoustnego zapalenia skóry, nie należy go również stosować na twarz, pachwiny ani pod pachami.
Wchłanianie ogólnoustrojowe kortykosteroidów do stosowania miejscowego może powodować odwracalną supresję osi HPA z możliwością niedoboru glikokortykosteroidów po odstawieniu leczenia. Objawy zespołu Cushinga, hiperglikemii i cukromoczu mogą również wystąpić u niektórych pacjentów w wyniku ogólnoustrojowego wchłaniania miejscowych kortykosteroidów podczas leczenia.
Pacjenci stosujący miejscowo steryd na dużą powierzchnię lub obszary pod okluzją powinni być okresowo oceniani pod kątem supresji osi HPA. Można to zrobić za pomocą stymulacji ACTH, kortyzolu w osoczu AM i testów wolnego kortyzolu w moczu. Pacjenci otrzymujący kortykosteroidy o bardzo silnym działaniu nie powinni być leczeni jednorazowo dłużej niż przez 2 tygodnie, a ze względu na zwiększone ryzyko supresji HPA należy jednorazowo leczyć tylko niewielkie obszary.
Krem i maść TEMOVATE® powodowały zahamowanie osi HPA, gdy były stosowane w dawkach tak niskich jak 2 g/dobę przez 1 tydzień u pacjentów z egzemą.
W przypadku stwierdzenia zahamowania osi HPA należy podjąć próbę odstawienia leku, zmniejszenia częstości stosowania lub zastąpienia kortykosteroidem o słabszym działaniu. Powrót funkcji osi HPA jest na ogół natychmiastowy po odstawieniu miejscowych kortykosteroidów. Rzadko mogą wystąpić oznaki i objawy niedoboru glikokortykosteroidów, które wymagają uzupełniających ogólnoustrojowych kortykosteroidów. Informacje na temat suplementacji ogólnoustrojowej można znaleźć w informacjach dotyczących przepisywania tych produktów.
Pacjenci pediatryczni mogą być bardziej podatni na toksyczność ogólnoustrojową po podaniu równoważnych dawek ze względu na większy stosunek powierzchni skóry do masy ciała (patrz ŚRODKI OSTROŻNOŚCI : Zastosowanie pediatryczne ).
przypadku wystąpienia podrażnienia należy przerwać stosowanie kremu i maści TEMOVATE® i wdrożyć odpowiednie leczenie. Alergiczne kontaktowe zapalenie skóry wywołane kortykosteroidami jest zwykle diagnozowane na podstawie obserwacji braku gojenia, a nie zaostrzenia klinicznego, jak w przypadku większości produktów do stosowania miejscowego niezawierających kortykosteroidów. Taka obserwacja powinna być potwierdzona odpowiednimi diagnostycznymi testami płatkowymi.
Jeśli występują lub rozwijają się współistniejące zakażenia skóry, należy zastosować odpowiedni lek przeciwgrzybiczy lub przeciwbakteryjny. Jeśli korzystna odpowiedź nie nastąpi szybko, stosowanie kremu i maści TEMOVATE® należy przerwać do czasu odpowiedniego opanowania zakażenia.
Testy laboratoryjne
W ocenie pacjentów pod kątem supresji osi HPA pomocne mogą być następujące testy:
Test stymulacji ACTH Test kortyzolu w osoczu AM Test wolnego kortyzolu w moczu
rakotwórczość, mutageneza, upośledzenie płodności
Nie przeprowadzono długoterminowych badań na zwierzętach w celu oceny potencjalnego działania rakotwórczego propionianu klobetazolu.
Badania na szczurach po podaniu podskórnym w dawkach do 50 mcg/kg/dobę wykazały, że samice wykazywały wzrost liczby wchłoniętych zarodków i spadek liczby żywych płodów przy najwyższej dawce.
Propionian klobetazolu nie był mutagenny w 3 różnych systemach testowych: teście Amesa, teście konwersji genu Saccharomyces cerevisiae i teście fluktuacji E. coli B WP2.
Ciąża
Efekty teratogenne
Ciąża Kategoria C. Wykazano, że kortykosteroidy są teratogenne u zwierząt laboratoryjnych, gdy są podawane ogólnoustrojowo w stosunkowo niskich dawkach. Wykazano, że niektóre kortykosteroidy mają działanie teratogenne po podaniu na skórę zwierzętom laboratoryjnym.
Propionian klobetazolu nie był badany pod kątem teratogenności podczas stosowania miejscowego; jednakże jest wchłaniany przezskórnie, a po podaniu podskórnym był znaczącym działaniem teratogennym zarówno u królików, jak i myszy. Propionian klobetazolu ma większy potencjał teratogenny niż sterydy, które są słabsze.
Badania teratogenności na myszach po podaniu podskórnym wykazały fetotoksyczność przy najwyższej badanej dawce (1 mg/kg) i teratogenność przy wszystkich badanych poziomach dawek, aż do 0,03 mg/kg. Dawki te są odpowiednio około 1,4 i 0,04 razy większe od miejscowej dawki kremu i maści TEMOVATE® stosowanej u ludzi. Obserwowane nieprawidłowości obejmowały rozszczep podniebienia i nieprawidłowości szkieletu.
U królików propionian klobetazolu wykazywał działanie teratogenne w dawkach 3 i 10 mcg/kg. Dawki te są odpowiednio około 0,02 i 0,05 razy większe od miejscowej dawki kremu i maści TEMOVATE® stosowanej u ludzi. Obserwowane nieprawidłowości obejmowały rozszczep podniebienia, kranioschizę i inne nieprawidłowości szkieletowe.
Nie ma odpowiednich i dobrze kontrolowanych badań potencjału teratogennego propionianu klobetazolu u kobiet w ciąży. Krem i maść TEMOVATE® należy stosować w okresie ciąży tylko wtedy, gdy potencjalna korzyść przewyższa potencjalne ryzyko dla płodu.
Matki karmiące
Kortykosteroidy podawane ogólnoustrojowo pojawiają się w mleku ludzkim i mogą hamować wzrost, zakłócać endogenną produkcję kortykosteroidów lub powodować inne niepożądane skutki. Nie wiadomo, czy miejscowe podawanie kortykosteroidów może spowodować wchłanianie ogólnoustrojowe wystarczające do wytworzenia wykrywalnych ilości w mleku ludzkim. Ponieważ wiele leków przenika do mleka ludzkiego, należy zachować ostrożność podając krem lub maść TEMOVATE kobiecie karmiącej piersią.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność kremu i maści TEMOVATE® u dzieci nie zostały ustalone. Nie zaleca się stosowania u dzieci w wieku poniżej 12 lat. Ze względu na wyższy stosunek powierzchni skóry do masy ciała, pacjenci pediatryczni są bardziej narażeni niż dorośli na zahamowanie osi HPA i zespół Cushinga, gdy są leczeni miejscowymi kortykosteroidami. W związku z tym są również bardziej narażeni na wystąpienie niewydolności nadnerczy w trakcie lub po zakończeniu leczenia. Zgłaszano działania niepożądane, w tym rozstępy, w przypadku niewłaściwego stosowania miejscowych kortykosteroidów u niemowląt i dzieci.
dzieci otrzymujących miejscowo kortykosteroidy zgłaszano zahamowanie osi HPA, zespół Cushinga, liniowe opóźnienie wzrostu, opóźniony przyrost masy ciała i nadciśnienie śródczaszkowe. Objawy supresji nadnerczy u dzieci obejmują niski poziom kortyzolu w osoczu i brak odpowiedzi na stymulację ACTH. Manifestacje nadciśnienia śródczaszkowego obejmują wybrzuszenia ciemiączek, bóle głowy i obustronny obrzęk tarczy nerwu wzrokowego.
Zastosowanie geriatryczne
Ograniczona liczba pacjentów w wieku 65 lat lub starszych była leczona kremem TEMOVATE® (n = 231) oraz maścią TEMOVATE® (n = 101) w badaniach klinicznych w USA i poza USA. Chociaż liczba pacjentów jest zbyt mała, aby umożliwić oddzielną analizę skuteczności i bezpieczeństwa, działania niepożądane zgłaszane w tej populacji były podobne do zgłaszanych przez młodszych pacjentów. Na podstawie dostępnych danych nie jest uzasadnione dostosowanie dawkowania kremu i maści TEMOVATE® u pacjentów geriatrycznych.
PRZEDAWKOWAĆ
Miejscowo stosowany krem i maść TEMOVATE® może być wchłonięty w ilości wystarczającej do wywołania efektów ogólnoustrojowych (patrz ŚRODKI OSTROŻNOŚCI ).
PRZECIWWSKAZANIA
TEMOVATE® (krem i maść propionian klobetazolu) Krem i maść 0,05% są przeciwwskazane u pacjentów z nadwrażliwością na którykolwiek ze składników preparatu.
FARMAKOLOGIA KLINICZNA
Podobnie jak inne kortykosteroidy do stosowania miejscowego, propionian klobetazolu ma właściwości przeciwzapalne, przeciwświądowe i zwężające naczynia. Mechanizm działania przeciwzapalnego steroidów do stosowania miejscowego jest ogólnie niejasny. Uważa się jednak, że kortykosteroidy działają poprzez indukcję białek hamujących fosfolipazę A2, zwanych łącznie lipokortynami. Postuluje się, że białka te kontrolują biosyntezę silnych mediatorów zapalenia, takich jak prostaglandyny i leukotrieny, poprzez hamowanie uwalniania ich wspólnego prekursora, kwasu arachidonowego. Kwas arachidonowy jest uwalniany z fosfolipidów błonowych przez fosfolipazę A2.
Farmakokinetyka
Stopień wchłaniania przezskórnego kortykosteroidów do stosowania miejscowego zależy od wielu czynników, w tym nośnika i integralności bariery naskórkowej. Nie wykazano, aby opatrunek okluzyjny z hydrokortyzonem do 24 godzin zwiększał penetrację; jednak okluzja hydrokortyzonu przez 96 godzin znacznie zwiększa penetrację. Miejscowe kortykosteroidy mogą być wchłaniane z normalnej, nienaruszonej skóry. Stan zapalny i/lub inne procesy chorobowe w skórze mogą zwiększać wchłanianie przezskórne.
Badania przeprowadzone z kremem i maścią TEMOVATE® wskazują, że są one w bardzo wysokim zakresie działania w porównaniu z innymi kortykosteroidami do stosowania miejscowego.
INFORMACJA O PACJENCIE
Pacjenci stosujący miejscowo kortykosteroidy powinni otrzymać następujące informacje i instrukcje:
