Crestor 10mg, 20mg, 5mg Rosuvastatin Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Crestor i jak jest używany?
Crestor to lek na receptę stosowany w celu obniżenia poziomu cholesterolu LDL (lipoprotein o niskiej gęstości) i trójglicerydów we krwi, spowolnienia postępu blaszek miażdżycowych w naczyniach krwionośnych, zmniejszenia ryzyka udaru i zawału serca. Crestor 20mg może być stosowany samodzielnie lub z innymi lekami.
Crestor to środki obniżające poziom lipidów, statyny, inhibitory reduktazy HMG-CoA.
Nie wiadomo, czy Crestor jest bezpieczny i skuteczny u dzieci w wieku poniżej 8 lat.
Jakie są możliwe skutki uboczne Crestor?
Crestor może powodować poważne działania niepożądane, w tym:
- niewyjaśniony ból mięśni
- tkliwość mięśni
- słabe mięśnie
- dezorientacja
- problemy z pamięcią
- ból w górnej części brzucha
- zmęczenie
- utrata apetytu
- ciemny mocz
- zażółcenie skóry lub oczu (żółtaczka)
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze działania niepożądane Crestor to:
- ból głowy
- słabość
- bóle mięśni
- mdłości
- ból brzucha
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Crestora. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
CRESTOR (rozuwastatyna wapniowa) to syntetyczny środek obniżający stężenie lipidów do podawania doustnego.
Nazwa chemiczna dla rozuwastatyny wapniowej to bis[(E)-7-[4-(4-fluorofenylo)-6-izopropylo-2-[metylo(metylosulfonylo)amino]pirymidyn-5-ylo](3R,5S)-3 sól wapniowa kwasu 1,5-dihydroksyhept-6-enowego o następującym wzorze strukturalnym:
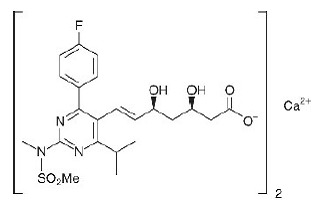
Wzór empiryczny dla rozuwastatyny wapniowej to (C22H27FN3O6S)2Ca, a masa cząsteczkowa wynosi 1001,14. Rozuwastatyna wapniowa jest białym bezpostaciowym proszkiem, który jest słabo rozpuszczalny w wodzie i metanolu oraz słabo rozpuszczalny w etanolu. Rozuwastatyna wapniowa jest związkiem hydrofilowym o współczynniku podziału (oktanol/woda) 0,13 przy pH 7,0.
Tabletki CRESTOR do podawania doustnego zawierają 5, 10, 20 lub 40 mg rozuwastatyny i następujące składniki nieaktywne: Każda tabletka zawiera: celulozę mikrokrystaliczną NF, laktozę jednowodną NF, trójzasadowy fosforan wapnia NF, krospowidon NF, stearynian magnezu NF, hypromelozę NF, triacetyna NF, dwutlenek tytanu USP, żółty tlenek żelazowy i czerwony tlenek żelazowy NF.
WSKAZANIA
Hiperlipidemia i mieszana dyslipidemia
CRESTOR jest wskazany jako terapia wspomagająca dietę w celu zmniejszenia podwyższonego stężenia całkowitego C, LDL-C, ApoB, nonHDL-C i triglicerydów oraz zwiększenia HDL-C u dorosłych pacjentów z pierwotną hiperlipidemią lub mieszaną dyslipidemią. Leki zmieniające lipidy powinny być stosowane jako dodatek do diety o ograniczonej zawartości tłuszczów nasyconych i cholesterolu, gdy sama reakcja na dietę i interwencje niefarmakologiczne jest niewystarczająca.
Pacjenci pediatryczni z rodzinną hipercholesterolemią
CRESTOR 10mg jest wskazany jako dodatek do diety:
- obniżenie stężenia całkowitego C, LDL-C i ApoB u dzieci i młodzieży w wieku od 8 do 17 lat z heterozygotyczną hipercholesterolemią rodzinną, jeśli po odpowiedniej próbie leczenia dietą stwierdza się: LDL-C >190 mg/dl lub >160 mg/dl wraz z dodatnim wywiadem rodzinnym w zakresie przedwczesnej choroby sercowo-naczyniowej (CVD) lub dwoma lub więcej innymi czynnikami ryzyka CVD.
- zmniejszenie stężenia LDL-C, całkowitego-C, nieHDL-C i ApoB u dzieci i młodzieży w wieku od 7 do 17 lat z homozygotyczną hipercholesterolemią rodzinną, samodzielnie lub z innymi lekami obniżającymi stężenie lipidów (np. afereza LDL).
Hipertriglicerydemia
CRESTOR jest wskazany jako terapia wspomagająca dietę w leczeniu dorosłych pacjentów z hipertriglicerydemią.
Pierwotna dysbetalipoproteinemia (hiperlipoproteinemia typu III)
CRESTOR jest wskazany jako uzupełnienie diety w leczeniu dorosłych pacjentów z pierwotną dysbetalipoproteinemią (hiperlipoproteinemią typu III).
Dorośli pacjenci z homozygotyczną hipercholesterolemią rodzinną
CRESTOR jest wskazany jako terapia wspomagająca z innymi terapiami obniżającymi poziom lipidów (np. afereza LDL) lub samodzielnie, jeśli takie terapie są niedostępne w celu zmniejszenia LDL-C, Całkowitego C i ApoB u dorosłych pacjentów z homozygotyczną hipercholesterolemią rodzinną.
Spowolnienie progresji miażdżycy
CRESTOR 5 mg jest wskazany jako terapia wspomagająca dietę w celu spowolnienia progresji miażdżycy u dorosłych pacjentów jako część strategii leczenia mającej na celu obniżenie całkowitego C i LDL-C do poziomów docelowych.
Pierwotna profilaktyka chorób układu krążenia
osób bez klinicznie ewidentnej choroby wieńcowej, ale ze zwiększonym ryzykiem choroby sercowo-naczyniowej w oparciu o wiek ≥50 lat u mężczyzn i ≥60 lat u kobiet, hsCRP ≥2 mg/l i obecność co najmniej jednej dodatkowej choroby układu krążenia czynnik ryzyka, taki jak nadciśnienie, niski poziom HDL-C, palenie tytoniu lub przedwczesna choroba wieńcowa w wywiadzie rodzinnym, CRESTOR jest wskazany do:
- zmniejszyć ryzyko udaru mózgu
- zmniejszyć ryzyko zawału mięśnia sercowego
- zmniejszyć ryzyko zabiegów rewaskularyzacji tętniczej
Ograniczenia użytkowania
Preparatu CRESTOR nie badano w dyslipidemii typu I i V Fredricksona.
DAWKOWANIE I SPOSÓB PODAWANIA
Ogólne informacje o dawkowaniu
Zakres dawek preparatu CRESTOR 5 mg u dorosłych wynosi od 5 do 40 mg doustnie raz na dobę. Zwykle dawka początkowa to 10 do 20 mg raz na dobę. Zazwyczaj stosowana dawka początkowa u dorosłych pacjentów z homozygotyczną hipercholesterolemią rodzinną wynosi 20 mg raz na dobę.
Maksymalną dawkę preparatu CRESTOR 20 mg wynoszącą 40 mg należy stosować wyłącznie u tych pacjentów, którzy nie osiągnęli docelowego stężenia cholesterolu LDL przy użyciu dawki 20 mg [patrz OSTRZEŻENIA I ŚRODKI ].
CRESTOR 5 mg można podawać w pojedynczej dawce o dowolnej porze dnia, z posiłkiem lub bez posiłku. Tabletkę należy połykać w całości.
Rozpoczynając terapię preparatem CRESTOR lub przechodząc z innego leczenia inhibitorem reduktazy HMG-CoA, należy najpierw zastosować odpowiednią dawkę początkową preparatu CRESTOR 10 mg, a dopiero potem dostosowywać dawkę w zależności od odpowiedzi pacjenta i indywidualnego celu leczenia.
Po rozpoczęciu lub po dostosowaniu dawki preparatu CRESTOR, w ciągu 2 do 4 tygodni należy zanalizować stężenie lipidów i odpowiednio dostosować dawkowanie.
Dawkowanie pediatryczne
W heterozygotycznej hipercholesterolemii rodzinnej zalecany zakres dawek wynosi od 5 do 10 mg doustnie raz na dobę u pacjentów w wieku od 8 do poniżej 10 lat oraz od 5 do 20 mg doustnie raz na dobę u pacjentów w wieku od 10 do 17 lat.
homozygotycznej hipercholesterolemii rodzinnej zalecana dawka wynosi 20 mg doustnie raz na dobę u pacjentów w wieku od 7 do 17 lat.
Dawkowanie u pacjentów azjatyckich
U pacjentów pochodzenia azjatyckiego należy rozważyć rozpoczęcie leczenia preparatem CRESTOR 20 mg dawką 5 mg raz na dobę ze względu na zwiększone stężenie rozuwastatyny w osoczu. Należy wziąć pod uwagę zwiększoną ekspozycję ogólnoustrojową podczas leczenia pacjentów pochodzenia azjatyckiego, którym nie udało się uzyskać odpowiedniej kontroli, w dawkach do 20 mg/dobę [patrz Używaj w określonych populacjach oraz FARMAKOLOGIA KLINICZNA ].
Używaj z równoczesną terapią
Pacjenci przyjmujący cyklosporynę
Dawka preparatu CRESTOR 20 mg nie powinna przekraczać 5 mg raz na dobę [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI oraz FARMAKOLOGIA KLINICZNA ].
Pacjenci przyjmujący Gemfibrozyl
Należy unikać jednoczesnego stosowania preparatu CRESTOR z gemfibrozylem. Jeśli nie można uniknąć jednoczesnego stosowania, należy rozpocząć podawanie leku CRESTOR w dawce 5 mg raz na dobę. Dawka preparatu CRESTOR nie powinna przekraczać 10 mg raz na dobę [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI oraz FARMAKOLOGIA KLINICZNA ].
Pacjenci przyjmujący atazanawir i rytonawir, lopinawir i rytonawir lub symeprewir
Rozpocznij terapię CRESTOR 10 mg dawką 5 mg raz na dobę. Dawka preparatu CRESTOR nie powinna przekraczać 10 mg raz na dobę [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI oraz FARMAKOLOGIA KLINICZNA ].
Dawkowanie u pacjentów z ciężką niewydolnością nerek
U pacjentów z ciężkimi zaburzeniami czynności nerek (CLcr Używaj w określonych populacjach oraz FARMAKOLOGIA KLINICZNA ].
JAK DOSTARCZONE
Formy dawkowania i mocne strony
5 mg: żółte, okrągłe, obustronnie wypukłe tabletki powlekane. Wytłoczone „CRESTOR” i „5” po jednej stronie tabletu.
10 mg: różowe, okrągłe, obustronnie wypukłe tabletki powlekane. Wytłoczone „CRESTOR” i „10” po jednej stronie tabletu.
20 mg: różowe, okrągłe, obustronnie wypukłe tabletki powlekane. Wytłoczone „CRESTOR” i „20” po jednej stronie tabletu.
40 mg: różowe, owalne, dwuwypukłe tabletki powlekane. Wytłoczony napis „CRESTOR” po jednej stronie i „40” po drugiej stronie tabletu.
Składowania i stosowania
CRESTOR® (rozuwastatyna wapnia) Tabletki są dostarczane jako:
NDC 0310-0755-90: 5 mg. Żółte, okrągłe, dwuwypukłe tabletki powlekane. Wytłoczone „CRESTOR” i „5” po jednej stronie; butelka 90 tabletek
NDC 0310-0751-90: 10 mg. Różowe, okrągłe, obustronnie wypukłe tabletki powlekane. Wytłoczone „CRESTOR” i „10” po jednej stronie; butelka 90 tabletek
NDC 0310-0751-39: 10 mg. Różowe, okrągłe, obustronnie wypukłe tabletki powlekane. Wytłoczone „CRESTOR” i „10” po jednej stronie; opakowania jednostkowe po 100
NDC 0310-0752-90: 20 mg. Różowe, okrągłe, obustronnie wypukłe tabletki powlekane. Wytłoczone „CRESTOR” i „20” po jednej stronie; butelki 90
NDC 0310-0752-39: 20 mg. Różowe, okrągłe, obustronnie wypukłe tabletki powlekane. Wytłoczone „CRESTOR” i „20” po jednej stronie; opakowania jednostkowe po 100
NDC 0310-0754-30: 40 mg. Różowe, owalne, dwuwypukłe tabletki powlekane. Wytłoczony napis „CRESTOR” po jednej stronie i „40” po drugiej; butelki 30
Magazynowanie
Przechowywać w kontrolowanej temperaturze pokojowej, 20-25°C (68-77°F) [patrz Temperatura pokojowa kontrolowana przez USP ]. Chronić przed wilgocią.
Dystrybutor: AstraZeneca Pharmaceuticals LP Wilmington, DE 19850. Aktualizacja: wrzesień 2018
SKUTKI UBOCZNE
Następujące poważne działania niepożądane omówiono bardziej szczegółowo w innych sekcjach etykiety:
- Rabdomioliza z mioglobinurią i ostrą niewydolnością nerek i miopatią (w tym zapalenie mięśni) [patrz OSTRZEŻENIA I ŚRODKI ]
- Nieprawidłowości enzymów wątrobowych [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce klinicznej.
W bazie danych kontrolowanych badań klinicznych CRESTOR (kontrolowanych placebo lub aktywnie) obejmującej 5394 pacjentów ze średnim czasem trwania leczenia wynoszącym 15 tygodni, 1,4% pacjentów przerwało leczenie z powodu działań niepożądanych. Najczęstszymi działaniami niepożądanymi, które doprowadziły do przerwania leczenia były:
- bóle mięśniowe
- ból brzucha
- mdłości
Najczęściej zgłaszanymi działaniami niepożądanymi (częstość ≥2%) w bazie danych kontrolowanych badań klinicznych CRESTOR 5 mg z udziałem 5394 pacjentów były:
- ból głowy
- bóle mięśniowe
- ból brzucha
- astenia
- mdłości
Działania niepożądane zgłaszane u ≥2% pacjentów w badaniach klinicznych kontrolowanych placebo i częściej niż placebo przedstawiono w Tabeli 1. W badaniach tych leczenie trwało do 12 tygodni.
Inne działania niepożądane zgłaszane w badaniach klinicznych to ból brzucha, zawroty głowy, nadwrażliwość (w tym wysypka, świąd, pokrzywka i obrzęk naczynioruchowy) oraz zapalenie trzustki. Zgłaszano również następujące nieprawidłowości laboratoryjne: białkomocz z dodatnim wynikiem testu paskowego i mikroskopijny krwiomocz [patrz OSTRZEŻENIA I ŚRODKI ]; podwyższona fosfokinaza kreatynowa, transaminazy, glukoza, transpeptydaza glutamylowa, fosfataza alkaliczna i bilirubina; i zaburzenia czynności tarczycy.
badaniu METEOR z udziałem 981 uczestników leczonych rozuwastatyną w dawce 40 mg (n=700) lub placebo (n=281) ze średnim czasem trwania leczenia 1,7 roku, 5,6% pacjentów leczonych preparatem CRESTOR 5 mg w porównaniu z 2,8% pacjentów otrzymujących placebo przerwane z powodu działań niepożądanych. Najczęstszymi działaniami niepożądanymi, które doprowadziły do przerwania leczenia były: ból mięśni, zwiększona aktywność enzymów wątrobowych, ból głowy i nudności [patrz Studia kliniczne ].
Działania niepożądane zgłaszane u ≥2% pacjentów i częściej niż placebo przedstawiono w Tabeli 2.
W badaniu JUPITER 17 802 uczestników otrzymywało rozuwastatynę w dawce 20 mg (n=8901) lub placebo (n=8901) przez średni okres 2 lat. Większy odsetek pacjentów leczonych rozuwastatyną w porównaniu z pacjentami otrzymującymi placebo, odpowiednio 6,6% i 6,2%, przerwał leczenie badanym lekiem z powodu zdarzenia niepożądanego, niezależnie od przyczynowości leczenia. Ból mięśni był najczęstszym działaniem niepożądanym, które doprowadziło do przerwania leczenia.
badaniu JUPITER zaobserwowano istotnie większą częstość występowania cukrzycy u pacjentów przyjmujących rozuwastatynę (2,8%) w porównaniu z pacjentami przyjmującymi placebo (2,3%). Średnia wartość HbA1c była istotnie zwiększona o 0,1% u pacjentów leczonych rosuwastatyną w porównaniu z pacjentami otrzymującymi placebo. Liczba pacjentów z HbA1c >6,5% pod koniec badania była znacząco wyższa u pacjentów leczonych rozuwastatyną w porównaniu z pacjentami otrzymującymi placebo [patrz OSTRZEŻENIA I ŚRODKI oraz Studia kliniczne ].
Działania niepożądane zgłaszane u ≥2% pacjentów i częściej niż placebo przedstawiono w Tabeli 3.
Pacjenci pediatryczni z heterozygotyczną hipercholesterolemią rodzinną
W 12-tygodniowym kontrolowanym badaniu z udziałem chłopców i dziewcząt po menarchezie w wieku od 10 do 17 lat z heterozygotyczną hipercholesterolemią rodzinną z CRESTOR 5 do 20 mg na dobę [patrz Używaj w określonych populacjach oraz Studia kliniczne ], zwiększenie aktywności fosfokinazy kreatynowej w surowicy (CK) >10 x GGN obserwowano częściej u dzieci leczonych rozuwastatyną niż u dzieci otrzymujących placebo. Czworo ze 130 (3%) dzieci leczonych rosuwastatyną (2 leczone 10 mg i 2 leczone 20 mg) miało podwyższoną CK >10 x GGN, w porównaniu do 0 z 46 dzieci otrzymujących placebo.
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania produktu CRESTOR po zatwierdzeniu produktu: bóle stawów, niewydolność wątroby prowadząca do zgonu lub nieprowadząca do zgonu, zapalenie wątroby, żółtaczka, trombocytopenia, depresja, zaburzenia snu (w tym bezsenność i koszmary senne), neuropatia obwodowa, śródmiąższowa choroba płuc i ginekomastia. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Istnieją rzadkie doniesienia o martwiczej miopatii o podłożu immunologicznym, związanej ze stosowaniem statyn [patrz OSTRZEŻENIA I ŚRODKI ].
Istnieją rzadkie doniesienia po wprowadzeniu do obrotu o zaburzeniach funkcji poznawczych (np. utrata pamięci, zapominanie, amnezja, zaburzenia pamięci i splątanie) związanych ze stosowaniem statyn. Te problemy poznawcze zostały zgłoszone dla wszystkich statyn. Zgłoszenia na ogół nie są poważne i ustępują po odstawieniu statyn, ze zmiennym czasem do wystąpienia objawów (1 dzień do lat) i ustąpienia objawów (mediana 3 tygodnie).
INTERAKCJE Z LEKAMI
Cyklosporyna
Cyklosporyna zwiększała ekspozycję na rozuwastatynę i może powodować zwiększone ryzyko miopatii. Dlatego u pacjentów przyjmujących cyklosporynę dawka preparatu CRESTOR 10 mg nie powinna przekraczać 5 mg raz na dobę [patrz DAWKOWANIE I SPOSÓB PODAWANIA , OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
Gemfibrozyl
Gemfibrozyl znacząco zwiększał ekspozycję na rozuwastatynę. Ze względu na obserwowane zwiększone ryzyko miopatii/rabdomiolizy należy unikać leczenia skojarzonego preparatem CRESTOR i gemfibrozylem. W przypadku jednoczesnego stosowania dawka leku CRESTOR 10 mg nie powinna przekraczać 10 mg raz na dobę [patrz FARMAKOLOGIA KLINICZNA ].
Inhibitory proteazy
Jednoczesne podawanie rozuwastatyny z niektórymi inhibitorami proteazy ma różny wpływ na ekspozycję na rozuwastatynę i może zwiększać ryzyko miopatii. Symeprewir, który jest inhibitorem proteazy wirusa zapalenia wątroby typu C (HCV), lub połączenia atazanawiru/rytonawiru lub lopinawiru/rytonawiru, które są inhibitorami proteazy HIV-1, zwiększają ekspozycję na rozuwastatynę [patrz Tabela 4 - FARMAKOLOGIA KLINICZNA ]. W przypadku tych inhibitorów proteazy dawka preparatu CRESTOR 5 mg nie powinna przekraczać 10 mg raz na dobę. Kombinacje fosamprenawiru/rytonawiru lub typranawiru/rytonawiru, które są inhibitorami proteazy HIV-1, powodują niewielkie lub żadne zmiany w ekspozycji na rozuwastatynę. Należy zachować ostrożność podczas jednoczesnego stosowania rozuwastatyny z inhibitorami proteazy [patrz DAWKOWANIE I SPOSÓB PODAWANIA , OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
Antykoagulanty kumaryny
CRESTOR 20mg znacząco zwiększał INR u pacjentów otrzymujących antykoagulanty kumaryny. Dlatego należy zachować ostrożność, gdy leki przeciwzakrzepowe z grupy kumaryny są podawane w połączeniu z preparatem CRESTOR. U pacjentów przyjmujących jednocześnie leki przeciwzakrzepowe z grupy kumaryny i preparat CRESTOR, wartość INR należy określić przed rozpoczęciem leczenia preparatem CRESTOR i wystarczająco często podczas wczesnego leczenia, aby upewnić się, że nie wystąpią żadne istotne zmiany wartości INR [patrz OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
Niacyna
Ryzyko wpływu na mięśnie szkieletowe może być zwiększone, gdy CRESTOR 5 mg jest stosowany w połączeniu z modyfikującymi lipidy dawkami (≥1 g/dobę) niacyny; należy zachować ostrożność przepisując preparat CRESTOR [patrz OSTRZEŻENIA I ŚRODKI ].
Fenofibrat
Gdy CRESTOR 20 mg podawano jednocześnie z fenofibratem, nie zaobserwowano klinicznie istotnego wzrostu AUC rozuwastatyny lub fenofibratu. Ponieważ wiadomo, że ryzyko miopatii podczas leczenia inhibitorami reduktazy HMG-CoA wzrasta podczas jednoczesnego stosowania fenofibratów, należy zachować ostrożność przepisując fenofibraty razem z preparatem CRESTOR [patrz OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
Kolchicyna
Przypadki miopatii, w tym rabdomiolizy, zgłaszano podczas stosowania inhibitorów reduktazy HMG-CoA, w tym rozuwastatyny, podawanych jednocześnie z kolchicyną, dlatego należy zachować ostrożność przepisując preparat CRESTOR z kolchicyną [patrz OSTRZEŻENIA I ŚRODKI ].
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Efekty mięśni szkieletowych
Podczas stosowania inhibitorów reduktazy HMG-CoA, w tym preparatu CRESTOR, zgłaszano przypadki miopatii i rabdomiolizy z ostrą niewydolnością nerek wtórną do mioglobinurii. Ryzyko to może wystąpić przy dowolnym poziomie dawki, ale zwiększa się przy najwyższej dawce (40 mg).
CRESTOR 5 mg należy przepisywać ostrożnie u pacjentów z czynnikami predysponującymi do miopatii (np. wiek ≥65 lat, niewłaściwie leczona niedoczynność tarczycy, zaburzenia czynności nerek). Ryzyko miopatii podczas leczenia preparatem CRESTOR 5 mg może być zwiększone przy jednoczesnym podawaniu niektórych innych leków hipolipemizujących (fibraty lub niacyna), gemfibrozylu, cyklosporyny, atazanawiru z rytonawirem, lopinawiru z rytonawirem lub symeprewiru [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz INTERAKCJE Z LEKAMI ]. Przypadki miopatii, w tym rabdomiolizy, zgłaszano podczas stosowania inhibitorów reduktazy HMG-CoA, w tym rozuwastatyny, podawanych jednocześnie z kolchicyną, dlatego należy zachować ostrożność przepisując preparat CRESTOR z kolchicyną [patrz INTERAKCJE Z LEKAMI ].
Leczenie preparatem CRESTOR należy przerwać w przypadku wystąpienia znacznego podwyższenia aktywności kinazy kreatynowej lub rozpoznania lub podejrzenia miopatii. Terapię preparatem CRESTOR 5 mg należy również czasowo wstrzymać u każdego pacjenta z ostrym, ciężkim stanem sugerującym miopatię lub predysponującym do rozwoju niewydolności nerek wtórnej do rabdomiolizy (np. posocznica, niedociśnienie, odwodnienie, poważny zabieg chirurgiczny, uraz, ciężkie zaburzenia metaboliczne, endokrynologiczne, i zaburzenia elektrolitowe lub niekontrolowane drgawki).
Istnieją rzadkie doniesienia o miopatii martwiczej o podłożu immunologicznym (IMNM), autoimmunologicznej miopatii związanej ze stosowaniem statyn. IMNM charakteryzuje się: osłabieniem mięśni proksymalnych oraz podwyższoną aktywnością kinazy kreatynowej w surowicy, która utrzymuje się pomimo przerwania leczenia statynami; biopsja mięśnia wykazująca martwiczą miopatię bez znaczącego stanu zapalnego; poprawa za pomocą środków immunosupresyjnych.
Wszystkim pacjentom należy zalecić, aby niezwłocznie zgłaszali lekarzowi niewyjaśnione bóle, tkliwość lub osłabienie mięśni, szczególnie jeśli towarzyszy im złe samopoczucie lub gorączka lub jeśli objawy przedmiotowe i podmiotowe dotyczące mięśni utrzymują się po odstawieniu leku CRESTOR.
Nieprawidłowości enzymów wątrobowych
Zaleca się wykonanie testów enzymów wątrobowych przed rozpoczęciem leczenia preparatem CRESTOR 10 mg oraz w przypadku wystąpienia oznak lub objawów uszkodzenia wątroby.
Podczas stosowania inhibitorów reduktazy HMG-CoA, w tym preparatu CRESTOR, zgłaszano zwiększenie aktywności aminotransferaz w surowicy [AST (SGOT) lub ALT (SGPT)]. W większości przypadków wzrosty były przemijające i ustąpiły lub uległy poprawie podczas kontynuacji terapii lub po krótkiej przerwie w terapii. Wystąpiły dwa przypadki żółtaczki, dla których nie udało się ustalić związku z leczeniem preparatem CRESTOR, które ustąpiły po przerwaniu terapii. W badaniach tych nie było przypadków niewydolności wątroby ani nieodwracalnej choroby wątroby. W zbiorczej analizie badań kontrolowanych placebo, zwiększenie aktywności aminotransferaz w surowicy do >3-krotności górnej granicy normy wystąpiło u 1,1% pacjentów przyjmujących CRESTOR w dawce 5 mg w porównaniu z 0,5% pacjentów otrzymujących placebo.
Po wprowadzeniu produktu do obrotu zgłaszano rzadkie przypadki niewydolności wątroby zakończonej zgonem lub niezakończonej zgonem u pacjentów przyjmujących statyny, w tym rozuwastatynę. Jeśli podczas leczenia preparatem CRESTOR 20 mg wystąpi poważne uszkodzenie wątroby z objawami klinicznymi i/lub hiperbilirubinemią lub żółtaczką, należy niezwłocznie przerwać leczenie. Jeśli nie znaleziono innej etiologii, nie uruchamiaj ponownie CRESTOR.
CRESTOR 5 mg należy stosować ostrożnie u pacjentów spożywających znaczne ilości alkoholu i (lub) z przewlekłą chorobą wątroby w wywiadzie [patrz FARMAKOLOGIA KLINICZNA ]. Aktywna choroba wątroby, która może obejmować niewyjaśnione uporczywe podwyższenie aktywności aminotransferaz, jest przeciwwskazaniem do stosowania preparatu CRESTOR [patrz PRZECIWWSKAZANIA ].
Jednoczesne stosowanie leków przeciwzakrzepowych kumaryny
Należy zachować ostrożność podczas jednoczesnego podawania leków przeciwzakrzepowych z preparatem CRESTOR, ponieważ nasila on działanie leków przeciwzakrzepowych z grupy kumaryny na wydłużanie czasu protrombinowego/INR. U pacjentów przyjmujących jednocześnie leki przeciwzakrzepowe z grupy kumaryny i preparat CRESTOR, wartość INR należy określić przed rozpoczęciem leczenia preparatem CRESTOR w dawce 10 mg i wystarczająco często podczas wczesnego leczenia, aby upewnić się, że nie wystąpią żadne istotne zmiany wartości INR [patrz INTERAKCJE Z LEKAMI ].
Proteinuria i krwiomocz
programie badań klinicznych CRESTOR u pacjentów leczonych preparatem CRESTOR obserwowano białkomocz z dodatnim wynikiem testu paskowego i mikroskopijny krwiomocz. Wyniki te były częstsze u pacjentów przyjmujących CRESTOR 40 mg w porównaniu z niższymi dawkami CRESTOR 20 mg lub porównawczymi inhibitorami reduktazy HMG-CoA, chociaż na ogół było to przemijające i nie było związane z pogorszeniem czynności nerek. Chociaż kliniczne znaczenie tego odkrycia nie jest znane, należy rozważyć zmniejszenie dawki u pacjentów leczonych preparatem CRESTOR z niewyjaśnionym przewlekłym białkomoczem i (lub) krwiomoczem podczas rutynowych badań moczu.
Efekty endokrynologiczne
W przypadku inhibitorów reduktazy HMG-CoA, w tym preparatu CRESTOR, zgłaszano wzrost stężenia HbA1c i stężenia glukozy w surowicy na czczo. W oparciu o dane z badań klinicznych z CRESTOR, w niektórych przypadkach wzrost ten może przekroczyć próg rozpoznania cukrzycy [patrz DZIAŁANIA NIEPOŻĄDANE ].
Chociaż badania kliniczne wykazały, że sam preparat CRESTOR 10 mg nie zmniejsza podstawowego stężenia kortyzolu w osoczu ani nie zaburza rezerwy nadnerczowej, należy zachować ostrożność, jeśli preparat CRESTOR jest podawany jednocześnie z lekami, które mogą zmniejszać stężenie lub aktywność endogennych hormonów steroidowych, takimi jak ketokonazol, spironolakton i cymetydyna.
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( INFORMACJA O PACJENCIE ).
Pacjentów należy pouczyć, aby nie przyjmowali 2 dawek preparatu CRESTOR w ciągu 12 godzin od siebie.
Efekty mięśni szkieletowych
Pacjentom należy zalecić, aby niezwłocznie zgłaszali niewyjaśniony ból, tkliwość lub osłabienie mięśni, szczególnie jeśli towarzyszy im złe samopoczucie lub gorączka lub jeśli te objawy przedmiotowe lub podmiotowe mięśni utrzymują się po odstawieniu leku CRESTOR.
Jednoczesne stosowanie leków zobojętniających kwas
W przypadku przyjmowania leku CRESTOR 5 mg z połączeniem leków zobojętniających wodorotlenek glinu i magnezu, lek zobojętniający należy przyjąć co najmniej 2 godziny po podaniu leku CRESTOR 10 mg.
Toksyczność zarodkowo-płodowa
Poinformuj kobiety o potencjale reprodukcyjnym ryzyka dla płodu, aby stosowały skuteczną antykoncepcję podczas leczenia i informowały swojego lekarza o stwierdzonej lub podejrzewanej ciąży. [Widzieć PRZECIWWSKAZANIA oraz Używaj w określonych populacjach ].
Laktacja
Poradzić kobietom, aby nie karmiły piersią podczas leczenia preparatem CRESTOR [patrz PRZECIWWSKAZANIA oraz Używaj w określonych populacjach ].
Enzymy wątrobowe
Zaleca się wykonanie testów enzymów wątrobowych przed rozpoczęciem leczenia preparatem CRESTOR oraz w przypadku wystąpienia objawów przedmiotowych lub podmiotowych uszkodzenia wątroby. Wszystkim pacjentom leczonym preparatem CRESTOR należy doradzić, aby niezwłocznie zgłaszali wszelkie objawy mogące wskazywać na uszkodzenie wątroby, w tym zmęczenie, jadłowstręt, dyskomfort w prawym nadbrzuszu, ciemny mocz lub żółtaczkę.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
W trwającym 104 tygodnie badaniu rakotwórczości u szczurów przy dawkach 2, 20, 60 lub 80 mg/kg mc./dobę podawanych przez zgłębnik doustny częstość występowania polipów podścieliska macicy była istotnie zwiększona u samic po podaniu dawki 80 mg/kg mc./dobę ekspozycja 20 razy większa niż ekspozycja człowieka przy dawce 40 mg/dobę na podstawie AUC. Przy niższych dawkach nie obserwowano zwiększonej częstości występowania polipów.
107-tygodniowym badaniu rakotwórczości u myszy, którym podawano 10, 60 lub 200 mg/kg/dobę przez zgłębnik doustny, zaobserwowano zwiększoną częstość występowania gruczolaka/raka wątrobowokomórkowego przy dawce 200 mg/kg/dobę przy ekspozycji ogólnoustrojowej 20-krotnie większej niż ekspozycja u ludzi przy 40 mg/dzień w oparciu o AUC. Przy niższych dawkach nie zaobserwowano zwiększonej częstości występowania guzów wątrobowokomórkowych.
Rozuwastatyna nie wykazywała działania mutagennego ani klastogennego z lub bez aktywacji metabolicznej w teście Amesa z Salmonella typhimurium i Escherichia coli, teście chłoniaka myszy oraz teście aberracji chromosomowych w komórkach płuc chomika chińskiego. Rozuwastatyna dała wynik ujemny w teście mikrojądrowym in vivo u myszy.
badaniach płodności szczurów z doustnymi dawkami 5, 15, 50 mg/kg/dobę, samce leczono przez 9 tygodni przed i podczas krycia, a samice 2 tygodnie przed kryciem i podczas krycia aż do 7. dnia ciąży. wpływ na płodność obserwowano przy dawce 50 mg/kg/dobę (narażenie ogólnoustrojowe do 10 razy większe niż narażenie człowieka po dawce 40 mg/dobę na podstawie AUC). W jądrach psów leczonych rosuwastatyną w dawce 30 mg/kg/dobę przez jeden miesiąc zaobserwowano olbrzymie komórki plemnikowe. Spermatyczne komórki olbrzymie obserwowano u małp po 6-miesięcznym leczeniu w dawce 30 mg/kg/dobę oprócz wakuolizacji nabłonka kanalików nasiennych. Ekspozycja u psa była 20-krotnie większa, a u małp 10-krotna ekspozycja u człowieka przy dawce 40 mg/dobę w oparciu o powierzchnię ciała. Podobne wyniki zaobserwowano w przypadku innych leków z tej klasy.
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
CRESTOR 5 mg jest przeciwwskazany do stosowania u kobiet w ciąży, ponieważ nie ustalono bezpieczeństwa stosowania u kobiet w ciąży i nie ma widocznych korzyści z leczenia preparatem CRESTOR 20 mg podczas ciąży. Ponieważ inhibitory reduktazy HMG-CoA zmniejszają syntezę cholesterolu i prawdopodobnie syntezę innych substancji biologicznie czynnych pochodzących z cholesterolu, CRESTOR może powodować uszkodzenie płodu, gdy jest podawany kobietom w ciąży. CRESTOR 5 mg należy odstawić natychmiast po stwierdzeniu ciąży [patrz PRZECIWWSKAZANIA ]. Ograniczone opublikowane dane dotyczące stosowania rosuwastatyny są niewystarczające do określenia związanego z lekiem ryzyka poważnych wad wrodzonych lub poronienia. W badaniach na zwierzętach dotyczących reprodukcji nie stwierdzono niekorzystnego wpływu na rozwój po doustnym podaniu rozuwastatyny podczas organogenezy przy ogólnoustrojowych ekspozycjach równoważnych maksymalnej zalecanej dawce u ludzi (MRHD) wynoszącej 40 mg/dobę u szczurów lub królików (na podstawie, odpowiednio, AUC i powierzchni ciała). ). U szczurów i królików zmniejszona przeżywalność młodych/płodów występowała odpowiednio 12 razy i była równoważna MRHD 40 mg/dobę [patrz Dane ].
Szacowane ryzyko tła poważnych wad wrodzonych i poronienia dla wskazanej populacji jest nieznane. W ogólnej populacji USA szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2-4% i 15-20%.
Dane
Dane ludzkie
Ograniczone opublikowane dane dotyczące rozuwastatyny nie wykazały zwiększonego ryzyka poważnych wad wrodzonych lub poronienia. Rzadko zgłaszano przypadki wad wrodzonych po wewnątrzmacicznej ekspozycji na inne statyny. W przeglądzie około 100 prospektywnie obserwowanych ciąż u kobiet narażonych na symwastatynę lub lowastatynę, częstość występowania wad wrodzonych, samoistnych poronień i zgonów/urodzeń martwych płodów nie przekroczyła oczekiwanej w populacji ogólnej. Liczba przypadków jest wystarczająca, aby wykluczyć ≥3 do 4-krotny wzrost wad wrodzonych w stosunku do podstawowej częstości występowania. W 89% ciąż obserwowanych prospektywnie leczenie farmakologiczne rozpoczęto przed zajściem w ciążę i przerwano w pewnym momencie pierwszego trymestru, po stwierdzeniu ciąży.
Dane zwierząt
Rozuwastatyna przenika przez łożysko u szczurów i królików i znajduje się w tkankach płodów i płynie owodniowym odpowiednio w 3% i 20% stężenia w osoczu matki po podaniu pojedynczej dawki doustnej 25 mg/kg przez zgłębnik w 16. dniu ciąży u szczurów. Większą dystrybucję w tkankach płodu (25% stężenia w osoczu matki) obserwowano u królików po jednorazowym podaniu przez zgłębnik pojedynczej dawki 1 mg/kg w 18. dniu ciąży.
Podawanie rozuwastatyny nie wykazało działania teratogennego u szczurów w dawce ≤25 mg/kg/dobę lub u królików ≤3 mg/kg/dobę (dawki odpowiadające MRHD wynoszące 40 mg/dobę odpowiednio na podstawie AUC i powierzchni ciała).
U samic szczurów, którym podawano 5, 15 i 50 mg/kg/dobę przed kryciem i kontynuowano do 7. dnia ciąży, skutkowało to zmniejszeniem masy ciała płodów (samice) i opóźnieniem kostnienia przy dawce 50 mg/kg/dobę (10-krotność ekspozycji u ludzi w dawka MRHD 40 mg/dobę na podstawie AUC).
ciężarnych szczurów, którym podawano rosuwastatynę w dawce 2, 10 i 50 mg/kg/dobę od 7. dnia ciąży do 21. dnia laktacji (odstawienie od matki), zmniejszona przeżywalność potomstwa wystąpiła przy dawce 50 mg/kg/dobę (dawka odpowiadająca 12-krotności MRHD wynoszącej 40 mg). /dzień w oparciu o powierzchnię ciała).
U ciężarnych królików, którym podawano rozuwastatynę w dawce 0,3, 1 i 3 mg/kg/dobę od 6. do 18. dnia ciąży, zaobserwowano zmniejszoną żywotność płodów i śmiertelność matek przy dawce 3 mg/kg/dobę (dawka równoważna MRHD 40 mg/dobę). dzień na podstawie powierzchni ciała).
Laktacja
Podsumowanie ryzyka
Stosowanie rozuwastatyny jest przeciwwskazane w okresie karmienia piersią [patrz PRZECIWWSKAZANIA ]. Ograniczone dane wskazują, że CRESTOR jest obecny w mleku ludzkim. Brak dostępnych informacji na temat wpływu leku na niemowlę karmione piersią lub wpływu leku na produkcję mleka. Ze względu na możliwość wystąpienia poważnych działań niepożądanych u niemowlęcia karmionego piersią należy poinformować pacjentki, że nie zaleca się karmienia piersią podczas leczenia preparatem CRESTOR.
Kobiety i mężczyźni o potencjale rozrodczym
Zapobieganie ciąży
CRESTOR może powodować uszkodzenie płodu, gdy jest podawany kobiecie w ciąży [patrz Używaj w określonych populacjach ]. Doradzić kobietom w wieku rozrodczym stosowanie skutecznej antykoncepcji podczas leczenia preparatem CRESTOR.
Zastosowanie pediatryczne
U dzieci i młodzieży w wieku od 8 do 17 lat z heterozygotyczną hipercholesterolemią rodzinną, bezpieczeństwo i skuteczność preparatu CRESTOR 10 mg jako dodatku do diety w celu obniżenia poziomu cholesterolu całkowitego, LDL-C i ApoB, gdy po odpowiedniej próbie leczenia dietą stężenie LDL -C przekracza 190 mg/dl lub gdy LDL-C przekracza 160 mg/dl i istnieje dodatni wywiad rodzinny dotyczący przedwczesnej CVD lub co najmniej dwóch innych czynników ryzyka CVD, ustalono w jednym kontrolowanym badaniu i w jednym otwartym, niekontrolowanym badaniu próba [patrz Studia kliniczne ]. Nie ustalono długoterminowej skuteczności terapii CRESTOR rozpoczętej w dzieciństwie w zakresie zmniejszenia zachorowalności i śmiertelności w wieku dorosłym.
Bezpieczeństwo i skuteczność preparatu CRESTOR 5 mg u dzieci i młodzieży w wieku od 10 do 17 lat z heterozygotyczną hipercholesterolemią rodzinną oceniano w kontrolowanym badaniu klinicznym trwającym 12 tygodni, po którym następowało 40 tygodni otwartej ekspozycji. Pacjenci leczeni 5 mg, 10 mg i 20 mg CRESTOR 10 mg na dobę mieli profil działań niepożądanych ogólnie podobny do profilu pacjentów otrzymujących placebo. Nie stwierdzono wykrywalnego wpływu preparatu CRESTOR na wzrost, wagę, BMI (wskaźnik masy ciała) lub dojrzewanie płciowe [patrz Studia kliniczne ] u dzieci i młodzieży (w wieku od 10 do 17 lat).
Preparat CRESTOR nie był badany w kontrolowanych badaniach klinicznych z udziałem pacjentów w wieku przedpokwitaniowym lub pacjentów w wieku poniżej 10 lat z heterozygotyczną hipercholesterolemią rodzinną. Jednak bezpieczeństwo i skuteczność preparatu CRESTOR zostały ocenione w dwuletnim, otwartym, niekontrolowanym badaniu obejmującym dzieci i młodzież w wieku od 8 do 17 lat z heterozygotyczną hipercholesterolemią rodzinną [patrz Studia kliniczne ]. Bezpieczeństwo i skuteczność preparatu CRESTOR 5 mg w obniżaniu stężenia LDL-C wydawały się zasadniczo zgodne z obserwowanymi u pacjentów dorosłych, pomimo ograniczeń projektu badania niekontrolowanego.
Dzieci i młodzież w wieku od 7 do 15 lat z homozygotyczną hipercholesterolemią rodzinną badano w 6-tygodniowym randomizowanym, naprzemiennym badaniu kontrolowanym placebo, w którym stosowano CRESTOR 20 mg raz na dobę, po którym następowało 12 tygodni otwartego leczenia [patrz Studia kliniczne ]. Ogólnie profil bezpieczeństwa w tym badaniu był zgodny z wcześniej ustalonym profilem bezpieczeństwa u dorosłych.
Chociaż nie wszystkie działania niepożądane zidentyfikowane w populacji dorosłych były obserwowane w badaniach klinicznych z udziałem dzieci i młodzieży, te same ostrzeżenia i środki ostrożności dla dorosłych należy rozważyć w przypadku dzieci i młodzieży. Nastoletnim kobietom należy doradzić odpowiednie metody antykoncepcji podczas leczenia preparatem CRESTOR 5 mg [patrz Używaj w określonych populacjach ].
Zastosowanie geriatryczne
Spośród 10 275 pacjentów w badaniach klinicznych z preparatem CRESTOR, 3159 (31%) miało 65 lat i więcej, a 698 (6,8%) miało 75 lat i więcej. Nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między tymi pacjentami a młodszymi pacjentami, a inne zgłoszone doświadczenia kliniczne nie wykazały różnic w odpowiedziach między pacjentami w podeszłym wieku i młodszymi, ale nie można wykluczyć większej wrażliwości niektórych osób starszych.
Pacjenci w podeszłym wieku są narażeni na większe ryzyko miopatii i CRESTOR należy przepisywać z ostrożnością osobom w podeszłym wieku [patrz OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
Zaburzenia czynności nerek
Na ekspozycję na rozuwastatynę nie wpływają łagodne do umiarkowanych zaburzenia czynności nerek (CLcr ≥30 ml/min/1,73 m²). U pacjentów z ciężkimi zaburzeniami czynności nerek (CLcr DAWKOWANIE I SPOSÓB PODAWANIA , OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
Niewydolność wątroby
Preparat CRESTOR jest przeciwwskazany u pacjentów z czynną chorobą wątroby, która może obejmować niewyjaśnione utrzymujące się podwyższenie aktywności aminotransferaz wątrobowych. Wiadomo, że przewlekła poalkoholowa choroba wątroby zwiększa ekspozycję na rozuwastatynę; U tych pacjentów CRESTOR 20 mg należy stosować ostrożnie [patrz PRZECIWWSKAZANIA , OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
Azjatyccy pacjenci
Badania farmakokinetyczne wykazały około 2-krotny wzrost mediany ekspozycji na rozuwastatynę u osób pochodzenia azjatyckiego w porównaniu z grupą kontrolną rasy kaukaskiej. U pacjentów pochodzenia azjatyckiego należy dostosować dawkę preparatu CRESTOR [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
Nie ma specyficznego leczenia w przypadku przedawkowania. W przypadku przedawkowania pacjenta należy leczyć objawowo i w razie potrzeby zastosować leczenie podtrzymujące. Hemodializa nie zwiększa znacząco klirensu rozuwastatyny.
PRZECIWWSKAZANIA
CRESTOR 20mg jest przeciwwskazany w następujących stanach:
- Pacjenci ze stwierdzoną nadwrażliwością na którykolwiek składnik tego produktu. Podczas stosowania produktu CRESTOR zgłaszano reakcje nadwrażliwości, w tym wysypkę, świąd, pokrzywkę i obrzęk naczynioruchowy [patrz DZIAŁANIA NIEPOŻĄDANE ].
- Pacjenci z czynną chorobą wątroby, która może obejmować niewyjaśnione utrzymujące się podwyższenie poziomu transaminaz wątrobowych [patrz OSTRZEŻENIA I ŚRODKI ].
- Ciąża [patrz Używaj w określonych populacjach ].
- Laktacja. Ograniczone dane wskazują, że CRESTOR 20 mg jest obecny w mleku ludzkim. Ponieważ statyny mogą wywoływać poważne reakcje niepożądane u niemowląt karmionych piersią, kobiety wymagające leczenia preparatem CRESTOR nie powinny karmić niemowląt piersią [patrz Używaj w określonych populacjach ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
CRESTOR 10mg jest selektywnym i konkurencyjnym inhibitorem reduktazy HMG-CoA, enzymu ograniczającego szybkość przemiany 3-hydroksy-3-metyloglutarylokoenzymu A do mewalonianu, prekursora cholesterolu. Badania in vivo na zwierzętach oraz badania in vitro na hodowanych komórkach zwierzęcych i ludzkich wykazały, że rozuwastatyna ma wysoki wychwyt i selektywność działania w wątrobie, narządzie docelowym dla obniżania poziomu cholesterolu. W badaniach in vivo i in vitro rozuwastatyna wywiera dwojakie działanie modyfikujące lipidy. Po pierwsze, zwiększa liczbę wątrobowych receptorów LDL na powierzchni komórki, aby zwiększyć wychwyt i katabolizm LDL. Po drugie, rosuwastatyna hamuje wątrobową syntezę VLDL, co zmniejsza całkowitą liczbę cząsteczek VLDL i LDL.
Farmakodynamika
CRESTOR 5 mg dawka w zależności od dawki obniża podwyższony poziom cholesterolu LDL oraz obniża poziom cholesterolu całkowitego i trójglicerydów oraz podwyższa poziom cholesterolu HDL [patrz Studia kliniczne ]. Odpowiedź terapeutyczna na CRESTOR 5 mg jest widoczna w ciągu 1 tygodnia od rozpoczęcia leczenia, a 90% maksymalnej odpowiedzi jest zwykle osiągane w ciągu 2 tygodni. Maksymalną odpowiedź uzyskuje się zwykle po 4 tygodniach i po tym okresie utrzymuje się. Indywidualizacja dawkowania leku powinna opierać się na odpowiedzi terapeutycznej [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Farmakokinetyka
Wchłanianie
W badaniach farmakologii klinicznej u ludzi maksymalne stężenie rozuwastatyny w osoczu było osiągane 3 do 5 godzin po podaniu doustnym. Zarówno Cmax, jak i AUC wzrosły w przybliżeniu proporcjonalnie do dawki 10 mg preparatu CRESTOR. Całkowita biodostępność rozuwastatyny wynosi około 20%.
Podawanie preparatu CRESTOR z jedzeniem nie miało wpływu na AUC rozuwastatyny.
AUC rozuwastatyny nie różni się po wieczornym lub porannym podaniu leku.
Dystrybucja
Średnia objętość dystrybucji w stanie stacjonarnym rozuwastatyny wynosi około 134 litrów. Rozuwastatyna wiąże się w 88% z białkami osocza, głównie albuminami. Wiązanie to jest odwracalne i niezależne od stężeń w osoczu.
Eliminacja
Rozuwastatyna jest wydalana głównie z kałem. Okres półtrwania rozuwastatyny w fazie eliminacji wynosi około 19 godzin.
Metabolizm
Rozuwastatyna nie jest intensywnie metabolizowana; około 10% radioznakowanej dawki jest odzyskiwane w postaci metabolitu. Głównym metabolitem jest N-desmetylorozuwastatyna, która jest tworzona głównie przez cytochrom P450\2C9, a badania in vitro wykazały, że N-desmetylorozuwastatyna ma w przybliżeniu jedną szóstą do połowy aktywności hamującej reduktazę HMG-CoA związku macierzystego . Ogólnie rzecz biorąc, związek macierzysty odpowiada za ponad 90% aktywnej aktywności hamującej reduktazę HMG-CoA w osoczu.
Wydalanie
Po podaniu doustnym rozuwastatyna i jej metabolity są wydalane głównie z kałem (90%). Po podaniu dożylnym około 28% całkowitego klirensu organizmu było drogą nerkową, a 72% drogą wątrobową.
Określone populacje
Grupy rasowe lub etniczne
Analiza farmakokinetyki populacyjnej nie wykazała klinicznie istotnych różnic w farmakokinetyce między grupami rasy białej, latynoskiej, czarnej lub afrokaraibskiej. Jednak badania farmakokinetyczne, w tym jedno przeprowadzone w USA, wykazały około 2-krotne zwiększenie mediany ekspozycji (AUC i Cmax) u pacjentów z Azji w porównaniu z grupą kontrolną rasy kaukaskiej.
Pacjenci płci męskiej i żeńskiej
Nie było różnic w stężeniach rozuwastatyny w osoczu pomiędzy mężczyznami i kobietami.
Pacjenci pediatryczni
W analizie farmakokinetyki populacyjnej dwóch badań pediatrycznych z udziałem pacjentów z heterozygotyczną hipercholesterolemią rodzinną, odpowiednio w wieku 10 do 17 lat i 8 do 17 lat, ekspozycja na rozuwastatynę u dorosłych pacjentów była porównywalna lub mniejsza niż ekspozycja na rozuwastatynę.
Pacjenci geriatryczni
Nie stwierdzono różnic w stężeniach rozuwastatyny w osoczu pomiędzy populacją osób w podeszłym wieku i osób w podeszłym wieku (w wieku ≥65 lat).
Pacjenci z niewydolnością nerek
Łagodne do umiarkowanych zaburzenia czynności nerek (CLcr ≥30 ml/min/1,73 m²) nie miały wpływu na stężenie rozuwastatyny w osoczu. Jednak u pacjentów z ciężką niewydolnością nerek (CLcr 80 ml/min/ 1,73 m²).
Hemodializa
Stężenia rozuwastatyny w osoczu w stanie stacjonarnym u pacjentów przewlekle hemodializowanych były o około 50% większe niż u zdrowych ochotników z prawidłową czynnością nerek.
Pacjenci z niewydolnością wątroby
U pacjentów z przewlekłą alkoholową chorobą wątroby stężenie rozuwastatyny w osoczu było nieznacznie zwiększone.
U pacjentów z chorobą A Child-Pugh, Cmax i AUC były zwiększone odpowiednio o 60% i 5% w porównaniu z pacjentami z prawidłową czynnością wątroby. U pacjentów z chorobą B Child-Pugh, Cmax i AUC były zwiększone odpowiednio o 100% i 21% w porównaniu z pacjentami z prawidłową czynnością wątroby.
Badania interakcji leków
Klirens rozuwastatyny nie zależy w istotnym klinicznie stopniu od metabolizmu przez cytochrom P450 3A4.
Rozuwastatyna jest substratem dla niektórych białek transportowych, w tym białka 1B1 transportującego aniony organiczne transportera wychwytu wątrobowego (OATP1B1) i białka oporności raka piersi transportera wypływowego (BCRP). Jednoczesne podawanie produktu CRESTOR 10 mg z lekami będącymi inhibitorami tych białek transportowych (np. cyklosporyna, niektóre inhibitory proteazy HIV) może powodować zwiększenie stężenia rozuwastatyny w osoczu [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz INTERAKCJE Z LEKAMI ].
Farmakogenomika
Dyspozycja inhibitorów reduktazy HMG-CoA, w tym rosuwastatyny, obejmuje OATP1B1 i inne białka transportowe. Większe stężenia rozuwastatyny w osoczu zgłaszano w bardzo małych grupach pacjentów (n=3 do 5), którzy mają dwa allele o obniżonej czynności genu kodującego OATP1B1 (SLCO1B1 521T > C). Częstość występowania tego genotypu (tj. SLCO1B1 521 C/C) jest generalnie niższa niż 5% w większości grup rasowych/etnicznych. Wpływ tego polimorfizmu na skuteczność i/lub bezpieczeństwo rozuwastatyny nie został jasno określony.
Toksykologia i/lub farmakologia zwierząt
Toksyczność ośrodkowego układu nerwowego
Zmiany naczyniowe OUN, charakteryzujące się krwotokami okołonaczyniowymi, obrzękiem i naciekiem komórek jednojądrzastych przestrzeni okołonaczyniowych, obserwowano u psów leczonych kilkoma innymi lekami z tej grupy leków. Chemicznie podobny lek z tej klasy powodował zależne od dawki zwyrodnienie nerwu wzrokowego (zwyrodnienie Walleriana włókien siatkówkowatych) u psów, w dawce, która powodowała stężenie leku w osoczu około 30 razy wyższe niż średni poziom leku u ludzi przyjmujących najwyższą zalecaną dawkę. Obrzęk, krwotok i częściową martwicę w śródmiąższu splotu naczyniówkowego zaobserwowano u samicy psa uśmierconej w konającym dniu 24 w dawce 90 mg/kg/dobę przez doustny zgłębnik (ekspozycja ogólnoustrojowa 100 razy większa niż ekspozycja u ludzi po dawce 40 mg/dobę na podstawie AUC). Zmętnienie rogówki obserwowano u psów leczonych przez 52 tygodnie dawką 6 mg/kg/dobę przez zgłębnik doustny (ekspozycja ogólnoustrojowa 20 razy większa niż ekspozycja u ludzi po dawce 40 mg/dobę w oparciu o AUC). Zaćmę obserwowano u psów leczonych przez 12 tygodni przez zgłębnik doustny w dawce 30 mg/kg/dobę (ekspozycja ogólnoustrojowa 60 razy większa niż ekspozycja u ludzi po dawce 40 mg/dobę w oparciu o AUC). Dysplazja siatkówki i utrata siatkówki obserwowano u psów leczonych przez 4 tygodnie przez zgłębnik doustny w dawce 90 mg/kg/dobę (ekspozycja ogólnoustrojowa 100 razy większa niż ekspozycja u ludzi po dawce 40 mg/dobę w oparciu o AUC). Dawki ≤30 mg/kg/dobę (ekspozycja ogólnoustrojowa ≤60-krotna ekspozycja u ludzi po dawce 40 mg/dobę na podstawie AUC) nie wykazały zmian w siatkówce podczas leczenia przez okres do jednego roku.
Badanie toksykologiczne dla nieletnich
W badaniu na młodych osobnikach szczurom podawano przez zgłębnik doustny 10 lub 50 mg/kg/dobę od odsadzenia przez 9 tygodni przed parowaniem, przez cały czas parowania i do dnia przed sekcją w przypadku samców lub do 7 dnia ciąży w przypadku samic. Nie zaobserwowano wpływu na rozwój płciowy, wygląd jąder i najądrzy ani płodność przy żadnej z dawek (2-krotność lub do 24-krotności ekspozycji u ludzi (AUC) przy maksymalnej dawce pediatrycznej wynoszącej 20 mg/dobę).
Studia kliniczne
Hiperlipidemia i mieszana dyslipidemia
CRESTOR 5 mg zmniejsza całkowity C, LDL-C, ApoB, nonHDL-C i TG oraz zwiększa HDL-C u dorosłych pacjentów z hiperlipidemią i mieszaną dyslipidemią.
Badanie zakresu dawkowania
W wieloośrodkowym, podwójnie zaślepionym, kontrolowanym placebo badaniu z zakresem dawek u pacjentów z hiperlipidemią, CRESTOR podawany w pojedynczej dawce dobowej przez 6 tygodni znacząco zmniejszał całkowity C, LDL-C, nonHDL-C i ApoB w całej dawce zasięg (tabela 6).
Aktywnie kontrolowane badanie
CRESTOR 5 mg porównywano z inhibitorami reduktazy HMG-CoA, atorwastatyną, simwastatyną i prawastatyną w wieloośrodkowym, otwartym badaniu z różnymi dawkami, obejmującym 2240 pacjentów z hiperlipidemią lub mieszaną dyslipidemią. Po randomizacji pacjenci byli leczeni przez 6 tygodni pojedynczą dzienną dawką preparatu CRESTOR 20 mg, atorwastatyny, simwastatyny lub prawastatyny (ryc. 1 i tabela 7).
Rycina 1: Procentowa zmiana LDL-C według dawki preparatu CRESTOR 20 mg, atorwastatyny, symwastatyny i prawastatyny w tygodniu 6 u pacjentów z hiperlipidemią lub mieszaną dyslipidemią 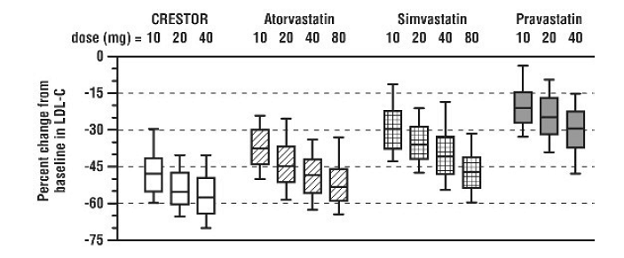
Wykresy pudełkowe przedstawiają wartości 25., 50. i 75. percentyla, z wąsami reprezentującymi wartości 10. i 90. percentyla. Średni wyjściowy poziom LDL-C: 189 mg/Dl
Heterozygotyczna hipercholesterolemia rodzinna
Aktywnie kontrolowane badanie
badaniu pacjentów z heterozygotyczną FH (wyjściowa średnia LDL wynosząca 291), pacjentów przydzielono losowo do grupy CRESTOR 20 mg lub atorwastatyny 20 mg. Dawkę zwiększano w odstępach 6-tygodniowych. Przy każdej dawce w obu leczonych grupach zaobserwowano istotne zmniejszenie stężenia LDL-C w stosunku do wartości wyjściowej (Tabela 8).
Hipertriglicerydemia
Badanie dawka-odpowiedź
W podwójnie zaślepionym, kontrolowanym placebo badaniu dawka-odpowiedź u pacjentów z początkowymi poziomami TG od 273 do 817 mg/dl, CRESTOR 10 mg podawany w pojedynczej dawce dobowej (5 do 40 mg) przez 6 tygodni znacząco obniżył poziom TG w surowicy ( Tabela 9).
Pierwotna dysbetalipoproteinemia (hiperlipoproteinemia typu III)
randomizowanym, wieloośrodkowym, podwójnie zaślepionym badaniu krzyżowym 32 pacjentów (27 z ε2/ε2 i 4 z mutacją apo E [Arg145Cys] z pierwotną dysbetalipoproteinemią (hiperlipoproteinemią typu III) weszło do 6-tygodniowego okresu wstępnego żywienia w NCEP Dieta terapeutycznej zmiany stylu życia (TLC) Po wprowadzeniu diety pacjenci zostali losowo przydzieleni do sekwencji terapii w połączeniu z dietą TLC przez 6 tygodni każdy: rozuwastatyna 10 mg, a następnie rozuwastatyna 20 mg lub rozuwastatyna 20 mg, a następnie rozuwastatyna 10 mg CRESTOR obniżył poziomy niezwiązanego HDL-C (pierwszorzędowy punkt końcowy) i krążącej pozostałości lipoproteiny.Wyniki przedstawiono w poniższej tabeli.
Homozygotyczna rodzinna hipercholesterolemia
Badanie miareczkowania dawki
otwartym badaniu z wymuszonym miareczkowaniem homozygotyczni pacjenci z FH (n=40, 8-63 lat) byli oceniani pod kątem odpowiedzi na preparat CRESTOR w dawce 20-40 mg, miareczkowany co 6 tygodni. W całej populacji średnie zmniejszenie stężenia LDL-C w stosunku do wartości wyjściowej wyniosło 22%. Około jedna trzecia pacjentów odniosła korzyści ze zwiększenia dawki z 20 mg do 40 mg z dalszym obniżeniem LDL o ponad 6%. U 27 pacjentów z co najmniej 15% redukcją LDL-C, średnia redukcja LDL-C wyniosła 30% (mediana 28% redukcji). Spośród 13 pacjentów z redukcją LDL-C
Pacjenci pediatryczni z homozygotyczną hipercholesterolemią rodzinną
CRESTOR badano w randomizowanym, podwójnie ślepym, wieloośrodkowym, krzyżowym badaniu kontrolowanym placebo z udziałem 14 dzieci i młodzieży z homozygotyczną hipercholesterolemią rodzinną. Badanie obejmowało 4-tygodniową fazę wstępną diety, podczas której pacjenci otrzymywali CRESTOR 10 mg na dobę, fazę krzyżową, która obejmowała dwa 6-tygodniowe okresy leczenia CRESTOR 20 mg lub placebo w kolejności losowej, a następnie 12-tygodniowe tygodniowa faza otwartej próby, podczas której wszyscy pacjenci otrzymywali CRESTOR 20 mg. Pacjenci byli w wieku od 7 do 15 lat (mediana 11 lat), 50% stanowili mężczyźni, 71% było rasy kaukaskiej, 21% było Azjatami, 7% było rasy czarnej i żaden pacjent nie był pochodzenia latynoskiego. Pięćdziesiąt procent stosowało terapię aferezą, a 57% przyjmowało ezetymib. Pacjenci, którzy przystąpili do badania stosując terapię aferezą lub ezetymibem, kontynuowali leczenie przez całe badanie. Średnie stężenie LDL-C na początku badania wynosiło 416 mg/dl (zakres od 152 do 716 mg/dl). W sumie 13 pacjentów ukończyło oba okresy leczenia randomizowanej fazy krzyżowej; jeden pacjent wycofał zgodę z powodu niemożności pobrania krwi w fazie krzyżowej.
CRESTOR 20 mg znacząco obniżył poziom LDL-C, cholesterolu całkowitego, ApoB i nie-HDL-C w porównaniu z placebo (Tabela 11).
Pacjenci pediatryczni z heterozygotyczną hipercholesterolemią rodzinną
W podwójnie zaślepionym, randomizowanym, wieloośrodkowym, 12-tygodniowym badaniu kontrolowanym placebo, 176 (97 mężczyzn i 79 kobiet) dzieci i młodzieży z heterozygotyczną hipercholesterolemią rodzinną zostało losowo przydzielonych do grupy otrzymującej rozuwastatynę w dawce 5, 10 lub 20 mg lub placebo na dobę. Pacjenci byli w wieku od 10 do 17 lat (mediana wieku 14 lat), przy czym około 30% pacjentów w wieku od 10 do 13 lat i około 17%, 18%, 40% i 25% w stopniu Tannera II, III, IV, i V, odpowiednio. Kobiety były co najmniej 1 rok po menarche. Średnie stężenie LDL-C na początku badania wynosiło 233 mg/dl (zakres od 129 do 399). Po 12-tygodniowej fazie podwójnie ślepej próby nastąpiła 40-tygodniowa otwarta faza miareczkowania dawki, w której wszyscy pacjenci (n=173) otrzymywali rozuwastatynę w dawce 5 mg, 10 mg lub 20 mg na dobę.
Rozuwastatyna znacząco obniżyła poziom LDL-C (pierwszorzędowy punkt końcowy), poziom cholesterolu całkowitego i ApoB w każdej dawce w porównaniu z placebo. Wyniki przedstawiono w tabeli 12 poniżej.
Pod koniec 12-tygodniowego okresu leczenia metodą podwójnie ślepej próby odsetek pacjentów, którzy osiągnęli cel LDL-C poniżej 110 mg/dl (2,8 mmol/l) wynosił 0% dla placebo, 12% dla rozuwastatyny 5 mg , 41% dla rozuwastatyny 10 mg i 41% dla rozuwastatyny 20 mg. W 40-tygodniowej fazie otwartej próby 71% pacjentów zwiększono do maksymalnej dawki 20 mg, a 41% pacjentów osiągnęło cel LDL-C 110 mg/dl.
Rozuwastatynę badano również w dwuletnim, otwartym, niekontrolowanym badaniu z miareczkowaniem do celu, w którym wzięło udział 175 dzieci i młodzieży z heterozygotyczną hipercholesterolemią rodzinną w wieku od 8 do 17 lat (79 chłopców i 96 dziewcząt). Wszyscy pacjenci mieli udokumentowany defekt genetyczny w receptorze LDL lub w ApoB. Około 89% to osoby rasy białej, 7% to Azjaci, 1% to osoby rasy czarnej i mniej niż 1% to Latynosi. Średnie stężenie LDL-C na początku badania wynosiło 236 mg/dl. Pięćdziesiąt osiem (33%) pacjentów było przed pokwitaniem na początku badania. Dawka początkowa rozuwastatyny dla wszystkich dzieci i młodzieży wynosiła 5 mg raz na dobę. Dzieci w wieku od 8 do mniej niż 10 lat (n=41 na początku badania) można dostosowywać do maksymalnej dawki 10 mg raz na dobę, a dzieci i młodzież w wieku od 10 do 17 lat do maksymalnej dawki 20 mg raz na dobę.
Zmniejszenie stężenia LDL-C w stosunku do wartości wyjściowej było zasadniczo zgodne we wszystkich grupach wiekowych w ramach badania, jak również z wcześniejszym doświadczeniem zarówno w kontrolowanych badaniach z udziałem dorosłych, jak i dzieci.
Nie ustalono długoterminowej skuteczności leczenia rozuwastatyną rozpoczętego w dzieciństwie w celu zmniejszenia zachorowalności i śmiertelności w wieku dorosłym.
Spowolnienie progresji miażdżycy
badaniu Measurements Effects on Intima Media Thickness: an Evaluation Of Rosuvastatin 40 mg (METEOR), wpływ leczenia preparatem CRESTOR na miażdżycę tętnic szyjnych oceniano za pomocą ultrasonografii w trybie B u pacjentów z podwyższonym poziomem LDL-C, z niskim ryzykiem (ryzyko Framingham
Roczny wskaźnik zmiany od wartości wyjściowej dla grupy placebo wynosił +0,0131 mm/rok (p
Na poziomie indywidualnego pacjenta w grupie leczonej preparatem CRESTOR, 52,1% pacjentów wykazało brak progresji choroby (definiowanej jako ujemna roczna stopa zmian), w porównaniu z 37,7% pacjentów w grupie placebo.
Pierwotna profilaktyka chorób układu krążenia
badaniu Uzasadnienie for the Use of Statins in Primary Prevention: An Intervention Trial Evaluating Rosuvastatin (JUPITER) u 17 802 mężczyzn (≥50 lat) oceniono wpływ CRESTOR (rozuwastatyny wapniowej) na występowanie poważnych zdarzeń sercowo-naczyniowych (CV). ) oraz kobiet (≥ 60 lat), u których nie występowała klinicznie widoczna choroba sercowo-naczyniowa, stężenie LDL-C
Pierwszorzędowym punktem końcowym był złożony punkt końcowy obejmujący czas do pierwszego wystąpienia któregokolwiek z następujących poważnych zdarzeń sercowo-naczyniowych: zgon z przyczyn sercowo-naczyniowych, zawał mięśnia sercowego niezakończony zgonem, udar mózgu niezakończony zgonem, hospitalizacja z powodu niestabilnej dławicy piersiowej lub zabieg rewaskularyzacji tętniczej.
Rozuwastatyna znacząco zmniejszyła ryzyko poważnych zdarzeń sercowo-naczyniowych (252 zdarzenia w grupie placebo vs. 142 zdarzenia w grupie rozuwastatyny) przy statystycznie istotnym (p
Rycina 2: Czas do pierwszego wystąpienia poważnych incydentów sercowo-naczyniowych w badaniu JUPITER 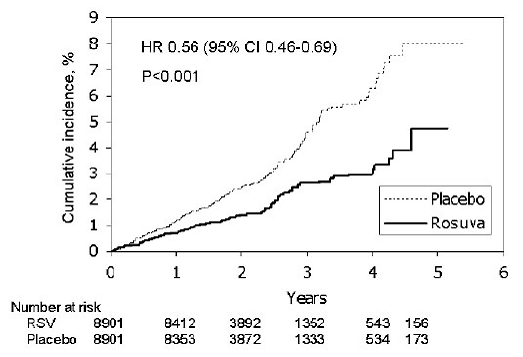
Poszczególne składowe pierwszorzędowego punktu końcowego przedstawiono na rycinie 3. Rozuwastatyna istotnie zmniejszyła ryzyko zawału mięśnia sercowego niezakończonego zgonem, udaru mózgu niezakończonego zgonem oraz zabiegów rewaskularyzacji tętniczej. Nie było istotnych różnic w leczeniu pomiędzy grupami rozuwastatyny i placebo w przypadku zgonów z przyczyn sercowo-naczyniowych lub hospitalizacji z powodu niestabilnej dławicy piersiowej.
Rozuwastatyna znacząco zmniejszała ryzyko zawału mięśnia sercowego (6 śmiertelnych i 62 niezakończonych zgonem przypadków u pacjentów otrzymujących placebo w porównaniu z 9 śmiertelnymi i 22 niezakończonymi zgonem pacjentów leczonych rozuwastatyną) oraz ryzyko udaru mózgu (6 śmiertelnych i 58 niezakończonych zgonem przypadków u pacjentów otrzymujących placebo). pacjentów otrzymujących placebo w porównaniu z 3 zdarzeniami śmiertelnymi i 30 zdarzeniami niezakończonymi zgonem u pacjentów leczonych rozuwastatyną).
analizie post hoc podgrup pacjentów JUPITER (n=1405; rozuwastatyna=725, placebo=680) z hsCRP ≥2 mg/l i bez innych tradycyjnych czynników ryzyka (palenie, ciśnienie krwi ≥140/90 lub przyjmowanie leków przeciwnadciśnieniowych, niskie HDL-C) innym niż wiek, po dostosowaniu do wysokiego HDL-C, nie było znaczących korzyści z leczenia rozuwastatyną.
Rycina 3: Poważne zdarzenia sercowo-naczyniowe według grup terapeutycznych w badaniu JUPITER 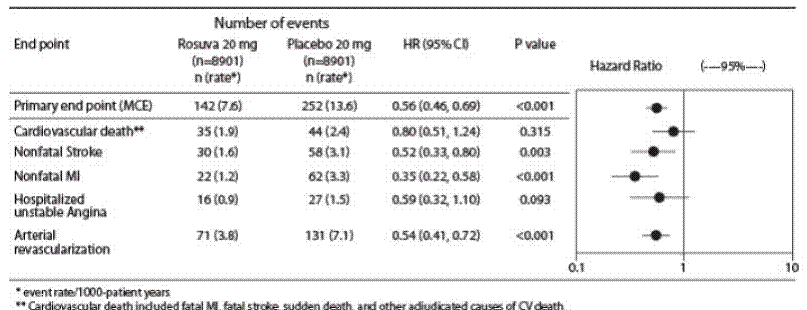
Po roku rozuwastatyna zwiększała HDL-C i obniżała stężenie LDL-C, hsCRP, cholesterolu całkowitego i triglicerydów w surowicy (p
INFORMACJA O PACJENCIE
CRESTOR® (Kres-tor) rozuwastatyny w postaci tabletek
Przeczytaj uważnie niniejszą Informację dla pacjenta przed rozpoczęciem przyjmowania leku CRESTOR 20 mg i za każdym razem, gdy otrzymujesz uzupełnienie. W przypadku jakichkolwiek pytań dotyczących preparatu CRESTOR, należy zwrócić się do lekarza. Tylko lekarz może określić, czy CRESTOR jest dla Ciebie odpowiedni.
Co to jest CRESTOR?
CRESTOR 20mg to lek na receptę, który zawiera lek obniżający poziom cholesterolu o nazwie rosuwastatyna wapniowa. Większość cholesterolu we krwi powstaje w wątrobie. CRESTOR 20 mg działa poprzez redukcję cholesterolu na dwa sposoby: CRESTOR 5 mg blokuje enzym w wątrobie, powodując, że wątroba wytwarza mniej cholesterolu, a CRESTOR 20 mg zwiększa wychwyt i rozkład cholesterolu już we krwi przez wątrobę.
- CRESTOR stosuje się wraz z dietą w celu:
- obniżyć poziom „złego” cholesterolu (LDL)
- zwiększyć poziom „dobrego” cholesterolu (HDL)
- obniżyć poziom tłuszczu we krwi (trójglicerydy)
- spowalniają odkładanie się złogów tłuszczowych (płytki nazębnej) w ścianach naczyń krwionośnych
- CRESTOR jest stosowany w leczeniu:
- osoby dorosłe, które nie są w stanie kontrolować poziomu cholesterolu wyłącznie za pomocą diety i ćwiczeń fizycznych
- dzieci w wieku od 8 do 17 lat z heterozygotyczną hipercholesterolemią rodzinną (choroba dziedziczna, która powoduje wysoki poziom LDL)
- dzieci w wieku od 7 do 17 lat z homozygotyczną hipercholesterolemią rodzinną (choroba dziedziczna, która powoduje wysoki poziom LDL).
CRESTOR 20mg nie jest zatwierdzony do stosowania u dzieci z heterozygotyczną hipercholesterolemią rodzinną w wieku poniżej 8 lat ani do stosowania u dzieci z homozygotyczną hipercholesterolemią rodzinną w wieku poniżej 7 lat.
CRESTOR 5 mg jest stosowany w celu zmniejszenia ryzyka zawału serca i udaru mózgu u mężczyzn w wieku 50 lat i starszych oraz kobiet w wieku 60 lat i starszych, u których nie stwierdzono chorób serca, ale występują pewne dodatkowe czynniki ryzyka.
Nie wiadomo, czy CRESTOR 10 mg jest bezpieczny i skuteczny u osób z dyslipidemią Fredricksona typu I i V.
Kto nie powinien brać CRESTOR?
Nie należy przyjmować leku CRESTOR, jeśli:
- jesteś uczulony na rozuwastatynę wapniową lub którykolwiek ze składników leku CRESTOR. Pełna lista składników leku CRESTOR znajduje się na końcu tej ulotki.
- masz problemy z wątrobą.
- jesteś w ciąży, podejrzewasz, że możesz być w ciąży lub planujesz zajść w ciążę. CRESTOR 20mg może zaszkodzić nienarodzonemu dziecku. W przypadku zajścia w ciążę należy przerwać stosowanie leku CRESTOR i natychmiast skontaktować się z lekarzem. Jeśli pacjentka nie planuje zajścia w ciążę, powinna stosować skuteczną kontrolę urodzeń (antykoncepcję) podczas przyjmowania leku CRESTOR.
- karmią piersią. Leki takie jak CRESTOR 5 mg mogą przenikać do mleka matki i mogą zaszkodzić dziecku.
O czym powinienem powiedzieć lekarzowi przed i podczas przyjmowania leku CRESTOR?
Należy poinformować lekarza, jeśli:
- mieć niewyjaśnione bóle lub osłabienie mięśni
- masz lub miałeś problemy z nerkami;
- masz lub miałeś problemy z wątrobą
- pij więcej niż 2 szklanki alkoholu dziennie
- masz problemy z tarczycą
- masz 65 lat lub więcej
- są pochodzenia azjatyckiego
- jesteś w ciąży lub podejrzewasz, że możesz być w ciąży lub planujesz zajść w ciążę
- karmią piersią
Poinformuj lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe.
Porozmawiaj z lekarzem przed rozpoczęciem przyjmowania nowych leków.
Przyjmowanie leku CRESTOR 20 mg z niektórymi innymi lekami może wzajemnie na siebie oddziaływać, powodując działania niepożądane. CRESTOR może wpływać na sposób działania innych leków, a inne leki mogą wpływać na działanie leku CRESTOR.
Szczególnie powiedz swojemu lekarzowi, jeśli przyjmujesz:
- cyklosporyna (lek na układ odpornościowy)
- gemfibrozyl (lek na kwas fibrynowy do obniżania poziomu cholesterolu)
- leki przeciwwirusowe, w tym inhibitory proteazy wirusa HIV lub wirusa zapalenia wątroby typu C (takie jak lopinawir, rytonawir, fosamprenawir, typranawir, atazanawir lub symeprewir)
- niektóre leki przeciwgrzybicze (takie jak itrakonazol, ketokonazol i flukonazol)
- leki przeciwzakrzepowe kumaryny (leki zapobiegające powstawaniu zakrzepów krwi, takie jak warfaryna)
- niacyna lub kwas nikotynowy
- pochodne kwasu fibrynowego (takie jak fenofibrat)
- kolchicyna (lek stosowany w leczeniu dny moczanowej)
W razie wątpliwości należy zapytać lekarza lub farmaceutę o listę tych leków.
Poznaj wszystkie leki, które przyjmujesz. Zachowaj ich listę, aby pokazać lekarzowi i farmaceucie, gdy otrzymasz nowy lek.
Jak powinienem zażywać CRESTOR 10mg?
- Lek CRESTOR należy przyjmować zgodnie z zaleceniami lekarza.
- Przyjmować CRESTOR doustnie, 1 raz dziennie. Tabletkę połknąć w całości.
- CRESTOR można przyjmować o dowolnej porze dnia, z jedzeniem lub bez.
- Nie rób zmienić dawkę lub odstawić lek CRESTOR 10 mg bez konsultacji z lekarzem, nawet jeśli pacjent czuje się dobrze.
- Lekarz może wykonać badania krwi w celu sprawdzenia poziomu cholesterolu przed i podczas leczenia lekiem CRESTOR. W razie potrzeby lekarz może zmienić dawkę leku CRESTOR 10 mg.
- Lekarz może rozpocząć dietę obniżającą poziom cholesterolu przed podaniem leku CRESTOR. Pozostań na tej diecie, kiedy bierzesz CRESTOR.
- Po przyjęciu leku CRESTOR należy odczekać co najmniej 2 godziny, aby zastosować środek zobojętniający kwas, który zawiera połączenie wodorotlenku glinu i magnezu.
- Jeśli pominiesz dawkę leku CRESTOR 10 mg, zażyj ją, gdy tylko sobie o tym przypomnisz. Jednakże, nie należy przyjmować 2 dawek leku CRESTOR 10 mg w odstępie 12 godzin.
- W przypadku zażycia zbyt dużej dawki leku CRESTOR 20 mg lub przedawkowania należy natychmiast skontaktować się z lekarzem lub udać się na pogotowie ratunkowe najbliższego szpitala.
Jakie są możliwe skutki uboczne leku CRESTOR 20mg?
CRESTOR 10mg może powodować poważne skutki uboczne, w tym:
- Ból, tkliwość i osłabienie mięśni (miopatia). U niektórych osób problemy z mięśniami, w tym rozpad mięśni, mogą być poważne i rzadko powodują uszkodzenie nerek, które może prowadzić do śmierci. Należy natychmiast poinformować lekarza, jeśli:
- u pacjenta wystąpi niewyjaśniony ból, tkliwość lub osłabienie mięśni, zwłaszcza w przypadku gorączki lub większego niż zwykle uczucia zmęczenia podczas przyjmowania leku CRESTOR.
- pacjenta występują problemy z mięśniami, które nie ustępują nawet po zaleceniu przez lekarza zaprzestania przyjmowania leku CRESTOR. Twój lekarz może wykonać dalsze testy, aby zdiagnozować przyczynę problemów z mięśniami.
Twoje szanse na problemy z mięśniami są większe, jeśli:
- pacjent przyjmuje niektóre inne leki podczas przyjmowania leku CRESTOR
- masz 65 lat lub więcej
- masz problemy z tarczycą (niedoczynność tarczycy), które nie są kontrolowane;
- masz problemy z nerkami
- przyjmują większe dawki leku CRESTOR
- Problemy z wątrobą. Lekarz powinien wykonać badania krwi w celu sprawdzenia wątroby przed rozpoczęciem przyjmowania leku CRESTOR 5 mg oraz w przypadku wystąpienia objawów problemów z wątrobą podczas przyjmowania leku CRESTOR. Natychmiast skontaktuj się z lekarzem, jeśli wystąpi którykolwiek z następujących objawów problemów z wątrobą:
- czuć się wyjątkowo zmęczonym lub słabym
- utrata apetytu
- ból w górnej części brzucha
- ciemny mocz
- zażółcenie skóry lub białek oczu
Najczęstsze działania niepożądane mogą obejmować: bóle głowy, bóle i bóle mięśni, bóle brzucha, osłabienie i nudności.
Dodatkowe działania niepożądane zgłoszone podczas stosowania leku CRESTOR obejmują utratę pamięci i splątanie.
Należy poinformować lekarza, jeśli wystąpią jakiekolwiek objawy niepożądane, które Cię niepokoją lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne stosowania preparatu CRESTOR. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać CRESTOR 20mg?
- Przechowywać CRESTOR 10mg w temperaturze pokojowej, między 68 ° F do 77 ° F (20 ° C do 25 ° C) iw suchym miejscu.
- Bezpiecznie wyrzuć lekarstwa, które są nieaktualne lub nie są już potrzebne.
Lek CRESTOR 10 mg i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Jakie są składniki w CRESTOR?
Składnik czynny: rozuwastatyna jako rozuwastatyna wapniowa
Nieaktywne składniki: celuloza mikrokrystaliczna NF, monohydrat laktozy NF, trójzasadowy fosforan wapnia NF, krospowidon NF, stearynian magnezu NF, hypromeloza NF, triacetyna NF, dwutlenek tytanu USP, żółty tlenek żelazowy i czerwony tlenek żelazowy NF.
Ogólne informacje o bezpiecznym i skutecznym korzystaniu z CRESTOR
Czasami leki są przepisywane do celów innych niż wymienione w ulotce informacyjnej dla pacjenta. Nie należy stosować leku CRESTOR 10 mg w stanach, na które nie został przepisany. Nie należy podawać leku CRESTOR 20 mg innym osobom, nawet jeśli mają one ten sam stan chorobowy co Ty. Może im to zaszkodzić.
Możesz poprosić farmaceutę lub lekarza o informacje na temat preparatu CRESTOR 5 mg, który jest przeznaczony dla pracowników służby zdrowia.
Niniejsza informacja dla pacjenta została zatwierdzona przez amerykańską Agencję ds. Żywności i Leków poprawione 9/2018
