Zocor 5mg, 10mg, 20mg, 40mg Simvastatin Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Zocor i jak się go stosuje?
Zocor (simwastatyna) to lek na receptę stosowany w celu obniżenia poziomu „złego” cholesterolu (lipoprotein o niskiej gęstości lub LDL) i zwiększenia poziomu „dobrego” cholesterolu (lipoprotein o dużej gęstości lub HDL) oraz trigliceryny, jak również zmniejszyć ryzyko udaru i zawału serca. Zocor może być stosowany samodzielnie lub z innymi lekami.
Zocor należy do klasy leków zwanych środkami obniżającymi poziom lipidów, statynami, inhibitorami reduktazy HMG-CoA.
Nie wiadomo, czy Zocor jest bezpieczny i skuteczny u dzieci w wieku poniżej 10 lat.
Jakie są możliwe skutki uboczne Zocoru?
Zocor 20mg może powodować poważne skutki uboczne, w tym:
- utrata apetytu,
- ból brzucha w prawym górnym rogu,
- zmęczenie,
- swędzący,
- ciemny mocz,
- stolec w kolorze gliny i
- zażółcenie skóry lub oczu
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Zocor to:
- ból głowy,
- mdłości,
- ból brzucha,
- zaparcia i
- objawy przeziębienia (zatkany nos, kichanie lub ból gardła)
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Zocoru. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
ZOCOR (simwastatyna) to środek obniżający poziom lipidów, pozyskiwany syntetycznie z produktu fermentacji Aspergillus terreus. Po spożyciu doustnym simwastatyna, która jest nieaktywnym laktonem, jest hydrolizowana do odpowiedniej postaci β-hydroksykwasu. Jest to inhibitor reduktazy 3-hydroksy-3-metyloglutarylo-koenzymu A (HMG-CoA). Enzym ten katalizuje konwersję HMG-CoA do mewalonianu, co jest wczesnym i ograniczającym tempo etapem biosyntezy cholesterolu.
Simwastatyna to kwas butanowy, 2,2-dimetylo-,1,2,3,7,8,8a-heksahydro-3,7-dimetylo-8-[2-(tetrahydro-4hydroksy-6-okso-2H-piran- Ester 2-ilo)etylo]-1-naftalenylowy, [1S-[1α,3α,7β,8β(2S*,4S*),-8aβ]]. Wzór empiryczny simwastatyny to C25H38O5, a jej masa cząsteczkowa to 418,57. Jego wzór strukturalny to:
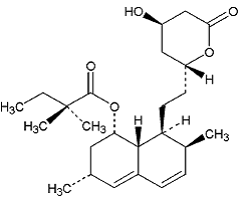
Simwastatyna jest białym lub prawie białym, niehigroskopijnym, krystalicznym proszkiem, który jest praktycznie nierozpuszczalny w wodzie i swobodnie rozpuszczalny w chloroformie, metanolu i etanolu.
Tabletki ZOCOR do podawania doustnego zawierają 5 mg, 10 mg, 20 mg, 40 mg lub 80 mg simwastatyny oraz następujące składniki nieaktywne: kwas askorbinowy, kwas cytrynowy, hydroksypropyloceluloza, hypromeloza, tlenki żelaza, laktoza, stearynian magnezu, celuloza mikrokrystaliczna , skrobia, talk i dwutlenek tytanu. Butylowany hydroksyanizol jest dodawany jako środek konserwujący.
WSKAZANIA
Terapia środkami zmieniającymi poziom lipidów powinna być tylko jednym z elementów interwencji wieloczynnikowej u osób ze znacznie zwiększonym ryzykiem miażdżycowej choroby naczyń z powodu hipercholesterolemii. Farmakoterapia jest wskazana jako uzupełnienie diety, gdy reakcja na samą dietę z ograniczeniem zawartości tłuszczów nasyconych i cholesterolu oraz inne niefarmakologiczne środki okazała się niewystarczająca. U pacjentów z chorobą niedokrwienną serca (CHD) lub z wysokim ryzykiem CHD, ZOCOR® można rozpocząć jednocześnie z dietą.
Zmniejszenie ryzyka śmiertelności z powodu CHD i incydentów sercowo-naczyniowych
pacjentów z wysokim ryzykiem incydentów wieńcowych z powodu istniejącej choroby wieńcowej, cukrzycy, choroby naczyń obwodowych, udaru mózgu lub innej choroby naczyń mózgowych w wywiadzie, ZOCOR 5 mg jest wskazany do:
- Zmniejsz ryzyko całkowitej śmiertelności poprzez zmniejszenie liczby zgonów z powodu CHD.
- Zmniejsz ryzyko zawału mięśnia sercowego i udaru mózgu niezakończonych zgonem.
- Zmniejsz potrzebę zabiegów rewaskularyzacji wieńcowej i niewieńcowej.
Hiperlipidemia
ZOCOR jest wskazany do:
- Zmniejszenie podwyższonego cholesterolu całkowitego (całkowitego C), cholesterolu lipoprotein o niskiej gęstości (LDL-C), apolipoproteiny B (Apo B) i triglicerydów (TG) oraz zwiększenie stężenia cholesterolu lipoprotein o wysokiej gęstości (HDL-C) u pacjentów z pierwotna hiperlipidemia (typ Fredrickson IIa, heterozygotyczna rodzinna i nierodzinna) lub dyslipidemia mieszana (typ Fredrickson IIb).
- Zmniejszenie podwyższonego TG u pacjentów z hipertriglicerydemią (hiperlipidemia typu IV Fredricksona).
- Zmniejszenie podwyższonego TG i VLDL-C u pacjentów z pierwotną dysbetalipoproteinemią (hiperlipidemia Fredricksona typu III).
- Zmniejszenie całkowitego C i LDL-C u pacjentów z homozygotyczną rodzinną hipercholesterolemią (HoFH) jako uzupełnienie innych terapii obniżających stężenie lipidów (np. afereza LDL) lub jeśli takie terapie są niedostępne.
Młodzież z heterozygotyczną hipercholesterolemią rodzinną (HeFH)
ZOCOR jest wskazany jako uzupełnienie diety w celu obniżenia poziomu całkowitego C, LDL-C i Apo B u dorastających chłopców i dziewcząt, którzy są co najmniej rok po pierwszej miesiączce, w wieku 10-17 lat, z HeFH, jeśli po odpowiednia próba terapii dietetycznej, następujące wyniki są obecne:
- Istnieje dodatni wywiad rodzinny dotyczący przedwczesnej choroby sercowo-naczyniowej (CVD) lub
- U młodocianego pacjenta występują dwa lub więcej innych czynników ryzyka CVD.
Minimalnym celem leczenia u dzieci i młodzieży jest osiągnięcie średniego stężenia cholesterolu LDL
Ograniczenia użytkowania
ZOCOR 20 mg nie był badany w warunkach, w których główną nieprawidłowością jest podwyższenie poziomu chylomikronów (tj. hiperlipidemia Fredrickson typu I i V).
DAWKOWANIE I SPOSÓB PODAWANIA
Zalecane dawkowanie
Zwykle zakres dawkowania wynosi od 5 do 40 mg/dzień. U pacjentów z CHD lub z wysokim ryzykiem CHD ZOCOR można rozpocząć jednocześnie z dietą. Zalecana zwykle dawka początkowa to 10 lub 20 mg raz na dobę wieczorem. U pacjentów z wysokim ryzykiem wystąpienia CHD z powodu istniejącej CHD, cukrzycy, choroby naczyń obwodowych, udaru lub innej choroby naczyń mózgowych w wywiadzie zalecana dawka początkowa wynosi 40 mg/dobę. Oznaczenia lipidów należy wykonywać po 4 tygodniach leczenia, a następnie okresowo.
Ograniczone dawkowanie dla 80 mg
Ze względu na zwiększone ryzyko miopatii, w tym rabdomiolizy, szczególnie w pierwszym roku leczenia, stosowanie leku ZOCOR w dawce 80 mg należy ograniczyć do pacjentów, którzy przewlekle przyjmowali symwastatynę w dawce 80 mg (np. przez 12 miesięcy lub dłużej). bez dowodów na toksyczność mięśni [patrz OSTRZEŻENIA I ŚRODKI ].
Pacjenci, którzy obecnie tolerują dawkę 80 mg preparatu ZOCOR, u których konieczne jest rozpoczęcie leczenia lekiem wchodzącym w interakcje, który jest przeciwwskazany lub związany z ograniczeniem dawki symwastatyny, powinni przejść na alternatywną statynę o mniejszym potencjale interakcji lek-lek.
Ze względu na zwiększone ryzyko miopatii, w tym rabdomiolizy, związane z dawką 80 mg ZOCOR 40 mg, pacjenci, którzy nie mogą osiągnąć swojego celu LDL-C przy użyciu dawki 40 mg ZOCOR 5 mg, nie powinni być zwiększani do dawki 80 mg , ale należy zastosować alternatywną terapię obniżającą LDL-C, która zapewnia większe obniżenie LDL-C.
Jednoczesne podawanie z innymi lekami
Pacjenci przyjmujący werapamil, diltiazem lub dronedaron
- Dawka ZOCOR nie powinna przekraczać 10 mg/dobę [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI , oraz FARMAKOLOGIA KLINICZNA ].
Pacjenci przyjmujący amiodaron, amlodypinę lub ranolazynę
- Dawka ZOCOR 10mg nie powinna przekraczać 20 mg/dobę [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI , oraz FARMAKOLOGIA KLINICZNA ].
Pacjenci z homozygotyczną hipercholesterolemią rodzinną
Zalecana dawka to 40 mg/dobę wieczorem [Patrz DAWKOWANIE I SPOSÓB PODAWANIA , Ograniczone dawkowanie dla 80 mg ]. ZOCOR 5 mg powinien być stosowany jako uzupełnienie innych metod leczenia hipolipemizującego (np. aferezy LDL) u tych pacjentów lub jeśli takie leczenie jest niedostępne.
Ekspozycja na symwastatynę jest w przybliżeniu podwojona przy jednoczesnym stosowaniu lomitapidu; dlatego dawkę ZOCOR należy zmniejszyć o 50%, jeśli rozpoczyna się leczenie lomitapidem. Dawka ZOCOR 5 mg nie powinna przekraczać 20 mg/dobę (lub 40 mg/dobę w przypadku pacjentów, którzy wcześniej przyjmowali ZOCOR 80 mg/dobę przewlekle, np. przez 12 miesięcy lub dłużej, bez objawów toksyczności mięśniowej) podczas przyjmowania lomitapidu.
Młodzież (10-17 lat) z heterozygotyczną hipercholesterolemią rodzinną
Zalecana zwykle dawka początkowa to 10 mg raz na dobę wieczorem. Zalecany zakres dawkowania wynosi od 10 do 40 mg/dzień; maksymalna zalecana dawka wynosi 40 mg/dobę. Dawki należy dobierać indywidualnie zgodnie z zalecanym celem terapii [patrz Wytyczne panelu pediatrycznego NCEP1 oraz Studia kliniczne ]. Korekty należy dokonywać w odstępach co 4 tygodnie lub więcej.
Pacjenci z niewydolnością nerek
Ponieważ ZOCOR 5 mg nie podlega znaczącemu wydalaniu przez nerki, modyfikacja dawkowania nie powinna być konieczna u pacjentów z łagodnymi lub umiarkowanymi zaburzeniami czynności nerek. Należy jednak zachować ostrożność podając ZOCOR 20 mg pacjentom z ciężkimi zaburzeniami czynności nerek; takich pacjentów należy rozpocząć od dawki 5 mg/dobę i ściśle monitorować [patrz OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
JAK DOSTARCZONE
Formy dawkowania i mocne strony
- Tabletki ZOCOR 5 mg to płowożółte, owalne tabletki powlekane oznaczone kodem MSD 726 po jednej stronie i ZOCOR 5 po drugiej.
- Tabletki ZOCOR 10 mg to brzoskwiniowe, owalne, powlekane tabletki, oznaczone kodem MSD 735 po jednej stronie i gładkie po drugiej.
- Tabletki ZOCOR 20 mg to beżowe, owalne tabletki powlekane, oznaczone kodem MSD 740 po jednej stronie i gładkie po drugiej.
- Tabletki ZOCOR 40 mg to ceglastoczerwone, owalne tabletki powlekane, oznaczone kodem MSD 749 po jednej stronie i gładkie po drugiej.
- Tabletki ZOCOR 80 mg to ceglastoczerwone tabletki powlekane w kształcie kapsułki, oznaczone kodem 543 po jednej stronie i 80 po drugiej.
Składowania i stosowania
Nr 8146 - Tabletki ZOCOR 10 mg to brzoskwiniowe, owalne tabletki powlekane oznaczone kodem MSD 735 po jednej stronie i gładkie po drugiej. Dostarczane są w następujący sposób:
NDC 0006-0735-31 szt. butelek 30 NDC 0006-0735-54 szt. butelek po 90 sztuk.
Nr 8147 - Tabletki ZOCOR 20 mg to beżowe, owalne tabletki powlekane, oznaczone kodem MSD 740 po jednej stronie i gładkie po drugiej. Dostarczane są w następujący sposób:
NDC 0006-0740-31 szt. butelek 30 NDC 0006-0740-54 szt. butelek po 90 sztuk.
Nr 8148 - Tabletki ZOCOR 40 mg to ceglastoczerwone, owalne tabletki powlekane oznaczone kodem MSD 749 po jednej stronie i gładkie po drugiej. Dostarczane są w następujący sposób:
NDC 0006-0749-31 szt. butelek 30 NDC 0006-0749-54 szt. butelek po 90 sztuk.
Nr 6577 - Tabletki ZOCOR 80 mg to ceglaste tabletki powlekane w kształcie kapsułki, oznaczone kodem 543 po jednej stronie i 80 po drugiej. Dostarczane są w następujący sposób:
NDC 0006-0543-31 szt. butelek 30 NDC 0006-0543-54 szt. butelek po 90 szt.
Magazynowanie
Przechowywać w temperaturze 5-30°C (41-86°F).
1National Cholesterol Education Program (NCEP): Najważniejsze informacje z raportu Panelu Ekspertów ds. Poziomów Cholesterolu we Krwi u Dzieci i Młodzieży. Pediatria. 89(3):495-501. 1992.
Producent: Merck Sharp & Dohme Ltd. Cramlington, Northumberland, Wielka Brytania NE23 3JU. Poprawiono: wrzesień 2020 r.
SKUTKI UBOCZNE
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
kontrolowanych badaniach klinicznych przed wprowadzeniem do obrotu i ich otwartych rozszerzeniach (2423 pacjentów z medianą czasu obserwacji około 18 miesięcy), 1,4% pacjentów przerwało leczenie z powodu działań niepożądanych. Najczęstszymi działaniami niepożądanymi, które doprowadziły do przerwania leczenia były: zaburzenia żołądkowo-jelitowe (0,5%), bóle mięśni (0,1%) i bóle stawów (0,1%). Najczęściej zgłaszanymi działaniami niepożądanymi (częstość ≥ 5%) w kontrolowanych badaniach klinicznych symwastatyną były: infekcje górnych dróg oddechowych (9,0%), ból głowy (7,4%), ból brzucha (7,3%), zaparcia (6,6%) i nudności (5,4 %).
Skandynawskie badanie przeżycia Simwastatyny
W 4S obejmującym 4444 (przedział wiekowy 35-71 lat, 19% kobiet, 100% rasy kaukaskiej) leczonych 20-40 mg/dobę ZOCOR (n=2221) lub placebo (n=2223) przez medianę 5,4 roku reakcje zgłaszane u ≥2% pacjentów i częściej niż placebo przedstawiono w Tabeli 2.
Badanie ochrony serca
badaniu ochrony serca (HPS) z udziałem 20 536 pacjentów (przedział wiekowy 40-80 lat, 25% kobiet, 97% rasy kaukaskiej, 3% innych ras) leczonych preparatem ZOCOR 40 mg/dobę (n=10 269) lub placebo (n= 10 267) w ciągu średnio 5 lat odnotowano tylko poważne działania niepożądane i przerwanie leczenia z powodu jakichkolwiek działań niepożądanych. Wskaźniki przerwania leczenia z powodu działań niepożądanych wynosiły 4,8% u pacjentów leczonych preparatem ZOCOR 10 mg w porównaniu z 5,1% u pacjentów otrzymujących placebo. Częstość występowania miopatii/rabdomiolizy wynosiła
Inne badania kliniczne
badaniu klinicznym, w którym 12 064 pacjentów z zawałem mięśnia sercowego w wywiadzie było leczonych ZOCOR (średni okres obserwacji 6,7 roku), częstość występowania miopatii (definiowanej jako niewyjaśnione osłabienie mięśni lub ból przy aktywności kinazy kreatynowej [CK] w surowicy >10 razy górna granica normy [GGN]) u pacjentów otrzymujących 80 mg/dobę wynosiła około 0,9% w porównaniu z 0,02% u pacjentów otrzymujących 20 mg/dobę. Częstość występowania rabdomiolizy (definiowanej jako miopatia z CK >40 razy GGN) u pacjentów otrzymujących 80 mg/dobę wynosiła około 0,4% w porównaniu z 0% u pacjentów otrzymujących 20 mg/dobę. Częstość występowania miopatii, w tym rabdomiolizy, była najwyższa w pierwszym roku, a następnie znacznie spadała w kolejnych latach leczenia. W tym badaniu pacjenci byli dokładnie monitorowani i niektóre wchodzące w interakcje produkty lecznicze zostały wykluczone.
Inne działania niepożądane zgłaszane w badaniach klinicznych to: biegunka, wysypka, niestrawność, wzdęcia i astenia.
Testy laboratoryjne
Odnotowano wyraźny, utrzymujący się wzrost aktywności aminotransferaz wątrobowych [patrz OSTRZEŻENIA I ŚRODKI ]. Donoszono również o podwyższonej aktywności fosfatazy alkalicznej i transpeptydazy γ-glutamylowej. Około 5% pacjentów miało podwyższenie poziomu CK 3 lub więcej razy w stosunku do normalnej wartości w jednym lub kilku przypadkach. Można to przypisać niesercowej frakcji CK. [Widzieć OSTRZEŻENIA I ŚRODKI ]
Pacjenci w wieku młodzieńczym (w wieku 10-17 lat)
W 48-tygodniowym, kontrolowanym badaniu z udziałem dorastających chłopców i dziewcząt, którzy byli co najmniej rok po pierwszej miesiączce, w wieku 10-17 lat (43,4% kobiet, 97,7% rasy kaukaskiej, 1,7% Latynosów, 0,6% osób wielorasowych) z heterozygotyczną hipercholesterolemią rodzinną (n=175), otrzymujących placebo lub ZOCOR (10-40 mg na dobę), najczęstszymi działaniami niepożądanymi obserwowanymi w obu grupach były zakażenia górnych dróg oddechowych, ból głowy, ból brzucha i nudności [patrz Używaj w określonych populacjach oraz Studia kliniczne ].
Doświadczenie postmarketingowe
Ponieważ poniższe reakcje są zgłaszane dobrowolnie z populacji o niepewnej wielkości, generalnie nie jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek. Następujące dodatkowe działania niepożądane zostały zidentyfikowane podczas stosowania symwastatyny po dopuszczeniu do obrotu: świąd, łysienie, różne zmiany skórne (np. guzki, przebarwienia, suchość skóry/błon śluzowych, zmiany włosów/paznokci), zawroty głowy, skurcze mięśni, ból mięśni , zapalenie trzustki, parestezje, neuropatia obwodowa, wymioty, niedokrwistość, zaburzenia erekcji, śródmiąższowa choroba płuc, rabdomioliza, zapalenie wątroby/żółtaczka, niewydolność wątroby prowadząca do zgonu i depresja.
Istnieją rzadkie doniesienia o martwiczej miopatii o podłożu immunologicznym, związanej ze stosowaniem statyn [patrz OSTRZEŻENIA I ŚRODKI ].
Rzadko zgłaszano pozorny zespół nadwrażliwości, który obejmował niektóre z następujących cech: anafilaksja, obrzęk naczynioruchowy, zespół toczniopodobny, zespół wielomięśniowy, zapalenie skórno-mięśniowe, zapalenie naczyń, plamica, małopłytkowość, leukopenia, niedokrwistość hemolityczna, dodatni wynik ANA, wzrost ESR, eozynofilia zapalenie stawów, ból stawów, pokrzywka, osłabienie, nadwrażliwość na światło, gorączka, dreszcze, uderzenia gorąca, złe samopoczucie, duszność, toksyczna nekroliza naskórka, rumień wielopostaciowy, w tym zespół Stevensa-Johnsona.
Po wprowadzeniu do obrotu rzadko zgłaszano zaburzenia funkcji poznawczych (np. utrata pamięci, zapominanie, amnezja, zaburzenia pamięci, splątanie) związane ze stosowaniem statyn. Te problemy poznawcze zostały zgłoszone dla wszystkich statyn. Zgłoszenia na ogół nie są poważne i ustępują po odstawieniu statyn, ze zmiennym czasem do wystąpienia objawów (1 dzień do lat) i ustąpienia objawów (mediana 3 tygodnie).
INTERAKCJE Z LEKAMI
Silne inhibitory CYP3A4, cyklosporyna lub danazol
Silne inhibitory CYP3A4: Symwastatyna, podobnie jak kilka innych inhibitorów reduktazy HMG-CoA, jest substratem CYP3A4. Symwastatyna jest metabolizowana przez CYP3A4, ale nie wykazuje działania hamującego CYP3A4; dlatego nie oczekuje się, aby wpływał na stężenia innych leków metabolizowanych przez CYP3A4 w osoczu.
Podwyższony poziom aktywności hamującej reduktazę HMG-CoA w osoczu zwiększa ryzyko miopatii i rabdomiolizy, szczególnie przy wyższych dawkach symwastatyny. [Widzieć OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ] Jednoczesne stosowanie leków oznaczonych jako silnie hamujące CYP3A4 jest przeciwwskazane [patrz PRZECIWWSKAZANIA ]. Jeśli leczenie itrakonazolem, ketokonazolem, pozakonazolem, worykonazolem, erytromycyną, klarytromycyną lub telitromycyną jest nieuniknione, leczenie symwastatyną należy przerwać na czas leczenia.
Cyklosporyna lub Danazol: Jednoczesne podawanie cyklosporyny lub danazolu zwiększa ryzyko miopatii, w tym rabdomiolizy. Dlatego jednoczesne stosowanie tych leków jest przeciwwskazane [patrz PRZECIWWSKAZANIA , OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
Leki obniżające poziom lipidów, które podawane same mogą powodować miopatię
Gemfibrozyl
Przeciwwskazane z symwastatyną [patrz PRZECIWWSKAZANIA oraz OSTRZEŻENIA I ŚRODKI ].
Inne Fibraty
Należy zachować ostrożność przepisując symwastatynę [patrz OSTRZEŻENIA I ŚRODKI ].
Amiodaron, dronedaron, ranolazyna lub blokery kanału wapniowego
Ryzyko miopatii, w tym rabdomiolizy, zwiększa się w przypadku jednoczesnego podawania amiodaronu, dronedaronu, ranolazyny lub blokerów kanału wapniowego, takich jak werapamil, diltiazem lub amlodypina [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz OSTRZEŻENIA I ŚRODKI , oraz Tabela 3 in FARMAKOLOGIA KLINICZNA ].
Niacyna
Przypadki miopatii/rabdomiolizy obserwowano podczas jednoczesnego stosowania symwastatyny z produktami zawierającymi niacynę w dawkach modyfikujących lipidy (≥1 g/dobę niacyny). Ryzyko miopatii jest większe u pacjentów chińskich. W badaniu klinicznym (mediana czasu obserwacji 3,9 roku) z udziałem pacjentów z wysokim ryzykiem chorób sercowo-naczyniowych i dobrze kontrolowanymi stężeniami LDL-C, którym podawano symwastatynę w dawce 40 mg/dobę z lub bez ezetymibu w dawce 10 mg/dobę, nie stwierdzono dodatkowych korzyści w sercowo-naczyniowych po dodaniu dawek modyfikujących lipidy (≥1 g/dobę) niacyny. Jednoczesne podawanie ZOCOR z dawkami modyfikującymi lipidy (≥1 g/dobę) niacyny nie jest zalecane u pacjentów chińskich. Nie wiadomo, czy to ryzyko dotyczy innych pacjentów pochodzenia azjatyckiego [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
Digoksyna
W jednym badaniu jednoczesne podawanie digoksyny i symwastatyny powodowało nieznaczne zwiększenie stężenia digoksyny w osoczu. Pacjenci przyjmujący digoksynę powinni być odpowiednio monitorowani podczas rozpoczynania stosowania symwastatyny [patrz FARMAKOLOGIA KLINICZNA ].
Antykoagulanty kumaryny
dwóch badaniach klinicznych, jedno z udziałem zdrowych ochotników, a drugie z udziałem pacjentów z hipercholesterolemią, symwastatyna w dawce 20-40 mg/dobę nieznacznie nasilała działanie leków przeciwzakrzepowych kumaryny: czas protrombinowy, zgłaszany jako międzynarodowy współczynnik znormalizowany (INR), wzrósł z wartości początkowej 1,7 do 1,8 i od 2,6 do 3,4 odpowiednio w badaniach na ochotnikach i pacjentach. W przypadku innych statyn, klinicznie widoczne krwawienie i (lub) wydłużenie czasu protrombinowego zgłoszono u kilku pacjentów przyjmujących jednocześnie leki przeciwzakrzepowe z grupy kumaryny. U takich pacjentów czas protrombinowy należy określić przed rozpoczęciem leczenia symwastatyną i wystarczająco często podczas wczesnego leczenia, aby nie doszło do istotnej zmiany czasu protrombinowego. Po udokumentowaniu stabilnego czasu protrombinowego można monitorować czas protrombinowy w odstępach zwykle zalecanych u pacjentów przyjmujących leki przeciwzakrzepowe z grupy kumaryny. Jeśli dawka symwastatyny zostanie zmieniona lub przerwana, należy powtórzyć tę samą procedurę. Terapia symwastatyną nie wiązała się z krwawieniem ani zmianami czasu protrombinowego u pacjentów nieprzyjmujących leków przeciwzakrzepowych.
Kolchicyna
Podczas jednoczesnego stosowania symwastatyny z kolchicyną zgłaszano przypadki miopatii, w tym rabdomiolizy, dlatego należy zachować ostrożność przepisując symwastatynę z kolchicyną.
Daptomycyna
Zgłaszano przypadki rabdomiolizy po podaniu symwastatyny z daptomycyną. Zarówno symwastatyna, jak i daptomycyna, podawane w monoterapii, mogą powodować miopatię i rabdomiolizę, a jednoczesne podawanie może zwiększyć ryzyko miopatii i rabdomiolizy. Tymczasowo zawiesić ZOCOR u pacjentów przyjmujących daptomycynę [patrz OSTRZEŻENIA I ŚRODKI ].
OSTRZEŻENIA
Zawarte jako część "ŚRODKI OSTROŻNOŚCI" Sekcja
ŚRODKI OSTROŻNOŚCI
Miopatia/rabdomioliza
Symwastatyna czasami powoduje miopatię objawiającą się bólem mięśni, tkliwością lub osłabieniem, przy czym kinaza kreatynowa (CK) przekracza dziesięciokrotnie górną granicę normy (GGN). Miopatia czasami przybiera postać rabdomiolizy z ostrą niewydolnością nerek wtórną do mioglobinurii lub bez niej i zdarzają się rzadkie przypadki zgonów. Zwiększone stężenie symwastatyny i kwasu symwastatyny w osoczu zwiększa ryzyko miopatii. Czynnikami predysponującymi do miopatii są zaawansowany wiek (≥65 lat), płeć żeńska, niekontrolowana niedoczynność tarczycy i zaburzenia czynności nerek. Chińscy pacjenci mogą być narażeni na zwiększone ryzyko miopatii [patrz Używaj w określonych populacjach ].
Ryzyko miopatii, w tym rabdomiolizy, jest zależne od dawki. bazie danych badań klinicznych, w których 41 413 pacjentów było leczonych preparatem ZOCOR 10 mg, z których 24 747 (około 60%) zostało włączonych do badań z medianą okresu obserwacji wynoszącą co najmniej 4 lata, częstość występowania miopatii wynosiła około 0,03% i 0,08% odpowiednio przy 20 i 40 mg/dzień. Częstość występowania miopatii po podaniu 80 mg (0,61%) była nieproporcjonalnie wyższa niż obserwowana przy niższych dawkach. W tych badaniach pacjenci byli dokładnie monitorowani i wykluczono niektóre wchodzące w interakcje produkty lecznicze.
badaniu klinicznym, w którym 12 064 pacjentów z zawałem mięśnia sercowego w wywiadzie było leczonych ZOCOR (średni okres obserwacji 6,7 roku), częstość występowania miopatii (definiowanej jako niewyjaśnione osłabienie mięśni lub ból przy aktywności kinazy kreatynowej [CK] w surowicy >10 razy górna granica normy [GGN]) u pacjentów otrzymujących 80 mg/dobę wynosiła około 0,9% w porównaniu z 0,02% u pacjentów otrzymujących 20 mg/dobę. Częstość występowania rabdomiolizy (definiowanej jako miopatia z CK >40 razy GGN) u pacjentów otrzymujących 80 mg/dobę wynosiła około 0,4% w porównaniu z 0% u pacjentów otrzymujących 20 mg/dobę. Częstość występowania miopatii, w tym rabdomiolizy, była najwyższa w pierwszym roku, a następnie znacznie spadała w kolejnych latach leczenia. W tym badaniu pacjenci byli dokładnie monitorowani i niektóre wchodzące w interakcje produkty lecznicze zostały wykluczone.
Ryzyko miopatii, w tym rabdomiolizy, jest większe u pacjentów przyjmujących symwastatynę w dawce 80 mg w porównaniu z innymi terapiami statynami o podobnej lub większej skuteczności obniżania LDL-C oraz w porównaniu z niższymi dawkami simwastatyny. Dlatego też dawkę 80 mg preparatu ZOCOR należy stosować wyłącznie u pacjentów hospitalizowanych, którzy przewlekle (np. przez 12 miesięcy lub dłużej) przyjmowali symwastatynę w dawce 80 mg bez objawów toksyczności mięśniowej. [Widzieć DAWKOWANIE I SPOSÓB PODAWANIA , Ograniczone dawkowanie dla 80 mg ]. Jeśli jednak u pacjenta, który obecnie toleruje dawkę 80 mg preparatu ZOCOR, konieczne jest rozpoczęcie leczenia przeciwwskazanego lub związanego z ograniczeniem dawki symwastatyny, należy go zmienić na alternatywną statynę o mniejszym potencjale interakcja lek-lek. Pacjentów należy poinformować o zwiększonym ryzyku miopatii, w tym rabdomiolizy, oraz o niezwłocznym zgłaszaniu wszelkich niewyjaśnionych bólów, tkliwości lub osłabienia mięśni. W przypadku wystąpienia objawów leczenie należy natychmiast przerwać. [Widzieć Miopatia martwicza o podłożu immunologicznym ]
Wszystkich pacjentów rozpoczynających leczenie preparatem ZOCOR 20 mg lub pacjentów, u których zwiększa się dawkę preparatu ZOCOR, należy poinformować o ryzyku wystąpienia miopatii, w tym rabdomiolizy, i poinformować o konieczności szybkiego zgłaszania wszelkich niewyjaśnionych bólów, tkliwości lub osłabienia mięśni, szczególnie jeśli towarzyszy im złe samopoczucie lub gorączka lub objawy ze strony mięśni a objawy utrzymują się po odstawieniu ZOCOR. Terapię ZOCOR należy natychmiast przerwać w przypadku rozpoznania lub podejrzenia miopatii. większości przypadków objawy mięśniowe i wzrost CK ustąpiły po natychmiastowym przerwaniu leczenia. Okresowe oznaczanie CK można rozważyć u pacjentów rozpoczynających leczenie preparatem ZOCOR 5 mg lub u których zwiększa się dawkę, ale nie ma pewności, że takie monitorowanie zapobiegnie miopatii.
Wielu pacjentów, u których rozwinęła się rabdomioliza podczas leczenia simwastatyną, miało skomplikowaną historię medyczną, w tym niewydolność nerek, zwykle będącą konsekwencją długotrwałej cukrzycy. Tacy pacjenci zasługują na dokładniejsze monitorowanie. Leczenie preparatem ZOCOR należy przerwać w przypadku wystąpienia znacznie podwyższonego stężenia CPK lub rozpoznania lub podejrzenia miopatii. Terapię ZOCOR należy również czasowo wstrzymać u każdego pacjenta z ostrym lub ciężkim stanem predysponującym do rozwoju niewydolności nerek wtórnej do rabdomiolizy, np. posocznicy; niedociśnienie; poważna operacja; uraz; ciężkie zaburzenia metaboliczne, endokrynologiczne lub elektrolitowe; lub niekontrolowana padaczka.
Interakcje leków
Zwiększone stężenie symwastatyny i kwasu symwastatyny w osoczu zwiększa ryzyko miopatii i rabdomiolizy. Symwastatyna jest metabolizowana przez izoformę 3A4 cytochromu P450. Niektóre leki hamujące ten szlak metaboliczny mogą zwiększać stężenie symwastatyny w osoczu i zwiększać ryzyko miopatii. Należą do nich itrakonazol, ketokonazol, posakonazol, worykonazol, antybiotyki makrolidowe erytromycyna i klarytromycyna oraz antybiotyk ketolidowy telitromycyna, inhibitory proteazy HIV, boceprewir, telaprewir, lek przeciwdepresyjny nefazodon, produkty zawierające kobicystat [patrz lub FARMAKOLOGIA KLINICZNA ]. Połączenie tych leków z simwastatyną jest przeciwwskazane. Jeśli krótkotrwałe leczenie silnymi inhibitorami CYP3A4 jest nieuniknione, leczenie symwastatyną należy przerwać na czas leczenia [patrz PRZECIWWSKAZANIA oraz INTERAKCJE Z LEKAMI ].
Jednoczesne stosowanie symwastatyny z gemfibrozylem, cyklosporyną lub danazolem jest przeciwwskazane [patrz PRZECIWWSKAZANIA oraz INTERAKCJE Z LEKAMI ].
Należy zachować ostrożność przepisując inne fibraty z simwastatyną, ponieważ leki te mogą powodować miopatię, gdy są podawane w monoterapii, a ryzyko jest zwiększone, gdy są podawane jednocześnie [patrz INTERAKCJE Z LEKAMI ].
Podczas jednoczesnego stosowania symwastatyny z kolchicyną zgłaszano przypadki miopatii, w tym rabdomiolizy, dlatego należy zachować ostrożność przepisując symwastatynę z kolchicyną [patrz INTERAKCJE Z LEKAMI ].
Korzyści ze skojarzonego stosowania symwastatyny z następującymi lekami należy dokładnie rozważyć w stosunku do potencjalnego ryzyka związanego ze skojarzeniem: inne leki hipolipemizujące (fibraty lub u pacjentów z HoFH lomitapid), amiodaron, dronedaron, werapamil, diltiazem, amlodypina, lub ranolazyna [Patrz DAWKOWANIE I SPOSÓB PODAWANIA , INTERAKCJE Z LEKAMI ].
Przypadki miopatii, w tym rabdomiolizy, obserwowano podczas jednoczesnego stosowania symwastatyny z modyfikującymi stężenie lipidów dawkami (≥1 g/dobę niacyny) produktów zawierających niacynę [patrz INTERAKCJE Z LEKAMI ].
Zgłaszano przypadki rabdomiolizy po podaniu symwastatyny z daptomycyną. Tymczasowo zawiesić ZOCOR u pacjentów przyjmujących daptomycynę [patrz INTERAKCJE Z LEKAMI ].
Zalecenia dotyczące przepisywania leków wchodzących w interakcje zostały podsumowane w Tabeli 1 [patrz także DAWKOWANIE I SPOSÓB PODAWANIA , INTERAKCJE Z LEKAMI , FARMAKOLOGIA KLINICZNA ].
Miopatia martwicza o podłożu immunologicznym
Istnieją rzadkie doniesienia o miopatii martwiczej o podłożu immunologicznym (IMNM), autoimmunologicznej miopatii związanej ze stosowaniem statyn. IMNM charakteryzuje się: osłabieniem mięśni proksymalnych oraz podwyższoną aktywnością kinazy kreatynowej w surowicy, która utrzymuje się pomimo przerwania leczenia statynami; pozytywne przeciwciało przeciw reduktazie HMG CoA; biopsja mięśnia wykazująca martwiczą miopatię; i poprawa za pomocą środków immunosupresyjnych. Konieczne mogą być dodatkowe badania nerwowo-mięśniowe i serologiczne. Może być konieczne leczenie środkami immunosupresyjnymi. Przed rozpoczęciem stosowania innej statyny należy dokładnie rozważyć ryzyko IMNM. Jeśli leczenie rozpoczyna się od innej statyny, należy monitorować objawy przedmiotowe i podmiotowe IMNM.
Dysfunkcja wątroby
Trwałe zwiększenie aktywności aminotransferaz w surowicy (ponad trzykrotność wartości górnej granicy normy) wystąpiło u około 1% pacjentów, którzy otrzymywali symwastatynę w badaniach klinicznych. Gdy leczenie farmakologiczne zostało przerwane lub przerwane u tych pacjentów, poziom transaminaz zwykle spadał powoli do poziomu sprzed leczenia. Wzrosty nie były związane z żółtaczką ani innymi klinicznymi oznakami lub objawami. Nie było dowodów na nadwrażliwość.
W skandynawskim badaniu przeżycia Simvastatin (4S) [patrz Studia kliniczne ], liczba pacjentów z więcej niż jednym podwyższeniem transaminazy do >3X GGN w trakcie badania nie różniła się istotnie między grupami simwastatyny i placebo (14 [0,7%] vs. 12 [0,6%]). Podwyższone transaminazy spowodowały przerwanie terapii 8 pacjentów w grupie symwastatyny (n=2221) i 5 w grupie placebo (n=2223). Spośród 1 986 pacjentów leczonych symwastatyną w 4S z prawidłowymi testami czynności wątroby (LFT) na początku badania, u 8 (0,4%) wystąpiło kolejne zwiększenie LFT do >3X GGN i/lub zostało przerwanych z powodu zwiększenia aktywności aminotransferaz w ciągu 5,4 roku (mediana okresu obserwacji ) badania. Spośród tych 8 pacjentów, 5 początkowo rozwinęło te nieprawidłowości w ciągu pierwszego roku. Wszyscy pacjenci w tym badaniu otrzymali dawkę początkową 20 mg simwastatyny; 37% zmiareczkowano do 40 mg.
2 kontrolowanych badaniach klinicznych z udziałem 1105 pacjentów, 12-miesięczna częstość występowania utrzymującego się wzrostu aktywności aminotransferaz wątrobowych, niezależnie od związku z lekiem, wynosiła odpowiednio 0,9% i 2,1% przy dawce 40 mg i 80 mg. U żadnego pacjenta nie wystąpiły trwałe zaburzenia czynności wątroby po pierwszych 6 miesiącach leczenia daną dawką.
Zaleca się wykonanie testów czynności wątroby przed rozpoczęciem leczenia, a następnie, gdy jest to wskazane klinicznie. Po wprowadzeniu produktu do obrotu odnotowano rzadkie przypadki niewydolności wątroby zakończonej zgonem lub niezakończonej zgonem u pacjentów przyjmujących statyny, w tym symwastatynę. Jeśli podczas leczenia preparatem ZOCOR 5 mg wystąpi poważne uszkodzenie wątroby z objawami klinicznymi i/lub hiperbilirubinemią lub żółtaczką, należy niezwłocznie przerwać leczenie. Jeśli nie zostanie znaleziona alternatywna etiologia, nie należy ponownie uruchamiać ZOCOR. Należy pamiętać, że ALT może pochodzić z mięśni, dlatego wzrost ALT wraz z CK może wskazywać na miopatię [patrz Miopatia/rabdomioliza ].
Lek należy stosować ostrożnie u pacjentów, którzy spożywają znaczne ilości alkoholu i (lub) przebyli chorobę wątroby. Aktywne choroby wątroby lub niewyjaśniony wzrost aktywności aminotransferaz stanowią przeciwwskazania do stosowania symwastatyny.
Po leczeniu symwastatyną zgłaszano umiarkowane (mniej niż 3x GGN) zwiększenie aktywności aminotransferaz w surowicy. Zmiany te pojawiły się wkrótce po rozpoczęciu leczenia simwastatyną, często były przemijające, nie towarzyszyły im żadne objawy i nie wymagały przerwania leczenia.
Funkcja hormonalna
W przypadku inhibitorów reduktazy HMG-CoA, w tym ZOCOR, zgłaszano wzrost stężenia HbA1c i stężenia glukozy w surowicy na czczo.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
72-tygodniowym badaniu rakotwórczości myszom podawano dobowe dawki simwastatyny 25, 100 i 400 mg/kg masy ciała, co skutkowało średnim poziomem leku w osoczu około 1, 4 i 8 razy wyższym niż średni poziom leku w ludzkim osoczu. (jako całkowita aktywność hamująca na podstawie AUC) po doustnym podaniu dawki 80 mg. Rak wątroby był znacząco zwiększony u kobiet otrzymujących dużą dawkę oraz u mężczyzn otrzymujących średnią i dużą dawkę, z maksymalną częstością występowania 90% u mężczyzn. Częstość występowania gruczolaków wątroby była znacznie zwiększona u kobiet otrzymujących średnią i wysoką dawkę. Leczenie farmakologiczne znacząco zwiększyło również częstość występowania gruczolaków płuc u mężczyzn i kobiet otrzymujących średnie i wysokie dawki. Gruczolaki gruczołu Hardera (gruczołu oka gryzoni) były znacznie wyższe u myszy otrzymujących duże dawki niż u myszy kontrolnych. Nie zaobserwowano żadnych dowodów działania rakotwórczego przy dawce 25 mg/kg/dobę.
oddzielnym 92-tygodniowym badaniu rakotwórczości u myszy przy dawkach do 25 mg/kg/dobę nie zaobserwowano dowodów działania rakotwórczego (średnie stężenia leku w osoczu były 1 razy wyższe niż u ludzi otrzymujących 80 mg symwastatyny, mierzone na podstawie AUC).
W dwuletnim badaniu na szczurach otrzymujących dawkę 25 mg/kg/dobę stwierdzono statystycznie istotny wzrost częstości występowania gruczolaków pęcherzykowych tarczycy u samic szczurów narażonych na około 11-krotnie wyższe stężenia symwastatyny niż u ludzi otrzymujących 80 mg symwastatyny (jak mierzone przez AUC).
Drugie dwuletnie badanie rakotwórczości na szczurach z dawkami 50 i 100 mg/kg/dobę dało gruczolaki i raki wątrobowokomórkowe (u samic szczurów przy obu dawkach iu samców przy 100 mg/kg/dobę). Gruczolaki komórek pęcherzykowych tarczycy były zwiększone u mężczyzn i kobiet po obu dawkach; rak komórek pęcherzykowych tarczycy był zwiększony u kobiet przy dawce 100 mg/kg/dobę. Zwiększona częstość występowania nowotworów tarczycy wydaje się być spójna z wynikami innych statyn. Te poziomy leczenia reprezentowały poziomy leku w osoczu (AUC) około 7 i 15 razy (mężczyźni) oraz 22 i 25 razy (kobiety) średnią ekspozycję na lek w ludzkim osoczu po 80 mg dziennej dawce.
Nie zaobserwowano dowodów na mutagenność w teście mutagenności drobnoustrojów (Ames) z lub bez aktywacji metabolicznej wątroby szczura lub myszy. Ponadto nie odnotowano dowodów na uszkodzenie materiału genetycznego w teście elucji alkalicznej in vitro z użyciem hepatocytów szczura, badaniu postępującej mutacji komórek ssaków V-79, badaniu aberracji chromosomowych in vitro w komórkach CHO lub teście aberracji chromosomowych in vivo w szpiku kostnym myszy.
Obserwowano zmniejszenie płodności u samców szczurów leczonych symwastatyną przez 34 tygodnie w dawce 25 mg/kg masy ciała (4-krotność maksymalnego poziomu narażenia u ludzi, na podstawie AUC, u pacjentów otrzymujących 80 mg/dobę); jednak tego efektu nie zaobserwowano podczas kolejnego badania płodności, w którym symwastatynę podawano w tej samej dawce samcom szczurów przez 11 tygodni (cały cykl spermatogenezy, w tym dojrzewanie najądrza). Nie zaobserwowano mikroskopijnych zmian w jądrach szczurów z obu badań. Przy dawce 180 mg/kg/dobę (co daje poziomy narażenia 22 razy wyższe niż u ludzi przyjmujących 80 mg/dobę w oparciu o powierzchnię, mg/m2), zaobserwowano zwyrodnienie kanalików nasiennych (martwicę i utratę nabłonka spermatogennego). U psów zaobserwowano zanik jąder związany z lekiem, zmniejszoną spermatogenezę, zwyrodnienie spermatocytów i tworzenie komórek olbrzymich przy dawce 10 mg/kg/dobę (około 2-krotność ekspozycji u ludzi, w oparciu o AUC, przy 80 mg/dobę). Znaczenie kliniczne tych wyników jest niejasne.
Używaj w określonych populacjach
Ciąża
Ciąża Kategoria X [Patrz PRZECIWWSKAZANIA ]
ZOCOR jest przeciwwskazany u kobiet, które są w ciąży lub mogą zajść w ciążę. Leki obniżające poziom lipidów nie przynoszą żadnych korzyści w czasie ciąży, ponieważ cholesterol i jego pochodne są potrzebne do prawidłowego rozwoju płodu. Miażdżyca jest procesem przewlekłym, a odstawienie leków hipolipemizujących w czasie ciąży powinno mieć niewielki wpływ na odległe wyniki leczenia pierwotnej hipercholesterolemii. Nie ma odpowiednich i dobrze kontrolowanych badań dotyczących stosowania leku ZOCOR w czasie ciąży; jednak istnieją rzadkie doniesienia o wadach wrodzonych u niemowląt narażonych na statyny w macicy. Badania rozrodczości symwastatyny na zwierzętach u szczurów i królików nie wykazały działania teratogennego. Poziom cholesterolu i trójglicerydów w surowicy wzrasta podczas normalnej ciąży, a cholesterol lub pochodne cholesterolu są niezbędne do rozwoju płodu. Ponieważ statyny zmniejszają syntezę cholesterolu i prawdopodobnie syntezę innych substancji biologicznie czynnych pochodzących z cholesterolu, ZOCOR może powodować uszkodzenie płodu po podaniu kobiecie w ciąży. Jeśli ZOCOR 5 mg jest stosowany w okresie ciąży lub jeśli pacjentka zajdzie w ciążę podczas przyjmowania tego leku, pacjentkę należy poinformować o potencjalnym zagrożeniu dla płodu.
Istnieją rzadkie doniesienia o wadach wrodzonych po wewnątrzmacicznej ekspozycji na statyny. W przeglądzie2 około 100 prospektywnie obserwowanych ciąż u kobiet narażonych na symwastatynę lub inne statyny o podobnej strukturze, częstość występowania wad wrodzonych, poronień samoistnych i zgonów/urodzeń martwych płodów nie przekraczała oczekiwanych w populacji ogólnej. Jednak badanie było w stanie wykluczyć jedynie 3- do 4-krotne zwiększenie ryzyka wad wrodzonych w stosunku do wskaźnika podstawowego. W 89% tych przypadków leczenie farmakologiczne rozpoczęto przed zajściem w ciążę i przerwano w pierwszym trymestrze po stwierdzeniu ciąży.
Symwastatyna nie wykazywała działania teratogennego u szczurów i królików w dawkach (odpowiednio 25, 10 mg/kg/dobę), które powodowały 3-krotną ekspozycję u ludzi w przeliczeniu na mg/m2 powierzchni. Jednak w badaniach z inną statyną o podobnej strukturze, u szczurów i myszy obserwowano wady rozwojowe szkieletu.
Manson, JM, Freyssinges, C., Ducrocq, MB, Stephenson, WP, Nadzór postmarketingowy nad ekspozycją na lowastatynę i symwastatynę podczas ciąży, Toksykologia reprodukcyjna, 10(6):439-446, 1996.
Kobietom w wieku rozrodczym, które z powodu zaburzeń lipidowych wymagają leczenia preparatem ZOCOR 5 mg, należy zalecić stosowanie skutecznej antykoncepcji. W przypadku kobiet próbujących zajść w ciążę należy rozważyć przerwanie leczenia ZOCOR. W przypadku zajścia w ciążę ZOCOR należy natychmiast przerwać.
Matki karmiące
Nie wiadomo, czy symwastatyna przenika do mleka ludzkiego. Ponieważ niewielka ilość innego leku z tej klasy przenika do mleka ludzkiego oraz ze względu na możliwość wystąpienia poważnych działań niepożądanych u niemowląt karmionych piersią, kobiety przyjmujące symwastatynę nie powinny karmić piersią. Należy podjąć decyzję, czy przerwać karmienie piersią, czy odstawić lek, biorąc pod uwagę znaczenie leku dla matki [zob. PRZECIWWSKAZANIA ].
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność symwastatyny u pacjentów w wieku 10-17 lat z heterozygotyczną hipercholesterolemią rodzinną oceniano w kontrolowanym badaniu klinicznym z udziałem dorastających chłopców i dziewcząt, którzy byli co najmniej 1 rok po pierwszej miesiączce. Profil działań niepożądanych u pacjentów leczonych symwastatyną był podobny do profilu pacjentów otrzymujących placebo. W tej populacji nie badano dawek większych niż 40 mg. W tym ograniczonym kontrolowanym badaniu nie stwierdzono istotnego wpływu na wzrost lub dojrzewanie płciowe u dorastających chłopców lub dziewcząt ani na długość cyklu miesiączkowego u dziewcząt. [Widzieć DAWKOWANIE I SPOSÓB PODAWANIA , DZIAŁANIA NIEPOŻĄDANE , Studia kliniczne ] Nastoletnim kobietom należy doradzać odpowiednie metody antykoncepcji podczas leczenia symwastatyną [patrz PRZECIWWSKAZANIA oraz Ciąża ]. Symwastatyny nie badano u pacjentów w wieku poniżej 10 lat ani u dziewcząt przed miesiączką.
Zastosowanie geriatryczne
Spośród 2423 pacjentów, którzy otrzymywali ZOCOR w dawce 5 mg w badaniach klinicznych III fazy i 10 269 pacjentów w badaniu ochrony serca, którzy otrzymywali ZOCOR w dawce 40 mg, odpowiednio 363 (15%) i 5366 (52%) było w wieku ≥65 lat. W HPS 615 (6%) było w wieku ≥75 lat. Nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między tymi pacjentami a młodszymi pacjentami, a inne zgłoszone doświadczenia kliniczne nie wykazały różnic w odpowiedziach między pacjentami w podeszłym wieku i młodszymi, ale nie można wykluczyć większej wrażliwości niektórych osób starszych. Ponieważ zaawansowany wiek (≥65 lat) jest czynnikiem predysponującym do miopatii, ZOCOR należy przepisywać ostrożnie u osób w podeszłym wieku. [Widzieć FARMAKOLOGIA KLINICZNA ]
Badanie farmakokinetyczne z symwastatyną wykazało, że średni poziom aktywności statyn w osoczu jest o około 45% wyższy u pacjentów w podeszłym wieku w wieku 70-78 lat w porównaniu z pacjentami w wieku 18-30 lat. W 4S 1021 (23%) z 4444 pacjentów miało 65 lub więcej lat. Skuteczność obniżania poziomu lipidów była co najmniej tak samo duża u pacjentów w podeszłym wieku w porównaniu z młodszymi pacjentami, a ZOCOR istotnie zmniejszał całkowitą śmiertelność i śmiertelność z powodu CHD u starszych pacjentów z CHD w wywiadzie. W HPS 52% pacjentów było w podeszłym wieku (4891 pacjentów 65-69 lat i 5806 pacjentów 70 lat lub starszych). Względne zmniejszenie ryzyka zgonu z powodu CHD, zawału serca niezakończonego zgonem, zabiegów rewaskularyzacji wieńcowej i niewieńcowej oraz udaru mózgu było podobne u starszych i młodszych pacjentów [patrz Studia kliniczne ]. W HPS wśród 32 145 pacjentów rozpoczynających aktywny okres rozruchu wystąpiły 2 przypadki miopatii/rabdomiolizy; ci pacjenci byli w wieku 67 i 73 lat. Spośród 7 przypadków miopatii/rabdomiolizy wśród 10 269 pacjentów przydzielonych do simwastatyny, 4 było w wieku 65 lub więcej (na początku badania), z których jeden miał więcej niż 75 lat. Nie było ogólnych różnic w bezpieczeństwie między starszymi i młodsi pacjenci w 4S lub HPS.
Ponieważ zaawansowany wiek (≥65 lat) jest czynnikiem predysponującym do miopatii, w tym rabdomiolizy, ZOCOR 40 mg należy przepisywać ostrożnie u osób w podeszłym wieku. W badaniu klinicznym pacjentów leczonych symwastatyną w dawce 80 mg/dobę u pacjentów w wieku ≥65 lat występowało zwiększone ryzyko miopatii, w tym rabdomiolizy, w porównaniu z pacjentami w wieku OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ]
Zaburzenia czynności nerek
Należy zachować ostrożność podając ZOCOR 20 mg pacjentom z ciężkimi zaburzeniami czynności nerek. [Patrz DAWKOWANIE I SPOSÓB PODAWANIA ]
Niewydolność wątroby
ZOCOR 10 mg jest przeciwwskazany u pacjentów z czynną chorobą wątroby, która może obejmować niewyjaśnione utrzymujące się podwyższenie aktywności aminotransferaz wątrobowych [patrz PRZECIWWSKAZANIA oraz OSTRZEŻENIA I ŚRODKI ].
Chińscy pacjenci
W badaniu klinicznym, w którym pacjenci z wysokim ryzykiem chorób sercowo-naczyniowych byli leczeni symwastatyną w dawce 40 mg/dobę (mediana okresu obserwacji 3,9 roku), częstość występowania miopatii wyniosła około 0,05% u pacjentów niebędących Chińczykami (n=7367) w porównaniu z 0,24% dla pacjentów chińskich (n=5468). Częstość występowania miopatii u chińskich pacjentów przyjmujących symwastatynę 40 mg/dobę lub ezetymib/simwastatynę 10/40 mg/dobę jednocześnie z niacyną o przedłużonym uwalnianiu 2 g/dobę wynosiła 1,24%.
Chińscy pacjenci mogą być bardziej narażeni na miopatię, należy odpowiednio monitorować pacjentów. Jednoczesne podawanie produktu ZOCOR 10 mg z dawkami modyfikującymi lipidy (≥1 g/dobę niacyny) produktów zawierających niacynę nie jest zalecane u pacjentów chińskich [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI ].
PRZEDAWKOWAĆ
Znaczącą śmiertelność zaobserwowano u myszy po pojedynczej doustnej dawce 9 g/m2. Nie zaobserwowano dowodów na śmiertelność u szczurów lub psów, którym podawano dawki odpowiednio 30 i 100 g/m2. U gryzoni nie zaobserwowano żadnych specyficznych objawów diagnostycznych. Przy tych dawkach jedynymi objawami obserwowanymi u psów były wymioty i śluzowe stolce.
Zgłoszono kilka przypadków przedawkowania ZOCOR; maksymalna przyjęta dawka wynosiła 3,6 g. Wszyscy pacjenci wyzdrowieli bez następstw. W przypadku przedawkowania należy zastosować środki wspomagające. Dializowalność simwastatyny i jej metabolitów u ludzi nie jest obecnie znana.
PRZECIWWSKAZANIA
ZOCOR 40mg jest przeciwwskazany w następujących stanach:
- Jednoczesne podawanie silnych inhibitorów CYP3A4 (np. itrakonazol, ketokonazol, posakonazol, worykonazol, inhibitory proteazy HIV, boceprewir, telaprewir, erytromycyna, klarytromycyna, telitromycyna, nefazodon i produkty zawierające kobicystat) [patrz OSTRZEŻENIA I ŚRODKI ].
- Jednoczesne podawanie gemfibrozylu, cyklosporyny lub danazolu [patrz OSTRZEŻENIA I ŚRODKI ].
- Nadwrażliwość na którykolwiek składnik tego leku [patrz DZIAŁANIA NIEPOŻĄDANE ].
- Aktywna choroba wątroby, która może obejmować niewyjaśnione, utrzymujące się podwyższenie poziomu transaminaz wątrobowych [patrz OSTRZEŻENIA I ŚRODKI ].
- Kobiety w ciąży lub mogące zajść w ciążę. Poziom cholesterolu i trójglicerydów w surowicy wzrasta podczas normalnej ciąży, a cholesterol lub pochodne cholesterolu są niezbędne do rozwoju płodu. Ponieważ inhibitory reduktazy HMG-CoA (statyny) zmniejszają syntezę cholesterolu i prawdopodobnie syntezę innych substancji biologicznie czynnych pochodzących z cholesterolu, ZOCOR 40mg może powodować uszkodzenie płodu po podaniu kobiecie w ciąży. Miażdżyca jest procesem przewlekłym i odstawienie leków hipolipemizujących w czasie ciąży powinno mieć niewielki wpływ na wynik długotrwałej terapii pierwotnej hipercholesterolemii. Nie ma odpowiednich i dobrze kontrolowanych badań dotyczących stosowania leku ZOCOR w czasie ciąży; jednak w rzadkich doniesieniach po wewnątrzmacicznej ekspozycji na statyny obserwowano wady wrodzone. W badaniach rozrodu szczurów i królików symwastatyna nie wykazała działania teratogennego. ZOCOR powinien być podawany kobietom w wieku rozrodczym tylko wtedy, gdy istnieje duże prawdopodobieństwo zajścia w ciążę. Jeśli pacjentka zajdzie w ciążę podczas przyjmowania tego leku, ZOCOR należy natychmiast odstawić, a pacjentkę należy poinformować o potencjalnym zagrożeniu dla płodu [patrz Używaj w określonych populacjach ].
- Matki karmiące. Nie wiadomo, czy symwastatyna przenika do mleka ludzkiego; jednak niewielka ilość innego leku z tej klasy przenika do mleka matki. Ponieważ statyny mogą wywoływać poważne działania niepożądane u niemowląt karmionych piersią, kobiety wymagające leczenia preparatem ZOCOR nie powinny karmić piersią swoich niemowląt [patrz Używaj w określonych populacjach ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Symwastatyna jest prolekiem i po podaniu ulega hydrolizie do aktywnej postaci β-hydroksykwasu, kwasu symwastatyny. Simwastatyna jest specyficznym inhibitorem reduktazy 3-hydroksy-3-metyloglutarylo-koenzymu A (HMG-CoA), enzymu, który katalizuje konwersję HMG-CoA do mewalonianu, wczesny i ograniczający szybkość etap szlaku biosyntezy cholesterolu. Ponadto simwastatyna zmniejsza VLDL i TG oraz zwiększa HDL-C.
Farmakodynamika
Badania epidemiologiczne wykazały, że podwyższone poziomy całkowitego C, LDL-C, a także obniżone poziomy HDL-C są związane z rozwojem miażdżycy i zwiększonym ryzykiem sercowo-naczyniowym. Obniżenie LDL-C zmniejsza to ryzyko. Nie ustalono jednak niezależnego wpływu podwyższenia HDL-C lub obniżenia TG na ryzyko zachorowalności i śmiertelności wieńcowej i sercowo-naczyniowej.
Farmakokinetyka
Symwastatyna jest laktonem, który łatwo hydrolizuje in vivo do odpowiedniego β-hydroksykwasu, silnego inhibitora reduktazy HMG-CoA. Hamowanie reduktazy HMG-CoA jest podstawą oznaczenia w badaniach farmakokinetycznych metabolitów β-hydroksykwasów (aktywnych inhibitorów) oraz, po hydrolizie zasady, aktywnych i utajonych inhibitorów (inhibitory całkowite) w osoczu po podaniu symwastatyny.
Po doustnym podaniu człowiekowi symwastatyny znakowanej węglem 14C, 13% dawki było wydalane z moczem, a 60% z kałem. Stężenie całkowitej radioaktywności w osoczu (simwastatyna plus metabolity 14C) osiągnęło maksimum po 4 godzinach i gwałtownie spadło do około 10% wartości szczytowej po 12 godzinach od podania dawki. Ponieważ symwastatyna jest poddawana intensywnej ekstrakcji pierwszego przejścia w wątrobie, dostępność leku do krążenia ogólnego jest niska (
Zarówno symwastatyna, jak i jej metabolit β-hydroksykwas w dużym stopniu (około 95%) wiążą się z białkami ludzkiego osocza. Badania na szczurach wskazują, że po podaniu znakowanej radioaktywnie simwastatyny radioaktywność pochodząca z symwastatyny przekraczała barierę krew-mózg.
Głównymi czynnymi metabolitami symwastatyny obecnymi w ludzkim osoczu są β-hydroksykwas symwastatyny i jej pochodne 6'-hydroksy, 6'-hydroksymetylowe i 6'-egzometylenowe. Maksymalne stężenia w osoczu zarówno czynnych, jak i całkowitych inhibitorów osiągnięto w ciągu 1,3 do 2,4 godziny po podaniu. Chociaż zalecany zakres dawek terapeutycznych wynosi od 5 do 40 mg/dobę, nie stwierdzono istotnego odchylenia od liniowości AUC inhibitorów w ogólnym krążeniu przy wzroście dawki aż do 120 mg. W porównaniu ze stanem na czczo, profil inhibitorów w osoczu nie ulegał zmianie, gdy symwastatynę podawano bezpośrednio przed posiłkiem niskotłuszczowym zalecanym przez American Heart Association.
badaniu obejmującym 16 pacjentów w podeszłym wieku w wieku od 70 do 78 lat, którzy otrzymywali ZOCOR w dawce 40 mg/dobę, średni poziom aktywności hamującej reduktazę HMG-CoA w osoczu wzrósł o około 45% w porównaniu z 18 pacjentami w wieku 18-30 lat. Doświadczenie z badań klinicznych u osób w podeszłym wieku (n=1522) sugeruje, że nie było ogólnych różnic w bezpieczeństwie między pacjentami w podeszłym wieku i młodszymi [patrz Używaj w określonych populacjach ].
Badania kinetyczne z inną statyną, o podobnej głównej drodze eliminacji, sugerują, że dla danego poziomu dawki można osiągnąć większą ekspozycję ogólnoustrojową u pacjentów z ciężką niewydolnością nerek (mierzoną na podstawie klirensu kreatyniny).
Kwas symwastatyny jest substratem białka transportowego OATP1B1. Jednoczesne podawanie produktów leczniczych będących inhibitorami białka transportowego OATP1B1 może prowadzić do zwiększenia stężenia kwasu symwastatyny w osoczu i zwiększonego ryzyka miopatii. Na przykład wykazano, że cyklosporyna zwiększa AUC statyn; chociaż mechanizm nie jest w pełni poznany, wzrost AUC kwasu symwastatyny jest prawdopodobnie częściowo spowodowany hamowaniem CYP3A4 i/lub OATP1B1.
Wysokie poziomy aktywności hamującej reduktazę HMG-CoA w osoczu zwiększają ryzyko miopatii. Inhibitory CYP3A4 mogą zwiększać poziom aktywności hamującej reduktazę HMG-CoA w osoczu i zwiększać ryzyko miopatii [patrz OSTRZEŻENIA I ŚRODKI oraz INTERAKCJE Z LEKAMI ].
badaniu z udziałem 12 zdrowych ochotników symwastatyna w dawce 80 mg nie miała wpływu na metabolizm próbnych substratów cytochromu P450 izoformy 3A4 (CYP3A4), midazolamu i erytromycyny. Wskazuje to, że symwastatyna nie jest inhibitorem CYP3A4, a zatem nie oczekuje się, że będzie miała wpływ na stężenie innych leków metabolizowanych przez CYP3A4 w osoczu.
Jednoczesne podawanie simwastatyny (40 mg QD przez 10 dni) powodowało wzrost maksymalnego średniego stężenia digoksyny działającej na serce (podanej jako pojedyncza dawka 0,4 mg w 10. dniu) o około 0,3 ng/ml.
Toksykologia i/lub farmakologia zwierząt
Toksyczność OUN
Zwyrodnienie nerwu wzrokowego obserwowano u zdrowych klinicznie psów leczonych simwastatyną przez 14 tygodni w dawce 180 mg/kg/dzień, dawki, która powodowała średni poziom leku w osoczu około 12 razy wyższy niż średni poziom leku w osoczu u ludzi przyjmujących 80 mg/dzień.
Chemicznie podobny lek w tej klasie powodował również zwyrodnienie nerwu wzrokowego (zwyrodnienie Walleriana włókien siatkówkowatych) u klinicznie zdrowych psów w sposób zależny od dawki, począwszy od 60 mg/kg/dobę, dawki, która powodowała średnie poziomy leku w osoczu około 30 razy wyższe. niż średnie stężenie leku w osoczu u ludzi przyjmujących najwyższą zalecaną dawkę (mierzoną na podstawie całkowitej aktywności hamującej enzymy). Ten sam lek powodował również zwyrodnienie przedsionkowo-ślimakowe podobne do Wallera i chromatolizę komórek zwojowych siatkówki u psów leczonych przez 14 tygodni dawką 180 mg/kg/dobę, dawką, która skutkowała średnim poziomem leku w osoczu podobnym do obserwowanego przy 60 mg/kg/dobę. dawka dzienna.
psów leczonych simwastatyną w dawce 360 mg/kg mc./dobę, w dawce dającej średnie stężenie w osoczu, obserwowano zmiany naczyniowe OUN, charakteryzujące się krwotokiem okołonaczyniowym i obrzękiem, naciekiem komórek jednojądrzastych przestrzeni okołonaczyniowych, okołonaczyniowymi złogami fibryny i martwicą małych naczyń. poziomy leku, które były około 14 razy wyższe niż średnie poziomy leku w osoczu u ludzi przyjmujących 80 mg/dzień. Podobne uszkodzenia naczyń OUN zaobserwowano w przypadku kilku innych leków z tej klasy.
Zaćma występowała u samic szczurów po dwóch latach leczenia 50 i 100 mg/kg/dobę (odpowiednio 22 i 25-krotność ludzkiego AUC przy 80 mg/dobę) oraz u psów po trzech miesiącach przy 90 mg/kg/dobę ( 19 razy) i po dwóch latach 50 mg/kg/dzień (5 razy).
Studia kliniczne
Badania kliniczne u dorosłych
Zmniejszenie ryzyka śmiertelności z powodu CHD i incydentów sercowo-naczyniowych
4S wpływ terapii ZOCOR 20mg na całkowitą śmiertelność oceniono u 4444 pacjentów z CHD i wyjściowym cholesterolem całkowitym 212-309 mg/dl (5,5-8,0 mmol/l). W tym wieloośrodkowym, randomizowanym, podwójnie zaślepionym, kontrolowanym placebo badaniu pacjenci otrzymywali standardową opiekę, w tym dietę i albo ZOCOR 20-40 mg/dobę (n=2221) albo placebo (n=2223) przez medianę czasu trwania 5,4 roku. W trakcie badania leczenie preparatem ZOCOR doprowadziło do średniego zmniejszenia stężenia całkowitego C, LDL-C i TG odpowiednio o 25%, 35% i 10% oraz średniego wzrostu HDL-C o 8%. ZOCOR znacząco zmniejszył ryzyko zgonu o 30% (p=0,0003, 182 zgony w grupie ZOCOR 40 mg vs 256 zgonów w grupie placebo). Ryzyko zgonu z powodu CHD zostało znacznie zmniejszone o 42% (p=0,00001, 111 vs 189 zgonów). Nie było statystycznie istotnej różnicy między grupami w śmiertelności z przyczyn innych niż sercowo-naczyniowe. ZOCOR znacząco zmniejszył ryzyko wystąpienia poważnych incydentów wieńcowych (śmiertelność z powodu CHD plus potwierdzony szpitalnie i niemy zawał serca niezakończony zgonem [MI]) o 34% (p
Badanie ochrony serca (HPS) było dużym, wieloośrodkowym, kontrolowanym placebo badaniem z podwójnie ślepą próbą, trwającym średnio 5 lat, przeprowadzonym z udziałem 20 536 pacjentów (10 269 w grupie ZOCOR 40 mg i 10267 w grupie placebo). Pacjentów przydzielono do leczenia za pomocą metody adaptacyjnej kowariancji3, która uwzględniała rozkład 10 ważnych cech wyjściowych pacjentów już włączonych i minimalizowała nierównowagę tych cech w grupach. Pacjenci byli w średnim wieku 64 lata (zakres 40-80 lat), byli w 97% rasy kaukaskiej i byli obarczeni wysokim ryzykiem wystąpienia poważnego incydentu wieńcowego z powodu istniejącej CHD (65%), cukrzycy (typ 2, 26%; typ 1 , 3%), udar lub inna choroba naczyniowa mózgu w wywiadzie (16%), choroba naczyń obwodowych (33%) lub nadciśnienie u mężczyzn w wieku ≥ 65 lat (6%). Wyjściowo 3421 pacjentów (17%) miało poziom LDL-C poniżej 100 mg/dl, z czego 953 (5%) miało poziom LDL-C poniżej 80 mg/dl; 7068 pacjentów (34%) miało poziomy od 100 do 130 mg/dl; a 10 047 pacjentów (49%) miało poziom powyżej 130 mg/dl.
DR Taves, Minimalizacja: nowa metoda przypisywania pacjentów do grup terapeutycznych i kontrolnych. Clin. Pharmacol. Tam. 15 (1974), s. 443-453
Wyniki HPS wykazały, że ZOCOR 40 mg/dzień istotnie zmniejszył: śmiertelność całkowitą i CHD; Zawał serca niezakończony zgonem, udar mózgu i zabiegi rewaskularyzacji (wieńcowe i niewieńcowe) (patrz Tabela 4).
Zdefiniowano dwa złożone punkty końcowe w celu uzyskania wystarczającej liczby zdarzeń do oceny względnego zmniejszenia ryzyka w zakresie cech wyjściowych (patrz Rysunek 1). Zbiór głównych zdarzeń wieńcowych (MCE) składał się ze śmiertelności z powodu CHD i zawału serca niezakończonego zgonem (analizowane według czasu do pierwszego zdarzenia; zdarzenia te wystąpiły u 898 pacjentów leczonych preparatem ZOCOR w dawce 5 mg, a u 1212 pacjentów otrzymujących placebo). Zbiór głównych zdarzeń naczyniowych (MVE) składał się z MCE, udaru mózgu i zabiegów rewaskularyzacji, w tym zabiegów wieńcowych, obwodowych i innych niewieńcowych (analizowanych według czasu do pierwszego zdarzenia; u 2033 pacjentów leczonych preparatem ZOCOR 10 mg wystąpiły zdarzenia, a 2585 pacjentów w placebo miało zdarzenia). Znaczące zmniejszenie względnego ryzyka zaobserwowano dla obu złożonych punktów końcowych (27% dla MCE i 24% dla MVE, p
Rycina 1 Wpływ leczenia preparatem ZOCOR 5 mg na poważne zdarzenia naczyniowe i poważne zdarzenia wieńcowe w HPS
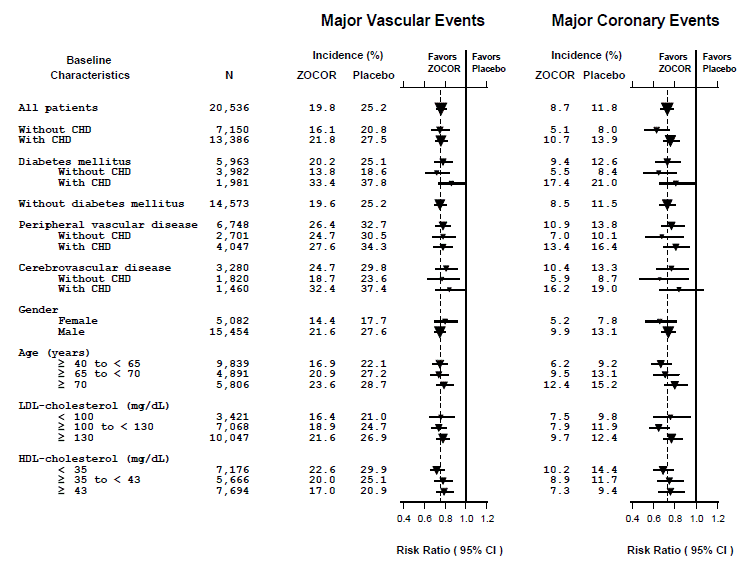
Studia Angiograficzne
W Multicenter Anti-Atheroma Study wpływ simwastatyny na miażdżycę oceniano za pomocą ilościowej koronarografii u pacjentów z hipercholesterolemią i CHD. W tym randomizowanym, podwójnie zaślepionym, kontrolowanym badaniu pacjenci otrzymywali symwastatynę w dawce 20 mg/dobę lub placebo. Angiogramy oceniano na początku, po dwóch i czterech latach. Równorzędnymi pierwszorzędowymi punktami końcowymi badania były średnie zmiany na pacjenta w minimalnej i średniej średnicy światła, wskazujące odpowiednio na ogniskową i rozlaną chorobę. ZOCOR istotnie spowalniał progresję zmian mierzonych w angiogramie 4. roku zarówno pod względem obu parametrów, jak i zmiany procentowej średnicy zwężenia. Ponadto simwastatyna znacząco zmniejszyła odsetek pacjentów z nowymi zmianami i nowymi całkowitymi niedrożnościami.
Modyfikacje profili lipidowych
Pierwotna hiperlipidemia (typ Fredrickson IIa i IIb)
Wykazano, że ZOCOR jest skuteczny w zmniejszaniu całkowitego C i LDL-C w heterozygotycznych rodzinnych i nierodzinnych postaciach hiperlipidemii oraz w mieszanej hiperlipidemii. Odpowiedź maksymalna do prawie maksymalnej jest zazwyczaj osiągana w ciągu 4-6 tygodni i utrzymuje się podczas przewlekłej terapii. ZOCOR znacząco zmniejszył stosunek C całkowitego, LDL-C, C całkowitego/HDL-C oraz LDL-C/HDL-C; ZOCOR obniżył również TG i podwyższył HDL-C (patrz Tabela 5).
Hipertriglicerydemia (typ Fredrickson IV)
Wyniki analizy podgrup u 74 pacjentów z hiperlipidemią typu IV z 130 pacjentów, podwójnie zaślepione, kontrolowane placebo, 3-okresowe badanie naprzemienne przedstawiono w Tabeli 6.
Dysbetalipoproteinemia (typ Fredricksona III)
Wyniki analizy podgrup u 7 pacjentów z hiperlipidemią typu III (dysbetalipoproteinemią) (apo E2/2) (VLDL-C/TG>0,25) w trzyokresowym badaniu naprzemiennym obejmującym 130 pacjentów przedstawiono w tabeli 7.
Homozygotyczna rodzinna hipercholesterolemia
W kontrolowanym badaniu klinicznym 12 pacjentów w wieku 15-39 lat z homozygotyczną hipercholesterolemią rodzinną otrzymywało symwastatynę 40 mg/dobę w dawce pojedynczej lub w 3 dawkach podzielonych lub 80 mg/dobę w 3 dawkach podzielonych. U 11 pacjentów ze zmniejszeniem stężenia LDL-C średnie zmiany LDL-C dla dawek 40 i 80 mg wyniosły 14% (zakres 8% do 23%, mediana 12%) i 30% (zakres 14% do 46%). , mediana 29%. Jeden pacjent miał 15% wzrost LDL-C. Inny pacjent z nieobecną funkcją receptora LDL-C miał zmniejszenie LDL-C o 41% przy dawce 80 mg.
Funkcja hormonalna
badaniach klinicznych symwastatyna nie zaburzała rezerwy nadnerczowej ani nie zmniejszała znacząco podstawowego stężenia kortyzolu w osoczu. W badaniach klinicznych z simwastatyną zaobserwowano niewielkie zmniejszenie podstawowego stężenia testosteronu w osoczu mężczyzn w stosunku do wartości wyjściowej, efekt obserwowany również w przypadku innych statyn i cholestyraminy będącej sekwestrantem kwasów żółciowych. Nie stwierdzono wpływu na stężenie gonadotropin w osoczu. W 12-tygodniowym badaniu kontrolowanym placebo nie stwierdzono istotnego wpływu 80 mg symwastatyny na odpowiedź testosteronu w osoczu na ludzką gonadotropinę kosmówkową. W innym 24-tygodniowym badaniu symwastatyna w dawce 20-40 mg nie miała wykrywalnego wpływu na spermatogenezę. W badaniu 4S, w którym 4444 pacjentów zostało losowo przydzielonych do grupy otrzymującej symwastatynę w dawce 20-40 mg/dobę lub placebo przez medianę czasu trwania wynoszącą 5,4 roku, częstość występowania niepożądanych zdarzeń seksualnych u mężczyzn w obu grupach leczenia nie różniła się znacząco. Ze względu na te czynniki, niewielkie zmiany testosteronu w osoczu prawdopodobnie nie będą miały znaczenia klinicznego. Ewentualny wpływ na oś przysadkowo-gonadową u kobiet przed menopauzą nie jest znany.
Badania kliniczne u młodzieży
W podwójnie zaślepionym, kontrolowanym placebo badaniu 175 pacjentów (99 nastoletnich chłopców i 76 dziewcząt po menarchii) w wieku 10-17 lat (średnia wieku 14,1 lat) z heterozygotyczną hipercholesterolemią rodzinną (HeFH) zostało losowo przydzielonych do grupy otrzymującej symwastatynę (n= 106) lub placebo (n=67) przez 24 tygodnie (badanie podstawowe). Włączenie do badania wymagało wyjściowego poziomu LDL-C między 160 a 400 mg/dl i co najmniej jednego rodzica z poziomem LDL-C >189 mg/dl. Dawka symwastatyny (raz na dobę wieczorem) wynosiła 10 mg przez pierwsze 8 tygodni, 20 mg przez kolejne 8 tygodni, a następnie 40 mg. W przedłużeniu trwającym 24 tygodnie 144 pacjentów wybrało kontynuację leczenia symwastatyną w dawce 40 mg lub placebo.
ZOCOR 20 mg znacząco obniżył poziomy całkowitego C, LDL-C i Apo B w osoczu (patrz Tabela 8). Wyniki z przedłużenia po 48 tygodniach były porównywalne z tymi obserwowanymi w badaniu podstawowym.
Po 24 tygodniach leczenia średnia osiągnięta wartość LDL-C wyniosła 124,9 mg/dl (zakres: 64.0289,0 mg/dl) w grupie ZOCOR 40 mg w porównaniu do 207,8 mg/dl (zakres: 128,0-334,0 mg/dl) w grupie placebo.
Nie badano bezpieczeństwa i skuteczności dawek powyżej 40 mg na dobę u dzieci z HeFH. Nie ustalono długoterminowej skuteczności leczenia symwastatyną w dzieciństwie w zakresie zmniejszania zachorowalności i śmiertelności w wieku dorosłym.
INFORMACJA O PACJENCIE
Pacjentom należy zalecić przestrzeganie diety zalecanej przez Narodowy Program Edukacji Cholesterolowej (NCEP), regularnego programu ćwiczeń i okresowych badań panelu lipidowego na czczo.
Należy pouczyć pacjentów o substancjach, których nie powinni przyjmować jednocześnie z symwastatyną [Widzieć PRZECIWWSKAZANIA oraz OSTRZEŻENIA I ŚRODKI ]. Pacjentom należy również doradzić, aby informowali innych pracowników służby zdrowia przepisujących nowy lek lub zwiększający dawkę istniejącego leku, że przyjmują ZOCOR.
Ból w mięśniach
Wszystkich pacjentów rozpoczynających leczenie preparatem ZOCOR należy poinformować o ryzyku wystąpienia miopatii, w tym rabdomiolizy, oraz poinformować o konieczności szybkiego zgłaszania wszelkich niewyjaśnionych bólów, tkliwości lub osłabienia mięśni, szczególnie jeśli towarzyszy im złe samopoczucie lub gorączka lub jeśli te objawy przedmiotowe lub podmiotowe mięśni utrzymują się po odstawieniu preparatu ZOCOR. Pacjentów stosujących dawkę 80 mg należy poinformować, że stosowanie dawki 80 mg zwiększa ryzyko miopatii, w tym rabdomiolizy. Ryzyko miopatii, w tym rabdomiolizy, występujące przy stosowaniu ZOCOR 40mg zwiększa się w przypadku przyjmowania niektórych leków lub spożywania soku grejpfrutowego. Pacjenci powinni omówić wszystkie leki, zarówno na receptę, jak i bez recepty, ze swoim lekarzem.
Enzymy wątrobowe
Zaleca się wykonanie testów czynności wątroby przed rozpoczęciem leczenia ZOCOR 20 mg, a następnie, gdy jest to klinicznie wskazane. Wszystkim pacjentom leczonym preparatem ZOCOR należy zalecić niezwłoczne zgłaszanie wszelkich objawów mogących wskazywać na uszkodzenie wątroby, w tym zmęczenia, anoreksji, dyskomfortu w prawym górnym odcinku brzucha, ciemnego moczu lub żółtaczki.
Ciąża
Kobietom w wieku rozrodczym należy zalecić stosowanie skutecznej metody antykoncepcji w celu zapobiegania ciąży podczas stosowania leku ZOCOR. Omów plany przyszłej ciąży ze swoimi pacjentkami i omów, kiedy przestać zażywać ZOCOR 40mg, jeśli próbują zajść w ciążę. Pacjentki należy pouczyć, że w przypadku zajścia w ciążę powinny przerwać przyjmowanie leku ZOCOR i skontaktować się z lekarzem.
Karmienie piersią
Kobiety karmiące piersią nie powinny stosować ZOCOR. Pacjentkom z zaburzeniami lipidowymi i karmiącym piersią należy zalecić omówienie możliwości z lekarzem.
