Leczenie cholesterolu: Lipitor 10mg, 20mg, 40mg Atorvastatin Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Lipitor 40mg i jak się go stosuje?
Lipitor 10 mg jest lekiem na receptę stosowanym w celu obniżenia poziomu „złego” cholesterolu we krwi (lipoproteiny o niskiej gęstości lub LDL), w celu zwiększenia poziomu „dobrego” cholesterolu (lipoproteiny o wysokiej gęstości lub HDL) oraz w celu obniżenia poziomu trójglicerydów i leczyć objawy wysokiego cholesterolu (hiperlipidemii) oraz zmniejszać ryzyko udaru, zawału serca lub innych powikłań sercowych. Lipitor 40mg może być stosowany samodzielnie lub z innymi lekami.
Lipitor 10mg należy do grupy leków zwanych środkami obniżającymi poziom lipidów, statynami, inhibitorami reduktazy HMG-CoA.
Nie wiadomo, czy Lipitor 10 mg jest bezpieczny i skuteczny u dzieci w wieku poniżej 10 lat.
Jakie są możliwe skutki uboczne Lipitor?
Lipitor 10mg może powodować poważne skutki uboczne, w tym:
- ból lub pieczenie podczas oddawania moczu,
- ból w górnej części brzucha,
- słabość,
- czuć się zmęczonym,
- utrata apetytu,
- ciemny mocz,
- zażółcenie skóry lub oczu (żółtaczka),
- mało lub brak oddawania moczu,
- obrzęk stóp lub kostek oraz
- zadyszka
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Lipitor to:
- ból stawu,
- zatkany nos,
- ból gardła,
- biegunka i
- ból rąk lub nóg
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Lipitor. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
LIPITOR to syntetyczny środek obniżający poziom lipidów. Atorwastatyna jest inhibitorem reduktazy 3-hydroksy-3-metyloglutarylo-koenzymu A (HMG-CoA). Enzym ten katalizuje konwersję HMG-CoA do mewalonianu, wczesny etap biosyntezy cholesterolu, ograniczający andrate.
Wapń atorwastatyny to [R-(R*, R*)]-2-(4-fluorofenylo)-β,δ-dihydroksy-5-(1-metyloetylo)-3-fenylo-4-[(fenyloamino)karbonylo]- Kwas 1-hpirolo-1-heptanowy, sól wapniowa (2:1) trihydrat. Empiryczny wzór wapnia atorwastatyny to (C33H34FN2O5)2Ca•3H2O, a jego masa cząsteczkowa wynosi 1209.42. Jego wzór strukturalny to:
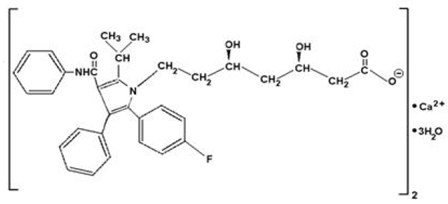
Atorwastatyna wapniowa jest krystalicznym proszkiem o barwie od białej do białawej, nierozpuszczalnym w wodnych roztworach o pH 4 i niższym. Wapń atorwastatyny jest bardzo słabo rozpuszczalny w wodzie destylowanej, buforze fosforanowym o pH 7,4 i acetonitrylu; słabo rozpuszczalny w etanolu; i swobodnie rozpuszczalny w metanolu.
Tabletki LIPITOR do podawania doustnego zawierają 10, 20, 40 lub 80 mg atorwastatyny oraz następujące składniki nieaktywne: węglan wapnia, USP; wosk kandelila,FCC; kroskarmeloza sodowa, NF; hydroksypropyloceluloza, NF; monohydrat laktozy, NF; stearynian magnezu, NF; celuloza mikrokrystaliczna, NF; Opadry White YS-1-7040 (hypromeloza, glikol polietylenowy, talk, dwutlenek tytanu); polisorbat 80, NF; emulsja symetykonowa.
WSKAZANIA
Terapia środkami zmieniającymi poziom lipidów powinna być tylko jednym z elementów interwencji wieloczynnikowej u osób ze znacznie zwiększonym ryzykiem miażdżycowej choroby naczyń z powodu hipercholesterolemii. Farmakoterapia jest zalecana jako uzupełnienie diety, gdy reakcja na samą dietę o ograniczonej zawartości tłuszczów nasyconych i cholesterolu oraz inne niefarmakologiczne środki okazała się niewystarczająca. U pacjentów z CHD lub wieloma czynnikami ryzyka CHD LIPITOR 20 mg można rozpocząć jednocześnie z dietą.
Zapobieganie chorobom układu krążenia u dorosłych
dorosłych pacjentów bez klinicznie ewidentnej choroby wieńcowej, ale z wieloma czynnikami ryzyka choroby wieńcowej, takimi jak wiek, palenie tytoniu, nadciśnienie, niski poziom HDL-C lub wczesna choroba wieńcowa w wywiadzie rodzinnym, LIPITOR 10 mg jest wskazany do:
- Zmniejsz ryzyko zawału mięśnia sercowego
- Zmniejsz ryzyko udaru mózgu
- Zmniejszenie ryzyka zabiegów rewaskularyzacji i dusznicy bolesnej
U dorosłych pacjentów z cukrzycą typu 2 i bez klinicznie widocznej choroby wieńcowej serca, ale z wieloma czynnikami ryzyka choroby wieńcowej, takimi jak retinopatia, albuminuria, palenie tytoniu lub nadciśnienie tętnicze, LIPITOR jest wskazany w:
- Zmniejsz ryzyko zawału mięśnia sercowego
- Zmniejsz ryzyko udaru mózgu
U dorosłych pacjentów z klinicznie jawną chorobą wieńcową, LIPITOR 20 mg jest wskazany do:
- Zmniejszenie ryzyka zawału mięśnia sercowego niezakończonego zgonem
- Zmniejsz ryzyko śmiertelnego i nie śmiertelnego udaru mózgu
- Zmniejszenie ryzyka zabiegów rewaskularyzacji
- Zmniejsz ryzyko hospitalizacji z powodu CHF
- Zmniejsz ryzyko dławicy piersiowej
Hiperlipidemia
LIPITOR 20mg jest wskazany:
- Jako uzupełnienie diety w celu obniżenia podwyższonego stężenia całkowitego C, LDL-C, apo B i TG oraz zwiększenia HDL-C u dorosłych pacjentów z pierwotną hipercholesterolemią (heterozygotyczna rodzinna i nierodzinna) oraz mieszaną dyslipidemią (typy Fredricksona IIa i IIb) ;
- Jako dodatek do diety w leczeniu dorosłych pacjentów z podwyższonym poziomem TG w surowicy (Fredrickson Typ IV);
- Do leczenia dorosłych pacjentów z pierwotną dysbetalipoproteinemią (typu Fredricksona III), którzy nie reagują odpowiednio na dietę;
- Zmniejszenie całkowitego C i LDL-C u pacjentów z homozygotyczną rodzinną hipercholesterolemią (HoFH) jako uzupełnienie innych terapii obniżających stężenie lipidów (np. afereza LDL) lub jeśli takie terapie są niedostępne;
- Jako uzupełnienie diety w celu obniżenia poziomu całkowitego C, LDL-C i apo B u pacjentów pediatrycznych w wieku od 10 do 17 lat z heterozygotyczną hipercholesterolemią rodzinną (HeFH), jeśli po odpowiedniej próbie leczenia dietą następujące wyniki są teraźniejszość:
- dodatni wywiad rodzinny dotyczący przedwczesnej choroby sercowo-naczyniowej lub
- u pacjenta pediatrycznego występują dwa lub więcej innych czynników ryzyka CVD
Ograniczenia użytkowania
LIPITOR 40 mg nie był badany w warunkach, w których główną nieprawidłowością lipoproteinową jest podwyższenie stężenia chylomikronów (typy I i V według Fredricksona).
DAWKOWANIE I SPOSÓB PODAWANIA
Hiperlipidemia i mieszana dyslipidemia
Zalecana dawka początkowa leku LIPITOR 10 mg wynosi 10 lub 20 mg raz na dobę. Pacjenci, którzy wymagają dużej redukcji LDL-C (ponad 45%), mogą rozpocząć leczenie od 40 mg raz na dobę. Zakres dawkowania preparatu LIPITOR wynosi od 10 do 80 mg raz na dobę. LIPITOR 10 mg można podawać w pojedynczej dawce o dowolnej porze dnia, z posiłkiem lub bez posiłku. Dawkę początkową i podtrzymującą LIPITOR należy dostosować indywidualnie do cech pacjenta, takich jak cel leczenia i odpowiedź. Po rozpoczęciu i (lub) dostosowaniu dawki LIPITOR 10 mg należy w ciągu 2 do 4 tygodni zbadać stężenie lipidów i odpowiednio dostosować dawkowanie.
Heterozygotyczna hipercholesterolemia rodzinna u pacjentów pediatrycznych (od 10 do 17 lat)
Zalecana dawka początkowa preparatu LIPITOR 10 mg wynosi 10 mg/dobę; zwykle zakres dawek wynosi od 10 do 20 mg doustnie raz na dobę [patrz Studia kliniczne ]. Dawki należy dobierać indywidualnie zgodnie z zalecanym celem terapii [patrz WSKAZANIA I ZASTOSOWANIE oraz FARMAKOLOGIA KLINICZNA ]. Korekty należy dokonywać w odstępach co 4 tygodnie lub więcej.
Homozygotyczna rodzinna hipercholesterolemia
Dawka LIPITORA 20mg u pacjentów z HoFH wynosi od 10 do 80 mg na dobę. LIPITOR 20 mg powinien być stosowany jako uzupełnienie innych terapii hipolipemizujących (np. aferezy LDL) u tych pacjentów lub jeśli takie terapie są niedostępne.
Jednoczesne leczenie obniżające poziom lipidów
LIPITOR 20mg może być stosowany z żywicami kwasów żółciowych. Połączenie inhibitorów reduktazy HMG-CoA (statyn) i fibratów należy zasadniczo stosować z ostrożnością [patrz OSTRZEŻENIA I ŚRODKI oraz INTERAKCJE Z LEKAMI ].
Dawkowanie u pacjentów z zaburzeniami czynności nerek
Choroba nerek nie wpływa na stężenie w osoczu ani na redukcję LDL-C LIPITORA; dlatego dostosowanie dawki u pacjentów z zaburzeniami czynności nerek nie jest konieczne [patrz OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
Dawkowanie u pacjentów przyjmujących cyklosporynę, klarytromycynę, itrakonazol, letermowir lub niektóre inhibitory proteazy
pacjentów przyjmujących cyklosporynę lub inhibitor proteazy wirusa HIV typranawir z rytonawirem lub inhibitor proteazy wirusa zapalenia wątroby typu C (HCV) glekaprewir z pibrentaswirem lub letermowirem w przypadku jednoczesnego podawania z cyklosporyną należy unikać leczenia preparatem LIPITOR 40 mg. U pacjentów z HIV przyjmujących lopinawir z rytonawirem należy stosować najmniejszą niezbędną dawkę leku LIPITOR. U pacjentów przyjmujących klarytromycynę, itrakonazol, elbaswir z grazoprewirem lub u pacjentów z HIV przyjmujących skojarzenie sakwinawiru z rytonawirem, darunawirem z rytonawirem, fosamprenawirem, fosamprenawirem z rytonawirem lub letermowirem leczenie LIPITORem powinno być ograniczone do 20 mg i należy przeprowadzić odpowiednią ocenę kliniczną zaleca się stosowanie najmniejszej niezbędnej dawki LIPITORA 20 mg. U pacjentów przyjmujących inhibitor proteazy HIV leczenie nelfinawirem z zastosowaniem preparatu LIPITOR 10 mg powinno być ograniczone do 40 mg [patrz OSTRZEŻENIA I ŚRODKI oraz INTERAKCJE Z LEKAMI ].
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Tabletki LIPITOR są białe, eliptyczne, powlekane i są dostępne w czterech mocach (patrz Tabela 1).
Składowania i stosowania
Tabletki 10 mg (10 mg atorwastatyny): kod „PD 155” po jednej stronie i „10” po drugiej.
NDC 0071-0155-23 butelki 90 NDC 0071-0155-40 10 blistrów po 10 dawek jednostkowych
Tabletki 20 mg (20 mg atorwastatyny): kod „PD 156” po jednej stronie i „20” po drugiej.
NDC 0071-0156-23 butelki 90 NDC 0071-0156-40 10 blistrów po 10 dawek jednostkowych
Tabletki 40 mg (40 mg atorwastatyny): kod „PD 157” po jednej stronie i „40” po drugiej.
NDC 0071-0157-23 butelki 90 NDC 0071-0157-40 10 blistrów po 10 dawek jednostkowych
Tabletki 80 mg (80 mg atorwastatyny): kod „PD 158” po jednej stronie i „80” po drugiej.
NDC 0071-0158-23 butelki 90 NDC 0071-0158-73 butelki po 500 NDC 0071-0158-92 8 blistrów po 8 dawek jednostkowych
Magazynowanie
Przechowywać w kontrolowanej temperaturze pokojowej 20–25°C (68–77°F) [patrz USP].
Dystrybutor: Parke-Davis, oddział Pfizer Inc., NY, NY 10017. Aktualizacja: sierpień 2021
SKUTKI UBOCZNE
Następujące poważne działania niepożądane omówiono bardziej szczegółowo w innych sekcjach etykiety:
- Miopatia i rabdomioliza [patrz OSTRZEŻENIA I ŚRODKI ]
- Nieprawidłowości enzymów wątrobowych [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
bazie danych kontrolowanych placebo badań klinicznych LIPITOR z udziałem 16 066 pacjentów (8755 LIPITOR vs. 7311 placebo; przedział wiekowy 10-93 lata, 39% kobiet, 91% rasy kaukaskiej, 3% rasy czarnej, 2% Azjatów, 4% innych) z medianą czas trwania leczenia wynoszący 53 tygodnie, 9,7% pacjentów przyjmujących LIPITOR 10 mg i 9,5% pacjentów otrzymujących placebo przerwało leczenie z powodu działań niepożądanych bez względu na przyczynę. Pięć najczęstszych działań niepożądanych u pacjentów leczonych preparatem LIPITOR 20 mg, które doprowadziły do przerwania leczenia i występowały z częstością większą niż placebo, to: ból mięśni (0,7%), biegunka (0,5%), nudności (0,4%), wzrost aktywności aminotransferazy alaninowej (0,4 %), oraz wzrost enzymów wątrobowych (0,4%).
Najczęściej zgłaszanymi działaniami niepożądanymi (częstość występowania ≥ 2% i większa niż w przypadku placebo) niezależnie od przyczyny, u pacjentów leczonych preparatem LIPITOR w badaniach kontrolowanych placebo (n=8755) były: zapalenie nosogardzieli (8,3%), ból stawów (6,9%), biegunka ( 6,8%, bóle kończyn (6,0%) i infekcje dróg moczowych (5,7%).
Tabeli 2 podsumowano częstość występowania klinicznych działań niepożądanych, niezależnie od przyczynowości, zgłaszanych u ≥ 2% i z częstością większą niż placebo u pacjentów leczonych preparatem LIPITOR (n=8755), w siedemnastu badaniach kontrolowanych placebo.
Inne działania niepożądane zgłaszane w badaniach kontrolowanych placebo obejmują:
Ciało jako całość: złe samopoczucie, gorączka; Układ trawienny: dyskomfort w jamie brzusznej, odbijanie się, wzdęcia, zapalenie wątroby, cholestaza; Układ mięśniowo-szkieletowy: ból mięśniowo-szkieletowy, zmęczenie mięśni, ból szyi, obrzęk stawów; Układ metaboliczny i żywieniowy: zwiększenie aktywności aminotransferaz, nieprawidłowe wyniki testów czynności wątroby, zwiększenie aktywności fosfatazy alkalicznej we krwi, zwiększenie aktywności fosfokinazy kreatynowej, hiperglikemia; System nerwowy: koszmar; Układ oddechowy: krwawienie z nosa; Skóra i przydatki: pokrzywka; Specjalne zmysły: niewyraźne widzenie, szum w uszach; Układ moczowo-płciowy: białe krwinki dodatnie w moczu.
Anglo-Scandinavian Cardiac Outcomes Trial (ASCOT)
W ASCOT [patrz Studia kliniczne z udziałem 10305 uczestników (przedział wiekowy 40-80 lat, 19% kobiet; 94,6% rasy kaukaskiej, 2,6% Afrykanów, 1,5% mieszkańców Azji Południowej, 1,3% osób mieszanych/innych) leczonych preparatem LIPITOR 10 mg na dobę (n=5168) lub placebo (n =5137), profil bezpieczeństwa i tolerancji w grupie leczonej LIPITOREM 10 mg był porównywalny z profilem w grupie leczonej placebo podczas mediany 3,3 roku obserwacji.
Wspólne badanie atorwastatyny na temat cukrzycy (CARDS)
W KARTACH [patrz Studia kliniczne ] z udziałem 2838 osób (przedział wiekowy 39-77 lat, 32% kobiet; 94,3% rasy kaukaskiej, 2,4% mieszkańców Azji Południowej, 2,3% mieszkańców afro-karaibskich, 1,0% innych) z cukrzycą typu 2 leczonych preparatem LIPITOR w dawce 10 mg na dobę (n = 1428) lub placebo (n=1410), nie było różnicy w ogólnej częstości występowania działań niepożądanych lub ciężkich działań niepożądanych między leczonymi grupami w okresie obserwacji o medianie 3,9 roku. Nie zgłoszono przypadków rabdomiolizy.
Badanie dotyczące nowych celów (TNT)
W TNT [patrz Studia kliniczne z udziałem 10 001 pacjentów (zakres wieku 29-78 lat, 19% kobiet; 94,1% rasy kaukaskiej, 2,9% rasy czarnej, 1,0% Azjatów, 2,0% innych) z klinicznie wyraźną CHD leczonych preparatem LIPITOR 10 mg na dobę (n=5006) lub LIPITOR 80 mg na dobę (n=4995), wystąpiły bardziej poważne działania niepożądane i przerwania leczenia z powodu działań niepożądanych w grupie otrzymującej duże dawki atorwastatyny (odpowiednio 92, 1,8%; 497, 9,9%) w porównaniu z grupą otrzymującą małą dawkę (69). , 1,4%; 404, 8,1%, odpowiednio) w okresie obserwacji o medianie 4,9 roku. Trwałe podwyższenie aktywności aminotransferaz (≥3 x GGN dwukrotnie w ciągu 4-10 dni) wystąpiło u 62 (1,3%) osób z atorwastatyną 80 mg i u dziewięciu (0,2%) osób z atorwastatyną w dawce 10 mg. Wzrost CK (≥ 10 x GGN) był ogólnie niski, ale był wyższy w grupie leczonej dużą dawką atorwastatyny (13, 0,3%) w porównaniu z grupą leczoną małą dawką atorwastatyny (6, 0,1%).
Przyrostowe zmniejszenie liczby punktów końcowych w badaniu agresywnego obniżania poziomu lipidów (IDEAL)
W IDEALNYM [patrz Studia kliniczne z udziałem 8888 pacjentów (przedział wiekowy 26-80 lat, 19% kobiet; 99,3% rasy kaukaskiej, 0,4% Azjatów, 0,3% rasy czarnej, 0,04% innych) leczonych preparatem LIPITOR 80 mg/dobę (n=4439) lub symwastatyną 20-40 mg dziennie (n=4449), nie było różnicy w ogólnej częstości występowania działań niepożądanych lub ciężkich działań niepożądanych między leczonymi grupami w okresie obserwacji o medianie 4,8 roku.
Zapobieganie udarom poprzez agresywną redukcję poziomu cholesterolu (SPARCL)
badaniu SPARCL obejmującym 4731 osób (zakres wieku 21-92 lata, 40% kobiet; 93,3% rasy kaukaskiej, 3,0% czarnoskórych, 0,6% Azjatów, 3,1% innych) bez klinicznie widocznej CHD, ale z udarem lub przemijającym napadem niedokrwiennym (TIA) w ciągu w ciągu ostatnich 6 miesięcy otrzymujących LIPITOR w dawce 80 mg (n=2365) lub placebo (n=2366) przez medianę okresu obserwacji wynoszącą 4,9 roku, występowała większa częstość występowania przetrwałego zwiększenia aktywności aminotransferaz wątrobowych (≥ 3 x GGN dwukrotnie w ciągu 4-10 lat). dni) w grupie atorwastatyny (0,9%) w porównaniu z placebo (0,1%). Zwiększenie aktywności CK (>10 x GGN) było rzadkie, ale większe w grupie atorwastatyny (0,1%) w porównaniu z placebo (0,0%). Cukrzycę jako działanie niepożądane zgłoszono u 144 pacjentów (6,1%) w grupie atorwastatyny i 89 pacjentów (3,8%) w grupie placebo [patrz OSTRZEŻENIA I ŚRODKI ].
analizie post-hoc LIPITOR 80 mg zmniejszył częstość występowania udaru niedokrwiennego mózgu (218/2365, 9,2% vs. 274/2366, 11,6%) i zwiększył częstość występowania udaru krwotocznego (55/2365, 2,3% vs. 33/ 2366, 1,4%) w porównaniu z placebo. Częstość występowania śmiertelnego udaru krwotocznego była podobna w obu grupach (17 LIPITOR 40 mg vs. 18 placebo). Częstość występowania udarów krwotocznych niezakończonych zgonem była istotnie większa w grupie atorwastatyny (38 udarów krwotocznych niezakończonych zgonem) w porównaniu z grupą placebo (16 udarów krwotocznych niezakończonych zgonem). Osoby, które zgłosiły się do badania z udarem krwotocznym, wydawały się mieć zwiększone ryzyko udaru krwotocznego [7 (16%) LIPITOR vs. 2 (4%) placebo].
Nie było istotnych różnic między grupami leczenia pod względem śmiertelności z jakiejkolwiek przyczyny: 216 (9,1%) w grupie LIPITOR 80 mg/dobę vs. 211 (8,9%) w grupie placebo. Odsetki osób, które doświadczyły zgonu z przyczyn sercowo-naczyniowych były liczbowo mniejsze w grupie LIPITOR 80 mg (3,3%) niż w grupie placebo (4,1%). Odsetki osób, które doświadczyły zgonu pozasercowo-naczyniowego, były liczbowo większe w grupie LIPITOR 80 mg (5,0%) niż w grupie placebo (4,0%).
Działania niepożądane z badań klinicznych LIPITOR 20 mg u pacjentów pediatrycznych
W 26-tygodniowym kontrolowanym badaniu z udziałem chłopców i dziewcząt w wieku pomenarchalnym z HeFH (w wieku od 10 do 17 lat) (n=140, 31% kobiet; 92% rasy kaukaskiej, 1,6% czarnoskórych, 1,6% Azjatów, 4,8% innych) bezpieczeństwo a profil tolerancji LIPITORA 10 do 20 mg na dobę, jako dodatku do diety w celu obniżenia poziomu cholesterolu całkowitego, LDL-C i apo B, był ogólnie podobny do placebo [patrz Używaj w specjalnych populacjach oraz Studia kliniczne ].
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania preparatu LIPITOR po dopuszczeniu do obrotu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Działania niepożądane związane z leczeniem LIPITOREM zgłaszane od momentu wprowadzenia na rynek, które nie zostały wymienione powyżej, niezależnie od oceny przyczynowości, obejmują: anafilaksję, obrzęk naczynioruchowy, wysypkę pęcherzową (w tym rumień wielopostaciowy, zespół Stevensa-Johnsona i toksyczne martwicze oddzielanie się naskórka), rabdomiolizę , zapalenie mięśni, zmęczenie, zerwanie ścięgna, śmiertelna i niezakończona zgonem niewydolność wątroby, zawroty głowy, depresja, neuropatia obwodowa, zapalenie trzustki i śródmiąższowa choroba płuc.
Istnieją rzadkie doniesienia o martwiczej miopatii o podłożu immunologicznym, związanej ze stosowaniem statyn [patrz OSTRZEŻENIA I ŚRODKI ].
Po wprowadzeniu do obrotu rzadko zgłaszano zaburzenia funkcji poznawczych (np. utrata pamięci, zapominanie, amnezja, zaburzenia pamięci, splątanie) związane ze stosowaniem statyn. Te problemy poznawcze zostały zgłoszone dla wszystkich statyn. Zgłoszenia na ogół nie są poważne i ustępują po odstawieniu statyn, ze zmiennym czasem do wystąpienia objawów (1 dzień do lat) i ustąpienia objawów (mediana 3 tygodnie).
INTERAKCJE Z LEKAMI
Interakcje leków, które mogą zwiększać ryzyko miopatii i rabdomiolizy z LIPITOREM
LIPITOR jest substratem CYP3A4 i transporterów (np. OATP1B1/1B3, P-gp lub BCRP). Podczas jednoczesnego podawania inhibitorów CYP3A4 i transporterów, stężenia LIPITORA w osoczu mogą być znacznie zwiększone. Tabela 3 zawiera listę leków, które mogą zwiększać ekspozycję na Lipitor i mogą zwiększać ryzyko miopatii i rabdomiolizy podczas jednoczesnego stosowania oraz instrukcje dotyczące ich zapobiegania lub postępowania [patrz OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
Interakcje leków, które mogą zmniejszyć ekspozycję na LIPITORY
tabeli 4 przedstawiono interakcje leków, które mogą zmniejszać ekspozycję na LIPITOR 20mg oraz instrukcje dotyczące ich zapobiegania lub postępowania.
LIPITOR 20mg Wpływ na inne leki
Tabela 5 przedstawia wpływ LIPITORA na inne leki oraz instrukcje dotyczące zapobiegania im lub postępowania z nimi.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Miopatia i rabdomioliza
LIPITOR 10 mg może powodować miopatię (bóle mięśni, tkliwość lub osłabienie z kinazą kreatynową (CK) powyżej dziesięciokrotności górnej granicy normy) i rabdomiolizę (z ostrą niewydolnością nerek wtórną do mioglobinurii lub bez). Rzadko zdarzały się zgony w wyniku rabdomiolizy po zastosowaniu statyn, w tym LIPITORA.
Czynniki ryzyka miopatii
Czynniki ryzyka miopatii obejmują wiek 65 lat lub więcej, niekontrolowaną niedoczynność tarczycy, zaburzenia czynności nerek, jednoczesne stosowanie niektórych innych leków oraz wyższą dawkę LIPITORA [patrz INTERAKCJE Z LEKAMI ].
Kroki, aby zapobiec lub zmniejszyć ryzyko miopatii i rabdomiolizy
Ekspozycja na LIPITOR może być zwiększona przez interakcje leków z powodu hamowania enzymu 3A4 cytochromu P450 (CYP3A4) i/lub transporterów (np. białka opornego na raka piersi [BCRP], polipeptydu transportującego aniony organiczne [OATP1B1/OATP1B3] i glikoproteiny P [P -gp]), co powoduje zwiększone ryzyko miopatii i rabdomiolizy. Nie zaleca się jednoczesnego stosowania cyklosporyny, gemfibrozylu, typranawiru z rytonawirem lub glekaprewiru z pibrentaswirem z preparatem LIPITOR. Modyfikacje dawki LIPITOR 40 mg są zalecane u pacjentów przyjmujących niektóre leki przeciwwirusowe, przeciwgrzybicze z grupy azoli lub antybiotyki makrolidowe [patrz DAWKOWANIE I SPOSÓB PODAWANIA ]. Zgłaszano przypadki miopatii/rabdomiolizy podczas jednoczesnego podawania atorwastatyny z dawkami modyfikującymi stężenie lipidów (>1 gram/dobę) niacyny, fibratów, kolchicyny i ledipaswiru z sofosbuwirem. Zastanów się, czy korzyści ze stosowania tych produktów przewyższają zwiększone ryzyko miopatii i rabdomiolizy [patrz INTERAKCJE Z LEKAMI ].
Nie zaleca się jednoczesnego spożywania dużych ilości, ponad 1,2 litra dziennie, soku grejpfrutowego u pacjentów przyjmujących LIPITOR [patrz INTERAKCJE Z LEKAMI ].
Odstawić LIPITOR, jeśli wystąpi znacznie podwyższony poziom CK lub zdiagnozowana lub podejrzewana jest miopatia. Objawy dotyczące mięśni i wzrost CK mogą ustąpić po odstawieniu leku LIPITOR. Tymczasowo odstawić LIPITOR 40 mg u pacjentów z ostrym lub poważnym stanem z wysokim ryzykiem rozwoju niewydolności nerek wtórnej do rabdomiolizy (np. posocznica; wstrząs; ciężka hipowolemia; poważny zabieg chirurgiczny; uraz; ciężkie zaburzenia metaboliczne, endokrynologiczne lub elektrolitowe; lub niekontrolowana padaczka) .
Poinformuj pacjentów o ryzyku miopatii i rabdomiolizy podczas rozpoczynania lub zwiększania dawki leku LIPITOR. Należy poinstruować pacjentów, aby niezwłocznie zgłaszali wszelkie niewyjaśnione bóle, tkliwość lub osłabienie mięśni, zwłaszcza jeśli towarzyszy im złe samopoczucie lub gorączka.
Miopatia martwicza o podłożu immunologicznym
Istnieją rzadkie doniesienia o miopatii martwiczej o podłożu immunologicznym (IMNM), autoimmunologicznej miopatii związanej ze stosowaniem statyn. IMNM charakteryzuje się: osłabieniem mięśni proksymalnych oraz podwyższoną aktywnością kinazy kreatynowej w surowicy, która utrzymuje się pomimo przerwania leczenia statynami; pozytywne przeciwciało przeciw reduktazie HMG CoA; biopsja mięśnia wykazująca martwiczą miopatię; i poprawa za pomocą środków immunosupresyjnych. Konieczne mogą być dodatkowe badania nerwowo-mięśniowe i serologiczne. Może być konieczne leczenie środkami immunosupresyjnymi. Przed rozpoczęciem stosowania innej statyny należy dokładnie rozważyć ryzyko IMNM. Jeśli leczenie rozpoczyna się od innej statyny, należy monitorować objawy przedmiotowe i podmiotowe IMNM.
Dysfunkcja wątroby
Statyny, podobnie jak niektóre inne terapie obniżające poziom lipidów, są związane z zaburzeniami biochemicznymi funkcji wątroby. Trwałe zwiększenie aktywności aminotransferaz w surowicy (>3-krotność górnej granicy normy [GGN] występujące co najmniej 2 razy) wystąpiło u 0,7% pacjentów, którzy otrzymywali LIPITOR w badaniach klinicznych. Częstość występowania tych nieprawidłowości wynosiła 0,2%, 0,2%, 0,6% i 2,3% dla odpowiednio 10, 20, 40 i 80 mg.
U jednego pacjenta w badaniach klinicznych rozwinęła się żółtaczka. Zwiększenie wyników testów czynności wątroby (LFT) u innych pacjentów nie było związane z żółtaczką ani innymi klinicznymi oznakami lub objawami. Po zmniejszeniu dawki, przerwaniu lub zaprzestaniu podawania leku, poziomy transaminaz powróciły do lub zbliżyły się do poziomów sprzed leczenia bez następstw. Osiemnastu z 30 pacjentów z utrzymującym się podwyższeniem LFT kontynuowało leczenie zmniejszoną dawką LIPITORA.
Zaleca się wykonanie testów enzymów wątrobowych przed rozpoczęciem leczenia preparatem LIPITOR 40 mg i powtórzenie ich zgodnie ze wskazaniami klinicznymi. Po wprowadzeniu produktu do obrotu odnotowano rzadkie przypadki niewydolności wątroby zakończonej zgonem lub niezakończonej zgonem u pacjentów przyjmujących statyny, w tym atorwastatynę. Jeśli podczas leczenia preparatem LIPITOR 10 mg wystąpi poważne uszkodzenie wątroby z objawami klinicznymi i/lub hiperbilirubinemią lub żółtaczką, należy niezwłocznie przerwać leczenie. Jeśli nie zostanie znaleziona alternatywna etiologia, nie uruchamiaj ponownie LIPITORA.
LIPITOR 10 mg należy stosować ostrożnie u pacjentów, którzy spożywają znaczne ilości alkoholu i (lub) mają historię choroby wątroby. Aktywna choroba wątroby lub niewyjaśnione utrzymujące się podwyższenie aktywności aminotransferaz są przeciwwskazaniami do stosowania LIPITORA [patrz PRZECIWWSKAZANIA ].
Funkcja hormonalna
W przypadku inhibitorów reduktazy HMG-CoA, w tym LIPITOR, zgłaszano wzrost stężenia HbA1c i stężenia glukozy w surowicy na czczo.
Statyny zakłócają syntezę cholesterolu i teoretycznie mogą osłabiać produkcję sterydów nadnerczy i/lub gonad. Badania kliniczne wykazały, że LIPITOR 20 mg nie zmniejsza podstawowego stężenia kortyzolu w osoczu ani nie zaburza rezerwy nadnerczowej. Wpływ statyn na płodność mężczyzn nie był badany na odpowiedniej liczbie pacjentów. Ewentualny wpływ na oś przysadkowo-gonadową u kobiet przed menopauzą nie jest znany. Należy zachować ostrożność w przypadku jednoczesnego podawania statyny z lekami, które mogą zmniejszać stężenie lub aktywność endogennych hormonów steroidowych, takimi jak ketokonazol, spironolakton i cymetydyna.
Toksyczność OUN
Krwotok do mózgu zaobserwowano u suki leczonej przez 3 miesiące w dawce 120 mg/kg/dzień. Krwotok mózgowy i wakuolizację nerwu wzrokowego obserwowano u innej suki, która została uśmiercona w stanie agonalnym po 11 tygodniach zwiększania dawek do 280 mg/kg/dzień. Dawka 120 mg/kg skutkowała ogólnoustrojową ekspozycją około 16 razy większą niż powierzchnia pod krzywą ludzkiego osocza (AUC, 0–24 godziny) w oparciu o maksymalną dawkę u ludzi wynoszącą 80 mg/dobę. W 2-letnim badaniu u każdego z 2 psów płci męskiej (jeden leczony dawką 10 mg/kg/dobę, a drugi 120 mg/kg/dobę) zaobserwowano pojedynczy drgawki toniczne. Nie zaobserwowano uszkodzeń OUN u myszy po długotrwałym leczeniu przez okres do 2 lat w dawkach do 400 mg/kg/dobę lub u szczurów w dawkach do 100 mg/kg/dobę. Dawki te były 6 do 11 razy (myszy) i 8 do 16 razy (szczury) większe od AUC u ludzi (0–24) w oparciu o maksymalną zalecaną dawkę u ludzi wynoszącą 80 mg/dobę.
psów leczonych innymi przedstawicielami tej klasy obserwowano zmiany naczyniowe OUN, charakteryzujące się krwotokami okołonaczyniowymi, obrzękiem i naciekiem komórek jednojądrzastych przestrzeni okołonaczyniowych. Chemicznie podobny lek w tej klasie powodował zwyrodnienie nerwu wzrokowego (zwyrodnienie Walleriana włókien siatkówkowatych) u klinicznie zdrowych psów w sposób zależny od dawki w dawce, która powodowała stężenie leku w osoczu około 30 razy wyższe niż średni poziom leku u ludzi przyjmujących najwyższe dawki. zalecana dawka.
Stosowanie u pacjentów z niedawno przebytym udarem mózgu lub TIA
analizie post hoc badania Stroke Prevention by Aggressive Reduction in Cholesterol Levels (SPARCL), w którym LIPITOR 80 mg w porównaniu z placebo podawano 4731 pacjentom bez CHD, którzy przebyli udar lub TIA w ciągu ostatnich 6 miesięcy, wyższa częstość występowania udar krwotoczny obserwowano w grupie LIPITOR 80 mg w porównaniu z placebo (55, 2,3% atorwastatyna vs. 33, 1,4% placebo; HR: 1,68, 95% CI: 1,09, 2,59; p=0,0168). Częstość występowania śmiertelnego udaru krwotocznego była podobna we wszystkich grupach terapeutycznych (odpowiednio 17 vs. 18 w grupach atorwastatyny i placebo). Częstość występowania udaru krwotocznego niezakończonego zgonem była istotnie wyższa w grupie atorwastatyny (38, 1,6%) w porównaniu z grupą placebo (16, 0,7%).
Niektóre cechy wyjściowe, w tym udar krwotoczny i udar lakunarny w momencie włączenia do badania, były związane z większą częstością występowania udaru krwotocznego w grupie atorwastatyny [patrz DZIAŁANIA NIEPOŻĄDANE ].
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( INFORMACJA O PACJENCIE ).
Pacjenci przyjmujący LIPITOR 10 mg powinni być poinformowani, że cholesterol jest chorobą przewlekłą i powinni stosować się do ich leków wraz z dietą zalecaną przez Narodowy Program Edukacji Cholesterolowej (NCEP), regularnymi ćwiczeniami fizycznymi oraz okresowymi testami panelu lipidowego na czczo w celu określić osiągnięcie celu.
Pacjentów należy poinformować o substancjach, których nie powinni przyjmować jednocześnie z atorwastatyną [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI]. Pacjentom należy również doradzić, aby informowali innych pracowników służby zdrowia przepisujących nowy lek, że przyjmują LIPITOR.
Ból w mięśniach
Wszystkich pacjentów rozpoczynających leczenie preparatem LIPITOR należy poinformować o ryzyku wystąpienia miopatii i poinstruować, aby niezwłocznie zgłaszali wszelkie niewyjaśnione bóle, tkliwość lub osłabienie mięśni, szczególnie jeśli towarzyszy im złe samopoczucie lub gorączka lub jeśli te objawy przedmiotowe lub podmiotowe mięśni utrzymują się po odstawieniu preparatu LIPITOR. Ryzyko takiego wystąpienia jest zwiększone w przypadku przyjmowania niektórych leków lub spożywania większych ilości (>1 litra) soku grejpfrutowego. Powinni omówić wszystkie leki, zarówno na receptę, jak i bez recepty, ze swoim lekarzem.
Enzymy wątrobowe
Zaleca się wykonanie testów enzymów wątrobowych przed rozpoczęciem stosowania leku LIPITOR 40 mg oraz w przypadku wystąpienia oznak lub objawów uszkodzenia wątroby. Wszystkim pacjentom leczonym preparatem LIPITOR należy zalecić niezwłoczne zgłaszanie wszelkich objawów mogących wskazywać na uszkodzenie wątroby, w tym zmęczenia, anoreksji, dyskomfortu w prawym nadbrzuszu, ciemnego moczu lub żółtaczki.
Toksyczność zarodkowo-płodowa
Poinformuj kobiety o potencjale reprodukcyjnym ryzyka dla płodu, aby stosowały skuteczną antykoncepcję podczas leczenia i informowały swojego lekarza o stwierdzonej lub podejrzewanej ciąży [patrz PRZECIWWSKAZANIA oraz Używaj w określonych populacjach ].
Laktacja
Poradzić kobietom, aby nie karmiły piersią podczas leczenia preparatem LIPITOR [patrz PRZECIWWSKAZANIA oraz Używaj w określonych populacjach ].
Etykieta tego produktu mogła zostać zaktualizowana. Najnowsze informacje na temat przepisywania leków można znaleźć na stronie www.pfizer.com.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
W 2-letnim badaniu rakotwórczości u szczurów przy dawkach 10, 30 i 100 mg/kg/dobę stwierdzono 2 rzadkie guzy mięśni u samic otrzymujących duże dawki: w jednym przypadku mięśniakomięsaka prążkowanokomórkowego, a w drugim, był włókniakomięsak. Ta dawka odpowiada wartości AUC (0–24) w osoczu około 16 razy większej od średniej ekspozycji na lek w osoczu człowieka po podaniu doustnym 80 mg.
Dwuletnie badanie rakotwórczości na myszach, którym podawano 100, 200 lub 400 mg/kg/dobę, spowodowało znaczny wzrost gruczolaków wątroby u samców otrzymujących dużą dawkę i raka wątroby u samic. Wyniki te wystąpiły przy wartościach AUC w osoczu (0–24) około 6 razy większych niż średnia ekspozycja na lek w osoczu u ludzi po podaniu doustnym dawki 80 mg.
In vitro atorwastatyna nie wykazywała działania mutagennego ani klastogennego w następujących testach z aktywacją metaboliczną i bez niej: test Amesa z Salmonella typhimurium i Escherichia coli, test mutacji postępującej HGPRT w komórkach płuc chomika chińskiego oraz test aberracji chromosomowych w komórkach płuc chomika chińskiego . Atorwastatyna dała wynik ujemny w teście mikrojądrowym in vivo u myszy.
samic szczurów atorwastatyna w dawkach do 225 mg/kg (56-krotność ekspozycji u ludzi) nie powodowała niekorzystnego wpływu na płodność. Badania na samcach szczurów przeprowadzone przy dawkach do 175 mg/kg (15-krotność ekspozycji u ludzi) nie wykazały zmian w płodności. U 2 z 10 szczurów, którym podawano atorwastatynę w dawce 100 mg/kg/dobę przez 3 miesiące (16-krotność ludzkiego AUC przy dawce 80 mg), wystąpiła aplazja i aspermia w najądrzach; masa jąder była znacznie niższa przy 30 i 100 mg/kg, a masa najądrza była niższa przy 100 mg/kg. Samce szczurów, którym podawano 100 mg/kg/dobę przez 11 tygodni przed kryciem, miały zmniejszoną ruchliwość plemników, koncentrację w główce plemników i zwiększoną liczbę nieprawidłowych plemników. Atorwastatyna nie wywierała niekorzystnego wpływu na parametry nasienia ani histopatologię narządów rozrodczych u psów, którym podawano dawki 10, 40 lub 120 mg/kg przez dwa lata.
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
LIPITOR 10 mg jest przeciwwskazany do stosowania u kobiet w ciąży, ponieważ bezpieczeństwo u kobiet w ciąży nie zostało ustalone i nie ma widocznych korzyści ze stosowania leków obniżających stężenie lipidów podczas ciąży. Ponieważ inhibitory reduktazy HMG-CoA zmniejszają syntezę cholesterolu i prawdopodobnie syntezę innych substancji biologicznie czynnych pochodzących z cholesterolu, LIPITOR może powodować uszkodzenie płodu po podaniu kobiecie w ciąży. Należy odstawić LIPITOR 40 mg natychmiast po stwierdzeniu ciąży [patrz PRZECIWWSKAZANIA ]. Ograniczone opublikowane dane dotyczące stosowania atorwastatyny są niewystarczające do określenia związanego z lekiem ryzyka poważnych wad wrodzonych lub poronienia. W badaniach na szczurach i królikach dotyczących reprodukcji na zwierzętach nie stwierdzono toksycznego działania na zarodek i płód ani wad wrodzonych po dawkach odpowiednio do 30 i 20-krotności ekspozycji u ludzi przy maksymalnej zalecanej dawce u ludzi (MRHD) wynoszącej 80 mg, w oparciu o powierzchnia (mg/m2). U szczurów, którym podawano atorwastatynę w okresie ciąży i laktacji, po dawkach ≥6 razy większych niż MRHD obserwowano spowolnienie wzrostu i rozwoju pourodzeniowego (patrz Dane ).
Szacowane ryzyko tła poważnych wad wrodzonych i poronienia dla wskazanej populacji jest nieznane. W ogólnej populacji USA szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2–4% i 15–20%.
Dane
Dane ludzkie
Ograniczone opublikowane dane dotyczące wapnia atorwastatyny pochodzące z badań obserwacyjnych, metaanaliz i opisów przypadków nie wykazały zwiększonego ryzyka poważnych wad wrodzonych lub poronienia. Rzadko zgłaszano przypadki wad wrodzonych po ekspozycji wewnątrzmacicznej na inne inhibitory reduktazy HMGCoA. W przeglądzie około 100 prospektywnie obserwowanych ciąż u kobiet narażonych na symwastatynę lub lowastatynę, częstość występowania wad wrodzonych, samoistnych poronień i zgonów/urodzeń martwych płodów nie przekroczyła oczekiwanej w populacji ogólnej. Liczba przypadków jest wystarczająca, aby wykluczyć ≥3 do 4-krotny wzrost wad wrodzonych w stosunku do podstawowej częstości występowania. W 89% ciąż obserwowanych prospektywnie leczenie farmakologiczne rozpoczęto przed zajściem w ciążę i przerwano w pewnym momencie pierwszego trymestru, po stwierdzeniu ciąży.
Dane zwierząt
Atorwastatyna przenika przez łożysko szczura i osiąga w wątrobie płodu poziom odpowiadający poziomowi w osoczu matki. Atorwastatynę podawano ciężarnym szczurom i królikom podczas organogenezy w dawkach doustnych odpowiednio do 300 mg/kg/dobę i 100 mg/kg/dobę. Atorwastatyna nie wykazywała działania teratogennego u szczurów w dawkach do 300 mg/kg/dobę ani u królików w dawkach do 100 mg/kg/dobę. Dawki te skutkowały wielokrotnością około 30-krotności (szczur) lub 20-krotności (królik) ekspozycji człowieka na MRHD w oparciu o powierzchnię (mg/m2). U szczurów dawka toksyczna dla matki 300 mg/kg powodowała zwiększenie poronień po implantacji i zmniejszenie masy ciała płodów. Przy dawkach toksycznych dla matki 50 i 100 mg/kg/dobę u królików obserwowano zwiększoną utratę poimplantacyjną, a przy 100 mg/kg/dobę masa ciała płodów była zmniejszona.
badaniu na ciężarnych szczurach, którym podawano 20, 100 lub 225 mg/kg/dobę od 7. dnia ciąży do 20. dnia laktacji (odstawienie od matki), zaobserwowano zmniejszenie przeżywalności po urodzeniu, 4. dniu po urodzeniu, odsadzeniu i po odsadzeniu u młodych. matek, którym podawano 225 mg/kg/dobę, dawkę, przy której zaobserwowano toksyczność matczyną. Masa ciała młodych zmniejszyła się do 21 dnia po urodzeniu o 100 mg/kg/dobę i do 91 dnia po urodzeniu o 225 mg/kg/dobę. Rozwój młodych był opóźniony (wydajność rotarod przy 100 mg/kg/dzień i przerażenie akustyczne przy 225 mg/kg/dzień; oderwanie małżowiny usznej i otwarcie oczu przy 225 mg/kg/dzień). Dawki te odpowiadają 6-krotności (100 mg/kg) i 22-krotności (225 mg/kg) ekspozycji u ludzi przy MRHD, na podstawie AUC.
Laktacja
Podsumowanie ryzyka
Stosowanie LIPITORa 40 mg jest przeciwwskazane w okresie karmienia piersią [patrz PRZECIWWSKAZANIA ]. Brak dostępnych informacji na temat wpływu leku na niemowlę karmione piersią lub wpływu leku na produkcję mleka. Nie wiadomo, czy atorwastatyna jest obecna w mleku ludzkim, ale wykazano, że inny lek z tej klasy przenika do mleka ludzkiego, a atorwastatyna jest obecna w mleku szczurzym. Ze względu na możliwość wystąpienia poważnych działań niepożądanych u niemowlęcia karmionego piersią należy poinformować kobiety, że nie zaleca się karmienia piersią podczas leczenia preparatem LIPITOR.
Kobiety i mężczyźni o potencjale rozrodczym
Zapobieganie ciąży
LIPITOR może spowodować uszkodzenie płodu, gdy zostanie podany kobiecie w ciąży. Doradzić kobietom o potencjale rozrodczym stosowanie skutecznej antykoncepcji podczas leczenia preparatem LIPITOR [patrz Używaj w określonych populacjach ].
Zastosowanie pediatryczne
Heterozygotyczna hipercholesterolemia rodzinna (HeFH)
Bezpieczeństwo i skuteczność preparatu LIPITOR 20 mg zostały ustalone u pacjentów pediatrycznych w wieku od 10 do 17 lat, z HeFH jako uzupełnieniem diety w celu obniżenia poziomu cholesterolu całkowitego, LDL-C i apo B, gdy po odpowiedniej próbie diety terapii, obecne są:
- LDL-C ≥ 190 mg/dl lub
- LDL-C ≥ 160 mg/dl i
- dodatni wywiad rodzinny w kierunku FH lub przedwczesnej CVD u krewnego pierwszego lub drugiego stopnia lub
- występują dwa lub więcej innych czynników ryzyka CVD.
Stosowanie preparatu LIPITOR 20 mg w tym wskazaniu jest poparte dowodami z [patrz DAWKOWANIE I SPOSÓB PODAWANIA , DZIAŁANIA NIEPOŻĄDANE , FARMAKOLOGIA KLINICZNA , oraz Studia kliniczne ]:
- Badanie kliniczne kontrolowane placebo trwające 6 miesięcy z udziałem 187 chłopców i dziewcząt w wieku od 10 do 17 lat po menarchii. Profil działań niepożądanych u pacjentów otrzymujących 10 mg lub 20 mg na dobę preparatu LIPITOR był zasadniczo podobny do profilu pacjentów otrzymujących placebo. W tym ograniczonym kontrolowanym badaniu nie stwierdzono znaczącego wpływu na wzrost lub dojrzewanie płciowe u chłopców ani na długość cyklu miesiączkowego u dziewcząt.
- Trzyletnie otwarte, niekontrolowane badanie, w którym wzięło udział 163 pacjentów pediatrycznych w wieku od 10 do 15 lat z HeFH, u których miareczkowano tak, aby osiągnąć docelowy poziom LDL-C
Poinformuj dziewczęta w wieku pomenarchalnym o zaleceniach dotyczących antykoncepcji, jeśli jest to właściwe dla pacjentki [patrz Używaj w określonych populacjach ].
Nie ustalono długoterminowej skuteczności terapii LIPITORem rozpoczętej w dzieciństwie w zmniejszaniu zachorowalności i śmiertelności w wieku dorosłym.
Nie ustalono bezpieczeństwa i skuteczności preparatu LIPITOR 10 mg u dzieci i młodzieży w wieku poniżej 10 lat z HeFH.
Homozygotyczna rodzinna hipercholesterolemia (HoFH)
Skuteczność kliniczną preparatu LIPITOR 20 mg w dawkach do 80 mg/dobę przez 1 rok oceniano w niekontrolowanym badaniu z udziałem pacjentów z HoFH obejmującym 8 pacjentów pediatrycznych [patrz Studia kliniczne ].
Zastosowanie geriatryczne
Spośród 39 828 pacjentów, którzy otrzymywali LIPITOR 40 mg w badaniach klinicznych, 15 813 (40%) było w wieku ≥65 lat, a 2800 (7%) miało ≥75 lat. Nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między tymi pacjentami a młodszymi pacjentami, a inne zgłoszone doświadczenia kliniczne nie wykazały różnic w odpowiedziach między pacjentami w podeszłym wieku i młodszymi, ale nie można wykluczyć większej wrażliwości niektórych osób w podeszłym wieku. Ponieważ zaawansowany wiek (≥65 lat) jest czynnikiem predysponującym do miopatii, LIPITOR należy przepisywać ostrożnie u osób w podeszłym wieku.
Niewydolność wątroby
Lipitor jest przeciwwskazany u pacjentów z czynną chorobą wątroby, która może obejmować niewyjaśnione utrzymujące się podwyższenie aktywności aminotransferaz wątrobowych [patrz PRZECIWWSKAZANIA oraz FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
Nie ma swoistego leczenia przedawkowania LIPITOR. W przypadku przedawkowania pacjent powinien być leczony objawowo i w razie potrzeby zastosować leczenie podtrzymujące. Ze względu na intensywne wiązanie leku z białkami osocza, nie oczekuje się, aby hemodializa znacząco zwiększyła klirens LIPITORA 20 mg.
PRZECIWWSKAZANIA
- Aktywna choroba wątroby, która może obejmować niewyjaśnione uporczywe podwyższenie poziomu transaminaz wątrobowych
- Nadwrażliwość na jakikolwiek składnik tego leku
- Ciąża [patrz Stosowanie w określonych populacjach].
- Laktacja [patrz Stosowanie w określonych populacjach].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
LIPITOR 20mg jest selektywnym, kompetycyjnym inhibitorem reduktazy HMG-CoA, enzymu ograniczającego szybkość przemiany 3-hydroksy-3-metyloglutarylo-koenzymu A do mewalonianu, prekursora steroli, w tym cholesterolu. W modelach zwierzęcych LIPITOR 40 mg obniża poziom cholesterolu i lipoprotein w osoczu poprzez hamowanie reduktazy HMG-CoA i syntezę cholesterolu w wątrobie oraz poprzez zwiększenie liczby wątrobowych receptorów LDL na powierzchni komórki w celu zwiększenia wychwytu i katabolizmu LDL; LIPITOR zmniejsza również produkcję LDL i liczbę cząsteczek LDL.
Farmakodynamika
LIPITOR, jak również niektóre jego metabolity, są farmakologicznie aktywne u ludzi. Wątroba jest głównym miejscem działania i głównym miejscem syntezy cholesterolu i usuwania LDL. Dawkowanie leku, a nie ogólnoustrojowe stężenie leku, lepiej koreluje z redukcją LDL-C. Indywidualizacja dawkowania leku powinna opierać się na odpowiedzi terapeutycznej [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Farmakokinetyka
Wchłanianie
LIPITOR jest szybko wchłaniany po podaniu doustnym; maksymalne stężenia w osoczu występują w ciągu 1 do 2 godzin. Stopień wchłaniania wzrasta proporcjonalnie do dawki LIPITORA. Całkowita biodostępność atorwastatyny (leku macierzystego) wynosi około 14%, a ogólnoustrojowa dostępność aktywności hamującej reduktazę HMG-CoA wynosi około 30%. Niską dostępność ogólnoustrojową przypisuje się klirensowi przedukładowemu w błonie śluzowej przewodu pokarmowego i (lub) metabolizmowi pierwszego przejścia w wątrobie. Chociaż jedzenie zmniejsza szybkość i stopień wchłaniania leku odpowiednio o około 25% i 9%, oceniane na podstawie Cmax i AUC, redukcja LDL-C jest podobna niezależnie od tego, czy LIPITOR 40 mg jest podawany z jedzeniem, czy bez jedzenia. Stężenia LIPITORA 20 mg w osoczu są niższe (około 30% dla Cmax i AUC) po podaniu leku wieczorem w porównaniu z porannym. Jednak redukcja LDL-C jest taka sama niezależnie od pory dnia podania leku [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Dystrybucja
Średnia objętość dystrybucji preparatu LIPITOR 20 mg wynosi około 381 litrów. LIPITOR 20 mg wiąże się z białkami osocza ≥98%. Stosunek krew/osocze około 0,25 wskazuje na słabą penetrację leku do czerwonych krwinek. Na podstawie obserwacji szczurów, LIPITOR 10 mg prawdopodobnie jest wydzielany do mleka ludzkiego [patrz PRZECIWWSKAZANIA oraz Używaj w określonych populacjach ].
Metabolizm
LIPITOR 20mg jest intensywnie metabolizowany do pochodnych orto- i parahydroksylowych oraz różnych produktów beta-oksydacji. In vitro hamowanie reduktazy HMG-CoA przez orto- i parahydroksylowane metabolity jest równoważne z hamowaniem LIPITORA. Około 70% aktywności hamującej krążenie reduktazy HMG-CoA przypisuje się aktywnym metabolitom. Badania in vitro sugerują znaczenie metabolizmu LIPITORa 40 mg przez cytochrom P450 3A4, zgodnie ze zwiększonym stężeniem LIPITORa 20 mg w osoczu u ludzi po jednoczesnym podaniu z erytromycyną, znanym inhibitorem tego izoenzymu [patrz INTERAKCJE Z LEKAMI ]. U zwierząt metabolit orto-hydroksylowy ulega dalszej glukuronidacji.
Wydalanie
LIPITOR 20 mg i jego metabolity są wydalane głównie z żółcią po metabolizmie wątrobowym i (lub) pozawątrobowym; wydaje się jednak, że lek nie podlega recyrkulacji jelitowo-wątrobowej. Średni okres półtrwania w fazie eliminacji preparatu LIPITOR z osocza u ludzi wynosi około 14 godzin, ale okres półtrwania aktywności hamującej reduktazy HMG-CoA wynosi od 20 do 30 godzin ze względu na udział aktywnych metabolitów. Mniej niż 2% dawki leku LIPITOR jest wydalane z moczem po podaniu doustnym.
Określone populacje
Geriatryczny
Stężenia LIPITORA w osoczu są wyższe (około 40% dla Cmax i 30% dla AUC) u zdrowych osób w podeszłym wieku (w wieku ≥ 65 lat) niż u młodych dorosłych. Dane kliniczne sugerują większy stopień obniżenia LDL przy każdej dawce leku w populacji pacjentów w podeszłym wieku w porównaniu z młodszymi dorosłymi [patrz Używaj w określonych populacjach ].
Pediatryczny
Pozorny klirens atorwastatyny po podaniu doustnym u dzieci i młodzieży wydawał się podobny do klirensu u dorosłych skalowanych allometrycznie według masy ciała, ponieważ masa ciała była jedyną istotną współzmienną w populacyjnym modelu farmakokinetycznym atorwastatyny z danymi obejmującymi dzieci i młodzież z HeFH (w wieku od 10 do 17 lat, n=29) w otwartym, 8-tygodniowym badaniu.
Płeć
Stężenia LIPITORA 40 mg w osoczu u kobiet różnią się od stężeń u mężczyzn (około 20% wyższe dla Cmax i 10% mniejsze dla AUC); jednak nie ma klinicznie istotnej różnicy w redukcji LDL-C po zastosowaniu LIPITORA 10 mg między mężczyznami i kobietami.
Zaburzenia czynności nerek
Choroba nerek nie ma wpływu na stężenie w osoczu lub redukcję LDL-C LIPITORA; dlatego dostosowanie dawki u pacjentów z zaburzeniami czynności nerek nie jest konieczne [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz OSTRZEŻENIA I ŚRODKI ].
Hemodializa
Chociaż nie przeprowadzono badań u pacjentów ze schyłkową niewydolnością nerek, nie oczekuje się, że hemodializa znacząco zwiększy klirens LIPITOR 10 mg, ponieważ lek silnie wiąże się z białkami osocza.
Niewydolność wątroby
pacjentów z przewlekłą alkoholową chorobą wątroby stężenie LIPITORA w osoczu jest znacznie zwiększone. Cmax i AUC są 4 razy większe u pacjentów z chorobą Childs-Pugh A. Cmax i AUC są odpowiednio około 16-krotnie i 11-krotnie większe u pacjentów z chorobą B Childs-Pugh [patrz PRZECIWWSKAZANIA ].
Badania interakcji leków
Atorwastatyna jest substratem transporterów wątrobowych, transportera OATP1B1 i OATP1B3. Metabolity atorwastatyny są substratami OATP1B1. Atorwastatyna jest również identyfikowana jako substrat transportera wypływowego BCRP, który może ograniczać wchłanianie jelitowe i klirens żółciowy atorwastatyny.
TABELA 6: Wpływ jednocześnie podawanych leków na farmakokinetykę atorwastatyny
TABELA 7: Wpływ atorwastatyny na farmakokinetykę jednocześnie podawanych leków
LIPITOR nie miał klinicznie istotnego wpływu na czas protrombinowy, gdy był podawany pacjentom przewlekle leczonym warfaryną.
Studia kliniczne
Zapobieganie chorobom układu krążenia
badaniu Anglo-Scandinavian Cardiac Outcomes Trial (ASCOT) wpływ preparatu LIPITOR 10 mg na chorobę wieńcową, która zakończyła się zgonem i która nie prowadziła do zgonu, oceniano u 10305 pacjentów z nadciśnieniem tętniczym w wieku 40–80 lat (średnio 63 lata), bez wcześniejszego zawału mięśnia sercowego. zawał i ze stężeniem TC ≤251 mg/dl (6,5 mmol/l). Dodatkowo wszyscy pacjenci mieli co najmniej 3 z następujących czynników ryzyka sercowo-naczyniowego: płeć męska (81,1%), wiek >55 lat (84,5%), palenie tytoniu (33,2%), cukrzyca (24,3%), wywiad CHD w względny stopień (26%), TC:HDL >6 (14,3%), choroba naczyń obwodowych (5,1%), przerost lewej komory (14,4%), wcześniejszy incydent naczyniowo-mózgowy (9,8%), swoiste nieprawidłowości EKG (14,3%), białkomocz /albuminuria (62,4%). W tym badaniu z podwójnie ślepą próbą, kontrolowanym placebo, pacjenci byli leczeni terapią przeciwnadciśnieniową (celowe BP
Wpływ 10 mg/dobę preparatu LIPITOR na poziom lipidów był podobny do obserwowanego w poprzednich badaniach klinicznych.
LIPITOR znacząco zmniejszył częstość występowania incydentów wieńcowych [albo śmiertelna choroba wieńcowa serca (46 zdarzeń w grupie placebo vs. 40 zdarzeń w grupie LIPITOR 40 mg) lub zawał serca niezakończony zgonem (108 zdarzeń w grupie placebo vs. 60 zdarzeń w grupie LIPITOR 20 mg)] ze względnym zmniejszeniem ryzyka o 36% [(na podstawie częstości występowania 1,9% dla LIPITOR 40 mg w porównaniu z 3,0% dla placebo), p=0,0005 (patrz Ryc. 1)]. Zmniejszenie ryzyka było stałe niezależnie od wieku, palenia tytoniu, otyłości lub obecności dysfunkcji nerek. Działanie LIPITORA było widoczne niezależnie od wyjściowego poziomu LDL. Ze względu na niewielką liczbę zdarzeń wyniki dla kobiet były niejednoznaczne.
Rycina 1: Wpływ leku LIPITOR 10 mg/dobę na łączną częstość występowania zawału mięśnia sercowego niezakończonego zgonem lub zgonu z powodu choroby wieńcowej serca (w ASCOT-LLA)
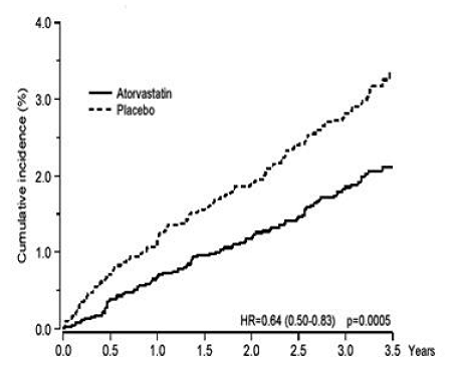
LIPITOR 40mg również znacząco zmniejszył względne ryzyko zabiegów rewaskularyzacji o 42% (częstość 1,4% dla LIPITOR 20mg i 2,5% dla placebo). Chociaż zmniejszenie liczby udarów śmiertelnych i niezakończonych zgonem nie osiągnęło wcześniej określonego poziomu istotności (p=0,01), zaobserwowano korzystną tendencję z 26% względną redukcją ryzyka (częstość występowania 1,7% dla LIPITORa i 2,3% dla placebo). . Nie było istotnej różnicy między grupami leczenia w przypadku zgonu z przyczyn sercowo-naczyniowych (p=0,51) lub przyczyn pozasercowych (p=0,17).
Collaborative Atorvastatin Diabetes Study (CARDS) wpływ preparatu LIPITOR na punkty końcowe choroby sercowo-naczyniowej (CVD) oceniano u 2838 pacjentów (94% rasy białej, 68% mężczyzn) w wieku 40–75 lat z cukrzycą typu 2 na podstawie kryteriów WHO, bez wcześniejszej choroby sercowo-naczyniowej oraz z LDL ≤ 160 mg/dl i TG ≤ 600 mg/dl. Oprócz cukrzycy u pacjentów występował co najmniej 1 z następujących czynników ryzyka: obecne palenie (23%), nadciśnienie (80%), retinopatia (30%) lub mikroalbuminuria (9%) lub makroalbuminuria (3%). Do badania nie włączono pacjentów poddawanych hemodializie. W tym wieloośrodkowym, kontrolowanym placebo badaniu klinicznym z podwójnie ślepą próbą, uczestników losowo przydzielono do grupy LIPITOR 10 mg na dobę (1429) lub placebo (1411) w stosunku 1:1 i byli obserwowani przez medianę czasu trwania wynoszącą 3,9 roku. Pierwszorzędowym punktem końcowym było wystąpienie któregokolwiek z głównych zdarzeń sercowo-naczyniowych: zawał mięśnia sercowego, zgon z powodu ostrej choroby niedokrwiennej serca, niestabilna dusznica bolesna, rewaskularyzacja wieńcowa lub udar mózgu. Analiza pierwotna obejmowała czas do pierwszego wystąpienia pierwszorzędowego punktu końcowego.
Wyjściowa charakterystyka badanych to: średni wiek 62 lata, średnia HbA 7,7%; mediana LDL-C 120 mg/dl; mediana TC 207 mg/dl; mediana TG 151 mg/dl; mediana HDL-C 52 mg/dl.
Wpływ preparatu LIPITOR 10 mg/dobę na poziom lipidów był podobny do obserwowanego w poprzednich badaniach klinicznych.
LIPITOR znacząco zmniejszył częstość występowania poważnych zdarzeń sercowo-naczyniowych (zdarzenia pierwszorzędowego punktu końcowego) (83 zdarzenia w grupie LIPITOR vs. 127 zdarzeń w grupie placebo) ze względną redukcją ryzyka o 37%, HR 0,63, 95% CI (0,48; 0,83) (p=0,001) (patrz Rysunek 2). Efekt stosowania LIPITORA był widoczny niezależnie od wieku, płci czy wyjściowych poziomów lipidów.
LIPITOR 20 mg istotnie zmniejszył ryzyko udaru mózgu o 48% (21 zdarzeń w grupie LIPITOR 10 mg vs 39 zdarzeń w grupie placebo), HR 0,52, 95% CI (0,31; 0,89) (p=0,016) i zmniejszył ryzyko MI o 42% (38 zdarzeń w grupie LIPITOR vs 64 zdarzenia w grupie placebo), HR 0,58, 95,1% CI (0,39, 0,86) (p=0,007). Nie było istotnej różnicy między grupami leczonymi pod względem dławicy piersiowej, zabiegów rewaskularyzacji i ostrej śmierci z powodu CHD.
Było 61 zgonów w grupie LIPITOR vs 82 zgony w grupie placebo (HR 0,73, p=0,059).
Rycina 2: Wpływ leku LIPITOR w dawce 10 mg/dobę na czas do wystąpienia poważnego incydentu sercowo-naczyniowego (zawał mięśnia sercowego, zgon z powodu ostrej choroby niedokrwiennej serca, niestabilna dusznica bolesna, rewaskularyzacja wieńcowa lub udar) w CARDS
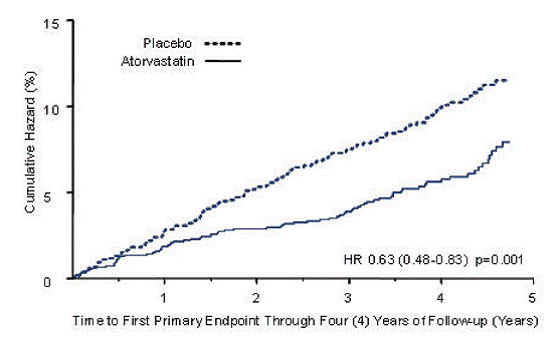
badaniu Treating to New Targets Study (TNT) wpływ leku LIPITOR 80 mg/dobę vs. LIPITOR 10 mg/dobę na zmniejszenie liczby incydentów sercowo-naczyniowych oceniano u 10 001 pacjentów (94% rasy białej, 81% mężczyzn, 38% ≥65). lat) z klinicznie ewidentną chorobą wieńcową serca, u których po zakończeniu 8-tygodniowego, otwartego okresu wstępnego z zastosowaniem leku LIPITOR 10 mg/dobę, docelowe stężenie LDL-C
Leczenie preparatem LIPITOR 80 mg/dobę znacząco zmniejszyło częstość występowania MCVE (434 zdarzenia w grupie 80 mg/dobę vs. 548 zdarzeń w grupie 10 mg/dobę) przy względnym zmniejszeniu ryzyka o 22%, HR 0,78, 95% CI (0,69; 0,89), p=0,0002 (patrz Ryc. 3 i Tabela 9). Całkowite zmniejszenie ryzyka było spójne niezależnie od wieku (
Rycina 3: Wpływ preparatu LIPITOR 80 mg/dobę vs. 10 mg/dobę na czas do wystąpienia poważnych incydentów sercowo-naczyniowych (TNT)
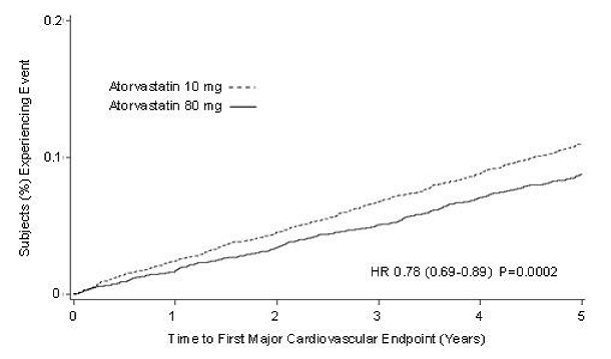
TABELA 8: Przegląd wyników skuteczności w TNT
Spośród zdarzeń składających się na pierwszorzędowy punkt końcowy skuteczności leczenie preparatem LIPITOR w dawce 80 mg/dobę znacząco zmniejszyło częstość występowania zawału serca niezakończonego zgonem, niezwiązanego z zabiegiem oraz udaru mózgu zakończonego i niezakończonego zgonem, ale nie zgonu z powodu CHD lub zatrzymania krążenia z powodu resuscytacji (Tabela 8). Spośród predefiniowanych drugorzędowych punktów końcowych leczenie preparatem LIPITOR w dawce 80 mg/dobę znacząco zmniejszyło częstość rewaskularyzacji wieńcowej, dusznicy bolesnej i hospitalizacji z powodu niewydolności serca, ale nie choroby naczyń obwodowych. Zmniejszenie częstości CHF podczas hospitalizacji zaobserwowano tylko u 8% pacjentów z wcześniejszą CHF.
Nie było istotnej różnicy między grupami leczenia pod względem śmiertelności z jakiejkolwiek przyczyny (Tabela 8). Odsetki osób, które doświadczyły zgonu z przyczyn sercowo-naczyniowych, w tym zgonów z powodu CHD i udaru śmiertelnego, były liczbowo mniejsze w grupie leczonej LIPITOR 80 mg niż w grupie leczonej LIPITOR 10 mg. Odsetki pacjentów, którzy doświadczyli zgonu z przyczyn pozasercowych, były liczbowo większe w grupie leczonej LIPITOR 80 mg niż w grupie leczonej LIPITOR 10 mg.
badaniu Incremental Decrease in Endpoints Through Aggressive Lipid Lowering Study (IDEAL) leczenie preparatem LIPITOR w dawce 80 mg/dobę porównywano z leczeniem symwastatyną w dawce 20–40 mg/dobę u 8888 pacjentów w wieku do 80 lat z wywiadem ocenić, czy można osiągnąć zmniejszenie ryzyka sercowo-naczyniowego. Pacjenci byli głównie mężczyznami (81%), rasy białej (99%) w średnim wieku 61,7 lat i średnim LDL-C 121,5 mg/dl w momencie randomizacji; 76% było na terapii statynami. W tym prospektywnym, randomizowanym, otwartym badaniu z zaślepionym punktem końcowym (PROBE) bez okresu wstępnego, pacjenci byli obserwowani przez medianę czasu trwania wynoszącą 4,8 roku. Średnie poziomy cholesterolu LDL-C, TC, TG, HDL i nie-HDL w Tygodniu 12 wynosiły 78, 145, 115, 45 i 100 mg/dl podczas leczenia 80 mg LIPITORA 40 mg i 105, 179, 142, 47 i 132 mg/dl podczas leczenia 20-40 mg symwastatyny.
Nie było istotnej różnicy między grupami leczenia dla pierwszorzędowego punktu końcowego, częstości występowania pierwszego poważnego incydentu wieńcowego (zakończony zgonem CHD, niezakończony zgonem MI i resuscytacyjne zatrzymanie krążenia): 411 (9,3%) w grupie LIPITOR 80 mg/dobę vs. 463 (10,4%) w grupie symwastatyny 20–40 mg/dobę, HR 0,89, 95% CI (0,78; 1,01), p=0,07.
Nie było istotnych różnic między grupami leczenia pod względem śmiertelności z jakiejkolwiek przyczyny: 366 (8,2%) w grupie LIPITOR 80 mg/dobę vs. 374 (8,4%) w grupie simwastatyny 20–40 mg/dobę. Odsetki osób, które doświadczyły zgonu z przyczyn sercowo-naczyniowych lub innych niż CV, były podobne w grupie LIPITOR 80 mg i simwastatyny 20-40 mg.
Hiperlipidemia i mieszana dyslipidemia
LIPITOR zmniejsza C całkowity, LDL-C, VLDL-C, apo B i TG oraz zwiększa HDL-C u pacjentów z hiperlipidemią (heterozygotyczna rodzinna i nierodzinna) i mieszaną dyslipidemią (typy Fredrickson IIa i IIb). Odpowiedź terapeutyczną obserwuje się w ciągu 2 tygodni, a maksymalna odpowiedź jest zwykle osiągana w ciągu 4 tygodni i utrzymuje się podczas przewlekłej terapii.
LIPITOR jest skuteczny w wielu różnych populacjach pacjentów z hiperlipidemią, z hipertriglicerydemią lub bez hipertriglicerydemii, u mężczyzn i kobiet oraz u osób starszych.
W dwóch wieloośrodkowych, kontrolowanych placebo badaniach zależności dawka-odpowiedź u pacjentów z hiperlipidemią, LIPITOR podawany w pojedynczej dawce przez 6 tygodni znacząco obniżył całkowity C, LDL-C, apo B i TG. (Wyniki zbiorcze przedstawiono w Tabeli 9.)
TABELA 9: Odpowiedź na dawkę u pacjentów z pierwotną hiperlipidemią (skorygowana średnia % zmiana w stosunku do wartości wyjściowych)*
pacjentów z hiperlipoproteinemią typu Fredricksona typu IIa i IIb zebranych w 24 kontrolowanych badaniach, mediana (25. i 75. percentyl) procentowe zmiany w stosunku do wartości wyjściowych w HDL-C dla LIPITOR 10, 20, 40 i 80 mg wyniosła 6,4 (-1,4; 14), odpowiednio 8,7 (0, 17), 7,8 (0, 16) i 5,1 (-2,7, 15). Ponadto analiza zebranych danych wykazała stałe i znaczące spadki C całkowitego, LDL-C, TG, C całkowitego/HDL-C i LDLC/HDL-C.
W trzech wieloośrodkowych badaniach z podwójnie ślepą próbą u pacjentów z hiperlipidemią LIPITOR porównywano z innymi statynami. Po randomizacji pacjenci byli leczeni przez 16 tygodni albo LIPITOREM 10 mg na dobę, albo ustaloną dawką środka porównawczego (Tabela 10).
TABELA 10: Średnia procentowa zmiana od wartości wyjściowej w punkcie końcowym (badania z podwójnie ślepą próbą, randomizowane, z aktywną kontrolą)
Wpływ na wyniki kliniczne różnic w działaniu zmieniającym lipidy między terapiami przedstawionymi w Tabeli 10 nie jest znany. Tabela 10 nie zawiera danych porównujących działanie preparatu LIPITOR 10 mg z wyższymi dawkami lowastatyny, prawastatyny i simwastatyny. Leki porównywane w badaniach podsumowanych w tabeli niekoniecznie są wymienne.
Hipertriglicerydemia
Odpowiedź na LIPITOR u 64 pacjentów z izolowaną hipertriglicerydemią (typ IV wg Fredricksona) leczonych w kilku badaniach klinicznych przedstawiono w poniższej tabeli (Tabela 11). W przypadku pacjentów leczonych preparatem LIPITOR mediana (min., maks.) wyjściowego poziomu TG wynosiła 565 (267–1502).
TABELA 11: Pacjenci skojarzeni z izolowanym podwyższonym TG: Mediana (min., maks.) Procentowa zmiana od wartości początkowej
Dysbetalipoproteinemia
Wyniki otwartego badania krzyżowego u 16 pacjentów (genotypy: 14 apo E2/E2 i 2 apo E3/E2) z dysbetalipoproteinemią (typ III wg Fredricksona) przedstawiono w poniższej tabeli (Tabela 12).
TABELA 12: Otwarte badanie krzyżowe z udziałem 16 pacjentów z dysbetalipoproteinemią (typ III wg Fredricksona)
Homozygotyczna rodzinna hipercholesterolemia
W badaniu bez jednoczesnej grupy kontrolnej 29 pacjentów w wieku od 6 do 37 lat z HoFH otrzymywało maksymalne dawki dobowe od 20 do 80 mg LIPITORA. Średnia redukcja LDL-C w tym badaniu wyniosła 18%. Dwudziestu pięciu pacjentów ze zmniejszeniem stężenia LDL-C miało średnią odpowiedź 20% (zakres od 7% do 53%, mediana 24%); pozostałych 4 pacjentów miało od 7% do 24% wzrost LDL-C. Pięciu z 29 pacjentów nie miało funkcji receptora LDL. Spośród nich 2 pacjentów miało również przeciek wrotny i nie miało znaczącego zmniejszenia stężenia LDL-C. U pozostałych 3 pacjentów z ujemnym receptorem średnia redukcja LDL-C wyniosła 22%.
Heterozygotyczna rodzinna hipercholesterolemia u pacjentów pediatrycznych
badaniu z podwójnie ślepą próbą, kontrolowanym placebo, po którym nastąpiła faza otwartej próby, 187 chłopców i dziewcząt w wieku od 10 do 17 lat w wieku od 10 do 17 lat (średnia wieku 14,1 lat) z heterozygotyczną hipercholesterolemią rodzinną (HeFH) lub ciężką hipercholesterolemią randomizowani do grupy LIPITOR (n=140) lub placebo (n=47) przez 26 tygodni, a następnie wszyscy otrzymywali LIPITOR 40 mg przez 26 tygodni. Włączenie do badania wymagało 1) wyjściowego stężenia LDL-C ≥ 190 mg/dl lub 2) wyjściowego stężenia LDL-C ≥ 160 mg/dl oraz dodatniego wywiadu rodzinnego FH lub udokumentowanej przedwczesnej choroby sercowo-naczyniowej w pierwszym lub drugim stopniu względny. Średnia wyjściowa wartość LDL-C wynosiła 218,6 mg/dl (zakres: 138,5–385,0 mg/dl) w grupie LIPITOR w porównaniu do 230,0 mg/dl (zakres: 160,0–324,5 mg/dl) w grupie placebo . Dawka LIPITORA (raz dziennie) wynosiła 10 mg przez pierwsze 4 tygodnie i była zwiększana do 20 mg, jeśli poziom LDL-C był > 130 mg/dl. Liczba pacjentów leczonych preparatem LIPITOR, którzy wymagali zwiększenia dawki do 20 mg po 4. tygodniu w fazie podwójnie ślepej próby, wyniosła 78 (55,7%).
LIPITOR 10 mg znacząco obniżył stężenie całkowitego C, LDL-C, triglicerydów i apolipoproteiny B w osoczu podczas 26-tygodniowej fazy podwójnie ślepej próby (patrz Tabela 13).
TABELA 13: Zmieniający lipidy wpływ LIPITORA u dorastających chłopców i dziewcząt z heterozygotyczną hipercholesterolemią rodzinną lub ciężką hipercholesterolemią (średnia zmiana procentowa od wartości wyjściowej w punkcie końcowym w populacji ITT)
Średnia osiągnięta wartość LDL-C wyniosła 130,7 mg/dl (zakres: 70,0–242,0 mg/dl) w grupie LIPITOR 10 mg w porównaniu do 228,5 mg/dl (zakres: 152,0–385,0 mg/dl) w grupie placebo grupy podczas 26-tygodniowej fazy podwójnie ślepej próby.
Atorwastatynę badano również w trzyletnim, otwartym, niekontrolowanym badaniu, w którym wzięło udział 163 pacjentów z HeFH w wieku od 10 do 15 lat (82 chłopców i 81 dziewcząt). Wszyscy pacjenci mieli diagnozę kliniczną HeFH potwierdzoną analizą genetyczną (jeśli nie została już potwierdzona w wywiadzie rodzinnym). Około 98% było rasy białej, a mniej niż 1% było rasy czarnej lub azjatyckiej. Średnie stężenie LDL-C na początku badania wynosiło 232 mg/dl. Dawka początkowa atorwastatyny wynosiła 10 mg raz na dobę, a dawki dostosowano tak, aby osiągnąć docelową wartość
Nie ustalono długoterminowej skuteczności terapii LIPITOR 20 mg w dzieciństwie w zmniejszaniu zachorowalności i śmiertelności w wieku dorosłym.
INFORMACJA O PACJENCIE
LIPITOR® tabletki z wapniem atorwastatyny (LIP-ih-tore))
Przeczytaj informacje dla pacjenta dołączone do LIPITORA 20 mg przed rozpoczęciem jego przyjmowania i za każdym razem, gdy otrzymujesz uzupełnienie. Mogą pojawić się nowe informacje. Ta ulotka nie zastępuje rozmowy z lekarzem na temat Twojego stanu zdrowia lub leczenia.
W przypadku jakichkolwiek pytań dotyczących LIPITORA należy zwrócić się do lekarza lub farmaceuty.
Co to jest LIPITOR?
LIPITOR to lek na receptę, który obniża poziom cholesterolu we krwi. Obniża poziom LDL-C („zły” cholesterol) i trójglicerydy we krwi. Może również podnieść poziom HDL-C („dobry” cholesterol). LIPITOR jest przeznaczony dla osób dorosłych i dzieci powyżej 10 roku życia, których poziom cholesterolu nie jest wystarczająco obniżany podczas ćwiczeń i samej diety niskotłuszczowej.
LIPITOR może obniżać ryzyko zawału serca, udaru mózgu, niektórych rodzajów operacji serca i bólu w klatce piersiowej u pacjentów z chorobami serca lub czynnikami ryzyka chorób serca, takimi jak:
- wiek, palenie tytoniu, wysokie ciśnienie krwi, niski poziom HDL-C, choroby serca w rodzinie.
LIPITOR 20mg może obniżyć ryzyko zawału serca lub udaru mózgu u pacjentów z cukrzycą i czynnikami ryzyka, takimi jak:
- problemy z oczami, problemy z nerkami, palenie tytoniu lub wysokie ciśnienie krwi.
LIPITOR 40mg zaczyna działać po około 2 tygodniach.
Co to jest cholesterol?
Cholesterol i trójglicerydy to tłuszcze wytwarzane w organizmie. Występują również w żywności. Potrzebujesz trochę cholesterolu dla dobrego zdrowia, ale zbyt dużo nie jest dla ciebie dobre. Cholesterol i trójglicerydy mogą zatykać naczynia krwionośne. Obniżenie poziomu cholesterolu jest szczególnie ważne, jeśli masz chorobę serca, palisz papierosy, masz cukrzycę lub wysokie ciśnienie krwi, jesteś starszy lub jeśli choroba serca zaczyna się wcześnie w Twojej rodzinie.
Kto nie powinien brać LIPITORA 40 mg?
Nie należy przyjmować leku LIPITOR 10 mg, jeśli:
- jesteś w ciąży, podejrzewasz, że możesz być w ciąży lub planujesz zajść w ciążę. LIPITOR może zaszkodzić nienarodzonemu dziecku. Jeśli zajdziesz w ciążę, przestań przyjmować LIPITOR 40 mg i natychmiast skontaktuj się z lekarzem.
- karmią piersią. LIPITOR 20 mg może przenikać do mleka matki i może zaszkodzić dziecku.
- masz problemy z wątrobą.
- jesteś uczulony na LIPITOR lub którykolwiek z jego składników. Substancją czynną jest atorwastatyna. Pełna lista składników leku LIPITOR znajduje się na końcu tej ulotki.
Nie ustalono dawkowania leku LIPITOR 20 mg u dzieci w wieku poniżej 10 lat.
Zanim zaczniesz LIPITOR
Należy poinformować lekarza, jeśli:
- mieć bóle lub osłabienie mięśni
- pij więcej niż 2 szklanki alkoholu dziennie
- mieć cukrzycę
- masz problem z tarczycą
- masz problemy z nerkami
Niektórych leków nie należy przyjmować razem z lekiem LIPITOR. Poinformuj lekarza o wszystkich przyjmowanych lekach, w tym o lekach na receptę i bez recepty, witaminach i suplementach ziołowych. LIPITOR i niektóre inne leki mogą wchodzić w interakcje, powodując poważne skutki uboczne. Szczególnie powiedz swojemu lekarzowi, jeśli przyjmujesz leki na:
- twój układ odpornościowy
- cholesterol
- infekcje
- kontrola urodzeń
- niewydolność serca
- HIV lub AIDS
- wirus zapalenia wątroby typu C
- leki przeciwwirusowe
Poznaj wszystkie leki, które przyjmujesz. Miej przy sobie ich listę, aby pokazać je lekarzowi i farmaceucie.
Jak powinienem przyjmować LIPITOR 40mg?
- Weź LIPITOR 20mg dokładnie zgodnie z zaleceniami lekarza. Nie należy zmieniać dawki ani przerywać stosowania leku LIPITOR bez konsultacji z lekarzem. Podczas leczenia lekiem LIPITOR lekarz może wykonać badania krwi w celu sprawdzenia poziomu cholesterolu. Na podstawie tych wyników badań krwi może zostać zmieniona dawka leku LIPITOR.
- Przyjmuj LIPITOR codziennie o dowolnej porze dnia, mniej więcej o tej samej porze każdego dnia. LIPITOR 10 mg można przyjmować z jedzeniem lub bez jedzenia. Nie łam tabletek LIPITOR przed zażyciem.
- Lekarz powinien rozpocząć dietę niskotłuszczową przed podaniem LIPITORA. Pozostań na tej niskotłuszczowej diecie, kiedy bierzesz LIPITOR.
- Jeśli pominiesz dawkę LIPITORA, zażyj ją, gdy tylko sobie przypomnisz. Nie należy przyjmować leku LIPITOR 10 mg, jeśli od pominięcia ostatniej dawki minęło więcej niż 12 godzin. Poczekaj i weź następną dawkę o zwykłej porze. Nie należy przyjmować jednocześnie 2 dawek LIPITORA 10mg.
- Jeśli zażyjesz zbyt dużo LIPITORA lub przedawkujesz, natychmiast skontaktuj się z lekarzem lub Centrum Kontroli Zatruć. Lub udaj się do najbliższej izby przyjęć.
Czego powinienem unikać biorąc LIPITOR 10mg?
- Porozmawiaj z lekarzem przed rozpoczęciem stosowania nowych leków. Obejmuje to leki na receptę i bez recepty, witaminy i suplementy ziołowe. LIPITOR i niektóre inne leki mogą wchodzić w interakcje, powodując poważne skutki uboczne.
- Nie zajść w ciążę. W przypadku zajścia w ciążę należy natychmiast przerwać stosowanie leku LIPITOR i skontaktować się z lekarzem.
Jakie są możliwe skutki uboczne stosowania LIPITOR 10mg?
LIPITOR może powodować poważne skutki uboczne. Te skutki uboczne przydarzyły się tylko niewielkiej liczbie osób. Twój lekarz może Cię monitorować. Te działania niepożądane zwykle ustępują po zmniejszeniu dawki lub przerwaniu stosowania leku LIPITOR. Te poważne skutki uboczne obejmują:
- Problemy z mięśniami. LIPITOR 40 mg może powodować poważne problemy z mięśniami, które mogą prowadzić do problemów z nerkami, w tym niewydolności nerek. W przypadku przyjmowania niektórych innych leków razem z lekiem LIPITOR istnieje większe prawdopodobieństwo wystąpienia problemów z mięśniami.
- Problemy z wątrobą. Lekarz powinien wykonać badania krwi w celu sprawdzenia wątroby przed rozpoczęciem przyjmowania leku LIPITOR 20 mg oraz w przypadku wystąpienia objawów problemów z wątrobą podczas przyjmowania leku LIPITOR. Natychmiast skontaktuj się z lekarzem, jeśli masz następujące objawy problemów z wątrobą:
- czuć się zmęczonym lub słabym
- utrata apetytu
- ból w górnej części brzucha
- mocz w kolorze ciemnobursztynowym
- zażółcenie skóry lub białek oczu
Zadzwoń do lekarza od razu, jeśli masz:
- problemy z mięśniami, takie jak osłabienie, tkliwość lub ból, które występują bez uzasadnionego powodu, zwłaszcza jeśli masz również gorączkę lub czujesz się bardziej zmęczony niż zwykle. Może to być wczesna oznaka rzadkiego problemu z mięśniami.
- problemy z mięśniami, które nie ustępują nawet po zaleceniu przez lekarza przerwania stosowania leku LIPITOR. Twój lekarz może wykonać dalsze testy, aby zdiagnozować przyczynę problemów z mięśniami.
- reakcje alergiczne, w tym obrzęk twarzy, warg, języka i (lub) gardła, które mogą powodować trudności w oddychaniu lub połykaniu, które mogą wymagać natychmiastowego leczenia.
- nudności i wymioty.
- oddawanie brązowego lub ciemnego moczu.
- czujesz się bardziej zmęczony niż zwykle
- Twoja skóra i białka oczu stają się żółte.
- ból brzucha.
- alergiczne reakcje skórne.
W badaniach klinicznych pacjenci zgłaszali następujące częste działania niepożądane podczas przyjmowania leku LIPITOR: biegunka, rozstrój żołądka, ból mięśni i stawów oraz zmiany w niektórych laboratoryjnych badaniach krwi.
Następujące dodatkowe działania niepożądane zostały zgłoszone podczas stosowania leku LIPITOR:
zmęczenie, problemy ze ścięgnami, utrata pamięci i dezorientacja.
Porozmawiaj z lekarzem lub farmaceutą, jeśli masz objawy niepożądane, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie skutki uboczne stosowania LIPITORA. Poproś lekarza lub farmaceutę o pełną listę.
Jak przechowywać LIPITOR
- Przechowywać LIPITOR w temperaturze pokojowej, 68 do 77 ° F (20 do 25 ° C).
- Nie przechowuj leków, które są nieaktualne lub których już nie potrzebujesz.
- Przechowuj LIPITOR i wszystkie leki w miejscu niedostępnym dla dzieci. Upewnij się, że wyrzucane lekarstwa są poza zasięgiem dzieci.
Ogólne informacje o LIPITORZE
Czasami przepisuje się leki na schorzenia, które nie są wymienione w ulotkach informacyjnych dla pacjentów. Nie należy stosować leku LIPITOR 10 mg na stan, na który nie został przepisany. Nie podawaj LIPITORA innym osobom, nawet jeśli mają ten sam problem co Ty. Może im to zaszkodzić.
Ta ulotka podsumowuje najważniejsze informacje o LIPITORZE. Jeśli chcesz uzyskać więcej informacji, porozmawiaj ze swoim lekarzem. Możesz poprosić swojego lekarza lub farmaceutę o informacje o LIPITORZE, które są napisane dla pracowników służby zdrowia. Możesz też wejść na stronę LIPITOR pod adresem www.lipitor.com.
Jakie są składniki LIPITORA?
Składnik czynny: wapń atorwastatyny
Nieaktywne składniki: węglan wapnia, USP; wosk kandelila, FCC; kroskarmeloza sodowa, NF; hydroksypropyloceluloza, NF; monohydrat laktozy, NF; stearynian magnezu, NF; celuloza mikrokrystaliczna, NF; Opadry White YS-1-7040 (hypromeloza, glikol polietylenowy, talk, dwutlenek tytanu); polisorbat 80, NF; emulsja symetykonowa.
