Ceftin 250mg, 500mg, 125mg Cefuroxime Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Ceftin 500mg i jak się go stosuje?
Ceftin 500mg to lek na receptę stosowany w leczeniu objawów infekcji bakteryjnych. Ceftin może być stosowany samodzielnie lub z innymi lekami.
Ceftin 250mg jest antybiotykiem cefalosporynowym.
Nie wiadomo, czy Ceftin jest bezpieczny i skuteczny u dzieci w wieku poniżej 3 miesięcy.
Jakie są możliwe skutki uboczne Ceftin?
Ceftin 250mg może powodować poważne skutki uboczne, w tym:
- silny ból brzucha,
- biegunka (z krwią lub bez),
- zażółcenie skóry lub oczu,
- wysypka na skórze,
- siniaki,
- silne mrowienie lub drętwienie,
- drgawki (drgawki),
- trudne lub bolesne oddawanie moczu,
- obrzęk stóp, kostek, twarzy lub języka,
- zmęczenie ,
- duszność,
- gorączka,
- ból gardła,
- płonący w twoich oczach,
- ból skóry z czerwoną lub fioletową wysypką,
- pęcherze i łuszczenie się skóry
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Do najczęstszych działań niepożądanych Ceftin należą:
- biegunka,
- mdłości,
- wymioty,
- nietypowy lub nieprzyjemny smak w ustach,
- wysypka pieluszkowa u niemowlęcia,
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Ceftinu. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
CEFTIN 500 mg tabletki i CEFTIN do sporządzania zawiesiny doustnej zawierają cefuroksym w postaci aksetylu cefuroksymu. CEFTIN jest półsyntetycznym, cefalosporynowym lekiem przeciwbakteryjnym do podawania doustnego.
Nazwa chemiczna aksetylu cefuroksymu (1-(acetyloksy)ester etylowy cefuroksymu) to (RS)-1-hydroksyetyl (6R,7R)-7-[2-(2-furylo)glioksyloamido]-3-(hydroksymetylo) )-8-okso-5-tia-1-azabicyklo[4.2.0]-okt-2-eno-2-karboksylan, 72-(Z)-(O-metylo-oksym), 1-octan 3-karbaminian. Jego wzór cząsteczkowy to C20H22N4O10S i ma masę cząsteczkową 510,48.
Aksetyl cefuroksymu występuje w formie amorficznej i ma następujący wzór strukturalny:
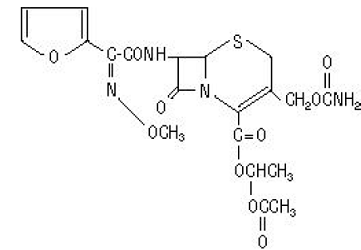
Tabletki są powlekane i zawierają odpowiednik 250 lub 500 mg cefuroksymu w postaci aksetylu cefuroksymu. Tabletki zawierają nieaktywne składniki koloidalny dwutlenek krzemu, kroskarmelozę sodową, uwodorniony olej roślinny, hypromelozę, metyloparaben, celulozę mikrokrystaliczną, glikol propylenowy, propyloparaben, benzoesan sodu, laurylosiarczan sodu i dwutlenek tytanu.
Zawiesina doustna po rozpuszczeniu w wodzie zapewnia równowartość 125 mg lub 250 mg cefuroksymu (w postaci aksetylu cefuroksymu) na 5 ml. Zawiesina doustna zawiera nieaktywne składniki acesulfam potasu, aspartam, powidon K30, kwas stearynowy, sacharozę, aromat tutti-frutti i gumę ksantanową.
WSKAZANIA
Zapalenie gardła / zapalenie migdałków
Tabletki CEFTIN 125 mg są wskazane w leczeniu pacjentów dorosłych i dzieci (13 lat i starszych) z łagodnym do umiarkowanego zapaleniem gardła/migdałków wywołanym przez wrażliwe szczepy Streptococcus pyogenes.
CEFTIN 500 mg do zawiesiny doustnej jest wskazany w leczeniu dzieci w wieku od 3 miesięcy do 12 lat z łagodnym do umiarkowanego zapaleniem gardła/migdałków wywołanym przez wrażliwe szczepy Streptococcus pyogenes.
Ograniczenia użytkowania
- W badaniach klinicznych nie ustalono skuteczności CEFTIN w zapobieganiu gorączce reumatycznej.
- Skuteczność CEFTIN 125 mg w leczeniu opornych na penicylinę szczepów Streptococcus pyogenes nie została wykazana w badaniach klinicznych.
Ostre bakteryjne zapalenie ucha środkowego
Tabletki CEFTIN 125 mg są wskazane w leczeniu pacjentów pediatrycznych (którzy mogą połykać tabletki w całości) z ostrym bakteryjnym zapaleniem ucha środkowego wywołanym przez wrażliwe szczepy Streptococcus pneumoniae, Haemophilus influenzae (w tym szczepy wytwarzające β-laktamazę), Moraxella catarrhalis (w tym β-laktamaza produkujące szczepy) lub Streptococcus pyogenes.
CEFTIN do zawiesiny doustnej jest wskazany w leczeniu dzieci w wieku od 3 miesięcy do 12 lat z ostrym bakteryjnym zapaleniem ucha środkowego wywołanym przez wrażliwe szczepy Streptococcus pneumoniae, Haemophilus influenzae (w tym szczepy wytwarzające β-laktamazę), Moraxella catarrhalis (w tym β-laktamaza produkujące szczepy) lub Streptococcus pyogenes.
Ostre bakteryjne zapalenie zatok szczękowych
Tabletki CEFTIN są wskazane w leczeniu pacjentów dorosłych i dzieci (13 lat i starszych) z łagodnym do umiarkowanego ostrym bakteryjnym zapaleniem zatok szczękowych wywołanym przez wrażliwe szczepy Streptococcus pneumoniae lub Haemophilus influenzae (wyłącznie szczepy nie wytwarzające β-laktamaz).
CEFTIN 250 mg do zawiesiny doustnej jest wskazany w leczeniu dzieci w wieku od 3 miesięcy do 12 lat z łagodnym do umiarkowanego ostrym bakteryjnym zapaleniem zatok szczękowych wywołanym przez wrażliwe szczepy Streptococcus pneumoniae lub Haemophilus influenzae (wyłącznie szczepy nie wytwarzające β-laktamaz). .
Ograniczenia użytkowania
Nie ustalono skuteczności CEFTIN w zakażeniach zatok wywołanych przez Haemophilus influenzae wytwarzający β-laktamazę lub Moraxella catarrhalis u pacjentów z ostrym bakteryjnym zapaleniem zatok szczękowych ze względu na niewystarczającą liczbę tych izolatów w badaniach klinicznych [patrz Studia kliniczne ].
Ostre bakteryjne zaostrzenia przewlekłego zapalenia oskrzeli
Tabletki CEFTIN są wskazane w leczeniu pacjentów dorosłych i dzieci (w wieku 13 lat i starszych) z łagodnymi lub umiarkowanymi ostrymi bakteryjnymi zaostrzeniami przewlekłego zapalenia oskrzeli wywołanymi przez wrażliwe szczepy Streptococcus pneumoniae, Haemophilus influenzae (szczepy β-laktamazy ujemne), lub Haemophilus para influenzae (szczepy β-laktamazo-ujemne).
Nieskomplikowane infekcje skóry i struktury skóry
Tabletki CEFTIN 250 mg są wskazane w leczeniu pacjentów dorosłych i dzieci (w wieku 13 lat i starszych) z niepowikłanymi zakażeniami skóry i struktury skóry wywołanymi przez wrażliwe szczepy Staphylococcus aureus (w tym szczepy wytwarzające β-laktamazę) lub Streptococcus pyogenes.
Nieskomplikowane infekcje dróg moczowych
Tabletki CEFTIN 500 mg są wskazane w leczeniu pacjentów dorosłych i dzieci (w wieku 13 lat i starszych) z niepowikłanymi zakażeniami dróg moczowych wywołanymi przez wrażliwe szczepy Escherichia coli lub Klebsiella pneumoniae.
Nieskomplikowana rzeżączka
Tabletki CEFTIN są wskazane w leczeniu pacjentów dorosłych i dzieci (w wieku 13 lat i starszych) z niepowikłaną rzeżączką, cewką moczową i szyjką macicy, wywołaną przez szczepy Neisseria gonorrhoeae wytwarzające penicylinazy i niewytwarzające penicylinazy oraz niepowikłaną rzeżączkę, odbytnicę, u kobiet , wywołane przez wrażliwe szczepy Neisseria gonorrhoeae nie wytwarzające penicylinazy.
Wczesna choroba z Lyme (rumień wędrujący)
Tabletki CEFTIN są wskazane w leczeniu pacjentów dorosłych i dzieci (w wieku 13 lat i starszych) z wczesną chorobą z Lyme (rumień wędrujący) wywołaną przez wrażliwe szczepy Borrelia burgdorferi.
Liszajec
CEFTIN 250 mg do zawiesiny doustnej jest wskazany w leczeniu dzieci i młodzieży w wieku od 3 miesięcy do 12 lat z liszajcem wywołanym przez wrażliwe szczepy Staphylococcus aureus (w tym szczepy wytwarzające Plactamazę) lub Streptococcus pyogenes.
Stosowanie
celu ograniczenia rozwoju bakterii lekoopornych i utrzymania skuteczności CEFTIN i innych leków przeciwbakteryjnych, CEFTIN 500 mg należy stosować wyłącznie w leczeniu lub zapobieganiu zakażeniom, co do których udowodniono lub z silnym podejrzeniem, że są wywołane przez wrażliwe bakterie. Gdy dostępne są informacje dotyczące hodowli i wrażliwości, należy je uwzględnić przy wyborze lub modyfikacji terapii przeciwbakteryjnej. W przypadku braku takich danych, lokalna epidemiologia i wzorce podatności mogą przyczynić się do empirycznego doboru terapii.
DAWKOWANIE I SPOSÓB PODAWANIA
Ważne instrukcje administracyjne
- CEFTIN tabletki i CEFTIN do sporządzania zawiesiny doustnej nie są biorównoważne i dlatego nie można ich zastąpić w przeliczeniu na miligram na miligram [patrz FARMAKOLOGIA KLINICZNA ].
- Podawać tabletki lub zawiesinę doustną CEFTIN zgodnie z odpowiednimi wytycznymi dotyczącymi dawkowania [patrz Dawkowanie dla tabletek CEFTIN 500 mg, Dawkowanie dla CEFTIN 250 mg do zawiesiny doustnej oraz Przygotowanie i podawanie CEFTIN 125 mg do zawiesiny doustnej ].
- Podawać CEFTIN 500mg tabletki z jedzeniem lub bez jedzenia.
- Podawać CEFTIN 500mg do sporządzania zawiesiny doustnej z jedzeniem.
- Pacjenci pediatryczni (w wieku 13 lat i starsi), którzy nie mogą połykać tabletek CEFTIN 125 mg w całości, powinni otrzymać CEFTIN w postaci zawiesiny doustnej, ponieważ tabletka po rozkruszeniu ma silny, utrzymujący się gorzki smak [patrz Dawkowanie tabletek CEFTIN ].
Dawkowanie dla tabletek CEFTIN 500 mg
Podawać CEFTIN 250 mg tabletki zgodnie z poniższą tabelą wytycznych dotyczących dawkowania z jedzeniem lub bez jedzenia.
Dawkowanie CEFTIN do zawiesiny doustnej
Podawać CEFTIN w postaci zawiesiny doustnej, jak opisano w poniższej tabeli wytycznych dotyczących dawkowania, z jedzeniem.
Przygotowanie i podawanie CEFTIN do zawiesiny doustnej
Przygotuj zawiesinę w momencie wydawania w następujący sposób:
- Przed każdym użyciem dobrze wstrząsnąć zawiesiną doustną.
- Po każdym otwarciu założyć zatyczkę.
- Odtworzoną zawiesinę przechowywać w lodówce w temperaturze od 2° do 8°C (36° do 46°F).
- Po 10 dniach wyrzucić przygotowaną zawiesinę.
Dawkowanie u pacjentów z zaburzeniami czynności nerek
U pacjentów, u których klirens kreatyniny jest mniejszy niż 30 ml/min, konieczna jest modyfikacja odstępów między dawkami, jak przedstawiono w Tabeli 4 poniżej, ponieważ cefuroksym jest wydalany głównie przez nerki [patrz FARMAKOLOGIA KLINICZNA ].
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Tabletki CEFTIN to białe tabletki powlekane w kształcie kapsułki, dostępne w następujących mocach:
- 250 mg cefuroksymu (jako aksetyl cefuroksymu) z wytłoczonym napisem „GX ES7” po jednej stronie i pustym po drugiej stronie.
- 500 mg cefuroksymu (jako aksetyl cefuroksymu) z wytłoczonym „GX EG2” po jednej stronie i pustym po drugiej stronie.
CEFTIN do sporządzania zawiesiny doustnej jest dostarczany w postaci suchego, białego lub prawie białego proszku o smaku tutti-frutti. Po rozpuszczeniu zgodnie z zaleceniami zawiesina zapewnia równowartość 125 mg lub 250 mg cefuroksymu (w postaci aksetylu cefuroksymu) na 5 ml.
Składowania i stosowania
Tabletki CEFTIN, 250 mg cefuroksymu (w postaci aksetylu cefuroksymu), to białe tabletki powlekane w kształcie kapsułki z wytłoczonym „GX ES7” po jednej stronie i pustym po drugiej stronie, w następujący sposób: 20 tabletek/butelka NDC 0173-0387-00
Tabletki CEFTIN, 500 mg cefuroksymu (jako aksetyl cefuroksymu), to białe tabletki powlekane w kształcie kapsułki z wytłoczonym „GX EG2” po jednej stronie i pustym po drugiej stronie, w następujący sposób: 20 tabletek/butelka NDC 0173-0394-00
Tabletki należy przechowywać w temperaturze od 15° do 30°C (59° do 86°F). Po każdym otwarciu założyć zatyczkę.
CEFTIN 500mg do sporządzania zawiesiny doustnej jest dostarczany w postaci suchego proszku o smaku od białego do prawie białego o smaku tutti-frutti. Po rozpuszczeniu zgodnie z zaleceniami zawiesina zapewnia równowartość 125 mg lub 250 mg cefuroksymu (w postaci aksetylu cefuroksymu) na 5 ml. Jest dostarczany w butelkach ze szkła bursztynowego w następujący sposób:
125 mg/5 ml
Zawiesina 100 ml NDC 0173-0740-00
250 mg/5 ml
Zawiesina 50 ml NDC 0173-0741-10 100-ml zawiesina NDC 0173-0741-00
Przed rozpuszczeniem suchy proszek przechowywać w temperaturze od 2° do 30°C (36° do 86°F).
Po rekonstytucji natychmiast przechowywać zawiesinę w lodówce w temperaturze od 2° do 8°C (36° do 46°F). WYRZUCAJ PO 10 DNIACH.
GlaxoSmithKline, Research Triangle Park, NC 27709. Aktualizacja: październik 2017
SKUTKI UBOCZNE
Następujące poważne i inne ważne działanie niepożądane opisano bardziej szczegółowo w części „Ostrzeżenia i środki ostrożności” na etykiecie:
Reakcje anafilaktyczne [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Tablety
Wielodawkowe schematy dawkowania o czasie trwania od 7 do 10 dni
badaniach klinicznych z wielokrotnymi dawkami 912 pacjentów otrzymywało CEFTIN (125 do 500 mg dwa razy na dobę). Należy zauważyć, że 125 mg dwa razy dziennie nie jest zatwierdzoną dawką. Dwadzieścia (2,2%) pacjentów przerwało leczenie z powodu działań niepożądanych. Siedemnastu (85%) z 20 pacjentów, którzy przerwali terapię, zrobiło to z powodu zaburzeń żołądkowo-jelitowych, w tym biegunki, nudności, wymiotów i bólu brzucha. Odsetek pacjentów leczonych CEFTIN, którzy przerwali stosowanie badanego leku z powodu działań niepożądanych, był podobny przy dawkach dobowych 1000, 500 i 250 mg (odpowiednio 2,3%, 2,1% i 2,2%). Jednak częstość występowania działań niepożądanych ze strony przewodu pokarmowego wzrastała wraz z większymi zalecanymi dawkami.
Działania niepożądane przedstawione w Tabeli 5 dotyczą pacjentów (n = 912) leczonych CEFTIN 250 mg w badaniach klinicznych z wielokrotnymi dawkami.
Następujące działania niepożądane wystąpiły u mniej niż 1%, ale u więcej niż 0,1% pacjentów (n = 912) leczonych CEFTIN w badaniach klinicznych z wielokrotnymi dawkami.
Zaburzenia układu immunologicznego Pokrzywka, obrzęk języka.
Zaburzenia metabolizmu i odżywiania : Anoreksja.
Zaburzenia układu nerwowego : Ból głowy.
Zaburzenia serca : Ból w klatce piersiowej.
Zaburzenia oddechowe : Duszność.
Zaburzenia żołądkowo-jelitowe : Ból brzucha, skurcze brzucha, wzdęcia, niestrawność, owrzodzenie jamy ustnej.
Zaburzenia skóry i tkanki podskórnej : Wysypka, swędzenie.
Zaburzenia nerek i dróg moczowych : Dyzuria.
Zaburzenia układu rozrodczego i piersi : Zapalenie pochwy, swędzenie sromu.
Ogólne zaburzenia i warunki miejsca administracji : Dreszcze, senność, pragnienie.
Dochodzenia : dodatni test Coombsa.
Wczesna choroba z Lyme w 20-dniowym schemacie
dwóch wieloośrodkowych badaniach oceniano CEFTIN 500 mg dwa razy na dobę przez 20 dni. Najczęstszymi działaniami niepożądanymi związanymi z lekiem były biegunka (10,6%), reakcja Jarischa-Herxheimera (5,6%) i zapalenie pochwy (5,4%). Inne działania niepożądane wystąpiły z częstością porównywalną do zgłaszanej przy dawkowaniu przez 7 do 10 dni.
Schemat pojedynczej dawki dla niepowikłanej rzeżączki
W badaniach klinicznych, w których stosowano pojedynczą dawkę 1000 mg CEFTIN 250 mg, 1061 pacjentów leczono z powodu niepowikłanej rzeżączki. Działania niepożądane przedstawione w Tabeli 6 dotyczyły pacjentów leczonych pojedynczą dawką 1000 mg CEFTIN w badaniach klinicznych w Stanach Zjednoczonych.
Następujące działania niepożądane wystąpiły u mniej niż 1%, ale więcej niż 0,1% pacjentów (n = 1061) leczonych pojedynczą dawką CEFTIN 1000 mg z powodu niepowikłanej rzeżączki w badaniach klinicznych w USA.
Infekcje i infestacje : Kandydoza pochwy.
Zaburzenia układu nerwowego : Ból głowy, zawroty głowy, senność.
Zaburzenia serca : Ucisk/ból w klatce piersiowej, tachykardia.
Zaburzenia żołądkowo-jelitowe : Ból brzucha, niestrawność.
Zaburzenia skóry i tkanki podskórnej : Rumień, wysypka, świąd.
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej : skurcze mięśni, sztywność mięśni, skurcze mięśni karku, reakcja typu szczękościsk.
Zaburzenia nerek i dróg moczowych : Krwawienie/ból w cewce moczowej, ból nerek.
Zaburzenia układu rozrodczego i piersi : Swędzenie pochwy, upławy.
Zawiesina doustna
W badaniach klinicznych z zastosowaniem wielokrotnych dawek CEFTIN 250 mg, dzieci (96,7% było w wieku poniżej 12 lat) były leczone CEFTIN (20 do 30 mg/kg/dobę podzielone dwa razy na dobę do maksymalnej dawki 500 lub 1000 mg/dobę, odpowiednio). Jedenaście (1,2%) pacjentów z USA przerwało leczenie z powodu działań niepożądanych. Odstawienia dotyczyły głównie zaburzeń żołądkowo-jelitowych, zwykle biegunki lub wymiotów. Trzynastu (1,4%) pacjentów pediatrycznych w USA przerwało terapię z powodu smaku i/lub problemów z podawaniem leku.
Działania niepożądane w Tabeli 7 dotyczą pacjentów ze Stanów Zjednoczonych (n = 931) leczonych CEFTIN w badaniach klinicznych z wielokrotnymi dawkami.
Następujące działania niepożądane wystąpiły u mniej niż 1%, ale więcej niż 0,1% pacjentów w Stanach Zjednoczonych (n = 931) leczonych CEFTIN w postaci zawiesiny doustnej w badaniach klinicznych z wielokrotnymi dawkami.
Infekcje i infestacje : Infekcja przewodu pokarmowego, kandydoza, choroba wirusowa, infekcja górnych dróg oddechowych, zapalenie zatok, infekcja dróg moczowych.
Zaburzenia krwi i układu chłonnego : Eozynofilia.
Zaburzenia psychiczne : Nadpobudliwość, drażliwe zachowanie.
Zaburzenia żołądkowo-jelitowe : Ból brzucha, wzdęcia, ból głowy.
Zaburzenia skóry i tkanki podskórnej : Wysypka.
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej : Obrzęk stawów, ból stawów.
Zaburzenia układu rozrodczego i piersi : Podrażnienie pochwy.
Ogólne zaburzenia i warunki miejsca administracji : Kaszel, gorączka.
Dochodzenia : Podwyższone enzymy wątrobowe, dodatni test Coombsa.
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania CEFTIN po dopuszczeniu do obrotu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Zaburzenia krwi i układu chłonnego
Niedokrwistość hemolityczna, leukopenia, pancytopenia, małopłytkowość.
Zaburzenia żołądkowo-jelitowe
Rzekomobłoniaste zapalenie jelita grubego [patrz OSTRZEŻENIA I ŚRODKI ].
Zaburzenia wątroby i dróg żółciowych
Zaburzenia czynności wątroby, w tym zapalenie wątroby i cholestaza, żółtaczka.
Zaburzenia układu immunologicznego
Anafilaksja, reakcja przypominająca chorobę posurowiczą.
Dochodzenia
Zwiększony czas protrombinowy.
Zaburzenia układu nerwowego
Napad, encefalopatia.
Zaburzenia nerek i dróg moczowych
Niewydolność nerek.
Zaburzenia skóry i tkanki podskórnej
Obrzęk naczynioruchowy, rumień wielopostaciowy, zespół Stevensa-Johnsona, martwica toksyczno-rozpływna naskórka, pokrzywka.
INTERAKCJE Z LEKAMI
Doustne środki antykoncepcyjne
Aksetyl cefuroksymu może wpływać na florę jelitową, prowadząc do mniejszego wchłaniania zwrotnego estrogenu i zmniejszonej skuteczności złożonych doustnych środków antykoncepcyjnych zawierających estrogen i progesteron. Poradzić pacjentkom, aby w trakcie leczenia rozważyły alternatywne dodatkowe (niehormonalne) środki antykoncepcyjne.
Leki zmniejszające kwasowość żołądka
Leki zmniejszające kwasowość żołądka mogą powodować niższą biodostępność CEFTIN w porównaniu z podawaniem na czczo. Podawanie leków zmniejszających kwaśność soku żołądkowego może zniwelować efekt pokarmowy zwiększonego wchłaniania CEFTIN 250 mg w stanie poposiłkowym. Podawać CEFTIN co najmniej 1 godzinę przed lub 2 godziny po podaniu krótko działających leków zobojętniających. Należy unikać antagonistów histaminy-2 (H2) i inhibitorów pompy protonowej.
Probenecyd
Jednoczesne podawanie probenecydu z tabletkami aksetylu cefuroksymu zwiększa stężenie cefuroksymu w surowicy [patrz FARMAKOLOGIA KLINICZNA ]. Nie zaleca się jednoczesnego podawania probenecydu z aksetylem cefuroksymu.
Interakcje leków/testów laboratoryjnych
Fałszywie dodatnia reakcja na glukozę w moczu może wystąpić w przypadku testów redukcji miedzi (np. roztwór Benedicta lub Fehlinga), ale nie w przypadku enzymatycznych testów glikozurii. Ponieważ w teście z żelazicyjankami może wystąpić wynik fałszywie ujemny, zaleca się stosowanie metody z oksydazą glukozową lub heksokinazą do oznaczania stężenia glukozy we krwi/osoczu u pacjentów otrzymujących aksetyl cefuroksymu. Obecność cefuroksymu nie wpływa na oznaczenie kreatyniny w surowicy i moczu metodą alkaliczną z pikrynianem.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Reakcje anafilaktyczne
pacjentów przyjmujących leki przeciwbakteryjne beta-laktamowe zgłaszano ciężkie i czasami prowadzące do zgonu reakcje nadwrażliwości (anafilaktyczne). Te reakcje są bardziej prawdopodobne u osób z historią nadwrażliwości na β-laktamy i (lub) nadwrażliwości na wiele alergenów. Istnieją doniesienia o osobach z nadwrażliwością na penicylinę w wywiadzie, u których wystąpiły ciężkie reakcje podczas leczenia cefalosporynami. CEFTIN 500 mg jest przeciwwskazany u pacjentów ze stwierdzoną nadwrażliwością na CEFTIN lub inne leki przeciwbakteryjne β-laktamowe [patrz PRZECIWWSKAZANIA ]. Przed rozpoczęciem leczenia CEFTIN należy zapytać o wcześniejsze reakcje nadwrażliwości na penicyliny, cefalosporyny lub inne alergeny. W przypadku wystąpienia reakcji alergicznej należy odstawić CEFTIN i wdrożyć odpowiednią terapię.
Biegunka związana z Clostridium Difficile
Biegunkę związaną z Clostridium difficile (CDAD) zgłaszano po zastosowaniu prawie wszystkich leków przeciwbakteryjnych, w tym CEFTIN, a jej nasilenie może wahać się od łagodnej biegunki do zapalenia okrężnicy zakończonego zgonem. Leczenie środkami przeciwbakteryjnymi zmienia normalną florę okrężnicy, prowadząc do przerostu C. difficile.
C. difficile wytwarza toksyny A i B, które przyczyniają się do rozwoju CDAD. Szczepy C. difficile wytwarzające hipertoksyny powodują zwiększoną zachorowalność i śmiertelność, ponieważ zakażenia te mogą być oporne na leczenie przeciwbakteryjne i mogą wymagać kolektomii. CDAD należy rozważyć u wszystkich pacjentów, u których po zastosowaniu antybiotyków wystąpi biegunka. Konieczna jest staranna historia choroby, ponieważ donoszono, że CDAD występuje w ciągu 2 miesięcy po podaniu leków przeciwbakteryjnych.
przypadku podejrzenia lub potwierdzenia CDAD, może być konieczne przerwanie trwającego stosowania antybiotyków, które nie są skierowane przeciwko C. difficile. W zależności od wskazań klinicznych należy wdrożyć odpowiednią gospodarkę wodno-elektrolitową, suplementację białka, antybiotykoterapię C. difficile oraz ocenę chirurgiczną.
Potencjał przerostu drobnoustrojów
Podczas terapii należy brać pod uwagę możliwość nadkażenia patogenami grzybiczymi lub bakteryjnymi.
Rozwój bakterii lekoopornych
Jest mało prawdopodobne, aby przepisywanie CEFTIN w przypadku braku potwierdzonego lub silnie podejrzewanego zakażenia bakteryjnego lub ze wskazań profilaktycznych przyniosło korzyść pacjentowi i zwiększyło ryzyko rozwoju bakterii lekoopornych.
Fenyloketonuria
CEFTIN 125 mg do sporządzania zawiesiny doustnej 125 mg/5 ml zawiera 11,8 mg fenyloalaniny w 5 ml (1 łyżeczka) przygotowanej zawiesiny. CEFTIN 250 mg do sporządzania zawiesiny doustnej 250 mg/5 ml zawiera 25,2 mg fenyloalaniny w 5 ml (1 łyżeczka do herbaty) przygotowanej zawiesiny.
Zakłócenia w testach glukozy
osób otrzymujących CEFTIN może wystąpić fałszywie dodatni wynik stężenia glukozy w moczu, a fałszywie ujemny wynik stężenia glukozy we krwi/osoczu może wystąpić w przypadku badań żelazicyjanków u osób otrzymujących CEFTIN [patrz INTERAKCJE Z LEKAMI ].
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Chociaż nie przeprowadzono badań na zwierzętach dotyczących całego życia w celu oceny potencjału rakotwórczego, nie stwierdzono działania mutagennego aksetylu cefuroksymu w serii testów mutacji bakteryjnych. Pozytywne wyniki uzyskano w teście aberracji chromosomowych in vitro; jednak negatywne wyniki uzyskano w teście mikrojądrowym in vivo przy dawkach do 1,5 g/kg. Badania rozrodczości przeprowadzone na szczurach w dawkach do 1000 mg/kg/dobę (9-krotność zalecanej maksymalnej dawki u ludzi w oparciu o powierzchnię ciała) nie wykazały zaburzeń płodności.
Używaj w określonych populacjach
Ciąża
Ciąża Kategoria B. Nie ma odpowiednich i dobrze kontrolowanych badań u kobiet w ciąży. Ponieważ badania reprodukcji na zwierzętach nie zawsze pozwalają przewidzieć odpowiedź człowieka, CEFTIN powinien być stosowany w czasie ciąży tylko wtedy, gdy jest to bezwzględnie konieczne.
Badania nad reprodukcją przeprowadzono na myszach w dawkach do 3200 mg/kg/dobę (14-krotność zalecanej maksymalnej dawki u ludzi w oparciu o powierzchnię ciała) oraz na szczurach w dawkach do 1000 mg/kg/dobę (9-krotność zalecanej maksymalnej dawki dawki stosowanej u ludzi w oparciu o powierzchnię ciała) i nie wykazały dowodów na zaburzenia płodności lub uszkodzenia płodu spowodowane przez aksetyl cefuroksymu.
Matki karmiące
Ponieważ cefuroksym przenika do mleka ludzkiego, należy zachować ostrożność podając CEFTIN 500 mg kobiecie karmiącej.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność preparatu CEFTIN 250 mg ustalono dla dzieci w wieku od 3 miesięcy do 12 lat z ostrym bakteryjnym zapaleniem zatok szczękowych na podstawie jego zatwierdzenia u dorosłych. Stosowanie CEFTIN u dzieci jest poparte danymi farmakokinetycznymi i dotyczącymi bezpieczeństwa u dorosłych i dzieci, a także danymi klinicznymi i mikrobiologicznymi z odpowiednich i dobrze kontrolowanych badań dotyczących leczenia ostrego bakteryjnego zapalenia zatok szczękowych u dorosłych oraz ostrego zapalenia ucha środkowego z wysiękiem u dorosłych pacjentów pediatrycznych. Jest również wspierany przez nadzór nad zdarzeniami niepożądanymi po wprowadzeniu do obrotu. [Widzieć WSKAZANIA I ZASTOSOWANIE , DAWKOWANIE I SPOSÓB PODAWANIA , DZIAŁANIA NIEPOŻĄDANE , FARMAKOLOGIA KLINICZNA ]
Zastosowanie geriatryczne
całkowitej liczby pacjentów, którzy otrzymywali CEFTIN 250 mg w 20 badaniach klinicznych, 375 było w wieku 65 lat i starszych, a 151 było w wieku 75 lat i starszych. Nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między tymi osobami a młodszymi dorosłymi osobami. Zgłoszone doświadczenie kliniczne nie wykazało różnic w odpowiedziach pomiędzy starszymi i młodszymi dorosłymi pacjentami, ale nie można wykluczyć większej wrażliwości niektórych osób starszych.
Cefuroksym jest w znacznym stopniu wydalany przez nerki, a ryzyko działań niepożądanych może być większe u pacjentów z zaburzeniami czynności nerek. Ponieważ u pacjentów w podeszłym wieku istnieje większe prawdopodobieństwo upośledzenia czynności nerek, należy zachować ostrożność przy doborze dawki i może być przydatne monitorowanie czynności nerek.
Zaburzenia czynności nerek
U dorosłych pacjentów z ciężkimi zaburzeniami czynności nerek (klirens kreatyniny DAWKOWANIE I SPOSÓB PODAWANIA , FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
Przedawkowanie cefalosporyn może powodować podrażnienie mózgu prowadzące do drgawek lub encefalopatii. Stężenie cefuroksymu w surowicy można zmniejszyć za pomocą hemodializy i dializy otrzewnowej.
PRZECIWWSKAZANIA
CEFTIN jest przeciwwskazany u pacjentów ze stwierdzoną nadwrażliwością (np. anafilaksję) na CEFTIN lub inne leki przeciwbakteryjne beta-laktamowe (np. penicyliny i cefalosporyny).
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
CEFTIN 250mg jest lekiem przeciwbakteryjnym [patrz Mikrobiologia ].
Farmakokinetyka
Wchłanianie
Po podaniu doustnym aksetyl cefuroksymu jest wchłaniany z przewodu pokarmowego i szybko hydrolizowany przez niespecyficzne esterazy w błonie śluzowej jelit i krwi do cefuroksymu. Parametry farmakokinetyczne cefuroksymu w surowicy po podaniu tabletek CEFTIN 250 mg dorosłym przedstawiono w Tabeli 8.
Efekt jedzenia
Wchłanianie tabletki jest większe po spożyciu po jedzeniu (bezwzględna biodostępność wzrasta z 37% do 52%). Pomimo tej różnicy we wchłanianiu, kliniczna i bakteriologiczna odpowiedź uczestników była niezależna od przyjmowania pokarmu w czasie podawania tabletek w 2 badaniach, w których to oceniano.
Wszystkie badania skuteczności farmakokinetycznej i klinicznej oraz bezpieczeństwa u pacjentów pediatrycznych z użyciem postaci zawiesiny przeprowadzono po posiłku. Brak danych dotyczących kinetyki wchłaniania postaci zawiesiny podawanej dzieciom na czczo.
Brak biorównoważności
Zawiesina doustna nie była biorównoważna z tabletkami podczas badania na zdrowych osobach dorosłych. Tabletki i zawiesiny doustne NIE są substytucyjne w przeliczeniu na miligram-permigram. Pole pod krzywą dla zawiesiny wynosiło średnio 91% tego dla tabletki, a maksymalne stężenie w osoczu dla zawiesiny średnio 71% maksymalnego stężenia tabletek. W związku z tym bezpieczeństwo i skuteczność zarówno postaci tabletek, jak i zawiesiny doustnej zostały ustalone w oddzielnych badaniach klinicznych.
Dystrybucja
Cefuroksym jest rozprowadzany w płynach pozakomórkowych. Około 50% cefuroksymu w surowicy wiąże się z białkami.
Metabolizm
Ugrupowanie aksetylu jest metabolizowane do aldehydu octowego i kwasu octowego.
Wydalanie
Cefuroksym jest wydalany z moczem w postaci niezmienionej; u dorosłych około 50% podanej dawki jest wydalane z moczem w ciągu 12 godzin. Nie badano farmakokinetyki cefuroksymu u dzieci i młodzieży. Do czasu uzyskania dalszych danych nie należy ekstrapolować wydalania nerkowego aksetylu cefuroksymu ustalonego u dorosłych na dzieci i młodzież.
Określone populacje
Zaburzenia czynności nerek
W badaniu z udziałem 28 osób dorosłych z prawidłową czynnością nerek lub ciężkimi zaburzeniami czynności nerek (klirens kreatyniny DAWKOWANIE I SPOSÓB PODAWANIA ].
Pacjenci pediatryczni
Parametry farmakokinetyczne cefuroksymu w surowicy u dzieci, którym podano CEFTIN w postaci zawiesiny doustnej przedstawiono w Tabeli 9.
Pacjenci geriatryczni
badaniu 20 osób w podeszłym wieku (średni wiek = 83,9 lat) ze średnim klirensem kreatyniny 34,9 ml/min, średni okres półtrwania w fazie eliminacji z surowicy wydłużył się do 3,5 godziny; jednak pomimo mniejszego wydalania cefuroksymu u pacjentów geriatrycznych, dostosowanie dawki w zależności od wieku nie jest konieczne [patrz Używaj w określonych populacjach ].
Interakcje leków
Jednoczesne podawanie probenecydu z tabletkami aksetylu cefuroksymu zwiększa powierzchnię cefuroksymu pod krzywą stężenia w surowicy w funkcji czasu i maksymalne stężenie w surowicy odpowiednio o 50% i 21%.
Mikrobiologia
Mechanizm akcji
Aksetyl cefuroksymu jest środkiem bakteriobójczym, który działa poprzez hamowanie syntezy ściany komórkowej bakterii. Aksetyl cefuroksymu wykazuje aktywność w obecności niektórych β-laktamaz, zarówno penicylinaz, jak i cefalosporynaz, bakterii Gram-ujemnych i Gram-dodatnich.
Mechanizm oporu
Oporność na aksetyl cefuroksymu wynika głównie z hydrolizy przez β-laktamazę, zmiany białek wiążących penicylinę (PBP), zmniejszonej przepuszczalności i obecności bakteryjnych pomp efluksowych.
Wrażliwość na aksetyl cefuroksymu różni się w zależności od położenia geograficznego i czasu; należy zapoznać się z lokalnymi danymi dotyczącymi wrażliwości, jeśli są dostępne. Izolaty H. influenzae, oporne na działanie beta-laktamazy, oporne na ampicylinę (BLNAR) należy uznać za oporne na aksetyl cefuroksymu.
Wykazano, że aksetyl cefuroksymu działa na większość izolatów następujących bakterii, zarówno in vitro, jak i w zakażeniach klinicznych [patrz WSKAZANIA I ZASTOSOWANIE ]:
Bakterie Gram-dodatnie
Staphylococcus aureus (tylko izolaty wrażliwe na metycylinę) Streptococcus pneumoniae Streptococcus pyogenes
Bakterie Gram-ujemne
Escherichia colia Klebsiella pneumoniaea Haemophilus influenzae Haemophilus parainfluenzae Moraxella catarrhalis Neisseria gonorrhoeae a Izolaty wytwarzające β-laktamazy o największym spektrum (ESBL) i wytwarzające karbapenemazy są oporne na aksetyl cefuroksymu. Krętki Borrelia Burgdorferi
Dostępne są następujące dane in vitro, ale ich znaczenie kliniczne nie jest znane. Co najmniej 90 procent następujących drobnoustrojów wykazuje in vitro minimalne stężenie hamujące (MIC) mniejsze lub równe wartości granicznej wrażliwości dla aksetylu cefuroksymu wynoszące 1 µg/ml. Jednak skuteczność aksetylu cefuroksymu w leczeniu zakażeń klinicznych wywoływanych przez te drobnoustroje nie została ustalona w odpowiednich i dobrze kontrolowanych badaniach klinicznych.
Bakterie Gram-dodatnie
Staphylococcus epidermidis (tylko izolaty wrażliwe na metycylinę) Staphylococcus saprophyticus (tylko izolaty wrażliwe na metycylinę) Streptococcus agalactiae
Bakterie Gram-ujemne
Morganella morganii Proteus inconstans Proteus mirabilis Providencia rettgeri Bakterie beztlenowe Peptococcus niger
Metody badania wrażliwości
Jeśli to możliwe, laboratorium mikrobiologii klinicznej powinno przekazywać lekarzowi wyniki testów wrażliwości in vitro na leki przeciwdrobnoustrojowe stosowane w lokalnych szpitalach i gabinetach lekarskich w formie raportów okresowych opisujących profil wrażliwości patogenów szpitalnych i pozaszpitalnych. Raporty te powinny pomóc lekarzowi w wyborze leku przeciwbakteryjnego do leczenia.
Techniki rozcieńczania
Do określenia wartości MIC środków przeciwdrobnoustrojowych stosuje się metody ilościowe. Te wartości MIC zapewniają powtarzalne szacunki wrażliwości bakterii na związki przeciwdrobnoustrojowe. Wartości MIC należy określić przy użyciu znormalizowanej metody badawczej (bulion lub agar).1, 2 Wartości MIC należy interpretować zgodnie z kryteriami przedstawionymi w tabeli 10.2,3
Techniki dyfuzji
Metody ilościowe, które wymagają pomiaru średnic stref, zapewniają również powtarzalne szacunki podatności bakterii na związki przeciwdrobnoustrojowe. Wielkość strefy pozwala oszacować podatność bakterii na związki przeciwdrobnoustrojowe. Wielkość strefy należy określić przy użyciu znormalizowanej metody badawczej.4 W tej procedurze wykorzystuje się krążki papierowe nasączone 30 µg aksetylu cefuroksymu w celu zbadania wrażliwości drobnoustrojów na aksetyl cefuroksymu. Kryteria interpretacji dyfuzji krążkowej przedstawiono w tabeli 10.3
Wrażliwość gronkowców na cefuroksym można wywnioskować na podstawie badania wyłącznie penicyliny i cefoksytyny lub oksacyliny.
Wrażliwość Streptococcus pyogenes można wydedukować na podstawie badania penicyliny.3
Raport „Podatny” wskazuje, że lek przeciwdrobnoustrojowy prawdopodobnie hamuje wzrost patogenu, jeśli lek przeciwdrobnoustrojowy osiągnie stężenie zwykle osiągalne w miejscu zakażenia. Raport „Pośredni” wskazuje, że wynik należy uznać za niejednoznaczny, a jeśli drobnoustrój nie jest w pełni podatny na alternatywne, klinicznie możliwe do zastosowania leki, badanie należy powtórzyć. Ta kategoria implikuje możliwość zastosowania klinicznego w miejscach ciała, w których lek jest stężony fizjologicznie lub w sytuacjach, w których można stosować duże dawki leku. Ta kategoria zapewnia również strefę buforową, która zapobiega powodowaniu poważnych rozbieżności w interpretacji przez małe, niekontrolowane czynniki techniczne. Raport „Odporny” wskazuje, że lek przeciwdrobnoustrojowy prawdopodobnie nie będzie hamował wzrostu patogenu, jeśli lek przeciwdrobnoustrojowy osiągnie stężenia zwykle osiągalne w miejscu zakażenia; należy wybrać inną terapię.
Kontrola jakości
Znormalizowane procedury badania wrażliwości wymagają stosowania laboratoryjnych kontroli w celu monitorowania i zapewnienia dokładności i precyzji materiałów eksploatacyjnych i odczynników stosowanych w teście, a także technik wykonywanych przez osobę wykonującą badanie.1,2,4 Zakresy QC dla wartości MIC i dyfuzji krążkowej testy z użyciem dysku 30-mcg przedstawiono w tabeli 11.3
Studia kliniczne
Ostre bakteryjne zapalenie zatok szczękowych
Jedno odpowiednie i dobrze kontrolowane badanie przeprowadzono u pacjentów z ostrym bakteryjnym zapaleniem zatok szczękowych. W tym badaniu każdy pacjent miał aspirat z zatoki szczękowej pobrany przez nakłucie zatok przed rozpoczęciem leczenia z powodu przypuszczalnego ostrego bakteryjnego zapalenia zatok. Wszyscy badani mieli radiologiczne i kliniczne dowody ostrego zapalenia zatok szczękowych. W badaniu kliniczna skuteczność CEFTIN w leczeniu ostrego zapalenia zatok szczękowych była porównywalna z doustnym środkiem przeciwdrobnoustrojowym zawierającym swoisty inhibitor β-laktamazy. Jednak dane mikrobiologiczne wykazały, że CEFTIN jest skuteczny w leczeniu ostrego bakteryjnego zapalenia zatok szczękowych wywołanego wyłącznie przez Streptococcus pneumoniae lub Haemophilus influenzae nie wytwarzający β-laktamaz. W tym badaniu uzyskano niewystarczającą liczbę izolatów Haemophilus influenzae i Moraxella catarrhalis wytwarzających β-laktamazę, aby odpowiednio ocenić skuteczność CEFTIN w leczeniu ostrego bakteryjnego zapalenia zatok szczękowych wywołanego przez te 2 drobnoustroje.
badaniu tym zrandomizowano 317 osób dorosłych, 132 osoby w USA i 185 osób w Ameryce Południowej. Tabela 12 przedstawia wyniki analizy zgodnej z zamiarem leczenia.
W tym badaniu oraz w pomocniczym badaniu nakłucia szczęki u 15 ocenianych pacjentów jako zidentyfikowany patogen Haemophilus influenzae nie wytwarzał β-laktamaz. Spośród nich u 67% (10/15) ten patogen został wyeliminowany. Osiemnastu (18) ocenianych pacjentów miało Streptococcus pneumoniae jako zidentyfikowany patogen. Spośród nich u 83% (15/18) ten patogen został wyeliminowany.
Wczesna choroba z Lyme
Przeprowadzono dwa odpowiednie i dobrze kontrolowane badania u pacjentów z wczesną chorobą z Lyme. Wszyscy pacjenci mieli udokumentowany przez lekarza rumień wędrujący, z ogólnoustrojowymi objawami infekcji lub bez nich. Pacjentów oceniano po 1 miesiącu po leczeniu pod kątem powodzenia w leczeniu wczesnej choroby z Lyme (Część I) i po 1 roku po leczeniu pod kątem powodzenia w zapobieganiu progresji do następstw późnej choroby z Lyme (Część II).
Łącznie 355 dorosłych pacjentów (181 leczonych aksetylem cefuroksymu i 174 leczonych doksycykliną) zostało zrandomizowanych do 2 badań, z rozpoznaniem wczesnej choroby z Lyme potwierdzoną u 79% (281/355). Kliniczna diagnoza wczesnej choroby z Lyme u tych pacjentów została potwierdzona przez 1) zaślepionego eksperta czytanie fotografii, jeśli były dostępne, zmian skórnych związanych z rumieniem wędrującym przed leczeniem oraz 2) potwierdzenie serologiczne (za pomocą testu immunoenzymatycznego [ELISA] i testu immunoblot [„Western blot”]) obecności przeciwciał swoistych dla Borrelia burgdorferi, czynnika etiologicznego boreliozy. Dane dotyczące skuteczności w Tabeli 13 są specyficzne dla tej „zwalidowanej” podgrupy pacjentów, natomiast poniższe dane dotyczące bezpieczeństwa odzwierciedlają całą populację pacjentów w 2 badaniach. Dane kliniczne dla ocenianych osobników w „zwalidowanej” podgrupie pacjentów przedstawiono w Tabeli 13.
CEFTIN i doksycyklina były skuteczne w zapobieganiu rozwojowi następstw późnej boreliozy.
Chociaż częstość występowania działań niepożądanych ze strony przewodu pokarmowego związanych z lekiem była podobna w 2 grupach terapeutycznych (aksetyl cefuroksymu - 13%; doksycyklina - 11%), częstość występowania biegunki związanej z lekiem była wyższa w ramieniu aksetylu cefuroksymu w porównaniu z ramieniem doksycykliny (11 % w porównaniu z 3%, odpowiednio).
BIBLIOGRAFIA
1. Instytut Norm Klinicznych i Laboratoryjnych (CLSI). Metody rozcieńczeń Testy wrażliwości drobnoustrojów na bakterie, które rosną w warunkach tlenowych; Zatwierdzony standard — wydanie dziesiąte. 2015. Dokument CLSI M07-A10, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pensylwania 19087, USA.
2. Instytut Norm Klinicznych i Laboratoryjnych (CLSI). Metody rozcieńczania środków przeciwdrobnoustrojowych i badania wrażliwości dysku w przypadku rzadko izolowanych lub wymagających bakterii: Zatwierdzone wytyczne — wydanie drugie. 2010. Dokument CLSI M45-A2, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pensylwania 19087, USA.
3. Instytut Norm Klinicznych i Laboratoryjnych (CLSI). Normy wydajności dla badań wrażliwości na środki przeciwdrobnoustrojowe; Dwudziesty piąty dodatek informacyjny. 2015. Dokument CLSI M100-S25, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pensylwania 19087, USA.
4. Instytut Norm Klinicznych i Laboratoryjnych (CLSI). Normy wydajności dla testów podatności na dyfuzję przeciwdrobnoustrojową; Zatwierdzony standard — wydanie dwunaste. 2015. Dokument CLSI M02-A12, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pensylwania 19087, USA.
INFORMACJA O PACJENCIE
Reakcje alergiczne
Poinformuj pacjentów, że CEFTIN jest cefalosporyną, która może powodować reakcje alergiczne u niektórych osób [patrz OSTRZEŻENIA I ŚRODKI ].
Biegunka związana z Clostridium Difficile
Poinformuj pacjentów, że biegunka jest częstym problemem powodowanym przez leki przeciwbakteryjne i zwykle kończy się wraz z odstawieniem leku przeciwbakteryjnego. Czasami po rozpoczęciu leczenia lekami przeciwbakteryjnymi u pacjentów mogą pojawić się wodniste i krwawe stolce (ze skurczami żołądka i gorączką lub bez nich), nawet po 2 lub więcej miesiącach od przyjęcia ostatniej dawki leku przeciwbakteryjnego. W takim przypadku należy doradzić pacjentom, aby jak najszybciej skontaktowali się z lekarzem.
Fenyloketonuria
Należy poinformować pacjentów i ich opiekunów, że CEFTIN 125 mg do sporządzania zawiesiny doustnej zawiera fenyloalaninę (składnik aspartamu) [patrz OSTRZEŻENIA I ŚRODKI ].
Kruszenie Tabletki
Należy poinstruować pacjentów, aby połknęli tabletkę w całości, bez kruszenia tabletki. Pacjenci, którzy nie mogą połknąć tabletki w całości, powinni otrzymać zawiesinę doustną.
Zawiesina doustna
Należy poinstruować pacjentów, aby dobrze wstrząsnąć zawiesiną doustną przed każdym użyciem, przechowywać w lodówce i wyrzucić po 10 dniach. Zawiesinę doustną należy przyjmować z jedzeniem.
Odporność na leki
Poinformuj pacjentów, że leki przeciwbakteryjne, w tym CEFTIN, powinny być stosowane wyłącznie w leczeniu infekcji bakteryjnych. Nie leczą infekcji wirusowych (np. przeziębienia). Kiedy CEFTIN 250 mg jest przepisywany w celu leczenia infekcji bakteryjnej, należy poinformować pacjentów, że chociaż często czuje się lepiej na początku terapii, lek należy przyjmować dokładnie zgodnie z zaleceniami. Pomijanie dawek lub nieukończenie pełnego cyklu terapii może: (1) zmniejszyć skuteczność natychmiastowego leczenia oraz (2) zwiększyć prawdopodobieństwo, że bakterie rozwiną się oporność i nie będą mogły być wyleczone za pomocą CEFTIN 500 mg lub innych leków przeciwbakteryjnych w przyszłości .
