Flonase Nasal Spray 50mcg Fluticasone Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Flonase i jak się go stosuje?
Flonase to lek na receptę stosowany w leczeniu objawów alergicznego nieżytu nosa (kichanie, katar oraz swędzenie lub łzawienie oczu) oraz polipów nosa. Flonase można stosować samodzielnie lub z innymi lekami.
Flonaza należy do klasy leków zwanych kortykosteroidami, donosowymi, immunosupresyjnymi, PHD.
Nie wiadomo, czy Flonase jest bezpieczna i skuteczna u dzieci w wieku poniżej 4 lat.
Jakie są możliwe skutki uboczne Flonase?
Flonaza może powodować poważne skutki uboczne, w tym:
- ciężkie lub trwające krwawienia z nosa,
- głośny oddech,
- katar,
- skorupa wokół twoich nozdrzy,
- zaczerwienienie, owrzodzenia lub białe plamy w jamie ustnej lub gardle,
- gorączka,
- dreszcze,
- bóle,
- rozmazany obraz,
- ból oka,
- widząc aureole wokół świateł,
- rany, które się nie goją,
- nasilające się zmęczenie,
- słabe mięśnie,
- zawroty,
- nudności i
- wymioty
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Flonase to:
- niewielkie krwawienie z nosa,
- pieczenie lub swędzenie w nosie,
- owrzodzenia lub białe plamy wewnątrz lub wokół nosa,
- kaszel,
- problemy z oddychaniem,
- ból głowy,
- ból pleców,
- ból zatok,
- ból gardła,
- gorączka,
- nudności i
- wymioty
OPIS
Aktywnym składnikiem preparatu FLONASE Nasal Spray 50mcg jest propionian flutykazonu, kortykosteroid o nazwie chemicznej S-(fluorometylo)6α,9-difluoro-11β,17-dihydroksy-16α-metylo-3oksoandrosta-1,4-dieno-17β-karboksylan , 17-propionian i następującą budowę chemiczną:
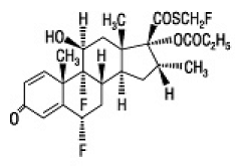
Propionian flutykazonu jest białym proszkiem o masie cząsteczkowej 500,6, a wzór empiryczny to C25H31F3O5S. Jest praktycznie nierozpuszczalny w wodzie, dobrze rozpuszczalny w dimetylosulfotlenku i dimetyloformamidzie oraz słabo rozpuszczalny w metanolu i 95% etanolu.
FLONASE Aerozol do nosa, 50 mcg, to wodna zawiesina mikrodrobnocząsteczkowego propionianu flutykazonu do podawania miejscowego na błonę śluzową nosa za pomocą dozującej, rozpylającej pompy rozpylającej. FLONASE aerozol do nosa 50mcg zawiera również mikrokrystaliczną celulozę i sól sodową karboksymetylocelulozy, dekstrozę, 0,02% w/w chlorek benzalkonium, polisorbat 80 i 0,25% w/w alkohol fenyloetylowy, a pH ma od 5 do 7.
Po wstępnym przygotowaniu, każde uruchomienie dostarcza 50 mcg propionianu flutykazonu w 100 mg preparatu przez nasadkę nosową.
WSKAZANIA
FLONASE® aerozol do nosa jest wskazany w leczeniu objawów nosowych całorocznego niealergicznego zapalenia błony śluzowej nosa u dorosłych i dzieci w wieku 4 lat i starszych.
DAWKOWANIE I SPOSÓB PODAWANIA
Podawać FLONASE aerozol do nosa wyłącznie drogą donosową. Przed pierwszym użyciem lub po okresie nieużywania (1 tydzień lub dłużej) należy zagruntować FLONASE aerozol do nosa, dobrze wstrząsając zawartością i wypuszczając 6 rozpyleń w powietrze z dala od twarzy. Lekko wstrząsnąć FLONASE aerozol do nosa przed każdym użyciem.
Pacjenci powinni stosować aerozol do nosa FLONASE w regularnych odstępach czasu, ponieważ jego skuteczność zależy od regularnego stosowania. Maksymalny efekt może potrwać kilka dni, a poszczególni pacjenci odczują różny czas do wystąpienia i różny stopień złagodzenia objawów.
Dorośli ludzie
Zalecana dawka początkowa u dorosłych to 2 rozpylenia (50 mcg propionianu flutykazonu każde) do każdego otworu nosowego raz na dobę (całkowita dawka dobowa 200 mcg). Ta sama całkowita dawka dzienna, 1 rozpylenie do każdego nozdrza podawane dwa razy dziennie (np. 8 rano i 20:00) jest również skuteczna. Po pierwszych kilku dniach pacjenci mogą być w stanie zmniejszyć dawkę do 1 rozpylenia do każdego otworu nosowego raz dziennie w celu leczenia podtrzymującego.
Maksymalna całkowita dawka dobowa nie powinna przekraczać 2 rozpyleń do każdego otworu nosowego (dawka całkowita 200 mcg/dobę). Nie ma dowodów na to, że przekroczenie zalecanej dawki jest skuteczniejsze.
Młodzież i dzieci (w wieku 4 lat i starsze)
Zalecana dawka początkowa u młodzieży i dzieci w wieku 4 lat i starszych to 1 rozpylenie do każdego otworu nosowego raz na dobę (całkowita dawka dobowa 100 mcg). Pacjenci niewystarczająco reagujący na 1 rozpylenie do każdego nozdrza mogą użyć 2 rozpyleń do każdego otworu nosowego raz dziennie (całkowita dawka dobowa 200 mcg). Po uzyskaniu odpowiedniej kontroli, dawkę należy zmniejszyć do 1 rozpylenia do każdego otworu nosowego raz na dobę.
Maksymalna całkowita dawka dobowa nie powinna przekraczać 2 rozpyleń do każdego otworu nosowego (200 mcg/dobę). Nie ma dowodów na to, że przekroczenie zalecanej dawki jest skuteczniejsze.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
FLONASE Aerozol do nosa jest zawiesiną aerozolu do nosa. Każde 100 mg sprayu dostarcza 50 mcg propionianu flutykazonu.
Składowania i stosowania
FLONASE Aerozol do nosa, 50 mcg jest dostarczany w butelce z oranżowego szkła wyposażonej w białą pompkę dozującą, białą nasadkę do nosa i zieloną osłonę przeciwpyłową w pudełku po 1 ( NDC 0173-0453-01) z aprobatą FDA Etykietowanie pacjenta (Widzieć Instrukcja obsługi dla pacjenta dotycząca prawidłowego uruchomienia urządzenia ). Każda butelka zawiera wagę netto 16 g i zapewnia 120 naciśnięć. Każde uruchomienie dostarcza 50 mcg propionianu flutykazonu w 100 mg preparatu przez nasadkę nosową. Prawidłowa ilość leku w każdym rozpyleniu nie może być zapewniona po 120 rozpyleniach, nawet jeśli butelka nie jest całkowicie pusta. Butelkę należy wyrzucić po użyciu podanej na etykiecie liczby naciśnięć.
Przechowywać w temperaturze od 4° do 30°C (39° i 86°F).
GlaxoSmithKline Research Triangle Park, NC 27709. Aktualizacja: styczeń 2015
SKUTKI UBOCZNE
Ogólnoustrojowe i miejscowe stosowanie kortykosteroidów może skutkować:
- Krwawienie z nosa, owrzodzenie nosa, zakażenie Candida albicans, perforacja przegrody nosowej i zaburzenia gojenia się ran [patrz OSTRZEŻENIA I ŚRODKI ]
- Zaćma i jaskra [patrz OSTRZEŻENIA I ŚRODKI ]
- Immunosupresja [patrz OSTRZEŻENIA I ŚRODKI ]
- Hiperkortyka i zahamowanie czynności kory nadnerczy [patrz OSTRZEŻENIA I ŚRODKI ]
- Wpływ na wzrost [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
W kontrolowanych badaniach klinicznych w USA ponad 3300 pacjentów z alergicznym i niealergicznym nieżytem nosa otrzymywało donosowe leczenie propionianem flutykazonu. Ogólnie rzecz biorąc, działania niepożądane w badaniach klinicznych wiązały się głównie z podrażnieniem błon śluzowych nosa, a działania niepożądane zgłaszano z mniej więcej taką samą częstością u osób otrzymujących placebo. Mniej niż 2% uczestników badań klinicznych przerwało badania z powodu działań niepożądanych; wskaźnik ten był podobny dla placebo i aktywnych komparatorów.
Opisane poniżej dane dotyczące bezpieczeństwa opierają się na 7 kontrolowanych placebo badaniach klinicznych u pacjentów z alergicznym nieżytem nosa. 7 badań obejmowało 536 pacjentów (57 dziewcząt i 108 chłopców w wieku od 4 do 11 lat, 137 kobiet i 234 nastolatków i dorosłych) leczonych produktem leczniczym FLONASE 200 µg raz na dobę przez 2 do 4 tygodni oraz 2 badania kliniczne kontrolowane placebo, które obejmowały 246 pacjentów (119 nastolatków płci żeńskiej i 127 nastolatków i dorosłych) leczonych produktem leczniczym FLONASE 200 mcg raz na dobę przez 6 miesięcy (Tabela 1). W Tabeli 1 uwzględniono również działania niepożądane z 2 badań, w których 167 dzieci (45 dziewcząt i 122 chłopców w wieku od 4 do 11 lat) leczono preparatem FLONASE 100 mcg raz na dobę przez 2 do 4 tygodni.
Inne działania niepożądane związane ze stosowaniem produktu FLONASE Aerozol do nosa 50 µg obserwowane z częstością mniejszą lub równą 3%, ale większą lub równą 1% i częściej niż w przypadku placebo obejmowały: krew w wydzielinie z nosa, katar, ból brzucha, biegunka, gorączka, objawy grypopodobne, bóle, zawroty głowy i zapalenie oskrzeli.
Doświadczenie postmarketingowe
Poza zdarzeniami niepożądanymi zgłoszonymi w badaniach klinicznych, podczas stosowania donosowego propionianu flutykazonu po jego zatwierdzeniu zidentyfikowano następujące zdarzenia niepożądane. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek. Zdarzenia te zostały wybrane do włączenia ze względu na ich powagę, częstotliwość zgłaszania lub związek przyczynowy z propionianem flutykazonu lub połączenie tych czynników.
Ogólne zaburzenia i warunki miejsca administracji
Reakcje nadwrażliwości, w tym obrzęk naczynioruchowy, wysypka skórna, obrzęk twarzy i języka, świąd, pokrzywka, skurcz oskrzeli, świszczący oddech, duszność i reakcje anafilaktyczne/anafilaktoidalne, które w rzadkich przypadkach były ciężkie.
Zaburzenia ucha i labiryntu
Zmiana lub utrata zmysłu smaku i (lub) węchu i rzadko perforacja przegrody nosowej, owrzodzenie nosa, ból gardła, podrażnienie i suchość gardła, kaszel, chrypka i zmiany głosu.
Zaburzenia oka
Suchość i podrażnienie, zapalenie spojówek, niewyraźne widzenie, jaskra, podwyższone ciśnienie śródgałkowe i zaćma.
Zgłaszano przypadki zahamowania wzrostu po podaniu donosowych kortykosteroidów, w tym leku FLONASE [patrz OSTRZEŻENIA I ŚRODKI ].
INTERAKCJE Z LEKAMI
Inhibitory cytochromu P450 3A4
Propionian flutykazonu jest substratem CYP3A4. Stosowanie silnych inhibitorów CYP3A4 (np. rytonawir, atazanawir, klarytromycyna, indynawir, itrakonazol, nefazodon, nelfinawir, sakwinawir, ketokonazol, telitromycyna, koniwaptan, lopinawir, nefazodon, worykonazol niezalecany ze względu na działanie niepożądane na układ doustny może wystąpić.
Rytonawir
Badanie interakcji leków z wodnym roztworem propionianu flutykazonu w aerozolu do nosa u zdrowych osób wykazało, że rytonawir (silny inhibitor CYP3A4) może znacząco zwiększać ekspozycję na propionian flutykazonu w osoczu, co skutkuje znacznym zmniejszeniem stężenia kortyzolu w surowicy [patrz FARMAKOLOGIA KLINICZNA ]. W okresie po wprowadzeniu produktu do obrotu zgłaszano klinicznie istotne interakcje u pacjentów otrzymujących produkty zawierające propionian flutykazonu, w tym FLONASE, z rytonawirem, powodujące ogólnoustrojowe działanie kortykosteroidów, w tym zespół Cushinga i zahamowanie czynności kory nadnerczy.
Ketokonazol
Jednoczesne podawanie wziewnego propionianu flutykazonu (1000 mcg) i ketokonazolu (200 mg raz na dobę) powodowało 1,9-krotne zwiększenie ekspozycji na propionian flutykazonu w osoczu i 45% zmniejszenie powierzchni kortyzolu w osoczu pod krzywą (AUC), ale nie miało żadnego wpływu na wydalanie kortyzolu z moczem.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Lokalne efekty nosowe
Krwawienie z nosa
badaniach klinicznych trwających od 2 do 26 tygodni krwawienie z nosa obserwowano częściej u osób leczonych produktem leczniczym FLONASE aerozol do nosa niż u osób otrzymujących placebo [patrz DZIAŁANIA NIEPOŻĄDANE ].
Owrzodzenie nosa
Po wprowadzeniu produktu do obrotu zgłaszano przypadki owrzodzenia nosa u pacjentów leczonych produktem leczniczym FLONASE aerozol do nosa [patrz DZIAŁANIA NIEPOŻĄDANE ].
Zakażenie Candida
W badaniach klinicznych z propionianem flutykazonu podawanym donosowo wystąpił rozwój miejscowych zakażeń nosa i gardła wywołanych przez Candida albicans. Gdy taka infekcja się rozwinie, może wymagać leczenia odpowiednią terapią miejscową i przerwania stosowania aerozolu do nosa FLONASE. Pacjenci stosujący aerozol do nosa FLONASE przez kilka miesięcy lub dłużej powinni być okresowo badani pod kątem obecności zakażenia Candida lub innych objawów niepożądanych działań na błonę śluzową nosa.
Perforacja przegrody nosowej
Po wprowadzeniu produktu do obrotu zgłaszano przypadki perforacji przegrody nosowej u pacjentów leczonych produktem leczniczym FLONASE aerozol do nosa [patrz DZIAŁANIA NIEPOŻĄDANE ].
Upośledzone gojenie się ran
Ze względu na hamujący wpływ kortykosteroidów na gojenie się ran, pacjenci, którzy niedawno przeszli owrzodzenie nosa, operację nosa lub uraz nosa, powinni unikać stosowania produktu FLONASE aerozol do nosa do czasu zagojenia.
Jaskra i zaćma
Stosowanie kortykosteroidów donosowych i wziewnych może spowodować rozwój jaskry i (lub) zaćmy. W związku z tym uzasadnione jest ścisłe monitorowanie pacjentów ze zmianami widzenia lub ze zwiększonym ciśnieniem wewnątrzgałkowym w wywiadzie, jaskrą i (lub) zaćmą.
Reakcje nadwrażliwości, w tym anafilaksja
Reakcje nadwrażliwości (np. anafilaksja, obrzęk naczynioruchowy, pokrzywka, kontaktowe zapalenie skóry i wysypka) były zgłaszane po podaniu produktu FLONASE aerozol do nosa. Przerwać FLONASE
Aerozol do nosa, jeśli takie reakcje wystąpią [patrz PRZECIWWSKAZANIA ]. Rzadko po podaniu produktu FLONASE aerozol do nosa mogą wystąpić natychmiastowe reakcje nadwrażliwości.
Immunosupresja
Osoby stosujące leki hamujące układ odpornościowy są bardziej podatne na infekcje niż osoby zdrowe. Na przykład ospa wietrzna i odra mogą mieć bardziej poważny, a nawet śmiertelny przebieg u podatnych dzieci lub dorosłych stosujących kortykosteroidy. W przypadku takich dzieci lub osób dorosłych, które nie miały tych chorób lub nie zostały odpowiednio zaszczepione, należy zachować szczególną ostrożność, aby uniknąć narażenia. Nie wiadomo, w jaki sposób dawka, droga i czas podawania kortykosteroidów wpływają na ryzyko rozwoju rozsianego zakażenia. Nie jest również znany wpływ choroby podstawowej i/lub wcześniejszego leczenia kortykosteroidami na ryzyko. Jeśli pacjent jest narażony na ospę wietrzną, może być wskazana profilaktyka immunoglobuliną ospy wietrznej i półpaśca (VZIG). Jeśli pacjent jest narażony na odrę, może być wskazana profilaktyka za pomocą puli immunoglobulin domięśniowych (IG). (Widzieć pełne informacje dotyczące przepisywania leków VZIG i IG. W przypadku rozwoju ospy wietrznej można rozważyć leczenie środkami przeciwwirusowymi.
Kortykosteroidy donosowe należy stosować ostrożnie, jeśli w ogóle, u pacjentów z czynnymi lub nieaktywnymi gruźliczymi zakażeniami dróg oddechowych; ogólnoustrojowe infekcje grzybicze, bakteryjne, wirusowe lub pasożytnicze; lub opryszczka oczna.
Hiperkortyka i zahamowanie czynności kory nadnerczy
Gdy kortykosteroidy donosowe są stosowane w dawkach większych niż zalecane lub u osób wrażliwych w zalecanych dawkach, mogą wystąpić ogólnoustrojowe działania kortykosteroidów, takie jak hiperkortyza i zahamowanie czynności kory nadnerczy. W przypadku wystąpienia takich zmian, dawkowanie produktu FLONASE aerozol do nosa należy odstawiać powoli, zgodnie z przyjętymi procedurami przerywania leczenia doustnymi kortykosteroidami.
Zastąpieniu kortykosteroidu ogólnoustrojowego kortykosteroidem stosowanym miejscowo mogą towarzyszyć objawy niewydolności nadnerczy. Ponadto niektórzy pacjenci mogą odczuwać objawy odstawienia kortykosteroidów (np. ból stawów i (lub) mięśni, zmęczenie, depresja). Pacjenci wcześniej leczeni przez dłuższy czas kortykosteroidami ogólnoustrojowymi i przeniesieni do miejscowych kortykosteroidów powinni być uważnie obserwowani pod kątem ostrej niewydolności nadnerczy w odpowiedzi na stres. U pacjentów z astmą lub innymi stanami klinicznymi wymagającymi długotrwałego ogólnoustrojowego leczenia kortykosteroidami, gwałtowne zmniejszanie ogólnoustrojowych dawek kortykosteroidów może spowodować poważne nasilenie objawów.
Interakcje leków z silnymi inhibitorami cytochromu P450 3A4
Stosowanie silnych inhibitorów cytochromu P450 3A4 (CYP3A4) (np. rytonawir, atazanawir, klarytromycyna, indynawir, itrakonazol, nefazodon, nelfinawir, sakwinawir, ketokonazol, telitromycyna, koniwaptan, lopinawir, neworofazodon w sprayu z nefazodonem zalecany) mogą wystąpić zwiększone ogólnoustrojowe działania niepożądane kortykosteroidów [patrz INTERAKCJE Z LEKAMI , FARMAKOLOGIA KLINICZNA ].
Wpływ na wzrost
Kortykosteroidy donosowe mogą powodować spowolnienie wzrostu, gdy są podawane pacjentom pediatrycznym [patrz Stosowanie w określonych populacjach ]. Rutynowo monitorować wzrost pacjentów pediatrycznych otrzymujących FLONASE aerozol do nosa. Aby zminimalizować ogólnoustrojowe działanie kortykosteroidów donosowych, w tym leku FLONASE w aerozolu do nosa, należy miareczkować dawkę każdego pacjenta do najniższej dawki, która skutecznie kontroluje jego objawy [patrz DAWKOWANIE I SPOSÓB PODAWANIA , Używaj w określonych populacjach ].
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( INFORMACJE DLA PACJENTA i instrukcje użytkowania ).
Lokalne efekty nosowe
Należy poinformować pacjentów, że leczenie lekiem FLONASE aerozol do nosa 50 mikrogramów może prowadzić do działań niepożądanych, w tym krwawienia z nosa i owrzodzenia nosa. Zakażenie Candida może również wystąpić podczas leczenia lekiem FLONASE aerozol do nosa. Ponadto, FLONASE Nasal Spray 50mcg wiązał się z perforacją przegrody nosowej i upośledzeniem gojenia się ran. Pacjenci, którzy niedawno doświadczyli owrzodzenia nosa, operacji nosa lub urazu nosa, nie powinni stosować leku FLONASE Aerozol do nosa 50mcg do czasu zagojenia [patrz OSTRZEŻENIA I ŚRODKI ].
Jaskra i zaćma
Poinformuj pacjentów, że jaskra i zaćma są związane ze stosowaniem kortykosteroidów donosowych i wziewnych. Doradzić pacjentom, aby powiadomili swoich lekarzy w przypadku zauważenia zmiany widzenia podczas stosowania leku FLONASE aerozol do nosa [patrz OSTRZEŻENIA I ŚRODKI ].
Reakcje nadwrażliwości, w tym anafilaksja
Należy poinformować pacjentów, że po podaniu produktu FLONASE aerozol do nosa mogą wystąpić reakcje nadwrażliwości, w tym anafilaksja, obrzęk naczynioruchowy, pokrzywka, kontaktowe zapalenie skóry i wysypka. W przypadku wystąpienia takich reakcji pacjenci powinni przerwać stosowanie leku FLONASE aerozol do nosa [patrz OSTRZEŻENIA I ŚRODKI ].
Immunosupresja
Ostrzeż pacjentów, którzy przyjmują immunosupresyjne dawki kortykosteroidów, aby uniknąć narażenia na ospę wietrzną lub odrę, a jeśli są narażeni, aby niezwłocznie skonsultować się z lekarzem. Poinformuj pacjentów o potencjalnym pogorszeniu istniejącej gruźlicy; infekcje grzybicze, bakteryjne, wirusowe lub pasożytnicze; lub opryszczka oczna [patrz OSTRZEŻENIA I ŚRODKI ].
Zmniejszona prędkość wzrostu
Poinformuj rodziców, że FLONASE Aerozol do nosa 50mcg może powodować spowolnienie wzrostu, gdy jest podawany pacjentom pediatrycznym. Lekarze powinni uważnie śledzić rozwój dzieci i młodzieży przyjmujących kortykosteroidy dowolną drogą [patrz OSTRZEŻENIA I ŚRODKI , Zastosowanie pediatryczne ].
Używaj codziennie, aby uzyskać najlepszy efekt
Poinformuj pacjentów, że powinni regularnie stosować FLONASE aerozol do nosa 50mcg. FLONASE Aerozol do nosa 50mcg, podobnie jak inne kortykosteroidy, nie ma natychmiastowego wpływu na objawy nieżytu nosa. Maksymalna korzyść może nie zostać osiągnięta przez kilka dni. Pacjenci nie powinni zwiększać przepisanej dawki, ale powinni skontaktować się z lekarzem, jeśli objawy nie ustąpią lub stan się pogorszy.
Trzymaj spray z dala od oczu i ust
Należy poinformować pacjentów, aby unikali rozpylania leku FLONASE aerozol do nosa do oczu i ust.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Propionian flutykazonu nie wykazał potencjału rakotwórczego u myszy przy dawkach doustnych do 1000 mcg/kg (około 20-krotność MRHDID u dorosłych i około 10-krotność MRHDID u dzieci w przeliczeniu na mcg/m²) przez 78 tygodni lub u szczurów przy dawkach wziewnych większych do 57 μg/kg (około 2 razy więcej niż MRHDID u dorosłych i w przybliżeniu równoważny MRHDID u dzieci na podstawie mcg/m²) przez 104 tygodnie.
Propionian flutykazonu nie indukował mutacji genów w komórkach prokariotycznych lub eukariotycznych in vitro. Nie zaobserwowano istotnego działania klastogennego w hodowlach ludzkich limfocytów obwodowych in vitro ani w teście mikrojądrowym u myszy.
Nie zaobserwowano dowodów na upośledzenie płodności u samców i samic szczurów po podaniu podskórnym dawek do 50 mcg/kg (około 2-krotność MRHDID u dorosłych w przeliczeniu na mcg/m²). Masa prostaty została znacznie zmniejszona przy podskórnej dawce 50 mcg/kg.
Studia kliniczne
Całoroczny niealergiczny nieżyt nosa
Przeprowadzono trzy randomizowane, podwójnie zaślepione, w grupach równoległych, kontrolowane placebo badania z zastosowaniem nośnika z udziałem 1191 pacjentów w celu zbadania regularnego stosowania produktu leczniczego FLONASE aerozol do nosa 50 µg u pacjentów z całorocznym niealergicznym nieżytem nosa. W badaniach tych oceniano ocenianą przez pacjenta całkowitą punktację objawów ze strony nosa (TNSS), która obejmowała niedrożność nosa, wyciek z nosa, wyciek z nosa u pacjentów leczonych przez 28 dni metodą podwójnie ślepej próby oraz w 1 z 3 badań przez 6 miesięcy leczenia metodą otwartej próby. W dwóch z tych badań wykazano, że osoby leczone preparatem FLONASE aerozol do nosa (100 µg dwa razy na dobę) wykazywały statystycznie istotne zmniejszenie TNSS w porównaniu z osobami, którym podawano nośnik.
Używaj w określonych populacjach
Ciąża
Efekty teratogenne
Ciąża Kategoria C. Nie przeprowadzono odpowiednich i dobrze kontrolowanych badań z użyciem preparatu FLONASE aerozol do nosa u kobiet w ciąży. Wykazano, że kortykosteroidy są teratogenne u zwierząt laboratoryjnych, gdy są podawane ogólnoustrojowo w stosunkowo niskich dawkach. Ponieważ badania na zwierzętach dotyczące reprodukcji nie zawsze pozwalają przewidzieć odpowiedź u ludzi, FLONASE aerozol do nosa należy stosować w okresie ciąży tylko wtedy, gdy potencjalna korzyść uzasadnia potencjalne ryzyko dla płodu. Należy doradzić kobietom, aby w przypadku zajścia w ciążę podczas stosowania leku FLONASE aerozol do nosa skontaktowały się z lekarzem.
Myszy i szczury otrzymujące propionian flutykazonu w dawkach odpowiednio około 1 i 4 razy większej od maksymalnej zalecanej dobowej dawki donosowej u ludzi (MRHDID) dla dorosłych (w przeliczeniu na mg/m² przy dawkach podskórnych u matki odpowiednio 45 i 100 mcg/kg/dobę) wykazały toksyczność płodową charakterystyczną dla silnych związków kortykosteroidowych, w tym opóźnienie wzrostu embrionów, przepuklinę pępkową, rozszczep podniebienia i opóźnione kostnienie czaszki. Nie zaobserwowano działania teratogennego u szczurów przy dawkach do 3 razy większych niż MRHDID (w przeliczeniu na mg/m² przy dawkach wziewnych do 68,7 µg/kg/dobę u matki).
królików zmniejszenie masy ciała płodów i rozszczep podniebienia obserwowano po podaniu propionianu flutykazonu w dawce około 0,3 razy większej niż MRHDID dla dorosłych (w przeliczeniu na mg/m² przy dawce podskórnej 4 µg/kg/dobę dla matki). Jednak nie zgłoszono żadnego działania teratogennego przy dawkach propionianu flutykazonu do około 20 razy większych od MRHDID u dorosłych (w przeliczeniu na mg/m² przy dawce doustnej do 300 mcg/kg/dobę dla matki). W tym badaniu nie wykryto propionianu flutykazonu w osoczu, co jest zgodne z ustaloną niską biodostępnością po podaniu doustnym [patrz FARMAKOLOGIA KLINICZNA ].
Propionian flutykazonu przenikał przez łożysko po podskórnym podaniu myszom i szczurom oraz doustnym podaniu królikom.
Doświadczenie z doustnymi kortykosteroidami od czasu ich wprowadzenia do dawek farmakologicznych, w przeciwieństwie do fizjologicznych, sugeruje, że gryzonie są bardziej podatne na działanie teratogenne kortykosteroidów niż ludzie. Ponadto, ponieważ w czasie ciąży występuje naturalny wzrost produkcji kortykosteroidów, większość kobiet będzie wymagała mniejszej dawki kortykosteroidów egzogennych, a wiele z nich nie będzie wymagało leczenia kortykosteroidami podczas ciąży.
Efekty nieteratogenne
Niedoczynność kory nadnerczy może wystąpić u niemowląt urodzonych przez matki otrzymujące kortykosteroidy w czasie ciąży. Takie niemowlęta powinny być dokładnie monitorowane.
Matki karmiące
Nie wiadomo, czy propionian flutykazonu przenika do mleka ludzkiego. Jednak w mleku ludzkim wykryto inne kortykosteroidy. Podskórne podanie trytowanym propionianowi flutykazonu trytowanemu propionianowi flutykazonu w okresie laktacji szczurom w dawce około 0,4 razy większej niż MRHDID dla dorosłych w przeliczeniu na mg/m2 powodowało mierzalną radioaktywność w mleku.
Ponieważ nie ma danych z kontrolowanych badań dotyczących stosowania donosowego produktu FLONASE Aerozol do nosa 50mcg przez matki karmiące piersią, należy zachować ostrożność przy podawaniu produktu FLONASE Aerozol do nosa 50mcg kobiecie karmiącej.
Zastosowanie pediatryczne
Ustalono bezpieczeństwo i skuteczność leku FLONASE aerozol do nosa u dzieci w wieku 4 lat i starszych [patrz DZIAŁANIA NIEPOŻĄDANE , FARMAKOLOGIA KLINICZNA Sześćset pięćdziesiąt (650) osób w wieku od 4 do 11 lat i 440 osób w wieku od 12 do 17 lat przebadano w amerykańskich badaniach klinicznych z zastosowaniem aerozolu do nosa z propionianem flutykazonu. Bezpieczeństwo i skuteczność leku FLONASE Aerozol do nosa 50mcg u dzieci w wieku poniżej 4 lat nie zostały ustalone.
Wpływ na wzrost
Kontrolowane badania kliniczne wykazały, że kortykosteroidy podawane donosowo mogą powodować spowolnienie wzrostu, gdy są podawane pacjentom pediatrycznym. Efekt ten zaobserwowano przy braku laboratoryjnych dowodów na zahamowanie osi podwzgórze-przysadka-nadnercza (HPA), co sugeruje, że szybkość wzrostu jest bardziej czułym wskaźnikiem ogólnoustrojowej ekspozycji na kortykosteroidy u dzieci niż niektóre powszechnie stosowane testy czynności osi HPA. Długoterminowe skutki tego zmniejszenia szybkości wzrostu związanego z donosowymi kortykosteroidami, w tym wpływ na ostateczny wzrost osoby dorosłej, są nieznane. Możliwość „nadrobienia” wzrostu po przerwaniu leczenia kortykosteroidami donosowymi nie została odpowiednio zbadana. Wzrost dzieci i młodzieży otrzymujących kortykosteroidy donosowe, w tym FLONASE aerozol do nosa, powinien być rutynowo monitorowany (np. za pomocą stadiometrii). Potencjalny wpływ przedłużonego leczenia na wzrost należy porównać z uzyskanymi korzyściami klinicznymi i ryzykiem związanym z terapiami alternatywnymi. Aby zminimalizować ogólnoustrojowe działanie kortykosteroidów donosowych, w tym produktu FLONASE aerozol do nosa, dawkę każdego pacjenta należy zmniejszać do najmniejszej dawki, która skutecznie kontroluje jego objawy.
Przeprowadzono roczne badanie kontrolowane placebo z udziałem 150 pacjentów pediatrycznych (w wieku od 3 do 9 lat) w celu oceny wpływu produktu FLONASE aerozol do nosa (pojedyncza dawka dobowa 200 mikrogramów) na szybkość wzrostu. W pierwotnej populacji otrzymującej FLONASE aerozol do nosa (n = 56) i placebo (n = 52), oszacowanie punktowe szybkości wzrostu po zastosowaniu produktu FLONASE aerozol do nosa 50 μg było o 0,14 cm/rok niższe niż w przypadku placebo (95% CI: -0,54, 0,27 cm /rok). Nie odnotowano zatem statystycznie istotnego wpływu na wzrost w porównaniu z placebo. Nie zaobserwowano żadnych dowodów klinicznie istotnych zmian w funkcji osi HPA lub gęstości mineralnej kości, ocenianych odpowiednio na podstawie 12-godzinnego wydalania kortyzolu z moczem i dwuenergetycznej absorpcjometrii rentgenowskiej.
Nie można wykluczyć, że FLONASE Aerozol do nosa 50mcg może powodować zahamowanie wzrostu u podatnych pacjentów lub gdy jest podawany w dawkach wyższych niż zalecane.
Zastosowanie geriatryczne
Ograniczona liczba pacjentów w wieku 65 lat i starszych (n = 129) lub 75 lat i starszych (n = 11) była leczona preparatem FLONASE aerozol do nosa w badaniach klinicznych. Chociaż liczba pacjentów jest zbyt mała, aby umożliwić oddzielną analizę skuteczności i bezpieczeństwa, działania niepożądane zgłaszane w tej populacji były podobne do zgłaszanych przez młodszych pacjentów. Ogólnie rzecz biorąc, dobór dawki u pacjentów w podeszłym wieku powinien być ostrożny, zwykle zaczynając od dolnej granicy zakresu dawkowania, co odzwierciedla większą częstość pogorszenia czynności wątroby, nerek lub serca oraz współistniejących chorób lub innych leków.
Niewydolność wątroby
Nie przeprowadzono formalnych badań farmakokinetycznych z użyciem preparatu FLONASE aerozol do nosa 50 mcg u osób z zaburzeniami czynności wątroby. Ponieważ propionian flutykazonu jest usuwany głównie w wyniku metabolizmu wątrobowego, zaburzenia czynności wątroby mogą prowadzić do akumulacji propionianu flutykazonu w osoczu. Dlatego pacjenci z chorobą wątroby powinni być ściśle monitorowani.

Zaburzenia czynności nerek
Nie przeprowadzono formalnych badań farmakokinetycznych z użyciem produktu FLONASE aerozol do nosa u osób z zaburzeniami czynności nerek.
PRZEDAWKOWAĆ
Przewlekłe przedawkowanie może skutkować oznakami/objawami hiperkortycyzmu (patrz ŚRODKI OSTROŻNOŚCI ). Donosowe podawanie 2 mg (10-krotność zalecanej dawki) propionianu flutykazonu dwa razy na dobę przez 7 dni zdrowym ochotnikom było dobrze tolerowane. U ochotników badano pojedyncze dawki doustne do 16 mg, nie zgłaszając żadnych ostrych skutków toksycznych. Powtarzane dawki doustne do 80 mg na dobę przez 10 dni u ochotników i powtarzane dawki doustne do 10 mg na dobę przez 14 dni u pacjentów były dobrze tolerowane. Działania niepożądane miały nasilenie łagodne lub umiarkowane, a częstość występowania była podobna w grupach otrzymujących lek aktywny i placebo. Ostre przedawkowanie tej postaci dawkowania jest mało prawdopodobne, ponieważ 1 butelka leku FLONASE (propionian flutykazonu) do nosa zawiera około 8 mg propionianu flutykazonu.
Średnie dawki śmiertelne podawane doustnie i podskórnie u myszy i szczurów wynosiły >1000 mg/kg (odpowiednio >20 000 i >41 000 razy maksymalna zalecana dobowa dawka donosowa u dorosłych oraz odpowiednio >10 000 i >20 000 razy maksymalna zalecana dobowa dawka donosowa). u dzieci w mg/m2).
PRZECIWWSKAZANIA
FLONASE (propionian flutykazonu) aerozol do nosa jest przeciwwskazany u pacjentów z nadwrażliwością na którykolwiek ze składników.
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Propionian flutykazonu jest syntetycznym trójfluorowanym kortykosteroidem o działaniu przeciwzapalnym. Wykazano in vitro, że propionian flutykazonu wykazuje 18-krotnie większe powinowactwo do ludzkiego receptora glukokortykoidowego niż deksametazon, prawie dwukrotnie większe niż 17-monopropionian beklometazonu (BMP), aktywny metabolit dipropionianu beklometazonu, i ponad 3 razy większe. budezonidu. Dane z testu zwężania naczyń McKenzie u człowieka są zgodne z tymi wynikami. Kliniczne znaczenie tych wyników nie jest znane.
Dokładny mechanizm wpływu propionianu flutykazonu na objawy nieżytu nosa nie jest znany. Wykazano, że kortykosteroidy mają szeroki zakres działania na wiele typów komórek (np. komórki tuczne, eozynofile, neutrofile, makrofagi, limfocyty) i mediatorów (np. histamina, eikozanoidy, leukotrieny, cytokiny) biorących udział w zapaleniu. W 7 badaniach z udziałem dorosłych, FLONASE aerozol do nosa spowodował zmniejszenie liczby eozynofili błony śluzowej nosa u 66% pacjentów (35% w przypadku placebo) i bazofilów u 39% pacjentów (28% w przypadku placebo). Nie jest znany bezpośredni związek tych wyników z długoterminowym łagodzeniem objawów.
Farmakodynamika
Efekt osi HPA
Oceniono potencjalny ogólnoustrojowy wpływ FLONASE Nasal Spray 50mcg na oś HPA. FLONASE Aerozol do nosa 50 mcg podawany jako 200 mcg raz na dobę lub 400 mcg dwa razy na dobę porównywano z placebo lub doustnym prednizonem w dawce 7,5 lub 15 mg podawanym rano. FLONASE aerozol do nosa w żadnej z dawek przez 4 tygodnie nie wpływał na odpowiedź nadnerczy na 6-godzinną stymulację kosyntropiną, podczas gdy obie dawki doustnego prednizonu znacząco zmniejszały odpowiedź na kosyntropinę.
Elektrofizjologia serca
Nie przeprowadzono badania zaprojektowanego specjalnie w celu oceny wpływu produktu FLONASE na odstęp QT.
Farmakokinetyka
Aktywność FLONASE Nasal Spray 50mcg zawdzięcza swojemu macierzystemu lekowi, propionianowi flutykazonu. Ze względu na niską biodostępność drogą donosową większość danych farmakokinetycznych uzyskano innymi drogami podania.
Wchłanianie
Obliczenia pośrednie wskazują, że propionian flutykazonu dostarczany drogą donosową ma bezwzględną biodostępność średnio poniżej 2%. Badania z zastosowaniem doustnego dawkowania znakowanego i nieznakowanego leku wykazały, że ogólnoustrojowa biodostępność flutykazonu propionianu jest znikoma (
Dystrybucja
Po podaniu dożylnym początkowa faza usuwania propionianu flutykazonu była szybka i zgodna z jego wysoką rozpuszczalnością w tłuszczach i wiązaniem z tkankami. Objętość dystrybucji wynosiła średnio 4,2 l/kg.
Odsetek propionianu flutykazonu związanego z białkami osocza ludzkiego wynosił średnio 99%. Propionian flutykazonu słabo i odwracalnie wiąże się z erytrocytami i nie wiąże się znacząco z ludzką transkortyną.
Eliminacja
Po podaniu dożylnym propionian flutykazonu wykazywał wielowykładniczą kinetykę i miał okres półtrwania w końcowej fazie eliminacji wynoszący około 7,8 godziny. Całkowity klirens flutykazonu propionianu jest wysoki (średnio: 1093 ml/min), przy czym klirens nerkowy stanowi mniej niż 0,02% całkowitego.
Metabolizm: Jedynym krążącym metabolitem wykrytym u człowieka jest pochodna kwasu 17β-karboksylowego propionianu flutykazonu, która powstaje na szlaku CYP3A4. Ten metabolit miał mniejsze powinowactwo (około 1/2000) niż lek macierzysty do receptora glukokortykoidowego ludzkiego cytozolu płucnego in vitro i znikomą aktywność farmakologiczną w badaniach na zwierzętach. Inne metabolity wykryte in vitro przy użyciu hodowanych ludzkich komórek wątrobiaka nie zostały wykryte u człowieka.
Wydalanie: Mniej niż 5% dawki doustnej znakowanej radioizotopem było wydalane z moczem w postaci metabolitów, a pozostała część była wydalana z kałem jako lek macierzysty i metabolity.
Specjalne populacje
Flutykazonu propionian w aerozolu do nosa nie był badany w żadnej szczególnej populacji i nie uzyskano danych farmakokinetycznych specyficznych dla płci.
Interakcje leków
Inhibitory cytochromu P450 3A4: Rytonawir: Propionian flutykazonu jest substratem CYP3A4. Jednoczesne podawanie propionianu flutykazonu i silnego inhibitora CYP3A4, rytonawiru, nie jest zalecane w oparciu o badanie interakcji krzyżowych z wielokrotnymi dawkami leku u 18 zdrowych osób. Wodny aerozol do nosa z propionianem flutykazonu (200 µg raz dziennie) podawano przez 7 dni jednocześnie z rytonawirem (100 mg dwa razy dziennie). Stężenia propionianu flutykazonu w osoczu po samym rozpylaniu do nosa flutykazonu propionianu były niewykrywalne (
Ketokonazol: Jednoczesne podawanie wziewnego propionianu flutykazonu (1000 mcg) i ketokonazolu (200 mg raz na dobę) powodowało 1,9-krotne zwiększenie ekspozycji na propionian flutykazonu w osoczu i 45% zmniejszenie AUC kortyzolu w osoczu, ale nie miało wpływu na wydalanie kortyzolu z moczem.
Erytromycyna: W badaniu interakcji z wielokrotnymi dawkami jednoczesne podawanie wziewnego propionianu flutykazonu (500 µg dwa razy na dobę) i erytromycyny (333 mg trzy razy na dobę) nie miało wpływu na farmakokinetykę propionianu flutykazonu.
INFORMACJA O PACJENCIE
FLONASE® [flow'naz] (propionian flutykazonu) aerozol do nosa, 50 mcg
Przeczytaj informacje dla pacjenta dołączone do aerozolu do nosa FLONASE, zanim zaczniesz go używać i za każdym razem, gdy otrzymasz uzupełnienie. Mogą pojawić się nowe informacje. Niniejsze Informacje dla pacjenta nie zastępują rozmowy z lekarzem o stanie zdrowia lub leczeniu.
Co to jest aerozol do nosa FLONASE?
FLONASE Nasal Spray 50mcg jest lekiem na receptę stosowanym w leczeniu niealergicznych objawów ze strony nosa, takich jak katar, zatkany nos, kichanie i swędzenie nosa u dorosłych i dzieci w wieku 4 lat i starszych.
Nie wiadomo, czy FLONASE aerozol do nosa 50mcg jest bezpieczny i skuteczny u dzieci w wieku poniżej 4 lat.
Kto nie powinien stosować aerozolu do nosa FLONASE 50mcg?
Nie należy stosować leku FLONASE aerozol do nosa 50mcg, jeśli pacjent ma uczulenie na propionian flutykazonu lub którykolwiek ze składników aerozolu do nosa FLONASE. Zobacz „Jakie są składniki w aerozolu do nosa FLONASE 50mcg?” poniżej pełna lista składników.
O czym powinienem powiedzieć lekarzowi przed zastosowaniem leku FLONASE Aerozol do nosa 50mcg?
Poinformuj swojego dostawcę opieki zdrowotnej o wszystkich swoich schorzeniach, w tym jeśli:
- masz lub miałeś owrzodzenie nosa, operację nosa lub uraz nosa.
- mieć problemy z oczami, takie jak zaćma lub jaskra.
- masz problem z układem odpornościowym.
- jesteś uczulony na którykolwiek ze składników aerozolu do nosa FLONASE, jakiekolwiek inne leki lub produkty spożywcze. Widzieć „Jakie są składniki aerozolu do nosa FLONASE?” poniżej pełna lista składników.
- mieć jakikolwiek rodzaj infekcji wirusowej, bakteryjnej lub grzybiczej.
- są narażone na ospę wietrzną lub odrę.
- masz jakiekolwiek inne schorzenia.
- są w ciąży lub planują zajść w ciążę. Nie wiadomo, czy FLONASE aerozol do nosa może zaszkodzić nienarodzonemu dziecku.
- karmisz piersią lub planujesz karmić piersią. Nie wiadomo, czy FLONASE Aerozol do nosa 50mcg przenika do mleka matki i czy może zaszkodzić dziecku.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe. FLONASE aerozol do nosa i niektóre inne leki mogą wchodzić ze sobą w interakcje. Może to spowodować poważne skutki uboczne. W szczególności poinformuj swojego lekarza o przyjmowaniu leków przeciwgrzybiczych lub przeciw HIV.
Poznaj leki, które przyjmujesz. Zachowaj ich listę, aby pokazać swojemu lekarzowi i farmaceucie, kiedy otrzymasz nowy lek.
Jak stosować aerozol do nosa FLONASE?
Przeczytaj szczegółowe instrukcje dotyczące stosowania leku FLONASE aerozol do nosa znajdujące się na końcu niniejszej Informacji dla pacjenta.
- FLONASE aerozol do nosa należy stosować wyłącznie do nosa. Nie rozpylaj go do oczu ani ust.
- Dzieci powinny stosować aerozol do nosa FLONASE z pomocą osoby dorosłej, zgodnie z instrukcjami lekarza dziecka.
- Stosuj FLONASE aerozol do nosa 50mcg dokładnie tak, jak mówi lekarz. Nie należy stosować leku FLONASE aerozol do nosa częściej niż zalecono.
- Regularne stosowanie leku FLONASE aerozol do nosa może potrwać kilka dni w celu złagodzenia objawów nieżytu nosa. Jeśli objawy nie ulegną poprawie lub się pogorszą, skontaktuj się z lekarzem.
- Najlepsze rezultaty osiągniesz, jeśli będziesz regularnie codziennie stosować FLONASE aerozol do nosa bez pominięcia jednej dawki. Gdy poczujesz się lepiej, Twój lekarz może zmniejszyć dawkę. Nie rób zaprzestać stosowania leku FLONASE aerozol do nosa 50mcg, chyba że zaleci to lekarz.
Jakie są możliwe skutki uboczne FLONASE Aerozol do nosa 50mcg?
FLONASE Aerozol do nosa 50mcg może powodować poważne skutki uboczne, w tym:
- problemy z nosem. Problemy z nosem mogą obejmować:
- krwotok z nosa.
- owrzodzenia (wrzody) w nosie.
- pewne zakażenie grzybicze nosa, jamy ustnej i (lub) gardła (pleśniawki).
- dziura w chrząstce nosa (perforacja przegrody nosowej). Objawy perforacji przegrody nosowej mogą obejmować:
- skorupa w nosie
- krwotok z nosa
- katar
- świszczący dźwięk podczas oddychania
- powolne gojenie się ran. Nie należy stosować leku FLONASE aerozol do nosa, dopóki nos się nie zagoi, jeśli masz ból w nosie, przeszedłeś operację nosa lub jeśli nos został uszkodzony.
- problemy z oczami, w tym jaskra i zaćma. Podczas stosowania aerozolu do nosa FLONASE należy regularnie poddawać się badaniom oczu.
- poważne reakcje alergiczne. Zadzwoń do swojego lekarza lub uzyskaj pomoc medyczną w nagłych wypadkach, jeśli wystąpi którykolwiek z następujących objawów poważnej reakcji alergicznej:
- wysypka
- pokrzywka
- obrzęk twarzy, ust i języka
- problemy z oddychaniem
- osłabiony układ odpornościowy i zwiększone ryzyko infekcji (immunosupresja). Przyjmowanie leków osłabiających układ odpornościowy zwiększa ryzyko infekcji i może pogorszyć niektóre infekcje. Zakażenia te mogą obejmować gruźlicę (TB), zakażenia oczu wirusem opryszczki pospolitej oraz zakażenia wywołane przez grzyby, bakterie, wirusy i pasożyty. Unikaj kontaktu z osobami cierpiącymi na choroby zakaźne, takie jak ospa wietrzna lub odra, podczas stosowania aerozolu do nosa FLONASE. Jeśli wejdziesz w kontakt z kimś, kto ma ospę wietrzną lub odrę, natychmiast skontaktuj się z lekarzem. Objawy infekcji mogą obejmować:
- gorączka
- czuć się zmęczonym
- ból
- mdłości
- bóle
- wymioty
- dreszcze
- obniżone poziomy hormonów steroidowych (niewydolność nadnerczy). Niewydolność nadnerczy ma miejsce, gdy nadnercza nie wytwarzają wystarczającej ilości hormonów steroidowych. Może się to zdarzyć po zaprzestaniu przyjmowania doustnych kortykosteroidów (takich jak prednizon) i rozpoczęciu przyjmowania leku zawierającego wziewny steroid (takiego jak FLONASE aerozol do nosa). Objawy niewydolności nadnerczy mogą obejmować:
- czuć się zmęczonym
- brak energii
- słabość
- nudności i wymioty
- niskie ciśnienie krwi
- spowolniony wzrost u dzieci. Rozwój dziecka powinien być często sprawdzany.
Najczęstsze skutki uboczne FLONASE Aerozol do nosa 50mcg to:
- ból głowy
- nudności i wymioty
- ból gardła
- problemy z oddychaniem
- krwotok z nosa
- kaszel
- pieczenie lub swędzenie nosa
Poinformuj swojego lekarza o wszelkich skutkach ubocznych, które Ci przeszkadzają lub nie ustępują.
To nie wszystkie skutki uboczne stosowania leku FLONASE aerozol do nosa. Zapytaj swojego lekarza lub farmaceutę o więcej informacji.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać FLONASE Aerozol do nosa 50mcg?
- Przechowywać FLONASE w temperaturze od 39°F do 86°F (4°C do 30°C).
Przechowywać FLONASE Aerozol do nosa 50mcg i wszystkie leki w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu aerozolu do nosa FLONASE.
Czasami leki są przepisywane do celów niewymienionych w ulotce informacyjnej dla pacjenta. Nie należy stosować leku FLONASE aerozol do nosa w stanach, na które nie został przepisany. Nie należy podawać leku FLONASE aerozol do nosa innym osobom, nawet jeśli mają one taki sam stan jak ty. Może im to zaszkodzić.
Niniejsza ulotka z informacjami dla pacjenta podsumowuje najważniejsze informacje dotyczące leku FLONASE aerozol do nosa. Jeśli chcesz uzyskać więcej informacji, porozmawiaj ze swoim lekarzem. Możesz poprosić farmaceutę lub pracownika służby zdrowia o informacje na temat leku FLONASE aerozol do nosa, który został napisany dla pracowników służby zdrowia.
Aby uzyskać więcej informacji o aerozolu do nosa FLONASE, zadzwoń pod numer 1-888-825-5249.
Jakie są składniki FLONASE aerozol do nosa 50mcg?
Składnik aktywny: propionian flutykazonu.
Składniki nieaktywne: celuloza mikrokrystaliczna, sól sodowa karboksymetylocelulozy, dekstroza, 0,02% w/w chlorek benzalkoniowy, polisorbat 80 i 0,25% w/w alkohol fenyloetylowy.
Instrukcja użycia
FLONASE® [flow'naz] (propionian flutykazonu) aerozol do nosa, 50 mcg
FLONASE Aerozol do nosa 50mcg należy stosować wyłącznie do nosa.
Przeczytaj te informacje przed rozpoczęciem stosowania aerozolu do nosa FLONASE.
Części twojego aerozolu do nosa FLONASE (Patrz Rysunek A)
Rysunek A 
Twój aerozol do nosa FLONASE 50mcg musi zostać zagruntowany przed użyciem go po raz pierwszy i gdy nie był używany przez tydzień lub dłużej.
Jak przygotować spray do nosa FLONASE?
- Delikatnie wstrząśnij butelką, a następnie zdejmij osłonę przeciwpyłową (Patrz Rysunek B).
Rysunek B 
- Trzymaj butelkę, jak pokazano (Patrz Rysunek C), aplikatorem do nosa skierowanym od siebie, palcem wskazującym i środkowym po obu stronach aplikatora do nosa, a kciukiem pod butelką.
- Naciśnij i zwolnij 6 razy, aż pojawi się drobny strumień (patrz Rysunek C). Pompa jest teraz gotowa do użycia.
Rysunek C 
Stosowanie aerozolu do nosa FLONASE:
Krok 1 . Wydmuchaj nos, aby oczyścić nozdrza.
Krok 2 . Zamknij 1 nozdrze. Lekko przechylić głowę do przodu i trzymając butelkę w pozycji pionowej, ostrożnie włożyć aplikator do nosa do drugiego nozdrza (patrz Rysunek D).
Rysunek D 
Krok 3 Zacznij robić wdech przez nos i podczas wdechu naciśnij mocno i szybko 1 raz aplikator, aby uwolnić spray. Aby uzyskać pełną dawkę, użyj palca wskazującego i środkowego do rozpylenia, podtrzymując jednocześnie podstawę butelki kciukiem. Unikaj rozpylania w oczach. Wykonać delikatny wdech przez nozdrze (Patrz Rysunek E).
Rysunek E 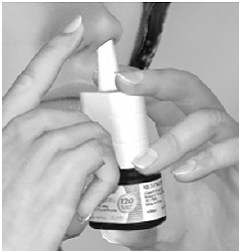
Krok 4 . Wydychaj przez usta.
Krok 5 . Jeśli wymagane jest drugie rozpylenie do tego nozdrza, powtórz kroki od 2 do 4.
Krok 6 . Powtórz kroki od 2 do 5 w drugim nozdrzu.
Krok 7 . Wytrzyj aplikator do nosa czystą chusteczką i załóż osłonę przeciwpyłową (Patrz Rysunek F).
Rysunek F 
Nie używaj tej butelki do więcej niż podanej liczby rozpyleń, nawet jeśli butelka nie jest całkowicie pusta. Zanim wyrzucisz butelkę, powinieneś porozmawiać z lekarzem, aby sprawdzić, czy potrzebne jest uzupełnienie. Nie należy przyjmować dodatkowych dawek ani przerywać stosowania leku FLONASE Aerozol do nosa 50mcg bez konsultacji z lekarzem.
Czyszczenie sprayu do nosa FLONASE:
Twój aerozol do nosa należy czyścić co najmniej 1 raz w tygodniu.
1. Zdejmij osłonę przeciwpyłową, a następnie delikatnie pociągnij w górę, aby uwolnić aplikator do nosa.
2. Umyj aplikator i osłonę przeciwpyłową pod ciepłą wodą z kranu. Pozostaw do wyschnięcia w temperaturze pokojowej.
3. Umieść aplikator i osłonę przeciwpyłową z powrotem na butelce.
4. Jeśli aplikator do nosa zostanie zablokowany, można go wyjąć i pozostawić do namoczenia w ciepłej wodzie. Wypłucz aplikator do nosa zimną wodą z kranu. Wysusz aplikator do nosa i umieść go z powrotem na butelce. Nie próbuj odblokowywać aplikatora do nosa przez wbicie szpilki lub innego ostrego przedmiotu.
Przechowywanie aerozolu do nosa FLONASE:
- Przechowywać FLONASE aerozol do nosa 50mcg w temperaturze od 39°F do 86°F (4°C do 30°C).
- Nie należy stosować aerozolu do nosa FLONASE po upływie daty oznaczonej jako „EXP” na etykiecie lub pudełku.
