Glucovance 400/2.50mg, 500/5mg Metformin Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Glucovance 2,50 mg i jak się go stosuje?
Glucovance 400mg to lek na receptę stosowany w leczeniu objawów cukrzycy typu 2. Glucovance może być stosowany samodzielnie lub z innymi lekami.
Glucovance należy do klasy leków zwanych przeciwcukrzycowymi, sulfonylomocznikami/biguanidami.
Nie wiadomo, czy Glucovance 2,50 mg jest bezpieczny i skuteczny u dzieci.
Jakie są możliwe skutki uboczne Glucovance 400mg?
Glucovance może powodować poważne skutki uboczne, w tym:
- pokrzywka,
- trudności w oddychaniu,
- obrzęk twarzy, warg, języka lub gardła,
- obrzęk,
- szybki przyrost masy ciała,
- duszność,
- skrajna słabość,
- rozmazany obraz,
- wyzysk,
- kłopoty z mówieniem,
- drżenia,
- ból brzucha,
- dezorientacja,
- drgawki,
- nietypowy ból mięśni,
- problemy z oddychaniem,
- ból brzucha,
- wymioty,
- nieregularne tętno,
- zawroty głowy,
- uczucie zimna,
- słabość i
- zmęczenie
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Glucovance to:
- niski poziom cukru we krwi,
- mdłości,
- biegunka,
- rozstrój żołądka i
- ból głowy
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Glucovance. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
Tabletki GLUCOVANCE® (gliburyd i metformina HCl) zawierają 2 doustne leki przeciwhiperglikemiczne stosowane w leczeniu cukrzycy typu 2, gliburyd i chlorowodorek metforminy.
Glyburyd jest doustnym lekiem przeciwhiperglikemicznym z klasy sulfonylomocznika. Nazwa chemiczna gliburydu to 1-[[p-[2-(5-chloro-o-anisamido)etylo]fenylo]sulfonylo]-3-cykloheksylomocznik. Glyburyd jest białym lub prawie białym krystalicznym związkiem o wzorze cząsteczkowym C23H28ClN3O5S i masie cząsteczkowej 494,01. Gliburyd stosowany w GLUCOVANCE 5 mg ma rozkład wielkości cząstek 25% podsitowy nie więcej niż 6 μm, 50% podsitowy nie większy niż 7 do 10 μm i 75% podsitowy nie większy niż 21 μm. Wzór strukturalny jest przedstawiony poniżej.
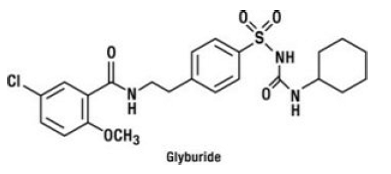
Chlorowodorek metforminy jest doustnym lekiem przeciwhiperglikemicznym stosowanym w leczeniu cukrzycy typu 2. Chlorowodorek metforminy (monochlorowodorek diamidu N,N-dimetyloimidodikarbonimidowego) nie jest chemicznie ani farmakologicznie spokrewniony z sulfonylomocznikami, tiazolidynodionami lub inhibitorami α-glukozydazy. Jest to biały lub prawie biały krystaliczny związek o wzorze cząsteczkowym C4H12ClN5 (monochlorowodorek) i masie cząsteczkowej 165,63. Chlorowodorek metforminy jest łatwo rozpuszczalny w wodzie i praktycznie nierozpuszczalny w acetonie, eterze i chloroformie. pKa metforminy wynosi 12,4. pH 1% wodnego roztworu chlorowodorku metforminy wynosi 6,68. Wzór strukturalny jest następujący:
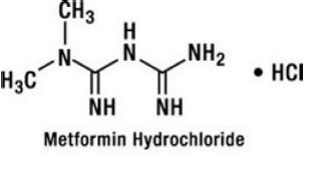
Produkt GLUCOVANCE 500 mg jest dostępny do podawania doustnego w tabletkach zawierających 1,25 mg gliburydu z 250 mg chlorowodorku metforminy, 2,5 mg gliburydu z 500 mg chlorowodorku metforminy i 5 mg gliburydu z 500 mg chlorowodorku metforminy. Dodatkowo każda tabletka zawiera następujące składniki nieaktywne: celulozę mikrokrystaliczną, powidon, kroskarmelozę sodową oraz stearynian magnezu. Tabletki są powlekane, co zapewnia rozróżnianie kolorów.
WSKAZANIA
Tabletki GLUCOVANCE (gliburyd i metformina HCl) są wskazane jako uzupełnienie diety i ćwiczeń fizycznych w celu poprawy kontroli glikemii u osób dorosłych z cukrzycą typu 2.
DAWKOWANIE I SPOSÓB PODAWANIA
Uwagi ogólne
Dawkowanie preparatu GLUCOVANCE należy dostosować indywidualnie na podstawie zarówno skuteczności, jak i tolerancji, nie przekraczając maksymalnej zalecanej dawki dobowej wynoszącej 20 mg gliburydu/2000 mg metforminy. GLUCOVANCE należy podawać z posiłkami i rozpoczynać od małej dawki, stopniowo zwiększając dawkę, jak opisano poniżej, w celu uniknięcia hipoglikemii (głównie z powodu gliburydu), zmniejszenia działań niepożądanych ze strony przewodu pokarmowego (głównie z powodu metforminy) i umożliwienia określenia minimalna skuteczna dawka zapewniająca odpowiednią kontrolę stężenia glukozy we krwi dla indywidualnego pacjenta.
Podczas początkowego leczenia i podczas zwiększania dawki należy monitorować stężenie glukozy we krwi w celu określenia odpowiedzi terapeutycznej na GLUCOVANCE 2,50 mg i określenia minimalnej skutecznej dawki dla pacjenta. Następnie należy mierzyć HbA1c w odstępach około 3 miesięcy, aby ocenić skuteczność terapii. Celem terapeutycznym u wszystkich pacjentów z cukrzycą typu 2 jest zmniejszenie FPG, PPG i HbA1c do wartości prawidłowych lub jak najbardziej zbliżonych do normy. Idealnie odpowiedź na leczenie powinna być oceniana przy użyciu HbA (hemoglobina glikozylowana), która jest lepszym wskaźnikiem długoterminowej kontroli glikemii niż sama FPG.
Nie przeprowadzono żadnych badań konkretnie oceniających bezpieczeństwo i skuteczność zmiany leczenia na GLUCOVANCE 400 mg u pacjentów przyjmujących jednocześnie gliburyd (lub inną sulfonylomocznik) w skojarzeniu z metforminą. U takich pacjentów mogą wystąpić zmiany w kontroli glikemii, z możliwą hiperglikemią lub hipoglikemią. Wszelkie zmiany w leczeniu cukrzycy typu 2 należy podejmować ostrożnie i pod odpowiednim nadzorem.
GLUCOVANCE u pacjentów z niewystarczającą kontrolą glikemii podczas diety i ćwiczeń fizycznych
Zalecana dawka początkowa: 1,25 mg/250 mg raz lub dwa razy dziennie z posiłkami.
pacjentów z cukrzycą typu 2, u których hiperglikemii nie można skutecznie opanować samą dietą i ćwiczeniami, zalecana dawka początkowa produktu GLUCOVANCE 400 mg wynosi 1,25 mg/250 mg raz na dobę z posiłkiem. Jako leczenie początkowe u pacjentów z wyjściową wartością HbA1c > 9% lub FPG > 200 mg/dl można zastosować dawkę początkową GLUCOVANCE 1,25 mg/250 mg dwa razy na dobę z porannymi i wieczornymi posiłkami. Dawkę należy zwiększać o 1,25 mg/250 mg na dobę co 2 tygodnie aż do minimalnej skutecznej dawki niezbędnej do uzyskania odpowiedniej kontroli stężenia glukozy we krwi. W badaniach klinicznych GLUCOVANCE jako terapii początkowej nie było doświadczenia z całkowitymi dawkami dobowymi > 10 mg/2000 mg na dobę. Produktu GLUCOVANCE 5 mg/500 mg nie należy stosować jako leczenia początkowego ze względu na zwiększone ryzyko hipoglikemii.
GLUCOVANCE 500 mg Stosowanie u pacjentów z niewystarczającą kontrolą glikemii po zastosowaniu sulfonylomocznika i/lub metforminy
Zalecana dawka początkowa: 2,5 mg/500 mg lub 5 mg/500 mg dwa razy dziennie z posiłkami.
pacjentów, u których nie uzyskano wystarczającej kontroli glikemii za pomocą gliburydu (lub innej pochodnej sulfonylomocznika) lub samej metforminy, zalecana dawka początkowa produktu GLUCOVANCE wynosi 2,5 mg/500 mg lub 5 mg/500 mg dwa razy na dobę z porannymi i wieczornymi posiłkami. Aby uniknąć hipoglikemii, dawka początkowa produktu GLUCOVANCE 2,50 mg nie powinna przekraczać dotychczas przyjmowanych dawek dobowych gliburydu lub metforminy. Dawkę dobową należy zwiększać o nie więcej niż 5 mg/500 mg aż do minimalnej skutecznej dawki w celu uzyskania odpowiedniej kontroli stężenia glukozy we krwi lub do maksymalnej dawki 20 mg/2000 mg na dobę.
przypadku pacjentów wcześniej leczonych terapią skojarzoną gliburydem (lub inną pochodną sulfonylomocznika) z metforminą, jeśli zmieniono leczenie na GLUCOVANCE, dawka początkowa nie powinna przekraczać dawki dobowej gliburydu (lub równoważnej dawki innej pochodnej sulfonylomocznika) i metforminy, które są już przyjmowane. Pacjentów należy ściśle monitorować pod kątem objawów przedmiotowych i podmiotowych hipoglikemii po takiej zmianie, a dawkę produktu GLUCOVANCE należy dostosowywać zgodnie z powyższym opisem, aby uzyskać odpowiednią kontrolę stężenia glukozy we krwi.
Dodanie tiazolidynodionów do terapii GLUCOVANCE
przypadku pacjentów, u których nie uzyskano wystarczającej kontroli za pomocą preparatu GLUCOVANCE, do leczenia preparatem GLUCOVANCE 400 mg można dodać tiazolidynodion. W przypadku dodania tiazolidynodionu do terapii GLUCOVANCE można kontynuować dotychczasową dawkę GLUCOVANCE 500 mg i rozpocząć leczenie tiazolidynodionem w zalecanej dawce początkowej. U pacjentów wymagających dodatkowej kontroli glikemii dawkę tiazolidynodionu można zwiększyć zgodnie z zalecanym schematem zwiększania dawki. Zwiększona kontrola glikemii możliwa do osiągnięcia dzięki GLUCOVANCE z tiazolidynodionem może zwiększać ryzyko hipoglikemii o dowolnej porze dnia. U pacjentów, u których wystąpiła hipoglikemia po podaniu produktu GLUCOVANCE 5 mg i tiazolidynodionu, należy rozważyć zmniejszenie dawki gliburydu jako składnika produktu GLUCOVANCE. Jeśli jest to uzasadnione klinicznie, należy również rozważyć dostosowanie dawek innych składników schematu przeciwcukrzycowego.
Pacjenci otrzymujący kolesewelam
Gdy kolesewelam jest podawany jednocześnie z gliburydem, maksymalne stężenie w osoczu i całkowita ekspozycja na gliburyd są zmniejszone. Dlatego GLUCOVANCE należy podawać co najmniej 4 godziny przed kolesewelamem.
Określone populacje pacjentów
GLUCOVANCE nie jest zalecany do stosowania w czasie ciąży. Początkowe i podtrzymujące dawkowanie produktu GLUCOVANCE powinno być zachowane u pacjentów w podeszłym wieku ze względu na możliwość pogorszenia czynności nerek w tej populacji. Każda zmiana dawkowania wymaga starannej oceny czynności nerek. Ogólnie rzecz biorąc, u pacjentów w podeszłym wieku, osłabionych i niedożywionych nie należy zwiększać dawki produktu GLUCOVANCE do maksymalnej dawki, aby uniknąć ryzyka hipoglikemii. Monitorowanie czynności nerek jest konieczne w celu zapobiegania kwasicy mleczanowej związanej z metforminą, szczególnie u osób starszych. (Widzieć OSTRZEŻENIA .)
JAK DOSTARCZONE
Tabletki GLUCOVANCE® (gliburyd i metformina HCl)
GLUKOVANCE 1,25 mg/250 mg Tabletka jest jasnożółtą, w kształcie kapsułki, o ściętych krawędziach, obustronnie wypukłą, powlekaną tabletką z „ BMS ” wytłoczone z jednej strony i “ 6072 ” wytłoczone po przeciwnej stronie.
GLUCOVANCE 2,5 mg/500 mg Tabletka jest jasnopomarańczową, w kształcie kapsułki, o ściętych krawędziach, obustronnie wypukłą, powlekaną tabletką z „ BMS ” wytłoczone z jednej strony i “ 6073 ” wytłoczone po przeciwnej stronie.
GLUCOVANCE 5 mg/500 mg tabletka jest żółta, w kształcie kapsułki, o ściętych brzegach, dwuwypukła, powlekana tabletka z „ BMS ” wytłoczone z jednej strony i “ 6074 ” wytłoczone po przeciwnej stronie.
Magazynowanie
Przechowywać w temperaturze do 25°C (77°F). [Widzieć Temperatura pokojowa kontrolowana przez USP .]
Dozować w pojemnikach odpornych na światło.
Dystrybutor: Bristol-Myers Squibb Company, Princeton, NJ 08543 USA 1158884A7. Wersja paź 2013
SKUTKI UBOCZNE
GLUKOWANCJA
badaniach klinicznych z podwójnie ślepą próbą z użyciem preparatu GLUCOVANCE 2,50 mg jako terapii początkowej lub jako terapii drugiego rzutu, łącznie 642 pacjentów otrzymywało preparat GLUCOVANCE 2,50 mg, 312 otrzymywało leczenie metforminą, 324 otrzymywało leczenie gliburydem, a 161 otrzymywało placebo. Odsetek pacjentów zgłaszających zdarzenia i rodzaje zdarzeń niepożądanych zgłoszonych w badaniach klinicznych produktu GLUCOVANCE (wszystkie moce) jako leczenie początkowe i leczenie drugiego rzutu przedstawiono w Tabeli 6.
W kontrolowanym badaniu klinicznym rozyglitazonu w porównaniu z placebo u pacjentów leczonych preparatem GLUCOVANCE (n=365), 181 pacjentów otrzymywało preparat GLUCOVANCE 5 mg z rozyglitazonem, a 184 otrzymywało preparat GLUCOVANCE z placebo.
Obrzęk zgłaszano u 7,7% (14/181) pacjentów leczonych rozyglitazonem w porównaniu z 2,2% (4/184) pacjentów otrzymujących placebo. U pacjentów leczonych rozyglitazonem obserwowano średni przyrost masy ciała o 3 kg.
U pacjentów leczonych gliburydem w tabletkach bardzo rzadko zgłaszano reakcje podobne do disulfiramu.
Hipoglikemia
kontrolowanych badaniach klinicznych produktu GLUCOVANCE 5 mg nie wystąpiły epizody hipoglikemii wymagające interwencji medycznej i (lub) leczenia farmakologicznego; wszystkie zdarzenia były zarządzane przez pacjentów. Częstość zgłaszanych objawów hipoglikemii (takich jak zawroty głowy, drżenie, pocenie się i głód) w początkowej próbie leczenia GLUCOVANCE 2,50 mg podsumowano w Tabeli 7. Częstość występowania objawów hipoglikemii u pacjentów leczonych preparatem GLUCOVANCE 1,25 mg/250 mg był najwyższy u pacjentów z wyjściową HbA1c 8%. U pacjentów z wyjściową wartością HbA1c między 8% a 11% leczonych GLUCOVANCE 2,5 mg/500 mg jako leczenie początkowe, częstość objawów hipoglikemii wynosiła od 30% do 35%. W leczeniu drugiego rzutu u pacjentów z niewystarczająco kontrolowaną glikemią samą pochodną sulfonylomocznika u około 6,8% wszystkich pacjentów leczonych preparatem GLUCOVANCE 2,50 mg wystąpiły objawy hipoglikemii. Po dodaniu rozyglitazonu do leczenia GLUCOVANCE 2,50 mg, 22% pacjentów zgłosiło co najmniej 1 pomiar stężenia glukozy z palca ≤ 50 mg/dl w porównaniu z 3,3% pacjentów otrzymujących placebo. Wszystkie zdarzenia hipoglikemii były leczone przez pacjentów i tylko 1 pacjent przerwał leczenie z powodu hipoglikemii. (Widzieć ŚRODKI OSTROŻNOŚCI : Ogólny : Dodanie tiazolidynodionów do terapii GLUCOVANCE .)
Reakcje żołądkowo-jelitowe
Częstość występowania działań niepożądanych ze strony przewodu pokarmowego (biegunka, nudności/wymioty i ból brzucha) w początkowym badaniu terapeutycznym podsumowano w Tabeli 7. We wszystkich badaniach GLUCOVANCE 500 mg objawy żołądkowo-jelitowe były najczęstszymi zdarzeniami niepożądanymi po podaniu GLUCOVANCE 400 mg i były częściej przy wyższych dawkach.
W kontrolowanych badaniach
W doniesieniach po wprowadzeniu produktu do obrotu rzadko może wystąpić żółtaczka cholestatyczna i zapalenie wątroby, które może prowadzić do niewydolności wątroby; W takim przypadku należy przerwać podawanie produktu Glucovance 5 mg.
INTERAKCJE Z LEKAMI
GLUKOWANCJA
Niektóre leki mają tendencję do wywoływania hiperglikemii i mogą prowadzić do utraty kontroli stężenia glukozy we krwi. Leki te obejmują tiazydy i inne leki moczopędne, kortykosteroidy, fenotiazyny, produkty tarczycy, estrogeny, doustne środki antykoncepcyjne, fenytoinę, kwas nikotynowy, sympatykomimetyki, leki blokujące kanały wapniowe i izoniazyd. Gdy takie leki są podawane pacjentowi otrzymującemu GLUCOVANCE 400 mg, należy uważnie obserwować pacjenta pod kątem utraty kontroli stężenia glukozy we krwi. Po odstawieniu takich leków pacjentowi otrzymującemu GLUCOVANCE należy uważnie obserwować pacjenta pod kątem hipoglikemii. Metformina w nieznacznym stopniu wiąże się z białkami osocza i dlatego jest mniej prawdopodobne, że będzie wchodzić w interakcje z lekami silnie wiążącymi się z białkami, takimi jak salicylany, sulfonamidy, chloramfenikol i probenecyd, w porównaniu z pochodnymi sulfonylomocznika, które silnie wiążą się z białkami surowicy.
Glyburyd
Działanie hipoglikemizujące sulfonylomoczników może być nasilane przez niektóre leki, w tym niesteroidowe leki przeciwzapalne i inne leki silnie związane z białkami, salicylany, sulfonamidy, chloramfenikol, probenecyd, kumaryny, inhibitory monoaminooksydazy i leki blokujące receptory beta-adrenergiczne. Gdy takie leki są podawane pacjentowi otrzymującemu GLUCOVANCE, należy uważnie obserwować pacjenta pod kątem hipoglikemii. Po odstawieniu takich leków pacjentowi otrzymującemu GLUCOVANCE 2,50 mg należy uważnie obserwować pacjenta pod kątem utraty kontroli stężenia glukozy we krwi.
U pacjentów otrzymujących gliburyd jednocześnie z bozentanem obserwowano zwiększone ryzyko zwiększenia aktywności enzymów wątrobowych. Dlatego jednoczesne podawanie produktu GLUCOVANCE i bozentanu jest przeciwwskazane.
Odnotowano możliwą interakcję między gliburydem a cyprofloksacyną, antybiotykiem fluorochinolonowym, skutkującą nasileniem hipoglikemicznego działania gliburydu. Mechanizm tej interakcji nie jest znany.
Zgłaszano potencjalną interakcję między doustnym mikonazolem i doustnymi środkami hipoglikemizującymi, prowadzącą do ciężkiej hipoglikemii. Nie wiadomo, czy ta interakcja występuje również w przypadku preparatów mikonazolu podawanych dożylnie, miejscowo lub dopochwowo.
Kolesewelam: Jednoczesne podawanie kolesewelamu i gliburydu powodowało zmniejszenie AUC i Cmax gliburydu odpowiednio o 32% i 47%. Zmniejszenie AUC i Cmax gliburydu wyniosło odpowiednio 20% i 15% po podaniu 1 godzinę przed i nie zmieniło się znacząco (odpowiednio -7% i 4%) po podaniu 4 godziny przed kolesewelamem.
Chlorowodorek metforminy
Furosemid
Badanie interakcji leków z pojedynczą dawką metformina-furosemid u zdrowych osób wykazało, że jednoczesne podawanie miało wpływ na parametry farmakokinetyczne obu związków. Furosemid zwiększał Cmax metforminy w osoczu i krwi o 22% i AUC we krwi o 15%, bez znaczącej zmiany klirensu nerkowego metforminy. Przy podawaniu z metforminą wartości Cmax i AUC furosemidu były odpowiednio o 31% i 12% mniejsze niż przy podawaniu w monoterapii, a końcowy okres półtrwania zmniejszył się o 32%, bez znaczącej zmiany klirensu nerkowego furosemidu. Brak dostępnych informacji na temat interakcji metforminy i furosemidu przy przewlekłym podawaniu.
Nifedypina
Badanie interakcji metforminy z nifedypiną po podaniu pojedynczej dawki u zdrowych ochotników wykazało, że jednoczesne podawanie nifedypiny zwiększało Cmax i AUC metforminy w osoczu odpowiednio o 20% i 9% oraz zwiększało ilość wydalaną z moczem. Tmax i okres półtrwania pozostały bez zmian. Wydaje się, że nifedypina zwiększa wchłanianie metforminy. Metformina miała minimalny wpływ na nifedypinę.
Leki kationowe
Leki kationowe (np. amiloryd, digoksyna, morfina, prokainamid, chinidyna, chinina, ranitydyna, triamteren, trimetoprim lub wankomycyna), które są eliminowane przez wydzielanie w kanalikach nerkowych, teoretycznie mogą wchodzić w interakcje z metforminą poprzez konkurowanie o wspólne systemy transportu w kanalikach nerkowych. Taką interakcję między metforminą a doustną cymetydyną obserwowano u zdrowych ochotników zarówno w badaniach interakcji metforminy z cymetydyną po podaniu pojedynczej, jak i wielokrotnej dawki, z 60% wzrostem maksymalnego stężenia metforminy w osoczu i pełnej krwi oraz 40% wzrostem w osoczu. i AUC metforminy w pełnej krwi. Nie było zmiany w okresie półtrwania eliminacji w badaniu z pojedynczą dawką. Metformina nie miała wpływu na farmakokinetykę cymetydyny. Chociaż takie interakcje pozostają teoretyczne (z wyjątkiem cymetydyny), u pacjentów przyjmujących leki kationowe wydalane przez układ wydzielniczy kanalików proksymalnych zaleca się uważne monitorowanie pacjenta i dostosowanie dawki produktu GLUCOVANCE i (lub) leku zakłócającego.
Inny
zdrowych ochotników farmakokinetyka metforminy i propranololu oraz metforminy i ibuprofenu nie ulegała zmianie podczas jednoczesnego podawania w badaniach interakcji po podaniu pojedynczej dawki.
OSTRZEŻENIA
Chlorowodorek metforminy
Kwasica mleczanowa
Kwasica mleczanowa jest rzadkim, ale poważnym powikłaniem metabolicznym, które może wystąpić z powodu kumulacji metforminy podczas leczenia tabletkami GLUCOVANCE (gliburyd i metformina chlorowodorek); kiedy to nastąpi, jest śmiertelne w około 50% przypadków. Kwasica mleczanowa może również wystąpić w połączeniu z szeregiem stanów patofizjologicznych, w tym z cukrzycą, oraz gdy występuje znaczna hipoperfuzja tkanek i hipoksemia. Kwasica mleczanowa charakteryzuje się podwyższonym poziomem mleczanów we krwi (> 5 mmol/L), obniżonym pH krwi, zaburzeniami elektrolitowymi ze zwiększoną luką anionową oraz zwiększonym stosunkiem mleczan/pirogronian. Gdy metformina jest uważana za przyczynę kwasicy mleczanowej, zwykle stwierdza się stężenie metforminy w osoczu > 5 μg/ml.
Zgłaszana częstość występowania kwasicy mleczanowej u pacjentów otrzymujących chlorowodorek metforminy jest bardzo mała (około 0,03 przypadku/1000 pacjento-lat, z około 0,015 przypadkiem śmiertelnym/1000 pacjento-lat). W badaniach klinicznych dotyczących ekspozycji na metforminę przez ponad 20 000 pacjento-lat nie było doniesień o kwasicy mleczanowej. Zgłoszone przypadki występowały głównie u pacjentów z cukrzycą ze znaczną niewydolnością nerek, w tym zarówno z wewnętrzną chorobą nerek, jak i hipoperfuzją nerek, często w sytuacji wielu współistniejących problemów medycznych/chirurgicznych i wielu jednocześnie przyjmowanych leków. Pacjenci z zastoinową niewydolnością serca wymagającą leczenia farmakologicznego, w szczególności ci z niestabilną lub ostrą zastoinową niewydolnością serca, narażeni na ryzyko hipoperfuzji i hipoksemii, są narażeni na zwiększone ryzyko kwasicy mleczanowej. Ryzyko kwasicy mleczanowej wzrasta wraz ze stopniem dysfunkcji nerek i wiekiem pacjenta. W związku z tym ryzyko kwasicy mleczanowej można znacznie zmniejszyć, regularnie monitorując czynność nerek u pacjentów przyjmujących metforminę oraz stosując minimalną skuteczną dawkę metforminy. W szczególności leczeniu osób starszych powinno towarzyszyć uważne monitorowanie czynności nerek. Leczenia preparatem GLUCOVANCE 2,50 mg nie należy rozpoczynać u pacjentów w wieku ≥ 80 lat, chyba że pomiar klirensu kreatyniny wykaże, że czynność nerek nie jest osłabiona, ponieważ pacjenci ci są bardziej podatni na rozwój kwasicy mleczanowej. Ponadto należy niezwłocznie odstawić GLUCOVANCE w przypadku wystąpienia jakiegokolwiek stanu związanego z hipoksemią, odwodnieniem lub sepsą. Ponieważ zaburzenia czynności wątroby mogą znacząco ograniczać zdolność do usuwania mleczanów, należy zasadniczo unikać stosowania produktu GLUCOVANCE u pacjentów z klinicznymi lub laboratoryjnymi objawami choroby wątroby. Należy ostrzec pacjentów przed nadmiernym spożyciem alkoholu, zarówno ostrym, jak i przewlekłym, podczas przyjmowania leku GLUCOVANCE 2,50 mg, ponieważ alkohol nasila działanie chlorowodorku metforminy na metabolizm mleczanów. Ponadto należy tymczasowo odstawić produkt Glucovance w dawce 5 mg przed jakimkolwiek badaniem dotyczącym wewnątrznaczyniowego kontrastu promieniotwórczego oraz przed jakimkolwiek zabiegiem chirurgicznym (patrz również ŚRODKI OSTROŻNOŚCI).
Początek kwasicy mleczanowej jest często nieznaczny i towarzyszą jej jedynie niespecyficzne objawy, takie jak złe samopoczucie, bóle mięśniowe, niewydolność oddechowa, narastająca senność i niespecyficzne dolegliwości brzuszne. Może towarzyszyć hipotermia, niedociśnienie i oporne bradyarytmie z bardziej nasiloną kwasicą. Pacjent i lekarz pacjenta muszą być świadomi możliwego znaczenia takich objawów, a pacjent powinien zostać poinstruowany, aby niezwłocznie powiadomił lekarza, jeśli wystąpią (patrz również ŚRODKI OSTROŻNOŚCI). GLUCOVANCE 500mg należy odstawić do czasu wyjaśnienia sytuacji. Przydatne mogą być elektrolity w surowicy, ketony, poziom glukozy we krwi, a jeśli jest to wskazane, pH krwi, poziom mleczanu, a nawet poziom metforminy we krwi. Gdy stan pacjenta ustabilizuje się na jakimkolwiek poziomie dawki produktu GLUCOVANCE, objawy żołądkowo-jelitowe, które są częste podczas rozpoczynania leczenia metforminą, prawdopodobnie nie mają związku z lekiem. Późniejsze wystąpienie objawów żołądkowo-jelitowych może być spowodowane kwasicą mleczanową lub inną poważną chorobą.
Poziomy mleczanu w osoczu żylnym na czczo powyżej górnej granicy normy, ale poniżej 5 mmol/l u pacjentów przyjmujących preparat GLUCOVANCE niekoniecznie wskazują na zbliżającą się kwasicę mleczanową i mogą być wyjaśnione innymi mechanizmami, takimi jak źle kontrolowana cukrzyca lub otyłość, intensywna aktywność fizyczna, lub problemy techniczne w prostej obsłudze. (Patrz także ŚRODKI OSTROŻNOŚCI.)
Kwasicę mleczanową należy podejrzewać u każdego chorego na cukrzycę z kwasicą metaboliczną bez objawów kwasicy ketonowej (ketonuria i ketonemia).
Kwasica mleczanowa to nagły przypadek medyczny, który należy leczyć w warunkach szpitalnych. U pacjenta z kwasicą mleczanową, który przyjmuje produkt GLUCOVANCE 500 mg, należy natychmiast odstawić lek i niezwłocznie zastosować ogólne leczenie wspomagające. Ponieważ chlorowodorek metforminy podlega dializie (z klirensem do 170 ml/min w dobrych warunkach hemodynamicznych), zaleca się szybką hemodializę w celu skorygowania kwasicy i usunięcia nagromadzonej metforminy. Takie postępowanie często skutkuje szybkim odwróceniem objawów i wyzdrowieniem. (Patrz także PRZECIWWSKAZANIA i ŚRODKI OSTROŻNOŚCI.)
SPECJALNE OSTRZEŻENIE DOTYCZĄCE WZROSTU RYZYKA ŚMIERTELNOŚCI SERCOWO-NACZYNIOWEJ
Istnieją doniesienia, że podawanie doustnych leków hipoglikemizujących wiąże się ze zwiększoną śmiertelnością sercowo-naczyniową w porównaniu z leczeniem samą dietą lub dietą z insuliną. To ostrzeżenie jest oparte na badaniu przeprowadzonym przez University Group Diabetes Program (UGDP), długoterminowe prospektywne badanie kliniczne mające na celu ocenę skuteczności leków hipoglikemizujących w zapobieganiu lub opóźnianiu powikłań naczyniowych u pacjentów z cukrzycą insulinoniezależną. W badaniu wzięło udział 823 pacjentów, których losowo przydzielono do 1 z 4 grup terapeutycznych (Diabetes 19 (Suppl. 2): 747-830, 1970).
UGDP donosi, że u pacjentów leczonych przez 5 do 8 lat dietą plus stałą dawką tolbutamidu (1,5 g dziennie) śmiertelność z przyczyn sercowo-naczyniowych była około 2,5 razy większa niż u pacjentów leczonych samą dietą. Nie zaobserwowano istotnego wzrostu śmiertelności całkowitej, ale zaprzestano stosowania tolbutamidu ze względu na wzrost śmiertelności z przyczyn sercowo-naczyniowych, co ograniczyło możliwość wykazania przez badanie wzrostu śmiertelności ogólnej. Pomimo kontrowersji dotyczących interpretacji tych wyników, wyniki badania UGDP stanowią odpowiednią podstawę dla tego ostrzeżenia. Pacjent powinien zostać poinformowany o potencjalnym ryzyku i korzyściach związanych ze stosowaniem gliburydu oraz o alternatywnych metodach terapii.
Chociaż w tym badaniu uwzględniono tylko 1 lek z klasy sulfonylomoczników (tolbutamid), ze względów bezpieczeństwa rozsądne jest rozważenie, że ostrzeżenie to może dotyczyć również innych leków hipoglikemizujących z tej klasy, ze względu na ich bliskie podobieństwo w sposobie działania i struktura chemiczna.
ŚRODKI OSTROŻNOŚCI
Ogólny
Wyniki makronaczyniowe
Nie przeprowadzono badań klinicznych, które wykazałyby jednoznaczne dowody na zmniejszenie ryzyka makronaczyniowego podczas stosowania produktu GLUCOVANCE 5 mg lub jakiegokolwiek innego leku przeciwcukrzycowego.
GLUKOWANCJA
Hipoglikemia
GLUCOVANCE 400 mg może wywoływać hipoglikemię lub objawy hipoglikemii, dlatego odpowiedni dobór pacjenta, dawkowanie i instrukcje są ważne, aby uniknąć potencjalnych epizodów hipoglikemii. Ryzyko hipoglikemii jest zwiększone, gdy spożycie kalorii jest niewystarczające, gdy intensywny wysiłek nie jest kompensowany suplementacją kalorii lub podczas jednoczesnego stosowania innych leków hipoglikemizujących lub etanolu. Niewydolność nerek lub wątroby może powodować podwyższony poziom zarówno gliburydu, jak i chlorowodorku metforminy, a niewydolność wątroby może również zmniejszać zdolność glukoneogenną, co zwiększa ryzyko reakcji hipoglikemicznych. Na wystąpienie hipoglikemii szczególnie podatni są pacjenci w podeszłym wieku, osłabieni, niedożywieni, z niewydolnością nadnerczy, przysadki lub zatrucia alkoholem. Hipoglikemia może być trudna do rozpoznania u osób starszych i osób przyjmujących leki blokujące receptory beta-adrenergiczne.
Glyburyd
Niedokrwistość hemolityczna
Leczenie pacjentów z niedoborem dehydrogenazy glukozo-6-fosforanowej (G6PD) środkami pochodnymi sulfonylomocznika może prowadzić do niedokrwistości hemolitycznej. Ponieważ GLUCOVANCE 400 mg należy do klasy pochodnych sulfonylomocznika, należy zachować ostrożność u pacjentów z niedoborem G6PD i rozważyć alternatywę bez sulfonylomocznika. W raportach po wprowadzeniu produktu do obrotu zgłaszano również niedokrwistość hemolityczną u pacjentów bez rozpoznanego niedoboru G6PD.
Chlorowodorek metforminy
Monitorowanie czynności nerek
Wiadomo, że metformina jest w znacznym stopniu wydalana przez nerki, a ryzyko kumulacji metforminy i kwasicy mleczanowej wzrasta wraz ze stopniem upośledzenia czynności nerek. Dlatego pacjenci ze stężeniem kreatyniny w surowicy powyżej górnej granicy normy dla ich wieku nie powinni otrzymywać produktu GLUCOVANCE. U pacjentów w podeszłym wieku należy ostrożnie zwiększać dawkę GLUCOVANCE 400 mg w celu ustalenia minimalnej dawki zapewniającej odpowiedni efekt glikemiczny, ponieważ starzenie się wiąże się z upośledzeniem czynności nerek. U pacjentów w podeszłym wieku, zwłaszcza w wieku ≥ 80 lat, należy regularnie monitorować czynność nerek i na ogół nie należy zwiększać dawki produktu GLUCOVANCE 2,50 mg do maksymalnej dawki (patrz OSTRZEŻENIA oraz DAWKOWANIE I SPOSÓB PODAWANIA ). Przed rozpoczęciem leczenia preparatem GLUCOVANCE 2,50 mg, a następnie co najmniej raz w roku, należy ocenić i zweryfikować czynność nerek jako prawidłową. U pacjentów, u których przewiduje się rozwój zaburzeń czynności nerek, czynność nerek należy oceniać częściej i odstawić preparat Glucovance, jeśli występują objawy niewydolności nerek.
Stosowanie jednocześnie leków, które mogą wpływać na czynność nerek lub dyspozycję metforminy
Jednoczesne leki, które mogą wpływać na czynność nerek lub powodować znaczne zmiany hemodynamiczne lub mogą wpływać na rozmieszczenie metforminy, takie jak leki kationowe, które są eliminowane przez wydzielanie kanalików nerkowych (patrz INTERAKCJE Z LEKAMI ), należy stosować ostrożnie.
Badania radiologiczne z użyciem donaczyniowych jodowanych materiałów kontrastowych (na przykład urogram dożylny, dożylna cholangiografia, angiografia i skany tomografii komputerowej (CT) z wewnątrznaczyniowymi materiałami kontrastowymi)
Badania kontrastu wewnątrznaczyniowego z materiałami jodowanymi mogą prowadzić do ostrych zmian czynności nerek i były związane z kwasicą mleczanową u pacjentów otrzymujących metforminę (patrz PRZECIWWSKAZANIA ). Dlatego u pacjentów, u których planowane jest takie badanie, należy czasowo odstawić produkt GLUCOVANCE 400 mg w czasie lub przed zabiegiem oraz wstrzymać się na 48 godzin po zabiegu i wznowić dopiero po ponownej ocenie czynności nerek i stwierdzeniu, że normalna.
Stany niedotlenienia
Zapaść sercowo-naczyniowa (wstrząs) z jakiejkolwiek przyczyny, ostra zastoinowa niewydolność serca, ostry zawał mięśnia sercowego i inne stany charakteryzujące się hipoksemią są związane z kwasicą mleczanową i mogą również powodować azotemię przednerkową. Jeśli takie zdarzenia wystąpią u pacjentów leczonych preparatem GLUCOVANCE 2,50 mg, lek należy natychmiast odstawić.
Zabiegi chirurgiczne
Leczenie preparatem GLUCOVANCE 400 mg należy tymczasowo zawiesić na wypadek jakichkolwiek zabiegów chirurgicznych (z wyjątkiem drobnych zabiegów niezwiązanych z ograniczeniem przyjmowania pokarmów i płynów) i nie należy wznawiać go do czasu wznowienia przyjmowania doustnego przez pacjenta i oceny czynności nerek jako normy.
Spożycie alkoholu
Wiadomo, że alkohol nasila działanie metforminy na metabolizm mleczanów. W związku z tym pacjentów należy ostrzec przed nadmiernym spożyciem alkoholu, ostrym lub przewlekłym, podczas przyjmowania preparatu GLUCOVANCE. Alkohol ze względu na wpływ na zdolność glukoneogenną wątroby może również zwiększać ryzyko hipoglikemii.
Upośledzona funkcja wątroby
Ponieważ zaburzenia czynności wątroby są związane z niektórymi przypadkami kwasicy mleczanowej, należy zasadniczo unikać stosowania produktu GLUCOVANCE 500 mg u pacjentów z klinicznymi lub laboratoryjnymi objawami choroby wątroby.
Poziomy witaminy B12
kontrolowanych badaniach klinicznych z metforminą trwających 29 tygodni, u około 7% pacjentów zaobserwowano obniżenie poziomu witaminy B12 w surowicy do poziomu poniżej normy, bez objawów klinicznych. Taki spadek, prawdopodobnie z powodu interferencji z wchłanianiem witaminy B12 z kompleksu czynnika wewnętrznego B12, jest jednak bardzo rzadko związany z anemią i wydaje się być szybko odwracalny po zaprzestaniu suplementacji metforminą lub witaminą B. Zaleca się coroczny pomiar parametrów hematologicznych u pacjentów leczonych metforminą, a wszelkie widoczne nieprawidłowości należy odpowiednio zbadać i leczyć (patrz ŚRODKI OSTROŻNOŚCI : Testy laboratoryjne ).
Niektóre osoby (osoby z niewystarczającym spożyciem lub wchłanianiem witaminy B12 lub wapnia) wydają się być predysponowane do rozwoju nieprawidłowego poziomu witaminy B12. U tych pacjentów przydatne mogą być rutynowe pomiary poziomu witaminy B12 w surowicy w odstępach 2–3 lat.
Zmiana stanu klinicznego pacjentów z wcześniej kontrolowaną cukrzycą typu 2
Pacjent z cukrzycą typu 2 wcześniej dobrze kontrolowaną metforminą, u którego wystąpią nieprawidłowe wyniki badań laboratoryjnych lub choroba kliniczna (zwłaszcza choroba niejasna i słabo zdefiniowana), należy niezwłocznie zbadać pod kątem objawów kwasicy ketonowej lub kwasicy mleczanowej. Ocena powinna obejmować elektrolity i ketony w surowicy, poziom glukozy we krwi oraz, jeśli jest to wskazane, pH krwi, poziom mleczanów, pirogronianu i metforminy. W przypadku wystąpienia kwasicy którejkolwiek postaci należy natychmiast przerwać stosowanie produktu GLUCOVANCE i podjąć inne odpowiednie działania naprawcze (patrz także: OSTRZEŻENIA ).
Dodanie tiazolidynodionów do terapii GLUCOVANCE 500 mg
Hipoglikemia
Pacjenci otrzymujący preparat GLUCOVANCE 2,50 mg w skojarzeniu z tiazolidynodionem mogą być narażeni na ryzyko hipoglikemii.
Przybranie na wadze
Po dodaniu rozyglitazonu do 5 mg preparatu GLUCOVANCE obserwowano przyrost masy ciała, podobny do odnotowanego w przypadku leczenia samym tiazolidynodionem.
Wpływ na wątrobę
Gdy tiazolidynodion jest stosowany w skojarzeniu z preparatem GLUCOVANCE 2,50 mg, należy okresowo monitorować testy czynności wątroby zgodnie z zaleceniami dotyczącymi tiazolidynodionu.
Informacje dla pacjentów
GLUKOWANCJA
Pacjentów należy poinformować o potencjalnym ryzyku i korzyściach związanych ze stosowaniem preparatu GLUCOVANCE 500 mg i alternatywnych metod leczenia. Powinni być również poinformowani o znaczeniu przestrzegania zaleceń dietetycznych; regularny program ćwiczeń; oraz regularne badanie poziomu glukozy we krwi, hemoglobiny glikozylowanej, funkcji nerek i parametrów hematologicznych.
Należy wyjaśnić pacjentom ryzyko kwasicy mleczanowej związane z leczeniem metforminą, jej objawy oraz stany predysponujące do jej rozwoju, jak wskazano w rozdziałach OSTRZEŻENIA i ŚRODKI OSTROŻNOŚCI. Pacjentom należy zalecić natychmiastowe przerwanie stosowania produktu GLUCOVANCE i niezwłoczne powiadomienie swojego lekarza w przypadku wystąpienia niewyjaśnionej hiperwentylacji, bólu mięśni, złego samopoczucia, nietypowej senności lub innych niespecyficznych objawów. Po ustabilizowaniu się stanu pacjenta na jakimkolwiek poziomie dawki produktu GLUCOVANCE, objawy żołądkowo-jelitowe, które są częste podczas rozpoczynania leczenia metforminą, prawdopodobnie nie mają związku z lekiem. Późniejsze wystąpienie objawów żołądkowo-jelitowych może być spowodowane kwasicą mleczanową lub inną poważną chorobą.
Należy wyjaśnić chorym i odpowiedzialnym członkom rodziny ryzyko hipoglikemii, jej objawy i leczenie oraz stany predysponujące do jej rozwoju.
Pacjentom należy odradzać nadmierne spożycie alkoholu, zarówno ostre, jak i przewlekłe, podczas przyjmowania preparatu GLUCOVANCE. (Widzieć INFORMACJE DLA PACJENTA wydrukowane poniżej.)
Testy laboratoryjne
W celu monitorowania odpowiedzi terapeutycznej należy wykonywać okresowe pomiary stężenia glukozy we krwi na czczo (FBG) i HbA1c.
Przynajmniej raz w roku należy przeprowadzać wstępne i okresowe monitorowanie parametrów hematologicznych (np. hemoglobiny/hematokrytu i wskaźników krwinek czerwonych) oraz czynności nerek (kreatynina w surowicy). Chociaż niedokrwistość megaloblastyczna jest rzadko obserwowana podczas leczenia metforminą, jeśli istnieje podejrzenie, należy wykluczyć niedobór witaminy B12.
rakotwórczość, mutageneza, upośledzenie płodności
Nie przeprowadzono badań na zwierzętach z połączonymi produktami w GLUCOVANCE. Poniższe dane są oparte na wynikach badań przeprowadzonych z poszczególnymi produktami.
Glyburyd
Badania na szczurach, którym podawano sam gliburyd w dawkach do 300 mg/kg/dobę (około 145-krotność maksymalnej zalecanej dawki dobowej u ludzi [MRHD] wynoszącej 20 mg dla składnika gliburydowego GLUCOVANCE 5 mg na podstawie porównania powierzchni ciała) przez 18 miesięcy wykazały brak efektów rakotwórczych. W 2-letnim badaniu onkogenności gliburydu u myszy nie było dowodów na występowanie guzów związanych z leczeniem.
Nie było dowodów na mutagenny potencjał samego gliburydu w następujących testach in vitro: test mikrosomowy Salmonella (test Amesa) oraz w teście uszkodzenia DNA / elucji zasadowej.
Chlorowodorek metforminy
Przeprowadzono długoterminowe badania rakotwórczości samej metforminy u szczurów (czas trwania dawki 104 tygodnie) i myszy (czas trwania dawki 91 tygodni) w dawkach odpowiednio do 900 mg/kg/dobę i 1500 mg/kg/dobę włącznie. Obie dawki są w przybliżeniu 4 razy większe od dawki MRHD wynoszącej 2000 mg składnika metforminy produktu GLUCOVANCE 400 mg na podstawie porównań powierzchni ciała. Nie stwierdzono rakotwórczości samej metforminy u samców ani u samic myszy. Podobnie, nie zaobserwowano potencjału rakotwórczego dla samej metforminy u samców szczurów. Zaobserwowano jednak zwiększoną częstość występowania łagodnych polipów zrębu macicy u samic szczurów leczonych samą metforminą w dawce 900 mg/kg/dobę.
Nie było dowodów na mutagenny potencjał samej metforminy w następujących testach in vitro: test Amesa (S. typhimurium), test mutacji genowych (komórki chłoniaka myszy) lub test aberracji chromosomowych (limfocyty ludzkie). Wyniki w teście mikrojądrowym in vivo u myszy były również negatywne.
Sama metformina podawana w dawkach do 600 mg/kg/dobę nie miała wpływu na płodność samców i samic szczurów, co stanowi około 3-krotność dawki MRHD składnika metforminy produktu GLUCOVANCE 400 mg na podstawie porównania powierzchni ciała.
Ciąża
Efekty teratogenne
Ciąża Kategoria B
Najnowsze informacje zdecydowanie sugerują, że nieprawidłowe poziomy glukozy we krwi w czasie ciąży są związane z większą częstością występowania wad wrodzonych. Większość ekspertów zaleca stosowanie insuliny w czasie ciąży, aby utrzymać poziom glukozy we krwi jak najbliżej normy. Ponieważ badania reprodukcji na zwierzętach nie zawsze pozwalają przewidzieć odpowiedź człowieka, GLUCOVANCE 400 mg nie należy stosować w okresie ciąży, chyba że jest to bezwzględnie konieczne. (Patrz poniżej.)

Nie ma odpowiednich i dobrze kontrolowanych badań GLUCOVANCE lub jego poszczególnych składników u kobiet w ciąży. Nie przeprowadzono badań na zwierzętach z połączonymi produktami w GLUCOVANCE. Poniższe dane są oparte na wynikach badań przeprowadzonych z poszczególnymi produktami.
Glyburyd
Badania rozrodczości przeprowadzono na szczurach i królikach przy dawkach do 500 razy większych od dawki MRHD 20 mg składnika gliburydowego produktu GLUCOVANCE 500 mg na podstawie porównania powierzchni ciała i nie wykazały dowodów na upośledzenie płodności lub uszkodzenie płodu spowodowane przez gliburyd.
Chlorowodorek metforminy
Sama metformina nie wykazywała działania teratogennego u szczurów i królików w dawkach do 600 mg/kg/dobę. Odpowiada to ekspozycji około 2 i 6 razy większej od dawki MRHD wynoszącej 2000 mg metforminy składnika preparatu GLUCOVANCE 500 mg na podstawie porównania powierzchni ciała odpowiednio dla szczurów i królików. Oznaczenie stężeń płodowych wykazało częściową barierę łożyskową dla metforminy.
Efekty nieteratogenne
noworodków urodzonych przez matki, które w momencie porodu otrzymywały pochodną sulfonylomocznika, opisywano przedłużającą się ciężką hipoglikemię (4-10 dni). Odnotowano to częściej przy stosowaniu środków o przedłużonym okresie półtrwania. Nie zaleca się stosowania preparatu GLUCOVANCE 400 mg w okresie ciąży. Jeśli jednak jest stosowany, GLUCOVANCE należy odstawić co najmniej 2 tygodnie przed przewidywaną datą porodu. (Widzieć Ciąża : Efekty teratogenne : Ciąża Kategoria B .)
Matki karmiące
Chociaż nie wiadomo, czy gliburyd przenika do mleka ludzkiego, wiadomo, że niektóre leki pochodne sulfonylomocznika przenikają do mleka ludzkiego. Badania na karmiących szczurach wykazały, że metformina przenika do mleka i osiąga poziom porównywalny do stężenia w osoczu. Podobnych badań nie przeprowadzono u matek karmiących. Ze względu na możliwość wystąpienia hipoglikemii u niemowląt karmionych piersią, należy podjąć decyzję, czy przerwać karmienie piersią, czy przerwać stosowanie preparatu GLUCOVANCE, biorąc pod uwagę znaczenie leku dla matki. Jeśli preparat Glucovance zostanie odstawiony, a sama dieta nie wystarcza do kontrolowania stężenia glukozy we krwi, należy rozważyć insulinoterapię.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność produktu GLUCOVANCE 500 mg zostały ocenione w 26-tygodniowym randomizowanym badaniu kontrolowanym metodą podwójnie ślepej próby z udziałem łącznie 167 pacjentów pediatrycznych (w wieku od 9 do 16 lat) z cukrzycą typu 2. Nie wykazano statystycznie, że produkt GLUCOVANCE 500 mg jest lepszy niż metformina lub gliburyd pod względem zmniejszania HbA1c w stosunku do wartości wyjściowych (patrz Tabela 5). W tym badaniu nie wiązały się żadne nieoczekiwane ustalenia dotyczące bezpieczeństwa stosowania preparatu GLUCOVANCE 2,50 mg.
Zastosowanie geriatryczne
Spośród 642 pacjentów, którzy otrzymywali GLUCOVANCE w badaniach klinicznych z podwójnie ślepą próbą, 23,8% miało 65 lat i więcej, a 2,8% miało 75 lat i więcej. Spośród 1302 pacjentów, którzy otrzymywali GLUCOVANCE 500 mg w otwartych badaniach klinicznych, 20,7% miało 65 lat i więcej, a 2,5% 75 lat i więcej. Nie zaobserwowano ogólnych różnic w skuteczności lub bezpieczeństwie między tymi pacjentami a młodszymi pacjentami, a inne zgłaszane doświadczenia kliniczne nie wykazały różnic w odpowiedzi między pacjentami w podeszłym wieku i młodszymi, ale nie można wykluczyć większej wrażliwości niektórych osób starszych.
Wiadomo, że chlorowodorek metforminy jest w znacznym stopniu wydalany przez nerki, a ponieważ ryzyko ciężkich działań niepożądanych leku jest większe u pacjentów z zaburzeniami czynności nerek, produkt GLUCOVANCE 500 mg należy stosować wyłącznie u pacjentów z prawidłową czynnością nerek (patrz PRZECIWWSKAZANIA , OSTRZEŻENIA , oraz FARMAKOLOGIA KLINICZNA : Farmakokinetyka ). Ponieważ starzenie się wiąże się z upośledzeniem czynności nerek, GLUCOVANCE 5 mg należy stosować ostrożnie wraz z wiekiem. Należy zachować ostrożność przy doborze dawki i opierać się na dokładnym i regularnym monitorowaniu czynności nerek. Zasadniczo u pacjentów w podeszłym wieku nie należy zwiększać dawki do maksymalnej dawki produktu GLUCOVANCE (patrz także: OSTRZEŻENIA oraz DAWKOWANIE I SPOSÓB PODAWANIA ).
PRZEDAWKOWAĆ
Glyburyd
Przedawkowanie pochodnych sulfonylomocznika, w tym tabletek gliburydu, może wywołać hipoglikemię. Łagodne objawy hipoglikemii, bez utraty przytomności lub objawów neurologicznych, należy leczyć agresywnie, podając doustnie glukozę i dostosowując dawkowanie leku i (lub) schemat posiłków. Należy kontynuować ścisłe monitorowanie, dopóki lekarz nie upewni się, że pacjentowi nie grozi żadne niebezpieczeństwo. Ciężkie reakcje hipoglikemiczne ze śpiączką, drgawkami lub innymi zaburzeniami neurologicznymi występują rzadko, ale stanowią nagłe przypadki wymagające natychmiastowej hospitalizacji. W przypadku rozpoznania lub podejrzenia śpiączki hipoglikemicznej pacjentowi należy podać szybko dożylnie stężony (50%) roztwór glukozy. Następnie należy wykonać ciągły wlew bardziej rozcieńczonego (10%) roztworu glukozy z szybkością, która utrzyma stężenie glukozy we krwi na poziomie powyżej 100 mg/dl. Pacjentów należy ściśle monitorować przez co najmniej 24 do 48 godzin, ponieważ hipoglikemia może nawrócić po widocznym wyzdrowieniu klinicznym.
Chlorowodorek metforminy
Nastąpiło przedawkowanie chlorowodorku metforminy, w tym połknięcie ilości > 50 g. Hipoglikemię zgłaszano w około 10% przypadków, ale nie ustalono związku przyczynowego z chlorowodorkiem metforminy. Kwasicę mleczanową zgłaszano w około 32% przypadków przedawkowania metforminy (patrz OSTRZEŻENIA ). Metformina może być dializowana z klirensem do 170 ml/min w dobrych warunkach hemodynamicznych. Dlatego hemodializa może być przydatna do usuwania nagromadzonego leku u pacjentów, u których podejrzewa się przedawkowanie metforminy.
PRZECIWWSKAZANIA
GLUCOVANCE 2,50 mg jest przeciwwskazany u pacjentów z:
Preparat Glucovance 500 mg należy czasowo odstawić u pacjentów poddawanych badaniom radiologicznym obejmującym donaczyniowe podawanie jodowych środków kontrastowych, ponieważ stosowanie takich produktów może spowodować ostrą zmianę czynności nerek. (Zobacz też ŚRODKI OSTROŻNOŚCI .)
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
GLUCOVANCE łączy gliburyd i chlorowodorek metforminy, 2 środki przeciwhiperglikemiczne o uzupełniających się mechanizmach działania, w celu poprawy kontroli glikemii u pacjentów z cukrzycą typu 2.
Wydaje się, że gliburyd gwałtownie obniża poziom glukozy we krwi poprzez stymulację uwalniania insuliny z trzustki, efekt zależny od funkcjonowania komórek beta w wyspach trzustkowych. Mechanizm, za pomocą którego gliburyd obniża stężenie glukozy we krwi podczas długotrwałego podawania, nie został jasno określony. Przy długotrwałym podawaniu pacjentom z cukrzycą typu 2 efekt obniżania stężenia glukozy we krwi utrzymuje się pomimo stopniowego zmniejszania się odpowiedzi sekrecyjnej insuliny na lek. Działanie pozatrzustkowe może być zaangażowane w mechanizm działania doustnych leków hipoglikemizujących zawierających pochodne sulfonylomocznika.
Chlorowodorek metforminy jest środkiem przeciwhiperglikemicznym, który poprawia tolerancję glukozy u pacjentów z cukrzycą typu 2, obniżając zarówno podstawowy, jak i poposiłkowy poziom glukozy w osoczu. Chlorowodorek metforminy zmniejsza wytwarzanie glukozy w wątrobie, zmniejsza wchłanianie glukozy w jelitach i poprawia wrażliwość na insulinę poprzez zwiększenie obwodowego wychwytu i wykorzystania glukozy.
Farmakokinetyka
Wchłanianie i biodostępność
GLUKOWANCJA
badaniach biodostępności GLUCOVANCE 2,5 mg/500 mg i 5 mg/500 mg średnie pole pod krzywą stężenia w osoczu w funkcji czasu (AUC) dla składnika gliburydowego było odpowiednio o 18% i 7% większe niż w przypadku Micronase® marka gliburydu podawanego razem z metforminą. Dlatego gliburydowy składnik preparatu GLUCOVANCE nie jest biorównoważny z Micronase®. Składnik metforminy produktu GLUCOVANCE 400 mg jest biorównoważny z metforminą połączoną z gliburydem.
Po podaniu pojedynczej tabletki GLUCOVANCE 5 mg/500 mg z 20% roztworem glukozy lub 20% roztworem glukozy z posiłkiem nie stwierdzono wpływu posiłku na Cmax i stosunkowo niewielki wpływ posiłku na AUC gliburydu składnik. Tmax dla składnika gliburydowego został skrócony z 7,5 godziny do 2,75 godziny z jedzeniem w porównaniu do tabletki o tej samej mocy podawanej na czczo z 20% roztworem glukozy. Kliniczne znaczenie wcześniejszego Tmax dla gliburydu po jedzeniu nie jest znane. Wpływ pokarmu na farmakokinetykę składnika metforminy był nieokreślony.
Glyburyd
Badania z pojedynczą dawką tabletek Micronase® u zdrowych osobników wykazały znaczące wchłanianie gliburydu w ciągu 1 godziny, szczytowe poziomy leku po około 4 godzinach i niskie, ale wykrywalne poziomy po 24 godzinach. Średnie stężenia gliburydu w surowicy, odzwierciedlone przez pola pod krzywą stężenia w surowicy w czasie, wzrastają proporcjonalnie do odpowiedniego wzrostu dawki. Nie ustalono biorównoważności pomiędzy preparatami GLUCOVANCE 500 mg i jednoskładnikowymi produktami gliburydowymi.
Chlorowodorek metforminy
Całkowita biodostępność tabletki chlorowodorku metforminy 500 mg podawanej na czczo wynosi około 50% do 60%. Badania z zastosowaniem pojedynczych dawek doustnych metforminy w tabletkach 500 mg i 1500 mg oraz 850 mg do 2550 mg wskazują, że nie ma proporcjonalności do dawki przy zwiększaniu dawek, co wynika raczej ze zmniejszonego wchłaniania niż ze zmian w wydalaniu. Pokarm zmniejsza zasięg i nieznacznie opóźnia wchłanianie metforminy, na co wskazuje około 40% mniejsze maksymalne stężenie i 25% mniejsze AUC w osoczu oraz 35-minutowe wydłużenie czasu do osiągnięcia maksymalnego stężenia w osoczu po podaniu pojedynczej dawki 850 mg tabletki metforminy z jedzeniem, w porównaniu z tabletkami o tej samej mocy podawanymi na czczo. Kliniczne znaczenie tych spadków jest nieznane.
Dystrybucja
Glyburyd
Leki sulfonylomocznikowe silnie wiążą się z białkami surowicy. Wypieranie z miejsc wiązania białek przez inne leki może prowadzić do nasilenia działania hipoglikemicznego. In vitro wiązanie białka wykazywane przez gliburyd jest głównie niejonowe, podczas gdy inne sulfonylomoczniki (chlorpropamid, tolbutamid, tolazamid) są głównie jonowe. Leki kwasowe, takie jak fenylobutazon, warfaryna i salicylany, wypierają wiążące jony sulfonylomoczniki z białek surowicy w znacznie większym stopniu niż niejonowy gliburyd. Nie wykazano, że ta różnica w wiązaniu białek skutkuje mniejszą liczbą interakcji lek-lek z tabletkami gliburydu w zastosowaniu klinicznym.
Chlorowodorek metforminy
Pozorna objętość dystrybucji (V/F) metforminy po podaniu pojedynczej dawki doustnej 850 mg wynosiła średnio 654±358 l. Metformina w nieznacznym stopniu wiąże się z białkami osocza. Metformina dzieli się na erytrocyty, najprawdopodobniej w funkcji czasu. Przy zwykłych dawkach klinicznych i schematach dawkowania metforminy stężenie metforminy w stanie stacjonarnym osiągane jest w ciągu 24 do 48 godzin i wynosi na ogół
Metabolizm i eliminacja
Glyburyd
Spadek gliburydu w surowicy zdrowych osób jest dwufazowy; końcowy okres półtrwania wynosi około 10 godzin. Głównym metabolitem gliburydu jest pochodna 4-trans-hydroksylowa. Występuje również drugi metabolit, pochodna 3-cis-hydroksy. Te metabolity prawdopodobnie nie wywierają znaczącego działania hipoglikemizującego u ludzi, ponieważ są tylko słabo aktywne (odpowiednio 1/400 i 1/40 jako gliburyd) u królików. Glyburyd jest wydalany w postaci metabolitów z żółcią i moczem, około 50% każdą drogą. Ta podwójna droga wydalnicza różni się jakościowo od innych pochodnych sulfonylomocznika, które są wydalane głównie z moczem.
Chlorowodorek metforminy
Badania z podaniem dożylnym pojedynczej dawki u zdrowych osób wykazały, że metformina jest wydalana w postaci niezmienionej z moczem i nie podlega metabolizmowi wątrobowemu (nie zidentyfikowano metabolitów u ludzi) ani wydalaniu z żółcią. Klirens nerkowy (patrz Tabela 1) jest około 3,5 razy większy niż klirens kreatyniny, co wskazuje, że wydzielanie kanalikowe jest główną drogą eliminacji metforminy. Po podaniu doustnym około 90% wchłoniętego leku jest wydalane przez nerki w ciągu pierwszych 24 godzin, a okres półtrwania w osoczu wynosi około 6,2 godziny. We krwi okres półtrwania w fazie eliminacji wynosi około 17,6 godzin, co sugeruje, że masa erytrocytów może być kompartmentem dystrybucji.
Specjalne populacje
Pacjenci z cukrzycą typu 2
Badania z wielokrotnymi dawkami gliburydu u pacjentów z cukrzycą typu 2 pokazują krzywe stężenie leku w funkcji czasu podobne do badań z pojedynczą dawką, co wskazuje na brak gromadzenia się leku w depotach w tkankach.
przypadku prawidłowej czynności nerek nie ma różnic w farmakokinetyce pojedynczej lub wielokrotnej dawki metforminy między pacjentami z cukrzycą typu 2 a osobami zdrowymi (patrz Tabela 1), nie ma też kumulacji metforminy w żadnej z grup w normalnych warunkach klinicznych. dawki.
Niewydolność wątroby
Nie przeprowadzono badań farmakokinetycznych gliburydu lub metforminy u pacjentów z niewydolnością wątroby.
Niewydolność nerek
Brak dostępnych informacji na temat farmakokinetyki gliburydu u pacjentów z niewydolnością nerek.
U pacjentów z obniżoną czynnością nerek (na podstawie klirensu kreatyniny) okres półtrwania metforminy w osoczu i krwi jest wydłużony, a klirens nerkowy jest zmniejszony proporcjonalnie do zmniejszenia klirensu kreatyniny (patrz Tabela 1; patrz także OSTRZEŻENIA ).
Geriatria
Brak informacji na temat farmakokinetyki gliburydu u pacjentów w podeszłym wieku.
Ograniczone dane z kontrolowanych badań farmakokinetycznych metforminy u zdrowych osób w podeszłym wieku sugerują, że całkowity klirens osoczowy jest zmniejszony, okres półtrwania wydłużony, a Cmax zwiększone w porównaniu ze zdrowymi młodymi osobami. Na podstawie tych danych wydaje się, że zmiana farmakokinetyki metforminy wraz ze starzeniem się wynika głównie ze zmiany czynności nerek (patrz Tabela 1). Nie należy rozpoczynać leczenia metforminą u pacjentów w wieku ≥ 80 lat, chyba że pomiar klirensu kreatyniny wykaże, że czynność nerek nie jest zmniejszona.
Pediatria
Po podaniu pojedynczej doustnej tabletki GLUCOPHAGE® (chlorowodorek metforminy) 500 mg z jedzeniem, średnia geometryczna Cmax i AUC metforminy różniła się
Po podaniu pojedynczej doustnej tabletki GLUCOVANCE z jedzeniem, znormalizowana względem dawki średnia geometryczna Cmax i AUC gliburydu u dzieci z cukrzycą typu 2 (11-16 lat, n=28, średnia masa ciała 97 kg) różniła się
Płeć
Brak informacji na temat wpływu płci na farmakokinetykę gliburydu.
Parametry farmakokinetyczne metforminy nie różniły się istotnie u pacjentów z cukrzycą typu 2 lub bez cukrzycy, analizowane według płci (mężczyźni=19, kobiety=16). Podobnie w kontrolowanych badaniach klinicznych u pacjentów z cukrzycą typu 2 działanie przeciwhiperglikemiczne metforminy było porównywalne u mężczyzn i kobiet.
Wyścig
Brak dostępnych informacji na temat różnic rasowych w farmakokinetyce gliburydu.
Nie przeprowadzono badań parametrów farmakokinetycznych metforminy w zależności od rasy. W kontrolowanych badaniach klinicznych metforminy u pacjentów z cukrzycą typu 2 działanie przeciwhiperglikemiczne było porównywalne u osób rasy białej (n=249), czarnej (n=51) i Latynosów (n=24).
Studia kliniczne
Pacjenci z niewystarczającą kontrolą glikemii przy samej diecie i ćwiczeniach
W 20-tygodniowym, podwójnie zaślepionym, wieloośrodkowym badaniu klinicznym w USA, w sumie 806 nieleczonych wcześniej pacjentów z cukrzycą typu 2, u których hiperglikemia nie była odpowiednio kontrolowana samą dietą i ćwiczeniami (wyjściowa glikemia na czczo [FPG]
Leczenie preparatem GLUCOVANCE skutkowało istotnie większą redukcją HbA i poposiłkowego stężenia glukozy (PPG) w porównaniu z gliburydem, metforminą lub placebo. Ponadto terapia GLUCOVANCE spowodowała większe zmniejszenie FPG w porównaniu z gliburydem, metforminą lub placebo, ale różnice między gliburydem i metforminą nie osiągnęły istotności statystycznej.
Zmiany profilu lipidowego związane z leczeniem GLUCOVANCE 2,50 mg były podobne do zmian obserwowanych w przypadku gliburydu, metforminy i placebo.
Opisane powyżej badanie z podwójnie ślepą próbą kontrolowane placebo ograniczyło rekrutację do pacjentów z HbA1c
Pacjenci z niewystarczającą kontrolą glikemii stosujący sam sulfonylomocznik
16-tygodniowym, podwójnie zaślepionym, aktywnie kontrolowanym badaniu klinicznym w USA, w sumie 639 pacjentów z niewystarczająco kontrolowaną cukrzycą typu 2 (średnia początkowa wartość HbA1c 9,5%, średnia początkowa wartość FPG 213 mg/dl) podczas leczenia co najmniej połowa maksymalnej dawki sulfonylomocznika (np. 10 mg gliburydu, 20 mg glipizydu) została losowo przydzielona do grupy otrzymującej gliburyd (stała dawka 20 mg), metforminę (500 mg), GLUCOVANCE 2,5 mg/500 mg lub GLUCOVANCE 5 mg /500 mg. Dawki metforminy i GLUCOVANCE zwiększono do maksymalnie 4 tabletek na dobę, zgodnie z potrzebami, aby osiągnąć FPG
Po 16 tygodniach nie było istotnej zmiany średniej HbA u pacjentów przydzielonych losowo do terapii gliburydem lub metforminą. Leczenie preparatem GLUCOVANCE 2,50 mg w dawkach do 20 mg/2000 mg na dobę spowodowało istotne obniżenie HbA, FPG i PPG od wartości wyjściowych w porównaniu z samym gliburydem lub metforminą.
Dodanie tiazolidynodionów do terapii GLUCOVANCE 400 mg
24-tygodniowym, podwójnie zaślepionym, wieloośrodkowym badaniu klinicznym w USA pacjenci z cukrzycą typu 2 niewystarczająco kontrolowaną za pomocą aktualnie stosowanego doustnego leczenia hipoglikemizującego (w monoterapii lub terapii skojarzonej) byli najpierw przestawiani na otwarty produkt GLUCOVANCE tabletki 2,5 mg/500 mg, a następnie miareczkowani. do maksymalnej dawki dobowej 10 mg/2000 mg. Łącznie 365 pacjentów z niewystarczająco wyrównaną kontrolą (HbA1c > 7,0% i ≤ 10%) po 10 do 12 tygodniach stosowania dobowej dawki 500 mg GLUCOVANCE co najmniej 7,5 mg/1500 mg zostało losowo przydzielonych do grupy otrzymującej terapię uzupełniającą rozyglitazonem w dawce 4 mg lub placebo raz na dobę. . Po 8 tygodniach dawkę rozyglitazonu zwiększono do maksymalnie 8 mg na dobę w razie potrzeby, aby osiągnąć docelową średnią dobową dawkę glukozy 126 mg/dl lub HbA1c
U pacjentów, którzy nie osiągnęli odpowiedniej kontroli glikemii po podaniu GLUCOVANCE 400 mg, dodanie rozyglitazonu w porównaniu z placebo spowodowało istotne obniżenie HbA i FPG.
INFORMACJA O PACJENCIE
GLUCOVANCE® (gliburyd i metformina HCl) Tabletki
OSTRZEŻENIE: U niewielkiej liczby osób, które przyjmowały chlorowodorek metforminy, rozwinął się poważny stan zwany kwasicą mleczanową. Prawidłowo funkcjonujące nerki są potrzebne, aby zapobiegać kwasicy mleczanowej. Większość osób z zaburzeniami czynności nerek nie powinna przyjmować preparatu GLUCOVANCE. (Patrz pytania nr 9-13.)
Q1. Dlaczego muszę zażywać GLUCOVANCE 5mg?
Lekarz przepisał GLUCOVANCE 500 mg w celu leczenia cukrzycy typu 2. Jest to również znane jako cukrzyca insulinoniezależna.
Q2. Co to jest cukrzyca typu 2?
Osoby z cukrzycą nie są w stanie wytwarzać wystarczającej ilości insuliny i/lub normalnie reagować na insulinę, którą wytwarza ich organizm. Kiedy tak się dzieje, we krwi gromadzi się cukier (glukoza). Może to prowadzić do poważnych problemów medycznych, w tym uszkodzenia nerek, amputacji i ślepoty. Cukrzyca jest również ściśle związana z chorobami serca. Głównym celem leczenia cukrzycy jest obniżenie poziomu cukru we krwi do normalnego poziomu.
Q3. Dlaczego kontrolowanie cukrzycy typu 2 jest ważne?
Głównym celem leczenia cukrzycy jest obniżenie poziomu cukru we krwi do normalnego poziomu. Badania wykazały, że dobra kontrola poziomu cukru we krwi może zapobiegać lub opóźniać powikłania, takie jak choroby serca, choroby nerek lub ślepota.
Q4. Jak zwykle kontroluje się cukrzycę typu 2?
Wysoki poziom cukru we krwi można obniżyć poprzez dietę i ćwiczenia, szereg leków doustnych i zastrzyki z insuliny. Przed przyjęciem leku GLUCOVANCE 2,50 mg należy najpierw spróbować kontrolować cukrzycę poprzez ćwiczenia fizyczne i utratę wagi. Nawet jeśli przyjmujesz GLUCOVANCE, powinieneś nadal ćwiczyć i przestrzegać diety zalecanej dla Twojej cukrzycy.
P5. Czy GLUCOVANCE 400mg działa inaczej niż inne leki kontrolujące glikemię?
Tak. GLUCOVANCE 400mg łączy w sobie 2 leki obniżające poziom glukozy, gliburyd i metforminę. Te 2 leki współpracują ze sobą, aby poprawić różne defekty metaboliczne występujące w cukrzycy typu 2. Glyburyd obniża poziom cukru we krwi przede wszystkim poprzez zwiększenie uwalniania własnej insuliny z organizmu, a metformina obniża poziom cukru we krwi, po części poprzez pomaganie organizmowi w efektywniejszym wykorzystaniu własnej insuliny. Razem skutecznie pomagają w osiągnięciu lepszej kontroli glikemii.
P6. Co się stanie, jeśli mój poziom cukru we krwi jest nadal zbyt wysoki?
Jeśli stężenie cukru we krwi nie może być wystarczająco obniżone przez GLUCOVANCE, lekarz może przepisać insulinę do wstrzykiwań lub zastosować inne środki w celu kontrolowania cukrzycy.
P7. Czy GLUCOVANCE 400mg może powodować działania niepożądane?
GLUCOVANCE 2,50 mg, podobnie jak wszystkie leki obniżające poziom cukru we krwi, może powodować u niektórych pacjentów działania niepożądane. Większość z tych skutków ubocznych jest niewielka. Istnieją jednak również poważne, ale rzadkie działania niepożądane związane ze stosowaniem GLUCOVANCE (patrz Q9-Q13).
P8. Jakie są najczęstsze skutki uboczne GLUCOVANCE 500mg?
Najczęstsze działania niepożądane GLUCOVANCE 5 mg są zwykle niewielkie, takie jak biegunka, nudności i rozstrój żołądka. Jeśli te działania niepożądane wystąpią, zwykle pojawiają się w ciągu pierwszych kilku tygodni terapii. Przyjmowanie leku GLUCOVANCE z posiłkami może pomóc w zmniejszeniu tych działań niepożądanych.
Rzadziej mogą wystąpić objawy hipoglikemii (niskiego poziomu cukru we krwi), takie jak zawroty głowy, zawroty głowy, drżenie lub głód. Ryzyko wystąpienia objawów hipoglikemii wzrasta w przypadku pomijania posiłków, spożywania zbyt dużej ilości alkoholu lub intensywnego wysiłku fizycznego bez wystarczającej ilości jedzenia. Postępowanie zgodnie z zaleceniami lekarza może pomóc w uniknięciu tych objawów.
P9. Czy są jakieś poważne skutki uboczne, które może wywołać GLUCOVANCE?
osób z niedoborem dehydrogenazy glukozo-6-fosforanowej (G6PD) i przyjmujących preparat GLUCOVANCE może wystąpić niedokrwistość hemolityczna (szybki rozpad krwinek czerwonych). Niedobór G6PD zwykle występuje w rodzinach. Należy poinformować lekarza, jeśli u pacjenta lub członka jego rodziny zdiagnozowano niedobór G6PD przed rozpoczęciem stosowania leku GLUCOVANCE.
GLUCOVANCE rzadko powoduje poważne skutki uboczne. Najpoważniejszym działaniem niepożądanym, jakie może wywołać lek GLUCOVANCE 2,50 mg, jest kwasica mleczanowa.
P10. Czym jest kwas mlekowy i czy może mi się przytrafić?
Kwasica mleczanowa jest spowodowana gromadzeniem się kwasu mlekowego we krwi. Kwasica mleczanowa związana z metforminą jest rzadka i występowała głównie u osób, których nerki nie pracowały normalnie. Kwasicę mleczanową zgłaszano u około 1 na 33 000 pacjentów przyjmujących metforminę w ciągu roku. Chociaż występuje rzadko, jeśli wystąpi kwasica mleczanowa, może być śmiertelna nawet w połowie przypadków.
Ważne jest również, aby wątroba działała normalnie podczas przyjmowania leku GLUCOVANCE. Twoja wątroba pomaga usunąć kwas mlekowy z krwiobiegu.
Lekarz będzie monitorował cukrzycę i może od czasu do czasu przeprowadzać badania krwi, aby upewnić się, że nerki i wątroba funkcjonują prawidłowo.
Nie ma dowodów na to, że GLUCOVANCE uszkadza nerki lub wątrobę.
P11. Czy istnieją inne czynniki ryzyka kwasicy mleczanowej?
Ryzyko rozwoju kwasicy mleczanowej w wyniku przyjmowania leku GLUCOVANCE 400 mg jest bardzo niskie, o ile nerki i wątroba są zdrowe. Jednak niektóre czynniki mogą zwiększać ryzyko, ponieważ mogą wpływać na czynność nerek i wątroby. Powinieneś omówić swoje ryzyko z lekarzem.
Nie należy przyjmować leku GLUCOVANCE 400 mg, jeśli:
- Masz przewlekłe problemy z nerkami lub wątrobą
- Masz zastoinową niewydolność serca, która jest leczona lekami, np. digoksyną (Lanoxin®) lub furosemidem (Lasix®)
- Nadmiernie pijesz alkohol (cały czas lub krótkotrwałe „picie napadowe”)
- Jesteś poważnie odwodniony (utraciłeś dużą ilość płynów ustrojowych)
- Będziesz mieć pewne zabiegi rentgenowskie z wstrzykiwanymi środkami kontrastowymi
- Będziesz mieć operację
- Pojawi się poważny stan, taki jak zawał serca, ciężka infekcja lub udar
- Masz ≥ 80 lat i NIE przeszłaś badania czynności nerek
P12. Jakie są objawy kwasicy mleczanowej?
Niektóre z objawów to: uczucie osłabienia, zmęczenia lub dyskomfortu; niezwykły ból mięśni; problemy z oddychaniem; niezwykły lub nieoczekiwany dyskomfort w żołądku; uczucie zimna; zawroty głowy lub oszołomienie; lub nagłe spowolnienie lub nieregularne bicie serca.
W przypadku zauważenia tych objawów lub nagłej zmiany stanu zdrowia należy zaprzestać przyjmowania tabletek GLUCOVANCE i natychmiast skontaktować się z lekarzem. Kwasica mleczanowa to nagły przypadek medyczny, który należy leczyć w szpitalu.
P13. Co powinien wiedzieć mój lekarz, aby zmniejszyć ryzyko kwasicy mleczanowej?
Należy poinformować lekarza, jeśli cierpisz na chorobę, która powoduje silne wymioty, biegunkę i (lub) gorączkę, lub jeśli przyjmowanie płynów jest znacznie zmniejszone. Takie sytuacje mogą prowadzić do ciężkiego odwodnienia i może być konieczne tymczasowe przerwanie stosowania leku GLUCOVANCE 400 mg.
Powinieneś poinformować swojego lekarza, jeśli będziesz miał jakąkolwiek operację lub specjalistyczne zabiegi rentgenowskie, które wymagają wstrzyknięcia środków kontrastowych. W takich przypadkach leczenie lekiem GLUCOVANCE 2,50 mg należy tymczasowo przerwać.
P14. Czy mogę przyjmować GLUCOVANCE 500mg z innymi lekami?
Przypomnij swojemu lekarzowi, że przyjmujesz lek GLUCOVANCE 2,50 mg w przypadku przepisania nowego leku lub zmiany sposobu przyjmowania przepisanego już leku. GLUCOVANCE 400mg może zaburzać działanie niektórych leków, a niektóre leki mogą zakłócać działanie GLUCOVANCE.
Nie należy przyjmować leku GLUCOVANCE, jeśli pacjent przyjmuje bozentan stosowany w leczeniu tętniczego nadciśnienia płucnego (PAH), czyli wysokiego ciśnienia krwi w naczyniach płucnych.
P15. Co się stanie, jeśli zajdę w ciążę podczas przyjmowania GLUCOVANCE 400mg?
Należy poinformować lekarza, jeśli planujesz zajść w ciążę lub zaszła w ciążę. Podobnie jak w przypadku innych doustnych leków kontrolujących stężenie glukozy, nie należy przyjmować leku GLUCOVANCE w okresie ciąży.
Zwykle lekarz przepisuje insulinę podczas ciąży. Podobnie jak w przypadku wszystkich leków, Ty i Twój lekarz powinniście przedyskutować stosowanie leku GLUCOVANCE 5mg, jeśli karmicie Państwo piersią.
P16. Jak zażywać GLUCOVANCE?
Lekarz poinformuje pacjenta, ile tabletek leku GLUCOVANCE należy przyjmować i jak często. Powinno to być również wydrukowane na etykiecie recepty. Prawdopodobnie zaczniesz od małej dawki GLUCOVANCE 400 mg, a Twoja dawka będzie stopniowo zwiększana, aż do uzyskania kontroli poziomu cukru we krwi.
P17. Gdzie mogę uzyskać więcej informacji o GLUCOVANCE 400mg?
Ta ulotka jest podsumowaniem najważniejszych informacji o GLUCOVANCE. Jeśli masz jakiekolwiek pytania lub problemy, powinieneś porozmawiać z lekarzem lub innym pracownikiem służby zdrowia na temat cukrzycy typu 2, a także GLUCOVANCE i jej skutków ubocznych. Istnieje również ulotka (wkładka do opakowania) napisana dla pracowników służby zdrowia, którą może przekazać farmaceuta.
