Precose 25mg, 50mg Acarbose Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Precose 50mg i jak się go stosuje?
Precose (tabletki akarbozy) to doustny inhibitor alfa-glukozydazy stosowany w leczeniu cukrzycy typu 2. Precose 50 mg jest czasami stosowany w połączeniu z insuliną lub innymi lekami przeciwcukrzycowymi przyjmowanymi doustnie. Precose 25mg jest dostępny w formie generycznej.
Jakie są skutki uboczne Precose 25mg?
Częste działania niepożądane Precose obejmują:
- biegunka,
- gaz,
- wzdęcia,
- rozstrój żołądka lub
- ból brzucha w pierwszych kilku tygodniach leczenia, ponieważ organizm dostosowuje się do tego leku, ale zwykle ustępuje z czasem.
Inne skutki uboczne Precose 50mg to wysypka skórna lub swędzenie. Należy poinformować lekarza, jeśli wystąpią rzadkie, ale bardzo poważne działania niepożądane leku Precose 25 mg, w tym:
- niezwykłe zmęczenie,
- uporczywe nudności lub wymioty,
- silny ból brzucha lub brzucha,
- krwawienie z odbytnicy,
- zażółcenie oczu lub skóry lub
- ciemny mocz.
OPIS
PRECOSE® (tabletki akarbozy) to doustny inhibitor alfa-glukozydazy do stosowania w leczeniu cukrzycy typu 2. Akarboza jest oligosacharydem otrzymywanym w procesie fermentacji mikroorganizmu Actinoplanes utahensis i jest chemicznie znany jako O-4,6-dideoksy4-[[(1S,4R,5S,6S)-4,5,6-trihydroksy- 3-(hydroksymetylo)-2-cykloheksen-1-ylo]amino]a-D-glukopiranozylo-(1 -> 4)-0-a-D-glukopiranozylo-(1 -> 4)-D-glukoza. Jest to biały lub prawie biały proszek o masie cząsteczkowej 645,6. Akarboza jest rozpuszczalna w wodzie i ma pKa 5,1. Jego wzór empiryczny to C25H43NO18, a struktura chemiczna jest następująca:
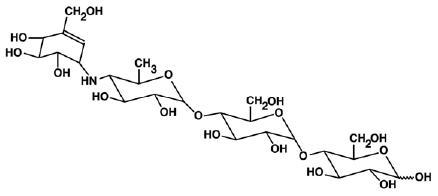
PRECOSE 50 mg jest dostępny w postaci tabletek 25 mg, 50 mg i 100 mg do stosowania doustnego. Nieaktywnymi składnikami są skrobia, celuloza mikrokrystaliczna, stearynian magnezu i koloidalny dwutlenek krzemu.
WSKAZANIA
PRECOSE jest wskazany jako dodatek do diety i ćwiczeń fizycznych w celu poprawy kontroli glikemii u osób dorosłych z cukrzycą typu 2.
DAWKOWANIE I SPOSÓB PODAWANIA
Nie ma ustalonego schematu dawkowania w leczeniu cukrzycy za pomocą PRECOSE lub jakiegokolwiek innego środka farmakologicznego. Dawkowanie PRECOSE 25mg należy dostosować indywidualnie na podstawie zarówno skuteczności, jak i tolerancji, nie przekraczając jednak maksymalnej zalecanej dawki 100 mg trzy razy dziennie PRECOSE należy przyjmować trzy razy dziennie na początku (przy pierwszym kęsie) każdego głównego posiłku.
PRECOSE należy rozpocząć od małej dawki, stopniowo zwiększając dawkę, jak opisano poniżej, zarówno w celu zmniejszenia żołądkowo-jelitowych działań niepożądanych, jak i umożliwienia określenia minimalnej dawki wymaganej do odpowiedniej kontroli glikemii pacjenta. W przypadku nieprzestrzegania przepisanej diety mogą nasilić się jelitowe skutki uboczne. W przypadku wystąpienia silnie dokuczliwych objawów pomimo przestrzegania przepisanej diety cukrzycowej należy skonsultować się z lekarzem i czasowo lub na stałe zmniejszyć dawkę.
Podczas rozpoczynania leczenia i dostosowywania dawki (patrz poniżej) można wykorzystać stężenie glukozy w osoczu godzinę po posiłku w celu określenia odpowiedzi terapeutycznej na PRECOSE i określenia minimalnej skutecznej dawki dla pacjenta. Następnie należy mierzyć hemoglobinę glikozylowaną w odstępach około trzech miesięcy. Celem terapeutycznym powinno być obniżenie zarówno poposiłkowych poziomów glukozy, jak i glikozylowanej hemoglobiny do wartości prawidłowych lub zbliżonych do prawidłowych poprzez zastosowanie najniższej skutecznej dawki preparatu PRECOSE w monoterapii lub w połączeniu z pochodnymi sulfonylomocznika, insuliną lub metforminą.
Dawka początkowa
Zalecana dawka początkowa PRECOSE 25mg to 25 mg podawane doustnie trzy razy dziennie na początku (przy pierwszym kęsie) każdego głównego posiłku. Jednak niektórzy pacjenci mogą odnieść korzyści z bardziej stopniowego dostosowywania dawki w celu zminimalizowania żołądkowo-jelitowych skutków ubocznych. Można to osiągnąć, rozpoczynając leczenie od dawki 25 mg raz na dobę, a następnie zwiększając częstość podawania do uzyskania 25 mg trzy razy dziennie.
Dawkowanie podtrzymujące
Po osiągnięciu schematu dawkowania 25 mg trzy razy na dobę, dawkę preparatu PRECOSE 50 mg należy dostosowywać w odstępach 4–8 tygodni na podstawie stężenia glukozy lub hemoglobiny glikozylowanej godzinę po posiłku oraz tolerancji. Dawkę można zwiększyć z 25 mg trzydz. do 50 mg trzydz. zwiększających ryzyko wystąpienia podwyższonej aktywności aminotransferaz w surowicy, tylko u pacjentów o masie ciała > 60 kg należy brać pod uwagę dostosowanie dawki powyżej 50 mg tid (patrz ŚRODKI OSTROŻNOŚCI ). Jeśli po zwiększeniu dawki do 100 mg trzy razy na dobę nie obserwuje się dalszego zmniejszenia stężenia glukozy lub hemoglobiny glikozylowanej po posiłku, należy rozważyć zmniejszenie dawki. Po ustaleniu skutecznej i tolerowanej dawki należy ją utrzymać.
Maksymalna dawka
Maksymalna zalecana dawka dla pacjentów ≤ 60 kg wynosi 50 mg tid Maksymalna zalecana dawka dla pacjentów > 60 kg wynosi 100 mg tid
Pacjenci otrzymujący sulfonylomoczniki lub insulinę
Leki sulfonylomocznikowe lub insulina mogą powodować hipoglikemię. PRECOSE podawany w połączeniu z sulfonylomocznikiem lub insuliną spowoduje dalsze obniżenie stężenia glukozy we krwi i może zwiększyć ryzyko hipoglikemii. W przypadku wystąpienia hipoglikemii należy odpowiednio dostosować dawkowanie tych środków.
JAK DOSTARCZONE
PRECOSE jest dostępny w postaci okrągłych tabletek 25 mg, 50 mg lub 100 mg bez rowka dzielącego. Każda tabletka ma kolor od białego do żółtego. Tabletka 25 mg jest oznaczona kodem „PRECOSE” po jednej stronie i „25” po drugiej stronie. Tabletka 50 mg jest opatrzona kodem „PRECOSE” i „50” po tej samej stronie. Tabletka 100 mg jest opatrzona kodem „PRECOSE” i „100” po tej samej stronie. PRECOSE jest dostępny w butelkach o mocy 100 i 50 mg w opakowaniach jednostkowych po 100.
Nie przechowywać w temperaturze powyżej 25°C (77°F). Chronić przed wilgocią. W przypadku butelek przechowywać pojemnik szczelnie zamknięty.
Bayer HealthCare Pharmaceuticals Inc. Wayne, NJ 07470. Wyprodukowano w Niemczech. 11/11
SKUTKI UBOCZNE
Przewód pokarmowy
Objawy żołądkowo-jelitowe są najczęstszymi reakcjami na PRECOSE. W badaniach kontrolowanych placebo w Stanach Zjednoczonych częstość występowania bólu brzucha, biegunki i wzdęć wynosiła odpowiednio 19%, 31% i 74% u 1255 pacjentów leczonych preparatem PRECOSE 50–300 mg 3xdz. i 29% u 999 pacjentów otrzymujących placebo.
rocznym badaniu bezpieczeństwa, podczas którego pacjenci prowadzili dzienniki objawów żołądkowo-jelitowych, bóle brzucha i biegunka z czasem powracały do poziomu sprzed leczenia, a częstotliwość i intensywność wzdęć zmniejszała się z czasem. Nasilone objawy ze strony przewodu pokarmowego u pacjentów leczonych PRECOSE 50mg są przejawem mechanizmu działania PRECOSE i są związane z obecnością niestrawionych węglowodanów w dolnym odcinku przewodu pokarmowego.
W przypadku nieprzestrzegania przepisanej diety mogą nasilić się jelitowe skutki uboczne. W przypadku wystąpienia silnie dokuczliwych objawów pomimo przestrzegania przepisanej diety cukrzycowej należy skonsultować się z lekarzem i czasowo lub na stałe zmniejszyć dawkę.
Podwyższony poziom transaminazy w surowicy
Widzieć ŚRODKI OSTROŻNOŚCI .
Inne nieprawidłowe wyniki badań laboratoryjnych
Niewielkie zmniejszenie hematokrytu występowało częściej u pacjentów leczonych PRECOSE niż u pacjentów otrzymujących placebo, ale nie było związane ze zmniejszeniem stężenia hemoglobiny. Niski poziom wapnia w surowicy i niski poziom witaminy B6 w osoczu były związane z terapią PRECOSE 50 mg, ale uważa się, że są one fałszywe lub nie mają znaczenia klinicznego.
Raporty o zdarzeniach niepożądanych po wprowadzeniu do obrotu
Dodatkowe zdarzenia niepożądane zgłaszane po wprowadzeniu do obrotu na całym świecie obejmują piorunujące zapalenie wątroby zakończone zgonem, reakcje skórne nadwrażliwości (na przykład wysypka, rumień, wysypka i pokrzywka), obrzęk, niedrożność/podniedrożność jelit, żółtaczka i (lub) zapalenie wątroby i związane z nimi uszkodzenie wątroby, małopłytkowość i pneumatoza cystoides intestinalis (patrz ŚRODKI OSTROŻNOŚCI ).
Pneumatosis Cystoides Intestinalis
Po wprowadzeniu produktu do obrotu rzadko zgłaszano przypadki odmy torbielowatej jelit związanej ze stosowaniem inhibitorów alfa-glukozydazy, w tym preparatu Precose. Pneumatosis cystoides intestinalis może objawiać się biegunką, wydzieliną śluzu, krwawieniem z odbytu i zaparciami. Powikłania mogą obejmować odmę otrzewnową, skręt, niedrożność jelit, wgłobienie, krwotok jelitowy i perforację jelit. W przypadku podejrzenia pneumatosis cystoides intestinalis należy odstawić Precose 25 mg i wykonać odpowiednią diagnostykę obrazową.
INTERAKCJE Z LEKAMI
Niektóre leki mają tendencję do wywoływania hiperglikemii i mogą prowadzić do utraty kontroli stężenia glukozy we krwi. Leki te obejmują tiazydy i inne leki moczopędne, kortykosteroidy, fenotiazyny, produkty tarczycy, estrogeny, doustne środki antykoncepcyjne, fenytoinę, kwas nikotynowy, sympatykomimetyki, leki blokujące kanały wapniowe i izoniazyd. Gdy takie leki są podawane pacjentowi otrzymującemu PRECOSE 25 mg, pacjent powinien być uważnie obserwowany pod kątem utraty kontroli stężenia glukozy we krwi. Po odstawieniu takich leków u pacjentów otrzymujących PRECOSE 50 mg w skojarzeniu z pochodnymi sulfonylomocznika lub insuliną, pacjenci powinni być uważnie obserwowani pod kątem jakichkolwiek objawów hipoglikemii.
Pacjenci otrzymujący sulfonylomocznik lub insulinę: Leki sulfonylomocznikowe lub insulina mogą powodować hipoglikemię. PRECOSE 25 mg podawany w połączeniu z pochodną sulfonylomocznika lub insuliną może powodować dalsze obniżenie stężenia glukozy we krwi i może zwiększać ryzyko hipoglikemii. W przypadku wystąpienia hipoglikemii należy odpowiednio dostosować dawkowanie tych środków. Bardzo rzadko zgłaszano pojedyncze przypadki wstrząsu hipoglikemicznego u pacjentów otrzymujących terapię PRECOSE w skojarzeniu z pochodnymi sulfonylomocznika i (lub) insuliną.
Adsorbenty jelitowe (np. węgiel drzewny) i preparaty enzymów trawiennych zawierające enzymy rozkładające węglowodany (np. amylaza, pankreatyna) mogą osłabiać działanie PRECOSE i nie należy ich stosować jednocześnie.
Wykazano, że PRECOSE 25 mg zmienia biodostępność digoksyny podczas ich jednoczesnego podawania, co może wymagać dostosowania dawki digoksyny. (Widzieć FARMAKOLOGIA KLINICZNA , Interakcje między lekami .)
OSTRZEŻENIA
Nie podano informacji
ŚRODKI OSTROŻNOŚCI
Ogólny
Wyniki makronaczyniowe
Nie przeprowadzono badań klinicznych, które wykazałyby jednoznaczne dowody na zmniejszenie ryzyka makronaczyniowego przy stosowaniu PRECOSE 25 mg lub jakiegokolwiek innego leku przeciwcukrzycowego.
Hipoglikemia
Ze względu na mechanizm działania PRECOSE podawany samodzielnie nie powinien powodować hipoglikemii na czczo lub po posiłku. Leki sulfonylomocznikowe lub insulina mogą powodować hipoglikemię. Ponieważ PRECOSE 50 mg podawany w połączeniu z sulfonylomocznikiem lub insuliną spowoduje dalsze obniżenie poziomu glukozy we krwi, może zwiększyć ryzyko hipoglikemii. Hipoglikemia nie występuje u pacjentów otrzymujących samą metforminę w zwykłych warunkach stosowania i nie zaobserwowano zwiększonej częstości występowania hipoglikemii u pacjentów, u których do leczenia metforminą dodano preparat PRECOSE 50 mg.
leczeniu łagodnej do umiarkowanej hipoglikemii zamiast sacharozy (cukru trzcinowego) należy stosować doustną glukozę (dekstrozę), której wchłanianie nie jest hamowane przez PRECOSE. Sacharoza, której hydroliza do glukozy i fruktozy jest hamowana przez PRECOSE, nie nadaje się do szybkiej korekty hipoglikemii. Ciężka hipoglikemia może wymagać dożylnego wlewu glukozy lub wstrzyknięcia glukagonu.
Podwyższony poziom transaminazy w surowicy
badaniach długoterminowych (do 12 miesięcy, obejmujących dawki PRECOSE 25 mg do 300 mg 3xdz) przeprowadzonych w Stanach Zjednoczonych, pojawiające się podczas leczenia zwiększenie aktywności aminotransferaz w surowicy (AspAT i/lub AlAT) powyżej górnej granicy normy (GGN). ), ponad 1,8-krotność GGN i ponad 3-krotność GGN wystąpiła odpowiednio u 14%, 6% i 3% pacjentów leczonych PRECOSE w porównaniu z odpowiednio 7%, 2% i 1%, pacjentów otrzymujących placebo. Chociaż te różnice między terapiami były statystycznie istotne, wzrosty te były bezobjawowe, odwracalne, częstsze u kobiet i generalnie nie były związane z innymi dowodami dysfunkcji wątroby. Ponadto wydaje się, że te podwyższenia aktywności aminotransferaz w surowicy są zależne od dawki. W badaniach w USA obejmujących dawki od 50 mg PRECOSE do maksymalnej zatwierdzonej dawki 100 mg trzy razy na dobę, pojawiające się podczas leczenia zwiększenie aktywności AspAT i (lub) AlAT na dowolnym poziomie nasilenia było podobne u pacjentów otrzymujących PRECOSE i u pacjentów otrzymujących placebo (p ≥ 0,496). .
ciągu około 3 milionów pacjentolat międzynarodowego doświadczenia po wprowadzeniu produktu PRECOSE 50 mg do obrotu zgłoszono 62 przypadki zwiększenia aktywności aminotransferaz w surowicy > 500 j.m./l (z których 29 było związanych z żółtaczką). Czterdziestu jeden z tych 62 pacjentów otrzymywało leczenie dawką 100 mg trzy razy dziennie lub większą, a 33 z 45 pacjentów, u których zgłoszono masę ciała
Utrata kontroli glukozy we krwi
Gdy pacjenci z cukrzycą są narażeni na stres, taki jak gorączka, uraz, infekcja lub zabieg chirurgiczny, może wystąpić chwilowa utrata kontroli stężenia glukozy we krwi. W takich przypadkach może być konieczna tymczasowa insulinoterapia.
Testy laboratoryjne
Odpowiedź terapeutyczną na PRECOSE należy monitorować za pomocą okresowych badań stężenia glukozy we krwi. Do monitorowania długoterminowej kontroli glikemii zaleca się pomiar stężenia hemoglobiny glikozylowanej.
PRECOSE 25 mg, szczególnie w dawkach przekraczających 50 mg 3xdz, może powodować zwiększenie aktywności aminotransferaz w surowicy i, w rzadkich przypadkach, hiperbilirubinemię. Zaleca się sprawdzanie poziomu transaminaz w surowicy co 3 miesiące przez pierwszy rok leczenia preparatem PRECOSE, a następnie okresowo. W przypadku zaobserwowania podwyższonej aktywności aminotransferaz wskazane może być zmniejszenie dawki lub przerwanie leczenia, szczególnie jeśli podwyższenie utrzymuje się.
Zaburzenia czynności nerek
Stężenie PRECOSE w osoczu u ochotników z zaburzeniami czynności nerek było proporcjonalnie zwiększone w stosunku do stopnia zaburzenia czynności nerek. Nie przeprowadzono długoterminowych badań klinicznych u chorych na cukrzycę z istotną dysfunkcją nerek (stężenie kreatyniny w surowicy > 2,0 mg/dl). Dlatego leczenie tych pacjentów preparatem PRECOSE 50 mg nie jest zalecane.
Karcynogeneza, mutageneza i upośledzenie płodności
Przeprowadzono osiem badań rakotwórczości z użyciem akarbozy. Sześć badań przeprowadzono na szczurach (dwa szczepy, Sprague-Dawley i Wistar), a dwa badania na chomikach.
pierwszym badaniu na szczurach szczury Sprague-Dawley otrzymywały akarbozę w paszy w dużych dawkach (do około 500 mg/kg masy ciała) przez 104 tygodnie. Leczenie akarbozą spowodowało znaczny wzrost częstości występowania guzów nerek (gruczolaków i gruczolakoraków) oraz łagodnych guzów z komórek Leydiga. To badanie zostało powtórzone z podobnym wynikiem. Przeprowadzono dalsze badania w celu oddzielenia bezpośredniego rakotwórczego działania akarbozy od skutków pośrednich wynikających z niedożywienia węglowodanowego wywołanego dużymi dawkami akarbozy zastosowanymi w badaniach. W jednym badaniu na szczurach Sprague-Dawley akarbozę zmieszano z paszą, ale pozbawieniu węglowodanów zapobiegło dodanie glukozy do diety.

26-miesięcznym badaniu na szczurach Sprague-Dawley akarbozę podawano codziennie przez zgłębnik poposiłkowy, aby uniknąć farmakologicznego działania leku. W obu tych badaniach nie wystąpiła zwiększona częstość występowania guzów nerek stwierdzona w badaniach pierwotnych. Akarbozę podawano również z pokarmem i przez zgłębnik poposiłkowy w dwóch oddzielnych badaniach na szczurach rasy Wistar. W żadnym z tych badań na szczurach Wistar nie stwierdzono zwiększonej częstości występowania nowotworów nerek. W dwóch badaniach żywienia chomików, z suplementacją glukozy i bez niej, również nie było dowodów na rakotwórczość.
Akarboza nie indukowała żadnych uszkodzeń DNA in vitro w teście aberracji chromosomowych CHO, teście mutagenezy bakteryjnej (Ames) ani teście wiązania DNA. In vivo nie wykryto uszkodzeń DNA w dominującym teście letalnym u samców myszy ani teście mikrojądrowym u myszy.
Badania płodności przeprowadzone na szczurach po podaniu doustnym nie wykazały niepożądanego wpływu na płodność lub ogólną zdolność do reprodukcji.
Ciąża
Działanie teratogenne: Ciąża Kategoria B.
Bezpieczeństwo PRECOSE u kobiet w ciąży nie zostało ustalone. Badania rozrodczości przeprowadzono na szczurach przy dawkach do 480 mg/kg (odpowiadających 9-krotności ekspozycji u ludzi, na podstawie stężenia leku we krwi) i nie wykazały dowodów na upośledzenie płodności lub uszkodzenie płodu z powodu akarbozy. U królików zmniejszony przyrost masy ciała matki, prawdopodobnie spowodowany działaniem farmakodynamicznym dużych dawek akarbozy w jelitach, mógł być odpowiedzialny za nieznaczny wzrost liczby ubytków embrionalnych. Jednakże u królików, którym podawano 160 mg/kg akarbozy (co odpowiada 10-krotności dawki u ludzi, w oparciu o powierzchnię ciała) nie wykryto dowodów na embriotoksyczność i brak dowodów na teratogenność przy dawce 32-krotności dawki u ludzi (na podstawie powierzchnia). Nie ma jednak odpowiednich i dobrze kontrolowanych badań PRECOSE 25 mg u kobiet w ciąży. Ponieważ badania reprodukcji na zwierzętach nie zawsze pozwalają przewidzieć reakcję człowieka, lek ten powinien być stosowany w czasie ciąży tylko wtedy, gdy jest to bezwzględnie konieczne. Ponieważ aktualne informacje zdecydowanie sugerują, że nieprawidłowe poziomy glukozy we krwi w czasie ciąży są związane z większą częstością występowania wad wrodzonych oraz zwiększoną zachorowalnością i śmiertelnością noworodków, większość ekspertów zaleca stosowanie insuliny w czasie ciąży w celu utrzymania poziomu glukozy we krwi tak blisko normy, jak to możliwe. .
Matki karmiące
Niewielką ilość radioaktywności wykryto w mleku karmiących szczurów po podaniu znakowanej radioaktywnie akarbozy. Nie wiadomo, czy lek ten przenika do mleka ludzkiego. Ponieważ wiele leków przenika do mleka ludzkiego, PRECOSE 25mg nie powinien być podawany kobiecie karmiącej.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność PRECOSE 25 mg u dzieci nie zostały ustalone.
Zastosowanie geriatryczne
Z całkowitej liczby pacjentów w badaniach klinicznych PRECOSE 25 mg w Stanach Zjednoczonych, 27% miało 65 lat i więcej, a 4% miało 75 lat i więcej. Nie zaobserwowano ogólnych różnic w bezpieczeństwie i skuteczności między tymi osobami a młodszymi osobami. Średnie pole pod krzywą w stanie stacjonarnym (AUC) i maksymalne stężenia akarbozy były około 1,5 raza większe u osób w podeszłym wieku w porównaniu z młodymi ochotnikami; jednak różnice te nie były istotne statystycznie.
PRZEDAWKOWAĆ
przeciwieństwie do pochodnych sulfonylomocznika lub insuliny, przedawkowanie PRECOSE nie spowoduje hipoglikemii. Przedawkowanie może spowodować przemijające nasilenie wzdęć, biegunki i dyskomfortu w jamie brzusznej, które wkrótce ustąpią. W przypadku przedawkowania choremu nie należy podawać napojów ani posiłków zawierających węglowodany (polisacharydy, oligosacharydy i disacharydy) przez kolejne 4–6 godzin.
PRZECIWWSKAZANIA
PRECOSE 25mg jest przeciwwskazany u pacjentów ze stwierdzoną nadwrażliwością na lek. Precose 25 mg jest przeciwwskazany u pacjentów z cukrzycową kwasicą ketonową lub marskością wątroby. PRECOSE 25mg jest również przeciwwskazany u pacjentów z nieswoistym zapaleniem jelit, owrzodzeniem okrężnicy, częściową niedrożnością jelit lub u pacjentów predysponowanych do niedrożności jelit. Ponadto PRECOSE jest przeciwwskazany u pacjentów z przewlekłymi chorobami jelit związanymi z wyraźnymi zaburzeniami trawienia lub wchłaniania oraz u pacjentów ze stanami, które mogą ulec pogorszeniu w wyniku zwiększonego tworzenia się gazów w jelicie.
FARMAKOLOGIA KLINICZNA
Akarboza jest złożonym oligosacharydem, który opóźnia trawienie spożytych węglowodanów, powodując w ten sposób mniejszy wzrost stężenia glukozy we krwi po posiłkach. W wyniku obniżenia poziomu glukozy w osoczu PRECOSE obniża poziom hemoglobiny glikozylowanej u pacjentów z cukrzycą typu 2. Ogólnoustrojowa nieenzymatyczna glikozylacja białek, odzwierciedlona w poziomach hemoglobiny glikozylowanej, jest funkcją średniego stężenia glukozy we krwi w czasie.
Mechanizm akcji
przeciwieństwie do sulfonylomoczników PRECOSE 50mg nie zwiększa wydzielania insuliny. Działanie przeciwhiperglikemiczne akarbozy wynika z konkurencyjnego, odwracalnego hamowania enzymów alfa-amylazy trzustkowej i jelitowej hydrolazy alfa-glukozydowej związanej z błoną błonową. Alfa-amylaza trzustkowa hydrolizuje złożone skrobie do oligosacharydów w świetle jelita cienkiego, podczas gdy związane z błoną jelitową alfa-glukozydazy hydrolizują oligosacharydy, trisacharydy i disacharydy do glukozy i innych monosacharydów w rąbku szczoteczkowym jelita cienkiego. U pacjentów z cukrzycą hamowanie tego enzymu powoduje opóźnione wchłanianie glukozy i obniżenie hiperglikemii poposiłkowej.
Ponieważ jego mechanizm działania jest inny, efekt PRECOSE w celu zwiększenia kontroli glikemii jest addytywny do działania sulfonylomoczników, insuliny lub metforminy stosowanych w skojarzeniu. Ponadto PRECOSE 50 mg zmniejsza insulinotropowe i zwiększające wagę działanie pochodnych sulfonylomocznika.
Akarboza nie działa hamująco na laktazę i w związku z tym nie oczekuje się, że będzie wywoływać nietolerancję laktozy.
Farmakokinetyka
Wchłanianie
badaniu z udziałem 6 zdrowych mężczyzn mniej niż 2% doustnej dawki akarbozy zostało wchłonięte jako aktywny lek, podczas gdy około 35% całkowitej radioaktywności z dawki doustnej znakowanej 14C zostało wchłonięte. Średnio 51% dawki doustnej zostało wydalone z kałem w postaci niewchłoniętej radioaktywności związanej z lekiem w ciągu 96 godzin po spożyciu. Ponieważ akarboza działa lokalnie w przewodzie pokarmowym, ta niska ogólnoustrojowa biodostępność związku macierzystego jest pożądana terapeutycznie. Po doustnym podaniu zdrowym ochotnikom akarbozy znakowanej węglem 14C, maksymalne stężenie radioaktywności w osoczu osiągnięto 14-24 godzin po podaniu, podczas gdy maksymalne stężenie substancji czynnej w osoczu było osiągane po około 1 godzinie. Opóźnione wchłanianie radioaktywności związanej z akarbozą odzwierciedla wchłanianie metabolitów, które mogą być tworzone przez bakterie jelitowe lub jelitową hydrolizę enzymatyczną.
Metabolizm
Akarboza jest metabolizowana wyłącznie w przewodzie pokarmowym, głównie przez bakterie jelitowe, ale także przez enzymy trawienne. Część tych metabolitów (około 34% dawki) została wchłonięta, a następnie wydalona z moczem. Co najmniej 13 metabolitów zostało oddzielonych chromatograficznie z próbek moczu. Główne metabolity zostały zidentyfikowane jako pochodne 4-metylopirogalolu (tj. koniugaty siarczanowe, metylowe i glukuronidowe). Jeden metabolit (powstały przez odszczepienie cząsteczki glukozy od akarbozy) ma również działanie hamujące alfa-glukozydazę. Metabolit ten, wraz ze związkiem macierzystym, odzyskiwany z moczu, stanowi mniej niż 2% całkowitej podanej dawki.
Wydalanie
Frakcja akarbozy, która jest wchłaniana w postaci nienaruszonego leku, jest prawie całkowicie wydalana przez nerki. Po podaniu dożylnym akarbozy 89% dawki odzyskano w moczu jako aktywny lek w ciągu 48 godzin. W przeciwieństwie do tego, mniej niż 2% dawki doustnej zostało odzyskane w moczu jako lek aktywny (tj. związek macierzysty i aktywny metabolit). Jest to zgodne z niską biodostępnością leku macierzystego. Okres półtrwania aktywności akarbozy w osoczu wynosi około 2 godzin u zdrowych ochotników. W konsekwencji akumulacja leku nie występuje przy podawaniu doustnym trzy razy dziennie (trzy razy dziennie).
Specjalne populacje
Średnie pole pod krzywą w stanie stacjonarnym (AUC) i maksymalne stężenia akarbozy były około 1,5 raza większe u osób w podeszłym wieku w porównaniu z młodymi ochotnikami; jednak różnice te nie były istotne statystycznie. Pacjenci z ciężkimi zaburzeniami czynności nerek (Clcr
Interakcje między lekami
Badania przeprowadzone na zdrowych ochotnikach wykazały, że PRECOSE nie ma wpływu na farmakokinetykę ani farmakodynamikę nifedypiny, propranololu ani ranitydyny. PRECOSE nie zaburzał wchłaniania ani rozmieszczania gliburydu sulfonylomocznika u pacjentów z cukrzycą. PRECOSE może wpływać na biodostępność digoksyny i może wymagać dostosowania dawki digoksyny o 16% (90% przedział ufności: 8-23%), zmniejszyć średnie Cmax digoksyny o 26% (90% przedział ufności: 16-34%) i zmniejszyć średnie minimalne stężenia digoksyny o 9% (90% granica ufności: 19% spadek do 2% wzrostu). (Widzieć ŚRODKI OSTROŻNOŚCI: INTERAKCJE Z LEKAMI .)
Ilość wchłoniętej metforminy podczas przyjmowania preparatu PRECOSE była biorównoważna ilości wchłoniętej podczas przyjmowania placebo, na co wskazują wartości AUC w osoczu. Jednak maksymalne stężenie metforminy w osoczu było zmniejszone o około 20% podczas przyjmowania preparatu PRECOSE z powodu niewielkiego opóźnienia we wchłanianiu metforminy. Interakcja między preparatem PRECOSE i metforminą jest niewielka lub w ogóle klinicznie istotna.
Badania kliniczne
Doświadczenie kliniczne z badań nad ustalaniem dawki u pacjentów z cukrzycą typu 2 leczonych wyłącznie dietą
Połączono wyniki sześciu kontrolowanych badań PRECOSE w monoterapii z zastosowaniem stałej dawki w leczeniu cukrzycy typu 2, obejmujących 769 pacjentów leczonych PRECOSE, i połączono średnią ważoną różnicy w porównaniu z placebo w średniej zmianie stężenia hemoglobiny glikozylowanej w porównaniu z wartością wyjściową ( HbA1c) obliczono dla każdego poziomu dawki, jak przedstawiono poniżej:
Chociaż w badaniach stosowano maksymalną dawkę 200 lub 300 mg tid, maksymalna zalecana dawka dla pacjentów o masie ciała 60 kg wynosi 100 mg tid
Wyniki z tych sześciu badań monoterapii z ustaloną dawką połączono również w celu uzyskania średniej ważonej różnicy w porównaniu z placebo w średniej zmianie od wartości początkowej dla poziomu glukozy w osoczu godzinę po posiłku, jak pokazano na poniższym rysunku:
Rysunek 1 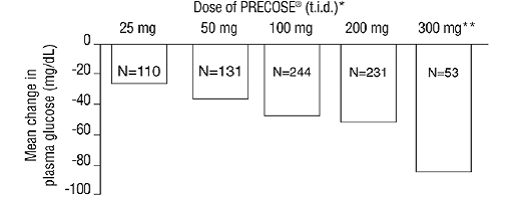
* PRECOSE 50 mg różnił się statystycznie istotnie od placebo we wszystkich dawkach pod względem wpływu na stężenie glukozy w osoczu godzinę po posiłku. **Schemat PRECOSE 300 mg 3xdz.
Doświadczenie kliniczne u pacjentów z cukrzycą typu 2 w monoterapii lub w skojarzeniu z pochodnymi sulfonylomocznika, metforminą lub insuliną
PRECOSE badano jako monoterapię oraz jako terapię skojarzoną z sulfonylomocznikiem, metforminą lub insuliną. Wpływ leczenia na poziomy HbA1c i poziom glukozy godzinę po posiłku podsumowano w czterech kontrolowanych placebo, podwójnie zaślepionych, randomizowanych badaniach przeprowadzonych w Stanach Zjednoczonych, odpowiednio w tabelach 2 i 3. Różnice w leczeniu po odjęciu placebo, które podsumowano poniżej, były statystycznie istotne dla obu zmiennych we wszystkich tych badaniach.
Badanie 1 (n=109) obejmowało pacjentów leczonych w tle wyłącznie dietą. Średnim efektem dodania PRECOSE do terapii dietetycznej była zmiana HbA1c o -0,78% i poprawa glikemii godzinę po posiłku o -74,4 mg/dl.
W badaniu 2 (n=137) średni efekt dodania PRECOSE 25 mg do maksymalnej terapii pochodnymi sulfonylomocznika to zmiana HbA1c o -0,54% i poprawa stężenia glukozy godzinę po posiłku o -33,5 mg/dl.
badaniu 3 (n=147) średni efekt dodania preparatu PRECOSE 50 mg do maksymalnego leczenia metforminą to zmiana HbA1c o -0,65% i poprawa stężenia glukozy godzinę po posiłku o -34,3 mg/dl.
W badaniu 4 (n=145) wykazano, że PRECOSE dodany pacjentom leczonym podstawowym insuliną spowodował średnią zmianę HbA1c o -0,69% i poprawę stężenia glukozy godzinę po posiłku o -36,0 mg/dl.
W Kanadzie przeprowadzono roczne badanie PRECOSE w monoterapii lub w skojarzeniu z sulfonylomocznikiem, metforminą lub insuliną, w którym do pierwotnej analizy skuteczności włączono 316 pacjentów (ryc. 2). W grupach otrzymujących dietę, pochodną sulfonylomocznika i metforminę, średni spadek HbA1c wywołany dodaniem PRECOSE 50 mg był statystycznie istotny po sześciu miesiącach, a efekt ten utrzymywał się przez rok. U pacjentów leczonych preparatem PRECOSE na insulinie wystąpiło statystycznie istotne zmniejszenie HbA1c po sześciu miesiącach i trend do zmniejszenia po roku.
Rysunek 2 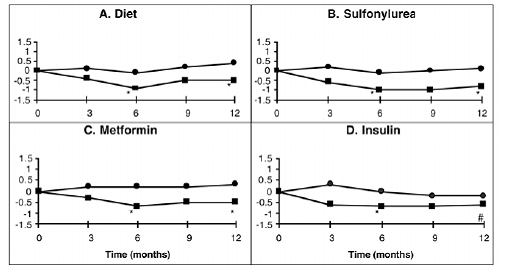
Rysunek 2: Wpływ PRECOSE (III ) i Placebo ( III ) na średnią zmianę poziomu HbA1c w stosunku do wartości wyjściowej w ciągu rocznego badania u pacjentów z cukrzycą typu 2 w połączeniu z: (A) samą dietą; (B) sulfonylomocznik; (C) metformina; lub (D) insulina. Zbadano różnice w leczeniu po 6 i 12 miesiącach: * p
INFORMACJA O PACJENCIE
Pacjentom należy zalecić przyjmowanie preparatu PRECOSE 50 mg doustnie trzy razy dziennie na początku (przy pierwszym kęsie) każdego głównego posiłku. Ważne jest, aby pacjenci nadal przestrzegali zaleceń dietetycznych, regularnego programu ćwiczeń oraz regularnego badania moczu i/lub stężenia glukozy we krwi.
Sam PRECOSE nie powoduje hipoglikemii nawet przy podawaniu pacjentom na czczo. Leki sulfonylomocznikowe i insulina mogą jednak obniżyć poziom cukru we krwi na tyle, aby wywołać objawy lub czasami zagrażającą życiu hipoglikemię. Ponieważ PRECOSE podawany w połączeniu z sulfonylomocznikiem lub insuliną spowoduje dalsze obniżenie poziomu cukru we krwi, może zwiększyć potencjał hipoglikemizujący tych leków. Hipoglikemia nie występuje u pacjentów otrzymujących samą metforminę w zwykłych warunkach stosowania i nie zaobserwowano zwiększonej częstości występowania hipoglikemii u pacjentów, u których do leczenia metforminą dodano PRECOSE. Ryzyko hipoglikemii, jej objawy i leczenie oraz stany predysponujące do jej rozwoju powinny być dobrze rozumiane przez pacjentów i odpowiedzialnych członków rodziny. Ponieważ PRECOSE 50 mg zapobiega rozkładowi cukru stołowego, pacjenci powinni mieć łatwo dostępne źródło glukozy (dekstroza, D-glukoza) w celu leczenia objawów niskiego poziomu cukru we krwi podczas przyjmowania PRECOSE w połączeniu z pochodną sulfonylomocznika lub insuliną.
Jeśli podczas stosowania PRECOSE wystąpią działania niepożądane, zwykle rozwijają się one w ciągu pierwszych kilku tygodni terapii. Są to najczęściej łagodne do umiarkowanych skutki żołądkowo-jelitowe, takie jak wzdęcia, biegunka lub dyskomfort w jamie brzusznej, i generalnie ich częstotliwość i intensywność zmniejszają się z czasem.
