Prandin 0.5mg, 1mg, 2mg Repaglinide Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Prandin 2mg i jak się go stosuje?
Prandin 1mg to lek na receptę stosowany w leczeniu objawów cukrzycy typu 2. Prandin może być stosowany samodzielnie lub z innymi lekami.
Prandin należy do klasy leków przeciwcukrzycowych, pochodnych Maglitinides.
Nie wiadomo, czy Prandin 1mg jest bezpieczny i skuteczny u dzieci.
Jakie są możliwe skutki uboczne Prandina?
Prandin może powodować poważne skutki uboczne, w tym:
- pokrzywka,
- trudności w oddychaniu,
- obrzęk twarzy, warg, języka lub gardła,
- silny ból w górnej części brzucha rozprzestrzeniający się na plecy,
- mdłości,
- wymioty,
- szybkie tętno,
- blada lub pożółkła skóra,
- ciemny kolor moczu,
- gorączka,
- dezorientacja,
- słabość,
- ból gardła,
- płonący w twoich oczach,
- ból skóry i
- następnie czerwona lub fioletowa wysypka skórna, która rozprzestrzenia się (szczególnie na twarzy lub górnej części ciała) i powoduje powstawanie pęcherzy i złuszczanie
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Prandina to:
- niski poziom cukru we krwi,
- mdłości,
- biegunka,
- ból głowy,
- ból pleców,
- ból stawów i
- objawy przeziębienia (zatkany nos, kichanie, ból gardła)
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Prandina. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
PRANDIN (repaglinid) jest doustnym lekiem obniżającym poziom glukozy we krwi z klasy glinidów. Repaglinid, kwas S(+)2-etoksy-4(2((3-metylo-1-(2-(1-piperydynylo)fenylo)-butylo)amino)-2-oksoetylo)benzoesowy, jest chemicznie niezwiązany z doustną insuliną sulfonylomocznikową sekretagogów.
Strukturalna formuła repaglinidu
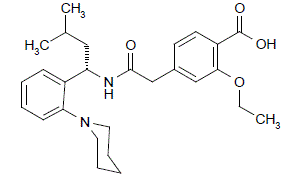
Repaglinid jest proszkiem o barwie od białej do białawej o wzorze cząsteczkowym C27H36N2O4 i masie cząsteczkowej 452,6. Tabletki PRANDIN zawierają 0,5 mg, 1 mg lub 2 mg repaglinidu. Dodatkowo każda tabletka zawiera następujące składniki nieaktywne: wodorofosforan wapnia (bezwodny), celulozę mikrokrystaliczną, skrobię kukurydzianą, polakrylinę potasową, powidon, glicerol (85%), stearynian magnezu, megluminę i poloksamer. Tabletki 1 mg i 2 mg zawierają tlenki żelaza (odpowiednio żółty i czerwony) jako barwniki.
WSKAZANIA
PRANDIN jest wskazany jako dodatek do diety i ćwiczeń fizycznych w celu poprawy kontroli glikemii u osób dorosłych z cukrzycą typu 2.
Ograniczenie użytkowania
Preparatu PRANDIN nie należy stosować u pacjentów z cukrzycą typu 1 ani w leczeniu cukrzycowej kwasicy ketonowej.
DAWKOWANIE I SPOSÓB PODAWANIA
Zalecane dawkowanie i administracja
Zalecana dawka początkowa dla pacjentów z HbA1c poniżej 8% wynosi 0,5 mg doustnie przed każdym posiłkiem. W przypadku pacjentów, u których HbA1c wynosi 8% lub więcej, dawka początkowa wynosi 1 lub 2 mg doustnie przed każdym posiłkiem.
Zalecany zakres dawek wynosi od 0,5 mg do 4 mg przed posiłkami, przy maksymalnej dawce dobowej 16 mg. Dawkę pacjenta należy podwoić do 4 mg z każdym posiłkiem, aż do uzyskania zadowalającej kontroli glikemii. Po każdym dostosowaniu dawki powinien upłynąć co najmniej tydzień, aby ocenić odpowiedź.
Należy poinstruować pacjentów, aby przyjmowali PRANDIN w ciągu 30 minut przed posiłkiem. PRANDIN 2 mg można podawać 2, 3 lub 4 razy dziennie w odpowiedzi na zmiany w diecie pacjenta.
pacjentów, którzy pomijają posiłki, należy poinstruować pacjentów, aby pominęli zaplanowaną dawkę PRANDIN 1 mg w celu zmniejszenia ryzyka hipoglikemii. U pacjentów, u których występuje hipoglikemia, należy zmniejszyć dawkę preparatu PRANDIN 1 mg [patrz OSTRZEŻENIA I ŚRODKI ].
Pacjenci z ciężką niewydolnością nerek
U pacjentów z ciężką niewydolnością nerek (CrCl = 20 do 40 ml/min) należy podawać PRANDIN 0,5 mg doustnie przed każdym posiłkiem. W razie potrzeby stopniowo miareczkować dawkę, aby uzyskać kontrolę glikemii.
Modyfikacje dawki w przypadku interakcji leków
Zaleca się dostosowanie dawkowania u pacjentów przyjmujących jednocześnie silne inhibitory CYP3A4 lub CYP2C8 lub silne induktory CYP3A4 lub CYP2C8 [patrz INTERAKCJE Z LEKAMI , FARMAKOLOGIA KLINICZNA ].
Jednoczesne stosowanie z gemfibrozylem jest przeciwwskazane [patrz PRZECIWWSKAZANIA ].
Należy unikać jednoczesnego stosowania preparatu PRANDIN 2 mg z klopidogrelem. Jeśli nie można uniknąć jednoczesnego stosowania produktu PRANDIN należy rozpocząć od 0,5 mg przed każdym posiłkiem i nie przekraczać całkowitej dawki dobowej 4 mg [patrz INTERAKCJE Z LEKAMI , FARMAKOLOGIA KLINICZNA ].
Nie należy przekraczać całkowitej dawki dobowej 6 mg preparatu PRANDIN 2 mg u pacjentów otrzymujących cyklosporynę [patrz INTERAKCJE Z LEKAMI , FARMAKOLOGIA KLINICZNA ].
JAK DOSTARCZONE
Formy dawkowania i mocne strony
- Tabletki 1 mg (żółte, okrągłe, obustronnie wypukłe tabletki z wytłoczonym napisem „745” po jednej stronie i „C” po drugiej stronie)
- Tabletki 2 mg (różowe, okrągłe, obustronnie wypukłe tabletki z wytłoczonym „747” po jednej stronie i „C” po drugiej stronie)
Tabletki PRANDIN (repaglinid), 1 mg , są dostarczane w postaci żółtych, okrągłych, obustronnie wypukłych tabletek z wytłoczonym napisem „745” po jednej stronie i „C” po drugiej stronie. Są dostępne w następujący sposób:
Butelki 100 NDC 60846-882-01
Prandin (repaglinid) tabletki, 2 mg , są dostarczane w postaci różowych, okrągłych, obustronnie wypukłych tabletek z wytłoczonym napisem „747” po jednej stronie i „C” po drugiej stronie. Są dostępne w następujący sposób:
Butelki 100 NDC 60846-884-01
Przechowywać w temperaturze 20° do 25°C (68° do 77°F) [patrz Kontrolowana temperatura pokojowa USP]. Chronić przed wilgocią. Trzymaj butelki szczelnie zamknięte.
Dozować w szczelnych pojemnikach z zamknięciami bezpieczeństwa.
Dystrybutor: Amneal Specialty, oddział Amneal Pharmaceuticals LLC Bridgewater, NJ 08807. Aktualizacja: marzec 2019 r.
SKUTKI UBOCZNE
innym miejscu na etykiecie opisano również następującą poważną reakcję niepożądaną:
Hipoglikemia [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne są prowadzone według bardzo różnych schematów, częstość występowania działań niepożądanych zgłoszonych w jednym badaniu klinicznym może nie być łatwa do porównania z częstością zgłaszaną w innym badaniu klinicznym i może nie odzwierciedlać częstości obserwowanych w praktyce klinicznej.
PRANDIN 1 mg podano 2931 osobom podczas badań klinicznych. Około 1500 osób z cukrzycą typu 2 było leczonych przez co najmniej 3 miesiące, 1000 przez co najmniej 6 miesięcy i 800 przez co najmniej 1 rok. Większość z tych osób (1228) otrzymywała PRANDIN w jednym z pięciu rocznych, aktywnie kontrolowanych badań. W ciągu jednego roku 13% pacjentów PRANDIN w dawce 1 mg przerwało leczenie z powodu działań niepożądanych. Najczęstszymi działaniami niepożądanymi prowadzącymi do odstawienia były hiperglikemia, hipoglikemia i związane z nimi objawy.
Tabeli 1 wymieniono częste działania niepożądane u pacjentów PRANDIN w porównaniu z placebo w badaniach trwających od 12 do 24 tygodni.
Hipoglikemia
W badaniach klinicznych z preparatem PRANDIN 1 mg hipoglikemia jest najczęściej obserwowanym działaniem niepożądanym. Łagodna lub umiarkowana hipoglikemia wystąpiła u 31% pacjentów leczonych PRANDIN 1 mg i 7% pacjentów otrzymujących placebo [patrz OSTRZEŻENIA I ŚRODKI ].
Hipoglikemię zgłoszono u 16% z 1228 pacjentów PRANDIN, 20% z 417 pacjentów z gliburydem i 19% z 81 pacjentów z glipizydem w rocznych kontrolowanych badaniach. Spośród leczonych preparatem PRANDIN pacjentów z objawową hipoglikemią żaden nie rozwinął śpiączki ani nie wymagał hospitalizacji.
W 24-tygodniowym badaniu kontrolowanym placebo pacjenci, którzy nie byli wcześniej leczeni doustnymi środkami hipoglikemizującymi, oraz pacjenci z HbA1c poniżej 8% na początku badania mieli większą częstość hipoglikemii.
Przybranie na wadze
Nie zaobserwowano średniego przyrostu masy ciała, gdy pacjenci wcześniej leczeni doustnymi środkami hipoglikemizującymi zostali przestawieni na PRANDIN. Średni przyrost masy ciała u pacjentów leczonych PRANDIN 0,5 mg i nieleczonych wcześniej lekami pochodnymi sulfonylomocznika wyniósł 3,3%.
Zdarzenia sercowo-naczyniowe
Częstość występowania poważnych sercowo-naczyniowych zdarzeń niepożądanych, w tym niedokrwienia, była wyższa dla PRANDIN (51/1228 lub 4%) niż dla leków sulfonylomocznikowych (13/498 lub 3%) w kontrolowanych porównawczych badaniach klinicznych.
Siedem kontrolowanych badań klinicznych obejmowało terapię skojarzoną PRANDIN z insuliną NPH (n=431), same preparaty insuliny (n=388) lub inne połączenia (sulfonylomocznik plus insulina NPH lub PRANDIN 1 mg plus metformina) (n=120). Wystąpiło sześć poważnych zdarzeń niepożądanych niedokrwienia mięśnia sercowego u pacjentów leczonych PRANDIN 0,5 mg plus insulina NPH z dwóch badań i jedno zdarzenie u pacjentów stosujących same preparaty insuliny z innego badania [patrz OSTRZEŻENIA I ŚRODKI ].
Terapia skojarzona z tiazolidynodionami
Hipoglikemia
Podczas 24-tygodniowych badań klinicznych leczenia skojarzonego PRANDIN-rozyglitazonem lub PRANDIN-pioglitazonem (łącznie 250 pacjentów w terapii skojarzonej) hipoglikemia (stężenie glukozy we krwi
Obrzęki obwodowe i niewydolność serca
Obrzęki obwodowe zgłoszono u 12 z 250 (4,8%) pacjentów leczonych preparatem PRANDIN i tiazolidynodionem w leczeniu skojarzonym oraz u 3 ze 124 (2,4%) pacjentów leczonych tiazolidynodionem w monoterapii. U 2 z 250 pacjentów (0,8%) leczonych preparatem PRANDIN tiazolidynodion zgłaszano przypadki obrzęku z zastoinową niewydolnością serca. Obaj pacjenci mieli wcześniej chorobę wieńcową i wyzdrowieli po leczeniu lekami moczopędnymi. Nie zgłoszono porównywalnych przypadków w grupach leczonych monoterapią.
Przybranie na wadze
Średnie przyrosty masy ciała związane z leczeniem skojarzonym, PRANDIN i pioglitazonem wynosiły odpowiednio 5,5 kg, 0,3 kg i 2,0 kg. Średnie przyrosty masy ciała związane z leczeniem skojarzonym, PRANDIN i rozyglitazonem wynosiły odpowiednio 4,5 kg, 1,3 kg i 3,3 kg.
Rzadkie zdarzenia niepożądane (
Mniej częste zdarzenia niepożądane kliniczne lub laboratoryjne obserwowane w badaniach klinicznych obejmowały zwiększenie aktywności enzymów wątrobowych, małopłytkowość, leukopenię i reakcje rzekomoanafilaktyczne.
Doświadczenie postmarketingowe
Następujące dodatkowe działania niepożądane zostały zidentyfikowane podczas stosowania produktu PRANDIN po zatwierdzeniu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, generalnie nie jest możliwe wiarygodne oszacowanie ich częstości lub związku przyczynowego z ekspozycją na lek.
- Łysienie
- Niedokrwistość hemolityczna
- Zapalenie trzustki
- Zespół Stevensa-Johnsona
- Ciężkie zaburzenia czynności wątroby, w tym żółtaczka i zapalenie wątroby
INTERAKCJE Z LEKAMI
Klinicznie ważne interakcje leków z PRANDIN
Tabela 3 zawiera listę leków z klinicznie istotnymi interakcjami lekowymi przy jednoczesnym podawaniu z preparatem PRANDIN 1 mg oraz instrukcje dotyczące ich zapobiegania lub postępowania.
OSTRZEŻENIA
Zawarte jako część "ŚRODKI OSTROŻNOŚCI" Sekcja
ŚRODKI OSTROŻNOŚCI
Hipoglikemia
Wszystkie glinidy, w tym PRANDIN 0,5 mg, mogą powodować hipoglikemię [patrz DZIAŁANIA NIEPOŻĄDANE ]. Ciężka hipoglikemia może powodować drgawki, może zagrażać życiu lub powodować śmierć. Hipoglikemia może zaburzać zdolność koncentracji i czas reakcji; może to narazić osobę i inne osoby na ryzyko w sytuacjach, w których te umiejętności są ważne (np. prowadzenie pojazdów lub obsługiwanie innych maszyn).
Hipoglikemia może wystąpić nagle, a objawy mogą się różnić u każdej osoby i zmieniać się w czasie u tej samej osoby. Świadomość objawowa hipoglikemii może być mniej wyraźna u pacjentów z długotrwałą cukrzycą, u pacjentów z chorobą nerwów cukrzycowych, u pacjentów stosujących leki blokujące współczulny układ nerwowy (np. beta-adrenolityki) [patrz INTERAKCJE Z LEKAMI ] lub u pacjentów, u których występuje nawracająca hipoglikemia.
Czynniki, które mogą zwiększać ryzyko hipoglikemii, obejmują zmiany wzorca posiłków (np. zawartości makroskładników), zmiany poziomu aktywności fizycznej, zmiany w przyjmowanych jednocześnie lekach [patrz INTERAKCJE Z LEKAMI ] i jednoczesne stosowanie z innymi lekami przeciwcukrzycowymi. Pacjenci z zaburzeniami czynności nerek lub wątroby mogą być bardziej narażeni na hipoglikemię [patrz Używaj w określonych populacjach ].
Pacjenci powinni podawać PRANDIN 0,5 mg przed posiłkami i zostać poinstruowani, aby pominąć dawkę PRANDIN w przypadku pominięcia posiłku. U pacjentów, u których występuje hipoglikemia, należy zmniejszyć dawkę preparatu PRANDIN [patrz DAWKOWANIE I SPOSÓB PODAWANIA ]. Pacjenci i opiekunowie muszą być przeszkoleni w zakresie rozpoznawania i leczenia hipoglikemii. Samokontrola stężenia glukozy we krwi odgrywa zasadniczą rolę w zapobieganiu i leczeniu hipoglikemii. U pacjentów z podwyższonym ryzykiem hipoglikemii oraz pacjentów z obniżoną świadomością objawów hipoglikemii zaleca się częstsze kontrolowanie stężenia glukozy we krwi.
Poważne działania niepożądane ze strony układu krążenia podczas jednoczesnego stosowania z insuliną NPH
siedmiu kontrolowanych badaniach wystąpiło sześć poważnych zdarzeń niepożądanych niedokrwienia mięśnia sercowego u pacjentów leczonych PRANDIN 0,5 mg plus insulina NPH z dwóch badań i jedno zdarzenie u pacjentów stosujących same preparaty insuliny z innego badania [patrz DZIAŁANIA NIEPOŻĄDANE ]. PANDIN nie jest wskazany do stosowania w połączeniu z insuliną NPH.
Wyniki makronaczyniowe
Nie przeprowadzono badań klinicznych, które dostarczyłyby rozstrzygających dowodów na zmniejszenie ryzyka makronaczyniowego podczas stosowania PRANDIN.

Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
104-tygodniowym badaniu rakotwórczości u szczurów przy dawkach do 120 mg/kg/dobę, co stanowi około 60-krotność ekspozycji klinicznej w przeliczeniu na mg/m2, częstość występowania łagodnych gruczolaków tarczycy i wątroby była zwiększona u samców szczurów. Nie znaleziono dowodów na rakotwórczość u samic szczurów. Większa częstość występowania guzów tarczycy i wątroby u samców szczurów nie była obserwowana przy niższych dawkach odpowiednio 30 mg/kg/dobę i 60 mg/kg/dobę (które są odpowiednio ponad 15 i 30-krotnością ekspozycji klinicznej na mg/m2 pc. podstawa). W 104-tygodniowym badaniu rakotwórczości u myszy przy dawkach do 500 mg/kg/dobę nie znaleziono dowodów na rakotwórczość u myszy (co stanowi około 125-krotność ekspozycji klinicznej w przeliczeniu na mg/m2).
Repaglinid nie był genotoksyczny w szeregu badań in vivo i in vitro: mutageneza bakteryjna (test Amesa), test postępującej mutacji komórek in vitro w komórkach V79 (HGPRT), test aberracji chromosomowych in vitro w ludzkich limfocytach, nieplanowa i replikacyjna synteza DNA w wątrobie szczura oraz w testach mikrojądrowych in vivo na myszach i szczurach.
W badaniu płodności szczurów repaglinid podawano samcom i samicom szczurów w dawkach odpowiednio do 300 i 80 mg/kg/dobę. Nie zaobserwowano niekorzystnego wpływu na płodność (który przekracza 40-krotność ekspozycji klinicznej w przeliczeniu na mg/m2).
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
Ograniczone dane dotyczące stosowania preparatu PRANDIN i repaglinidu u kobiet w ciąży są niewystarczające, aby poinformować o związanym z lekiem ryzyku wystąpienia poważnych wad wrodzonych lub poronienia. Istnieje ryzyko dla matki i płodu związane ze źle kontrolowaną cukrzycą w ciąży [patrz Rozważania kliniczne ].
badaniach na zwierzętach (szczury i króliki) nie wykazano działania teratogennego repaglidyny. U samic szczurów narażonych na duże dawki w ostatnim okresie ciąży obserwowano embriotoksyczność, nieprawidłowy rozwój kończyn u płodu szczura.
Szacunkowe ryzyko wystąpienia poważnych wad wrodzonych wynosi od 6% do 10% u kobiet z cukrzycą przedciążową z HbA1c >7 i zgłoszono, że wynosi nawet 20% do 25% u kobiet z HbA1c >10. Szacowane podstawowe ryzyko poronienia dla wskazanej populacji jest nieznane. W ogólnej populacji Stanów Zjednoczonych szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2% do 4% i 15% do 20%.
Rozważania kliniczne
Związane z chorobą ryzyko dla matki i/lub zarodka/płodu
Źle kontrolowana cukrzyca w ciąży zwiększa ryzyko wystąpienia cukrzycowej kwasicy ketonowej, stanu przedrzucawkowego, samoistnych poronień, porodów przedwczesnych, martwych porodów i powikłań porodowych. Źle kontrolowana cukrzyca zwiększa ryzyko wystąpienia u płodu poważnych wad wrodzonych, martwych urodzeń i zachorowalności na makrosomię.
Dane
Dane ludzkie
Brak odpowiednich danych dotyczących ryzyka rozwoju związanego ze stosowaniem preparatu PRANDIN 2 mg u kobiet w ciąży.
Dane zwierząt
Repaglinid nie wykazywał działania teratogennego u szczurów i królików w dawkach 40-krotności (szczury) i około 0,8-krotności (królik) ekspozycji klinicznej (w przeliczeniu na mg/m2) podczas całej ciąży. Potomstwo samic szczurów narażone na 15-krotność ekspozycji klinicznej na repaglinid w przeliczeniu na mg/m2 w dniach od 17 do 22 ciąży i podczas laktacji rozwinęło nieteratogenne deformacje szkieletu polegające na skróceniu, pogrubieniu i zgięciu kości ramiennej w okresie poporodowym. Efekt ten nie był obserwowany przy dawkach do 2,5-krotności ekspozycji klinicznej (w przeliczeniu na mg/m2) w dniach od 1 do 22 ciąży lub przy większych dawkach podawanych w dniach od 1 do 16 ciąży.
Laktacja
Podsumowanie ryzyka
Nie ma informacji dotyczących obecności 0,5 mg PRANDIN w mleku ludzkim, wpływu na niemowlę karmione piersią lub wpływu na produkcję mleka. Repaglinid wykryto w mleku szczurów, chociaż ze względu na specyficzne dla gatunku różnice w fizjologii laktacji dane na zwierzętach mogą nie przewidywać w sposób wiarygodny poziomów leku w mleku ludzkim. Należy wziąć pod uwagę korzyści rozwojowe i zdrowotne wynikające z karmienia piersią, a także kliniczne zapotrzebowanie matki na PRANDIN i wszelkie potencjalne niepożądane skutki działania PRANDIN na karmione piersią niemowlę lub wynikające z tego schorzenia matki.
Rozważania kliniczne
Chociaż nie wiadomo, czy repaglinid przenika do mleka ludzkiego, wiadomo, że niektóre środki doustne są wydalane tą drogą. Ze względu na możliwość wystąpienia hipoglikemii u niemowląt karmionych piersią oraz ze względu na wpływ na karmione zwierzęta, należy podjąć decyzję, czy preparat PRANDIN należy przerwać u matek karmiących piersią, czy też matki powinny przerwać karmienie piersią. W przypadku przerwania leczenia preparatem PRANDIN, a sama dieta jest niewystarczająca do kontrolowania stężenia glukozy we krwi, należy rozważyć insulinoterapię.
Dane
W badaniach rozrodczości szczurów wykryto mierzalne poziomy repaglinidu w mleku matek, au młodych zaobserwowano obniżone stężenie glukozy we krwi. Badania krzyżowej opieki zastępczej wykazały, że zmiany szkieletowe [zob Ciąża ] można wywołać u szczeniąt kontrolnych karmionych przez matki leczone, chociaż zdarzało się to w mniejszym stopniu niż u szczeniąt leczonych in utero.
Zastosowanie pediatryczne
Nie ustalono bezpieczeństwa i skuteczności u pacjentów pediatrycznych.
Zastosowanie geriatryczne
badaniach klinicznych trwających 24 tygodnie lub dłużej, 415 pacjentów było w wieku powyżej 65 lat i żaden z pacjentów nie był w wieku powyżej 75 lat. W rocznych badaniach z aktywną kontrolą nie zaobserwowano różnic w skuteczności lub działaniach niepożądanych między tymi osobami a osobami w wieku poniżej 65 lat. Nie stwierdzono zwiększenia częstości ani nasilenia hipoglikemii u osób starszych, ale większa wrażliwość niektórych osób starszych na Nie można wykluczyć terapii PRANDIN 0,5 mg.
Zaburzenia czynności nerek
Badania farmakokinetyczne repaglinidu przeprowadzono u pacjentów z łagodnymi do umiarkowanych zaburzeniami czynności nerek (CrCl = 40 do 80 ml/min) i ciężkimi zaburzeniami czynności nerek (CrCl = 20 do 40 ml/min). Dostosowanie dawki początkowej nie jest konieczne u pacjentów z łagodnymi lub umiarkowanymi zaburzeniami czynności nerek. Jednak pacjenci z ciężkimi zaburzeniami czynności nerek powinni rozpocząć leczenie preparatem PRANDIN od dawki 0,5 mg i ostrożnie dostosowywać dawkę [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Nie przeprowadzono badań u pacjentów z klirensem kreatyniny poniżej 20 ml/min ani u pacjentów z niewydolnością nerek wymagającą hemodializy.
Niewydolność wątroby
Badanie pojedynczej dawki przeprowadzono u 12 pacjentów z przewlekłą chorobą wątroby. U pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby stężenia w surowicy były wyższe i bardziej przedłużone. Dlatego PRANDIN 0,5 mg należy stosować ostrożnie u pacjentów z zaburzeniami czynności wątroby. W celu pełnej oceny odpowiedzi mogą być konieczne dłuższe odstępy między dostosowaniami dawki.
PRZEDAWKOWAĆ
Mogą wystąpić ciężkie reakcje hipoglikemiczne ze śpiączką, drgawkami lub innymi zaburzeniami neurologicznymi, które stanowią nagłe przypadki wymagające natychmiastowej hospitalizacji. Objawy hipoglikemii bez utraty przytomności lub objawów neurologicznych należy leczyć agresywnie, podając doustnie glukozę i dostosowując dawkowanie leku i (lub) schemat posiłków. Ścisłe monitorowanie może być kontynuowane, dopóki lekarz nie upewni się, że pacjentowi nie grozi żadne niebezpieczeństwo. Pacjentów należy ściśle monitorować przez co najmniej 24 do 48 godzin, ponieważ hipoglikemia może nawrócić po widocznym wyzdrowieniu klinicznym. Nie ma dowodów na to, że PRANDIN można dializować za pomocą hemodializy.
PRZECIWWSKAZANIA
PRANDIN jest przeciwwskazany u pacjentów z:
- Jednoczesne stosowanie gemfibrozylu [patrz INTERAKCJE Z LEKAMI ]
- Znana nadwrażliwość na repaglinid lub jakiekolwiek składniki nieaktywne
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Repaglinid obniża poziom glukozy we krwi poprzez stymulację uwalniania insuliny z trzustki. To działanie jest zależne od funkcjonowania komórek beta (β) w wyspach trzustkowych. Uwalnianie insuliny jest zależne od glukozy i zmniejsza się przy niskich stężeniach glukozy.
Repaglinid zamyka zależne od ATP kanały potasowe w błonie komórek β, wiążąc się w charakterystycznych miejscach. Ta blokada kanału potasowego depolaryzuje komórkę β, co prowadzi do otwarcia kanałów wapniowych. Wynikający z tego zwiększony napływ wapnia indukuje wydzielanie insuliny. Mechanizm kanału jonowego jest wysoce selektywny tkankowo z niskim powinowactwem do serca i mięśni szkieletowych.
Farmakodynamika
138 pacjentów z cukrzycą typu 2 przeprowadzono czterotygodniowe, podwójnie zaślepione, kontrolowane placebo badanie dawka-odpowiedź, stosując dawki w zakresie od 0,25 (niezatwierdzona dawka) do 4 mg przyjmowanych z każdym z trzech posiłków. Terapia PRANDIN spowodowała proporcjonalne do dawki obniżenie stężenia glukozy w całym zakresie dawek. Poziomy insuliny w osoczu wzrosły po posiłkach i powróciły do wartości wyjściowych przed następnym posiłkiem. Większość efektu obniżenia stężenia glukozy we krwi na czczo została wykazana w ciągu 1 do 2 tygodni.
badaniu z podwójnie ślepą próbą, kontrolowanym placebo, trwającym 3 miesiące miareczkowania dawki, dawki PRANDIN 0,5 mg lub placebo dla każdego pacjenta były zwiększane co tydzień z 0,25 mg (niezatwierdzona dawka) do 0,5, 1 i 2 mg, do maksymalnej 4 mg, aż do osiągnięcia poziomu glukozy na czczo (FPG)
Dawkowanie produktu PRANDIN 0,5 mg w stosunku do uwalniania insuliny podczas posiłku badano w trzech badaniach obejmujących 58 pacjentów. Kontrola glikemii była utrzymywana w okresie, w którym posiłki i schematy dawkowania były zróżnicowane (2, 3 lub 4 posiłki dziennie; przed posiłkami x 2, 3 lub 4) w porównaniu z okresem 3 regularnych posiłków i 3 dawek dziennie ( przed posiłkami x 3). Efekt obniżenia stężenia glukozy we krwi nie różnił się, gdy PRANDIN 0,5 mg podawano na początku posiłku, 15 minut przed lub 30 minut przed posiłkiem.
Farmakokinetyka
Parametry farmakokinetyczne repaglinidu uzyskane w badaniu krzyżowym z pojedynczą dawką u zdrowych osób oraz w badaniu proporcjonalności dawki wielokrotnej dawki (0,5, 1, 2 i 4 mg) u pacjentów z cukrzycą typu 2 podsumowano w tabelach 5 i 6. Dane te wskazują, że repaglinid nie kumulował się w surowicy. Klirens doustnego repaglinidu nie zmienił się w zakresie dawek od 0,5 do 4 mg, co wskazuje na liniową zależność między dawką a stężeniem leku w osoczu.
Wchłanianie
Po podaniu doustnym repaglinid jest całkowicie wchłaniany z przewodu pokarmowego. Po podaniu pojedynczej i wielokrotnej dawki doustnej zdrowym ochotnikom lub pacjentom, maksymalne stężenie leku w osoczu (Cmax) występuje w ciągu 1 godziny (Tmax). Repaglinid jest eliminowany z krwiobiegu z okresem półtrwania około 1 godziny. Średnia bezwzględna biodostępność wynosi 56%. Gdy repaglinid podawano z pokarmem, średni Tmax nie uległ zmianie, ale średnie Cmax i AUC (powierzchnia pod krzywą czas/stężenie w osoczu) zmniejszyły się odpowiednio o 20% i 12,4%.
Dystrybucja
Po podaniu dożylnym (IV) zdrowym ochotnikom objętość dystrybucji w stanie stacjonarnym (Vss) wynosiła 31 l, a całkowity klirens (CL) wynosił 38 l/h. Wiązanie z białkami i wiązanie z albuminą surowicy ludzkiej było większe niż 98%.
Metabolizm i eliminacja
Repaglinid jest całkowicie metabolizowany przez biotransformację oksydacyjną i bezpośrednie sprzęganie z kwasem glukuronowym po podaniu dożylnym lub doustnym. Główne metabolity to utleniony kwas dikarboksylowy (M2), amina aromatyczna (M1) i acyloglukuronid (M7). Wykazano, że układ enzymatyczny cytochromu P-450, w szczególności 2C8 i 3A4, bierze udział w N-dealkilacji repaglinidu do M2 i dalszym utlenianiu do M1. Metabolity nie przyczyniają się do obniżania poziomu glukozy przez repaglinid. W ciągu 96 godzin po podaniu pojedynczej dawki doustnej repaglinidu znakowanego 14C około 90% radioznacznika odzyskano w kale, a około 8% w moczu. Tylko 0,1% dawki jest wydalane z moczem jako związek macierzysty. Główny metabolit (M2) stanowił 60% podanej dawki. Mniej niż 2% leku macierzystego odzyskano w kale. Repaglinid wydaje się być substratem dla aktywnego transportera wychwytu wątrobowego (białko OATP1B1 transportujące aniony organiczne).
Zmienność ekspozycji
AUC repaglinidu po wielokrotnych dawkach od 0,25 do 4 mg z każdym posiłkiem zmienia się w szerokim zakresie. Wewnątrzosobnicze i międzyosobnicze współczynniki zmienności wynosiły odpowiednio 36% i 69%. AUC w zakresie dawek terapeutycznych obejmowało 69 do 1005 ng/ml*h, ale ekspozycja AUC do 5417 ng/ml*h została osiągnięta w badaniach zwiększania dawki bez widocznych działań niepożądanych.
Określone populacje
Geriatryczny
Zdrowi ochotnicy byli leczeni schematem 2 mg PRANDIN 0,5 mg przed każdym z 3 posiłków. Nie stwierdzono istotnych różnic w farmakokinetyce repaglinidu między grupą pacjentów Używaj w określonych populacjach ].
Płeć
Porównanie farmakokinetyki u mężczyzn i kobiet wykazało, że AUC w zakresie dawek od 0,5 mg do 4 mg jest o 15% do 70% większe u kobiet z cukrzycą typu 2. Różnica ta nie była odzwierciedlona w częstości epizodów hipoglikemii (mężczyźni: 16%; kobiety: 17%) lub innych zdarzeń niepożądanych.
Wyścig
Nie przeprowadzono badań farmakokinetycznych oceniających wpływ rasy, ale w rocznym badaniu w Stanach Zjednoczonych u pacjentów z cukrzycą typu 2 efekt obniżenia stężenia glukozy we krwi był porównywalny u osób rasy kaukaskiej (n=297) i Afroamerykanów (n= 33). W amerykańskim badaniu dawka-odpowiedź nie stwierdzono wyraźnej różnicy w ekspozycji (AUC) między osobami rasy kaukaskiej (n=74) a Latynosami (n=33).
Zaburzenia czynności nerek
Farmakokinetykę repaglinidu po podaniu pojedynczej dawki i w stanie stacjonarnym porównano między pacjentami z cukrzycą typu 2 i prawidłową czynnością nerek (CrCl > 80 ml/min), łagodnymi do umiarkowanych zaburzeniami czynności nerek (CrCl = 40 do 80 ml/min) i ciężkimi zaburzenia czynności nerek (CrCl = 20 do 40 ml/min). Zarówno AUC, jak i Cmax repaglinidu były podobne u pacjentów z prawidłową i łagodną lub umiarkowaną niewydolnością nerek (odpowiednio średnie 56,7 ng/ml*h vs 57,2 ng/ml*h i 37,5 ng/ml vs 37,7 ng/ml). z ciężkimi zaburzeniami czynności nerek miał podwyższone średnie wartości AUC i Cmax (odpowiednio 98,0 ng/ml*h i 50,7 ng/ml), ale badanie to wykazało jedynie słabą korelację między poziomami repaglinidu a klirensem kreatyniny.
Niewydolność wątroby
Otwarte badanie z pojedynczą dawką przeprowadzono z udziałem 12 zdrowych osób i 12 pacjentów z przewlekłą chorobą wątroby (CLD) sklasyfikowaną według skali Child-Pugh i klirensu kofeiny. Pacjenci z umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby mieli wyższe i dłuższe stężenia w surowicy zarówno całkowitego, jak i niezwiązanego repaglinidu niż osoby zdrowe (AUCzdrowy: 91,6 ng/ml*godz; pacjenci z AUCCLD: 368,9 ng/ml*godz; Cmax, zdrowy: 46,7 ng/ml; Cmax, pacjenci z CLD: 105,4 ng/ml). AUC było statystycznie skorelowane z klirensem kofeiny. Nie zaobserwowano różnic w profilach glukozy między grupami pacjentów.
Interakcje między lekami
Badania interakcji leków przeprowadzone na zdrowych ochotnikach wykazały, że PRANDIN 0,5 mg nie miał klinicznie istotnego wpływu na właściwości farmakokinetyczne digoksyny, teofiliny lub warfaryny. Jednoczesne podawanie cymetydyny z PRANDIN 1 mg nie zmieniało znacząco wchłaniania i wydalania repaglinidu.
Dodatkowo u zdrowych ochotników badano następujące leki, którym podawano jednocześnie PRANDIN.
Studia kliniczne
Próby monoterapii
Badanie z podwójnie ślepą próbą, kontrolowane placebo przeprowadzono u 362 pacjentów leczonych przez 24 tygodnie. HbA1c dla grup leczonych preparatem PRANDIN (łącznie grupy 1 i 4 mg) pod koniec badania była obniżona w porównaniu z grupą otrzymującą placebo u pacjentów nieleczonych wcześniej oraz u pacjentów wcześniej leczonych doustnymi środkami hipoglikemizującymi o 2,1% i 1,7%, odpowiednio. W tym badaniu z ustaloną dawką pacjenci, którzy nie byli wcześniej leczeni doustnymi środkami hipoglikemizującymi, oraz pacjenci z wyjściowym HbA1c poniżej 8% wykazywali większe obniżenie stężenia glukozy we krwi.
Próby kombinowane
PRANDIN w połączeniu z metforminą
PRANDIN badano w skojarzeniu z metforminą u 83 pacjentów, u których nie uzyskano zadowalającej kontroli za pomocą ćwiczeń, diety i samej metforminy. Dawkę PRANDIN 2 mg miareczkowano przez 4 do 8 tygodni, po czym następował 3-miesięczny okres podtrzymywania. Terapia skojarzona z PRANDIN 1 mg i metforminą spowodowała statystycznie istotną poprawę HbA1c i glikemii na czczo (FPG) w porównaniu z PRANDIN 2 mg lub monoterapią metforminą (Tabela 8). W tym badaniu, w którym dawkowanie metforminy było utrzymywane na stałym poziomie, terapia skojarzona PRANDIN i metforminą wykazała efekty oszczędzania dawki w odniesieniu do PRANDIN. Poprawę HbA1c i FPG w grupie skojarzonej osiągnięto przy niższej dziennej dawce PRANDIN 0,5 mg niż w grupie monoterapii PRANDIN (Tabela 8).
PRANDIN 1 mg w połączeniu z pioglitazonem
Schemat terapii skojarzonej PRANDIN i pioglitazonem (N=123) porównano z samym PRANDIN (N=61) i samym pioglitazonem (N=62) w 24-tygodniowym badaniu obejmującym 246 pacjentów wcześniej leczonych sulfonylomocznikiem lub metforminą w monoterapii (HbA1c > 7,0%). Dawkę PRANDIN 1 mg miareczkowano w ciągu pierwszych 12 tygodni, po czym następował 12-tygodniowy okres podtrzymywania. Terapia skojarzona spowodowała statystycznie istotną poprawę HbA1c i FPG w porównaniu z monoterapią (ryc. 1). Zmiany w stosunku do wartości wyjściowych dla osób, które ukończyły leczenie w FPG (mg/dl) i HbA1c (%), odpowiednio: -39,8 mg/dl i -0,1% dla PRANDIN, -35,3 mg/dl i -0,1% dla pioglitazonu i -92,4 mg/ dL i -1,9% dla kombinacji. W tym badaniu, w którym dawka pioglitazonu była utrzymywana na stałym poziomie, grupa terapii skojarzonej wykazała efekty oszczędzania dawki w odniesieniu do PRANDIN (patrz Legenda Ryc. 1). Poprawę HbA1c i FPG w grupie skojarzonej osiągnięto przy niższej dziennej dawce PRANDIN niż w grupie monoterapii PRANDIN.
Rycina 1: PRANDIN w połączeniu z pioglitazonem: wartości HbA1c
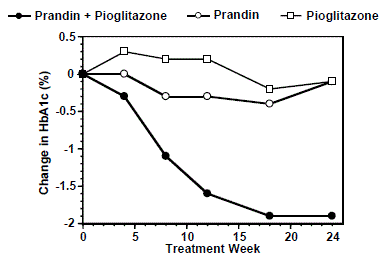
LEGENDA
Wartości HbA1c według tygodnia badania dla pacjentów, którzy ukończyli badanie (połączenie, N = 101; PRANDIN 1 mg, N = 35, pioglitazon, N = 26). Osoby z FPG powyżej 270 mg/dl zostały wycofane z badania.
Dawka pioglitazonu: ustalona na 30 mg/dzień; Mediana dawki końcowej PRANDIN 1 mg: 6 mg/dobę w przypadku leczenia skojarzonego i 10 mg/dobę w przypadku monoterapii.
PRANDIN w połączeniu z rozyglitazonem
Schemat terapii skojarzonej PRANDIN i rozyglitazonem porównano z monoterapią jednym z tych środków w 24-tygodniowym badaniu obejmującym 252 pacjentów wcześniej leczonych pochodną sulfonylomocznika lub metforminą (HbA1c > 7,0%). Terapia skojarzona spowodowała statystycznie istotną poprawę HbA1c i FPG w porównaniu z monoterapią (Tabela 9 poniżej). Efekty glikemiczne terapii skojarzonej oszczędzały dawkę w odniesieniu zarówno do całkowitej dziennej dawki PRANDIN 1 mg, jak i całkowitej dobowej dawki rozyglitazonu (patrz Tabela 9 Legenda). Poprawę HbA1c i FPG w grupie terapii skojarzonej uzyskano przy niższej dawce dobowej PRANDIN 1 mg i rozyglitazonu w porównaniu z odpowiednimi grupami monoterapii.
INFORMACJA O PACJENCIE
Hipoglikemia
Poinformuj pacjentów, że PRANDIN 2 mg może powodować hipoglikemię oraz poinstruuj pacjentów i ich opiekunów o procedurach samodzielnego leczenia, w tym monitorowaniu stężenia glukozy i leczeniu hipoglikemii. Poinformuj pacjentów, że ich zdolność koncentracji i reagowania może być osłabiona w wyniku hipoglikemii. U pacjentów z podwyższonym ryzykiem hipoglikemii i pacjentów z obniżoną świadomością objawów hipoglikemii zaleca się zwiększenie częstotliwości monitorowania stężenia glukozy we krwi [patrz OSTRZEŻENIA I ŚRODKI ].
Administracja
Należy poinstruować pacjentów, aby przyjmowali PRANDIN 0,5 mg w ciągu 30 minut przed posiłkiem. Poinstruuj pacjentów, aby pominęli dawkę PRANDIN w przypadku pominięcia posiłku [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Interakcje leków
Omów potencjalne interakcje leków z pacjentami i poinformuj ich o potencjalnych interakcjach lek-lek z PRANDIN [patrz INTERAKCJE Z LEKAMI ].
