Cardizem 30mg, 60mg, 90mg, 120mg, 180mg Diltiazem Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Cardizem 120mg i jak się go stosuje?
Cardizem to lek na receptę stosowany w leczeniu objawów bólu w klatce piersiowej (dławicy piersiowej), wysokiego ciśnienia krwi (nadciśnienia), a także niektórych zaburzeń rytmu serca, takich jak niebezpiecznie szybkie bicie serca (napadowy częstoskurcz nadkomorowy) i migotanie/trzepotanie przedsionków. Cardizem można stosować samodzielnie lub z innymi lekami.
Cardizem należy do klasy leków o nazwie Antidysrhythmics, IV; blokery kanału wapniowego; Blokery kanału wapniowego, niedihydropirydyna.
Jakie są możliwe skutki uboczne Cardizem 120mg?
Cardizem może powodować poważne skutki uboczne, w tym:
- ból w klatce piersiowej,
- wolne bicie serca,
- bicie serca lub trzepotanie w klatce piersiowej,
- zawroty,
- obrzęk,
- szybki przyrost masy ciała oraz
- uczucie zadyszki
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze działania niepożądane Cardizem to:
- obrzęk,
- zawroty głowy,
- słabość,
- ból głowy,
- nudności i
- wysypka
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Cardizem. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
CARDIZEM® (chlorowodorek diltiazemu) jest inhibitorem komórkowego napływu jonów wapnia (bloker wolnego kanału lub antagonista wapnia). Chemicznie chlorowodorek diltiazemu to 1,5-benzotiazepin-4(5H)-on, 3-(acetyloksy)-5-[2-(dimetyloamino)etylo]-2,3-dihydro-2-(4-metoksyfenylo)-, monochlorowodorek,(+)-cis-. Struktura chemiczna to:
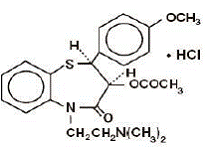
Chlorowodorek diltiazemu jest krystalicznym proszkiem o barwie od białej do prawie białej o gorzkim smaku. Jest rozpuszczalny w wodzie, metanolu i chloroformie. Ma masę cząsteczkową 450,98. Każda tabletka leku CARDIZEM 60 mg zawiera 30 mg, 60 mg, 90 mg lub 120 mg chlorowodorku diltiazemu.
Zawiera również: koloidalny dwutlenek krzemu, lak aluminiowy D&C Yellow #10, lak aluminiowy FD&C Blue #1 (30 mg i 90 mg), lak aluminiowy FD&C Yellow #6 (60 mg i 120 mg), hydroksypropylocelulozę, hypromelozę, laktozę, magnez stearynian, metyloparaben, celuloza mikrokrystaliczna i glikol polietylenowy.
Do podawania doustnego.
WSKAZANIA
CARDIZEM 120 mg jest wskazany w leczeniu przewlekłej stabilnej dusznicy bolesnej i dusznicy bolesnej spowodowanej skurczem tętnic wieńcowych.
DAWKOWANIE I SPOSÓB PODAWANIA
Wysiłkowa dusznica bolesna z powodu miażdżycowej choroby wieńcowej lub dusznica bolesna w spoczynku z powodu skurczu tętnicy wieńcowej
Dawkowanie należy dostosować do potrzeb każdego pacjenta. Zaczynając od 30 mg cztery razy na dobę, przed posiłkami i przed snem, dawkę należy zwiększać stopniowo (podawaną w dawkach podzielonych trzy lub cztery razy na dobę) w odstępach od 1 do 2 dni, aż do uzyskania optymalnej odpowiedzi. Chociaż poszczególni pacjenci mogą reagować na dowolny poziom dawkowania, średni optymalny zakres dawkowania wydaje się wynosić 180 do 360 mg/dzień. Brak dostępnych danych dotyczących wymagań dotyczących dawkowania u pacjentów z zaburzeniami czynności nerek lub wątroby. Jeśli lek musi być stosowany u takich pacjentów, miareczkowanie należy przeprowadzać ze szczególną ostrożnością.
Jednoczesne stosowanie z innymi środkami sercowo-naczyniowymi
Tabletki Cardizem należy połknąć w całości; tabletek nie należy dzielić, kruszyć ani żuć.
JAK DOSTARCZONE
CARDIZEM 30 mg tabletki są dostarczane w butelkach po 100 ( NDC 0187-0771-47) i 500 ( NDC 0187-0771-55). Każda jasnozielona, okrągła tabletka ma wygrawerowany napis MARION po jednej stronie i 1771 po drugiej.
CARDIZEM 60 mg tabletki z rowkiem są dostarczane w butelkach po 100 ( NDC 0187-0772-47). Każda jasnożółta, okrągła tabletka ma wygrawerowany napis MARION po jednej stronie i 1772 po drugiej.
CARDIZEM 90 mg tabletki z rowkiem są dostarczane w butelkach po 100 ( NDC 0187-0791-47). Każda zielona, podłużna tabletka ma wygrawerowany napis CARDIZEM po jednej stronie i 90 mg po drugiej.
CARDIZEM 120 mg tabletki z rowkiem są dostarczane w butelkach po 100 ( NDC 0187-0792-47). Każda jasnożółta tabletka w kształcie kapsułki ma wygrawerowany napis CARDIZEM po jednej stronie i 120 mg po drugiej.
Przechowywać w 25°C (77°); dozwolone wycieczki do 15-30°C (59-86°) [patrz Temperatura pokojowa kontrolowana przez USP ].
Unikaj nadmiernej wilgotności.
Dystrybutor: Valeant Pharmaceuticals North America LLC Bridgewater, NJ 08807 USA. Wyprodukowano w Kanadzie. Poprawiony. 11/14
SKUTKI UBOCZNE
W dotychczas przeprowadzonych badaniach poważne działania niepożądane były rzadkie, należy jednak pamiętać, że zwykle wykluczano pacjentów z zaburzeniami czynności komór i zaburzeniami przewodzenia w sercu.
W krajowych badaniach dławicowych kontrolowanych placebo, częstość występowania działań niepożądanych zgłaszanych podczas leczenia produktem CARDIZEM nie była większa niż podczas leczenia placebo.
Poniżej przedstawiono zdarzenia obserwowane w badaniach klinicznych pacjentów z dusznicą bolesną. W wielu przypadkach nie ustalono związku z CARDIZEM. Najczęstszymi zdarzeniami w tych badaniach, a także ich częstością występowania, są obrzęk (2,4%), ból głowy (2,1%), nudności (1,9%), zawroty głowy (1,5%), wysypka (1,3%) i astenia (1,2) %). Ponadto rzadko zgłaszano następujące zdarzenia (mniej niż 1%):
Układ sercowo-naczyniowy
dusznica bolesna, arytmia, blok przedsionkowo-komorowy (I stopnia), blok przedsionkowo-komorowy (II lub III stopnia – patrz OSTRZEŻENIA , Przewodnictwo serca ), bradykardia, blok odnogi pęczka Hisa, zastoinowa niewydolność serca, nieprawidłowości w zapisie EKG, uderzenia gorąca, niedociśnienie, kołatanie serca, omdlenie, tachykardia, skurcze dodatkowe komorowe.
System nerwowy
Nieprawidłowe sny, amnezja, depresja, zaburzenia chodu, omamy, bezsenność, nerwowość, parestezje, zmiany osobowości, senność, drżenie.
Przewód pokarmowy
Anoreksja, zaparcia, biegunka, zaburzenia smaku, niestrawność, łagodne podwyższenie poziomu fosfatazy alkalicznej, SGOT, SGPT i LDH (patrz OSTRZEŻENIA , Ostre uszkodzenie wątroby ), pragnienie, wymioty, wzrost masy ciała.
Dermatologiczny
Wybroczyny, nadwrażliwość na światło, świąd, pokrzywka.
Inny
Niedowidzenie, podwyższenie CPK, suchość w ustach, duszność, krwawienie z nosa, podrażnienie oczu, hiperglikemia, hiperurykemia, impotencja, skurcze mięśni, przekrwienie błony śluzowej nosa, nokturia, ból kostno-stawowy, wielomocz, trudności seksualne, szum w uszach.
Następujące zdarzenia po wprowadzeniu produktu do obrotu zgłaszano rzadko u pacjentów otrzymujących CARDIZEM: ostra uogólniona osutka krostkowa, reakcje alergiczne, łysienie, obrzęk naczynioruchowy (w tym obrzęk twarzy lub oczodołu), asystolia, rumień wielopostaciowy (w tym zespół Stevensa-Johnsona, martwica toksyczno-rozpływna naskórka), objawy pozapiramidowe , przerost dziąseł, niedokrwistość hemolityczna, wydłużony czas krwawienia, leukopenia, nadwrażliwość na światło (w tym rogowacenie liszajowate i przebarwienia w miejscach wystawionych na działanie słońca), plamica, retinopatia, miopatia i małopłytkowość. Zaobserwowano przypadki uogólnionej wysypki, niektóre określane jako leukocytoklastyczne zapalenie naczyń. Ponadto zaobserwowano zdarzenia, takie jak zawał mięśnia sercowego, których nie da się łatwo odróżnić od naturalnego przebiegu choroby u tych pacjentów. Nie można jeszcze ustalić ostatecznego związku przyczynowo-skutkowego między tymi zdarzeniami a terapią CARDIZEM. Zgłaszano również złuszczające zapalenie skóry (potwierdzone przez ponowne prowokowanie).
INTERAKCJE Z LEKAMI
Ze względu na możliwość wystąpienia działania addytywnego, należy zachować ostrożność i ostrożne dostosowywanie dawki u pacjentów otrzymujących CARDIZEM 180 mg jednocześnie z jakimikolwiek lekami, o których wiadomo, że wpływają na kurczliwość i (lub) przewodnictwo mięśnia sercowego (patrz OSTRZEŻENIA ).
Badania farmakologiczne wskazują, że w przypadku jednoczesnego stosowania beta-adrenolityków lub naparstnicy z CARDIZEM może wystąpić addytywne wydłużenie przewodzenia przedsionkowo-komorowego (patrz OSTRZEŻENIA ).
Podobnie jak w przypadku wszystkich leków, należy zachować ostrożność podczas leczenia pacjentów wieloma lekami. Diltiazem jest zarówno substratem, jak i inhibitorem układu enzymatycznego cytochromu P-450 3A4. Inne leki będące specyficznymi substratami, inhibitorami lub induktorami tego układu enzymatycznego mogą mieć istotny wpływ na skuteczność i profil działań niepożądanych diltiazemu. Pacjenci przyjmujący inne leki będące substratami CYP450 3A4, zwłaszcza pacjenci z zaburzeniami czynności nerek i (lub) wątroby, mogą wymagać dostosowania dawki podczas rozpoczynania lub kończenia jednoczesnego podawania diltiazemu w celu utrzymania optymalnych terapeutycznych stężeń we krwi.
Środki znieczulające
Blokery kanału wapniowego mogą nasilać osłabienie kurczliwości, przewodnictwa i automatyzmu serca, a także rozszerzenie naczyń związane ze znieczuleniem. Podczas jednoczesnego stosowania należy ostrożnie dobierać środki znieczulające i blokery wapnia.
Benzodiazepiny
Badania wykazały, że diltiazem zwiększał AUC midazolamu i triazolamu od 3 do 4 razy, a Cmax 2 razy w porównaniu z placebo. Okres półtrwania midazolamu i triazolamu w fazie eliminacji również wydłużył się (1,5 do 2,5 razy) podczas jednoczesnego podawania z diltiazemem. Te działania farmakokinetyczne obserwowane podczas jednoczesnego podawania diltiazemu mogą prowadzić do nasilenia działania klinicznego (np. przedłużonej sedacji) zarówno midazolamu, jak i triazolamu.
Beta-blokery
Kontrolowane i niekontrolowane badania domowe sugerują, że jednoczesne stosowanie CARDIZEM 180 mg i beta-adrenolityków jest zwykle dobrze tolerowane. Dostępne dane nie są jednak wystarczające do przewidzenia efektów jednoczesnego leczenia, zwłaszcza u pacjentów z dysfunkcją lewej komory lub zaburzeniami przewodzenia w sercu.
Podawanie CARDIZEM (chlorowodorek diltiazemu) jednocześnie z propranololem u pięciu zdrowych ochotników spowodowało zwiększenie stężenia propranololu u wszystkich pacjentów, a biodostępność propranololu wzrosła o około 50%. In vitro wydaje się, że propranolol jest wypierany z miejsc wiązania przez diltiazem. Jeśli leczenie skojarzone zostanie rozpoczęte lub przerwane w skojarzeniu z propranololem, może być uzasadnione dostosowanie dawki propranololu (patrz OSTRZEŻENIA ).
Buspiron
U dziewięciu zdrowych ochotników diltiazem znacząco zwiększył średnie AUC buspironu 5,5-krotnie i Cmax 4,1-krotnie w porównaniu z placebo. Diltiazem nie wpływał znacząco na T½ i Tmax buspironu. Podczas jednoczesnego podawania z diltiazemem może być możliwe nasilenie działania i zwiększona toksyczność buspironu. Podczas równoczesnego podawania może być konieczne późniejsze dostosowanie dawki, które powinno być oparte na ocenie klinicznej.

Karbamazepina
Donoszono, że równoczesne podawanie diltiazemu z karbamazepiną prowadziło do zwiększenia stężenia karbamazepiny w surowicy (wzrost o 40% do 72%), co w niektórych przypadkach powodowało toksyczność. Pacjenci otrzymujący te leki jednocześnie powinni być monitorowani pod kątem potencjalnej interakcji leków.
Cymetydyna
Badanie z udziałem sześciu zdrowych ochotników wykazało znaczny wzrost szczytowych poziomów diltiazemu w osoczu (58%) i powierzchni pod krzywą (53%) po tygodniowym cyklu cymetydyny w dawce 1200 mg na dobę i pojedynczej dawce diltiazem 60 mg. Ranitydyna powodowała mniejsze, nieistotne wzrosty. W efekcie może pośredniczyć znane hamowanie przez cymetydynę wątrobowego cytochromu P-450, układu enzymatycznego odpowiedzialnego za metabolizm pierwszego przejścia diltiazemu. Pacjenci obecnie otrzymujący diltiazem powinni być uważnie obserwowani pod kątem zmiany działania farmakologicznego podczas rozpoczynania i kończenia leczenia cymetydyną. Może być uzasadnione dostosowanie dawki diltiazemu.
klonidyna
Bradykardia zatokowa skutkująca hospitalizacją i wstawieniem stymulatora była opisywana w związku ze stosowaniem klonidyny jednocześnie z diltiazemem. Monitoruj częstość akcji serca u pacjentów otrzymujących jednocześnie diltiazem i klonidynę.
Cyklosporyna
Podczas badań z udziałem pacjentów po przeszczepieniu nerki i serca obserwowano interakcje farmakokinetyczne między diltiazemem i cyklosporyną. U biorców przeszczepu nerki i serca konieczne było zmniejszenie dawki minimalnej cyklosporyny w zakresie od 15% do 48% w celu utrzymania stężeń podobnych do obserwowanych przed dodaniem diltiazemu. Jeśli te leki mają być podawane jednocześnie, należy monitorować stężenia cyklosporyny, zwłaszcza gdy leczenie diltiazemem jest rozpoczynane, dostosowywane lub przerywane. Nie oceniano wpływu cyklosporyny na stężenie diltiazemu w osoczu.
Naparstnica
Podawanie CARDIZEM 180 mg z digoksyną 24 zdrowym mężczyznom spowodowało zwiększenie stężenia digoksyny w osoczu o około 20%. Inny badacz nie stwierdził wzrostu poziomu digoksyny u 12 pacjentów z chorobą wieńcową. Ponieważ uzyskano sprzeczne wyniki dotyczące wpływu stężenia digoksyny, zaleca się monitorowanie stężenia digoksyny podczas rozpoczynania, dostosowywania i przerywania terapii CARDIZEM 60 mg, aby uniknąć możliwej nadmiernej lub niedostatecznej cyfryzacji (patrz OSTRZEŻENIA ).
Chinidyna
Diltiazem znacząco zwiększa AUC (0→infin;) chinidyny o 51%, T½ o 36% i zmniejsza jej CLoral o 33%. Może być uzasadnione monitorowanie działań niepożądanych chinidyny i odpowiednie dostosowanie dawki.
ryfampicyna
Jednoczesne podawanie ryfampicyny z diltiazemem obniżyło stężenie diltiazemu w osoczu do niewykrywalnych poziomów. Jeśli to możliwe, należy unikać jednoczesnego podawania diltiazemu z ryfampicyną lub innym znanym induktorem CYP3A4 i rozważyć alternatywne leczenie.
Statyny
Diltiazem jest inhibitorem CYP3A4 i wykazano, że znacząco zwiększa AUC niektórych statyn. Ryzyko miopatii i rabdomiolizy w przypadku statyn metabolizowanych przez CYP3A4 może być zwiększone podczas jednoczesnego stosowania diltiazemu. Jeśli to możliwe, stosuj statyny niemetabolizowane przez CYP3A4 razem z diltiazemem; w przeciwnym razie należy rozważyć dostosowanie dawki zarówno diltiazemu, jak i statyny oraz ścisłe monitorowanie objawów przedmiotowych i podmiotowych wszelkich działań niepożądanych związanych ze statynami.
badaniu krzyżowym u zdrowych ochotników (N=10), jednoczesne podanie pojedynczej dawki 20 mg symwastatyny pod koniec 14-dniowego schematu leczenia z diltiazemem SR w dawce 120 mg dwa razy na dobę powodowało 5-krotne zwiększenie średniej wartości AUC symwastatyny. w porównaniu z samą simwastatyną. U osób ze zwiększoną średnią ekspozycją na diltiazem w stanie stacjonarnym stwierdzono większy krotny wzrost ekspozycji na symwastatynę. Symulacje komputerowe wykazały, że przy dziennej dawce 480 mg diltiazemu można oczekiwać 8-9-krotnego średniego wzrostu AUC symwastatyny. Jeśli konieczne jest jednoczesne podawanie symwastatyny z diltiazemem, należy ograniczyć dobowe dawki symwastatyny do 10 mg, a diltiazemu do 240 mg.
randomizowanym, otwartym, czterokierunkowym badaniu krzyżowym obejmującym dziesięć osób, jednoczesne podawanie diltiazemu (120 mg dwa razy na dobę diltiazemu SR przez 2 tygodnie) z pojedynczą dawką 20 mg lowastatyny powodowało 3- do 4-krotne zwiększenie średnie wartości AUC i Cmax dla lowastatyny w porównaniu do samej lowastatyny. W tym samym badaniu nie stwierdzono istotnej zmiany AUC i Cmax prawastatyny w dawce 20 mg podczas jednoczesnego podawania diltiazemu. Lowastatyna lub prawastatyna nie wpływały znacząco na stężenie diltiazemu w osoczu.
OSTRZEŻENIA
ŚRODKI OSTROŻNOŚCI
Ogólny
CARDIZEM (chlorowodorek diltiazemu) jest intensywnie metabolizowany w wątrobie i wydalany przez nerki oraz z żółcią. Podobnie jak w przypadku każdego leku podawanego przez dłuższy czas, należy w regularnych odstępach czasu monitorować parametry laboratoryjne czynności nerek i wątroby. Lek należy stosować ostrożnie u pacjentów z zaburzeniami czynności nerek lub wątroby. W podostrych i przewlekłych badaniach na psach i szczurach, mających na celu wywołanie toksyczności, wysokie dawki diltiazemu wiązały się z uszkodzeniem wątroby. W specjalnych badaniach podostrej wątroby, doustne dawki 125 mg/kg i wyższe u szczurów wiązały się ze zmianami histologicznymi w wątrobie, które ustępowały po odstawieniu leku. U psów dawki 20 mg/kg były również związane ze zmianami w wątrobie; jednak zmiany te były odwracalne przy dalszym dawkowaniu. Zdarzenia dermatologiczne (patrz DZIAŁANIA NIEPOŻĄDANE może być przemijający i może zniknąć pomimo dalszego używania CARDIZEM. Jednak rzadko zgłaszano również wykwity skórne przechodzące w rumień wielopostaciowy i/lub złuszczające zapalenie skóry. W przypadku utrzymywania się reakcji dermatologicznej lek należy odstawić.
rakotwórczość, mutageneza, upośledzenie płodności
24-miesięczne badanie na szczurach i 21-miesięczne badanie na myszach nie wykazało dowodów na rakotwórczość. Nie było również odpowiedzi mutagennej w testach bakteryjnych in vitro. U szczurów nie zaobserwowano wewnętrznego wpływu na płodność.
Ciąża
Kategoria C
Badania reprodukcji przeprowadzono na myszach, szczurach i królikach. Podawanie dawek od pięciu do dziesięciu razy większych (w przeliczeniu na mg/kg) niż dzienna zalecana dawka terapeutyczna spowodowało śmiertelność zarodków i płodów. W niektórych badaniach stwierdzono, że te dawki powodują nieprawidłowości szkieletu. W badaniach okołoporodowych/poporodowych zaobserwowano pewne zmniejszenie wczesnej wagi poszczególnych młodych i współczynników przeżycia. Przy dawkach 20-krotnie większych od dawek stosowanych u ludzi występowała zwiększona częstość martwych urodzeń.
Nie ma dobrze kontrolowanych badań u kobiet w ciąży; dlatego należy stosować CARDIZEM u kobiet w ciąży tylko wtedy, gdy potencjalna korzyść uzasadnia potencjalne ryzyko dla płodu.
Matki karmiące
Diltiazem przenika do mleka ludzkiego. Jeden raport sugeruje, że stężenia w mleku matki mogą być zbliżone do poziomów w surowicy. Jeśli stosowanie CARDIZEM zostanie uznane za konieczne, należy wprowadzić alternatywną metodę karmienia niemowląt.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność u pacjentów pediatrycznych nie zostały ustalone.
Zastosowanie geriatryczne
Badania kliniczne diltiazemu nie obejmowały wystarczającej liczby osób w wieku 65 lat i starszych, aby ustalić, czy reagują oni inaczej niż osoby młodsze. Inne zgłoszone doświadczenia kliniczne nie wykazały różnic w odpowiedziach między pacjentami w podeszłym wieku i młodszymi. Ogólnie rzecz biorąc, dobór dawki u pacjentów w podeszłym wieku powinien być ostrożny, zwykle zaczynając od dolnej granicy zakresu dawkowania, co odzwierciedla większą częstość pogorszenia czynności wątroby, nerek lub serca oraz współistniejących chorób lub innych leków.
PRZEDAWKOWAĆ
Doustne dawki LD50 u myszy i szczurów wahają się odpowiednio od 415 do 740 mg/kg i od 560 do 810 mg/kg. Dożylne dawki LD50 u tych gatunków wynosiły odpowiednio 60 i 38 mg/kg. Uważa się, że doustna dawka LD50 u psów przekracza 50 mg/kg, podczas gdy śmiertelność zaobserwowano u małp przy 360 mg/kg.
Toksyczna dawka u człowieka nie jest znana. Ze względu na intensywny metabolizm, poziom we krwi po standardowej dawce diltiazemu może różnić się ponad dziesięciokrotnie, co ogranicza przydatność poziomów we krwi w przypadkach przedawkowania.
Istnieją doniesienia o przedawkowaniu diltiazemu w ilościach od
Zdarzenia obserwowane po przedawkowaniu diltiazemu obejmowały bradykardię, niedociśnienie, blok serca i niewydolność serca. Większość zgłoszeń przedawkowania opisywała pewne wspomagające środki medyczne i/lub leczenie farmakologiczne. Bradykardia często reagowała korzystnie na atropinę, podobnie jak blok serca, chociaż stymulację serca często stosowano również w leczeniu bloku serca. W celu utrzymania ciśnienia tętniczego stosowano płyny i wazopresory, aw przypadku niewydolności serca podawano środki inotropowe. Ponadto niektórzy pacjenci otrzymywali leczenie ze wspomaganiem wentylacji, płukaniem żołądka, węglem aktywowanym i/lub dożylnym wapniem.
Skuteczność dożylnego podawania wapnia w celu odwrócenia farmakologicznych skutków przedawkowania diltiazemu była niespójna. W kilku zgłoszonych przypadkach przedawkowanie blokerów kanału wapniowego związane z niedociśnieniem i bradykardią, które początkowo były oporne na atropinę, stawało się bardziej wrażliwe na atropinę po tym, jak pacjenci otrzymali dożylnie wapń. W niektórych przypadkach dożylnie podawano wapń (1 g chlorku wapnia lub 3 g glukonianu wapnia) w ciągu 5 minut i powtarzano co 10 do 20 minut w razie potrzeby. Glukonian wapnia podawano również w postaci ciągłego wlewu z szybkością 2 g na godzinę przez 10 godzin. Mogą być wymagane wlewy wapnia przez 24 godziny lub dłużej. Pacjentów należy monitorować pod kątem objawów hiperkalcemii.
przypadku przedawkowania lub nadmiernej reakcji, oprócz odkażania przewodu pokarmowego należy zastosować odpowiednie środki wspomagające. Wydaje się, że diltiazem nie jest usuwany przez otrzewnową lub hemodializę. Ograniczone dane sugerują, że plazmafereza lub hemoperfuzja z węglem drzewnym mogą przyspieszyć eliminację diltiazemu po przedawkowaniu. W oparciu o znane działanie farmakologiczne diltiazemu i/lub zgłoszone doświadczenia kliniczne, można rozważyć następujące środki:
Bradykardia: Podać atropinę (0,60 do 1,0 mg). Jeśli nie ma odpowiedzi na blokadę nerwu błędnego, należy ostrożnie podawać izoproterenol.
Blok AV wysokiego stopnia: Traktuj jak w przypadku bradykardii powyżej. Stały blok przedsionkowo-komorowy wysokiego stopnia powinien być leczony stymulacją serca.
Zawał serca: Podawać leki inotropowe (izoproterenol, dopaminę lub dobutaminę) i leki moczopędne.
Niedociśnienie: Wazopresory (np. dopamina lub noradrenalina).
Rzeczywiste leczenie i dawkowanie powinny zależeć od ciężkości sytuacji klinicznej oraz oceny i doświadczenia lekarza prowadzącego.
PRZECIWWSKAZANIA
CARDIZEM jest przeciwwskazany u (1) pacjentów z zespołem chorej zatoki, z wyjątkiem obecności sprawnego stymulatora komorowego, (2) pacjentów z blokiem pk II lub III stopnia, z wyjątkiem obecności sprawnego stymulatora komorowego, (3) pacjentów z niedociśnienie (skurczowe poniżej 90 mm Hg), (4) pacjenci z nadwrażliwością na lek oraz (5) pacjenci z ostrym zawałem mięśnia sercowego i przekrwieniem płuc potwierdzonym badaniem rentgenowskim przy przyjęciu.
FARMAKOLOGIA KLINICZNA
Uważa się, że korzyści terapeutyczne osiągane dzięki CARDIZEM 180 mg są związane z jego zdolnością do hamowania napływu jonów wapnia podczas depolaryzacji błony mięśni gładkich serca i naczyń.
Mechanizmy działania
Chociaż dokładne mechanizmy jego działania przeciwdławicowego są wciąż opracowywane, uważa się, że CARDIZEM 120 mg działa w następujący sposób:
modelach zwierzęcych diltiazem zakłóca powolny prąd wewnętrzny (depolaryzujący) w tkance pobudliwej. Powoduje rozprzęganie pobudzenie-skurcz w różnych tkankach mięśnia sercowego bez zmian w konfiguracji potencjału czynnościowego. Diltiazem powoduje rozluźnienie mięśni gładkich naczyń wieńcowych i rozszerzenie zarówno dużych, jak i małych tętnic wieńcowych przy poziomach leku, które powodują niewielki lub żaden negatywny efekt inotropowy. Wynikające z tego wzrosty przepływu wieńcowego (nasierdziowego i podwsierdziowego) występują w modelach niedokrwiennych i nieniedokrwiennych i towarzyszą im zależne od dawki spadki systemowego ciśnienia krwi i zmniejszenie oporu obwodowego.
Efekty hemodynamiczne i elektrofizjologiczne
Podobnie jak inni antagoniści wapnia, diltiazem zmniejsza przewodzenie zatokowo-przedsionkowe i przedsionkowo-komorowe w izolowanych tkankach oraz ma ujemne działanie inotropowe w izolowanych preparatach. W nienaruszonym zwierzęciu wydłużenie odstępu AH można zaobserwować przy wyższych dawkach.
ludzi diltiazem zapobiega spontanicznemu i wywołanemu przez ergonowinę skurczowi tętnicy wieńcowej. Powoduje zmniejszenie obwodowego oporu naczyniowego i niewielki spadek ciśnienia krwi, a w badaniach tolerancji wysiłku u pacjentów z chorobą niedokrwienną serca zmniejsza iloczyn tętna-ciśnienie krwi przy dowolnym obciążeniu pracą. Dotychczasowe badania, głównie u pacjentów z dobrą czynnością komór, nie ujawniły dowodów na negatywne działanie inotropowe; rzut serca, frakcja wyrzutowa i ciśnienie końcoworozkurczowe lewej komory nie uległy zmianie. Jak dotąd niewiele jest danych dotyczących interakcji diltiazemu i beta-blokerów. Tętno spoczynkowe jest zwykle niezmienione lub nieznacznie zmniejszone przez diltiazem.
Dożylny diltiazem w dawkach 20 mg wydłuża czas przewodzenia AH oraz czynnościowe i efektywne okresy refrakcji węzła pk o około 20%. W badaniu obejmującym pojedyncze doustne dawki 300 mg CARDIZEM 60 mg sześciu zdrowym ochotnikom, średnie maksymalne wydłużenie PR wynosiło 14% bez przypadków większego niż blok przedsionkowo-komorowy pierwszego stopnia. Związane z diltiazemem wydłużenie odstępu AH nie jest bardziej wyraźne u pacjentów z blokiem serca pierwszego stopnia. U pacjentów z zespołem chorej zatoki diltiazem znacznie wydłuża cykl zatokowy (w niektórych przypadkach nawet o 50%).
Przewlekłe doustne podawanie CARDIZEM w dawkach do 240 mg/dobę powodowało niewielkie wydłużenie odstępu PR, ale zwykle nie powodowało nieprawidłowego wydłużenia.
Farmakokinetyka i metabolizm
Diltiazem jest dobrze wchłaniany z przewodu pokarmowego i podlega silnemu efektowi pierwszego przejścia, dając bezwzględną biodostępność (w porównaniu z dawkowaniem dożylnym) około 40%. CARDIZEM podlega intensywnemu metabolizmowi, w którym od 2% do 4% niezmienionego leku pojawia się w moczu. Badania wiązania in vitro wykazały, że CARDIZEM 90 mg wiąże się w 70% do 80% z białkami osocza. Konkurencyjne badania wiązania ligandów in vitro wykazały również, że wiązanie CARDIZEM 120 mg nie jest zmienione przez stężenia terapeutyczne digoksyny, hydrochlorotiazydu, fenylobutazonu, propranololu, kwasu salicylowego lub warfaryny. Okres półtrwania eliminacji z osocza po podaniu jednego lub wielu leków wynosi około 3,0 do 4,5 godziny. Desacetylodiltiazem jest również obecny w osoczu na poziomie 10% do 20% leku macierzystego i jest od 25% do 50% tak samo silny jak diltiazem jako środek rozszerzający naczynia wieńcowe. Wydaje się, że minimalne terapeutyczne stężenia preparatu CARDIZEM 120 mg w osoczu mieszczą się w zakresie od 50 do 200 ng/ml. W przypadku zwiększenia mocy dawek następuje odejście od liniowości. Badanie, w którym porównywano pacjentów z prawidłową czynnością wątroby z pacjentami z marskością wątroby, wykazało wydłużenie okresu półtrwania i 69% wzrost AUC (stężenie obszaru pod osoczem w funkcji krzywej czasu) u pacjentów z zaburzeniami czynności wątroby. Jedno badanie z udziałem dziewięciu pacjentów z ciężkimi zaburzeniami czynności nerek nie wykazało różnic w profilu farmakokinetycznym diltiazemu w porównaniu z pacjentami z prawidłową czynnością nerek.
Tabletki CARDIZEM 120 mg . Diltiazem jest wchłaniany z preparatu tabletki do około 98% roztworu odniesienia. Pojedyncze dawki doustne 30 do 120 mg tabletek CARDIZEM 30 mg powodują wykrywalne stężenia w osoczu w ciągu 30 do 60 minut, a maksymalne stężenie w osoczu 2 do 4 godzin po podaniu leku. W miarę zwiększania dawki tabletek CARDIZEM 120 mg z dziennej dawki 120 mg (30 mg qid) do 240 mg (60 mg qid) na dobę, obszar pod krzywą zwiększa się 2,3 razy. Gdy dawkę zwiększa się z 240 mg do 360 mg dziennie, obszar pod krzywą zwiększa się 1,8 razy.
INFORMACJA O PACJENCIE
Tabletki Cardizem należy połknąć w całości; nie dzielić, miażdżyć ani żuć. Lek Cardizem 180 mg został opracowany tak, aby powoli się uwalniał.
