Nimotop 30mg Nimodipine Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Nimotop 30mg i jak się go stosuje?
Nimotop to lek na receptę stosowany w leczeniu objawów tętniaka (krwotoku podpajęczynówkowego). Nimotop może być stosowany samodzielnie lub z innymi lekami.
Nimotop należy do klasy leków zwanych blokerami kanału wapniowego; neurologia, inne; Blokery kanału wapniowego, dihydrofirydyna.
Nie wiadomo, czy Nimotop 30 mg jest bezpieczny i skuteczny u dzieci.
Jakie są możliwe skutki uboczne Nimotop?
Nimotop może powodować poważne skutki uboczne, w tym:
- pokrzywka,
- trudności w oddychaniu,
- obrzęk twarzy, warg, języka lub gardła,
- zawroty,
- szybkie lub wolne tętno oraz
- obrzęk kostek lub stóp
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Nimotop to:
- niskie ciśnienie krwi (uczucie oszołomienia),
- mdłości,
- rozstrój żołądka,
- wolne bicie serca i
- ból w mięśniach
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Nimotop. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
NIE WOLNO PODAWAĆ NIMOTOP (nimodypiny) DOŻYLNIE ANI INNYMI DROGAMI RODZICIELSKIMI. ZGODY I POWAŻNE ZDARZENIA NIEPOŻĄDANE ZAGRAŻAJĄCE ŻYCIU WYSTĄPIŁY, GDY ZAWARTOŚĆ KAPSUŁEK NIMOTOP (nimodypina) ZOSTAŁA WSTRZYKANA RODZICIELSKIM (Patrz OSTRZEŻENIA i DAWKOWANIE I PODAWANIE).
OPIS
Nimotop® (nimodypina) należy do klasy środków farmakologicznych znanych jako blokery kanału wapniowego. Nimodypina to 1,4-dihydro-2,6-dimetylo-4-(m-nitrofenylo)-3,5-pirydynodikarboksylan izopropylo-2-metoksyetylu. Ma masę cząsteczkową 418,5 i wzór cząsteczkowy C21H26N2O7. Wzór strukturalny to:
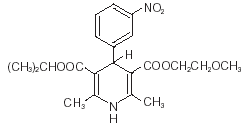
Nimodypina jest żółtą substancją krystaliczną, praktycznie nierozpuszczalną w wodzie.
Kapsułki NIMOTOP® (nimodypina) mają postać miękkich kapsułek żelatynowych do podawania doustnego. Każda kapsułka wypełniona płynem zawiera 30 mg nimodypiny w podłożu gliceryny, olejku miętowego, oczyszczonej wody i glikolu polietylenowego 400. Miękka żelatynowa otoczka kapsułki zawiera żelatynę, glicerynę, oczyszczoną wodę i dwutlenek tytanu.
WSKAZANIA
Nimotop® (nimodypina) jest wskazany do poprawy wyników neurologicznych poprzez zmniejszenie częstości występowania i nasilenia deficytów niedokrwiennych u pacjentów z krwotokiem podpajęczynówkowym z pękniętych tętniaków jagodowych wewnątrzczaszkowych, niezależnie od ich stanu neurologicznego po napadu (tj. stopień IV wg Hunta i Hessa).
DAWKOWANIE I SPOSÓB PODAWANIA
NIE PODAWAJ KAPSUŁEK NIMOTOP (nimodypina) DOŻYLNIE LUB INNYMI DROGAMI RODZICIELSKIMI (patrz OSTRZEŻENIA). Jeśli Nimotop (nimodypina) zostanie nieumyślnie podany dożylnie, klinicznie istotne niedociśnienie może wymagać wspomagania układu krążenia środkami zwiększającymi ciśnienie. Należy również niezwłocznie zastosować specyficzne leczenie przedawkowania blokera kanału wapniowego.
Nimotop (nimodypina) jest podawany doustnie w postaci miękkich kapsułek żelatynowych w kolorze kości słoniowej 30 mg na krwotok podpajęczynówkowy.
Dawka doustna wynosi 60 mg (dwie kapsułki 30 mg) co 4 godziny przez 21 kolejnych dni, najlepiej nie mniej niż godzinę przed posiłkiem lub dwie godziny po posiłku. Terapię Oral Nimotop® (nimodypiną) należy rozpocząć w ciągu 96 godzin od krwotoku podpajęczynówkowego.
Jeśli kapsułka nie może zostać połknięta, np. w czasie zabiegu chirurgicznego, lub jeśli pacjent jest nieprzytomny, na obu końcach kapsułki należy wykonać otwór igłą 18 G i pobrać zawartość kapsułki do strzykawki. Do ekstrakcji płynu z kapsułki można użyć strzykawki pozajelitowej, ale płyn należy zawsze przenieść do strzykawki, która nie może przyjąć igły i jest przeznaczona do podawania doustnego lub przez sondę nosowo-żołądkową lub PEG. Aby zminimalizować błędy w podawaniu, zaleca się, aby strzykawka używana do podawania była oznaczona „Nie do użytku dożylnego”. Następnie zawartość należy opróżnić do zgłębnika in situnaso-żołądkowego pacjenta i przepłukać zgłębnik 30 ml soli fizjologicznej (0,9%). Skuteczność i bezpieczeństwo tej metody podawania nie zostały wykazane w badaniach klinicznych.
Pacjenci z marskością wątroby mają znacznie zmniejszony klirens i około dwukrotnie większe Cmax. Dawkę należy zmniejszyć do 30 mg co 4 godziny, ściśle monitorując ciśnienie krwi i częstość akcji serca.
JAK DOSTARCZONE
Każda kapsułka z miękkiej żelatyny NIMOTOP® (nimodypina) w kolorze kości słoniowej ma nadrukowany napis Nimotop 30 mg i zawiera 30 mg nimodypiny. Kapsułki 30 mg są pakowane w torebki foliowe z dawką jednostkową i dostarczane w kartonikach zawierających 100 kapsułek. Produkt jest również dostępny w opakowaniach foliowych pak zabezpieczających przed dostępem dzieci, zawierających 30 kapsułek w kartonie. Kapsułki powinny być przechowywane w oryginalnym opakowaniu foliowym producenta w temperaturze 25°C (77°F), dopuszczalne odchylenia do 15-30°C (59-86°F) [Patrz kontrolowana temperatura pokojowa USP.]
Kapsułki należy chronić przed światłem i zamarzaniem.
Dystrybutor: Bayer Pharmaceuticals Corporation, 400 Morgan Lane, West Haven, CT 06516. Producent: Catalent Pharma Solutions St. Petersburg, FL 33716. Data aktualizacji FDA: 20.01.2006
SKUTKI UBOCZNE
Niepożądane doświadczenia zgłosiło 92 z 823 pacjentów z krwotokiem podpajęczynówkowym (11,2%), którym podawano nimodypinę. Najczęściej zgłaszanym działaniem niepożądanym było obniżenie ciśnienia krwi u 4,4% tych pacjentów. Dwudziestu dziewięciu z 479 (6,1%) pacjentów otrzymujących placebo również zgłosiło działania niepożądane. Zdarzenia zgłaszane z częstością większą niż 1% są przedstawione poniżej według dawki.
DAWKA co 4 godziny Liczba pacjentów (%) Nimodypina
Nie było innych niepożądanych doświadczeń zgłaszanych przez pacjentów, którym podawano 0,35 mg/kg co 4 godziny, 30 mg co 4 godziny lub 120 mg co 4 godziny. Działania niepożądane z częstością występowania mniejszą niż 1% w grupie otrzymującej dawkę 60 mg co 4 godziny to: zapalenie wątroby; swędzący; krwotok żołądkowo-jelitowy; małopłytkowość; niedokrwistość; kołatanie serca; wymioty; płukanie; pocenie się; świszczący oddech; toksyczność fenytoiny; zawroty; zawroty głowy; skurcz naczyń z odbicia; żółtaczka; nadciśnienie; krwiak.
Działania niepożądane z częstością występowania mniejszą niż 1% w grupie otrzymującej dawkę 90 mg co 4 godziny to: swędzenie, krwotok z przewodu pokarmowego; małopłytkowość; pogorszenie neurologiczne; wymioty; pocenie się; zastoinowa niewydolność serca; hiponatremia; zmniejszająca się liczba płytek krwi; rozsiane wykrzepianie wewnątrznaczyniowe; Zakrzepica żył głębokich.
Jak widać z tabeli, działania niepożądane, które wydają się być związane ze stosowaniem nimodypiny na podstawie zwiększonej częstości występowania przy większej dawce lub wyższej częstości w porównaniu z grupą kontrolną placebo, obejmowały obniżenie ciśnienia krwi, obrzęki i bóle głowy, które są znanymi działaniami farmakologicznymi blokerów kanału wapniowego. Należy jednak zauważyć, że SAH często towarzyszą zmiany świadomości, które prowadzą do niewystarczającego zgłaszania działań niepożądanych. Pacjenci, którzy otrzymywali nimodypinę w badaniach klinicznych z innych wskazań, zgłaszali uderzenia gorąca (2,1%), bóle głowy (4,1%) i zatrzymanie płynów (0,3%), typowe odpowiedzi na blokery kanału wapniowego. Jako bloker kanału wapniowego nimodypina może zaostrzać niewydolność serca u podatnych pacjentów lub wpływać na przewodzenie przedsionkowo-komorowe, ale takich zdarzeń nie obserwowano.
Po podaniu doustnym nimodypiny nie wiązano przyczynowo żadnego klinicznie istotnego wpływu na czynniki hematologiczne, czynność nerek lub wątroby lub metabolizm węglowodanów. Zgłaszano pojedyncze przypadki podwyższonych poziomów glukozy w surowicy (0,8%), podwyższonych poziomów LDH (0,4%), zmniejszonej liczby płytek krwi (0,3%), podwyższonych poziomów fosfatazy alkalicznej (0,2%) i podwyższonych poziomów SGPT (0,2%) rzadko.

Nadużywanie i uzależnienie od narkotyków
Nie odnotowano przypadków nadużywania lub uzależnienia od narkotyków Nimotop® (nimodypina).
INTERAKCJE Z LEKAMI
Możliwe, że działanie sercowo-naczyniowe innych blokerów kanału wapniowego mogłoby zostać wzmocnione przez dodanie Nimotop® (nimodypiny).
W Europie zaobserwowano, że Nimotop® (nimodypina) sporadycznie nasilał działanie związków przeciwnadciśnieniowych przyjmowanych jednocześnie przez pacjentów cierpiących na nadciśnienie; zjawiska tego nie zaobserwowano w badaniach klinicznych w Ameryce Północnej.
Badanie z udziałem ośmiu zdrowych ochotników wykazało 50% wzrost średnich maksymalnych stężeń nimodypiny w osoczu i 90% wzrost średniego pola pod krzywą po tygodniowym kursie cymetydyny w dawce 1000 mg/dobę i nimodypiny w dawce 90 mg/dobę . W tym działaniu może pośredniczyć znane hamowanie cytochromu P-450 w wątrobie przez cymetydynę, co może zmniejszać metabolizm pierwszego przejścia nimodypiny.
OSTRZEŻENIA
ŚMIERĆ SPOWODOWANA NIEUMYŚLNYM PODANIEM DOŻYLNYM: NIE PODAWAJ NIMOTOP (nimodypiny) DOŻYLNIE LUB INNYMI DROGAMI RODZICIELSKIMI. ŚMIERCI I POWAŻNE ZDARZENIA NIEPOŻĄDANE ZAGRAŻAJĄCE ŻYCIU, W TYM ZATRZYMANIE SERCA, ZAPALENIE SERCOWO-NACZYNIOWE, NIEDOCIŚNIĘCIE I BRADYKARDIA, WYSTĄPIŁY W PRZYPADKU WSTRZYKNIĘCIA KAPSUŁEK NIMOTOP (NIMODYPINY) I WPROWADZENIA W DZIEDZINIE.
ŚRODKI OSTROŻNOŚCI
Ogólny: Ciśnienie krwi: Nimodypina ma działanie hemodynamiczne oczekiwane od blokera kanału wapniowego, chociaż na ogół nie są one zaznaczone. Jednak dożylne podanie zawartości Nimotop (nimodypiny) Capsules spowodowało poważne niepożądane konsekwencje, w tym zgon, zatrzymanie akcji serca, zapaść sercowo-naczyniową, niedociśnienie i bradykardię. U pacjentów z krwotokiem podpajęczynówkowym, którym podano Nimotop® (nimodypina) w badaniach klinicznych, około 5% zgłoszono obniżenie ciśnienia krwi i około 1% opuściło badanie z tego powodu (nie wszystkie można było przypisać nimodypinie). Niemniej jednak ciśnienie krwi powinno być dokładnie monitorowane podczas leczenia Nimotop® (nimodypina) w oparciu o jego znaną farmakologię i znane działanie blokerów kanału wapniowego. (Widzieć OSTRZEŻENIA oraz DAWKOWANIE I SPOSÓB PODAWANIA )
Choroba wątroby: Metabolizm Nimotop® (nimodypiny) jest zmniejszony u pacjentów z zaburzeniami czynności wątroby. Takim pacjentom należy ściśle monitorować ciśnienie krwi i częstość tętna oraz podawać mniejszą dawkę (patrz DAWKOWANIE I SPOSÓB PODAWANIA ).
U pacjentów leczonych nimodypiną rzadko zgłaszano rzekomą niedrożność jelit i niedrożność jelit. Związek przyczynowy nie został ustalony. Stan zareagował na konserwatywne zarządzanie.
Interakcje testów laboratoryjnych: Nieznane.
Karcynogeneza, mutageneza, upośledzenie płodności: dwuletnim badaniu zaobserwowano większą częstość występowania gruczolakoraka macicy i gruczolaka z komórek Leydiga jąder u szczurów, którym podawano dietę zawierającą 1800 ppm nimodypiny (co odpowiada 91 do 121 mg/kg mc./dobę nimodypiny) niż w grupie kontrolnej otrzymującej placebo. . Różnice nie były jednak statystycznie istotne, a wyższe wskaźniki mieściły się w historycznym zakresie kontrolnym dla tych guzów w szczepie Wistar.
91-tygodniowym badaniu na myszach stwierdzono, że nimodypina nie jest rakotwórcza, ale wysoka dawka 1800 ppm nimodypiny w paszy (546 do 774 mg/kg/dzień) skróciła oczekiwaną długość życia zwierząt. Badania mutagenności, w tym testy Amesa, testy mikrojądrowe i dominujące śmiertelność były negatywne. Nimodypina nie zaburzała płodności i ogólnej zdolności rozrodczej samców i samic szczurów rasy Wistar po podaniu doustnym w dawkach do 30 mg/kg/dobę przez ponad 10 tygodni u samców i 3 tygodnie u samic przed kryciem i kontynuowana do 7 dnia ciąży. Ta dawka u szczura jest około 4 razy większa od równoważnej dawki klinicznej 60 mg co 4 godziny u pacjenta o masie 50 kg.
Ciąża: Ciąża Kategoria C. Wykazano, że nimodypina ma działanie teratogenne u królików himalajskich. W jednym z dwóch identycznych badań na królikach częstość występowania wad rozwojowych i karłowatości płodów wzrastała przy dawkach doustnych 1 i 10 mg/kg/dobę podawanych (przez zgłębnik) od 6 do 18 dnia ciąży, ale nie przy 3,0 mg/kg/dobę. W drugim badaniu zaobserwowano zwiększoną częstość występowania karłowatości płodów przy dawce 1,0 mg/kg/dobę, ale nie przy wyższych dawkach. Nimodypina wykazywała działanie embriotoksyczne, powodując resorpcję i zahamowanie wzrostu płodów u szczurów Long Evans w dawce 100 mg/kg/dobę podawanej przez zgłębnik od 6. do 15. dnia ciąży. W dwóch innych badaniach na szczurach, dawki nimodypiny 30 mg/kg/dobę podawane przez zgłębnik od 16. dnia ciąży i kontynuowane do uśmiercania (20. dzień ciąży lub 21. dzień po porodzie) wiązały się z częstszym występowaniem zmienności szkieletu, karłowatości płodów i martwe urodzenia, ale bez wad rozwojowych. Nie ma odpowiednich i dobrze kontrolowanych badań u kobiet w ciąży, aby bezpośrednio ocenić wpływ na ludzkie płody. Nimodypinę należy stosować w okresie ciąży tylko wtedy, gdy potencjalna korzyść przewyższa potencjalne ryzyko dla płodu.
Matki karmiące: Wykazano, że nimodypina i (lub) jej metabolity pojawiają się w mleku szczurów w stężeniach znacznie wyższych niż w osoczu matki. Nie wiadomo, czy lek przenika do mleka ludzkiego. Ponieważ wiele leków przenika do mleka ludzkiego, matkom karmiącym zaleca się, aby nie karmiły piersią podczas przyjmowania leku.
Zastosowanie pediatryczne: Bezpieczeństwo i skuteczność u dzieci nie zostały ustalone.
Zastosowanie geriatryczne: Badania kliniczne nimodypiny nie obejmowały wystarczającej liczby osób w wieku 65 lat i starszych, aby ustalić, czy reagują oni inaczej niż osoby młodsze. Inne zgłoszone doświadczenia kliniczne nie wykazały różnic w odpowiedziach między pacjentami w podeszłym wieku i młodszymi. Ogólnie rzecz biorąc, dawkowanie u pacjentów w podeszłym wieku powinno być ostrożne, ze względu na większą częstość występowania pogorszenia czynności wątroby, nerek lub serca oraz współistniejących chorób lub innych leków.
PRZEDAWKOWAĆ
Nie ma doniesień o przedawkowaniu po doustnym podaniu Nimotop® (nimodypina). Oczekuje się, że objawy przedawkowania będą związane z działaniami sercowo-naczyniowymi, takimi jak nadmierne rozszerzenie naczyń obwodowych z wyraźnym niedociśnieniem układowym. Klinicznie istotne niedociśnienie spowodowane przedawkowaniem Nimotopu® (nimodypiny) może wymagać aktywnego wspomagania układu krążenia środkami zwiększającymi ciśnienie. Należy również niezwłocznie zastosować specyficzne leczenie przedawkowania blokera kanału wapniowego. Ponieważ Nimotop® (nimodypina) silnie wiąże się z białkami, dializa prawdopodobnie nie przyniesie korzyści.
PRZECIWWSKAZANIA
Nieznane.
FARMAKOLOGIA KLINICZNA
Mechanizm akcji: Nimodypina jest blokerem kanału wapniowego. Procesy kurczliwości komórek mięśni gładkich są zależne od jonów wapnia, które dostają się do tych komórek podczas depolaryzacji w postaci wolnych jonowych prądów transbłonowych. Nimodypina hamuje transfer jonów wapnia do tych komórek, a tym samym hamuje skurcze mięśni gładkich naczyń. W doświadczeniach na zwierzętach nimodypina miała większy wpływ na tętnice mózgowe niż na tętnice w innych częściach ciała, być może dlatego, że jest wysoce lipofilna, umożliwiając jej przekraczanie bariery krew-mózg; stężenia nimodypiny sięgające 12,5 ng/ml wykryto w płynie mózgowo-rdzeniowym pacjentów z krwotokiem podpajęczynówkowym (SAH) leczonych nimodypiną. Dokładny mechanizm działania nimodypiny u ludzi nie jest znany. Chociaż opisane poniżej badania kliniczne wykazują korzystny wpływ nimodypiny na nasilenie deficytów neurologicznych spowodowanych skurczem naczyń mózgowych po SAH, nie ma dowodów arteriograficznych na to, że lek zapobiega lub łagodzi skurcz tych tętnic. Nie wiadomo jednak, czy zastosowana metodologia arteriograficzna była wystarczająca do wykrycia klinicznie znaczącego wpływu na skurcz naczyń.
Farmakokinetyka i metabolizm: ludzi nimodypina jest szybko wchłaniana po podaniu doustnym, a maksymalne stężenie jest na ogół osiągane w ciągu jednej godziny. Okres półtrwania w końcowej fazie eliminacji wynosi około 8 do 9 godzin, ale wcześniejsze szybkości eliminacji są znacznie szybsze, co odpowiada okresowi półtrwania 1-2 godzin; konsekwencją jest konieczność częstego (co 4 godziny) dawkowania. Nie stwierdzono oznak kumulacji, gdy nimodypina była podawana trzy razy dziennie przez siedem dni. Nimodypina wiąże się z białkami osocza w ponad 95%. Wiązanie było niezależne od stężenia w zakresie od 10 ng/ml do 10 µg/ml. Nimodypina jest wydalana prawie wyłącznie w postaci metabolitów, a mniej niż 1% jest wydalane z moczem w postaci niezmienionej. Zidentyfikowano wiele metabolitów, z których wszystkie są albo nieaktywne, albo znacznie mniej aktywne niż związek macierzysty. Ze względu na wysoki metabolizm pierwszego przejścia biodostępność nimodypiny po podaniu doustnym wynosi średnio 13%. Biodostępność jest znacząco zwiększona u pacjentów z marskością wątroby, z Cmax około dwukrotnie wyższym niż u zdrowych, co wymaga zmniejszenia dawki w tej grupie pacjentów (patrz DAWKOWANIE I SPOSÓB PODAWANIA ). W badaniu przeprowadzonym na 24 zdrowych ochotnikach płci męskiej, podawanie kapsułek nimodypiny po standardowym śniadaniu skutkowało 68% niższym maksymalnym stężeniem w osoczu i 38% niższą biodostępnością w porównaniu z dawkowaniem na czczo.
W pojedynczym badaniu w grupach równoległych z udziałem 24 osób w podeszłym wieku (59-79 lat) i 24 młodszych osób (w wieku 22-40 lat) obserwowane AUC i Cmax nimodypiny były około 2-krotnie większe w populacji osób w podeszłym wieku w porównaniu z młodszym badaniem pacjentów po podaniu doustnym (podawana jako pojedyncza dawka 30 mg i podawana do stanu stacjonarnego 30 mg trzy razy na dobę przez 6 dni). Jednak odpowiedź kliniczna na te związane z wiekiem różnice farmakokinetyczne nie została uznana za istotną. (Widzieć ŚRODKI OSTROŻNOŚCI : Geriatryczne.)
Badania kliniczne: 4 randomizowanych, kontrolowanych placebo badaniach z podwójnie ślepą próbą wykazano, że nimodypina zmniejsza nasilenie deficytów neurologicznych wynikających ze skurczu naczyń u pacjentów, którzy niedawno przebyli krwotok podpajęczynówkowy (SAH). W badaniach stosowano dawki od 20-30 mg do 90 mg co 4 godziny, przy czym lek podawany był przez 21 dni w 3 badaniach, a przez co najmniej 18 dni w pozostałych. W trzech z czterech badań obserwowano pacjentów przez 3-6 miesięcy. W trzech z nich badano stosunkowo dobrze pacjentów, z wszystkimi lub większością pacjentów w stopniach I-III w skali Hunta i Hessa (zasadniczo pozbawionych deficytów ogniskowych po początkowym krwawieniu), w czwartym badano znacznie bardziej chorych pacjentów, stopień III-V w skali Hunta i Hessa. Dwa badania , jedno USA, jedno francuskie, miały podobny projekt, ze stosunkowo zdrowymi pacjentami z SAH przydzielonymi losowo do grupy otrzymującej nimodypinę lub placebo. W każdym z nich oceniano, czy jakikolwiek późno rozwijający się deficyt był spowodowany skurczem lub innymi przyczynami, i oceniano deficyty. Oba badania wykazały znacznie mniej poważnych deficytów spowodowanych skurczem w grupie nimodypiny; drugie (francuskie) badanie wykazało mniej deficytów związanych ze skurczem we wszystkich stopniach nasilenia. Nie zaobserwowano wpływu na deficyty niezwiązane ze skurczem.
Trzecie, duże badanie przeprowadzono w Wielkiej Brytanii u pacjentów z SAH ze wszystkimi stopniami zaawansowania (ale 89% było w stopniach I-III). Nimodypinę podawano 60 mg co 4 godziny. Wyniki nie zostały zdefiniowane jako związane ze skurczem lub nie, ale wystąpiło znaczne zmniejszenie ogólnego wskaźnika zawałów i ciężkiego upośledzenia neurologicznego po 3 miesiącach:
Do kanadyjskiego badania włączono znacznie bardziej chorych pacjentów (stopnie III-V wg Hunta i Hessa), którzy mieli wysoki wskaźnik zgonów i niepełnosprawności, i stosowali dawkę 90 mg co 4 godziny, ale poza tym były podobne do pierwszych dwóch badań. Analiza opóźnionych deficytów niedokrwiennych, z których wiele wynika ze skurczu, wykazała znaczne zmniejszenie deficytów związanych ze skurczem. Wśród analizowanych pacjentów (72 nimodypina, 82 placebo) wystąpiły następujące wyniki.
Gdy połączono dane z badań kanadyjskich i brytyjskich, różnica w leczeniu pod względem wskaźnika powodzenia (tj. dobrego powrotu do zdrowia) w Skali Wyników Glasgow wyniosła 25,3% (nimodypina) w porównaniu z 10,9% (placebo) dla stopni IV lub V wg Hunta i Hessa. Poniższa tabela pokazuje, że nimodypina poprawia powrót do zdrowia pacjentów z SAH ze złym stanem neurologicznym po napadach, przy jednoczesnym zmniejszeniu liczby pacjentów z ciężką niepełnosprawnością i przeżywalnością wegetatywną.
Badanie dawki, porównujące dawki 30, 60 i 90 mg, wykazało ogólnie niski odsetek deficytów neurologicznych związanych ze skurczem, ale brak zależności dawka-odpowiedź.
INFORMACJA O PACJENCIE
Brak informacji. Proszę odnieść się do OSTRZEŻENIA oraz ŚRODKI OSTROŻNOŚCI Sekcje.
