Cordarone 100mg, 50mg Amiodarone Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Cordarone 100mg i jak się go stosuje?
Cordarone 100mg IV to lek na receptę stosowany w leczeniu objawów zaburzeń rytmu serca (komorowych zaburzeń rytmu serca).
- Cordarone IV może być stosowany samodzielnie lub z innymi lekami.
- Cordarone 50mg IV należy do klasy leków o nazwie Antidysrhythmisc, III.
Jakie są możliwe skutki uboczne Cordarone 100mg?
Cordarone 100mg może powodować poważne skutki uboczne, w tym:
- duszność,
- półomdlały,
- szybkie lub nieregularne bicie serca,
- ból w klatce piersiowej,
- świszczący oddech i
- trudności w oddychaniu
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Cordarone 100mg IV to:
- niskie ciśnienie krwi (niedociśnienie),
- wolne tętno,
- zatrzymanie akcji serca,
- mdłości,
- gorączka,
- zastoinowa niewydolność serca,
- nieprawidłowy rytm serca,
- wstrząs kardiogenny oraz
- nieprawidłowości w testach czynności wątroby
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Cordarone. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OSTRZEŻENIE
TOKSYCZNOŚĆ PŁUC, WĄTROBY I SERCA
CORDARONE 100mg przeznaczony jest do stosowania wyłącznie u pacjentów ze wskazanymi, zagrażającymi życiu zaburzeniami rytmu serca, ponieważ jego stosowaniu towarzyszy znaczna toksyczność [patrz WSKAZANIA I STOSOWANIE].
CORDARONE może powodować toksyczność płucną (zapalenie płuc z nadwrażliwości lub śródmiąższowe/pęcherzykowe zapalenie płuc), które w niektórych seriach pacjentów spowodowało klinicznie manifestowaną chorobę z częstością sięgającą nawet 17%. Toksyczność płucna była śmiertelna w około 10% przypadków. Po rozpoczęciu leczenia preparatem CORDARONE 100 mg należy wykonać podstawowe badania rentgenowskie klatki piersiowej i badania czynnościowe płuc, w tym zdolność dyfuzyjną. Powtarzaj historię, badanie fizykalne i prześwietlenie klatki piersiowej co 3 do 6 miesięcy [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
CORDARONE może powodować hepatotoksyczność, która może być śmiertelna. Uzyskuj wyjściowe i okresowe transaminazy wątrobowe i przerwij lub zmniejsz dawkę, jeśli wzrost przekracza trzykrotnie normalny lub podwaja się u pacjenta z podwyższonym poziomem wyjściowym. Przerwać stosowanie produktu CORDARONE, jeśli u pacjenta wystąpią objawy klinicznego uszkodzenia wątroby [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
CORDARONE może nasilać arytmie. Rozpocznij CORDARONE 50 mg w warunkach klinicznych, w których dostępne są ciągłe elektrokardiogramy i resuscytacja serca [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
OPIS
CORDARONE (amiodaron HCl) to lek przeciwarytmiczny, dostępny do podawania doustnego w postaci różowych tabletek z rowkiem, zawierających 200 mg amiodaronu chlorowodorku. Obecne składniki nieaktywne to koloidalny dwutlenek krzemu, laktoza, stearynian magnezu, powidon, skrobia i FD&C Red 40. CORDARONE jest pochodną benzofuranu: 2-butylo-3-benzofuranylo 4-[2-(dietyloamino)-etoksy]-3, Chlorowodorek ketonu 5-dijodofenylowego.
Wzór strukturalny jest następujący:
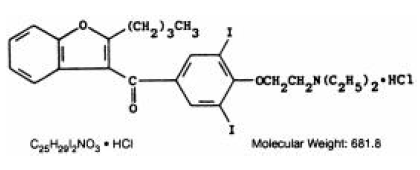
Amiodaron HCl jest krystalicznym proszkiem o barwie białej do kremowej. Jest słabo rozpuszczalny w wodzie, rozpuszczalny w alkoholu i dobrze rozpuszczalny w chloroformie. Zawiera wagowo 37,3% jodu.
WSKAZANIA
Produkt CORDARONE jest wskazany w leczeniu udokumentowanego, zagrażającego życiu nawracającego migotania komór i zagrażającego życiu nawracającego częstoskurczu niestabilnego hemodynamicznie u dorosłych, którzy nie zareagowali na odpowiednie dawki innych dostępnych leków przeciwarytmicznych lub gdy nie można tolerować alternatywnych leków.
DAWKOWANIE I SPOSÓB PODAWANIA
Dawkowanie należy dostosować indywidualnie w zależności od nasilenia arytmii i odpowiedzi. Użyj najniższej skutecznej dawki. Uzyskaj podstawowe prześwietlenie klatki piersiowej, testy czynnościowe płuc, testy czynnościowe tarczycy i aminotransferazy wątrobowe. Skorygować hipokaliemię, hipomagnezemię i hipokalcemię przed rozpoczęciem leczenia
Rekomendowana dawka
Rozpocząć leczenie dawkami nasycającymi 800 do 1600 mg/dobę, aż do wystąpienia początkowej odpowiedzi terapeutycznej (zwykle 1 do 3 tygodni). Po uzyskaniu odpowiedniej kontroli arytmii lub w przypadku nasilenia się działań niepożądanych należy zmniejszyć dawkę produktu CORDARONE 50 mg do 600 do 800 mg/dobę przez okres jednego miesiąca, a następnie do dawki podtrzymującej, zwykle 400 mg/dobę.
Administracja
Podawać CORDARONE konsekwentnie w odniesieniu do posiłków [patrz FARMAKOLOGIA KLINICZNA ]. Podawanie produktu CORDARONE w dawkach podzielonych z posiłkami jest sugerowane w przypadku całkowitej dawki dobowej wynoszącej 1000 mg lub większej lub w przypadku wystąpienia nietolerancji żołądkowo-jelitowej.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Tabletki 200 mg: okrągłe, wypukłe, różowe tabletki z wypukłym „C” i oznakowaniem „200” po jednej stronie, z linią podziału na drugiej stronie i oznakowaniem „WYETH” i „4188”.
Składowania i stosowania
CORDARONE® (chlorowodorek amiodaronu) Tabletki są dostępne w butelkach po 60 tabletek w następujący sposób:
200 mg , NDC 0008-4188-04, okrągłe, wypukłe, różowe tabletki z wypukłym „C” i oznakowaniem „200” po jednej stronie, z linią podziału na drugiej stronie i oznakowaniem „WYETH” i „4188”.
Przechowywać szczelnie zamknięte.
Przechowywać w kontrolowanej temperaturze pokojowej, od 20° do 25°C (68° do 77°F).
Chronić przed światłem.
Dozować w odpornym na światło, szczelnym pojemniku.
Wyprodukowano przez Sanofi Winthrop Industrie, 1, rue de la Vierge, 33440 Ambares, Francja. Dystrybutor: Wyeth Pharmaceuticals Inc., podmiot zależny Pfizer Inc., Filadelfia, PA 19101. Wersja: październik 2018
SKUTKI UBOCZNE
Następujące ciężkie działania niepożądane opisano bardziej szczegółowo w innych punktach informacji o przepisaniu leku:
- Toksyczność płucna [patrz OSTRZEŻENIA I ŚRODKI ]
- Uraz wątroby [patrz OSTRZEŻENIA I ŚRODKI ]
- Pogorszenie arytmii [patrz OSTRZEŻENIA I ŚRODKI ]
- Utrata wzroku i utrata wzroku [patrz OSTRZEŻENIA I ŚRODKI ]
- Nieprawidłowości tarczycy [patrz OSTRZEŻENIA I ŚRODKI ]
- Bradykardia [patrz OSTRZEŻENIA I ŚRODKI ]
- Neuropatia obwodowa [patrz OSTRZEŻENIA I ŚRODKI ]
- Nadwrażliwość na światło i przebarwienia skóry [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Przy zwykłej dawce podtrzymującej (400 mg/dobę) i wyższej, CORDARONE 100 mg powoduje działania niepożądane u około trzech czwartych wszystkich pacjentów, skutkując przerwaniem leczenia u 7 do 18%.
W badaniach ankietowych obejmujących prawie 5000 pacjentów leczonych w otwartych badaniach w Stanach Zjednoczonych oraz w opublikowanych raportach dotyczących leczenia produktem CORDARONE działania niepożądane najczęściej wymagające przerwania leczenia produktem CORDARONE obejmowały nacieki w płucach lub zwłóknienie, napadowy częstoskurcz komorowy, zastoinową niewydolność serca i podwyższenie aktywności enzymów wątrobowych. Inne objawy powodujące odstawienie rzadziej to zaburzenia widzenia, nadwrażliwość na światło, niebieskie zabarwienie skóry, nadczynność i niedoczynność tarczycy.
Poniższe częstości występowania działań niepożądanych oparto na retrospektywnym badaniu 241 pacjentów leczonych przez 2 do 1515 dni (średnio 441,3 dni):
Tarczyca
Często: niedoczynność tarczycy, nadczynność tarczycy.
Układ sercowo-naczyniowy
Często: zastoinowa niewydolność serca, zaburzenia rytmu serca, dysfunkcja węzła SA.
Przewód pokarmowy
Bardzo często: nudności, wymioty.
Często: zaparcia, anoreksja, ból brzucha.
Dermatologiczne
Często: słoneczne zapalenie skóry / nadwrażliwość na światło.
Neurologia
Często: złe samopoczucie i zmęczenie, drżenie/nieprawidłowe ruchy mimowolne, brak koordynacji, nieprawidłowy chód/ataksja, zawroty głowy, parestezje, zmniejszenie libido, bezsenność, ból głowy, zaburzenia snu.
Oczny
Często: zaburzenia widzenia.
Wątrobiany
Często: nieprawidłowe wyniki testów czynności wątroby, nieswoiste zaburzenia czynności wątroby.
Oddechowy
Często: zapalenie lub zwłóknienie płuc.
Inny
Często: zaczerwienienie twarzy, zaburzenia smaku i zapachu, obrzęk, nieprawidłowe wydzielanie śliny, zaburzenia krzepnięcia.
Niezbyt często: Zasinienie skóry, wysypka, samoistne wybroczyny, łysienie, niedociśnienie i zaburzenia przewodzenia w sercu.
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania produktu CORDARONE po zatwierdzeniu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Hematologiczny niedokrwistość hemolityczna, niedokrwistość aplastyczna, pancytopenia, neutropenia, małopłytkowość, agranulocytoza, ziarniniak.
Odporny : reakcja anafilaktyczna/anafilaktoidalna (w tym wstrząs), obrzęk naczynioruchowy.
Neurologia : guz rzekomy mózgu, objawy parkinsonizmu, takie jak akinezja i bradykinezja (czasami przemijające po przerwaniu leczenia), polineuropatia demielinizacyjna.
Psychiatryczny : omamy, stan splątania, dezorientacja, majaczenie.
Sercowy : niedociśnienie (czasami śmiertelne), zatrzymanie zatok.
Oddechowy : eozynofilowe zapalenie płuc, zespół ostrej niewydolności oddechowej w stanie pooperacyjnym, skurcz oskrzeli, zarostowe zapalenie oskrzelików z organizującym się zapaleniem płuc, krwotok do pęcherzyków płucnych, wysięk opłucnowy, zapalenie opłucnej.
Przewód pokarmowy : zapalenie trzustki, ostre zapalenie trzustki.
Wątrobiany : zapalenie wątroby, cholestatyczne zapalenie wątroby, marskość wątroby.
Zaburzenia skóry i tkanki podskórnej pokrzywka, martwica toksyczno-rozpływna naskórka (czasami śmiertelna), rumień wielopostaciowy, zespół Stevensa-Johnsona, złuszczające zapalenie skóry, pęcherzowe zapalenie skóry, wysypka polekowa z eozynofilią i objawami ogólnoustrojowymi (DRESS), wyprysk, świąd, rak skóry, zespół toczniopodobny.
Układ mięśniowo-szkieletowy : miopatia, osłabienie mięśni, rabdomioliza.
Nerkowy : zaburzenia czynności nerek, niewydolność nerek, ostra niewydolność nerek.
Rozrodczy : zapalenie najądrza, impotencja.
Ciało jako całość : gorączka, suchość w ustach.
Endokrynologiczne i metaboliczne : guzki tarczycy/rak tarczycy, zespół nieprawidłowego wydzielania hormonu antydiuretycznego (SIADH).
Naczyniowy : zapalenie naczyń.
INTERAKCJE Z LEKAMI
Ze względu na długi okres półtrwania amiodaronu należy oczekiwać, że interakcje między lekami będą utrzymywać się przez kilka tygodni lub miesięcy po odstawieniu amiodaronu.
Interakcje leków z amiodaronem opisano w Tabeli 1 poniżej.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Trwałość niekorzystnych skutków
Ze względu na długi okres półtrwania amiodaronu (15 do 142 dni) i jego aktywnego metabolitu dezetyloamiodaronu (14 do 75 dni), działania niepożądane i interakcje między lekami mogą utrzymywać się przez kilka tygodni po odstawieniu amiodaronu [patrz FARMAKOLOGIA KLINICZNA ].
Toksyczność płucna
CORDARONE może powodować kliniczny zespół kaszlu i postępującej duszności, któremu towarzyszą dane czynnościowe, radiologiczne, skaningowe galu i patologiczne, zgodne z toksycznością płucną. Toksyczność płucna wtórna do produktu CORDARONE może wynikać z toksyczności pośredniej lub bezpośredniej, reprezentowanej odpowiednio przez zapalenie płuc z nadwrażliwości (w tym eozynofilowe zapalenie płuc) lub śródmiąższowe/pęcherzykowe zapalenie płuc. Stwierdzono, że wskaźniki toksyczności płucnej sięgają 17% i są śmiertelne w około 10% przypadków. Po rozpoczęciu leczenia preparatem CORDARONE 50 mg należy wykonać podstawowe badania rentgenowskie klatki piersiowej i badania czynnościowe płuc, w tym zdolność dyfuzyjną. Powtarzaj historię, badanie fizykalne i prześwietlenie klatki piersiowej co 3 do 6 miesięcy lub w przypadku wystąpienia objawów. Rozważ alternatywną terapię antyarytmiczną, jeśli u pacjenta wystąpią oznaki lub objawy toksyczności płucnej. W leczeniu toksyczności płucnej pomocny może być prednizon w dawce 40-60 mg/dobę, stopniowo zmniejszający się przez kilka tygodni.
Zespół niewydolności oddechowej dorosłych (ARDS)
Po operacji zgłaszano występowanie ARDS u pacjentów otrzymujących terapię CORDARONE, którzy przeszli operację kardiochirurgiczną lub niekardiologiczną. Chociaż pacjenci zwykle dobrze reagują na energiczną terapię oddechową, w rzadkich przypadkach wynik był śmiertelny.
Uraz wątroby
Często obserwuje się bezobjawowe podwyższenie poziomu enzymów wątrobowych, ale lek CORDARONE 100 mg może powodować zagrażające życiu uszkodzenie wątroby. Histologia przypominała alkoholowe zapalenie wątroby lub marskość wątroby. Uzyskaj wyjściowe i okresowe transaminazy wątrobowe. Jeśli transaminazy przekraczają trzykrotnie normalne lub podwajają się u pacjenta z podwyższonym poziomem wyjściowym, należy przerwać lub zmniejszyć dawkę CORDARONE 100 mg, wykonać badania kontrolne i odpowiednio leczyć.
Pogorszona arytmia
Lek CORDARONE 100 mg może zaostrzyć występującą arytmię u około 2 do 5% pacjentów lub spowodować nowe migotanie komór, nieustanny częstoskurcz komorowy, zwiększoną odporność na kardiowersję i wielokształtny częstoskurcz komorowy związany z wydłużeniem odstępu QT (Torsade de Pointes [TdP]).
Przed rozpoczęciem leczenia preparatem CORDARONE należy skorygować hipokaliemię, hipomagnezemię i hipokalcemię, ponieważ zaburzenia te mogą nasilać stopień wydłużenia odstępu QTc i zwiększać potencjał TdP. Należy zwrócić szczególną uwagę na równowagę elektrolitową i kwasowo-zasadową u pacjentów z ciężką lub przedłużającą się biegunką lub przyjmujących leki wpływające na poziom elektrolitów, takie jak leki moczopędne, przeczyszczające, ogólnoustrojowe kortykosteroidy lub amfoterycyna B.
Utrata wzroku i utrata wzroku
Neuropatia wzrokowa i zapalenie nerwu wzrokowego
pacjentów leczonych amiodaronem zgłaszano przypadki neuropatii nerwu wzrokowego i zapalenia nerwu wzrokowego, zwykle prowadzące do zaburzeń widzenia, a czasem trwałej ślepoty, które mogą wystąpić w dowolnym momencie leczenia. W przypadku wystąpienia objawów zaburzeń widzenia, takich jak zmiany ostrości wzroku i pogorszenie widzenia peryferyjnego, należy rozważyć przerwanie stosowania produktu CORDARONE 100 mg i niezwłocznie skierować na badanie okulistyczne. Podczas podawania produktu CORDARONE zaleca się regularne badanie okulistyczne, w tym badanie dna oka i badanie w lampie szczelinowej [patrz DZIAŁANIA NIEPOŻĄDANE ].
Mikrodepozyty rogówki
Mikrodepozyty w rogówce pojawiają się u większości osób dorosłych leczonych preparatem CORDARONE. Są one zwykle dostrzegalne tylko w badaniu w lampie szczelinowej, ale powodują objawy, takie jak aureole wzrokowe lub niewyraźne widzenie nawet u 10% pacjentów. Mikrodepozyty w rogówce są odwracalne po zmniejszeniu dawki lub zakończeniu leczenia. Same bezobjawowe mikrodepozyty nie są powodem do zmniejszenia dawki lub przerwania leczenia [patrz DZIAŁANIA NIEPOŻĄDANE ].
Nieprawidłowości tarczycy
CORDARONE 50 mg hamuje obwodową konwersję tyroksyny (T4) do trójjodotyroniny (T3) i może powodować podwyższony poziom tyroksyny, obniżony poziom T3 i podwyższony poziom nieaktywnego odwrotnego T3 (rT3) u pacjentów z kliniczną eutyreozyą. CORDARONE 50mg może powodować niedoczynność tarczycy (zgłaszaną do 10% pacjentów) lub nadczynność tarczycy (występującą u około 2% pacjentów). Monitorować czynność tarczycy przed leczeniem i okresowo po jego zakończeniu, szczególnie u pacjentów w podeszłym wieku oraz u każdego pacjenta z guzkami tarczycy, wolem lub inną dysfunkcją tarczycy w wywiadzie.
Nadczynność tarczycy może wywołać przełom arytmii. W przypadku pojawienia się nowych objawów arytmii należy rozważyć możliwość wystąpienia nadczynności tarczycy. Leki przeciwtarczycowe, blokery β-adrenergiczne, czasowa terapia kortykosteroidami mogą być konieczne do leczenia objawów nadczynności tarczycy. W przypadku tyreotoksykozy indukowanej amiodaronem działanie leków przeciwtarczycowych może być opóźnione z powodu gromadzenia się w gruczole znacznych ilości preformowanych hormonów tarczycy. Terapia jodem radioaktywnym jest przeciwwskazana ze względu na niski wychwyt radiojodu związany z nadczynnością tarczycy wywołaną amiodaronem. Po nadczynności tarczycy wywołanej przez CORDARONE może wystąpić przejściowa niedoczynność tarczycy.
Niedoczynność tarczycy może być pierwotna lub następująca po ustąpieniu wcześniejszej nadczynności tarczycy wywołanej amiodaronem. W związku z leczeniem amiodaronem zgłaszano ciężką niedoczynność tarczycy i śpiączkę śluzowatą, czasami śmiertelną. U niektórych pacjentów z kliniczną niedoczynnością tarczycy leczonych amiodaronem wartości wskaźnika wolnej tyroksyny mogą być prawidłowe. Zwalczaj niedoczynność tarczycy poprzez zmniejszenie dawki lub zaprzestanie suplementacji CORDARONE i hormonami tarczycy.
Bradykardia
CORDARONE powoduje objawową bradykardię lub zatrzymanie zatok z tłumieniem ognisk ucieczki u 2 do 4% pacjentów. Ryzyko jest zwiększone w przypadku zaburzeń elektrolitowych lub jednoczesnego stosowania leków przeciwarytmicznych lub ujemnych chronotropów [patrz INTERAKCJE Z LEKAMI ]. Bradykardia może wymagać rozrusznika serca w celu kontroli częstości.
Po wprowadzeniu do obrotu zgłaszano przypadki objawowej bradykardii, niektóre wymagające wszczepienia stymulatora i co najmniej jeden przypadek śmiertelny, gdy u pacjentów leczonych amiodaronem rozpoczęto leczenie ledipaswirem/sofosbuwirem lub sofosbuwirem z symeprewirem. Bradykardia zwykle występowała w ciągu kilku godzin do kilku dni, ale w niektórych przypadkach występowała do 2 tygodni po rozpoczęciu leczenia przeciwwirusowego. Bradykardia na ogół ustępowała po przerwaniu leczenia przeciwwirusowego. Mechanizm tego efektu jest nieznany. Monitoruj częstość akcji serca u pacjentów przyjmujących lub niedawno zaprzestających leczenia amiodaronem podczas rozpoczynania leczenia przeciwwirusowego [patrz INTERAKCJE Z LEKAMI ].
Wszczepialne urządzenia kardiologiczne
U pacjentów z wszczepionymi defibrylatorami lub rozrusznikami serca długotrwałe podawanie leków antyarytmicznych może wpływać na progi stymulacji lub defibrylacji. Dlatego na początku i podczas leczenia amiodaronem należy ocenić progi stymulacji i defibrylacji.
Toksyczność płodu
CORDARONE może powodować uszkodzenie płodu w przypadku podania kobiecie w ciąży. Ekspozycja płodu może zwiększać potencjalne skutki kardiologiczne, tarczycowe, neurorozwojowe, neurologiczne i wzrostowe u noworodków [patrz Używaj w określonych populacjach ].
Neuropatia obwodowa
Przewlekłe podawanie produktu CORDARONE może prowadzić do neuropatii obwodowej, która może nie ustąpić po odstawieniu produktu CORDARONE.
Nadwrażliwość na światło i przebarwienia skóry
CORDARONE indukuje fotosensybilizację u około 10% pacjentów; pewną ochronę mogą zapewnić kremy przeciwsłoneczne lub odzież ochronna. Podczas długotrwałego leczenia może wystąpić niebiesko-szare przebarwienie odsłoniętej skóry. Ryzyko może być zwiększone u pacjentów o jasnej karnacji lub nadmiernie nasłonecznionych. Po odstawieniu leku może nastąpić odwrócenie przebarwienia.
Chirurgia
Lotne środki znieczulające
Pacjenci stosujący lek CORDARONE 100 mg mogą być bardziej wrażliwi na działanie hamujące mięsień sercowy i przewodnictwo halogenowych wziewnych środków znieczulających.
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( Przewodnik po lekach ).
Poinformuj kobiety w ciąży o potencjalnym ryzyku dla płodu. Poinformuj kobiety o potencjale rozrodczym, aby poinformowały swojego lekarza o stwierdzonej lub podejrzewanej ciąży [patrz Używaj w określonych populacjach ].
Poinformuj kobiety, że nie zaleca się karmienia piersią podczas leczenia lekiem CORDARONE [patrz Używaj w określonych populacjach ].
Doradź pacjentom, aby unikali soku grejpfrutowego i dziurawca.
Należy doradzić pacjentom, aby zgłosili się po pomoc medyczną, jeśli wystąpią u nich objawy toksyczności płucnej, pogorszenie arytmii, bradykardia, zaburzenia widzenia lub niedoczynność i nadczynność tarczycy.
Etykieta tego produktu mogła zostać zaktualizowana. Aby uzyskać pełne informacje na temat przepisywania, odwiedź stronę www.pfizer.com.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Stosowanie amiodaronu HCl było związane ze statystycznie istotnym, zależnym od dawki wzrostem częstości występowania guzów tarczycy (gruczolak i (lub) rak pęcherzykowy) u szczurów. Częstość występowania guzów tarczycy była większa niż w grupie kontrolnej przy najniższym badanym poziomie dawki, tj. 5 mg/kg/dobę (około 0,08-krotność maksymalnej zalecanej dawki podtrzymującej dla ludzi*).
Badania mutagenności (testy Amesa, testy mikrojądrowe i lizogenne) produktu CORDARONE były ujemne.
W badaniu, w którym amiodaron HCl podawano samcom i samicom szczurów, począwszy od 9 tygodni przed kryciem, obserwowano zmniejszoną płodność po podaniu dawki 90 mg/kg/dobę (około 1,4-krotności maksymalnej zalecanej dawki podtrzymującej u ludzi*).
*600 mg u pacjenta o masie 60 kg (dawka porównana na podstawie powierzchni ciała)
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
Dostępne dane z raportów postmarketingowych i opublikowanych serii przypadków wskazują, że stosowanie amiodaronu u kobiet w ciąży może zwiększać ryzyko wystąpienia działań niepożądanych u płodu, w tym niedoczynności i nadczynności tarczycy u noworodków, bradykardii u noworodków, nieprawidłowości neurorozwojowych, porodu przedwczesnego i ograniczenia wzrostu płodu. Amiodaron i jego metabolit deetyloamiodaron (DEA) przenikają przez łożysko. Nieleczone podstawowe zaburzenia rytmu, w tym arytmie komorowe, w czasie ciąży stanowią zagrożenie dla matki i płodu (patrz Rozważania kliniczne ). W badaniach na zwierzętach podawanie amiodaronu królikom, szczurom i myszom podczas organogenezy powodowało toksyczne działanie na zarodek i płód w dawkach mniejszych niż maksymalna zalecana dawka podtrzymująca u ludzi (patrz Dane ). Poinformuj kobiety w ciąży o potencjalnym ryzyku dla płodu.
Szacowane ryzyko tła poważnych wad wrodzonych i poronienia dla wskazanej populacji jest nieznane. Wszystkie ciąże wiążą się z ryzykiem wady wrodzonej, utraty lub innych niekorzystnych skutków. W ogólnej populacji USA szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2%-4% i 15%-20%.
Rozważania kliniczne
Ryzyko związane z chorobą u matki i/lub zarodka/płodu
Częstość występowania częstoskurczu komorowego jest zwiększona i może być bardziej objawowa w czasie ciąży. Komorowe zaburzenia rytmu występują najczęściej u kobiet w ciąży z podstawową kardiomiopatią, wrodzoną wadą serca, wadą zastawkową lub wypadaniem płatka zastawki mitralnej. Większość epizodów tachykardii jest inicjowanych przez uderzenia ektopowe, a zatem występowanie epizodów arytmii może nasilać się w czasie ciąży ze względu na zwiększoną skłonność do aktywności ektopowej. Przełomowe zaburzenia rytmu serca mogą również wystąpić w czasie ciąży, ponieważ utrzymanie dawek terapeutycznych może być trudne z powodu zwiększonej objętości dystrybucji i zwiększonego metabolizmu leku związanego ze stanem ciąży.
Działania niepożądane u płodu/noworodka
Wykazano, że amiodaron i jego metabolit przenikają przez łożysko. Działania niepożądane na płód związane ze stosowaniem amiodaronu przez matkę w czasie ciąży mogą obejmować noworodkową bradykardię, wydłużenie odstępu QT i okresowe dodatkowe skurcze komór, niedoczynność tarczycy u noworodków (z wolem lub bez) wykrytą przed porodem lub u noworodka i zgłaszaną nawet po kilku dniach ekspozycji, hipertyroksynemię u noworodków, zaburzenia neurorozwojowe niezależne od czynności tarczycy, w tym opóźnienie mowy i trudności z językiem pisanym i arytmetykami, opóźniony rozwój motoryczny i ataksja, oczopląs szarpnięcia z synchronicznym ruchem głowy, zahamowanie wzrostu płodu i przedwczesny poród. Monitoruj noworodka pod kątem oznak i objawów zaburzeń tarczycy i zaburzeń rytmu serca.
Praca i dostawa
Ryzyko arytmii może wzrosnąć podczas porodu i porodu. Pacjenci leczeni produktem CORDARONE powinni być stale monitorowani podczas porodu i porodu [patrz OSTRZEŻENIA I ŚRODKI ].
Dane
Dane zwierząt
ciężarnych szczurów i królików w okresie organogenezy amiodaron HCl w dawkach 25 mg/kg/dobę (odpowiednio około 0,4 i 0,9-krotność maksymalnej zalecanej dawki podtrzymującej u ludzi*) nie wywierał niekorzystnego wpływu na płód. U królików 75 mg/kg/dobę (około 2,7-krotność maksymalnej zalecanej dawki podtrzymującej dla ludzi*) powodowało poronienia u ponad 90% zwierząt. U szczurów dawki 50 mg/kg/dobę lub więcej wiązały się z niewielkim przemieszczeniem jąder i zwiększoną częstością niepełnego skostnienia niektórych kości czaszki i palców; przy 100 mg/kg/dzień lub więcej masa ciała płodu była zmniejszona; przy 200 mg/kg/dobę obserwowano zwiększoną częstość resorpcji płodu. (Te dawki u szczurów są około 0,8, 1,6 i 3,2 razy większe od maksymalnej zalecanej dawki podtrzymującej u ludzi*) Niekorzystny wpływ na wzrost i przeżycie płodu zaobserwowano również u jednego z dwóch szczepów myszy przy dawce 5 mg/kg/dobę ( około 0,04-krotność maksymalnej zalecanej dawki podtrzymującej dla ludzi*).
*600 mg u pacjenta o wadze 60 kg (dawki porównane na podstawie powierzchni ciała)
Laktacja
Podsumowanie ryzyka
Amiodaron i jeden z jego głównych metabolitów, DEA, są obecne w mleku matki w ilości od 3,5% do 45% dawki amiodaronu dostosowanej do wagi matki. Istnieją przypadki niedoczynności tarczycy i bradykardii u niemowląt karmionych piersią, chociaż nie jest jasne, czy skutki te są spowodowane ekspozycją na amiodaron w mleku matki. Nie zaleca się karmienia piersią podczas leczenia produktem CORDARONE [patrz OSTRZEŻENIA I ŚRODKI ].
Kobiety i mężczyźni o potencjale rozrodczym
Bezpłodność
W oparciu o badania płodności zwierząt, CORDARONE może zmniejszać płodność kobiet i mężczyzn. Nie wiadomo, czy efekt ten jest odwracalny. [Widzieć Toksykologia niekliniczna ].
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność produktu CORDARONE u dzieci nie zostały ustalone.
Zastosowanie geriatryczne
Osoby zdrowe w wieku powyżej 65 lat wykazują niższy klirens i dłuższy okres półtrwania leku niż osoby młodsze [patrz FARMAKOLOGIA KLINICZNA ]. Ogólnie rzecz biorąc, dobór dawki u pacjentów w podeszłym wieku powinien być ostrożny, zwykle zaczynając od dolnej granicy zakresu dawkowania, co odzwierciedla większą częstość pogorszenia czynności wątroby, nerek lub serca oraz współistniejących chorób lub innych leków.
PRZEDAWKOWAĆ
Zdarzały się przypadki, niektóre śmiertelne, przedawkowania CORDARONE 50mg.
Monitoruj rytm serca i ciśnienie krwi pacjenta, a jeśli wystąpi bradykardia, można zastosować agonistę receptora β-adrenergicznego lub rozrusznik serca. Leczyć niedociśnienie z niedostateczną perfuzją tkankową za pomocą dodatnich środków inotropowych i wazopresyjnych. Ani CORDARONE 50mg, ani jego metabolit nie podlegają dializie.
PRZECIWWSKAZANIA
- Wstrząs kardiogenny.
- Zespół chorej zatoki, blok przedsionkowo-komorowy II lub III stopnia, bradykardia prowadząca do omdlenia bez działającego rozrusznika.
- Znana nadwrażliwość na lek lub którykolwiek z jego składników, w tym jod.
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Amiodaron jest uważany za lek antyarytmiczny klasy III, ale posiada właściwości elektrofizjologiczne wszystkich czterech klas Vaughana Williamsa. Podobnie jak leki klasy I, amiodaron blokuje kanały sodowe przy szybkiej stymulacji i podobnie jak leki klasy II, amiodaron wywiera niekonkurencyjne działanie przeciwsympatyczne. Jednym z jego głównych efektów, przy długotrwałym podawaniu, jest wydłużenie potencjału czynnościowego serca, efekt klasy III. Negatywny efekt chronotropowy amiodaronu w tkankach węzłowych jest podobny do działania leków klasy IV. Oprócz blokowania kanałów sodowych, amiodaron blokuje kanały potasowe mięśnia sercowego, co przyczynia się do spowolnienia przewodzenia i wydłużenia oporności. Działanie przeciwsympatyczne oraz blokada kanałów wapniowych i potasowych są odpowiedzialne za negatywny wpływ dromotropowy na węzeł zatokowy oraz za spowolnienie przewodzenia i wydłużenie refrakcji w węźle przedsionkowo-komorowym (AV). Jego działanie rozszerzające naczynia krwionośne może zmniejszyć obciążenie serca, a w konsekwencji zużycie tlenu przez mięsień sercowy.
CORDARONE wydłuża czas trwania potencjału czynnościowego wszystkich włókien sercowych, jednocześnie powodując minimalną redukcję dV/dt (maksymalna prędkość wyrzutu potencjału czynnościowego). Okres refrakcji jest wydłużony we wszystkich tkankach serca. CORDARONE wydłuża okres refrakcji serca bez wpływu na spoczynkowy potencjał błonowy, z wyjątkiem komórek automatycznych, w których nachylenie potencjału prepotencjalnego jest zmniejszone, ogólnie zmniejszając automatyzację. Te efekty elektrofizjologiczne znajdują odzwierciedlenie w zmniejszeniu częstości zatok o 15 do 20%, wydłużeniu odstępów PR i QT o około 10%, rozwoju załamków U i zmianach konturu załamka T. Zmiany te nie powinny wymagać odstawienia leku CORDARONE 50 mg, ponieważ świadczą one o jego działaniu farmakologicznym, chociaż CORDARONE może powodować wyraźną bradykardię zatokową lub zatrzymanie zatok i blok serca [patrz OSTRZEŻENIA I ŚRODKI ].
Hemodynamika
badaniach na zwierzętach i po podaniu dożylnym u ludzi, CORDARONE 100 mg rozluźnia mięśnie gładkie naczyń, zmniejsza obwodowy opór naczyniowy (obciążenie następcze) i nieznacznie zwiększa wskaźnik sercowy. Jednak po podaniu doustnym CORDARONE 100 mg nie powoduje istotnej zmiany frakcji wyrzutowej lewej komory (LVEF), nawet u pacjentów z obniżoną LVEF. Po ostrym podaniu dożylnym u ludzi, CORDARONE 100 mg może mieć łagodne ujemne działanie inotropowe.
Farmakodynamika
Nie ma dobrze ustalonego związku między stężeniem w osoczu a skutecznością, ale wydaje się, że stężenia znacznie poniżej 1 mg/l są często nieskuteczne, a stężenia powyżej 2,5 mg/l na ogół nie są potrzebne. Pomiary stężenia w osoczu można wykorzystać do identyfikacji pacjentów, u których poziomy są niezwykle niskie i którzy mogą odnieść korzyści ze zwiększenia dawki lub niezwykle wysokiego, i u których można zmniejszyć dawkę w nadziei na zminimalizowanie skutków ubocznych.
Wpływ na nieprawidłowe rytmy nie jest widoczny przed 2 do 3 dniami i zwykle wymaga 1 do 3 tygodni, nawet w przypadku zastosowania dawki nasycającej. Może występować ciągły wzrost efektu przez dłuższe okresy. Istnieją dowody, że czas do uzyskania efektu jest krótszy, gdy stosuje się schemat dawki nasycającej.
Zgodnie z powolnym tempem eliminacji, efekty antyarytmiczne utrzymują się przez tygodnie lub miesiące po odstawieniu preparatu CORDARONE 50 mg, ale czas nawrotu jest zmienny i nieprzewidywalny. Ogólnie rzecz biorąc, po wznowieniu podawania leku po nawrocie arytmii, kontrola ustala się stosunkowo szybko w porównaniu z początkową odpowiedzią, prawdopodobnie dlatego, że zapasy tkanek nie zostały całkowicie wyczerpane.
Farmakokinetyka
Wchłanianie
Po podaniu doustnym u ludzi, CORDARONE wchłania się powoli i zmiennie. Biodostępność CORDARONE wynosi około 50%. Maksymalne stężenie w osoczu osiągane jest po 3 do 7 godzinach po podaniu pojedynczej dawki. Stężenia w osoczu przy długotrwałym dawkowaniu 100 do 600 mg/dobę są w przybliżeniu proporcjonalne do dawki, ze średnim wzrostem o 0,5 mg/l na każde 100 mg/dobę. Środki te obejmują jednak znaczną zmienność osobniczą.
Pokarm zwiększa szybkość i stopień wchłaniania CORDARONE. Wpływ pokarmu na biodostępność produktu CORDARONE badano u 30 zdrowych osób, które otrzymały pojedynczą dawkę 600 mg bezpośrednio po spożyciu wysokotłuszczowego posiłku i po całonocnym poszczeniu. Pole pod krzywą zależności stężenia w osoczu od czasu (AUC) i maksymalne stężenie w osoczu (Cmax) amiodaronu zwiększały się odpowiednio 2,3 (zakres od 1,7 do 3,6) i 3,8 (zakres od 2,7 do 4,4) razy w obecności pokarmu. Pokarm zwiększał również szybkość wchłaniania amiodaronu, skracając czas do osiągnięcia maksymalnego stężenia w osoczu (Tmax) o 37%. Średnie AUC i średnie Cmax głównego metabolitu amiodaronu, DEA, wzrosły odpowiednio o 55% (zakres 58 do 101%) i 32% (zakres od 4 do 84%), ale nie było zmiany w Tmax w obecności jedzenie.
Dystrybucja
CORDARONE silnie wiąże się z białkami (około 96%). CORDARONE ma bardzo dużą, ale zmienną objętość dystrybucji, średnio około 60 l/kg, ze względu na rozległą akumulację w różnych miejscach, zwłaszcza w tkance tłuszczowej i narządach o dużej perfuzji, takich jak wątroba, płuca i śledziona.
Jeden z głównych metabolitów CORDARONE 50 mg, DEA, został zidentyfikowany u ludzi; w jeszcze większym stopniu gromadzi się w prawie wszystkich tkankach. Brak danych na temat aktywności DEA u ludzi, ale u zwierząt ma on istotne działanie elektrofizjologiczne i antyarytmiczne, ogólnie podobne do samego amiodaronu. Dokładna rola i wkład DEA w antyarytmiczne działanie amiodaronu podawanego doustnie nie są pewne. Rozwój maksymalnych efektów komorowych klasy III po doustnym podaniu produktu CORDARONE 100 mg u ludzi koreluje ściślej z kumulacją DEA w czasie niż z kumulacją amiodaronu.
Eliminacja
Po podaniu pojedynczej dawki 12 zdrowym ochotnikom, CORDARONE wykazywał farmakokinetykę wieloprzedziałową ze średnim pozornym okresem półtrwania w końcowej fazie eliminacji z osocza wynoszącym 58 dni (zakres od 15 do 142 dni) dla amiodaronu i 36 dni (zakres od 14 do 75 dni) dla substancji czynnej. metabolit (DEA). Wykazano, że u pacjentów po przerwaniu długotrwałego leczenia doustnego preparat CORDARONE 100 mg ma dwufazową eliminację z początkowym 50% zmniejszeniem stężenia w osoczu po 2,5 do 10 dniach. Znacznie wolniejsza faza końcowej eliminacji z osocza wykazuje okres półtrwania związku macierzystego w zakresie od 26 do 107 dni, ze średnią około 53 dni, a większość pacjentów w zakresie od 40 do 55 dni. W przypadku braku okresu podawania dawki nasycającej, stężenie w osoczu w stanie stacjonarnym przy stałym dawkowaniu doustnym byłoby zatem osiągane między 130 a 535 dniem, średnio 265 dni. W przypadku metabolitu średni okres półtrwania w fazie eliminacji z osocza wynosił około 61 dni. Dane te prawdopodobnie odzwierciedlają początkową eliminację leku z dobrze perfundowanej tkanki (faza półtrwania 2,5 do 10 dni), po której następuje faza końcowa reprezentująca niezwykle powolną eliminację ze słabo perfundowanych przedziałów tkankowych, takich jak tłuszcz.
Znaczne zróżnicowanie międzyosobnicze w obu fazach eliminacji, a także niepewność co do tego, który kompartment jest krytyczny dla działania leku, wymaga zwrócenia uwagi na indywidualne reakcje po uzyskaniu kontroli arytmii za pomocą dawek nasycających, ponieważ po części określa się prawidłową dawkę podtrzymującą, według wskaźników eliminacji. Indywidualizacja dawek podtrzymujących CORDARONE [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Metabolizm
Amiodaron jest metabolizowany do DEA przez grupę enzymów cytochromu P450 (CYP), konkretnie CYP3A i CYP2C8. Izoenzym CYP3A jest obecny zarówno w wątrobie, jak i jelitach. In vitro amiodaron i DEA mogą hamować CYP2C9, CYP2C19, CYP2D6, CYP3A, CYP2A6, CYP2B6 i CYP2C8. Amiodaron i DEA mogą również hamować niektóre transportery, takie jak glikoproteina P i transporter kationów organicznych (OCT2).
Wydalanie
Amiodaron jest eliminowany głównie przez metabolizm wątrobowy i wydalanie z żółcią, a wydalanie amiodaronu lub DEA z moczem jest znikome. Ani amiodaron, ani DEA nie podlegają dializie.
Określone populacje
Efekt wieku
Osoby zdrowe powyżej 65 roku życia wykazują niższy klirens (około 100 ml/h/kg) niż osoby młodsze (około 150 ml/h/kg) oraz wzrost t½ z około 20 do 47 dni.
Zaburzenia czynności nerek
Zaburzenia czynności nerek nie wpływają na farmakokinetykę amiodaronu ani DEA.
Niewydolność wątroby
Po podaniu pojedynczej dawki dożylnej amiodaronu pacjentom z marskością wątroby obserwuje się istotnie niższe wartości Cmax i średniego stężenia dla DEA, ale średnie stężenia amiodaronu pozostają niezmienione.
Choroba serca
U pacjentów z ciężką dysfunkcją lewej komory farmakokinetyka amiodaronu nie jest istotnie zmieniona, ale końcowy t½ eliminacji DEA jest wydłużony.
Chociaż podczas przewlekłego leczenia doustnym amiodaronem nie określono dostosowania dawki u pacjentów z zaburzeniami czynności nerek, wątroby lub serca, rozważne jest ścisłe monitorowanie kliniczne pacjentów w podeszłym wieku oraz osób z ciężkimi zaburzeniami czynności lewej komory.
Interakcje leków
Wpływ innych środków na amiodaron
Sok grejpfrutowy: Sok grejpfrutowy podawany zdrowym ochotnikom zwiększał AUC amiodaronu o 50% i Cmax o 84% oraz zmniejszał DEA do niemierzalnych stężeń.
Cymetydyna hamuje CYP3A i może zwiększać stężenie amiodaronu w surowicy.
Cholestyramina zmniejsza krążenie jelitowo-wątrobowe amiodaronu, zwiększając tym samym jego eliminację. Powoduje to zmniejszenie poziomu amiodaronu w surowicy i okresu półtrwania.
Wpływ amiodaronu na agentów
Substraty CYP3A
Amiodaron przyjmowany jednocześnie z chinidyną zwiększa stężenie chinidyny w surowicy o 33% po dwóch dniach. Amiodaron przyjmowany jednocześnie z prokainamidem przez mniej niż siedem dni zwiększa stężenie prokainamidu i n-acetyloprokainamidu w osoczu odpowiednio o 55% i 33%.
Loratadyna, niedziałający uspokajająco lek przeciwhistaminowy, jest metabolizowana głównie przez CYP3A, a jej metabolizm może być hamowany przez amiodaron.
Metabolizm lidokainy może być hamowany przez amiodaron.
Cyklofosfamid jest prolekiem metabolizowanym przez CYP450, w tym CYP3A, do aktywnego metabolitu. Metabolizm cyklofosfamidu może być hamowany przez amiodaron.
Klopidogrel, nieaktywny prolek tienopirydyny, jest metabolizowany w wątrobie przez CYP3A do aktywnego metabolitu. Odnotowano potencjalną interakcję między klopidogrelem i amiodaronem skutkującą nieskutecznym hamowaniem agregacji płytek krwi.
Antybiotyki makrolidowe/ketolidowe
Amiodaron może hamować metabolizm antybiotyków makrolidowych/ketolidowych (z wyjątkiem azytromycyny) i ogólnoustrojowych leków przeciwgrzybiczych z grupy azoli.
Substraty glikoproteiny P
Amiodaron przyjmowany jednocześnie z digoksyną zwiększa stężenie digoksyny w surowicy o 70% po jednym dniu.
Eteksylan dabigatranu przyjmowany jednocześnie z doustnym amiodaronem może powodować zwiększenie stężenia dabigatranu w surowicy.
Dekstrometorfan jest substratem zarówno dla CYP2D6, jak i CYP3A. Amiodaron hamuje CYP2D6. Przewlekłe (> 2 tygodnie) doustne podawanie amiodaronu zaburza metabolizm dekstrometorfanu może prowadzić do zwiększenia stężenia w surowicy.
INFORMACJA O PACJENCIE
CORDARONE® (KOR-DU-RON) (amiodaron) tabletki
Jakie są najważniejsze informacje, które powinienem wiedzieć o CORDARONE 50mg?
CORDARONE może powodować poważne skutki uboczne, które mogą prowadzić do śmierci, w tym:
- problemy z płucami
- problemy z wątrobą
- pogorszenie problemów z biciem serca
Zadzwoń do swojego lekarza lub natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z poniższych objawów podczas leczenia lekiem CORDARONE:
- trudności w oddychaniu, świszczący oddech, duszność, kaszel, ból w klatce piersiowej, plucie krwi lub gorączka
- nudności lub wymioty, brązowy lub ciemny kolor moczu, uczucie większego niż zwykle zmęczenia, zażółcenie skóry lub białkówek oczu (żółtaczka) lub ból w prawej górnej części brzucha
- bicie serca, pomijanie rytmu, bicie szybko lub wolno, zawroty głowy lub omdlenia
- problemy ze wzrokiem, w tym niewyraźne widzenie, zobacz aureole lub twoje oczy stają się wrażliwe na światło. Powinieneś mieć regularne badania wzroku przed i podczas leczenia lekiem CORDARONE.
Lek CORDARONE należy rozpocząć w szpitalu, aby można było dokładnie monitorować stan zdrowia pacjenta.
Lek CORDARONE powinien być stosowany w leczeniu osób, u których zdiagnozowano zagrażające życiu zaburzenia rytmu serca zwane komorowymi zaburzeniami rytmu, gdy inne metody leczenia nie były skuteczne lub nie można ich tolerować.
CORDARONE 50mg może powodować inne poważne skutki uboczne. Zobacz „Jakie są możliwe skutki uboczne CORDARONE 100mg?” Jeśli podczas leczenia wystąpią poważne działania niepożądane, może być konieczne odstawienie leku CORDARONE, zmiana dawki lub leczenie. Przed przerwaniem stosowania leku CORDARONE należy porozmawiać z lekarzem.
Po odstawieniu leku CORDARONE mogą nadal występować działania niepożądane, ponieważ lek pozostaje w organizmie przez kilka miesięcy po zakończeniu leczenia.
Należy regularnie przeprowadzać kontrole, badania krwi, prześwietlenia klatki piersiowej przed iw trakcie leczenia preparatem CORDARONE 100 mg, aby sprawdzić, czy nie występują poważne skutki uboczne. Przed rozpoczęciem leczenia lekiem CORDARONE należy również wykonać testy czynnościowe płuc.
Co to jest CORDARONE?
CORDARONE jest lekiem na receptę stosowanym w leczeniu osób, u których zdiagnozowano zagrażające życiu zaburzenia rytmu serca zwane komorowymi zaburzeniami rytmu, gdy inne metody leczenia nie działały lub nie można ich tolerować. Nie wiadomo, czy CORDARONE jest bezpieczny i skuteczny u dzieci.
Kto nie powinien brać CORDARONE 100mg?
Nie należy przyjmować leku CORDARONE 100 mg, jeśli:
- masz poważny problem z sercem zwany wstrząsem kardiogennym
- masz pewne rodzaje choroby serca zwane blokiem serca, z lub bez wolnego tętna;
- masz wolne tętno z zawrotami głowy lub oszołomieniem i nie masz wszczepionego rozrusznika
- jesteś uczulony na amiodaron, jod lub którykolwiek z pozostałych składników leku CORDARONE. Pełna lista składników CORDARONE znajduje się na końcu niniejszego Przewodnika po lekach.
Przed przyjęciem leku CORDARONE 100 mg należy poinformować lekarza o wszystkich swoich schorzeniach, w tym o:
- masz problemy z płucami lub oddychaniem
- masz problemy z wątrobą
- masz lub miałeś problemy z tarczycą
- masz wolne tętno lub problemy z ciśnieniem krwi
- masz biegunkę lub masz biegunkę od dłuższego czasu
- powiedziano, że pacjent ma niski poziom potasu, magnezu lub wapnia we krwi;
- mieć wszczepiony rozrusznik serca lub defibrylator
- jeśli planujesz operację w znieczuleniu ogólnym
- są w ciąży lub planują zajść w ciążę. CORDARONE może zaszkodzić nienarodzonemu dziecku. Należy natychmiast poinformować swojego lekarza, jeśli zajdziesz w ciążę podczas leczenia lekiem CORDARONE. Lek CORDARONE 100 mg może pozostawać w organizmie przez miesiące po zakończeniu leczenia.
- karmisz piersią lub planujesz karmić piersią. Lek CORDARONE 100 mg może przenikać do mleka matki i może zaszkodzić dziecku. Nie należy karmić piersią podczas przyjmowania leku CORDARONE. CORDARONE może pozostawać w organizmie przez miesiące po zakończeniu leczenia. Porozmawiaj ze swoim lekarzem o najlepszym sposobie karmienia dziecka w tym czasie.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym o lekach na receptę i dostępnych bez recepty, witaminach i suplementach ziołowych. Lek CORDARONE 50 mg i niektóre inne leki mogą wpływać na siebie nawzajem i powodować poważne działania niepożądane. Możesz poprosić farmaceutę o listę leków, które wchodzą w interakcje z lekiem CORDARONE.
Jak powinienem przyjmować CORDARONE?
- Po wypisaniu ze szpitala należy przyjmować lek CORDARONE zgodnie z zaleceniami lekarza.
- Twój lekarz poinformuje Cię, ile leku CORDARONE należy zażywać i kiedy.
- Twój lekarz może zmienić dawkę leku CORDARONE 50 mg w razie potrzeby, jeśli rytm serca jest kontrolowany lub jeśli masz pewne działania niepożądane. Lekarz prowadzący powinien uważnie monitorować stan pacjenta w przypadku zmiany dawki leku CORDARONE 50 mg.
- Dawkę leku CORDARONE należy za każdym razem przyjmować w ten sam sposób, z posiłkiem lub bez posiłku.
- W przypadku przyjęcia zbyt dużej dawki leku CORDARONE 100 mg należy natychmiast skontaktować się z lekarzem lub udać się na pogotowie ratunkowe najbliższego szpitala. W przypadku pominięcia dawki należy odczekać i przyjąć następną dawkę o zwykłej porze. Nie należy przyjmować dwóch dawek jednocześnie. Kontynuuj z następną regularnie zaplanowaną dawką.
Czego powinienem unikać podczas przyjmowania CORDARONE?
- Unikaj picia soku grejpfrutowego podczas leczenia preparatem CORDARONE. Picie soku grejpfrutowego z lekiem CORDARONE 50 mg może zwiększyć ilość leku CORDARONE we krwi, co może prowadzić do działań niepożądanych.
- CORDARONE 100mg może sprawić, że Twoja skóra stanie się wrażliwa na światło słoneczne. Możesz doznać poważnych oparzeń słonecznych. Używaj kremu z filtrem i noś czapkę i ubrania zakrywające skórę, aby chronić cię, jeśli musisz przebywać w słońcu. Porozmawiaj z lekarzem, jeśli doznasz oparzenia słonecznego. Zobacz „Problemy skórne” w rozdziale Przewodnik po lekach „Jakie są możliwe skutki uboczne CORDARONE?” poniżej.
Jakie są możliwe skutki uboczne CORDARONE?
CORADARONE może powodować poważne skutki uboczne, w tym:
- Widzieć „Jakie są najważniejsze informacje, które powinienem wiedzieć o CORDARONE?”
- Problemy z nerwami. CORDARONE 100mg może powodować problemy z nerwami. Zadzwoń do swojego lekarza, jeśli wystąpią objawy problemów nerwowych, w tym: uczucie „mrowienia” lub drętwienie rąk, nóg lub stóp, osłabienie mięśni, niekontrolowane ruchy, słaba koordynacja lub problemy z chodzeniem.
- Problemy skórne. CORDARONE może sprawić, że Twoja skóra stanie się bardziej wrażliwa na słońce lub zmieni kolor na niebiesko-szary. Osoby o jasnej karnacji lub osoby, które dużo przebywają na słońcu, mogą być bardziej narażone na te problemy skórne. Po odstawieniu leku CORDARONE część niebieskawo-szarego koloru skóry może powrócić do normy.
- Problemy z tarczycą. Lek CORDARONE może powodować zmniejszoną czynność tarczycy (niedoczynność tarczycy), która czasami może być ciężka, lub nadczynność tarczycy (nadczynność tarczycy), która może być ciężka.
- Jeśli podczas leczenia lekiem CORDARONE wystąpi pogorszenie czynności tarczycy, lekarz może zmniejszyć dawkę lub przerwać leczenie lekiem CORDARONE i ewentualnie przepisać lek zastępujący hormon tarczycy.
- Nadczynność tarczycy może powodować wytwarzanie zbyt dużej ilości hormonu tarczycy. Możesz mieć nieprawidłowe bicie serca nawet podczas przyjmowania CORDARONE. Twój lekarz może przepisać pewne leki w celu leczenia nadczynności tarczycy. Zadzwoń do swojego lekarza, jeśli podczas leczenia lekiem CORDARONE wystąpią jakiekolwiek nieprawidłowe bicie serca. Może to oznaczać, że masz nadczynność tarczycy.
- Twój lekarz powinien wykonać testy sprawdzające czynność tarczycy przed rozpoczęciem i podczas leczenia lekiem CORDARONE.
- Zadzwoń do swojego lekarza, jeśli podczas leczenia lekiem CORDARONE wystąpi którykolwiek z poniższych objawów problemów z tarczycą:
- słabość
- utrata masy ciała lub przyrost masy ciała
- nietolerancja ciepła lub zimna
- przerzedzenie włosów
- wyzysk
- zmiany w twoich okresach menstruacyjnych
- obrzęk szyi (wole)
- nerwowość
- drażliwość
- niepokój
- zmniejszona koncentracja
- uczucie depresji (u osób starszych)
- drżenie
Najczęstsze skutki uboczne CORDARONE to:
- problemy z płucami
- problemy z biciem serca
- problemy sercowe
- problemy z wątrobą
CORDARONE 50 mg może wpływać na płodność u mężczyzn i kobiet. Nie wiadomo, czy efekty są odwracalne. Porozmawiaj ze swoim lekarzem, jeśli masz obawy dotyczące płodności.
To nie wszystkie możliwe skutki uboczne CORDARONE. Aby uzyskać więcej informacji, zapytaj swojego lekarza lub farmaceutę.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać CORDARONE?
- Przechowywać CORDARONE 100 mg w temperaturze pokojowej od 20 ° do 25 ° C (68 ° do 77 ° F).
- Przechowywać CORDARONE w szczelnie zamkniętym pojemniku i przechowywać CORDARONE 50 mg z dala od światła.
Lek CORDARONE 50 mg i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu CORDARONE
Leki są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Nie należy stosować leku CORDARONE w stanach, na które nie został przepisany. Nie należy podawać leku CORDARONE innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić. Możesz poprosić farmaceutę lub pracownika służby zdrowia o informacje na temat CORDARONE, które są przeznaczone dla pracowników służby zdrowia.
Jakie są składniki CORDARONE 100mg?
Składnik czynny: chlorowodorek amiodaronu
Nieaktywne składniki: koloidalny dwutlenek krzemu, laktoza, stearynian magnezu, powidon, skrobia i FD&C Red 40.
Ten przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków.
