Leczenie chorób układu krążenia: Coumadin 1mg, 2mg, 5mg Warfarin Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Coumadin i jak się go stosuje?
Coumadin jest lekiem na receptę stosowanym w leczeniu zakrzepów krwi i zmniejszaniu ryzyka powstawania zakrzepów krwi w organizmie. Zakrzepy krwi mogą powodować udar, zawał serca lub inne poważne schorzenia, jeśli tworzą się w nogach lub płucach.
Jakie są skutki uboczne Coumadin?
Coumadin może powodować poważne działania niepożądane, w tym:
- Śmierć tkanki skórnej (martwica skóry lub gangrena). To może się zdarzyć wkrótce po rozpoczęciu Coumadin. Dzieje się tak, ponieważ tworzą się skrzepy krwi i blokują przepływ krwi do obszaru twojego ciała. Zadzwoń do swojego lekarza natychmiast, jeśli odczuwasz ból, kolor lub zmianę temperatury w dowolnym obszarze ciała. Możesz potrzebować natychmiastowej opieki medycznej, aby zapobiec śmierci lub utracie (amputacji) dotkniętej chorobą części ciała.
- Problemy z nerkami. U osób przyjmujących Coumadin może dojść do uszkodzenia nerek. Poinformuj natychmiast swojego lekarza, jeśli w moczu pojawi się krew. Twój lekarz może częściej wykonywać badania podczas leczenia lekiem Coumadin, aby sprawdzić, czy nie ma krwawienia, jeśli masz już problemy z nerkami.
- „Syndrom fioletowych palców”. Zadzwoń do swojego lekarza natychmiast, jeśli odczuwasz ból w palcach u nóg i wyglądają one na fioletowe lub ciemne.
To nie są wszystkie efekty uboczne Kumadyny. Aby uzyskać więcej informacji, zapytaj swojego lekarza lub farmaceutę. Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OSTRZEŻENIE
RYZYKO KRWAWIENIA
- COUMADIN może powodować poważne lub śmiertelne krwawienie [patrz OSTRZEŻENIA I ŚRODKI ].
- Regularnie monitoruj INR u wszystkich leczonych pacjentów [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
- Leki, zmiany w diecie i inne czynniki wpływają na poziomy INR osiągane podczas terapii COUMADIN 5 mg [patrz INTERAKCJE Z LEKAMI ].
- Poinstruuj pacjentów o środkach zapobiegawczych, aby zminimalizować ryzyko krwawienia i zgłaszać oznaki i objawy krwawienia [patrz INFORMACJA O PACJENCIE ].
OPIS
Tabletki COUMADIN (sodowa warfaryna) i COUMADIN (sól sodowa warfaryny) do wstrzykiwań zawierają sól sodową warfaryny, antykoagulant, który działa poprzez hamowanie czynników krzepnięcia zależnych od witaminy K⌈. Nazwa chemiczna soli sodowej warfaryny to sól sodowa 3-(α-acetonylobenzylo)-4-hydroksykumaryny, która jest mieszaniną racemiczną enancjomerów R- i S-. Krystaliczna sól sodowa warfaryny jest klatratem izopropanolu. Jego wzór empiryczny to C19H15NaO4, a wzór strukturalny przedstawia się następująco:
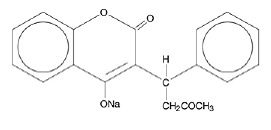
Krystaliczna sól sodowa warfaryny występuje w postaci białego, bezwonnego, krystalicznego proszku, który ulega odbarwieniu pod wpływem światła. Jest bardzo dobrze rozpuszczalny w wodzie, dobrze rozpuszczalny w alkoholu i bardzo słabo rozpuszczalny w chloroformie i eterze.
Tabletki COUMADIN do stosowania doustnego zawierają również:
COUMADIN 1 mg do wstrzykiwań do podawania dożylnego jest dostarczany w postaci sterylnego, liofilizowanego proszku, który po rozpuszczeniu w 2,7 ml sterylnej wody do wstrzykiwań zawiera:
WSKAZANIA
COUMADIN® jest wskazany do:
- Profilaktyka i leczenie zakrzepicy żylnej i jej rozszerzenia, zatorowości płucnej (ZP).
- Profilaktyka i leczenie powikłań zakrzepowo-zatorowych związanych z migotaniem przedsionków (AF) i/lub wymianą zastawki serca.
- Zmniejszenie ryzyka zgonu, nawrotowego zawału mięśnia sercowego (MI) i zdarzeń zakrzepowo-zatorowych, takich jak udar lub zatorowość układowa po zawale mięśnia sercowego.
Ograniczenia użytkowania
COUMADIN 2mg nie ma bezpośredniego wpływu na zakrzep, ani nie odwraca niedokrwiennego uszkodzenia tkanki. Jednak po wystąpieniu zakrzepu, celem leczenia przeciwzakrzepowego jest zapobieganie dalszemu rozszerzaniu się utworzonego skrzepu i zapobieganie wtórnym powikłaniom zakrzepowo-zatorowym, które mogą prowadzić do poważnych i potencjalnie śmiertelnych następstw.
DAWKOWANIE I SPOSÓB PODAWANIA
Zindywidualizowane dozowanie
Dawkowanie i sposób podawania leku COUMADIN 2 mg należy dostosować indywidualnie dla każdego pacjenta, zgodnie z odpowiedzią INR pacjenta na lek. Dostosuj dawkę na podstawie INR pacjenta i leczonego stanu. Należy zapoznać się z najnowszymi, opartymi na dowodach wytycznymi praktyki klinicznej dotyczącymi czasu trwania i intensywności antykoagulacji we wskazanych stanach.
Zalecane docelowe zakresy INR i czas trwania dla poszczególnych wskazań
Wydaje się, że INR większy niż 4,0 nie zapewnia dodatkowych korzyści terapeutycznych u pacjentów z mosami i wiąże się z wyższym ryzykiem krwawienia.
Żylna choroba zakrzepowo-zatorowa (w tym zakrzepica żył głębokich [DVT] i PE)
Dostosuj dawkę warfaryny, aby utrzymać docelowy INR na poziomie 2,5 (zakres INR, 2,0-3,0) dla wszystkich czasów trwania leczenia.
Czas trwania leczenia opiera się na następującym wskazaniu:
- U pacjentów z ZŻG lub ZTP wtórnym do przemijającego (odwracalnego) czynnika ryzyka zaleca się leczenie warfaryną przez 3 miesiące.
- pacjentów z niesprowokowaną ZŻG lub ZP zaleca się leczenie warfaryną przez co najmniej 3 miesiące. Po 3 miesiącach terapii oceń stosunek ryzyka do korzyści długotrwałego leczenia dla indywidualnego pacjenta.
- U pacjentów z dwoma epizodami niesprowokowanej ZŻG lub ZP zaleca się długotrwałe leczenie warfaryną. W przypadku pacjenta otrzymującego długotrwałe leczenie przeciwzakrzepowe należy okresowo ponownie oceniać stosunek ryzyka do korzyści kontynuacji takiego leczenia u danego pacjenta.
Migotanie przedsionków
U pacjentów z niezastawkowym AF należy zastosować antykoagulację warfaryną, aby osiągnąć wartość INR wynoszącą 2,5 (zakres 2,0-3,0).
- pacjentów z niezastawkowym AF, które jest przetrwałe lub napadowe i jest obarczone wysokim ryzykiem udaru mózgu (tj. z którymkolwiek z następujących objawów: wcześniejszy udar niedokrwienny, przemijający napad niedokrwienny lub zatorowość ogólnoustrojowa lub 2 z następujących czynników ryzyka: wiek wiekszy powyżej 75 lat, umiarkowana lub ciężka niewydolność skurczowa lewej komory i/lub niewydolność serca, nadciśnienie tętnicze w wywiadzie lub cukrzyca), zaleca się długotrwałe leczenie przeciwzakrzepowe warfaryną.
- U pacjentów z niezastawkowym AF, które jest przetrwałe lub napadowe i występuje u nich pośrednie ryzyko udaru niedokrwiennego (tj. u których występuje jeden z następujących czynników ryzyka: wiek powyżej 75 lat, umiarkowane lub ciężkie upośledzenie funkcji skurczowej lewej komory i/lub niewydolność serca , nadciśnienie tętnicze w wywiadzie lub cukrzyca), zaleca się długotrwałe leczenie przeciwzakrzepowe warfaryną.
- U chorych z AF i zwężeniem zastawki mitralnej zaleca się długotrwałą antykoagulację warfaryną.
- pacjentów z AF i protezami zastawek serca zaleca się długotrwałą antykoagulację warfaryną; docelową wartość INR można zwiększyć i dodać aspirynę w zależności od typu i pozycji zastawki oraz czynników pacjenta.
Mechaniczne i bioprotetyczne zastawki serca
- U pacjentów z mechaniczną zastawką żółciową lub zastawką uchylną Medtronic Hall (Minneapolis, MN) w pozycji aortalnej, którzy są w rytmie zatokowym i bez powiększenia lewego przedsionka, leczenie warfaryną do docelowego INR 2,5 (zakres 2,0-3,0) jest polecany.
- U pacjentów z uchylnymi zastawkami krążkowymi i mechanicznymi zastawkami żółcieniowymi w pozycji mitralnej zaleca się leczenie warfaryną do docelowego INR 3,0 (zakres 2,5-3,5).
- W przypadku pacjentów z zamkniętymi zastawkami kulkowymi lub krążkowymi z klatką zaleca się leczenie warfaryną do docelowego INR wynoszącego 3,0 (zakres 2,5-3,5).
- pacjentów z bioprotezą w pozycji mitralnej zaleca się leczenie warfaryną do docelowego INR 2,5 (zakres 2,0-3,0) przez pierwsze 3 miesiące po założeniu zastawki. W przypadku obecności dodatkowych czynników ryzyka wystąpienia choroby zakrzepowo-zatorowej (AF, przebyta choroba zakrzepowo-zatorowa, dysfunkcja lewej komory) zalecany docelowy INR wynosi 2,5 (zakres 2,0-3,0).
Po zawale mięśnia sercowego
- W przypadku pacjentów z MI wysokiego ryzyka (np. z rozległym MI w odcinku przednim, ze znaczną niewydolnością serca, z zakrzepicą wewnątrzsercową widoczną w echokardiografii przezklatkowej, z AF oraz z incydentem zakrzepowo-zatorowym w wywiadzie) leczenie skojarzone zalecana jest warfaryna o umiarkowanej intensywności (INR, 2,0-3,0) plus niska dawka aspiryny (≤100 mg/dobę) przez co najmniej 3 miesiące po zawale serca.
Nawracający zator systemowy i inne wskazania
Doustne leczenie przeciwzakrzepowe warfaryną nie zostało w pełni ocenione w badaniach klinicznych u pacjentów z wadą zastawkową związaną z AF, pacjentów ze zwężeniem zastawki mitralnej oraz pacjentów z nawracającą zatorowością układową o nieznanej etiologii. Jednak u tych pacjentów można zastosować umiarkowany schemat dawkowania (INR 2,0-3,0).
Dawkowanie początkowe i podtrzymujące
Odpowiednia dawka początkowa COUMADIN 2mg jest bardzo zróżnicowana dla różnych pacjentów. Nie wszystkie czynniki odpowiedzialne za zmienność dawki warfaryny są znane, a na początkową dawkę wpływają:
- Czynniki kliniczne, w tym wiek, rasa, masa ciała, płeć, przyjmowane jednocześnie leki i choroby współistniejące
- Czynniki genetyczne (genotypy CYP2C9 i VKORC1) [patrz FARMAKOLOGIA KLINICZNA ].
Wybierz dawkę początkową na podstawie oczekiwanej dawki podtrzymującej, biorąc pod uwagę powyższe czynniki. Zmodyfikuj tę dawkę, biorąc pod uwagę specyficzne dla pacjenta czynniki kliniczne. Rozważyć niższe dawki początkowe i podtrzymujące u pacjentów w podeszłym wieku i (lub) osłabionych oraz u pacjentów pochodzenia azjatyckiego [patrz Używaj w określonych populacjach oraz FARMAKOLOGIA KLINICZNA ]. Nie zaleca się rutynowego stosowania dawek nasycających, ponieważ taka praktyka może nasilać powikłania krwotoczne i inne oraz nie zapewnia szybszej ochrony przed tworzeniem się skrzepów.
Zindywidualizuj czas trwania terapii dla każdego pacjenta. Ogólnie rzecz biorąc, leczenie przeciwzakrzepowe powinno być kontynuowane do czasu ustąpienia niebezpieczeństwa zakrzepicy i zatorowości [patrz Zalecane docelowe zakresy INR i czas trwania dla poszczególnych wskazań ].
Zalecenia dotyczące dawkowania bez uwzględnienia genotypu
Jeśli genotypy CYP2C9 i VKORC1 pacjenta nie są znane, początkowa dawka produktu COUMADIN 1 mg wynosi zwykle od 2 do 5 mg raz na dobę. Należy określić zapotrzebowanie każdego pacjenta na dawkowanie, ściśle monitorując odpowiedź INR i biorąc pod uwagę leczone wskazanie. Typowe dawki podtrzymujące wynoszą od 2 do 10 mg raz na dobę.
Zalecenia dotyczące dawkowania z uwzględnieniem genotypu
Tabela 1 przedstawia trzy zakresy oczekiwanych dawek podtrzymujących COUMADIN obserwowanych w podgrupach pacjentów z różnymi kombinacjami wariantów genu CYP2C9 i VKORC1 [patrz FARMAKOLOGIA KLINICZNA ]. Jeśli znany jest genotyp CYP2C9 i/lub VKORC1 pacjenta, należy wziąć pod uwagę te zakresy przy wyborze dawki początkowej. Pacjenci z CYP2C9 *1/*3, *2/*2, *2/*3 i *3/*3 mogą wymagać dłuższego czasu (>2 do 4 tygodni), aby osiągnąć maksymalny efekt INR dla danego schematu dawkowania niż pacjentów bez tych wariantów CYP.
Monitorowanie w celu uzyskania optymalnej antykoagulacji
COUMADIN ma wąski zakres terapeutyczny (wskaźnik), a na jego działanie mogą wpływać takie czynniki, jak inne leki i witamina K w diecie. Dlatego podczas leczenia lekiem COUMADIN należy uważnie monitorować leczenie przeciwzakrzepowe. INR należy określać codziennie po podaniu dawki początkowej, aż wyniki INR ustabilizują się w zakresie terapeutycznym. Po stabilizacji utrzymać dawkowanie w zakresie terapeutycznym, wykonując okresowe INR. Częstotliwość wykonywania INR powinna być oparta na sytuacji klinicznej, ale ogólnie akceptowalne odstępy czasu dla określenia INR wynoszą od 1 do 4 tygodni. Wykonaj dodatkowe badania INR, gdy inne produkty warfaryny są zamieniane z COUMADIN, a także gdy inne leki są rozpoczynane, przerywane lub przyjmowane nieregularnie. Heparyna, często stosowany jednocześnie lek, zwiększa INR [patrz Konwersja z innych antykoagulantów oraz INTERAKCJE Z LEKAMI ].
Oznaczenia czasu krzepnięcia krwi pełnej i czasu krwawienia nie są skutecznymi miarami monitorowania leczenia COUMADIN 5 mg.
Zaburzenia czynności nerek
Nie ma konieczności dostosowania dawkowania u pacjentów z niewydolnością nerek. Częściej monitoruj INR u pacjentów z upośledzoną czynnością nerek, aby utrzymać INR w zakresie terapeutycznym [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
Pominięta dawka
Działanie przeciwzakrzepowe COUMADIN utrzymuje się dłużej niż 24 godziny. Jeśli pacjent pominie dawkę leku COUMADIN o zamierzonej porze dnia, powinien jak najszybciej przyjąć dawkę tego samego dnia. Pacjent nie powinien podwajać dawki następnego dnia w celu uzupełnienia pominiętej dawki.
Dożylna droga podania
Dawka dożylna leku COUMADIN 1 mg jest taka sama jak dawka doustna. Po rekonstytucji podawać COUMADIN do wstrzykiwań w powolnym bolusie do żyły obwodowej przez 1 do 2 minut.
COUMADIN 2 mg do wstrzykiwań nie jest zalecany do podawania domięśniowego.
Rozpuścić fiolkę w 2,7 ml jałowej wody do wstrzykiwań. Otrzymana wydajność wynosi 2,5 ml roztworu 2 mg na ml (łącznie 5 mg). Produkty lecznicze do podawania pozajelitowego należy przed podaniem skontrolować wzrokowo pod kątem obecności cząstek stałych i przebarwień, o ile pozwala na to roztwór i pojemnik. Nie używać, jeśli zauważono cząstki stałe lub przebarwienia.
Po odtworzeniu COUMADIN do wstrzykiwań jest stabilny przez 4 godziny w temperaturze pokojowej. Nie zawiera żadnych konserwantów przeciwdrobnoustrojowych, dlatego należy zadbać o zapewnienie sterylności przygotowanego roztworu. Fiolka jest przeznaczona wyłącznie do jednorazowego użytku, wszelkie niewykorzystane resztki roztworu należy wyrzucić.
Leczenie podczas stomatologii i chirurgii
Niektóre zabiegi stomatologiczne lub chirurgiczne mogą wymagać przerwania lub zmiany dawki leczenia lekiem COUMADIN. Rozważ korzyści i ryzyko podczas odstawiania COUMADIN 2mg nawet na krótki okres czasu. Określ INR bezpośrednio przed jakimkolwiek zabiegiem stomatologicznym lub chirurgicznym. U pacjentów poddawanych minimalnie inwazyjnym zabiegom, u których należy zastosować antykoagulację przed, w trakcie lub bezpośrednio po tych zabiegach, dostosowanie dawki produktu COUMADIN w celu utrzymania wartości INR na dolnym końcu zakresu terapeutycznego może bezpiecznie pozwolić na kontynuację leczenia przeciwzakrzepowego.
Konwersja z innych antykoagulantów
Heparyna
Ponieważ pełny efekt przeciwzakrzepowy COUMADIN 2 mg nie jest osiągany przez kilka dni, heparyna jest preferowana do początkowej szybkiej antykoagulacji. Podczas początkowego leczenia preparatem COUMADIN wpływ na antykoagulację heparyną ma minimalne znaczenie kliniczne. Konwersja na COUMADIN może rozpocząć się jednocześnie z leczeniem heparyną lub może być opóźniona o 3 do 6 dni. Aby zapewnić terapeutyczną antykoagulację, należy kontynuować terapię pełną dawką heparyny i nakładać terapię COUMADIN na heparynę przez 4 do 5 dni i do momentu uzyskania przez produkt COUMADIN 2 mg pożądanej odpowiedzi terapeutycznej określonej na podstawie wskaźnika INR, kiedy to można odstawić heparynę.
Ponieważ heparyna może wpływać na INR, u pacjentów otrzymujących zarówno heparynę, jak i COUMADIN 1 mg należy monitorować INR co najmniej:
- 5 godzin po ostatniej dożylnej dawce heparyny w bolusie lub
- 4 godziny po zaprzestaniu ciągłego dożylnego wlewu heparyny lub
- 24 godziny po ostatnim podskórnym wstrzyknięciu heparyny.
COUMADIN 1 mg może wydłużyć czas częściowej tromboplastyny po aktywacji (APTT), nawet przy braku heparyny. Poważne podwyższenie (>50 sekund) w aPTT z INR w pożądanym zakresie zostało zidentyfikowane jako wskaźnik zwiększonego ryzyka krwotoku pooperacyjnego.
Inne antykoagulanty
Instrukcje dotyczące konwersji na COUMADIN znajdują się na etykietach innych antykoagulantów.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Tablety
Tabletki z pojedynczą punktacją COUMADIN
Do wstrzykiwań
Do wstrzykiwań: 5 mg liofilizowanego proszku w fiolce jednodawkowej.
Składowania i stosowania
Tablety
Tabletki COUMADIN są z pojedynczą linią podziału, na jednej stronie nadrukowano numerycznie 1, 2, 2-1/2, 3, 4, 5, 6, 7-1/2 lub 10 nałożonych na siebie i z napisem „COUMADIN” oraz z przeciwną stroną zwykły. COUMADIN jest dostępny w butelkach i opakowaniach jednostkowych dawek szpitalnych w następujących mocach i kolorach:
Chronić przed światłem i wilgocią. Przechowywać w kontrolowanej temperaturze pokojowej (59°-86°F, 15°-30°C). Dozować w szczelnym, odpornym na światło pojemniku, zgodnie z definicją w USP.
Przechowywać szpitalne blistry z dawką jednostkową w kartoniku do czasu wykorzystania zawartości.
Zastrzyk
KUMADYNA w przypadku fiolek do wstrzykiwań uzyskuje się 5 mg warfaryny po rozpuszczeniu w 2,7 ml jałowej wody do wstrzykiwań (maksymalna wydajność wynosi 2,5 ml roztworu 2 mg/ml). Zawartość netto fiolki to 5,4 mg liofilizowanego proszku.
Fiolka 5 mg (pudełko 6 szt.) - NDC 0590-0324-35
Chronić przed światłem. Fiolkę przechowywać w pudełku do czasu użycia. Przechowywać w kontrolowanej temperaturze pokojowej (59°-86°F, 15°-30°C).
Po rekonstytucji przechowywać w kontrolowanej temperaturze pokojowej (59-86°F, 15-30°C) i zużyć w ciągu 4 godzin.
Nie przechowywać w lodówce. Wyrzucić niewykorzystane rozwiązanie.
Specjalne postępowanie
Należy wziąć pod uwagę procedury właściwego obchodzenia się i usuwania potencjalnie niebezpiecznych leków.
Wytyczne na ten temat zostały opublikowane [ zobacz REFERENCJE ].
Personel farmaceutyczny i kliniczny w ciąży powinien unikać narażenia na zmiażdżone lub przełamane tabletki [patrz Używaj w określonych populacjach ].
BIBLIOGRAFIA
Niebezpieczne leki OSHA. OSHA. http://www.osha.gov/SLTC/hazardousdrugs/index.html.
Dystrybutor: Bristol-Myers Squibb Company, Princeton, New Jersey 08543 USA. Aktualizacja: czerwiec 2017
SKUTKI UBOCZNE
Następujące poważne działania niepożądane leku COUMADIN 2 mg omówiono bardziej szczegółowo w innych sekcjach oznakowania:
- Krwotok [patrz PUDEŁKO OSTRZEŻENIE , OSTRZEŻENIA I ŚRODKI oraz PRZEDAWKOWAĆ ]
- Martwica tkanek [patrz OSTRZEŻENIA I ŚRODKI ]
- Kalcyfilaksja [patrz OSTRZEŻENIA I ŚRODKI ]
- Ostre uszkodzenie nerek [patrz OSTRZEŻENIA I ŚRODKI ]
- Ogólnoustrojowe miażdżyce zatorowe i cholesterolowe mikrozatory [patrz OSTRZEŻENIA I ŚRODKI ]
- Niedokrwienie kończyn, martwica i zgorzel u pacjentów z HIT i HITTS [patrz OSTRZEŻENIA I ŚRODKI ]
- Inne ustawienia kliniczne o zwiększonym ryzyku [patrz OSTRZEŻENIA I ŚRODKI ]
Inne działania niepożądane leku COUMADIN 1 mg obejmują:
- Zaburzenia układu immunologicznego: nadwrażliwość/reakcje alergiczne (w tym pokrzywka i reakcje anafilaktyczne)
- Zaburzenia naczyniowe: zapalenie naczyń
- Zaburzenia wątroby i dróg żółciowych: zapalenie wątroby, podwyższona aktywność enzymów wątrobowych. Cholestatyczne zapalenie wątroby było związane z jednoczesnym podawaniem produktu COUMADIN i tyklopidyny.
- Zaburzenia żołądka i jelit: nudności, wymioty, biegunka, zaburzenia smaku, ból brzucha, wzdęcia, wzdęcia
- Zaburzenia skóry: wysypka, zapalenie skóry (w tym wykwity pęcherzowe), świąd, łysienie
- Zaburzenia układu oddechowego: zwapnienie tchawicy lub oskrzeli
- Zaburzenia ogólne: dreszcze
INTERAKCJE Z LEKAMI
Leki mogą wchodzić w interakcje z COUMADIN 5 mg poprzez mechanizmy farmakodynamiczne lub farmakokinetyczne. Farmakodynamiczne mechanizmy interakcji z lekiem COUMADIN 2 mg to synergizm (zaburzona hemostaza, zmniejszona synteza czynnika krzepnięcia), antagonizm kompetycyjny (witamina K) i zmiana pętli kontroli fizjologicznej metabolizmu witaminy K (oporność dziedziczna). Mechanizmy farmakokinetyczne interakcji leków z COUMADIN to głównie indukcja enzymów, hamowanie enzymów i zmniejszone wiązanie z białkami osocza. Należy zauważyć, że niektóre leki mogą oddziaływać na więcej niż jeden mechanizm. Częstsze monitorowanie INR należy wykonywać przy rozpoczynaniu lub odstawianiu innych leków, w tym roślinnych, lub przy zmianie dawkowania innych leków, w tym leków przeznaczonych do krótkotrwałego stosowania (np. antybiotyków, leków przeciwgrzybiczych, kortykosteroidów) [patrz PUDEŁKO OSTRZEŻENIE ].
Należy zapoznać się z etykietami wszystkich jednocześnie stosowanych leków, aby uzyskać dalsze informacje na temat interakcji z COUMADIN lub działań niepożądanych związanych z krwawieniem.
Interakcje z CYP450
Do izoenzymów CYP450 biorących udział w metabolizmie warfaryny należą CYP2C9, 2C19, 2C8, 2C18, 1A2 i 3A4. Silniejszy enancjomer warfaryny S jest metabolizowany przez CYP2C9, podczas gdy enancjomer R jest metabolizowany przez CYP1A2 i 3A4.
- Inhibitory CYP2C9, 1A2 i/lub 3A4 mogą potencjalnie nasilać działanie (podwyższenie INR) warfaryny poprzez zwiększenie ekspozycji na warfarynę.
- Induktory CYP2C9, 1A2 i/lub 3A4 mogą potencjalnie zmniejszać działanie (zmniejszenie INR) warfaryny poprzez zmniejszenie ekspozycji na warfarynę.
Przykłady inhibitorów i induktorów CYP2C9, 1A2 i 3A4 przedstawiono poniżej w Tabeli 2; jednak ta lista nie powinna być uważana za kompletną. Więcej informacji na temat potencjalnej interakcji z CYP450 można znaleźć na etykietach wszystkich jednocześnie stosowanych leków. Potencjał hamowania i indukcji CYP450 należy wziąć pod uwagę podczas rozpoczynania, kończenia lub zmiany dawki jednocześnie stosowanych leków. Uważnie monitoruj INR, jeśli jednocześnie podawany lek jest inhibitorem lub induktorem CYP2C9, 1A2 i/lub 3A4.
Leki zwiększające ryzyko krwawienia
Przykłady leków, o których wiadomo, że zwiększają ryzyko krwawienia, przedstawiono w tabeli 3. Ponieważ ryzyko krwawienia zwiększa się, gdy leki te są stosowane jednocześnie z warfaryną, należy ściśle monitorować pacjentów otrzymujących jakikolwiek taki lek z warfaryną.
Antybiotyki i leki przeciwgrzybicze
Istnieją doniesienia o zmianach wskaźnika INR u pacjentów przyjmujących warfarynę i antybiotyki lub leki przeciwgrzybicze, ale kliniczne badania farmakokinetyczne nie wykazały stałego wpływu tych leków na stężenie warfaryny w osoczu.
Ściśle monitoruj INR podczas rozpoczynania lub kończenia stosowania jakiegokolwiek antybiotyku lub leku przeciwgrzybiczego u pacjentów przyjmujących warfarynę.
Produkty i żywność botaniczna (ziołowa)
Częstsze monitorowanie INR powinno być wykonywane podczas uruchamiania lub zatrzymywania środków botanicznych.
Istnieje kilka odpowiednich, dobrze kontrolowanych badań oceniających potencjalne interakcje metaboliczne i/lub farmakologiczne między środkami botanicznymi a COUMADIN 2 mg. Ze względu na brak standaryzacji produkcji z botanicznymi preparatami leczniczymi, ilość składników aktywnych może się różnić. Mogłoby to jeszcze bardziej utrudnić ocenę potencjalnych interakcji i wpływu na antykoagulację.
Niektóre środki botaniczne mogą powodować krwawienia, gdy są przyjmowane same (np. czosnek i miłorząb dwuklapowy) i mogą mieć właściwości przeciwzakrzepowe, przeciwpłytkowe i/lub fibrynolityczne. Oczekuje się, że efekty te będą się sumować z przeciwzakrzepowymi efektami COUMADIN. I odwrotnie, niektóre środki botaniczne mogą zmniejszać działanie COUMADIN (np. koenzym Q10, ziele dziurawca, żeń-szeń). Niektóre produkty roślinne i pokarmy mogą wchodzić w interakcje z COUMADIN 2mg poprzez interakcje z CYP450 (np. echinacea, sok grejpfrutowy, miłorząb, gorzknik kanadyjski, ziele dziurawca).
Ilość witaminy K w jedzeniu może wpływać na terapię COUMADIN. Należy doradzić pacjentom przyjmującym COUMADIN 1 mg normalną, zbilansowaną dietę utrzymującą stałą ilość witaminy K. Pacjenci przyjmujący COUMADIN 5 mg powinni unikać drastycznych zmian w nawykach żywieniowych, takich jak spożywanie dużych ilości zielonych warzyw liściastych.
OSTRZEŻENIA
Zawarte jako część "ŚRODKI OSTROŻNOŚCI" Sekcja
ŚRODKI OSTROŻNOŚCI
Krwotok
COUMADIN może spowodować poważne lub śmiertelne krwawienie. Krwawienie jest bardziej prawdopodobne w ciągu pierwszego miesiąca. Czynniki ryzyka krwawienia obejmują wysoką intensywność antykoagulacji (INR >4,0), wiek powyżej lub równy 65 lat, historię wysoce zmiennych wartości INR, historię krwawień z przewodu pokarmowego, nadciśnienie, chorobę naczyń mózgowych, niedokrwistość, nowotwór złośliwy, uraz, zaburzenia czynności nerek, niektóre czynniki genetyczne czynniki [patrz FARMAKOLOGIA KLINICZNA ], niektóre leki towarzyszące [patrz INTERAKCJE Z LEKAMI ] oraz długi czas leczenia warfaryną.
Regularnie monitoruj INR u wszystkich leczonych pacjentów. Osoby o wysokim ryzyku krwawienia mogą odnieść korzyści z częstszego monitorowania INR, starannego dostosowania dawki do pożądanego INR i najkrótszego czasu leczenia odpowiedniego dla stanu klinicznego. Jednak utrzymanie INR w zakresie terapeutycznym nie eliminuje ryzyka krwawienia.
Leki, zmiany w diecie i inne czynniki wpływają na poziomy INR osiągane podczas terapii COUMADIN 1 mg. Częstsze monitorowanie INR podczas rozpoczynania lub kończenia innych leków, w tym roślinnych, lub przy zmianie dawek innych leków [patrz INTERAKCJE Z LEKAMI ].
Poinstruuj pacjentów o środkach zapobiegawczych, aby zminimalizować ryzyko krwawienia i zgłaszać oznaki i objawy krwawienia [patrz INFORMACJA O PACJENCIE ].
Martwica tkanek
Martwica i/lub zgorzel skóry i innych tkanek to rzadkie, ale poważne ryzyko (
Dokładna ocena kliniczna jest wymagana w celu ustalenia, czy martwica jest spowodowana chorobą podstawową. Chociaż próbowano różnych metod leczenia, żadne leczenie martwicy nie zostało uznane za jednolicie skuteczne. W przypadku wystąpienia martwicy należy przerwać terapię COUMADIN 5 mg. Rozważ alternatywne leki, jeśli konieczne jest kontynuowanie leczenia przeciwzakrzepowego.
Kalcyfilaksja
U pacjentów ze schyłkową niewydolnością nerek i bez nich obserwowano przypadki śmiertelnej i poważnej kalcyfilaksji lub arteriolopatii wapniowo-mocznicowej. W przypadku rozpoznania kalcyfilaksji u tych pacjentów należy przerwać stosowanie produktu COUMADIN 5 mg i odpowiednio leczyć kalcyfilaksję. Rozważ alternatywną terapię przeciwzakrzepową.
Ostre uszkodzenie nerek
U pacjentów ze zmienioną integralnością kłębuszków nerkowych lub z chorobą nerek w wywiadzie, po podaniu leku COUMADIN 2 mg może wystąpić ostre uszkodzenie nerek, prawdopodobnie w związku z epizodami nadmiernej antykoagulacji i krwiomoczem [patrz Używaj w określonych populacjach ]. Częstsze monitorowanie leczenia przeciwzakrzepowego jest zalecane u pacjentów z zaburzeniami czynności nerek.
Układowe miażdżycy miażdżycowe i cholesterol mikrozatorowy
Terapia przeciwzakrzepowa z COUMADIN może nasilać uwalnianie zatorów płytek miażdżycowych. Miażdżycowe miażdżycy i mikrozatory cholesterolowe mogą objawiać się różnymi oznakami i objawami w zależności od miejsca embolizacji. Najczęściej zajętymi narządami trzewnymi są nerki, a następnie trzustka, śledziona i wątroba. Niektóre przypadki rozwinęły się w martwicę lub śmierć. Odrębny zespół wynikający z mikrozatorów na stopach jest znany jako „syndrom fioletowych palców”. W przypadku zaobserwowania takich zjawisk należy przerwać terapię COUMADIN. Rozważ alternatywne leki, jeśli konieczne jest kontynuowanie leczenia przeciwzakrzepowego.
Niedokrwienie kończyn, martwica i gangrena u pacjentów z HIT i HITTS
Nie należy stosować leku COUMADIN jako terapii początkowej u pacjentów z trombocytopenią indukowaną heparyną (HIT) oraz z małopłytkowością indukowaną heparyną z zespołem zakrzepicy (HITTS). Przypadki niedokrwienia kończyn, martwicy i zgorzeli występowały u pacjentów z HIT i HITTS po przerwaniu leczenia heparyną i rozpoczęciu lub kontynuowaniu leczenia warfaryną. U niektórych pacjentów następstwa obejmowały amputację zajętego obszaru i/lub śmierć. Leczenie preparatem COUMADIN można rozważyć po normalizacji liczby płytek krwi.
Stosowanie u kobiet w ciąży z mechanicznymi zastawkami serca
COUMADIN może powodować uszkodzenie płodu, gdy jest podawany kobiecie w ciąży. Chociaż COUMADIN jest przeciwwskazany w czasie ciąży, potencjalne korzyści ze stosowania COUMADIN 1 mg mogą przewyższać ryzyko dla kobiet w ciąży z mechanicznymi zastawkami serca, u których występuje wysokie ryzyko wystąpienia choroby zakrzepowo-zatorowej. W takich indywidualnych sytuacjach decyzja o rozpoczęciu lub kontynuacji leczenia COUMADIN 2 mg powinna zostać omówiona z pacjentem, biorąc pod uwagę konkretne zagrożenia i korzyści związane z indywidualną sytuacją medyczną pacjenta, a także najbardziej aktualne wytyczne medyczne. Ekspozycja na COUMADIN podczas ciąży powoduje rozpoznany wzorzec poważnych wad wrodzonych (embriopatia warfarynowa i toksyczność płodowa), śmiertelny krwotok płodowy oraz zwiększone ryzyko samoistnych poronień i śmiertelności płodów. Jeśli lek ten jest stosowany w okresie ciąży lub jeśli pacjentka zajdzie w ciążę podczas przyjmowania tego leku, pacjentkę należy poinformować o potencjalnym zagrożeniu dla płodu [patrz Używaj w określonych populacjach ].
Inne ustawienia kliniczne o zwiększonym ryzyku
następujących warunkach klinicznych ryzyko terapii COUMADIN może być zwiększone:
- Umiarkowane do ciężkiego zaburzenia czynności wątroby
- Choroby zakaźne lub zaburzenia flory jelitowej (np. sprue, antybiotykoterapia)
- Korzystanie z cewnika na stałe
- Nadciśnienie ciężkie do umiarkowanego
- Niedobór odpowiedzi przeciwzakrzepowej, w której pośredniczy białko C: COUMADIN zmniejsza syntezę naturalnie występujących leków przeciwzakrzepowych, białka C i białka S. Dziedziczne lub nabyte niedobory białka C lub jego kofaktora, białka S, są związane z martwicą tkanek po podaniu warfaryny. Jednoczesne leczenie przeciwzakrzepowe heparyną przez 5 do 7 dni na początku leczenia produktem COUMADIN 2 mg może zminimalizować częstość występowania martwicy tkanek u tych pacjentów.
- Chirurgia oka: W operacji zaćmy stosowanie COUMADIN wiązało się ze znacznym wzrostem drobnych powikłań związanych z ostrą igłą i znieczuleniem miejscowym, ale nie było związane z potencjalnie zagrażającymi wzrokiem powikłaniami krwotocznymi. Ponieważ zaprzestanie lub zmniejszenie dawki leku COUMADIN w dawce 5 mg może prowadzić do poważnych powikłań zakrzepowo-zatorowych, decyzja o przerwaniu leczenia produktem COUMADIN przed stosunkowo mniej inwazyjną i złożoną operacją oka, taką jak chirurgia soczewek, powinna być oparta na ocenie ryzyka leczenia przeciwzakrzepowego w stosunku do korzyści.
- Czerwienica prawdziwa
- Zapalenie naczyń
- Cukrzyca
Endogenne czynniki wpływające na INR
Za zwiększoną odpowiedź INR mogą odpowiadać następujące czynniki: biegunka, zaburzenia czynności wątroby, zły stan odżywienia, biegunka tłuszczowa lub niedobór witaminy K.
Za zmniejszoną odpowiedź INR mogą odpowiadać następujące czynniki: zwiększone spożycie witaminy K lub dziedziczna oporność na warfarynę.
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( Przewodnik po lekach ).
Instrukcje dla pacjentów
Doradź pacjentom:
- Ściśle przestrzegaj przepisanego schematu dawkowania [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
- W przypadku pominięcia przepisanej dawki leku COUMADIN 1 mg, należy przyjąć dawkę tak szybko, jak to możliwe tego samego dnia, ale nie należy stosować dawki podwójnej leku COUMADIN 5 mg następnego dnia w celu uzupełnienia pominiętych dawek [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
- Uzyskaj testy czasu protrombinowego i regularnie odwiedzaj swojego lekarza lub klinikę w celu monitorowania terapii [patrz DAWKOWANIE I SPOSÓB PODAWANIA ] .
- Należy pamiętać, że jeśli leczenie preparatem COUMADIN zostanie przerwane, działanie przeciwzakrzepowe preparatu COUMADIN 5 mg może utrzymywać się przez około 2 do 5 dni [patrz FARMAKOLOGIA KLINICZNA ].
- Unikaj wszelkiej aktywności lub sportu, które mogą spowodować urazy [patrz Używaj w określonych populacjach ]. I powiedzieć swojemu lekarzowi, jeśli często upada, ponieważ może to zwiększyć ryzyko powikłań.
- Stosuj normalną, zbilansowaną dietę, aby utrzymać stałe spożycie witaminy K. Unikaj drastycznych zmian w nawykach żywieniowych, takich jak spożywanie dużych ilości zielonych warzyw liściastych [patrz INTERAKCJE Z LEKAMI ].
- Skontaktuj się ze swoim lekarzem, aby zgłosić każdą poważną chorobę, taką jak ciężka biegunka, infekcja lub gorączka [patrz OSTRZEŻENIA I ŚRODKI oraz DZIAŁANIA NIEPOŻĄDANE ].
- Nosić przy sobie dowód potwierdzający, że biorą COUMADIN.
Ryzyko krwawienia
Doradź pacjentom
- Należy natychmiast powiadomić lekarza, jeśli wystąpią jakiekolwiek nietypowe krwawienia lub objawy. Oznaki i objawy krwawienia obejmują: ból, obrzęk lub dyskomfort, przedłużone krwawienie z ran ciętych, zwiększone krwawienie miesiączkowe lub krwawienie z pochwy, krwawienie z nosa, krwawienie z dziąseł podczas szczotkowania, nietypowe krwawienie lub zasinienie, czerwony lub ciemnobrązowy mocz, czerwone lub smoliste czarne stolce, ból głowy, zawroty głowy lub osłabienie [patrz PUDEŁKO OSTRZEŻENIE oraz OSTRZEŻENIA I ŚRODKI ].
Jednoczesne Leki I Rośliny (Zioła)
Doradź pacjentom:
- Nie zażywaj ani nie odstawiaj żadnych innych leków, w tym salicylanów (np. aspiryny i miejscowych środków przeciwbólowych), innych leków dostępnych bez recepty oraz produktów botanicznych (ziołowych), chyba że za poradą lekarza [patrz INTERAKCJE Z LEKAMI ].
Ciąża i karmienie
Doradź pacjentom:
- Skontaktuj się ze swoim lekarzem
- natychmiast, jeśli myślą, że są w ciąży [patrz Używaj w określonych populacjach ],
- omówić planowanie ciąży [patrz Używaj w określonych populacjach ],
- jeśli rozważają karmienie piersią [patrz Używaj w określonych populacjach ].
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Nie przeprowadzono badań rakotwórczości, mutagenności ani płodności warfaryny.
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
COUMADIN 1 mg jest przeciwwskazany u kobiet w ciąży, z wyjątkiem kobiet w ciąży z mechanicznymi zastawkami serca, u których występuje wysokie ryzyko wystąpienia choroby zakrzepowo-zatorowej, i dla których korzyści wynikające ze stosowania leku COUMADIN 5 mg mogą przewyższać ryzyko [patrz OSTRZEŻENIA I ŚRODKI ]. COUMADIN 1mg może spowodować uszkodzenie płodu. Ekspozycja na warfarynę w pierwszym trymestrze ciąży spowodowała występowanie wad wrodzonych u około 5% narażonego potomstwa. Ponieważ dane te nie zostały zebrane w odpowiednich i dobrze kontrolowanych badaniach, częstość występowania poważnych wad wrodzonych nie jest odpowiednią podstawą do porównania z szacowaną częstością występowania w grupie kontrolnej lub w populacji ogólnej USA i może nie odzwierciedlać częstości występowania obserwowanych w praktyce. Rozważ korzyści i ryzyko związane z COUMADIN i możliwe ryzyko dla płodu przepisując COUMADIN kobiecie w ciąży.
Niekorzystne skutki ciąży występują niezależnie od stanu zdrowia matki czy stosowania leków. Szacowane ryzyko tła poważnych wad wrodzonych i poronienia dla wskazanej populacji jest nieznane. W ogólnej populacji Stanów Zjednoczonych szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2% do 4% i 15% do 20%.
Rozważania kliniczne
Działania niepożądane u płodu/noworodka
ludzi warfaryna przenika przez łożysko, a jej stężenia w osoczu płodowym zbliżają się do wartości matczynych. Ekspozycja na warfarynę w pierwszym trymestrze ciąży spowodowała występowanie wad wrodzonych u około 5% narażonego potomstwa. Embriopatia warfarynowa charakteryzuje się hipoplazją nosa z nasadami nasadowymi lub bez (chondrodysplasia punctata) oraz opóźnieniem wzrostu (w tym niską masą urodzeniową). Zgłaszano również nieprawidłowości ośrodkowego układu nerwowego i oka, w tym dysplazję grzbietowej linii środkowej charakteryzującą się agenezją ciała modzelowatego, malformację Dandy-Walkera, zanik móżdżku linii środkowej i dysplazję linii środkowej brzusznej charakteryzującą się zanikiem nerwu wzrokowego. Po ekspozycji na warfarynę w drugim i trzecim trymestrze ciąży zgłaszano opóźnienie umysłowe, ślepotę, schizencefalię, małogłowie, wodogłowie i inne niepożądane skutki ciąży [patrz PRZECIWWSKAZANIA ].
Laktacja
Podsumowanie ryzyka
ograniczonym opublikowanym badaniu warfaryna nie była obecna w mleku matek leczonych warfaryną. Ze względu na możliwość wystąpienia poważnych działań niepożądanych, w tym krwawienia u niemowlęcia karmionego piersią, należy wziąć pod uwagę korzyści rozwojowe i zdrowotne wynikające z karmienia piersią, a także kliniczne zapotrzebowanie matki na COUMADIN oraz wszelkie potencjalne niepożądane skutki stosowania COUMADIN 2 mg na karmione piersią niemowlę przed przepisaniem COUMADIN 5mg kobiecie w okresie laktacji.
Rozważania kliniczne
Monitoruj niemowlęta karmiące piersią pod kątem siniaków lub krwawień.
Dane
Dane ludzkie
Na podstawie opublikowanych danych dotyczących 15 matek karmiących piersią nie wykryto warfaryny w mleku ludzkim. Spośród 15 noworodków urodzonych o czasie, 6 niemowląt karmionych piersią miało udokumentowane czasy protrombinowe w oczekiwanym zakresie. Nie uzyskano czasów protrombinowych dla pozostałych 9 niemowląt karmionych piersią. Skutki u wcześniaków nie zostały ocenione.
Kobiety i mężczyźni o potencjale rozrodczym
Testy ciążowe
COUMADIN może spowodować uszkodzenie płodu [patrz Używaj w określonych populacjach ].
Przed rozpoczęciem terapii COUMADIN należy zweryfikować stan ciąży samic o potencjale rozrodczym.
Zapobieganie ciąży
Kobiety
Doradzić kobietom w wieku rozrodczym stosowanie skutecznej antykoncepcji podczas leczenia i przez co najmniej 1 miesiąc po przyjęciu ostatniej dawki leku COUMADIN.
Zastosowanie pediatryczne
Nie przeprowadzono odpowiednich i dobrze kontrolowanych badań produktu COUMADIN w żadnej populacji pediatrycznej, a optymalne dawkowanie, bezpieczeństwo i skuteczność u dzieci nie są znane. Stosowanie leku COUMADIN w pediatrii opiera się na danych i zaleceniach dotyczących dorosłych oraz dostępnych ograniczonych danych dotyczących dzieci z badań obserwacyjnych i rejestrów pacjentów. Pacjenci pediatryczni, którym podawano COUMADIN 1 mg, powinni unikać jakiejkolwiek aktywności lub sportu, które mogą skutkować urazem.
Rozwijający się układ hemostatyczny u niemowląt i dzieci powoduje zmianę fizjologii zakrzepicy i odpowiedzi na leki przeciwzakrzepowe. Dawkowanie warfaryny w populacji pediatrycznej różni się w zależności od wieku pacjenta, przy czym niemowlęta na ogół mają najwyższe, a młodzież najmniejsze dawki w miligramach na kilogram, aby utrzymać docelowe wartości INR. Ze względu na zmieniające się zapotrzebowanie na warfarynę ze względu na wiek, stosowane jednocześnie leki, dietę i istniejący stan chorobowy, osiągnięcie i utrzymanie docelowych zakresów INR może być trudne do osiągnięcia i utrzymania u pacjentów pediatrycznych, dlatego zaleca się częstsze określanie INR.
Częstość krwawień różniła się w zależności od populacji pacjentów i ośrodka opieki klinicznej w pediatrycznych badaniach obserwacyjnych i rejestrach pacjentów.
Niemowlęta i dzieci otrzymujące żywienie suplementowane witaminą K, w tym preparaty dla niemowląt, mogą być oporne na leczenie warfaryną, podczas gdy niemowlęta karmione mlekiem kobiecym mogą być wrażliwe na leczenie warfaryną.
Zastosowanie geriatryczne
Spośród całkowitej liczby pacjentów otrzymujących warfarynę sodową w kontrolowanych badaniach klinicznych, dla których dostępne były dane do analizy, 1885 pacjentów (24,4%) miało 65 lat i więcej, a 185 pacjentów (2,4%) miało 75 lat i więcej. Nie zaobserwowano ogólnych różnic w skuteczności lub bezpieczeństwie między tymi pacjentami a młodszymi pacjentami, ale nie można wykluczyć większej wrażliwości niektórych starszych osób.
Pacjenci w wieku 60 lat lub starsi wydają się wykazywać większą niż oczekiwano odpowiedź INR na przeciwzakrzepowe działanie warfaryny [patrz FARMAKOLOGIA KLINICZNA ]. COUMADIN jest przeciwwskazany u każdego nienadzorowanego pacjenta ze starością. Należy zachować ostrożność podczas podawania leku COUMADIN pacjentom w podeszłym wieku w każdej sytuacji lub w jakimkolwiek stanie fizycznym, w którym występuje dodatkowe ryzyko krwotoku. Rozważyć mniejsze dawki początkowe i podtrzymujące produktu COUMADIN u pacjentów w podeszłym wieku [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Zaburzenia czynności nerek
Uważa się, że klirens nerkowy jest drugorzędnym wyznacznikiem odpowiedzi przeciwzakrzepowej na warfarynę. Nie ma konieczności dostosowania dawki u pacjentów z zaburzeniami czynności nerek. Należy poinstruować pacjentów z zaburzeniami czynności nerek przyjmujących warfarynę, aby częściej monitorowali swój wskaźnik INR [patrz OSTRZEŻENIA I ŚRODKI ].
Niewydolność wątroby
Zaburzenia czynności wątroby mogą nasilać odpowiedź na warfarynę poprzez upośledzoną syntezę czynników krzepnięcia i zmniejszony metabolizm warfaryny. Należy zachować ostrożność podczas stosowania leku COUMADIN u tych pacjentów.
PRZEDAWKOWAĆ
Objawy i symptomy
Krwawienie (np. pojawienie się krwi w kale lub moczu, krwiomocz, nadmierne krwawienie miesiączkowe, smoliste stolce, wybroczyny, nadmierne siniaczenie lub uporczywe sączenie z powierzchownych urazów, niewyjaśniony spadek stężenia hemoglobiny) jest przejawem nadmiernej antykoagulacji.
Leczenie
Leczenie nadmiernej antykoagulacji opiera się na poziomie INR, obecności lub braku krwawienia oraz okolicznościach klinicznych. Odwrócenie działania przeciwzakrzepowego preparatu COUMADIN 2 mg można uzyskać, przerywając leczenie preparatem COUMADIN 1 mg i, jeśli to konieczne, podając witaminę K1 doustnie lub pozajelitowo.
Zastosowanie witaminy K1 zmniejsza odpowiedź na dalszą terapię COUMADIN, a pacjenci mogą powrócić do stanu zakrzepowego sprzed leczenia po szybkim odwróceniu przedłużonego INR. Wznowienie podawania COUMADIN 2 mg odwraca działanie witaminy K, a terapeutyczny INR można ponownie uzyskać poprzez staranne dostosowanie dawki. Jeśli wskazana jest szybka powtórna antykoagulacja, heparyna może być preferowana w początkowym leczeniu.
Koncentrat kompleksu protrombiny (PCC), świeżo mrożone osocze lub leczenie aktywowanym czynnikiem VII można rozważyć, jeśli konieczne jest pilne odwrócenie działania produktu COUMADIN 2 mg. Stosowanie produktów krwiopochodnych wiąże się z ryzykiem zapalenia wątroby i innych chorób wirusowych; PCC i aktywowany czynnik VII są również związane ze zwiększonym ryzykiem zakrzepicy. Dlatego preparaty te należy stosować wyłącznie w wyjątkowych lub zagrażających życiu epizodach krwawienia w następstwie przedawkowania produktu COUMADIN 2 mg.
PRZECIWWSKAZANIA
COUMADIN 1mg jest przeciwwskazany w:
- Ciąża
COUMADIN 2 mg jest przeciwwskazany u kobiet w ciąży, z wyjątkiem kobiet w ciąży z mechanicznymi zastawkami serca, u których występuje wysokie ryzyko wystąpienia choroby zakrzepowo-zatorowej [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ]. COUMADIN 2 mg może powodować uszkodzenie płodu, gdy jest podawany kobiecie w ciąży. Ekspozycja na COUMADIN podczas ciąży powoduje rozpoznany wzorzec poważnych wad wrodzonych (embriopatia warfarynowa i toksyczność płodowa), śmiertelny krwotok płodowy oraz zwiększone ryzyko samoistnych poronień i śmiertelności płodów. Jeśli COUMADIN jest stosowany w okresie ciąży lub jeśli pacjentka zajdzie w ciążę podczas przyjmowania tego leku, pacjentkę należy poinformować o potencjalnym zagrożeniu dla płodu [patrz Używaj w określonych populacjach ].
COUMADIN jest przeciwwskazany u pacjentów z:
- Skłonności krwotoczne lub dyskrazja krwi
- Niedawna lub planowana operacja ośrodkowego układu nerwowego lub oka albo operacja pourazowa skutkująca dużymi otwartymi powierzchniami [patrz OSTRZEŻENIA I ŚRODKI ]
- Tendencje krwawień związane z:
- Czynne owrzodzenie lub jawne krwawienie z przewodu pokarmowego, układu moczowo-płciowego lub układu oddechowego
- Krwotok do ośrodkowego układu nerwowego
- Tętniaki mózgu, preparowanie aorty
- Zapalenie osierdzia i wysięk osierdziowy
- Bakteryjne zapalenie wsierdzia
- Zagrożona aborcja, rzucawka i stan przedrzucawkowy
- Nienadzorowani pacjenci ze stanami związanymi z potencjalnie wysokim poziomem niezgodności
- Nakłucie kręgosłupa i inne procedury diagnostyczne lub terapeutyczne z możliwością niekontrolowanego krwawienia
- Nadwrażliwość na warfarynę lub jakikolwiek inny składnik tego produktu (np. anafilaksja) [patrz DZIAŁANIA NIEPOŻĄDANE ]
- Duże znieczulenie przewodowe lub lędźwiowe
- Nadciśnienie złośliwe
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Warfaryna działa poprzez hamowanie syntezy czynników krzepnięcia zależnych od witaminy K, w tym czynników II, VII, IX i X oraz białek przeciwzakrzepowych C i S. Witamina K jest niezbędnym kofaktorem w postrysomalnej syntezie witaminy K- zależne czynniki krzepnięcia. Witamina K promuje biosyntezę reszt kwasu γ-karboksyglutaminowego w białkach niezbędnych do aktywności biologicznej. Uważa się, że warfaryna zakłóca syntezę czynnika krzepnięcia poprzez hamowanie podjednostki C1 kompleksu enzymu reduktazy epoksydowej witaminy K (VKORC1), zmniejszając tym samym regenerację epoksydu witaminy K1 [patrz Farmakogenomika ].
Farmakodynamika
Efekt przeciwzakrzepowy na ogół występuje w ciągu 24 godzin po podaniu warfaryny. Jednak maksymalne działanie przeciwzakrzepowe może być opóźnione o 72 do 96 godzin. Czas działania pojedynczej dawki racemicznej warfaryny wynosi od 2 do 5 dni. Efekty COUMADIN 1mg mogą stać się bardziej wyraźne, gdy efekty dziennych dawek podtrzymujących nakładają się. Jest to zgodne z okresami półtrwania zaatakowanych czynników krzepnięcia zależnych od witaminy K i białek przeciwkrzepliwych: czynnik II – 60 godzin, VII – 4 do 6 godzin, IX – 24 godziny, X – 48 do 72 godzin, a białka C i S są odpowiednio około 8 godzin i 30 godzin.
Farmakokinetyka
COUMADIN jest mieszaniną racemiczną enancjomerów R i S warfaryny. Enancjomer S wykazuje 2 do 5 razy większą aktywność antykoagulacyjną niż enancjomer R u ludzi, ale generalnie ma szybszy klirens.
Wchłanianie
Warfaryna jest zasadniczo całkowicie wchłaniana po podaniu doustnym, osiągając maksymalne stężenie w ciągu pierwszych 4 godzin.
Dystrybucja
Warfaryna podlega dystrybucji w stosunkowo małej pozornej objętości dystrybucji wynoszącej około 0,14 l/kg. Fazę dystrybucji trwającą od 6 do 12 godzin można odróżnić po szybkim dożylnym lub doustnym podaniu roztworu wodnego. Około 99% leku wiąże się z białkami osocza.
Metabolizm
Eliminacja warfaryny odbywa się prawie całkowicie poprzez metabolizm. Warfaryna jest metabolizowana stereoselektywnie przez enzymy mikrosomalne wątrobowego cytochromu P-450 (CYP450) do nieaktywnych hydroksylowanych metabolitów (główna droga) oraz przez reduktazy do zredukowanych metabolitów (alkohole warfaryny) przy minimalnym działaniu przeciwzakrzepowym. Zidentyfikowane metabolity warfaryny obejmują dehydrowarfarynę, dwa alkohole diastereoizomeryczne oraz 4'-, 6-, 7-, 8- i 10-hydroksywarfarynę. Do izoenzymów CYP450 biorących udział w metabolizmie warfaryny należą CYP2C9, 2C19, 2C8, 2C18, 1A2 i 3A4. CYP2C9, enzym polimorficzny, jest prawdopodobnie główną postacią CYP450 ludzkiej wątroby, która moduluje aktywność przeciwzakrzepową warfaryny in vivo. Pacjenci z jednym lub większą liczbą wariantów alleli CYP2C9 mają zmniejszony klirens S-warfaryny [patrz Farmakogenomika ].
Wydalanie
Końcowy okres półtrwania warfaryny po podaniu pojedynczej dawki wynosi około 1 tygodnia; jednak efektywny okres półtrwania wynosi od 20 do 60 godzin, ze średnią około 40 godzin. Klirens R-warfaryny jest na ogół o połowę mniejszy niż S-warfaryny, a zatem ponieważ objętości dystrybucji są podobne, okres półtrwania Rwarfaryny jest dłuższy niż S-warfaryny. Okres półtrwania R-warfaryny wynosi od 37 do 89 godzin, a S-warfaryny od 21 do 43 godzin. Badania z radioznakowanym lekiem wykazały, że do 92% podanej doustnie dawki jest wydalane z moczem. Bardzo mało warfaryny jest wydalane w postaci niezmienionej z moczem. Wydalanie z moczem ma postać metabolitów.
Pacjenci geriatryczni
Pacjenci w wieku 60 lat lub starsi wydają się wykazywać większą niż oczekiwano odpowiedź INR na przeciwzakrzepowe działanie warfaryny. Przyczyna zwiększonej wrażliwości na działanie przeciwzakrzepowe warfaryny w tej grupie wiekowej jest nieznana, ale może wynikać z połączenia czynników farmakokinetycznych i farmakodynamicznych. Ograniczone informacje sugerują, że nie ma różnicy w klirensie S-warfaryny; jednak może wystąpić nieznaczny spadek klirensu R-warfaryny u osób starszych w porównaniu z młodymi. Dlatego wraz ze wzrostem wieku pacjenta zwykle wymagana jest mniejsza dawka warfaryny, aby uzyskać terapeutyczny poziom antykoagulacji [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Azjatyccy pacjenci
Pacjenci pochodzenia azjatyckiego mogą wymagać mniejszych początkowych i podtrzymujących dawek warfaryny. W niekontrolowanym badaniu 151 chińskich pacjentów ambulatoryjnych, ustabilizowanych na warfarynie z różnych wskazań, średnie dzienne zapotrzebowanie na warfarynę wynosiło 3,3 ± 1,4 mg, aby osiągnąć INR od 2 do 2,5. Najważniejszym wyznacznikiem zapotrzebowania na warfarynę u tych pacjentów był wiek pacjentów, przy czym zapotrzebowanie na warfarynę stopniowo zmniejszało się wraz z wiekiem.
Farmakogenomika
Polimorfizmy CYP2C9 i VKORC1
Enancjomer S warfaryny jest metabolizowany głównie do 7-hydroksywarfaryny przez CYP2C9, enzym polimorficzny. Warianty alleli, CYP2C9*2 i CYP2C9*3, powodują zmniejszoną in vitro 7-hydroksylację enzymatyczną CYP2C9 S-warfaryny. Częstość występowania tych alleli u osób rasy kaukaskiej wynosi około 11% i 7% odpowiednio dla CYP2C9*2 i CYP2C9*3.
Inne allele CYP2C9 związane ze zmniejszoną aktywnością enzymatyczną występują z mniejszą częstością, w tym allele *5, *6 i *11 w populacjach pochodzenia afrykańskiego oraz allele *5, *9 i *11 u rasy kaukaskiej.
Warfaryna ogranicza regenerację witaminy K z epoksydu witaminy K w cyklu witaminy K poprzez hamowanie VKOR, kompleksu enzymów wielobiałkowych. Pewne polimorfizmy pojedynczego nukleotydu w genie VKORC1 (np. .1639G>A) są związane ze zmiennymi wymaganiami w zakresie dawki warfaryny.
Warianty genów VKORC1 i CYP2C9 generalnie wyjaśniają największy odsetek znanych zmienności wymagań dotyczących dawki warfaryny.
Informacje o genotypie CYP2C9 i VKORC1, jeśli są dostępne, mogą pomóc w wyborze początkowej dawki warfaryny [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Studia kliniczne
Migotanie przedsionków
pięciu prospektywnych, randomizowanych, kontrolowanych badaniach klinicznych obejmujących 3711 pacjentów z niereumatycznym AF, warfaryna znacząco zmniejszała ryzyko ogólnoustrojowej choroby zakrzepowo-zatorowej, w tym udaru mózgu (patrz Tabela 4). Zmniejszenie ryzyka wahało się od 60% do 86% we wszystkich z wyjątkiem jednego badania (CAFA: 45%), które zostało wcześnie przerwane z powodu opublikowanych pozytywnych wyników z dwóch z tych badań. Częstość występowania poważnych krwawień w tych badaniach wahała się od 0,6% do 2,7% (patrz Tabela 4).
Badania u pacjentów z AF i zwężeniem zastawki mitralnej sugerują korzyści z leczenia przeciwzakrzepowego COUMADIN [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Mechaniczne i bioprotetyczne zastawki serca
W prospektywnym, randomizowanym, otwartym badaniu z kontrolą dodatnią z udziałem 254 pacjentów z mechanicznymi protezami zastawek serca stwierdzono, że odstęp bez zakrzepowo-zatorowy był znacząco większy u pacjentów leczonych samą warfaryną w porównaniu z pacjentami leczonymi dipirydamolem/aspiryną (p
prospektywnym, otwartym badaniu klinicznym porównującym terapie warfaryną o umiarkowanej (INR 2,65) i wysokiej intensywności (INR 9,0) u 258 pacjentów z mechanicznymi protezami zastawek serca, choroba zakrzepowo-zatorowa występowała z podobną częstością w obu grupach (4,0 i 3,7 zdarzeń na 100). pacjento-lat). Poważne krwawienie było częstsze w grupie o dużym nasileniu. Wyniki tego badania przedstawiono w tabeli 6.
W randomizowanym badaniu z udziałem 210 pacjentów porównującym dwie intensywności terapii warfaryną (INR 2,0-2,25 w porównaniu z INR 2,5-4,0) przez okres trzech miesięcy po wymianie zastawki tkankowej, choroba zakrzepowo-zatorowa występowała z podobną częstością w obu grupach (poważne zdarzenia zatorowe 2,0% w porównaniu z 1,9%, a drobne zdarzenia zatorowe odpowiednio 10,8% w porównaniu z 10,2%). Duże krwotoki wystąpiły u 4,6% pacjentów w grupie o wyższym natężeniu INR w porównaniu do zera w grupie o niższym nasileniu INR.
Zawał mięśnia sercowego
WARIS (The Warfarin Re-Infarction Study) było randomizowanym badaniem z podwójnie ślepą próbą, w którym wzięło udział 1214 pacjentów 2 do 4 tygodni po zawale leczonych warfaryną do docelowego INR wynoszącego 2,8 do 4,8. Pierwszorzędowy punkt końcowy składał się z całkowitej śmiertelności i nawrotowego zawału. Oceniono drugorzędowy punkt końcowy zdarzeń mózgowo-naczyniowych. Średni czas obserwacji pacjentów wyniósł 37 miesięcy. Wyniki dla każdego punktu końcowego oddzielnie, w tym analizę śmierci naczyniowej, przedstawiono w Tabeli 7.
WARIS II (The Warfarin, Aspirin, Re-Infarction Study) było otwartym, randomizowanym badaniem obejmującym 3630 pacjentów hospitalizowanych z powodu ostrego zawału mięśnia sercowego leczonych warfaryną do docelowego INR 2,8 do 4,2, aspiryną 160 mg na dobę lub warfaryną do docelowy INR 2,0 do 2,5 plus aspiryna 75 mg dziennie przed wypisem ze szpitala. Pierwszorzędowy punkt końcowy obejmował zgon, ponowny zawał serca niezakończony zgonem lub udar zakrzepowo-zatorowy. Średni czas obserwacji wynosił około 4 lata. Wyniki dla WARIS II przedstawiono w tabeli 8.
dwóch grupach otrzymujących warfarynę wystąpiło około cztery razy więcej epizodów poważnych krwawień niż w grupie otrzymującej samą aspirynę. Poważne epizody krwawienia nie występowały częściej wśród pacjentów otrzymujących aspirynę z warfaryną niż wśród pacjentów otrzymujących samą warfarynę, ale częstość występowania drobnych krwawień była wyższa w grupie terapii skojarzonej.
INFORMACJA O PACJENCIE
COUMADIN® (COU-ma-din) (warfaryna sodowa)
Jakie są najważniejsze informacje, które powinienem wiedzieć o COUMADIN 5mg?
COUMADIN może powodować krwawienie, które może być poważne i czasami prowadzić do śmierci. Dzieje się tak, ponieważ COUMADIN jest lekiem rozrzedzającym krew, który zmniejsza ryzyko powstawania zakrzepów krwi w organizmie.
- Możesz mieć większe ryzyko krwawienia, jeśli przyjmujesz COUMADIN i:
- masz 65 lat lub więcej
- masz historię krwawienia z żołądka lub jelit
- mieć wysokie ciśnienie krwi (nadciśnienie)
- mieć historię udaru lub „mini udaru” (przejściowy atak niedokrwienny lub TIA)
- masz poważną chorobę serca
- masz niską liczbę krwinek lub raka
- miał uraz, taki jak wypadek lub operacja;
- masz problemy z nerkami
- przyjmować inne leki zwiększające ryzyko krwawienia, w tym:
- lek zawierający heparynę
- inne leki zapobiegające zakrzepom krwi lub ich leczenie
- niesteroidowe leki przeciwzapalne (NLPZ)
- przyjmować sól sodową warfaryny przez długi czas. Substancją czynną leku COUMADIN jest sól sodowa warfaryny.
Poinformuj swojego lekarza, jeśli przyjmujesz którykolwiek z tych leków. Zapytaj swojego lekarza, jeśli nie jesteś pewien, czy Twój lek jest jednym z wymienionych powyżej.
Wiele innych leków może wchodzić w interakcje z COUMADIN 1mg i wpływać na potrzebną dawkę lub zwiększać efekty uboczne COUMADIN 1mg. Nie zmieniaj ani nie odstawiaj żadnych leków ani nie rozpoczynaj nowych leków przed rozmową z lekarzem.
Podczas przyjmowania leku COUMADIN nie należy przyjmować innych leków zawierających sól sodową warfaryny.
- Dostań, żeby twoje regularne badanie krwi sprawdziło twoją odpowiedź na COUMADIN. To badanie krwi nazywa się testem INR. Test INR sprawdza, jak szybko krzepnie Twoja krew. Twój lekarz zdecyduje, które numery INR są dla Ciebie najlepsze. Twoja dawka COUMADIN 2 mg zostanie dostosowana, aby utrzymać INR w docelowym zakresie.
- Zadzwoń do swojego lekarza natychmiast, jeśli wystąpi którykolwiek z następujących objawów krwawienia:
- ból, obrzęk lub dyskomfort
- bóle głowy, zawroty głowy lub osłabienie
- nietypowe siniaki (siniaki, które rozwijają się bez znanej przyczyny lub powiększają się)
- krwotok z nosa
- krwawiące dziąsła
- krwawienie z cięć trwa długo
- krwawienie miesiączkowe lub krwawienie z pochwy, które jest cięższe niż normalnie
- różowy lub brązowy mocz
- czerwone lub czarne stołki
- kaszel krwią
- wymioty krwią lub materiał przypominający fusy z kawy
- Niektóre pokarmy i napoje mogą wchodzić w interakcje z COUMADIN i wpływać na twoje leczenie i dawkę.
- Jedz normalną, zbilansowaną dietę. Porozmawiaj ze swoim lekarzem przed wprowadzeniem jakichkolwiek zmian w diecie. Nie jedz dużych ilości zielonych warzyw liściastych. Zielone warzywa liściaste zawierają witaminę K. Niektóre oleje roślinne zawierają również duże ilości witaminy K. Zbyt dużo witaminy K może osłabić działanie COUMADIN.
- Zawsze mów wszystkim swoim świadczeniodawcom opieki zdrowotnej, że bierzesz COUMADIN.
- Noś lub noś informacje, które bierzesz COUMADIN.
Zobacz „Jakie są możliwe skutki uboczne COUMADIN 1mg?” aby uzyskać więcej informacji na temat skutków ubocznych.
Co to jest KUMADYNA?
COUMADIN jest lekiem na receptę stosowanym do leczenia zakrzepów krwi i zmniejszania szansy tworzenia się zakrzepów krwi w twoim ciele. Zakrzepy krwi mogą powodować udar, zawał serca lub inne poważne schorzenia, jeśli tworzą się w nogach lub płucach.
Kto nie powinien brać COUMADIN?
Nie należy przyjmować leku COUMADIN 5 mg, jeśli:
- ryzyko wystąpienia problemów z krwawieniem jest większe niż możliwe korzyści z leczenia. Twój lekarz zdecyduje, czy COUMADIN jest właśnie dla Ciebie.
- jesteś w ciąży, chyba że masz mechaniczną zastawkę serca. COUMADIN może powodować wady wrodzone, poronienie lub śmierć nienarodzonego dziecka.
- jesteś uczulony na warfarynę lub którykolwiek z pozostałych składników leku COUMADIN. Pełna lista składników leku COUMADIN znajduje się na końcu tej ulotki.
Przed zażyciem COUMADIN
Poinformuj swojego dostawcę opieki zdrowotnej o wszystkich swoich schorzeniach, w tym jeśli:
- masz problemy z krwawieniem
- często spadać
- masz problemy z wątrobą
- masz problemy z nerkami lub jesteś w trakcie dializy
- mieć wysokie ciśnienie krwi
- masz problem z sercem zwany zastoinową niewydolnością serca;
- mieć cukrzycę
- planują operację lub zabieg dentystyczny
- masz jakiekolwiek inne schorzenia
- są w ciąży lub planują zajść w ciążę. Zobacz „Kto nie powinien brać COUMADIN 2mg?” Twój lekarz wykona test ciążowy przed rozpoczęciem leczenia lekiem COUMADIN. Kobiety, które mogą zajść w ciążę, powinny stosować skuteczną antykoncepcję podczas leczenia i przez co najmniej 1 miesiąc po podaniu ostatniej dawki leku COUMADIN.
- karmią piersią. Ty i Twój lekarz powinniście zdecydować, czy będziecie przyjmować COUMADIN i karmić piersią. Sprawdź, czy dziecko nie ma siniaków lub krwawienia, jeśli bierzesz COUMADIN i karmisz piersią.
Powiedz wszystkim swoim świadczeniodawcom i dentystom, że bierzesz COUMADIN. Powinni porozmawiać z lekarzem, który przepisał Ci COUMADIN 1mg, zanim będziesz miał każdy zabieg chirurgiczny lub stomatologiczny. Może być konieczne zatrzymanie leku COUMADIN na krótki czas lub dostosowanie dawki.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe. Niektóre z innych leków mogą wpływać na sposób działania leku COUMADIN. Niektóre leki mogą zwiększać ryzyko krwawienia. Widzieć „Jakie są najważniejsze informacje, które powinienem wiedzieć o COUMADIN?”
Jak powinienem wziąć COUMADIN 1mg?
- Weź COUMADIN 1mg dokładnie jak przepisano. Twój lekarz będzie od czasu do czasu dostosowywał dawkę w zależności od odpowiedzi na COUMADIN.
- Musisz regularnie wykonywać badania krwi i odwiedzać swojego lekarza, aby monitorować swój stan.
- Jeśli przegapisz dawkę COUMADIN, zadzwoń do swojego lekarza. Dawkę należy przyjąć tak szybko, jak to możliwe, tego samego dnia. Nie rób weź podwójną dawkę COUMADIN 5mg następnego dnia, aby uzupełnić pominiętą dawkę.
- Zadzwoń od razu do swojego lekarza, jeśli:
- weź za dużo COUMADIN
- masz biegunkę, infekcję lub gorączkę
- upaść lub zranić się, zwłaszcza jeśli uderzysz się w głowę. Twój lekarz może Cię sprawdzić.
Czego powinienem unikać podczas przyjmowania COUMADIN 5mg?
- Nie uprawiaj żadnej aktywności lub sportu, które mogą spowodować poważne obrażenia.
Jakie są możliwe skutki uboczne COUMADIN?
COUMADIN może powodować poważne skutki uboczne, w tym:
- Widzieć „Jakie są najważniejsze informacje, które powinienem wiedzieć o COUMADIN?”
- Śmierć tkanki skórnej (martwica skóry lub gangrena). Może się to zdarzyć wkrótce po uruchomieniu COUMADIN. Dzieje się tak, ponieważ tworzą się skrzepy krwi i blokują przepływ krwi do obszaru twojego ciała. Zadzwoń do swojego lekarza natychmiast, jeśli odczuwasz ból, kolor lub zmianę temperatury w dowolnym obszarze ciała. Możesz potrzebować natychmiastowej opieki medycznej, aby zapobiec śmierci lub utracie (amputacji) dotkniętej chorobą części ciała.
- Problemy z nerkami. U osób przyjmujących COUMADIN może dojść do uszkodzenia nerek. Poinformuj natychmiast swojego lekarza, jeśli w moczu pojawi się krew. Twój lekarz może częściej wykonywać badania podczas leczenia lekiem COUMADIN 2 mg, aby sprawdzić, czy nie ma krwawienia, jeśli masz już problemy z nerkami.
- „Syndrom fioletowych palców”. Zadzwoń do swojego lekarza natychmiast, jeśli odczuwasz ból w palcach u nóg i wyglądają one na fioletowe lub ciemne.
To nie są wszystkie efekty uboczne COUMADIN. Aby uzyskać więcej informacji, zapytaj swojego lekarza lub farmaceutę. Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1.800-FDA-1088.
Jak przechowywać COUMADIN 5mg?
- Przechowywać COUMADIN w 59 ° F do 86 ° F (15 ° C do 30 ° C).
- Przechowywać COUMADIN 2mg w szczelnie zamkniętym pojemniku
- Trzymaj COUMADIN z dala od światła i wilgoci.
- Postępuj zgodnie z instrukcjami lekarza lub farmaceuty, aby wyrzucić przestarzałą lub nieużywaną COUMADIN.
- Kobiety w ciąży nie powinny dotykać pokruszonych lub przełamanych tabletek COUMADIN.
Lek COUMADIN 1 mg i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu COUMADIN.
Leki są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Nie używaj COUMADIN 5mg w przypadku stanu, na który nie został przepisany. Nie dawaj COUMADIN 2mg innym ludziom, nawet jeśli mają te same objawy, które masz. Może im to zaszkodzić.
Możesz poprosić swojego lekarza lub farmaceutę o informacje o COUMADIN, które są napisane dla pracowników służby zdrowia.
Jakie są składniki tabletek COUMADIN 1mg?
Składnik czynny: sól sodowa warfaryny
Nieaktywne składniki : laktoza, skrobia i stearynian magnezu, dodatkowo:
1 mg: D&C czerwony nr 6 Barium Lake
2 mg: Lak aluminiowy FD&C Blue nr 2 i Lak aluminiowy FD&C Red nr 40
2,5 mg: lak aluminiowy D&C Yellow nr 10 i lak aluminiowy FD&C Blue nr 1
3 mg: lak aluminiowy FD&C Yellow nr 6, lak aluminiowy FD&C Blue nr 2 i lak aluminiowy FD&C Red nr 40
4 mg: FD&C Blue nr 1 Aluminium Lake
5 mg: FD&C Yellow nr 6 Aluminium Lake
mg: FD&C Yellow nr 6 Aluminium Lake i FD&C Blue nr 1 Aluminium Lake
7,5 mg: lak aluminiowy D&C Yellow nr 10 i lak aluminiowy FD&C Yellow nr 6
Ten przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków.
