Prilosec 40mg, 10mg, 20mg Omeprazole Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Prilosec 40mg i jak się go stosuje?
Prilosec 40mg jest lekiem na receptę i dostępnym bez recepty, stosowanym w leczeniu objawów choroby refluksowej przełyku (GERD), wrzodów żołądka i innych stanów spowodowanych nadmiernym wydzielaniem kwasu żołądkowego. Prilosec 10 mg może być stosowany samodzielnie lub z innymi lekami.
Prilosec należy do klasy leków zwanych inhibitorami pompy protonowej.
Nie wiadomo, czy Prilosec 40 mg jest bezpieczny i skuteczny u dzieci w wieku poniżej 1 miesiąca.
Jakie są możliwe skutki uboczne Prilosec 10mg?
Prilosec może powodować poważne działania niepożądane, w tym:
- silny ból brzucha,
- biegunka wodnista lub krwawa,
- nowy lub nietypowy ból nadgarstka, uda, biodra lub pleców,
- drgawki (drgawki),
- małe lub brak oddawania moczu,
- krew w moczu,
- obrzęk,
- szybki przyrost masy ciała,
- zawroty głowy,
- nieregularne bicie serca,
- uczucie zdenerwowania,
- skurcze mięśni,
- skurcze mięśni,
- kaszel,
- uczucie dławienia,
- ból stawów i
- wysypka skórna na policzkach lub ramionach, która pogarsza się pod wpływem światła słonecznego
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze działania niepożądane leku Prilosec obejmują:
- ból brzucha,
- gaz,
- mdłości,
- wymioty,
- biegunka i
- ból głowy
OPIS
Substancją czynną leku PRILOSEC (omeprazol) kapsułki o opóźnionym uwalnianiu jest podstawiony benzimidazol, 5-metoksy-2-[[(4-metoksy-3,5-dimetylo-2-pirydynylo)metylo]sulfinylo]-1H-benzimidazol, związek hamujący wydzielanie kwasu żołądkowego. Jego wzór empiryczny to C17H19N3O3S, o masie cząsteczkowej 345,42. Wzór strukturalny to:
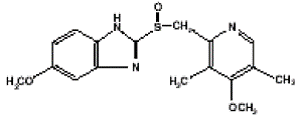
Omeprazol jest krystalicznym proszkiem o barwie od białej do białawej, który topi się z rozkładem w temperaturze około 155°C. Jest słabą zasadą, dobrze rozpuszczalną w etanolu i metanolu, słabo rozpuszczalną w acetonie i izopropanolu oraz bardzo słabo rozpuszczalną w wodzie. Stabilność omeprazolu jest funkcją pH; ulega szybkiej degradacji w środowisku kwaśnym, ale ma akceptowalną stabilność w warunkach alkalicznych.
Substancją czynną preparatu PRILOSEC (omeprazol magnez) do zawiesiny doustnej o opóźnionym uwalnianiu jest 5-metoksy-2-[[(4-metoksy-3,5-dimetylo-2-pirydynylo)metylo]sulfinylo]-1H-benzimidazol, magnez sól (2:1)
Omeprazol magnezowy jest proszkiem o barwie od białej do białawej o temperaturze topnienia z rozkładem w 200°C. Sól jest słabo rozpuszczalna (0,25 mg/ml) w wodzie w 25°C i jest rozpuszczalna w metanolu. Okres półtrwania jest silnie zależny od pH.
Empiryczny wzór omeprazolu magnezowego to (C17H18N3O3S)2 Mg, masa cząsteczkowa to 713,12, a wzór strukturalny to:
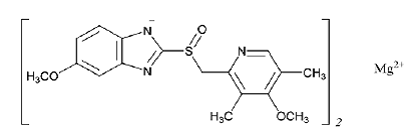
PRILOSEC jest dostarczany w postaci kapsułek o opóźnionym uwalnianiu do podawania doustnego. Każda kapsułka o opóźnionym uwalnianiu zawiera 10 mg, 20 mg lub 40 mg omeprazolu w postaci granulek dojelitowych z następującymi składnikami nieaktywnymi: celuloza, wodorofosforan disodowy, hydroksypropyloceluloza, hypromeloza, laktoza, mannitol, laurylosiarczan sodu i inne składniki. Otoczka kapsułki zawiera następujące składniki nieaktywne: żelatyna-NF, FD&C Blue #1, FD&C Red #40, D&C Red #28, dwutlenek tytanu, syntetyczny czarny tlenek żelaza, izopropanol, alkohol butylowy, FD&C Blue #2, D&C Red #7 Calcium Lake, a ponadto otoczki kapsułek 10 mg i 40 mg zawierają również D&C Yellow #10.
Każde opakowanie leku PRILOSEC do zawiesiny doustnej o opóźnionym uwalnianiu zawiera 2,8 mg lub 11,2 mg omeprazolu magnezowego (co odpowiada 2,5 mg lub 10 mg omeprazolu) w postaci granulek dojelitowych z następującymi składnikami nieaktywnymi: monostearynian glicerolu, hydroksypropyl celuloza, hypromeloza, stearynian magnezu, kopolimer C kwasu metakrylowego, polisorbat, kulki cukrowe, talk i cytrynian trietylu, a także nieaktywne granulki. Granulat nieaktywny składa się z następujących składników: kwas cytrynowy, krospowidon, dekstroza, hydroksypropyloceluloza, tlenek żelaza i guma ksantamowa. Granulki omeprazolu i granulki nieaktywne składają się z wody z wytworzeniem zawiesiny i podaje się je drogą doustną, nosowo-żołądkową lub bezpośrednio dożołądkową.
WSKAZANIA
Leczenie aktywnego wrzodu dwunastnicy
PRILOSEC 20 mg jest wskazany do krótkotrwałego leczenia czynnej choroby wrzodowej dwunastnicy u dorosłych. Większość pacjentów goi się w ciągu czterech tygodni. Niektórzy pacjenci mogą wymagać dodatkowych czterech tygodni terapii.
Eliminacja Helicobacter pylori w celu zmniejszenia ryzyka nawrotu wrzodów dwunastnicy
Wykazano, że eradykacja H. pylori zmniejsza ryzyko nawrotu wrzodu dwunastnicy.
Terapia potrójna
PRILOSEC 40 mg w skojarzeniu z klarytromycyną i amoksycyliną jest wskazany w leczeniu pacjentów z zakażeniem H. pylori i chorobą wrzodową dwunastnicy (czynną lub do 1 roku w wywiadzie) w celu eradykacji H. pylori u dorosłych.
Terapia podwójna
PRILOSEC w skojarzeniu z klarytromycyną jest wskazany w leczeniu pacjentów z zakażeniem H. pylori i chorobą wrzodową dwunastnicy w celu eradykacji H. pylori u dorosłych.
Wśród pacjentów, u których terapia nie powiodła się, PRILOSEC z klarytromycyną jest bardziej prawdopodobnie związany z rozwojem oporności na klarytromycynę w porównaniu z terapią potrójną. U pacjentów, u których terapia nie powiedzie się, należy wykonać badanie lekowrażliwości. W przypadku wykazania oporności na klarytromycynę lub braku możliwości wykonania badania wrażliwości, należy zastosować alternatywne leczenie przeciwbakteryjne [patrz FARMAKOLOGIA KLINICZNA oraz informacje dotyczące przepisywania klarytromycyny, rozdział Mikrobiologia].
Leczenie aktywnego łagodnego wrzodu żołądka
PRILOSEC jest wskazany do krótkotrwałego leczenia (od 4 do 8 tygodni) czynnego, łagodnego wrzodu żołądka u dorosłych.
Leczenie objawowej choroby refluksowej przełyku (GERD)
PRILOSEC jest wskazany w leczeniu zgagi i innych objawów związanych z GERD przez okres do 4 tygodni u pacjentów w wieku 1 roku i starszych.
Leczenie erozyjnego zapalenia przełyku (EE) z powodu GERD za pośrednictwem kwasu
Pacjenci pediatryczni od 1 roku życia do dorosłych
PRILOSEC 20 mg jest wskazany do krótkotrwałego leczenia (4 do 8 tygodni) EE z powodu GERD zależnego od kwasu, który został zdiagnozowany za pomocą endoskopii u pacjentów w wieku 1 roku i starszych.
Skuteczność PRILOSEC 10 mg stosowanego dłużej niż 8 tygodni u pacjentów z EE nie została ustalona. Jeśli pacjent nie zareaguje na 8 tygodni leczenia, można zastosować dodatkowe 4 tygodnie leczenia. W przypadku nawrotu objawów EE lub GERD (np. zgagi) można rozważyć dodatkowe 4-8 tygodniowe kursy PRILOSEC.
Pacjenci pediatryczni od 1 miesiąca do mniej niż 1 roku życia
PRILOSEC jest wskazany do krótkotrwałego leczenia (do 6 tygodni) EE z powodu GERD zależnej od kwasu u dzieci w wieku od 1 miesiąca do mniej niż 1 roku.
Utrzymanie gojenia EE z powodu GERD za pośrednictwem kwasu
PRILOSEC 40 mg jest wskazany do podtrzymującego gojenia EE spowodowanego kwasowym GERD u pacjentów w wieku 1 roku i starszych.
Badania kontrolowane nie trwają dłużej niż 12 miesięcy.
Patologiczne stany nadmiernego wydzielania
PRILOSEC 40 mg jest wskazany do długotrwałego leczenia patologicznych stanów nadmiernego wydzielania (np. zespołu Zollingera-Ellisona, mnogich gruczolaków wewnątrzwydzielniczych i mastocytozy układowej) u dorosłych.
DAWKOWANIE I SPOSÓB PODAWANIA
Zalecany schemat dawkowania dla dorosłych według wskazań
Tabela 1 przedstawia zalecane dawkowanie produktu PRILOSEC 40 mg u dorosłych pacjentów według wskazań.
Zalecany schemat dawkowania u dzieci według wskazań
Tabela 2 przedstawia zalecane dawkowanie produktu PRILOSEC u dzieci i młodzieży według wskazań.
Instrukcje administracyjne
- PRILOSEC 40 mg należy przygotowywać w wodzie i podawać doustnie lub przez sondę nosowo-żołądkową (NG) lub żołądkową.
- Przyjmować PRILOSEC 40mg przed posiłkami.
- Jednocześnie z PRILOSEC można stosować leki zobojętniające sok żołądkowy.
- Pominięte dawki: W przypadku pominięcia dawki należy podać jak najszybciej. Jeśli jednak zbliża się kolejna zaplanowana dawka, nie należy przyjmować pominiętej dawki, a następną należy przyjąć na czas. Nie należy przyjmować dwóch dawek jednocześnie w celu uzupełnienia pominiętej dawki.
Podawanie ustne w wodzie
Podawanie z wodą przez sondę NG lub zgłębnik żołądkowy (rozmiar 6 lub większy)
JAK DOSTARCZONE
Formy dawkowania i mocne strony
PRILOSEC do zawiesiny doustnej o opóźnionym uwalnianiu: 2,5 mg i 10 mg omeprazolu w opakowaniach jednostkowych zawierających drobny żółty proszek, składający się z białych do brązowawych granulek omeprazolu magnezowego i jasnożółtych nieaktywnych granulek.
Składowania i stosowania
PRILOSEC (omeprazol magnezowy) do sporządzania zawiesiny doustnej o opóźnionym uwalnianiu, 2,5 mg lub 10 mg omeprazolu, jest dostarczany w postaci opakowania jednostkowego zawierającego drobny żółty proszek składający się z białych do brązowawych granulek omeprazolu magnezowego i jasnożółtych nieaktywnych granulek. Opakowania jednostkowe PRILOSEC są dostarczane w następujący sposób:
NDC 70515-625-01 opakowania jednostkowe po 30 sztuk: opakowania 2,5 mg NDC 70515-610–01 opakowania jednostkowe po 30 sztuk: opakowania 10 mg
Magazynowanie
Przechowywać PRILOSEC do sporządzania zawiesiny doustnej o opóźnionym uwalnianiu w temperaturze 25°C (77°F); wycieczki dozwolone do 15 – 30°C (59 – 86°F). [Widzieć Temperatura pokojowa kontrolowana przez USP .]
Wyprodukowano dla: Covis Pharma, Zug, 6300 Szwajcaria. Poprawiono: marzec 2022
SKUTKI UBOCZNE
Poniżej oraz w innych miejscach na etykiecie opisano następujące poważne działania niepożądane:
- Ostre cewkowo-śródmiąższowe zapalenie nerek [patrz OSTRZEŻENIA I ŚRODKI ]
- Biegunka związana z Clostridium difficile [patrz OSTRZEŻENIA I ŚRODKI ]
- Złamanie kości [patrz OSTRZEŻENIA I ŚRODKI ]
- Ciężkie skórne reakcje niepożądane [patrz OSTRZEŻENIA I ŚRODKI ]
- Toczeń rumieniowaty skórny i układowy [patrz OSTRZEŻENIA I ŚRODKI ]
- Niedobór cyjanokobalaminy (witaminy B-12) [patrz OSTRZEŻENIA I ŚRODKI ]
- Hipomagnezemia i metabolizm mineralny [patrz OSTRZEŻENIA I ŚRODKI ]
- Polipy gruczołu dna [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych z PRILOSEC
Monoterapia
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Opisane poniżej dane dotyczące bezpieczeństwa odzwierciedlają ekspozycję na kapsułki omeprazolu magnezowego o opóźnionym uwalnianiu u 3096 pacjentów z ogólnoświatowych badań klinicznych (465 pacjentów z badań w USA i 2631 pacjentów z badań międzynarodowych). Wskazania badane klinicznie w badaniach amerykańskich obejmowały wrzód dwunastnicy, wrzód oporny i zespół Zollingera-Ellisona. Międzynarodowe badania kliniczne były projektowane metodą podwójnie ślepej próby i otwartej próby. Najczęściej zgłaszane działania niepożądane (tj. z częstością występowania ≥2%) u pacjentów leczonych PRILOSEC włączonych do tych badań obejmowały ból głowy (7%), ból brzucha (5%), nudności (4%), biegunkę (4%). ), wymioty (3%) i wzdęcia (3%).
Dodatkowe działania niepożądane, które zgłaszano z częstością ≥1%, obejmowały cofanie się kwasu (2%), zakażenie górnych dróg oddechowych (2%), zaparcia (2%), zawroty głowy (2%), wysypkę (2%), astenia (1%). ), ból pleców (1%) i kaszel (1%).
Profil bezpieczeństwa badania klinicznego u pacjentów w wieku powyżej 65 lat był podobny do tego u pacjentów w wieku 65 lat lub młodszych.
Profil bezpieczeństwa badania klinicznego u dzieci i młodzieży otrzymujących kapsułki zawierające omeprazol magnezowy o opóźnionym uwalnianiu był podobny jak u pacjentów dorosłych. Jednak unikalne dla populacji pediatrycznej działania niepożądane ze strony układu oddechowego były często zgłaszane w grupie wiekowej od 1 miesiąca do Używaj w określonych populacjach ].
Doświadczenie w badaniach klinicznych z PRILOSEC 20 mg w terapii skojarzonej w celu eradykacji H. pylori
badaniach klinicznych z zastosowaniem podwójnej terapii omeprazolem magnezowym w kapsułkach o opóźnionym uwalnianiu i klarytromycyną lub potrójnej terapii omeprazolem magnezowym w kapsułkach o opóźnionym uwalnianiu, klarytromycyną i amoksycyliną nie zaobserwowano działań niepożądanych charakterystycznych dla tych skojarzeń leków. Obserwowane działania niepożądane ograniczały się do tych, które zgłaszano wcześniej podczas stosowania samego omeprazolu, klarytromycyny lub amoksycyliny.
Terapia podwójna (omeprazol magnez w kapsułkach o opóźnionym uwalnianiu/klarytromycyna)
Działania niepożądane obserwowane w kontrolowanych badaniach klinicznych z zastosowaniem terapii skojarzonej z omeprazolem w postaci kapsułek o opóźnionym uwalnianiu i klarytromycyną (n = 346), które różniły się od tych opisanych wcześniej dla samego omeprazolu w postaci kapsułek o opóźnionym uwalnianiu, to zaburzenia smaku (15%), przebarwienia języka (2 %), nieżyt nosa (2%), zapalenie gardła (1%) i zespół grypowy (1%). (Aby uzyskać więcej informacji na temat klarytromycyny, należy zapoznać się z informacjami dotyczącymi przepisywania klarytromycyny, punkt „Działania niepożądane”).
Terapia potrójna (omeprazol magnez w kapsułkach o opóźnionym uwalnianiu/klarytromycyna/amoksycylina)
Najczęstszymi działaniami niepożądanymi obserwowanymi w badaniach klinicznych z zastosowaniem terapii skojarzonej z omeprazolem w postaci kapsułek o opóźnionym uwalnianiu, klarytromycyną i amoksycyliną (n = 274) były biegunka (14%), zaburzenia smaku (10%) i ból głowy (7%). Żadne z nich nie występowało z większą częstością niż zgłaszana przez pacjentów przyjmujących same środki przeciwdrobnoustrojowe. (Aby uzyskać więcej informacji na temat klarytromycyny lub amoksycyliny, należy zapoznać się z odpowiednimi informacjami dotyczącymi przepisywania leków, punktami Działania niepożądane).
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania omeprazolu po dopuszczeniu do obrotu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich rzeczywistej częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Ciało jako całość: Reakcje nadwrażliwości, w tym anafilaksja, wstrząs anafilaktyczny, obrzęk naczynioruchowy, skurcz oskrzeli, śródmiąższowe zapalenie nerek, pokrzywka (patrz również Skóra poniżej); gorączka; ból; zmęczenie; złe samopoczucie; toczeń rumieniowaty układowy
Układ sercowo-naczyniowy: Ból w klatce piersiowej lub dusznica bolesna, tachykardia, bradykardia, kołatanie serca, podwyższone ciśnienie krwi, obrzęki obwodowe
Wewnątrzwydzielniczy: Ginekomastia
Przewód pokarmowy: Zapalenie trzustki (niektóre śmiertelne), jadłowstręt, podrażnienie okrężnicy, przebarwienia kału, kandydoza przełyku, zanik błony śluzowej języka, zapalenie jamy ustnej, obrzęk brzucha, suchość w jamie ustnej, mikroskopowe zapalenie okrężnicy, polipy dna.
U pacjentów z zespołem ZE podczas długotrwałego leczenia omeprazolem zgłaszano występowanie rakowiaka żołądka i dwunastnicy. Uważa się, że odkrycie to jest przejawem stanu podstawowego, o którym wiadomo, że jest związany z takimi nowotworami.
Wątrobiany: Choroba wątroby, w tym niewydolność wątroby (niektóre śmiertelne), martwica wątroby (niektóre śmiertelne), encefalopatia wątrobowa choroba komórek wątrobowych, choroba cholestatyczna, mieszane zapalenie wątroby, żółtaczka i podwyższenie wyników testów czynności wątroby [ALT, AST, GGT, fosfataza alkaliczna i bilirubina]
Infekcje i infestacje: Biegunka związana z Clostridium difficile
Zaburzenia metabolizmu i odżywiania: Hipomagnezemia, hipokalcemia, hipokaliemia [Ostrzeżenia i środki ostrożności 5.9], hiponatremia, hipoglikemia, przyrost masy ciała
Układ mięśniowo-szkieletowy: Osłabienie mięśni, ból mięśni, skurcze mięśni, ból stawów, ból nóg, złamanie kości
Układ nerwowy/psychiatryczny: Zaburzenia psychiczne i zaburzenia snu, w tym depresja, pobudzenie, agresja, omamy, splątanie, bezsenność, nerwowość, apatia, senność, lęk i zaburzenia snu; drżenia, parestezje; zawrót głowy
Oddechowy: Krwawienie z nosa, ból gardła
Skóra: Ciężkie uogólnione reakcje skórne, w tym toksyczne SJS/TEN (niektóre śmiertelne), DRESS, AGEP, skórny toczeń rumieniowaty i rumień wielopostaciowy; światłoczułość; pokrzywka; wysypka; zapalenie skóry; świąd; wybroczyny; plamica; łysienie; sucha skóra; nadpotliwość
Zmysły specjalne: Szum w uszach, perwersja smaku
Okular: Zanik nerwu wzrokowego, przednia niedokrwienna neuropatia nerwu wzrokowego, zapalenie nerwu wzrokowego, zespół suchego oka, podrażnienie oka, niewyraźne widzenie, podwójne widzenie
Układ moczowo-płciowy: Śródmiąższowe zapalenie nerek, krwiomocz, białkomocz, podwyższone stężenie kreatyniny w surowicy, mikroskopijny ropomocz, zakażenie dróg moczowych, glikozuria, częste oddawanie moczu, ból jąder
Hematologiczny: Agranulocytoza (niektóre śmiertelne), niedokrwistość hemolityczna, pancytopenia, neutropenia, niedokrwistość, trombocytopenia, leukopenia, leukocytoza
INTERAKCJE Z LEKAMI
Tabele 3 i 4 zawierają leki o klinicznie istotnych interakcjach lekowych i interakcji z diagnostyką, gdy są podawane jednocześnie z omeprazolem, oraz instrukcje dotyczące ich zapobiegania lub postępowania.
Więcej informacji na temat interakcji z IPP można znaleźć na etykietach jednocześnie stosowanych leków.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Obecność nowotworu żołądka
dorosłych objawowa odpowiedź na leczenie PRILOSEC nie wyklucza obecności nowotworu żołądka. Rozważyć dodatkowe badania kontrolne i diagnostyczne u dorosłych pacjentów z suboptymalną odpowiedzią lub wczesnym nawrotem objawów po zakończeniu leczenia PPI. U starszych pacjentów rozważ również endoskopię.
Ostre cewkowo-śródmiąższowe zapalenie nerek
U pacjentów przyjmujących PPI obserwowano ostre cewkowo-śródmiąższowe zapalenie nerek (TIN), które może wystąpić w dowolnym momencie leczenia PPI. Pacjenci mogą wykazywać różne objawy przedmiotowe i podmiotowe, od objawowych reakcji nadwrażliwości po niespecyficzne objawy osłabienia czynności nerek (np. złe samopoczucie, nudności, jadłowstręt). W opisywanych seriach przypadków u niektórych pacjentów zdiagnozowano biopsję i bez objawów pozanerkowych (np. gorączka, wysypka lub ból stawów). Przerwać PRILOSEC 40 mg i ocenić pacjentów z podejrzeniem ostrego TIN [patrz PRZECIWWSKAZANIA ].
Biegunka związana z Clostridium Difficile
Opublikowane badania obserwacyjne sugerują, że terapia PPI, taka jak PRILOSEC, może wiązać się ze zwiększonym ryzykiem biegunki związanej z Clostridium difficile, zwłaszcza u pacjentów hospitalizowanych. Ta diagnoza powinna być brana pod uwagę w przypadku biegunki, która nie ustępuje [patrz DZIAŁANIA NIEPOŻĄDANE ].
Pacjenci powinni stosować najmniejszą dawkę i najkrótszy czas trwania terapii PPI odpowiednio do leczonego stanu.
Biegunkę związaną z Clostridium difficile (CDAD) zgłaszano po zastosowaniu prawie wszystkich środków przeciwbakteryjnych. Więcej informacji dotyczących środków przeciwbakteryjnych (klarytromycyny i amoksycyliny) wskazanych do stosowania w skojarzeniu z preparatem PRILOSEC można znaleźć w punktach Ostrzeżenia i środki ostrożności w odpowiednich informacjach dotyczących przepisywania.
Struktura kości
Kilka opublikowanych badań obserwacyjnych sugeruje, że terapia inhibitorem pompy protonowej (PPI) może wiązać się ze zwiększonym ryzykiem złamań kości udowej, nadgarstka lub kręgosłupa związanych z osteoporozą. Ryzyko złamań było zwiększone u pacjentów otrzymujących duże dawki, definiowane jako wielokrotne dawki dobowe, oraz długotrwałą terapię PPI (rok lub dłużej). Pacjenci powinni stosować najmniejszą dawkę i najkrótszy czas trwania terapii PPI odpowiednio do leczonego stanu. Pacjenci z ryzykiem złamań związanych z osteoporozą powinni być leczeni zgodnie z ustalonymi wytycznymi terapeutycznymi [patrz DAWKOWANIE I SPOSÓB PODAWANIA , DZIAŁANIA NIEPOŻĄDANE ].
Ciężkie skórne reakcje niepożądane
W związku ze stosowaniem IPP zgłaszano występowanie ciężkich skórnych działań niepożądanych, w tym zespołu Stevensa-Johnsona (SJS) i toksycznej martwicy naskórka (TEN), reakcji na lek z eozynofilią i objawami ogólnoustrojowymi (DRESS) oraz ostrej uogólnionej osutki krostkowej (AGEP). [Widzieć DZIAŁANIA NIEPOŻĄDANE ]. Należy odstawić PRILOSEC w przypadku wystąpienia pierwszych oznak lub objawów ciężkich skórnych działań niepożądanych lub innych oznak nadwrażliwości i rozważyć dalszą ocenę.
Toczeń rumieniowaty skórny i układowy
pacjentów przyjmujących IPP, w tym omeprazol, zgłaszano toczeń rumieniowaty skórny (CLE) i toczeń rumieniowaty układowy (SLE). Zdarzenia te miały miejsce zarówno jako nowy początek, jak i zaostrzenie istniejącej choroby autoimmunologicznej. Większość przypadków tocznia rumieniowatego wywołanego przez PPI to CLE.
Najczęstszą postacią CLE zgłaszaną u pacjentów leczonych PPI był podostry CLE (SCLE) i występował w ciągu kilku tygodni lub lat po ciągłej terapii lekowej u pacjentów od niemowląt po osoby starsze. Generalnie zmiany histologiczne były obserwowane bez zajęcia narządów.
Toczeń rumieniowaty układowy (SLE) jest rzadziej zgłaszany niż CLE u pacjentów otrzymujących PPI. SLE związany z PPI jest zwykle łagodniejszy niż SLE nie wywołany lekami. Początek SLE zwykle występował w ciągu kilku dni lub lat po rozpoczęciu leczenia, głównie u pacjentów, od młodych dorosłych po osoby starsze. U większości pacjentów pojawiła się wysypka; jednak zgłaszano również bóle stawów i cytopenię.
Unikaj podawania PPI dłużej niż jest to wskazane medycznie. Jeśli u pacjentów otrzymujących PRILOSEC 10 mg zauważą się objawy przedmiotowe lub podmiotowe zgodne z CLE lub SLE, należy odstawić lek i skierować pacjenta do odpowiedniego specjalisty w celu oceny. Większość pacjentów poprawia się po odstawieniu samego PPI w ciągu 4 do 12 tygodni. Testy serologiczne (np. ANA) mogą być dodatnie, a podwyższone wyniki testów serologicznych mogą ustąpić dłużej niż objawy kliniczne.
Interakcja z klopidogrelem
Należy unikać jednoczesnego stosowania PRILOSEC 10 mg z klopidogrelem. Klopidogrel jest prolekiem. Hamowanie agregacji płytek krwi przez klopidogrel jest w całości spowodowane aktywnym metabolitem. Metabolizm klopidogrelu do jego aktywnego metabolitu może być zaburzony przez jednoczesne stosowanie leków, takich jak omeprazol, które hamują aktywność CYP2C19. Jednoczesne stosowanie klopidogrelu z 80 mg omeprazolu zmniejsza aktywność farmakologiczną klopidogrelu, nawet przy podawaniu w odstępie 12 godzin.
Stosując PRILOSEC, należy rozważyć alternatywną terapię przeciwpłytkową [patrz INTERAKCJE Z LEKAMI oraz FARMAKOLOGIA KLINICZNA ].
Niedobór cyjanokobalaminy (witaminy B-12)
Codzienne leczenie jakimikolwiek lekami hamującymi wydzielanie kwasu przez długi okres czasu (np. dłużej niż 3 lata) może prowadzić do złego wchłaniania cyjanokobalaminy (witaminy B-12) spowodowanego hipo- lub achlorhydrią. W literaturze donoszono o rzadkich przypadkach niedoboru cyjanokobalaminy występującego podczas terapii hamującej wydzielanie kwasu. Rozpoznanie to należy rozważyć, jeśli u pacjentów leczonych produktem PRILOSEC zaobserwuje się objawy kliniczne odpowiadające niedoborowi cyjanokobalaminy.
Hipomagnezemia i metabolizm minerałów
Hipomagnezemię, objawową i bezobjawową, zgłaszano rzadko u pacjentów leczonych IPP przez co najmniej trzy miesiące, w większości przypadków po roku leczenia. Poważne zdarzenia niepożądane obejmują tężyczkę, arytmie i drgawki. Hipomagnezemia może prowadzić do hipokalcemii i/lub hipokaliemii i może nasilać leżącą u podstaw hipokalcemię u pacjentów z grup ryzyka. U większości pacjentów leczenie hipomagnezemii wymagało zastąpienia magnezu i odstawienia PPI.
W przypadku pacjentów, którzy mają być długotrwale leczeni lub przyjmują PPI z lekami, takimi jak digoksyna lub leki, które mogą powodować hipomagnezemię (np. diuretyki), pracownicy służby zdrowia mogą rozważyć monitorowanie poziomu magnezu przed rozpoczęciem leczenia PPI i okresowo [patrz DZIAŁANIA NIEPOŻĄDANE ].
Należy rozważyć monitorowanie stężenia magnezu i wapnia przed rozpoczęciem stosowania produktu PRILOSEC oraz okresowo w trakcie leczenia u pacjentów z wcześniej istniejącym ryzykiem hipokalcemii (np. niedoczynność przytarczyc). W razie potrzeby uzupełnij magnez i/lub wapń. Jeśli hipokalcemia jest oporna na leczenie, należy rozważyć przerwanie PPI.
Interakcja z dziurawcem lub ryfampiną
Leki indukujące CYP2C19 lub CYP3A4 (takie jak ziele dziurawca lub ryfampicyna) mogą znacząco zmniejszać stężenie omeprazolu [patrz INTERAKCJE Z LEKAMI ]. Unikaj jednoczesnego stosowania PRILOSEC z dziurawcem lub ryfampicyną.
Interakcje z badaniami diagnostycznymi guzów neuroendokrynnych
Stężenie chromograniny A (CgA) w surowicy wzrasta wtórnie do wywołanego lekiem zmniejszenia kwasowości żołądka. Podwyższony poziom CgA może powodować fałszywie dodatnie wyniki w badaniach diagnostycznych guzów neuroendokrynnych. Pracownicy służby zdrowia powinni tymczasowo przerwać leczenie PRILOSEC 20 mg co najmniej 14 dni przed oceną poziomu CgA i rozważyć powtórzenie testu, jeśli początkowe poziomy CgA są wysokie. W przypadku wykonywania testów seryjnych (np. w celu monitorowania) do testów należy wykorzystać to samo laboratorium komercyjne, ponieważ zakresy referencyjne między testami mogą się różnić [patrz INTERAKCJE Z LEKAMI ].
Interakcja z metotreksatem
Literatura sugeruje, że jednoczesne stosowanie PPI z metotreksatem (głównie w dużych dawkach) może podwyższać i wydłużać stężenie metotreksatu i/lub jego metabolitu w surowicy, co może prowadzić do toksyczności metotreksatu. W przypadku podawania dużych dawek metotreksatu u niektórych pacjentów można rozważyć tymczasowe odstawienie PPI [patrz INTERAKCJE Z LEKAMI ].
Polipy dna żołądka
Stosowanie PPI wiąże się ze zwiększonym ryzykiem wystąpienia polipów gruczołu dna, które wzrasta przy długotrwałym stosowaniu, zwłaszcza powyżej jednego roku. Większość użytkowników PPI, u których wystąpiły polipy gruczołu dna, była bezobjawowa, a polipy gruczołu dna wykryto przypadkowo podczas endoskopii. Stosuj najkrótszy czas trwania terapii PPI odpowiedni do leczonego stanu.
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( Przewodnik po lekach i instrukcje użytkowania ).
Ostre cewkowo-śródmiąższowe zapalenie nerek
Poinformuj pacjenta lub opiekuna, aby natychmiast skontaktował się z lekarzem pacjenta, jeśli wystąpią objawy związane z ostrym cewkowo-śródmiąższowym zapaleniem nerek [patrz OSTRZEŻENIA I ŚRODKI ].
Biegunka związana z Clostridium Difficile
Poradź pacjentowi lub opiekunowi, aby natychmiast skontaktował się z lekarzem pacjenta, jeśli wystąpi biegunka, która nie ustępuje [patrz OSTRZEŻENIA I ŚRODKI ].
Struktura kości
Poinformuj pacjenta lub opiekuna, aby zgłaszał wszelkie złamania, zwłaszcza biodra, nadgarstka lub kręgosłupa, lekarzowi prowadzącemu pacjenta [patrz OSTRZEŻENIA I ŚRODKI ].
Ciężkie skórne reakcje niepożądane
Poradzić pacjentowi lub opiekunowi, aby zaprzestał stosowania produktu PRILOSEC 40 mg i zgłosił swojemu lekarzowi po pierwszym pojawieniu się ciężkiej skórnej reakcji niepożądanej lub innej oznaki nadwrażliwości [patrz OSTRZEŻENIA I ŚRODKI ].
Toczeń rumieniowaty skórny i układowy
Poradź pacjentowi lub opiekunowi, aby natychmiast skontaktował się z lekarzem pacjenta w przypadku pojawienia się nowych lub pogorszenia objawów związanych z toczniem rumieniowatym skórnym lub układowym [patrz OSTRZEŻENIA I ŚRODKI ]
Niedobór cyjanokobalaminy (witaminy B-12)
Poinformuj pacjenta lub opiekuna, aby zgłaszał lekarzowi pacjenta wszelkie objawy kliniczne, które mogą być związane z niedoborem cyjanokobalaminy, jeśli otrzymywał on PRILOSEC przez okres dłuższy niż 3 lata [patrz OSTRZEŻENIA I ŚRODKI ].
Hipomagnezemia i metabolizm minerałów
Poinformuj pacjenta lub opiekuna, aby zgłaszał lekarzowi pacjenta wszelkie objawy kliniczne, które mogą być związane z hipomagnezemią, hipokalcemią i/lub hipokaliemią, jeśli otrzymywał on PRILOSEC przez co najmniej 3 miesiące [patrz OSTRZEŻENIA I ŚRODKI ].
Interakcje leków
Poradzić pacjentom, aby zgłaszali swojemu lekarzowi, jeśli rozpoczną leczenie produktami zawierającymi rylpiwirynę, klopidogrelem, dziurawcem zwyczajnym lub ryfampiną; lub, jeśli przyjmują duże dawki metotreksatu [patrz PRZECIWWSKAZANIA , OSTRZEŻENIA I ŚRODKI ].
Administracja
- PRILOSEC należy przygotowywać w wodzie i podawać doustnie lub przez sondę nosowo-żołądkową (NG) lub żołądkową, jak opisano w Przewodniku po lekach.
- Przyjmować PRILOSEC przed posiłkami.
- Jednocześnie z PRILOSEC można stosować leki zobojętniające sok żołądkowy.
- Pominięte dawki: W przypadku pominięcia dawki należy podać jak najszybciej. Jeśli jednak zbliża się kolejna zaplanowana dawka, nie należy przyjmować pominiętej dawki, a następną należy przyjąć na czas. Nie należy przyjmować dwóch dawek jednocześnie w celu uzupełnienia pominiętej dawki.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
dwóch 24-miesięcznych badaniach rakotwórczości na szczurach omeprazol w dawkach dobowych 1,7, 3,4, 13,8, 44,0 i 140,8 mg/kg/dobę (około 0,4 do 34 razy większych niż dawka u ludzi 40 mg/dobę wyrażona na powierzchni ciała) powierzchni) wytwarzały rakowiaki z komórek ECL żołądka w sposób zależny od dawki zarówno u samców, jak i samic szczurów; częstość występowania tego efektu była znacznie większa u samic szczurów, które miały wyższe stężenie omeprazolu we krwi. U nieleczonych szczurów rzadko występują rakowiaki żołądka. Ponadto hiperplazja komórek ECL była obecna we wszystkich leczonych grupach obu płci. W jednym z tych badań samicom szczurów podawano 13,8 mg omeprazolu/kg/dobę (około 3,4-krotność dawki ludzkiej 40 mg/dobę, w oparciu o powierzchnię ciała) przez jeden rok, a następnie obserwowano przez kolejny rok bez lek. U tych szczurów nie zaobserwowano rakowiaków. Zwiększoną częstość występowania przerostu komórek ECL związanego z leczeniem zaobserwowano pod koniec jednego roku (94% leczonych vs. 10% grupy kontrolnej). W drugim roku różnica między szczurami leczonymi i kontrolnymi była znacznie mniejsza (46% vs. 26%), ale nadal wykazywała większą hiperplazję w grupie leczonej. Gruczolakorak żołądka zaobserwowano u jednego szczura (2%). Nie zaobserwowano podobnego guza u samców i samic szczurów leczonych przez dwa lata. W przypadku tego szczepu szczura nie odnotowano historycznie podobnego guza, ale stwierdzenie dotyczące tylko jednego guza jest trudne do interpretacji. W 52-tygodniowym badaniu toksyczności u szczurów rasy Sprague-Dawley, gwiaździaki mózgu wykryto u niewielkiej liczby samców, którzy otrzymywali omeprazol w dawkach 0,4, 2 i 16 mg/kg/dobę (około 0,1 do 3,9 razy większych od dawek stosowanych u ludzi 40 mg/dobę, w oparciu o powierzchnię ciała). W tym badaniu nie zaobserwowano gwiaździaków u samic szczurów. W 2-letnim badaniu rakotwórczości u szczurów rasy Sprague-Dawley nie wykryto gwiaździaków u samców ani samic przy dużej dawce 140,8 mg/kg/dobę (około 34-krotność dawki ludzkiej 40 mg/dobę na podstawie powierzchni ciała). . 78-tygodniowe badanie rakotwórczości omeprazolu na myszach nie wykazało zwiększonej częstości występowania guza, ale badanie nie było rozstrzygające. 26-tygodniowe badanie rakotwórczości na myszach transgenicznych p53 (+/-) nie było pozytywne.
Omeprazol wykazał działanie klastogenne w teście aberracji chromosomowych ludzkich limfocytów in vitro, w jednym z dwóch testów mikrojądrowych u myszy in vivo oraz w teście aberracji chromosomowych komórek szpiku kostnego in vivo. Omeprazol dał wynik ujemny w teście Amesa in vitro, teście postępującej mutacji komórek chłoniaka myszy in vitro oraz teście uszkodzenia DNA wątroby szczura in vivo.
Stwierdzono, że omeprazol w dawkach doustnych do 138 mg/kg/dobę u szczurów (około 34-krotność dawki doustnej 40 mg dla ludzi w przeliczeniu na powierzchnię ciała) nie ma wpływu na płodność i zdolności reprodukcyjne.
W 24-miesięcznych badaniach rakotwórczości na szczurach zaobserwowano zależne od dawki, istotne zwiększenie liczby rakowiaków żołądka i przerostu komórek ECL zarówno u samców, jak iu samic [patrz OSTRZEŻENIA I ŚRODKI ]. Nowotwory rakowiaka obserwowano również u szczurów poddanych wycięciu dna oka lub długotrwałemu leczeniu innymi inhibitorami pompy protonowej lub dużymi dawkami antagonistów receptora H2.
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
Nie ma odpowiednich i dobrze kontrolowanych badań omeprazolu u kobiet w ciąży. Dostępne dane epidemiologiczne nie wykazują zwiększonego ryzyka poważnych wrodzonych wad rozwojowych lub innych niepożądanych skutków ciąży w przypadku stosowania omeprazolu w pierwszym trymestrze ciąży. Badania reprodukcji przeprowadzone na szczurach i królikach wykazały zależną od dawki śmiertelność zarodków przy dawkach omeprazolu około 3,4 do 34 razy większych od dawki doustnej 40 mg stosowanej u ludzi (w oparciu o powierzchnię ciała osoby o masie 60 kg).
Nie zaobserwowano działania teratogennego w badaniach reprodukcji na zwierzętach, w których podawano doustnie esomeprazol (enancjomer omeprazolu) magnezowego szczurom i królikom podczas organogenezy w dawkach odpowiednio około 68-krotnych i 42-krotnych po doustnym podaniu ludziom 40 mg esomeprazolu lub 40 mg omeprazolu ( w oparciu o powierzchnię ciała osoby o wadze 60 kg).
Zmiany w morfologii kości obserwowano u potomstwa szczurów, którym przez większą część ciąży i laktacji podawano dawki równe lub większe niż około 34-krotność doustnej dawki 40 mg esomeprazolu lub 40 mg omeprazolu stosowanej u ludzi. Gdy podawanie matczyne ograniczało się tylko do okresu ciąży, nie stwierdzono wpływu na morfologię nasad kości u potomstwa w każdym wieku [patrz Dane ].
Szacowane ryzyko tła poważnych wad wrodzonych i poronienia dla wskazanej populacji jest nieznane. Wszystkie ciąże wiążą się z ryzykiem wady wrodzonej, utraty lub innych niekorzystnych skutków. W ogólnej populacji Stanów Zjednoczonych szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2% do 4% i 15% do 20%.
Dane
Dane ludzkie
czterech opublikowanych badaniach epidemiologicznych porównywano częstość nieprawidłowości wrodzonych u niemowląt urodzonych przez kobiety, które stosowały omeprazol w czasie ciąży, z częstością nieprawidłowości u niemowląt kobiet narażonych na antagonistów receptora H2 lub innych grup kontrolnych.
Populacyjne retrospektywne badanie epidemiologiczne kohortowe ze Szwedzkiego Rejestru Narodzin, obejmujące około 99% ciąż, w latach 1995-99, zgłoszono na 955 niemowlętach (824 narażonych w pierwszym trymestrze, 39 z nich narażonych po pierwszym trymestrze, a 131 narażonych po pierwszym trymestrze), których matki stosowały omeprazol w okresie ciąży. Liczba niemowląt narażonych w okresie życia płodowego na omeprazol, u których wystąpiły jakiekolwiek wady rozwojowe, niska masa urodzeniowa, niska punktacja w skali Apgar lub hospitalizacja była podobna do liczby obserwowanej w tej populacji. Liczba niemowląt urodzonych z wadami przegrody międzykomorowej oraz liczba niemowląt martwo urodzonych była nieco wyższa u niemowląt narażonych na działanie omeprazolu niż oczekiwana liczba w tej populacji.
Populacyjne retrospektywne badanie kohortowe obejmujące wszystkie żywe urodzenia w Danii w latach 1996-2009 wykazało 1800 żywych urodzeń, których matki stosowały omeprazol w pierwszym trymestrze ciąży i 837 317 żywych urodzeń, których matki nie stosowały żadnego inhibitora pompy protonowej. Ogólny odsetek wad wrodzonych u niemowląt matek narażonych w pierwszym trymestrze na omeprazol wynosił 2,9% i 2,6% u niemowląt urodzonych przez matki nienarażone na żaden inhibitor pompy protonowej w pierwszym trymestrze ciąży.
W retrospektywnym badaniu kohortowym zgłoszono 689 ciężarnych kobiet narażonych na H2-blokery lub omeprazol w pierwszym trymestrze (134 narażonych na omeprazol) i 1572 ciężarnych nienarażonych na którykolwiek z nich w pierwszym trymestrze ciąży. Całkowity odsetek wad rozwojowych u potomstwa matek, które w pierwszym trymestrze narażono na omeprazol, bloker receptora H2 lub które nie były narażone, wynosił odpowiednio 3,6%, 5,5% i 4,1%.
Małe prospektywne obserwacyjne badanie kohortowe objęło 113 kobiet narażonych na omeprazol w czasie ciąży (89% w pierwszym trymestrze). Zgłaszany odsetek poważnych wrodzonych wad rozwojowych wynosił 4% w grupie omeprazolu, 2% w grupie kontrolnej eksponowanej na substancje nie teratogenne i 2,8% w grupie kontrolnej z parami choroby. Wskaźniki poronień samoistnych i planowych, porodów przedwczesnych, wieku ciążowego w momencie porodu oraz średniej masy urodzeniowej były podobne w obu grupach.
W kilku badaniach nie stwierdzono widocznych krótkoterminowych skutków ubocznych dla niemowlęcia, gdy pojedyncza dawka omeprazolu doustnie lub dożylnie została podana ponad 200 kobietom w ciąży jako premedykacja do cięcia cesarskiego w znieczuleniu ogólnym.
Dane zwierząt
Omeprazol
Badania reprodukcyjne przeprowadzone z omeprazolem na szczurach w dawkach doustnych do 138 mg/kg/dobę (około 34-krotność dawki doustnej 40 mg dla ludzi w przeliczeniu na powierzchnię ciała) i u królików w dawkach do 69,1 mg/kg/dobę ( około 34-krotność doustnej dawki 40 mg dla człowieka na podstawie powierzchni ciała) podczas organogenezy nie ujawniono żadnych dowodów na teratogenny potencjał omeprazolu. U królików omeprazol w dawkach w zakresie od 6,9 do 69,1 mg/kg/dobę (około 3,4 do 34 razy większa od dawki doustnej 40 mg u ludzi na podstawie powierzchni ciała) podawany podczas organogenezy powodował zależne od dawki zwiększenie śmiertelności zarodków. resorpcje płodu i zaburzenia ciąży. U szczurów zaobserwowano zależną od dawki toksyczność embrionalną/płodową oraz toksyczność rozwojową po urodzeniu u potomstwa, którego rodzice byli leczeni omeprazolem w dawce 13,8 do 138,0 mg/kg/dobę (około 3,4 do 34 razy większe niż dawki doustne 40 mg stosowane u ludzi na powierzchni ciała). powierzchni), podawane przed kryciem przez okres laktacji.
Ezomeprazol
Opisane poniżej dane zostały wygenerowane z badań z użyciem esomeprazolu, enancjomeru omeprazolu. Wielokrotność dawek podawanych zwierzętom w stosunku do ludzi opiera się na założeniu równej ogólnoustrojowej ekspozycji na esomeprazol u ludzi po doustnym podaniu 40 mg esomeprazolu lub 40 mg omeprazolu.
Nie zaobserwowano wpływu na rozwój zarodka i płodu w badaniach rozrodu z zastosowaniem ezomeprazolu magnezowego u szczurów w dawkach doustnych do 280 mg/kg mc./dobę (około 68-krotność dawki doustnej 40 mg u ludzi w przeliczeniu na powierzchnię ciała) lub u królików w dawki doustne do 86 mg/kg/dobę (około 42-krotność dawki doustnej 40 mg esomeprazolu lub 40 mg omeprazolu u ludzi na podstawie powierzchni ciała) podawane podczas organogenezy.
Przed- i pourodzeniowe badanie toksyczności rozwojowej u szczurów z dodatkowymi punktami końcowymi w celu oceny rozwoju kości przeprowadzono z zastosowaniem ezomeprazolu magnezowego w dawkach doustnych od 14 do 280 mg/kg mc./dobę (około 3,4 do 68-krotności dawki doustnej 40 mg ezomeprazolu lub 40 mg omeprazolu w przeliczeniu na powierzchnię ciała). Przeżycie noworodkowe/wczesne po urodzeniu (od urodzenia do odstawienia od matki) zmniejszyło się przy dawkach równych lub większych niż 138 mg/kg/dobę (około 34-krotność dawki doustnej 40 mg esomeprazolu lub 40 mg omeprazolu u ludzi na podstawie powierzchni ciała). Masa ciała i przyrost masy ciała uległy zmniejszeniu, a neurobehawioralne lub ogólne opóźnienia rozwojowe w okresie bezpośrednio po odsadzeniu były widoczne przy dawkach równych lub większych niż 69 mg/kg mc./dobę (około 17-krotność doustnej dawki 40 mg ezomeprazolu lub 40 mg omeprazolu w przeliczeniu na powierzchnię ciała). Ponadto zaobserwowano zmniejszoną długość, szerokość i grubość kości udowej, zmniejszoną grubość płytki wzrostowej kości piszczelowej oraz minimalną lub łagodną hipokomórkowość szpiku kostnego przy dawkach równych lub większych niż 14 mg/kg/dobę (około 3,4-krotność 40 mg esomeprazolu lub 40 mg omeprazolu na podstawie powierzchni ciała). Dysplazja nasad kości udowej była obserwowana u potomstwa szczurów, którym podawano doustne dawki ezomeprazolu magnezowego w dawkach równych lub większych niż 138 mg/kg mc./dobę (około 34-krotność dawki doustnej 40 mg esomeprazolu lub 40 mg omeprazolu stosowanego u ludzi na organizm). podstawy powierzchni).
Wpływ na kości matki obserwowano u ciężarnych i karmiących samic szczurów w badaniu toksyczności przed- i poporodowej, gdy esomeprazol magnezowy podawano doustnie w dawkach od 14 do 280 mg/kg mc./dobę (około 3,4 do 68 razy więcej niż doustna dawka 40 mg esomeprazolu u ludzi lub 40 mg omeprazolu na powierzchnię ciała). Gdy szczurom podawano dawkę od 7. dnia ciąży do odsadzenia w 21. dniu po urodzeniu, zaobserwowano statystycznie istotny spadek masy kości udowej matki do 14% (w porównaniu z leczeniem placebo) przy dawkach równych lub większych niż 138 mg/kg/dobę (około 34-krotność doustnej dawki 40 mg esomeprazolu lub 40 mg omeprazolu dla człowieka na podstawie powierzchni ciała).
Badanie rozwoju przed- i pourodzeniowego u szczurów, którym podawano ezomeprazol stront (stosując dawki równomolowe w porównaniu z badaniem ezomeprazolu magnezowego) dało podobne wyniki u matek i młodych, jak opisano powyżej.
Dalsze badanie toksyczności rozwojowej u szczurów z kolejnymi punktami czasowymi w celu oceny rozwoju kości u młodych od 2. dnia po urodzeniu do dorosłości przeprowadzono z zastosowaniem ezomeprazolu magnezowego w dawkach doustnych 280 mg/kg mc./dobę (około 68-krotność dawki doustnej 40 mg u ludzi w oparciu o powierzchnię ciała), gdzie esomeprazol podawano od 7. dnia ciąży lub od 16. dnia ciąży do porodu. Gdy podawanie matce ograniczało się tylko do okresu ciąży, nie stwierdzono wpływu na morfologię nasad kości u potomstwa w każdym wieku.
Laktacja
Podsumowanie ryzyka
Ograniczone dane sugerują, że omeprazol może być obecny w mleku ludzkim. Brak danych klinicznych dotyczących wpływu omeprazolu na niemowlę karmione piersią lub na produkcję mleka. Należy wziąć pod uwagę korzyści rozwojowe i zdrowotne wynikające z karmienia piersią, a także kliniczne zapotrzebowanie matki na PRILOSEC 40 mg oraz wszelkie potencjalne niepożądane skutki stosowania PRILOSEC 20 mg na karmione piersią niemowlę lub wynikające z podstawowej choroby matki.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność PRILOSEC 40 mg zostały ustalone u pacjentów pediatrycznych w wieku od 1 do 16 lat w leczeniu objawowego GERD, leczenia EE spowodowanego GERD za pośrednictwem kwasu oraz podtrzymania gojenia EE spowodowanego GERD za pośrednictwem kwasu. Stosowanie PRILOSEC 10 mg w tej grupie wiekowej jest poparte odpowiednimi i dobrze kontrolowanymi badaniami u dorosłych oraz niekontrolowanymi badaniami bezpieczeństwa, skuteczności i farmakokinetyki przeprowadzonymi u dzieci i młodzieży [patrz FARMAKOLOGIA KLINICZNA , Studia kliniczne ].
Bezpieczeństwo i skuteczność PRILOSEC 10 mg zostały ustalone u dzieci w wieku od 1 miesiąca do mniej niż 1 roku w leczeniu EE spowodowanego kwasowym GERD i są poparte odpowiednimi i dobrze kontrolowanymi badaniami u dorosłych oraz bezpieczeństwa, farmakokinetyki, oraz badania farmakodynamiczne przeprowadzone u pacjentów pediatrycznych [patrz FARMAKOLOGIA KLINICZNA ].
W populacji pediatrycznej działania niepożądane ze strony układu oddechowego były często zgłaszane w całej grupie wiekowej (od 1 miesiąca do 16 lat). Zapalenie ucha środkowego było często zgłaszane w grupie wiekowej od 1 miesiąca do DZIAŁANIA NIEPOŻĄDANE ].
Bezpieczeństwo i skuteczność PRILOSEC nie zostały ustalone w:
- pacjenci w wieku poniżej 1 roku na:
- Leczenie objawowego GERD
- Utrzymanie gojenia EE z powodu GERD za pośrednictwem kwasu
- pacjenci pediatryczni na:
- Leczenie czynnego wrzodu dwunastnicy
- Eradykacja H. pylori w celu zmniejszenia ryzyka nawrotu choroby wrzodowej dwunastnicy
- Leczenie czynnego łagodnego wrzodu żołądka
- Patologiczne stany nadmiernego wydzielania
- pacjentów w wieku poniżej 1 miesiąca dla dowolnego wskazania.
Dane dotyczące młodych zwierząt
Wykazano, że esomeprazol, enancjomer omeprazolu, zmniejsza masę ciała, przyrost masy ciała, masę kości udowej, długość kości udowej i ogólny wzrost przy dawkach doustnych około 34 do 68 razy więcej niż dawka dobowa 40 mg esomeprazolu lub 40 mg omeprazolu u ludzi w zależności od ciała powierzchni w badaniu toksyczności na młodych szczurach. Wielokrotność dawek podawanych zwierzętom w stosunku do ludzi opiera się na założeniu równej ogólnoustrojowej ekspozycji na esomeprazol u ludzi po doustnym podaniu 40 mg esomeprazolu lub 40 mg omeprazolu.
Przeprowadzono 28-dniowe badanie toksyczności z 14-dniową fazą regeneracji u młodych szczurów, którym podawano ezomeprazol magnezowy w dawkach od 70 do 280 mg/kg/dobę (około 17 do 68 razy więcej niż doustna dawka 40 mg ezomeprazolu u ludzi lub 40 mg na dobę). omeprazol na podstawie powierzchni ciała). Zaobserwowano wzrost liczby zgonów po podaniu dużej dawki 280 mg/kg/dobę, gdy młodym szczurom podawano esomeprazol magnezowy od 7. do 35. dnia po urodzeniu. Ponadto dawki równe lub większe niż 140 mg/kg/dobę (około 34 razy dziennie doustna dawka 40 mg esomeprazolu lub 40 mg omeprazolu na podstawie powierzchni ciała) powodowała związane z leczeniem zmniejszenie masy ciała (około 14%) i przyrost masy ciała, zmniejszenie masy kości udowej i kości udowej długość i wpłynęły na ogólny wzrost. Porównywalne wyniki opisane powyżej zaobserwowano również w tym badaniu z inną solą esomeprazolu, esomeprazolem strontem, w równomolowych dawkach esomeprazolu.
Zastosowanie geriatryczne
Omeprazol podawano ponad 2000 osobom w podeszłym wieku (≥ 65 lat) w badaniach klinicznych w Stanach Zjednoczonych i Europie. Nie było różnic w bezpieczeństwie i skuteczności między osobami starszymi i młodszymi. Inne zgłoszone doświadczenia kliniczne nie wykazały różnic w odpowiedzi między osobami starszymi i młodszymi, ale nie można wykluczyć większej wrażliwości niektórych osób starszych.
Badania farmakokinetyczne wykazały, że szybkość eliminacji była nieco zmniejszona u osób w podeszłym wieku, a biodostępność była zwiększona. Klirens osoczowy omeprazolu wynosił 250 ml/min (około połowy tego u młodych ochotników), a jego okres półtrwania w osoczu wynosił średnio jedną godzinę, około dwa razy w porównaniu z młodymi zdrowymi ochotnikami. Nie ma jednak konieczności dostosowania dawkowania u osób w podeszłym wieku [patrz FARMAKOLOGIA KLINICZNA ].
Niewydolność wątroby
pacjentów z zaburzeniami czynności wątroby (klasa A, B lub C w skali Child-Pugh) ekspozycja na omeprazol znacznie wzrosła w porównaniu do osób zdrowych. U pacjentów z zaburzeniami czynności wątroby w celu podtrzymania gojenia EE zaleca się zmniejszenie dawki produktu PRILOSEC 10 mg do 10 mg raz na dobę [patrz DAWKOWANIE I SPOSÓB PODAWANIA , FARMAKOLOGIA KLINICZNA ].
Populacja azjatycka
W badaniach zdrowych osób Azjaci mieli około czterokrotnie większą ekspozycję niż osoby rasy kaukaskiej. U pacjentów azjatyckich w celu podtrzymania gojenia EE zaleca się zmniejszenie dawki PRILOSEC 20 mg do 10 mg raz na dobę [patrz DAWKOWANIE I SPOSÓB PODAWANIA , FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
Otrzymano doniesienia o przedawkowaniu omeprazolu u ludzi. Dawki mieściły się w zakresie do 2400 mg (120-krotność zwykłej zalecanej dawki klinicznej). Objawy były różne, ale obejmowały splątanie, senność, niewyraźne widzenie, tachykardię, nudności, wymioty, pocenie się, uderzenia gorąca, bóle głowy, suchość w ustach i inne działania niepożądane podobne do obserwowanych w normalnym doświadczeniu klinicznym [patrz DZIAŁANIA NIEPOŻĄDANE ]. Objawy były przemijające i nie zgłoszono żadnych poważnych objawów klinicznych, gdy stosowano sam PRILOSEC 20 mg. Nie jest znana swoista odtrutka na przedawkowanie omeprazolu.
Omeprazol w znacznym stopniu wiąże się z białkami i dlatego nie jest łatwo dializowany. W przypadku przedawkowania leczenie powinno być objawowe i podtrzymujące.
Jeśli dojdzie do nadmiernej ekspozycji, zadzwoń do Centrum Kontroli Zatruć pod numer 1-800-222-1222, aby uzyskać aktualne informacje na temat postępowania w przypadku zatrucia lub przedawkowania.
PRZECIWWSKAZANIA
- PRILOSEC jest przeciwwskazany u pacjentów ze znaną nadwrażliwością na podstawione benzimidazole lub którykolwiek składnik preparatu. Reakcje nadwrażliwości mogą obejmować anafilaksję, wstrząs anafilaktyczny, obrzęk naczynioruchowy, skurcz oskrzeli, ostre cewkowo-śródmiąższowe zapalenie nerek i pokrzywkę [patrz OSTRZEŻENIA I ŚRODKI , DZIAŁANIA NIEPOŻĄDANE ].
- Inhibitory pompy protonowej (PPI), w tym PRILOSEC 10 mg, są przeciwwskazane u pacjentów otrzymujących produkty zawierające rylpiwirynę [patrz INTERAKCJE Z LEKAMI ].
- Informacje o przeciwwskazaniach do stosowania środków przeciwbakteryjnych (klarytromycyny i amoksycyliny) wskazanych w połączeniu z PRILOSEC 40 mg można znaleźć w części PRZECIWWSKAZANIA na ulotkach dołączonych do opakowania.
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Omeprazol należy do klasy związków przeciwwydzielniczych, podstawionych benzimidazoli, które hamują wydzielanie kwasu żołądkowego poprzez specyficzne hamowanie układu enzymatycznego H+/K+ ATPazy na powierzchni wydzielniczej komórki okładzinowej żołądka. Ponieważ ten układ enzymatyczny jest uważany za pompę kwasu (protonową) w błonie śluzowej żołądka, omeprazol został scharakteryzowany jako inhibitor pompy kwasu żołądkowego, ponieważ blokuje końcowy etap wytwarzania kwasu. Efekt ten jest zależny od dawki i prowadzi do zahamowania zarówno podstawowego, jak i stymulowanego wydzielania kwasu, niezależnie od bodźca.
Farmakodynamika
Aktywność antywydzielnicza
Po podaniu doustnym początek działania przeciwwydzielniczego omeprazolu występuje w ciągu jednej godziny, przy czym maksymalne działanie występuje w ciągu dwóch godzin. Hamowanie wydzielania wynosi około 50% maksimum po 24 godzinach, a czas trwania hamowania trwa do 72 godzin. Efekt przeciwwydzielniczy trwa zatem znacznie dłużej niż można by oczekiwać po bardzo krótkim (poniżej jednej godziny) okresie półtrwania w osoczu, najwyraźniej z powodu przedłużonego wiązania z ciemieniowym enzymem ATP-azy H+/K+. Po odstawieniu leku aktywność wydzielnicza powraca stopniowo, w ciągu 3 do 5 dni. Hamujące działanie omeprazolu na wydzielanie onacidu nasila się przy wielokrotnym podawaniu raz na dobę, osiągając plateau po czterech dniach.
Poniżej przedstawiono wyniki licznych badań działania przeciwwydzielniczego wielokrotnych dawek 20 mg i 40 mg omeprazolu u zdrowych osób i pacjentów. Wartość „max” reprezentuje oznaczenia w czasie maksymalnego działania (2 do 6 godzin po podaniu), podczas gdy wartości „min” to te 24 godziny po ostatniej dawce omeprazolu.
Pojedyncza dobowa doustna dawka omeprazolu w zakresie od 10 mg do 40 mg powodowała u niektórych pacjentów 100% zahamowanie 24-godzinnej kwasowości żołądkowej.
Efekty gastryny w surowicy
badaniach z udziałem ponad 200 pacjentów stężenie gastryny w surowicy zwiększało się w ciągu pierwszych 1-2 tygodni podawania omeprazolu raz na dobę, równolegle z hamowaniem wydzielania kwasu. Przy dalszym leczeniu nie wystąpił dalszy wzrost gastryny w surowicy. W porównaniu z antagonistami receptora histaminowego H2, mediana wzrostu wywołanego przez dawki 20 mg omeprazolu była większa (1,3 do 3,6-krotnego w porównaniu do 1,1 do 1,8-krotnego wzrostu). Wartości gastryny powracały do wartości sprzed leczenia, zwykle w ciągu 1 do 2 tygodni po zakończeniu leczenia.
Zwiększona gastryna powoduje hiperplazję komórek podobnych do enterochromafin i podwyższony poziom chromograniny A (CgA) w surowicy. Podwyższony poziom CgA może powodować fałszywie dodatnie wyniki w badaniach diagnostycznych guzów neuroendokrynnych [patrz OSTRZEŻENIA I ŚRODKI ].
Efekty komórek enterochromafinopodobnych (ECL)
Próbki z biopsji żołądka ludzkiego uzyskano od ponad 3000 pacjentów (zarówno dzieci, jak i dorosłych) leczonych omeprazolem w długoterminowych badaniach klinicznych. Częstość występowania hiperplazji komórek ECL w tych badaniach wzrastała z czasem; jednak u tych pacjentów nie stwierdzono żadnego przypadku rakowiaka z komórek ECL, dysplazji ani neoplazji. Jednak badania te mają niewystarczający czas trwania i rozmiar, aby wykluczyć możliwy wpływ długotrwałego podawania omeprazolu na rozwój jakichkolwiek stanów przednowotworowych lub nowotworowych.
Inne efekty
Dotychczas nie stwierdzono ogólnoustrojowego działania omeprazolu na ośrodkowy układ nerwowy, układ sercowo-naczyniowy i oddechowy. Omeprazol podawany w dawkach doustnych 30 lub 40 mg przez 2 do 4 tygodni nie miał wpływu na czynność tarczycy, metabolizm węglowodanów, poziom parathormonu, kortyzolu, estradiolu, testosteronu, prolaktyny, cholecystokininy czy sekretyny w krążeniu.
Po podaniu pojedynczej dawki 90 mg omeprazolu nie wykazano wpływu na opróżnianie żołądka ze składników stałych i płynnych posiłku testowego. U zdrowych osób pojedyncza dożylna dawka omeprazolu (0,35 mg/kg) nie miała wpływu na wydzielanie czynnika wewnętrznego. Nie zaobserwowano żadnego systematycznego, zależnego od dawki, wpływu na podstawową lub stymulowaną produkcję pepsyny u ludzi.
Jednakże, gdy wewnątrzżołądkowe pH utrzymuje się na poziomie 4,0 lub wyższym, podstawowa produkcja pepsyny jest niska, a aktywność pepsyny jest zmniejszona.
Podobnie jak inne środki podnoszące pH w żołądku, omeprazol podawany przez 14 dni zdrowym ochotnikom powodował znaczne zwiększenie wewnątrzżołądkowego stężenia żywych bakterii. Wzór gatunku bakterii pozostał niezmieniony w stosunku do tego powszechnie występującego w ślinie. Wszystkie zmiany ustąpiły w ciągu trzech dni od zaprzestania leczenia.
Przebieg przełyku Barretta u 106 pacjentów oceniano w badaniu prowadzonym metodą podwójnie ślepej próby w Stanach Zjednoczonych, w którym podawano PRILOSEC 40 mg dwa razy na dobę przez 12 miesięcy, a następnie 20 mg dwa razy na dobę przez 12 miesięcy lub 300 mg ranitydyny dwa razy na dobę przez 24 miesiące. Nie zaobserwowano klinicznie istotnego wpływu terapii przeciwwydzielniczej na błonę śluzową Barretta. Chociaż podczas terapii przeciwwydzielniczej rozwinął się nabłonek neopłaskonabłonkowy, nie osiągnięto całkowitego usunięcia błony śluzowej Barretta. Nie zaobserwowano istotnej różnicy między leczonymi grupami w rozwoju dysplazji błony śluzowej Barretta iu żadnego pacjenta nie rozwinął się rak przełyku podczas leczenia. Nie zaobserwowano istotnych różnic między grupami leczenia w rozwoju hiperplazji komórek ECL, zanikowego zapalenia żołądka, metaplazji ciałka jelitowego lub polipów okrężnicy o średnicy przekraczającej 3 mm.
Farmakokinetyka
Wchłanianie
PRILOSEC 20 mg do sporządzania zawiesiny doustnej o opóźnionym uwalnianiu zawiera omeprazol w granulkach magnezowych i nieaktywne granulki do podawania w wodzie. Wchłanianie omeprazolu rozpoczyna się dopiero po opuszczeniu żołądka przez granulki dojelitowe. Farmakokinetyka omeprazolu zależy od czasu, przy czym stężenia w osoczu są wyższe w stanie stacjonarnym niż po podaniu pojedynczej dawki. Ekspozycja ogólnoustrojowa (AUC i Cmax) na omeprazol po podawaniu raz na dobę 20 mg zawiesiny doustnej o opóźnionym uwalnianiu przez 5 dni jest odpowiednio o 51% i 58% większa niż po podaniu pierwszej dawki. Maksymalne stężenie omeprazolu w osoczu po wielokrotnych dawkach zawiesiny doustnej o opóźnionym uwalnianiu występuje w ciągu 1,5 do 2 godzin. U zdrowych osób okres półtrwania w osoczu wynosi od 0,5 do 1 godziny.
Dystrybucja
Wiązanie z białkami wynosi około 95%.
Eliminacja
Metabolizm
Omeprazol jest intensywnie metabolizowany przez układ enzymatyczny cytochromu P450 (CYP). Większa część jego metabolizmu jest zależna od polimorficznie wyrażanego CYP2C19, odpowiedzialnego za tworzenie hydroksyomeprazolu, głównego metabolitu w osoczu. Pozostała część zależna jest od innej specyficznej izoformy, CYP3A4, odpowiedzialnej za tworzenie sulfonu omeprazolu.
Wydalanie
Po podaniu doustnym pojedynczej dawki zbuforowanego roztworu omeprazolu, niewielka ilość niezmienionego leku była wydalana z moczem. Większość dawki (około 77%) została wydalona z moczem w postaci co najmniej sześciu metabolitów. Dwa zostały zidentyfikowane jako hydroksyomeprazol i odpowiedni kwas karboksylowy. Pozostałą część dawki można było odzyskać w kale. Oznacza to znaczne wydalanie z żółcią metabolitów omeprazolu. W osoczu zidentyfikowano trzy metabolity: siarczkowe i sulfonowe pochodne omeprazolu oraz hydroksyomeprazol. Te metabolity mają bardzo małą lub żadną aktywność przeciwwydzielniczą.
Terapia skojarzona z lekami przeciwdrobnoustrojowymi
Omeprazol w dawce 40 mg na dobę podawano w skojarzeniu z klarytromycyną w dawce 500 mg co 8 godzin zdrowym dorosłym mężczyznom. Stężenie omeprazolu w osoczu w stanie stacjonarnym zwiększało się (wzrost Cmax, AUC0-24 i T½ odpowiednio o 30%, 89% i 34%) po jednoczesnym podaniu klarytromycyny. Obserwowane zwiększenie stężenia omeprazolu w osoczu było związane z następującymi efektami farmakologicznymi. Średnia wartość pH w żołądku w ciągu doby wynosiła w przypadku samego omeprazolu i 5,7 w przypadku jednoczesnego podawania z klarytromycyną.
Stężenie klarytromycyny i 14-hydroksyklarytromycyny w osoczu zwiększało się podczas jednoczesnego podawania omeprazolu. W przypadku klarytromycyny średnie Cmax było o 10% większe, średnie Cmin było o 27% większe, a średnie AUC0-8 było o 15% większe, gdy klarytromycyna była podawana z omeprazolem, niż gdy podawano samą klarytromycynę. Podobne wyniki zaobserwowano dla 14-hydroksyklarytromycyny, średnie Cmax było o 45% większe, średnie Cmin było większe o 57%, a średnie AUC0-8 było większe o 45%. Stężenie klarytromycyny w tkance żołądka i śluzie również zwiększało się po jednoczesnym podaniu omeprazolu.
Określone populacje
Pacjenci geriatryczni
Szybkość eliminacji omeprazolu była nieco zmniejszona u osób starszych, a biodostępność była zwiększona. Biodostępność omeprazolu wynosiła 76%, gdy pojedynczą doustną dawkę 40 mg omeprazolu (roztwór buforowy) podano zdrowym ochotnikom w podeszłym wieku, w porównaniu do 58% młodych ochotników otrzymujących tę samą dawkę. Prawie 70% dawki odzyskano w moczu w postaci metabolitów omeprazolu i nie wykryto niezmienionego leku. Klirens osoczowy omeprazolu wynosił 250 ml/min (około połowy tego u młodych ochotników), a jego okres półtrwania w osoczu wynosił średnio jedną godzinę, około dwa razy w porównaniu z młodymi zdrowymi ochotnikami.
Pacjenci pediatryczni
2 do 16 lat
Farmakokinetykę omeprazolu badano u dzieci w wieku od 2 do 16 lat:
Po porównywalnych dawkach omeprazolu w mg/kg młodsze dzieci (w wieku od 2 do 5 lat) mają niższe AUC niż dzieci w wieku od 6 do 16 lat lub dorośli; AUC tych dwóch ostatnich grup nie różniły się [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
1 do 11 miesięcy życia
celu określenia odpowiednich dawek produktu PRILOSEC 40 mg u dzieci zastosowano model farmakokinetyki populacyjnej
Od 1 miesiąca do mniej niż 1 roku życia w leczeniu (do 6 tygodni) nadżerkowego zapalenia przełyku spowodowanego kwasowym GERD. Model oparto na danych 64 dzieci w wieku od 0,5 miesiąca do 16 roku życia. Dostępne były tylko ograniczone dane dotyczące dzieci w wieku poniżej 1 roku. Omeprazol podawano w tych badaniach pacjentom pediatrycznym w postaci zawiesiny doustnej przygotowanej z kapsułek o opóźnionym uwalnianiu. Dawki pediatryczne symulowano w grupie wiekowej od 1 do 11 miesięcy w celu uzyskania porównywalnej ekspozycji na omeprazol u dorosłych po leczeniu 20 mg raz na dobę [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Grupy rasowe lub etniczne
[Widzieć FARMAKOLOGIA KLINICZNA ].
Pacjenci z niewydolnością nerek
pacjentów z przewlekłą niewydolnością nerek (klirens kreatyniny od 10 do 62 ml/min/1,73 m²) dystrybucja omeprazolu była bardzo podobna do tej u zdrowych osób, chociaż obserwowano nieznaczny wzrost biodostępności. Ponieważ wydalanie z moczem jest główną drogą wydalania metabolitów omeprazolu, ich eliminacja ulegała spowolnieniu proporcjonalnie do zmniejszonego klirensu kreatyniny. Ten wzrost biodostępności nie jest uważany za klinicznie istotny.
Pacjenci z niewydolnością wątroby
U pacjentów z przewlekłą chorobą wątroby zaklasyfikowaną do klasy A w skali Child-Pugh (n=3), B (n=4) i C (n=1), biodostępność wzrosła do około 100% w porównaniu ze zdrowymi osobami, odzwierciedlając zmniejszony efekt pierwszego przejścia i okres półtrwania leku w osoczu wzrósł do prawie 3 godzin w porównaniu z okresem półtrwania u zdrowych osób wynoszącym 0,5 do 1 godziny. Klirens osocza wynosił średnio 70 ml/min, w porównaniu z wartością od 500 do 600 ml/min u zdrowych osób [patrz DAWKOWANIE I SPOSÓB PODAWANIA , Używaj w określonych populacjach ].
Badania interakcji leków
Wpływ omeprazolu na inne leki
Omeprazol jest zależnym od czasu inhibitorem CYP2C19 i może zwiększać ogólnoustrojową ekspozycję na jednocześnie podawane leki będące substratami CYP2C19. Ponadto podawanie omeprazolu zwiększa wewnątrzżołądkowe pH i może zmieniać ogólnoustrojową ekspozycję na niektóre leki, które wykazują rozpuszczalność zależną od pH.
Leki przeciwretrowirusowe
W przypadku niektórych leków przeciwretrowirusowych, takich jak rylpiwiryna, atazanawir i nelfinawir, zgłaszano zmniejszenie stężenia w surowicy podczas jednoczesnego podawania z omeprazolem [patrz INTERAKCJE Z LEKAMI ].
Rilpiwiryna: Po wielokrotnych dawkach rylpiwiryny (150 mg na dobę) i omeprazolu (20 mg na dobę) AUC zmniejszyło się o 40%, Cmax o 40%, a Cmin o 33% dla rylpiwiryny.
Nelfinawir: Po wielokrotnych dawkach nelfinawiru (1250 mg, dwa razy na dobę) i omeprazolu (40 mg na dobę), AUC zmniejszyło się o 36% i 92%, Cmax o 37% i 89% oraz Cmin o 39% i 75% odpowiednio dla nelfinawiru i M8 .
Atazanawir: Po wielokrotnych dawkach atazanawiru (400 mg na dobę) i omeprazolu (40 mg na dobę, 2 godziny przed atazanawirem), AUC zmniejszyło się o 94%, Cmax o 96%, a Cmin o 95%.
Sakwinawir: Po wielokrotnym podawaniu sakwinawiru/rytonawiru (1000/100 mg) dwa razy na dobę przez 15 dni z omeprazolem 40 mg na dobę jednocześnie podawanym w dniach od 11 do 15.
AUC zwiększyło się o 82%, Cmax o 75%, a Cmin o 106%. Mechanizm tej interakcji nie jest w pełni wyjaśniony.
Klopidogrel
W krzyżowym badaniu klinicznym 72 zdrowym ochotnikom podawano klopidogrel (300 mg dawka wysycająca, a następnie 75 mg na dobę) sam iz omeprazolem (80 mg jednocześnie z klopidogrelem) przez 5 dni. Ekspozycja na aktywny metabolit klopidogrelu zmniejszyła się o 46% (dzień 1.) i 42% (dzień 5.), gdy klopidogrel i omeprazol były podawane razem.
Wyniki innego badania krzyżowego u zdrowych ochotników wykazały podobną interakcję farmakokinetyczną między klopidogrelem (300 mg dawka nasycająca/75 mg dobowa dawka podtrzymująca) a omeprazolem 80 mg na dobę przy jednoczesnym podawaniu przez 30 dni. W tym okresie ekspozycja na aktywny metabolit klopidogrelu zmniejszyła się o 41% do 46%.
W innym badaniu 72 zdrowym osobom podano te same dawki klopidogrelu i 80 mg omeprazolu, ale leki podawano w odstępie 12 godzin; wyniki były podobne, co wskazuje, że podawanie klopidogrelu i omeprazolu w różnym czasie nie zapobiega ich interakcji [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI ].
mykofenolan mofetylu
Podawanie omeprazolu 20 mg dwa razy na dobę przez 4 dni i pojedynczej dawki 1000 mg MMF około jednej godziny po ostatniej dawce omeprazolu 12 zdrowym ochotnikom w badaniu krzyżowym spowodowało zmniejszenie Cmax o 52% i zmniejszenie o 23% w AUC MPA [patrz INTERAKCJE Z LEKAMI ].
Cilostazol
Omeprazol działa jako inhibitor CYP2C19. Omeprazol, podawany w dawkach 40 mg na dobę przez jeden tydzień 20 zdrowym ochotnikom w badaniu krzyżowym, zwiększał Cmax i AUC cilostazolu odpowiednio o 18% i 26%. Cmax i AUC jednego z aktywnych metabolitów, 3,4-dihydrocilostazolu, który ma 4-7 razy większą aktywność niż cilostazol, wzrosły odpowiednio o 29% i 69%. Oczekuje się, że równoczesne podawanie cilostazolu z omeprazolem zwiększy stężenia cilostazolu i wyżej wymienionego czynnego metabolitu [patrz INTERAKCJE Z LEKAMI ].
Diazepam
Jednoczesne podawanie omeprazolu 20 mg raz na dobę i diazepamu w dawce 0,1 mg/kg podawanego dożylnie powodowało 27% zmniejszenie klirensu i 36% wydłużenie okresu półtrwania diazepamu [patrz INTERAKCJE Z LEKAMI ].
Digoksyna
Jednoczesne podawanie omeprazolu 20 mg raz na dobę i digoksyny zdrowym osobom zwiększało biodostępność digoksyny o 10% (30% u dwóch osób) [patrz INTERAKCJE Z LEKAMI ].
Wpływ innych leków na omeprazol
Worykonazol
Jednoczesne podawanie omeprazolu i worykonazolu (połączonego inhibitora CYP2C19 i CYP3A4) powodowało ponad dwukrotne zwiększenie ekspozycji na omeprazol. Gdy zdrowym ochotnikom podawano worykonazol (400 mg co 12 godzin przez jeden dzień, a następnie 200 mg raz na dobę przez 6 dni) z omeprazolem (40 mg raz na dobę przez 7 dni), wartości Cmax i AUC0-24 omeprazolu w stanie stacjonarnym znacznie zwiększone: odpowiednio średnio 2-krotnie (90% CI: 1,8, 2,6) i 4-krotnie (90% CI: 3,3, 4,4), w porównaniu z omeprazolem podawanym bez worykonazolu [patrz INTERAKCJE Z LEKAMI ].
Mikrobiologia
Wykazano, że podwójne leczenie omeprazolem i klarytromycyną oraz potrójne leczenie omeprazolem, klarytromycyną i amoksycyliną jest aktywne przeciwko większości szczepów Helicobacter pylori in vitro i w zakażeniach klinicznych [patrz WSKAZANIA I ZASTOSOWANIE , Studia kliniczne ].
Helicobacter pylori
Testy wrażliwości izolatów H. pylori przeprowadzono na amoksycylinę i klarytromycynę stosując metodologię rozcieńczeń w agarze1 i określono minimalne stężenia hamujące (MIC).
Znormalizowane procedury badania wrażliwości wymagają użycia laboratoryjnych mikroorganizmów kontrolnych do kontroli technicznych aspektów procedur laboratoryjnych.
Odporność na obróbkę wstępną
Wskaźniki oporności na klarytromycynę przed leczeniem wynosiły 3,5% (4/113) w badaniach terapii podwójnej omeprazol/klarytromycyna (4 i 5) oraz 9,3% (41/439) w badaniach terapii potrójnej omeprazol/klarytromycyna/amoksycylina (1, 2 i 3).
Izolaty wrażliwe na amoksycylinę przed leczeniem (≤ 0,25 μg/ml) stwierdzono u 99,3% (436/439) pacjentów w badaniach terapii potrójnej omeprazolem/klarytromycyną/amoksycyliną (1, 2 i 3). Minimalne stężenia hamujące (MIC) amoksycyliny przed leczeniem > 0,25 μg/ml wystąpiły u 0,7% (3/439) pacjentów, z których wszyscy byli w ramieniu badania klarytromycyny i amoksycyliny. Jeden pacjent miał niepotwierdzone przed leczeniem minimalne hamujące stężenie amoksycyliny (MIC) > 256 μg/ml według Etest®.
pacjentów, u których nie przeprowadzono eradykacji H. pylori po potrójnej terapii omeprazol/klarytromycyna/amoksycylina lub podwójnej terapii omeprazol/klarytromycyna, izolaty H. pylori oporne na klarytromycynę. Dlatego, jeśli to możliwe, należy wykonać badanie wrażliwości na klarytromycynę. Pacjenci z bakteriami H. pylori opornymi na klarytromycynę nie powinni być leczeni żadnym z poniższych: terapia dwulekowa omeprazol/klarytromycyna, terapia trójlekowa omeprazol/klarytromycyna/amoksycylina lub inne schematy leczenia, w których klarytromycyna jest jedynym lekiem przeciwbakteryjnym.
Wyniki testu wrażliwości na amoksycylinę i wyniki kliniczne/bateriologiczne
badaniach klinicznych dotyczących potrójnej terapii 84,9% (157/185) pacjentów w grupie leczonej omeprazolem/klarytromycyną/amoksycyliną, u których przed leczeniem stwierdzono wartości MIC wrażliwe na amoksycylinę (≤ 0,25 μg/ml), zostało wyleczonych z H. pylori i 15,1% (28). /185) nieudana terapia. Spośród 28 pacjentów, u których terapia potrójna nie powiodła się, 11 nie miało wyników testów wrażliwości po leczeniu, a 17 miało po leczeniu izolaty H. pylori z wartościami MIC wrażliwości na amoksycylinę. Jedenastu pacjentów, u których nie powiodła się terapia potrójna, miało również po leczeniu izolaty H. pylori z wartościami MIC oporności na klarytromycynę.
Test wrażliwości na Helicobacter pylori
Informacje dotyczące badań wrażliwości na Helicobacter pylori znajdują się w części Mikrobiologia w informacjach dotyczących przepisywania klarytromycyny i amoksycyliny.
Wpływ na ekologię drobnoustrojów żołądkowo-jelitowych
Zmniejszona kwasowość żołądka z powodu jakichkolwiek środków, w tym inhibitorów pompy protonowej, zwiększa liczbę bakterii normalnie obecnych w przewodzie pokarmowym. Leczenie inhibitorami pompy protonowej może prowadzić do nieznacznie zwiększonego ryzyka zakażeń przewodu pokarmowego, takich jak Salmonella i Campylobacter, au pacjentów hospitalizowanych prawdopodobnie także Clostridium difficile.
Farmakogenomika
CYP2C19, enzym polimorficzny, bierze udział w metabolizmie omeprazolu. Allel CYP2C19*1 jest w pełni funkcjonalny, podczas gdy allele CYP2C19*2 i *3 są niefunkcjonalne. Istnieją inne allele związane z brakiem lub zmniejszoną funkcją enzymatyczną. Pacjenci niosący dwa w pełni funkcjonalne allele to osoby intensywnie metabolizujące, a ci, którzy noszą dwa allele utraty funkcji, słabo metabolizują. U osób intensywnie metabolizujących omeprazol jest metabolizowany głównie przez CYP2C19.
Ekspozycja ogólnoustrojowa na omeprazol różni się w zależności od stanu metabolizmu pacjenta: osoby słabo metabolizujące > osoby średnio metabolizujące > osoby intensywnie metabolizujące. Około 3% rasy kaukaskiej i 15 do 20% Azjatów to osoby słabo metabolizujące CYP2C19.
W badaniu farmakokinetycznym pojedynczej dawki 20 mg omeprazolu, AUC omeprazolu u Azjatów było około czterokrotnie większe niż u osób rasy kaukaskiej [patrz DAWKOWANIE I SPOSÓB PODAWANIA , Używaj w określonych populacjach ].
Studia kliniczne
Aktywny owrzodzenie dwunastnicy
wieloośrodkowym, podwójnie zaślepionym, kontrolowanym placebo badaniu z udziałem 147 pacjentów z endoskopowo udokumentowaną chorobą wrzodową dwunastnicy, odsetek pacjentów wyleczonych (zgodnie z protokołem) po 2 i 4 tygodniach był znacząco wyższy w przypadku omeprazolu w postaci kapsułek o opóźnionym uwalnianiu w dawce 20 mg raz na dobę niż z placebo (p ≤ 0,01).
Leczenie czynnego owrzodzenia dwunastnicy % wyleczonych pacjentów
Całkowite złagodzenie bólu w ciągu dnia i nocy wystąpiło znacznie szybciej (p ≤ 0,01) u pacjentów leczonych omeprazolem w postaci kapsułek o opóźnionym uwalnianiu w dawce 20 mg niż u pacjentów otrzymujących placebo. Pod koniec badania znacznie więcej pacjentów, którzy otrzymywali kapsułki zawierające omeprazol magnezowy o opóźnionym uwalnianiu, odczuło całkowite złagodzenie bólu w ciągu dnia (p ≤ 0,05) i bólu w nocy (p ≤ 0,01).
wieloośrodkowym, podwójnie zaślepionym badaniu z udziałem 293 pacjentów z endoskopowo udokumentowaną chorobą wrzodową dwunastnicy, odsetek pacjentów wyleczonych (zgodnie z protokołem) po 4 tygodniach był znacząco wyższy po zastosowaniu kapsułek omeprazolu magnezowego o opóźnionym uwalnianiu 20 mg raz na dobę niż po ranitydynie 150 mg dwa razy na dobę ( p
Leczenie czynnego owrzodzenia dwunastnicy % wyleczonych pacjentów
Gojenie przebiegało znacznie szybciej u pacjentów leczonych omeprazolem w postaci kapsułek magnezowych o opóźnionym uwalnianiu niż u pacjentów leczonych ranitydyną 150 mg dwa razy na dobę (p
W międzynarodowym, międzynarodowym, randomizowanym, podwójnie zaślepionym badaniu obejmującym 105 pacjentów z endoskopowo udokumentowaną chorobą wrzodową dwunastnicy, porównywano 20 mg i 40 mg kapsułek omeprazolu magnezowego o opóźnionym uwalnianiu z ranitydyną 150 mg dwa razy na dobę w 2, 4 i 8 tygodniu. Po 2 i 4 tygodniach obie dawki PRILOSEC 10 mg były statystycznie lepsze (zgodnie z protokołem) niż ranitydyna, ale 40 mg nie przewyższało 20 mg kapsułek omeprazolu magnezowego o opóźnionym uwalnianiu, a po 8 tygodniach nie było znaczącej różnicy między żadną z aktywne leki.
Leczenie czynnego owrzodzenia dwunastnicy % wyleczonych pacjentów
Eradykacja H. pylori u pacjentów z chorobą wrzodową dwunastnicy
Terapia potrójna (omeprazol magnez w kapsułkach o opóźnionym uwalnianiu/klarytromycyna/amoksycylina)
trzech badaniach klinicznych z randomizacją prowadzonych metodą podwójnie ślepej próby w Stanach Zjednoczonych u pacjentów z zakażeniem H. pylori i chorobą wrzodową dwunastnicy (n=558) porównywano kapsułki omeprazolu magnezowego o opóźnionym uwalnianiu z klarytromycyną i amoksycyliną z klarytromycyną i amoksycyliną. Dwa badania (1 i 2) przeprowadzono u pacjentów z czynną chorobą wrzodową dwunastnicy, a drugie badanie (3) przeprowadzono u pacjentów z chorobą wrzodową dwunastnicy w wywiadzie w ciągu ostatnich 5 lat, ale bez wrzodu obecnego w momencie włączenia do badania. . Schemat dawkowania w badaniach obejmował kapsułki omeprazolu magnezowego o opóźnionym uwalnianiu 20 mg dwa razy na dobę plus klarytromycyna 500 mg dwa razy na dobę plus amoksycylina 1 g dwa razy na dobę przez 10 dni; lub klarytromycyna 500 mg dwa razy na dobę plus amoksycylina 1 g dwa razy na dobę przez 10 dni. W badaniach 1 i 2 pacjenci przyjmujący omeprazol otrzymywali dodatkowo przez 18 dni omeprazol magnezowy w postaci kapsułek o opóźnionym uwalnianiu w dawce 20 mg raz na dobę. Badanymi punktami końcowymi były eradykacja H. pylori i gojenie wrzodów dwunastnicy (tylko badania 1 i 2). Status H. pylori został określony przez CLOtest®, histologię i hodowlę we wszystkich trzech badaniach. U danego pacjenta H. pylori uznawano za eradykację, jeśli co najmniej dwa z tych testów były negatywne, a żaden nie był pozytywny.
Połączenie omeprazolu z klarytromycyną i amoksycyliną było skuteczne w eradykacji H. pylori.
Terapia podwójna (omeprazol magnez w kapsułkach o opóźnionym uwalnianiu/klarytromycyna)
czterech randomizowanych, podwójnie zaślepionych, wieloośrodkowych badaniach (4, 5, 6 i 7) oceniano kapsułki zawierające omeprazol magnezowy o opóźnionym uwalnianiu 40 mg raz na dobę plus klarytromycynę 500 mg trzy razy na dobę przez 14 dni, a następnie omeprazol magnezowy w postaci o opóźnionym uwalnianiu kapsułki 20 mg raz na dobę (Badanie 4, 5 i 7) lub kapsułki omeprazolu magnezowego o opóźnionym uwalnianiu 40 mg raz na dobę (Badanie 6) przez dodatkowe 14 dni u pacjentów z czynną chorobą wrzodową dwunastnicy związaną z H. pylori. Badania 4 i 5 przeprowadzono w USA i Kanadzie i objęły odpowiednio 242 i 256 pacjentów. Zakażenie H. pylori i owrzodzenie dwunastnicy potwierdzono u 219 pacjentów w badaniu 4 i 228 pacjentów w badaniu 5. W badaniach tych porównano schemat leczenia skojarzonego z kapsułkami omeprazolu magnezowego o opóźnionym uwalnianiu i monoterapią klarytromycyną. Badania 6 i 7 zostały przeprowadzone w Europie i objęły odpowiednio 154 i 215 pacjentów. Zakażenie H. pylori i wrzód dwunastnicy potwierdzono u 148 pacjentów w badaniu 6 i 208 pacjentów w badaniu 7. W badaniach tych porównywano schemat leczenia skojarzonego z monoterapią omeprazolem. Wyniki analiz skuteczności dla tych badań opisano poniżej. Eradykację H. pylori zdefiniowano jako brak dodatniego wyniku testu (hodowli lub histologii) po 4 tygodniach od zakończenia leczenia, a dwa ujemne testy należało uznać za eradykację H. pylori. Z analizy zgodnej z protokołem wykluczono następujących pacjentów: osoby, które przedwcześnie zakończyły leczenie, pacjenci z brakującymi testami na obecność H. pylori po zakończeniu leczenia oraz pacjenci, u których nie przeprowadzono oceny pod kątem eradykacji H. pylori, ponieważ stwierdzono u nich owrzodzenie pod koniec leczenia .
Połączenie omeprazolu i klarytromycyny było skuteczne w eradykacji H. pylori.
Gojenie owrzodzeń nie różniło się istotnie, gdy do terapii omeprazolem dodano klarytromycynę, w porównaniu z samą terapią omeprazolem.
Połączenie omeprazolu i klarytromycyny było skuteczne w eradykacji H. pylori i zmniejszeniu nawrotów wrzodów dwunastnicy.
Aktywny łagodny wrzód żołądka
W wieloośrodkowym amerykańskim badaniu z podwójnie ślepą próbą omeprazolu 40 mg raz dziennie, 20 mg raz dziennie i placebo u 520 pacjentów z endoskopowo zdiagnozowanym wrzodem żołądka uzyskano następujące wyniki.
Leczenie wrzodów żołądka % wyleczonych pacjentów (wszyscy leczeni pacjenci)
W przypadku stratyfikowanych grup pacjentów z rozmiarem owrzodzenia mniejszym lub równym 1 cm, nie wykryto różnicy w szybkości gojenia między 40 mg a 20 mg po 4 lub 8 tygodniach. W przypadku pacjentów z owrzodzeniem większym niż 1 cm dawka 40 mg była znacznie skuteczniejsza niż 20 mg po 8 tygodniach.
międzynarodowym, międzynarodowym, podwójnie zaślepionym badaniu 602 pacjentów z endoskopowo zdiagnozowanym wrzodem żołądka oceniano omeprazol w dawce 40 mg raz na dobę, 20 mg raz na dobę i ranitydynę 150 mg dwa razy na dobę.
Leczenie wrzodów żołądka % wyleczonych pacjentów (wszyscy leczeni pacjenci)
Objawowy GERD
W Skandynawii przeprowadzono badanie kontrolowane placebo w celu porównania skuteczności omeprazolu w dawce 20 mg lub 10 mg raz na dobę przez okres do 4 tygodni w leczeniu zgagi i innych objawów u pacjentów z GERD bez EE. Wyniki przedstawiono poniżej.
% pomyślnego wyniku objawowego1
EE z powodu GERD za pośrednictwem kwasu
W wieloośrodkowym, podwójnie zaślepionym badaniu kontrolowanym placebo w USA, obejmującym 20 mg lub 40 mg kapsułek omeprazolu magnezowego o opóźnionym uwalnianiu u pacjentów z objawami GERD i endoskopowo zdiagnozowanym EE stopnia 2 lub wyższego, procentowe wskaźniki gojenia (według protokołu) były następujące :
tym badaniu dawka 40 mg nie przewyższała dawki 20 mg kapsułek omeprazolu magnezowego o opóźnionym uwalnianiu pod względem odsetka szybkości gojenia. Inne kontrolowane badania kliniczne wykazały również, że kapsułki zawierające omeprazol magnezowy o opóźnionym uwalnianiu są skuteczne w ciężkiej postaci GERD. W porównaniu z antagonistami receptora histaminowego H2 u pacjentów z EE stopnia 2 lub wyższego, kapsułki omeprazolu magnezowego o opóźnionym uwalnianiu w dawce 20 mg były znacznie skuteczniejsze niż aktywne grupy kontrolne. Całkowite złagodzenie zgagi w ciągu dnia i nocy wystąpiło znacznie szybciej (p
W tym i pięciu innych kontrolowanych badaniach GERD znacznie więcej pacjentów przyjmujących 20 mg omeprazolu (84%) zgłaszało całkowite ustąpienie objawów GERD niż pacjentów otrzymujących placebo (12%).
Utrzymanie gojenia EE z powodu GERD za pośrednictwem kwasu
amerykańskim, podwójnie zaślepionym, randomizowanym, wieloośrodkowym badaniu kontrolowanym placebo, badano dwa schematy dawkowania omeprazolu w postaci kapsułek o opóźnionym uwalnianiu u pacjentów z endoskopowo potwierdzonym wygojonym zapaleniem przełyku. Wyniki określające utrzymanie gojenia EE przedstawiono poniżej.
Analiza Tabeli Życia
W międzynarodowym, wieloośrodkowym badaniu z podwójnie ślepą próbą, omeprazol magnezowy w kapsułkach o opóźnionym uwalnianiu 20 mg na dobę i 10 mg na dobę porównywano z ranitydyną 150 mg dwa razy na dobę u pacjentów z endoskopowo potwierdzonym wyleczonym zapaleniem przełyku. Poniższa tabela przedstawia wyniki tego badania dotyczące utrzymania gojenia EE.
Analiza Tabeli Życia
U pacjentów, którzy początkowo mieli nadżerkowe zapalenie przełyku stopnia 3 lub 4, do podtrzymania po wygojeniu skuteczne było 20 mg omeprazolu w kapsułkach o opóźnionym uwalnianiu na dobę, podczas gdy 10 mg nie wykazało skuteczności.
Patologiczne stany nadmiernego wydzielania
otwartych badaniach z udziałem 136 pacjentów z patologicznymi stanami nadmiernego wydzielania, takimi jak zespół Zollingera-Ellisona (ZE) z lub bez wielu gruczolaków endokrynnych, kapsułki zawierające omeprazol o opóźnionym uwalnianiu w postaci magnezu znacząco hamowały wydzielanie kwasu żołądkowego i kontrolowały towarzyszące objawy biegunki, anoreksji i bólu. Dawki w zakresie od 20 mg co drugi dzień do 360 mg na dobę utrzymywały podstawowe wydzielanie kwasu poniżej 10 mEq/h u pacjentów bez wcześniejszej operacji żołądka i poniżej 5 mEq/h u pacjentów po przebytej operacji żołądka.
Dawki początkowe dostosowywano do indywidualnych potrzeb pacjenta, au niektórych pacjentów z czasem konieczne było dostosowanie [patrz DAWKOWANIE I SPOSÓB PODAWANIA ]. Kapsułki omeprazolu magnezowego o opóźnionym uwalnianiu były dobrze tolerowane przy tych wysokich dawkach przez dłuższy czas (>5 lat u niektórych pacjentów). U większości pacjentów z ZE stężenie gastryny w surowicy nie było modyfikowane przez kapsułki omeprazolu magnezowego o opóźnionym uwalnianiu. Jednak u niektórych pacjentów stężenie gastryny w surowicy wzrastało do poziomów większych niż te obecne przed rozpoczęciem leczenia omeprazolem. U co najmniej 11 pacjentów z zespołem ZE leczonych długotrwale omeprazolem w postaci kapsułek o opóźnionym uwalnianiu doszło do rozwoju rakowiaka żołądka. Uważa się, że odkrycia te są raczej przejawem choroby podstawowej, o której wiadomo, że jest związana z takimi nowotworami, niż wynikiem podawania kapsułek omeprazolu magnezowego o opóźnionym uwalnianiu [patrz DZIAŁANIA NIEPOŻĄDANE ].
Badania pediatryczne dotyczące leczenia objawowego GERD, leczenia EE z powodu GERD za pośrednictwem kwasu oraz utrzymania gojenia EE z powodu GERD za pośrednictwem kwasu
Leczenie objawowego GERD
Skuteczność omeprazolu w postaci kapsułek magnezowych o opóźnionym uwalnianiu w leczeniu objawowej GERD u dzieci w wieku od 1 do 16 lat opiera się częściowo na danych uzyskanych od 125 pacjentów pediatrycznych w dwóch niekontrolowanych badaniach klinicznych.
Do pierwszego badania włączono 12 pacjentów pediatrycznych w wieku od 1 do 2 lat z wywiadem klinicznie rozpoznanym GERD. Pacjentom podawano pojedynczą dawkę omeprazolu (0,5 mg/kg, 1 mg/kg lub 1,5 mg/kg) przez 8 tygodni w postaci otwartej kapsułki w 8,4% roztworze wodorowęglanu sodu. Siedemdziesiąt pięć procent (9/12) pacjentów miało epizody wymiotów/wymiotów zmniejszone w stosunku do wartości wyjściowej o co najmniej 50%.
Do drugiego badania włączono 113 pacjentów pediatrycznych w wieku od 2 do 16 lat z objawami sugerującymi objawową GERD w wywiadzie. Pacjentom podawano pojedynczą dawkę omeprazolu (10 mg lub 20 mg, w oparciu o masę ciała) przez 4 tygodnie albo jako nienaruszoną kapsułkę, albo jako otwartą kapsułkę w sosie jabłkowym. Pomyślną odpowiedź zdefiniowano jako brak umiarkowanych lub ciężkich epizodów objawów bólowych lub wymiotów/wymiotów w ciągu ostatnich 4 dni leczenia. Wyniki wykazały, że odsetek powodzeń wynosił odpowiednio 60% (9/15; 10 mg omeprazolu) i 59% (58/98; 20 mg omeprazolu).
Leczenie EE z powodu GERD za pośrednictwem kwasu
niekontrolowanym, otwartym badaniu miareczkowania dawki, w leczeniu EE u dzieci w wieku od 1 do 16 lat, wymagane dawki wahały się od 0,7 do 3,5 mg/kg/dobę (80 mg/dobę). Dawki rozpoczęto od 0,7 mg/kg/dzień. Dawki zwiększano o 0,7 mg/kg/dobę (jeśli pH w przełyku wykazywało pH
Utrzymanie gojenia EE z powodu GERD za pośrednictwem kwasu
niekontrolowanym, otwartym badaniu utrzymywania gojenia EE u 46 pacjentów pediatrycznych w wieku od 1 do 16 lat, 54% pacjentów wymagało połowy dawki leczniczej. Pozostali pacjenci zwiększyli dawkę leczniczą (0,7 do maksymalnie 2,8 mg/kg/dobę) przez cały okres podtrzymujący lub wrócili do połowy dawki przed zakończeniem. Spośród 46 pacjentów, którzy weszli w fazę podtrzymującą, 19 (41%) nie miało nawrotu podczas obserwacji (zakres od 4 do 25 miesięcy). Ponadto terapia podtrzymująca u pacjentów z EE spowodowała, że 63% pacjentów nie miało ogólnych objawów.
BIBLIOGRAFIA
1. Instytut Norm Klinicznych i Laboratoryjnych (CLSI). Metody rozcieńczeń Testy wrażliwości drobnoustrojów na bakterie, które rosną w warunkach tlenowych; Zatwierdzony standard — wydanie dziesiąte. Dokument CLSI M07-A10, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pensylwania, 19087, USA 2015.
INFORMACJA O PACJENCIE
PRILOSEC® (pry-lo-sec) (omeprazol magnezowy) do sporządzania zawiesiny doustnej o opóźnionym uwalnianiu
Jakie są najważniejsze informacje, które powinienem wiedzieć o PRILOSEC?
PRILOSEC 10 mg może złagodzić objawy związane z nadkwaśnością, ale nadal możesz mieć poważne problemy żołądkowe. Porozmawiaj ze swoim lekarzem.
PRILOSEC może powodować poważne skutki uboczne, w tym:
- Rodzaj problemu z nerkami (ostre cewkowo-śródmiąższowe zapalenie nerek). U niektórych osób przyjmujących leki z grupy inhibitorów pompy protonowej (PPI), w tym PRILOSEC, może wystąpić choroba nerek zwana ostrym cewkowo-śródmiąższowym zapaleniem nerek, która może wystąpić w dowolnym momencie leczenia lekiem PRILOSEC. Zadzwoń do lekarza natychmiast, jeśli masz zmniejszenie ilości oddanego moczu lub jeśli masz krew w moczu.
- Biegunka spowodowana infekcją (Clostridium difficile) w jelitach. Natychmiast skontaktuj się z lekarzem, jeśli masz wodniste stolce lub ból brzucha, który nie ustępuje. Możesz mieć gorączkę lub nie.
- Złamania kości (biodra, nadgarstka lub kręgosłupa). Złamania kości biodra, nadgarstka lub kręgosłupa mogą wystąpić u osób, które przyjmują wielokrotne dzienne dawki leków PPI i przez długi okres czasu (rok lub dłużej). Należy poinformować lekarza o złamaniu kości, zwłaszcza biodra, nadgarstka lub kręgosłupa.
- Niektóre rodzaje tocznia rumieniowatego. Toczeń rumieniowaty to choroba autoimmunologiczna (komórki odpornościowe organizmu atakują inne komórki lub narządy w organizmie). U niektórych osób przyjmujących leki PPI, w tym PRILOSEC 10 mg, mogą wystąpić pewne rodzaje tocznia rumieniowatego lub pogorszenie stanu tocznia, którego już mają. Natychmiast skontaktuj się z lekarzem, jeśli masz nowy lub nasilający się ból stawów lub wysypkę na policzkach lub ramionach, która nasila się na słońcu.
Porozmawiaj z lekarzem o ryzyku wystąpienia tych poważnych działań niepożądanych. PRILOSEC 10mg może powodować inne poważne skutki uboczne. Zobacz „Jakie są możliwe skutki uboczne PRILOSEC 20mg?”
Co to jest PRILOSEC 20mg?
Lek na receptę zwany inhibitorem pompy protonowej (PPI) stosowany w celu zmniejszenia ilości kwasu w żołądku.
U dorosłych PRILOSEC 20mg służy do:
- do 8 tygodni na gojenie się wrzodów dwunastnicy.
- 10 do 14 dni z niektórymi antybiotykami w celu leczenia infekcji wywołanej przez bakterie H. pylori. W razie potrzeby lekarz może przepisać kolejne 14 do 18 dni PRILOSEC po leczeniu antybiotykami.
- do 8 tygodni w leczeniu wrzodów żołądka.
- do 4 tygodni w leczeniu zgagi i innych objawów choroby refluksowej przełyku (GERD).
- do 8 tygodni w celu wyleczenia i złagodzenia objawów związanych z kwasami uszkodzeń wyściółki przełyku (tzw. nadżerkowe zapalenie przełyku lub EE). Lekarz może przepisać kolejne 4 tygodnie PRILOSEC 20 mg pacjentom, których EE nie goi się.
- utrzymanie gojenia EE i zapobieganie nawrotom objawów zgagi spowodowanych przez GERD. Nie wiadomo, czy PRILOSEC jest bezpieczny i skuteczny, gdy jest stosowany w tym celu przez okres dłuższy niż 12 miesięcy.
- długotrwałe leczenie stanów, w których żołądek wytwarza zbyt dużo kwasu. Obejmuje to rzadki stan zwany zespołem Zollingera-Ellisona.
U dzieci w wieku od 1 do 16 lat PRILOSEC 20mg służy do:
- do 4 tygodni w leczeniu zgagi i innych objawów związanych z GERD.
- do 8 tygodni w leczeniu GERD za pomocą EE.
- utrzymanie gojenia EE i zapobieganie nawrotom objawów zgagi spowodowanych przez GERD. Nie wiadomo, czy PRILOSEC jest bezpieczny i skuteczny, gdy jest stosowany w tym celu dłużej niż 12 miesięcy.
U dzieci w wieku od 1 miesiąca do poniżej 12 miesiąca życia, PRILOSEC 10mg służy do:
- do 6 tygodni w leczeniu GERD za pomocą EE. Nie wiadomo, czy PRILOSEC jest bezpieczny i skuteczny w innych zastosowaniach u dzieci w wieku od 1 miesiąca do mniej niż 12 miesięcy lub u dzieci w wieku poniżej 1 miesiąca.
Nie należy przyjmować leku PRILOSEC, jeśli:
- uczulenie na omeprazol, jakikolwiek inny lek PPI lub którykolwiek ze składników leku PRILOSEC. Pełna lista składników znajduje się na końcu niniejszego Przewodnika po lekach.
- przyjmowanie leku zawierającego rylpiwirynę (EDURANT, COMPLERA, ODEFSEY) stosowanego w leczeniu wirusa HIV-1 (ludzki wirus niedoboru odporności).
Przed przyjęciem PRILOSEC 20 mg należy poinformować lekarza o wszystkich swoich chorobach, w tym o:
- mają niski poziom magnezu, niski poziom wapnia i niski poziom potasu we krwi.
- są w ciąży lub planują zajść w ciążę. Nie wiadomo, czy PRILOSEC 10 mg zaszkodzi nienarodzonemu dziecku.
- karmisz piersią lub planujesz karmić piersią. PRILOSEC 40 mg może przenikać do mleka matki. Porozmawiaj z lekarzem o najlepszym sposobie karmienia dziecka, jeśli przyjmujesz PRILOSEC.
- Poinformuj lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe. Szczególnie powiedz swojemu lekarzowi, jeśli przyjmujesz lek zawierający klarytromycynę lub amoksycylinę, klopidogrel (Plavix), metotreksat (Otrxup, Rasuvo, Trexall, XATMEP), digoksynę (LANOXIN), pigułkę na wodę (diuretyk), ziele dziurawca (Hypericum perforatum) lub ryfampinę (Rimactane, Rifater, Rifamate).
Jak powinienem przyjmować PRILOSEC 20mg?
- Lek PRILOSEC 20mg należy przyjmować zgodnie z zaleceniami lekarza.
- Nie należy zmieniać dawki ani przerywać stosowania leku PRILOSEC 40 mg bez konsultacji z lekarzem.
- PRILOSEC przyjmuje się zwykle 1 raz dziennie.
- Przyjmować PRILOSEC 20mg przed posiłkiem.
- Leki zobojętniające sok żołądkowy można przyjmować razem z PRILOSEC.
- PRILOSEC miesza się z wodą i można go przyjmować doustnie lub podawać przez zgłębnik nosowo-żołądkowy lub zgłębnik żołądkowy.
- Zobacz "Instrukcja użycia" na końcu niniejszego Przewodnika po lekach, gdzie znajdują się instrukcje dotyczące mieszania i przyjmowania PRILOSEC 10 mg doustnie w wodzie lub sposobu mieszania i podawania PRILOSEC przez sondę żołądkową lub zgłębnik żołądkowy zmieszany z wodą.
- Jeśli pominiesz dawkę leku PRILOSEC, zażyj ją tak szybko, jak sobie przypomnisz. Jeśli zbliża się pora przyjęcia kolejnej dawki, nie należy przyjmować pominiętej dawki. Następną dawkę należy przyjąć o zwykłej porze. Nie należy przyjmować 2 dawek jednocześnie.
- Jeśli zażyjesz za dużo PRILOSEC, natychmiast skontaktuj się z lekarzem lub centrum kontroli zatruć pod numerem 1-800-222-1222 lub udaj się do najbliższej izby przyjęć.
Jakie są możliwe skutki uboczne PRILOSEC 40mg?
PRILOSEC może powodować poważne skutki uboczne, w tym:
- Widzieć „Jakie są najważniejsze informacje, które powinienem wiedzieć o PRILOSEC 40mg?”
- Niski poziom witaminy B-12 organizmie może wystąpić u osób, które przyjmowały PRILOSEC 40 mg przez długi czas (ponad 3 lata). Należy poinformować lekarza, jeśli wystąpią objawy niskiego poziomu witaminy B12, w tym duszność, zawroty głowy, nieregularne bicie serca, osłabienie mięśni, bladość skóry, uczucie zmęczenia, zmiany nastroju oraz mrowienie lub drętwienie rąk i nóg.
- Niski poziom magnezu i metabolizm minerałów w Twoim organizmie może się zdarzyć u osób, które przyjmowały PRILOSEC przez co najmniej 3 miesiące. Należy poinformować lekarza, jeśli występują objawy niskiego poziomu magnezu, w tym drgawki, zawroty głowy, nieregularne bicie serca, drżenie, bóle lub osłabienie mięśni oraz skurcze rąk, stóp lub głosu.
- Narośle żołądka (polipy gruczołów dna). Osoby przyjmujące leki PPI przez długi czas mają zwiększone ryzyko rozwoju pewnego rodzaju narośli żołądka zwanego polipami gruczołu dna, szczególnie po przyjmowaniu leków PPI przez ponad 1 rok.
- Ciężkie reakcje skórne. PRILOSEC może powodować rzadkie, ale ciężkie reakcje skórne, które mogą dotyczyć dowolnej części ciała. Te poważne reakcje skórne mogą wymagać leczenia w szpitalu i mogą zagrażać życiu:
- Wysypka skórna, która może objawiać się powstawaniem pęcherzy, łuszczeniem się lub krwawieniem na dowolnej części skóry (w tym na ustach, oczach, ustach, nosie, narządach płciowych, dłoniach lub stopach).
- Możesz również mieć gorączkę, dreszcze, bóle ciała, duszność lub powiększone węzły chłonne.
Należy przerwać przyjmowanie PRILOSEC 20mg i natychmiast skontaktować się z lekarzem. Objawy te mogą być pierwszą oznaką ciężkiej reakcji skórnej.
Najczęstsze działania niepożądane PRILOSEC 40 mg u dorosłych obejmują: ból głowy, ból brzucha, nudności, biegunka, wymioty i gazy.
Najczęstsze działania niepożądane leku PRILOSEC u dzieci w wieku od 1 do 16 lat obejmują: infekcja górnych dróg oddechowych, gorączka, ból głowy, ból brzucha (brzucha), nudności, biegunka, wymioty i gazy. To nie wszystkie możliwe skutki uboczne PRILOSEC. Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać PRILOSEC 40mg?
Przechowywać PRILOSEC w temperaturze pokojowej między 68 ° F do 77 ° F (20 ° C do 25 ° C).
Przechowywać PRILOSEC 20 mg i wszystkie leki w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu PRILOSEC.
Leki są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Nie należy stosować leku PRILOSEC w stanach, na które nie został przepisany. Nie należy podawać leku PRILOSEC 40 mg innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić. Możesz poprosić swojego lekarza lub farmaceutę o informacje o PRILOSEC 20mg, które są przeznaczone dla pracowników służby zdrowia.
Jakie są składniki PRILOSEC?
Składnik czynny: omeprazol magnez
Nieaktywne składniki: monostearynian glicerolu, hydroksypropyloceluloza, hypromeloza, stearynian magnezu, kopolimer C kwasu metakrylowego, polisorbat, kulki cukrowe, talk i cytrynian trietylu, a także nieaktywne granulki. Nieaktywne granulki składają się z kwasu cytrynowego, krospowidonu, dekstrozy, hydroksypropylocelulozy, tlenku żelaza i gumy ksantanowej.
INSTRUKCJA UŻYCIA
PRILOSEC® (pry-lo-sec) (omeprazol magnezowy) do sporządzania zawiesiny doustnej o opóźnionym uwalnianiu
Przyjmowanie PRILOSEC 40mg w wodzie:
Podawanie PRILOSEC z wodą przez sondę nosowo-żołądkową (NG) lub sondę żołądkową:
Osobom, które mają zgłębnik nosowo-żołądkowy lub zgłębnik żołądkowy w rozmiarze 6 lub większym, PRILOSEC można podać w następujący sposób:
Ten przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków
