Clozaril 25mg, 50mg, 100mg Clozapine Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Klozaril i jak się go stosuje?
Clozaril 100mg jest lekiem na receptę stosowanym w leczeniu objawów schizofrenii. Clozaril 50mg może być stosowany samodzielnie lub z innymi lekami.
Clozaril 100mg należy do klasy leków przeciwpsychotycznych drugiej generacji.
Nie wiadomo, czy Clozaril 25 mg jest bezpieczny i skuteczny u dzieci.
Jakie są możliwe skutki uboczne leku Clozaril?
Clozaril może powodować poważne działania niepożądane, w tym:
- słabość,
- gorączka,
- obrzęk dziąseł,
- ból gardła,
- bolesne owrzodzenia jamy ustnej,
- ból podczas połykania,
- owrzodzenia skóry,
- objawy przeziębienia lub grypy,
- kaszel,
- problemy z oddychaniem,
- niekontrolowane ruchy mięśni warg, języka, oczu, twarzy, rąk lub nóg,
- ból głowy z bólem w klatce piersiowej i silnymi zawrotami głowy,
- bicie serca,
- fruwające w piersi,
- zawroty,
- nagły kaszel,
- szybkie oddychanie,
- kaszel krwią,
- uczucie ucisku w szyi lub szczęce,
- drganie lub niekontrolowane ruchy mięśni,
- napady padaczkowe (zaciemnienia lub drgawki),
- małe lub brak oddawania moczu,
- obrzęk stóp lub kostek,
- zmęczenie,
- duszność,
- mdłości,
- ból w górnej części brzucha,
- utrata apetytu,
- nietypowe krwawienie,
- ciemny mocz,
- stołki w kolorze gliny,
- zażółcenie skóry lub oczu (żółtaczka),
- bardzo sztywne (sztywne) mięśnie,
- wysoka gorączka,
- wyzysk,
- dezorientacja,
- szybkie lub nierówne bicie serca,
- drżenia,
- zwiększone pragnienie,
- zwiększone oddawanie moczu,
- głód,
- suchość w ustach,
- owocowy zapach oddechu,
- senność,
- sucha skóra,
- rozmazany obraz,
- odchudzanie,
- łatwe siniaczenie lub krwawienie,
- silne mrowienie lub drętwienie,
- słabe mięśnie,
- ból w górnej części brzucha,
- ból w klatce piersiowej,
- nowy lub pogarszający się kaszel oraz
- problemy z oddychaniem
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze działania niepożądane leku Clozaril to:
- przybranie na wadze,
- drżenie,
- zawroty głowy,
- uczucie wirowania,
- ból głowy,
- senność,
- mdłości,
- zaparcie,
- suchość w ustach,
- zwiększone wydzielanie śliny,
- rozmazany obraz,
- szybkie tętno i
- zwiększona potliwość
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne leku Clozaril. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OSTRZEŻENIE
CIĘŻKA NEUTROPENIA; NIEDOCIŚNIENIE ORTOSTATYCZNE, BRADYKARDIA I OMDLE; KONFISKATA; Zapalenie mięśnia sercowego i kardiomiopatia; ZWIĘKSZONA ŚMIERTELNOŚĆ U PACJENTÓW W PODESZŁYM WIEKU Z PSYCHOZĄ ZWIĄZANĄ Z ODMĘDZENIEM
Ciężka neutropenia
Leczenie produktem CLOZARIL spowodowało ciężką neutropenię, definiowaną jako bezwzględna liczba neutrofili (ANC) poniżej 500/μl. Ciężka neutropenia może prowadzić do poważnej infekcji i śmierci. Przed rozpoczęciem leczenia produktem leczniczym CLOZARIL wyjściowa wartość ANC musi wynosić co najmniej 1500/ μl dla populacji ogólnej; i musi wynosić co najmniej 1000/μl u pacjentów z udokumentowaną łagodną neutropenią etniczną (BEN). Podczas leczenia pacjenci muszą regularnie monitorować ANC. Należy doradzić pacjentom, aby natychmiast zgłaszali objawy odpowiadające ciężkiej neutropenii lub infekcji (np. gorączka, osłabienie, letarg lub ból gardła) [patrz DAWKOWANIE I PODAWANIE oraz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
Ze względu na ryzyko ciężkiej neutropenii, CLOZARIL jest dostępny tylko w ramach ograniczonego programu w ramach strategii łagodzenia ryzyka (REMS) zwanej Clozapine REMS Program. [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
Niedociśnienie ortostatyczne, bradykardia, omdlenia
Podczas leczenia produktem leczniczym CLOZARIL występowało niedociśnienie ortostatyczne, bradykardia, omdlenia i zatrzymanie akcji serca. Ryzyko jest największe w początkowym okresie zwiększania dawki, szczególnie w przypadku szybkiego zwiększania dawki. Reakcje te mogą wystąpić przy pierwszej dawce, przy dawkach tak niskich, jak 12,5 mg na dobę. Rozpocznij leczenie od 12,5 mg raz lub dwa razy dziennie; miareczkować powoli; i stosować podzielone dawki. Należy zachować ostrożność podczas stosowania leku Clozarilu u pacjentów z chorobami układu krążenia lub naczyń mózgowych lub ze stanami predysponującymi do niedociśnienia (np. odwodnienie, stosowanie leków przeciwnadciśnieniowych) [patrz DAWKOWANIE I PODAWANIE oraz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
Napady padaczkowe
Podczas leczenia lekiem CLOZARIL 25 mg wystąpiły napady drgawkowe. Ryzyko jest zależne od dawki. Rozpocznij leczenie od 12,5 mg, stopniowo miareczkuj i stosuj dawki podzielone. Należy zachować ostrożność podczas podawania leku Clozarilu 50 mg pacjentom z napadami drgawkowymi w wywiadzie lub innymi czynnikami predysponującymi do wystąpienia napadów (patologia OUN, leki obniżające próg drgawkowy, nadużywanie alkoholu). Należy ostrzec pacjentów przed wykonywaniem jakichkolwiek czynności, w których nagła utrata przytomności może spowodować poważne zagrożenie dla nich samych lub innych [patrz DAWKOWANIE I PODAWANIE, OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
Zapalenie mięśnia sercowego i kardiomiopatia
Podczas leczenia produktem leczniczym CLOZARIL wystąpiło śmiertelne zapalenie mięśnia sercowego i kardiomiopatia. W przypadku podejrzenia wystąpienia tych reakcji należy odstawić lek CLOZARIL 25 mg i wykonać ocenę serca. Zasadniczo pacjenci z zapaleniem mięśnia sercowego lub kardiomiopatią związanym z klozarylem nie powinni być ponownie leczeni produktem CLOZARIL. Rozważ możliwość zapalenia mięśnia sercowego lub kardiomiopatii, jeśli wystąpi ból w klatce piersiowej, tachykardia, kołatanie serca, duszność, gorączka, objawy grypopodobne, niedociśnienie lub zmiany w EKG [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
Zwiększona śmiertelność u starszych pacjentów z psychozą związaną z demencją
Pacjenci w podeszłym wieku z psychozą otępienną leczeni lekami przeciwpsychotycznymi są narażeni na zwiększone ryzyko zgonu. CLOZARIL nie jest zatwierdzony do stosowania u pacjentów z psychozą związaną z otępieniem [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
OPIS
CLOZARIL® (klozapina), atypowy lek przeciwpsychotyczny, jest tricykliczną pochodną dibenzodiazepiny, 8-chloro-11-(4-metylo-1-piperazynylo)-5H-dibenzo[b,e][1,4]diazepiną. Wzór strukturalny to
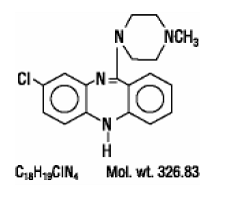
CLOZARIL jest dostępny w jasnożółtych tabletkach 25 mg i 100 mg do podawania doustnego.
Składnik czynny: klozapina
Składniki nieaktywne to koloidalny dwutlenek krzemu, laktoza, stearynian magnezu, powidon, skrobia (kukurydza) i talk.
WSKAZANIA
Schizofrenia oporna na leczenie
CLOZARIL 50 mg jest wskazany w leczeniu ciężko chorych pacjentów ze schizofrenią, którzy nie reagują odpowiednio na standardowe leczenie przeciwpsychotyczne. Ze względu na związane z jego stosowaniem ryzyko ciężkiej neutropenii i napadów drgawkowych, produkt leczniczy CLOZARIL należy stosować wyłącznie u pacjentów, którzy nie zareagowali odpowiednio na standardowe leczenie przeciwpsychotyczne [patrz OSTRZEŻENIA I ŚRODKI ].
Skuteczność preparatu CLOZARIL w leczeniu schizofrenii opornej na leczenie wykazano w 6-tygodniowym, randomizowanym, podwójnie zaślepionym, aktywnie kontrolowanym badaniu porównującym preparat CLOZARIL i chlorpromazynę u pacjentów, u których inne leki przeciwpsychotyczne nie powiodły się [patrz Studia kliniczne ].
Zmniejszenie ryzyka nawrotów zachowań samobójczych w schizofrenii lub zaburzeniu schizoafektywnym
CLOZARIL jest wskazany w celu zmniejszenia ryzyka nawrotów zachowań samobójczych u pacjentów ze schizofrenią lub zaburzeniami schizoafektywnymi, u których stwierdzono przewlekłe ryzyko ponownego wystąpienia zachowań samobójczych, na podstawie wywiadu i niedawnego stanu klinicznego. Zachowania samobójcze odnoszą się do działań pacjenta, które narażają go na ryzyko śmierci.
Skuteczność preparatu CLOZARIL w zmniejszaniu ryzyka nawrotów zachowań samobójczych została wykazana w ciągu dwuletniego okresu leczenia w badaniu InterSePT™ [patrz Studia kliniczne ].
DAWKOWANIE I SPOSÓB PODAWANIA
Wymagane badania laboratoryjne przed rozpoczęciem i podczas terapii
Przed rozpoczęciem leczenia produktem leczniczym CLOZARIL należy uzyskać wyjściową wartość ANC. Wyjściowa wartość ANC musi wynosić co najmniej 1500/μl w populacji ogólnej i co najmniej 1000/μl u pacjentów z udokumentowaną łagodną neutropenią etniczną (BEN). Aby kontynuować leczenie, ANC musi być regularnie monitorowana [patrz OSTRZEŻENIA I ŚRODKI ].
Informacje o dawkowaniu
Dawka początkowa wynosi 12,5 mg raz na dobę lub dwa razy na dobę. Całkowitą dawkę dobową można zwiększać o 25 mg do 50 mg na dobę, jeśli jest dobrze tolerowana, aby osiągnąć docelową dawkę 300 mg do 450 mg na dobę (podawaną w dawkach podzielonych) przed końcem 2 tygodni. Następnie dawkę można zwiększać raz w tygodniu lub dwa razy w tygodniu, w przyrostach do 100 mg. Maksymalna dawka to 900 mg na dobę. Aby zminimalizować ryzyko niedociśnienia ortostatycznego, bradykardii i omdleń, konieczne jest stosowanie tej małej dawki początkowej, schematu stopniowego zwiększania dawki i dawek podzielonych [patrz OSTRZEŻENIA I ŚRODKI ].
CLOZARIL można przyjmować z jedzeniem lub bez jedzenia [patrz Farmakokinetyka ].
Leczenie podtrzymujące
Ogólnie rzecz biorąc, pacjenci reagujący na leczenie produktem leczniczym CLOZARIL powinni kontynuować leczenie podtrzymujące skuteczną dawką poza ostrym epizodem.
Przerwanie leczenia
Sposób przerwania leczenia będzie się różnić w zależności od ostatniego ANC pacjenta:
- Odpowiednie monitorowanie ANC na podstawie poziomu neutropenii, jeśli nagłe przerwanie leczenia jest konieczne z powodu umiarkowanej do ciężkiej neutropenii, przedstawiono w Tabelach 2 lub 3.
- Dawkę należy zmniejszać stopniowo przez okres od 1 do 2 tygodni, jeśli planowane jest przerwanie leczenia produktem leczniczym CLOZARIL 50 mg i nie ma dowodów na umiarkowaną lub ciężką neutropenię.
- W przypadku nagłego przerwania leczenia klozapiną z powodu niezwiązanego z neutropenią, u pacjentów z populacji ogólnej zaleca się kontynuację dotychczasowego monitorowania ANC do czasu, gdy ANC wyniesie ≥1500/μl oraz u pacjentów z BEN do czasu, gdy ANC będzie ≥1000/μl lub powyżej wartości wyjściowej.
- Dodatkowe monitorowanie ANC jest wymagane w przypadku każdego pacjenta zgłaszającego wystąpienie gorączki (temperatura 38,5°C lub 101,3°F lub wyższa) w ciągu 2 tygodni po odstawieniu [patrz OSTRZEŻENIA I ŚRODKI ].
- Uważnie monitoruj wszystkich pacjentów pod kątem nawrotu objawów psychotycznych i objawów związanych z nawrotem cholinergicznym, takich jak obfite pocenie się, ból głowy, nudności, wymioty i biegunka.
Ponowne rozpoczęcie leczenia
W przypadku wznowienia leczenia produktem leczniczym Clozaryl u pacjentów, którzy przerwali leczenie produktem leczniczym Clozaryl (tj. 2 dni lub więcej od ostatniej dawki), należy ponownie rozpocząć leczenie od dawki 12,5 mg raz na dobę lub dwa razy na dobę. Jest to konieczne, aby zminimalizować ryzyko niedociśnienia, bradykardii i omdleń [patrz OSTRZEŻENIA I ŚRODKI ]. Jeśli ta dawka jest dobrze tolerowana, dawkę można zwiększyć do poprzedniej dawki terapeutycznej szybciej niż zalecana w początkowym leczeniu.
Dostosowanie dawkowania przy jednoczesnym stosowaniu inhibitorów CYP1A2, CYP2D6, CYP3A4 lub induktorów CYP1A2, CYP3A4
Dostosowanie dawki może być konieczne u pacjentów stosujących jednocześnie: silne inhibitory CYP1A2 (np. fluwoksamina, cyprofloksacyna lub enoksacyna); umiarkowane lub słabe inhibitory CYP1A2 (np. doustne środki antykoncepcyjne lub kofeina); inhibitory CYP2D6 lub CYP3A4 (np. cymetydyna, escitalopram, erytromycyna, paroksetyna, bupropion, fluoksetyna, chinidyna, duloksetyna, terbinafina lub sertralina); induktory CYP3A4 (np. fenytoina, karbamazepina, ziele dziurawca i ryfampicyna); lub induktory CYP1A2 (np. palenie tytoniu) (Tabela 1) [patrz INTERAKCJE Z LEKAMI ].
Zaburzenia czynności nerek lub wątroby lub słabe metabolizmy CYP2D6
Może być konieczne zmniejszenie dawki 50 mg produktu Clozarilu u pacjentów ze znacznymi zaburzeniami czynności nerek lub wątroby lub u pacjentów słabo metabolizujących z udziałem CYP2D6 [patrz Używaj w określonych populacjach ].
JAK DOSTARCZONE
Formy dawkowania i mocne strony
CLOZARIL (klozapina) jest dostępny w postaci okrągłych, bladożółtych, niepowlekanych tabletek 25 mg, 50 mg i 100 mg, z rowkiem dzielącym po jednej stronie. Lek Clozaril (klozapina) 200 mg to bladożółte, niepowlekane tabletki w kształcie kapsułki, z rowkiem dzielącym po jednej stronie.
Tabletki CLOZARIL® (klozapina)
25 mg
Okrągła, bladożółta, niepowlekana tabletka. Z wytłoczonym napisem „CLOZARIL” po jednej stronie. Wytłoczony z ułatwionym wynikiem i jednorazowo „25” po drugiej stronie. Butelka 100 .......... NDC 69809-0126-05
50 mg
Okrągła, bladożółta, niepowlekana tabletka. Z wytłoczonym napisem „CLOZARIL” po jednej stronie. Wytłoczone „50”, ułatwiony wynik i „mg” po drugiej stronie. Butelka 100 .......... NDC 69809-0130-05
100 mg
Okrągła, bladożółta, niepowlekana tabletka. Z wytłoczonym napisem „CLOZARIL” po jednej stronie. Wytłoczony z ułatwionym wynikiem i jednorazowo „100” po drugiej stronie. Butelka 100 .......... NDC 69809-0127-05
200 mg
Bladożółta, niepowlekana tabletka w kształcie kapsułki. Z wytłoczonym napisem „CLOZARIL” po jednej stronie. Z wytłoczonym „200”, uproszczoną punktacją i „mg” po drugiej stronie. Butelka 100 .......... NDC 69809-0135-05
Składowania i stosowania
Temperatura przechowywania nie powinna przekraczać 30°C (86°F).
Trzymać poza zasięgiem dzieci.
Dystrybucja: HLS Therapeutics (USA), Inc., Rosemont, PA 19010, (844) 457-8721. Zmieniono: luty 2021
SKUTKI UBOCZNE
Następujące działania niepożądane omówiono bardziej szczegółowo w innych punktach oznakowania:
- Ciężka neutropenia [patrz OSTRZEŻENIA I ŚRODKI ]
- Niedociśnienie ortostatyczne, bradykardia i omdlenia [patrz OSTRZEŻENIA I ŚRODKI ]
- Upadki [patrz OSTRZEŻENIA I ŚRODKI ]
- Napady [patrz OSTRZEŻENIA I ŚRODKI ]
- Zapalenie mięśnia sercowego, kardiomiopatia i niedomykalność zastawki mitralnej [patrz OSTRZEŻENIA I ŚRODKI ]
- Zwiększona śmiertelność u starszych pacjentów z psychozą związaną z demencją [patrz OSTRZEŻENIA I ŚRODKI ]
- Nieruchomość przewodu pokarmowego z poważnymi powikłaniami [Patrz OSTRZEŻENIA I ŚRODKI ]
- Eozynofilia [patrz OSTRZEŻENIA I ŚRODKI ]
- Wydłużenie odstępu QT [patrz OSTRZEŻENIA I ŚRODKI ]
- Zmiany metaboliczne (hiperglikemia i cukrzyca, dyslipidemia i przyrost masy ciała) [patrz OSTRZEŻENIA I ŚRODKI ]
- Złośliwy Zespół Neuroleptyczny [patrz OSTRZEŻENIA I ŚRODKI ]
- Hepatotoksyczność [patrz OSTRZEŻENIA I ŚRODKI ]
- Gorączka [patrz OSTRZEŻENIA I ŚRODKI ]
- Zator płucny [patrz OSTRZEŻENIA I ŚRODKI ]
- Toksyczność antycholinergiczna [patrz OSTRZEŻENIA I ŚRODKI ]
- Zakłócanie sprawności poznawczej i ruchowej [patrz OSTRZEŻENIA I ŚRODKI ]
- Późne dyskinezy [patrz OSTRZEŻENIA I ŚRODKI ]
- Działania niepożądane dotyczące naczyń mózgowych [patrz OSTRZEŻENIA I ŚRODKI ]
- Nawrót psychozy i nawrót cholinergiczny po nagłym odstawieniu [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce klinicznej.
Najczęściej zgłaszanymi działaniami niepożądanymi (≥5%) w badaniach klinicznych produktu CLOZARIL były: reakcje ośrodkowego układu nerwowego, w tym uspokojenie polekowe, zawroty głowy/zawroty głowy, ból głowy i drżenie; reakcje sercowo-naczyniowe, w tym tachykardia, niedociśnienie i omdlenia; reakcje autonomicznego układu nerwowego, w tym nadmierne ślinienie się, pocenie się, suchość w ustach i zaburzenia widzenia; reakcje żołądkowo-jelitowe, w tym zaparcia i nudności; i gorączka. W Tabeli 9 podsumowano najczęściej zgłaszane działania niepożądane (≥5%) u pacjentów leczonych produktem leczniczym CLOZARIL (w porównaniu z pacjentami leczonymi chlorpromazyną) w głównym, 6-tygodniowym, kontrolowanym badaniu dotyczącym schizofrenii opornej na leczenie.
Tabeli 10 podsumowano działania niepożądane zgłaszane u pacjentów leczonych preparatem CLOZARIL z częstością 2% lub większą we wszystkich badaniach preparatu CLOZARIL (z wyjątkiem 2-letniego badania InterSePT™). Stawki te nie są dostosowywane do czasu trwania ekspozycji.
Tabela 11 podsumowuje najczęściej zgłaszane działania niepożądane (>10% w grupie CLOZARIL lub olanzapiny) w badaniu InterSePT™. Było to odpowiednie i dobrze kontrolowane, dwuletnie badanie oceniające skuteczność produktu CLOZARIL w porównaniu z olanzapiną w zmniejszaniu ryzyka zachowań samobójczych u pacjentów ze schizofrenią lub zaburzeniami schizoafektywnymi. Stawki nie są dostosowywane do czasu trwania ekspozycji.
Dystonia
Efekt klasowy
Objawy dystonii, przedłużające się nieprawidłowe skurcze grup mięśni, mogą wystąpić u osób podatnych w ciągu pierwszych kilku dni leczenia. Objawy dystoniczne obejmują: skurcz mięśni szyi, czasami przechodzący w ucisk w gardle, trudności w połykaniu, trudności w oddychaniu i (lub) wysunięcie języka. Chociaż objawy te mogą wystąpić przy niskich dawkach, występują częściej i z większym nasileniem przy dużej sile działania i przy wyższych dawkach leków przeciwpsychotycznych pierwszej generacji. Podwyższone ryzyko ostrej dystonii obserwuje się u mężczyzn i młodszych grup wiekowych.
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania klozapiny po dopuszczeniu do obrotu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Ośrodkowy układ nerwowy
Majaczenie, nieprawidłowy zapis EEG, mioklonie, parestezje, możliwa katapleksja, stan padaczkowy, objawy obsesyjno-kompulsyjne, zespół niespokojnych nóg i niepożądane reakcje cholinergiczne po odstawieniu leku.
Układu sercowo-naczyniowego
Migotanie przedsionków lub komór, częstoskurcz komorowy, kołatanie serca, wydłużenie odstępu QT, Torsades de Pointes, niedomykalność zastawki mitralnej związana z kardiomiopatią związaną z klozapiną, zawał mięśnia sercowego, zatrzymanie akcji serca, zapalenie mięśnia sercowego i obrzęk okołooczodołowy.
Układ hormonalny
Pseudopheochromocytoma
Układ pokarmowy
Ostre zapalenie trzustki, dysfagia, obrzęk ślinianek, zapalenie okrężnicy, rozdęcie okrężnicy, niedokrwienie jelit lub zawał.
Układ wątrobowo-żółciowy
Cholestaza, zapalenie wątroby, żółtaczka, hepatotoksyczność, stłuszczenie wątroby, martwica wątroby, zwłóknienie wątroby, marskość wątroby, uszkodzenie wątroby (wątrobowe, cholestatyczne i mieszane) i niewydolność wątroby.
Zaburzenia układu immunologicznego
Obrzęk naczynioruchowy, leukocytoklastyczne zapalenie naczyń.
Układ moczowo-płciowy
Ostre śródmiąższowe zapalenie nerek, moczenie nocne, priapizm, niewydolność nerek i wytrysk wsteczny.
Zaburzenia skóry i tkanki podskórnej
Reakcje nadwrażliwości: nadwrażliwość na światło, zapalenie naczyń, rumień wielopostaciowy, zaburzenia pigmentacji skóry i zespół Stevensa-Johnsona.
Zaburzenia układu mięśniowo-szkieletowego i tkanki łącznej
Zespół miasteniczny, rabdomioliza i toczeń rumieniowaty układowy.
Układ oddechowy
Aspiracja, wysięk opłucnowy, zapalenie płuc, infekcja dolnych dróg oddechowych, bezdech senny.
Układ hemiczny i limfatyczny
Łagodna, umiarkowana lub ciężka leukopenia, agranulocytoza, granulocytopenia, zmniejszenie liczby białych krwinek, zakrzepica żył głębokich, podwyższony poziom hemoglobiny/hematokrytu, zwiększona szybkość sedymentacji erytrocytów (OB), posocznica, trombocytoza i trombocytopenia.
Zaburzenia widzenia
Jaskra z wąskim kątem przesączania.
Różnorodny
Zwiększenie aktywności fosfokinazy kreatynowej, hiperurykemia, hiponatremia, zapalenie błon surowiczych i utrata masy ciała.
INTERAKCJE Z LEKAMI
Potencjalny wpływ innych leków na CLOZARIL®
Klozapina jest substratem wielu izoenzymów cytochromu P450, w szczególności CYP1A2, CYP3A4 i CYP2D6. Należy zachować ostrożność, podając 100 mg leku Clozarilu jednocześnie z lekami, które są induktorami lub inhibitorami tych enzymów.
Inhibitory CYP1A2
Jednoczesne stosowanie produktu CLOZARIL i inhibitorów CYP1A2 może zwiększać stężenie klozapiny w osoczu, potencjalnie prowadząc do działań niepożądanych. Zmniejsz dawkę produktu CLOZARIL do jednej trzeciej dawki początkowej, gdy produkt CLOZARIL jest podawany jednocześnie z silnymi inhibitorami CYP1A2 (np. fluwoksaminą, cyprofloksacyną lub enoksacyną). Dawkę produktu CLOZARIL należy zwiększyć do pierwotnej dawki w przypadku przerwania jednoczesnego podawania silnych inhibitorów CYP1A2 [patrz DAWKOWANIE I SPOSÓB PODAWANIA , FARMAKOLOGIA KLINICZNA ].
Umiarkowane lub słabe inhibitory CYP1A2 obejmują doustne środki antykoncepcyjne i kofeinę. Uważnie monitorować pacjentów, gdy CLOZARIL jest podawany jednocześnie z tymi inhibitorami. W razie potrzeby rozważ zmniejszenie dawki 25 mg preparatu CLOZARIL [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Inhibitory CYP2D6 i CYP3A4
Jednoczesne leczenie produktem CLOZARIL i inhibitorami CYP2D6 lub CYP3A4 (np. cymetydyna, escitalopram, erytromycyna, paroksetyna, bupropion, fluoksetyna, chinidyna, duloksetyna, terbinafina lub sertralina) może zwiększać stężenie klozapiny i prowadzić do działań niepożądanych [patrz FARMAKOLOGIA KLINICZNA ]. Należy zachować ostrożność i uważnie monitorować pacjentów podczas stosowania takich inhibitorów. Rozważyć zmniejszenie dawki leku Clozarilu 100 mg [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Induktory CYP1A2 i CYP3A4
Jednoczesne leczenie lekami, które indukują CYP1A2 lub CYP3A4 może zmniejszać stężenie klozapiny w osoczu, co skutkuje zmniejszoną skutecznością produktu CLOZARIL. Dym tytoniowy jest umiarkowanym induktorem CYP1A2. Silne induktory CYP3A4 obejmują karbamazepinę, fenytoinę, ziele dziurawca i ryfampicynę. Może zaistnieć konieczność zwiększenia dawki leku Clozarilu 50 mg w przypadku jednoczesnego stosowania z induktorami tych enzymów. Nie zaleca się jednak jednoczesnego stosowania produktu CLOZARIL i silnych induktorów CYP3A4 [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Rozważyć zmniejszenie dawki leku Clozarilu 50 mg w przypadku odstawienia jednocześnie podawanych induktorów enzymów; ponieważ odstawienie induktorów może spowodować zwiększenie stężenia klozapiny w osoczu i zwiększone ryzyko działań niepożądanych [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Leki antycholinergiczne
Jednoczesne leczenie klozapiną i innymi lekami o działaniu przeciwcholinergicznym (np. benztropiną, cyklobenzapryną, difenhydraminą) może zwiększać ryzyko toksyczności przeciwcholinergicznej i ciężkich działań niepożądanych ze strony przewodu pokarmowego związanych z osłabieniem ruchliwości. Jeśli to możliwe, należy unikać jednoczesnego stosowania produktu leczniczego CLOZARIL z lekami antycholinergicznymi [patrz OSTRZEŻENIA I ŚRODKI ].
Leki powodujące wydłużenie odstępu QT
Należy zachować ostrożność podczas jednoczesnego podawania leków wydłużających odstęp QT lub hamujących metabolizm klozapiny. Leki powodujące wydłużenie odstępu QT obejmują: specyficzne leki przeciwpsychotyczne (np. zyprazydon, iloperidon, chlorpromazyna, tiorydazyna, mesorydazyna, droperydol i pimozyd), specyficzne antybiotyki (np. erytromycyna, gatifloksacyna, moksyfloksacyna, sparfloksacyna, antysachina, klasa 1 prokainamid) lub leki przeciwarytmiczne klasy III (np. amiodaron, sotalol) i inne (np. pentamidyna, octan lewometadylu, metadon, halofantryna, meflochina, mesylan dolasetronu, probukol lub takrolimus) [patrz OSTRZEŻENIA I ŚRODKI ].
Potencjał działania CLOZARILU na inne leki
Jednoczesne stosowanie produktu CLOZARIL 25 mg z innymi lekami metabolizowanymi przez CYP2D6 może zwiększać poziomy tych substratów CYP2D6. Należy zachować ostrożność podczas jednoczesnego podawania produktu Clozaryl 50 mg z innymi lekami metabolizowanymi przez CYP2D6. Może być konieczne stosowanie mniejszych dawek takich leków niż zwykle przepisywane. Takie leki obejmują specyficzne antydepresanty, fenotiazyny, karbamazepinę i leki przeciwarytmiczne typu 1C (np. propafenon, flekainid i enkainid).
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Ciężka neutropenia
Tło
CLOZARIL może powodować neutropenię (niską bezwzględną liczbę neutrofili (ANC)), definiowaną jako zmniejszenie liczby neutrofili we krwi poniżej prawidłowego poziomu przed leczeniem. ANC jest zwykle dostępny jako składnik pełnej morfologii krwi (CBC), w tym rozmazu, i ma większe znaczenie dla neutropenii polekowej niż liczba białych krwinek (WBC). ANC można również obliczyć przy użyciu następującego wzoru: ANC równa się całkowitej liczbie WBC pomnożonej przez całkowity odsetek neutrofili uzyskanych z różnicowania ("segs" neutrofili plus "prążki" neutrofili). Inne granulocyty (bazofile i eozynofile) w minimalnym stopniu przyczyniają się do neutropenii i ich pomiar nie jest konieczny [patrz DZIAŁANIA NIEPOŻĄDANE ]. Neutropenia może być łagodna, umiarkowana lub ciężka (patrz Tabele 2 i 3). Aby poprawić i ujednolicić zrozumienie, „ciężka neutropenia” zastępuje poprzednie terminy: ciężka leukopenia, ciężka granulocytopenia lub agranulocytoza.
Ciężka neutropenia, ANC poniżej (
Poniżej przedstawiono dwa oddzielne algorytmy postępowania, pierwszy dla pacjentów w populacji ogólnej, a drugi dla pacjentów z wyjściową neutropenią.
Leczenie i monitorowanie produktu CLOZARIL w ogólnej populacji pacjentów (patrz Tabela 2)
Przed rozpoczęciem leczenia produktem leczniczym CLOZARIL 25 mg należy uzyskać CBC, w tym wartość ANC, aby upewnić się, że wyjściowa liczba neutrofili jest prawidłowa (równa lub większa niż 1500/μl) i aby umożliwić późniejsze porównania. Pacjenci w populacji ogólnej z ANC równym lub większym niż (≥)1500/μl są uważani za mieszczących się w normalnym zakresie (Tabela 2) i kwalifikują się do rozpoczęcia leczenia. Cotygodniowe monitorowanie ANC jest wymagane u wszystkich pacjentów w ciągu pierwszych 6 miesięcy leczenia. Jeśli ANC pacjenta utrzymuje się na poziomie lub większym niż 1500/μl przez pierwsze 6 miesięcy leczenia, częstotliwość monitorowania można zmniejszyć do co 2 tygodni przez kolejne 6 miesięcy. Jeśli ANC pozostaje równe lub większe niż 1500/μl przez drugie 6 miesięcy ciągłej terapii, częstotliwość monitorowania ANC można następnie zmniejszyć do 1 raz na 4 tygodnie.
CLOZARIL Leczenie i monitorowanie pacjentów z łagodną neutropenią etniczną (patrz Tabela 3)
Łagodna neutropenia etniczna (BEN) jest stanem obserwowanym w pewnych grupach etnicznych, których średnie wartości ANC są niższe niż „standardowe” zakresy laboratoryjne dla neutrofili. Najczęściej obserwuje się ją u osób pochodzenia afrykańskiego (przybliżona częstość występowania 25-50%), niektórych grup etnicznych Bliskiego Wschodu oraz innych niekaukaskich grup etnicznych o ciemniejszej skórze. BEN występuje częściej u mężczyzn. Pacjenci z BEN mają prawidłową liczbę hematopoetycznych komórek macierzystych i dojrzewanie szpiku, są zdrowi i nie cierpią na powtarzające się lub ciężkie infekcje. Nie są narażeni na zwiększone ryzyko rozwoju neutropenii wywołanej przez CLOZARIL. Może być konieczna dodatkowa ocena w celu ustalenia, czy wyjściowa neutropenia jest spowodowana BEN. W razie potrzeby należy rozważyć konsultację hematologiczną przed rozpoczęciem lub w trakcie leczenia lekiem CLOZARIL 50 mg.
Pacjenci z BEN wymagają innego algorytmu ANC do leczenia produktem CLOZARIL ze względu na niższe wyjściowe poziomy ANC. W Tabeli 3 przedstawiono wytyczne dotyczące prowadzenia leczenia produktem leczniczym CLOZARIL 100 mg i monitorowania ANC u pacjentów z BEN.
Ogólne wytyczne dotyczące postępowania u wszystkich pacjentów z gorączką lub neutropenią
- Gorączka: zapobiegawczo należy przerwać stosowanie produktu CLOZARIL u każdego pacjenta, u którego wystąpi gorączka, definiowana jako temperatura 38,5°C [101,3°F] lub wyższa i uzyskać poziom ANC. Gorączka jest często pierwszą oznaką infekcji neutropenicznej.
- ANC poniżej 1000/μl: Jeśli u dowolnego pacjenta z ANC poniżej 1000/μl wystąpi gorączka, należy rozpocząć odpowiednie leczenie i leczenie zakażenia i zapoznać się z tabelami 2 lub 3 dotyczącymi postępowania.
- Rozważ konsultację hematologiczną.
- Złośliwy zespół neuroleptyczny [NMS] i gorączka poniżej OSTRZEŻENIA I ŚRODKI i Instrukcje dla Pacjentów, pod INFORMACJA O PACJENCIE .
Ponowne wyzwanie po ANC poniżej 500/μl (ciężka neutropenia)
przypadku niektórych pacjentów, u których występuje ciężka neutropenia związana z lekiem Clozarilem, ryzyko poważnej choroby psychicznej związane z przerwaniem leczenia lekiem Clozarilem może być większe niż ryzyko ponownego rozpoczęcia leczenia (np. pacjenci z ciężką chorobą schizofreniczną, którzy nie mają innych możliwości leczenia niż Clozarilem). Konsultacja hematologiczna może być przydatna w podjęciu decyzji o ponownym rzuceniu pacjentowi wyzwania. Ogólnie jednak nie należy ponownie prowokować pacjentów, u których rozwinęła się ciężka neutropenia, lekiem CLOZARIL lub produktem z klozapiną.
Jeśli pacjent będzie ponownie prowokowany, klinicysta powinien wziąć pod uwagę wartości progowe podane w Tabelach 2 i 3, historię medyczną i psychiatryczną pacjenta, dyskusję z pacjentem i jego opiekunem na temat korzyści i ryzyka ponownego prowokacji lekiem CLOZARIL 50 mg oraz nasilenie i charakterystykę epizodu neutropenicznego.
Stosowanie leku CLOZARIL z innymi lekami związanymi z neutropenią
Nie jest jasne, czy jednoczesne stosowanie innych leków, o których wiadomo, że powodują neutropenię, zwiększa ryzyko lub nasilenie neutropenii wywołanej przez Clozaryl. Nie ma mocnego naukowego uzasadnienia, aby unikać leczenia preparatem CLOZARIL u pacjentów jednocześnie leczonych tymi lekami. Jeśli CLOZARIL 100 mg jest stosowany jednocześnie ze środkiem, o którym wiadomo, że powoduje neutropenię (np. niektóre środki chemioterapeutyczne), należy rozważyć ściślejsze monitorowanie pacjentów niż wytyczne dotyczące leczenia przedstawione w Tabelach 2 i 3. U pacjentów otrzymujących jednocześnie chemioterapię należy skonsultować się z lekarzem onkologiem.
Program klozapina REMS
CLOZARIL jest dostępny tylko w ramach ograniczonego programu w ramach REMS o nazwie Clozapine REMS Program ze względu na ryzyko ciężkiej neutropenii.
Godne uwagi wymagania programu Clozapine REMS obejmują:
- Pracownicy służby zdrowia, którzy przepisują CLOZARIL 25 mg, muszą uzyskać certyfikat programu poprzez zapisanie się i ukończenie szkolenia
- Pacjenci otrzymujący CLOZARIL 100 mg muszą być zapisani do programu i spełniać wymagania dotyczące testowania i monitorowania ANC
- Apteki wydające CLOZARIL 50 mg muszą być certyfikowane w programie poprzez zapisanie się i ukończenie szkolenia i muszą wydawać leki tylko pacjentom, którzy są uprawnieni do otrzymywania leku CLOZARIL
Więcej informacji można znaleźć na stronie www.clozapinerems.com lub 1-844-267-8678.
Niedociśnienie ortostatyczne, bradykardia i omdlenia
Podczas leczenia klozapiną występowało niedociśnienie, bradykardia, omdlenia i zatrzymanie akcji serca. Ryzyko jest największe w początkowym okresie zwiększania dawki, szczególnie w przypadku szybkiego zwiększania dawki. Reakcje te mogą wystąpić po podaniu pierwszej dawki, już przy dawkach 12,5 mg. Te reakcje mogą być śmiertelne. Zespół jest zgodny z nerwowo zależną bradykardią odruchową (NMRB).
Leczenie należy rozpocząć od maksymalnej dawki 12,5 mg raz na dobę lub dwa razy na dobę. Całkowitą dawkę dobową można zwiększać o 25 mg do 50 mg na dobę, jeśli jest dobrze tolerowana, do dawki docelowej od 300 mg do 450 mg na dobę (podawanej w dawkach podzielonych) przed końcem 2 tygodni. Następnie dawkę można zwiększać co tydzień lub dwa razy w tygodniu, w krokach do 100 mg. Maksymalna dawka to 900 mg na dobę. Stosuj ostrożne dobieranie dawki i podzieloną dawkę, aby zminimalizować ryzyko poważnych reakcji sercowo-naczyniowych [patrz DAWKOWANIE I SPOSÓB PODAWANIA ]. W przypadku wystąpienia niedociśnienia należy rozważyć zmniejszenie dawki. W przypadku wznowienia leczenia u pacjentów, którzy mieli nawet krótką przerwę w odstawieniu leku Clozaryl (tj. 2 dni lub więcej od ostatniej dawki), należy ponownie rozpocząć leczenie dawką 12,5 mg raz na dobę lub dwa razy na dobę [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Należy zachować ostrożność stosując produkt leczniczy Clozaryl u pacjentów z chorobami układu krążenia (przebyty zawał lub niedokrwienie mięśnia sercowego, niewydolność serca lub zaburzenia przewodzenia), chorobami naczyń mózgowych i stanami predysponującymi pacjentów do niedociśnienia (np. jednoczesne stosowanie leków przeciwnadciśnieniowych, odwodnienie i hipowolemia).
Spada
CLOZARIL 25 mg może powodować senność, niedociśnienie ortostatyczne, niestabilność ruchową i czuciową, co może prowadzić do upadków, a w konsekwencji złamań lub innych urazów. W przypadku pacjentów z chorobami, schorzeniami lub lekami, które mogą nasilać te skutki, należy przeprowadzić pełną ocenę ryzyka upadków na początku leczenia przeciwpsychotycznego oraz ponownie w przypadku pacjentów poddawanych długotrwałemu leczeniu przeciwpsychotycznemu.
Napady padaczkowe
Oszacowano, że w związku ze stosowaniem klozapiny napady padaczkowe występują ze skumulowaną częstością po roku około 5%, w oparciu o wystąpienie jednego lub więcej napadów u 61 z 1743 pacjentów narażonych na klozapinę podczas badań klinicznych przed wprowadzeniem do obrotu (tj. , surowa stawka 3,5%). Ryzyko napadu jest zależne od dawki. Leczenie należy rozpocząć od małej dawki (12,5 mg), powoli miareczkować i stosować dawki podzielone.
Należy zachować ostrożność podczas podawania leku Clozarilu 50 mg pacjentom z napadami drgawkowymi w wywiadzie lub innymi czynnikami predysponującymi do wystąpienia napadów (np. uraz głowy lub inna patologia ośrodkowego układu nerwowego, stosowanie leków obniżających próg drgawkowy lub nadużywanie alkoholu). Ze względu na znaczne ryzyko wystąpienia drgawek związanych ze stosowaniem leku Clozarilu należy ostrzec pacjentów przed podejmowaniem jakichkolwiek czynności, w których nagła utrata przytomności może spowodować poważne ryzyko dla nich samych lub innych osób (np. prowadzenie samochodu, obsługa skomplikowanych maszyn, pływanie, wspinanie się).
Zapalenie mięśnia sercowego, kardiomiopatia i niedomykalność zastawki mitralnej
Podczas stosowania produktu Clozari wystąpiło zapalenie mięśnia sercowego i kardiomiopatia. Te reakcje mogą być śmiertelne. W przypadku podejrzenia zapalenia mięśnia sercowego lub kardiomiopatii należy odstawić lek CLOZARIL 25 mg i wykonać ocenę serca. Ogólnie rzecz biorąc, pacjenci z zapaleniem mięśnia sercowego lub kardiomiopatią związanym z klozapiną w wywiadzie nie powinni być ponownie leczeni produktem leczniczym CLOZARIL. Jednakże, jeśli uzna się, że korzyści z leczenia produktem leczniczym CLOZARIL w dawce 25 mg przewyższają potencjalne ryzyko nawrotu zapalenia mięśnia sercowego lub kardiomiopatii, klinicysta może rozważyć ponowne podanie leku CLOZARIL w porozumieniu z kardiologiem, po przeprowadzeniu pełnej oceny kardiologicznej i pod ścisłą kontrolą.
Należy rozważyć możliwość zapalenia mięśnia sercowego lub kardiomiopatii u pacjentów otrzymujących produkt leczniczy Clozari, u których występują bóle w klatce piersiowej, duszność, utrzymujący się tachykardia w spoczynku, kołatanie serca, gorączka, objawy grypopodobne, niedociśnienie, inne objawy przedmiotowe lub podmiotowe niewydolności serca lub wyniki elektrokardiograficzne (niskie napięcia, nieprawidłowości ST-T, arytmie, odchylenie prawej osi i słaba progresja załamka R). Zapalenie mięśnia sercowego najczęściej pojawia się w ciągu pierwszych 2 miesięcy leczenia klozapiną. Objawy kardiomiopatii zwykle pojawiają się później niż zapalenie mięśnia sercowego związane z klozapiną i zwykle po 8 tygodniach leczenia. Jednak zapalenie mięśnia sercowego i kardiomiopatia mogą wystąpić w dowolnym okresie leczenia produktem leczniczym Clozari. Często niespecyficzne objawy grypopodobne, takie jak złe samopoczucie, bóle mięśni, opłucnowy ból w klatce piersiowej i stany podgorączkowe, poprzedzają bardziej jawne objawy niewydolności serca. Typowe wyniki badań laboratoryjnych obejmują podwyższony poziom troponiny I lub T, podwyższony poziom kinazy kreatyninowej MB, obwodową eozynofilię i podwyższony poziom białka C-reaktywnego (CRP). Rentgenogram klatki piersiowej może wykazać powiększenie sylwetki serca, a obrazowanie serca (echokardiogram, badania radionukleotydowe lub cewnikowanie serca) może ujawnić dowody dysfunkcji lewej komory. U pacjentów, u których rozpoznano kardiomiopatię podczas przyjmowania leku Clozarilem 50 mg, zgłaszano niewydolność zastawki mitralnej. Przypadki te zgłaszały łagodną lub umiarkowaną niedomykalność mitralną w dwuwymiarowej echokardiografii. U pacjentów z podejrzeniem kardiomiopatii należy rozważyć wykonanie badania 2D-echo Doppler w celu wykrycia niewydolności zastawki mitralnej.
Zwiększona śmiertelność u starszych pacjentów z psychozą związaną z demencją
Pacjenci w podeszłym wieku z psychozą otępienną leczeni lekami przeciwpsychotycznymi są narażeni na zwiększone ryzyko zgonu. Analizy 17 badań kontrolowanych placebo (modalny czas trwania 10 tygodni), głównie z udziałem pacjentów przyjmujących atypowe leki przeciwpsychotyczne, wykazały ryzyko zgonu u pacjentów leczonych lekami od 1,6 do 1,7 razy większe od ryzyka zgonu u pacjentów otrzymujących placebo. W trakcie typowego 10-tygodniowego kontrolowanego badania wskaźnik zgonów u pacjentów leczonych lekiem wynosił około 4,5%, w porównaniu do około 2,6% w grupie placebo. Chociaż przyczyny zgonów były różne, większość zgonów wydawała się mieć charakter sercowo-naczyniowy (np. niewydolność serca, nagła śmierć) lub zakaźny (np. zapalenie płuc). Badania obserwacyjne sugerują, że podobnie jak w przypadku atypowych leków przeciwpsychotycznych, leczenie konwencjonalnymi lekami przeciwpsychotycznymi może zwiększać śmiertelność w tej populacji. Nie jest jasne, w jakim stopniu wyniki zwiększonej śmiertelności w badaniach obserwacyjnych można przypisać lekowi przeciwpsychotycznemu w przeciwieństwie do niektórych cech pacjentów. CLOZARIL nie jest zatwierdzony do leczenia pacjentów z psychozą związaną z otępieniem [patrz OSTRZEŻENIE W PUDEŁKU ].
Niedoczynność przewodu pokarmowego z ciężkimi powikłaniami
Ciężkie działania niepożądane ze strony przewodu pokarmowego wystąpiły podczas stosowania produktu Clozaryl, głównie ze względu na jego silne działanie przeciwcholinergiczne i wynikającą z niego hiporuchliwość przewodu pokarmowego. W doświadczeniach po wprowadzeniu produktu do obrotu zgłaszane skutki wahają się od zaparć do porażennej niedrożności jelit. Zwiększona częstość zaparć oraz opóźniona diagnostyka i leczenie zwiększały ryzyko poważnych powikłań związanych z zaburzeniami motoryki przewodu pokarmowego, skutkujących niedrożnością jelit, zatkaniem kału, rozdęciem okrężnicy i niedokrwieniem lub zawałem jelit [patrz DZIAŁANIE NIEPOŻĄDANE ]. Reakcje te doprowadziły do hospitalizacji, operacji i śmierci. Ryzyko ciężkich działań niepożądanych jest dodatkowo zwiększone w przypadku leków antycholinergicznych (i innych leków zmniejszających perystaltykę przewodu pokarmowego); dlatego w miarę możliwości należy unikać jednoczesnego stosowania [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI ].
Przed rozpoczęciem stosowania leku Clozarilu 50 mg należy przebadać pod kątem zaparć i leczyć w razie potrzeby. Subiektywne objawy zaparcia mogą nie odzwierciedlać dokładnie stopnia upośledzenia ruchliwości przewodu pokarmowego u pacjentów leczonych produktem leczniczym Clozaryl. W związku z tym często należy ponownie oceniać czynność jelit, zwracając szczególną uwagę na wszelkie zmiany w częstotliwości lub charakterze wypróżnień, a także na objawy przedmiotowe i podmiotowe powikłań niedoczynności ruchowej (np. nudności, wymioty, wzdęcia brzucha, bóle brzucha). W przypadku wykrycia zaparć lub zaburzeń motoryki przewodu pokarmowego należy ściśle monitorować i w razie potrzeby niezwłocznie leczyć odpowiednimi środkami przeczyszczającymi, aby zapobiec poważnym powikłaniom. Rozważ profilaktyczne środki przeczyszczające u pacjentów wysokiego ryzyka.
Eozynofilia
Eozynofilia, definiowana jako liczba eozynofili we krwi większa niż 700/μl, występowała podczas leczenia lekiem Clozarilem 100 mg. W badaniach klinicznych około 1% pacjentów rozwinęła eozynofilię. Eozynofilia związana z klozapiną występuje zwykle w pierwszym miesiącu leczenia. U niektórych pacjentów wiąże się to z zapaleniem mięśnia sercowego, zapaleniem trzustki, zapaleniem wątroby, zapaleniem okrężnicy i zapaleniem nerek. Takie zajęcie narządów może być zgodne z reakcją na lek z eozynofilią i zespołem objawów ogólnoustrojowych (DRESS), znanym również jako zespół nadwrażliwości wywołanej lekiem (DIHS). Jeśli eozynofilia rozwinie się podczas leczenia produktem leczniczym CLOZARIL, należy niezwłocznie ocenić objawy przedmiotowe i podmiotowe reakcji ogólnoustrojowych, takich jak wysypka lub inne objawy alergiczne, zapalenie mięśnia sercowego lub inna narządowa choroba związana z eozynofilią. W przypadku podejrzenia choroby ogólnoustrojowej związanej z lekiem CLOZARIL, należy natychmiast przerwać stosowanie leku Clozarilu 50 mg.
Jeśli zostanie zidentyfikowana przyczyna eozynofilii niezwiązana ze stosowaniem leku Clozarilu 50 mg (np. astma, alergie, choroba kolagenowa naczyń krwionośnych, infekcje pasożytnicze i określone nowotwory), wylecz przyczynę leżącą u podstaw i kontynuuj stosowanie leku Clozariol.
Eozynofilia związana z klozapiną występowała również przy braku zajęcia narządów i może ustąpić bez interwencji. Istnieją doniesienia o udanym wznowieniu leczenia po odstawieniu klozapiny bez nawrotu eozynofilii. W przypadku braku zajęcia narządów, kontynuować stosowanie leku Clozari pod ścisłą obserwacją. Jeśli całkowita liczba eozynofili wzrasta przez kilka tygodni bez choroby ogólnoustrojowej, decyzja o przerwaniu leczenia produktem leczniczym CLOZARIL 25 mg i wznowieniu leczenia po zmniejszeniu się liczby eozynofilów powinna być oparta na ogólnej ocenie klinicznej, po konsultacji z internistą lub hematologiem.
Wydłużenie odstępu QT
Podczas leczenia produktem leczniczym CLOZARIL w dawce 100 mg występowały wydłużenie odstępu QT, torsade de pointes i inne zagrażające życiu komorowe zaburzenia rytmu, zatrzymanie akcji serca i nagły zgon. Przepisując CLOZARIL, należy wziąć pod uwagę obecność dodatkowych czynników ryzyka wydłużenia odstępu QT i poważnych reakcji sercowo-naczyniowych. Stany zwiększające to ryzyko to: wydłużenie odstępu QT w wywiadzie, zespół wydłużenia odstępu QT w wywiadzie, zespół wydłużenia odstępu QT w wywiadzie rodzinnym lub nagła śmierć sercowa, znaczna arytmia serca, niedawno przebyty zawał mięśnia sercowego, niewyrównana niewydolność serca, leczenie innymi lekami powodującymi wydłużenie odstępu QT, leczenie lekami hamującymi metabolizm klozapiny i zaburzenia elektrolitowe.
Przed rozpoczęciem leczenia preparatem CLOZARIL 25 mg należy przeprowadzić dokładne badanie fizykalne, wywiad chorobowy oraz wywiad dotyczący jednoczesnego leczenia. Rozważ uzyskanie wyjściowego EKG i panelu chemii surowicy. Popraw nieprawidłowości elektrolitów. Jeśli odstęp QTc przekracza 500 ms, należy przerwać podawanie leku CLOZARIL 25 mg. Jeśli u pacjenta wystąpią objawy odpowiadające Torsades de Pointes lub inne zaburzenia rytmu (np. omdlenie, stan przedomdleniowy, zawroty głowy lub kołatanie serca), należy przeprowadzić ocenę kardiologiczną i przerwać stosowanie produktu Clozarel.
Należy zachować ostrożność podczas jednoczesnego podawania leków, które wydłużają odstęp QT lub hamują metabolizm produktu leczniczego Clozaryl. Leki, które powodują wydłużenie odstępu QT obejmują: specyficzne leki przeciwpsychotyczne (np. zyprazydon, iloperidon, chlorpromazyna, tiorydazyna, mesorydazyna, droperydol, pimozyd), specyficzne antybiotyki (np. erytromycyna, gatifloksacyna, moksyfloksacyna, sparfloksacyna prokainamid) lub leki przeciwarytmiczne klasy III (np. amiodaron, sotalol) i inne (np. pentamidyna, octan lewometadylu, metadon, halofantryna, meflochina, mesylan dolasetronu, probukol lub takrolimus). Klozapina jest metabolizowana głównie przez izoenzymy CYP 1A2, 2D6 i 3A4. Jednoczesne leczenie inhibitorami tych enzymów może zwiększać stężenie produktu Clozaryl [patrz INTERAKCJE Z LEKAMI oraz FARMAKOLOGIA KLINICZNA ].
Hipokaliemia i hipomagnezemia zwiększają ryzyko wydłużenia odstępu QT. Hipokaliemia może wynikać z leczenia moczopędnego, biegunki i innych przyczyn. Należy zachować ostrożność podczas leczenia pacjentów zagrożonych poważnymi zaburzeniami elektrolitowymi, zwłaszcza hipokaliemią. Wykonać podstawowe pomiary stężenia potasu i magnezu w surowicy i okresowo monitorować elektrolity. Skorygować nieprawidłowości elektrolitowe przed rozpoczęciem leczenia lekiem CLOZARIL.
Zmiany metaboliczne
Atypowe leki przeciwpsychotyczne, w tym CLOZARIL 50 mg, były związane ze zmianami metabolicznymi, które mogą zwiększać ryzyko sercowo-naczyniowe i mózgowo-naczyniowe. Te zmiany metaboliczne obejmują hiperglikemię, dyslipidemię i przyrost masy ciała. Chociaż atypowe leki przeciwpsychotyczne mogą powodować pewne zmiany metaboliczne, każdy lek z tej klasy ma swój własny profil ryzyka.
Hiperglikemia i cukrzyca
pacjentów leczonych atypowymi lekami przeciwpsychotycznymi, w tym produktem leczniczym CLOZARIL, zgłaszano hiperglikemię, w niektórych przypadkach skrajną i związaną z kwasicą ketonową, śpiączką hiperosmolarną lub zgonem. Ocenę związku między stosowaniem atypowych leków przeciwpsychotycznych a nieprawidłowościami glikemii komplikuje możliwość zwiększonego podstawowego ryzyka cukrzycy u pacjentów ze schizofrenią oraz wzrastająca częstość występowania cukrzycy w populacji ogólnej. Biorąc pod uwagę te czynniki, związek między stosowaniem atypowych leków przeciwpsychotycznych a działaniami niepożądanymi związanymi z hiperglikemią nie jest w pełni zrozumiały. Jednak badania epidemiologiczne wskazują na zwiększone ryzyko wystąpienia działań niepożądanych związanych z hiperglikemią związanych z leczeniem u pacjentów leczonych atypowymi lekami przeciwpsychotycznymi. Dokładne szacunki ryzyka wystąpienia działań niepożądanych związanych z hiperglikemią u pacjentów leczonych atypowymi lekami przeciwpsychotycznymi nie są dostępne.
Pacjenci z ustaloną diagnozą cukrzycy, którzy rozpoczęli leczenie produktem CLOZARIL 100 mg, powinni być regularnie monitorowani pod kątem pogorszenia kontroli glikemii. U pacjentów z czynnikami ryzyka cukrzycy (np. otyłość, cukrzyca w wywiadzie rodzinnym), którzy rozpoczynają leczenie atypowymi lekami przeciwpsychotycznymi, należy wykonać badanie stężenia glukozy we krwi na czczo na początku leczenia oraz okresowo w trakcie leczenia. Każdy pacjent leczony atypowymi lekami przeciwpsychotycznymi powinien być monitorowany pod kątem objawów hiperglikemii, w tym polidypsji, wielomoczu, polifagii i osłabienia. U pacjentów, u których podczas leczenia atypowymi lekami przeciwpsychotycznymi wystąpią objawy hiperglikemii, należy wykonać badanie stężenia glukozy we krwi na czczo. W niektórych przypadkach hiperglikemia ustąpiła po odstawieniu atypowego leku przeciwpsychotycznego; jednak niektórzy pacjenci wymagali kontynuacji leczenia przeciwcukrzycowego pomimo odstawienia podejrzanego leku.
zbiorczej analizie danych z 8 badań z udziałem dorosłych pacjentów ze schizofrenią średnie zmiany stężenia glukozy na czczo w grupach otrzymujących produkt CLOZARIL 50 mg i chlorpromazynę wynosiły odpowiednio +11 mg/dl i +4 mg/dl. Większy odsetek grupy otrzymującej CLOZARIL wykazywał kategoryczny wzrost stężenia glukozy na czczo od wartości wyjściowej w porównaniu z grupą chloropromazyną (Tabela 4). Dawki preparatu CLOZARIL 25 mg wynosiły 100–900 mg dziennie (średnia dawka modalna: 512 mg dziennie). Maksymalna dawka chloropromazyny wynosiła 1800 mg dziennie (średnia dawka modalna: 1029 mg dziennie). Mediana czasu trwania ekspozycji wyniosła 42 dni dla produktu CLOZARIL i chlorpromazyny.
Dyslipidemia
U pacjentów leczonych atypowymi lekami przeciwpsychotycznymi, w tym produktem leczniczym CLOZARIL, wystąpiły niepożądane zmiany stężenia lipidów. Zaleca się monitorowanie kliniczne, w tym ocenę stężenia lipidów w punkcie wyjściowym i okresową obserwację u pacjentów stosujących produkt leczniczy Clozaryl.
zbiorczej analizie danych z 10 badań z udziałem dorosłych pacjentów ze schizofrenią, leczenie produktem leczniczym CLOZARIL wiązało się ze zwiększeniem stężenia całkowitego cholesterolu w surowicy. Nie zebrano danych dotyczących cholesterolu LDL i HDL. Średni wzrost całkowitego cholesterolu wyniósł 13 mg/dl w grupie 25 mg CLOZARIL i 15 mg/dl w grupie chlorpromazyny. W zbiorczej analizie danych z 2 badań z udziałem dorosłych pacjentów ze schizofrenią, leczenie produktem leczniczym CLOZARIL 50 mg wiązało się ze zwiększeniem stężenia triglicerydów w surowicy na czczo. Średni wzrost trójglicerydów na czczo wyniósł 71 mg/dl (54%) w grupie CLOZARIL 100 mg i 39 mg/dl (35%) w grupie chlorpromazyny (Tabela 5). Ponadto leczenie produktem leczniczym CLOZARIL wiązało się z kategorycznym wzrostem stężenia cholesterolu całkowitego i triglicerydów w surowicy, co przedstawiono w Tabeli 6. Odsetek pacjentów z kategorycznym wzrostem stężenia cholesterolu całkowitego lub triglicerydów na czczo zwiększał się wraz z czasem ekspozycji. Mediana czasu trwania ekspozycji na produkt CLOZARIL 50 mg i chlorpromazynę wyniosła odpowiednio 45 dni i 38 dni. Zakres dawek CLOZARILU wynosił od 100 mg do 900 mg na dobę; maksymalna dawka chloropromazyny wynosiła 1800 mg na dobę.
Przybranie na wadze
Przyrost masy ciała wystąpił podczas stosowania leków przeciwpsychotycznych, w tym CLOZARILU. Monitoruj wagę podczas leczenia lekiem CLOZARIL. Tabela 7 podsumowuje dane dotyczące przyrostu masy ciała przez czas trwania ekspozycji zebrane z 11 badań z zastosowaniem produktu CLOZARIL i aktywnych leków porównawczych. Mediana czasu trwania ekspozycji wyniosła odpowiednio 609, 728 i 42 dni w grupie otrzymującej produkt CLOZARIL 25 mg, olanzapinę i chlorpromazynę.
Tabela 8 podsumowuje zbiorcze dane z 11 badań z udziałem dorosłych pacjentów ze schizofrenią, wykazujących przyrost masy ciała o ≥7% masy ciała w stosunku do wartości wyjściowej. Mediana czasu trwania ekspozycji wyniosła 609, 728 i 42 dni odpowiednio w grupie CLOZARIL, olanzapiny i chlorpromazyny.
Złośliwy zespół neuroleptyczny
Leki przeciwpsychotyczne, w tym CLOZARIL 50 mg, mogą powodować potencjalnie śmiertelny zespół objawów określany jako złośliwy zespół neuroleptyczny (NMS). Objawy kliniczne NMS obejmują nadmierną gorączkę, sztywność mięśni, zmieniony stan psychiczny i niestabilność autonomiczną (nieregularne tętno lub ciśnienie krwi, tachykardia, pocenie się i arytmie serca). Powiązane objawy mogą obejmować podwyższoną aktywność fosfokinazy kreatynowej (CPK), mioglobinurię, rabdomiolizę i ostrą niewydolność nerek.
Diagnostyczna ocena pacjentów z tym zespołem jest skomplikowana. Ważne jest, aby wziąć pod uwagę obecność innych poważnych schorzeń (np. ciężka neutropenia, infekcja, udar cieplny, pierwotna patologia OUN, ośrodkowa toksyczność antycholinergiczna, objawy pozapiramidowe i gorączka polekowa).
Postępowanie w NMS powinno obejmować (1) natychmiastowe odstawienie leków przeciwpsychotycznych i innych leków, które nie są niezbędne do jednoczesnego leczenia, (2) intensywne leczenie objawowe i monitorowanie medyczne oraz (3) leczenie chorób współistniejących. Nie ma ogólnej zgody co do konkretnych metod leczenia farmakologicznego NMS.
Jeśli pacjent wymaga leczenia przeciwpsychotycznego po wyzdrowieniu z NMS, należy dokładnie rozważyć możliwość ponownego włączenia terapii lekowej. NMS może się powtarzać. Uważnie monitoruj, jeśli wznawiasz leczenie lekami przeciwpsychotycznymi.
NMS wystąpił podczas monoterapii produktem CLOZARIL i jednocześnie stosowanych leków działających na OUN, w tym litu.
Hepatotoksyczność
W badaniach po wprowadzeniu do obrotu u pacjentów leczonych klozapiną zgłaszano ciężkie, zagrażające życiu, aw niektórych przypadkach prowadzące do zgonu, hepatotoksyczność, w tym niewydolność wątroby, martwicę wątroby i zapalenie wątroby [patrz DZIAŁANIA NIEPOŻĄDANE ]. Należy monitorować objawy przedmiotowe i podmiotowe hepatotoksyczności, takie jak zmęczenie, złe samopoczucie, anoreksja, nudności, żółtaczka, bilirubinemia, koagulopatia i encefalopatia wątrobowa. Wykonać badania surowicy w kierunku uszkodzenia wątroby i rozważyć trwałe przerwanie leczenia, jeśli klozapina powoduje zapalenie wątroby lub zwiększenie aktywności aminotransferaz w połączeniu z innymi objawami ogólnoustrojowymi.
Gorączka
Podczas leczenia klozapiną u pacjentów występowała przejściowa, związana z klozapiną gorączka. Szczytowa częstość występowania przypada na pierwsze 3 tygodnie leczenia. Chociaż gorączka ta jest na ogół łagodna i ustępuje samoistnie, może wymagać przerwania leczenia. Gorączka może być związana ze wzrostem lub spadkiem liczby krwinek białych. Dokładnie oceniaj pacjentów z gorączką, aby wykluczyć ciężką neutropenię lub infekcję. Rozważ możliwość NMS [patrz OSTRZEŻENIA I ŚRODKI ].
Zatorowość płucna
pacjentów leczonych produktem leczniczym CLOZARIL wystąpiła zatorowość płucna i zakrzepica żył głębokich. Rozważ możliwość wystąpienia zatorowości płucnej u pacjentów z zakrzepicą żył głębokich, ostrą dusznością, bólem w klatce piersiowej lub innymi objawami ze strony układu oddechowego. Nie jest jasne, czy zatorowość płucną i zakrzepicę żył głębokich można przypisać klozapinie, czy też niektórym cechom charakterystycznym pacjentów.
Toksyczność antycholinergiczna
CLOZARIL 50mg ma silne działanie antycholinergiczne. Leczenie produktem leczniczym CLOZARIL może powodować toksyczne działanie przeciwcholinergiczne na ośrodkowy układ nerwowy i obwodowy, zwłaszcza przy wyższych dawkach lub w przypadku przedawkowania [patrz PRZEDAWKOWANIE ]. Stosować ostrożnie u pacjentów z aktualnym rozpoznaniem lub w wywiadzie zaparciami, zatrzymaniem moczu, klinicznie istotnym przerostem gruczołu krokowego lub innymi stanami, w których działanie antycholinergiczne może prowadzić do istotnych działań niepożądanych. Jeśli to możliwe, należy unikać jednoczesnego stosowania z innymi lekami antycholinergicznymi, ponieważ zwiększa się ryzyko toksyczności antycholinergicznej lub ciężkich działań niepożądanych ze strony przewodu pokarmowego [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI ].
Zakłócenia sprawności poznawczej i motorycznej
CLOZARIL może powodować sedację oraz upośledzenie funkcji poznawczych i motorycznych. Należy ostrzec pacjentów przed obsługą niebezpiecznych maszyn, w tym samochodów, dopóki nie upewnią się, że CLOZARIL nie ma na nich niekorzystnego wpływu. Reakcje te mogą być zależne od dawki. Rozważ zmniejszenie dawki, jeśli wystąpią.
Późne dyskinezy
Późne dyskinezy (TD) występowały u pacjentów leczonych lekami przeciwpsychotycznymi, w tym produktem leczniczym CLOZARIL. Zespół składa się z potencjalnie nieodwracalnych, mimowolnych ruchów dyskinetycznych. Uważa się, że ryzyko wystąpienia TD i prawdopodobieństwo, że stanie się nieodwracalne, wzrasta wraz z dłuższym czasem trwania leczenia i wyższymi całkowitymi dawkami skumulowanymi. Zespół może jednak rozwinąć się po stosunkowo krótkich okresach leczenia małymi dawkami. Przepisać CLOZARIL w sposób, który najprawdopodobniej zminimalizuje ryzyko rozwoju TD. Stosuj najmniejszą skuteczną dawkę i najkrótszy czas niezbędny do opanowania objawów. Okresowo oceniaj potrzebę kontynuacji leczenia. Rozważ przerwanie leczenia, jeśli wystąpi TD. Jednak niektórzy pacjenci mogą wymagać leczenia lekiem CLOZARIL 100 mg pomimo obecności zespołu.
Nie jest znane leczenie TD. Jednak zespół może ustąpić częściowo lub całkowicie, jeśli leczenie zostanie przerwane. Samo leczenie przeciwpsychotyczne może tłumić (lub częściowo tłumić) oznaki i objawy oraz może maskować proces leżący u podstaw. Wpływ tłumienia objawów na odległy przebieg TD nie jest znany.
Działania niepożądane dotyczące naczyń mózgowych
W kontrolowanych badaniach u pacjentów w podeszłym wieku z psychozą związaną z otępieniem, leczonych niektórymi atypowymi lekami przeciwpsychotycznymi, występowało zwiększone ryzyko (w porównaniu z placebo) działań niepożądanych naczyniowo-mózgowych (np. udar, przemijający napad niedokrwienny), w tym zgonów. Mechanizm tego zwiększonego ryzyka nie jest znany. Nie można wykluczyć zwiększonego ryzyka dla produktu CLOZARIL lub innych leków przeciwpsychotycznych lub innych populacji pacjentów. CLOZARIL 50 mg należy stosować ostrożnie u pacjentów z czynnikami ryzyka wystąpienia działań niepożądanych ze strony naczyń mózgowych.
Nawrót psychozy i nawrót cholinergiczny po nagłym odstawieniu leku Clozaril®
Jeśli konieczne jest nagłe odstawienie leku Clozaryl (na przykład z powodu ciężkiej neutropenii lub innego stanu chorobowego) [patrz DAWKOWANIE I SPOSÓB PODAWANIA , OSTRZEŻENIA I ŚRODKI ], należy uważnie monitorować nawroty objawów psychotycznych i działań niepożądanych związanych z nawrotem cholinergicznym, takich jak obfite pocenie się, ból głowy, nudności, wymioty i biegunka.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Karcynogeneza
Nie wykazano działania rakotwórczego w długoterminowych badaniach na myszach i szczurach przy dawkach odpowiednio do 0,3-krotności i 0,4-krotności maksymalnej zalecanej dawki u ludzi (MRHD) wynoszącej 900 mg/dobę w przeliczeniu na mg/m2 powierzchni ciała.
Mutageneza
Klozapina nie wykazywała działania genotoksycznego w następujących testach mutacji genowych i aberracji chromosomowych: bakteryjny test Amesa, ssaczy V79 in vitro w komórkach chomika chińskiego, nieplanowana synteza DNA in vitro w hepatocytach szczura lub test mikrojądrowy in vivo u myszy.
Upośledzenie płodności
Klozapina nie miała wpływu na żadne parametry płodności, ciąży, masy płodu ani rozwoju pourodzeniowego po podaniu doustnym samcom szczurów 70 dni przed kryciem i samicom szczurów przez 14 dni przed kryciem w dawkach do 0,4 razy większych niż MRHD 900 mg/dobę w dniu krycia. w mg/m² powierzchni ciała.
Używaj w określonych populacjach
Ciąża
Ciąża Kategoria B
Podsumowanie ryzyka
Nie ma odpowiednich lub dobrze kontrolowanych badań klozapiny u kobiet w ciąży.
Badania nad reprodukcją przeprowadzono na szczurach i królikach przy dawkach odpowiednio do 0,4 i 0,9-krotności maksymalnej zalecanej dawki u ludzi (MRHD) wynoszącej 900 mg/dobę w przeliczeniu na mg/m2 powierzchni ciała. Badania nie ujawniły dowodów na upośledzenie płodności lub uszkodzenie płodu spowodowane przez klozapinę. Ponieważ badania na zwierzętach dotyczące reprodukcji nie zawsze pozwalają przewidzieć odpowiedź u ludzi, CLOZARIL należy stosować w okresie ciąży tylko wtedy, gdy jest to bezwzględnie konieczne.
Rozważania kliniczne
Należy rozważyć ryzyko zaostrzenia psychozy w przypadku przerwania lub zmiany leczenia lekami przeciwpsychotycznymi w czasie ciąży i połogu. Rozważ wczesne badanie przesiewowe w kierunku cukrzycy ciążowej u pacjentek leczonych lekami przeciwpsychotycznymi [patrz OSTRZEŻENIA I ŚRODKI ]. Noworodki narażone na leki przeciwpsychotyczne w trzecim trymestrze ciąży są narażone na wystąpienie objawów pozapiramidowych i/lub objawów odstawienia po porodzie. Monitorować noworodki pod kątem objawów pobudzenia, hipertonii, hipotonii, drżenia, senności, niewydolności oddechowej i trudności w karmieniu. Nasilenie powikłań może być różne, od samoograniczających się objawów do niektórych noworodków wymagających wsparcia na oddziale intensywnej terapii i przedłużonej hospitalizacji.
Dane zwierząt
badaniach dotyczących rozwoju zarodka i płodu klozapina nie miała wpływu na parametry matczyne, wielkość miotu ani parametry płodu, gdy była podawana doustnie ciężarnym szczurom i królikom w okresie organogenezy w dawkach odpowiednio do 0,4 i 0,9 razy MRHD 900 mg/dobę w mg/m² powierzchni ciała.
W badaniach rozwoju około- i poporodowego ciężarnym samicom szczurów podawano klozapinę przez ostatnią trzecią część ciąży i do 21 dnia po porodzie. Prowadzono obserwacje płodów przy urodzeniu iw okresie poporodowym; potomstwu pozwolono osiągnąć dojrzałość płciową i pokryć. Klozapina powodowała zmniejszenie masy ciała matki, ale nie miała wpływu na wielkość miotu ani masę ciała pokoleń F1 lub F2 w dawkach do 0,4 razy większych niż MRHD 900 mg/dobę w przeliczeniu na mg/m2 powierzchni ciała.
Matki karmiące
CLOZARIL 50 mg jest obecny w mleku ludzkim. Ze względu na możliwość wystąpienia poważnych działań niepożądanych u niemowląt karmionych produktem leczniczym CLOZARIL, należy podjąć decyzję, czy przerwać karmienie piersią, czy przerwać stosowanie leku, biorąc pod uwagę znaczenie leku dla matki.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność u pacjentów pediatrycznych nie zostały ustalone.
Zastosowanie geriatryczne
Nie było wystarczającej liczby pacjentów w podeszłym wieku w badaniach klinicznych, w których stosowano CLOZARIL 50 mg, aby ustalić, czy osoby w wieku powyżej 65 lat różnią się od młodszych pacjentów pod względem odpowiedzi na Clozarilu.
Niedociśnienie ortostatyczne i tachykardia mogą wystąpić podczas leczenia produktem leczniczym CLOZARIL 50 mg [patrz OSTRZEŻENIE W PUDEŁKU oraz OSTRZEŻENIA I ŚRODKI ]. Pacjenci w podeszłym wieku, szczególnie ci z upośledzonym funkcjonowaniem układu sercowo-naczyniowego, mogą być bardziej podatni na te efekty.
Pacjenci w podeszłym wieku mogą być szczególnie podatni na antycholinergiczne działanie produktu Clozaryl, takie jak zatrzymanie moczu i zaparcia [patrz OSTRZEŻENIA I ŚRODKI ].
Starannie dobieraj dawki leku Clozarilu 50 mg u pacjentów w podeszłym wieku, biorąc pod uwagę większą częstość występowania pogorszenia czynności wątroby, nerek lub serca, a także innych chorób współistniejących i innych leków. Doświadczenie kliniczne sugeruje, że częstość występowania późnych dyskinez wydaje się być najwyższa wśród osób starszych; zwłaszcza starsze kobiety [patrz OSTRZEŻENIA I ŚRODKI ].
Pacjenci z niewydolnością nerek lub wątroby
U pacjentów z istotnymi zaburzeniami czynności nerek lub wątroby może być konieczne zmniejszenie dawki. U tych pacjentów może dojść do zwiększenia stężenia klozapiny, ponieważ klozapina jest prawie całkowicie metabolizowana, a następnie wydalana [patrz DAWKOWANIE I SPOSÓB PODAWANIA , FARMAKOLOGIA KLINICZNA ].
Słabe metabolizmy CYP2D6
Zmniejszenie dawki może być konieczne u pacjentów ze słabym metabolizmem CYP2D6. U tych pacjentów może dojść do zwiększenia stężenia klozapiny, ponieważ klozapina jest prawie całkowicie metabolizowana, a następnie wydalana [patrz DAWKOWANIE I SPOSÓB PODAWANIA , FARMAKOLOGIA KLINICZNA ].
Pacjenci hospicjum
przypadku pacjentów hospicyjnych (tj. pacjentów nieuleczalnie chorych, których przewidywana długość życia wynosi sześć miesięcy lub mniej), lekarz przepisujący może zmniejszyć częstotliwość monitorowania ANC do raz na 6 miesięcy, po rozmowie z pacjentem i jego opiekunem. Indywidualne decyzje terapeutyczne powinny uwzględniać znaczenie monitorowania ANC w kontekście konieczności kontrolowania objawów psychicznych i terminalnej choroby pacjenta.
PRZEDAWKOWAĆ
Doświadczenie przedawkowania
Najczęściej zgłaszanymi oznakami i objawami związanymi z przedawkowaniem klozapiny są: uspokojenie polekowe, majaczenie, śpiączka, tachykardia, niedociśnienie, depresja oddechowa lub niewydolność; i nadmierne ślinienie. Istnieją doniesienia o zachłystowym zapaleniu płuc, zaburzeniach rytmu serca i napadach padaczkowych. Zgłaszano przypadki śmiertelnego przedawkowania klozapiny, zwykle w dawkach powyżej 2500 mg. Odnotowano również przypadki powrotu do zdrowia pacjentów po przedawkowaniu znacznie przekraczającym 4 g.
Zarządzanie przedawkowaniem
Nie ma dostępnego swoistego antidotum na przedawkowanie produktu Clozaryl. Ustanowienie i utrzymanie dróg oddechowych; zapewnić odpowiednie dotlenienie i wentylację. Monitoruj stan serca i parametry życiowe. Stosuj ogólne środki objawowe i podtrzymujące. Rozważ możliwość zaangażowania wielu leków.
Skontaktuj się z Certyfikowanym Centrum Kontroli Zatruć, aby uzyskać najbardziej aktualne informacje na temat postępowania w przypadku przedawkowania (1-800Â222-1222).
PRZECIWWSKAZANIA
CLOZARIL jest przeciwwskazany u pacjentów z ciężką nadwrażliwością na klozapinę w wywiadzie (np. nadwrażliwość na światło, zapalenie naczyń, rumień wielopostaciowy lub zespół Stevensa-Johnsona) lub jakikolwiek inny składnik DZIAŁANIA NIEPOŻĄDANE ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Mechanizm działania klozapiny jest nieznany. Zaproponowano jednak, że skuteczność terapeutyczna klozapiny w schizofrenii jest pośredniczona przez antagonizm receptorów dopaminy typu 2 (D2) i serotoniny typu 2A (5HT2A). CLOZARIL działa również jako antagonista receptorów adrenergicznych, cholinergicznych, histaminergicznych i innych receptorów dopaminergicznych i serotoninergicznych.
Farmakodynamika
Klozapina wykazała powinowactwo wiązania z następującymi receptorami: histaminowym H1 (Ki 1,1 nM), adrenergicznym α1A (Ki 1,6 nM), serotoninowym 5-HT6 (Ki 4 nM), serotoninowym 5-HT2A (Ki 5,4 nM), muskarynowym M1 (Ki 6,2 nM), serotonina 5-HT7 (Ki 6,3 nM), serotonina 5-HT2C (Ki 9,4 nM), dopamina D4 (Ki 24 nM), adrenergiczna α2A (Ki 90 nM), serotonina 5-HT3 (Ki 95 nM), serotonina 5-HT1A (Ki 120 nM), dopamina D2 (Ki 160 nM), dopamina D1 (Ki 270 nM), dopamina D5 (Ki 454 nM) i dopamina D3 (Ki 555 nM).
Klozapina powoduje niewielki lub żaden wzrost poziomu prolaktyny.
Kliniczne badania elektroencefalogramu (EEG) wykazały, że klozapina zwiększa aktywność delta i theta oraz spowalnia dominujące częstotliwości alfa. Następuje ulepszona synchronizacja. Może również rozwinąć się aktywność fal ostrych oraz kompleksy kolców i fal. Pacjenci zgłaszali nasilenie aktywności snu podczas terapii klozapiną. Stwierdzono, że sen REM wydłuża się do 85% całkowitego czasu snu. U tych pacjentów początek snu REM nastąpił niemal natychmiast po zaśnięciu.
Farmakokinetyka
Wchłanianie
ludzi tabletki CLOZARIL (25 mg i 100 mg) mają taką samą biodostępność jak roztwór CLOZARIL. Po podaniu doustnym 100 mg produktu leczniczego Clozarix dwa razy na dobę średnie maksymalne stężenie w osoczu w stanie stacjonarnym wynosiło 319 ng/ml (zakres: 102 do 771 ng/ml), występujące średnio po 2,5 godzinie (zakres: 1 do 6 godzin) po dawkowanie. Średnie minimalne stężenie w stanie stacjonarnym wynosiło 122 ng/ml (zakres: 41 do 343 ng/ml) po podaniu 100 mg dwa razy na dobę. Pokarm nie wydaje się wpływać na ogólnoustrojową biodostępność produktu Clozaryl. W związku z tym produkt leczniczy CLOZARIL 50 mg można podawać z posiłkiem lub bez posiłku.
Dystrybucja
Klozapina wiąże się w około 97% z białkami surowicy. Interakcja między klozapiną a innymi lekami silnie wiążącymi się z białkami nie została w pełni zbadana, ale może być ważna [patrz INTERAKCJE Z LEKAMI ].
Metabolizm i wydalanie
Klozapina jest prawie całkowicie metabolizowana przed wydaleniem i tylko śladowe ilości niezmienionego leku są wykrywane w moczu i kale. Klozapina jest substratem wielu izoenzymów cytochromu P450, w szczególności CYP1A2, CYP2D6 i CYP3A4. Około 50% podanej dawki jest wydalane z moczem, a 30% z kałem. Pochodne demetylowane, hydroksylowane i N-tlenkowe są składnikami zarówno moczu, jak i kału. Badania farmakologiczne wykazały, że metabolit demetylowy (norklozapina) ma jedynie ograniczoną aktywność, podczas gdy pochodne hydroksylowane i N-tlenkowe były nieaktywne. Średni okres półtrwania w fazie eliminacji klozapiny po podaniu pojedynczej dawki 75 mg wynosił 8 godzin (zakres: od 4 do 12 godzin), w porównaniu ze średnim okresem półtrwania w fazie eliminacji wynoszącym 12 godzin (zakres: od 4 do 66 godzin), po osiągnięciu stanu stacjonarnego w dawce 100 mg dwa razy na dobę.
Porównanie jednodawkowej i wielokrotnej dawki klozapiny wykazało, że okres półtrwania w fazie eliminacji znacznie się wydłużył po podaniu wielokrotnym w porównaniu z podaniem pojedynczej dawki, co sugeruje możliwość farmakokinetyki zależnej od stężenia. Jednak w stanie stacjonarnym po podaniu 37,5, 75 i 150 mg dwa razy na dobę obserwowano w przybliżeniu proporcjonalne do dawki zmiany w odniesieniu do AUC (powierzchnia pod krzywą), maksymalnego i minimalnego stężenia klozapiny w osoczu.
Badania interakcji między lekami
Fluwoksamina
Badanie farmakokinetyczne przeprowadzono u 16 pacjentów ze schizofrenią, którzy otrzymywali klozapinę w stanie stacjonarnym. Po jednoczesnym podawaniu fluwoksaminy przez 14 dni, średnie minimalne stężenia klozapiny i jej metabolitów, N-demetyloklozapiny i N-tlenku klozapiny, były około trzykrotnie podwyższone w porównaniu z wyjściowymi stężeniami w stanie stacjonarnym.
Paroksetyna, fluoksetyna i sertralina
badaniu pacjentów ze schizofrenią (n=14), którzy otrzymywali klozapinę w stanie stacjonarnym, jednoczesne podawanie paroksetyny powodowało jedynie niewielkie zmiany w stężeniach klozapiny i jej metabolitów. Jednak inne opublikowane doniesienia opisują niewielkie (mniej niż dwukrotne) zwiększenie stężenia klozapiny i metabolitów, gdy klozapina była przyjmowana z paroksetyną, fluoksetyną i sertraliną.
Specyficzne badania populacji
Niewydolność nerek lub wątroby
Nie przeprowadzono specjalnych badań farmakokinetycznych w celu zbadania wpływu zaburzeń czynności nerek lub wątroby na farmakokinetykę klozapiny. Większe stężenia klozapiny w osoczu są prawdopodobne u pacjentów z poważnymi zaburzeniami czynności nerek lub wątroby w przypadku stosowania zwykłych dawek.
Słabe metabolizmy CYP2D6
Podzbiór (3% – 10%) populacji ma zmniejszoną aktywność CYP2D6 (osoby słabo metabolizujące CYP2D6). U tych osób może wystąpić wyższe niż oczekiwane stężenie klozapiny w osoczu po podaniu zwykłych dawek.
Studia kliniczne
Schizofrenia oporna na leczenie
Skuteczność preparatu CLOZARIL 100 mg w leczeniu opornej na leczenie schizofrenii ustalono w wieloośrodkowym, randomizowanym, podwójnie zaślepionym, aktywnie kontrolowanym badaniu (chloropromazyna) u pacjentów z rozpoznaniem schizofrenii DSM-III, u których odpowiedź na co najmniej 3 różne leki przeciwpsychotyczne była niewystarczająca ( z co najmniej 2 różnych klas chemicznych) w ciągu ostatnich 5 lat. Badania przeciwpsychotyczne musiały zostać uznane za odpowiednie; dawki leków przeciwpsychotycznych muszą być równoważne lub większe niż 1000 mg chloropromazyny na dzień przez okres co najmniej 6 tygodni, bez znaczącego zmniejszenia objawów. Nie mogło być żadnego okresu dobrego funkcjonowania w ciągu ostatnich 5 lat. Pacjenci musieli mieć wyjściowy wynik co najmniej 45 w ocenianej przez badacza Krótkiej Skali Oceny Psychiatrycznej (BPRS). W 18-punktowym BPRS 1 wskazuje na brak objawów, a 7 wskazuje na ciężkie objawy; maksymalny potencjalny całkowity wynik BPRS wynosi 126. Na początku średni wynik BPRS wynosił 61. Ponadto pacjenci musieli mieć wynik co najmniej 4 w co najmniej dwóch z następujących czterech pojedynczych elementów BPRS: dezorganizacja pojęciowa, podejrzliwość, omamy zachowanie i niezwykła treść myśli. Pacjenci musieli mieć wynik w skali Clinical Global Impressions ? co najmniej 4 (umiarkowanie chory).
prospektywnej, wstępnej fazie badania wszyscy pacjenci (N=305) początkowo otrzymywali pojedynczą ślepą terapię haloperidolem (średnia dawka wynosiła 61 mg na dobę) przez 6 tygodni. Ponad 80% pacjentów ukończyło 6-tygodniowe badanie. Pacjenci z niewystarczającą odpowiedzią na haloperidol (n=268) zostali losowo przydzieleni do podwójnie ślepego leczenia preparatem CLOZARIL (N=126) lub chlorpromazyną (N=142). Maksymalna dobowa dawka produktu Clozarilu wynosiła 900 mg; średnia dawka dobowa wynosiła >600 mg. Maksymalna dzienna dawka chloropromazyny wynosiła 1800 mg; średnia dawka dobowa wynosiła >1200 mg.
Pierwszorzędowym punktem końcowym była odpowiedź na leczenie, wstępnie zdefiniowana jako zmniejszenie wyniku BPRS o co najmniej 20% i albo (1) wynik CGI-S
Nawracające zachowania samobójcze w schizofrenii lub zaburzeniu schizoafektywnym
Skuteczność preparatu CLOZARIL w zmniejszaniu ryzyka nawrotów zachowań samobójczych została oceniona w międzynarodowym badaniu dotyczącym zapobiegania samobójstwom (InterSePT™, znak towarowy firmy Novartis Pharmaceuticals Corporation). Było to prospektywne, randomizowane, otwarte, aktywnie kontrolowane, wieloośrodkowe, międzynarodowe, porównanie w grupach równoległych preparatu CLOZARIL z olanzapiną (*Zyprexa®, zarejestrowany znak towarowy firmy Eli Lilly and Company) u 956 pacjentów ze schizofrenią lub zaburzeniami schizoafektywnymi ( DSM-IV), które zostały ocenione jako narażone na nawracające zachowania samobójcze. Tylko około jedną czwartą tych pacjentów (27%) uznano za oporną na standardowe leczenie lekami przeciwpsychotycznymi. Aby wziąć udział w badaniu, pacjenci muszą spełnić jedno z następujących kryteriów:
- Próbowali popełnić samobójstwo w ciągu trzech lat przed oceną wyjściową.
- Byli hospitalizowani, aby zapobiec próbie samobójczej w ciągu trzech lat przed ich podstawową oceną.
- Wykazali myśli samobójcze o nasileniu od umiarkowanego do ciężkiego z komponentem depresyjnym w ciągu jednego tygodnia przed oceną wyjściową.
- Wykazali oni myśli samobójcze o nasileniu od umiarkowanego do ciężkiego, którym towarzyszyły halucynacje dowodzenia w celu dokonania samookaleczenia w ciągu tygodnia przed oceną wyjściową.
Schematy dawkowania dla każdej leczonej grupy zostały określone przez indywidualnych badaczy i zindywidualizowane przez pacjenta. Dawkowanie było elastyczne, z zakresem dawek 200-900 mg/dzień dla CLOZARILU i 5-20 mg/dzień dla olanzapiny. U 956 pacjentów, którzy otrzymywali CLOZARIL lub olanzapinę w tym badaniu, intensywnie stosowano jednocześnie psychotropy: 84% z lekami przeciwpsychotycznymi, 65% z lekami przeciwlękowymi, 53% z lekami przeciwdepresyjnymi i 28% z lekami normotymicznymi. W grupie olanzapiny istotnie częściej stosowano jednocześnie leki psychotropowe.
Podstawowym miernikiem skuteczności był czas do (1) znaczącej próby samobójczej, w tym samobójstwa dokonanego; (2) hospitalizacja z powodu zbliżającego się ryzyka samobójstwa, w tym zwiększony poziom nadzoru pod kątem samobójstw u pacjentów już hospitalizowanych; lub (3) pogorszenie nasilenia myśli samobójczych, wykazane przez „znaczne pogorszenie” lub „bardzo znaczne pogorszenie” w stosunku do wartości wyjściowej w Clinical Global Impression of Severity of Suicydality ocenianej za pomocą skali CGI-SS-BP (ang. Blinded Psychiatrist). Ustalenia, czy zgłoszone zdarzenie spełniło kryterium 1 lub 2 powyżej, dokonała Rada Monitorująca Samobójstwa (SMB), grupa ekspertów nie mająca dostępu do danych pacjentów.
Do badania losowo przydzielono łącznie 980 pacjentów, a 956 otrzymało badany lek. Sześćdziesiąt dwa procent pacjentów zdiagnozowano schizofrenię, au pozostałych (38%) zdiagnozowano zaburzenie schizoafektywne. Tylko około jedną czwartą całej populacji pacjentów (27%) na początku badania zidentyfikowano jako „odporną na leczenie”. W badaniu było więcej mężczyzn niż kobiet (61% wszystkich pacjentów stanowili mężczyźni). Średni wiek pacjentów przystępujących do badania wynosił 37 lat (zakres 18–69 lat). Większość pacjentów była rasy kaukaskiej (71%), 15% było rasy czarnej, 1% było Azjatami, a 13% zaklasyfikowano do „innej” rasy.
Pacjenci leczeni preparatem CLOZARIL 100 mg mieli statystycznie istotnie dłuższe opóźnienie czasu do nawrotów zachowań samobójczych w porównaniu z olanzapiną. Wynik ten należy interpretować jedynie jako dowód skuteczności produktu CLOZARIL w opóźnianiu nawrotu zachowań samobójczych, a nie jako dowód lepszej skuteczności produktu Clozarilu 50 mg w porównaniu z olanzapiną.
Prawdopodobieństwo wystąpienia (1) znaczącej próby samobójczej, w tym samobójstwa zakończonego, lub (2) hospitalizacji z powodu zbliżającego się ryzyka samobójstwa, w tym zwiększonego poziomu nadzoru nad samobójstwami u pacjentów już hospitalizowanych, było niższe u pacjentów leczonych produktem leczniczym CLOZARIL niż u pacjentów leczonych Tydzień 104: CLOZARIL 24% w porównaniu z olanzapiną 32%; 95% CI różnicy: 2%, 14% (ryc. 1).
Rycina 1: Skumulowane prawdopodobieństwo znaczącej próby samobójczej lub hospitalizacji w celu zapobiegania samobójstwom u pacjentów ze schizofrenią lub zaburzeniem schizoafektywnym z wysokim ryzykiem samobójstwa
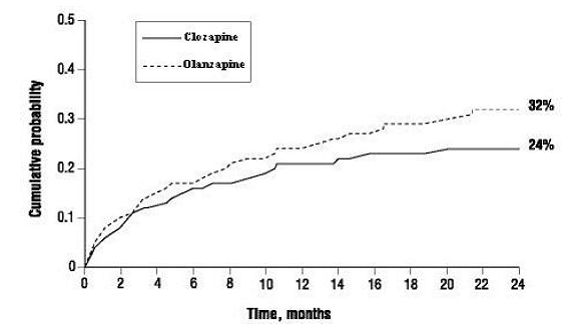
INFORMACJA O PACJENCIE
Omów następujące kwestie z pacjentami i opiekunami:
- Ciężka neutropenia:
- Należy poinstruować pacjentów (i opiekunów) rozpoczynających leczenie lekiem CLOZARIL o ryzyku wystąpienia ciężkiej neutropenii i zakażenia.
- Poinstruuj pacjentów, aby natychmiast zgłaszali lekarzowi wszelkie objawy lub oznaki infekcji (np. choroba grypopodobna; gorączka; letarg; ogólne osłabienie lub złe samopoczucie; owrzodzenie błony śluzowej; zakażenie skóry, gardła, pochwy, dróg moczowych lub płuc; lub skrajne osłabienie lub letarg) występujące w dowolnym momencie leczenia produktem leczniczym CLOZARIL w dawce 100 mg, aby pomóc w ocenie neutropenii oraz we wdrożeniu szybkiego i odpowiedniego leczenia. [Widzieć OSTRZEŻENIA I ŚRODKI ].
- Poinformuj pacjentów i opiekunów CLOZARIL 25 mg jest dostępny wyłącznie w ramach ograniczonego programu o nazwie Clozapine REMS Program, którego celem jest zapewnienie wymaganego monitorowania krwi w celu zmniejszenia ryzyka rozwoju ciężkiej neutropenii. Poinformuj pacjentów i opiekunów o znaczeniu wykonywania badań krwi w następujący sposób:
- Cotygodniowe badania krwi są wymagane przez pierwsze 6 miesięcy.
- ANC jest wymagane co 2 tygodnie przez kolejne 6 miesięcy, jeśli akceptowalny ANC utrzymuje się w ciągu pierwszych 6 miesięcy ciągłej terapii,
- Następnie ANC jest wymagany raz na 4 tygodnie, jeśli akceptowalny ANC utrzymuje się w ciągu kolejnych 6 miesięcy ciągłej terapii.
- CLOZARIL 50mg jest dostępny tylko w certyfikowanych aptekach uczestniczących w programie. Zapewnij pacjentom (i opiekunom) informacje na stronie internetowej oraz numer telefonu, w jaki sposób uzyskać produkt (www.clozapinerems.com lub 1-844-267-8678) [patrz OSTRZEŻENIA I ŚRODKI ].
- Niedociśnienie ortostatyczne, bradykardia i omdlenia: Należy poinformować pacjentów i opiekunów o ryzyku wystąpienia niedociśnienia ortostatycznego i omdleń, zwłaszcza w okresie początkowego dostosowywania dawki. Poinstruuj ich, aby ściśle przestrzegali zaleceń lekarza dotyczących dawkowania i podawania. Poradź pacjentom, aby natychmiast skonsultowali się z lekarzem, jeśli poczują się słabo, stracą przytomność lub wystąpią objawy wskazujące na bradykardię lub arytmię [patrz DAWKOWANIE I SPOSÓB PODAWANIA , OSTRZEŻENIA I ŚRODKI ].
- Napady padaczkowe: Należy poinformować pacjentów i opiekunów o istotnym ryzyku wystąpienia napadów padaczkowych podczas leczenia lekiem CLOZARIL 100 mg. Przestrzegaj ich przed prowadzeniem pojazdu i innymi potencjalnie niebezpiecznymi czynnościami podczas przyjmowania leku CLOZARIL [patrz OSTRZEŻENIA I ŚRODKI ].
- Niedoczynność przewodu pokarmowego z ciężkimi powikłaniami: należy edukować pacjentów i opiekunów w zakresie ryzyka, zapobiegania i leczenia zaparć wywołanych klozapiną, w tym leków, których należy unikać, jeśli to możliwe (np. leków o działaniu antycholinergicznym). Zachęcaj do odpowiedniego nawadniania, aktywności fizycznej i przyjmowania błonnika oraz podkreślaj, że natychmiastowa uwaga i leczenie rozwoju zaparć lub innych objawów żołądkowo-jelitowych ma kluczowe znaczenie w zapobieganiu poważnym powikłaniom. Poradź pacjentom i opiekunom, aby skontaktowali się z lekarzem, jeśli wystąpią objawy zaparcia (np. trudności w oddawaniu stolca, niepełne oddawanie stolca, zmniejszona częstotliwość wypróżnień) lub inne objawy związane z osłabieniem motoryki przewodu pokarmowego (np. nudności, wzdęcie lub ból brzucha, wymioty) [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI ].
- Wydłużenie odstępu QT: Należy doradzić pacjentom, aby w przypadku omdlenia, utraty przytomności lub objawów sugerujących arytmię natychmiast skonsultowali się z lekarzem. Należy poinstruować pacjentów, aby nie przyjmowali leku CLOZARIL jednocześnie z innymi lekami, które powodują wydłużenie odstępu QT. Poinstruuj pacjentów, aby poinformowali swoich lekarzy, że przyjmują CLOZARIL 25 mg przed każdym nowym lekiem [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI ].
- Zmiany metaboliczne (hiperglikemia i cukrzyca, dyslipidemia, przyrost masy ciała): edukować pacjentów i opiekunów o ryzyku zmian metabolicznych i konieczności szczególnego monitorowania. Zagrożenia obejmują hiperglikemię i cukrzycę, dyslipidemię, przyrost masy ciała i reakcje sercowo-naczyniowe. Edukuj pacjentów i opiekunów o objawach hiperglikemii (wysokiego poziomu cukru we krwi) i cukrzycy (np. polidypsja, wielomocz, polifagia i osłabienie). Monitoruj wszystkich pacjentów pod kątem tych objawów. U pacjentów ze zdiagnozowaną cukrzycą lub z czynnikami ryzyka cukrzycy (otyłość, cukrzyca w wywiadzie rodzinnym) należy kontrolować stężenie glukozy we krwi na czczo przed rozpoczęciem leczenia oraz okresowo w trakcie leczenia. U pacjentów, u których wystąpią objawy hiperglikemii, należy ocenić stężenie glukozy na czczo. Zalecane jest kliniczne monitorowanie masy ciała [patrz OSTRZEŻENIA I ŚRODKI ].
- Zakłócenia funkcji poznawczych i motorycznych: Ponieważ CLOZARIL może potencjalnie zaburzać osąd, myślenie lub zdolności motoryczne, pacjentów należy ostrzec przed obsługą niebezpiecznych maszyn, w tym samochodów, dopóki nie upewnią się, że terapia lekiem CLOZARIL nie wpływa na nich niekorzystnie [patrz OSTRZEŻENIA I ŚRODKI ].
- Pominięte dawki i ponowne rozpoczęcie leczenia: Poinformuj pacjentów i opiekunów, że jeśli pacjent opuszcza przyjmowanie leku Clozarilu 50 mg przez więcej niż 2 dni, nie powinien wznawiać leczenia w tej samej dawce, ale powinien skontaktować się z lekarzem w celu uzyskania instrukcji dawkowania [patrz DAWKOWANIE I SPOSÓB PODAWANIA , OSTRZEŻENIA I ŚRODKI ].
- Ciąża: Pacjenci i opiekunowie powinni powiadomić lekarza, jeśli pacjentka zajdzie w ciążę lub zamierza zajść w ciążę podczas leczenia [patrz Używaj w określonych populacjach ].
- Pielęgniarstwo: Poinformuj pacjentów i opiekunów, że pacjentka nie powinna karmić piersią niemowlęcia, jeśli przyjmuje CLOZARIL [patrz Używaj w określonych populacjach ].
- Leki towarzyszące: Doradzać pacjentom, aby informowali swojego lekarza, jeśli przyjmują lub planują przyjmować leki na receptę lub leki dostępne bez recepty; istnieje możliwość znaczących interakcji między lekami [patrz DAWKOWANIE I SPOSÓB PODAWANIA , INTERAKCJE Z LEKAMI ].
