Pulmicort 100mcg, 200mcg Budesonide Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Pulmicort 100mcg Turbuhaler i jak się go stosuje?
Pulmicort 100mcg Turbuhaler to lek na receptę stosowany w leczeniu objawów astmy. Pulmicort 100mcg Turbuhaler może być stosowany samodzielnie lub z innymi lekami.
Pulmicort Turbuhaler należy do klasy leków zwanych kortykosteroidami, inhalantami.
Nie wiadomo, czy Pulmicort Turbuhaler jest bezpieczny i skuteczny u dzieci w wieku poniżej 1 roku.
Jakie są możliwe skutki uboczne leku Pulmicort 200mcg Turbuhaler?
Pulmicort 100mcg Turbuhaler może powodować poważne skutki uboczne, w tym:
- pokrzywka,
- trudności w oddychaniu,
- obrzęk twarzy, warg, języka lub gardła,
- niezwykłe zmęczenie,
- Problemy ze wzrokiem,
- łatwe siniaczenie lub krwawienie,
- opuchnięta twarz,
- niezwykły wzrost włosów,
- zmiany nastroju,
- depresja,
- wahania nastroju,
- podniecenie,
- osłabienie lub ból mięśni,
- ścieńczenie skóry,
- powolne gojenie się ran i
- zwiększone pragnienie lub oddawanie moczu
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze działania niepożądane leku Pulmicort 100mcg Turbuhaler obejmują:
- suchość, podrażnienie lub ból gardła,
- chrypka,
- zmiany głosu,
- zły smak w ustach,
- katar lub zatkany nos oraz
- krwotok z nosa
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe działania niepożądane leku Pulmicort Turbuhaler. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Wyłącznie do inhalacji doustnej.
OPIS
Budezonid, aktywny składnik PULMICORT TURBUHALER (budezonid) 200 mcg, jest kortykosteroidem określanym chemicznie jako (RS)-11β,16α,17,21-Tetrahydroksypregna-1,4-dieno-3,20-dionowy cykl 16,17- acetal z aldehydem masłowym. Budezonid jest dostarczany jako mieszanina dwóch epimerów (22R i 22S). Empiryczny wzór budezonidu to C25H34O6, a jego masa cząsteczkowa wynosi 430,5. Jego wzór strukturalny to:
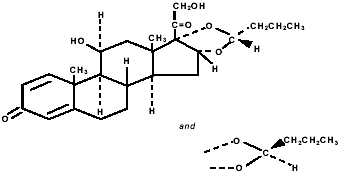
Budezonid jest proszkiem o barwie od białej do prawie białej, bez smaku i zapachu, który jest praktycznie nierozpuszczalny w wodzie i heptanie, słabo rozpuszczalny w etanolu i swobodnie rozpuszczalny w chloroformie. Jego współczynnik podziału między oktanol i wodę przy pH 7,4 wynosi 1,6 x 103.
PULMICORT 100mcg TURBUHALER (budezonid) to wielodawkowy inhalator proszkowy do inhalacji, który zawiera tylko zmikronizowany budezonid. Każde naciśnięcie PULMICORT 100 mcg TURBUHALER dostarcza 200 mcg budezonidu na odmierzoną dawkę, co dostarcza około 160 mcg budezonidu z ustnika (na podstawie badań in vitro przy 60 l/min przez 2 sekundy).
Testy in vitro wykazały, że dostarczanie dawki dla PULMICORT 100mcg TURBUHALER (budezonid) jest w znacznym stopniu zależne od przepływu powietrza przez urządzenie. Czynniki pacjenta, takie jak szybkość przepływu wdechowego, będą również wpływać na dawkę dostarczoną do płuc pacjentów faktycznie stosowanych (patrz Instrukcja użytkowania dla pacjenta ). U dorosłych pacjentów z astmą (średnia FEV1 2,9 l [0,8 - 5,1 l]) średni szczytowy przepływ wdechowy (PIF) przez PULMICORT TURBUHALER (budezonid) wynosił 78 (40-111) l/min. Podobne wyniki (średnia PIF 82 [43-125] l/min) uzyskano u dzieci chorych na astmę (6 do 15 lat, średnia FEV1 2,1 l [0,9 - 5,4 l]). Pacjentów należy dokładnie poinstruować o stosowaniu tego produktu leczniczego, aby zapewnić optymalne dostarczanie dawki.
WSKAZANIA
PULMICORT TURBUHALER (budezonid) jest wskazany w leczeniu podtrzymującym astmy jako terapia profilaktyczna u dorosłych i dzieci w wieku sześciu lat lub starszych. Jest również wskazany dla pacjentów wymagających terapii doustnymi kortykosteroidami z powodu astmy. Wielu z tych pacjentów może z czasem zmniejszyć lub wyeliminować zapotrzebowanie na doustne kortykosteroidy.
PULMICORT 100mcg TURBUHALER (budezonid) NIE jest wskazany do łagodzenia ostrego skurczu oskrzeli.
DAWKOWANIE I SPOSÓB PODAWANIA
PULMICORT 200mcg TURBUHALER (budezonid) należy podawać drogą wziewną doustnie pacjentom z astmą w wieku 6 lat i starszym. Poszczególni pacjenci odczują zmienny początek i stopień złagodzenia objawów. Ogólnie rzecz biorąc, PULMICORT TURBUHALER (budezonid) ma stosunkowo szybki początek działania jak na wziewny kortykosteroid. Poprawa kontroli astmy po wziewnym podaniu produktu PULMICORT 200 µg TURBUHALER (budezonid) może nastąpić w ciągu 24 godzin od rozpoczęcia leczenia, chociaż maksymalne korzyści mogą nie zostać osiągnięte przez 1 do 2 tygodni lub dłużej. Bezpieczeństwo i skuteczność produktu PULMICORT TURBUHALER (budezonid) podawanego w ilościach przekraczających zalecane dawki nie zostały ustalone.
Zalecana dawka początkowa i najwyższa zalecana dawka produktu PULMICORT TURBUHALER (budezonid) na podstawie wcześniejszego leczenia astmy wymieniono w poniższej tabeli.
*U pacjentów z łagodną lub umiarkowaną astmą, którzy są dobrze kontrolowani za pomocą wziewnych kortykosteroidów, można rozważyć podanie leku PULMICORT 100 mcg TURBUHALER (budezonid) 200 mcg lub 400 mcg raz na dobę. PULMICORT 200mcg TURBUHALER (budezonid) można podawać raz dziennie rano lub wieczorem.
Jeśli podawanie raz na dobę produktu PULMICORT 200 µg TURBUHALER (budezonid) nie zapewnia odpowiedniej kontroli objawów astmy, całkowitą dawkę dobową należy zwiększyć i (lub) podawać w dawce podzielonej.
Pacjenci leczeni przewlekłymi doustnymi kortykosteroidami
Początkowo PULMICORT TURBUHALER (budezonid) należy stosować jednocześnie ze zwykłą podtrzymującą dawką kortykosteroidu ogólnoustrojowego. Po około tygodniu rozpoczyna się stopniowe odstawianie kortykosteroidu ogólnoustrojowego poprzez zmniejszenie dawki dobowej lub naprzemiennej. Kolejna redukcja następuje po upływie jednego lub dwóch tygodni, w zależności od odpowiedzi pacjenta. Ogólnie rzecz biorąc, te ubytki nie powinny przekraczać 2,5 mg prednizonu lub jego odpowiednika. Zdecydowanie zaleca się powolne tempo wycofywania. Podczas zmniejszania dawki doustnych kortykosteroidów należy uważnie monitorować pacjentów pod kątem niestabilności astmy, w tym obiektywnych pomiarów czynności dróg oddechowych i niewydolności nadnerczy (patrz OSTRZEŻENIA ). Podczas odstawienia niektórzy pacjenci mogą odczuwać objawy ogólnoustrojowego odstawienia kortykosteroidów, np. ból stawów i (lub) mięśni, zmęczenie i depresję, pomimo utrzymania lub nawet poprawy czynności płuc. Takich pacjentów należy zachęcać do kontynuowania leczenia PULMICORT TURBUHALER (budezonid), ale należy ich monitorować pod kątem obiektywnych objawów niewydolności nadnerczy. W przypadku wystąpienia objawów niewydolności kory nadnerczy należy tymczasowo zwiększyć dawki kortykosteroidów ogólnoustrojowych, a następnie odstawiać je wolniej. W okresach stresu lub ciężkiego ataku astmy pacjenci przenoszeni mogą wymagać dodatkowego leczenia kortykosteroidami ogólnoustrojowymi.
NOTATKA: U wszystkich pacjentów pożądane jest dostosowanie dawki do najniższej skutecznej dawki po osiągnięciu stabilności astmy.
Wskazówki dotyczące zastosowania
Ilustrowane instrukcje dla pacjenta do stosowania dołączyć do każdego opakowania PULMICORT 200mcg TURBUHALER (budezonid).
Pacjentów należy poinstruować, aby przygotowali PULMICORT TURBUHALER (budezonid) przed pierwszym użyciem, a także wykonać głęboki i silny wdech przy każdym użyciu urządzenia. Zaleca się również płukanie jamy ustnej po inhalacji.
JAK DOSTARCZONE
PULMICORT TURBUHALER (budesonid) składa się z szeregu złożonych elementów z tworzywa sztucznego, których głównymi częściami są mechanizm dozujący, pojemnik na substancję leczniczą i ustnik. Inhalator jest chroniony białą zewnętrzną osłoną rurkową przykręconą do inhalatora. Korpus inhalatora jest biały, a uchwyt obrotowy brązowy. Na uchwycie wydrukowano wypukłym napisem „Pulmicort™ 200 mcg”. Inhalatora TURBUHALER nie można ponownie napełnić i należy go wyrzucić, gdy jest pusty.
PULMICORT TURBUHALER (budezonid) jest dostępny w postaci 200 mcg/dawkę, 200 dawek (NDC 0186-0915-42) i ma docelowy ciężar wypełnienia 104 mg.
Gdy w PULMICORT 200mcg TURBUHALER (budezonid) pozostało 20 dawek, w okienku wskaźnika pojawi się czerwony znak. Jeśli urządzenie jest używane poza punktem, w którym na dole okienka pojawia się czerwony znak, może nie zostać uzyskana prawidłowa ilość leku. Urządzenie należy wyrzucić.
Przechowywać z dokręconą pokrywą w suchym miejscu w kontrolowanej temperaturze pokojowej 20-25°C (68-77°F) [patrz USP]. Trzymać z dala od dzieci.
Wszystkie znaki towarowe są własnością grupy firm AstraZeneca. ©AstraZeneca 2001, 2006. Wyprodukowano dla: AstraZeneca LP, Wilmington, DE 19850 Autor: AstraZeneca AB, Södertälje, Szwecja 33020-00. Rev. 10/06. Data aktualizacji FDA: 20.08.2007
SKUTKI UBOCZNE
U pacjentów leczonych produktem PULMICORT 100 µg TURBUHALER (budezonid) zgłoszono następujące działania niepożądane.
Częstość występowania częstych zdarzeń niepożądanych jest oparta na podwójnie ślepych, kontrolowanych placebo badaniach klinicznych w Stanach Zjednoczonych, w których 1116 dorosłych i dzieci w wieku od 6 do 70 lat (472 kobiety i 644 mężczyźni) było leczonych produktem PULMICORT TURBUHALER (budezonid) (200 do 800). mcg dwa razy dziennie przez 12 do 20 tygodni) lub placebo.
Poniższa tabela przedstawia częstość występowania zdarzeń niepożądanych u pacjentów, którzy wcześniej otrzymywali leki rozszerzające oskrzela i (lub) kortykosteroidy wziewne w kontrolowanych badaniach klinicznych w USA. Populacja ta obejmowała 232 pacjentów pediatrycznych płci męskiej i 62 płci żeńskiej (w wieku od 6 do 17 lat) oraz 332 dorosłych pacjentów płci męskiej i 331 płci żeńskiej (w wieku 18 lat i więcej).
Zdarzenia niepożądane z częstością ≥ 3% zgłaszane przez pacjentów stosujących PULMICORT 100 mcg TURBUHALER (budezonid)
Powyższa tabela zawiera wszystkie zdarzenia (uznane przez badaczy za związane z lekiem lub niezwiązane z lekiem), które wystąpiły z częstością ≥3% w dowolnej grupie PULMICORT TURBUHALER (budezonid) i były częstsze niż w grupie placebo. Biorąc pod uwagę te dane, należy wziąć pod uwagę wydłużony średni czas ekspozycji u pacjentów z produktem PULMICORT 200 µg TURBUHALER (budezonid).
Następujące inne działania niepożądane wystąpiły w tych badaniach klinicznych z zastosowaniem PULMICORT 100 mcg TURBUHALER (budezonid) z częstością od 1 do 3% i były częstsze w przypadku PULMICORT 200 mcg TURBUHALER (budezonid) niż w przypadku placebo.
Ciało jako całość: ból szyi
Układ sercowo-naczyniowy: omdlenie
Trawienny: ból brzucha, suchość w ustach, wymioty
Metaboliczne i odżywcze: przybranie na wadze
Układ mięśniowo-szkieletowy: złamanie, ból mięśni
Nerwowy: hipertonia, migrena
Płytki krwi, krwawienie i krzepnięcie: wybroczyny
Psychiatryczny: bezsenność
Mechanizmy oporu: infekcja
Zmysły specjalne: perwersja smaku
20-tygodniowym badaniu z udziałem dorosłych astmatyków, którzy wcześniej wymagali doustnych kortykosteroidów, działanie preparatu PULMICORT TURBUHALER (budezonid) 400 µg dwa razy dziennie (N=53) i 800 µg dwa razy dziennie (N=53) porównano z placebo (N=53). ) na temat częstości zgłaszanych zdarzeń niepożądanych. Zdarzenia niepożądane, uznane przez badaczy za związane z lekiem lub niezwiązane z lekiem, zgłoszone u więcej niż pięciu pacjentów w grupie PULMICORT 200mcg TURBUHALER (budezonid) i które występowały częściej podczas stosowania PULMICORT TURBUHALER (budezonid) niż placebo, przedstawiono poniżej ( % PULMICORT TURBUHALER (budezonid) i % placebo). Biorąc pod uwagę te dane, należy wziąć pod uwagę wydłużony średni czas ekspozycji u pacjentów z PULMICORT 200 mcg TURBUHALER (budezonid) (78 dni dla PULMICORT TURBUHALER (budezonid) w porównaniu do 41 dni dla placebo).
Pacjenci otrzymujący PULMICORT TURBUHALER (budezonid) raz dziennie
Profil zdarzeń niepożądanych przy podawaniu raz dziennie PULMICORT 100 mcg TURBUHALER (budezonid) 200 mcg i 400 mcg oraz placebo oceniano u 309 dorosłych pacjentów z astmą w 18-tygodniowym badaniu. Populacja badana obejmowała zarówno pacjentów wcześniej leczonych kortykosteroidami wziewnymi, jak i pacjentów nieotrzymujących wcześniej terapii kortykosteroidami. Nie stwierdzono klinicznie istotnych różnic w schemacie działań niepożądanych po jednorazowym podawaniu produktu PULMICORT 200 µg TURBUHALER (budezonid) raz na dobę w porównaniu z dawkowaniem dwa razy na dobę.
Badania pediatryczne: 12-tygodniowym badaniu kontrolowanym placebo z udziałem 404 pacjentów pediatrycznych w wieku od 6 do 18 lat, którym wcześniej leczono wziewne kortykosteroidy, częstość działań niepożądanych w każdej kategorii wiekowej (6 do 12 lat, 13 do 18 lat) była porównywalna dla produktu PULMICORT TURBUHALER (budezonid) (w dawce 100, 200 i 400 mcg dwa razy dziennie) oraz placebo. Nie było klinicznie istotnych różnic w schemacie lub nasileniu zdarzeń niepożądanych u dzieci w porównaniu z tymi zgłaszanymi u dorosłych.
Raporty o zdarzeniach niepożądanych z innych źródeł: Rzadkie zdarzenia niepożądane zgłoszone w opublikowanym piśmiennictwie lub z doświadczeń marketingowych na całym świecie związane z jakąkolwiek postacią wziewnego budezonidu obejmują: natychmiastowe i opóźnione reakcje nadwrażliwości, w tym wysypkę, kontaktowe zapalenie skóry, pokrzywkę, obrzęk naczynioruchowy i skurcz oskrzeli; objawy hipokortycyzmu i hiperkortycyzmu; jaskra, zaćma; objawy psychiatryczne, w tym depresja, reakcje agresywne, drażliwość, lęk i psychoza.
INTERAKCJE Z LEKAMI
badaniach klinicznych jednoczesne podawanie budezonidu i innych leków powszechnie stosowanych w leczeniu astmy nie powodowało zwiększonej częstości działań niepożądanych. Główną drogą metabolizmu budezonidu, jak również innych kortykosteroidów, jest izoenzym 3A4 cytochromu P450 (CYP) (CYP3A4). Po podaniu doustnym ketokonazolu, silnego inhibitora CYP3A4, wzrosło średnie stężenie budezonidu podawanego doustnie. Jednoczesne podawanie innych znanych inhibitorów CYP3A4 (np. itrakonazolu, klarytromycyny, erytromycyny itp.) może hamować metabolizm i zwiększać ogólnoustrojową ekspozycję na budezonid. Należy zachować ostrożność podczas jednoczesnego podawania budezonidu z ketokonazolem i innymi znanymi inhibitorami CYP3A4.
OSTRZEŻENIA
Szczególną ostrożność należy zachować w przypadku pacjentów, którzy przeszli z kortykosteroidów o działaniu ogólnoustrojowym na PULMICORT 200 µg TURBUHALER (budezonid), ponieważ u pacjentów z astmą w trakcie i po przejściu z kortykosteroidów ogólnoustrojowych na kortykosteroidy wziewne o mniejszej dostępności ogólnoustrojowej występowały zgony z powodu niewydolności kory nadnerczy. Po odstawieniu kortykosteroidów ogólnoustrojowych do przywrócenia czynności podwzgórzowo-przysadkowo-nadnerczowej (HPA) potrzeba kilku miesięcy.
Pacjenci, którzy wcześniej otrzymywali prednizon w dawce 20 mg lub więcej na dobę (lub jego odpowiednik), mogą być najbardziej podatni, szczególnie gdy ich ogólnoustrojowe kortykosteroidy zostały prawie całkowicie odstawione. W tym okresie supresji HPA pacjenci mogą wykazywać oznaki i objawy niewydolności nadnerczy, gdy są narażeni na uraz, zabieg chirurgiczny lub infekcję (szczególnie zapalenie żołądka i jelit) lub inne stany związane z ciężką utratą elektrolitów. Chociaż PULMICORT TURBUHALER (budezonid) może zapewnić kontrolę objawów astmy podczas tych epizodów, w zalecanych dawkach dostarcza mniej niż normalne fizjologiczne ilości glikokortykosteroidów ogólnoustrojowo i NIE zapewnia aktywności mineralokortykoidów niezbędnej do radzenia sobie z tymi nagłymi przypadkami.
okresach stresu lub ciężkiego ataku astmy, pacjentów, którym odstawiono kortykosteroidy ogólnoustrojowe, należy poinstruować, aby natychmiast wznowili podawanie doustnych kortykosteroidów (w dużych dawkach) i skontaktowali się z lekarzem w celu uzyskania dalszych instrukcji. Pacjentów tych należy również poinstruować, aby mieli przy sobie kartę identyfikacyjną medyczną wskazującą, że mogą potrzebować uzupełniających kortykosteroidów ogólnoustrojowych w okresach stresu lub ciężkiego ataku astmy.
Pacjenci wymagający doustnych kortykosteroidów powinni być powoli odstawieni od ogólnoustrojowego stosowania kortykosteroidów po przejściu na PULMICORT 100mcg TURBUHALER (budezonid). Podczas odstawiania doustnych kortykosteroidów należy dokładnie monitorować czynność płuc (FEV1 lub AM PEF), stosowanie beta-agonistów i objawy astmy. Oprócz monitorowania objawów podmiotowych i przedmiotowych astmy, pacjentów należy obserwować pod kątem oznak i objawów niewydolności nadnerczy, takich jak zmęczenie, zmęczenie, osłabienie, nudności i wymioty oraz niedociśnienie.
Przeniesienie pacjentów z leczenia kortykosteroidami systemowymi na PULMICORT 200mcg TURBUHALER (budezonid) może ujawnić stany alergiczne tłumione wcześniej przez leczenie kortykosteroidami systemowymi, np. nieżyt nosa, zapalenie spojówek, zapalenie stawów, stany eozynofilowe i egzema (patrz DAWKOWANIE I SPOSÓB PODAWANIA ).
Pacjenci przyjmujący leki hamujące układ odpornościowy są bardziej podatni na infekcje niż osoby zdrowe. Na przykład ospa wietrzna i odra mogą mieć cięższy, a nawet śmiertelny przebieg u podatnych pacjentów pediatrycznych lub dorosłych przyjmujących immunosupresyjne dawki kortykosteroidów. U pacjentów pediatrycznych lub dorosłych, którzy nie chorowali na te choroby, należy zachować szczególną ostrożność, aby uniknąć narażenia. Nie wiadomo, w jaki sposób dawka, droga i czas podawania kortykosteroidów wpływają na ryzyko rozwoju rozsianego zakażenia. Nie jest również znany wpływ choroby podstawowej i/lub wcześniejszego leczenia kortykosteroidami na ryzyko. W przypadku narażenia wskazane może być leczenie immunoglobuliną przeciwko ospie wietrznej i półpaścowi (VZIG) lub połączonej immunoglobuliny dożylnej (IVIG). W przypadku narażenia na odrę, może być wskazana profilaktyka za pomocą połączonej domięśniowej immunoglobuliny (IG). (Patrz odpowiednie ulotki informacyjne w celu uzyskania pełnych informacji na temat przepisywania VZIG i IG.) Jeśli rozwinie się ospa wietrzna, można rozważyć leczenie środkami przeciwwirusowymi.
PULMICORT 200mcg TURBUHALER (budezonid) nie jest lekiem rozszerzającym oskrzela i nie jest wskazany do szybkiego łagodzenia skurczu oskrzeli lub innych ostrych epizodów astmy.
Podobnie jak w przypadku innych wziewnych leków na astmę, po podaniu może wystąpić skurcz oskrzeli z natychmiastowym nasileniem świszczącego oddechu. Jeśli po podaniu produktu PULMICORT TURBUHALER (budezonid) wystąpi skurcz oskrzeli, należy go natychmiast leczyć szybko działającym wziewnym lekiem rozszerzającym oskrzela. Leczenie produktem PULMICORT TURBUHALER (budezonid) należy przerwać i zastosować terapię alternatywną.
Pacjentów należy poinstruować, aby natychmiast skontaktowali się z lekarzem w przypadku wystąpienia epizodów astmy niereagującej na zwykłe dawki leków rozszerzających oskrzela podczas leczenia produktem PULMICORT TURBUHALER (budezonid). Podczas takich epizodów pacjenci mogą wymagać leczenia doustnymi kortykosteroidami.
ŚRODKI OSTROŻNOŚCI
Ogólny
Podczas odstawiania doustnych kortykosteroidów u niektórych pacjentów mogą wystąpić objawy odstawienia kortykosteroidów o działaniu ogólnoustrojowym, np. ból stawów i (lub) mięśni, zmęczenie i depresja, pomimo utrzymania lub nawet poprawy czynności układu oddechowego (patrz DAWKOWANIE I SPOSÓB PODAWANIA ).
U pacjentów reagujących na leczenie PULMICORT TURBUHALER (budezonid) może pozwolić na kontrolowanie objawów astmy przy mniejszym tłumieniu czynności osi HPA niż terapeutycznie równoważne doustne dawki prednizonu. Ponieważ budezonid jest wchłaniany do krążenia i może być aktywny ogólnoustrojowo, korzystnego działania PULMICORT 100 µg TURBUHALER (budezonid) w minimalizowaniu dysfunkcji HPA można oczekiwać tylko wtedy, gdy zalecane dawki nie są przekraczane, a u poszczególnych pacjentów miareczkuje się najmniejszą skuteczną dawkę. Ponieważ istnieje indywidualna wrażliwość na wpływ na produkcję kortyzolu, lekarze powinni wziąć pod uwagę tę informację, przepisując PULMICORT 100mcg TURBUHALER (budezonid).
Ze względu na możliwość ogólnoustrojowego wchłaniania kortykosteroidów wziewnych, pacjentów leczonych produktem PULMICORT 200 µg TURBUHALER (budezonid) należy uważnie obserwować pod kątem jakichkolwiek objawów ogólnoustrojowego działania kortykosteroidów. Szczególną ostrożność należy zachować podczas obserwacji pacjentów po operacji lub w okresach stresu pod kątem oznak niewystarczającej odpowiedzi nadnerczy.
Możliwe, że ogólnoustrojowe działanie kortykosteroidów, takie jak hiperkortyza, zmniejszona gęstość mineralna kości i zahamowanie czynności kory nadnerczy, mogą wystąpić u niewielkiej liczby pacjentów, szczególnie przy wyższych dawkach. W przypadku wystąpienia takich zmian należy powoli zmniejszać dawkę PULMICORT 100mcg TURBUHALER (budezonid), zgodnie z przyjętymi procedurami postępowania w przypadku objawów astmy i zmniejszania dawki steroidów ogólnoustrojowych.
Kortykosteroidy wziewne doustnie, w tym budezonid, mogą powodować spowolnienie wzrostu u dzieci i młodzieży. Zmniejszenie szybkości wzrostu może wystąpić w wyniku niedostatecznej kontroli astmy lub stosowania w leczeniu kortykosteroidów. Potencjalny wpływ przedłużonego leczenia na szybkość wzrostu należy porównać z uzyskanymi korzyściami klinicznymi i ryzykiem związanym z alternatywnymi terapiami. Aby zminimalizować działanie ogólnoustrojowe doustnych wziewnych kortykosteroidów, w tym PULMICORT 200mcg TURBUHALER (budezonid), każdemu pacjentowi należy dostosować dawkę do najmniejszej skutecznej dawki (patrz ŚRODKI OSTROŻNOŚCI, zastosowanie pediatryczne ).
Chociaż pacjenci biorący udział w badaniach klinicznych otrzymywali PULMICORT TURBUHALER (budezonid) w sposób ciągły przez okres od 1 do 2 lat, długoterminowe miejscowe i ogólnoustrojowe działanie PULMICORT 200 mcg TURBUHALER (budezonid) u ludzi nie jest w pełni poznane. W szczególności nieznane są skutki wynikające z przewlekłego stosowania PULMICORT TURBUHALER (budezonid) na procesy rozwojowe lub immunologiczne w jamie ustnej, gardle, tchawicy i płucach.
W badaniach klinicznych z PULMICORT TURBUHALER (budezonid) u niektórych pacjentów występowały zlokalizowane zakażenia Candida albicans w jamie ustnej i gardle. Zakażenia te mogą wymagać odpowiedniego leczenia przeciwgrzybiczego i/lub przerwania leczenia produktem PULMICORT TURBUHALER (budezonid).
Kortykosteroidy wziewne należy stosować ostrożnie, jeśli w ogóle, u pacjentów z czynną lub nieaktywną gruźlicą dróg oddechowych, nieleczonymi ogólnoustrojowymi zakażeniami grzybiczymi, bakteryjnymi, wirusowymi lub pasożytniczymi lub opryszczką oczu.
Rzadko zgłaszano przypadki jaskry, podwyższonego ciśnienia śródgałkowego i zaćmy po wziewnym podaniu kortykosteroidów.
Informacje dla pacjentów
Pacjenci leczeni produktem PULMICORT TURBUHALER (budezonid) powinni otrzymać następujące informacje i instrukcje. Informacje te mają na celu pomóc pacjentowi w bezpiecznym i skutecznym stosowaniu leku. Nie jest to ujawnienie wszystkich możliwych działań niepożądanych lub zamierzonych. W celu prawidłowego stosowania PULMICORT 200mcg TURBUHALER (budezonid) i osiągnięcia maksymalnej poprawy pacjent powinien przeczytać i postępować zgodnie z załączonym Instrukcje dla pacjenta do Używaj ostrożnie.
- Pacjenci powinni stosować PULMICORT 200mcg TURBUHALER (budezonid) w regularnych odstępach czasu, zgodnie z zaleceniami, ponieważ jego skuteczność zależy od regularnego stosowania. Pacjent nie powinien zmieniać przepisanej dawki, chyba że zaleci to lekarz.
- Należy poinformować pacjentów, że PULMICORT 100mcg TURBUHALER (budezonid) nie jest lekiem rozszerzającym oskrzela i nie jest przeznaczony do leczenia ostrych lub zagrażających życiu epizodów astmy.
- Należy pouczyć pacjentów, że skuteczność PULMICORT 100mcg TURBUHALER (budezonid) zależy od prawidłowego użytkowania urządzenia i techniki inhalacji:
- 1. PULMICORT TURBUHALER (budezonid) musi znajdować się w pozycji pionowej (ustnik na górze) podczas ładowania, aby podać odpowiednią dawkę.
- 2. PULMICORT 100mcg TURBUHALER (budezonid) musi być zagruntowany, gdy urządzenie jest używane po raz pierwszy. Aby przygotować urządzenie, należy je trzymać w pozycji pionowej, a brązowy uchwyt przekręcić całkowicie w prawo, a następnie przekręcić całkowicie w lewo, aż usłyszysz kliknięcie. Powtarzać.
- 3. Aby załadować pierwszą dawkę, uchwyt należy przekręcić maksymalnie w prawo i maksymalnie w lewo, aż do usłyszenia kliknięcia.
- 4. Po pierwszej dawce nie jest konieczne zalewanie urządzenia. Jednak musi być załadowany w pozycji pionowej bezpośrednio przed użyciem, jak opisano powyżej.
- 5. Pacjentom należy zalecić, aby nie potrząsali inhalatorem.
- Pacjenci powinni umieścić ustnik między ustami i wykonać silny i głęboki wdech. Proszek jest następnie dostarczany do płuc.
- Pacjenci nie powinni wydychać powietrza przez PULMICORT TURBUHALER (budezonid).
- Ze względu na małą objętość proszku, podczas inhalacji z inhalatora TURBUHALER pacjent może nie smakować ani nie odczuwać obecności jakiegokolwiek leku dostającego się do płuc. Ten brak czucia nie wskazuje, że pacjent nie odnosi korzyści ze stosowania PULMICORT TURBUHALER (budezonid).
- Należy pouczyć pacjentów, że płukanie jamy ustnej wodą bez połykania po każdym podaniu może zmniejszyć ryzyko rozwoju kandydozy jamy ustnej.
- Pacjentów należy poinstruować, że otrzymają nowy zestaw PULMICORT TURBUHALER (budezonid) za każdym razem, gdy wypełnią receptę. Należy pouczyć pacjentów, aby wyrzucili całe urządzenie po wykorzystaniu podanej liczby inhalacji. Gdy w PULMICORT TURBUHALER (budezonid) pozostało 20 dawek, w okienku wskaźnika pojawi się czerwony znak.
- PULMICORT TURBUHALER (budesonid) nie powinien być stosowany z przekładką.
- Ustnika nie należy gryźć ani żuć.
- Pokrywę należy bezpiecznie wymieniać po każdym otwarciu.
- Pacjenci powinni przez cały czas utrzymywać PULMICORT TURBUHALER (budezonid) w czystości i suchości.
- Należy poinformować pacjentów, że poprawa kontroli astmy po inhalacji produktu PULMICORT TURBUHALER (budezonid) może nastąpić w ciągu 24 godzin od rozpoczęcia leczenia, chociaż maksymalne korzyści mogą nie być osiągnięte przez 1 do 2 tygodni lub dłużej. Jeśli w tym czasie objawy nie ustąpią lub stan się pogorszy, należy poinstruować pacjenta, aby nie zwiększał dawki, ale skontaktował się z lekarzem.
- Pacjentów, których kortykosteroidy ogólnoustrojowe zmniejszono lub odstawiono, należy poinstruować, aby mieli przy sobie kartę ostrzegawczą wskazującą, że mogą potrzebować uzupełniających kortykosteroidów ogólnoustrojowych w okresach stresu lub napadu astmy, które nie reagują na leki rozszerzające oskrzela.
- Należy poinformować pacjentów, aby nie przerywali nagle stosowania leku PULMICORT TURBUHALER (budezonid).
- Pacjentów należy ostrzec, aby unikali narażenia na ospę wietrzną lub odrę, a jeśli są narażeni, powinni niezwłocznie skonsultować się z lekarzem.
- Długotrwałe stosowanie wziewnych kortykosteroidów, w tym budezonidu, może zwiększać ryzyko niektórych problemów z oczami (zaćmy lub jaskry). Należy rozważyć regularne badania wzroku.
- Kobiety rozważające zastosowanie PULMICORT TURBUHALER (budezonid) powinny skonsultować się z lekarzem, jeśli są w ciąży lub zamierzają zajść w ciążę lub karmią piersią.
- Pacjenci rozważający zastosowanie PULMICORT TURBUHALER (budezonid) powinni skonsultować się z lekarzem, jeśli mają uczulenie na budezonid lub jakikolwiek inny kortykosteroid wziewny doustnie.
- Pacjenci powinni poinformować swojego lekarza o innych przyjmowanych lekach, ponieważ PULMICORT 100mcg TURBUHALER (budezonid) może nie być odpowiedni w niektórych okolicznościach i lekarz może chcieć zastosować inny lek.
Karcynogeneza, mutageneza, upośledzenie płodności
Przeprowadzono długoterminowe badania na szczurach i myszach po podaniu doustnym w celu oceny potencjalnego działania rakotwórczego budezonidu.
104-tygodniowym badaniu na szczurach Sprague-Dawley statystycznie istotny wzrost częstości występowania glejaków zaobserwowano u samców szczurów otrzymujących doustną dawkę 50 mikrogramów/kg mc./dobę (mniej niż maksymalna zalecana dobowa dawka wziewna u dorosłych i dzieci na podstawie mcg/m2). Nie zaobserwowano rakotwórczości u samców i samic szczurów po podaniu odpowiednich dawek doustnych do 25 i 50 mcg/kg (mniej niż maksymalna zalecana dobowa dawka wziewna u dorosłych i dzieci na podstawie mcg/m2). W dwóch dodatkowych dwuletnich badaniach na samcach szczurów Fischer i Sprague-Dawley budezonid nie powodował glejaków w dawce doustnej 50 μg/kg (mniej niż maksymalna zalecana dobowa dawka wziewna u dorosłych i dzieci wyrażona w μg/m2). Jednak u samców szczurów rasy Sprague-Dawley budezonid powodował statystycznie istotny wzrost częstości występowania guzów wątrobowokomórkowych po podaniu doustnym dawki 50 μg/kg (mniej niż maksymalna zalecana dzienna dawka wziewna u dorosłych i dzieci w przeliczeniu na μg/m2). ). Jednoczesne referencyjne kortykosteroidy (prednizon i acetonid triamcynolonu) w tych dwóch badaniach wykazały podobne wyniki.
Nie stwierdzono działania rakotwórczego budezonidu podawanego doustnie myszom przez 91 tygodni w dawkach do 200 mikrogramów/kg/dobę (mniej niż maksymalna zalecana dobowa dawka wziewna u dorosłych i dzieci wyrażona w mikrogramach/m2).
Budezonid nie wykazywał działania mutagennego ani klastogennego w sześciu różnych testach: test Ames Salmonella/płytka mikrosomowa, test mikrojądrowy u myszy, test chłoniaka u myszy, test aberracji chromosomowych w ludzkich limfocytach, test letalny recesywny sprzężony z płcią u Drosophila melanogaster oraz analiza naprawy DNA u szczura hodowla hepatocytów.
U szczurów budezonid nie miał wpływu na płodność w dawkach podskórnych do 80 mikrogramów/kg (mniej niż maksymalna zalecana dobowa dawka dobowa dla człowieka w przeliczeniu na mikrogramy/m2).
Przy dawce 20 mcg/kg/dobę (mniej niż maksymalna zalecana dobowa dawka wziewna dla człowieka wyrażona w mcg/m2) zaobserwowano zmniejszenie przyrostu masy ciała matki, żywotności prenatalnej i żywotności młodych przy urodzeniu i podczas laktacji. Nie zaobserwowano takich efektów przy 5 mcg/kg (mniej niż maksymalna zalecana dobowa dawka inhalacyjna u ludzi dorosłych na podstawie mcg/m2).
Ciąża: działanie teratogenne
Kategoria ciąży B: Podobnie jak w przypadku innych glikokortykosteroidów, budezonid powodował utratę płodów, zmniejszoną masę młodych i nieprawidłowości szkieletowe przy podskórnych dawkach 25 mcg/kg/dobę u królików (mniej niż maksymalna zalecana dobowa dawka wziewna dla człowieka w przeliczeniu na mcg/m2) oraz 500 µg/kg/dobę u szczurów (około 3-krotność maksymalnej zalecanej dobowej dawki wziewnej dla człowieka w przeliczeniu na µg/m2).
Nie zaobserwowano działania teratogennego ani embriobójczego u szczurów, gdy budezonid podawano wziewnie w dawkach do 250 μg/kg/dobę (co odpowiada maksymalnej zalecanej dobowej dawce wziewnej dla człowieka wyrażonej w mikrogramach/m2).
Doświadczenie z doustnymi kortykosteroidami od czasu ich wprowadzenia do dawek farmakologicznych, w przeciwieństwie do dawek fizjologicznych, sugeruje, że gryzonie są bardziej podatne na działanie teratogenne kortykosteroidów niż ludzie.
Badania kobiet w ciąży nie wykazały jednak, aby PULMICORT TURBUHALER (budezonid) zwiększał ryzyko nieprawidłowości w przypadku podawania w okresie ciąży. Wyniki dużego, populacyjnego, prospektywnego kohortowego badania epidemiologicznego, oceniającego dane z trzech szwedzkich rejestrów obejmujących około 99% ciąż z lat 1995-1997 (tj. Szwedzki Rejestr Urodzeń Medycznych; Rejestr Wad Wrodzonych; Rejestr Kardiologii Dziecięcej) wskazują na brak zwiększonego ryzyka w przypadku wad wrodzonych po zastosowaniu wziewnego budezonidu we wczesnej ciąży. Wady wrodzone badano u 2014 niemowląt urodzonych przez matki zgłaszające stosowanie wziewnego budezonidu w leczeniu astmy we wczesnej ciąży (zwykle 10-12 tygodni po ostatniej miesiączce), w okresie, w którym występuje większość poważnych wad rozwojowych narządów. Odsetek stwierdzonych wad wrodzonych był podobny w porównaniu z populacją ogólną (odpowiednio 3,8% vs 3,5%). Ponadto, po ekspozycji na budezonid wziewny, liczba niemowląt urodzonych z rozszczepami twarzoczaszki była podobna do oczekiwanej liczby w normalnej populacji (odpowiednio 4 dzieci vs. 3,3).
Te same dane wykorzystano w drugim badaniu obejmującym łącznie 2534 niemowląt, których matki były narażone na wdychany budezonid. W tym badaniu odsetek wad wrodzonych u niemowląt, których matki były narażone na wdychany budezonid we wczesnej ciąży, nie różnił się od odsetka wszystkich noworodków w tym samym okresie (3,6%).
Pomimo badań na zwierzętach wydaje się, że możliwość uszkodzenia płodu jest znikoma, jeśli lek jest stosowany w czasie ciąży. Niemniej jednak, ponieważ badania na ludziach nie mogą wykluczyć możliwości wystąpienia szkody, PULMICORT TURBUHALER (budezonid) należy stosować w okresie ciąży tylko w przypadku wyraźnej potrzeby.

Efekty nieteratogenne
Niedoczynność kory nadnerczy może wystąpić u niemowląt urodzonych przez matki otrzymujące kortykosteroidy w czasie ciąży. Takie niemowlęta należy uważnie obserwować.
Matki karmiące
Kortykosteroidy są wydzielane z mlekiem kobiecym. Ze względu na możliwość wystąpienia działań niepożądanych u karmionych niemowląt po zastosowaniu dowolnego kortykosteroidu, należy podjąć decyzję, czy przerwać karmienie piersią, czy przerwać stosowanie leku, biorąc pod uwagę znaczenie leku dla matki. Brakuje rzeczywistych danych dotyczących budezonidu.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność PULMICORT 100mcg TURBUHALER (budezonid) u dzieci w wieku poniżej 6 lat nie zostały ustalone.
U dzieci i młodzieży z astmą częstość działań niepożądanych obserwowanych po zastosowaniu produktu PULMICORT 100 mcg TURBUHALER (budezonid) była podobna w grupie wiekowej od 6 do 12 lat (N=172) w porównaniu z grupą wiekową od 13 do 17 lat (N=124). .
Kontrolowane badania kliniczne wykazały, że kortykosteroidy podawane doustnie mogą powodować zmniejszenie szybkości wzrostu u dzieci. Efekt ten zaobserwowano przy braku laboratoryjnych dowodów na zahamowanie osi podwzgórze-przysadka-nadnercza (HPA), co sugeruje, że szybkość wzrostu jest bardziej czułym wskaźnikiem ogólnoustrojowej ekspozycji na kortykosteroidy u dzieci niż niektóre powszechnie stosowane testy czynności osi HPA. Długoterminowe skutki tego zmniejszenia szybkości wzrostu związane z doustnymi wziewnymi kortykosteroidami, w tym wpływ na ostateczny wzrost osoby dorosłej, są nieznane. Możliwość „nadrobienia” wzrostu po przerwaniu leczenia doustnymi kortykosteroidami wziewnymi nie została odpowiednio zbadana.
badaniu z udziałem dzieci z astmą w wieku 5-12 lat, u dzieci leczonych produktem PULMICORT 200 µg TURBUHALER (budezonid) 200 µg dwa razy na dobę (n=311) nastąpiło zmniejszenie wzrostu o 1,1 centymetra w porównaniu z osobami otrzymującymi placebo (n=418) w koniec roku; różnica między tymi dwiema grupami leczenia nie zwiększyła się dalej w ciągu trzech lat dodatkowego leczenia. Pod koniec czterech lat dzieci otrzymujące PULMICORT TURBUHALER (budezonid) i dzieci otrzymujące placebo miały podobne szybkości wzrostu. Wnioski wyciągnięte z tego badania mogą być mylone z powodu nierównego stosowania kortykosteroidów w grupach terapeutycznych i włączenia danych od pacjentów osiągających dojrzałość płciową w trakcie badania.
Wzrost pacjentów pediatrycznych otrzymujących doustnie wziewne kortykosteroidy, w tym PULMICORT TURBUHALER (budezonid), powinien być rutynowo monitorowany (np. za pomocą stadiometrii). Potencjalny wpływ przedłużonego leczenia na wzrost należy porównać z uzyskanymi korzyściami klinicznymi oraz ryzykiem i korzyściami związanymi z terapiami alternatywnymi. Aby zminimalizować ogólnoustrojowe działanie wziewnych kortykosteroidów, w tym PULMICORT 100 mcg TURBUHALER (budezonid), każdemu pacjentowi należy dostosować dawkę do najniższej skutecznej dawki.
Zastosowanie geriatryczne
Stu pacjentów w wieku 65 lat lub starszych wzięło udział w amerykańskich i nieamerykańskich kontrolowanych badaniach klinicznych PULMICORT 100mcg TURBUHALER (budezonid). Nie było różnic w bezpieczeństwie i skuteczności leku w porównaniu z obserwowanymi u młodszych pacjentów.
Ogólnie rzecz biorąc, dobór dawki u pacjentów w podeszłym wieku powinien być ostrożny, zwykle zaczynając od dolnej granicy zakresu dawkowania, co odzwierciedla większą częstość pogorszenia czynności wątroby, nerek lub serca oraz współistniejących chorób lub innych leków.
PRZEDAWKOWAĆ
Potencjał ostrego działania toksycznego po przedawkowaniu PULMICORT 100mcg TURBUHALER (budezonid) jest niski. W przypadku stosowania nadmiernych dawek przez dłuższy czas może wystąpić ogólnoustrojowe działanie kortykosteroidów, takie jak hiperkortyza (patrz ŚRODKI OSTROŻNOŚCI ). PULMICORT TURBUHALER w dwukrotnej najwyższej zalecanej dawce (3200 mcg na dobę) podawany przez 6 tygodni powodował istotne zmniejszenie (27%) odpowiedzi kortyzolu w osoczu na 6-godzinny wlew ACTH w porównaniu z placebo (+1%). Odpowiednim efektem 10 mg prednizonu na dobę było 35% zmniejszenie odpowiedzi kortyzolu w osoczu na ACTH.
Minimalna śmiertelna dawka wziewna u myszy wynosiła 100 mg/kg (około 320-krotność maksymalnej zalecanej dobowej dawki wziewnej u dorosłych i około 380-krotność maksymalnej zalecanej dobowej dawki wziewnej u dzieci w mcg/m2). Nie było zgonów po podaniu szczurom dawki wziewnej 68 mg/kg (około 430-krotność maksymalnej zalecanej dobowej dawki wziewnej u dorosłych i około 510-krotność maksymalnej zalecanej dobowej dawki wziewnej u dzieci w mcg/m2). Minimalna śmiertelna dawka doustna wynosiła 200 mg/kg u myszy (około 630-krotność maksymalnej zalecanej dziennej dawki wziewnej u dorosłych i około 750-krotność maksymalnej zalecanej dziennej dawki wziewnej u dzieci na podstawie mcg/m2) i mniej niż 100 mg/kg u szczurów (około 630-krotność maksymalnej zalecanej dobowej dawki wziewnej u dorosłych i około 750-krotność maksymalnej zalecanej dobowej dawki wziewnej u dzieci na podstawie mcg/m2).
Doświadczenie po wprowadzeniu produktu do obrotu wykazało, że u pacjentów, u których wystąpiło ostre przedawkowanie wziewnego budezonidu, często nie występowały objawy. Stosowanie nadmiernych dawek (do 6400 mcg na dobę) przez dłuższy czas wykazało ogólnoustrojowe działanie kortykosteroidów, takie jak hiperkortyza.
PRZECIWWSKAZANIA
PULMICORT TURBUHALER (budezonid) jest przeciwwskazany w pierwotnym leczeniu stanu astmatycznego lub innych ostrych epizodów astmy, wymagających intensywnego leczenia.
Nadwrażliwość na budezonid jest przeciwwskazaniem do stosowania PULMICORT TURBUHALER (budezonid).
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Budezonid jest kortykosteroidem o działaniu przeciwzapalnym, który wykazuje silne działanie glikokortykoidowe i słabe działanie mineralokortykoidowe. W standardowych modelach in vitro i zwierzęcych budezonid ma około 200-krotnie większe powinowactwo do receptora glukokortykoidowego i 1000-krotnie większą siłę działania przeciwzapalnego do stosowania miejscowego niż kortyzol (test obrzęku ucha wywołanego olejem krotonowym u szczurów). Jako miara aktywności ogólnoustrojowej budezonid jest 40 razy silniejszy niż kortyzol przy podawaniu podskórnym i 25 razy silniejszy przy podawaniu doustnym w teście inwolucji grasicy szczura.
Aktywność PULMICORT 100mcg TURBUHALER wynika z leku macierzystego, budezonidu. W badaniach powinowactwa receptora glukokortykoidowego forma 22R była dwa razy bardziej aktywna niż epimer 22S. Badania in vitro wykazały, że dwie formy budezonidu nie ulegają wzajemnej konwersji.
Dokładny mechanizm działania kortykosteroidów na zapalenie w astmie nie jest znany. Stan zapalny jest ważnym elementem patogenezy astmy. Wykazano, że kortykosteroidy mają szeroki zakres działań hamujących wiele typów komórek (np. komórki tuczne, eozynofile, neutrofile, makrofagi i limfocyty) i mediatorów (np. histamina, eikozanoidy, leukotrieny i cytokiny) zaangażowanych w reakcje alergiczne i nie -zapalenie alergiczne. Te przeciwzapalne działania kortykosteroidów mogą przyczyniać się do ich skuteczności w astmie.
Badania u pacjentów z astmą wykazały korzystny stosunek między miejscowym działaniem przeciwzapalnym a ogólnoustrojowym działaniem kortykosteroidów w szerokim zakresie dawek PULMICORT 200mcg TURBUHALER (budezonid). Tłumaczy się to połączeniem stosunkowo silnego miejscowego działania przeciwzapalnego, znacznej degradacji pierwszego przejścia przez wątrobę leku wchłanianego doustnie (85-95%) oraz słabej siły powstających metabolitów (patrz poniżej).
Farmakokinetyka
Wchłanianie:
Po doustnym podaniu budezonidu maksymalne stężenie w osoczu osiągano po około 1 do 2 godzinach, a bezwzględna dostępność ogólnoustrojowa wynosiła 6-13%. Natomiast większość budezonidu dostarczonego do płuc jest wchłaniana ogólnoustrojowo. U osób zdrowych 34% odmierzonej dawki odkładało się w płucach (według oceny metodą stężenia w osoczu) przy bezwzględnej dostępności ogólnoustrojowej wynoszącej 39% odmierzonej dawki. Farmakokinetyka budezonidu nie różni się istotnie u zdrowych ochotników i pacjentów z astmą. Maksymalne stężenie budezonidu w osoczu wystąpiło w ciągu 30 minut od inhalacji produktu PULMICORT 200 µg TURBUHALER.U pacjentów z astmą budezonid wykazywał liniowy wzrost AUC i Cmax wraz ze wzrostem dawki zarówno po podaniu pojedynczej dawki, jak i po podaniu wielokrotnym PULMICORT 200 µg TURBUHALER (budezonid).
Dystrybucja:
Objętość dystrybucji budezonidu wynosiła około 3 l/kg. Wiązał się w 85-90% z białkami osocza. Wiązanie z białkami było stałe w zakresie stężeń (1-100 nmol/l) osiągniętym przy stosowaniu i przekraczaniu zalecanych dawek PULMICORT TURBUHALER. Budezonid wykazywał niewielkie lub żadne wiązanie z globuliną wiążącą kortykosteroidy. Budezonid szybko równoważył się z czerwonymi krwinkami w sposób niezależny od stężenia, przy stosunku krew/osocze wynoszącym około 0,8.Metabolizm:
Badania in vitro z homogenatami wątroby ludzkiej wykazały, że budezonid jest szybko i intensywnie metabolizowany. Wyizolowano i zidentyfikowano dwa główne metabolity powstałe w wyniku biotransformacji katalizowanej przez izoenzym 3A4 (CYP3A4) cytochromu P450 (CYP) izoenzymu 3A4 (CYP3A4) i zidentyfikowano je jako 16α-hydroksyprednizolon i 6β-hydroksybudezonid. Aktywność kortykosteroidowa każdego z tych dwóch metabolitów jest mniejsza niż 1% aktywności związku macierzystego. Nie wykryto jakościowych różnic między wzorcami metabolicznymi in vitro i in vivo. W preparatach ludzkich płuc i surowicy zaobserwowano znikomą inaktywację metaboliczną.Wydalanie/eliminacja:
Forma 22R budezonidu była preferencyjnie usuwana przez wątrobę z klirensem ogólnoustrojowym 1,4 l/min wobec 1,0 l/min dla formy 22S. Końcowy okres półtrwania, 2 do 3 godzin, był taki sam dla obu epimerów i niezależny od dawki. Budezonid był wydalany z moczem i kałem w postaci metabolitów. Około 60% dożylnie znakowanej radioaktywnie dawki odzyskano w moczu. W moczu nie wykryto budezonidu w postaci niezmienionej.Specjalne populacje:
Nie stwierdzono różnic farmakokinetycznych ze względu na rasę, płeć lub zaawansowany wiek.Pediatryczny:
Po podaniu dożylnym u dzieci w wieku 10-14 lat okres półtrwania w osoczu był krótszy niż u dorosłych (1,5 godziny w porównaniu z 2,0 godziny u dorosłych). W tej samej populacji po inhalacji budezonidu za pomocą inhalatora ciśnieniowego z dozownikiem bezwzględna dostępność ogólnoustrojowa była podobna jak u dorosłych.Niewydolność wątroby:
Zaburzenia czynności wątroby mogą wpływać na eliminację kortykosteroidów. Na farmakokinetykę budezonidu wpływały zaburzenia czynności wątroby, o czym świadczy podwojenie dostępności ogólnoustrojowej po przyjęciu doustnym. Farmakokinetyka dożylnego budezonidu była jednak podobna u pacjentów z marskością wątroby iu osób zdrowych.Interakcje między lekami:
Ketokonazol, silny inhibitor izoenzymu 3A4 (CYP3A4) cytochromu P450 (CYP), głównego enzymu metabolicznego kortykosteroidów, zwiększał stężenie budezonidu przyjmowanego doustnie w osoczu. W zalecanych dawkach cymetydyna miała niewielki, ale klinicznie nieistotny wpływ na farmakokinetykę budezonidu podawanego doustnie.Farmakodynamika
Aby potwierdzić, że wchłanianie ogólnoustrojowe nie jest istotnym czynnikiem skuteczności klinicznej wziewnego budezonidu, przeprowadzono badanie kliniczne u pacjentów z astmą porównujące 400 µg budezonidu podawanego za pomocą ciśnieniowego inhalatora z dozownikiem z łącznikiem rurkowym z 1400 µg budezonidu podawanego doustnie i placebo. Badanie wykazało skuteczność wziewnego budezonidu, ale nie doustnie, pomimo porównywalnych poziomów ogólnoustrojowych. Zatem efekt terapeutyczny konwencjonalnych dawek wziewnego budezonidu doustnie tłumaczy się w dużej mierze jego bezpośrednim działaniem na drogi oddechowe.
Ogólnie rzecz biorąc, PULMICORT TURBUHALER (budezonid) ma stosunkowo szybki początek działania jak na wziewny kortykosteroid. Poprawa kontroli astmy po inhalacji PULMICORT TURBUHALER (budezonid) może wystąpić w ciągu 24 godzin od rozpoczęcia leczenia, chociaż maksymalne korzyści mogą nie być osiągnięte przez 1 do 2 tygodni lub dłużej.
Wykazano, że PULMICORT TURBUHALER (budezonid) zmniejsza reaktywność dróg oddechowych w różnych modelach prowokacji, w tym histaminie, metacholinie, pirosiarczynie sodu i monofosforanie adenozyny u pacjentów z nadreaktywnością dróg oddechowych. Znaczenie kliniczne tych modeli nie jest pewne.
Wstępne leczenie PULMICORT 200mcg TURBUHALER (budezonid) 1600mcg dziennie (800mcg dwa razy dziennie) przez 2 tygodnie zmniejszyło ostry (reakcja wczesna faza) i opóźniony (reakcja późna faza) spadek FEV1 po prowokacji wziewnymi alergenami.
Wpływ preparatu PULMICORT 200 mcg TURBUHALER (budezonid) na oś podwzgórze-przysadka-nadnercza (HPA) zbadano u 905 osób dorosłych i 404 pacjentów pediatrycznych z astmą. U większości pacjentów zdolność do zwiększania produkcji kortyzolu w odpowiedzi na stres, oceniana za pomocą testu stymulacji kosyntropiny (ACTH), pozostała nienaruszona po leczeniu PULMICORT TURBUHALER (budezonid) w zalecanych dawkach. W przypadku dorosłych pacjentów leczonych 100, 200, 400 lub 800 mcg dwa razy dziennie przez 12 tygodni, odpowiednio 4%, 2%, 6% i 13% miało nieprawidłową odpowiedź na stymulowany kortyzol (szczyt kortyzolu
Podawanie budezonidu za pomocą PULMICORT 200mcg TURBUHALER (budezonid) w dawkach do 800 mcg/dobę (średnia dawka dobowa 445 mcg/dobę) lub za pomocą ciśnieniowego inhalatora z dozownikiem w dawkach do 1200 mcg/dobę (średnia dawka dobowa 620 mcg /dzień) u 216 pacjentów pediatrycznych (w wieku od 3 do 11 lat) przez 2 do 6 lat nie miało znaczącego wpływu na wzrost wzrostu w porównaniu z leczeniem bez kortykosteroidów u 62 dopasowanych pacjentów z grupy kontrolnej. Jednak długoterminowy wpływ PULMICORT TURBUHALER (budezonid) na wzrost nie jest w pełni poznany.
Ścieżki kliniczne
Skuteczność terapeutyczna preparatu PULMICORT 100 µg TURBUHALER (budezonid) została oceniona w kontrolowanych badaniach klinicznych z udziałem ponad 1300 pacjentów (6 lat i starszych) z astmą o różnym czasie trwania choroby (20 lat) i nasileniu.
Równoległe, prowadzone metodą podwójnie ślepej próby, kontrolowane placebo badania kliniczne trwające 12 tygodni i dłużej wykazały, że w porównaniu z placebo, PULMICORT TURBUHALER (budezonid) znacząco poprawiał czynność płuc (mierzoną za pomocą PEF i FEV1), znacząco zmniejszał poranne i wieczorne objawy astmy i znacząco zmniejszyło potrzebę stosowania wziewnych agonistów receptorów beta2 w razie potrzeby w dawkach od 400 mcg do 1600 mcg dziennie (200 mcg do 800 mcg dwa razy dziennie) u dorosłych i 400 mcg do 800 mcg dziennie (200 mcg do 400 mcg). dwa razy na dobę) u dzieci w wieku 6 lat i starszych.
Poprawę czynności płuc (poranny PEF) obserwowano w ciągu 24 godzin od rozpoczęcia leczenia zarówno u pacjentów dorosłych, jak i dzieci w wieku 6 lat i starszych, chociaż maksymalnych korzyści nie osiągnięto przez 1 do 2 tygodni lub dłużej po rozpoczęciu leczenia. Poprawa czynności płuc utrzymywała się przez 12 tygodni części badań z podwójnie ślepą próbą.
Pacjenci nieotrzymujący terapii kortykosteroidami
12-tygodniowym badaniu klinicznym z udziałem 273 pacjentów z astmą łagodną do umiarkowanej (średnia wyjściowa FEV1 2,27 l), którzy nie byli dobrze kontrolowani samymi lekami rozszerzającymi oskrzela, oceniano PULMICORT 200 mcg TURBUHALER (budezonid) w dawkach 200 mcg dwa razy na dobę i 400 mcg dwa razy codziennie w porównaniu z placebo. Wyniki FEV1 z tego badania przedstawiono na poniższym rysunku. Czynność płuc uległa znacznej poprawie po obu dawkach preparatu PULMICORT 100 µg TURBUHALER (budezonid) w porównaniu z placebo.
12-tygodniowe badanie u pacjentów nieotrzymujących terapii kortykosteroidami przed wejściem do badania
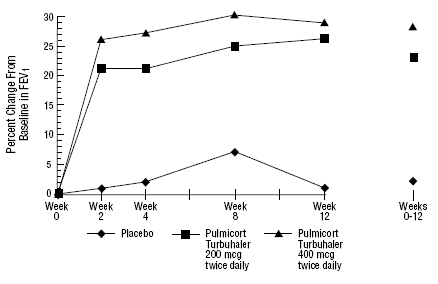
W 12-miesięcznym kontrolowanym badaniu z udziałem 75 pacjentów, którzy wcześniej nie otrzymywali kortykosteroidów, PULMICORT TURBUHALER (budezonid) w dawce 200 mcg dwa razy na dobę powodował poprawę czynności płuc (mierzoną za pomocą PEF) i zmniejszenie nadreaktywności oskrzeli w porównaniu z placebo.
Pacjenci, którzy wcześniej otrzymywali wziewne kortykosteroidy
Bezpieczeństwo i skuteczność produktu PULMICORT 200 mcg TURBUHALER (budezonid) oceniano również u pacjentów dorosłych i dzieci (w wieku od 6 do 18 lat) wcześniej leczonych wziewnymi kortykosteroidami (dorośli: N=473, średnia wyjściowa FEV1 2,04 l, początkowe dawki dipropionianu beklometazonu 126 -1008 µg/dobę; dzieci: N=404, średnia początkowa FEV1 2,09 l, początkowe dawki dipropionianu beklometazonu 126-672 µg/dobę lub acetonid triamcynolonu 300-1800 µg/dobę). Wyniki FEV1 z tych dwóch badań, oba trwające 12 tygodni, przedstawiono na poniższych rysunkach. Czynność płuc uległa znacznej poprawie po wszystkich dawkach produktu PULMICORT TURBUHALER (budezonid) w porównaniu z placebo w obu badaniach.
Dorośli pacjenci, którzy wcześniej otrzymywali wziewne kortykosteroidy
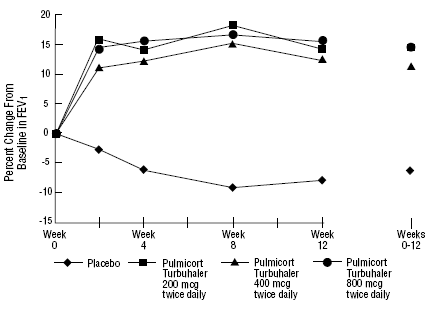
Pacjenci pediatryczni w wieku od 6 do 18 lat, którzy wcześniej otrzymywali wziewne kortykosteroidy
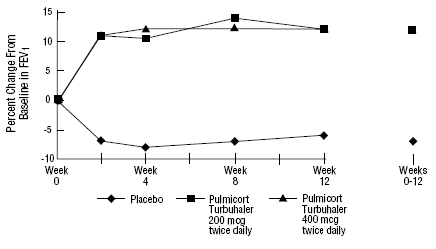
Pacjenci otrzymujący PULMICORT TURBUHALER (budezonid) raz dziennie
Skuteczność i bezpieczeństwo podawania raz na dobę produktu PULMICORT 100 mcg TURBUHALER (budezonid) 200 mcg i 400 mcg oraz placebo oceniano również u 309 dorosłych pacjentów z astmą (średnia wyjściowa FEV1 2,7 l) w 18-tygodniowym badaniu. W porównaniu z placebo, pacjenci otrzymujący Pulmicort 200 lub 400 mcg raz na dobę wykazywali znacznie lepszą stabilność astmy, ocenianą za pomocą PEF i FEV1 w początkowym 6-tygodniowym okresie leczenia, która utrzymywała się przy dawce 200 mcg na dobę przez kolejne 12 tygodni. Chociaż badana populacja obejmowała zarówno pacjentów wcześniej leczonych kortykosteroidami wziewnymi, jak i pacjentów nieotrzymujących wcześniej terapii kortykosteroidami, wyniki wykazały, że dawkowanie raz na dobę było najwyraźniejsze w przypadku pacjentów, u których wcześniej stosowano kortykosteroidy wziewne (patrz DAWKOWANIE I SPOSÓB PODAWANIA ).
Pacjenci, którzy wcześniej otrzymywali doustne kortykosteroidy
badaniu klinicznym z udziałem 159 pacjentów z ciężką astmą wymagających przewlekłego doustnego leczenia prednizonem (średnia wyjściowa dawka prednizonu 19,3 mg/dobę) PULMICORT TURBUHALER (budezonid) w dawkach 400 mcg dwa razy na dobę i 800 mcg dwa razy na dobę porównywano z placebo przez 20 tygodni Kropka. Około dwie trzecie (68% przy 400 mcg dwa razy na dobę i 64% przy 800 mcg dwa razy na dobę) pacjentów leczonych PULMICORT TURBUHALER (budezonid) było w stanie osiągnąć trwałe (co najmniej 2 tygodnie) zaprzestanie stosowania doustnych kortykosteroidów (w porównaniu z 8% otrzymujących placebo) i lepszą kontrolę astmy. Średnia dawka doustnych kortykosteroidów została zmniejszona o 83% w przypadku 400 mcg dwa razy na dobę i 79% w przypadku 800 mcg dwa razy na dobę w przypadku pacjentów leczonych PULMICORT TURBUHALER (budezonid) w porównaniu z 27% w przypadku placebo. Ponadto, 58 z 64 pacjentów (91%), którzy całkowicie wyeliminowali doustne kortykosteroidy podczas fazy badania z podwójnie ślepą próbą, nie przyjmowało doustnych kortykosteroidów przez dodatkowe 12 miesięcy podczas otrzymywania PULMICORT 200 mcg TURBUHALER (budezonid).
INFORMACJA O PACJENCIE
Instrukcja użytkowania dla pacjenta
Przed rozpoczęciem przyjmowania leku należy uważnie przeczytać tę ulotkę. Zawiera podsumowanie informacji o leku. Postępowanie zgodnie z tymi instrukcjami pomaga zapewnić prawidłowe wdychanie leku.
WIĘCEJ INFORMACJI ZADAĆ LEKARZE LUB FARMACEUCIE.
CO WARTO WIEDZIEĆ O PULMICORT TURBUHALER (budezonid)
Lekarz przepisał PULMICORT TURBUHALER 200 mcg. Zawiera lek o nazwie budezonid, który jest syntetycznym kortykosteroidem. Kortykosteroidy to naturalne substancje znajdujące się w organizmie, które pomagają zwalczać stany zapalne. Są stosowane w leczeniu astmy, ponieważ zmniejszają obrzęk i podrażnienie ścian małych dróg oddechowych w płucach i łagodzą problemy z oddychaniem. Przy regularnym wdychaniu kortykosteroidy pomagają również zapobiegać atakom astmy.
PULMICORT TURBUHALER (budezonid) leczy stan zapalny – „cichą część” astmy, której nie można usłyszeć, zobaczyć ani poczuć. Gdy stan zapalny nie jest leczony, objawy astmy i ataki mogą się nasilić. PULMICORT 200mcg TURBUHALER (budezonid) działa w celu zapobiegania i zmniejszania objawów i ataków astmy.
WAŻNE PUNKTY DO PAMIĘTANIA O PULMICORT TURBUHALER (budezonid)
NALEŻY UPEWNIĆ SIĘ, że ten lek jest odpowiedni dla pacjenta (patrz „PRZED UŻYCIEM PULMICORT TURBUHALER (budezonid)”).
Ważne jest, aby wdychać każdą dawkę zgodnie z zaleceniami lekarza.
Turbuhaler należy stosować zgodnie z zaleceniami lekarza. NIE PRZERYWAJ LECZENIA ANI NIE REDUKUJ DAWKI, NAWET JEŚLI POCZUJESZ SIĘ LEPIEJ, chyba że zaleci to lekarz.
NIE RÓB wdychać więcej dawek lub stosować Turbuhaler częściej niż zalecił lekarz.
Ten lek jest NIE przeznaczony do szybkiego złagodzenia trudności w oddychaniu podczas ataku astmy. Musi być przyjmowany w regularnych odstępach czasu, zgodnie z zaleceniami lekarza, a nie jako środek doraźny.
Lekarz może przepisać dodatkowe leki (takie jak leki rozszerzające oskrzela) w nagłych przypadkach
Jeśli stosujesz również inny lek do inhalacji, powinieneś skonsultować się z lekarzem w celu uzyskania instrukcji, kiedy go stosować w związku ze stosowaniem PULMICORT 100mcg TURBUHALER (budezonid).
PRZED UŻYCIEM TURBUHALERA PULMICORT (budezonid)
POINFORMUJ LEKARZA PRZED ROZPOCZĘCIEM STOSOWANIA TEGO LEKU, JEŚLI:
- są w ciąży (lub zamierzają zajść w ciążę),
- karmisz piersią dziecko,
- jesteś uczulony na budezonid lub jakikolwiek inny kortykosteroid wziewny,
- masz jakiekolwiek infekcje,
- masz lub miał gruźlicę,
- masz osteoporozę,
- ostatnio był w pobliżu każdego chorego na ospę wietrzną lub odrę,
- planują operację,
- przyjmował doustny lek kortykosteroidowy, taki jak prednizon. Być może będziesz musiał postępować zgodnie z określonymi instrukcjami, aby uniknąć zagrożeń dla zdrowia związanych z zaprzestaniem stosowania tego rodzaju leków.
W pewnych okolicznościach ten lek może nie być odpowiedni i lekarz może chcieć przepisać inny lek. Upewnij się, że Twój lekarz wie, jakie inne leki przyjmujesz, w tym leki na receptę i bez recepty, a także wszelkie witaminy lub suplementy diety i ziołowe.
JAKIE SĄ MOŻLIWE SKUTKI UBOCZNE TURBUHALERA PULMICORT (budezonid)?
Podobnie jak w przypadku wszystkich wziewnych kortykosteroidów, należy pamiętać o następujących działaniach niepożądanych:
- Nasilenie świszczącego oddechu zaraz po zażyciu PULMICORT 100mcg TURBUHALER (budezonid) . Zawsze miej przy sobie krótko działający lek rozszerzający oskrzela, aby leczyć nagły świszczący oddech. Krótko działające leki rozszerzające oskrzela pomagają rozluźnić mięśnie wokół dróg oddechowych w płucach. Świszczący oddech występuje, gdy mięśnie wokół dróg oddechowych napinają się. To utrudnia oddychanie. W ciężkich przypadkach świszczący oddech może zatrzymać oddychanie i spowodować śmierć, jeśli nie zostanie od razu leczony.
- Skutki układu odpornościowego i większa szansa na infekcje.
- Problemy z oczami, w tym jaskra i zaćma. W przypadku stosowania PULMICORT TURBUHALER (budezonid) należy rozważyć badanie oczu.
- Wzrost dziecka powinien być regularnie kontrolowany podczas przyjmowania PULMICOR TURBUHALER ze względu na możliwość spowolnienia wzrostu.
Na podstawie badań klinicznych najczęstsze działania niepożądane zgłaszane przez pacjentów stosujących PULMICORT 100mcg TURBUHALER (budezonid) to:
- infekcja drog oddechowych
- ból głowy
- Objawy grypy
- ból gardła
- zapalenie zatok
To nie wszystkie możliwe skutki uboczne stosowania PULMICORT TURBUHALER (budezonid). Aby uzyskać więcej informacji, zapytaj swojego lekarza, pracownika służby zdrowia lub farmaceuty.
KORZYSTANIE Z TURBUHALERA PULMICORT (budezonid)
- Postępuj zgodnie z instrukcjami podanymi w części „JAK UŻYWAĆ TURBUHALERA PULMICORT 200mcg”. Jeśli masz jakiekolwiek problemy, powiedz o tym lekarzowi lub farmaceucie.
- Ważne jest, aby wdychać każdą dawkę zgodnie z zaleceniami lekarza. Etykieta apteki zazwyczaj informuje, jaką dawkę należy przyjmować i jak często. Jeśli tak nie jest lub nie masz pewności, zapytaj lekarza lub farmaceutę.
DAWKOWANIE
- Stosuj zgodnie z zaleceniami lekarza.
- To jest BARDZO WAŻNE należy postępować zgodnie z zaleceniami lekarza dotyczącymi liczby inhalacji i częstotliwości stosowania PULMICORT TURBUHALER (budezonid) .
- NIE RÓB wdychać więcej dawek lub stosować PULMICORT TURBUHALER (budezonid) częściej niż zalecił lekarz.
- Może upłynąć od 1 do 2 tygodni lub dłużej, zanim poczujesz maksymalną poprawę, więc BARDZO WAŻNE JEST, ABY REGULARNIE UŻYWAĆ PULMICORT 100mcg TURBUHALER (budezonid). NIE PRZERYWAJ LECZENIA ANI NIE REDUKUJ DAWKI, NAWET JEŚLI POCZUJESZ SIĘ LEPIEJ, chyba że zaleci to lekarz.
- Jeśli pominiesz dawkę, po prostu zażyj regularnie zaplanowaną następną dawkę, kiedy jest to konieczne. NIE PODWOJAJ dawki.
JAK UŻYWAĆ TURBUHALERA PULMICORT (budezonid)
Przeczytaj uważnie całą instrukcję i używaj tylko zgodnie z zaleceniami.
INSTRUKCJE GRUNTOWANIA:
Przed pierwszym użyciem nowego PULMICORT 200mcg TURBUHALER (budezonid) należy go zagruntować. Aby to zrobić, obróć pokrywę i zdejmij. Trzymaj PULMICORT TURBUHALER (budezonid) pionowo (ustnikiem do góry), następnie przekręć brązowy uchwyt całkowicie w prawo iz powrotem w lewo. Powtarzać. Teraz jesteś gotowy do przyjęcia pierwszej dawki (patrz instrukcja „POBIERANIE DAWKI”). Po tym czasie nie musisz go przygotowywać, nawet jeśli odłożysz go na dłuższy czas.
PRZYJMOWANIE DAWKI:
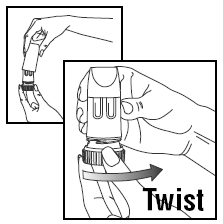
ŁADOWANIE DAWKI
- Przekręć pokrywę i zdejmij.
- Aby zapewnić odpowiednią dawkę, PULMICORT TURBUHALER (budezonid) musi być trzymany w pozycji pionowej (ustnik do góry) za każdym razem, gdy ładowana jest dawka leku.
- Przekręć brązowy uchwyt do oporu w prawo. Przekręć go ponownie całkowicie w lewo.
- Usłyszysz kliknięcie.
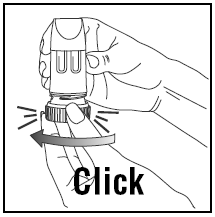
WDYCHANIE DAWKI
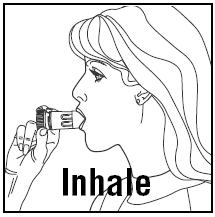
- Podczas wdechu PULMICORT 200mcg TURBUHALER (budezonid) musi być trzymany w pozycji pionowej (ustnik do góry) lub poziomej.
- Odwróć głowę od inhalatora i zrób wydech. Nie wstrząsać inhalatorem po załadowaniu.
- Umieścić ustnik między ustami i wykonać głęboki i silny wdech. Możesz nie smakować lub czuć leku.
- Nie żuć ani nie gryźć ustnika.
- Wyjmij inhalator z ust i zrób wydech. Nie dmuchać ani nie wydychać do ustnika.
- Jeśli potrzebna jest więcej niż jedna dawka, po prostu powtórz powyższe kroki.
- Po zakończeniu załóż z powrotem osłonkę na inhalator i zakręć. Wypłucz usta wodą. Nie połykaj.
- Utrzymuj swój PULMICORT TURBUHALER (budezonid) zawsze czysty i suchy.
- Nie stosować PULMICORT TURBUHALER (budezonid), jeśli został uszkodzony lub jeśli ustnik został odłączony.
PRZECHOWYWANIE TURBUHALERA PULMICORT (budezonid)
- Po każdym użyciu załóż z powrotem białą osłonę i mocno ją dokręć.
- Przechowywać PULMICORT TURBUHALER (budezonid) w suchym miejscu w kontrolowanej temperaturze pokojowej, 68-77°F (20-25°C).
- Trzymaj PULMICORT TURBUHALER (budezonid) w bezpiecznym miejscu z dala od zasięg małych dzieci.
- NIE RÓB stosować po dacie wskazanej na korpusie inhalatora Turbuhaler.
JAK WIEDZIEĆ, KIEDY TURBUHALER PULMICORT (budezonid) JEST PUSTY
Etykieta na pudełku lub na okładce zawiera informację, ile dawek znajduje się w urządzeniu PULMICORT TURBUHALER. Twój PULMICORT TURBUHALER (budezonid) ma wygodne okienko wskaźnika dawki tuż pod ustnikiem.
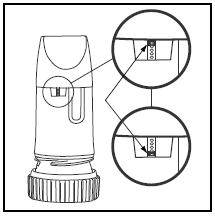
- Gdy w górnej części okienka pojawi się czerwony znak, oznacza to, że pozostało 20 dawek leku. Teraz nadszedł czas na zakup kolejnego PULMICORT 100mcg TURBUHALER (budezonid).
- Gdy czerwony znak dotrze do dna okienka, należy wyrzucić inhalator, ponieważ może nie dostarczać odpowiedniej ilości leku. (Nadal możesz słyszeć dźwięk, jeśli nim potrząsniesz – to nie jest dźwięk leku. Ten dźwięk jest wytwarzany przez środek osuszający wewnątrz Turbuhalera.)
- Pamiętaj, że za każdym razem, gdy uzupełnisz receptę, otrzymasz nowy inhalator.
- Nie zanurzaj go w wodzie, aby sprawdzić, czy jest pusty. Po prostu sprawdź okienko wskaźnika dawki.
DALSZE INFORMACJE O PULMICORT TURBUHALER (budezonid)
- PULMICORT 200mcg TURBUHALER (budezonid) dostarcza lek w postaci bardzo drobnego proszku. Z tego powodu nie możesz smak, zapach lub dotyk jakiekolwiek leki dostające się do płuc podczas inhalacji z PULMICORT TURBUHALER (budezonid) Nie oznacza to, że nie otrzymujesz leków.
- PULMICORT 100mcg TURBUHALER (budesonid) nie powinien być stosowany z przekładką.
- PULMICORT 100mcg TURBUHALER zawiera tylko budezonid i nie zawiera żadnych nieaktywnych składników.
- PULMICORT TURBUHALER (budezonid) jest specjalnie zaprojektowany do podawania tylko jednej dawki na raz, bez względu na to, jak często klikasz brązowy uchwyt. Jeśli przypadkowo wdmuchniesz powietrze do inhalatora po załadowaniu dawki, po prostu postępuj zgodnie z instrukcjami dotyczącymi ładowania nowej dawki.
Ta ulotka nie zawiera pełnych informacji o leku. Jeśli masz jakieś pytania lub nie jesteś czegoś pewien, skontaktuj się z lekarzem lub farmaceutą.
Możesz ponownie przeczytać tę ulotkę. Proszę NIE WYRZUCAĆ przed zakończeniem przyjmowania leku.
PAMIĘTAJ: Ten lek został przepisany przez lekarza. NIE podawaj tego leku nikomu innemu.
UŻYWAJ TEGO PRODUKTU ZGODNIE Z WSKAZANIAMI, CHYBA ŻE LEKARZ NIE POleci inaczej.
Jeśli masz dodatkowe pytania dotyczące stosowania PULMICORT 100mcg TURBUHALER (budezonid), zadzwoń: 1-800-236-9933.
