Spiriva 9mcg Tiotropium Bromide Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Spiriva 9mcg HandiHaler i jak się go stosuje?
Spiriva HandiHaler (bromek tiotropium) Inhalation Powder to lek antycholinergiczny stosowany w zapobieganiu skurczowi oskrzeli (zwężenie dróg oddechowych w płucach) u osób z zapaleniem oskrzeli, rozedmą lub POChP (przewlekła obturacyjna choroba płuc).
Jakie są skutki uboczne Spiriva 9mcg HandiHaler?
Częste działania niepożądane Spiriva 9mcg HandiHaler obejmują:
- suchość w ustach,
- zaparcie,
- rozstrój żołądka,
- wymioty,
- objawy przeziębienia (zatkany nos, kichanie, ból gardła),
- krwawienie z nosa lub
- ból w mięśniach.
Należy poinformować lekarza, jeśli wystąpią jakiekolwiek poważne działania niepożądane leku Spiriva 9mcg HandiHaler, w tym:
- trudne lub bolesne oddawanie moczu lub
- szybkie bicie serca.
OPIS
SPIRIVA 9mcg HANDIHALER składa się z kapsułek SPIRIVA oraz urządzenia HANDIHALER. Każda jasnozielona, twarda kapsułka żelatynowa SPIRIVA 9 mcg zawiera suchy proszek składający się z 18 mcg tiotropium (co odpowiada 22,5 mcg jednowodnego bromku tiotropium) zmieszanego z jednowodną laktozą (która może zawierać białka mleka).
Zawartość kapsułek SPIRIVA jest przeznaczona wyłącznie do inhalacji doustnej i jest przeznaczona do podawania wyłącznie za pomocą urządzenia HANDIHALER.
Aktywnym składnikiem SPIRIVA HANDIHALER jest tiotropium. Substancja lecznicza, monohydrat bromku tiotropium, jest środkiem antycholinergicznym o specyficznym działaniu na receptory muskarynowe. Jest chemicznie opisany jako (1α, 2β, 4β, 5α, 7β)-7-[(hydroksydi-2-tienyloacetylo)oksy]-9,9-dimetylo-3-oksa-9-azoniatricyklo[3.3.1.02,4] monohydrat bromku nonanu. Jest to syntetyczny, niechiralny, czwartorzędowy związek amoniowy. Bromek tiotropium jest białym lub żółtawobiałym proszkiem. Jest słabo rozpuszczalny w wodzie i rozpuszczalny w metanolu.
Wzór strukturalny to:
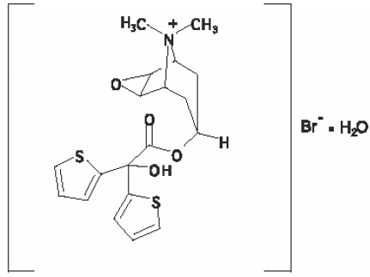
Bromek tiotropium (monohydrat) ma masę cząsteczkową 490,4 i wzór cząsteczkowy C19H22NO4S2Br • H2O.
Urządzenie HANDIHALER to inhalator służący do inhalacji suchego proszku zawartego w kapsułce SPIRIVA 9mcg. Suchy proszek jest dostarczany z urządzenia HANDIHALER z szybkością przepływu nawet 20 l/min. W standaryzowanych testach in vitro urządzenie HANDIHALER dostarcza średnio 10,4 mcg tiotropium podczas badania przy natężeniu przepływu 39 l/min przez 3,1 sekundy (łącznie 2 l). W badaniu 26 dorosłych pacjentów z POChP i ciężkimi zaburzeniami czynności płuc [średnia FEV1 1,02 l (zakres 0,45 do 2,24 l); 37,6% przewidywanych (zakres 16% do 65%)], mediana szczytowego przepływu wdechowego (PIF) przez urządzenie HANDIHALER wynosiła 30,0 l/min (zakres 20,4 do 45,6 l/min). Ilość leku dostarczonego do płuc będzie się różnić w zależności od czynników pacjenta, takich jak przepływ wdechowy i szczytowy przepływ wdechowy przez urządzenie HANDIHALER, które mogą się różnić w zależności od pacjenta i mogą różnić się w zależności od czasu ekspozycji kapsułki SPIRIVA 9mcg poza blistrami Pakiet.
WSKAZANIA
SPIRIVA HANDIHALER (proszek do inhalacji bromku tiotropium) jest wskazany do długotrwałego, raz dziennie, podtrzymującego leczenia skurczu oskrzeli związanego z przewlekłą obturacyjną chorobą płuc (POChP), w tym przewlekłego zapalenia oskrzeli i rozedmy płuc. SPIRIVA 9mcg Handihaler jest wskazany w celu zmniejszenia zaostrzeń u pacjentów z POChP.
DAWKOWANIE I SPOSÓB PODAWANIA
Wyłącznie do inhalacji doustnej. Nie należy połykać kapsułek SPIRIVA 9mcg, ponieważ zamierzony wpływ na płuca nie zostanie osiągnięty. Zawartość kapsułek SPIRIVA należy stosować wyłącznie z urządzeniem HANDIHALER [Widzieć PRZEDAWKOWAĆ ].
Zalecana dawka preparatu SPIRIVA HANDIHALER to dwie inhalacje zawartości proszku z jednej kapsułki SPIRIVA raz dziennie za pomocą urządzenia HANDIHALER [patrz INFORMACJA O PACJENCIE ]. Nie należy przyjmować więcej niż jednej dawki w ciągu 24 godzin.
celu podania SPIRIVA HANDIHALER kapsułkę SPIRIVA 9mcg umieszcza się w środkowej komorze urządzenia HANDIHALER. Kapsułkę SPIRIVA 9mcg przekłuwa się, naciskając i zwalniając zielony przycisk przebijający z boku urządzenia HANDIHALER. Preparat tiotropium jest rozpraszany w strumieniu powietrza, gdy pacjent wdycha przez ustnik [patrz INFORMACJA O PACJENCIE ].
Nie ma konieczności dostosowania dawkowania u pacjentów w podeszłym wieku, pacjentów z zaburzeniami czynności wątroby lub nerek. Jednakże pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności nerek, którym podawano produkt SPIRIVA 9mcg Handihaler, należy ściśle monitorować pod kątem działania przeciwcholinergicznego [patrz OSTRZEŻENIA I ŚRODKI , Używaj w określonych populacjach , oraz FARMAKOLOGIA KLINICZNA ].
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Proszek do inhalacji
SPIRIVA 9mcg HANDIHALER składa się z kapsułek SPIRIVA zawierających proszek tiotropium do inhalacji doustnej oraz urządzenia HANDIHALER. Kapsułki SPIRIVA 9mcg zawierają 18 mcg tiotropium w jasnozielonej, twardej kapsułce żelatynowej z nadrukiem TI 01 po jednej stronie i logo firmy Boehringer Ingelheim po drugiej stronie. Urządzenie HANDIHALER jest przeznaczone wyłącznie do użytku z kapsułkami SPIRIVA.
Składowania i stosowania
SPIRIVA HANDIHALER składa się z kapsułek SPIRIVA 9mcg oraz urządzenia HANDIHALER. Kapsułki SPIRIVA 9mcg zawierają 18 mcg tiotropium i są jasnozielone, z logo firmy Boehringer Ingelheim na wieczku kapsułki SPIRIVA i TI 01 na korpusie kapsułki SPIRIVA lub odwrotnie.
Urządzenie HANDIHALER jest koloru szarego z zielonym guzikiem do przekłuwania. Nadrukowany jest SPIRIVA HANDIHALER (proszek do inhalacji bromkiem tiotropium), logo firmy Boehringer Ingelheim. Jest również nadruk, aby wskazać, że kapsułki SPIRIVA nie powinny być przechowywane w urządzeniu HANDIHALER i że urządzenie HANDIHALER może być używane wyłącznie z kapsułkami SPIRIVA 9mcg.
Kapsułki SPIRIVA 9mcg są pakowane w blistry aluminiowo-aluminiowe i łączone wzdłuż perforowanej linii cięcia. Kapsułki SPIRIVA 9mcg należy zawsze przechowywać w blistrze i wyjmować dopiero bezpośrednio przed użyciem. Lek należy zużyć natychmiast po otwarciu opakowania nad pojedynczą kapsułką SPIRIVA.
Dostępne są następujące pakiety:
- pudełko tekturowe zawierające 5 kapsułek SPIRIVA 9mcg (1 blister z pojedynczą dawką) i 1 inhalator HANDIHALER ( NDC 0597-0075-75) (pakiet instytucjonalny)
- karton zawierający 30 kapsułek SPIRIVA 9mcg (3 blistry z pojedynczą dawką) i 1 inhalator HANDIHALER ( NDC 0597-0075-41)
- pudełko tekturowe zawierające 90 kapsułek produktu SPIRIVA (9 blistrów z pojedynczą dawką) i 1 inhalator HANDIHALER ( NDC 0597-0075-47)
Trzymać poza zasięgiem dzieci. Nie dostaniesz proszku do oczu.
Magazynowanie
Przechowywać w 25°C (77°F); dopuszczalne odchylenia do 15° do 30°C (59° do 86°F) [patrz Kontrolowana temperatura pokojowa USP].
Kapsułki SPIRIVA nie powinny być wystawiane na działanie ekstremalnych temperatur ani wilgoci. Nie przechowywać kapsułek SPIRIVA 9mcg w urządzeniu HANDIHALER.
Dystrybutor: Boehringer Ingelheim Pharmaceuticals, Inc. Ridgefield, CT 06877 USA. Aktualizacja: luty 2018 r.
SKUTKI UBOCZNE
Następujące działania niepożądane opisano lub opisano bardziej szczegółowo w innych punktach:
- Natychmiastowe reakcje nadwrażliwości [patrz OSTRZEŻENIA I ŚRODKI ]
- Paradoksalny skurcz oskrzeli [patrz OSTRZEŻENIA I ŚRODKI ]
- Pogorszenie jaskry z wąskim kątem [patrz OSTRZEŻENIA I ŚRODKI ]
- Pogorszenie zatrzymania moczu [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością występowania w badaniach klinicznych innego leku i może nie odzwierciedlać częstości występowania obserwowanej w praktyce.
Okres próbny od 6 miesięcy do 1 roku
Opisane poniżej dane odzwierciedlają ekspozycję na produkt SPIRIVA 9mcg HANDIHALER u 2663 pacjentów. Produkt SPIRIVA 9mcg HANDIHALER badano w dwóch rocznych badaniach kontrolowanych placebo, dwóch rocznych badaniach z aktywną kontrolą oraz dwóch 6-miesięcznych badaniach kontrolowanych placebo u pacjentów z POChP. W tych badaniach 1308 pacjentów było leczonych produktem SPIRIVA HANDIHALER w zalecanej dawce 18 mikrogramów raz na dobę. Populacja była w wieku od 39 do 87 lat, z 65% do 85% mężczyznami, 95% rasy białej i POChP ze średnią przewidywaną natężoną objętością wydechową w ciągu jednej sekundy (FEV1) przed lekiem rozszerzającym oskrzela na poziomie 39% do 43%. Z badań tych wykluczono pacjentów z jaskrą z wąskim kątem, objawowym przerostem gruczołu krokowego lub niedrożnością ujścia pęcherza moczowego. Dodatkowe 6-miesięczne badanie przeprowadzone w środowisku Veteran's Affairs nie jest uwzględnione w tej bazie danych bezpieczeństwa, ponieważ zebrano tylko poważne zdarzenia niepożądane.
Najczęściej zgłaszanym działaniem niepożądanym leku była suchość w ustach. Suchość w jamie ustnej była zwykle łagodna i często ustępowała podczas kontynuacji leczenia. Inne reakcje zgłaszane u poszczególnych pacjentów i zgodne z możliwym działaniem antycholinergicznym obejmowały zaparcia, tachykardię, niewyraźne widzenie, jaskra (nowy początek lub pogorszenie), bolesne oddawanie moczu i zatrzymanie moczu.
W czterech wieloośrodkowych, rocznych badaniach kontrolowanych placebo i aktywnie kontrolowanych oceniano produkt SPIRIVA HANDIHALER u pacjentów z POChP. W Tabeli 1 przedstawiono wszystkie działania niepożądane, które wystąpiły z częstością ≥3% w grupie produktu SPIRIVA 9mcg HANDIHALER w rocznych badaniach kontrolowanych placebo, w których częstość występowania w grupie produktu SPIRIVA HANDIHALER przewyższała placebo o ≥1%. Dla porównania uwzględniono częstość odpowiednich reakcji w badaniach kontrolowanych ipratropium.
Zapalenie stawów, kaszel i objawy grypopodobne występowały z częstością ≥3% w grupie leczonej produktem SPIRIVA 9mcg Handihaler, ale były o
Inne reakcje, które wystąpiły w grupie produktu SPIRIVA HANDIHALER z częstością od 1% do 3% w badaniach kontrolowanych placebo, w których częstość była większa niż w grupie placebo, obejmują:
Ciało jako całość: reakcja alergiczna, ból nóg;
Centralny i obwodowy układ nerwowy: dysfonia, parestezje;
Zaburzenia układu pokarmowego: zaburzenia żołądkowo-jelitowe nieokreślone inaczej (NOS), refluks żołądkowo-przełykowy, zapalenie jamy ustnej (w tym wrzodziejące zapalenie jamy ustnej);
Zaburzenia metabolizmu i odżywiania: hipercholesterolemia, hiperglikemia;
Zaburzenia układu mięśniowo-szkieletowego: ból szkieletu;
Wydarzenia kardiologiczne: dusznica bolesna (w tym zaostrzona dusznica bolesna);
Zaburzenie psychiczne: depresja; Infekcje: półpasiec;
Zaburzenia układu oddechowego (górne): zapalenie krtani;
Zaburzenia widzenia: zaćma.
Ponadto wśród działań niepożądanych obserwowanych w badaniach klinicznych z częstością
rocznych badaniach częstość występowania suchości w ustach, zaparć i infekcji dróg moczowych wzrastała wraz z wiekiem [patrz Używaj w określonych populacjach ].
W dwóch wieloośrodkowych, 6-miesięcznych, kontrolowanych badaniach oceniano produkt SPIRIVA 9mcg Handihaler u pacjentów z POChP. Działania niepożądane i częstość występowania były podobne do obserwowanych w rocznych kontrolowanych badaniach.
4-letni okres próbny
Opisane poniżej dane odzwierciedlają ekspozycję na produkt SPIRIVA 9mcg Handihaler u 5992 pacjentów z POChP w 4-letnim badaniu kontrolowanym placebo. W tym badaniu 2986 pacjentów było leczonych produktem SPIRIVA 9mcg Handihaler w zalecanej dawce 18 mcg raz na dobę. Populacja była w wieku od 40 do 88 lat, 75% mężczyzn, 90% rasy kaukaskiej, z POChP ze średnim oczekiwanym procentem FEV1 przed lekiem rozszerzającym oskrzela 40%. Z badań tych wykluczono pacjentów z jaskrą z wąskim kątem, objawowym przerostem gruczołu krokowego lub niedrożnością ujścia pęcherza moczowego. Gdy działania niepożądane były analizowane z częstością ≥3% w grupie produktu SPIRIVA 9mcg Handihaler, gdzie wskaźniki w grupie produktu SPIRIVA 9mcg Handihaler przewyższały placebo o ≥1%, działania niepożądane obejmowały (SPIRIVA 9mcg Handihaler, placebo): zapalenie gardła (12,5% , 10,8%), zapalenie zatok (6,5%, 5,3%), ból głowy (5,7%, 4,5%), zaparcia (5,1%, 3,7%), suchość w ustach (5,1%, 2,7%), depresja (4,4%, 3,3%) , bezsenność (4,4%, 3,0%) i bóle stawów (4,2%, 3,1%).
Dodatkowe działania niepożądane
Inne niewymienione wcześniej działania niepożądane, które zgłaszano częściej u pacjentów z POChP leczonych produktem SPIRIVA 9mcg Handihaler niż placebo obejmują: odwodnienie, owrzodzenie skóry, zapalenie jamy ustnej, zapalenie dziąseł, kandydozę jamy ustnej i gardła, suchość skóry, zakażenie skóry i obrzęk stawów.
Doświadczenie postmarketingowe
Działania niepożądane zostały zidentyfikowane podczas stosowania produktu SPIRIVA Handihaler na całym świecie po jego dopuszczeniu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek. Te działania niepożądane to: podrażnienie w miejscu podania (zapalenie języka, owrzodzenie jamy ustnej i ból gardła i krtani), zawroty głowy, dysfagia, chrypka, niedrożność jelit, w tym porażenna niedrożność jelit, podwyższone ciśnienie śródgałkowe, kandydoza jamy ustnej, kołatanie serca, świąd, tachykardia, podrażnienie gardła i pokrzywka.
INTERAKCJE Z LEKAMI
Sympatykomimetyki, metyloksantyny, sterydy
Produkt SPIRIVA 9mcg Handihaler stosowano jednocześnie z krótko i długo działającymi sympatykomimetykami (beta-agonistami), lekami rozszerzającymi oskrzela, metyloksantynami oraz doustnymi i wziewnymi steroidami bez nasilenia działań niepożądanych.
Antycholinergiczne
Istnieje możliwość addytywnej interakcji z jednocześnie stosowanymi lekami antycholinergicznymi. Dlatego należy unikać jednoczesnego podawania produktu SPIRIVA 9mcg Handihaler z innymi lekami zawierającymi antycholinergiczne, ponieważ może to prowadzić do nasilenia działań niepożądanych o działaniu antycholinergicznym [patrz OSTRZEŻENIA I ŚRODKI oraz DZIAŁANIA NIEPOŻĄDANE ].
OSTRZEŻENIA
Zawarte jako część "ŚRODKI OSTROŻNOŚCI" Sekcja
ŚRODKI OSTROŻNOŚCI
Nie do ostrego użytku
SPIRIVA 9mcg HANDIHALER jest przeznaczony do codziennego leczenia podtrzymującego POChP i nie powinien być stosowany w celu łagodzenia ostrych objawów, tj. jako terapia ratunkowa w leczeniu ostrych epizodów skurczu oskrzeli.
Natychmiastowe reakcje nadwrażliwości
Po podaniu produktu SPIRIVA 9mcg Handihaler mogą wystąpić natychmiastowe reakcje nadwrażliwości, w tym pokrzywka, obrzęk naczynioruchowy (w tym obrzęk warg, języka lub gardła), wysypka, skurcz oskrzeli, anafilaksja lub swędzenie. W przypadku wystąpienia takiej reakcji należy natychmiast przerwać leczenie produktem SPIRIVA 9mcg Handihaler i rozważyć alternatywne metody leczenia. Biorąc pod uwagę podobny wzór strukturalny atropiny do tiotropium, pacjentów z reakcjami nadwrażliwości na atropinę lub jej pochodne w wywiadzie należy ściśle monitorować pod kątem podobnych reakcji nadwrażliwości na produkt SPIRIVA Handihaler. Ponadto produkt SPIRIVA HANDIHALER należy stosować ostrożnie u pacjentów z ciężką nadwrażliwością na białka mleka.
Paradoksalny skurcz oskrzeli
Leki wziewne, w tym SPIRIVA HANDIHALER, mogą powodować paradoksalny skurcz oskrzeli. W takim przypadku należy natychmiast zastosować wziewny krótko działający beta2-mimetyk, taki jak albuterol. Leczenie produktem SPIRIVA HANDIHALER należy przerwać i rozważyć inne metody leczenia.
Pogorszenie jaskry wąskiego kąta
Produkt SPIRIVA 9mcg Handihaler należy stosować ostrożnie u pacjentów z jaskrą z wąskim kątem przesączania. Lekarze przepisujący lek i pacjenci powinni być wyczuleni na oznaki i objawy ostrej jaskry z wąskim kątem przesączania (np. ból oka lub dyskomfort, niewyraźne widzenie, aureole wzrokowe lub kolorowe obrazy w połączeniu z zaczerwienieniem oczu spowodowanym przekrwieniem spojówki i obrzękiem rogówki). Należy poinstruować pacjentów, aby w przypadku pojawienia się któregokolwiek z tych objawów lub objawów natychmiast skonsultowali się z lekarzem.
Pogorszenie zatrzymania moczu
Produkt SPIRIVA Handihaler należy stosować ostrożnie u pacjentów z zatrzymaniem moczu. Lekarze przepisujący lek i pacjenci powinni być wyczuleni na oznaki i objawy zatrzymania moczu (np. trudności w oddawaniu moczu, bolesne oddawanie moczu), zwłaszcza u pacjentów z przerostem gruczołu krokowego lub niedrożnością szyi pęcherza moczowego. Należy poinstruować pacjentów, aby w przypadku pojawienia się któregokolwiek z tych objawów lub objawów natychmiast skonsultowali się z lekarzem.
Zaburzenia czynności nerek
Ponieważ lek jest wydalany głównie przez nerki, pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności nerek (klirens kreatyniny FARMAKOLOGIA KLINICZNA ].
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( INFORMACJE DLA PACJENTA i instrukcje użytkowania ).
Nie do ostrego użytku
Należy poinstruować pacjentów, że produkt SPIRIVA HANDIHALER jest lekiem rozszerzającym oskrzela stosowanym raz na dobę i nie powinien być stosowany do natychmiastowego łagodzenia problemów z oddychaniem (tj. jako lek ratunkowy).
Natychmiastowe reakcje nadwrażliwości
Należy poinformować pacjentów, że po podaniu produktu SPIRIVA 9mcg Handihaler może wystąpić anafilaksja, obrzęk naczynioruchowy (w tym obrzęk warg, języka lub gardła), pokrzywka, wysypka, skurcz oskrzeli lub świąd. Należy doradzić pacjentowi, aby natychmiast przerwał leczenie i skonsultował się z lekarzem w przypadku pojawienia się któregokolwiek z tych objawów.
Paradoksalny skurcz oskrzeli
Poinformuj pacjentów, że produkt SPIRIVA HANDIHALER może wywołać paradoksalny skurcz oskrzeli. Należy poinformować pacjentów, że jeśli wystąpi paradoksalny skurcz oskrzeli, należy przerwać stosowanie produktu SPIRIVA HANDIHALER.
Pogorszenie jaskry wąskiego kąta
Należy poinstruować pacjentów, aby zwracali uwagę na oznaki i objawy jaskry z wąskim kątem przesączania (np. ból oka lub dyskomfort, niewyraźne widzenie, aureole wzrokowe lub kolorowe obrazy w połączeniu z zaczerwienieniem oczu spowodowanym przekrwieniem spojówki i obrzękiem rogówki). Należy poinstruować pacjentów, aby niezwłocznie skonsultowali się z lekarzem w przypadku pojawienia się któregokolwiek z tych objawów.
Należy poinformować pacjentów, że należy uważać, aby proszek nie dostał się do oczu, ponieważ może to spowodować niewyraźne widzenie i rozszerzenie źrenic.
Ponieważ podczas stosowania produktu SPIRIVA Handihaler mogą wystąpić zawroty głowy i niewyraźne widzenie, należy ostrzec pacjentów przed wykonywaniem takich czynności, jak prowadzenie pojazdu lub obsługa urządzeń lub maszyn.
Pogorszenie zatrzymania moczu
Należy poinstruować pacjentów, aby zwracali uwagę na oznaki i objawy zatrzymania moczu (np. trudności w oddawaniu moczu, bolesne oddawanie moczu). Należy poinstruować pacjentów, aby w przypadku pojawienia się któregokolwiek z tych objawów lub objawów natychmiast skonsultowali się z lekarzem.
Instrukcja podawania SPIRIVA HANDIHALER
Poinstruuj pacjentów, jak prawidłowo podawać kapsułki SPIRIVA 9mcg za pomocą urządzenia HANDIHALER [patrz INFORMACJA O PACJENCIE ]. Należy poinstruować pacjentów, że kapsułki SPIRIVA 9mcg należy podawać wyłącznie za pomocą urządzenia HANDIHALER, a urządzenie HANDIHALER nie powinno być używane do podawania innych leków. Należy przypomnieć pacjentom, że zawartość kapsułek SPIRIVA 9mcg jest przeznaczona wyłącznie do inhalacji doustnej i nie wolno jej połykać.
Należy poinstruować pacjentów, aby zawsze przechowywali kapsułki SPIRIVA 9mcg w zamkniętych blistrach i aby wyjęli tylko jedną kapsułkę SPIRIVA bezpośrednio przed użyciem, w przeciwnym razie jej skuteczność może być zmniejszona. Należy poinstruować pacjentów, aby wyrzucili niewykorzystane dodatkowe kapsułki SPIRIVA, które są wystawione na działanie powietrza (tj. nieprzeznaczone do natychmiastowego użycia).
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Nie zaobserwowano dowodów na rakotwórczość w 104-tygodniowym badaniu inhalacyjnym u szczurów przy dawkach tiotropium do 59 μg/kg/dobę, w 83-tygodniowym badaniu inhalacyjnym u samic myszy przy dawkach do 145 μg/kg/dobę oraz 101-tygodniowe badanie inhalacji u samców myszy w dawkach do 2 mcg/kg/dzień. Dawki te odpowiadają odpowiednio około 30, 40 i 0,5-krotności zalecanej dziennej dawki wziewnej dla człowieka (MRHDID) w przeliczeniu na mcg/m2.
Bromek tiotropiowy nie wykazał działania mutagennego ani klastogennego w następujących testach: test mutacji genów bakterii, test mutagenezy komórek chomika chińskiego V79, testy aberracji chromosomowych w ludzkich limfocytach in vitro i tworzenia mikrojąder u myszy in vivo oraz nieplanowana synteza DNA w pierwotne hepatocyty szczura in vitro.
szczurów po podaniu wziewnych dawek tiotropium 78 µg/kg/dobę lub większych (około 40-krotność MRHDID w przeliczeniu na µg/m2) zaobserwowano zmniejszenie liczby ciałek żółtych i odsetka implantów. Nie zaobserwowano takich efektów przy 9 mcg/kg/dzień (około 5-krotność MRHDID na podstawie mcg/m2). Jednakże wskaźnik płodności nie uległ zmianie przy dawkach wziewnych do 1689 mcg/kg/dobę (około 910-krotność MRHDID na podstawie mcg/m2).
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
Ograniczone dane dotyczące stosowania produktu SPIRIVA 9mcg HANDIHALER w czasie ciąży u ludzi są niewystarczające, aby poinformować o związanym z lekiem ryzyku wystąpienia działań niepożądanych związanych z ciążą. Na podstawie badań dotyczących reprodukcji na zwierzętach nie zaobserwowano żadnych nieprawidłowości strukturalnych, gdy tiotropium podawano wziewnie ciężarnym szczurom i królikom w okresie organogenezy w dawkach, odpowiednio, 790 i 8-krotności maksymalnej zalecanej dobowej dawki wziewnej dla ludzi (MRHDID). U szczurów i królików, którym podawano tiotropium w dawkach toksycznych dla matki odpowiednio 430-krotnie i 40-krotnie większych od MRHDID, obserwowano zwiększoną utratę po implantacji [patrz Dane ].
Szacowane ryzyko tła poważnych wad wrodzonych i poronienia dla wskazanej populacji jest nieznane. Wszystkie ciąże wiążą się z ryzykiem wady wrodzonej, utraty lub innych niekorzystnych skutków. W ogólnej populacji Stanów Zjednoczonych szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2% do 4% i 15% do 20%.
Dane
Dane zwierząt
2 oddzielnych badaniach dotyczących rozwoju zarodkowo-płodowego ciężarne szczury i króliki otrzymywały tiotropium w okresie organogenezy w dawkach odpowiednio do około 790 i 8-krotności MRHDID (w przeliczeniu na mcg/m2 w dawkach wziewnych 1471 i 7 mcg/kg). /dzień odpowiednio u szczurów i królików). U szczurów i królików nie zaobserwowano dowodów na nieprawidłowości strukturalne. Jednak u szczurów tiotropium powodowało resorpcję płodu, utratę miotu, zmniejszenie liczby żywych młodych przy urodzeniu i średniej masy młodych oraz opóźnienie dojrzewania płciowego młodych przy dawkach tiotropium około 40 razy większych niż MRHDID (w mcg/m2 na podstawie dawki wziewnej dla matki wynoszącej 78 mikrogramów/kg/dobę). U królików tiotropium powodowało zwiększenie utraty po implantacji przy dawce tiotropium około 430 razy większej niż MRHDID (w przeliczeniu na mcg/m2 przy dawce wziewnej 400 mcg/kg/dobę u matki). Takich efektów nie obserwowano przy odpowiednio około 5 i 95-krotności MRHDID (w przeliczeniu na mcg/m2 przy dawkach wziewnych 9 i 88 mcg/kg/dobę odpowiednio u szczurów i królików).
Laktacja
Podsumowanie ryzyka
Brak danych dotyczących obecności tiotropium w mleku ludzkim, wpływu na niemowlę karmione piersią lub wpływu na produkcję mleka. Tiotropium jest obecne w mleku karmiących szczurów; jednak ze względu na specyficzne gatunkowo różnice w fizjologii laktacji, kliniczne znaczenie tych danych nie jest jasne [patrz Dane ]. Należy wziąć pod uwagę korzyści rozwojowe i zdrowotne wynikające z karmienia piersią, a także kliniczne zapotrzebowanie matki na produkt SPIRIVA 9mcg Handihaler oraz wszelkie potencjalne niekorzystne skutki stosowania produktu SPIRIVA Handihaler na dziecko karmione piersią lub związane z tym schorzeniem matki.
Dane
Dystrybucję bromku tiotropium do mleka badano po jednorazowym podaniu dożylnym 10 mg/kg karmiącym szczurom. Tiotropium i (lub) jego metabolity są obecne w mleku karmiących samic szczurów w stężeniach wyższych niż stężenia w osoczu.
Zastosowanie pediatryczne
SPIRIVA HANDIHALER nie jest wskazany do stosowania u dzieci. Bezpieczeństwo i skuteczność produktu SPIRIVA 9mcg HANDIHALER u dzieci nie zostały ustalone.
Zastosowanie geriatryczne
Na podstawie dostępnych danych nie jest uzasadnione dostosowanie dawkowania produktu SPIRIVA HANDIHALER u pacjentów w podeszłym wieku [patrz FARMAKOLOGIA KLINICZNA ].
Spośród całkowitej liczby pacjentów, którzy otrzymywali produkt SPIRIVA 9 mcg HANDIHALER w rocznych badaniach klinicznych, 426 było w wieku
Zaburzenia czynności nerek
Pacjenci z umiarkowanymi lub ciężkimi zaburzeniami czynności nerek (klirens kreatyniny DAWKOWANIE I SPOSÓB PODAWANIA , OSTRZEŻENIA I ŚRODKI , oraz FARMAKOLOGIA KLINICZNA ].
Niewydolność wątroby
Nie badano wpływu zaburzeń czynności wątroby na farmakokinetykę tiotropium.
PRZEDAWKOWAĆ
Wysokie dawki tiotropium mogą wywoływać oznaki i objawy antycholinergiczne. Jednak nie stwierdzono ogólnoustrojowych działań niepożądanych antycholinergicznych po podaniu pojedynczej dawki wziewnej do 282 mcg tiotropium u 6 zdrowych ochotników. W badaniu z udziałem 12 zdrowych ochotników zaobserwowano obustronne zapalenie spojówek i suchość w ustach po powtarzanej raz dziennie inhalacji 141 mcg tiotropium.
Leczenie przedawkowania polega na odstawieniu produktu SPIRIVA Handihaler wraz z wdrożeniem odpowiedniego leczenia objawowego i (lub) podtrzymującego.
Przypadkowe spożycie
Ostre zatrucie przez nieumyślne doustne przyjęcie kapsułek produktu SPIRIVA jest mało prawdopodobne, ponieważ nie są one dobrze wchłaniane ogólnoustrojowo.
Po wprowadzeniu produktu do obrotu zgłoszono przypadek przedawkowania. Zgłoszono, że pacjentka wdychała 30 kapsułek w ciągu 2,5 dnia i rozwinęła zmiany stanu psychicznego, drżenie, ból brzucha i ciężkie zaparcia. Pacjentkę hospitalizowano, SPIRIVA HANDIHALER odstawiono, a zaparcia leczono lewatywą. Pacjent wyzdrowiał i został wypisany tego samego dnia.
PRZECIWWSKAZANIA
SPIRIVA 9mcg Handihaler jest przeciwwskazany u pacjentów z nadwrażliwością na tiotropium, ipratropium lub którykolwiek składnik tego produktu [patrz OSTRZEŻENIA I ŚRODKI ]. W badaniach klinicznych i po wprowadzeniu do obrotu produktu SPIRIVA 9mcg Handihaler zgłaszano natychmiastowe reakcje nadwrażliwości, w tym obrzęk naczynioruchowy (w tym obrzęk warg, języka lub gardła), świąd lub wysypkę [patrz OSTRZEŻENIA I ŚRODKI ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Tiotropium to długo działający środek przeciwmuskarynowy, często określany jako antycholinergiczny. Wykazuje podobne powinowactwo do podtypów receptorów muskarynowych, od M1 do M5. W drogach oddechowych wykazuje działanie farmakologiczne poprzez hamowanie receptorów M3 w mięśniach gładkich, co prowadzi do rozszerzenia oskrzeli. Wykazano konkurencyjny i odwracalny charakter antagonizmu z receptorami pochodzenia ludzkiego i zwierzęcego oraz preparatami izolowanych narządów. W badaniach przedklinicznych in vitro oraz in vivo zapobieganie skurczowi oskrzeli wywołanemu przez metacholinę było zależne od dawki i trwało dłużej niż 24 godziny. Rozszerzenie oskrzeli po inhalacji tiotropium jest głównie efektem miejscowo specyficznym.
Farmakodynamika
Elektrofizjologia serca
wieloośrodkowym, randomizowanym, podwójnie zaślepionym badaniu z zastosowaniem suchego proszku tiotropium do inhalacji, w którym wzięło udział 198 pacjentów z POChP, liczba pacjentów ze zmianami odstępu QT skorygowanego względem wartości początkowej od 30 do 60 ms była wyższa w grupie produktu SPIRIVA 9mcg Handihaler w porównaniu z placebo. Ta różnica była widoczna przy użyciu korekcji zarówno Bazetta (QTcB) [20 (20%) pacjentów vs. 12 (12%) pacjentów], jak i Fredericia (QTcF) [16 (16%) pacjentów vs. 1 (1%) pacjentów] QT dla tętna. Żaden pacjent w żadnej grupie nie miał QTcB ani QTcF >500 ms. Inne badania kliniczne produktu SPIRIVA HANDIHALER nie wykazały wpływu leku na odstępy QTc.
Wpływ suchego proszku tiotropium do inhalacji na odstęp QT oceniano również w randomizowanym, krzyżowym badaniu kontrolowanym placebo i dodatnim, obejmującym 53 zdrowych ochotników. Badani otrzymywali suchy proszek tiotropium do inhalacji 18 mcg, 54 mcg (3-krotność zalecanej dawki) lub placebo przez 12 dni. Ocenę EKG przeprowadzono na początku i podczas przerwy w dawkowaniu po pierwszej i ostatniej dawce badanego leku. W porównaniu z placebo, maksymalna średnia zmiana odstępu QTc od wartości początkowej w badaniu wyniosła 3,2 ms i 0,8 ms dla suchego proszku tiotropium do inhalacji odpowiednio 18 µg i 54 µg. U żadnego pacjenta nie wystąpił nowy początek QTc >500 ms lub zmiany QTc od wartości początkowej ≥60 ms.
Farmakokinetyka
Tiotropium podaje się poprzez inhalację suchego proszku. Niektóre z opisanych poniżej danych farmakokinetycznych uzyskano przy dawkach wyższych niż zalecane w terapii. Specjalne badanie farmakokinetyczne u pacjentów z POChP oceniające tiotropium podawane raz dziennie z inhalatora RESPIMAT (5 µg) oraz jako proszek do inhalacji (18 µg) z urządzenia HANDIHALER wykazało podobną ekspozycję ogólnoustrojową na oba produkty.
Wchłanianie
Po inhalacji suchego proszku przez młodych zdrowych ochotników bezwzględna biodostępność 19,5% sugeruje, że frakcja docierająca do płuc jest wysoce biodostępna. Doustne roztwory tiotropium mają bezwzględną biodostępność 2-3%. Nie oczekuje się, aby pokarm wpływał na wchłanianie tiotropium. Maksymalne stężenie tiotropium w osoczu zaobserwowano 7 minut po inhalacji.
Dystrybucja
Tiotropium wiąże się w 72% z białkami osocza i ma objętość dystrybucji 32 l/kg po podaniu dożylnym młodym zdrowym ochotnikom. Miejscowe stężenia w płucach nie są znane, ale sposób podawania sugeruje znacznie wyższe stężenia w płucach. Badania na szczurach wykazały, że tiotropium nie przenika łatwo przez barierę krew-mózg.
Eliminacja
Końcowy okres półtrwania tiotropium u pacjentów z POChP po inhalacji 5 µg tiotropium raz na dobę wynosił około 25 godzin. Całkowity klirens wynosił 880 ml/min po podaniu dożylnym młodym zdrowym ochotnikom. Po przewlekłej, raz na dobę inhalacji suchego proszku przez pacjentów z POChP, farmakokinetyczny stan stacjonarny został osiągnięty do dnia 7 bez kumulacji w późniejszym okresie.
Metabolizm
Stopień metabolizmu jest niewielki. Wynika to z wydalania z moczem 74% niezmienionej substancji po podaniu dożylnym młodym zdrowym ochotnikom. Ester tiotropium jest nieenzymatycznie rozszczepiany do alkoholu N-metyloskopiny i kwasu ditienyloglikolowego, z których żaden nie wiąże się z receptorami muskarynowymi.
Eksperymenty in vitro z ludzkimi mikrosomami wątroby i ludzkimi hepatocytami sugerują, że część podanej dawki (74% dawki dożylnej jest wydalana w postaci niezmienionej z moczem, pozostawiając 25% do metabolizmu) jest metabolizowana przez zależne od cytochromu P450 utlenianie, a następnie sprzęganie z glutationem do różnych metabolitów fazy II. Ten szlak enzymatyczny może być hamowany przez inhibitory CYP450 2D6 i 3A4, takie jak chinidyna, ketokonazol i gestoden. Zatem CYP450 2D6 i 3A4 biorą udział w szlaku metabolicznym, który jest odpowiedzialny za eliminację niewielkiej części podanej dawki. Badania in vitro z użyciem mikrosomów wątroby ludzkiej wykazały, że tiotropium w stężeniach ponadterapeutycznych nie hamuje CYP450 1A1, 1A2, 2B6, 2C9, 2C19, 2D6, 2E1 ani 3A4.
Wydalanie
Bromek tiotropium podawany dożylnie jest wydalany głównie w postaci niezmienionej z moczem (74%). Po inhalacji suchego proszku pacjentom z POChP w stanie stacjonarnym wydalanie z moczem wynosiło 7% (1,3 mcg) niezmienionej dawki w ciągu 24 godzin. Klirens nerkowy tiotropium przewyższa klirens kreatyniny, co wskazuje na wydzielanie do moczu.
Określone populacje
Pacjenci geriatryczni
Jak oczekiwano w przypadku wszystkich leków wydalanych głównie przez nerki, zaawansowany wiek był związany ze zmniejszeniem klirensu nerkowego tiotropium (365 ml/min u pacjentów z POChP w wieku
Zaburzenia czynności nerek
Po 4 tygodniach stosowania produktu SPIRIVA 9 mcg HANDIHALER lub produktu SPIRIVA 9 mcg RESPIMAT raz na dobę u pacjentów z POChP, łagodne zaburzenia czynności nerek (klirens kreatyniny 60-
Niewydolność wątroby
Nie badano wpływu zaburzeń czynności wątroby na farmakokinetykę tiotropium.
Interakcje leków
Przeprowadzono badanie interakcji z tiotropium (14,4 µg wlew dożylny trwający 15 minut) i cymetydyną 400 mg trzy razy na dobę lub ranitydyną 300 mg raz na dobę. Jednoczesne podawanie cymetydyny z tiotropium powodowało 20% wzrost AUC0-4h, 28% zmniejszenie klirensu nerkowego tiotropium i brak istotnej zmiany Cmax i ilości wydalanej z moczem w ciągu 96 godzin. Jednoczesne podawanie tiotropium z ranitydyną nie wpływało na farmakokinetykę tiotropium.
Nie stwierdzono, aby często stosowane jednocześnie leki (długodziałający agoniści receptorów beta2-adrenergicznych (LABA), kortykosteroidy wziewne (ICS)) stosowane przez pacjentów z POChP zmieniały ekspozycję na tiotropium.
Studia kliniczne
Program rozwoju klinicznego produktu SPIRIVA 9mcg HANDIHALER (proszek do inhalacji bromku tiotropium) składał się z sześciu badań fazy 3 z udziałem 2663 pacjentów z POChP (1308 otrzymujących produkt SPIRIVA 9mcg HANDIHALER): dwa roczne badania kontrolowane placebo, dwa 6-miesięczne badania kontrolowane placebo badania i dwa roczne badania kontrolowane ipratropium. Do badań tych włączono pacjentów, u których klinicznie rozpoznano POChP, byli w wieku 40 lat lub więcej, palili papierosy w wywiadzie dłuższym niż 10 paczkolat, mieli natężoną objętość wydechową w ciągu jednej sekundy (FEV1) mniejszą lub równą 60% lub 65% przewidywanych i stosunek FEV1/FVC mniejszy lub równy 0,7.
W badaniach tych produkt SPIRIVA HANDIHALER, podawany raz na dobę, rano, zapewniał poprawę czynności płuc (FEV1), ze szczytowym działaniem występującym w ciągu 3 godzin po podaniu pierwszej dawki.
Dwa dodatkowe badania oceniały zaostrzenia: 6-miesięczne, randomizowane, podwójnie zaślepione, kontrolowane placebo, wieloośrodkowe badanie kliniczne obejmujące 1829 pacjentów z POChP w warunkach US Veterans Affairs i 4-letnie, randomizowane, podwójnie zaślepione, kontrolowane placebo, wieloośrodkowe badanie kliniczne obejmujące 5992 pacjentów z POChP. Długoterminowy wpływ na czynność płuc i inne wyniki oceniano również w 4-letnim wieloośrodkowym badaniu.
Efekty od 6 miesięcy do 1 roku na czynność płuc
rocznych badaniach kontrolowanych placebo średnia poprawa FEV1 po 30 minutach wyniosła 0,13 litra (13%) ze szczytową poprawą o 0,24 litra (24%) w stosunku do wartości wyjściowej po pierwszej dawce (dzień 1.). Dalszą poprawę FEV1 i natężonej pojemności życiowej (FVC) obserwowano po osiągnięciu farmakodynamicznego stanu stacjonarnego do dnia 8 przy leczeniu raz na dobę. Średnia szczytowa poprawa FEV1 w stosunku do wartości wyjściowej wyniosła 0,28 do 0,31 litra (28% do 31%), po 1 tygodniu (dzień 8) leczenia raz na dobę. Poprawa czynności płuc utrzymywała się przez 24 godziny po podaniu pojedynczej dawki i konsekwentnie utrzymywała się przez 1 rok leczenia bez oznak tolerancji.
dwóch 6-miesięcznych badaniach kontrolowanych placebo seryjne oceny spirometryczne były wykonywane w ciągu dnia w Badaniu A (12 godzin) i ograniczone do 3 godzin w Badaniu B. Seryjne wartości FEV1 w ciągu 12 godzin (Badanie A) przedstawiono w Rycina 1. Badania te dodatkowo potwierdzają poprawę czynności płuc (FEV1) po zastosowaniu produktu SPIRIVA 9mcg HANDIHALER, która utrzymywała się przez cały okres obserwacji spirometrycznej. Skuteczność utrzymywała się przez 24 godziny po podaniu przez 6-miesięczny okres leczenia.
Rycina 1: Średnia FEV1 w czasie (przed i po podaniu badanego leku) w dniach 1 i 169 w badaniu A (sześciomiesięczne badanie kontrolowane placebo)* 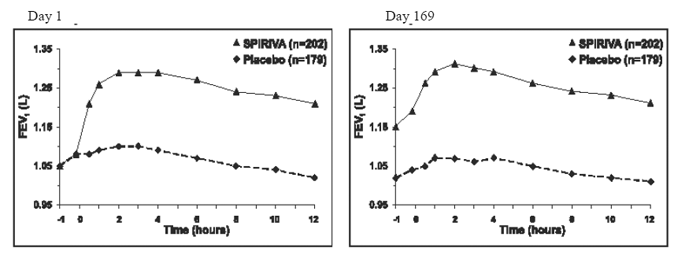
*Średnie skorygowane ze względu na środek, leczenie i efekt wyjściowy. W 169. dniu badanie ukończyło łącznie 183 i 149 pacjentów odpowiednio w grupach SPIRIVA HANDIHALER i placebo. Dane dla pozostałych pacjentów zostały imputowane przy użyciu ostatniej obserwacji lub najmniej korzystnej obserwacji przeniesionej.
Wyniki każdego z rocznych badań kontrolowanych ipratropium były podobne do wyników rocznych badań kontrolowanych placebo. Wyniki jednej z tych prób przedstawiono na rysunku 2.
Rycina 2: Średnia wartość FEV1 w czasie (0 do 6 godzin po podaniu dawki) w dniach 1 i 92, odpowiednio dla jednego z dwóch badań kontrolowanych ipratropium* 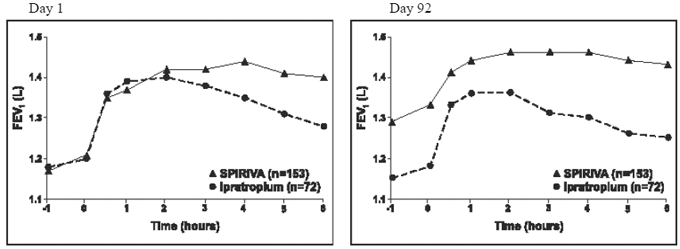
*Średnie skorygowane ze względu na środek, leczenie i efekt wyjściowy. W 92. dniu (pierwszorzędowy punkt końcowy) łącznie 151 i 69 pacjentów odpowiednio w grupach SPIRIVA HANDIHALER i ipratropium ukończyło 3 miesiące obserwacji. Dane dla pozostałych pacjentów zostały imputowane przy użyciu ostatniej obserwacji lub najmniej korzystnej obserwacji przeniesionej.
W randomizowanym, kontrolowanym placebo badaniu klinicznym z udziałem 105 pacjentów z POChP wykazano, że rozszerzenie oskrzeli utrzymywało się przez 24-godzinny odstęp pomiędzy dawkami w porównaniu z placebo, niezależnie od tego, czy produkt leczniczy SPIRIVA 9mcg Handihaler był podawany rano, czy wieczorem.
ciągu każdego tygodnia rocznego okresu leczenia w dwóch badaniach kontrolowanych placebo u pacjentów przyjmujących produkt SPIRIVA 9mcg HANDIHALER zmniejszono zapotrzebowanie na doraźne stosowanie krótko działających beta2-mimetyków. W jednym z dwóch 6-miesięcznych badań wykazano zmniejszenie stosowania doraźnych krótko działających beta2-mimetyków w porównaniu z placebo.
4-letnie efekty na czynność płuc
Przeprowadzono 4-letnie, randomizowane, podwójnie zaślepione, kontrolowane placebo, wieloośrodkowe badanie kliniczne z udziałem 5992 pacjentów z POChP w celu oceny długoterminowego wpływu produktu SPIRIVA HANDIHALER na progresję choroby (tempo spadku FEV1). Pacjenci mogli stosować wszystkie leki działające na układ oddechowy (w tym krótko i długo działające beta-agoniści, steroidy wziewne i ogólnoustrojowe oraz teofiliny) inne niż wziewne leki antycholinergiczne. Pacjenci byli w wieku od 40 do 88 lat, 75% płci męskiej i 90% rasy kaukaskiej, z rozpoznaniem POChP i średnim FEV1 przed lekiem rozszerzającym oskrzela wynoszącym 39% wartości należnej (zakres = 9% do 76%) w momencie włączenia do badania. Nie było różnicy między grupami w żadnym z równorzędnych pierwszorzędowych punktów końcowych skuteczności, rocznym tempie spadku FEV1 przed i po podaniu leku rozszerzającego oskrzela, co wykazano przez podobne spadki spadku FEV1 w czasie (Rycina 3).
Produkt SPIRIVA HANDIHALER utrzymał poprawę minimalnego (przed podaniem dawki) FEV1 (dostosowane średnie w czasie: 87 do 103 ml) przez 4 lata badania (ryc. 3).
Rysunek 3: Minimalne (przed dawką) średnie wartości FEV1 w każdym punkcie czasowym 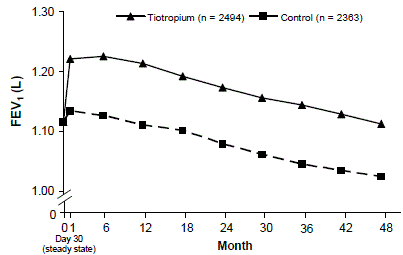
Do oszacowania średnich zastosowano ANOVA z powtarzanym pomiarem. Średnie są dostosowywane do pomiarów podstawowych. Minimalna wartość wyjściowa FEV1 (obserwowana średnia) = 1,12. Do analizy włączono pacjentów z ≥3 akceptowalnymi testami czynności płuc po 30. dniu i niebrakującą wartością wyjściową.
Zaostrzenia
Wpływ produktu SPIRIVA 9mcg Handihaler na zaostrzenia POChP oceniano w dwóch badaniach klinicznych: 4-letnim badaniu klinicznym opisanym powyżej oraz 6-miesięcznym badaniu klinicznym obejmującym 1829 pacjentów z POChP w środowisku Veterans Affairs. W 6-miesięcznym badaniu zaostrzenia POChP zdefiniowano jako zespół objawów ze strony układu oddechowego (nasilenie lub nowy początek) więcej niż jednego z następujących: kaszel, plwocina, świszczący oddech, duszność lub ucisk w klatce piersiowej trwający co najmniej 3 dni wymagające leczenia antybiotykami, sterydami ogólnoustrojowymi lub hospitalizacji. Populacja była w wieku od 40 do 90 lat, 99% mężczyzn, 91% rasy kaukaskiej i POChP ze średnim oczekiwanym procentem FEV1 przed rozszerzeniem oskrzeli wynoszącym 36% (zakres = 8% do 93%). Pacjenci mogli stosować leki działające na układ oddechowy (w tym krótko i długo działające beta-agoniści, steroidy wziewne i ogólnoustrojowe oraz teofiliny) inne niż wziewne leki antycholinergiczne. W 6-miesięcznym badaniu równorzędnymi pierwszorzędowymi punktami końcowymi był odsetek pacjentów z zaostrzeniem POChP oraz odsetek pacjentów hospitalizowanych z powodu zaostrzenia POChP. Produkt SPIRIVA 9mcg HANDIHALER znacząco zmniejszył odsetek pacjentów z POChP, u których wystąpiły zaostrzenia w porównaniu z placebo (odpowiednio 27,9% vs 32,3%; iloraz szans (OR) (tiotropium/placebo) = 0,81; 95% CI = 0,66, 0,99; p = 0,037 ). Odsetek pacjentów hospitalizowanych z powodu zaostrzeń POChP u pacjentów stosujących produkt SPIRIVA 9mcg HANDIHALER w porównaniu z placebo wynosił odpowiednio 7,0% vs. 9,5%; LUB = 0,72; 95% CI = 0,51, 1,01; p = 0,056.
Zaostrzenia oceniano jako drugorzędowy punkt końcowy w 4-letnim wieloośrodkowym badaniu. W tym badaniu zaostrzenia POChP zdefiniowano jako nasilenie lub pojawienie się więcej niż jednego z następujących objawów ze strony układu oddechowego (kaszel, plwocina, ropna plwocina, świszczący oddech, duszność) trwające trzy lub więcej dni wymagające leczenia antybiotykami i/lub steroidy ogólnoustrojowe (doustne, domięśniowe lub dożylne). Produkt SPIRIVA HANDIHALER istotnie zmniejszył ryzyko zaostrzenia o 14% (współczynnik ryzyka (HR) = 0,86; 95% CI = 0,81, 0,91; p
Wszechstronna śmiertelność
opisanym powyżej 4-letnim kontrolowanym placebo badaniu dotyczącym czynności płuc oceniano śmiertelność z jakiejkolwiek przyczyny w porównaniu z placebo. Nie było istotnych różnic w śmiertelności z jakiejkolwiek przyczyny między produktem SPIRIVA 9mcg Handihaler a placebo.
Śmiertelność ogólną produktu SPIRIVA HANDIHALER porównano również z tiotropium w postaci aerozolu do inhalacji 5 µg (SPIRIVA RESPIMAT 5 µg) w dodatkowym długoterminowym, randomizowanym, podwójnie ślepym, podwójnie pozorowanym badaniu z aktywną kontrolą z okresem obserwacji do 3 lat. Śmiertelność z jakiejkolwiek przyczyny była podobna między produktami SPIRIVA 9mcg HANDIHALER i SPIRIVA RESPIMAT.
INFORMACJA O PACJENCIE
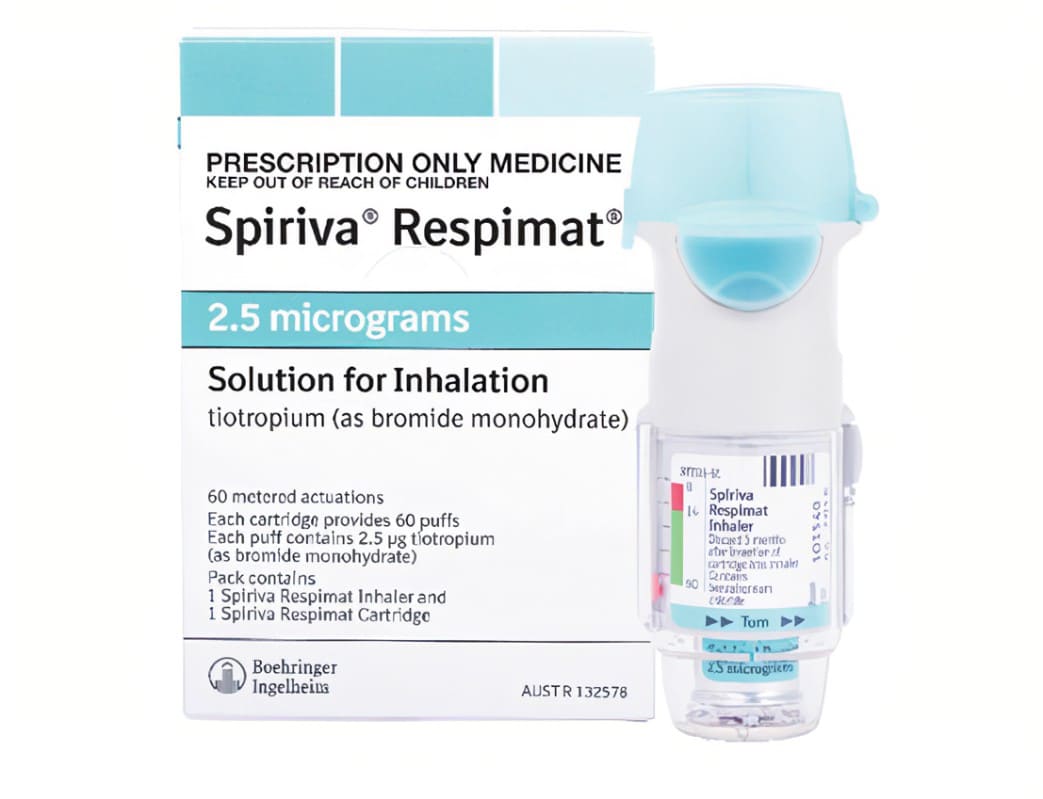
SPIRIVA 9mcgR® (speh REE vah) HANDIHALER® (bromek tiotropium) Proszek do inhalacji, do inhalacji doustnej
NIE połykać kapsułek SPIRIVA.
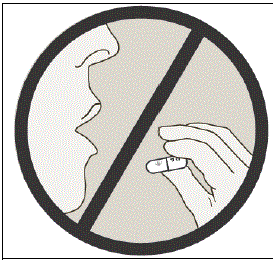
Ważna informacja: Nie połykać kapsułek SPIRIVA. Kapsułki SPIRIVA 9mcg należy stosować wyłącznie z urządzeniem HANDIHALER i wdychać przez usta (inhalacja doustna).
Przeczytaj informacje dołączone do urządzenia SPIRIVA Handihaler, zanim zaczniesz go używać i za każdym razem, gdy uzupełniasz receptę. Mogą pojawić się nowe informacje. Ta ulotka nie zastępuje rozmowy z lekarzem na temat stanu zdrowia lub leczenia.
Co to jest HANDIHALER SPIRIVA?
- SPIRIVA HANDIHALER to lek na receptę stosowany codziennie (lek podtrzymujący) w celu kontrolowania objawów przewlekłej obturacyjnej choroby płuc (POChP), w tym przewlekłego zapalenia oskrzeli i rozedmy płuc.
- SPIRIVA HANDIHALER pomaga poprawić pracę płuc przez 24 godziny. SPIRIVA 9mcg HANDIHALER rozluźnia drogi oddechowe i pomaga utrzymać je otwarte. Pierwszego dnia możesz poczuć, że łatwiej jest oddychać, ale odczucie pełnych efektów leku może zająć więcej czasu. SPIRIVA HANDIHALER działa najlepiej i może ułatwić oddychanie podczas codziennego stosowania.
- SPIRIVA 9mcg HANDIHALER zmniejsza prawdopodobieństwo zaostrzeń i nasilenia objawów POChP (zaostrzenia POChP). Zaostrzenie POChP definiuje się jako nasilenie lub pojawienie się więcej niż jednego objawu POChP, takiego jak kaszel, śluz, duszność i świszczący oddech, które wymagają zastosowania leków wykraczających poza lek ratunkowy.
SPIRIVA 9mcg HANDIHALER nie jest lekiem ratunkowym i nie należy go stosować w leczeniu nagłych problemów z oddychaniem. Lekarz może przepisać inny lek w przypadku nagłych problemów z oddychaniem.
Nie wiadomo, czy SPIRIVA 9mcg Handihaler jest bezpieczny i skuteczny u dzieci.
Kto nie powinien przyjmować SPIRIVA 9mcg Handihaler?
Nie używaj SPIRIVA 9mcg Handihaler, jeśli:
- jesteś uczulony na tiotropium, ipratropium (Atrovent®) lub którykolwiek ze składników preparatu SPIRIVA 9mcg Handihaler. Pełny wykaz składników leku SPIRIVA 9mcg Handihaler znajduje się na końcu tej ulotki.
Objawy ciężkiej reakcji alergicznej na SPIRIVA 9mcg Handihaler mogą obejmować:
- wypukłe czerwone plamy na skórze (pokrzywka)
- swędzący
- wysypka
- obrzęk twarzy, warg, języka i gardła, który może powodować trudności w oddychaniu lub połykaniu
W przypadku wystąpienia tych objawów reakcji alergicznej należy przerwać stosowanie leku SPIRIVA HANDIHALER i natychmiast skontaktować się z lekarzem lub udać się na izbę przyjęć najbliższego szpitala.
O czym powinienem powiedzieć lekarzowi przed zastosowaniem leku SPIRIVA HANDIHALER?
Przed przyjęciem leku SPIRIVA HANDIHALER należy poinformować lekarza o wszystkich swoich schorzeniach, w tym o:
- mają problemy z nerkami.
- mieć jaskrę. SPIRIVA HANDIHALER może pogorszyć jaskrę.
- masz powiększoną prostatę, problemy z oddawaniem moczu lub niedrożność pęcherza. SPIRIVA 9mcg HANDIHALER może pogorszyć te problemy.
- są w ciąży lub planują zajść w ciążę. Nie wiadomo, czy SPIRIVA HANDIHALER może zaszkodzić nienarodzonemu dziecku.
- karmisz piersią lub planujesz karmić piersią. Nie wiadomo, czy lek SPIRIVA HANDIHALER przenika do mleka matki. Wspólnie z lekarzem zdecydujecie, czy lek SPIRIVA 9mcg Handihaler jest odpowiedni dla kobiety podczas karmienia piersią.
- mają ciężką alergię na białka mleka. Zapytaj swojego lekarza, jeśli nie jesteś pewien.
Poinformuj lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty oraz krople do oczu, witaminy i suplementy ziołowe. Niektóre inne leki lub suplementy mogą wpływać na działanie leku SPIRIVA HANDIHALER. SPIRIVA 9mcg HANDIHALER to lek antycholinergiczny. Podczas stosowania leku SPIRIVA 9mcg Handihaler nie należy przyjmować innych leków przeciwcholinergicznych, w tym ipratropium. Zapytaj swojego lekarza lub farmaceutę, jeśli nie jesteś pewien, czy któryś z twoich leków jest antycholinergiczny.
Poznaj leki, które przyjmujesz. Miej przy sobie listę swoich leków, aby pokazać lekarzowi i farmaceucie, kiedy otrzymasz nowy lek.
Jak stosować SPIRIVA 9mcg Handihaler?
- Używaj SPIRIVA 9mcg Handihaler dokładnie zgodnie z zaleceniami. Używaj SPIRIVA HANDIHALER jeden raz dziennie.
- Przed zastosowaniem leku SPIRIVA Handihaler należy zapoznać się z „Instrukcją użycia” na końcu tej ulotki. Porozmawiaj z lekarzem, jeśli nie rozumiesz instrukcji.
- Nie połykać kapsułek SPIRIVA 9mcg.
- Z urządzeniem HANDIHALER należy używać wyłącznie kapsułek SPIRIVA 9mcg.
- Nie używać urządzenia HANDIHALER do przyjmowania innych leków.
- SPIRIVA 9mcg HANDIHALER występuje w postaci proszku w kapsułce SPIRIVA 9mcg, która pasuje do urządzenia HANDIHALER. Każda kapsułka SPIRIVA, zawierająca tylko niewielką ilość proszku SPIRIVA, to jedna pełna dawka leku.
- Oddzielić jeden blister od blistra. Następnie wyjmij jedną z kapsułek SPIRIVA 9mcg z blistra tuż przed jej użyciem.
- Po przebiciu kapsułki należy przyjąć pełną dawkę preparatu SPIRIVA HANDIHALER poprzez dwukrotne wdychanie proszku doustnie za pomocą urządzenia HANDIHALER (zażyć 2 inhalacje z jednej kapsułki SPIRIVA). Zobacz "Instrukcja użycia" na końcu tej ulotki.
- Wyrzucić każdą kapsułkę SPIRIVA, która nie jest używana od razu po wyjęciu z opakowania blistrowego. Nie pozostawiaj kapsułek SPIRIVA otwartych na powietrze; mogą nie działać tak dobrze.
- Jeśli pominiesz dawkę, zażyj ją tak szybko, jak sobie przypomnisz. SPIRIVA HANDIHALER nie należy stosować częściej niż raz na 24 godziny. ? W przypadku zastosowania większej niż przepisana dawki leku SPIRIVA HANDIHALER należy skontaktować się z lekarzem lub centrum kontroli zatruć.
Czego powinienem unikać stosując SPIRIVA 9mcg HANDIHALER?
- Nie pozwól, aby proszek z kapsułki SPIRIVA dostał się do oczu. Twoje widzenie może stać się niewyraźne, a źrenica w oku może się powiększyć (rozszerzyć). Jeśli tak się stanie, skontaktuj się z lekarzem.
- SPIRIVA 9mcg Handihaler może powodować zawroty głowy i niewyraźne widzenie. W przypadku wystąpienia tych objawów należy zachować ostrożność podczas wykonywania czynności, takich jak prowadzenie samochodu lub obsługiwanie urządzeń lub innych maszyn.
Jakie są możliwe skutki uboczne SPIRIVA HANDIHALER?
SPIRIVA 9mcg Handihaler może powodować poważne skutki uboczne, w tym: Reakcję alergiczną. Objawy mogą obejmować:
- wypukłe czerwone plamy na skórze (pokrzywka)
- swędzący
- wysypka
- obrzęk warg, języka lub gardła, który może powodować trudności w oddychaniu lub połykaniu
W przypadku wystąpienia tych objawów reakcji alergicznej należy przerwać stosowanie leku SPIRIVA HANDIHALER i natychmiast skontaktować się z lekarzem lub udać się na izbę przyjęć najbliższego szpitala.
- Nagłe zwężenie i zablokowanie dróg oddechowych do płuc (skurcz oskrzeli) . Twój oddech nagle się pogarsza.
Jeśli wystąpią takie objawy skurczu oskrzeli, należy przerwać stosowanie leku SPIRIVA 9mcg Handihaler i natychmiast skontaktować się z lekarzem lub udać się na izbę przyjęć najbliższego szpitala.
- Nowe lub pogorszone zwiększone ciśnienie w oczach (ostra jaskra z wąskim kątem przesączania). Objawy ostrej jaskry z wąskim kątem mogą obejmować:
- ból oka
- rozmazany obraz
- widzenie aureoli (aureoli wizualnych) lub kolorowych obrazów wraz z czerwonymi oczami
Stosowanie wyłącznie kropli do oczu w celu leczenia tych objawów może nie działać. W przypadku wystąpienia tych objawów należy przerwać stosowanie leku SPIRIVA Handihaler i natychmiast skontaktować się z lekarzem.
- Nowe lub pogorszone zatrzymanie moczu. Objawy zablokowania pęcherza i (lub) przerostu prostaty mogą obejmować: trudności w oddawaniu moczu, bolesne oddawanie moczu.
W przypadku wystąpienia tych objawów zatrzymania moczu należy przerwać stosowanie leku SPIRIVA HANDIHALER i natychmiast skontaktować się z lekarzem.
Inne działania niepożądane związane ze stosowaniem SPIRIVA 9mcg Handihaler obejmują:
- zakażenia górnych dróg oddechowych
- suchość w ustach
- infekcja zatok
- ból gardła
- niespecyficzny ból w klatce piersiowej
- zakażenie dróg moczowych
- niestrawność
- katar
- zaparcie
- zwiększone tętno
- rozmazany obraz
To nie wszystkie możliwe działania niepożądane związane ze stosowaniem SPIRIVA HANDIHALER. Należy poinformować lekarza, jeśli wystąpią jakiekolwiek objawy niepożądane, które Cię niepokoją lub które nie ustępują.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać SPIRIVA HANDIHALER?
- Nie przechowywać kapsułek SPIRIVA w urządzeniu HANDIHALER.
- Kapsułki SPIRIVA należy przechowywać w szczelnie zamkniętym opakowaniu blistrowym w temperaturze pokojowej od 20°C do 25°C.
- Kapsułki SPIRIVA należy przechowywać z dala od ciepła i zimna (nie zamrażać).
- Kapsułki SPIRIVA 9mcg przechowywać w suchym miejscu. Wyrzuć wszelkie niewykorzystane kapsułki SPIRIVA 9mcg, które zostały otwarte na powietrze.
Zapytaj swojego lekarza lub farmaceutę, jeśli masz jakiekolwiek pytania dotyczące przechowywania kapsułek SPIRIVA 9mcg.
Kapsułki SPIRIVA HANDIHALER, SPIRIVA 9mcg i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Ogólne informacje o SPIRIVA HANDIHALER
Leki są czasami przepisywane do celów innych niż wymienione w ulotkach dla pacjenta. Nie należy stosować leku SPIRIVA 9mcg Handihaler do celów, do których nie został przepisany. Nie należy podawać leku SPIRIVA Handihaler innym osobom, nawet jeśli mają takie same objawy, jak u pacjenta. Może im to zaszkodzić.
Aby uzyskać więcej informacji o produkcie SPIRIVA HANDIHALER, porozmawiaj ze swoim lekarzem. Możesz poprosić swojego lekarza lub farmaceutę o informacje na temat produktu SPIRIVA 9mcg Handihaler, który jest przeznaczony dla pracowników służby zdrowia.
Aby uzyskać więcej informacji na temat produktu SPIRIVA 9mcg HANDIHALER, odwiedź stronę www.SPIRIVA.com, zeskanuj poniższy kod lub zadzwoń do Boehringer Ingelheim Pharmaceuticals, Inc. pod numer 1-800-542-6257 lub (TTY) 1-800-459-9906.
Jakie są składniki SPIRIVA 9mcg Handihaler?
Składnik czynny: tiotropium
Składnik nieaktywny: monohydrat laktozy
Co to jest POChP (przewlekła obturacyjna choroba płuc)?
POChP to poważna choroba płuc, która obejmuje przewlekłe zapalenie oskrzeli, rozedmę lub oba te objawy. Większość POChP jest spowodowana paleniem. Kiedy masz POChP, twoje drogi oddechowe stają się zwężone. Powietrze wydostaje się więc z płuc wolniej. To utrudnia oddychanie.
Niniejsza informacja dla pacjenta została zatwierdzona przez amerykańską Agencję ds. Żywności i Leków.
INSTRUKCJA UŻYCIASPIRIVA® (speh REE vah) HANDIHALER® (bromek tiotropium) proszek do inhalacji do inhalacji doustnej
Nie połykać kapsułek SPIRIVA.
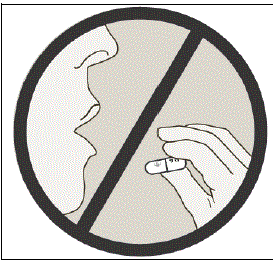
Ważne informacje dotyczące korzystania z aparatu SPIRIVA HANDIHALER
- Nie połykać kapsułek SPIRIVA 9mcg.
- Kapsułki SPIRIVA należy stosować wyłącznie z urządzeniem HANDIHALER i wdychać przez usta (inhalacja doustna).
- Nie należy używać urządzenia HANDIHALER do przyjmowania innych leków.
Przed rozpoczęciem stosowania produktu SPIRIVA Handihaler i za każdym razem, gdy uzupełniasz receptę, przeczytaj najpierw informacje dla pacjenta, a następnie niniejszą instrukcję użycia. Mogą pojawić się nowe informacje.
Zapoznanie się z urządzeniem HANDIHALER i kapsułkami SPIRIVA:
Twój SPIRIVA HANDIHALER jest dostarczany z kapsułkami SPIRIVA 9mcg w opakowaniu blistrowym i urządzeniem HANDIHALER. Użyj nowego urządzenia HANDIHALER dostarczonego z lekiem.
Części urządzenia HANDIHALER obejmują:
(Patrz Rysunek A)
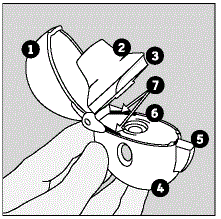
Rysunek A
Każda kapsułka SPIRIVA 9mcg jest pakowana w blister. (Patrz Rysunek B)
Rysunek B
- Każda kapsułka SPIRIVA zawiera tylko niewielką ilość proszku. (Patrz Rysunek C) To jest 1 pełna dawka.
- Nie otwierać kapsułki SPIRIVA 9mcg lub może nie działać.

Rysunek C
Przyjęcie pełnej dziennej dawki leku wymaga 4 głównych kroków.
Krok 1. Otwieranie urządzenia HANDIHALER:
Po wyjęciu urządzenia HANDIHALER z etui:
- Otwórz osłonkę przeciwkurzową (pokrywkę), naciskając zielony przycisk przekłuwania. (Patrz Rysunek D)
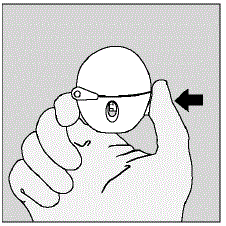
Rysunek D
- Odciągnąć nasadkę przeciwkurzową (pokrywkę) do góry od podstawy, aby odsłonić ustnik. (Patrz Rysunek E)
Rysunek E
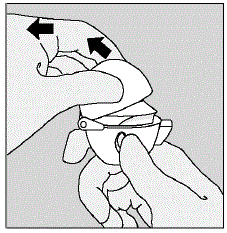
- Otworzyć ustnik, pociągając grzbiet ustnika w górę i od podstawy, tak aby widoczna była komora środkowa. (Patrz Rysunek F)

Rysunek F
Krok 2. Wkładanie kapsułki SPIRIVA 9mcg do urządzenia HANDIHALER:
Każdego dnia oddzielić tylko 1 blistry od blistra poprzez oderwanie wzdłuż perforowanej linii. (Patrz Rysunek G)
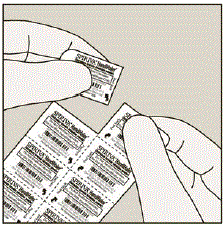
Rysunek G
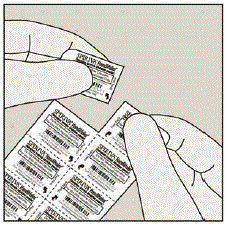
Wyjąć kapsułkę SPIRIVA z blistra:
- Nie rób przeciąć folię lub za pomocą ostrych narzędzi wyjąć kapsułkę SPIRIVA z blistra.
- Zagnij 1 z rogów blistra za pomocą strzałki i oddziel warstwy folii aluminiowej.
- Odklej zadrukowaną folię, aż zobaczysz całą kapsułkę SPIRIVA. (Patrz Rysunek H)
- W przypadku otwarcia więcej niż 1 blistra w powietrze, nie należy używać dodatkowej kapsułki SPIRIVA 9mcg i należy ją wyrzucić.
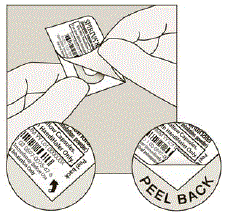
Rysunek H
Umieść kapsułkę SPIRIVA 9mcg w środkowej komorze urządzenia HANDIHALER. (Patrz Rysunek I)
Rysunek I
Mocno docisnąć ustnik do szarej podstawy, aż usłyszysz kliknięcie. Pozostaw osłonę przeciwkurzową (pokrywę) otwartą. (Patrz Rysunek J)
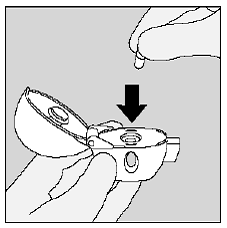
Rysunek J
Krok 3. Przebicie kapsułki SPIRIVA 9mcg:
- Trzymaj urządzenie HANDIHALER ustnikiem skierowanym do góry. (Patrz Rysunek K)
- Naciśnij jeden raz zielony przycisk przekłuwania, aż będzie płasko przylegał do podstawy, a następnie zwolnij. W ten sposób robi się otwory w kapsułce SPIRIVA, aby pobrać lek podczas wdechu.
- Nie rób naciśnij zielony przycisk więcej niż jeden raz.
- Nie rób potrząśnij urządzeniem HANDIHALER.
- Przebicie kapsułki SPIRIVA 9mcg może spowodować powstanie małych kawałki żelatyny. Niektóre z tych małych kawałków mogą przedostać się przez ekran urządzenia HANDIHALER do ust lub gardła podczas wdychania leku. To normalne. Małe kawałki żelatyny nie powinny ci zaszkodzić.
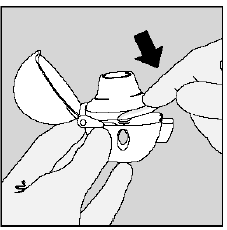
Rysunek K
Krok 4. Przyjęcie pełnej dziennej dawki (2 inhalacje z tej samej kapsułki SPIRIVA 9mcg):
Wydychaj całkowicie w 1 wdechu, opróżnianie płuc z powietrza. (Patrz Rysunek L)
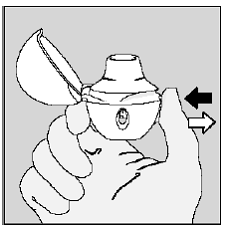
Rysunek L
Ważne: nie oddychać do urządzenia HANDIHALER.
Przy następnym oddechu weź lekarstwo:
- Trzymaj głowę w pozycji pionowej, patrząc prosto przed siebie. (Patrz Rysunek M)
- Podnieś urządzenie HANDIHALER do ust w pozycji poziomej. Nie rób zablokować wloty powietrza.
- Zamknij mocno usta wokół ustnika.
- Oddychaj głęboko aż twoje płuca będą pełne. Powinieneś usłyszeć lub poczuć wibrację kapsułki SPIRIVA (grzechotka). (Patrz Rysunek M)
- Wstrzymaj oddech na kilka sekund i jednocześnie wyjmij urządzenie HANDIHALER z ust.
- Oddychaj normalnie.
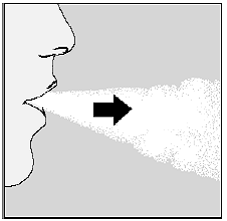
Rysunek M
Grzechotka mówi ci, że prawidłowo oddychałeś. Jeśli nie słyszysz lub nie czujesz grzechotania, patrz rozdział „Jeśli nie słyszysz lub nie czujesz grzechotania kapsułki SPIRIVA podczas wdychania leku”.
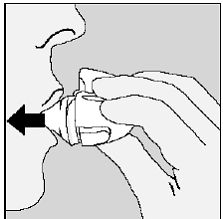
Rysunek N
Aby otrzymać pełną dawkę dobową, należy ponownie wykonać pełny wydech (Patrz Rysunek N) i ponownie wykonać wdech (Patrz Rysunek O) z tej samej kapsułki SPIRIVA.
Ważne: nie naciśnij ponownie zielony przycisk przekłuwania.
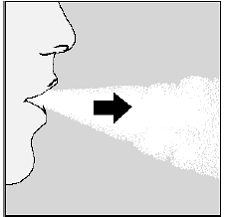
Postać O
Pamiętać: Aby otrzymać pełną dawkę leku każdego dnia, należy wykonać 2 wdechy z tej samej kapsułki SPIRIVA 9mcg. Upewnij się, że wykonałeś pełny wydech za każdym razem, zanim zrobisz wdech z urządzenia HANDIHALER.
Pielęgnacja i przechowywanie Twojego SPIRIVA HANDIHALER:
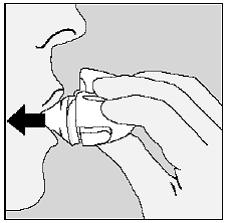
Rysunek P
- Po przyjęciu dziennej dawki otwórz ustnik i wyrzuć zużytą kapsułkę SPIRIVA 9mcg do kosza na śmieci, nie dotykając jej.
- Usuń wszelkie kawałki kapsułek SPIRIVA 9mcg lub nagromadzony proszek SPIRIVA 9mcg, obracając urządzenie HANDIHALER do góry nogami i delikatnie, ale stanowczo, stukając w nie. (Patrz Rysunek P) Następnie zamknij ustnik i nasadkę do przechowywania.
- Nie rób przechowywać urządzenie HANDIHALER i kapsułki SPIRIVA 9mcg (blistry) w wilgotnym i wilgotnym miejscu. Kapsułki SPIRIVA należy zawsze przechowywać w zamkniętych blistrach.
Jeśli nie słyszysz lub nie czujesz grzechotania kapsułki SPIRIVA 9mcg podczas wdychania leku:
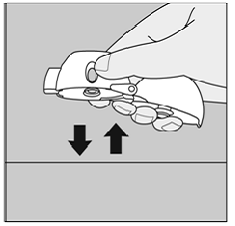
Rysunek Q
Nie rób naciśnij ponownie zielony przycisk przekłuwania.
Trzymaj urządzenie HANDIHALER ustnikiem skierowanym do góry i delikatnie uderzaj urządzeniem HANDIHALER o stół. (Patrz rysunek Q)
Sprawdź, czy ustnik jest całkowicie zamknięty. Wykonać pełny wydech przed ponownym głębokim wdechem z ustnikiem w ustach. (Patrz Rysunek O)
Jeśli po powtórzeniu powyższych kroków nadal nie słyszysz ani nie czujesz grzechotania kapsułek SPIRIVA:
- Wyrzuć kapsułkę SPIRIVA.
- Otwórz podstawę, podnosząc zielony przycisk przekłuwania i sprawdź, czy w środkowej komorze nie ma kawałków kapsułki SPIRIVA 9mcg. Kawałki kapsułek SPIRIVA 9mcg w środkowej komorze mogą spowodować, że kapsułka SPIRIVA 9mcg nie będzie grzechotać.
- Odwróć urządzenie HANDIHALER do góry nogami i delikatnie, ale zdecydowanie stuknij, aby usunąć kawałki kapsułek SPIRIVA. Zadzwoń do lekarza po instrukcje.
Czyszczenie urządzenia HANDIHALER:
W razie potrzeby wyczyść urządzenie HANDIHALER. (Patrz Rysunek R)
- Wysuszenie urządzenia HANDIHALER na powietrzu po wyczyszczeniu zajmuje 24 godziny.
- Nie rób używać środków czyszczących lub detergentów.
- Nie rób umieść urządzenie HANDIHALER w zmywarce do czyszczenia.
Kroki czyszczenia:
- Otwórz wieczko i ustnik.
- Otwórz podstawę, podnosząc zielony przycisk przekłuwania.
- Poszukaj w środkowej komorze kawałków kapsułek SPIRIVA 9mcg lub nagromadzonego proszku. Jeśli widzisz, stuknij.
- Opłucz urządzenie HANDIHALER ciepłą wodą, naciskając kilka razy zielony przycisk przekłuwania, tak aby komora środkowa i igła przekłuwająca znalazły się pod bieżącą wodą. Sprawdź, czy usunięto nagromadzony proszek lub kawałki kapsułek SPIRIVA.
- Dobrze osusz urządzenie HANDIHALER, wylewając nadmiar wody na ręcznik papierowy. Następnie wysuszyć na powietrzu, pozostawiając otwartą nasadkę przeciwpyłową, ustnik i podstawę, całkowicie rozprowadzając je, aby całkowicie wyschły.
- Nie rób użyj suszarki do włosów, aby wysuszyć urządzenie HANDIHALER.
- Nie rób używać urządzenia HANDIHALER, gdy jest mokre. W razie potrzeby zewnętrzną część ustnika można wyczyścić czystą, wilgotną ściereczką.
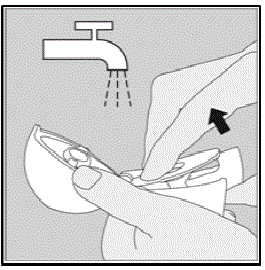
Rysunek R
Przydatne wskazówki, które pomogą zapewnić prawidłowe przyjmowanie pełnej dziennej dawki leku SPIRIVA 9mcg Handihaler:
- Naciskać zielony przycisk przekłuwania raz; Oddychaj 2 razy; Wydychaj całkowicie przed każdą z 2 inhalacji.
- Zawsze używaj nowego urządzenia HANDIHALER dostarczonego z lekiem.
- Trzymaj urządzenie HANDIHALER z ustnikiem skierowanym do góry podczas naciskania zielonego przycisku przekłuwania.
- Naciśnij zielony przycisk przekłuwania 1 raz przebić kapsułkę SPIRIVA.
- Nie wydychaj powietrza do urządzenia HANDIHALER.
- Podczas wdechu trzymaj urządzenie HANDIHALER w pozycji poziomej i utrzymuj głowę w pozycji pionowej, patrząc prosto przed siebie.
- Sprawdź środkową komorę urządzenia HANDIHALER pod kątem kawałków kapsułek SPIRIVA 9mcg lub nagromadzenia proszku. Jeśli widoczne są kawałki lub proszek, wytrzep go przed użyciem.
- W razie potrzeby wyczyść HANDIHALER i dokładnie wysusz.
Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą, odwiedź stronę www.spiriva.com, zeskanuj poniższy kod lub zadzwoń pod numer 1-800-542-6257 lub (TTY) 1-800-459-9906.
Niniejsza instrukcja użytkowania została zatwierdzona przez amerykańską Agencję ds. Żywności i Leków.
