Symbicort 160/4.5mcg Budesonide Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Symbicort 4,5mcg i jak się go stosuje?
Symbicort 4,5mcg to lek na receptę stosowany w leczeniu objawów astmy i przewlekłej obturacyjnej choroby płuc. Symbicort może być stosowany samodzielnie lub z innymi lekami.
Symbicort należy do klasy leków o nazwie Respiratory Inhalant Combo.
Nie wiadomo, czy Symbicort 4,5mcg jest bezpieczny i skuteczny u dzieci w wieku poniżej 6 lat.
Jakie są możliwe skutki uboczne Symbicort 4.5mcg?
Symbicort może powodować poważne działania niepożądane, w tym:
- nasilające się problemy z oddychaniem,
- owrzodzenia lub białe plamy w jamie ustnej lub gardle,
- ból podczas połykania,
- drżenia,
- nerwowość,
- ból w klatce piersiowej,
- szybkie lub mocno bijące bicie serca,
- kaszel ze śluzem,
- uczucie zadyszki,
- świszczący oddech,
- dławiąc się,
- inne problemy z oddychaniem,
- rozmazany obraz,
- widzenie tunelowe,
- ból lub zaczerwienienie oka,
- widząc aureole wokół świateł,
- gorączka,
- dreszcze,
- bóle,
- niezwykłe zmęczenie,
- zwiększone pragnienie,
- zwiększone oddawanie moczu,
- suchość w ustach,
- owocowy zapach oddechu,
- kurcze nóg,
- zaparcie,
- nieregularne bicie serca,
- fruwające w piersi,
- drętwienie lub mrowienie,
- słabe mięśnie,
- wiotkość uczucie,
- zmęczenie,
- słabość,
- zawroty,
- nudności i
- wymioty
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Do najczęstszych działań niepożądanych leku Symbicort należą:
- ból lub podrażnienie gardła,
- białe plamy w jamie ustnej lub gardle,
- dyskomfort w żołądku,
- wymioty,
- ból pleców,
- ból głowy,
- objawy grypy i
- objawy przeziębienia (zatkany nos lub katar, kichanie, ból zatok lub ból gardła)
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Symbicort. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
SYMBICORT 80/4,5 i SYMBICORT 160/4,5 zawierają mikronizowany budezonid i mikronizowany fumaran formoterolu dwuwodny wyłącznie do inhalacji doustnej.
Każdy pojemnik SYMBICORT 80/4,5 i SYMBICORT 160/4,5 ma postać hydrofluoroalkanu (HFA 227; 1,1,1,2,3,3,3-heptafluoropropan) ciśnieniowego inhalatora ciśnieniowego z dozownikiem, zawierającego 60 lub 120 dawek [patrz Formy dawkowania i mocne strony oraz JAK DOSTARCZONE / Składowania i stosowania ]. Po zalewaniu, każde uruchomienie odmierza 91/5,1 mcg lub 181/5,1 mcg z zaworu i dostarcza 80/4,5 mcg lub 160/4,5 mcg (zmikronizowany budezonid/mikronizowany dwuwodny fumaran formoterolu) z siłownika. Rzeczywista ilość leku dostarczonego do płuc może zależeć od czynników pacjenta, takich jak koordynacja między uruchomieniem urządzenia a wdechem przez system dostarczania. SYMBICORT 160mg zawiera również powidon K25 USP jako środek zawieszający oraz glikol polietylenowy 1000 NF jako środek poślizgowy.
SYMBICORT 160mg należy zagruntować przed pierwszym użyciem, wypuszczając dwa rozpylenia testowe w powietrze z dala od twarzy, dobrze wstrząsając przez 5 sekund przed każdym rozpyleniem. W przypadkach, gdy inhalator nie był używany przez ponad 7 dni lub gdy został upuszczony, należy ponownie napełnić inhalator, dobrze wstrząsając przez 5 sekund przed każdym rozpyleniem i wypuszczając dwa rozpylenia testowe w powietrze z dala od twarzy.
Jednym z aktywnych składników SYMBICORT 4,5 mcg jest budezonid, kortykosteroid oznaczony chemicznie jako (RS)11β,16α,17,21-tetrahydroksypregna-1,4-dieno-3,20-dion cykliczny 16,17-acetal z aldehydem masłowym. Budezonid jest dostarczany jako mieszanina dwóch epimerów (22R i 22S). Empiryczny wzór budezonidu to C25H34O6, a jego masa cząsteczkowa wynosi 430,5. Jego wzór strukturalny to:
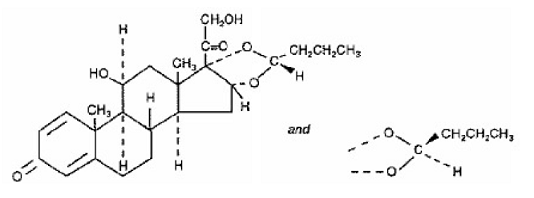
Budezonid jest proszkiem o barwie białej lub prawie białej, bez smaku i zapachu, który jest praktycznie nierozpuszczalny w wodzie i heptanie, słabo rozpuszczalny w etanolu i łatwo rozpuszczalny w chloroformie. Jego współczynnik podziału między oktanol i wodę przy pH 7,4 wynosi 1,6 x 103.
Innym aktywnym składnikiem leku SYMBICORT 160 mg jest dwuwodny fumaran formoterolu, selektywny beta2-agonista określany chemicznie jako (R*,R*)-(±)-N-[2-hydroksy-5-[1-hydroksy-2-[[ 2-(4-metoksyfenylo)-1metyloetylo]amino]etylo]fenylo]formamid, (E)-2-butenodianian (2:1), dihydrat. Wzór empiryczny formoterolu to C42H56N4O14, a jego masa cząsteczkowa wynosi 840,9. Jego wzór strukturalny to:
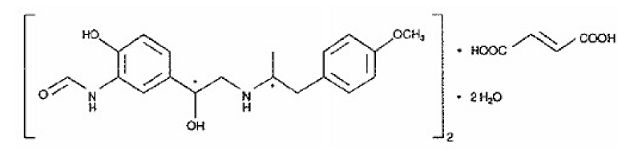
Dwuwodny fumaran formoterolu jest proszkiem słabo rozpuszczalnym w wodzie. Jego współczynnik podziału oktanol-woda przy pH 7,4 wynosi 2,6. Wartość pKa dihydratu fumaranu formoterolu w temperaturze 25°C wynosi 7,9 dla grupy fenolowej i 9,2 dla grupy aminowej.
WSKAZANIA
Leczenie astmy
SYMBICORT 4,5 mcg jest wskazany w leczeniu astmy u pacjentów w wieku 6 lat i starszych.
SYMBICORT powinien być stosowany u pacjentów, u których nie uzyskano wystarczającej kontroli astmy za pomocą długotrwałego leku kontrolującego astmę, takiego jak wziewny kortykosteroid (ICS) lub u których choroba uzasadnia rozpoczęcie leczenia zarówno wziewnym kortykosteroidem, jak i długo działającym agonistą receptorów beta2-adrenergicznych (LABA).
Ważne ograniczenia użytkowania
- SYMBICORT NIE jest wskazany do łagodzenia ostrego skurczu oskrzeli.
Leczenie podtrzymujące przewlekłej obturacyjnej choroby płuc
SYMBICORT 160/4,5 jest wskazany w leczeniu podtrzymującym obturacji dróg oddechowych u pacjentów z przewlekłą obturacyjną chorobą płuc (POChP), w tym przewlekłym zapaleniem oskrzeli i (lub) rozedmą płuc. SYMBICORT 160/4,5 jest również wskazany do zmniejszania zaostrzeń POChP. SYMBICORT 160/4,5 jest jedyną mocą wskazaną w leczeniu POChP.
Ważne ograniczenia użytkowania
- SYMBICORT 4,5 mcg NIE jest wskazany do łagodzenia ostrego skurczu oskrzeli.
DAWKOWANIE I SPOSÓB PODAWANIA
Informacje administracyjne
SYMBICORT 160 mg należy podawać w postaci 2 inhalacji dwa razy na dobę (rano i wieczorem, w odstępie około 12 godzin), codziennie wyłącznie drogą wziewną doustnie. Po inhalacji pacjent powinien przepłukać usta wodą bez połykania.
Przed pierwszym użyciem zagruntuj SYMBICORT 4,5mcg, wypuszczając dwa rozpylone spraye testowe w powietrze z dala od twarzy, dobrze wstrząsając przez 5 sekund przed każdym rozpyleniem. W przypadkach, gdy inhalator nie był używany przez ponad 7 dni lub gdy został upuszczony, należy go ponownie napełnić, dobrze wstrząsając przed każdym rozpyleniem i wypuszczając dwa rozpylenia testowe w powietrze z dala od twarzy.
Nie zaleca się częstszego podawania lub większej liczby inhalacji (więcej niż 2 inhalacje dwa razy na dobę) przepisanej mocy produktu SYMBICORT, ponieważ niektórzy pacjenci są bardziej narażeni na wystąpienie działań niepożądanych przy wyższych dawkach formoterolu. Pacjenci stosujący SYMBICORT nie powinni stosować dodatkowego LABA z jakiegokolwiek powodu [patrz OSTRZEŻENIA I ŚRODKI ].
Astma
Jeśli objawy astmy pojawią się w okresie między dawkami, należy zastosować wziewny, krótko działający beta2-mimetyk w celu natychmiastowej ulgi.
Pacjenci dorośli i młodzież w wieku 12 lat i starsi
Dla pacjentów w wieku 12 lat i starszych dawka wynosi 2 inhalacje SYMBICORT 80/4,5 lub SYMBICORT 160/4,5 dwa razy na dobę.
Zalecane dawki początkowe produktu SYMBICORT u pacjentów w wieku 12 lat i starszych są uzależnione od ciężkości astmy lub poziomu kontroli objawów astmy oraz ryzyka zaostrzeń podczas stosowania aktualnie stosowanych wziewnych kortykosteroidów.
Maksymalna zalecana dawka u dorosłych i młodzieży w wieku 12 lat i starszych to SYMBICORT 160/4,5, dwie inhalacje dwa razy na dobę.
Poprawa kontroli astmy po wziewnym podaniu produktu SYMBICORT może nastąpić w ciągu 15 minut od rozpoczęcia leczenia, chociaż maksymalne korzyści mogą nie zostać osiągnięte przez 2 tygodnie lub dłużej po rozpoczęciu leczenia. Poszczególni pacjenci odczują zmienny czas do wystąpienia i stopień złagodzenia objawów.
pacjentów, którzy nie reagują odpowiednio na dawkę początkową po 1-2 tygodniach leczenia SYMBICORT 80/4,5, zastąpienie SYMBICORT 160/4,5 może zapewnić dodatkową kontrolę astmy.
Jeśli wcześniej skuteczny schemat dawkowania produktu SYMBICORT 4,5 mikrograma nie zapewnia odpowiedniej kontroli astmy, należy ponownie ocenić schemat terapeutyczny i zastosować dodatkowe opcje terapeutyczne (np. zastąpienie mniejszej mocy produktu SYMBICORT 4,5 mikrograma mocniejszym, dodanie dodatkowych środków wziewnych). należy rozważyć podanie kortykosteroidu lub rozpoczęcie stosowania doustnych kortykosteroidów).
Pacjenci pediatryczni w wieku od 6 do mniej niż 12 lat
U pacjentów w wieku od 6 do mniej niż 12 lat dawka wynosi 2 inhalacje produktu SYMBICORT 80/4,5 dwa razy na dobę.
Przewlekła obturacyjna choroba płuc
Dla pacjentów z POChP zalecana dawka to SYMBICORT 160/4,5, dwie inhalacje dwa razy na dobę.
Jeśli duszność wystąpi w okresie między dawkami, w celu natychmiastowej ulgi należy zastosować wziewny, krótko działający beta2-mimetyk.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
SYMBICORT jest dostępny jako inhalator z dozownikiem zawierający połączenie budezonidu (80 lub 160 mikrogramów) i formoterolu (4,5 mikrograma) w postaci aerozolu do inhalacji w dwóch mocach: 80/4,5 i 160/4,5. Każda moc dawki zawiera 60 lub 120 dawek na pojemnik. Każda moc SYMBICORT 160 mg jest dostarczana z czerwonym plastikowym aktywatorem z szarą nasadką przeciwpyłową.
Składowania i stosowania
SYMBICORT jest dostępny w dwóch mocach i jest dostarczany w następujących wielkościach opakowań:
Formy dawkowania i mocne strony
Każda moc jest dostarczana jako ciśnieniowy pojemnik aluminiowy z dołączonym urządzeniem liczącym, czerwonym plastikowym korpusem siłownika z białym ustnikiem i dołączoną szarą nasadką przeciwpyłową. Każdy pojemnik do inhalacji 120 ma masę netto wypełnienia 10,2 grama, a każdy pojemnik 60 inhalacji ma masę netto wypełnienia 6,9 grama (SYMBICORT 80/4,5) lub 6 gramów (SYMBICORT 160/4,5). Każdy kanister jest zapakowany w foliową saszetkę z saszetką ze środkiem osuszającym i umieszczony w kartonie. Każde pudełko zawiera jeden pojemnik i ulotkę z informacjami dla pacjenta.
Pojemnika SYMBICORT 4,5 mcg należy używać wyłącznie z urządzeniem uruchamiającym SYMBICORT 4,5 mcg, a urządzenia uruchamiającego SYMBICORT nie należy używać z żadnym innym lekiem do inhalacji.
Nie można zapewnić prawidłowej ilości leku w każdej inhalacji po użyciu podanej liczby inhalacji z pojemnika, nawet jeśli inhalator może nie wydawać się całkowicie pusty i może nadal działać. Inhalator należy wyrzucić po użyciu podanej liczby inhalacji lub w ciągu 3 miesięcy po wyjęciu z torebki foliowej. Nigdy nie zanurzaj kanistra w wodzie w celu określenia ilości pozostałej w kanistrze („test pływaka”).
Przechowywać w kontrolowanej temperaturze pokojowej 20°C do 25°C (68°F do 77°F) [patrz USP]. Przechowywać inhalator z ustnikiem w dół.
Aby uzyskać najlepsze wyniki, przed użyciem pojemnik powinien mieć temperaturę pokojową. Dobrze wstrząsnąć przez 5 sekund przed użyciem.
Trzymać z dala od dzieci. Unikaj rozpylania w oczach.
ZAWARTOŚĆ POD CIŚNIENIEM.
Nie przekłuwać ani nie spalać. Nie przechowywać w pobliżu źródeł ciepła lub otwartego ognia. Ekspozycja na temperatury powyżej 120°F może spowodować pęknięcie. Nigdy nie wrzucaj pojemnika do ognia ani do spalarni.
Wyprodukowano dla: AstraZeneca Pharmaceuticals LP, Wilmington, DE 19850 Przez: AstraZeneca Dunkerque Production, Dunkierka, Francja. Aktualizacja: grudzień 2017 r.
SKUTKI UBOCZNE
Użycie LABA może skutkować:
- Poważne zdarzenia związane z astmą – hospitalizacje, intubacje, zgon [patrz OSTRZEŻENIA I ŚRODKI ].
- Wpływ na układ sercowo-naczyniowy i ośrodkowy układ nerwowy [patrz OSTRZEŻENIA I ŚRODKI ].
Ogólnoustrojowe i wziewne stosowanie kortykosteroidów może skutkować:
- Zakażenie Candida albicans [patrz OSTRZEŻENIA I ŚRODKI ]
- Zapalenie płuc lub infekcje dolnych dróg oddechowych u pacjentów z POChP [patrz OSTRZEŻENIA I ŚRODKI ]
- Immunosupresja [patrz OSTRZEŻENIA I ŚRODKI ]
- Hiperkortyka i zahamowanie czynności kory nadnerczy [patrz OSTRZEŻENIA I ŚRODKI ]
- Wpływ na wzrost u pacjentów pediatrycznych [patrz OSTRZEŻENIA I ŚRODKI ]
- Jaskra i zaćma [patrz OSTRZEŻENIA I ŚRODKI ]
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Doświadczenie w badaniach klinicznych w astmie
Pacjenci dorośli i młodzież w wieku 12 lat i starsi
Ogólne dane dotyczące bezpieczeństwa u dorosłych i młodzieży oparte są na 10 badaniach klinicznych kontrolowanych preparatem aktywnym i placebo, w których 3393 pacjentów w wieku 12 lat i starszych (2052 kobiety i 1341 mężczyzn) z astmą o różnym nasileniu leczono preparatem SYMBICORT 80/4,5 lub 160 /4,5 2 inhalacje raz lub dwa razy dziennie przez 12 do 52 tygodni. W tych badaniach pacjenci otrzymujący SYMBICORT mieli średni wiek 38 lat i byli głównie rasy kaukaskiej (82%).
Częstość występowania częstych zdarzeń niepożądanych w Tabeli 2 poniżej jest oparta na zbiorczych danych z trzech 12-tygodniowych, podwójnie zaślepionych, kontrolowanych placebo badań klinicznych, w których 401 pacjentów dorosłych i młodzieży (148 mężczyzn i 253 kobiety) w wieku 12 lat i starszych było leczony 2 inhalacjami SYMBICORT 80/4,5 lub SYMBICORT 160/4,5 dwa razy dziennie. Grupa SYMBICORT składała się głównie z pacjentów rasy kaukaskiej (84%) w średnim wieku 38 lat, a średni procent przewidywanej wartości FEV1 na początku badania wynosił 76 i 68 odpowiednio dla grup leczonych 80/4,5 mcg i 160/4,5 mcg. Ramiona kontrolne dla porównania obejmowały 2 inhalacje budezonidu HFA z odmierzaną dawką (MDI) 80 lub 160 mcg, formoterolu inhalatora suchego proszku (DPI) 4,5 mcg lub placebo (MDI i DPI) dwa razy dziennie. Tabela 2 zawiera wszystkie zdarzenia niepożądane, które wystąpiły z częstością > 3% w dowolnej grupie SYMBICORT i częściej niż w grupie placebo przy dawkowaniu dwa razy na dobę. Rozważając te dane, należy wziąć pod uwagę wydłużony średni czas ekspozycji pacjentów leczonych produktem SYMBICORT, ponieważ częstości nie są korygowane o nierównowagę czasu trwania leczenia.
Długoterminowe bezpieczeństwo — badania kliniczne astmy u pacjentów w wieku 12 lat i starszych
Długoterminowe badania bezpieczeństwa u młodzieży i dorosłych pacjentów w wieku 12 lat i starszych, leczonych przez okres do 1 roku dawkami do 1280/36 mikrogramów/dobę (640/18 mikrogramów dwa razy na dobę), nie wykazały klinicznie istotnych zmian częstości występowania ani nowych rodzajów zdarzeń niepożądanych pojawiających się po dłuższym okresie leczenia. Podobnie nie zaobserwowano żadnych znaczących ani nieoczekiwanych wzorców nieprawidłowości przez okres do 1 roku w środkach bezpieczeństwa, w tym chemii, hematologii, EKG, monitorze Holtera i ocenie osi HPA.
Pacjenci pediatryczni w wieku od 6 do mniej niż 12 lat
Dane dotyczące bezpieczeństwa dla pacjentów pediatrycznych w wieku od 6 do mniej niż 12 lat opierają się na 1 badaniu trwającym 12 tygodni. Pacjenci (79 kobiet i 105 mężczyzn) otrzymujący kortykosteroid wziewny w momencie włączenia do badania zostali losowo przydzieleni do grupy SYMBICORT 80/4,5 (n=92) lub budezonidu pMDI 80 mcg (n=92), 2 inhalacje dwa razy na dobę. Ogólny profil bezpieczeństwa tych pacjentów był podobny do obserwowanego u pacjentów w wieku 12 lat i starszych, którzy otrzymywali SYMBICORT 80/4,5 dwa razy na dobę w badaniach o podobnym projekcie. Częste działania niepożądane, które występowały u pacjentów leczonych SYMBICORT 80/4,5 z częstością ≥3% i częściej niż u pacjentów leczonych tylko budezonidem pMDI 80 mcg, obejmowały zakażenie górnych dróg oddechowych, zapalenie gardła, ból głowy i nieżyt nosa.
Doświadczenie w badaniach klinicznych w przewlekłej obturacyjnej chorobie płuc
Opisane poniżej dane dotyczące bezpieczeństwa odzwierciedlają ekspozycję na SYMBICORT 160/4,5 u 1783 pacjentów. SYMBICORT 160/4,5 badano w dwóch kontrolowanych placebo badaniach czynności płuc (trwających 6 i 12 miesięcy) oraz dwóch kontrolowanych aktywnie kontrolowanych badaniach zaostrzeń (trwających 6 i 12 miesięcy) u pacjentów z POChP.
Częstość występowania częstych zdarzeń niepożądanych w Tabeli 3 poniżej opiera się na zbiorczych danych z dwóch podwójnie zaślepionych, kontrolowanych placebo badań klinicznych dotyczących czynności płuc (trwających 6 i 12 miesięcy), w których 771 dorosłych pacjentów z POChP (496 mężczyzn i 275 kobiet) 40 w wieku i starszym leczono preparatem SYMBICORT 160/4,5, dwie inhalacje dwa razy na dobę. Spośród tych pacjentów 651 było leczonych przez 6 miesięcy, a 366 przez 12 miesięcy. Grupa SYMBICORT składała się głównie z pacjentów rasy kaukaskiej (93%) w średnim wieku 63 lat, a średni procent przewidywanej wartości FEV1 na początku badania wynosił 33%. Ramiona kontrolne dla porównania obejmowały 2 inhalacje budezonidu HFA (MDI) 160 µg, formoterolu (DPI) 4,5 µg lub placebo (MDI i DPI) dwa razy dziennie. Tabela 3 zawiera wszystkie zdarzenia niepożądane, które wystąpiły z częstością ≥3% w grupie SYMBICORT i częściej niż w grupie placebo. Rozważając te dane, należy wziąć pod uwagę wydłużony średni czas ekspozycji pacjenta na produkt SYMBICORT 4,5 mcg, ponieważ częstość występowania nie jest korygowana o nierównowagę czasu trwania leczenia.
Infekcje płuc inne niż zapalenie płuc (głównie zapalenie oskrzeli) wystąpiły u większego odsetka pacjentów leczonych produktem SYMBICORT 160/4,5 w porównaniu z placebo (odpowiednio 7,9% w porównaniu z 5,1%). Nie zaobserwowano klinicznie istotnych ani nieoczekiwanych wzorców nieprawidłowości przez okres do 1 roku w badaniach chemii, hematologii, EKG, EKG (Holter), osi HPA, gęstości mineralnej kości i okulistyki.
Dane dotyczące bezpieczeństwa z dwóch podwójnie zaślepionych, aktywnie kontrolowanych badań zaostrzeń (trwających 6 i 12 miesięcy), w których 1012 dorosłych pacjentów z POChP (616 mężczyzn i 396 kobiet) w wieku 40 lat i starszych było leczonych produktem SYMBICORT 160/4,5, dwie inhalacje dwa razy dziennie były zgodne z wynikami badań czynności płuc.
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania produktu SYMBICORT po dopuszczeniu do obrotu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek. Niektóre z tych działań niepożądanych mogły być również obserwowane w badaniach klinicznych produktu SYMBICORT.
Zaburzenia serca: dusznica bolesna, tachykardia, tachyarytmie przedsionkowe i komorowe, migotanie przedsionków, skurcze dodatkowe, kołatanie serca
Zaburzenia endokrynologiczne: hiperkortyzm, zmniejszenie szybkości wzrostu u dzieci i młodzieży
Zaburzenia oka: zaćma, jaskra, podwyższone ciśnienie śródgałkowe
Zaburzenia żołądkowo-jelitowe: kandydoza jamy ustnej i gardła, nudności
Zaburzenia układu immunologicznego: natychmiastowe i opóźnione reakcje nadwrażliwości, takie jak reakcja anafilaktyczna, obrzęk naczynioruchowy, skurcz oskrzeli, pokrzywka, wysypka, zapalenie skóry, świąd
Zaburzenia metabolizmu i odżywiania: hiperglikemia, hipokaliemia
Zaburzenia mięśniowo-szkieletowe, tkanki łącznej i kości: skurcze mięśni
Zaburzenia układu nerwowego: drżenie, zawroty głowy
Zaburzenia psychiczne: zaburzenia zachowania, zaburzenia snu, nerwowość, pobudzenie, depresja, niepokój
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia: dysfonia, kaszel, podrażnienie gardła
Zaburzenia skóry i tkanki podskórnej: siniaki na skórze
Zaburzenia naczyniowe: niedociśnienie, nadciśnienie
INTERAKCJE Z LEKAMI
W badaniach klinicznych jednoczesne podawanie produktu SYMBICORT i innych leków, takich jak krótko działający beta 2agoniści, donosowe kortykosteroidy i leki przeciwhistaminowe/leki zmniejszające przekrwienie, nie powodowało zwiększonej częstości działań niepożądanych. Nie przeprowadzono formalnych badań dotyczących interakcji z produktem SYMBICORT.
Inhibitory cytochromu P4503A4
Główną drogą metabolizmu kortykosteroidów, w tym budezonidu, składnika leku SYMBICORT, jest izoenzym 3A4 (CYP3A4) cytochromu P450 (CYP). Po podaniu doustnym ketokonazolu, silnego inhibitora CYP3A4, wzrosło średnie stężenie budezonidu podawanego doustnie. Jednoczesne podawanie CYP3A4 może hamować metabolizm i zwiększać ogólnoustrojową ekspozycję na budezonid. Należy zachować ostrożność rozważając jednoczesne podawanie produktu SYMBICORT 4,5 µg z ketokonazolem o długotrwałym działaniu i innymi znanymi silnymi inhibitorami CYP3A4 (np. rytonawir, atazanawir, klarytromycyna, indynawir, itrakonazol, nefazodon, nelfinawir, sakwinawir, telitromycyna) [patrz OSTRZEŻENIA I ŚRODKI ].
Inhibitory monoaminooksydazy i trójpierścieniowe leki przeciwdepresyjne
SYMBICORT należy podawać ostrożnie pacjentom leczonym inhibitorami monoaminooksydazy lub trójpierścieniowymi lekami przeciwdepresyjnymi lub w ciągu 2 tygodni od odstawienia takich leków, ponieważ leki te mogą nasilać działanie formoterolu, składnika leku SYMBICORT 160 mg, na układ naczyniowy . W badaniach klinicznych produktu SYMBICORT ograniczona liczba pacjentów z POChP i astmą otrzymywała trójpierścieniowe leki przeciwdepresyjne, a zatem nie można wyciągnąć istotnych klinicznie wniosków dotyczących zdarzeń niepożądanych.
Środki blokujące receptory beta-adrenergiczne
Beta-adrenolityki (w tym krople do oczu) mogą nie tylko blokować płucne działanie beta-agonistów, takich jak formoterol, składnik preparatu SYMBICORT, ale mogą powodować silny skurcz oskrzeli u pacjentów z astmą. Dlatego pacjenci z astmą zwykle nie powinni być leczeni beta-blokerami. Jednak w pewnych okolicznościach może nie być akceptowalnych alternatyw dla stosowania leków blokujących receptory beta-adrenergiczne u pacjentów z astmą. W takim przypadku można rozważyć kardioselektywne beta-adrenolityki, chociaż należy je podawać ostrożnie.
Diuretyki
Zmiany w zapisie EKG i (lub) hipokaliemia, które mogą wynikać z podawania leków moczopędnych nie oszczędzających potasu (takich jak diuretyki pętlowe lub tiazydowe), mogą być poważnie nasilone przez beta-agonistów, zwłaszcza po przekroczeniu zalecanej dawki beta-agonisty. Chociaż znaczenie kliniczne tych działań nie jest znane, zaleca się ostrożność podczas jednoczesnego podawania produktu SYMBICORT z lekami moczopędnymi nieoszczędzającymi potasu.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Poważne zdarzenia związane z astmą – hospitalizacje, intubacje i zgony
Stosowanie LABA w monoterapii (bez ICS) w przypadku astmy wiąże się ze zwiększonym ryzykiem zgonu związanego z astmą [patrz Salmeterol Multicenter Asthma Research Trial (SMART)]. Dostępne dane z kontrolowanych badań klinicznych sugerują również, że stosowanie LABA w monoterapii zwiększa ryzyko hospitalizacji z powodu astmy u dzieci i młodzieży. Te wyniki są uważane za efekt klasy LABA. Gdy LABA stosuje się w skojarzeniu o ustalonej dawce z ICS, dane z dużych badań klinicznych nie wykazują istotnego wzrostu ryzyka poważnych zdarzeń związanych z astmą (hospitalizacje, intubacje, zgon) w porównaniu z samym ICS (patrz Poważne zdarzenia związane z astmą z ICS/LABA).
Poważne zdarzenia związane z astmą z ICS/LABA
Przeprowadzono cztery duże, 26-tygodniowe, randomizowane, zaślepione, aktywnie kontrolowane kliniczne badania bezpieczeństwa w celu oceny ryzyka poważnych zdarzeń związanych z astmą, gdy LABA stosowano w połączeniu z ustaloną dawką z ICS w porównaniu z samym ICS u pacjentów z astmą. Trzy badania obejmowały pacjentów dorosłych i młodzież w wieku ≥12 lat: w jednym badaniu porównywano budezonid/formoterol (SYMBICORT) z budezonidem [patrz Studia kliniczne ]; w jednym badaniu porównywano proszek propionianu flutykazonu/salmeterolu do inhalacji z proszkiem propionianu flutykazonu; aw jednym badaniu porównano furoinian mometazonu/formoterol z furoinianem mometazonu. W czwartym badaniu wzięło udział dzieci w wieku od 4 do 11 lat i porównano propionian flutykazonu/salmeterol w postaci proszku do inhalacji z propionianem flutykazonu w postaci proszku. Pierwszorzędowym punktem końcowym bezpieczeństwa we wszystkich czterech badaniach były poważne zdarzenia związane z astmą (hospitalizacje, intubacje i zgon). Zaślepiony komitet orzekający ustalił, czy zdarzenia były związane z astmą.
Trzy badania z udziałem dorosłych i młodzieży zostały zaprojektowane tak, aby wykluczyć margines ryzyka na poziomie 2,0, a badanie pediatryczne zaprojektowano tak, aby wykluczyć ryzyko na poziomie 2,7. Każde indywidualne badanie osiągnęło wcześniej określony cel i wykazało równoważność ICS/LABA z samym ICS. Metaanaliza trzech badań z udziałem dorosłych i młodzieży nie wykazała istotnego wzrostu ryzyka wystąpienia poważnego zdarzenia związanego z astmą przy stosowaniu kombinacji ICS/LABA o ustalonej dawce w porównaniu z samym ICS (Tabela 1). Badania te nie miały na celu wykluczenia całego ryzyka wystąpienia poważnych zdarzeń związanych z astmą podczas stosowania ICS/LABA w porównaniu z ICS.
Badanie bezpieczeństwa pediatrycznego obejmowało 6208 pacjentów pediatrycznych w wieku od 4 do 11 lat, którzy otrzymywali ICS/LABA (propionian flutykazonu/salmeterol w proszku do inhalacji) lub ICS (propionian flutykazonu w inhalacji). W badaniu tym 27/3107 (0,9%) pacjentów przydzielonych losowo do ICS/LABA i 21/3101 (0,7%) pacjentów przydzielonych losowo do ICS doświadczyło poważnego zdarzenia związanego z astmą. Nie było zgonów ani intubacji związanych z astmą. ICS/LABA nie wykazały istotnie zwiększonego ryzyka poważnego zdarzenia związanego z astmą w porównaniu z ICS na podstawie wcześniej określonego marginesu ryzyka (2,7), z szacowanym współczynnikiem ryzyka czasu do pierwszego zdarzenia wynoszącym 1,29 (95% CI: 0,73 , 2,27).
Salmeterol Wieloośrodkowe badanie astmy (SMART)
28-tygodniowe, kontrolowane placebo badanie w USA, w którym porównywano bezpieczeństwo salmeterolu z placebo, dodanym do zwykłej terapii astmy, wykazało wzrost liczby zgonów związanych z astmą u pacjentów otrzymujących salmeterol (13/13 176 u pacjentów leczonych salmeterolem w porównaniu z 3 /13 179 u pacjentów leczonych placebo; ryzyko względne: 4,37 [95% CI 1,25, 15,34]). Korzystanie z ICS w tle nie było wymagane w SMART. Zwiększone ryzyko zgonu z powodu astmy jest uważane za efekt klasowy monoterapii LABA.
Badania monoterapii formoterolem
Badania kliniczne formoterolu stosowanego w monoterapii sugerowały większą częstość występowania ciężkich zaostrzeń astmy u pacjentów otrzymujących formoterol niż u pacjentów otrzymujących placebo. Rozmiary tych badań nie były wystarczające, aby precyzyjnie określić ilościowo różnicę w ciężkich zaostrzeniach astmy między grupami terapeutycznymi.
Pogorszenie choroby i ostre epizody
SYMBICORT 4,5 mcg nie powinien być rozpoczynany u pacjentów w trakcie szybko pogarszających się lub potencjalnie zagrażających życiu epizodów astmy lub POChP. SYMBICORT nie był badany u pacjentów z astmą o ostrym przebiegu lub POChP. Inicjacja SYMBICORT 4.5mcg w tym ustawieniu nie jest odpowiednia.
Coraz częstsze stosowanie wziewnych, krótko działających beta2-mimetyków jest markerem pogarszającej się astmy. W takiej sytuacji pacjent wymaga natychmiastowej ponownej oceny z ponowną oceną schematu leczenia, ze szczególnym uwzględnieniem ewentualnej potrzeby zastąpienia dotychczasowej mocy SYMBICORT wyższą mocą, dodania dodatkowego kortykosteroidu wziewnego lub rozpoczęcia stosowania kortykosteroidów ogólnoustrojowych. Pacjenci nie powinni stosować więcej niż 2 inhalacje dwa razy na dobę (rano i wieczorem) produktu SYMBICORT.
SYMBICORT 160 mg nie powinien być stosowany w celu łagodzenia ostrych objawów, tj. jako terapia ratunkowa w leczeniu ostrych epizodów skurczu oskrzeli. W celu złagodzenia ostrych objawów, takich jak duszność, należy stosować wziewny, krótko działający beta2-mimetyk, a nie SYMBICORT.
Przed rozpoczęciem leczenia produktem SYMBICORT 4,5 mikrograma należy pouczyć pacjentów, którzy regularnie przyjmowali doustnie lub wziewnie krótko działające beta2-mimetyki (np. 4 razy dziennie), aby zaprzestali regularnego stosowania tych leków.
Nadmierne stosowanie SYMBICORT 4,5 mcg i stosowanie z innymi długo działającymi beta2-mimetykami
Podobnie jak w przypadku innych leków wziewnych zawierających leki beta2-adrenergiczne, SYMBICORT 4,5 mikrograma nie powinien być stosowany częściej niż jest to zalecane, w dawkach większych niż zalecane lub w połączeniu z innymi lekami zawierającymi LABA, ponieważ może to spowodować przedawkowanie. W związku z nadmiernym stosowaniem wziewnych leków sympatykomimetycznych zgłaszano klinicznie istotne skutki sercowo-naczyniowe i zgony. Pacjenci stosujący SYMBICORT nie powinni stosować dodatkowego LABA (np. salmeterolu, fumaranu formoterolu, winianu arformoterolu) z jakiegokolwiek powodu, w tym z powodu zapobiegania skurczowi oskrzeli wywołanemu wysiłkiem (EIB) lub leczenia astmy lub POChP.
Efekty lokalne
badaniach klinicznych u pacjentów leczonych produktem SYMBICORT wystąpił rozwój zlokalizowanych zakażeń jamy ustnej i gardła wywołanych przez Candida albicans. Gdy taka infekcja się rozwinie, należy ją leczyć odpowiednią terapią miejscową lub ogólnoustrojową (tj. doustnym lekiem przeciwgrzybiczym), podczas gdy leczenie SYMBICORT 160 mg jest kontynuowane, ale czasami leczenie SYMBICORT 4,5 mcg może wymagać przerwania. Poradzić pacjentowi, aby po inhalacji wypłukał usta wodą bez połykania, aby zmniejszyć ryzyko kandydozy jamy ustnej i gardła.
Zapalenie płuc i inne infekcje dolnych dróg oddechowych
Lekarze powinni zachować czujność pod kątem możliwego rozwoju zapalenia płuc u pacjentów z POChP, ponieważ kliniczne objawy zapalenia płuc i zaostrzeń często się pokrywają. Infekcje dolnych dróg oddechowych, w tym zapalenie płuc, zgłaszano po wziewnym podaniu kortykosteroidów.
6-miesięcznym badaniu czynności płuc obejmującym 1704 pacjentów z POChP stwierdzono częstsze występowanie infekcji płuc innych niż zapalenie płuc (np. zapalenie oskrzeli, wirusowe infekcje dolnych dróg oddechowych itp.) u pacjentów otrzymujących SYMBICORT 160/4,5 (7,6%) niż u osób otrzymujących SYMBICORT 80/4,5 (3,2%), formoterol 4,5 mcg (4,6%) lub placebo (3,3%). Zapalenie płuc nie występowało z większą częstością w grupie SYMBICORT 160/4,5 (1,1%) w porównaniu z placebo (1,3%). W 12-miesięcznym badaniu czynności płuc z udziałem 1964 pacjentów z POChP stwierdzono również większą częstość występowania zakażeń płuc innych niż zapalenie płuc u pacjentów otrzymujących SYMBICORT 160/4,5 (8,1%) niż u pacjentów otrzymujących SYMBICORT 80/4,5 (6,9%), formoterol 4,5 mcg (7,1%) lub placebo (6,2%). Podobnie jak w 6-miesięcznym badaniu, zapalenie płuc nie występowało z większą częstością w grupie SYMBICORT 160/4,5 (4,0%) w porównaniu z placebo (5,0%).
Immunosupresja
Pacjenci przyjmujący leki hamujące układ odpornościowy są bardziej podatni na infekcje niż osoby zdrowe. Na przykład ospa wietrzna i odra mogą mieć bardziej poważny, a nawet śmiertelny przebieg u podatnych dzieci lub dorosłych stosujących kortykosteroidy. W przypadku takich dzieci lub osób dorosłych, które nie miały tych chorób lub nie zostały odpowiednio zaszczepione, należy zachować szczególną ostrożność, aby uniknąć narażenia. Nie wiadomo, w jaki sposób dawka, droga i czas podawania kortykosteroidów wpływają na ryzyko rozwoju rozsianego zakażenia. Nie jest również znany wpływ choroby podstawowej i/lub wcześniejszego leczenia kortykosteroidami na ryzyko. W przypadku narażenia wskazane może być leczenie immunoglobuliną przeciwko ospie wietrznej i półpaścowi (VZIG) lub połączonej immunoglobuliny dożylnej (IVIG). W przypadku narażenia na odrę, może być wskazana profilaktyka za pomocą puli immunoglobulin domięśniowych (IG) (pełne informacje dotyczące przepisywania VZIG i IG znajdują się w odpowiednich ulotkach informacyjnych). Jeśli rozwinie się ospa wietrzna, można rozważyć leczenie środkami przeciwwirusowymi. Odpowiedź immunologiczną na szczepionkę przeciwko ospie wietrznej oceniano u dzieci i młodzieży z astmą w wieku od 12 miesięcy do 8 lat stosujących budezonid w postaci zawiesiny do inhalacji.
otwartym, nierandomizowanym badaniu klinicznym oceniano odpowiedź immunologiczną na szczepionkę przeciwko ospie wietrznej u 243 pacjentów z astmą w wieku od 12 miesięcy do 8 lat, którzy byli leczeni budezonidem w postaci zawiesiny do inhalacji w dawce 0,25 mg do 1 mg na dobę (n=151) lub na astmę niekortykosteroidową (n =92) (tj. beta2-agoniści, antagoniści receptora leukotrienowego, kromony). Odsetek pacjentów, u których wystąpiło miano przeciwciał seroprotekcyjnych >5,0 (wartość gpELISA) w odpowiedzi na szczepienie, był podobny u pacjentów leczonych wziewną zawiesiną budezonidu (85%) w porównaniu do pacjentów leczonych astmą niekortykosteroidową (90%). U żadnego pacjenta leczonego budezonidem w postaci zawiesiny do inhalacji nie rozwinęła się ospa wietrzna w wyniku szczepienia.
Kortykosteroidy wziewne należy stosować ostrożnie, jeśli w ogóle, u pacjentów z czynną lub nieaktywną gruźlicą dróg oddechowych; nieleczone ogólnoustrojowe zakażenia grzybicze, bakteryjne, wirusowe lub pasożytnicze; lub opryszczka oczna.
Przenoszenie pacjentów z terapii kortykosteroidami systemowymi
Szczególną ostrożność należy zachować u pacjentów, którzy zostali przeniesieni z kortykosteroidów działających ogólnoustrojowo na kortykosteroidy wziewne, ponieważ u pacjentów z astmą podczas i po zmianie z kortykosteroidów ogólnoustrojowych na kortykosteroidy wziewne o mniejszej dostępności ogólnoustrojowej dochodziło do zgonów z powodu niewydolności nadnerczy. Po odstawieniu kortykosteroidów ogólnoustrojowych do przywrócenia czynności podwzgórzowo-przysadkowo-nadnerczowej (HPA) potrzeba kilku miesięcy.
Pacjenci, którzy wcześniej otrzymywali prednizon w dawce 20 mg lub więcej na dobę (lub jego odpowiednik), mogą być najbardziej podatni, szczególnie gdy ich ogólnoustrojowe kortykosteroidy zostały prawie całkowicie odstawione. W tym okresie supresji HPA pacjenci mogą wykazywać oznaki i objawy niewydolności nadnerczy, gdy są narażeni na uraz, zabieg chirurgiczny lub infekcję (szczególnie zapalenie żołądka i jelit) lub inne stany związane z ciężką utratą elektrolitów. Chociaż SYMBICORT może zapewnić kontrolę objawów astmy podczas tych epizodów, w zalecanych dawkach dostarcza układowo mniej niż normalne fizjologiczne ilości glikokortykosteroidów i NIE zapewnia aktywności mineralokortykoidów niezbędnej do radzenia sobie z tymi nagłymi przypadkami.
okresach stresu, ciężkiego ataku astmy lub ciężkiego zaostrzenia POChP pacjentów, którym odstawiono kortykosteroidy ogólnoustrojowe, należy poinstruować, aby natychmiast wznowili podawanie doustnych kortykosteroidów (w dużych dawkach) i skontaktowali się z lekarzem w celu uzyskania dalszych instrukcji. Pacjentów tych należy również poinstruować, aby mieli przy sobie kartę ostrzegawczą wskazującą, że mogą potrzebować uzupełniających kortykosteroidów ogólnoustrojowych w okresach stresu, ciężkiego ataku astmy lub ciężkiego zaostrzenia POChP.
Pacjenci wymagający doustnych kortykosteroidów powinni być powoli odzwyczajani od stosowania kortykosteroidów ogólnoustrojowych po przejściu na SYMBICORT. Zmniejszenie prednizonu można osiągnąć zmniejszając dobową dawkę prednizonu o 2,5 mg raz w tygodniu podczas leczenia produktem SYMBICORT. Podczas odstawiania doustnych kortykosteroidów należy dokładnie monitorować czynność płuc (średnia natężona objętość wydechowa w ciągu 1 sekundy [FEV1] lub poranny szczytowy przepływ wydechowy [PEF]), stosowanie beta-agonistów oraz objawy astmy lub POChP. Ponadto pacjentów należy obserwować pod kątem oznak i objawów niewydolności nadnerczy, takich jak zmęczenie, zmęczenie, osłabienie, nudności i wymioty oraz niedociśnienie.
Przeniesienie pacjentów z terapii kortykosteroidami systemowymi na kortykosteroidy wziewne lub SYMBICORT może ujawnić stany uprzednio tłumione przez leczenie kortykosteroidami systemowymi (np. nieżyt nosa, zapalenie spojówek, egzema, zapalenie stawów, stany eozynofilowe). U niektórych pacjentów mogą wystąpić objawy odstawienia czynnego układowo kortykosteroidów (np. ból stawów i (lub) mięśni, zmęczenie, depresja) pomimo utrzymania lub nawet poprawy czynności układu oddechowego.
Hiperkortyka i zahamowanie czynności kory nadnerczy
Budezonid, składnik preparatu SYMBICORT, często pomaga kontrolować objawy astmy i POChP przy mniejszym tłumieniu czynności HPA niż terapeutycznie równoważne doustne dawki prednizonu. Ponieważ budezonid jest wchłaniany do krążenia i może działać ogólnoustrojowo w większych dawkach, korzystnych efektów działania produktu SYMBICORT w zakresie minimalizowania dysfunkcji HPA można oczekiwać tylko wtedy, gdy nie są przekraczane zalecane dawki, a u poszczególnych pacjentów miareczkuje się najmniejszą skuteczną dawkę.
Ze względu na możliwość ogólnoustrojowego wchłaniania kortykosteroidów wziewnych, pacjentów leczonych produktem SYMBICORT 160 mg należy uważnie obserwować pod kątem oznak ogólnoustrojowego działania kortykosteroidów. Szczególną ostrożność należy zachować podczas obserwacji pacjentów po operacji lub w okresach stresu pod kątem oznak niewystarczającej odpowiedzi nadnerczy.
Możliwe jest, że u niewielkiej liczby pacjentów mogą wystąpić ogólnoustrojowe działania kortykosteroidów, takie jak hiperkortyza i zahamowanie czynności kory nadnerczy (w tym przełom nadnerczowy), zwłaszcza gdy budezonid podawany jest w dawkach większych niż zalecane przez dłuższy czas. Jeśli wystąpią takie objawy, dawkę produktu SYMBICORT należy zmniejszać powoli, zgodnie z przyjętymi procedurami ograniczania kortykosteroidów ogólnoustrojowych i postępowania w przypadku objawów astmy.
Interakcje leków z silnymi inhibitorami cytochromu P450 3A4
Należy zachować ostrożność rozważając jednoczesne podawanie produktu SYMBICORT 4,5 µg z ketokonazolem i innymi znanymi silnymi inhibitorami CYP3A4 (np. rytonawirem, atazanawirem, klarytromycyną, indynawirem, itrakonazolem, nefazodonem, nelfinawirem, sakwinawirem, telitromycyną), ponieważ do budezonidu może wystąpić [patrz INTERAKCJE Z LEKAMI oraz FARMAKOLOGIA KLINICZNA ].
Paradoksalny skurcz oskrzeli i objawy górnych dróg oddechowych
Podobnie jak w przypadku innych leków wziewnych, SYMBICORT 160 mg może wywołać paradoksalny skurcz oskrzeli, który może zagrażać życiu. Jeśli po podaniu 160 mg produktu SYMBICORT wystąpi paradoksalny skurcz oskrzeli, należy natychmiast zastosować wziewny, krótko działający lek rozszerzający oskrzela, należy natychmiast odstawić produkt SYMBICORT i zastosować alternatywne leczenie.
Natychmiastowe reakcje nadwrażliwości
Po podaniu produktu SYMBICORT 160 mg mogą wystąpić natychmiastowe reakcje nadwrażliwości, czego dowodem są przypadki pokrzywki, obrzęku naczynioruchowego, wysypki i skurczu oskrzeli.
Wpływ na układ sercowo-naczyniowy i ośrodkowy układ nerwowy
Nadmierna stymulacja beta-adrenergiczna była związana z drgawkami, dusznicą bolesną, nadciśnieniem lub niedociśnieniem, tachykardią z częstością do 200 uderzeń/min, arytmiami, nerwowością, bólem głowy, drżeniem, kołataniem serca, nudnościami, zawrotami głowy, zmęczeniem, złym samopoczuciem i bezsennością [patrz PRZEDAWKOWANIE ]. Dlatego SYMBICORT 160 mg, podobnie jak wszystkie produkty zawierające aminy sympatykomimetyczne, należy stosować ostrożnie u pacjentów z zaburzeniami sercowo-naczyniowymi, zwłaszcza niewydolnością wieńcową, zaburzeniami rytmu serca i nadciśnieniem.
Formoterol, składnik preparatu SYMBICORT, może wywoływać klinicznie istotne działanie sercowo-naczyniowe u niektórych pacjentów, mierzone na podstawie częstości tętna, ciśnienia krwi i (lub) objawów. Chociaż takie działania są rzadkie po podaniu formoterolu w zalecanych dawkach, jeśli wystąpią, może być konieczne odstawienie leku. Ponadto doniesiono, że beta-agoniści wywołują zmiany w EKG, takie jak spłaszczenie załamka T, wydłużenie odstępu QTc i obniżenie odcinka ST. Kliniczne znaczenie tych wyników nie jest znane. Zgłaszano przypadki zgonów w związku z nadmiernym stosowaniem wziewnych leków sympatykomimetycznych.
Zmniejszenie gęstości mineralnej kości
Podczas długotrwałego podawania produktów zawierających wziewne kortykosteroidy obserwowano zmniejszenie gęstości mineralnej kości (BMD). Kliniczne znaczenie niewielkich zmian BMD w odniesieniu do odległych konsekwencji, takich jak złamania, jest nieznane. Pacjenci z głównymi czynnikami ryzyka zmniejszonej zawartości minerałów w kości, takimi jak długotrwałe unieruchomienie, osteoporoza w wywiadzie rodzinnym, stan pomenopauzalny, palenie tytoniu, podeszły wiek, złe odżywianie lub przewlekłe stosowanie leków, które mogą zmniejszać masę kostną (np. leki przeciwdrgawkowe, doustne kortykosteroidy ) należy monitorować i leczyć z zachowaniem ustalonych standardów opieki. Ponieważ u pacjentów z POChP często występuje wiele czynników ryzyka obniżonego BMD, zaleca się ocenę BMD przed rozpoczęciem leczenia SYMBICORT 160 mg, a następnie okresowo. Jeśli obserwuje się znaczne zmniejszenie BMD, a SYMBICORT jest nadal uważany za ważny z medycznego punktu widzenia w leczeniu POChP u danego pacjenta, należy zdecydowanie rozważyć zastosowanie leków do leczenia lub zapobiegania osteoporozie.
Wpływ leczenia SYMBICORT 160/4,5, SYMBICORT 80/4,5, formoterolem 4,5 mcg lub placebo na BMD oceniano w podgrupie 326 pacjentów (kobiety i mężczyźni w wieku 41 do 88 lat) z POChP w 12-miesięcznej czynności płuc nauka. Ocenę BMD regionu biodrowego i lędźwiowego kręgosłupa przeprowadzono na początku i 52 tygodniach przy użyciu skanów absorpcjometrii rentgenowskiej o podwójnej energii (DEXA). Średnie zmiany BMD od wartości początkowej do zakończenia leczenia były niewielkie (średnie zmiany wahały się od -0,01 -0,01 g/cm²). Wyniki ANCOVA dla całkowitego BMD kręgosłupa i całkowitego BMD w oparciu o punkt czasowy zakończenia leczenia wykazały, że wszystkie proporcje geometryczne średniej LS dla porównań parami grup leczenia były bliskie 1, co wskazuje, że ogólnie BMD dla całkowitego obszaru biodra i całego kręgosłupa dla 12 -miesiąc był stabilny przez cały okres leczenia.
Wpływ na wzrost
Kortykosteroidy wziewne doustnie mogą powodować spowolnienie wzrostu, gdy są podawane pacjentom pediatrycznym. Monitoruj wzrost pacjentów pediatrycznych rutynowo otrzymujących SYMBICORT (np. za pomocą stadiometrii). Aby zminimalizować ogólnoustrojowe działanie kortykosteroidów wziewnych doustnie, w tym SYMBICORT, należy miareczkować dawkę każdego pacjenta do najniższej dawki, która skutecznie kontroluje jego/jej objawy [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz Używaj w określonych populacjach ].
Jaskra i zaćma
U pacjentów z astmą i POChP po długotrwałym podawaniu wziewnych kortykosteroidów, w tym budezonidu, składnika produktu SYMBICORT, zgłaszano występowanie jaskry, zwiększonego ciśnienia wewnątrzgałkowego i zaćmy. W związku z tym uzasadnione jest ścisłe monitorowanie pacjentów ze zmianami widzenia lub z wywiadem podwyższonego ciśnienia śródgałkowego, jaskry i (lub) zaćmy.
Wpływ leczenia SYMBICORT 160/4,5, SYMBICORT 80/4,5, formoterolem 4,5 mcg lub placebo na rozwój zaćmy lub jaskry oceniano w podgrupie 461 pacjentów z POChP w 12-miesięcznym badaniu czynności płuc. Badania okulistyczne przeprowadzono na początku badania, po 24 tygodniach i 52 tygodniach. W randomizowanym okresie leczenia wystąpiło 26 pacjentów (6%) ze wzrostem wyniku podtorebkowego w tylnej części od wartości początkowej do wartości maksymalnej (>0,7). Zmiany w punktacji tylnej części podtorebkowej >0,7 od wartości początkowej do maksimum leczenia wystąpiły u 11 pacjentów (9,0%) w grupie SYMBICORT 160/4,5, 4 pacjentów (3,8%) w grupie SYMBICORT 80/4,5, 5 pacjentów (4,2%) w w grupie formoterolu i 6 pacjentów (5,2%) w grupie placebo.
Choroby eozynofilowe i zespół Churga-Straussa
rzadkich przypadkach u pacjentów przyjmujących wziewne kortykosteroidy mogą wystąpić ogólnoustrojowe choroby eozynofilowe. Niektórzy z tych pacjentów mają kliniczne cechy zapalenia naczyń zgodne z zespołem Churga-Straussa, stanem często leczonym ogólnoustrojową terapią kortykosteroidami. Zdarzenia te zwykle, ale nie zawsze, były związane ze zmniejszeniem i/lub odstawieniem leczenia kortykosteroidami doustnymi po wprowadzeniu kortykosteroidów wziewnych. Lekarze powinni być wyczuleni na eozynofilię, wysypkę naczyniową, nasilenie objawów ze strony płuc, powikłania sercowe i/lub neuropatię u swoich pacjentów. Nie ustalono związku przyczynowego między budezonidem a tymi podstawowymi warunkami.
Współistniejące warunki
SYMBICORT 4,5 mcg, podobnie jak wszystkie leki zawierające aminy sympatykomimetyczne, należy stosować ostrożnie u pacjentów z drgawkami lub tyreotoksykozą oraz u tych, którzy wykazują niezwykłą reakcję na aminy sympatykomimetyczne. Istnieją doniesienia, że dawki albuterolu, agonisty receptorów beta2-adrenergicznych, podawanego dożylnie, nasilają istniejącą wcześniej cukrzycę i kwasicę ketonową.
Hipokaliemia i hiperglikemia
Leki będące agonistami receptorów beta-adrenergicznych mogą wywoływać u niektórych pacjentów znaczną hipokaliemię, prawdopodobnie poprzez przeciek wewnątrzkomórkowy, co może powodować niepożądane skutki sercowo-naczyniowe [patrz FARMAKOLOGIA KLINICZNA ]. Spadek stężenia potasu w surowicy jest zwykle przemijający, niewymagający suplementacji. Klinicznie istotne zmiany stężenia glukozy we krwi i (lub) potasu w surowicy były rzadko obserwowane podczas badań klinicznych produktu SYMBICORT w zalecanych dawkach.
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( INFORMACJE DLA PACJENTA i instrukcje użytkowania ).
Poważne zdarzenia związane z astmą
Poinformuj pacjentów z astmą, że LABA stosowana samodzielnie zwiększa ryzyko związanej z astmą hospitalizacji lub zgonu z powodu astmy. Dostępne dane pokazują, że gdy ICS i LABA są stosowane razem, na przykład z SYMBICORT, nie ma znaczącego wzrostu ryzyka tych zdarzeń.
Nie na ostre objawy
Poinformuj pacjentów, że SYMBICORT 160 mg nie jest przeznaczony do łagodzenia ostrych objawów astmy lub POChP i nie należy w tym celu stosować dodatkowych dawek. Należy doradzić pacjentom leczenie ostrych objawów za pomocą wziewnego, krótko działającego beta2-mimetyku, takiego jak albuterol. Zapewnij pacjentom takie leki i poinstruuj ich, w jaki sposób należy je stosować.
Poinstruuj pacjentów, aby natychmiast zwrócili się o pomoc lekarską, jeśli wystąpią którekolwiek z poniższych:
- Zmniejszenie skuteczności wziewnych, krótko działających beta2-mimetyków
- Potrzeba większej liczby inhalacji niż zwykle w przypadku wziewnych, krótko działających beta2-mimetyków
- Znaczący spadek czynności płuc zgodnie z zaleceniami lekarza
Należy poinformować pacjentów, że nie powinni przerywać leczenia produktem SYMBICORT bez wskazówek lekarza lub świadczeniodawcy, ponieważ objawy mogą powrócić po przerwaniu leczenia.
Nie używaj dodatkowych długo działających beta2-mimetyków
Poinstruuj pacjentów, aby nie stosowali innych LABA w astmie i POChP.
Efekty lokalne
Należy poinformować pacjentów, że u niektórych pacjentów wystąpiły zlokalizowane zakażenia Candida albicans w jamie ustnej i gardle. Jeśli rozwinie się kandydoza jamy ustnej i gardła, należy ją leczyć odpowiednią miejscową lub ogólnoustrojową (tj. doustną) terapią przeciwgrzybiczą, kontynuując leczenie produktem SYMBICORT 4,5 mcg, ale czasami konieczne może być czasowe przerwanie leczenia produktem SYMBICORT pod ścisłą kontrolą lekarską. Zaleca się płukanie ust wodą bez połykania po inhalacji, aby zmniejszyć ryzyko pleśniawki.
Zapalenie płuc
Pacjenci z POChP mają większe ryzyko zapalenia płuc; poinstruuj ich, aby skontaktowali się ze swoim lekarzem, jeśli wystąpią u nich objawy zapalenia płuc.
Immunosupresja
Ostrzeż pacjentów, którzy przyjmują immunosupresyjne dawki kortykosteroidów, aby unikali narażenia na ospę wietrzną lub odrę, a w przypadku narażenia niezwłocznie skonsultuj się z lekarzem. Poinformuj pacjentów o potencjalnym pogorszeniu istniejącej gruźlicy, infekcji grzybiczych, bakteryjnych, wirusowych lub pasożytniczych lub opryszczki ocznej.
Hiperkortyka i zahamowanie czynności kory nadnerczy
Należy poinformować pacjentów, że SYMBICORT może powodować ogólnoustrojowe działanie kortykosteroidów w postaci hiperkortycyzmu i zahamowania czynności kory nadnerczy. Dodatkowo należy poinformować pacjentów, że zgony z powodu niewydolności nadnerczy miały miejsce w trakcie i po przejściu z kortykosteroidów ogólnoustrojowych. Pacjenci powinni powoli odstawiać kortykosteroidy ogólnoustrojowe w przypadku przejścia na SYMBICORT.
Zmniejszenie gęstości mineralnej kości
Należy doradzić pacjentom, u których występuje zwiększone ryzyko zmniejszenia BMD, że stosowanie kortykosteroidów może stwarzać dodatkowe ryzyko.
Zmniejszona prędkość wzrostu
Należy poinformować pacjentów, że kortykosteroidy wziewne doustnie, składnik preparatu SYMBICORT, mogą powodować spowolnienie wzrostu, gdy są podawane dzieciom. Lekarze powinni uważnie śledzić rozwój dzieci i młodzieży przyjmujących kortykosteroidy dowolną drogą.
Efekty na oczy
Długotrwałe stosowanie wziewnych kortykosteroidów może zwiększać ryzyko niektórych problemów z oczami (zaćmy lub jaskry); rozważ regularne badania wzroku.
Ryzyko związane z terapią beta-agonistami
Poinformuj pacjentów o działaniach niepożądanych związanych z beta2agonistami, takich jak kołatanie serca, ból w klatce piersiowej, szybkie bicie serca, drżenie lub nerwowość.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Budezonid
Przeprowadzono długoterminowe badania na szczurach i myszach po podaniu doustnym w celu oceny potencjalnego działania rakotwórczego budezonidu.
2-letnim badaniu na szczurach rasy Sprague-Dawley budezonid powodował statystycznie istotny wzrost częstości występowania glejaków u samców szczurów po podaniu doustnym dawki 50 μg/kg (w przybliżeniu równoważnej MRHDID u dorosłych i dzieci na mcg/m2 pc. podstawa). Nie zaobserwowano rakotwórczości u samców i samic szczurów po podaniu odpowiednich dawek doustnych do 25 i 50 mcg/kg (w przybliżeniu równoważne MRHDID u dorosłych i dzieci w mcg/m²). W dwóch dodatkowych dwuletnich badaniach na samcach szczurów Fischer i Sprague-Dawley budezonid nie powodował glejaków w dawce doustnej 50 μg/kg (w przybliżeniu równoważnej MRHDID u dorosłych i dzieci w mcg/m²). Jednak u samców szczurów rasy Sprague-Dawley budezonid powodował statystycznie istotny wzrost częstości występowania guzów wątrobowokomórkowych po podaniu doustnym dawki 50 µg/kg (w przybliżeniu równoważnej MRHDID u dorosłych i dzieci w przeliczeniu na mcg/m²). Jednoczesne referencyjne kortykosteroidy (prednizolon i acetonid triamcynolonu) w tych dwóch badaniach wykazały podobne wyniki.
91-tygodniowym badaniu na myszach budezonid nie powodował rakotwórczości związanej z leczeniem w dawkach doustnych do 200 μg/kg (około 2 razy większe niż MRHDID u dorosłych i dzieci w przeliczeniu na μg/m2).
Budezonid nie wykazywał działania mutagennego ani klastogennego w sześciu różnych testach: test Ames Salmonella/płytka mikrosomowa, test mikrojądrowy u myszy, test chłoniaka u myszy, test aberracji chromosomowych w ludzkich limfocytach, test letalny recesywny sprzężony z płcią u Drosophila melanogaster oraz analiza naprawy DNA u szczura hodowla hepatocytów.
Płodność i zdolności reprodukcyjne szczurów nie miały wpływu na dawki podskórne do 80 mcg/kg (w przybliżeniu równe MRHDID na podstawie mcg/m²). Spowodowało to jednak zmniejszenie żywotności prenatalnej i żywotności u szczeniąt przy urodzeniu i podczas laktacji, wraz ze spadkiem przyrostu masy ciała matki, przy podskórnych dawkach 20 mcg/kg i większych (mniej niż MRHDID na podstawie mcg/m²). ). Nie odnotowano takich efektów przy 5 mcg/kg (mniej niż MRHDID na podstawie mcg/m²).
Formoterol
Przeprowadzono długoterminowe badania na myszach po podaniu doustnym i szczurach po podaniu wziewnym w celu oceny potencjalnego działania rakotwórczego fumaranu formoterolu.
W 24-miesięcznym badaniu rakotwórczości u myszy CD-1, formoterol w dawkach doustnych 100 mcg/kg i większych (około 30 i 15-krotność MRHDID odpowiednio u dorosłych i dzieci, w przeliczeniu na mcg/m²) powodował: związany z tym wzrost częstości występowania mięśniaków gładkokomórkowych macicy.
W 24-miesięcznym badaniu rakotwórczości u szczurów rasy Sprague-Dawley zaobserwowano zwiększoną częstość występowania mięśniaka gładkokomórkowego śródbłonka i mięśniakomięsaka gładkokomórkowego macicy po podaniu wziewnej dawki 130 µg/kg (około 70 i 35 razy większej niż MRHDID, odpowiednio u dorosłych i dzieci, w mcg/m²). Nie zaobserwowano guzów przy 22 mcg/kg (około 12 i 6 razy więcej niż MRHDID u dorosłych i dzieci odpowiednio w mcg/m²).
Inne beta-agonistyczne leki w podobny sposób wykazywały wzrost liczby mięśniaków gładkich dróg rodnych u samic gryzoni. Znaczenie tych wyników dla stosowania u ludzi nie jest znane.
Formoterol nie wykazywał działania mutagennego ani klastogennego w teście Amesa na obecność salmonelli/płytek mikrosomowych, teście chłoniaka myszy, teście aberracji chromosomowych w ludzkich limfocytach i teście mikrojądrowym u szczura.
samców szczurów leczonych formoterolem w dawce doustnej 15 000 mcg/kg (około 2200-krotność MRHDID na podstawie AUC) stwierdzono zmniejszenie płodności i (lub) zdolności rozrodczej. Nie zaobserwowano takiego efektu przy 3000 mcg/kg (około 1600 razy MRHDID na podstawie mcg/m²). W oddzielnym badaniu z udziałem samców szczurów, którym podawano doustną dawkę 15 000 mcg/kg (około 8000 razy większą od MRHDID na podstawie mcg/m²), stwierdzono atrofię kanalików jąder i resztki nasienia w jądrach oraz oligospermię w najądrzach. Nie wykryto wpływu na płodność u samic szczurów przy dawkach do 15 000 mcg/kg (około 1100-krotność MRHDID na podstawie AUC).
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
Nie ma odpowiednich i dobrze kontrolowanych badań SYMBICORT 160 mg lub jednego z jego poszczególnych składników, fumaranu formoterolu, u kobiet w ciąży; dostępne są jednak badania dla drugiego składnika budezonidu. W badaniach reprodukcji na zwierzętach SYMBICORT 4,5 µg, podawany drogą wziewną, wykazywał działanie teratogenne, embriobójcze i zmniejszał masę płodów u szczurów w dawkach mniejszych niż maksymalna zalecana dobowa dawka dobowa dla człowieka (MRHDID) w przeliczeniu na µg/m². Sam budezonid, podawany drogą podskórną, wykazywał działanie teratogenne, embriobójcze i zmniejszał masę płodów u szczurów i królików przy dawce mniejszej niż MRHDID, ale tych działań nie obserwowano u szczurów, które otrzymały wziewne dawki do 4 razy większe niż MRHDID. Badania kobiet w ciąży nie wykazały, aby sam wziewny budezonid zwiększał ryzyko nieprawidłowości w przypadku podawania w czasie ciąży. Doświadczenie z doustnymi kortykosteroidami sugeruje, że gryzonie są bardziej podatne na działanie teratogenne w wyniku ekspozycji na kortykosteroidy niż ludzie. Sam fumaran formoterolu, podawany drogą doustną, wykazywał działanie teratogenne u szczurów i królików w dawce odpowiednio 1600 i 65 000 razy większej niż MRHDID. Fumaran formoterolu wykazywał również działanie embriocydowe, zwiększając utratę potomstwa po urodzeniu i podczas laktacji oraz zmniejszając masę potomstwa u szczurów przy 110-krotności MRHDID. Te działania niepożądane występowały na ogół przy dużych wielokrotnościach MRHDID, gdy fumaran formoterolu podawano drogą doustną w celu uzyskania dużej ekspozycji ogólnoustrojowej. Nie zaobserwowano działania teratogennego, embriobójczego ani rozwojowego u szczurów, które otrzymały dawki wziewne do 375 razy większe niż MRHDID.
Szacowane ryzyko tła poważnych wad wrodzonych i poronienia we wskazanych populacjach jest nieznane. W ogólnej populacji Stanów Zjednoczonych szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2% do 4% i 15% do 20%.
Rozważania kliniczne
Związane z chorobą ryzyko u matki i/lub zarodka/płodu
U kobiet ze słabo lub umiarkowanie kontrolowaną astmą istnieje zwiększone ryzyko kilku działań niepożądanych w okresie okołoporodowym, takich jak stan przedrzucawkowy u matki i wcześniactwo, niska masa urodzeniowa i niski wiek ciążowy u noworodka. Kobiety ciężarne z astmą powinny być ściśle monitorowane, aw razie potrzeby dostosowywane leki w celu utrzymania optymalnej kontroli astmy.
Praca lub dostawa
Nie ma dobrze kontrolowanych badań na ludziach, w których oceniano działanie produktu SYMBICORT 4,5 mcg podczas porodu i porodu. Ze względu na możliwość wpływu beta-agonistów na kurczliwość macicy, stosowanie produktu SYMBICORT 4,5 mikrograma podczas porodu należy ograniczyć do tych pacjentek, u których korzyści wyraźnie przewyższają ryzyko.
Dane
Dane ludzkie
Badania kobiet w ciąży nie wykazały, aby wziewny budezonid zwiększał ryzyko nieprawidłowości w przypadku podawania w okresie ciąży. Wyniki dużego, populacyjnego, prospektywnego kohortowego badania epidemiologicznego, oceniającego dane z trzech szwedzkich rejestrów obejmujących około 99% ciąż z lat 1995-1997 (tj. Szwedzki Rejestr Urodzeń Medycznych; Rejestr Wad Wrodzonych; Rejestr Kardiologii Dziecięcej) wskazują na brak zwiększonego ryzyka w przypadku wad wrodzonych po zastosowaniu wziewnego budezonidu we wczesnej ciąży. Wady wrodzone badano u dzieci urodzonych w 2014 roku przez matki zgłaszające stosowanie wziewnego budezonidu w leczeniu astmy we wczesnej ciąży (zwykle 10-12 tygodni po ostatniej miesiączce), okresie, w którym występuje większość poważnych wad rozwojowych narządów. Odsetek stwierdzonych wad wrodzonych był podobny w porównaniu z populacją ogólną (odpowiednio 3,8% vs 3,5%). Ponadto, po ekspozycji na budezonid wziewny, liczba niemowląt urodzonych z rozszczepami twarzoczaszki była podobna do oczekiwanej liczby w normalnej populacji (odpowiednio 4 dzieci vs. 3,3).
Te same dane wykorzystano w drugim badaniu obejmującym łącznie 2534 niemowląt, których matki były narażone na wdychany budezonid. W tym badaniu odsetek wad wrodzonych u niemowląt, których matki były narażone na wdychany budezonid we wczesnej ciąży, nie różnił się od odsetka wszystkich noworodków w tym samym okresie (3,6%).
Dane zwierząt
SYMBORYT
W badaniu rozwoju embrionalnego i płodowego u ciężarnych szczurów, którym podawano dawki w okresie organogenezy od 6 do 16 dnia ciąży, SYMBICORT 160 mg powodował przepuklinę pępkową u płodów w dawkach mniejszych niż MRHDID (w przeliczeniu na mcg/m² przy dawkach wziewnych 12/ 0,66 mcg/kg/dzień i więcej). Masy płodów zmniejszyły się odpowiednio przy około 5 i 3 razy MRHDID (na podstawie AUC przy dawce wziewnej 80/4,4 µg/kg u matki (budezonid/formoterol)). Nie wykryto działania teratogennego ani embriobójczego przy dawkach mniejszych niż MRHDID (w przeliczeniu na mcg/m² przy dawce wziewnej 2,5/0,14 mcg/kg/dobę dla matki).
Budezonid
badaniu płodności i reprodukcji samcom szczurów podawano podskórnie dawki przez 9 tygodni, a samicom przez 2 tygodnie przed parowaniem i przez cały okres krycia. Samicom podawano dawki do czasu odsadzenia ich potomstwa. Budezonid w dawkach mniejszych niż MRHDID (w przeliczeniu na mcg/m2 przy podskórnych dawkach 20 mcg/ kg/dzień i więcej). Nie zaobserwowano takich efektów przy dawce mniejszej niż MRHDID (w przeliczeniu na mcg/m² przy podskórnej dawce matczynej wynoszącej 5 mcg/kg/dzień).
badaniu dotyczącym rozwoju zarodka i płodu u ciężarnych królików, którym podawano dawki w okresie organogenezy od 6 do 18 dnia ciąży, budezonid powodował utratę płodu, zmniejszenie masy płodu i nieprawidłowości szkieletu w dawkach mniejszych niż MRHDID (w przeliczeniu na mcg/m2 dawka podskórna matki 25 mcg/kg/dobę). W badaniu dotyczącym rozwoju zarodka i płodu u ciężarnych szczurów, którym podawano budezonid w okresie organogenezy od 6 do 15 dnia ciąży, budezonid wywoływał podobne niekorzystne działanie na płód w dawkach około 8-krotnie większych niż MRHDID (w przeliczeniu na mcg/m² przy dawce 500 podawanej podskórnie matce). mcg/kg/dzień). W innym badaniu dotyczącym rozwoju zarodka i płodu u ciężarnych szczurów nie zaobserwowano działania teratogennego ani embriobójczego przy dawkach do 4 razy większych od MRHDID (w przeliczeniu na mcg/m² przy dawkach wziewnych do 250 mcg/kg mc./dobę u matki).
badaniu rozwoju około- i poporodowego szczurom, którym podawano od 15. dnia ciąży do 21. dnia poporodowego budezonid, nie miał wpływu na poród, ale miał wpływ na wzrost i rozwój potomstwa. Przeżycie potomstwa było zmniejszone, a potomstwo, które przeżyło, miało zmniejszoną średnią masę ciała przy urodzeniu i podczas laktacji przy dawkach mniejszych niż MRHDID i wyższych (w przeliczeniu na mcg/m² przy dawkach podskórnych matki 20 mcg/kg/dobę i wyższych). Wyniki te wystąpiły w obecności toksyczności matczynej.
Formoterol
badaniu płodności i reprodukcji samcom szczurów podawano doustnie przez 9 tygodni, a samicom przez 2 tygodnie przed parowaniem i przez cały okres krycia. Samice otrzymywały dawki do 19. dnia ciąży lub do odsadzenia ich potomstwa. Samce otrzymywały dawkę do 25 tygodni. Przepuklinę pępkową obserwowano u płodów szczurów przy dawkach doustnych 1600 razy i większych niż MRHDID (w przeliczeniu na mcg/m² przy doustnych dawkach matki 3000 mcg/kg/dobę i wyższych). Brachygnatia była obserwowana u płodów szczurów po dawce 8000 razy większej niż MRHDID (w przeliczeniu na mcg/m² przy dawce doustnej wynoszącej 15 000 mcg/kg mc./dobę dla matki). Ciąża została przedłużona przy dawce 8000 razy większej niż MRHDID (w przeliczeniu na mcg/m2 przy doustnej dawce matki wynoszącej 15 000 mcg/kg/dobę). Zgony płodów i młodych występowały po dawkach około 1600 razy większych od MRHDID i wyższych (w przeliczeniu na mcg/m2 przy dawkach doustnych 3000 mcg/kg/dobę i wyższych) podczas ciąży.
badaniu dotyczącym rozwoju zarodka i płodu u ciężarnych samic szczura, którym podawano dawki w okresie organogenezy od 6 do 15 dnia ciąży, nie zaobserwowano działania teratogennego, embriobójczego ani rozwojowego przy dawkach do 375 razy większych od MRHDID (w przeliczeniu na mcg/m² z inhalacją matczyną). dawki do 690 mcg/kg/dobę).
W badaniu rozwoju zarodkowo-płodowego u ciężarnych królików, którym podawano dawkę w okresie organogenezy od 6-18 dnia ciąży, torbiele podtorebkowe na wątrobie obserwowano u płodów w dawce 65 000 razy większej niż MRHDID (w mcg/m² u matki dawka doustna 60 000 mcg/kg/dobę). Nie zaobserwowano działania teratogennego przy dawkach do 3800 razy większych niż MRHDID (w przeliczeniu na mcg/m² przy dawkach doustnych do 3500 mcg/kg/dobę u matki).
badaniu rozwoju przed- i pourodzeniowego ciężarne samice szczurów otrzymywały formoterol w dawkach doustnych 0, 210, 840 i 3400 µg/kg/dobę od 6. dnia ciąży do okresu laktacji. Przeżycie potomstwa zmniejszyło się od urodzenia do 26. dnia poporodowego przy dawkach 110 razy większych niż MRHDID i wyższych (w przeliczeniu na mcg/m² przy doustnych dawkach matczynych 210 mcg/kg/dobę i wyższych), chociaż nie było dowodów na odpowiedź na dawkę relacja. Nie stwierdzono wpływu leczenia na fizyczny, funkcjonalny i behawioralny rozwój młodych szczurów.
Laktacja
Podsumowanie ryzyka
Brak dostępnych danych dotyczących wpływu produktu SYMBICORT 4,5 µg, budezonidu lub fumaranu formoterolu na dziecko karmione piersią lub na produkcję mleka. Budezonid, podobnie jak inne kortykosteroidy wziewne, jest obecny w mleku ludzkim [patrz Dane ]. Brak dostępnych danych dotyczących obecności fumaranu formoterolu w mleku ludzkim. Fumaran formoterolu jest obecny w mleku szczurów [patrz Dane ]. Należy wziąć pod uwagę korzyści rozwojowe i zdrowotne wynikające z karmienia piersią, a także kliniczne zapotrzebowanie matki na SYMBICORT 4,5 mcg oraz wszelkie potencjalne niekorzystne skutki stosowania SYMBICORT 160 mg na niemowlę karmione piersią lub wynikające z tego schorzenia.
Dane
Dane z badań u ludzi dotyczące podawania budezonidu za pomocą inhalatora proszkowego wskazują, że całkowita dobowa doustna dawka budezonidu dostępna w mleku matki dla niemowlęcia wynosi około 0,3% do 1% dawki wziewnej przez matkę [patrz FARMAKOLOGIA KLINICZNA ]. Oczekuje się, że w przypadku produktu SYMBICORT 4,5 mcg dawka budezonidu dostępna dla niemowlęcia w mleku matki, wyrażona jako procent dawki matczynej, będzie podobna.
W badaniu płodności i reprodukcji u szczurów, poziomy formoterolu w osoczu były mierzone u młodych w 15. dniu po urodzeniu [patrz Używaj w określonych populacjach ]. Oszacowano, że maksymalne stężenie w osoczu, jakie szczenięta otrzymywały od matki, przy najwyższej dawce 15 mg/kg po karmieniu, wyniosło 4,4% (0,24 nmol/L dla miotu vs. 5,5 nmol/L dla matki). .
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność produktu SYMBICORT u pacjentów z astmą w wieku 12 lat i starszych ustalono w badaniach trwających do 12 miesięcy. W dwóch 12-tygodniowych, podwójnie zaślepionych, kontrolowanych placebo, kluczowych badaniach w USA, 25 pacjentów w wieku od 12 do 17 lat leczono preparatem SYMBICORT dwa razy na dobę [patrz Studia kliniczne ]. Wyniki skuteczności w tej grupie wiekowej były podobne do obserwowanych u pacjentów w wieku 18 lat i starszych. Nie było oczywistych różnic w rodzaju lub częstości działań niepożądanych zgłaszanych w tej grupie wiekowej w porównaniu z pacjentami w wieku 18 lat i starszymi.
Bezpieczeństwo i skuteczność SYMBICORT 80/4,5 u pacjentów z astmą w wieku od 6 do mniej niż 12 lat zostały ustalone w badaniach trwających do 12 tygodni [patrz Studia kliniczne ]. Profil bezpieczeństwa u tych pacjentów był zgodny z obserwowanym u pacjentów w wieku 12 lat i starszych, którzy również otrzymywali SYMBICORT [patrz DZIAŁANIA NIEPOŻĄDANE ].
Bezpieczeństwo i skuteczność SYMBICORT 160 mg u pacjentów z astmą w wieku poniżej 6 lat nie zostały ustalone.
Kontrolowane badania kliniczne wykazały, że doustne wziewne kortykosteroidy, w tym budezonid, składnik produktu SYMBICORT, mogą powodować zmniejszenie szybkości wzrostu u dzieci i młodzieży. Efekt ten zaobserwowano przy braku laboratoryjnych dowodów na zahamowanie osi HPA, co sugeruje, że szybkość wzrostu jest bardziej czułym wskaźnikiem ogólnoustrojowej ekspozycji na kortykosteroidy u dzieci niż niektóre powszechnie stosowane testy funkcji osi HPA. Długoterminowy wpływ tego zmniejszenia szybkości wzrostu związanego z doustnymi wziewnymi kortykosteroidami, w tym wpływ na ostateczny wzrost, jest nieznany. Możliwość „nadrobienia” wzrostu po przerwaniu leczenia doustnymi kortykosteroidami wziewnymi nie została odpowiednio zbadana.
badaniu dzieci z astmą w wieku od 5 do 12 lat, u dzieci otrzymujących budezonid DPI w dawce 200 mcg dwa razy na dobę (n=311) nastąpiło zmniejszenie wzrostu o 1,1 centymetra w porównaniu z osobami otrzymującymi placebo (n=418) pod koniec roku ; różnica między tymi dwiema grupami leczenia nie zwiększyła się dalej w ciągu trzech lat dodatkowego leczenia. Pod koniec 4 lat dzieci leczone budesonidem DPI i dzieci leczone placebo miały podobne prędkości wzrostu. Wnioski wyciągnięte z tego badania mogą być mylone z powodu nierównego stosowania kortykosteroidów w grupach terapeutycznych i włączenia danych od pacjentów osiągających dojrzałość płciową w trakcie badania.
Należy monitorować wzrost pacjentów pediatrycznych otrzymujących doustnie wziewne kortykosteroidy, w tym SYMBICORT. Jeśli u dziecka lub nastolatka przyjmującego jakikolwiek kortykosteroid wydaje się występować zahamowanie wzrostu, należy wziąć pod uwagę możliwość, że jest on szczególnie wrażliwy na ten efekt. Potencjalny wpływ przedłużonego leczenia na wzrost należy porównać z uzyskanymi korzyściami klinicznymi. Aby zminimalizować ogólnoustrojowe działanie kortykosteroidów wziewnych doustnie, w tym SYMBICORT, każdemu pacjentowi należy miareczkować do najmniejszej dawki, która skutecznie kontroluje jego/jej astmę [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Zastosowanie geriatryczne
Z całkowitej liczby pacjentów z astmą leczonych SYMBICORT 160 mg dwa razy na dobę w dwóch 12-tygodniowych badaniach i 26-tygodniowym badaniu po wprowadzeniu produktu do obrotu, 791 było w wieku 65 lat lub starszych, z czego 141 miało 75 lat lub więcej.
badaniach POChP trwających od 6 do 12 miesięcy 810 pacjentów leczonych produktem SYMBICORT 160/4,5, dwie inhalacje dwa razy na dobę, miało 65 lat i więcej, a 177 pacjentów miało 75 lat i więcej. Nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między tymi pacjentami a młodszymi pacjentami, a inne zgłoszone doświadczenia kliniczne nie wykazały różnic w odpowiedziach między pacjentami w podeszłym wieku i młodszymi.
Podobnie jak w przypadku innych produktów zawierających beta2-mimetyków, należy zachować szczególną ostrożność stosując SYMBICORT u pacjentów w podeszłym wieku ze współistniejącą chorobą układu krążenia, na którą mogą niekorzystnie wpływać beta2-mimetyki.
W oparciu o dostępne dane dotyczące produktu SYMBICORT lub jego aktywnych składników nie jest uzasadnione dostosowanie dawki 4,5 mcg produktu SYMBICORT u pacjentów geriatrycznych.
Niewydolność wątroby
Nie przeprowadzono formalnych badań farmakokinetycznych z użyciem produktu SYMBICORT u pacjentów z zaburzeniami czynności wątroby. Jednakże, ponieważ zarówno budezonid, jak i fumaran formoterolu są usuwane głównie w wyniku metabolizmu wątrobowego, zaburzenia czynności wątroby mogą prowadzić do kumulacji budezonidu i fumaranu formoterolu w osoczu. Dlatego pacjenci z chorobą wątroby powinni być ściśle monitorowani.
Zaburzenia czynności nerek
Nie przeprowadzono formalnych badań farmakokinetycznych produktu SYMBICORT u pacjentów z zaburzeniami czynności nerek.
PRZEDAWKOWAĆ
SYMBORYT
SYMBICORT zawiera zarówno budezonid, jak i formoterol; dlatego ryzyko związane z przedawkowaniem poszczególnych składników opisanych poniżej dotyczy produktu SYMBICORT. W badaniach farmakokinetycznych pacjentom z POChP podawano pojedyncze dawki 960/54 µg (12 dawek SYMBICORT 80/4,5) i 1280/36 µg (8 dawek 160/4,5). W sumie 1920/54 mcg (12 dawek SYMBICORT 160/4,5) podano jako pojedynczą dawkę zarówno zdrowym osobom, jak i pacjentom z astmą. W długoterminowym, aktywnie kontrolowanym badaniu bezpieczeństwa u młodzieży i dorosłych pacjentów z astmą w wieku 12 lat i starszych, SYMBICORT 160/4,5 podawano przez okres do 12 miesięcy w dawkach do dwukrotności najwyższej zalecanej dawki dobowej. W żadnym z tych badań nie zaobserwowano klinicznie istotnych działań niepożądanych.
Budezonid
Możliwość ostrego działania toksycznego po przedawkowaniu budezonidu jest niewielka. W przypadku stosowania nadmiernych dawek przez dłuższy czas może wystąpić ogólnoustrojowe działanie kortykosteroidów, takie jak hiperkortyza [patrz OSTRZEŻENIA I ŚRODKI ]. Budezonid w pięciokrotnie wyższej zalecanej dawce (3200 mcg na dobę) podawany ludziom przez 6 tygodni powodował istotne zmniejszenie (27%) odpowiedzi kortyzolu w osoczu na 6-godzinny wlew ACTH w porównaniu z placebo (+1%). Odpowiednim efektem 10 mg prednizonu na dobę było 35% zmniejszenie odpowiedzi kortyzolu w osoczu na ACTH.
Formoterol
Przedawkowanie formoterolu prawdopodobnie doprowadziłoby do nasilenia działań typowych dla agonistów beta2: drgawki, dusznica bolesna, nadciśnienie, niedociśnienie, tachykardia, tachyarytmie przedsionkowe i komorowe, nerwowość, ból głowy, drżenie, kołatanie serca, skurcze mięśni, nudności, zawroty głowy, zaburzenia snu , kwasica metaboliczna, hiperglikemia, hipokaliemia. Podobnie jak w przypadku wszystkich leków sympatykomimetycznych, zatrzymanie akcji serca, a nawet śmierć mogą być związane z nadużywaniem formoterolu. Nie zaobserwowano klinicznie istotnych działań niepożądanych, gdy formoterol podawano dorosłym pacjentom z ostrym skurczem oskrzeli w dawce 90 µg/dobę przez 3 godziny lub stabilnym astmatykom 3 razy na dobę w łącznej dawce 54 µg/dobę przez 3 dni.
Leczenie przedawkowania formoterolu polega na odstawieniu leku wraz z wdrożeniem odpowiedniego leczenia objawowego i/lub wspomagającego. Można rozważyć rozważne zastosowanie kardioselektywnego beta-blokera receptorów beta, pamiętając, że taki lek może wywołać skurcz oskrzeli. Nie ma wystarczających dowodów, aby określić, czy dializa jest korzystna w przypadku przedawkowania formoterolu. W przypadku przedawkowania zaleca się monitorowanie pracy serca.
PRZECIWWSKAZANIA
Stosowanie leku SYMBICORT jest przeciwwskazane w następujących warunkach:
- Pierwotne leczenie stanu astmatycznego lub innych ostrych epizodów astmy lub POChP, w przypadku których wymagane są intensywne działania.
- Nadwrażliwość na którykolwiek ze składników preparatu SYMBICORT.
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
SYMBORYT
SYMBICORT zawiera zarówno budezonid, jak i formoterol; dlatego mechanizmy działania opisane poniżej dla poszczególnych składników dotyczą SYMBICORT. Leki te reprezentują dwie klasy leków (syntetyczny kortykosteroid i długo działający selektywny agonista receptorów beta2-adrenergicznych), które mają różny wpływ na kliniczne, fizjologiczne i zapalne wskaźniki POChP i astmy.
Budezonid
Budezonid jest kortykosteroidem o działaniu przeciwzapalnym, który wykazuje silne działanie glikokortykoidowe i słabe działanie mineralokortykoidowe. W standardowych modelach in vitro i zwierzęcych budezonid ma około 200-krotnie większe powinowactwo do receptora glukokortykoidowego i 1000-krotnie większą siłę działania przeciwzapalnego do stosowania miejscowego niż kortyzol (test obrzęku ucha wywołanego olejem krotonowym u szczurów). Jako miara aktywności ogólnoustrojowej budezonid jest 40 razy silniejszy niż kortyzol przy podawaniu podskórnym i 25 razy silniejszy przy podawaniu doustnym w teście inwolucji grasicy szczura.
badaniach powinowactwa do receptora glukokortykoidowego, forma 22R budezonidu była dwa razy bardziej aktywna niż epimer 22S. Badania in vitro wykazały, że dwie formy budezonidu nie ulegają wzajemnej konwersji.
Stan zapalny jest ważnym elementem patogenezy POChP i astmy. Kortykosteroidy mają szeroki zakres działań hamujących wiele typów komórek (np. komórki tuczne, eozynofile, neutrofile, makrofagi i limfocyty) i mediatorów (np. histamina, eikozanoidy, leukotrieny i cytokiny) biorących udział w alergiach i niealergicznych zapalenie. Te przeciwzapalne działania kortykosteroidów mogą przyczyniać się do ich skuteczności w POChP i astmie.
Badania u pacjentów z astmą wykazały korzystny stosunek między miejscowym działaniem przeciwzapalnym a ogólnoustrojowym działaniem kortykosteroidów w szerokim zakresie dawek budezonidu. Tłumaczy się to połączeniem stosunkowo silnego miejscowego działania przeciwzapalnego, znacznej degradacji w wątrobie leku wchłanianego doustnie w pierwszym przejściu (85%-95%) oraz słabej siły powstających metabolitów.
Formoterol
Fumaran formoterolu jest długo działającym selektywnym agonistą receptorów beta2-adrenergicznych (beta2-agonistą) o szybkim początku działania. Wziewny fumaran formoterolu działa miejscowo w płucach jako lek rozszerzający oskrzela. Badania in vitro wykazały, że formoterol ma ponad 200-krotnie większą aktywność agonistyczną w stosunku do receptorów beta2 niż receptorów beta1. Selektywność wiązania in vitro do receptorów beta2-adrenergicznych w stosunku do receptorów beta1-adrenergicznych jest wyższa dla formoterolu niż dla albuterolu (5-krotnie), podczas gdy salmeterol ma wyższy (3-krotnie) współczynnik selektywności beta2-adrenergicznej niż formoterol.
Chociaż receptory beta2 są dominującymi receptorami adrenergicznymi w mięśniach gładkich oskrzeli, a receptory beta1 dominującymi receptorami w sercu, w ludzkim sercu istnieją również receptory beta2, stanowiące 10% do 50% wszystkich receptorów beta-adrenergicznych. Dokładna funkcja tych receptorów nie została ustalona, ale stwarzają one możliwość, że nawet wysoce selektywni agoniści receptorów beta2 mogą mieć wpływ na serce.
Efekty farmakologiczne leków będących agonistami receptorów beta2-adrenergicznych, w tym formoterolu, można przynajmniej częściowo przypisać stymulacji wewnątrzkomórkowej cyklazy adenylowej, enzymu katalizującego konwersję adenozynotrójfosforanu (ATP) do cyklicznego 3',5'-adenozynomonofosforanu ( cykliczny AMP). Podwyższone poziomy cyklicznego AMP powodują rozluźnienie mięśni gładkich oskrzeli i zahamowanie uwalniania mediatorów nadwrażliwości natychmiastowej z komórek, zwłaszcza z komórek tucznych.
Badania in vitro wykazały, że formoterol jest inhibitorem uwalniania mediatorów komórek tucznych, takich jak histamina i leukotrieny, z ludzkiego płuca. Formoterol hamuje również wywołane histaminą wynaczynienie albumin osocza u znieczulonych świnek morskich i hamuje wywołany alergenem napływ eozynofili u psów z nadreaktywnością dróg oddechowych. Znaczenie tych wyników badań in vitro i na zwierzętach dla ludzi nie jest znane.
Farmakodynamika
Astma
Wpływ na układ sercowo-naczyniowy
krzyżowym badaniu z zastosowaniem pojedynczej dawki, obejmującym 201 pacjentów z astmą przewlekłą, porównywano pojedyncze dawki 4,5, 9 i 18 mcg formoterolu w skojarzeniu z 320 mcg budezonidu dostarczanego za pomocą SYMBICORT z samym budezonidem 320 mcg. W porównaniu z budezonidem wykazano poprawę FEV1 uporządkowaną według dawki. EKG i próbki krwi dla glukozy i potasu pobrano po podaniu dawki. W przypadku produktu SYMBICORT 4,5 mcg, niewielkie średnie zwiększenie stężenia glukozy w surowicy i zmniejszenie stężenia potasu w surowicy (odpowiednio +0,44 mmol/l i -0,18 mmol/l przy najwyższej dawce) obserwowano przy zwiększaniu dawek formoterolu w porównaniu z budezonidem. W EKG SYMBICORT powodował niewielkie, zależne od dawki, średnie zwiększenie częstości akcji serca (około 3 uderzeń na minutę przy najwyższej dawce) i odstępów QTc (3-6 ms) w porównaniu z samym budezonidem. Żaden pacjent nie miał wartości QT lub QTc ≥500 ms.
Stanach Zjednoczonych w pięciu 12-tygodniowych badaniach kontrolowanych substancją czynną i placebo oraz jednym 6-miesięcznym badaniu kontrolowanym substancją czynną oceniono 2976 pacjentów w wieku 6 lat i starszych z astmą. Ogólnoustrojowe działanie farmakodynamiczne formoterolu (częstość akcji serca/tętna, ciśnienie krwi, odstęp QTc, potas i glukoza) były podobne u pacjentów leczonych produktem SYMBICORT w porównaniu z pacjentami leczonymi formoterolem w postaci suchego proszku do inhalacji 4,5 µg, 2 inhalacje dwa razy na dobę. Żaden pacjent nie miał wartości QT lub QTc ≥500 ms podczas leczenia.
W trzech kontrolowanych placebo badaniach u młodzieży i dorosłych z astmą w wieku 12 lat i starszych łącznie 1232 pacjentów (553 pacjentów w grupie SYMBICORT 160 mg) poddano ocenie ciągłemu 24-godzinnemu monitorowaniu elektrokardiograficznemu. Ogólnie rzecz biorąc, nie stwierdzono istotnych różnic w występowaniu ektopii komorowej lub nadkomorowej oraz brak dowodów na zwiększone ryzyko klinicznie istotnej arytmii w grupie otrzymującej SYMBICORT 160 mg w porównaniu z placebo.
Efekty osi HPA
Ogólnie rzecz biorąc, u pacjentów dorosłych lub młodzieży leczonych produktem SYMBICORT w dawkach do 640/18 mcg/dobę w porównaniu z budezonidem nie zaobserwowano klinicznie istotnego wpływu na oś HPA, mierzonego przez 24-godzinny poziom kortyzolu w moczu.
Przewlekła obturacyjna choroba płuc
Wpływ na układ sercowo-naczyniowy
W dwóch badaniach dotyczących czynności płuc w przebiegu POChP, trwających 6 i 12 miesięcy, obejmujących 3668 pacjentów z POChP, nie zaobserwowano klinicznie istotnych różnic w częstości tętna, ciśnieniu krwi, potasu i glukozy pomiędzy produktem SYMBICORT, poszczególnymi składnikami produktu SYMBICORT 160 mg, a placebo [patrz Studia kliniczne ].
EKG zarejestrowane podczas wielu wizyt klinicznych podczas leczenia w obu badaniach nie wykazały klinicznie istotnych różnic w częstości akcji serca, odstępie PR, czasie trwania zespołu QRS, częstości akcji serca, objawach niedokrwienia serca lub arytmii między SYMBICORT 160/4,5 monoproduktem a placebo, wszystkie podawane w 2 inhalacjach dwa razy dziennie. Na podstawie EKG, 6 pacjentów leczonych SYMBICORT 160/4,5, 6 pacjentów leczonych formoterolem 4,5 mcg i 6 pacjentów z grupy placebo doświadczyło migotania lub trzepotania przedsionków, które nie występowały na początku badania. Nie było przypadków nieutrwalonego częstoskurczu komorowego w grupach otrzymujących SYMBICORT 160/4,5, formoterol 4,5 mcg lub placebo.
12-miesięcznym badaniu, 520 pacjentów miało możliwe do oceny ciągłe 24-godzinne monitorowanie EKG (Holter) przed pierwszą dawką oraz po około 1 i 4 miesiącach leczenia. W grupach leczonych produktem SYMBICORT 160/4,5, formoterolem lub placebo w postaci 2 inhalacji dwa razy na dobę nie zaobserwowano klinicznie istotnych różnic w komorowych lub nadkomorowych zaburzeniach rytmu, komorowych lub nadkomorowych pobudzeniach ektopowych lub częstości akcji serca. W oparciu o monitorowanie EKG (Holter), jeden pacjent otrzymujący SYMBICORT 160/4,5, żaden pacjent otrzymujący formoterol 4,5 mcg i trzech pacjentów z grupy placebo doświadczyło migotania lub trzepotania przedsionków, które nie występowały na początku badania.
Efekty osi HPA
Dwudziestoczterogodzinne pomiary kortyzolu w moczu zebrano w łącznej podgrupie (n=616) pacjentów z dwóch badań funkcji płuc POChP. Dane wskazują na około 30% niższe średnie wartości stężenia wolnego kortyzolu w 24-godzinnym moczu po długotrwałym podawaniu (>6 miesięcy) produktu SYMBICORT w porównaniu z placebo. Wydaje się, że SYMBICORT 4,5 mcg wykazywał porównywalną supresję kortyzolu do samego budezonidu 160 mcg lub jednoczesnego podawania budezonidu 160 mcg i formoterolu 4,5 mcg. W przypadku pacjentów leczonych SYMBICORT 160 mg lub placebo przez okres do 12 miesięcy, odsetek pacjentów, którzy przesunęli się z normalnego do niskiego dla tej miary, był ogólnie porównywalny.
Inne produkty budezonidowe
Aby potwierdzić, że wchłanianie ogólnoustrojowe nie jest istotnym czynnikiem skuteczności klinicznej wziewnego budezonidu, przeprowadzono badanie kliniczne u pacjentów z astmą, w którym porównywano 400 µg budezonidu podawanego za pomocą ciśnieniowego inhalatora z dozownikiem z łącznikiem rurkowym z 1400 µg budezonidu podawanego doustnie i placebo. . Badanie wykazało skuteczność budezonidu podawanego wziewnie, ale nie przyjmowanego doustnie, pomimo porównywalnych poziomów ogólnoustrojowych. Zatem efekt terapeutyczny konwencjonalnych dawek wziewnego budezonidu doustnie tłumaczy się w dużej mierze jego bezpośrednim działaniem na drogi oddechowe.
Wykazano, że wziewny budezonid zmniejsza reaktywność dróg oddechowych na różne modele prowokacji, w tym histaminę, metacholinę, pirosiarczyn sodu i monofosforan adenozyny u pacjentów z nadreaktywnymi drogami oddechowymi. Znaczenie kliniczne tych modeli nie jest pewne.
Wstępne leczenie wziewnym budezonidem w dawce 1600 µg dziennie (800 µg dwa razy dziennie) przez 2 tygodnie zmniejszyło ostry (reakcja wczesna faza) i opóźniony (reakcja późnej fazy) spadek FEV1 po prowokacji wziewnym alergenem.
Ogólnoustrojowe działanie wziewnych kortykosteroidów jest związane z ogólnoustrojową ekspozycją na takie leki. Badania farmakokinetyczne wykazały, że zarówno u dorosłych, jak i u dzieci z astmą ogólnoustrojowa ekspozycja na budezonid jest mniejsza po podaniu produktu SYMBICORT 160 mg w porównaniu z budezonidem podawanym w postaci wziewnej w tej samej dawce dostarczanej za pomocą inhalatora suchego proszku [patrz FARMAKOLOGIA KLINICZNA ]. W związku z tym można oczekiwać, że działanie ogólnoustrojowe (oś HPA i wzrost) budezonidu dostarczanego z produktu SYMBICORT nie będzie większe niż zgłaszane dla budezonidu podawanego wziewnie w porównywalnych dawkach za pomocą inhalatora proszkowego [patrz Używaj w określonych populacjach ].
Efekty osi HPA
Wpływ wziewnego budezonidu podawanego za pomocą inhalatora suchego proszku na oś HPA zbadano u 905 osób dorosłych i 404 pacjentów pediatrycznych z astmą. U większości pacjentów zdolność do zwiększania produkcji kortyzolu w odpowiedzi na stres, oceniana za pomocą testu stymulacji kosyntropiny (ACTH), pozostała nienaruszona po leczeniu budezonidem w zalecanych dawkach. W przypadku dorosłych pacjentów leczonych 100, 200, 400 lub 800 mcg dwa razy na dobę przez 12 tygodni, odpowiednio 4%, 2%, 6% i 13% miało nieprawidłową odpowiedź na stymulowany kortyzol (szczyt kortyzolu
Inne produkty z formoterolem
Chociaż działanie farmakodynamiczne polega na stymulacji receptorów beta-adrenergicznych, nadmierna aktywacja tych receptorów często prowadzi do drżenia i skurczów mięśni szkieletowych, bezsenności, tachykardii, zmniejszenia stężenia potasu w osoczu i wzrostu stężenia glukozy w osoczu. Formoterol wziewny, podobnie jak inne leki będące agonistami receptorów beta2-adrenergicznych, może wywoływać zależne od dawki działanie sercowo-naczyniowe oraz wpływ na stężenie glukozy we krwi i/lub stężenie potasu w surowicy [patrz OSTRZEŻENIA I ŚRODKI ]. W przypadku produktu SYMBICORT 160 mg efekty te są szczegółowo opisane w rozdziale Farmakologia kliniczna, farmakodynamika, SYMBICORT (12.2).
Stosowanie leków LABA może powodować tolerancję na działanie bronchoprotekcyjne i rozszerzające oskrzela.
Nie obserwowano nadreaktywności oskrzeli z odbicia po zaprzestaniu przewlekłego długo działającego leczenia beta-agonistami.
Farmakokinetyka
SYMBORYT
Wchłanianie
Budezonid
Osoby zdrowe
Budezonid podawany wziewnie jest szybko wchłaniany w płucach, a maksymalne stężenie jest zwykle osiągane w ciągu 20 minut. Po doustnym podaniu budezonidu maksymalne stężenie w osoczu osiągano po około 1 do 2 godzinach, a bezwzględna dostępność ogólnoustrojowa wynosiła 6%-13% z powodu intensywnego metabolizmu pierwszego przejścia. W przeciwieństwie do tego większość budezonidu dostarczonego do płuc była wchłaniana ogólnoustrojowo. U zdrowych ochotników 34% odmierzonej dawki zdeponowało się w płucach (według oceny metodą stężenia w osoczu i przy użyciu inhalatora proszkowego zawierającego budezonid) przy bezwzględnej dostępności ogólnoustrojowej wynoszącej 39% odmierzonej dawki.
Po podaniu produktu SYMBICORT 160/4,5, dwie lub cztery inhalacje dwa razy na dobę przez 5 dni zdrowym ochotnikom, stężenie budezonidu w osoczu na ogół wzrastało proporcjonalnie do dawki. Wskaźnik akumulacji dla grupy otrzymującej 2 inhalacje dwa razy dziennie wyniósł 1,32 dla budezonidu.
Pacjenci z astmą
badaniu z pojedynczą dawką pacjentom z umiarkowaną astmą podawano wyższe niż zalecane dawki produktu SYMBICORT (12 inhalacji produktu SYMBICORT 160/4,5). Maksymalne stężenie budezonidu w osoczu wynoszące 4,5 nmol/l wystąpiło 20 minut po podaniu. Badanie to wykazało, że całkowita ogólnoustrojowa ekspozycja na budezonid z produktu SYMBICORT 4,5 mcg była o około 30% mniejsza niż w przypadku budezonidu wziewnego za pomocą inhalatora suchego proszku (DPI) w tej samej dostarczonej dawce. Po podaniu produktu SYMBICORT okres półtrwania budezonidu wynosił 4,7 godziny.
badaniu z dawką wielokrotną najwyższą zalecaną dawkę produktu SYMBICORT (160/4,5, dwie inhalacje dwa razy na dobę) podawano pacjentom z umiarkowaną astmą i osobom zdrowym przez 1 tydzień. Maksymalne stężenie budezonidu w osoczu wynoszące 1,2 nmol/l wystąpiło po 21 minutach u pacjentów z astmą. Maksymalne stężenie budezonidu w osoczu było o 27% mniejsze u pacjentów z astmą w porównaniu z osobami zdrowymi. Jednak całkowita ogólnoustrojowa ekspozycja na budezonid była porównywalna z ekspozycją u pacjentów z astmą.
Maksymalne stężenie budezonidu w osoczu w stanie stacjonarnym podawanego przez DPI dorosłym z astmą wynosiło średnio 0,6 i 1,6 nmol/l w dawkach odpowiednio 180 µg i 360 µg dwa razy na dobę. U pacjentów z astmą budezonid wykazywał liniowy wzrost AUC i Cmax wraz ze wzrostem dawki zarówno po jednorazowym, jak i wielokrotnym podaniu wziewnego budezonidu.
Pacjenci z POChP
badaniu z pojedynczą dawką pacjentom z POChP podano 12 inhalacji produktu SYMBICORT 80/4,5 (całkowita dawka 960/54 µg). Średnie maksymalne stężenie budezonidu w osoczu wynoszące 3,3 nmol/l wystąpiło po 30 minutach od podania. Ekspozycja ogólnoustrojowa na budezonid była porównywalna dla produktu SYMBICORT pMDI i jednoczesnego podawania budezonidu za pomocą inhalatora z dozownikiem i formoterolu za pomocą inhalatora proszkowego (budezonid 960 µg i formoterol 54 µg). W tym samym badaniu otwarta grupa pacjentów z umiarkowaną astmą również otrzymała tę samą wyższą dawkę SYMBICORT. W przypadku budezonidu pacjenci z POChP wykazywali o 12% większe AUC i 10% niższe Cmax w porównaniu z pacjentami z astmą.
6-miesięcznym głównym badaniu klinicznym dotyczącym czynności płuc uzyskano dane farmakokinetyczne budezonidu w stanie stacjonarnym w podgrupie pacjentów z POChP z grupami leczenia SYMBICORT 4,5 mcg pMDI 160/4,5, SYMBICORT 160 mg pMDI 80/4,5, budezonid 160 mcg, budezonid 160 µg i 4,5 µg formoterolu podawane razem, wszystkie podawane w postaci 2 inhalacji dwa razy dziennie. Ekspozycja ogólnoustrojowa na budezonid (AUC i Cmax) wzrastała proporcjonalnie do dawek od 80 mcg do 160 mcg i była generalnie podobna w 3 leczonych grupach otrzymujących tę samą dawkę budezonidu (SYMBICORT 4,5 mcg pMDI 160/4,5, budezonid 160 mcg, budezonid 160 mcg i formoterolu 4,5 mikrograma podawanego razem).
Formoterol
Formoterol wziewny jest szybko wchłaniany; maksymalne stężenia w osoczu są zazwyczaj osiągane w czasie pierwszego pobierania próbek osocza, w ciągu 5-10 minut po podaniu. Podobnie jak w przypadku wielu produktów leczniczych do inhalacji doustnej, prawdopodobnie większość dostarczanego wziewnego formoterolu jest połykana, a następnie wchłaniana z przewodu pokarmowego.
Osoby zdrowe
Po podaniu preparatu SYMBICORT (160/4,5, dwie lub cztery inhalacje dwa razy na dobę) przez 5 dni zdrowym osobom, stężenie formoterolu w osoczu na ogół wzrastało proporcjonalnie do dawki. Wskaźnik akumulacji dla grupy otrzymującej 2 inhalacje dwa razy dziennie wyniósł 1,77 dla formoterolu.
Pacjenci z astmą
W badaniu z pojedynczą dawką pacjentom z umiarkowaną astmą podawano wyższe niż zalecane dawki produktu SYMBICORT (12 inhalacji produktu SYMBICORT 160/4,5). Maksymalne stężenie formoterolu w osoczu wynoszące 136 pmol wystąpiło po 10 minutach od podania. Około 8% dostarczonej dawki formoterolu zostało wydalone z moczem w postaci niezmienionej.
badaniu z dawką wielokrotną najwyższą zalecaną dawkę produktu SYMBICORT (160/4,5, dwie inhalacje dwa razy na dobę) podawano pacjentom z umiarkowaną astmą i osobom zdrowym przez 1 tydzień. Maksymalne stężenie formoterolu w osoczu, wynoszące 28 pmol/l, wystąpiło po 10 minutach u pacjentów z astmą. Maksymalne stężenie formoterolu w osoczu było o około 42% niższe u pacjentów z astmą w porównaniu z osobami zdrowymi. Jednak całkowita ogólnoustrojowa ekspozycja na formoterol była porównywalna z ekspozycją u pacjentów z astmą.
Pacjenci z POChP
Po podaniu pojedynczej dawki 12 inhalacji produktu SYMBICORT 80/4,5, średnie maksymalne stężenie formoterolu w osoczu wynoszące 167 pmol/l zostało szybko osiągnięte po 15 minutach od podania. Ekspozycja na formoterol była nieco większa (~16-18%) po podaniu produktu SYMBICORT 160 mg pMDI w porównaniu do jednoczesnego podawania budezonidu za pomocą inhalatora z dozownikiem i formoterolu za pomocą inhalatora suchego proszku (całkowita dawka budezonidu 960 µg i formoterolu 54 µg). W tym samym badaniu otwarta grupa pacjentów z umiarkowaną astmą otrzymywała tę samą dawkę SYMBICORT. Pacjenci z POChP wykazywali o 12-15% większe wartości AUC i Cmax formoterolu w porównaniu z pacjentami z astmą.
6-miesięcznym głównym badaniu klinicznym dotyczącym czynności płuc uzyskano dane farmakokinetyczne formoterolu w stanie stacjonarnym w podgrupie pacjentów z POChP z ramionami leczenia SYMBICORT 160 mg pMDI 160/4,5, SYMBICORT 160 mg pMDI 80/4,5, formoterol 4,5 mcg, budezonid 160 mcg i formoterol 4,5 mcg podawane razem, wszystkie podawane w postaci 2 inhalacji dwa razy dziennie. Ekspozycja ogólnoustrojowa na formoterol, o czym świadczy AUC, była odpowiednio o około 30% i 16% większa w przypadku produktu SYMBICORT pMDI w porównaniu z ramieniem leczenia samym formoterolem i równoczesnym podawaniem poszczególnych składników budezonidu i ramienia leczenia formoterolem.
Dystrybucja
Budezonid
Objętość dystrybucji budezonidu wynosiła około 3 l/kg. Wiązał się w 85%-90% z białkami osocza. Wiązanie z białkami było stałe w zakresie stężeń (1-100 nmol/l) osiągniętym przy i przekraczaniu zalecanych dawek wziewnych. Budezonid wykazywał niewielkie lub żadne wiązanie z globuliną wiążącą kortykosteroidy. Budezonid szybko równoważył się z czerwonymi krwinkami w sposób niezależny od stężenia, przy stosunku osocza krwi wynoszącym około 0,8.
Formoterol
W zakresie stężeń 10-500 nmol/l wiązanie z białkami osocza dla enancjomerów RR i SS formoterolu wynosiło odpowiednio 46% i 58%. Stężenia formoterolu stosowane do oceny wiązania z białkami osocza były wyższe niż stężenia uzyskiwane w osoczu po inhalacji pojedynczej dawki 54 μg.
Metabolizm
Budezonid
Badania in vitro z homogenatami wątroby ludzkiej wykazały, że budezonid był szybko i intensywnie metabolizowany. Wyizolowano i zidentyfikowano dwa główne metabolity powstałe w wyniku biotransformacji katalizowanej przez izoenzym 3A4 (CYP3A4) cytochromu P450 (CYP) izoenzymu 3A4 (CYP3A4) i zidentyfikowano je jako 16α-hydroksyprednizolon i 6β-hydroksybudezonid. Aktywność kortykosteroidowa każdego z tych dwóch metabolitów była mniejsza niż 1% aktywności związku macierzystego. Nie wykryto jakościowych różnic między wzorcami metabolicznymi in vitro i in vivo. W preparatach ludzkich płuc i surowicy zaobserwowano znikomą inaktywację metaboliczną.
Formoterol
Podstawowy metabolizm formoterolu odbywa się na drodze bezpośredniej glukuronidacji i O-demetylacji, a następnie sprzęgania do nieaktywnych metabolitów. Wtórne szlaki metaboliczne obejmują deformację i koniugację siarczanów. CYP2D6 i CYP2C zidentyfikowano jako główne odpowiedzialne za odemetylację.
Eliminacja
Budezonid
Budezonid był wydalany z moczem i kałem w postaci metabolitów. Około 60% dożylnie znakowanej radioaktywnie dawki odzyskano w moczu.
W moczu nie wykryto budezonidu w postaci niezmienionej. Forma 22R budezonidu była preferencyjnie usuwana przez wątrobę z klirensem ogólnoustrojowym 1,4 l/min wobec 1,0 l/min dla formy 22S. Końcowy okres półtrwania, 2 do 3 godzin, był taki sam dla obu epimerów i niezależny od dawki.
Formoterol
Wydalanie formoterolu badano u czterech zdrowych osób po jednoczesnym podaniu formoterolu znakowanego radioizotopem drogą doustną i dożylną. W tym badaniu 62% znakowanego radioaktywnie formoterolu było wydalane z moczem, a 24% z kałem.
Specjalne populacje
Geriatryczny
Farmakokinetyka produktu SYMBICORT 4,5 mikrograma u pacjentów w podeszłym wieku nie była szczegółowo badana.
Pediatryczny
Stężenia budezonidu w osoczu mierzono po podaniu czterech inhalacji produktu SYMBICORT 160/4,5 w badaniu pojedynczej dawki u dzieci z astmą w wieku od 6 do mniej niż 12 lat. Maksymalne stężenia budezonidu wynoszące 1,4 nmol/l wystąpiły 20 minut po podaniu. Badanie to wykazało również, że całkowita ogólnoustrojowa ekspozycja na budezonid z produktu SYMBICORT 4,5 mcg była o około 30% niższa niż w przypadku budezonidu podawanego wziewnie za pomocą inhalatora proszkowego, który również oceniano przy tej samej dostarczonej dawce. Znormalizowane względem dawki Cmax i AUC0-inf budezonidu po inhalacji pojedynczej dawki u dzieci w wieku od 6 do mniej niż 12 lat były liczbowo niższe niż obserwowane u dorosłych.
Po 2 inhalacjach produktu SYMBICORT 160/4,5 dwa razy na dobę, wartości Cmax i AUC0-6 formoterolu w stanie stacjonarnym u dzieci w wieku od 6 do mniej niż 12 lat były porównywalne z wartościami obserwowanymi u dorosłych.
Płeć/Rasa
Nie przeprowadzono specjalnych badań oceniających wpływ płci i rasy na farmakokinetykę produktu SYMBICORT. Analiza farmakokinetyki populacyjnej danych SYMBICORT 4,5 µg wskazuje, że płeć nie wpływa na farmakokinetykę budezonidu i formoterolu. Nie można wyciągnąć żadnych wniosków na temat wpływu rasy ze względu na małą liczbę osób niekaukaskich ocenianych pod kątem PK.
Matki karmiące
Dyspozycje budezonidu podawanego wziewnie z inhalatora proszkowego w dawkach 200 lub 400 mcg dwa razy dziennie przez co najmniej 3 miesiące badano u ośmiu kobiet karmiących piersią z astmą od 1 do 6 miesięcy po porodzie. Ekspozycja ogólnoustrojowa na budezonid u tych kobiet wydaje się być porównywalna z wynikami innych badań, które stwierdzono u kobiet nie karmiących piersią z astmą. Mleko z piersi uzyskane w ciągu ośmiu godzin po podaniu wykazało, że maksymalne stężenie budezonidu dla całkowitych dawek dobowych 400 i 800 mcg wyniosło odpowiednio 0,39 i 0,78 nmol/l i wystąpiło w ciągu 45 minut po podaniu. Szacunkowa doustna dawka budezonidu z mleka matki dla niemowlęcia wynosi około 0,007 i 0,014 mcg/kg/dobę dla dwóch schematów dawkowania stosowanych w tym badaniu, co stanowi około 0,3% do 1% dawki wdychanej przez matkę. Stężenia budezonidu w próbkach osocza pobranych od pięciu niemowląt około 90 minut po karmieniu piersią (i około 140 minut po podaniu leku matce) były poniżej mierzalnych poziomów ( Używaj w określonych populacjach ].
Niewydolność nerek lub wątroby
Brak danych dotyczących specyficznego stosowania produktu SYMBICORT u pacjentów z zaburzeniami czynności wątroby lub nerek. Zaburzenia czynności wątroby mogą wpływać na eliminację kortykosteroidów. Na farmakokinetykę budezonidu wpływały zaburzenia czynności wątroby, o czym świadczy podwojenie dostępności ogólnoustrojowej po przyjęciu doustnym. Farmakokinetyka dożylnego budezonidu była jednak podobna u pacjentów z marskością wątroby iu osób zdrowych. Konkretne dane dotyczące formoterolu nie są dostępne, ale ponieważ formoterol jest eliminowany głównie poprzez metabolizm wątrobowy, można spodziewać się zwiększonej ekspozycji u pacjentów z ciężkimi zaburzeniami czynności wątroby.
Interakcje między lekami
Przeprowadzono badanie krzyżowe z pojedynczą dawką w celu porównania farmakokinetyki ośmiu inhalacji następujących jednocześnie: budezonidu, formoterolu i budezonidu z formoterolem. Wyniki badania wykazały, że nie ma dowodów na interakcje farmakokinetyczne między dwoma składnikami leku SYMBICORT.
Inhibitory enzymów cytochromu P450
Ketokonazol
Ketokonazol, silny inhibitor izoenzymu 3A4 (CYP3A4) cytochromu P450 (CYP), głównego enzymu metabolicznego kortykosteroidów, zwiększał stężenie budezonidu przyjmowanego doustnie w osoczu.
Cymetydyna
W zalecanych dawkach cymetydyna, nieswoisty inhibitor enzymów CYP, wywierała niewielki, ale klinicznie nieistotny wpływ na farmakokinetykę budezonidu podawanego doustnie.
Nie przeprowadzono specyficznych badań interakcji typu lek-lek z formoterolem.
Toksykologia i/lub farmakologia zwierząt
Przedkliniczne
Badania na zwierzętach laboratoryjnych (świnki miniaturowe, gryzonie i psy) wykazały występowanie zaburzeń rytmu serca i nagłej śmierci (z histologicznymi dowodami martwicy mięśnia sercowego) w przypadku jednoczesnego podawania beta-agonistów i metyloksantyn. Kliniczne znaczenie tych wyników nie jest znane.
Studia kliniczne
Astma
Pacjenci z astmą w wieku 12 lat i starsi
dwóch badaniach klinicznych porównujących SYMBICORT 4,5 mcg z poszczególnymi składnikami poprawa w większości punktów końcowych skuteczności była większa w przypadku SYMBICORT niż w przypadku stosowania samego budezonidu lub formoterolu. Ponadto w jednym badaniu klinicznym wykazano podobne wyniki pomiędzy produktem SYMBICORT a jednoczesnym stosowaniem budezonidu i formoterolu w odpowiednich dawkach z oddzielnych inhalatorów.
Bezpieczeństwo i skuteczność produktu SYMBICORT 160 mg wykazano w dwóch randomizowanych, podwójnie zaślepionych, kontrolowanych placebo badaniach klinicznych w Stanach Zjednoczonych z udziałem 1076 pacjentów w wieku 12 lat i starszych. Stałe dawki produktu SYMBICORT wynoszące 160/9 mcg i 320/9 mcg dwa razy na dobę (każda dawka podana w 2 inhalacjach o mocy odpowiednio 80/4,5 i 160/4,5 mcg) porównano z monoskładnikami (budezonid i formoterol) oraz placebo do podać informacje o odpowiednim dawkowaniu w celu uwzględnienia zakresu ciężkości astmy.
Badanie 1: Badanie kliniczne z SYMBICORT 160/4,5
tym 12-tygodniowym badaniu oceniono 596 pacjentów w wieku 12 lat i starszych, porównując SYMBICORT 160/4,5, wolne połączenie budezonidu 160 mcg z formoterolem 4,5 mcg w oddzielnych inhalatorach, budezonid 160 mcg, formoterol 4,5 mcg i placebo; każda podawana jako 2 inhalacje dwa razy dziennie. Badanie obejmowało 2-tygodniowy okres wstępny z budezonidem 80 mcg, 2 inhalacje dwa razy dziennie. Większość pacjentów cierpiała na astmę umiarkowaną do ciężkiej i przed przystąpieniem do badania stosowała umiarkowane do dużych dawek wziewnych kortykosteroidów. Randomizacja była stratyfikowana według wcześniejszego leczenia wziewnymi kortykosteroidami (71,6% w przypadku umiarkowanej dawki i 28,4% w przypadku dużej dawki wziewnego kortykosteroidu). Średni procent przewidywanej wartości FEV1 na początku badania wynosił 68,1% i był podobny we wszystkich leczonych grupach. Równorzędnymi pierwszorzędowymi punktami końcowymi skuteczności były: średnia 12-godzinna po podaniu dawki FEV1 w 2. tygodniu i FEV1 przed podaniem uśredniona w trakcie badania. Badanie wymagało również wycofania pacjentów, którzy spełnili predefiniowane kryterium zaostrzenia astmy. Wstępnie zdefiniowane kryteria pogorszenia astmy obejmowały klinicznie istotne zmniejszenie FEV1 lub PEF, zwiększenie stosowania ratunkowego albuterolu, nocne wybudzenie z powodu astmy, interwencja w nagłych wypadkach lub hospitalizacja z powodu astmy lub konieczność stosowania leków przeciwastmatycznych niedozwolonych protokołem. Jeśli chodzi o kryterium przebudzenia w nocy z powodu astmy, pacjenci mogli pozostać w badaniu według uznania badacza, jeśli żadne z pozostałych kryteriów zaostrzenia astmy nie zostało spełnione. Odsetek pacjentów, którzy wycofali się z powodu lub spełniających predefiniowane kryteria pogorszenia astmy, przedstawiono w Tabeli 4.
Średnia procentowa zmiana w stosunku do wartości wyjściowej FEV1 mierzonej bezpośrednio przed dawkowaniem (przed dawką) w ciągu 12 tygodni jest przedstawiona na Rycinie 1. Ponieważ w tym badaniu stosowano wstępnie zdefiniowane kryteria odstawienia dla pogorszenia astmy, co spowodowało zróżnicowaną częstość odstawienia w grupach terapeutycznych, przed Przedstawiono również wyniki dotyczące dawki FEV1 z ostatniej dostępnej wizyty w ramach badania (koniec leczenia, EOT). Pacjenci otrzymujący SYMBICORT 160/4,5 wykazywali znacznie większą średnią poprawę FEV1 przed podaniem dawki pod koniec leczenia (0,19 l, 9,4%) w porównaniu z wartością wyjściową (0,19 l, 9,4%), w porównaniu z budezonidem 160 mcg (0,10 l, 4,9%), formoterolem 4,5 mcg (-0,12 L, -4,8% i placebo (-0,17 L, -6,9%).
Rycina 1 : Średnia procentowa zmiana od wartości początkowej FEV1 przed podaniem dawki w ciągu 12 tygodni (Badanie 1)
INFORMACJA O PACJENCIE
SYMBORYT (SIM-bi-kort) (budezonid 80 µg i dwuwodny fumaran formoterolu 4,5 µg) Wdychanie Aerozol
SYMBORYT (SIM-bi-kort) (budezonid 160 µg i fumaran formoterolu dwuwodny 4,5 µg) Wdychanie Aerozol
Co to jest SYMBICORT?
SYMBICORT łączy wziewny lek kortykosteroidowy (ICS), budezonid i długo działający agonista receptorów beta2-adrenergicznych (LABA), formoterol.
- Wziewne kortykosteroidy pomagają zmniejszyć stan zapalny w płucach. Zapalenie płuc może prowadzić do problemów z oddychaniem.
- Leki LABA stosuje się u osób z przewlekłą obturacyjną chorobą płuc (POChP) i astmą. Leki LABA pomagają rozluźnić mięśnie wokół dróg oddechowych w płucach, aby zapobiec objawom, takim jak świszczący oddech, kaszel, ucisk w klatce piersiowej i duszność. Objawy te mogą wystąpić, gdy mięśnie wokół dróg oddechowych napinają się. To utrudnia oddychanie. W ciężkich przypadkach świszczący oddech może zatrzymać oddychanie i może prowadzić do śmierci, jeśli nie zostanie od razu leczony.
SYMBICORT 4,5 mcg nie jest stosowany do łagodzenia nagłych problemów z oddychaniem i nie zastąpi inhalatora ratunkowego. SYMBICORT stosuje się w leczeniu astmy i POChP w następujący sposób:
- Astma: SYMBICORT stosuje się w celu kontrolowania objawów astmy i zapobiegania objawom, takim jak świszczący oddech u dorosłych i dzieci w wieku 6 lat i starszych. SYMBICORT 4,5 mcg zawiera formoterol. Leki LABA, takie jak formoterol, stosowane samodzielnie zwiększają ryzyko zgonu i hospitalizacji z powodu problemów z astmą. SYMBICORT zawiera ICS i LABA. Gdy ICS i LABA są stosowane razem, nie ma znaczącego zwiększonego ryzyka hospitalizacji i zgonu z powodu problemów z astmą. SYMBICORT 160 mg nie jest przeznaczony dla dorosłych i dzieci z astmą, które są dobrze kontrolowane za pomocą leków kontrolujących astmę, takich jak niska lub średnia dawka ICS. SYMBICORT 160mg jest przeznaczony dla dorosłych i dzieci z astmą, które potrzebują zarówno leku ICS, jak i LABA. Nie wiadomo, czy SYMBICORT jest bezpieczny i skuteczny u dzieci w wieku poniżej 6 lat z astmą.
- POChP: POChP to długotrwała (przewlekła) choroba płuc, która obejmuje przewlekłe zapalenie oskrzeli, rozedmę lub oba te objawy. SYMBICORT 160/4,5 mcg stosuje się długotrwale, jako 2 inhalacje 2 razy dziennie, w celu złagodzenia objawów POChP, lepszego oddychania i zmniejszenia liczby zaostrzeń (pogorszenia objawów POChP przez kilka dni).
Nie używaj SYMBICORT:
- w leczeniu nagłych ciężkich objawów astmy lub POChP.
- jeśli pacjent ma uczulenie na którykolwiek ze składników leku SYMBICORT. Lista składników leku SYMBICORT znajduje się na końcu tej ulotki.
Przed użyciem SYMBICORT poinformuj swojego lekarza o wszystkich swoich schorzeniach, w tym jeśli:
- mieć problemy z sercem.
- mieć wysokie ciśnienie krwi.
- mieć drgawki.
- masz problemy z tarczycą.
- mieć cukrzycę.
- masz problemy z wątrobą.
- mają osteoporozę.
- masz problem z układem odpornościowym.
- mieć problemy z oczami, takie jak zwiększone ciśnienie w oku, jaskra lub zaćma.
- jesteś uczulony na jakiekolwiek leki.
- mieć jakikolwiek rodzaj infekcji wirusowej, bakteryjnej, grzybiczej lub pasożytniczej.
- są narażone na ospę wietrzną lub odrę.
- są w ciąży lub planują zajść w ciążę. Nie wiadomo, czy SYMBICORT 4,5 mcg może zaszkodzić nienarodzonemu dziecku.
- karmią piersią. Budezonid, jeden z aktywnych składników leku SYMBICORT, przenika do mleka matki. Ty i Twój lekarz powinniście zdecydować, czy będziecie przyjmować SYMBICORT 160 mg podczas karmienia piersią.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym o lekach na receptę i dostępnych bez recepty, witaminach i suplementach ziołowych. SYMBICORT i niektóre inne leki mogą wchodzić ze sobą w interakcje. Może to spowodować poważne skutki uboczne. W szczególności powiedz swojemu lekarzowi, jeśli przyjmujesz leki przeciwgrzybicze lub przeciw HIV.
Poznaj wszystkie leki, które przyjmujesz. Zachowaj listę i pokazuj ją swojemu lekarzowi i farmaceucie za każdym razem, gdy otrzymasz nowy lek.
Jak używać SYMBICORT?
Zobacz instrukcje krok po kroku dotyczące korzystania z produktu SYMBICORT na końcu tej ulotki z informacjami dla pacjenta. Nie używaj SYMBICORT 4,5 mcg, chyba że Twój lekarz Cię nauczył i wszystko rozumiesz. Zapytaj swojego lekarza lub farmaceutę, jeśli masz jakiekolwiek pytania.
- Użyj SYMBICORT dokładnie zgodnie z zaleceniami. Nie należy stosować leku SYMBICORT 160 mg częściej niż zalecono. SYMBICORT ma 2 mocne strony. Twój lekarz przepisał moc, która jest dla Ciebie najlepsza. Zwróć uwagę na różnice między lekiem SYMBICORT a innymi lekami wziewnymi, w tym różnice w przepisanym stosowaniu i wyglądzie fizycznym.
- Dzieci powinny używać SYMBICORT z pomocą osoby dorosłej, zgodnie z instrukcjami lekarza dziecka.
- SYMBICORT 160 mg powinien być przyjmowany codziennie jako 2 wdechy rano i 2 wdechy wieczorem w odstępie około 12 godzin.
- przypadku pominięcia dawki leku SYMBICORT 160 mg, następną dawkę należy przyjąć o zwykłej porze.
- Wypłukać usta wodą i wypluć wodę po każdej dawce (2 wdechy) SYMBICORT. Nie połykaj wody. Pomoże to zmniejszyć ryzyko infekcji grzybiczej (pleśniawki) w jamie ustnej i gardle.
- Jeśli zażyjesz zbyt dużo leku SYMBICORT, skontaktuj się z lekarzem lub natychmiast udaj się na pogotowie ratunkowe najbliższego szpitala, jeśli wystąpią jakiekolwiek nietypowe objawy, takie jak nasilenie duszności, ból w klatce piersiowej, przyspieszenie akcji serca lub drżenie.
- Nie spryskuj oczu SYMBICORT 4.5mcg. Jeśli przypadkowo dostaniesz SYMBICORT 160 mg do oczu, przemyj oczy wodą, a jeśli zaczerwienienie lub podrażnienie nie ustąpi, skonsultuj się z lekarzem.
- Nie należy zmieniać ani odstawiać leków stosowanych do kontrolowania lub leczenia problemów z oddychaniem. Twój lekarz zmieni Twoje leki w razie potrzeby.
- Podczas stosowania leku SYMBICORT 2 razy dziennie, z jakiegokolwiek powodu nie należy stosować innych leków zawierających LABA. Zapytaj swojego lekarza lub farmaceutę, czy którykolwiek z twoich innych leków to leki LABA.
- SYMBICORT 4,5mcg nie łagodzi nagłych objawów. Zawsze należy mieć przy sobie inhalator ratunkowy w celu leczenia nagłych objawów. Jeśli nie masz inhalatora ratunkowego, skontaktuj się z lekarzem, aby przepisał Ci go.
- Zadzwoń do swojego lekarza lub natychmiast uzyskaj opiekę medyczną, jeśli:
- Twoje problemy z oddychaniem nasilają się z SYMBICORT.
- lek ratunkowy należy stosować częściej niż zwykle.
- lek ratunkowy wziewny nie jest skuteczny w łagodzeniu objawów.
- Twoje wyniki szczytowego przepływomierza spadają. Twój lekarz poinformuje Cię o numerach, które są dla Ciebie odpowiednie.
- objawy nie ustępują po regularnym stosowaniu SYMBICORT 160 mg przez 1 tydzień.
Jakie są możliwe skutki uboczne SYMBICORT?
SYMBICORT 4,5mcg może powodować poważne skutki uboczne, w tym:
- Stosowanie zbyt dużej ilości leku LABA może spowodować:
- ból w klatce piersiowej
- podwyższone ciśnienie krwi
- szybkie i nieregularne bicie serca
- ból głowy
- drżenie
- nerwowość
- Zakażenie grzybicze jamy ustnej lub gardła (pleśniawki). Wypłucz usta wodą bez połykania po użyciu SYMBICORT 4,5 mcg, aby zmniejszyć ryzyko zachorowania na pleśniawki.
- Zapalenie płuc i inne infekcje dolnych dróg oddechowych. Osoby z POChP mają większą szansę na zapalenie płuc i inne infekcje płuc. Kortykosteroidy wziewne mogą zwiększać ryzyko zapalenia płuc. Zadzwoń do swojego lekarza, jeśli zauważysz którykolwiek z tych objawów:
- wzrost produkcji śluzu (plwociny)
- zmiana koloru śluzu
- gorączka
- dreszcze
- zwiększony kaszel
- zwiększone problemy z oddychaniem
- Wpływ na układ odpornościowy i większa szansa na infekcje. Poinformuj swojego lekarza o wszelkich oznakach infekcji, takich jak:
- gorączka
- ból
- bóle
- dreszcze
- czuć się zmęczonym
- mdłości
- wymioty
- Niewydolność nadnerczy. Niewydolność nadnerczy to stan, w którym nadnercza nie wytwarzają wystarczającej ilości hormonów steroidowych. Może się to zdarzyć po zaprzestaniu przyjmowania doustnych leków kortykosteroidowych i rozpoczęciu stosowania wziewnych leków kortykosteroidowych.
- Zwiększony świszczący oddech zaraz po zażyciu SYMBICORT. Zawsze miej przy sobie inhalator ratunkowy, aby leczyć nagły świszczący oddech.
- Poważne reakcje alergiczne, w tym wysypka, pokrzywka, obrzęk twarzy, ust i języka oraz problemy z oddychaniem. Zadzwoń do swojego lekarza lub uzyskaj pomoc medyczną w nagłych wypadkach, jeśli wystąpią jakiekolwiek objawy poważnej reakcji alergicznej.
- Niższa gęstość mineralna kości. Może się to zdarzyć u osób, które mają dużą szansę na niską gęstość mineralną kości (osteoporozę). Twój lekarz powinien to sprawdzić podczas leczenia lekiem SYMBICORT.
- Spowolniony wzrost u dzieci. Podczas stosowania SYMBICORT należy regularnie kontrolować wzrost dziecka.
- Problemy z oczami, w tym jaskra i zaćma. Powinieneś mieć regularne badania wzroku podczas korzystania z SYMBICORT.
- Obrzęk naczyń krwionośnych. Może się to zdarzyć u osób z astmą. Poinformuj swojego lekarza od razu, jeśli masz:
- uczucie mrowienia lub igieł lub
- objawy grypopodobne drętwienie rąk lub nóg
- ból i obrzęk zatok
- wysypka
- Spadek poziomu potasu we krwi (hipokaliemia).
- Wzrost poziomu cukru we krwi (hiperglikemia).
Do najczęstszych skutków ubocznych SYMBICORT należą:
Osoby z astmą:
- podrażnienie gardła
- ból głowy
- zakażenia górnych dróg oddechowych
- ból gardła
- zapalenie błon śluzowych zatok
- grypa (zapalenie zatok)
- zatkany nos
- ból pleców
- wymioty
- dyskomfort w żołądku
- pleśniawki w jamie ustnej i gardle. Po użyciu wypłucz usta wodą bez połykania, aby zapobiec pleśniawce
Osoby z POChP:
- podrażnienie gardła.
- pleśniawki w jamie ustnej i gardle. Po użyciu wypłucz usta wodą bez połykania, aby zapobiec pleśniawce.
- infekcja i zapalenie błon śluzowych oskrzeli (zapalenie oskrzeli).
- zapalenie błon śluzowych zatok (zapalenie zatok).
- zakażenia górnych dróg oddechowych.
Poinformuj swojego lekarza o wszelkich skutkach ubocznych, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne SYMBICORT.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Możesz również zgłaszać działania niepożądane firmie AstraZeneca pod numerem 1-800-236-9933.
Jak przechowywać SYMBICORT?
- Przechowuj SYMBICORT w temperaturze pokojowej między 68 ° F do 77 ° F (20 ° C do 25 ° C).
- Przechowuj SYMBICORT z opuszczonym ustnikiem.
- Zawartość twojego kanistra SYMBICORT jest pod ciśnieniem. Nie przekłuwać ani nie wrzucać kanistra do ognia lub spalarni. Nie używaj ani nie przechowuj go w pobliżu źródeł ciepła lub otwartego ognia. Przechowywanie w temperaturze powyżej 120°F może spowodować pęknięcie kanistra.
- Wyrzuć SYMBICORT 160 mg, gdy licznik osiągnie zero („0”) lub 3 miesiące po wyjęciu SYMBICORT z torebki foliowej, w zależności od tego, co nastąpi wcześniej.
- Przechowuj SYMBICORT 4,5 mcg i wszystkie leki w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i efektywnym korzystaniu z SYMBICORT.
Czasami leki są przepisywane do celów innych niż wymienione w ulotce informacyjnej dla pacjenta. Nie należy stosować leku SYMBICORT 4,5 mcg w przypadku schorzenia, na które nie został przepisany. Nie podawaj leku SYMBICORT innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić.
Możesz poprosić swojego lekarza lub farmaceutę o informacje na temat produktu SYMBICORT 4.5mcg, który jest przeznaczony dla pracowników służby zdrowia.
Jakie są składniki SYMBICORT 4,5mcg?
Składniki aktywne: mikronizowany budezonid i mikronizowany dwuwodny fumaran formoterolu
Składniki nieaktywne: hydrofluoroalkan (HFA 227), powidon K25 USP i glikol polietylenowy 1000 NF
Instrukcja użycia
SYMBORYT (SIM-bi-kort) (budezonid 80 µg i formoterolu fumaran dwuwodny 4,5 µg) Wdychanie Aerozol
SYMBORYT (SIM-bi-kort) (budezonid 160 µg i fumaran formoterolu dwuwodny 4,5 µg) Wdychanie Aerozol
Rysunek 1 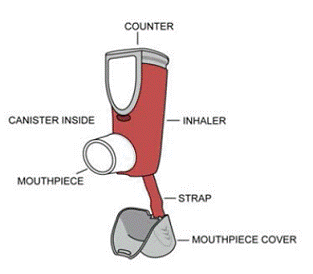 W pozycji pionowej
W pozycji pionowej
Jak korzystać z SYMBICORT
Postępuj zgodnie z poniższymi instrukcjami, aby korzystać z SYMBICORT. Będziesz wdychać (wdychać) lek. W razie jakichkolwiek pytań należy zwrócić się do lekarza lub farmaceuty.
Przygotowanie inhalatora SYMBICORT do użycia
Rysunek 2 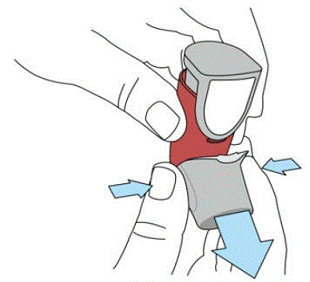
5. Przygotowanie inhalatora SYMBICORT
Zanim użyjesz SYMBICORT po raz pierwszy, musisz go zagruntować. Aby zagruntować SYMBICORT 160mg, trzymaj go w pozycji pionowej. Patrz Rycina 1. Wstrząsaj dobrze inhalatorem SYMBICORT 4,5 mcg przez 5 sekund. Trzymaj inhalator SYMBICORT 160 mg tyłem do siebie i mocno i do końca naciśnij górną część blatu inhalatora SYMBICORT 160 mg, aby uwolnić aerozol testowy. Następnie wstrząsaj nim ponownie przez 5 sekund i wypuść drugi spray testowy. Twój inhalator SYMBICORT 160 mg jest teraz przygotowany i gotowy do użycia. Po pierwszym napełnieniu inhalatora SYMBICORT licznik wskaże 120 lub 60, w zależności od dostarczonego rozmiaru.
Jeśli inhalator SYMBICORT nie będzie używany przez ponad 7 dni lub jeśli zostanie upuszczony, konieczne będzie ponowne przygotowanie inhalatora.
Sposoby przechowywania inhalatora SYMBICORT 160 mg do użytku
Rysunek 3 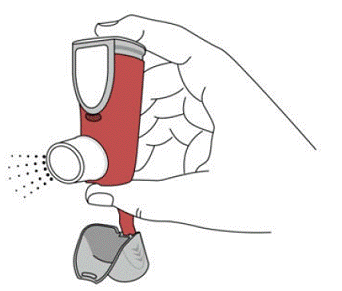
LUB
Rysunek 4 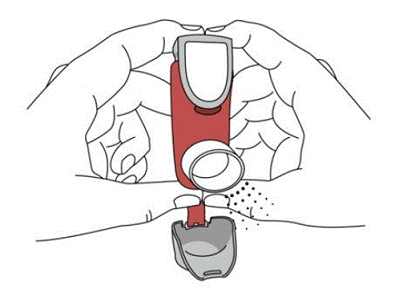
Korzystanie z inhalatora SYMBICORT
6. Wstrząsaj dobrze inhalatorem SYMBICORT 160 mg przez 5 sekund. Zdjąć nasadkę ustnika. Sprawdź ustnik pod kątem ciał obcych.
7. Wykonaj pełny wydech (wydech). Trzymaj inhalator SYMBICORT przy ustach. Włóż biały ustnik całkowicie do ust i zamknij wokół niego usta. Upewnij się, że inhalator SYMBICORT 4,5 mcg jest ustawiony pionowo, a otwór ustnika skierowany jest w stronę tylnej części gardła (patrz Rysunek 5).
Rysunek 5 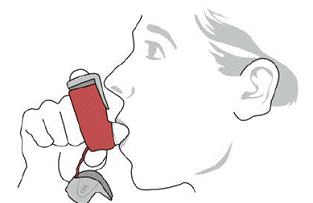
8. Wykonać głęboki i powolny wdech przez usta. Mocno i całkowicie nacisnąć górną część blatu inhalatora SYMBICORT, aby uwolnić lek (patrz Ryciny 3 i 4).
9. Kontynuuj wdech (wdech) i wstrzymaj oddech na około 10 sekund lub tak długo, jak jest to wygodne. Zanim zrobisz wydech (wydech), zwolnij palec z blatu. Trzymać inhalator SYMBICORT w pozycji pionowej i wyjąć z ust.
10. Ponownie wstrząśnij inhalatorem SYMBICORT przez 5 sekund i powtórz kroki od 7 do 9.
Po użyciu inhalatora SYMBICORT
11. Po użyciu zamknij nasadkę ustnika, naciskając, aż zatrzaśnie się na swoim miejscu.
12. Po zakończeniu przyjmowania SYMBICORT (2 wdechy) przepłucz usta wodą. Wypluj wodę. Nie połykaj tego.
Czytanie licznika
- Strzałka na blacie na górze inhalatora SYMBICORT wskazuje liczbę inhalacji (rozciągnięć) pozostałych w inhalatorze.
LICZNIK 
- Licznik będzie odliczał za każdym razem, gdy uwolnisz dawkę leku (albo podczas przygotowywania inhalatora SYMBICORT, albo podczas przyjmowania leku).
- Kiedy strzałka na liczniku zbliża się do 20, zauważysz początek żółtego obszaru informującego, że nadszedł czas, aby zadzwonić do swojego lekarza w celu uzupełnienia.
LICZNIK 
- Ważne jest, aby zwracać uwagę na liczbę inhalacji (rozciągnięć) pozostałych w inhalatorze SYMBICORT 160 mg, odczytując licznik. Wyrzuć SYMBICORT, gdy licznik wskazuje zero („0”) lub 3 miesiące po wyjęciu inhalatora SYMBICORT 160 mg z foliowej saszetki, w zależności od tego, co nastąpi wcześniej. Twój inhalator SYMBICORT może nie wydawać się pusty i może nadal działać, ale nie otrzymasz odpowiedniej ilości leku, jeśli będziesz go nadal stosować. Użyć nowego inhalatora SYMBICORT i postępować zgodnie z instrukcjami dotyczącymi napełniania (patrz instrukcja 5 powyżej).
Jak czyścić inhalator SYMBICORT
Czyść biały ustnik inhalatora SYMBICORT 4,5 mcg co 7 dni. Aby wyczyścić ustnik:
- Zdejmij szarą osłonę ustnika
- Wytrzyj wnętrze i zewnętrzną stronę białego otworu ustnika czystą, suchą ściereczką
- Wymień nasadkę ustnika
- Nie wkładać inhalatora SYMBICORT do wody
- Nie próbuj rozbierać swojego SYMBORYT inhalator
Niniejsze informacje dla pacjenta i instrukcje użytkowania zostały zatwierdzone przez amerykańską Agencję ds. Żywności i Leków.
