Leczenie chorób psychicznych: Strattera 10mg, 18mg, 25mg, 40mg Atomoxetine Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Strattera 40mg i jak się go stosuje?
Strattera to lek na receptę stosowany w leczeniu objawów zespołu nadpobudliwości psychoruchowej z deficytem uwagi (ADHD). Strattera 18mg może być stosowany samodzielnie lub z innymi lekami.
Strattera 10mg jest selektywnym inhibitorem wychwytu zwrotnego noradrenaliny.
Nie wiadomo, czy Strattera jest bezpieczna i skuteczna u dzieci w wieku poniżej 2 lat.
Jakie są możliwe skutki uboczne Strattery?
Strattera 25mg może powodować poważne skutki uboczne, w tym:
- ból w klatce piersiowej,
- problemy z oddychaniem,
- zawroty ,
- halucynacje,
- nowe problemy z zachowaniem,
- agresja,
- wrogość,
- paranoja,
- ból brzucha,
- swędzący,
- objawy grypopodobne,
- ciemny mocz,
- żółtaczka (zażółcenie skóry lub oczu),
- bolesne lub trudne oddawanie moczu oraz
- bolesna lub trwająca dłużej niż 4 godziny erekcja
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Strattera 40mg to:
- mdłości,
- wymioty,
- rozstrój żołądka,
- zaparcie,
- suchość w ustach,
- utrata apetytu,
- zmiany nastroju,
- czuć się zmęczonym,
- zawroty głowy,
- problemy z oddawaniem moczu i
- impotencja, kłopoty z erekcją,
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Strattery. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OSTRZEŻENIE
MYŚLI SAMOBÓJCZE U DZIECI I MŁODZIEŻY
STRATTERA (atomoksetyna) zwiększał ryzyko myśli samobójczych w krótkoterminowych badaniach u dzieci i młodzieży z zespołem nadpobudliwości psychoruchowej z deficytem uwagi (ADHD). Każdy, kto rozważa zastosowanie STRATTERA 18 mg u dzieci lub młodzieży, musi zrównoważyć to ryzyko z potrzebą kliniczną. Choroby współistniejące z ADHD mogą być związane ze wzrostem ryzyka myśli i/lub zachowań samobójczych. Pacjentów rozpoczynających leczenie należy ściśle monitorować pod kątem występowania samobójstw (myśli i zachowań samobójczych), pogorszenia stanu klinicznego lub nietypowych zmian w zachowaniu. Rodziny i opiekunowie powinni być poinformowani o potrzebie ścisłej obserwacji i komunikacji z lekarzem. STRATTERA 10mg jest dopuszczona do ADHD u dzieci i dorosłych. STRATTERA 40mg nie jest zatwierdzona do leczenia dużych zaburzeń depresyjnych. Zbiorcze analizy krótkoterminowych (6 do 18 tygodni) badań kontrolowanych placebo z zastosowaniem preparatu STRATTERA 10 mg u dzieci i młodzieży (w sumie 12 badań z udziałem ponad 2200 pacjentów, w tym 11 badań z ADHD i 1 badanie dotyczące moczenia nocnego) wykazały większe ryzyko myśli samobójczych na początku leczenia u osób otrzymujących produkt STRATTERA w porównaniu z placebo. Średnie ryzyko wystąpienia myśli samobójczych u pacjentów otrzymujących preparat STRATTERA 25 mg wynosiło 0,4% (5/1357 pacjentów), w porównaniu z brakiem u pacjentów otrzymujących placebo (851 pacjentów). W tych próbach nie doszło do samobójstw [zob OSTRZEŻENIA I ŚRODKI ].
OPIS
STRATTERA® (atomoksetyna) jest selektywnym inhibitorem wychwytu zwrotnego noradrenaliny. Chlorowodorek atomoksetyny jest izomerem R(-), co oznaczono metodą dyfrakcji rentgenowskiej. Oznaczenie chemiczne to chlorowodorek (-)-N-metylo-3-fenylo-3-(o-toliloksy)-propyloaminy. Wzór cząsteczkowy to C17H21NO•HCl, co odpowiada masie cząsteczkowej 291,82. Struktura chemiczna to:
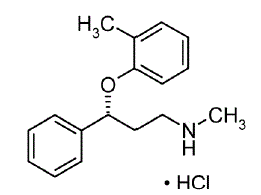
Chlorowodorek atomoksetyny jest białym lub praktycznie białym ciałem stałym, którego rozpuszczalność w wodzie wynosi 27,8 mg/ml.
Kapsułki STRATTERA przeznaczone są wyłącznie do podawania doustnego.
Każda kapsułka zawiera atomoksetyny HCl w ilości odpowiadającej 10, 18, 25, 40, 60, 80 lub 100 mg atomoksetyny. Kapsułki zawierają również wstępnie żelowaną skrobię i dimetikon. Osłonki kapsułek zawierają żelatynę, laurylosiarczan sodu i inne nieaktywne składniki. Osłonki kapsułek zawierają również co najmniej jeden z następujących składników:
FD&C Blue nr 2, syntetyczny żółty tlenek żelaza, dwutlenek tytanu, czerwony tlenek żelaza. Kapsułki są nadrukowane jadalnym czarnym tuszem.
WSKAZANIA
Zespół nadpobudliwości psychoruchowej z deficytem uwagi (ADHD)
STRATTERA 25mg jest wskazana w leczeniu zespołu nadpobudliwości psychoruchowej z deficytem uwagi (ADHD).
Skuteczność preparatu STRATTERA Capsules ustalono w siedmiu badaniach klinicznych u pacjentów ambulatoryjnych z ADHD: czterech trwających od 6 do 9 tygodni badaniach z udziałem dzieci (w wieku od 6 do 18 lat), dwóch 10-tygodniowych badań u dorosłych i jednego badania podtrzymującego u dzieci (6–6 lat). do 15) [patrz Studia kliniczne ].
Rozważania diagnostyczne
Rozpoznanie ADHD (DSM-IV) wskazuje na obecność objawów nadpobudliwości, impulsywności lub braku uwagi, które powodują upośledzenie i które występowały przed ukończeniem 7 roku życia. Objawy muszą być trwałe, muszą być bardziej nasilone niż zwykle obserwowane u osób na porównywalnym poziomie rozwoju, muszą powodować klinicznie istotne upośledzenie, np. w funkcjonowaniu społecznym, akademickim lub zawodowym, oraz muszą występować w 2 lub więcej miejscach, np. w szkole (lub pracy) iw domu. Objawy nie mogą być lepiej wyjaśniane przez inne zaburzenie psychiczne.
Specyficzna etiologia ADHD jest nieznana i nie ma jednego testu diagnostycznego. Właściwa diagnoza wymaga wykorzystania nie tylko medycznych, ale także specjalnych zasobów psychologicznych, edukacyjnych i społecznych. Uczenie się może, ale nie musi być upośledzone. Diagnoza musi opierać się na pełnej historii i ocenie pacjenta, a nie wyłącznie na obecności wymaganej liczby cech DSM-IV.
przypadku typu nieuważnego co najmniej 6 z następujących objawów musi utrzymywać się przez co najmniej 6 miesięcy: brak dbałości o szczegóły/nieostrożne błędy, brak ciągłej uwagi, słaby słuchacz, niewykonanie zadań, zła organizacja, unikanie zadań wymaga ciągłego wysiłku umysłowego, gubi rzeczy, łatwo się rozprasza, zapomina. W przypadku typu hiperaktywno-impulsywnego co najmniej 6 z następujących objawów musi utrzymywać się przez co najmniej 6 miesięcy: wiercenie się/wiercenie się, wstawanie z siedzenia, niewłaściwe bieganie/wspinanie się, trudności z cichymi czynnościami, „w biegu”, nadmierne mówienie, gadanie odpowiedzi, nie mogę się doczekać kolej, natrętny. W przypadku diagnozy typu złożonego muszą być spełnione zarówno kryteria nieuważności, jak i nadpobudliwości i impulsywności.
Potrzeba kompleksowego programu leczenia
STRATTERA 18mg jest wskazana jako integralna część kompleksowego programu leczenia ADHD, który może obejmować inne środki (psychologiczne, edukacyjne, społeczne) dla pacjentów z tym zespołem. Leczenie farmakologiczne może nie być wskazane u wszystkich pacjentów z tym zespołem. Farmakoterapia nie jest przeznaczona do stosowania u pacjenta, który wykazuje objawy wtórne do czynników środowiskowych i/lub innych pierwotnych zaburzeń psychicznych, w tym psychozy. W przypadku dzieci i młodzieży z tą diagnozą odpowiednie umiejscowienie edukacyjne jest niezbędne, a interwencja psychospołeczna jest często pomocna. Gdy same środki zaradcze są niewystarczające, decyzja o przepisaniu leków leczniczych będzie zależeć od oceny przez lekarza przewlekłości i nasilenia objawów u pacjenta.
DAWKOWANIE I SPOSÓB PODAWANIA
Ostre leczenie
Dawkowanie u dzieci i młodzieży do 70 kg masy ciała
STRATTERA 40 mg należy rozpocząć od całkowitej dawki dobowej około 0,5 mg/kg i zwiększać po co najmniej 3 dniach do docelowej całkowitej dawki dobowej wynoszącej około 1,2 mg/kg podawanej albo jako pojedynczą dawkę dobową rano, albo jako równomiernie podzieloną dawki rano i późnym popołudniem/wczesnym wieczorem. Nie wykazano dodatkowych korzyści w przypadku dawek większych niż 1,2 mg/kg/dobę [patrz Studia kliniczne ].
Całkowita dawka dobowa u dzieci i młodzieży nie powinna przekraczać 1,4 mg/kg lub 100 mg, w zależności od tego, która z tych wartości jest mniejsza.
Dawkowanie u dzieci i młodzieży powyżej 70 kg masy ciała i dorosłych
STRATTERA 18 mg należy rozpocząć od całkowitej dawki dobowej 40 mg i zwiększyć po co najmniej 3 dniach do docelowej całkowitej dawki dobowej około 80 mg podawanej albo jako pojedynczą dawkę dobową rano, albo jako równomiernie podzielone dawki rano i późne popołudnie/wczesny wieczór. Po 2 do 4 dodatkowych tygodniach dawkę można zwiększyć do maksymalnie 100 mg u pacjentów, u których nie uzyskano optymalnej odpowiedzi. Nie ma danych potwierdzających zwiększoną skuteczność przy wyższych dawkach [patrz Studia kliniczne ].
Maksymalna zalecana całkowita dawka dobowa u dzieci i młodzieży powyżej 70 kg oraz dorosłych wynosi 100 mg.
Konserwacja/przedłużone leczenie
Powszechnie uważa się, że leczenie farmakologiczne ADHD może być konieczne przez dłuższy czas. W kontrolowanym badaniu wykazano korzyści z utrzymania pacjentów pediatrycznych (w wieku 6-15 lat) z ADHD na STRATTERA 18 mg po uzyskaniu odpowiedzi w zakresie dawek od 1,2 do 1,8 mg/kg/dobę. Pacjenci przydzieleni do grupy STRATTERA w fazie podtrzymującej na ogół otrzymywali tę samą dawkę, jaką stosowano do uzyskania odpowiedzi w fazie otwartej próby. Lekarz decydujący się na stosowanie preparatu STRATTERA przez dłuższy czas powinien okresowo dokonywać ponownej oceny długoterminowej przydatności leku dla indywidualnego pacjenta [patrz Studia kliniczne ].
Ogólne informacje o dawkowaniu
STRATTERA można przyjmować z jedzeniem lub bez jedzenia.
STRATTERA 40 mg można odstawić bez zmniejszania dawki.
Kapsułki STRATTERA nie są przeznaczone do otwierania, należy je przyjmować w całości [patrz INFORMACJA O PACJENCIE ].
Bezpieczeństwo pojedynczych dawek powyżej 120 mg i całkowitych dawek dobowych powyżej 150 mg nie było systematycznie oceniane.
Dawkowanie w określonych populacjach
Dostosowanie dawkowania u pacjentów z zaburzeniami czynności wątroby
W przypadku pacjentów z ADHD i niewydolnością wątroby (HI) zaleca się następujące dostosowanie dawki: U pacjentów z umiarkowanym HI (klasa B w skali Childa-Pugha) dawkę początkową i docelową należy zmniejszyć do 50% normalnej dawki (u pacjentów bez CZEŚĆ). W przypadku pacjentów z ciężkim HI (klasa C wg Childa-Pugha) dawkę początkową i dawki docelowe należy zmniejszyć do 25% normy [patrz Używaj w określonych populacjach ].
Dostosowanie dawkowania do stosowania z silnym inhibitorem CYP2D6 lub u pacjentów, o których wiadomo, że są PM-y CYP2D6
U dzieci i młodzieży o masie ciała do 70 kg, którym podaje się silne inhibitory CYP2D6, np. paroksetynę, fluoksetynę i chinidynę, lub u pacjentów, o których wiadomo, że są PM CYP2D6, stosowanie produktu STRATTERA należy rozpocząć od 0,5 mg/kg/dobę i tylko zwiększyć do zazwyczaj stosowana dawka docelowa to 1,2 mg/kg/dobę, jeśli objawy nie ustępują po 4 tygodniach, a dawka początkowa jest dobrze tolerowana.
dzieci i młodzieży o masie ciała powyżej 70 kg oraz dorosłych otrzymujących silne inhibitory CYP2D6, np. paroksetynę, fluoksetynę i chinidynę, STRATTERA należy rozpocząć od dawki 40 mg/dobę i zwiększać ją do zwykłej dawki docelowej 80 mg/dobę tylko w przypadku ustąpienia objawów poprawa po 4 tygodniach, a początkowa dawka jest dobrze tolerowana.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Każda kapsułka zawiera atomoksetyny HCl w ilości odpowiadającej 10 mg (nieprzezroczysty biały, nieprzezroczysty biały), 18 mg (złoty, nieprzezroczysty biały), 25 mg (nieprzezroczysty niebieski, nieprzezroczysty biały), 40 mg (nieprzezroczysty niebieski, nieprzezroczysty niebieski), 60 mg (nieprzezroczysty Niebieski, złoty), 80 mg (nieprzezroczysty brąz, nieprzezroczysty biały) lub 100 mg (nieprzezroczysty brąz, nieprzezroczysty brąz) atomoksetyny.
Składowania i stosowania
Przechowywać w 25°C (77°F); dopuszczalne odchylenia do 15° do 30°C (59° do 86°F) [patrz Kontrolowana temperatura pokojowa USP].
Sprzedawane przez: Lilly USA, LLC Indianapolis, IN 46285, USA. Aktualizacja: maj 2017 r.
SKUTKI UBOCZNE
Doświadczenie w badaniach klinicznych
STRATTERA 10 mg została podana 5382 dzieciom lub młodzieży z ADHD i 1007 dorosłym z ADHD w badaniach klinicznych. Podczas badań klinicznych ADHD 1625 dzieci i młodzieży leczono dłużej niż 1 rok, a 2529 dzieci i młodzieży leczono przez ponad 6 miesięcy.
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Badania kliniczne dla dzieci i młodzieży
Przyczyny przerwania leczenia z powodu działań niepożądanych w badaniach klinicznych u dzieci i młodzieży
ostrych badaniach kontrolowanych placebo u dzieci i młodzieży 3,0% (48/1613) pacjentów stosujących atomoksetynę i 1,4% (13/945) pacjentów otrzymujących placebo przerwało leczenie z powodu działań niepożądanych. We wszystkich badaniach (w tym badaniach otwartych i badaniach długoterminowych) 6,3% pacjentów z intensywnym metabolizmem (EM) i 11,2% pacjentów ze słabym metabolizmem (PM) przerwało leczenie z powodu działań niepożądanych. Wśród pacjentów leczonych STRATTERA drażliwość (0,3%, N=5); senność (0,3%, N=5); agresja (0,2%, N=4); nudności (0,2%, N=4); wymioty (0,2%, N=4); ból brzucha (0,2%, N=4); zaparcia (0,1%, N=2); zmęczenie (0,1%, N=2); nieprawidłowe samopoczucie (0,1%, N=2); i ból głowy (0,1%, N=2) były powodem przerwania leczenia zgłaszanym przez więcej niż 1 pacjenta.
Napady padaczkowe
Produkt STRATTERA nie był systematycznie oceniany u dzieci z zaburzeniami drgawkowymi, ponieważ pacjenci ci zostali wykluczeni z badań klinicznych podczas badań przed wprowadzeniem produktu do obrotu. W programie rozwoju klinicznego drgawki zgłoszono u 0,2% (12/5073) dzieci w średnim wieku 10 lat (zakres od 6 do 16 lat). W tych badaniach klinicznych ryzyko drgawek wśród osób słabo metabolizujących wynosiło 0,3% (1/293) w porównaniu z 0,2% (11/4741) dla osób intensywnie metabolizujących.
Często obserwowane działania niepożądane w ostrych badaniach kontrolowanych placebo u dzieci i młodzieży
Często obserwowane działania niepożądane związane ze stosowaniem preparatu STRATTERA (częstość występowania 2% lub więcej) i nieobserwowane z równoważną częstością wśród pacjentów otrzymujących placebo (częstość występowania STRATTERA 40 mg większa niż placebo) wymieniono w Tabeli 2. Wyniki były podobne w przypadku BID oraz badanie QD, z wyjątkiem przedstawionych w Tabeli 3, w których przedstawiono wyniki zarówno BID, jak i QD dla wybranych działań niepożądanych na podstawie statystycznie istotnych testów Breslow-Day. Najczęściej obserwowanymi działaniami niepożądanymi u pacjentów leczonych preparatem STRATTERA (częstość występowania 5% lub większa i co najmniej dwukrotnie częściej niż u pacjentów otrzymujących placebo, przy dawkowaniu dwa razy na dobę lub raz na dobę) były: nudności, wymioty, zmęczenie, zmniejszony apetyt, ból brzucha i senność (patrz tabele 2 i 3).
Dodatkowe dane z badań klinicznych ADHD (kontrolowanych i niekontrolowanych) wykazały, że około 5 do 10% pacjentów pediatrycznych doświadczyło potencjalnie klinicznie istotnych zmian w częstości akcji serca (≥20 uderzeń na minutę) lub ciśnieniu krwi (≥15 do 20 mm Hg) [patrz PRZECIWWSKAZANIA oraz OSTRZEŻENIA I ŚRODKI ].
Następujące działania niepożądane wystąpiły u co najmniej 2% dzieci i młodzieży z CYP2D6 PM i były statystycznie istotnie częstsze u pacjentów z PM w porównaniu z pacjentami z CYP2D6 EM: bezsenność (11% PM, 6% EM); waga spadła (7% PM, 4% EM); zaparcia (7% PM, 4% EM); depresja1 (7% PM, 4% EM); drżenie (5% PM, 1% EM); otarcia (4% PM, 2% EM); średnia bezsenność (3% PM, 1% EM); zapalenie spojówek (3% PM, 1% EM); omdlenia (3% PM, 1% EM); przebudzenie wcześnie rano (2% PM, 1% EM); rozszerzenie źrenic (2% PM, 1% EM); sedacja (4% PM, 2% EM).
1Depresja obejmuje następujące terminy: depresja, duża depresja, objawy depresyjne, obniżony nastrój, dysforia.
Badania kliniczne dla dorosłych
Przyczyny przerwania leczenia z powodu działań niepożądanych w ostrych badaniach kontrolowanych placebo u dorosłych
ostrych badaniach kontrolowanych placebo u dorosłych, 11,3% (61/541) pacjentów z atomoksetyną i 3,0% (12/405) pacjentów z grupy placebo przerwało leczenie z powodu działań niepożądanych. Wśród pacjentów leczonych STRATTERA bezsenność (0,9%, N=5); nudności (0,9%, N=5); ból w klatce piersiowej (0,6%, N=3); zmęczenie (0,6%, N=3); lęk (0,4%, N=2); zaburzenia erekcji (0,4%, N=2); wahania nastroju (0,4%, N=2); nerwowość (0,4%, N=2); kołatanie serca (0,4%, N=2); zatrzymanie moczu (0,4%, N=2) były powodem przerwania leczenia zgłaszanym przez więcej niż 1 pacjenta.
Napady padaczkowe
STRATTERA nie była systematycznie oceniana u dorosłych pacjentów z napadami padaczkowymi, ponieważ ci pacjenci zostali wykluczeni z badań klinicznych podczas badań przed wprowadzeniem produktu do obrotu. W programie rozwoju klinicznego drgawki zgłoszono u 0,1% (1/748) dorosłych pacjentów. W tych badaniach klinicznych żaden z osób słabo metabolizujących (0/43) nie zgłosił napadów padaczkowych w porównaniu z 0,1% (1/705) w przypadku osób intensywnie metabolizujących.
Często obserwowane działania niepożądane w ostrych badaniach kontrolowanych placebo u dorosłych
Często obserwowane działania niepożądane związane ze stosowaniem preparatu STRATTERA (częstość występowania 2% lub większa) i nieobserwowane z równoważną częstością wśród pacjentów otrzymujących placebo (częstość występowania STRATTERA 25 mg większa niż placebo) wymieniono w Tabeli 4. Najczęściej obserwowane działania niepożądane u pacjentów leczonych preparatem STRATTERA (częstość występowania 5% lub większa i co najmniej dwukrotnie większa niż u pacjentów otrzymujących placebo) były: zaparcia, suchość w ustach, nudności, zmniejszony apetyt, zawroty głowy, zaburzenia erekcji i zaburzenia oddawania moczu (patrz Tabela 4). Dodatkowe dane z badań klinicznych ADHD (kontrolowanych i niekontrolowanych) wykazały, że około 5 do 10% dorosłych pacjentów doświadczyło potencjalnie klinicznie istotnych zmian w częstości akcji serca (≥20 uderzeń na minutę) lub ciśnieniu krwi (≥15 do 20 mm Hg) [patrz PRZECIWWSKAZANIA oraz OSTRZEŻENIA I ŚRODKI ].
Następujące działania niepożądane wystąpiły u co najmniej 2% dorosłych pacjentów ze słabym metabolizmem (PM) z udziałem CYP2D6 i były statystycznie istotnie częstsze u pacjentów z PM w porównaniu z pacjentami z intensywnym metabolizmem (EM) z udziałem CYP2D6: niewyraźne widzenie (4% PM, 1% EM) ); suchość w ustach (35% PM, 17% EM); zaparcia (11% PM, 7% EM); uczucie zdenerwowania (5% PM, 2% EM); zmniejszony apetyt (23% PM, 15% EM); drżenie (5% PM, 1% EM); bezsenność (19% PM, 11% EM); zaburzenia snu (7% PM, 3% EM); średnia bezsenność (5% PM, 3% EM); bezsenność końcowa (3% PM, 1% EM); zatrzymanie moczu (6% PM, 1% EM); zaburzenia erekcji (21% PM, 9% EM); zaburzenia wytrysku (6% PM, 2% EM); nadpotliwość (15% PM, 7% EM); chłód obwodowy (3% PM, 1% EM).
Zaburzenia seksualne u mężczyzn i kobiet
Wydaje się, że atomoksetyna zaburza funkcje seksualne u niektórych pacjentów. Zmiany w pożądaniu seksualnym, sprawności seksualnej i satysfakcji seksualnej nie są dobrze oceniane w większości badań klinicznych, ponieważ wymagają one szczególnej uwagi, a pacjenci i lekarze mogą niechętnie je omawiać. W związku z tym szacunki częstości występowania nieprzewidzianych doświadczeń seksualnych i wydajności, przytaczane na etykietach produktów, prawdopodobnie zaniżają rzeczywistą częstość występowania. W tabeli 4 powyżej przedstawiono częstość występowania seksualnych działań niepożądanych zgłaszanych przez co najmniej 2% dorosłych pacjentów przyjmujących STRATTERA w badaniach kontrolowanych placebo.
Nie ma odpowiednich i dobrze kontrolowanych badań oceniających dysfunkcje seksualne przy leczeniu STRATTERA 40 mg. Chociaż trudno jest dokładnie określić ryzyko dysfunkcji seksualnych związanych ze stosowaniem STRATTERA 40 mg, lekarze powinni rutynowo wypytywać o takie możliwe skutki uboczne.
Spontaniczne raporty postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania produktu STRATTERA po dopuszczeniu do obrotu. O ile nie określono inaczej, te działania niepożądane wystąpiły u dorosłych, dzieci i młodzieży. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Układu sercowo-naczyniowego - Wydłużenie odstępu QT, omdlenia.
Wpływ na naczynia obwodowe - Fenomen Raynauda.
Zaburzenia ogólne i stany w miejscu podania - Letarg.
Układ mięśniowo-szkieletowy - Rabdomioliza.
Zaburzenia układu nerwowego - Niedoczulica; parestezje u dzieci i młodzieży; zaburzenia czuciowe; tiki.
Zaburzenia psychiczne - Depresja i obniżony nastrój; niepokój, zmiany libido.
Napady padaczkowe W okresie po wprowadzeniu produktu do obrotu zgłaszano napady padaczkowe. Przypadki napadów po wprowadzeniu do obrotu obejmują pacjentów z istniejącymi wcześniej zaburzeniami napadowymi oraz tych, u których zidentyfikowano czynniki ryzyka napadów, jak również pacjentów bez historii ani zidentyfikowanych czynników ryzyka napadów. Dokładny związek między STRATTERA 40 mg a napadami jest trudny do oceny ze względu na niepewność co do podstawowego ryzyka napadów u pacjentów z ADHD.
Zaburzenia skóry i tkanki podskórnej - Łysienie, nadmierne pocenie się.
Układ moczowo-płciowy - Ból miednicy u mężczyzn; wahanie moczu u dzieci i młodzieży; zatrzymanie moczu u dzieci i młodzieży.
INTERAKCJE Z LEKAMI
Inhibitory monoaminooksydazy
przypadku innych leków, które wpływają na stężenie monoaminy w mózgu, zgłaszano poważne reakcje, czasami prowadzące do zgonu (w tym hipertermię, sztywność mięśni, mioklonie, niestabilność autonomiczną z możliwymi szybkimi wahaniami parametrów życiowych oraz zmiany stanu psychicznego, w tym skrajne pobudzenie przechodzące w majaczenie i śpiączkę). ) w połączeniu z IMAO. Niektóre przypadki prezentowały cechy przypominające złośliwy zespół neuroleptyczny. Takie reakcje mogą wystąpić, gdy leki te są podawane jednocześnie lub w bliskim sąsiedztwie [patrz PRZECIWWSKAZANIA ].
Wpływ inhibitorów CYP2D6 na atomoksetynę
U osób intensywnie metabolizujących (EM) inhibitory CYP2D6 (np. paroksetyna, fluoksetyna i chinidyna) zwiększają stężenia atomoksetyny w osoczu w stanie stacjonarnym do ekspozycji podobnych do obserwowanych u osób słabo metabolizujących (PM). U osobników z EM leczonych paroksetyną lub fluoksetyną, AUC atomoksetyny jest około 6 do 8 razy, a Css, max jest około 3 do 4 razy większe niż sama atomoksetyna.
Badania in vitro sugerują, że jednoczesne podawanie inhibitorów cytochromu P450 do PM nie zwiększy stężenia atomoksetyny w osoczu.
Leki przeciwnadciśnieniowe i środki ciśnieniowe
Ze względu na możliwy wpływ na ciśnienie krwi, STRATTERA należy stosować ostrożnie z lekami przeciwnadciśnieniowymi i presyjnymi (np. dopaminą, dobutaminą) lub innymi lekami podwyższającymi ciśnienie krwi.
Albuterol
Produkt STRATTERA należy stosować ostrożnie u pacjentów leczonych ogólnie (doustnie lub dożylnie) albuterolem (lub innymi beta2-agonistami), ponieważ działanie albuterolu na układ sercowo-naczyniowy może być nasilone, powodując zwiększenie częstości akcji serca i ciśnienia krwi. Albuterol (600 mcg dożylnie przez 2 godziny) wywoływał wzrost częstości akcji serca i ciśnienia krwi. Efekty te nasilały się po zastosowaniu atomoksetyny (60 mg dwa razy na dobę przez 5 dni) i były najbardziej widoczne po początkowym równoczesnym podaniu albuterolu i atomoksetyny. Jednak w innym badaniu po jednoczesnym podaniu wziewnej dawki albuterolu (200-800 mikrogramów) i atomoksetyny (80 mg QD przez 5 dni) u 21 zdrowych Azjatów, których wykluczono z powodu złego stan metabolizatora.
Wpływ atomoksetyny na enzymy P450
Atomoksetyna nie powodowała klinicznie istotnego hamowania ani indukcji enzymów cytochromu P450, w tym CYP1A2, CYP3A, CYP2D6 i CYP2C9.
Substrat CYP3A (np. Midazolam)
Jednoczesne podawanie produktu STRATTERA (60 mg dwa razy na dobę przez 12 dni) z midazolamem, związkiem modelowym dla leków metabolizowanych przez CYP3A4 (pojedyncza dawka 5 mg), spowodowało 15% wzrost AUC midazolamu. Nie zaleca się dostosowywania dawki leków metabolizowanych przez CYP3A.
Substrat CYP2D6 (np. dezypramina)
Jednoczesne podawanie STRATTERA (40 lub 60 mg dwa razy na dobę przez 13 dni) z dezypraminą, związkiem modelowym dla leków metabolizowanych przez CYP2D6 (pojedyncza dawka 50 mg), nie zmieniło farmakokinetyki dezypraminy. Nie zaleca się dostosowywania dawki leków metabolizowanych przez CYP2D6.
Alkohol
Spożywanie etanolu z STRATTERA 18mg nie zmieniło odurzającego działania etanolu.
Metylofenidat
Jednoczesne podawanie metylofenidatu z STRATTERA 18 mg nie zwiększało wpływu na układ sercowo-naczyniowy poza obserwowanym w przypadku samego metylofenidatu.
Leki silnie związane z białkiem osocza
Przeprowadzono badania wypierania leku in vitro z atomoksetyną i innymi silnie związanymi lekami w stężeniach terapeutycznych. Atomoksetyna nie wpływała na wiązanie warfaryny, kwasu acetylosalicylowego, fenytoiny ani diazepamu z ludzką albuminą. Podobnie związki te nie wpływają na wiązanie atomoksetyny z ludzką albuminą.
Leki wpływające na pH żołądka
Leki podnoszące pH żołądka (wodorotlenek magnezu/wodorotlenek glinu, omeprazol) nie miały wpływu na biodostępność produktu STRATTERA.
Nadużywanie i uzależnienie od narkotyków
Substancja kontrolowana
STRATTERA nie jest substancją kontrolowaną.
Nadużywać
W randomizowanym, podwójnie zaślepionym, kontrolowanym placebo badaniu dotyczącym potencjalnego nadużywania u dorosłych, porównującym działanie STRATTERA i placebo, STRATTERA nie była związana z wzorcem odpowiedzi sugerującym właściwości pobudzające lub euforyczne.
Zależność
Dane z badań klinicznych z udziałem ponad 2000 dzieci, młodzieży i dorosłych z ADHD oraz ponad 1200 dorosłych z depresją wykazały jedynie pojedyncze przypadki odejścia od narkotyków lub niewłaściwego samopodawania związane z STRATTERA. Nie było dowodów na nawrót objawów lub działań niepożądanych sugerujących zespół odstawienia leku lub zespół odstawienia.
Doświadczenie zwierząt
Badania nad dyskryminacją leków na szczurach i małpach wykazały niespójne uogólnianie bodźców między atomoksetyną a kokainą.
OSTRZEŻENIA
Zawarte jako część "ŚRODKI OSTROŻNOŚCI" Sekcja
ŚRODKI OSTROŻNOŚCI
Myśl samobójcza
STRATTERA zwiększał ryzyko myśli samobójczych w krótkoterminowych badaniach u dzieci i młodzieży z zespołem nadpobudliwości psychoruchowej z deficytem uwagi (ADHD). Zbiorcze analizy krótkoterminowych (6 do 18 tygodni) kontrolowanych placebo badań klinicznych produktu STRATTERA u dzieci i młodzieży wykazały większe ryzyko wystąpienia myśli samobójczych we wczesnym okresie leczenia u osób otrzymujących STRATTERA. Przeprowadzono w sumie 12 badań (11 z ADHD i 1 z moczeniem) z udziałem ponad 2200 pacjentów (w tym 1357 pacjentów otrzymujących STRATTERA i 851 otrzymujących placebo). Średnie ryzyko wystąpienia myśli samobójczych u pacjentów otrzymujących preparat STRATTERA wynosiło 0,4% (5/1357 pacjentów), w porównaniu z brakiem u pacjentów otrzymujących placebo. Wśród tych około 2200 pacjentów wystąpiła 1 próba samobójcza, która wystąpiła u pacjenta leczonego preparatem STRATTERA. W tych próbach nie doszło do samobójstw. Wszystkie reakcje wystąpiły u dzieci w wieku 12 lat lub młodszych. Wszystkie reakcje wystąpiły w pierwszym miesiącu leczenia. Nie wiadomo, czy ryzyko myśli samobójczych u pacjentów pediatrycznych rozciąga się na długotrwałe stosowanie. Podobna analiza u dorosłych pacjentów leczonych preparatem STRATTERA z powodu ADHD lub dużej depresji (MDD) nie wykazała zwiększonego ryzyka myśli lub zachowań samobójczych w związku ze stosowaniem preparatu STRATTERA.
Wszyscy pacjenci pediatryczni leczeni produktem STRATTERA powinni być odpowiednio monitorowani i ściśle obserwowani pod kątem pogorszenia stanu klinicznego, skłonności samobójczych i nietypowych zmian w zachowaniu, zwłaszcza w ciągu pierwszych kilku miesięcy leczenia farmakologicznego lub w momencie zmiany dawki, zwiększania lub zmniejszania .
Podczas stosowania produktu STRATTERA zgłaszano następujące objawy: lęk, pobudzenie, ataki paniki, bezsenność, drażliwość, wrogość, agresywność, impulsywność, akatyzję (niepokój psychoruchowy), hipomania i mania. Chociaż nie ustalono związku przyczynowo-skutkowego między pojawieniem się takich objawów a pojawieniem się impulsów samobójczych, istnieje obawa, że takie objawy mogą być prekursorem pojawiania się samobójstw. Dlatego pacjenci leczeni preparatem STRATTERA 40 mg powinni być obserwowani pod kątem wystąpienia takich objawów.
Należy rozważyć zmianę schematu leczenia, w tym ewentualnie odstawienie leku, u pacjentów, u których występują pojawiające się myśli samobójcze lub objawy, które mogą być prekursorem pojawiających się myśli samobójczych, zwłaszcza jeśli objawy te są ciężkie lub nagłe, lub nie były częścią objawy u pacjenta.
Rodziny i opiekunów pacjentów pediatrycznych leczonych preparatem STRATTERA 10 mg należy ostrzec o konieczności monitorowania pacjentów pod kątem pojawienia się pobudzenia, drażliwości, nietypowych zmian w zachowaniu i innych objawów opisanych powyżej, a także wystąpienia myśli samobójczych oraz natychmiast zgłoś takie objawy świadczeniodawcy. Taki monitoring powinien obejmować codzienną obserwację rodzin i opiekunów.
Ciężkie uszkodzenie wątroby
Raporty postmarketingowe wskazują, że STRATTERA może powodować poważne uszkodzenie wątroby. Chociaż w badaniach klinicznych z udziałem około 6000 pacjentów nie wykryto dowodów na uszkodzenie wątroby, po wprowadzeniu produktu do obrotu występowały rzadkie przypadki klinicznie istotnego uszkodzenia wątroby, które uznano za prawdopodobnie lub prawdopodobnie związane ze stosowaniem produktu STRATTERA 40 mg. Zgłaszano również rzadkie przypadki niewydolności wątroby, w tym przypadek, w którym doszło do przeszczepu wątroby. Z powodu prawdopodobnego zaniżania danych nie jest możliwe dokładne oszacowanie rzeczywistej częstości występowania tych reakcji. Zgłoszone przypadki uszkodzenia wątroby wystąpiły w większości przypadków w ciągu 120 dni od rozpoczęcia stosowania atomoksetyny, au niektórych pacjentów stwierdzono znacznie podwyższony poziom enzymów wątrobowych [>20 x górna granica normy (ULN)] oraz żółtaczkę ze znacznie podwyższonym poziomem bilirubiny (>2 X GGN), a następnie powrót do zdrowia po odstawieniu atomoksetyny. U jednego pacjenta uszkodzenie wątroby, objawiające się podwyższeniem enzymów wątrobowych do 40 x GGN i żółtaczką z bilirubiną do 12 x GGN, powróciło po ponownym podaniu leku, a następnie nastąpiło wyzdrowienie po odstawieniu leku, dostarczając dowodów na to, że STRATTERA prawdopodobnie spowodowała uszkodzenie wątroby. Takie reakcje mogą wystąpić kilka miesięcy po rozpoczęciu leczenia, ale nieprawidłowości laboratoryjne mogą się nasilać jeszcze przez kilka tygodni po odstawieniu leku. Opisany powyżej pacjent wyzdrowiał po uszkodzeniu wątroby i nie wymagał przeszczepu wątroby.
Leczenie produktem STRATTERA należy przerwać u pacjentów z żółtaczką lub laboratoryjnie potwierdzonym uszkodzeniem wątroby i nie należy go wznawiać. Testy laboratoryjne w celu określenia poziomu enzymów wątrobowych należy wykonać po pojawieniu się pierwszych objawów lub oznak dysfunkcji wątroby (np. świąd, ciemny mocz, żółtaczka, tkliwość w prawym górnym kwadrancie lub niewyjaśnione objawy grypopodobne) [patrz Testy laboratoryjne , INFORMACJA O PACJENCIE ].
Poważne zdarzenia sercowo-naczyniowe
Nagła śmierć i istniejące wcześniej strukturalne zaburzenia serca lub inne poważne problemy z sercem
Dzieci i młodzież
związku z leczeniem atomoksetyną w zwykłych dawkach u dzieci i młodzieży z wadami strukturalnymi serca lub innymi poważnymi chorobami serca zgłaszano nagły zgon. Chociaż niektóre poważne problemy z sercem same w sobie niosą ze sobą zwiększone ryzyko nagłej śmierci, atomoksetyny generalnie nie należy stosować u dzieci i młodzieży ze znanymi poważnymi nieprawidłowościami strukturalnymi serca, kardiomiopatią, poważnymi zaburzeniami rytmu serca lub innymi poważnymi problemami kardiologicznymi, które mogą narazić ich na zwiększoną wrażliwość na noradrenergiczne działanie atomoksetyny.
Dorośli ludzie
osób dorosłych przyjmujących atomoksetynę w zwykłych dawkach w leczeniu ADHD zgłaszano nagłe zgony, udar mózgu i zawał mięśnia sercowego. Chociaż rola atomoksetyny w tych dorosłych przypadkach jest również nieznana, prawdopodobieństwo wystąpienia poważnych strukturalnych zaburzeń serca, kardiomiopatii, poważnych zaburzeń rytmu serca, choroby wieńcowej lub innych poważnych problemów kardiologicznych u dorosłych jest większe niż u dzieci. Należy rozważyć nieleczenie dorosłych z klinicznie istotnymi nieprawidłowościami serca.
Ocena stanu sercowo-naczyniowego u pacjentów leczonych atomoksetyną
Dzieci, młodzież lub dorośli, u których rozważane jest leczenie atomoksetyną, powinni mieć dokładny wywiad (w tym ocenę rodzinnego wywiadu nagłego zgonu lub arytmii komorowej) oraz badanie fizykalne w celu oceny obecności choroby serca i powinni otrzymać dalsze badania kardiologiczne. ocena, czy wyniki sugerują taką chorobę (np. elektrokardiogram i echokardiogram). Pacjenci, u których podczas leczenia atomoksetyną wystąpią takie objawy, jak wysiłkowy ból w klatce piersiowej, omdlenia o niewyjaśnionej przyczynie lub inne objawy wskazujące na chorobę serca, należy niezwłocznie poddać ocenie kardiologicznej.
Wpływ na ciśnienie krwi i tętno
Produkt STRATTERA należy stosować ostrożnie u pacjentów, których podstawowe schorzenia mogą ulec pogorszeniu w wyniku wzrostu ciśnienia krwi lub częstości akcji serca, takich jak niektórzy pacjenci z nadciśnieniem, tachykardią lub chorobą sercowo-naczyniową lub mózgowo-naczyniową. Nie należy go stosować u pacjentów z ciężkimi zaburzeniami serca lub naczyń, których stan może ulec pogorszeniu w przypadku klinicznie istotnego wzrostu ciśnienia krwi lub częstości akcji serca [patrz PRZECIWWSKAZANIA ]. Tętno i ciśnienie krwi należy mierzyć przed rozpoczęciem leczenia, po zwiększeniu dawki produktu STRATTERA oraz okresowo podczas leczenia, aby wykryć możliwe klinicznie istotne wzrosty.
Poniższa tabela przedstawia dane z krótkoterminowych, kontrolowanych placebo badań klinicznych dla odsetka pacjentów, u których wystąpił wzrost: rozkurczowego ciśnienia krwi ≥15 mm Hg; skurczowe ciśnienie krwi ≥20 mm Hg; częstość akcji serca większa lub równa 20 uderzeń na minutę, zarówno w populacji pediatrycznej, jak i dorosłych (patrz Tabela 1).
kontrolowanych placebo badaniach rejestracyjnych z udziałem pacjentów pediatrycznych tachykardia została zidentyfikowana jako zdarzenie niepożądane u 0,3% (5/1597) pacjentów z grupy STRATTERA 10 mg w porównaniu z 0% (0/934) pacjentów otrzymujących placebo. Średni wzrost częstości akcji serca u pacjentów z intensywnym metabolizmem (EM) wyniósł 5,0 uderzeń/minutę, au pacjentów ze słabym metabolizmem (PM) 9,4 uderzeń/minutę.
W badaniach klinicznych z udziałem dorosłych, w których dostępny był status EM/PM, średni wzrost częstości akcji serca u pacjentów z PM był znacznie wyższy niż u pacjentów z EM (11 uderzeń/minutę w porównaniu z 7,5 uderzeń/minutę). Wpływ na tętno może mieć znaczenie kliniczne u niektórych pacjentów z PM.
W kontrolowanych placebo badaniach rejestracyjnych z udziałem dorosłych pacjentów tachykardię zidentyfikowano jako zdarzenie niepożądane u 1,5% (8/540) pacjentów otrzymujących produkt STRATTERA 25 mg w porównaniu z 0,5% (2/402) pacjentów otrzymujących placebo.
badaniach klinicznych z udziałem dorosłych, w których dostępny był stan EM/PM, średnia zmiana rozkurczowego ciśnienia krwi od wartości początkowej u pacjentów z PM była wyższa niż u pacjentów z PM (4,21 w porównaniu z 2,13 mm Hg), podobnie jak średnia zmiana od wartości wyjściowej ciśnienia skurczowego (PM : 2,75 w porównaniu z EM: 2,40 mm Hg). Wpływ ciśnienia krwi może mieć znaczenie kliniczne u niektórych pacjentów z PM.
pacjentów przyjmujących STRATTERA zgłaszano niedociśnienie ortostatyczne i omdlenia. W badaniach rejestracyjnych dzieci i młodzieży u 0,2% (12/5596) pacjentów leczonych produktem STRATTERA wystąpiło niedociśnienie ortostatyczne, au 0,8% (46/5596) omdlenia. W krótkoterminowych badaniach rejestracyjnych dzieci i młodzieży u 1,8% (6/340) pacjentów leczonych produktem STRATTERA wystąpiło niedociśnienie ortostatyczne w porównaniu z 0,5% (1/207) pacjentów otrzymujących placebo. W krótkoterminowych badaniach rejestracyjnych ADHD kontrolowanych placebo u dzieci i młodzieży nie zgłaszano omdlenia. STRATTERA 10 mg należy stosować ostrożnie w każdym stanie, który może predysponować pacjentów do niedociśnienia lub stanów związanych z nagłymi zmianami częstości akcji serca lub ciśnienia krwi.
Pojawienie się nowych objawów psychotycznych lub maniakalnych
Pojawiające się w leczeniu objawy psychotyczne lub maniakalne, np. halucynacje, urojenia lub mania u dzieci i młodzieży bez wcześniejszej choroby psychotycznej lub manii w wywiadzie, mogą być spowodowane przez atomoksetynę w zwykłych dawkach. W przypadku wystąpienia takich objawów należy rozważyć możliwą przyczynową rolę atomoksetyny i rozważyć przerwanie leczenia. W zbiorczej analizie wielu krótkoterminowych badań z grupą kontrolną otrzymującą placebo takie objawy wystąpiły u około 0,2% (4 pacjentów z reakcjami od 1939 roku narażonych na atomoksetynę przez kilka tygodni w zwykłych dawkach) pacjentów leczonych atomoksetyną w porównaniu z 0 z 1056 pacjentów otrzymujących placebo.
Badanie przesiewowe pacjentów pod kątem choroby afektywnej dwubiegunowej
Ogólnie należy zachować szczególną ostrożność w leczeniu ADHD u pacjentów ze współistniejącą chorobą afektywną dwubiegunową ze względu na możliwość wywołania epizodu mieszanego/maniakalnego u pacjentów z ryzykiem choroby afektywnej dwubiegunowej. Nie wiadomo, czy którykolwiek z objawów opisanych powyżej reprezentuje taką konwersję. Jednak przed rozpoczęciem leczenia preparatem STRATTERA 40 mg pacjenci ze współistniejącymi objawami depresyjnymi powinni zostać odpowiednio przebadani w celu określenia, czy są oni narażeni na chorobę afektywną dwubiegunową; takie badania przesiewowe powinny obejmować szczegółowy wywiad psychiatryczny, w tym wywiad rodzinny dotyczący samobójstw, choroby afektywnej dwubiegunowej i depresji.
Agresywne zachowanie lub wrogość
Pacjenci rozpoczynający leczenie ADHD powinni być monitorowani pod kątem pojawienia się lub pogorszenia zachowania agresywnego lub wrogości. Agresywne zachowanie lub wrogość często obserwuje się u dzieci i młodzieży z ADHD. W krótkoterminowych kontrolowanych badaniach klinicznych z udziałem dzieci i młodzieży, 21/1308 (1,6%) pacjentów otrzymujących atomoksetynę w porównaniu z 9/806 (1,1%) pacjentów otrzymujących placebo spontanicznie zgłaszało pojawiające się podczas leczenia zdarzenia niepożądane związane z wrogością (ogólny współczynnik ryzyka 1,33 [95%) CI 0,67-2,64 – nieistotny statystycznie]). W badaniach klinicznych z udziałem dorosłych, kontrolowanych placebo, 6/1697 (0,35%) pacjentów otrzymujących atomoksetynę w porównaniu z 4/1560 (0,26%) pacjentów otrzymujących placebo spontanicznie zgłaszało zdarzenia niepożądane związane z leczeniem związane z wrogością (ogólny współczynnik ryzyka 1,38 [95% CI). 0,39-4,88 – nieistotne statystycznie]). Chociaż nie jest to rozstrzygający dowód na to, że STRATTERA 10 mg powoduje agresywne zachowanie lub wrogość, zachowania te były częściej obserwowane w badaniach klinicznych wśród dzieci, młodzieży i dorosłych leczonych STRATTERA w porównaniu z placebo.
Wydarzenia alergiczne
Chociaż niezbyt często, u pacjentów przyjmujących STRATTERA zgłaszano reakcje alergiczne, w tym reakcje anafilaktyczne, obrzęk naczynioruchowy, pokrzywkę i wysypkę.
Wpływ na odpływ moczu z pęcherza
W kontrolowanych badaniach ADHD z dorosłymi, częstość zatrzymania moczu (1,7%, 9/540) i wahania moczu (5,6%, 30/540) była wyższa wśród pacjentów otrzymujących atomoksetynę w porównaniu z pacjentami otrzymującymi placebo (0%, 0/402; 0,5%, 2/402). Dwóch dorosłych pacjentów z atomoksetyną i żaden z pacjentów otrzymujących placebo nie przerwało udziału w kontrolowanych badaniach klinicznych z powodu zatrzymania moczu. Skargę dotyczącą zatrzymania moczu lub wahania w oddawaniu moczu należy uznać za potencjalnie związaną z atomoksetyną.
Priapizm
Po wprowadzeniu produktu do obrotu zgłaszano rzadkie przypadki priapizmu, definiowane jako bolesny i bezbolesny wzwód prącia trwający dłużej niż 4 godziny, u dzieci i dorosłych leczonych produktem STRATTERA. Erekcje ustąpiły w przypadkach, w których dostępne były dalsze informacje, niektóre po odstawieniu leku STRATTERA. W przypadku podejrzenia priapizmu wymagana jest natychmiastowa pomoc medyczna.
Wpływ na wzrost
Dane dotyczące długoterminowego wpływu produktu STRATTERA 25 mg na wzrost pochodzą z badań otwartych, a zmiany masy ciała i wzrostu porównano z normatywnymi danymi populacyjnymi. Ogólnie rzecz biorąc, przyrost masy ciała i wzrostu u pacjentów pediatrycznych leczonych preparatem STRATTERA pozostaje w tyle za przewidywanym na podstawie normatywnych danych populacyjnych w ciągu pierwszych 9-12 miesięcy leczenia. Następnie, po około 3 latach leczenia, pacjenci leczeni produktem STRATTERA przytyli średnio o 17,9 kg, czyli o 0,5 kg więcej niż przewidywano na podstawie danych wyjściowych. Po około 12 miesiącach przyrost wzrostu stabilizuje się, a po 3 latach pacjenci leczeni preparatem STRATTERA 40 mg przybrali średnio 19,4 cm, czyli 0,4 cm mniej niż przewidywali ich dane wyjściowe (patrz Rysunek 1 poniżej).
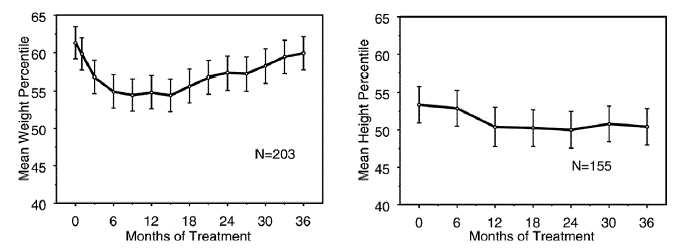
Rysunek 1: Średnie percentyle masy ciała i wzrostu w czasie dla pacjentów z trzyletnim leczeniem STRATTERA 40 mg
Ten wzorzec wzrostu był na ogół podobny, niezależnie od stanu pokwitania w momencie rozpoczęcia leczenia. Pacjenci, którzy byli przed okresem dojrzewania na początku leczenia (dziewczęta ≤8 lat, chłopcy ≤9 lat) przytyli średnio o 2,1 kg i 1,2 cm mniej niż przewidywano po trzech latach. U pacjentów w wieku pokwitania (dziewczynki >8 do ≤13 lat, chłopców w wieku >9 do ≤14 lat) lub późnego dojrzewania (dziewczęta >13 lat, chłopców >14 lat) średni przyrost masy ciała i wzrostu był bliski lub przekroczyły przewidywane po trzech latach leczenia.
Wzrost przebiegał według podobnego wzorca zarówno u osób intensywnie i słabo metabolizujących (EM, PM). PM leczone przez co najmniej dwa lata zyskały średnio 2,4 kg i 1,1 cm mniej niż przewidywano, podczas gdy EM zyskały średnio 0,2 kg i 0,4 cm mniej niż przewidywano.
krótkoterminowych badaniach kontrolowanych (do 9 tygodni) pacjenci leczeni STRATTERA stracili średnio 0,4 kg i przytyli średnio o 0,9 cm, w porównaniu z przyrostem 1,5 kg i 1,1 cm u pacjentów otrzymujących placebo. W kontrolowanym badaniu ze stałą dawką 1,3%, 7,1%, 19,3% i 29,1% pacjentów straciło co najmniej 3,5% masy ciała w grupach otrzymujących placebo, 0,5, 1,2 i 1,8 mg/kg/dobę.
Podczas leczenia produktem STRATTERA należy monitorować wzrost.
Testy laboratoryjne
Rutynowe testy laboratoryjne nie są wymagane.
Metabolizm CYP2D6
Osoby słabo metabolizujące (PM) CYP2D6 mają 10-krotnie wyższe AUC i 5-krotnie wyższe stężenie szczytowe dla danej dawki STRATTERA 25 mg w porównaniu z osobami intensywnie metabolizującymi (EM). Około 7% populacji rasy kaukaskiej to PM. Dostępne są testy laboratoryjne do identyfikacji cząstek stałych CYP2D6. Poziomy we krwi w PM są podobne do tych osiąganych przez przyjmowanie silnych inhibitorów CYP2D6. Wyższy poziom we krwi w PM prowadzi do wyższego wskaźnika niektórych niepożądanych skutków STRATTERY [patrz DZIAŁANIA NIEPOŻĄDANE ].
Jednoczesne stosowanie silnych inhibitorów CYP2D6 lub stosowanie u pacjentów, o których wiadomo, że są PM-y CYP2D6
Atomoksetyna jest metabolizowana głównie na szlaku CYP2D6 do 4-hydroksyatomoksetyny. Dostosowanie dawki produktu STRATTERA może być konieczne w przypadku jednoczesnego podawania z silnymi inhibitorami CYP2D6 (np. paroksetyną, fluoksetyną i chinidyną) lub w przypadku podawania z PM CYP2D6. [Widzieć DAWKOWANIE I SPOSÓB PODAWANIA oraz INTERAKCJE Z LEKAMI ].
Informacje dotyczące poradnictwa dla pacjentów
Zobacz zatwierdzone przez FDA INFORMACJA O PACJENCIE .
Informacje ogólne
Lekarze powinni poinstruować swoich pacjentów, aby przed rozpoczęciem leczenia preparatem STRATTERA przeczytali Przewodnik dotyczący leków i ponownie przeczytali go za każdym razem, gdy recepta jest odnawiana.
Lekarze przepisujący leki lub inni pracownicy służby zdrowia powinni informować pacjentów, ich rodziny i ich opiekunów o korzyściach i zagrożeniach związanych z leczeniem preparatem STRATTERA oraz powinni doradzać im w zakresie jego właściwego stosowania. Lekarz lub pracownik służby zdrowia powinien poinstruować pacjentów, ich rodziny i ich opiekunów, aby przeczytali Przewodnik po lekach i powinni pomóc im w zrozumieniu jego treści. Pacjenci powinni mieć możliwość omówienia treści Przewodnika po lekach i uzyskania odpowiedzi na wszelkie pytania, jakie mogą mieć.
Pacjentów należy poinformować o następujących problemach i poprosić ich o powiadomienie lekarza, jeśli wystąpią one podczas przyjmowania leku STRATTERA.
Ryzyko samobójstwa
Należy zachęcać pacjentów, ich rodziny i ich opiekunów do wyczulenia na pojawienie się lęku, pobudzenia, ataków paniki, bezsenności, drażliwości, wrogości, agresywności, impulsywności, akatyzji (niepokoju psychoruchowego), hipomanii, manii i innych nietypowych zmian w zachowaniu , depresja i myśli samobójcze, szczególnie na początku leczenia produktem STRATTERA i po dostosowaniu dawki. Rodzinom i opiekunom pacjentów należy zalecić codzienne obserwowanie pojawienia się takich objawów, ponieważ zmiany mogą być nagłe. Takie objawy należy zgłaszać lekarzowi lub pracownikowi służby zdrowia, zwłaszcza jeśli są one ciężkie, mają nagły początek lub nie były częścią objawów występujących u pacjenta. Takie objawy mogą wiązać się ze zwiększonym ryzykiem myśli i zachowań samobójczych i wskazują na potrzebę bardzo ścisłego monitorowania i ewentualnie zmian w leczeniu.
Ciężkie uszkodzenie wątroby
Pacjentów rozpoczynających leczenie produktem STRATTERA należy ostrzec, że może dojść do ciężkiego uszkodzenia wątroby. Pacjentów należy poinstruować, aby niezwłocznie skontaktowali się z lekarzem w przypadku wystąpienia świądu, ciemnego moczu, żółtaczki, tkliwości w prawym górnym kwadrancie lub niewyjaśnionych objawów grypopodobnych [patrz OSTRZEŻENIA I ŚRODKI ].
Agresja lub wrogość
Pacjentów należy poinstruować, aby jak najszybciej skontaktowali się z lekarzem, jeśli zauważą wzrost agresji lub wrogości.
Priapizm
Po wprowadzeniu produktu do obrotu zgłaszano rzadkie przypadki priapizmu, definiowane jako bolesny i bezbolesny wzwód prącia trwający dłużej niż 4 godziny, u dzieci i dorosłych leczonych produktem STRATTERA. Rodziców lub opiekunów pacjentów pediatrycznych przyjmujących STRATTERA 25 mg i dorosłych pacjentów przyjmujących STRATTERA należy pouczyć, że priapizm wymaga natychmiastowej pomocy lekarskiej.
Drażniący dla oczu
STRATTERA działa drażniąco na oczy. Kapsułki STRATTERA nie są przeznaczone do otwierania. W przypadku kontaktu zawartości kapsułki z okiem, chore oko należy natychmiast przepłukać wodą i zasięgnąć porady lekarza. Ręce i wszelkie potencjalnie skażone powierzchnie należy jak najszybciej umyć.
Interakcje między lekami
Pacjentów należy poinstruować, aby skonsultowali się z lekarzem, jeśli przyjmują lub planują przyjmować leki na receptę lub dostępne bez recepty, suplementy diety lub preparaty ziołowe.
Ciąża
Pacjentki należy poinstruować, aby skonsultowały się z lekarzem, jeśli karmią piersią, są w ciąży lub myślą o zajściu w ciążę podczas przyjmowania leku STRATTERA.
Żywność
Pacjenci mogą przyjmować STRATTERA 25 mg z jedzeniem lub bez jedzenia.
Pominięta dawka
Jeśli pacjent pominie dawkę, należy go poinstruować, aby przyjął ją tak szybko, jak to możliwe, ale nie powinien przyjmować więcej niż przepisana całkowita dobowa dawka produktu STRATTERA w ciągu 24 godzin.
Zakłócanie sprawności psychomotorycznej
Pacjentów należy poinstruować, aby zachowywali ostrożność podczas prowadzenia samochodu lub obsługiwania niebezpiecznych maszyn, dopóki nie upewnią się, że atomoksetyna nie wpływa na ich działanie.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Karcynogeneza
Chlorowodorek atomoksetyny nie wykazywał działania rakotwórczego u szczurów i myszy, gdy był podawany w diecie przez 2 lata w średnich dawkach ważonych w czasie do, odpowiednio, 47 i 458 mg/kg/dobę. Najwyższa dawka stosowana u szczurów jest około 8 i 5 razy większa od maksymalnej dawki u ludzi, odpowiednio, u dzieci i dorosłych, w przeliczeniu na mg/m2. Szacuje się, że poziomy w osoczu (AUC) atomoksetyny w tej dawce u szczurów są 1,8 razy większe (osoby intensywnie metabolizujące) lub 0,2 razy większe (osoby słabo metabolizujące) niż u ludzi otrzymujących maksymalną dawkę u ludzi. Najwyższa dawka stosowana u myszy jest około 39 i 26 razy większa od maksymalnej dawki u ludzi, odpowiednio, u dzieci i dorosłych, w przeliczeniu na mg/m2.
Mutageneza
Atomoksetyna HCl dała wynik ujemny w szeregu badań genotoksyczności, które obejmowały test mutacji odwrotnych (test Amesa), test chłoniaka myszy in vitro, test aberracji chromosomowych w komórkach jajnika chomika chińskiego, test nieplanowej syntezy DNA w hepatocytach szczura oraz test mikrojądrowy in vivo u myszy. Zaobserwowano jednak nieznaczny wzrost odsetka komórek jajnika chomika chińskiego z diplochromosomami, co sugeruje endoreduplikację (aberrację liczbową).
Metabolit chlorowodorek N-desmetyloatomoksetyny był ujemny w teście Amesa, teście chłoniaka myszy i teście nieplanowanej syntezy DNA.
Upośledzenie płodności
Atomoksetyna HCl nie zaburzała płodności u szczurów, gdy była podawana w diecie w dawkach do 57 mg/kg/dobę, co stanowi około 6-krotność maksymalnej dawki u ludzi w przeliczeniu na mg/m2.
Używaj w określonych populacjach
Ciąża
Ciąża Kategoria C
Ciężarnym królikom przez cały okres organogenezy podawano atomoksetynę w dawce do 100 mg/kg/dzień przez zgłębnik. Przy tej dawce w 1 z 3 badań zaobserwowano zmniejszenie liczby żywych płodów i wzrost wczesnych resorpcji. Zaobserwowano nieznaczny wzrost częstości występowania nietypowego pochodzenia tętnicy szyjnej i brak tętnicy podobojczykowej. Wyniki te zaobserwowano przy dawkach, które powodowały niewielką toksyczność matczyną. Dawka niepowodująca tych zmian wynosiła 30 mg/kg/dobę. Dawka 100 mg/kg jest około 23 razy większa od maksymalnej dawki dla człowieka w przeliczeniu na mg/m2; Szacuje się, że stężenie w osoczu (AUC) atomoksetyny w tej dawce u królików wynosi 3,3 razy (osoby intensywnie metabolizujące) lub 0,4 razy (osoby słabo metabolizujące) niż u ludzi otrzymujących maksymalną dawkę u ludzi.
Szczury otrzymywały do około 50 mg/kg/dobę atomoksetyny (około 6-krotność maksymalnej dawki dla ludzi w przeliczeniu na mg/m2) w diecie od 2 tygodni (samice) lub 10 tygodni (samce) przed kryciem przez okresy organogenezy i laktacji. W 1 z 2 badań zaobserwowano zmniejszenie masy i przeżycia młodych. Zmniejszone przeżycie potomstwa zaobserwowano również przy 25 mg/kg (ale nie przy 13 mg/kg). W badaniu, w którym szczurom podawano atomoksetynę w diecie od 2 tygodni (samice) lub 10 tygodni (samce) przed kryciem przez cały okres organogenezy, zmniejszenie masy płodu (tylko samice) i zwiększenie częstości występowania niepełne skostnienie łuku kręgowego u płodów obserwowano przy dawce 40 mg/kg/dzień (około 5-krotność maksymalnej dawki dla człowieka w przeliczeniu na mg/m2), ale nie przy 20 mg/kg/dzień.
Nie zaobserwowano niekorzystnego wpływu na płód, gdy ciężarnym szczurom podawano przez zgłębnik do 150 mg/kg/dobę (około 17-krotność maksymalnej dawki u ludzi w mg/m2) przez zgłębnik w okresie organogenezy. Nie przeprowadzono odpowiednich i dobrze kontrolowanych badań u kobiet w ciąży. STRATTERA 18 mg nie należy stosować w okresie ciąży, chyba że potencjalne korzyści uzasadniają potencjalne ryzyko dla płodu.
Praca i dostawa
Atomoksetyna nie miała wpływu na poród u szczurów. Wpływ STRATTERY na poród i poród u ludzi jest nieznany.
Matki karmiące
Atomoksetyna i (lub) jej metabolity przenikały do mleka szczurów. Nie wiadomo, czy atomoksetyna przenika do mleka ludzkiego. Należy zachować ostrożność w przypadku podawania produktu STRATTERA kobiecie karmiącej.
Zastosowanie pediatryczne
Każdy, kto rozważa zastosowanie preparatu STRATTERA u dzieci lub młodzieży, musi zrównoważyć potencjalne ryzyko z potrzebą kliniczną [patrz PUDEŁKO OSTRZEŻENIE oraz OSTRZEŻENIA I ŚRODKI ]. Farmakokinetyka atomoksetyny u dzieci i młodzieży jest podobna do farmakokinetyki u dorosłych. Nie oceniano bezpieczeństwa, skuteczności i farmakokinetyki produktu STRATTERA u dzieci w wieku poniżej 6 lat.
Przeprowadzono badanie na młodych szczurach w celu oceny wpływu atomoksetyny na wzrost oraz rozwój neurobehawioralny i płciowy. Szczurom podawano 1, 10 lub 50 mg/kg/dobę (odpowiednio około 0,2, 2 i 8-krotność maksymalnej dawki u ludzi w przeliczeniu na mg/m2) atomoksetyny podawanej przez zgłębnik od wczesnego okresu poporodowego (dzień 10 lat) przez dorosłość. Niewielkie opóźnienie początku drożności pochwy (wszystkie dawki) i rozdzielenia napletka (10 i 50 mg/kg), niewielkie zmniejszenie masy najądrza i liczby plemników (10 i 50 mg/kg) oraz niewielkie zmniejszenie ciałka żółtego (50 mg) /kg), ale nie stwierdzono wpływu na płodność ani zdolności reprodukcyjne. Niewielkie opóźnienie początku wyrzynania siekaczy zaobserwowano przy dawce 50 mg/kg. Niewielki wzrost aktywności motorycznej zaobserwowano w dniu 15 (mężczyźni przy 10 i 50 mg/kg i kobiety przy 50 mg/kg) oraz w dniu 30 (kobiety przy 50 mg/kg), ale nie w dniu 60. Nie było wpływu na testy uczenia się i pamięci. Znaczenie tych odkryć dla ludzi nie jest znane.
Zastosowanie geriatryczne
Bezpieczeństwo, skuteczność i farmakokinetyka produktu STRATTERA 10 mg u pacjentów w podeszłym wieku nie zostały ocenione.
Niewydolność wątroby
Ekspozycja na atomoksetynę (AUC) jest zwiększona w porównaniu z osobami zdrowymi u pacjentów z EM z umiarkowaną (klasa B w skali Child-Pugh) (2-krotny wzrost) i ciężką (klasa C w skali Child-Pugh) (4-krotne zwiększenie) niewydolnością wątroby. Zaleca się dostosowanie dawkowania u pacjentów z umiarkowaną lub ciężką niewydolnością wątroby [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Niewydolność nerek
Pacjenci EM ze schyłkową niewydolnością nerek mieli wyższą ogólnoustrojową ekspozycję na atomoksetynę niż osoby zdrowe (wzrost o około 65%), ale nie było różnicy, gdy ekspozycja została skorygowana o dawkę mg/kg. STRATTERA 25 mg może być zatem podawana pacjentom z ADHD ze schyłkową niewydolnością nerek lub mniejszymi stopniami niewydolności nerek przy normalnym schemacie dawkowania.
Płeć
Płeć nie miała wpływu na dyspozycję atomoksetyny.
Etniczne pochodzenie
Pochodzenie etniczne nie miało wpływu na dyspozycję atomoksetyny (poza tym, że PM są częstsze u osób rasy kaukaskiej).
Pacjenci ze współistniejącą chorobą
Tiki u pacjentów z ADHD i współistniejącą chorobą Tourette'a
Porównywano atomoksetynę w elastycznym zakresie dawek od 0,5 do 1,5 mg/kg/dobę (średnia dawka 1,3 mg/kg/dobę) i placebo u 148 randomizowanych dzieci (w wieku 717 lat) z rozpoznaniem ADHD i DSM-IV. współwystępujące zaburzenie tikowe w 18-tygodniowym, podwójnie zaślepionym, kontrolowanym placebo badaniu, w którym większość (80%) wzięła udział w tym badaniu z zespołem Tourette'a (zaburzenie Tourette'a: 116 pacjentów; przewlekłe zaburzenie tikowe: 29 pacjentów). Analiza non-inferiority wykazała, że STRATTERA 10 mg nie pogorszyła tików u tych pacjentów, co określono na podstawie całkowitego wyniku skali Yale Global Tic Severity Scale (YGTSS). Spośród 148 pacjentów, którzy weszli w ostrą fazę leczenia, 103 (69,6%) przerwało badanie. Głównym powodem przerwania leczenia zarówno w grupie otrzymującej atomoksetynę (38 z 76 pacjentów, 50,0%), jak i placebo (45 z 72 pacjentów, 62,5%) był brak skuteczności, przy czym większość pacjentów przerwała leczenie w 12. tygodniu. pierwsza wizyta, podczas której pacjenci z CGI-S≥4 mogli również spełniać kryteria „nieodpowiadającego na leczenie kliniczne” (CGI-S pozostał taki sam lub wzrósł w stosunku do wartości początkowej badania) i kwalifikowali się do udziału w otwartym badaniu rozszerzonym z zastosowaniem atomoksetyny. Pojawiły się doniesienia po wprowadzeniu do obrotu o tikach [patrz DZIAŁANIA NIEPOŻĄDANE ].
Lęk u pacjentów z ADHD i współistniejącymi zaburzeniami lękowymi
W dwóch po wprowadzeniu do obrotu, podwójnie ślepych, kontrolowanych placebo badaniach klinicznych wykazano, że leczenie pacjentów z ADHD i współistniejącymi zaburzeniami lękowymi za pomocą preparatu STRATTERA 10 mg nie nasila ich lęku.
W 12-tygodniowym badaniu z podwójnie ślepą próbą, kontrolowanym placebo, 176 pacjentów w wieku 8-17 lat, którzy spełniali kryteria ADHD DSM-IV i co najmniej jedno z zaburzeń lękowych w postaci lęku separacyjnego, zaburzenia lęku uogólnionego lub fobii społecznej, zostało losowo. Po 2-tygodniowym, podwójnie zaślepionym wstępnym wprowadzeniu placebo, STRATTERA 25 mg została rozpoczęta w dawce 0,8 mg/kg/dobę ze wzrostem do dawki docelowej 1,2 mg/kg/dobę (mediana dawki 1,30 mg/kg/dobę +/-0,29 mg/kg/dzień). STRATTERA nie nasilała lęku u tych pacjentów, co określono za pomocą Pediatric Anxiety Rating Scale (PARS). Spośród 158 pacjentów, którzy ukończyli podwójnie ślepą próbę wstępną placebo, 26 (16%) przerwało badanie.
oddzielnym 16-tygodniowym, podwójnie zaślepionym, kontrolowanym placebo badaniu klinicznym zrandomizowano 442 pacjentów w wieku 18-65 lat, którzy spełniali kryteria DSM-IV dla ADHD u dorosłych i zespołu lęku społecznego (23% z nich również miało zespół lęku uogólnionego). Po 2-tygodniowym, podwójnie zaślepionym wstępnym wprowadzeniu placebo, STRATTERA 10 mg została rozpoczęta w dawce 40 mg/dobę do maksymalnej dawki 100 mg/dobę (średnia dzienna dawka 83 mg/dobę +/-19,5 mg/dobę). STRATTERA 18 mg nie nasila lęku u tych pacjentów, co określono za pomocą Skali Lęku Społecznego Liebowitza (LSAS). Spośród 413 pacjentów, którzy ukończyli podwójnie ślepą próbę wstępną placebo, 149 (36,1%) przerwało badanie. Pojawiły się doniesienia o lęku po wprowadzeniu do obrotu [patrz DZIAŁANIA NIEPOŻĄDANE ] .
PRZEDAWKOWAĆ
Ludzkie doświadczenie
Doświadczenie z badań klinicznych dotyczących przedawkowania produktu STRATTERA jest ograniczone. W okresie po wprowadzeniu produktu do obrotu zgłaszano przypadki zgonów związane z przedawkowaniem mieszanych dawek leku STRATTERA 10 mg i co najmniej jednego innego leku. Nie ma doniesień o zgonach związanych z przedawkowaniem samego produktu STRATTERA, w tym zamierzonym przedawkowaniem dawek do 1400 mg. W niektórych przypadkach przedawkowania produktu STRATTERA zgłaszano drgawki. Najczęściej zgłaszanymi objawami towarzyszącymi ostremu i przewlekłemu przedawkowaniu produktu STRATTERA były objawy żołądkowo-jelitowe, senność, zawroty głowy, drżenie i nieprawidłowe zachowanie. Zgłaszano również nadpobudliwość i pobudzenie. Obserwowano również objawy przedmiotowe i podmiotowe odpowiadające łagodnej do umiarkowanej aktywacji współczulnego układu nerwowego (np. tachykardia, podwyższone ciśnienie krwi, rozszerzenie źrenic, suchość w ustach). Większość zdarzeń miała charakter łagodny do umiarkowanego. Rzadziej pojawiają się doniesienia o wydłużeniu odstępu QT i zmianach psychicznych, w tym dezorientacji i halucynacjach [patrz FARMAKOLOGIA KLINICZNA ].
Postępowanie w przypadku przedawkowania
Skonsultuj się z Certyfikowanym Centrum Kontroli Zatruć, aby uzyskać aktualne wskazówki i porady. Ponieważ atomoksetyna silnie wiąże się z białkami, dializa prawdopodobnie nie będzie przydatna w leczeniu przedawkowania.
PRZECIWWSKAZANIA
Nadwrażliwość
STRATTERA jest przeciwwskazana u pacjentów, u których stwierdzono nadwrażliwość na atomoksetynę lub inne składniki produktu [patrz OSTRZEŻENIA I ŚRODKI ].
Inhibitory monoaminooksydazy (MAOI)
STRATTERA nie należy przyjmować z MAOI ani w ciągu 2 tygodni po odstawieniu MAOI. Leczenia IMAO nie należy rozpoczynać w ciągu 2 tygodni po odstawieniu preparatu STRATTERA. W przypadku innych leków, które wpływają na stężenie monoaminy w mózgu, zgłaszano poważne reakcje, czasami prowadzące do zgonu (w tym hipertermię, sztywność mięśni, mioklonie, niestabilność układu autonomicznego z możliwymi gwałtownymi wahaniami parametrów życiowych oraz zmiany stanu psychicznego obejmujące skrajne pobudzenie przechodzące w majaczenie i śpiączka) w połączeniu z IMAO. Niektóre przypadki prezentowały cechy przypominające złośliwy zespół neuroleptyczny. Takie reakcje mogą wystąpić, gdy leki te są podawane jednocześnie lub w bliskim sąsiedztwie [patrz INTERAKCJE Z LEKAMI ].
Jaskra z wąskim kątem
W badaniach klinicznych stosowanie produktu STRATTERA wiązało się ze zwiększonym ryzykiem rozszerzenia źrenic i dlatego nie zaleca się jego stosowania u pacjentów z jaskrą z wąskim kątem przesączania.
Guz chromochłonny
Poważne reakcje, w tym podwyższone ciśnienie krwi i tachyarytmię, zgłaszano u pacjentów z guzem chromochłonnym nadnerczy lub guzem chromochłonnym nadnerczy w wywiadzie, którzy otrzymywali produkt STRATTERA. Dlatego STRATTERA 18 mg nie powinna być przyjmowana przez pacjentów z guzem chromochłonnym lub guzem chromochłonnym w wywiadzie.
Ciężkie zaburzenia sercowo-naczyniowe
Produktu STRATTERA 40 mg nie należy stosować u pacjentów z ciężkimi chorobami serca lub naczyń, których stan może ulec pogorszeniu, jeśli wystąpi wzrost ciśnienia krwi lub częstości akcji serca, co może mieć znaczenie kliniczne (na przykład 15 do 20 mm Hg w ciśnieniu krwi lub 20 uderzeń na minutę w tętnie). [Widzieć OSTRZEŻENIA I ŚRODKI ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Dokładny mechanizm działania terapeutycznego atomoksetyny w zespole nadpobudliwości psychoruchowej z deficytem uwagi (ADHD) jest nieznany, ale uważa się, że jest on związany z selektywnym hamowaniem presynaptycznego transportera norepinefryny, co określono w badaniach ex vivo wychwytu i wyczerpania neuroprzekaźników .
Farmakodynamika
Analiza reakcji na ekspozycję obejmująca dawki atomoksetyny (0,5, 1,2 lub 1,8 mg/kg/dobę) lub placebo wykazała, że narażenie na atomoksetynę koreluje ze skutecznością mierzoną za pomocą Skali Oceny Deficytu Uwagi/Nadpobudliwości zdobył. Zależność między ekspozycją a skutecznością była podobna do tej obserwowanej między dawką a skutecznością, przy medianie ekspozycji przy dwóch najwyższych dawkach, co powodowało prawie maksymalne zmiany w stosunku do wartości wyjściowych [patrz Studia kliniczne ].
Elektrofizjologia serca
Wpływ produktu STRATTERA na wydłużenie odstępu QTc oceniano w randomizowanym, podwójnie zaślepionym, dodatnim (moksyfloksacyna 400 mg) i kontrolowanym placebo badaniu krzyżowym u zdrowych mężczyzn słabo metabolizujących CYP2D6. W sumie 120 zdrowym osobom podawano STRATTERA (20 mg i 60 mg) dwa razy dziennie przez 7 dni. W badaniu nie zaobserwowano dużych zmian odstępu QTc (tj. wydłużenia >60 ms od wartości wyjściowej, bezwzględnego odstępu QTc >480 ms). Nie można jednak wykluczyć z obecnego badania niewielkich zmian odstępu QTc, ponieważ badanie to nie wykazało czułości testu. Wystąpił niewielki wzrost odstępu QTc wraz ze wzrostem stężenia atomoksetyny.
Farmakokinetyka
Atomoksetyna jest dobrze wchłaniana po podaniu doustnym i pokarm ma na nią minimalny wpływ. Jest eliminowany głównie na drodze metabolizmu oksydacyjnego na szlaku enzymatycznym cytochromu P450 2D6 (CYP2D6), a następnie glukuronidacji. Okres półtrwania atomoksetyny wynosi około 5 godzin. Część populacji (około 7% rasy białej i 2% Afroamerykanów) to osoby słabo metabolizujące (PM) leki metabolizowane przez CYP2D6. Osoby te mają zmniejszoną aktywność w tym szlaku, co skutkuje 10-krotnie wyższymi AUC, 5-krotnie wyższymi maksymalnymi stężeniami w osoczu i wolniejszą eliminacją (okres półtrwania w osoczu około 24 godzin) atomoksetyny w porównaniu z osobami o normalnej aktywności [osoby intensywnie metabolizujące )]. Leki hamujące CYP2D6, takie jak fluoksetyna, paroksetyna i chinidyna, powodują podobny wzrost ekspozycji.
Farmakokinetykę atomoksetyny oceniano u ponad 400 dzieci i młodzieży w wybranych badaniach klinicznych, głównie z wykorzystaniem populacyjnych badań farmakokinetycznych. U dzieci, młodzieży i dorosłych uzyskano również indywidualne dane farmakokinetyczne po podaniu pojedynczej dawki iw stanie stacjonarnym. Gdy dawki znormalizowano do mg/kg, podobne wartości okresu półtrwania, Cmax i AUC obserwowano u dzieci, młodzieży i dorosłych. Klirens i objętość dystrybucji po dostosowaniu do masy ciała również były podobne.
Absorpcja i dystrybucja
Atomoksetyna jest szybko wchłaniana po podaniu doustnym, przy bezwzględnej biodostępności około 63% w EM i 94% w PM. Maksymalne stężenie w osoczu (Cmax) osiągane jest około 1 do 2 godzin po podaniu.
STRATTERA 18mg może być podawana z jedzeniem lub bez jedzenia. Podawanie preparatu STRATTERA ze standardowym wysokotłuszczowym posiłkiem u dorosłych nie miało wpływu na stopień doustnego wchłaniania atomoksetyny (AUC), ale zmniejszyło szybkość wchłaniania, powodując 37% niższe Cmax i opóźnienie Tmax o 3 godziny. W badaniach klinicznych z dziećmi i młodzieżą podawanie produktu STRATTERA z jedzeniem skutkowało zmniejszeniem Cmax o 9%.
Objętość dystrybucji w stanie stacjonarnym po podaniu dożylnym wynosi 0,85 l/kg, co wskazuje, że atomoksetyna jest dystrybuowana głównie do całkowitej wody ustrojowej. Objętość dystrybucji jest podobna w całym zakresie masy ciała pacjenta po normalizacji pod kątem masy ciała.
W stężeniach terapeutycznych 98% atomoksetyny w osoczu wiąże się z białkami, głównie albuminami.
Metabolizm i eliminacja
Atomoksetyna jest metabolizowana głównie na szlaku enzymatycznym CYP2D6. Osoby o obniżonej aktywności w tym szlaku (PM) mają wyższe stężenie atomoksetyny w osoczu w porównaniu z osobami o normalnej aktywności (EM). W przypadku PM, AUC atomoksetyny jest około 10-krotnie większe, a Css, max jest około 5-krotnie większe niż EM. Dostępne są testy laboratoryjne do identyfikacji cząstek stałych CYP2D6. Jednoczesne podawanie produktu STRATTERA z silnymi inhibitorami CYP2D6, takimi jak fluoksetyna, paroksetyna lub chinidyna, powoduje znaczne zwiększenie ekspozycji osoczowej na atomoksetynę i może być konieczne dostosowanie dawki [patrz OSTRZEŻENIA I ŚRODKI ]. Atomoksetyna nie hamowała ani nie indukowała szlaku CYP2D6.
Głównym powstającym metabolitem oksydacyjnym, niezależnie od statusu CYP2D6, jest 4-hydroksyatomoksetyna, która jest glukuronidowana. 4-Hydroksyatomoksetyna jest tak samo silna jak atomoksetyna jako inhibitor transportera norepinefryny, ale krąży w osoczu w znacznie niższych stężeniach (1% stężenia atomoksetyny w EM i 0,1% stężenia atomoksetyny w PM). 4-hydroksyatomoksetyna jest tworzona głównie przez CYP2D6, ale w PM 4-hydroksyatomoksetyna jest tworzona w wolniejszym tempie przez kilka innych enzymów cytochromu P450. N-desmetyloatomoksetyna jest tworzona przez CYP2C19 i inne enzymy cytochromu P450, ale ma znacznie mniejszą aktywność farmakologiczną w porównaniu z atomoksetyną i krąży w osoczu w niższych stężeniach (5% stężenia atomoksetyny w EM i 45% stężenia atomoksetyny w PM).
Średni pozorny klirens osoczowy atomoksetyny po podaniu doustnym w dorosłych EM wynosi 0,35 l/h/kg, a średni okres półtrwania wynosi 5,2 godziny. Po doustnym podaniu atomoksetyny osobom PM średni pozorny klirens osoczowy wynosi 0,03 l/h/kg, a średni okres półtrwania wynosi 21,6 godziny. W przypadku PM, AUC atomoksetyny jest około 10-krotnie większe, a Css, max jest około 5-krotnie większe niż EM. Okres półtrwania 4-hydroksyatomoksetyny w fazie eliminacji jest podobny do okresu półtrwania N-desmetyloatomoksetyny (6 do 8 godzin) u pacjentów z EM, natomiast okres półtrwania N-desmetyloatomoksetyny jest znacznie dłuższy u pacjentów z PM (34 do 40 godzin).
Atomoksetyna jest wydalana głównie w postaci O-glukuronidu 4-hydroksyatomoksetyny, głównie z moczem (więcej niż 80% dawki) oraz w mniejszym stopniu z kałem (mniej niż 17% dawki). Tylko niewielka część dawki 40 mg produktu STRATTERA jest wydalana w postaci niezmienionej atomoksetyny (mniej niż 3% dawki), co wskazuje na intensywną biotransformację.
[Widzieć Używaj w określonych populacjach ].
Studia kliniczne
Badania ADHD u dzieci i młodzieży
Badania ostre
Skuteczność preparatu STRATTERA 40 mg w leczeniu ADHD została potwierdzona w 4 randomizowanych, podwójnie zaślepionych, kontrolowanych placebo badaniach pacjentów pediatrycznych (w wieku od 6 do 18 lat). Około jedna trzecia pacjentów spełniała kryteria DSM-IV dla podtypu nieuważnego, a dwie trzecie spełniała kryteria zarówno dla podtypu nieuważnego, jak i nadpobudliwego/impulsywnego.
Objawy przedmiotowe i podmiotowe ADHD zostały ocenione przez porównanie średniej zmiany od punktu początkowego do punktu końcowego u pacjentów otrzymujących STRATTERA i placebo przy użyciu analizy intent-to-treat pierwszorzędowej miary wyniku, którą badacz podał i ocenił Skala oceny ADHD-IV- Całkowity wynik wersji rodzica (ADHDRS) obejmujący podskale nadpobudliwości/impulsu i nieuwagi. Każda pozycja w ADHDRS odwzorowuje bezpośrednio jedno kryterium objawów ADHD w DSM-IV.
badaniu 1, 8-tygodniowym randomizowanym, podwójnie zaślepionym, kontrolowanym placebo badaniu zależności od dawki, w leczeniu doraźnym dzieci i młodzieży w wieku od 8 do 18 lat (N=297), pacjenci otrzymywali albo stałą dawkę preparatu STRATTERA (0,5; 1,2 lub 1,8 mg/kg/dzień) lub placebo. STRATTERA 10 mg podawano w dawce podzielonej wczesnym rankiem i późnym popołudniem/wczesnym wieczorem. Przy 2 wyższych dawkach poprawa objawów ADHD była statystycznie istotnie lepsza u pacjentów leczonych STRATTERA w porównaniu z pacjentami otrzymującymi placebo, mierzoną w skali ADHDRS. Dawka 1,8 mg/kg/dobę STRATTERA 25 mg nie przyniosła żadnych dodatkowych korzyści w porównaniu z dawką obserwowaną przy dawce 1,2 mg/kg/dobę. Dawka 0,5 mg/kg/dobę STRATTERA nie była lepsza niż placebo.
Badaniu 2, 6-tygodniowym randomizowanym, podwójnie zaślepionym, kontrolowanym placebo badaniu doraźnego leczenia dzieci i młodzieży w wieku od 6 do 16 lat (N=171), pacjenci otrzymywali albo preparat STRATTERA w dawce 40 mg, albo placebo. STRATTERA podawano jako pojedynczą dawkę wczesnym rankiem i miareczkowano w zależności od masy ciała w zależności od odpowiedzi klinicznej, do maksymalnej dawki 1,5 mg/kg/dobę. Średnia końcowa dawka produktu STRATTERA 10 mg wynosiła około 1,3 mg/kg/dobę. Objawy ADHD uległy statystycznie istotnej poprawie w grupie STRATTERA w porównaniu z placebo, mierzonej w skali ADHDRS. Badanie to pokazuje, że STRATTERA jest skuteczna przy podawaniu raz dziennie rano.
2 identycznych, 9-tygodniowych, randomizowanych, podwójnie zaślepionych, kontrolowanych placebo badaniach z udziałem dzieci w wieku od 7 do 13 lat (Badanie 3, N=147; Badanie 4, N=144), STRATTERA 40 mg i metylofenidat porównywano z placebo. . STRATTERA 18 mg była podawana jako dawka podzielona wczesnym rankiem i późnym popołudniem (po szkole) i dostosowywana w zależności od masy ciała w zależności od odpowiedzi klinicznej. Maksymalna zalecana dawka produktu STRATTERA wynosiła 2,0 mg/kg/dobę. Średnia końcowa dawka preparatu STRATTERA 18 mg w obu badaniach wynosiła około 1,6 mg/kg/dobę. W obu badaniach objawy ADHD istotnie statystycznie poprawiły się bardziej po podaniu preparatu STRATTERA 10 mg niż po placebo, co mierzono w skali ADHDRS.
Badanie podzbiorów populacji w oparciu o płeć i wiek (
Badanie konserwacji
Skuteczność preparatu STRATTERA 18 mg w leczeniu podtrzymującym ADHD ustalono w badaniu ambulatoryjnym z udziałem dzieci i młodzieży (w wieku 6-15 lat). Pacjenci spełniający kryteria DSM-IV dla ADHD, którzy wykazywali ciągłą odpowiedź przez około 4 tygodnie podczas początkowej 10-tygodniowej otwartej fazy leczenia preparatem STRATTERA (1,2 do 1,8 mg/kg/dobę) zostali losowo przydzieleni do kontynuacji dotychczasowej dawki preparatu STRATTERA (N =292) lub placebo (N=124) w ramach leczenia metodą podwójnie ślepej próby w celu obserwacji nawrotu. Odpowiedź podczas fazy otwartej zdefiniowano jako wynik ≤2 w skali CGI-ADHD-S i zmniejszenie o co najmniej 25% całkowitego wyniku w skali ADHDRS-IV-Parent:Inv w stosunku do wartości wyjściowej. Pacjenci, którzy zostali przydzieleni do grupy STRATTERA i wykazywali ciągłą odpowiedź przez około 8 miesięcy podczas pierwszej fazy leczenia metodą podwójnie ślepej próby, ponownie zostali losowo przydzieleni do kontynuacji ich obecnej dawki leku STRATTERA (N=81) lub do placebo (N=82) w ramach podwójnie ślepej próby. leczenie do obserwacji nawrotu. Nawrót podczas fazy podwójnie ślepej próby zdefiniowano jako wzrost wyniku CGI-ADHD-S o co najmniej 2 od końca fazy otwartej, a całkowity wynik ADHDRS-IV-Parent:Inv powraca do ≥90% wyniku włączenia do badania przez 2 kolejne wizyty. W obu fazach podwójnie ślepej próby u pacjentów otrzymujących kontynuowane leczenie STRATTERA czas do nawrotu był znacznie dłuższy niż u pacjentów otrzymujących placebo.
Badania ADHD u dorosłych
Skuteczność preparatu STRATTERA w leczeniu ADHD ustalono w 2 randomizowanych, podwójnie zaślepionych, kontrolowanych placebo badaniach klinicznych z udziałem dorosłych pacjentów w wieku 18 lat i starszych, którzy spełniali kryteria ADHD DSM-IV.
Oznaki i objawy ADHD oceniano stosując podawaną przez badacza 30-punktową skalę Conners Adult ADHD Rating Scale Screening Version (CAARS). Główną miarą skuteczności był 18-punktowy wynik całkowitego objawu ADHD (suma podskal nieuwagi i nadpobudliwości/impulsywności z CAARS) oceniany przez porównanie średniej zmiany od punktu początkowego do punktu końcowego przy użyciu analizy zamiaru leczenia.
2 identycznych, 10-tygodniowych, randomizowanych, podwójnie zaślepionych, kontrolowanych placebo badaniach ostrego leczenia ostrego leczenia (Badanie 5, N=280; Badanie 6, N=256), pacjenci otrzymywali albo STRATTERA 25 mg albo placebo. STRATTERA podawano w dawce podzielonej wczesnym rankiem i późnym popołudniem/wczesnym wieczorem i dostosowywano dawkę w zależności od odpowiedzi klinicznej w zakresie od 60 do 120 mg/dobę. Średnia końcowa dawka produktu STRATTERA 40 mg w obu badaniach wynosiła około 95 mg/dobę. W obu badaniach objawy ADHD uległy statystycznie istotnej poprawie w badaniu STRATTERA, mierzonej w skali objawów ADHD w skali CAARS.
Badanie podzbiorów populacji w oparciu o płeć i wiek (
INFORMACJA O PACJENCIE
STRATTERA® (Stra-TAIR-a) (atomoksetyna) Kapsułki
Przeczytaj Przewodnik po lekach dołączony do STRATTERA®, zanim Ty lub Twoje dziecko zaczniecie go brać i za każdym razem, gdy otrzymacie uzupełnienie. Mogą pojawić się nowe informacje. Niniejszy Przewodnik po lekach nie zastępuje rozmowy z lekarzem na temat leczenia lub leczenia dziecka preparatem STRATTERA.
Jakie są najważniejsze informacje, które powinienem wiedzieć o STRATTERA 18mg?
Przy stosowaniu STRATTERA zgłaszano następujące przypadki:
Dzieci i nastolatki czasami myślą o samobójstwie, a wiele z nich zgłasza próby samobójstwa. Wyniki badań klinicznych STRATTERA z udziałem ponad 2200 dzieci lub nastolatków z ADHD sugerują, że niektóre dzieci i nastolatki mogą mieć większe prawdopodobieństwo wystąpienia myśli lub działań samobójczych. Chociaż w tych badaniach nie wystąpiły żadne samobójstwa, myśli samobójcze pojawiły się u 4 na 1000 pacjentów. Poinformuj lekarza dziecka lub nastolatka, jeśli Twoje dziecko lub nastolatek (lub ma historię rodzinną):
- ma chorobę afektywną dwubiegunową (choroba maniakalno-depresyjna)
- miał myśli lub działania samobójcze przed rozpoczęciem STRATTERA
Szansa na myśli i działania samobójcze może być większa:
- wcześnie w trakcie leczenia STRATTERA 10mg
- podczas dostosowywania dawki
Zapobiegaj myślom i działaniom samobójczym u swojego dziecka lub nastolatka poprzez:
- zwracanie szczególnej uwagi na nastroje, zachowania, myśli i uczucia dziecka lub nastolatka podczas leczenia STRATTERA 25 mg
- prowadzenie wszystkich wizyt kontrolnych u lekarza dziecka lub nastolatka zgodnie z planem
Zwróć uwagę na następujące objawy u swojego dziecka lub nastolatka podczas leczenia STRATTERA 25 mg:
- lęk
- podniecenie
- atak paniki
- problemy ze snem
- drażliwość
- wrogość
- agresywność
- impulsywność
- niepokój
- mania
- depresja
- myśli samobójcze
Zadzwoń do lekarza dziecka lub nastolatka natychmiast, jeśli wystąpi którykolwiek z powyższych objawów, zwłaszcza jeśli są nowe, nagłe lub ciężkie. Twoje dziecko lub nastolatek może wymagać uważnej obserwacji pod kątem myśli i działań samobójczych lub zmiany w medycynie.
STRATTERA może u niektórych pacjentów powodować uszkodzenie wątroby. Natychmiast skontaktuj się z lekarzem, jeśli u Ciebie lub Twojego dziecka występują następujące objawy problemów z wątrobą:
- swędzący
- ból w prawym górnym brzuchu
- ciemny mocz
- żółta skóra lub oczy
- niewyjaśnione objawy grypopodobne
- nagła śmierć u pacjentów z chorobami serca lub wadami serca
- udar i zawał serca u dorosłych
- podwyższone ciśnienie krwi i tętno
Należy poinformować lekarza, jeśli Ty lub Twoje dziecko ma jakiekolwiek problemy z sercem, wady serca, wysokie ciśnienie krwi lub rodzinną historię tych problemów. Lekarz powinien dokładnie zbadać pacjenta lub dziecko pod kątem problemów z sercem przed rozpoczęciem stosowania leku STRATTERA.
Podczas leczenia lekiem STRATTERA lekarz powinien regularnie sprawdzać ciśnienie krwi lub ciśnienie krwi i tętno dziecka.
Należy natychmiast skontaktować się z lekarzem, jeśli podczas przyjmowania leku STRATTERA wystąpią jakiekolwiek objawy problemów z sercem, takie jak ból w klatce piersiowej, duszność lub omdlenia.
- nowe objawy psychotyczne (takie jak słyszenie głosów, wierzenie w rzeczy, które nie są prawdziwe, bycie podejrzliwym) lub nowe objawy maniakalne
Natychmiast zadzwoń do lekarza dziecka lub nastolatka o wszelkich nowych objawach psychicznych ponieważ może być konieczne dostosowanie lub przerwanie leczenia produktem STRATTERA 40 mg.
Co to jest STRATTERA 18mg?
STRATTERA to selektywny lek hamujący wychwyt zwrotny noradrenaliny. Jest stosowany w leczeniu zespołu nadpobudliwości psychoruchowej z deficytem uwagi (ADHD). STRATTERA może pomóc zwiększyć uwagę oraz zmniejszyć impulsywność i nadpobudliwość u pacjentów z ADHD.
STRATTERA 10 mg powinna być stosowana jako część całkowitego programu leczenia ADHD, który może obejmować poradnictwo lub inne terapie.
STRATTERA nie była badana u dzieci w wieku poniżej 6 lat.
Kto nie powinien brać STRATTERY?
Lek STRATTERA nie powinien być stosowany, jeśli Ty lub Twoje dziecko:
- przyjmujesz lub przyjmowałeś w ciągu ostatnich 14 dni lek przeciwdepresyjny zwany inhibitorem monoaminooksydazy lub MAOI. Niektóre nazwy leków MAOI to Nardil® (siarczan fenelzyny), Parnate® (siarczan tranylcyprominy) i Emsam® (system transdermalny selegiliny).
- masz problem ze wzrokiem zwany jaskrą z wąskim kątem;
- jesteś uczulony na cokolwiek w STRATTERA. Pełna lista składników znajduje się na końcu niniejszego Przewodnika po lekach.
- masz lub miałeś rzadki nowotwór zwany guzem chromochłonnym.
STRATTERA może nie być odpowiednia dla Ciebie lub Twojego dziecka. Przed rozpoczęciem stosowania leku STRATTERA należy poinformować lekarza lub lekarza dziecka o wszystkich stanach zdrowia (lub wywiadzie rodzinnym), w tym:
- masz lub miałeś myśli lub działania samobójcze;
- problemy z sercem, wady serca, nieregularne bicie serca, wysokie ciśnienie krwi lub niskie ciśnienie krwi
- problemy psychiczne, psychoza, mania, choroba afektywna dwubiegunowa lub depresja
- problemy z wątrobą Należy poinformować lekarza, jeśli pacjentka lub dziecko jest w ciąży, planuje zajść w ciążę lub karmi piersią.
Czy STRATTERA można przyjmować z innymi lekami?
Poinformuj swojego lekarza o wszystkich lekach, które Ty lub Twoje dziecko przyjmuje, w tym o lekach wydawanych na receptę i bez recepty, witaminach i suplementach ziołowych. STRATTERA i niektóre leki mogą wchodzić ze sobą w interakcje i powodować poważne skutki uboczne. Lekarz zadecyduje, czy STRATTERA może być przyjmowana z innymi lekami.
Szczególnie powiedz swojemu lekarzowi, jeśli Ty lub Twoje dziecko przyjmuje:
- leki na astmę
- leki przeciwdepresyjne, w tym IMAO
- leki na ciśnienie krwi
- leki na przeziębienie lub alergie, które zawierają leki zmniejszające przekrwienie
Poznaj leki, które Ty lub Twoje dziecko przyjmujesz. Miej przy sobie listę swoich leków, aby pokazać je lekarzowi i farmaceucie.
Nie należy rozpoczynać przyjmowania nowego leku podczas przyjmowania leku STRATTERA bez wcześniejszej konsultacji z lekarzem.
Jak należy przyjmować STRATTERA?
- Weź STRATTERA 40mg dokładnie zgodnie z zaleceniami. STRATTERA 18mg występuje w kapsułkach o różnej mocy dawki. Lekarz może dostosować dawkę tak, aby była odpowiednia dla Ciebie lub Twojego dziecka.
- Nie żuć, nie kruszyć ani nie otwierać kapsułek. Kapsułki STRATTERA połykać w całości popijając wodą lub innym płynem. Należy poinformować lekarza, jeśli pacjent nie może połknąć leku STRATTERA 10 mg w całości. Może być konieczne przepisanie innego leku.
- Unikaj dotykania uszkodzonej kapsułki STRATTERA 18mg. Umyć ręce i powierzchnie, które dotykały otwartej kapsułki STRATTERA 10 mg. Jeśli jakikolwiek proszek dostanie się do twoich oczu lub oczu dziecka, natychmiast przepłucz je wodą i skontaktuj się z lekarzem.
- STRATTERA można przyjmować z jedzeniem lub bez jedzenia.
- STRATTERA 10mg jest zwykle przyjmowana raz lub dwa razy dziennie. Przyjmuj STRATTERA 25mg o tej samej porze każdego dnia, aby pomóc Ci zapamiętać. Jeśli pominiesz dawkę STRATTERY, zażyj ją, gdy tylko przypomnisz sobie ten dzień. W przypadku pominięcia jednego dnia stosowania leku STRATTERA 10 mg, nie należy podwajać dawki następnego dnia. Po prostu pomiń dzień, który opuściłeś.
- Od czasu do czasu lekarz może przerwać na jakiś czas leczenie lekiem STRATTERA 25 mg, aby sprawdzić objawy ADHD.
- Lekarz może przeprowadzać regularne kontrole krwi, serca i ciśnienia krwi podczas przyjmowania leku STRATTERA. Dzieci powinny często sprawdzać wzrost i wagę podczas przyjmowania STRATTERY. Leczenie STRATTERA można przerwać, jeśli podczas tych kontroli wystąpi problem.
- Jeśli Ty lub Twoje dziecko zażyjesz zbyt dużo leku STRATTERA lub przedawkujesz, natychmiast skontaktuj się z lekarzem lub centrum kontroli zatruć, albo skorzystaj z pomocy w nagłych wypadkach.
Jakie są możliwe skutki uboczne STRATTERY?
Widzieć „Jakie są najważniejsze informacje, które powinienem wiedzieć o STRATTERA 10mg?” w celu uzyskania informacji o zgłoszonych myślach i działaniach samobójczych, innych problemach psychicznych, ciężkim uszkodzeniu wątroby i problemach z sercem.
Inne poważne skutki uboczne to:
- ciężkie reakcje alergiczne (wezwij lekarza, jeśli masz problemy z oddychaniem, widzisz obrzęk lub pokrzywkę lub doświadczasz innych reakcji alergicznych)
- spowolnienie wzrostu (wzrostu i masy ciała) u dzieci
- problemy z oddawaniem moczu, w tym
- kłopoty z uruchomieniem lub utrzymaniem strumienia moczu
- nie może całkowicie opróżnić pęcherza
Częste działania niepożądane u dzieci i młodzieży obejmują:
- rozstrój żołądka
- zmniejszony apetyt
- nudności lub wymioty
- zawroty głowy
- zmęczenie
- wahania nastroju
Częste działania niepożądane u dorosłych obejmują:
- zaparcie
- suchość w ustach
- mdłości
- zmniejszony apetyt
- zawroty głowy
- seksualne skutki uboczne
- problemy z oddawaniem moczu
Inne informacje dla dzieci, młodzieży i dorosłych:
- Nieustępujące erekcje (priapizm) występowały rzadko podczas leczenia lekiem STRATTERA. Jeśli masz erekcję, która trwa dłużej niż 4 godziny, natychmiast zwróć się o pomoc medyczną. Ze względu na możliwość trwałego uszkodzenia, w tym potencjalną niezdolność do erekcji, priapizm powinien zostać natychmiast oceniony przez lekarza.
- STRATTERA 10 mg może wpływać na zdolność prowadzenia pojazdów lub obsługi ciężkich maszyn przez Twoje dziecko lub dziecko. Zachowaj ostrożność, dopóki nie dowiesz się, jak STRATTERA 25 mg wpływa na Ciebie lub Twoje dziecko.
- Porozmawiaj z lekarzem, jeśli u Ciebie lub Twojego dziecka wystąpią objawy niepożądane, które są uciążliwe lub nie ustępują.
To nie jest pełna lista możliwych skutków ubocznych. Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać STRATTERA?
- Przechowuj STRATTERA w bezpiecznym miejscu w temperaturze pokojowej, 59 do 86°F (15 do 30°C).
- Przechowuj STRATTERA 40 mg i wszystkie leki w miejscu niedostępnym dla dzieci.
Ogólne informacje o STRATTERA
Leki są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Nie należy stosować leku STRATTERA 25 mg na stan, na który nie został przepisany. Nie podawaj STRATTERY innym osobom, nawet jeśli mają ten sam stan. Może im to zaszkodzić.
Ten przewodnik po lekach podsumowuje najważniejsze informacje na temat STRATTERY. Jeśli chcesz uzyskać więcej informacji, porozmawiaj ze swoim lekarzem. Możesz poprosić swojego lekarza lub farmaceutę o informacje na temat STRATTERA, które zostały napisane dla pracowników służby zdrowia. Aby uzyskać więcej informacji na temat STRATTERA, zadzwoń pod numer 1-800-Lilly-Rx (1-800-545-5979) lub odwiedź stronę www.strattera.com.
Jakie są składniki STRATTERA 40mg?
Składnik czynny: chlorowodorek atomoksetyny.
Nieaktywne składniki: wstępnie żelatynizowana skrobia, dimetikon, żelatyna, laurylosiarczan sodu, FD&CBlue nr 2, syntetyczny żółty tlenek żelaza, dwutlenek tytanu, czerwony tlenek żelaza i jadalny czarny tusz.
Ten przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków.
