Sustiva 200mg, 600mg Efavirenz Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Sustiva 600mg i jak się go stosuje?
Sustiva to lek na receptę stosowany w leczeniu objawów zakażenia wirusem HIV. Sustiva może być stosowany samodzielnie lub z innymi lekami.
Sustiva należy do klasy leków zwanych HIV, NNRTI.
Nie wiadomo, czy Sustiva jest bezpieczna i skuteczna u dzieci w wieku poniżej 3 miesięcy.
Jakie są możliwe skutki uboczne Sustiva?
Sustiva może powodować poważne skutki uboczne, w tym:
- pokrzywka,
- trudności w oddychaniu,
- obrzęk twarzy, warg, języka lub gardła,
- gorączka,
- ból gardła,
- płonące oczy,
- ból skóry,
- czerwona lub fioletowa wysypka skórna z powstawaniem pęcherzy i łuszczeniem się,
- konfiskata,
- halucynacje,
- problemy z koncentracją,
- problemy z mówieniem lub poruszaniem się (mogą wystąpić miesiące lub lata po rozpoczęciu przyjmowania leku),
- zawroty głowy,
- senność,
- dezorientacja,
- problemy z koncentracją,
- dziwne sny,
- bezsenność,
- problemy z mową,
- trudności z równowagą lub ruchem mięśni,
- lęk,
- paranoja,
- nietypowe zachowanie,
- uczucie smutku lub beznadziejności,
- myśli samobójcze,
- mdłości,
- ból brzucha,
- utrata apetytu,
- ciemny mocz,
- stołki w kolorze gliny,
- zażółcenie skóry lub oczu (żółtaczka),
- nocne poty,
- obrzęk gruczołów,
- opryszczka,
- kaszel,
- świszczący oddech,
- biegunka,
- odchudzanie,
- trudności z połykaniem,
- problemy z równowagą lub ruchem gałek ocznych,
- słabość,
- kłujące uczucie,
- obrzęk szyi lub gardła (powiększenie tarczycy),
- zmiany menstruacyjne i
- impotencja
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Do najczęstszych skutków ubocznych Sustiva należą:
- mdłości,
- wymioty,
- zawroty głowy,
- senność,
- problemy z koncentracją,
- wysypka,
- ból głowy,
- zmęczenie,
- problemy ze snem (bezsenność),
- dziwne sny i
- zmiany kształtu lub lokalizacji tkanki tłuszczowej (zwłaszcza w ramionach, nogach, twarzy, szyi, piersiach i talii)
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Sustiva. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
SUSTIVA® (efavirenz) jest swoistym dla HIV-1, nienukleozydowym inhibitorem odwrotnej transkryptazy (NNRTI). Efawirenz jest chemicznie opisany jako (S)-6-chloro-4-(cyklopropyloetynylo)-1,4-dihydro4-(trifluorometylo)-2H-3,1-benzoksazyn-2-on. Jego wzór empiryczny to C14H9ClF3NO2, a wzór strukturalny to:
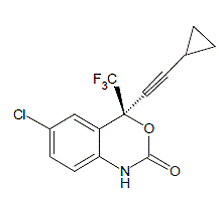
Efawirenz jest krystalicznym proszkiem o barwie od białej do lekko różowej o masie cząsteczkowej 315,68. Jest praktycznie nierozpuszczalny w wodzie (
Kapsułki
SUSTIVA jest dostępny w postaci kapsułek do podawania doustnego zawierających 50 mg lub 200 mg efawirenzu oraz następujące składniki nieaktywne: jednowodna laktoza, stearynian magnezu, laurylosiarczan sodu i glikolan sodowy skrobi. Otoczka kapsułki zawiera następujące nieaktywne składniki i barwniki: żelatynę, laurylosiarczan sodu, dwutlenek tytanu i/lub żółty tlenek żelaza. Osłonki kapsułek mogą również zawierać dwutlenek krzemu. Kapsułki są nadrukowane tuszem zawierającym błękit karminowy 40, błękit FD&C nr 2 i dwutlenek tytanu.
Tablety
SUSTIVA 600 mg jest dostępny w postaci tabletek powlekanych do podawania doustnego zawierających 600 mg efawirenzu i następujące składniki nieaktywne: kroskarmeloza sodowa, hydroksypropyloceluloza, laktoza jednowodna, stearynian magnezu, celuloza mikrokrystaliczna i laurylosiarczan sodu. Powłoka zawiera Opadry Yellow i Opadry Clear. Tabletki są polerowane woskiem Carnauba i nadrukowane fioletowym tuszem, Opacode WB.
WSKAZANIA
SUSTIVA® (efawirenz) w połączeniu z innymi lekami przeciwretrowirusowymi jest wskazany w leczeniu zakażenia ludzkim wirusem niedoboru odporności typu 1 (HIV-1) u dorosłych i dzieci w wieku co najmniej 3 miesięcy i masie ciała co najmniej 3,5 kg.
DAWKOWANIE I SPOSÓB PODAWANIA
Funkcja wątroby
Monitorować czynność wątroby przed i w trakcie leczenia preparatem SUSTIVA [patrz OSTRZEŻENIA I ŚRODKI ]. SUSTIVA 600 mg nie jest zalecany u pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby (stopień B lub C w skali Child Pugh) [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
Dorośli ludzie
Zalecana dawka preparatu SUSTIVA (efawirenz) wynosi 600 mg doustnie, raz na dobę, w skojarzeniu z inhibitorem proteazy i/lub analogowymi inhibitorami odwrotnej transkryptazy nukleozydowej (NRTI). Zaleca się przyjmowanie preparatu SUSTIVA na pusty żołądek, najlepiej przed snem. Zwiększone stężenia efawirenzu obserwowane po podaniu preparatu SUSTIVA 600 mg z pokarmem mogą prowadzić do zwiększenia częstości występowania działań niepożądanych [patrz FARMAKOLOGIA KLINICZNA ]. Dawkowanie przed snem może poprawić tolerancję objawów układu nerwowego [patrz OSTRZEŻENIA I ŚRODKI , DZIAŁANIA NIEPOŻĄDANE , oraz INFORMACJA O PACJENCIE ]. Kapsułki lub tabletki SUSTIVA należy połykać w całości popijając płynem. W przypadku pacjentów, którzy nie mogą połykać kapsułek lub tabletek, zaleca się podawanie kapsułek metodą posypywania [patrz Sposób podawania kapsułki posypki ].
Jednoczesna terapia przeciwretrowirusowa
SUSTIVA należy podawać w skojarzeniu z innymi lekami przeciwretrowirusowymi [patrz WSKAZANIA , OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI , oraz FARMAKOLOGIA KLINICZNA ].
Dostosowanie dawkowania
Jeśli preparat SUSTIVA 200 mg jest podawany jednocześnie z worykonazolem, dawkę podtrzymującą worykonazolu należy zwiększać do 400 mg co 12 godzin, a dawkę 200 mg preparatu SUSTIVA należy zmniejszać do 300 mg raz na dobę, stosując kapsułki (jedna kapsułka 200 mg i dwie kapsułki 50 mg lub sześć kapsułek 50 mg). kapsułki mg). Tabletek SUSTIVA 600 mg nie wolno łamać. [Widzieć INTERAKCJE Z LEKAMI oraz FARMAKOLOGIA KLINICZNA .]
Jeśli preparat SUSTIVA podawany jest jednocześnie z ryfampiną pacjentom o masie ciała 50 kg lub większej, zaleca się zwiększenie dawki preparatu SUSTIVA 200 mg do 800 mg raz na dobę [patrz INTERAKCJE Z LEKAMI oraz FARMAKOLOGIA KLINICZNA ].
Pacjenci pediatryczni
Zaleca się przyjmowanie preparatu SUSTIVA 600 mg na pusty żołądek, najlepiej przed snem. Tabela 1 opisuje zalecaną dawkę preparatu SUSTIVA dla dzieci w wieku 3 miesięcy lub starszych i ważących od 3,5 kg do 40 kg [patrz FARMAKOLOGIA KLINICZNA ]. Zalecana dawka preparatu SUSTIVA dla dzieci o masie ciała 40 kg lub większej wynosi 600 mg raz na dobę. W przypadku pacjentów pediatrycznych, którzy nie mogą połykać kapsułek, zawartość kapsułki można podawać z niewielką ilością pokarmu lub odżywki dla niemowląt, stosując metodę posypywania kapsułek [patrz Sposób podawania kapsułki posypki ].
Sposób podawania kapsułki posypki
przypadku pacjentów pediatrycznych w wieku co najmniej 3 miesięcy i ważących co najmniej 3,5 kg oraz dorosłych, którzy nie mogą połykać kapsułek lub tabletek, zawartość kapsułki można podać z niewielką ilością (1 do 2 łyżeczek) pokarmu. Stosowanie mieszanek dla niemowląt do mieszania powinno być brane pod uwagę tylko w przypadku tych małych niemowląt, które nie mogą rzetelnie spożywać pokarmów stałych. Należy poinstruować pacjentów i opiekunów, aby ostrożnie otwierali kapsułkę, aby uniknąć rozlania lub rozproszenia zawartości kapsułki w powietrzu. Kapsułkę należy trzymać poziomo nad małym pojemnikiem i ostrożnie przekręcić w celu otwarcia. W przypadku pacjentów, którzy tolerują pokarmy stałe, całą zawartość kapsułki należy delikatnie wymieszać z odpowiednim dla wieku pokarmem miękkim, takim jak mus jabłkowy, galaretka winogronowa lub jogurt, w małym pojemniku. W przypadku małych niemowląt otrzymujących mieszankę mieszanki dla niemowląt w kapsułkach, całą zawartość kapsułki należy delikatnie wymieszać z 2 łyżeczkami odtworzonej mieszanki dla niemowląt o temperaturze pokojowej w małym pojemniku, ostrożnie mieszając małą łyżeczką, a następnie pobrać mieszaninę do 10 Strzykawka do podawania doustnego o pojemności ml do podawania. Po podaniu mieszanki SUSTIVA-pokarm lub formuła, do pustego pojemnika do mieszania należy dodać dodatkową niewielką ilość (około 2 łyżeczki) pokarmu lub mieszanki, wymieszać w celu rozproszenia wszelkich pozostałych pozostałości SUSTIVA i podać pacjentowi. Mieszankę pokarmu lub formuły SUSTIVA należy podać w ciągu 30 minut od wymieszania. Nie należy spożywać dodatkowego pokarmu przez 2 godziny po podaniu preparatu SUSTIVA.
Dalsze instrukcje dla pacjenta dotyczące sposobu podawania posypki kapsułki znajdują się w zatwierdzonym przez FDA oznakowaniu pacjenta (patrz INFORMACJA O PACJENCIE oraz INSTRUKCJA UŻYCIA ).
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Kapsułki
Kapsułki 200 mg są koloru złotego, z nadrukiem „SUSTIVA” na korpusie i „200 mg” na wieczku.
Kapsułki 50 mg są koloru złotego i białego, z nadrukiem „SUSTIVA” na złotym wieczku i odwróconym nadrukiem „50 mg” na białym korpusie.
Tablety
Tabletki 600 mg to żółte tabletki powlekane w kształcie kapsułki, z nadrukowanym po obu stronach napisem „SUSTIVA”.
Składowania i stosowania
Kapsułki
Kapsułki SUSTIVA® (efavirenz) są dostępne w następujący sposób:
Kapsułki 200 mg są koloru złotego, z nadrukiem „SUSTIVA” na korpusie i „200 mg” na wieczku.
Butelki 90 - NDC 0056-0474-92
Kapsułki 50 mg są koloru złotego i białego, z nadrukiem „SUSTIVA” na złotym wieczku i odwrotnym nadrukiem „50 mg” na białym korpusie.
Butelki po 30 - NDC 0056-0470-30
Tablety
Tabletki SUSTIVA® (efavirenz) są dostępne w następujący sposób:
Tabletki 600 mg to żółte tabletki powlekane w kształcie kapsułki, z nadrukowanym po obu stronach napisem „SUSTIVA”.
Butelki po 30 - NDC 0056-0510-30
Magazynowanie
Kapsułki SUSTIVA 600 mg i tabletki SUSTIVA należy przechowywać w temperaturze 25°C (77°F); dopuszczalne odchylenia do 15°C-30°C (59°F-86°F) [patrz Kontrolowana temperatura pokojowa USP].
Dystrybutor: Bristol-Myers Squibb Company Princeton, NJ 08543 USA. Poprawiono: październik 2020 r.
SKUTKI UBOCZNE
Najistotniejsze działania niepożądane obserwowane u pacjentów leczonych preparatem SUSTIVA to:
- objawy psychiatryczne [patrz OSTRZEŻENIA I ŚRODKI ],
- objawy układu nerwowego [patrz OSTRZEŻENIA I ŚRODKI ],
- wysypka [patrz OSTRZEŻENIA I ŚRODKI ].
- hepatotoksyczność [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość zgłaszanych działań niepożądanych nie może być bezpośrednio porównywana z częstością w innych badaniach klinicznych i może nie odzwierciedlać częstości obserwowanych w praktyce klinicznej.
Działania niepożądane u dorosłych
Najczęstszymi (>5% w każdej grupie leczonej efawirenzem) działaniami niepożądanymi o co najmniej umiarkowanym nasileniu wśród pacjentów w badaniu 006 leczonych preparatem SUSTIVA 200 mg w skojarzeniu z zydowudyną/lamiwudyną lub indynawirem były wysypka, zawroty głowy, nudności, ból głowy, zmęczenie, bezsenność, i wymioty.
Wybrane kliniczne działania niepożądane o umiarkowanym lub ciężkim nasileniu obserwowane u ≥2% pacjentów leczonych preparatem SUSTIVA w dwóch kontrolowanych badaniach klinicznych przedstawiono w Tabeli 2.
Zgłaszano zapalenie trzustki, chociaż nie ustalono związku przyczynowego z efawirenzem. Bezobjawowe zwiększenie stężenia amylazy w surowicy obserwowano u znacznie większej liczby pacjentów leczonych efawirenzem w dawce 600 mg niż u pacjentów z grupy kontrolnej (patrz Nieprawidłowości laboratoryjne ).
Objawy układu nerwowego
przypadku 1008 pacjentów leczonych schematami zawierającymi SUSTIVA i 635 pacjentów leczonych schematem kontrolnym w kontrolowanych badaniach, w Tabeli 3 wymieniono częstość objawów o różnym stopniu nasilenia i podano częstość przerwania leczenia w przypadku jednego lub więcej z następujących objawów ze strony układu nerwowego: zawroty głowy, bezsenność, zaburzenia koncentracji, senność, nieprawidłowe sny, euforia, splątanie, pobudzenie, amnezja, omamy, otępienie, nieprawidłowe myślenie i depersonalizacja [patrz OSTRZEŻENIA I ŚRODKI ]. Częstość występowania poszczególnych objawów ze strony ośrodkowego i obwodowego układu nerwowego przedstawia tabela 2.
Objawy psychiatryczne
U pacjentów leczonych preparatem SUSTIVA zgłaszano poważne zaburzenia psychiczne. W kontrolowanych badaniach objawami psychicznymi obserwowanymi z częstością większą niż 2% wśród pacjentów leczonych odpowiednio SUSTIVA 600 mg lub schematami kontrolnymi były: depresja (19%, 16%), lęk (13%, 9%) i nerwowość (7%). , 2%).
Wysypka
kontrolowanych badaniach klinicznych częstość wysypki (wszystkich stopni, niezależnie od przyczyny) wynosiła 26% u 1008 osób dorosłych leczonych schematami zawierającymi SUSTIVA 200 mg i 17% u 635 osób dorosłych leczonych schematem kontrolnym. Większość zgłoszeń wysypki miała nasilenie łagodne lub umiarkowane. Częstość wysypki stopnia 3. wynosiła 0,8% dla pacjentów leczonych SUSTIVA i 0,3% dla grup kontrolnych, a częstość wysypki stopnia 4. wynosiła 0,1% dla pacjentów leczonych SUSTIVA i 0 dla grup kontrolnych. Wskaźniki przerwania leczenia z powodu wysypki wynosiły 1,7% dla pacjentów leczonych SUSTIVA i 0,3% dla grup kontrolnych [patrz OSTRZEŻENIA I ŚRODKI ].
Doświadczenie ze stosowaniem preparatu SUSTIVA u pacjentów, którzy przerwali stosowanie innych leków przeciwretrowirusowych z klasy NNRTI, jest ograniczone. Dziewiętnastu pacjentów, którzy przerwali leczenie newirapiną z powodu wysypki, leczono preparatem SUSTIVA. U dziewięciu z tych pacjentów wystąpiła wysypka o nasileniu od łagodnej do umiarkowanej podczas leczenia preparatem SUSTIVA, a dwóch z nich przerwało leczenie z powodu wysypki.
Nieprawidłowości laboratoryjne
Wybrane nieprawidłowości laboratoryjne stopnia 3-4 zgłoszone u ≥2% pacjentów leczonych preparatem SUSTIVA w dwóch badaniach klinicznych przedstawiono w Tabeli 4.
Pacjenci współzakażeni wirusowym zapaleniem wątroby typu B lub C
Testy czynności wątroby należy monitorować u pacjentów z wirusowym zapaleniem wątroby typu B i (lub) C w wywiadzie. W zestawie danych długoterminowych z badania 006, 137 pacjentów leczonych schematami zawierającymi SUSTIVA (mediana czasu trwania leczenia 68 tygodni) i 84 leczonych w schemacie kontrolnym (mediana czasu trwania, 56 tygodni) były seropozytywne w badaniu przesiewowym w kierunku wirusowego zapalenia wątroby typu B (dodatni antygen powierzchniowy) i/lub C (dodatnie przeciwciała przeciwko wirusowemu zapaleniu wątroby typu C). Wśród tych pacjentów z równoczesnym zakażeniem podwyższenie AST do ponad 5-krotności GGN wystąpiło u 13% pacjentów w grupie SUSTIVA i 7% w ramieniu kontrolnym, a podwyższenie ALT do ponad 5-krotności GGN wystąpiło u 20% pacjentów w ramionach SUSTIVA i 7% pacjentów w ramieniu kontrolnym. Wśród pacjentów z koinfekcją 3% leczonych schematami zawierającymi SUSTIVA i 2% w grupie kontrolnej przerwało udział w badaniu z powodu zaburzeń wątroby lub dróg żółciowych [patrz OSTRZEŻENIA I ŚRODKI ].
Lipidy
niektórych niezakażonych ochotników otrzymujących preparat SUSTIVA zaobserwowano wzrost stężenia całkowitego cholesterolu w stosunku do wartości wyjściowej o 10-20%. U pacjentów leczonych preparatem SUSTIVA + zydowudyna + lamiwudyna obserwowano zwiększenie stężenia cholesterolu całkowitego i HDL na czczo w stosunku do wartości wyjściowych odpowiednio o około 20% i 25%. U pacjentów leczonych preparatem SUSTIVA + indynawir zaobserwowano wzrost stężenia cholesterolu nie na czczo i HDL w stosunku do wartości wyjściowej odpowiednio o około 40% i 35%. Stężenia cholesterolu całkowitego na czczo ≥240 mg/dl i ≥300 mg/dl zgłaszano odpowiednio u 34% i 9% pacjentów leczonych preparatem SUSTIVA + zydowudyna + lamiwudyna; Odpowiednio 54% i 20% pacjentów leczonych SUSTIVA + indynawir; oraz odpowiednio 28% i 4% pacjentów leczonych indynawirem + zydowudyną + lamiwudyną. Wpływ SUSTIVA 600 mg na triglicerydy i LDL w tym badaniu nie został dobrze scharakteryzowany, ponieważ próbki pobrano od pacjentów nie będących na czczo. Kliniczne znaczenie tych wyników nie jest znane [patrz OSTRZEŻENIA I ŚRODKI ].
Działania niepożądane u pacjentów pediatrycznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość zgłaszanych działań niepożądanych nie może być bezpośrednio porównywana z częstością w innych badaniach klinicznych i może nie odzwierciedlać częstości obserwowanych w praktyce klinicznej.
Ocena działań niepożądanych opiera się na trzech badaniach klinicznych z udziałem 182 pacjentów pediatrycznych zakażonych HIV-1 (w wieku od 3 miesięcy do 21 lat), którzy otrzymywali SUSTIVA 200 mg w skojarzeniu z innymi lekami przeciwretrowirusowymi przez medianę 123 tygodni. Działania niepożądane obserwowane w trzech badaniach były podobne do tych obserwowanych w badaniach klinicznych u dorosłych, z wyjątkiem tego, że wysypka występowała częściej u dzieci (32% dla wszystkich stopni niezależnie od przyczyny) i częściej o wyższym stopniu nasilenia (tj. cięższym). U dwóch (1,1%) pacjentów pediatrycznych wystąpiła wysypka stopnia 3 (zlewająca się wysypka z gorączką, wysypka uogólniona), a czterech (2,2%) pacjentów pediatrycznych wystąpiła wysypka stopnia 4 (cały rumień wielopostaciowy). Pięciu pacjentów pediatrycznych (2,7%) przerwało udział w badaniu z powodu wysypki [patrz OSTRZEŻENIA I ŚRODKI ].
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane po zatwierdzeniu produktu SUSTIVA. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o nieznanej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Ciało jako całość: reakcje alergiczne, osłabienie, redystrybucja/nagromadzenie tkanki tłuszczowej [patrz OSTRZEŻENIA I ŚRODKI ]
Centralny i obwodowy układ nerwowy: nieprawidłowa koordynacja, ataksja, encefalopatia, zaburzenia koordynacji i równowagi móżdżkowej, drgawki, niedoczulica, parestezje, neuropatia, drżenie, zawroty głowy
Wewnątrzwydzielniczy: ginekomastia
Przewód pokarmowy: zaparcia, zaburzenia wchłaniania
Układ sercowo-naczyniowy: uderzenia gorąca, kołatanie serca
Wątroba i układ żółciowy: zwiększenie aktywności enzymów wątrobowych, niewydolność wątroby, zapalenie wątroby.
Metaboliczne i odżywcze: hipercholesterolemia, hipertriglicerydemia
Układ mięśniowo-szkieletowy: bóle stawów, bóle mięśni, miopatia
Psychiatryczny: reakcje agresywne, pobudzenie, urojenia, labilność emocjonalna, mania, nerwica, paranoja, psychoza, samobójstwo, katatonia
Oddechowy: duszność
Skóra i przydatki: rumień wielopostaciowy, fotoalergiczne zapalenie skóry, zespół Stevensa-Johnsona
Zmysły specjalne: zaburzenia widzenia, szum w uszach
INTERAKCJE Z LEKAMI
Potencjał SUSTIVA do wpływania na inne leki
Wykazano, że in vivo efawirenz indukuje CYP3A i CYP2B6. Inne związki będące substratami CYP3A lub CYP2B6 mogą mieć zmniejszone stężenia w osoczu, gdy są podawane jednocześnie z preparatem SUSTIVA.
Potencjalny wpływ innych leków na SUSTIVA
Oczekuje się, że leki indukujące aktywność CYP3A (np. fenobarbital, ryfampicyna, ryfabutyna) będą zwiększać klirens efawirenzu, powodując zmniejszenie stężenia w osoczu [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Leki wydłużające odstęp QT
Dostępne są ograniczone informacje na temat możliwości interakcji farmakodynamicznej między preparatem SUSTIVA 600 mg a lekami wydłużającymi odstęp QTc. Podczas stosowania efawirenzu obserwowano wydłużenie odstępu QTc [patrz FARMAKOLOGIA KLINICZNA ]. Rozważ alternatywy dla SUSTIVA 600 mg w przypadku jednoczesnego podawania z lekiem o znanym ryzyku Torsade de Pointes.
Ustalone i inne potencjalnie istotne interakcje leków
Interakcje leków z SUSTIVA podsumowano w Tabeli 5. Dane farmakokinetyczne [patrz FARMAKOLOGIA KLINICZNA ] Tabele 7 i 8. Ta tabela zawiera potencjalnie istotne interakcje, ale nie jest wyczerpująca.
Leki bez klinicznie istotnych interakcji z SUSTIVA
Nie zaleca się zmiany dawkowania, gdy SUSTIVA 600 mg jest podawany z następującymi lekami zobojętniającymi kwas żołądkowo-glinowy/magnezowy, azytromycyną, cetyryzyną, famotydyną, flukonazolem, lorazepamem, nelfinawirem, nukleozydowymi inhibitorami odwrotnej transkryptazy (abakawir, emtrycytabina, lamiwudyna, stawowirydyna, ), paroksetyna i raltegrawir.
Interakcja testu kannabinoidowego
Efawirenz nie wiąże się z receptorami kannabinoidowymi. Fałszywie dodatnie wyniki testu na kannabinoidy w moczu były zgłaszane w niektórych testach przesiewowych u osób niezakażonych i zakażonych wirusem HIV otrzymujących efawirenz. Zalecane jest potwierdzenie pozytywnych testów przesiewowych na kannabinoidy bardziej specyficzną metodą.
OSTRZEŻENIA
Zawarte jako część "ŚRODKI OSTROŻNOŚCI" Sekcja
ŚRODKI OSTROŻNOŚCI
Interakcje leków
Substraty, inhibitory lub induktory CYP3A mogą zmieniać stężenia efawirenzu w osoczu. Podobnie efawirenz może zmieniać stężenia leków metabolizowanych przez CYP3A lub CYP2B6 w osoczu. Najbardziej widocznym działaniem efawirenzu w stanie stacjonarnym jest indukcja CYP3A i CYP2B6 [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz INTERAKCJE Z LEKAMI ].
Przedłużenie QTc
Podczas stosowania efawirenzu obserwowano wydłużenie odstępu QTc [patrz INTERAKCJE Z LEKAMI oraz FARMAKOLOGIA KLINICZNA ]. Rozważ alternatywy dla SUSTIVA 600 mg w przypadku jednoczesnego podawania z lekiem o znanym ryzyku Torsade de Pointes lub w przypadku podawania pacjentom z wyższym ryzykiem Torsade de Pointes.
Opór
SUSTIVA 200mg nie może być stosowany jako pojedynczy środek do leczenia zakażenia HIV-1 ani jako jedyny środek do nieudanego schematu leczenia. Wirus oporny pojawia się szybko, gdy efawirenz jest podawany w monoterapii. Przy wyborze nowych leków przeciwretrowirusowych do stosowania w skojarzeniu z efawirenzem należy wziąć pod uwagę możliwość wystąpienia wirusowej oporności krzyżowej.
Współadministracja z powiązanymi produktami
Jednoczesne podawanie preparatu SUSTIVA z preparatem ATRIPLA (efawirenz 600 mg/emtrycytabina 200 mg/fumaran dizoproksylu tenofowiru 300 mg) nie jest zalecane, chyba że jest to konieczne w celu dostosowania dawki (np. z ryfampiną), ponieważ efawirenz jest jedną z jego substancji czynnych.
Objawy psychiatryczne
pacjentów leczonych preparatem SUSTIVA zgłaszano poważne zaburzenia psychiczne. W kontrolowanych badaniach obejmujących 1008 pacjentów leczonych schematami zawierającymi SUSTIVA 600 mg przez średnio 2,1 roku i 635 pacjentów leczonych schematami kontrolnymi przez średnio 1,5 roku, częstość (niezależnie od przyczynowości) określonych ciężkich zaburzeń psychicznych wśród pacjentów, którzy otrzymywali SUSTIVA lub schematami kontrolnymi były odpowiednio ciężka depresja (2,4%, 0,9%), myśli samobójcze (0,7%, 0,3%), próby samobójcze niezakończone zgonem (0,5%, 0), agresywne zachowanie (0,4%, 0,5%), reakcje paranoidalne (0,4 %, 0,3% i reakcje maniakalne (0,2%, 0,3%). Gdy objawy psychiczne podobne do wymienionych powyżej zostały połączone i ocenione jako grupa w wieloczynnikowej analizie danych z badania 006, leczenie efawirenzem wiązało się ze wzrostem występowania tych wybranych objawów psychicznych. Inne czynniki związane ze wzrostem występowania tych objawów psychiatrycznych to historia zażywania narkotyków w iniekcjach, wywiad psychiatryczny i przyjmowanie leków psychiatrycznych w momencie włączenia do badania; podobne związki zaobserwowano zarówno w grupie leczonej SUSTIVA, jak iw grupie kontrolnej. W badaniu 006 w trakcie całego badania pojawiły się nowe poważne objawy psychiczne, zarówno u pacjentów leczonych SUSTIVA, jak i grupy kontrolnej. Jeden procent pacjentów leczonych SUSTIVA przerwał lub przerwał leczenie z powodu jednego lub więcej z tych wybranych objawów psychicznych. Istnieją również sporadyczne doniesienia po wprowadzeniu do obrotu o zgonach w wyniku samobójstwa, urojeniach i zachowaniach podobnych do psychozy, chociaż na podstawie tych doniesień nie można ustalić związku przyczynowego ze stosowaniem preparatu SUSTIVA. Zgłaszano również przypadki katatonii po wprowadzeniu do obrotu, które mogą być związane ze zwiększoną ekspozycją na efawirenz. Pacjenci z poważnymi psychiatrycznymi doświadczeniami niepożądanymi powinni zasięgnąć natychmiastowej oceny lekarskiej, aby ocenić możliwość, że objawy mogą być związane ze stosowaniem SUSTIVA, a jeśli tak, aby ustalić, czy ryzyko kontynuacji leczenia przewyższa korzyści. [Widzieć DZIAŁANIA NIEPOŻĄDANE .]
Objawy układu nerwowego
Pięćdziesiąt trzy procent (531/1008) pacjentów otrzymujących SUSTIVA 600 mg w kontrolowanych badaniach zgłosiło objawy ze strony ośrodkowego układu nerwowego (dowolnego stopnia, niezależnie od przyczynowości) w porównaniu z 25% (156/635) pacjentów otrzymujących schematy kontrolne [patrz DZIAŁANIA NIEPOŻĄDANE ]. Objawy te obejmowały m.in. zawroty głowy (28,1% ze 1008 pacjentów), bezsenność (16,3%), zaburzenia koncentracji (8,3%), senność (7,0%), nietypowe sny (6,2%) i omamy (1,2 %). Objawy te były ciężkie u 2,0% pacjentów; w rezultacie 2,1% pacjentów przerwało terapię. Objawy te zwykle pojawiają się w pierwszym lub drugim dniu leczenia i zwykle ustępują po pierwszych 2-4 tygodniach leczenia. Po 4 tygodniach leczenia częstość występowania objawów ze strony układu nerwowego o co najmniej umiarkowanym nasileniu wahała się od 5% do 9% u pacjentów leczonych schematami zawierającymi SUSTIVA i od 3% do 5% u pacjentów leczonych schematem kontrolnym. Należy poinformować pacjentów, że te częste objawy prawdopodobnie ulegną poprawie wraz z kontynuacją leczenia i nie są predyktorem późniejszego wystąpienia rzadszych objawów psychicznych [patrz Objawy psychiatryczne ]. Dawkowanie przed snem może poprawić tolerancję tych objawów układu nerwowego [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Analiza danych długoterminowych z badania 006 (mediana okresu obserwacji odpowiednio 180 tygodni, 102 tygodnie i 76 tygodni w przypadku pacjentów leczonych preparatami SUSTIVA + zydowudyna + lamiwudyna, SUSTIVA + indynawir i indynawir + zydowudyna + lamiwudyna) wykazała, że ponad Po 24 tygodniach leczenia częstość występowania nowych objawów ze strony układu nerwowego wśród pacjentów leczonych preparatem SUSTIVA była zasadniczo podobna do częstości występowania w grupie kontrolnej zawierającej indynawir.
Neurotoksyczność o późnym początku, w tym ataksja i encefalopatia (upośledzenie świadomości, splątanie, spowolnienie psychoruchowe, psychoza, majaczenie), może wystąpić kilka miesięcy lub lat po rozpoczęciu leczenia efawirenzem. Niektóre zdarzenia neurotoksyczności o późnym początku wystąpiły u pacjentów z polimorfizmami genetycznymi CYP2B6, które są związane ze zwiększonym stężeniem efawirenzu pomimo standardowego dawkowania preparatu SUSTIVA. Pacjentów z objawami przedmiotowymi i podmiotowymi poważnych neurologicznych działań niepożądanych należy niezwłocznie ocenić, aby ocenić możliwość, że zdarzenia te mogą mieć związek ze stosowaniem efawirenzu oraz czy uzasadnione jest przerwanie leczenia produktem SUSTIVA 600 mg.
Pacjentów otrzymujących SUSTIVA 600 mg należy ostrzec o możliwości addytywnego działania na ośrodkowy układ nerwowy, gdy SUSTIVA 200 mg jest stosowany jednocześnie z alkoholem lub lekami psychoaktywnymi.
Pacjenci, u których występują objawy ze strony ośrodkowego układu nerwowego, takie jak zawroty głowy, zaburzenia koncentracji i (lub) senność, powinni unikać potencjalnie niebezpiecznych czynności, takich jak prowadzenie pojazdów lub obsługiwanie maszyn.
Toksyczność zarodkowo-płodowa
Efawirenz podawany kobiecie w ciąży w pierwszym trymestrze może powodować uszkodzenie płodu. Doradź kobietom o potencjale rozrodczym, które otrzymują SUSTIVA 600 mg, aby uniknąć ciąży. [Widzieć Używaj w określonych populacjach .]
Wysypka
W kontrolowanych badaniach klinicznych u 26% (266/1008) dorosłych pacjentów leczonych preparatem SUSTIVA w dawce 600 mg wystąpiła nowa wysypka skórna w porównaniu z 17% (111/635) pacjentów leczonych w grupach kontrolnych [patrz DZIAŁANIA NIEPOŻĄDANE ]. Wysypka związana z powstawaniem pęcherzy, wilgotnym łuszczeniem lub owrzodzeniem wystąpiła u 0,9% (9/1008) pacjentów leczonych preparatem SUSTIVA. Częstość występowania wysypki stopnia 4. (np. rumienia wielopostaciowego, zespołu Stevensa-Johnsona) u dorosłych pacjentów leczonych preparatem SUSTIVA we wszystkich badaniach i poszerzonym dostępem wynosiła 0,1%. Wysypki są zwykle łagodnymi do umiarkowanych wykwitami plamisto-grudkowymi, które występują w ciągu pierwszych 2 tygodni od rozpoczęcia leczenia efawirenzem (mediana czasu do wystąpienia wysypki u dorosłych wynosiła 11 dni), a u większości pacjentów kontynuujących leczenie efawirenzem wysypka ustępuje w ciągu 1 miesiąc (mediana czasu trwania, 16 dni). Wskaźnik przerwania leczenia z powodu wysypki w badaniach klinicznych z udziałem dorosłych wyniósł 1,7% (17/08).
Wysypkę zgłoszono u 59 ze 182 pacjentów pediatrycznych (32%) leczonych preparatem SUSTIVA [patrz DZIAŁANIA NIEPOŻĄDANE ]. U dwóch pacjentów pediatrycznych wystąpiła wysypka stopnia 3. (zlewająca się wysypka z gorączką, wysypka uogólniona), a czterech pacjentów wysypka stopnia 4. (rumień wielopostaciowy). Mediana czasu do wystąpienia wysypki u dzieci i młodzieży wynosiła 28 dni (zakres 3-1642 dni). Należy rozważyć profilaktykę odpowiednimi lekami przeciwhistaminowymi przed rozpoczęciem leczenia preparatem SUSTIVA u dzieci i młodzieży.
SUSTIVA 600 mg można na ogół wznowić u pacjentów przerywających terapię z powodu wysypki. SUSTIVA 200 mg należy odstawić u pacjentów, u których wystąpi ciężka wysypka związana z powstawaniem pęcherzy, łuszczeniem, zajęciem błon śluzowych lub gorączką. Odpowiednie leki przeciwhistaminowe i/lub kortykosteroidy mogą poprawić tolerancję i przyspieszyć ustępowanie wysypki. W przypadku pacjentów, u których wystąpiła zagrażająca życiu reakcja skórna (np. zespół Stevensa-Johnsona), należy rozważyć alternatywne leczenie [patrz PRZECIWWSKAZANIA ].
Hepatotoksyczność
Po wprowadzeniu produktu do obrotu zgłaszano przypadki zapalenia wątroby, w tym piorunującego zapalenia wątroby postępującego do niewydolności wątroby wymagającej przeszczepu lub skutkującej zgonem, u pacjentów leczonych preparatem SUSTIVA. Zgłoszenia obejmowały pacjentów z podstawową chorobą wątroby, w tym ze współistniejącym zapaleniem wątroby typu B lub C, oraz pacjentów bez wcześniejszej choroby wątroby lub innych możliwych do zidentyfikowania czynników ryzyka.
SUSTIVA 600 mg nie jest zalecany u pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby. Zaleca się uważne monitorowanie pacjentów z łagodnymi zaburzeniami czynności wątroby otrzymujących SUSTIVA. [Widzieć DZIAŁANIA NIEPOŻĄDANE oraz Używaj w określonych populacjach ].
U wszystkich pacjentów zaleca się monitorowanie enzymów wątrobowych przed i w trakcie leczenia [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Należy rozważyć przerwanie stosowania preparatu SUSTIVA 600 mg u pacjentów z utrzymującym się wzrostem aktywności aminotransferaz w surowicy ponad pięciokrotność górnej granicy normy.Należy przerwać stosowanie preparatu SUSTIVA 200 mg, jeśli zwiększeniu aktywności aminotransferaz w surowicy towarzyszą objawy kliniczne zapalenia wątroby lub dekompensacji czynności wątroby.
Drgawki
U dorosłych i dzieci otrzymujących efawirenz obserwowano drgawki, zwykle w przypadku występowania drgawek w wywiadzie [patrz Toksykologia niekliniczna ]. Należy zachować ostrożność u każdego pacjenta z napadami drgawkowymi w wywiadzie. Pacjenci otrzymujący jednocześnie leki przeciwdrgawkowe metabolizowane głównie w wątrobie, takie jak fenytoina i fenobarbital, mogą wymagać okresowego monitorowania stężenia w osoczu [patrz INTERAKCJE Z LEKAMI ].
Elewacje lipidowe
Leczenie preparatem SUSTIVA spowodowało wzrost stężenia całkowitego cholesterolu i triglicerydów [patrz DZIAŁANIA NIEPOŻĄDANE ]. Testy cholesterolu i triglicerydów należy wykonać przed rozpoczęciem leczenia SUSTIVA 200 mg oraz okresowo w trakcie leczenia.
Zespół rekonstytucji immunologicznej
Zespół rekonstytucji immunologicznej zgłaszano u pacjentów leczonych skojarzoną terapią przeciwretrowirusową, w tym SUSTIVA. W początkowej fazie skojarzonego leczenia przeciwretrowirusowego u pacjentów, u których odpowiada układ odpornościowy, może rozwinąć się odpowiedź zapalna na powolne lub resztkowe zakażenia oportunistyczne (takie jak zakażenie Mycobacterium avium, wirus cytomegalii, zapalenie płuc wywołane przez Pneumocystis jiroveci [PCP] lub gruźlica), co może wymagać dalszej oceny i leczenie.
Donoszono również o występowaniu zaburzeń autoimmunologicznych (takich jak choroba Gravesa, zapalenie wielomięśniowe, zespół Guillain-Barré i autoimmunologiczne zapalenie wątroby) w warunkach regeneracji immunologicznej; jednak czas do wystąpienia jest bardziej zmienny i może wystąpić wiele miesięcy po rozpoczęciu leczenia.
Redystrybucja tłuszczu
pacjentów otrzymujących leczenie przeciwretrowirusowe obserwowano redystrybucję/nagromadzenie tkanki tłuszczowej, w tym otyłość centralną, powiększenie tkanki tłuszczowej grzbietowo-szyjkowej (bawole garb), wyniszczenie obwodowe, wyniszczenie twarzy, powiększenie piersi i „wygląd cushingoidalny”. Mechanizm i długofalowe konsekwencje tych wydarzeń nie są obecnie znane. Związek przyczynowy nie został ustalony.
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( INFORMACJA O PACJENCIE oraz Instrukcja użycia ).
Interakcje leków
Oświadczenie skierowane do pacjentów i pracowników służby zdrowia znajduje się na etykietach butelek produktu: UWAGA: Dowiedz się o lekach, których NIE należy przyjmować razem z lekiem SUSTIVA.
SUSTIVA może wchodzić w interakcje z niektórymi lekami; dlatego należy doradzić pacjentom, aby zgłaszali swojemu lekarzowi stosowanie jakichkolwiek innych leków wydawanych na receptę lub bez recepty.
Ogólne informacje dla pacjentów
Poinformuj pacjentów, że SUSTIVA 200 mg nie jest lekarstwem na zakażenie HIV-1 i pacjenci mogą nadal doświadczać chorób związanych z zakażeniem HIV-1, w tym zakażeń oportunistycznych. Podczas przyjmowania leku SUSTIVA pacjenci powinni pozostawać pod opieką lekarza.
Doradź pacjentom, aby unikali robienia rzeczy, które mogą przenosić zakażenie HIV-1 na innych.
- Nie należy udostępniać ani ponownie używać igieł ani innego sprzętu do wstrzykiwań.
- Nie udostępniaj przedmiotów osobistych, które mogą mieć na sobie krew lub płyny ustrojowe, takich jak szczoteczki do zębów i żyletki.
- Nie uprawiaj żadnego seksu bez zabezpieczenia. Zawsze uprawiaj bezpieczniejszy seks, używając prezerwatywy lateksowej lub poliuretanowej, aby zmniejszyć ryzyko kontaktu seksualnego z nasieniem, wydzielinami pochwy lub krwią.
- Nie karmić piersią. Matki z HIV-1 nie powinny karmić piersią, ponieważ HIV-1 może zostać przeniesiony na dziecko w mleku matki.
Instrukcje dotyczące dawkowania
Należy doradzić pacjentom przyjmowanie leku SUSTIVA codziennie, zgodnie z zaleceniami. Jeśli pacjent zapomni o zażyciu leku SUSTIVA, należy powiedzieć mu, aby natychmiast przyjął pominiętą dawkę, chyba że zbliża się pora przyjęcia kolejnej dawki. Poradzić pacjentowi, aby nie przyjmował 2 dawek za jednym razem i przyjął następną dawkę o wyznaczonej porze. Poradź pacjentowi, aby zapytał lekarza, czy potrzebuje pomocy w zaplanowaniu najlepszego czasu na przyjmowanie leku.
SUSTIVA 200mg należy zawsze stosować w połączeniu z innymi lekami przeciwretrowirusowymi. Należy doradzić pacjentom przyjmowanie preparatu SUSTIVA 600 mg na pusty żołądek, najlepiej przed snem. Przyjmowanie preparatu SUSTIVA z jedzeniem zwiększa stężenie efawirenzu i może zwiększać częstość występowania działań niepożądanych. Dawkowanie przed snem może poprawić tolerancję objawów układu nerwowego [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz DZIAŁANIA NIEPOŻĄDANE ]. Pracownicy służby zdrowia powinni pomagać rodzicom lub opiekunom w ustaleniu najlepszego schematu dawkowania SUSTIVA dla niemowląt i małych dzieci.
przypadku pacjentów dorosłych i dzieci, którzy nie mogą połykać kapsułek lub tabletek, należy zalecić pacjentom lub ich opiekunom uważne przeczytanie instrukcji dotyczących podawania zawartości kapsułki w niewielkiej ilości pokarmu lub mieszanki dla niemowląt [patrz DAWKOWANIE I SPOSÓB PODAWANIA i zatwierdzone przez FDA oznakowanie pacjenta ( INFORMACJA O PACJENCIE oraz INSTRUKCJA UŻYCIA )]. Pacjenci powinni skontaktować się z lekarzem lub farmaceutą, jeśli mają jakiekolwiek pytania.
Objawy układu nerwowego
Należy poinformować pacjentów, że objawy ze strony ośrodkowego układu nerwowego (NSS), w tym zawroty głowy, bezsenność, zaburzenia koncentracji, senność i nietypowe sny są często zgłaszane podczas pierwszych tygodni leczenia preparatem SUSTIVA [patrz OSTRZEŻENIA I ŚRODKI ]. Dawkowanie przed snem może poprawić tolerancję tych objawów, które prawdopodobnie ulegną poprawie wraz z kontynuacją leczenia. Ostrzegać pacjentów o potencjalnym działaniu addytywnym, gdy SUSTIVA jest stosowany jednocześnie z alkoholem lub lekami psychoaktywnymi. Poinstruuj pacjentów, że jeśli wystąpią NSS, powinni unikać potencjalnie niebezpiecznych zadań, takich jak prowadzenie pojazdów lub obsługiwanie maszyn.
Należy poinformować pacjentów, że istnieje ryzyko rozwoju neurotoksyczności o późnym początku, w tym ataksji i encefalopatii, które mogą wystąpić miesiące lub lata po rozpoczęciu leczenia SUSTIVA [patrz OSTRZEŻENIA I ŚRODKI ].
Objawy psychiatryczne
Należy poinformować pacjentów, że u pacjentów otrzymujących SUSTIVA zgłaszano poważne objawy psychiczne, w tym ciężką depresję, próby samobójcze, agresywne zachowanie, urojenia, paranoję, objawy psychozopodobne i katatonię [patrz OSTRZEŻENIA I ŚRODKI ]. Jeśli doświadczą poważnych negatywnych doświadczeń psychiatrycznych, powinni natychmiast zgłosić się do lekarza. Doradź pacjentom, aby informowali swojego lekarza o jakiejkolwiek historii choroby psychicznej lub nadużywania substancji.
Wysypka
Poinformuj pacjentów, że częstym działaniem niepożądanym jest wysypka [patrz OSTRZEŻENIA I ŚRODKI ]. Wysypki zwykle ustępują bez zmiany leczenia. Jednakże, ponieważ wysypka może być poważna, należy doradzić pacjentom, aby w przypadku wystąpienia wysypki niezwłocznie skontaktowali się z lekarzem.
Hepatotoksyczność
Poinformuj pacjentów, aby zwracali uwagę na wczesne oznaki zapalenia lub niewydolności wątroby, takie jak zmęczenie, osłabienie, brak apetytu, nudności i wymioty, a także na późniejsze objawy, takie jak żółtaczka, splątanie, obrzęk brzucha i odbarwienie kału, i skonsultowali się z ich pracownik służby zdrowia niezwłocznie, jeśli takie objawy wystąpią [patrz OSTRZEŻENIA I ŚRODKI oraz DZIAŁANIA NIEPOŻĄDANE ].
Kobiety o potencjale rozrodczym
Doradzić kobietom o potencjale rozrodczym stosowanie skutecznej antykoncepcji oraz metody barierowej podczas leczenia preparatem SUSTIVA 600 mg i przez 12 tygodni po odstawieniu preparatu SUSTIVA. Należy doradzić pacjentkom, aby skontaktowały się ze swoim lekarzem, jeśli planują zajść w ciążę, zajść w ciążę lub jeśli podejrzewa się ciążę podczas leczenia lekiem SUSTIVA [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
Rejestr ekspozycji w ciąży
Poinformuj pacjentki, że istnieje rejestr ekspozycji w czasie ciąży, który monitoruje przebieg ciąży u kobiet narażonych na działanie preparatu SUSTIVA podczas ciąży [patrz Używaj w określonych populacjach ].
Redystrybucja tłuszczu
Należy poinformować pacjentów, że u pacjentów otrzymujących terapię przeciwretrowirusową może wystąpić redystrybucja lub akumulacja tkanki tłuszczowej oraz że przyczyna i długoterminowe skutki zdrowotne tych stanów nie są znane [patrz OSTRZEŻENIA I ŚRODKI ].
SUSTIVA jest zastrzeżonym znakiem towarowym firmy Bristol-Myers Squibb Pharma Company. ATRIPLA jest znakiem towarowym firmy Bristol-Myers Squibb & Gilead Sciences, LLC.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Karcynogeneza
Przeprowadzono długoterminowe badania rakotwórczości na myszach i szczurach z użyciem efawirenzu. Myszom podawano 0, 25, 75, 150 lub 300 mg/kg/dzień przez 2 lata. Częstość występowania gruczolaków i raków wątrobowokomórkowych oraz gruczolaków pęcherzyków płucnych/oskrzelików była wyższa u kobiet. U mężczyzn nie zaobserwowano wzrostu częstości występowania guza powyżej tła. Nie ustalono NOAEL u samic dla tego badania, ponieważ zmiany nowotworowe wystąpiły przy wszystkich dawkach. AUC przy NOAEL (150 mg/kg) u samców było około 0,9 razy większe niż u ludzi przy zalecanej dawce klinicznej. W badaniu na szczurach nie zaobserwowano zwiększenia częstości występowania nowotworów przy dawkach do 100 mg/kg/dobę, dla których AUC były 0,1 (mężczyźni) lub 0,2 (samice) razy większe niż u ludzi przy zalecanej dawce klinicznej.
Mutageneza
Efawirenz uzyskał wynik ujemny w szeregu testów genotoksyczności in vitro i in vivo. Obejmowały one testy mutacji bakteryjnych w S. typhimurium i E. coli, testy mutacji ssaków w komórkach jajnika chomika chińskiego, testy aberracji chromosomowych w ludzkich limfocytach krwi obwodowej lub komórkach jajnika chomika chińskiego oraz test mikrojądrowy szpiku kostnego myszy in vivo.
Upośledzenie płodności
Efawirenz nie zaburzał parowania ani płodności samców i samic szczurów oraz nie wpływał na nasienie leczonych samców szczurów. Wydajność reprodukcyjna potomstwa samic szczurów, którym podawano efawirenz nie uległa zmianie. AUC przy wartościach NOAEL u samców (200 mg/kg) i samic (100 mg/kg) szczurów były około ≤0,15 razy większe niż u ludzi przy zalecanej dawce klinicznej.
Używaj w określonych populacjach
Ciąża
Rejestr ekspozycji w ciąży
Istnieje rejestr narażenia na ciążę, który monitoruje przebieg ciąży u kobiet narażonych na działanie preparatu SUSTIVA 600 mg podczas ciąży. Lekarze są zachęcani do rejestrowania pacjentów dzwoniąc do Antiretroviral Pregnancy Registry pod numer 1-800-258-4263.
Podsumowanie ryzyka
Istnieją retrospektywne opisy przypadków wad cewy nerwowej u niemowląt, których matki były narażone na schematy leczenia zawierające efawirenz w pierwszym trymestrze ciąży. Dane prospektywne dotyczące ciąży z Antyretrowirusowego Rejestru Ciąży nie są wystarczające do właściwej oceny tego ryzyka. Dostępne dane z Antyretrowirusowego Rejestru Ciąży nie wykazują różnicy w ryzyku ogólnych poważnych wad wrodzonych w porównaniu z 2,7% odsetkiem głównych wad wrodzonych w amerykańskiej populacji referencyjnej programu Metropolitan Atlanta Congenital Defects Program (MACDP). Chociaż nie ustalono związku przyczynowego między ekspozycją na efawirenz w pierwszym trymestrze a wadami cewy nerwowej, podobne wady rozwojowe obserwowano w badaniach przeprowadzonych na małpach w dawkach podobnych do dawek stosowanych u ludzi. Ponadto u szczurów wystąpiła toksyczność dla płodów i embrionów po dawkach dziesięciokrotnie mniejszych niż ekspozycja u ludzi w zalecanej dawce klinicznej. Ze względu na potencjalne ryzyko wad cewy nerwowej, efawirenzu nie należy stosować w pierwszym trymestrze ciąży. Poinformuj kobiety w ciąży o potencjalnym ryzyku dla płodu.
Dane
Dane ludzkie
Istnieją retrospektywne doniesienia po wprowadzeniu do obrotu o objawach odpowiadających wadom cewy nerwowej, w tym przepuklinie oponowo-rdzeniowej, wszystkie u niemowląt matek narażonych na schematy leczenia zawierające efawirenz w pierwszym trymestrze ciąży.
Na podstawie prospektywnych raportów z Antyretrowirusowego Rejestru Ciąży (APR) około 1000 żywych urodzeń po ekspozycji na schematy zawierające efawirenz (w tym ponad 800 żywych urodzeń narażonych w pierwszym trymestrze), nie stwierdzono różnicy między efawirenzem a ogólnymi wadami wrodzonymi w porównaniu z wskaźnik wad wrodzonych w tle wynosi 2,7% w amerykańskiej populacji referencyjnej programu Metropolitan Atlanta Congenital Defects Program. Według tymczasowego raportu APR opublikowanego w grudniu 2014 r. częstość występowania wad wrodzonych po ekspozycji w pierwszym trymestrze wynosiła 2,3% (95% CI: 1,4%-3,6%). Jedną z tych prospektywnie zgłaszanych wad z ekspozycją w pierwszym trymestrze była wada cewy nerwowej. Prospektywnie zgłoszono również pojedynczy przypadek braku oka z ekspozycją na efawirenz w pierwszym trymestrze ciąży. Przypadek ten obejmował również ciężkie, skośne rozszczepy twarzy i opaski owodniowe, które mają znany związek z brakiem oka.
Dane zwierząt
Wpływ efawirenzu na rozwój zarodka i płodu badano na trzech nieklinicznych gatunkach (małpy cynomolgus, szczury i króliki). U małp efawirenz w dawce 60 mg/kg/dobę podawano ciężarnym samicom przez cały okres ciąży (od 20 do 150 dnia ciąży). Ogólnoustrojowe narażenie matki na lek (AUC) było 1,3 razy większe niż narażenie u ludzi przy zalecanej dawce klinicznej (600 mg/dobę), przy czym stężenie leku w żyle pępowinowej u płodu było około 0,7 razy większe niż u matki. Trzy z 20 płodów/niemowląt miały jedną lub więcej wad rozwojowych; nie było wad rozwojowych płodów ani niemowląt od matek otrzymujących placebo. Wady rozwojowe, które wystąpiły u tych trzech małpich płodów, obejmowały bezmózgowie i jednostronny brak oka u jednego płodu, mikroftalmię u drugiego i rozszczep podniebienia u trzeciego. W tym badaniu nie ustalono poziomu NOAEL (brak widocznego poziomu działań niepożądanych), ponieważ oceniono tylko jedną dawkę. Szczurom efawirenz podawano w trakcie organogenezy (od 7. do 18. dnia ciąży) lub od 7. do 21. dnia laktacji w dawce 50, 100 lub 200 mg/kg/dobę. Podawanie 200 mg/kg/dobę szczurom wiązało się ze wzrostem częstości wczesnych resorpcji; a dawki 100 mg/kg/dobę i większe były związane z wczesną śmiertelnością noworodków. AUC przy NOAEL (50 mg/kg/dobę) w tym badaniu na szczurach było 0,1 razy większe niż u ludzi przy zalecanej dawce klinicznej. Stężenia leku w mleku w 10. dniu laktacji były około 8 razy wyższe niż w osoczu matki. U ciężarnych królików efawirenz nie powodował śmierci zarodków ani działania teratogennego, gdy był podawany w dawkach 25, 50 i 75 mg/kg/dobę w okresie organogenezy (od 6. do 18. dnia ciąży). AUC przy NOAEL (75 mg/kg/dobę) u królików było 0,4 razy większe niż u ludzi przy zalecanej dawce klinicznej.
Laktacja
Podsumowanie ryzyka
Centers for Disease Control and Prevention zaleca, aby matki zakażone wirusem HIV nie karmiły piersią swoich dzieci, aby uniknąć ryzyka przeniesienia wirusa HIV po urodzeniu. Ze względu na możliwość przenoszenia wirusa HIV u niemowląt karmionych piersią, odradzać kobietom karmienie piersią.
Kobiety i mężczyźni o potencjale rozrodczym
Ze względu na potencjalne działanie teratogenne kobietom otrzymującym preparat SUSTIVA należy unikać ciąży. [Widzieć Ciąża .]
Testy ciążowe
Kobiety w wieku rozrodczym powinny przejść testy ciążowe przed rozpoczęciem stosowania preparatu SUSTIVA.
Zapobieganie ciąży
Kobiety w wieku rozrodczym powinny stosować skuteczną antykoncepcję podczas leczenia preparatem SUSTIVA 200 mg oraz przez 12 tygodni po odstawieniu preparatu SUSTIVA 200 mg ze względu na długi okres półtrwania efawirenzu. Antykoncepcję barierową należy zawsze stosować w połączeniu z innymi metodami antykoncepcji. Metody hormonalne zawierające progesteron mogą mieć zmniejszoną skuteczność [patrz INTERAKCJE Z LEKAMI ].
Zastosowanie pediatryczne
Bezpieczeństwo, profil farmakokinetyczny oraz odpowiedź wirusologiczną i immunologiczną produktu SUSTIVA 600 mg oceniano u dzieci i młodzieży w wieku od 3 miesięcy do 21 lat, nie leczonych przeciwretrowirusowo i wcześniej zakażonych wirusem HIV-1, w trzech otwartych badaniach klinicznych [patrz DZIAŁANIA NIEPOŻĄDANE , FARMAKOLOGIA KLINICZNA , oraz Studia kliniczne ]. Rodzaj i częstość działań niepożądanych w tych badaniach były zasadniczo podobne do tych u pacjentów dorosłych, z wyjątkiem częstszego występowania wysypki, w tym wysypki stopnia 3. lub 4., u dzieci w porównaniu z dorosłymi [patrz OSTRZEŻENIA I ŚRODKI oraz DZIAŁANIA NIEPOŻĄDANE ].
Nie zaleca się stosowania preparatu SUSTIVA u pacjentów w wieku poniżej 3 miesięcy LUB o masie ciała mniejszej niż 3,5 kg, ponieważ bezpieczeństwo, farmakokinetyka i działanie przeciwwirusowe preparatu SUSTIVA 600 mg nie zostały ocenione w tej grupie wiekowej i istnieje ryzyko rozwoju oporności na HIV jeśli SUSTIVA jest za mały. Widzieć DAWKOWANIE I SPOSÓB PODAWANIA zalecenia dotyczące dawkowania u dzieci.
Zastosowanie geriatryczne
Badania kliniczne preparatu SUSTIVA 200 mg nie obejmowały wystarczającej liczby osób w wieku 65 lat i starszych, aby ustalić, czy reagują oni inaczej niż osoby młodsze. Ogólnie rzecz biorąc, przy doborze dawki u pacjentów w podeszłym wieku należy zachować ostrożność, odzwierciedlając większą częstość pogorszenia czynności wątroby, nerek lub serca oraz współistniejących chorób lub innych terapii.
Niewydolność wątroby
SUSTIVA nie jest zalecany u pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby, ponieważ nie ma wystarczających danych, aby określić, czy konieczne jest dostosowanie dawki. Pacjenci z łagodnymi zaburzeniami czynności wątroby mogą być leczeni efawirenzem bez jakiejkolwiek modyfikacji dawki. Ze względu na intensywny metabolizm efawirenzu z udziałem cytochromu P450 i ograniczone doświadczenie kliniczne u pacjentów z zaburzeniami czynności wątroby, należy zachować ostrożność przy podawaniu preparatu SUSTIVA tym pacjentom [patrz OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
Niektórzy pacjenci przypadkowo przyjmujący 600 mg dwa razy na dobę zgłaszali nasilenie objawów ze strony układu nerwowego. Jeden pacjent doświadczył mimowolnych skurczów mięśni.
Leczenie przedawkowania produktu SUSTIVA 200 mg powinno obejmować ogólne działania wspomagające, w tym monitorowanie parametrów życiowych i obserwację stanu klinicznego pacjenta. W celu ułatwienia usunięcia niewchłoniętego leku można zastosować węgiel aktywowany. Nie ma swoistego antidotum w przypadku przedawkowania preparatu SUSTIVA. Ponieważ efawirenz silnie wiąże się z białkami, dializa prawdopodobnie nie spowoduje znaczącego usunięcia leku z krwi.
PRZECIWWSKAZANIA
- SUSTIVA jest przeciwwskazany u pacjentów z wcześniej wykazaną klinicznie istotną nadwrażliwością (np. zespół Stevensa-Johnsona, rumień wielopostaciowy lub toksyczne wykwity skórne) na którykolwiek ze składników tego produktu.
- Jednoczesne podawanie efawirenzu z elbaswirem i grazoprewirem jest przeciwwskazane [patrz OSTRZEŻENIA I ŚRODKI oraz INTERAKCJE Z LEKAMI ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Efawirenz jest lekiem przeciwwirusowym [patrz Mikrobiologia ].
Farmakodynamika
Elektrofizjologia serca
Wpływ preparatu SUSTIVA 600 mg na odstęp QTc oceniano w otwartym, kontrolowanym placebo badaniu QT z jedną sekwencją, z kontrolą dodatnią i placebo, obejmującym 3 okresy i 3 dawki, w układzie naprzemiennym, obejmującym 58 zdrowych osób, wzbogacony o polimorfizmy CYP2B6. Średnie Cmax efawirenzu u osób z genotypem CYP2B6 *6/*6 po podawaniu dawki dobowej 600 mg przez 14 dni było 2,25 razy większe od średniego Cmax obserwowanego u osób z genotypem CYP2B6 *1/*1. Zaobserwowano dodatnią zależność między stężeniem efawirenzu a wydłużeniem odstępu QTc. Na podstawie zależności stężenie-QTc średnie wydłużenie odstępu QTc i jego górna granica 90% przedział ufności wynosi 8,7 ms i 11,3 ms u osób z genotypem CYP2B6*6/*6 po podaniu dawki dobowej 600 mg przez 14 dni [patrz OSTRZEŻENIA I ŚRODKI ].
Farmakokinetyka
Wchłanianie
Maksymalne stężenie efawirenzu w osoczu wynoszące 1,6-9,1 μM osiągnięto w ciągu 5 godzin po podaniu pojedynczej dawki doustnej od 100 mg do 1600 mg niezakażonym ochotnikom. Dla dawek do 1600 mg zaobserwowano zależne od dawki zwiększenie Cmax i AUC; wzrosty były mniejsze niż proporcjonalne, co sugeruje zmniejszone wchłanianie przy wyższych dawkach.
U pacjentów zakażonych HIV-1 w stanie stacjonarnym średnie Cmax, średnie Cmin i średnie AUC były proporcjonalne do dawki po dawkach dobowych 200 mg, 400 mg i 600 mg. Czas do osiągnięcia maksymalnego stężenia w osoczu wynosił około 3-5 godzin, a stężenia w osoczu w stanie stacjonarnym były osiągane po 6-10 dniach. U 35 pacjentów otrzymujących SUSTIVA w dawce 600 mg raz na dobę Cmax w stanie stacjonarnym wynosiło 12,9 ± 3,7 μM (średnia ± SD), Cmin w stanie stacjonarnym 5,6 ± 3,2 μM, a AUC 184 ± 73 μM•h.
Wpływ pokarmu na wchłanianie doustne:
Kapsułki
Podanie pojedynczej dawki 600 mg kapsułek efawirenzu z wysokotłuszczowym/wysokokalorycznym posiłkiem (894 kcal, 54 g tłuszczu, 54% kalorii z tłuszczu) lub niskotłuszczowym/normalnie kalorycznym posiłkiem (440 kcal, 2 g tłuszczu, 4% kalorii pochodzących z tłuszczu) wiązało się ze średnim wzrostem AUC∞ efawirenzu o 22% i 17% oraz średnim wzrostem Cmax efawirenzu o odpowiednio 39% i 51% w porównaniu z ekspozycją uzyskaną po podaniu na czczo . [Widzieć DAWKOWANIE I SPOSÓB PODAWANIA oraz INFORMACJA O PACJENCIE .]
Tablety
Podanie pojedynczej tabletki 600 mg efawirenzu z wysokotłuszczowym/wysokokalorycznym posiłkiem (około 1000 kcal, 500-600 kcal z tłuszczu) wiązało się z 28% wzrostem średniej wartości AUC∞ efawirenzu i 79% wzrostem średniej wartości Cmax efawirenzu w stosunku do ekspozycji uzyskanych na czczo. [Widzieć DAWKOWANIE I SPOSÓB PODAWANIA oraz INFORMACJA O PACJENCIE .]
Biodostępność zawartości kapsułki zmieszanej z nośnikami żywności
zdrowych osób dorosłych AUC efawirenzu podawanego jako zawartość trzech kapsułek 200 mg zmieszanych z 2 łyżeczkami niektórych nośników pokarmowych (musu jabłkowego, galaretki winogronowej lub jogurtu lub mieszanki dla niemowląt) spełnia kryteria biorównoważności dla AUC nienaruszonej postaci kapsułki podanej na czczo.
Dystrybucja
Efawirenz w dużym stopniu (około 99,5-99,75%) wiąże się z białkami osocza ludzkiego, głównie z albuminami. U pacjentów zakażonych HIV-1 (n=9), którzy otrzymywali SUSTIVA 200 do 600 mg raz na dobę przez co najmniej jeden miesiąc, stężenie płynu mózgowo-rdzeniowego wahało się od 0,26 do 1,19% (średnio 0,69%) odpowiedniego stężenia w osoczu. Odsetek ten jest około 3-krotnie wyższy niż niezwiązana z białkami (wolna) frakcja efawirenzu w osoczu.
Metabolizm
Badania na ludziach oraz badania in vitro z użyciem mikrosomów wątroby ludzkiej wykazały, że efawirenz jest głównie metabolizowany przez układ cytochromu P450 do hydroksylowanych metabolitów, a następnie glukuronidacji tych hydroksylowanych metabolitów. Te metabolity są zasadniczo nieaktywne wobec HIV-1. Badania in vitro sugerują, że CYP3A i CYP2B6 są głównymi izoenzymami odpowiedzialnymi za metabolizm efawirenzu.
Wykazano, że efawirenz indukuje enzymy CYP, co powoduje indukcję własnego metabolizmu. Wielokrotne dawki 200-400 mg na dobę przez 10 dni skutkowały mniejszym niż przewidywany zakresem kumulacji (niższy o 22-42%) i krótszym końcowym okresem półtrwania wynoszącym 40-55 godzin (okres półtrwania pojedynczej dawki 52-76 godzin ).
Eliminacja
Efawirenz ma końcowy okres półtrwania 52-76 godzin po podaniu pojedynczej dawki i 40-55 godzin po podaniu dawek wielokrotnych. Jednomiesięczne badanie bilansu masy/wydalania przeprowadzono, stosując dawkę 400 mg na dobę z dawką znakowaną C podawaną w dniu 8. Około 14-34% radioznacznika odzyskano w moczu, a 16-61% w kale. . Prawie całe wydalanie z moczem radioznakowanego leku miało postać metabolitów. Efawirenz stanowił większość całkowitej radioaktywności mierzonej w kale.
Specjalne populacje
Pediatryczny
Parametry farmakokinetyczne efawirenzu w stanie stacjonarnym u dzieci zostały przewidziane na podstawie modelu farmakokinetyki populacyjnej i zostały podsumowane w Tabeli 6 według zakresów masy ciała, które odpowiadają zalecanym dawkom.
Płeć i rasa
Wydaje się, że farmakokinetyka efawirenzu u pacjentów jest podobna w przypadku mężczyzn i kobiet oraz w badanych grupach rasowych.
Zaburzenia czynności nerek
Nie badano farmakokinetyki efawirenzu u pacjentów z niewydolnością nerek; jednak mniej niż 1% efawirenzu jest wydalane z moczem w postaci niezmienionej, dlatego wpływ zaburzeń czynności nerek na eliminację efawirenzu powinien być minimalny.
Niewydolność wątroby
Badanie z zastosowaniem dawek wielokrotnych nie wykazało istotnego wpływu na farmakokinetykę efawirenzu u pacjentów z łagodnymi zaburzeniami czynności wątroby (klasa A w skali Childa-Pugha) w porównaniu z grupą kontrolną. Nie było wystarczających danych, aby określić, czy umiarkowane lub ciężkie zaburzenia czynności wątroby (klasa B lub C w skali Child-Pugh) wpływają na farmakokinetykę efawirenzu.
Badania interakcji leków
Wykazano in vivo, że efawirenz powoduje indukcję enzymów wątrobowych, zwiększając w ten sposób biotransformację niektórych leków metabolizowanych przez CYP3A i CYP2B6. Badania in vitro wykazały, że efawirenz hamował izoenzymy CYP 2C9 i 2C19 z wartościami Ki (8,5-17 μM) w zakresie obserwowanych stężeń efawirenzu w osoczu. W badaniach in vitro efawirenz nie hamował CYP2E1 i hamował CYP2D6 i CYP1A2 (wartości Ki 82-160 μM) tylko w stężeniach znacznie przekraczających stężenia osiągane klinicznie. Jednoczesne podawanie efawirenzu z lekami metabolizowanymi głównie przez izoenzymy CYP2C9, CYP2C19, CYP3A lub CYP2B6 może spowodować zmianę stężenia jednocześnie podawanego leku w osoczu. Oczekuje się, że leki indukujące aktywność CYP3A i CYP2B6 będą zwiększać klirens efawirenzu, powodując zmniejszenie stężenia w osoczu.
Badania interakcji leków przeprowadzono z efawirenzem i innymi lekami, które prawdopodobnie będą podawane jednocześnie, lub lekami powszechnie stosowanymi jako sondy do interakcji farmakokinetycznych. Wpływ równoczesnego podawania efawirenzu na Cmax, AUC i Cmin podsumowano w Tabeli 7 (wpływ efawirenzu na inne leki) i Tabeli 8 (wpływ innych leków na efawirenz). Aby uzyskać informacje dotyczące zaleceń klinicznych, zobacz INTERAKCJE Z LEKAMI .
Mikrobiologia
Mechanizm akcji
Efawirenz jest NNRTI wirusa HIV-1. W działaniu efawirenzu pośredniczy głównie niekompetycyjne hamowanie odwrotnej transkryptazy HIV-1. Odwrotna transkryptaza HIV-2 i polimerazy ludzkiego DNA komórkowego α, β, γ i δ nie są hamowane przez efawirenz.
Aktywność przeciwwirusowa w hodowli komórkowej
Stężenie efawirenzu hamującego replikację dzikich szczepów laboratoryjnych i izolatów klinicznych w hodowli komórkowej o 90-95% (EC90-95) wahało się od 1,7 do 25 nM w liniach komórek limfoblastoidalnych, jednojądrzastych komórkach krwi obwodowej (PBMC) i makrofagach /hodowle monocytów. Efawirenz wykazał działanie przeciwwirusowe na klad B i większość izolatów nie należących do kladu B (podtypy A, AE, AG, C, D, F, G, J, N), ale obniżył działanie przeciwwirusowe na wirusy z grupy O. Efawirenz wykazał addytywne działanie przeciwwirusowe bez cytotoksyczności wobec HIV-1 w hodowli komórkowej w połączeniu z NNRTI delawirdyną i newirapiną, NRTI (abakawir, didanozyna, emtrycytabina, lamiwudyna, stawudyna, tenofowir, zalcytabina, zydowudyna), PI, inwirinawirna nelfinawir, rytonawir, sakwinawir) oraz inhibitor fuzji enfuwirtyd. Efawirenz wykazał dodatek do antagonistycznego działania przeciwwirusowego w hodowli komórkowej z atazanawirem. Efawirenz nie działał antagonistycznie w stosunku do adefowiru stosowanego w leczeniu zakażenia wirusem zapalenia wątroby typu B ani rybawiryny stosowanej w skojarzeniu z interferonem w leczeniu zakażenia wirusem zapalenia wątroby typu C.
Opór
hodowli komórkowej
W hodowli komórkowej izolaty HIV-1 o zmniejszonej wrażliwości na efawirenz (>380-krotny wzrost wartości EC90) pojawiały się szybko w obecności leku. Charakterystyka genotypowa tych wirusów zidentyfikowała pojedyncze podstawienia aminokwasowe L100I lub V179D, podwójne podstawienia L100I/V108I i potrójne podstawienia L100I/V179D/Y181C w odwrotnej transkryptazie.
Studia kliniczne
Uzyskano izolaty kliniczne o zmniejszonej wrażliwości w hodowli komórkowej na efawirenz. U pacjentów, u których nie powiodło się leczenie efawirenzem w skojarzeniu z indynawirem lub zydowudyną z lamiwudyną, zaobserwowano jedno lub więcej podstawień w pozycjach aminokwasów 98, 100, 101, 103, 106, 108, 188, 190, 225 i 227 w odwrotnej transkryptazie. Najczęściej obserwowana była substytucja K103N. Długoterminowa obserwacja oporności (średnia 52 tygodnie, zakres 4-106 tygodni) przeanalizowała 28 zgodnych izolatów wyjściowych i niepowodzeń wirusologicznych. Sześćdziesiąt jeden procent (17/28) tych niepowodzeń izolatów miało zmniejszoną wrażliwość na efawirenz w hodowli komórkowej z medianą 88-krotnej zmiany wrażliwości na efawirenz (wartość EC50) w porównaniu z wartością odniesienia. Najczęstszą substytucją NNRTI, która rozwinęła się w tych izolatach pacjentów, była K103N (54%). Inne powstałe podstawienia NNRTI obejmowały L100I (7%), K101E/Q/R (14%), V108I (11%), G190S/T/A (7%), P225H (18%) i M230I/L (11 %).
Opór krzyżowy
Zaobserwowano oporność krzyżową wśród NNRTI. Izolaty kliniczne wcześniej scharakteryzowane jako oporne na efawirenz były również fenotypowo oporne w hodowli komórkowej na delawirdynę i newirapinę w porównaniu ze stanem wyjściowym. Kliniczne izolaty wirusa oporne na delawirdynę i (lub) newirapinę z podstawieniami związanymi z opornością na NNRTI (A98G, L100I, K101E/P, K103N/S, V106A, Y181X, Y188X, G190X, P225H, F227L lub M230L) wykazywały zmniejszoną wrażliwość na efawirenz w hodowli komórkowej. Ponad 90% izolatów klinicznych opornych na NRTI badanych w hodowli komórkowej zachowało wrażliwość na efawirenz.
Toksykologia zwierząt
Nieutrzymujące się drgawki zaobserwowano u 6 z 20 małp otrzymujących efawirenz w dawkach dających wartości AUC w osoczu od 4 do 13 razy większe niż u ludzi otrzymujących zalecaną dawkę [patrz OSTRZEŻENIA I ŚRODKI ].
Studia kliniczne
Dorośli ludzie
Badanie 006 randomizowane, otwarte badanie porównywało SUSTIVA (600 mg raz na dobę) + zydowudyna (ZDV, 300 mg co 12 h) + lamiwudyna (LAM, 150 mg co 12 h) lub SUSTIVA (600 mg raz na dobę) + indynawir (IDV, 1000 mg co 8 h) z indynawirem (800 mg co 8 h) + zydowudyną (300 mg co 12 h) + lamiwudyną (150 mg co 12 h). Do badania włączono dwunastu sześćdziesięciu sześciu pacjentów (średni wiek 36,5 lat [zakres 18-81], 60% rasy kaukaskiej, 83% mężczyzn). Wszyscy pacjenci w momencie rozpoczęcia badania nie byli dotychczas leczeni efawirenzem, lamiwudyną, NNRTI i PI. Mediana wyjściowej liczby komórek CD4+ wynosiła 320 komórek/mm3, a średni początkowy poziom RNA HIV-1 wynosił 4,8 log kopii/ml. Wyniki leczenia standardowym testem (limit testu 400 kopii/ml) do 48 i 168 tygodni przedstawiono w Tabeli 9. Poziomy HIV RNA w osoczu zostały określone ilościowo za pomocą standardowego (limit testu 400 kopii/ml) i ultraczułego (limit testu 50 kopii/ml) wersje testu AMPLICOR HIV-1 MONITOR. Podczas badania w Europie wprowadzono wersję 1.5 testu, aby zwiększyć wykrywalność wirusa niebędącego kladem B.
pacjentów leczonych preparatami SUSTIVA + zydowudyna + lamiwudyna, SUSTIVA + indynawir lub indynawir + zydowudyna + lamiwudyna odsetek osób odpowiadających na leczenie z RNA HIV-1
ACT 364 jest randomizowanym, prowadzonym metodą podwójnie ślepej próby, kontrolowanym placebo, 48-tygodniowym badaniem z udziałem pacjentów doświadczonych w leczeniu NRTI, którzy ukończyli dwa wcześniejsze badania ACTG. Stu dziewięćdziesięciu sześciu pacjentów (średni wiek 41 lat [zakres 18-76], 74% rasy kaukaskiej, 88% mężczyźni) otrzymywało NRTI w skojarzeniu z SUSTIVA (600 mg raz na dobę) lub nelfinawirem (NFV, 750 mg trzy razy na dobę ) lub SUSTIVA (600 mg raz na dobę) + nelfinawir w sposób randomizowany z podwójnie ślepą próbą. Średnia początkowa liczba komórek CD4+ wynosiła 389 komórek/mm3, a średni początkowy poziom RNA HIV-1 wynosił 8130 kopii/ml. Po wejściu do badania wszystkim pacjentom przypisano nowy otwarty schemat leczenia NRTI, który był zależny od ich wcześniejszego doświadczenia w leczeniu NRTI. Nie było znaczącej różnicy w średniej liczbie komórek CD4+ między grupami leczenia; ogólny średni wzrost wyniósł około 100 komórek w 48. tygodniu wśród pacjentów, którzy kontynuowali leczenie według schematów badania. Wyniki leczenia przedstawiono w Tabeli 10. Poziomy HIV RNA w osoczu oznaczono ilościowo za pomocą testu AMPLICOR HIV-1 MONITOR, stosując dolną granicę oznaczalności 500 kopii/ml.
Analiza Kaplana-Meiera dotycząca czasu do niepowodzenia leczenia przez 72 tygodnie wykazuje dłuższy czas trwania supresji wirusologicznej (HIV RNA
Pacjenci pediatryczni
Badanie AI266922 jest badaniem otwartym, mającym na celu ocenę farmakokinetyki, bezpieczeństwa, tolerancji i działania przeciwwirusowego preparatu SUSTIVA 200 mg w skojarzeniu z didanozyną i emtrycytabiną u pacjentów pediatrycznych nieleczonych wcześniej i wcześniej leczonych przeciwretrowirusowo. 37 pacjentów w wieku od 3 miesięcy do 6 lat (mediana 0,7 roku) leczono preparatem SUSTIVA. Na początku mediana RNA HIV-1 w osoczu wynosiła 5,88 log kopii/ml, mediana liczby komórek CD4+ wynosiła 1144 komórek/mm3, a mediana odsetka CD4+ wynosiła 25%. Mediana czasu leczenia w ramach badania wynosiła 60 tygodni; 27% pacjentów przerwało leczenie przed 48. tygodniem. Korzystając z analizy ITT, całkowity odsetek pacjentów z HIV RNA
Badanie PACTG 1021 było badaniem otwartym, mającym na celu ocenę farmakokinetyki, bezpieczeństwa, tolerancji i działania przeciwwirusowego preparatu SUSTIVA 200 mg w skojarzeniu z didanozyną i emtrycytabiną u dzieci i młodzieży nieleczonych wcześniej terapią przeciwretrowirusową. Czterdziestu trzech pacjentów w wieku od 3 miesięcy do 21 lat (mediana 9,6 lat) otrzymało lek SUSTIVA. Na początku mediana RNA HIV-1 w osoczu wynosiła 4,8 log kopii/ml, mediana liczby komórek CD4+ wynosiła 367 komórek/mm3, a mediana odsetka CD4+ wynosiła 18%. Mediana czasu leczenia w ramach badania wyniosła 181 tygodni; 16% pacjentów przerwało leczenie przed 48. tygodniem. Korzystając z analizy ITT, całkowity odsetek pacjentów z HIV RNA
Badanie PACTG 382 było badaniem otwartym, mającym na celu ocenę farmakokinetyki, bezpieczeństwa, tolerancji i działania przeciwwirusowego preparatu SUSTIVA w skojarzeniu z nelfinawirem i NRTI u pacjentów pediatrycznych dotychczas nieleczonych przeciwretrowirusowo i z doświadczeniem NRTI. Sto dwóch pacjentów w wieku od 3 miesięcy do 16 lat (mediana 5,7 lat) leczono preparatem SUSTIVA. Osiemdziesiąt siedem procent pacjentów otrzymywało wcześniej terapię antyretrowirusową. Na początku mediana RNA HIV-1 w osoczu wynosiła 4,57 log kopii/ml, mediana liczby komórek CD4+ wynosiła 755 komórek/mm3, a mediana odsetka CD4+ wynosiła 30%. Mediana czasu leczenia w ramach badania wyniosła 118 tygodni; 25% pacjentów przerwało leczenie przed 48. tygodniem. Korzystając z analizy ITT, całkowity odsetek pacjentów z HIV RNA
INFORMACJA O PACJENCIE
SUSTIVA® (sus-TEE-vah) (efavirenz) kapsułki
SUSTIVA® (sus-TEE-vah) (efawirenz) tabletki
Ważne: Należy zapytać lekarza lub farmaceutę o leki, których nie należy przyjmować z lekiem SUSTIVA. Aby uzyskać więcej informacji, zobacz sekcję „O czym powinienem powiedzieć lekarzowi przed zażyciem leku SUSTIVA?”
Przeczytaj tę Informację dla Pacjenta przed rozpoczęciem stosowania leku SUSTIVA i za każdym razem, gdy otrzymasz uzupełnienie. Mogą pojawić się nowe informacje. Informacje te nie zastępują rozmowy z lekarzem o stanie zdrowia lub leczeniu.
Co to jest SUSTIVA?
SUSTIVA 600 mg jest lekiem na receptę HIV-1 (ludzkim wirusem niedoboru odporności typu 1) stosowanym z innymi lekami przeciwretrowirusowymi w leczeniu zakażenia HIV-1 u dorosłych i dzieci w wieku co najmniej 3 miesięcy i ważących co najmniej 7 funtów 12 uncji (3,5 kg). HIV to wirus wywołujący AIDS (zespół nabytego niedoboru odporności).
Nie wiadomo, czy SUSTIVA jest bezpieczna i skuteczna u dzieci w wieku poniżej 3 miesięcy lub ważących mniej niż 7 funtów i 12 uncji (3,5 kg).
przypadku stosowania z innymi lekami przeciwretrowirusowymi do leczenia zakażenia HIV-1 SUSTIVA 600 mg może pomóc:
- zmniejszyć ilość wirusa HIV-1 we krwi. Nazywa się to obciążeniem wirusem.
- zwiększyć liczbę komórek CD4+ (T) we krwi, które pomagają zwalczać inne infekcje.
Zmniejszenie ilości wirusa HIV-1 i zwiększenie liczby limfocytów CD4+ (T) we krwi może pomóc w poprawie układu odpornościowego. Może to zmniejszyć ryzyko zgonu lub infekcji, które mogą wystąpić w przypadku osłabienia układu odpornościowego (infekcje oportunistyczne).
SUSTIVA 600mg nie leczy zakażenia HIV-1 ani AIDS. Należy kontynuować przyjmowanie leków HIV-1 w celu kontrolowania zakażenia HIV-1 i zmniejszenia chorób związanych z HIV.
Unikaj robienia rzeczy, które mogą przenosić zakażenie HIV-1 na innych:
- Nie należy udostępniać ani ponownie używać igieł ani innego sprzętu do wstrzykiwań.
- Nie udostępniaj przedmiotów osobistych, które mogą mieć na sobie krew lub płyny ustrojowe, takich jak szczoteczki do zębów i żyletki.
- Nie uprawiaj żadnego seksu bez zabezpieczenia. Zawsze uprawiaj bezpieczniejszy seks, używając prezerwatywy lateksowej lub poliuretanowej, aby zmniejszyć ryzyko kontaktu seksualnego z jakimikolwiek płynami ustrojowymi, takimi jak nasienie, wydzieliny pochwy lub krew.
Zapytaj swojego lekarza, jeśli masz jakiekolwiek pytania dotyczące zapobiegania przenoszeniu wirusa HIV na inne osoby.
Kto nie powinien brać SUSTIVA 600mg?
Nie stosować leku SUSTIVA, jeśli pacjent ma uczulenie na efawirenz lub którykolwiek ze składników leku SUSTIVA. Pełna lista składników leku SUSTIVA znajduje się na końcu tej ulotki.
Nie należy przyjmować leku SUSTIVA, jeśli pacjent przyjmuje obecnie elbaswir i grazoprewir (ZEPATIER®).
O czym powinienem powiedzieć lekarzowi przed zażyciem preparatu SUSTIVA 200mg?
Przed przyjęciem leku SUSTIVA należy poinformować lekarza o jakichkolwiek schorzeniach, a w szczególności o:
- mieć chorobę serca
- kiedykolwiek miałeś problem ze zdrowiem psychicznym
- kiedykolwiek zażywałeś narkotyki uliczne lub duże ilości alkoholu
- masz problemy z wątrobą, w tym zakażenie wirusem zapalenia wątroby typu B lub C
- mieć historię napadów
- są w ciąży lub planują zajść w ciążę. SUSTIVA 600 mg może zaszkodzić nienarodzonemu dziecku. Jeśli jesteś w stanie zajść w ciążę, Twój lekarz powinien wykonać test ciążowy przed rozpoczęciem stosowania leku SUSTIVA. Nie należy zachodzić w ciążę podczas przyjmowania leku SUSTIVA i przez 12 tygodni po zakończeniu leczenia lekiem SUSTIVA. Kobiety zdolne do zajścia w ciążę powinny stosować 2 skuteczne formy antykoncepcji w trakcie leczenia i przez 12 tygodni po zakończeniu leczenia preparatem SUSTIVA. Barierową formę kontroli urodzeń należy zawsze stosować wraz z innym rodzajem kontroli urodzeń.
- Barierowe formy kontroli urodzeń mogą obejmować prezerwatywę lateksową lub poliuretanową, gąbkę antykoncepcyjną, diafragmę ze środkiem plemnikobójczym i kapturek naszyjkowy.
- Hormonalne formy kontroli urodzeń, takie jak pigułki antykoncepcyjne, zastrzyki, pierścienie dopochwowe lub implanty, mogą nie działać podczas leczenia lekiem SUSTIVA.
- Porozmawiaj z lekarzem o formach antykoncepcji, które mogą być stosowane podczas leczenia lekiem SUSTIVA.
- Rejestr ciąż. Istnieje rejestr ciąż dla kobiet, które przyjmują leki przeciwretrowirusowe w czasie ciąży. Celem tego rejestru jest zbieranie informacji o stanie zdrowia Twojego i Twojego dziecka. Porozmawiaj ze swoim lekarzem o tym, jak możesz wziąć udział w tym rejestrze.
- Nie należy karmić piersią podczas przyjmowania leku SUSTIVA.
- Nie należy karmić piersią, jeśli jesteś zarażona wirusem HIV ze względu na ryzyko przeniesienia wirusa HIV na dziecko.
Należy poinformować lekarza i farmaceutę o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe.
SUSTIVA 600 mg może wpływać na działanie innych leków, a inne leki mogą wpływać na działanie leku SUSTIVA 600 mg, i może powodować poważne skutki uboczne. W przypadku przyjmowania niektórych leków razem z lekiem SUSTIVA ilość leku SUSTIVA 600 mg w organizmie może być zbyt mała i może nie pomóc w kontrolowaniu zakażenia wirusem HIV. Wirus HIV w organizmie może stać się oporny na SUSTIVA lub inne podobne leki przeciw HIV.
Nie należy przyjmować leku SUSTIVA 600 mg, jeśli pacjent przyjmuje lek ATRIPLA (efawirenz, emtrycytabina, fumaran dizoproksylu tenofowiru), chyba że tak zaleci lekarz.
Należy poinformować lekarza i farmaceutę o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe. Niektóre leki wchodzą w interakcje z lekiem SUSTIVA.
Zachowaj listę swoich leków, aby pokazać je lekarzowi i farmaceucie.
- Możesz poprosić swojego lekarza lub farmaceutę o listę leków, które wchodzą w interakcje z lekiem SUSTIVA.
- Nie należy rozpoczynać przyjmowania nowego leku bez poinformowania lekarza. Lekarz może powiedzieć, czy stosowanie leku SUSTIVA z innymi lekami jest bezpieczne.
Jak powinienem przyjmować SUSTIVA?
- SUSTIVA 600 mg należy przyjmować zgodnie z zaleceniami lekarza.
- Nie należy zmieniać dawki ani przerywać przyjmowania leku SUSTIVA, chyba że tak zaleci lekarz.
- Pozostań pod opieką lekarza podczas leczenia lekiem SUSTIVA.
- SUSTIVA musi być stosowany z innymi lekami przeciwretrowirusowymi.
- SUSTIVA należy przyjmować 1 raz dziennie.
- SUSTIVA występuje w postaci tabletek lub kapsułek.
- Tabletek SUSTIVA nie wolno łamać.
- Tabletki lub kapsułki SUSTIVA należy połykać w całości popijając płynem.
Jak i kiedy przyjmować lek SUSTIVA.
- Należy przyjmować SUSTIVA 600 mg na pusty żołądek przed snem. Przyjmowanie leku SUSTIVA 200mg z jedzeniem zwiększa ilość leku w organizmie. Niektóre działania niepożądane mogą mniej przeszkadzać w przypadku przyjmowania leku SUSTIVA 600 mg na pusty żołądek i przed snem.
- Lekarz dziecka przepisze odpowiednią dawkę SUSTIVA 200 mg w zależności od wagi dziecka.
- W przypadku trudności z połykaniem tabletek lub kapsułek należy poinformować o tym lekarza. Lekarz może zalecić otwarcie kapsułki SUSTIVA i wymieszanie jej zawartości z pokarmem lub mieszanką dla niemowląt. Zapoznaj się ze szczegółową „Instrukcją użycia” na końcu niniejszej Informacji dla pacjenta, aby dowiedzieć się, w jaki sposób należy przyjmować SUSTIVA 600 mg metodą posypywania kapsułek.
- Dorośli i dzieci, które przyjmują SUSTIVA 600mg metodą posypywania kapsułek, nie powinny jeść przez 2 godziny po przyjęciu dawki SUSTIVA.
- Niemowlętom nie należy podawać odżywki dla niemowląt przez 2 godziny po przyjęciu dawki preparatu SUSTIVA metodą posypywania kapsułek.
- Nie przegap żadnej dawki leku SUSTIVA. W przypadku pominięcia dawki leku SUSTIVA należy natychmiast przyjąć pominiętą dawkę, chyba że zbliża się pora przyjęcia kolejnej dawki. Nie należy przyjmować 2 dawek jednorazowo. Po prostu weź kolejną dawkę o wyznaczonej porze. Jeśli potrzebujesz pomocy w zaplanowaniu najlepszego czasu na przyjmowanie leku, zwróć się do lekarza lub farmaceuty.
- W przypadku przyjęcia zbyt dużej dawki leku SUSTIVA należy natychmiast skontaktować się z lekarzem lub udać się na pogotowie ratunkowe najbliższego szpitala.
- Kiedy zapas SUSTIVA 600 mg zacznie się wyczerpywać, uzyskaj więcej od swojego lekarza lub apteki. Ważne, aby nie zabrakło SUSTIVA. Ilość wirusa HIV-1 we krwi może się zwiększyć, jeśli lek zostanie odstawiony nawet na krótki czas. Wirus może stać się oporny na SUSTIVA 600mg i trudniejszy do wyleczenia.
Jakie są możliwe skutki uboczne SUSTIVA?
SUSTIVA 600mg może powodować poważne skutki uboczne, w tym:
Jeśli masz zawroty głowy, problemy z koncentracją lub senność, nie prowadź samochodu, nie używaj maszyn ani nie rób niczego, co wymaga czujności.
Niektóre objawy ze strony układu nerwowego (np. splątanie, powolne myśli i ruchy fizyczne oraz urojenia [fałszywe przekonania] lub halucynacje [widzenie lub słyszenie rzeczy, których inni nie widzą lub nie słyszą]) mogą wystąpić miesiące lub lata po rozpoczęciu leczenia SUSTIVA 600 mg. Niezwłocznie skontaktuj się z lekarzem, jeśli wystąpi którykolwiek z tych objawów.
Należy natychmiast poinformować lekarza, jeśli wystąpi którykolwiek z następujących objawów:
- Poważne problemy ze zdrowiem psychicznym może się zdarzyć u osób, które przyjmują SUSTIVA. Należy natychmiast poinformować lekarza, jeśli wystąpi którykolwiek z następujących objawów:
- czuć się smutnym lub beznadziejnym nie ufać innym ludziom
- odczuwać niepokój lub niepokój, słyszeć lub widzieć rzeczy, które nie są prawdziwe
- myśli o zranieniu siebie (samobójstwie) lub próbie zranienia siebie lub innych osób;
- nie są w stanie normalnie się poruszać ani mówić
- nie potrafią odróżnić tego, co jest prawdziwe, a co fałszywe, a co nierzeczywiste;
- Objawy układu nerwowego są powszechne u osób przyjmujących SUSTIVA 200 mg i mogą być ciężkie. Objawy te zwykle pojawiają się w pierwszym lub drugim dniu leczenia preparatem SUSTIVA 200 mg i zwykle ustępują po 2 do 4 tygodniach leczenia. Niektóre objawy mogą wystąpić od miesięcy do lat po rozpoczęciu leczenia preparatem SUSTIVA. Objawy te mogą się nasilić, jeśli pijesz alkohol, przyjmujesz leki na problemy ze zdrowiem psychicznym lub stosujesz określone leki uliczne podczas leczenia lekiem SUSTIVA. Objawy mogą obejmować:
- zawroty głowy
- problemy z koncentracją
- problemy ze snem
- senność
- niezwykłe sny
- brak koordynacji lub trudności z równowagą
- Wysypka na skórze jest powszechny w przypadku SUSTIVA 600 mg, ale czasami może być ciężki. Wysypka skórna zwykle ustępuje bez zmiany leczenia. Jeśli pojawi się wysypka z którymkolwiek z poniższych objawów, natychmiast poinformuj o tym lekarza:
- wysypka skórna ze świądem lub bez
- peeling skóry
- gorączka
- owrzodzenia jamy ustnej
- obrzęk twarzy
- czerwone lub zaognione oczy, takie jak „różowe oko” (zapalenie spojówek)
- pęcherze lub zmiany skórne
- Problemy z wątrobą, w tym niewydolność wątroby i śmierć może się zdarzyć u osób przyjmujących SUSTIVA. Problemy z wątrobą mogą wystąpić u osób bez historii problemów z wątrobą. Lekarz wykona badania krwi w celu sprawdzenia wątroby przed rozpoczęciem stosowania leku SUSTIVA 200 mg oraz w trakcie leczenia.
- skóra lub biała część oczu zmienia kolor na żółty (żółtaczka)
- nie masz ochoty na jedzenie przez kilka dni lub dłużej
- Twój mocz staje się ciemny
- czujesz mdłości w żołądku (nudności)
- Twoje wypróżnienia (stolce) zmieniają kolor na jasny
- odczuwasz ból w podbrzuszu (brzucha)
- Napady padaczkowe może się zdarzyć u osób przyjmujących SUSTIVA. Napady są bardziej prawdopodobne, jeśli miałeś napady w przeszłości. Należy poinformować lekarza, jeśli wystąpiły napady padaczkowe lub jeśli przyjmuje się leki zapobiegające napadom.
- Zmiany w układzie odpornościowym (zespół rekonstytucji immunologicznej) może się zdarzyć, gdy zaczniesz przyjmować leki na HIV-1. Twój układ odpornościowy może się wzmocnić i zacząć zwalczać infekcje, które przez długi czas były ukryte w twoim ciele. Należy poinformować lekarza, jeśli po rozpoczęciu przyjmowania leku HIV-1 pojawią się nowe objawy.
- Zmiany w tkance tłuszczowej może się zdarzyć u osób przyjmujących lek na HIV-1. Zmiany te mogą obejmować zwiększoną ilość tłuszczu w górnej części pleców i szyi ("bawole garb"), piersi i wokół głównej części ciała (tułów). Może również wystąpić utrata tłuszczu z nóg, ramion i twarzy. Przyczyna i długoterminowe skutki zdrowotne tych stanów nie są znane.
Do najczęstszych skutków ubocznych SUSTIVA 600mg należą:
- wysypka
- nienormalne sny
- zawroty głowy
- zmęczenie
- mdłości
- problemy ze snem
- ból głowy
- wymioty
- Trudności z koncentracją
U niektórych pacjentów przyjmujących lek SUSTIVA wystąpił podwyższony poziom lipidów (cholesterolu i trójglicerydów) we krwi. Należy poinformować lekarza, jeśli wystąpią jakiekolwiek objawy niepożądane, które Cię niepokoją lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne SUSTIVA. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać SUSTIVA?
- Przechowuj kapsułki i tabletki SUSTIVA w temperaturze pokojowej między 68 ° F do 77 ° F (20 ° C do 25 ° C).
Lek SUSTIVA i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Ogólne informacje o SUSTIVA
Czasami leki są przepisywane do celów innych niż wymienione w ulotce informacyjnej dla pacjenta. Nie należy stosować leku SUSTIVA 600mg w przypadku schorzenia, na które nie został przepisany. Nie podawaj SUSTIVA 600mg innym osobom, nawet jeśli mają takie same objawy jak Ty. Może im to zaszkodzić.
Jeśli chcesz uzyskać więcej informacji, porozmawiaj ze swoim lekarzem. Możesz poprosić farmaceutę lub lekarza o informacje o SUSTIVA, które są przeznaczone dla pracowników służby zdrowia. Aby uzyskać więcej informacji, odwiedź stronę www.sustiva.com lub zadzwoń pod numer 1-800-321-1335.
Jakie są składniki SUSTIVA?
Składnik czynny: efawirenz
Nieaktywne składniki:
Kapsułki SUSTIVA 600mg: monohydrat laktozy, stearynian magnezu, laurylosiarczan sodu i glikolan sodowy skrobi. Otoczka kapsułki zawiera żelatynę, laurylosiarczan sodu, dwutlenek tytanu i/lub żółty tlenek żelaza. Otoczka kapsułki może również zawierać dwutlenek krzemu. Kapsułki są nadrukowane tuszem zawierającym błękit karminowy 40, błękit FD&C nr 2 i dwutlenek tytanu.
Tabletki SUSTIVA: kroskarmeloza sodowa, hydroksypropyloceluloza, laktoza jednowodna, stearynian magnezu, celuloza mikrokrystaliczna i laurylosiarczan sodu. Powłoka tabletki zawiera Opadry Yellow i Opadry Clear. Tabletki są polerowane woskiem Carnauba i nadrukowane fioletowym tuszem, Opacode WB.
Niniejsza informacja dla pacjenta została zatwierdzona przez amerykańską Agencję ds. Żywności i Leków.
Instrukcja użycia
SUSTIVA® (sus-TEE-vah) (efavirenz) kapsułki
Przygotowanie dawki SUSTIVA 600mg metodą posypania kapsułkami
Przeczytaj tę instrukcję użycia przed przygotowaniem pierwszej dawki preparatu SUSTIVA zmieszanego z pokarmem lub mieszanką dla niemowląt metodą posypywania kapsułek, za każdym razem po uzupełnieniu i w razie potrzeby. Mogą pojawić się nowe informacje. Informacje te nie zastępują rozmowy z lekarzem o stanie zdrowia lub leczeniu. W przypadku jakichkolwiek pytań dotyczących sposobu mieszania lub podawania dawki preparatu SUSTIVA 200mg należy zwrócić się do lekarza lub farmaceuty, stosując metodę posypywania kapsułek.
Ważna informacja:
- Więcej informacji na temat kapsułek SUSTIVA 600 mg można znaleźć w ulotce informacyjnej dla pacjenta.
- Metoda posypywania kapsułek do mieszania zawartości kapsułek SUSTIVA z pokarmem miękkim lub odżywką dla niemowląt może być stosowana u dorosłych lub dzieci, które nie mogą połykać kapsułek lub tabletek.
- Należy przyjmować SUSTIVA 600 mg na pusty żołądek przed snem.
- Nie należy jeść przez 2 godziny po zażyciu preparatu SUSTIVA zmieszanego z jedzeniem.
- Niemowlęta, które są na tyle duże, aby połykać pokarm, należy podawać SUSTIVA metodą posypywania kapsułek zmieszanych z pokarmem zamiast z mieszanką dla niemowląt.
- Porozmawiaj ze swoim lekarzem, aby pomóc w ustaleniu najlepszego harmonogramu podawania dziecku SUSTIVA zmieszanego z mieszanką dla niemowląt metodą posypywania kapsułek.
Przygotowanie dawki SUSTIVA 600mg wymieszanej z karmą metodą posypywania kapsułek.
Zanim przygotujesz dawkę SUSTIVA 200mg wymieszaną z jedzeniem metodą posypywania kapsułek, zbierz następujące zapasy:
- papierowe ręczniki
- łyżeczka do odmierzania
- mała łyżeczka do mieszania i karmienia
- mały czysty pojemnik (taki jak mały kubek lub miska)
- miękkie jedzenie, takie jak mus jabłkowy, galaretka winogronowa lub jogurt
Krok 1. Wybierz czystą, płaską powierzchnię roboczą. Połóż czysty ręcznik papierowy na powierzchni roboczej. Następnie umieść pozostałe materiały na ręczniku papierowym.
Krok 2. Dobrze umyj i osusz ręce.
Krok 3. Umieść 1 do 2 łyżeczek miękkiej żywności, takiej jak mus jabłkowy, galaretka winogronowa lub jogurt w małym pojemniku (patrz Rysunek A ). Kolor i grubość pokarmu mogą ulec zmianie po zmieszaniu z lekiem.
Rysunek A
Krok 4. Kapsułki SUSTIVA 200mg składają się z 2 części. Spójrz na kapsułkę SUSTIVA, aby zobaczyć, która część kapsułki zachodzi na drugą część (patrz Rysunek B ).
Rysunek B
Krok 5. Trzymaj kapsułkę SUSTIVA w pozycji bocznej (poziomej) bezpośrednio nad pojemnikiem z żywnością. Trzymaj każdy koniec kapsułki SUSTIVA między kciukami a palcami wskazującymi (patrz Rysunek C ).
Rysunek C
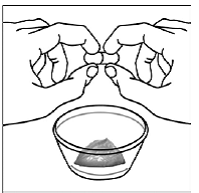
Krok 6. Za pomocą kciuka i palca wskazującego uszczypnąć koniec nakładającej się części kapsułki SUSTIVA 600 mg (patrz Rysunek D ).
Rysunek D
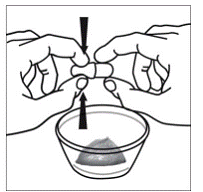
Następnie ostrożnie przekręć oba końce kapsułki SUSTIVA 600 mg w przeciwnych kierunkach, aby ją otworzyć (patrz Rysunek E ). Uważaj, aby nie rozlać zawartości kapsułki ani nie rozsypać jej w powietrzu.
Rysunek E

Krok 7. Wysyp zawartość kapsułki SUSTIVA na pokarm (patrz Rysunek F ).
- Sprawdź otoczki kapsułek, aby upewnić się, że są puste.
- Wyrzuć puste otoczki kapsułek.
Rysunek F

Jeśli całkowita przepisana dawka wynosi więcej niż 1 kapsułkę, należy wykonać kroki od 4 do 7 dla każdej kapsułki. Nie dodawaj więcej jedzenia.
Należy wykonać kroki od 8 do 11 w ciągu 30 minut mieszania leku (patrz Rysunek G ).
Rysunek G

Krok 8. Użyj małej łyżeczki, aby delikatnie wymieszać zawartość kapsułki z jedzeniem (patrz Rysunek H ). Posypki nie rozpuszczają się. Mieszanka będzie wyglądać ziarnisto, ale nie powinna być grudkowata.
Rysunek H
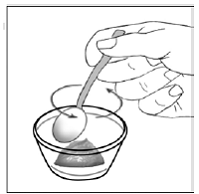
Krok 9. Użyj małej łyżeczki, aby podać lub wziąć mieszankę pokarmu i zawartości kapsułki. Upewnij się, że cała mieszanka została połknięta.
Krok 10. Dodaj około 2 łyżeczki więcej jedzenia do pustego pojemnika i delikatnie wymieszaj małą łyżeczką, aby wymieszać z zawartością kapsułek, która może nadal znajdować się w pojemniku.
Krok 11. Użyj małej łyżeczki, aby podać lub wziąć mieszankę pokarmu i zawartości kapsułki. Upewnij się, że cała mieszanina została połknięta.
Krok 12. Umyj pojemnik i łyżki. Wyrzuć ręcznik papierowy i wyczyść powierzchnię roboczą. Umyj ręce.
Przygotowanie dawki SUSTIVA 600mg zmieszanej z odżywką dla niemowląt metodą posypywania kapsułek
Aby upewnić się, że dziecko otrzyma cały lek, nie należy podawać dziecku zawartości kapsułek SUSTIVA w butelce.
Zanim przygotujesz porcję preparatu SUSTIVA wymieszanego z mieszanką dla niemowląt metodą posypywania kapsułek, zbierz następujące zapasy:
- papierowe ręczniki
- łyżeczka do mieszania i odmierzania
- mały czysty pojemnik (taki jak mały filiżanka lub miska) (patrz Rysunek I ).
- 10 ml strzykawka do podawania doustnego (należy zapytać o to farmaceutę) (patrz Rysunek I ).
- mieszanka dla niemowląt w temperaturze pokojowej.
Rysunek I
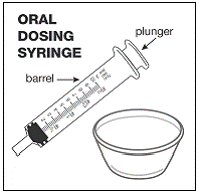
Krok 1. Przygotuj odżywkę dla niemowląt zgodnie ze wskazówkami na opakowaniu odżywki dla niemowląt. Do podania leku zużyjesz około 1 uncji formuły. Resztki preparatu nie należy podawać dziecku przez 2 godziny.
Krok 2. Wybierz czystą, płaską powierzchnię roboczą. Połóż czysty ręcznik papierowy na powierzchni roboczej. Umieść potrzebne materiały na ręczniku papierowym.
Krok 3. Dobrze umyj i osusz ręce.
Krok 4. Wlej 2 łyżeczki mieszanki dla niemowląt o temperaturze pokojowej do pojemnika (patrz Rysunek J ).
Rysunek J
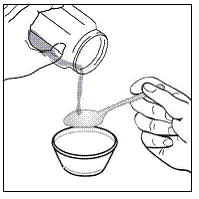
Krok 5. Kapsuła SUSTIVA składa się z 2 części. Spójrz na kapsułkę SUSTIVA, aby zobaczyć, która część kapsułki zachodzi na drugą część (patrz Rysunek K ).
Rysunek K
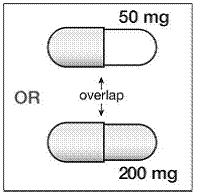
Krok 6. Trzymaj kapsułkę SUSTIVA w pozycji bocznej (poziomej) bezpośrednio nad pojemnikiem z mieszanką dla niemowląt. Trzymaj każdy koniec kapsułki SUSTIVA 600 mg między kciukami a palcami wskazującymi (patrz Rysunek L ).
Rysunek L
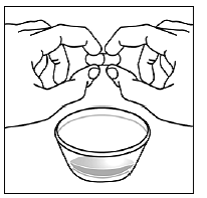
Krok 7. Za pomocą kciuka i palca wskazującego uszczypnąć koniec nakładającej się części kapsułki SUSTIVA (patrz Rysunek M ).
Rysunek M
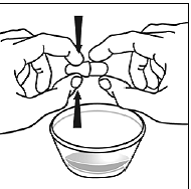
Następnie ostrożnie przekręć oba końce kapsułki SUSTIVA w przeciwnych kierunkach, aby ją otworzyć (patrz Rysunek N ). Uważaj, aby nie rozlać zawartości kapsułki ani nie rozsypać jej w powietrzu.
Rysunek N
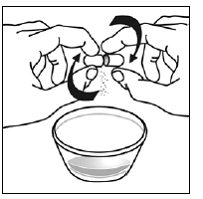
Krok 8. Wysyp zawartość kapsułki SUSTIVA 600 mg na mieszankę dla niemowląt (patrz Postać O ).
- Sprawdź otoczki kapsułek, aby upewnić się, że są puste.
- Wyrzuć puste otoczki kapsułek.
Postać O
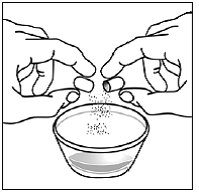
Jeśli całkowita przepisana dawka wynosi więcej niż 1 kapsułkę, należy wykonać kroki od 5 do 8 dla każdej kapsułki. Nie dodawaj więcej mieszanki dla niemowląt.
Należy wykonać kroki od 9 do 12 w ciągu 30 minut mieszania leku (patrz Rysunek P ).
Rysunek P

Krok 9. Trzymaj pojemnik jedną ręką. Drugą ręką użyj łyżeczki do delikatnego wymieszania zawartości kapsułki i mieszanki dla niemowląt (patrz Rysunek Q ). Posypki nie rozpuszczają się. Mieszanka będzie wyglądać ziarnisto, ale nie powinna być grudkowata.
Rysunek Q
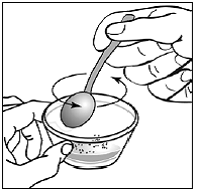
Krok 10. Aby pobrać całą mieszaninę do doustnej strzykawki dozującej:
Rysunek R
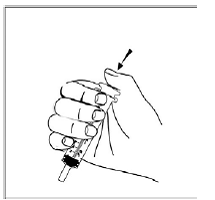
Rysunek S
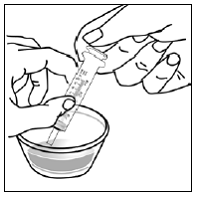
Rysunek T
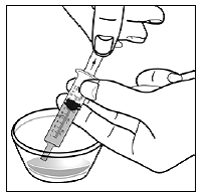
- Sprawdź, czy tłok jest całkowicie wciśnięty w cylinder strzykawki (patrz Rysunek R ).
- Umieścić końcówkę strzykawki w mieszaninie w pojemniku (patrz Rysunek S ).
- Powoli odciągnąć tłok i pobrać całą mieszaninę (patrz Rysunek T ).
Krok 11. Umieść końcówkę strzykawki w buzi dziecka wzdłuż wewnętrznego policzka (patrz Rysunek U ). Powoli naciskaj tłoczek, aby podać dziecku całą mieszankę.
Rysunek U
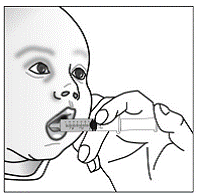
Krok 12. Aby upewnić się, że całe lekarstwo zostało podane dziecku:
- Powtórz krok 4 powyżej.
- Wymieszać łyżeczką.
- Następnie powtórz Kroki 10 i 11 powyżej (Widzieć Rysunek V ).
Rysunek V
Krok 13. Wyjąć tłok z doustnej strzykawki dozującej. Umyj pojemnik, łyżeczkę i strzykawkę doustną. Poczekać, aż tłok i cylinder strzykawki wyschną przed ponownym złożeniem.
Krok 14. Wyrzuć ręcznik papierowy i wyczyść powierzchnię roboczą. Umyj ręce.
Jak przechowywać kapsułki SUSTIVA 600mg?
- Przechowuj kapsułki SUSTIVA w temperaturze pokojowej między 68 ° F do 77 ° F (20 ° C do 25 ° C).
Kapsułki SUSTIVA 600 mg i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Niniejsza instrukcja użytkowania została zatwierdzona przez amerykańską Agencję ds. Żywności i Leków.
