Ditropan 2.5mg, 5mg Oxybutynin Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Ditropan i jak się go stosuje?
Ditropan to lek na receptę stosowany w leczeniu objawów nadreaktywnego pęcherza moczowego. Ditropan 5 mg może być stosowany samodzielnie lub z innymi lekami.
Ditropan należy do klasy leków zwanych środkami przeciwskurczowymi, moczowymi.
Nie wiadomo, czy Ditropan jest bezpieczny i skuteczny u dzieci w wieku poniżej 5 lat.
Jakie są możliwe skutki uboczne Ditropanu?
Ditropan może powodować poważne skutki uboczne, w tym:
- silny ból brzucha,
- zaparcie,
- rozmazany obraz,
- widzenie tunelowe,
- ból oka,
- widząc aureole wokół świateł,
- małe lub brak oddawania moczu,
- bolesne lub utrudnione oddawanie moczu,
- uczucie pragnienia lub gorąca,
- niemożność oddania moczu,
- silne pocenie się i
- gorąca i sucha skóra
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Ditropanu to:
- zawroty głowy,
- senność,
- rozmazany obraz,
- suchość w ustach,
- biegunka i
- zaparcie
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Ditropanu. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
Każda tabletka z linią podziału, obustronnie wypukła, grawerowana w kolorze niebieskim DITROPAN® (chlorek oksybutyniny) zawiera 5 mg chlorku oksybutyniny. Chemicznie, chlorek oksybutyniny to chlorowodorek fenylocykloheksyloglikolanu d,l (racemiczny) 4-dietyloamino-2-butynylu. The
empiryczny wzór chlorku oksybutyniny to C22H31NO3•HCl. Wzór strukturalny znajduje się poniżej:
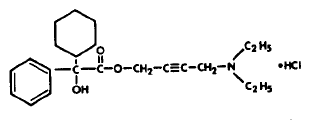
Chlorek oksybutyniny jest białym krystalicznym ciałem stałym o masie cząsteczkowej 393,9. Jest łatwo rozpuszczalny w wodzie i kwasach, ale stosunkowo nierozpuszczalny w alkaliach.
Tabletki DITROPAN zawierają również stearynian wapnia, FD&C Blue #1 Lake, laktozę i celulozę mikrokrystaliczną.
Tabletki DITROPAN są przeznaczone do podawania doustnego.
Kategoria terapeutyczna: przeciwskurczowe, przeciwcholinergiczne.
WSKAZANIA
DITROPAN 2,5 mg XL® (chlorek oksybutyniny) jest antagonistą receptora muskarynowego wskazanym w leczeniu nadreaktywnego pęcherza moczowego z objawami nietrzymania moczu z parcia, parcia naglącego i częstego.
DITROPAN XL® jest również wskazany do leczenia pacjentów pediatrycznych w wieku 6 lat i starszych z objawami nadczynności wypieracza związanego ze stanem neurologicznym (np. rozszczep kręgosłupa).
DAWKOWANIE I SPOSÓB PODAWANIA
DITROPAN 2,5 mg XL® należy połykać w całości, popijając płynem i nie wolno go żuć, dzielić ani kruszyć.
DITROPAN XL® może być podawany z jedzeniem lub bez jedzenia.
Dorośli ludzie
Zalecana dawka początkowa leku DITROPAN 5 mg XL® wynosi 5 lub 10 mg raz na dobę, mniej więcej o tej samej porze każdego dnia. Dawkowanie można dostosowywać w krokach co 5 mg, aby osiągnąć równowagę skuteczności i tolerancji (maksymalnie do 30 mg/dobę). Zasadniczo dostosowanie dawki może następować w przybliżeniu w odstępach tygodniowych.
Pacjenci pediatryczni w wieku 6 lat i starsi
Zalecana dawka początkowa leku DITROPAN 5 mg XL® wynosi 5 mg raz na dobę, w przybliżeniu o tej samej porze każdego dnia. Dawkowanie można dostosowywać w krokach co 5 mg, aby osiągnąć równowagę skuteczności i tolerancji (maksymalnie do 20 mg/dobę).
JAK DOSTARCZONE
Formy dawkowania i mocne strony
DITROPAN 5mg XL® tabletki o przedłużonym uwalnianiu są dostępne w postaci tabletek 5 i 10 mg do stosowania doustnego:
5 mg Bladożółta, okrągła tabletka z czarnym tuszem nadrukowanym po jednej stronie „5 XL”.
10 mg Różowa, okrągła tabletka z nadrukiem „10 XL” na jednej stronie czarnym tuszem.
Składowania i stosowania
DITROPAN XL® tabletki o przedłużonym uwalnianiu są dostępne w dwóch mocach dawkowania, 5 mg (jasnożółty) i 10 mg (różowy) i mają na jednej stronie nadruk „5 XL” lub „10 XL” z czarnym tuszem. Tabletki o przedłużonym uwalnianiu DITROPAN XL® są dostarczane w butelkach po 100 tabletek.
Magazynowanie
Przechowywać w 25°C (77°F); wycieczki dozwolone do 15-30°C (59-86°F) [patrz Temperatura pokojowa kontrolowana przez USP ]. Chronić przed wilgocią i wilgocią.
Trzymać poza zasięgiem dzieci.
Producent: ALZA Corporation, Vacaville, CA 95688, Produkt technologiczny ALZA OROS. Wyprodukowano dla: Janssen Pharmaceuticals, Inc., Titusville, NJ 08560. Aktualizacja: wrzesień 2019 r.
SKUTKI UBOCZNE
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce klinicznej.
Bezpieczeństwo i skuteczność preparatu DITROPAN 2,5 mg XL® (5 do 30 mg/dzień) oceniono u 774 dorosłych pacjentów, którzy uczestniczyli w pięciu podwójnie ślepych, kontrolowanych badaniach klinicznych. W czterech z pięciu badań Ditropan 5 mg IR (5 do 20 mg/dobę u 199 pacjentów) był aktywnym lekiem porównawczym. Działania niepożądane zgłaszane przez ≥ 1% uczestników przedstawiono w Tabeli 1.
Odsetek przerwania leczenia z powodu działań niepożądanych wyniósł 4,4% w przypadku preparatu DITROPAN XL® w porównaniu do 0% w przypadku preparatu Ditropan IR. Najczęstszym działaniem niepożądanym powodującym odstawienie badanego leku była suchość w ustach (0,7%).
Następujące działania niepożądane były zgłaszane przez Zaburzenia metabolizmu i odżywiania: anoreksja, zatrzymanie płynów; Zaburzenia naczyniowe: uderzenie gorąca; Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia: dysfonia; Zaburzenia żołądkowo-jelitowe: dysfagia, częste wypróżnienia; Zaburzenia ogólne i stany w miejscu podania: dyskomfort w klatce piersiowej, pragnienie.
Doświadczenie postmarketingowe
Następujące dodatkowe działania niepożądane zostały zgłoszone na podstawie ogólnoświatowych doświadczeń po wprowadzeniu preparatu DITROPAN 5 mg XL® do obrotu. Ponieważ reakcje po wprowadzeniu do obrotu zgłaszane są dobrowolnie z populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Infekcje i infestacje: Zakażenie dróg moczowych; Zaburzenia psychiczne: zaburzenia psychotyczne, pobudzenie, stan splątania, omamy, zaburzenia pamięci, nieprawidłowe zachowanie; Zaburzenia układu nerwowego: drgawki; Zaburzenia oka: jaskra; Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia: zatkany nos; Zaburzenia serca: arytmia, tachykardia, kołatanie serca, wydłużenie odstępu QT; Zaburzenia naczyniowe: uderzenia gorąca, nadciśnienie; Zaburzenia skóry i tkanki podskórnej: wysypka; Zaburzenia nerek i dróg moczowych: impotencja; Ogólne Zaburzenia i Warunki Miejsca Administracji: reakcje nadwrażliwości, w tym obrzęk naczynioruchowy z niedrożnością dróg oddechowych, pokrzywką i obrzękiem twarzy; reakcje anafilaktyczne wymagające hospitalizacji w celu leczenia doraźnego; Urazy, zatrucia i powikłania po zabiegach: upadek.
Dodatkowe działania niepożądane zgłaszane w przypadku niektórych innych preparatów chlorku oksybutyniny obejmują: cykloplegię, rozszerzenie źrenic i zahamowanie laktacji. W jednym zgłoszonym przypadku jednoczesne stosowanie oksybutyniny z karbamazepiną i dantrolenem wiązało się z wystąpieniem działań niepożądanych w postaci wymiotów, senności, splątania, chwiejności, niewyraźnej mowy i oczopląsu, co wskazywało na toksyczność karbamazepiny.
INTERAKCJE Z LEKAMI
Jednoczesne stosowanie oksybutyniny z innymi lekami antycholinergicznymi lub innymi środkami powodującymi suchość w ustach, zaparcia, senność (senność) i (lub) inne działania antycholinergiczne może zwiększyć częstość i (lub) nasilenie takich działań.
Leki antycholinergiczne mogą potencjalnie zmieniać wchłanianie niektórych jednocześnie podawanych leków ze względu na działanie antycholinergiczne na motorykę przewodu pokarmowego. Może to stanowić problem w przypadku leków o wąskim indeksie terapeutycznym. Środki antycholinergiczne mogą również antagonizować działanie środków prokinetycznych, takich jak metoklopramid.
Średnie stężenia oksybutyniny w osoczu były około 2 razy wyższe, gdy DITROPAN 5 mg XL® podawano z ketokonazolem, silnym inhibitorem CYP3A4. Inne inhibitory układu enzymatycznego cytochromu P450 3A4, takie jak środki przeciwgrzybicze (np. itrakonazol i mikonazol) lub antybiotyki makrolidowe (np. erytromycyna i klarytromycyna), mogą zmieniać średnie parametry farmakokinetyczne oksybutyniny (tj. Cmax i AUC). Znaczenie kliniczne takich potencjalnych interakcji nie jest znane. Należy zachować ostrożność podczas jednoczesnego podawania takich leków.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Obrzęk naczynioruchowy
Podczas stosowania oksybutyniny zgłaszano obrzęk naczynioruchowy twarzy, warg, języka i (lub) krtani. W niektórych przypadkach obrzęk naczynioruchowy wystąpił po pierwszej dawce. Obrzęk naczynioruchowy związany z obrzękiem górnych dróg oddechowych może zagrażać życiu. W przypadku zajęcia języka, gardła dolnego lub krtani należy niezwłocznie przerwać podawanie oksybutyniny i niezwłocznie zastosować odpowiednie leczenie i/lub środki niezbędne do zapewnienia drożności dróg oddechowych.
Skutki dla centralnego układu nerwowego
Oksybutynina ma działanie antycholinergiczne na ośrodkowy układ nerwowy (OUN) [patrz DZIAŁANIA NIEPOŻĄDANE ]. Zgłaszano różne działania antycholinergiczne na OUN, w tym halucynacje, pobudzenie, splątanie i senność. Pacjentów należy monitorować pod kątem objawów działania antycholinergicznego na OUN, szczególnie w ciągu pierwszych kilku miesięcy po rozpoczęciu leczenia lub zwiększeniu dawki. Doradź pacjentom, aby nie prowadzili pojazdów ani nie obsługiwali ciężkich maszyn, dopóki nie dowiedzą się, jak DITROPAN XL® na nich wpływa. Jeśli u pacjenta wystąpi działanie antycholinergiczne na OUN, należy rozważyć zmniejszenie dawki lub odstawienie leku.
DITROPAN XL® należy stosować ostrożnie u pacjentów z wcześniej istniejącym otępieniem leczonych inhibitorami cholinesterazy ze względu na ryzyko nasilenia objawów.
DITROPAN XL® należy stosować ostrożnie u pacjentów z chorobą Parkinsona ze względu na ryzyko nasilenia objawów.
Pogorszenie objawów miastenii Gravis
DITROPAN XL® należy stosować ostrożnie u pacjentów z miastenią ze względu na ryzyko nasilenia objawów.
Pogorszenie objawów zmniejszonej motoryki przewodu pokarmowego u pacjentów z neuropatią autonomiczną
DITROPAN 2,5 mg XL® należy stosować ostrożnie u pacjentów z neuropatią autonomiczną ze względu na ryzyko nasilenia objawów zmniejszonej motoryki przewodu pokarmowego.
Zatrzymanie moczu
DITROPAN 5 mg XL® należy podawać ostrożnie pacjentom z klinicznie istotną niedrożnością odpływu moczu z pęcherza, ze względu na ryzyko zatrzymania moczu [patrz PRZECIWWSKAZANIA ].
Działania niepożądane ze strony przewodu pokarmowego
DITROPAN 2,5 mg XL® należy podawać ostrożnie pacjentom z zaburzeniami obturacyjnymi przewodu pokarmowego ze względu na ryzyko zatrzymania żołądka [patrz PRZECIWWSKAZANIA ].
DITROPAN XL®, podobnie jak inne leki antycholinergiczne, może zmniejszać motorykę przewodu pokarmowego i należy go stosować ostrożnie u pacjentów z takimi stanami jak wrzodziejące zapalenie jelita grubego i atonia jelit.
DITROPAN 2,5 mg XL® należy stosować ostrożnie u pacjentów z refluksem żołądkowo-przełykowym i/lub przyjmujących jednocześnie leki (takie jak bisfosfoniany), które mogą powodować lub zaostrzać zapalenie przełyku.
Podobnie jak w przypadku każdego innego nieodkształcalnego materiału, należy zachować ostrożność przy podawaniu DITROPAN XL® pacjentom z istniejącym wcześniej ciężkim zwężeniem przewodu pokarmowego (patologicznym lub jatrogennym). Istnieją rzadkie doniesienia o objawach obturacyjnych u pacjentów ze znanymi zwężeniami w związku z przyjmowaniem innych leków w postaciach o kontrolowanym uwalnianiu, które nie ulegają deformacji.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
24-miesięczne badanie na szczurach przy dawkach chlorku oksybutyniny 20, 80 i 160 mg/kg/dobę nie wykazało dowodów na działanie rakotwórcze. Dawki te są około 6, 25 i 50 razy większe od maksymalnej ekspozycji u ludzi, w oparciu o równoważną dawkę u ludzi, z uwzględnieniem normalizacji powierzchni ciała.
Chlorek oksybutyniny nie wykazywał wzrostu aktywności mutagennej w testach na Schizosaccharomyces pompholiciformis, Saccharomyces cerevisiae i Salmonella typhimurium.
Badania reprodukcji z chlorkiem oksybutyniny na myszach, szczurach, chomikach i królikach nie wykazały zaburzeń płodności.
Używaj w określonych populacjach
Ciąża
Ciąża Kategoria B
Nie ma odpowiednich i dobrze kontrolowanych badań z zastosowaniem DITROPAN 5mg XL® u kobiet w ciąży. DITROPAN XL® powinien być stosowany w okresie ciąży tylko wtedy, gdy potencjalne korzyści dla pacjentki przewyższają ryzyko dla pacjentki i płodu. Kobiety, które zajdą w ciążę podczas leczenia preparatem DITROPAN XL®, zachęca się do kontaktu z lekarzem.
Podsumowanie ryzyka
Na podstawie danych na zwierzętach przewiduje się, że oksybutynina ma małe prawdopodobieństwo zwiększenia ryzyka niekorzystnych skutków rozwojowych ponad ryzyko podstawowe.
Dane zwierząt
Badania reprodukcji z chlorkiem oksybutyniny na myszach, szczurach, chomikach i królikach nie wykazały zaburzeń płodności lub uszkodzenia płodu zwierzęcego.
Matki karmiące
Nie wiadomo, czy oksybutynina przenika do mleka ludzkiego. Ponieważ wiele leków przenika do mleka ludzkiego, należy zachować ostrożność podając DITROPAN 5 mg XL kobiecie karmiącej piersią.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność preparatu DITROPAN XL® badano u 60 dzieci w 24-tygodniowym, otwartym, nierandomizowanym badaniu. Pacjenci byli w wieku 6-15 lat, wszyscy mieli objawy nadreaktywności wypieracza w związku ze stanem neurologicznym (np. rozszczep kręgosłupa), wszyscy stosowali czyste przerywane cewnikowanie i wszyscy byli aktualnymi użytkownikami chlorku oksybutyniny. Wyniki badań wykazały, że podawanie DITROPAN 2,5 mg XL® 5 do 20 mg/dobę wiązało się ze wzrostem średniej objętości moczu na cewnikowanie w stosunku do wartości wyjściowej ze 108 ml do 136 ml, wzrostem średniej objętości moczu po porannym przebudzeniu ze 148 ml w stosunku do wartości wyjściowej. mL do 189 mL oraz wzrost średniego odsetka cewnikowań bez epizodu nieszczelności w stosunku do wartości wyjściowej z 34% do 51%.
Wyniki urodynamiczne były zgodne z wynikami klinicznymi. Podanie DITROPAN XL® spowodowało wzrost średniej maksymalnej pojemności cystometrycznej w stosunku do wartości wyjściowej ze 185 ml do 254 ml, zmniejszenie w stosunku do wartości wyjściowej średniego ciśnienia wypieracza przy maksymalnej pojemności cystometrycznej z 44 cm H2O do 33 cm H2O oraz zmniejszenie odsetka pacjentów wykazujących niehamowane skurcze wypieracza (co najmniej 15 cm HO) od 60% do 28%.
Farmakokinetyka preparatu DITROPAN 5mg XL® u tych pacjentów była zgodna z farmakokinetyką zgłaszaną u dorosłych [patrz FARMAKOLOGIA KLINICZNA ].
Nie zaleca się stosowania leku DITROPAN 5 mg XL® u dzieci, które nie mogą połykać tabletki w całości bez żucia, dzielenia lub kruszenia, ani u dzieci w wieku poniżej 6 lat.
Zastosowanie geriatryczne
Częstość i nasilenie działań antycholinergicznych zgłaszanych przez pacjentów w wieku poniżej 65 lat oraz pacjentów w wieku 65 lat i starszych były podobne. Farmakokinetyka preparatu DITROPAN XL® była podobna u wszystkich badanych pacjentów (do 78 lat).
Zaburzenia czynności nerek
Nie przeprowadzono badań z DITROPAN XL® u pacjentów z zaburzeniami czynności nerek.
Niewydolność wątroby
Nie przeprowadzono badań z DITROPAN 2,5 mg XL® u pacjentów z zaburzeniami czynności wątroby.
PRZEDAWKOWAĆ
W leczeniu przedawkowania należy rozważyć ciągłe uwalnianie oksybutyniny z DITROPAN 5mg XL®. Pacjenci powinni być monitorowani przez co najmniej 24 godziny. Leczenie powinno być objawowe i podtrzymujące. Można podać środek przeczyszczający.
Przedawkowanie chlorku oksybutyniny wiąże się z działaniem antycholinergicznym, w tym pobudzeniem ośrodkowego układu nerwowego, uderzeniami gorąca, gorączką, odwodnieniem, zaburzeniami rytmu serca, wymiotami i zatrzymaniem moczu.
Przyjęto 100 mg chlorku oksybutyniny w połączeniu z alkoholem u 13-letniego chłopca, który doświadczył utraty pamięci i 34-letniej kobiety, u której wystąpił otępienie, a następnie dezorientacja i pobudzenie po przebudzeniu, rozszerzone źrenice, suchość skóry, zaburzenia rytmu serca i zatrzymanie moczu. Obaj pacjenci całkowicie wyzdrowieli dzięki leczeniu objawowemu.
PRZECIWWSKAZANIA
DITROPAN 2,5 mg XL® jest przeciwwskazany u pacjentów z zatrzymaniem moczu, zatrzymaniem żołądka i innymi ciężkimi stanami obniżonej motoryki przewodu pokarmowego, niekontrolowaną jaskrą z wąskim kątem.
DITROPAN 2,5mg XL® jest również przeciwwskazany u pacjentów, u których stwierdzono nadwrażliwość na substancję leczniczą lub inne składniki produktu. Istnieją doniesienia o reakcjach nadwrażliwości, w tym anafilaksji i obrzęku naczynioruchowym.
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Oksybutynina rozluźnia mięśnie gładkie pęcherza. Chlorek oksybutyniny wywiera bezpośrednie działanie przeciwskurczowe na mięśnie gładkie i hamuje muskarynowe działanie acetylocholiny na mięśnie gładkie. Nie występują efekty blokujące w połączeniach nerwowo-mięśniowych szkieletu lub zwojach autonomicznych (działanie antynikotynowe).
Aktywność antymuskarynowa dotyczy głównie izomeru R. Metabolit, deetylooksybutynina, wykazuje aktywność farmakologiczną podobną do oksybutyniny w badaniach in vitro.
Farmakodynamika
U pacjentów ze stanami charakteryzującymi się mimowolnymi skurczami pęcherza, badania cystometryczne wykazały, że oksybutynina zwiększa pojemność pęcherza (pęcherzowego), zmniejsza częstotliwość niezahamowanych skurczów mięśnia wypieracza i opóźnia początkowe pragnienie oddania moczu.
Farmakokinetyka
Wchłanianie
Po podaniu pierwszej dawki DITROPAN XL® stężenie oksybutyniny w osoczu wzrasta na 4 do 6 godzin; następnie stałe stężenie utrzymuje się do 24 godzin, minimalizując wahania pomiędzy maksymalnym i minimalnym stężeniem związanym z oksybutyniną.
Względna biodostępność R- i S-oksybutyniny z DITROPAN XL® wynosi odpowiednio 156% i 187% w porównaniu z oksybutyniną. Średnie parametry farmakokinetyczne dla R- i S-oksybutyniny podsumowano w Tabeli 2. Profile stężenie w osoczu-czas dla R- i S-oksybutyniny mają podobny kształt; Rysunek 1 przedstawia profil dla R-oksybutyniny.
Rysunek 1: Średnie stężenia R-oksybutyniny w osoczu po podaniu pojedynczej dawki DITROPAN XL® 10 mg i 5 mg oksybutyniny co 8 godzin (n=23 dla każdego leczenia).
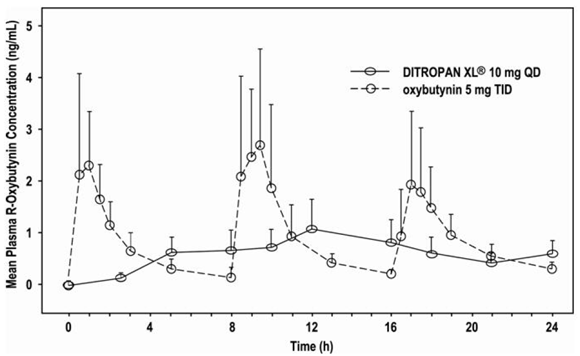
Stężenia oksybutyniny w stanie stacjonarnym w osoczu są osiągane do dnia 3 powtarzanego dawkowania DITROPAN XL®, bez obserwowanej kumulacji leku lub zmiany parametrów farmakokinetycznych oksybutyniny i deetylooksybutyniny.
Farmakokinetykę leku DITROPAN 5 mg XL® w stanie stacjonarnym badano u 19 dzieci w wieku od 5 do 15 lat z nadczynnością wypieracza związaną ze stanem neurologicznym (np. rozszczep kręgosłupa). Dzieci otrzymywały całkowitą dawkę dobową DITROPAN 2,5 mg XL® w zakresie od 5 do 20 mg (0,10 do 0,77 mg/kg). Do uzyskania próbek surowicy zastosowano technikę rzadkiego pobierania próbek. Gdy wszystkie dostępne dane zostaną znormalizowane do ekwiwalentu 5 mg dziennie DITROPAN XL®, średnie parametry farmakokinetyczne wyprowadzone dla R- i S-oksybutyniny oraz R- i S-desetylooksybutyniny podsumowano w Tabeli 3. Profile stężenia w osoczu w czasie dla R- i S-oksybutyniny mają podobny kształt; Rysunek 2 przedstawia profil dla R-oksybutyniny, gdy wszystkie dostępne dane są znormalizowane do ekwiwalentu 5 mg dziennie.
Rycina 2: Średnie stężenia w stanie stacjonarnym (± SD) R-oksybutyniny w osoczu po podaniu od 5 do 20 mg DITROPAN 5 mg XL® raz na dobę dzieciom w wieku od 5 do 15 lat. Wykres przedstawia wszystkie dostępne dane znormalizowane do odpowiednika DITROPAN XL® 5 mg raz na dobę.
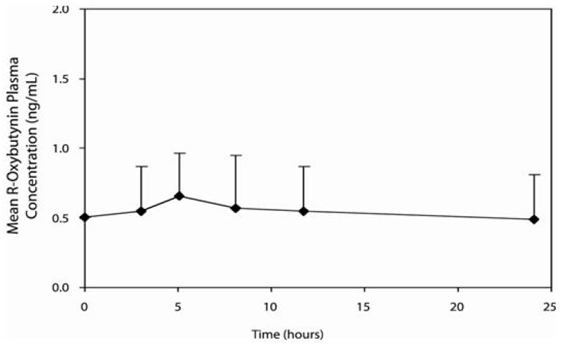
Efekty żywności
Szybkość i zakres wchłaniania i metabolizmu oksybutyniny są podobne w warunkach po posiłku i na czczo.
Dystrybucja
Oksybutynina jest szeroko dystrybuowana w tkankach organizmu po wchłonięciu ogólnoustrojowym. Objętość dystrybucji wynosi 193 l po dożylnym podaniu 5 mg chlorku oksybutyniny. Oba enancjomery oksybutyniny silnie wiążą się (>99%) z białkami osocza. Oba enancjomery N-desetylooksybutyniny wiążą się również w wysokim stopniu (>97%) z białkami osocza. Głównym białkiem wiążącym jest kwaśna glikoproteina alfa-1.
Metabolizm
Oksybutynina jest metabolizowana głównie przez układy enzymatyczne cytochromu P450, szczególnie CYP3A4 znajdujące się głównie w wątrobie i ścianie jelita. Jej produktami przemiany materii są kwas fenylocykloheksyloglikolowy, który jest farmakologicznie nieaktywny oraz dezetylooksybutynina, która jest farmakologicznie aktywna. Po podaniu DITROPAN 2,5 mg XL® stężenia R- i S-desetylooksybutyniny w osoczu wynoszą odpowiednio 73% i 92% stężeń obserwowanych dla oksybutyniny.
Wydalanie
Oksybutynina jest intensywnie metabolizowana przez wątrobę, a mniej niż 0,1% podanej dawki jest wydalane w postaci niezmienionej z moczem. Ponadto mniej niż 0,1% podanej dawki jest wydalane w postaci metabolitu deetylooksybutyniny.
Proporcjonalność dawki
Parametry farmakokinetyczne oksybutyniny i dezetylooksybutyniny (Cmax i AUC) po podaniu 5-20 mg DITROPAN 5mg XL® są proporcjonalne do dawki.
Używaj w określonych populacjach
Pediatryczny
Farmakokinetykę preparatu DITROPAN 2,5 mg XL® oceniano u 19 dzieci w wieku 5-15 lat z nadczynnością wypieracza związaną ze stanem neurologicznym (np. rozszczep kręgosłupa). Farmakokinetyka preparatu DITROPAN 2,5 mg XL® u tych pacjentów pediatrycznych była zgodna z wartościami odnotowanymi dla dorosłych (patrz Tabele 2 i 3 oraz Ryciny 1 i 2 powyżej).
Płeć
Nie ma istotnych różnic w farmakokinetyce oksybutyniny u zdrowych ochotników płci męskiej i żeńskiej po podaniu preparatu DITROPAN 2,5 mg XL®.
Wyścig
Dostępne dane sugerują, że nie ma istotnych różnic w farmakokinetyce oksybutyniny w zależności od rasy u zdrowych ochotników po podaniu preparatu DITROPAN 2,5 mg XL®.
Studia kliniczne
DITROPAN 5mg XL® oceniano pod kątem leczenia pacjentów z nadreaktywnym pęcherzem moczowym z objawami nietrzymania moczu z parcia naglącego i częstością parcia w trzech kontrolowanych badaniach skuteczności. Większość pacjentów była rasy białej (89,0%) i płci żeńskiej (91,9%) w średnim wieku 59 lat (zakres od 18 do 98 lat). Kryteria włączenia wymagały, aby pacjenci mieli nietrzymanie z parcia lub mieszane (z przewagą parcia), czego dowodem jest ≥ 6 epizodów nietrzymania moczu z parcia na tydzień i ≥ 10 oddawania moczu na dobę. Badanie 1 było projektem ze stałą dawką, podczas gdy w pozostałych dwóch badaniach zastosowano projekt z dostosowaniem dawki, w którym ostateczną dawkę każdego pacjenta dostosowano do równowagi między poprawą objawów nietrzymania moczu a tolerancją działań niepożądanych. Wszystkie trzy badania obejmowały pacjentów, o których wiadomo, że odpowiadają na oksybutyninę lub inne leki antycholinergiczne i ci pacjenci otrzymywali ostateczną dawkę przez okres do 2 tygodni.
Wyniki skuteczności z trzech kontrolowanych badań przedstawiono w poniższych tabelach 4, 5 i 6 oraz na rycinach 3, 4 i 5.
Rycina 3: Średnia zmiana (±SD) w epizodach nietrzymania moczu z parcia na tydzień od wartości początkowej (Badanie 1)
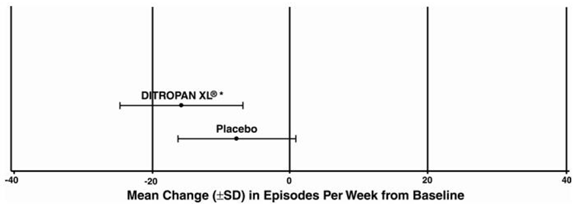
Rycina 4: Średnia zmiana (±SD) w epizodach nietrzymania moczu z parcia na tydzień od wartości początkowej (Badanie 2)
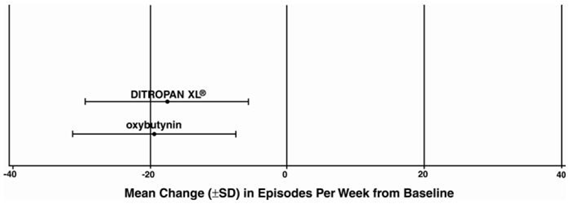
Rycina 5: Średnia zmiana (±SD) w epizodach nietrzymania moczu z parcia na tydzień od wartości początkowej (Badanie 3)
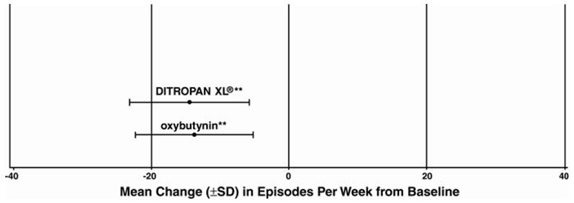
INFORMACJA O PACJENCIE
- Należy poinformować pacjentów, że oksybutynina może powodować obrzęk naczynioruchowy, który może prowadzić do zagrażającej życiu niedrożności dróg oddechowych. Pacjentom należy zalecić natychmiastowe przerwanie leczenia oksybutyniną i natychmiastowe zwrócenie się o pomoc lekarską w przypadku wystąpienia obrzęku języka, obrzęku krtani lub trudności w oddychaniu.
- Należy poinformować pacjentów, że środki antycholinergiczne (przeciwmuskarynowe), takie jak DITROPAN XL®, mogą powodować klinicznie istotne działania niepożądane związane z działaniem antycholinergicznym, takie jak:
- Zatrzymanie moczu i zaparcia
- Prostracja cieplna z powodu zmniejszonej potliwości. Gdy leki antycholinergiczne są podawane w obecności wysokiej temperatury otoczenia, może wystąpić prostracja cieplna.
- Należy poinformować pacjentów, że leki antycholinergiczne, takie jak DITROPAN 5 mg XL®, mogą powodować senność, zawroty głowy lub niewyraźne widzenie. Należy pouczyć pacjentów, aby zachowali ostrożność przy podejmowaniu decyzji o wykonywaniu potencjalnie niebezpiecznych czynności do czasu stwierdzenia działania leku DITROPAN XL®.
- Należy poinformować pacjentów, że alkohol może nasilać senność wywołaną przez środki antycholinergiczne, takie jak DITROPAN XL®.
- Należy poinformować pacjentów, że DITROPAN 5mg XL® należy połykać w całości, popijając płynami. Pacjenci nie powinni żuć, dzielić ani kruszyć tabletek. Lek znajduje się w niewchłanialnej powłoce zaprojektowanej do uwalniania leku z kontrolowaną szybkością. Powłoka tabletki jest eliminowana z organizmu; pacjenci nie powinni się martwić, jeśli od czasu do czasu zauważą w swoim stolcu coś, co wygląda jak tabletka.
- DITROPAN 5mg XL® powinien być przyjmowany mniej więcej o tej samej porze każdego dnia.
