Neurontin 100mg, 300mg, 400mg, 600mg Gabapentin Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Neurontin i jak się go stosuje?
Neurontin 400mg to lek na receptę stosowany w leczeniu objawów nerwobólu i drgawek. Neurontin może być stosowany samodzielnie lub z innymi lekami.
Neurontin jest analogiem GABA, lekiem przeciwpadaczkowym.
Nie wiadomo, czy Neurontin jest bezpieczny i skuteczny u dzieci w wieku poniżej 3 lat.
Jakie są możliwe skutki uboczne Neurontin 400mg?
Neurontin może powodować poważne skutki uboczne, w tym:
- zwiększone napady
- silne osłabienie lub zmęczenie
- problemy z równowagą lub ruchem mięśni
- ból w górnej części brzucha
- ból w klatce piersiowej
- nowy lub nasilający się kaszel z gorączką
- problemy z oddychaniem
- silne mrowienie lub drętwienie
- szybki ruch gałek ocznych
- małe lub brak oddawania moczu
- bolesne lub utrudnione oddawanie moczu
- obrzęk stóp lub kostek
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze działania niepożądane Neurontin to:
- ból głowy
- zawroty głowy
- senność
- zmęczenie
- obrzęk dłoni lub stóp
- problemy z oczami
- problemy z koordynacją
- Najczęstsze skutki uboczne Neurontin 600mg u dzieci to:
- gorączka
- mdłości
- wymioty
- zmiany w zachowaniu
- problemy z pamięcią
- problemy z koncentracją
- zachowywanie się niespokojnie, wrogo lub agresywnie
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Neurontinu. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
Substancją czynną kapsułek, tabletek i roztworu doustnego NEURONTIN jest gabapentyna, której nazwa chemiczna to kwas 1-(aminometylo)cykloheksanooctowy.
Wzór cząsteczkowy gabapentyny to C9H17NO2, a masa cząsteczkowa to 171,24. Wzór strukturalny gabapentyny to:
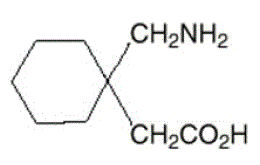
Gabapentyna jest białym lub prawie białym krystalicznym ciałem stałym o pKa1 3,7 i pKa2 10,7. Jest swobodnie rozpuszczalny w wodzie oraz zarówno zasadowych, jak i kwaśnych roztworach wodnych. Logarytm współczynnika podziału (noktanol/0,05 M bufor fosforanowy) przy pH 7,4 wynosi –1,25.
Każda kapsułka Neurontin 100 mg zawiera 100 mg, 300 mg lub 400 mg gabapentyny i następujące składniki nieaktywne: laktoza, skrobia kukurydziana, talk, żelatyna, dwutlenek tytanu, FD&C Blue nr 2, żółty tlenek żelaza (tylko 300 mg i 400 mg) i czerwony tlenek żelaza (tylko 400 mg).
Każda tabletka Neurontin zawiera 600 mg lub 800 mg gabapentyny i następujące składniki nieaktywne: poloksamer 407, kopowidon, skrobia kukurydziana, stearynian magnezu, hydroksypropyloceluloza, talk i wosk kandelila
Roztwór doustny Neurontin zawiera 250 mg gabapentyny na 5 ml (50 mg na ml) oraz następujące składniki nieaktywne: glicerynę, ksylitol, wodę oczyszczoną i sztuczny aromat chłodnego anyżu truskawkowego.
WSKAZANIA
NEURONTIN® jest wskazany do:
- Postępowanie w neuralgii popółpaścowej u dorosłych
- Terapia wspomagająca w leczeniu napadów częściowych i częściowych wtórnie uogólnionych u dorosłych i dzieci w wieku 3 lat i starszych z padaczką
DAWKOWANIE I SPOSÓB PODAWANIA
Dawkowanie w przypadku neuralgii popółpaścowej
U dorosłych z neuralgią popółpaścową NEURONTIN można rozpocząć w 1. dniu jako pojedynczą dawkę 300 mg, w 2. dniu jako 600 mg/dobę (300 mg dwa razy na dobę), a w 3. dniu jako 900 mg/dobę (300 mg trzy razy na dobę). razy dziennie). Dawkę można następnie zwiększać w razie potrzeby w celu złagodzenia bólu do dawki 1800 mg/dobę (600 mg trzy razy na dobę). W badaniach klinicznych skuteczność wykazano w zakresie dawek od 1800 mg/dobę do 3600 mg/dobę z porównywalnymi efektami w całym zakresie dawek; jednak w tych badaniach klinicznych nie wykazano dodatkowej korzyści ze stosowania dawek większych niż 1800 mg/dobę.
Dawkowanie w przypadku padaczki z częściowymi napadami padaczkowymi
Pacjenci w wieku 12 lat i powyżej
Dawka początkowa wynosi 300 mg trzy razy na dobę. Zalecana dawka podtrzymująca preparatu NEURONTIN wynosi od 300 mg do 600 mg trzy razy na dobę. Dawki do 2400 mg/dobę były dobrze tolerowane w długoterminowych badaniach klinicznych. Dawki 3600 mg/dobę podawano również niewielkiej liczbie pacjentów przez stosunkowo krótki czas i były dobrze tolerowane. Podawać NEURONTIN trzy razy dziennie w postaci kapsułek 300 mg lub 400 mg lub tabletek 600 mg lub 800 mg. Maksymalny czas pomiędzy dawkami nie powinien przekraczać 12 godzin.
Pacjenci pediatryczni w wieku od 3 do 11 lat
Zakres dawek początkowych wynosi od 10 mg/kg/dobę do 15 mg/kg/dobę, podawanych w trzech dawkach podzielonych, a zalecaną dawkę podtrzymującą osiąga się poprzez zwiększanie dawki przez okres około 3 dni. Zalecana dawka podtrzymująca preparatu NEURONTIN u pacjentów w wieku od 3 do 4 lat wynosi 40 mg/kg/dobę, podawana w trzech dawkach podzielonych. Zalecana dawka podtrzymująca preparatu NEURONTIN 100 mg u pacjentów w wieku od 5 do 11 lat wynosi od 25 mg/kg/dobę do 35 mg/kg/dobę, podawana w trzech dawkach podzielonych. NEURONTIN 300 mg może być podawany jako roztwór doustny, kapsułka lub tabletka, lub przy użyciu kombinacji tych preparatów. Dawki do 50 mg/kg/dobę były dobrze tolerowane w długoterminowym badaniu klinicznym. Maksymalny odstęp czasu między dawkami nie powinien przekraczać 12 godzin.
Dostosowanie dawkowania u pacjentów z zaburzeniami czynności nerek
U pacjentów w wieku 12 lat i starszych z zaburzeniami czynności nerek lub poddawanych hemodializie zaleca się następujące dostosowanie dawkowania (patrz zalecenia dotyczące dawkowania powyżej dla skutecznych dawek w każdym wskazaniu):
TABELA 1: Dawkowanie NEURONTINY w zależności od czynności nerek
Klirens kreatyniny (CLCr) jest trudny do zmierzenia u pacjentów ambulatoryjnych. U pacjentów ze stabilną czynnością nerek klirens kreatyniny można dość dobrze oszacować za pomocą równania Cockcrofta i Gaulta:
Nie badano stosowania preparatu NEURONTIN u pacjentów w wieku poniżej 12 lat z zaburzoną czynnością nerek.
Dawkowanie u osób starszych
Ponieważ u pacjentów w podeszłym wieku istnieje większe prawdopodobieństwo upośledzenia czynności nerek, należy zachować ostrożność przy doborze dawki i dostosować dawkę na podstawie wartości klirensu kreatyniny u tych pacjentów.
Informacje administracyjne
Podawać NEURONTIN doustnie z jedzeniem lub bez jedzenia.
Kapsułki NEURONTIN 100 mg należy połykać w całości, popijając wodą.
Należy poinformować pacjentów, że jeśli podzielą podzieloną tabletkę 600 mg lub 800 mg NEURONTIN w celu podania połówki tabletki, powinni przyjąć niewykorzystaną połówkę tabletki jako kolejną dawkę. Połówki tabletek, które nie zostały zużyte w ciągu 28 dni od podzielenia tabletki z linią podziału, należy wyrzucić.
Jeśli dawka NEURONTIN zostanie zmniejszona, przerwana lub zastąpiona innym lekiem, należy to robić stopniowo przez co najmniej 1 tydzień (może być potrzebny dłuższy okres według uznania lekarza).
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Kapsułki
- 100 mg: białe twarde kapsułki żelatynowe z nadrukiem „PD” na korpusie i „Neurontin/100 mg” na wieczku
- 300 mg: żółte twarde kapsułki żelatynowe z nadrukiem „PD” na korpusie i „Neurontin/300 mg” na wieczku
- 400 mg: pomarańczowe twarde kapsułki żelatynowe z nadrukiem „PD” na korpusie i „Neurontin/400 mg” na wieczku
Tablety
- 600 mg: białe eliptyczne tabletki powlekane z linią podziału z wytłoczonym napisem „NT” i „16” po jednej stronie
- 800 mg: białe eliptyczne tabletki powlekane z linią podziału z wytłoczonym napisem „NT” i „26” po jednej stronie
Rozwiązanie doustne
- 250 mg na 5 ml (50 mg na ml), przezroczysty, bezbarwny do lekko żółtego roztwór
Składowania i stosowania
NEURONTYNA (gabapentyna) kapsułki, tabletki i roztwór doustny są dostarczane w następujący sposób:
Kapsułki 100 mg
Białe twarde kapsułki żelatynowe z nadrukiem „PD” na korpusie i „Neurontin/100 mg” na wieczku; dostępne w:
Butelki po 100 sztuk: NDC 0071-0803-24
Kapsułki 300 mg
Żółte twarde kapsułki żelatynowe z nadrukiem „PD” na korpusie i „Neurontin/300 mg” na wieczku; dostępne w:
Butelki po 100 sztuk: NDC 0071-0805-24 Dawka jednostkowa 50 lat: NDC 0071-0805-40
Kapsułki 400 mg
Pomarańczowe twarde kapsułki żelatynowe z nadrukiem „PD” na korpusie i „Neurontin/400 mg” na wieczku; dostępne w:
Butelki po 100 sztuk: NDC 0071-0806-24 Dawka jednostkowa 50’s: NDC 0071-0806-40
Tabletki 600 mg
Białe, eliptyczne tabletki powlekane z linią podziału, z wytłoczonym napisem „NT” i „16” po jednej stronie; dostępne w:
Butelki po 100 sztuk: NDC 0071-0513-24
Tabletki 800 mg
Białe, eliptyczne tabletki powlekane z linią podziału, z wytłoczonym napisem „NT” i „26” po jednej stronie; dostępne w:
Butelki po 100 sztuk: NDC 0071-0401-24
250 mg na 5 ml roztworu doustnego
Przejrzysty, bezbarwny do lekko żółtego roztwór; każde 5 ml roztworu doustnego zawiera 250 mg gabapentyny; dostępne w:
Butelki szklane zawierające 470 ml: NDC 0071-2012-23 Butelki zawierające 470 ml: NDC 0071-2012-44
Tabletki i kapsułki NEURONTIN 400 mg należy przechowywać w temperaturze 25°C (77°F); dopuszczalne odchylenia od 15°C do 30°C (59°F do 86°F) [patrz Temperatura pokojowa kontrolowana przez USP ].
Przechowywać roztwór doustny NEURONTIN w lodówce, od 2°C do 8°C (36°F do 46°F).
Dystrybutor: Parke-Davis, Oddział Pfizer Inc., NY, NY 10017. Aktualizacja: grudzień 2020
SKUTKI UBOCZNE
Następujące poważne działania niepożądane omówiono bardziej szczegółowo w innych rozdziałach:
- Reakcja polekowa z eozynofilią i objawami ogólnoustrojowymi (DRESS)/nadwrażliwość wielonarządowa [patrz OSTRZEŻENIA I ŚRODKI ]
- Anafilaksja i obrzęk naczynioruchowy [patrz OSTRZEŻENIA I ŚRODKI ]
- Senność/Sedacja i zawroty głowy [patrz OSTRZEŻENIA I ŚRODKI ]
- Napad padaczkowy z odstawienia, stan padaczkowy [patrz OSTRZEŻENIA I ŚRODKI ]
- Zachowania samobójcze i myśli samobójcze [patrz OSTRZEŻENIA I ŚRODKI ]
- Depresja oddechowa [patrz OSTRZEŻENIA I ŚRODKI ]
- Neuropsychiatryczne reakcje niepożądane (pacjenci pediatryczni w wieku od 3 do 12 lat) [patrz OSTRZEŻENIA I ŚRODKI ]
- Nagła i niewyjaśniona śmierć u pacjentów z padaczką [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Neuralgia popółpaścowa
Najczęstszymi działaniami niepożądanymi związanymi ze stosowaniem preparatu NEURONTIN u dorosłych, nie obserwowanymi z podobną częstością wśród pacjentów otrzymujących placebo, były zawroty głowy, senność i obrzęki obwodowe.
2 kontrolowanych badaniach dotyczących neuralgii popółpaścowej 16% z 336 pacjentów, którzy otrzymywali NEURONTIN i 9% z 227 pacjentów, którzy otrzymywali placebo przerwało leczenie z powodu działania niepożądanego. Działania niepożądane, które najczęściej prowadziły do odstawienia leku u pacjentów leczonych NEURONTIN, to zawroty głowy, senność i nudności.
W tabeli 3 wymieniono działania niepożądane, które wystąpiły u co najmniej 1% leczonych NEURONTIN pacjentów z nerwobólem popółpaścowym uczestniczących w badaniach kontrolowanych placebo i które były liczbowo częstsze w grupie NEURONTIN niż w grupie placebo.
TABELA 3: Działania niepożądane w zbiorczych badaniach kontrolowanych placebo dotyczących neuralgii popółpaścowej
Inne reakcje u ponad 1% pacjentów, ale równie lub częściej w grupie placebo obejmowały ból, drżenie, nerwoból, ból pleców, niestrawność, duszność i zespół grypowy.
Nie stwierdzono klinicznie istotnych różnic między mężczyznami i kobietami w rodzaju i częstości występowania działań niepożądanych. Ponieważ było niewielu pacjentów, których rasa została zgłoszona jako inna niż biała, nie ma wystarczających danych na poparcie stwierdzenia dotyczącego podziału działań niepożądanych według rasy.
Padaczka z częściowymi napadami (terapia wspomagająca)
Najczęstszymi działaniami niepożądanymi leku NEURONTIN 300 mg w skojarzeniu z innymi lekami przeciwpadaczkowymi u pacjentów w wieku >12 lat, nie obserwowanymi z podobną częstością wśród pacjentów otrzymujących placebo, były senność, zawroty głowy, ataksja, zmęczenie i oczopląs.
Najczęstszymi działaniami niepożądanymi związanymi ze stosowaniem preparatu NEURONTIN w skojarzeniu z innymi lekami przeciwpadaczkowymi u dzieci w wieku od 3 do 12 lat, nie obserwowanymi z taką samą częstością wśród pacjentów otrzymujących placebo, były zakażenia wirusowe, gorączka, nudności i (lub) wymioty, senność i wrogość [patrz OSTRZEŻENIA I ŚRODKI ].
Około 7% z 2074 pacjentów w wieku >12 lat i około 7% z 449 pacjentów pediatrycznych w wieku od 3 do 12 lat, którzy otrzymywali NEURONTIN w badaniach klinicznych przed wprowadzeniem do obrotu, przerwało leczenie z powodu działania niepożądanego. Działania niepożądane najczęściej związane z odstawieniem u pacjentów w wieku >12 lat to senność (1,2%), ataksja (0,8%), zmęczenie (0,6%), nudności i (lub) wymioty (0,6%) oraz zawroty głowy (0,6%). . Działania niepożądane najczęściej związane z odstawieniem leku u dzieci to chwiejność emocjonalna (1,6%), wrogość (1,3%) i hiperkinezja (1,1%).
W tabeli 4 wymieniono działania niepożądane, które wystąpiły u co najmniej 1% leczonych NEURONTIN pacjentów w wieku >12 lat z padaczką uczestniczących w badaniach kontrolowanych placebo i były liczbowo częstsze w grupie NEURONTIN. W tych badaniach do aktualnej terapii przeciwpadaczkowej pacjenta dodano albo NEURONTIN 300 mg, albo placebo.
TABELA 4: Działania niepożądane w zbiorczych, kontrolowanych placebo badaniach dodatkowych u pacjentów z padaczką w wieku >12 lat
Wśród działań niepożądanych występujących z częstością co najmniej 10% u pacjentów leczonych NEURONTIN, senność i ataksja wydawały się wykazywać dodatnią zależność dawka-odpowiedź.
Ogólna częstość występowania działań niepożądanych i rodzaje obserwowanych działań niepożądanych były podobne u mężczyzn i kobiet leczonych preparatem NEURONTIN. Częstość występowania działań niepożądanych wzrosła nieznacznie wraz z wiekiem u pacjentów leczonych NEURONTIN lub placebo. Ponieważ tylko 3% pacjentów (28/921) w badaniach kontrolowanych placebo zostało zidentyfikowanych jako osoby rasy innej niż biała (czarna lub inna), nie ma wystarczających danych na poparcie stwierdzenia dotyczącego podziału działań niepożądanych według rasy.
Tabeli 5 wymieniono działania niepożądane, które wystąpiły u co najmniej 2% pacjentów leczonych NEURONTIN w wieku od 3 do 12 lat z padaczką uczestniczących w badaniach kontrolowanych placebo i które były liczbowo częstsze w grupie NEURONTIN.
TABELA 5: Działania niepożądane w kontrolowanym placebo badaniu dodatkowym u dzieci z padaczką w wieku od 3 do 12 lat
Inne reakcje u ponad 2% dzieci w wieku od 3 do 12 lat, ale równie lub częściej w grupie placebo obejmowały: zapalenie gardła, zakażenie górnych dróg oddechowych, ból głowy, nieżyt nosa, drgawki, biegunkę, anoreksję, kaszel i zapalenie ucha środkowego.
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania preparatu NEURONTIN po wprowadzeniu do obrotu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Zaburzenia wątroby i dróg żółciowych: żółtaczka
Dochodzenia: podwyższona kinaza kreatynowa, podwyższone testy czynności wątroby
Zaburzenia metabolizmu i odżywiania: hiponatremia
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej: rabdomioliza
Zaburzenia układu nerwowego: zaburzenia ruchu
Zaburzenia psychiczne: podniecenie
Zaburzenia układu rozrodczego i piersi: powiększenie piersi, zmiany libido, zaburzenia wytrysku i anorgazmia
Zaburzenia skóry i tkanki podskórnej: obrzęk naczynioruchowy [patrz OSTRZEŻENIA I ŚRODKI ], pemfigoid pęcherzowy, rumień wielopostaciowy, zespół Stevensa-Johnsona.
Istnieją doniesienia po wprowadzeniu do obrotu o zagrażającej życiu lub prowadzącej do zgonu depresji oddechowej u pacjentów przyjmujących NEURONTIN z opioidami lub innymi lekami działającymi depresyjnie na ośrodkowy układ nerwowy lub w przypadku współistniejących zaburzeń oddychania [patrz OSTRZEŻENIA I ŚRODKI ].
Zgłaszano również działania niepożądane po nagłym odstawieniu gabapentyny. Najczęściej zgłaszanymi reakcjami były lęk, bezsenność, nudności, ból i pocenie się.
INTERAKCJE Z LEKAMI
Opioidy
Po jednoczesnym podaniu gabapentyny z opioidami (np. morfina, hydrokodon, oksykodon, buprenorfina) zgłaszano depresję oddechową i sedację, czasami prowadzące do zgonu [patrz OSTRZEŻENIA I ŚRODKI ].
hydrokodon
Jednoczesne podawanie NEURONTIN 300 mg z hydrokodonem zmniejsza ekspozycję na hydrokodon [patrz FARMAKOLOGIA KLINICZNA ]. Należy wziąć pod uwagę możliwość zmiany ekspozycji i działania hydrokodonu, rozpoczynając lub przerywając leczenie produktem NEURONTIN 100 mg u pacjenta przyjmującego hydrokodon.
Morfina
Gdy gabapentyna jest podawana z morfiną, pacjentów należy obserwować pod kątem objawów depresji ośrodkowego układu nerwowego, takich jak senność, uspokojenie polekowe i depresja oddechowa [patrz FARMAKOLOGIA KLINICZNA ].
Inne leki przeciwpadaczkowe
Gabapentyna nie jest metabolizowana w znacznym stopniu ani nie wpływa na metabolizm powszechnie stosowanych jednocześnie leków przeciwpadaczkowych [patrz FARMAKOLOGIA KLINICZNA ].
Maalox® (wodorotlenek glinu, wodorotlenek magnezu)
Średnia biodostępność gabapentyny zmniejszyła się o około 20% przy jednoczesnym stosowaniu środka zobojętniającego kwas (Maalox) zawierającego wodorotlenki magnezu i glinu. Zaleca się przyjmowanie gabapentyny co najmniej 2 godziny po podaniu preparatu Maalox [patrz FARMAKOLOGIA KLINICZNA ].
Interakcje leków/testów laboratoryjnych
Ponieważ po dodaniu gabapentyny do innych leków przeciwpadaczkowych, po dodaniu gabapentyny do innych leków przeciwpadaczkowych, za pomocą testu paskowego Ames N-Multistix SG stwierdzono fałszywie dodatnie odczyty, zaleca się bardziej specyficzną procedurę wytrącania kwasu sulfosalicylowego w celu określenia obecności białka w moczu.
Nadużywanie i uzależnienie od narkotyków
Substancja kontrolowana
Gabapentyna nie jest lekiem zaplanowanym.
Nadużywać
Nadużycie to celowe, nieterapeutyczne użycie leku, nawet jednorazowo, ze względu na jego pożądane skutki psychologiczne lub fizjologiczne. Nadużycie to zamierzone użycie leku w celach terapeutycznych przez osobę w sposób inny niż przepisany przez świadczeniodawcę lub osobie, której nie został przepisany.
Gabapentyna nie wykazuje powinowactwa do receptorów benzodiazepinowych, opioidowych (mu, delta lub kappa) ani kanabinoidów 1. Niewłaściwe stosowanie i nadużywanie gabapentyny zgłaszano w okresie po wprowadzeniu produktu do obrotu i w opublikowanym piśmiennictwie. Większość osób opisanych w tych raportach miała historię nadużywania wielu substancji. Niektóre z tych osób przyjmowały wyższe niż zalecane dawki gabapentyny w przypadku niezatwierdzonych zastosowań. Przepisując NEURONTIN, należy dokładnie ocenić pacjentów pod kątem historii nadużywania leków i obserwować ich pod kątem oznak i objawów niewłaściwego stosowania lub nadużywania gabapentyny (np. zwiększania dawki i poszukiwania leków). W badaniach na ludziach nie oceniano możliwości nadużywania gabapentyny.
Zależność
Uzależnienie fizyczne to stan, który rozwija się w wyniku adaptacji fizjologicznej w odpowiedzi na wielokrotne zażywanie leku, objawiający się objawami odstawienia po nagłym odstawieniu lub znacznym zmniejszeniu dawki leku. Istnieją rzadkie doniesienia postmarketingowe o osobach doświadczających objawów odstawienia wkrótce po odstawieniu większych niż zalecane dawek gabapentyny stosowanej w leczeniu chorób, w których lek nie jest zatwierdzony. Takie objawy obejmowały pobudzenie, dezorientację i splątanie po nagłym odstawieniu gabapentyny, które ustąpiły po ponownym włączeniu gabapentyny. Potencjał uzależniający gabapentyny nie był oceniany w badaniach na ludziach.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Reakcja polekowa z eozynofilią i objawami ogólnoustrojowymi (DRESS)/nadwrażliwość wielonarządowa
Po podaniu NEURONTIN wystąpiła polekowa reakcja z eozynofilią i objawami ogólnoustrojowymi (DRESS), znana również jako nadwrażliwość wielonarządowa. Niektóre z tych reakcji były śmiertelne lub zagrażały życiu. DRESS zazwyczaj, choć nie wyłącznie, objawia się gorączką, wysypką i/lub powiększeniem węzłów chłonnych w połączeniu z zajęciem innych narządów, takich jak zapalenie wątroby, zapalenie nerek, nieprawidłowości hematologiczne, zapalenie mięśnia sercowego lub zapalenie mięśni, czasami przypominające ostrą infekcję wirusową. Często występuje eozynofilia. To zaburzenie ma zmienną ekspresję i mogą być zaangażowane inne układy narządów nie wymienione tutaj.
Należy zauważyć, że wczesne objawy nadwrażliwości, takie jak gorączka lub powiększenie węzłów chłonnych, mogą być obecne, nawet jeśli wysypka nie jest widoczna. Jeśli takie oznaki lub objawy są obecne, pacjenta należy natychmiast poddać ocenie. NEURONTIN należy przerwać, jeśli nie można ustalić innej etiologii objawów przedmiotowych lub podmiotowych.
Anafilaksja i obrzęk naczynioruchowy
NEURONTIN może powodować anafilaksję i obrzęk naczynioruchowy po podaniu pierwszej dawki lub w dowolnym momencie leczenia. Objawy przedmiotowe i podmiotowe w zgłoszonych przypadkach obejmowały trudności w oddychaniu, obrzęk warg, gardła i języka oraz niedociśnienie wymagające leczenia doraźnego. Pacjentów należy poinstruować, aby przerwali stosowanie leku NEURONTIN 300 mg i natychmiast zgłosili się do lekarza, jeśli wystąpią u nich objawy anafilaksji lub obrzęku naczynioruchowego.
Wpływ na prowadzenie i obsługę ciężkich maszyn
Pacjenci przyjmujący NEURONTIN nie powinni prowadzić pojazdów, dopóki nie zdobędą wystarczającego doświadczenia, aby ocenić, czy NEURONTIN 100 mg zaburza ich zdolność do prowadzenia pojazdów. Badania zdolności prowadzenia pojazdów przeprowadzone z użyciem proleku gabapentyny (tabletki gabapentyny enacarbil o przedłużonym uwalnianiu) wskazują, że gabapentyna może powodować znaczne zaburzenia prowadzenia pojazdów. Lekarze przepisujący lek i pacjenci powinni mieć świadomość, że pacjenci umiejętność oceny własnych umiejętności prowadzenia pojazdu, a także ich umiejętność oceny stopnia senności spowodowanej przez NEURONTIN, mogą być niedoskonałe. Czas trwania upośledzenia prowadzenia pojazdów po rozpoczęciu leczenia lekiem NEURONTIN 300 mg jest nieznany. Czy utrata wartości jest związana z sennością [zob OSTRZEŻENIA I ŚRODKI ] lub inne skutki działania leku NEURONTIN są nieznane.
Ponadto, ponieważ NEURONTIN 300mg powoduje senność i zawroty głowy [patrz OSTRZEŻENIA I ŚRODKI ], pacjentom należy zalecić, aby nie obsługiwali skomplikowanych maszyn, dopóki nie zdobędą wystarczającego doświadczenia w stosowaniu NEURONTIN, aby ocenić, czy NEURONTIN 300 mg osłabia ich zdolność do wykonywania takich zadań.
Senność/Sedacja i zawroty głowy
W kontrolowanych badaniach padaczki u pacjentów w wieku powyżej 12 lat otrzymujących NEURONTIN w dawkach 100 mg do 1800 mg na dobę senność, zawroty głowy i ataksja były zgłaszane częściej u pacjentów otrzymujących NEURONTIN w porównaniu z placebo: tj. 19% w przypadku w porównaniu z 9% w grupie placebo na senność, 17% w przypadku leku w porównaniu z 7% w przypadku placebo w przypadku zawrotów głowy i 13% w przypadku leku w porównaniu z 6% w przypadku placebo w przypadku ataksji. W tych badaniach senność, ataksja i zmęczenie były częstymi działaniami niepożądanymi prowadzącymi do przerwania leczenia produktem NEURONTIN u pacjentów w wieku powyżej 12 lat, przy czym odpowiednio 1,2%, 0,8% i 0,6% przerwało leczenie z powodu tych zdarzeń.
kontrolowanych badaniach u pacjentów z neuralgią popółpaścową senność i zawroty głowy zgłaszano częściej niż w grupie placebo u pacjentów otrzymujących NEURONTIN w dawkach do 3600 mg na dobę: tj. 21% u pacjentów leczonych NEURONTIN w porównaniu z 5 % u pacjentów otrzymujących placebo na senność i 28% u pacjentów otrzymujących NEURONTIN w porównaniu do 8% u pacjentów otrzymujących placebo na zawroty głowy. Zawroty głowy i senność były jednymi z najczęstszych działań niepożądanych prowadzących do przerwania leczenia NEURONTIN.
Pacjenci powinni być uważnie obserwowani pod kątem objawów depresji ośrodkowego układu nerwowego (OUN), takich jak senność i sedacja, gdy NEURONTIN 400 mg jest stosowany z innymi lekami o właściwościach uspokajających ze względu na potencjalną synergię. Ponadto u pacjentów, którzy wymagają jednoczesnego leczenia morfiną, może wystąpić zwiększenie stężenia gabapentyny i może być konieczne dostosowanie dawki [patrz INTERAKCJE Z LEKAMI ].
Wycofanie Wytrącony napad, stan padaczkowy
Nie należy nagle odstawiać leków przeciwpadaczkowych ze względu na możliwość zwiększenia częstości napadów.
W kontrolowanych placebo badaniach padaczki u pacjentów w wieku >12 lat częstość występowania stanu padaczkowego u pacjentów otrzymujących NEURONTIN wynosiła 0,6% (3 z 543) w porównaniu do 0,5% u pacjentów otrzymujących placebo (2 z 378). Spośród 2074 pacjentów w wieku >12 lat leczonych preparatem NEURONTIN 300 mg we wszystkich badaniach nad padaczką (kontrolowanych i niekontrolowanych), stan padaczkowy wystąpił u 31 (1,5%). Spośród nich 14 pacjentów nie miało wcześniej stanu padaczkowego ani przed leczeniem, ani podczas przyjmowania innych leków. Ponieważ nie są dostępne odpowiednie dane historyczne, nie można stwierdzić, czy leczenie preparatem NEURONTIN wiąże się z wyższym lub niższym wskaźnikiem stanu padaczkowego, niż można by się spodziewać w podobnej populacji nieleczonej preparatem NEURONTIN.
Zachowania samobójcze i myśli samobójcze
Leki przeciwpadaczkowe (LPP), w tym NEURONTIN 100 mg, zwiększają ryzyko myśli lub zachowań samobójczych u pacjentów przyjmujących te leki z dowolnego wskazania. Pacjenci leczeni dowolnymi lekami przeciwpadaczkowymi w jakimkolwiek wskazaniu powinni być monitorowani pod kątem pojawienia się lub nasilenia depresji, myśli lub zachowań samobójczych i/lub jakichkolwiek nietypowych zmian nastroju lub zachowania.
Zbiorcze analizy 199 badań klinicznych kontrolowanych placebo (terapia mono- i skojarzona) 11 różnych leków przeciwpadaczkowych wykazały, że pacjenci przydzieleni losowo do jednego z leków przeciwpadaczkowych mieli około dwukrotnie większe ryzyko (skorygowane ryzyko względne 1,8, 95% CI: 1,2, 2,7) myślenie lub zachowanie w porównaniu z pacjentami przydzielonymi losowo do grupy placebo. W tych badaniach, w których mediana czasu trwania leczenia wynosiła 12 tygodni, szacunkowa częstość występowania zachowań lub myśli samobójczych wśród 27 863 pacjentów leczonych LPP wynosiła 0,43% w porównaniu z 0,24% wśród 16 029 pacjentów otrzymujących placebo, co stanowi wzrost o około jeden przypadku myśli lub zachowań samobójczych na każdych 530 leczonych pacjentów. W badaniach odnotowano cztery samobójstwa u pacjentów leczonych lekami i żadnego u pacjentów otrzymujących placebo, ale liczba ta jest zbyt mała, aby można było wyciągnąć jakiekolwiek wnioski na temat wpływu leku na samobójstwo.
Zwiększone ryzyko myśli lub zachowań samobójczych związanych z lekami przeciwpadaczkowymi zaobserwowano już tydzień po rozpoczęciu leczenia lekami przeciwpadaczkowymi i utrzymywało się przez czas trwania ocenianego leczenia. Ponieważ większość badań włączonych do analizy nie trwała dłużej niż 24 tygodnie, nie można było ocenić ryzyka myśli lub zachowań samobójczych po 24 tygodniach.
W analizowanych danych ryzyko wystąpienia myśli lub zachowań samobójczych było ogólnie zgodne w przypadku narkotyków. Stwierdzenie zwiększonego ryzyka w przypadku LPP o różnych mechanizmach działania i przy wielu wskazaniach sugeruje, że ryzyko dotyczy wszystkich LPP stosowanych w dowolnym wskazaniu. W analizowanych badaniach klinicznych ryzyko nie różniło się znacząco w zależności od wieku (5–100 lat). Tabela 2 przedstawia bezwzględne i względne ryzyko według wskazań dla wszystkich ocenianych LPP.
TABELA 2: Ryzyko według wskazań dla leków przeciwpadaczkowych w analizie zbiorczej
Względne ryzyko myśli lub zachowań samobójczych było wyższe w badaniach klinicznych dotyczących padaczki niż w badaniach klinicznych dotyczących zaburzeń psychicznych lub innych, ale bezwzględne różnice ryzyka były podobne dla padaczki i wskazań psychiatrycznych.
Każdy, kto rozważa przepisanie leku NEURONTIN 100 mg lub innego LPP, musi zrównoważyć ryzyko myśli lub zachowań samobójczych z ryzykiem nieleczonej choroby. Padaczka i wiele innych chorób, na które przepisywane są leki przeciwpadaczkowe, same w sobie wiążą się z zachorowalnością i śmiertelnością oraz zwiększonym ryzykiem myśli i zachowań samobójczych. Jeśli myśli i zachowania samobójcze pojawią się podczas leczenia, lekarz przepisujący lek powinien rozważyć, czy pojawienie się tych objawów u danego pacjenta może być związane z leczoną chorobą.
Należy poinformować pacjentów, ich opiekunów i rodziny, że leki przeciwpadaczkowe zwiększają ryzyko myśli i zachowań samobójczych oraz o konieczności zachowania czujności w przypadku pojawienia się lub nasilenia objawów depresji, wszelkich nietypowych zmian nastroju lub zachowania lub pojawienie się myśli samobójczych, zachowań lub myśli o samookaleczeniu. Zachowania budzące niepokój należy niezwłocznie zgłaszać świadczeniodawcom.
Niewydolność oddechowa
Istnieją dowody z opisów przypadków, badań na ludziach i badaniach na zwierzętach, łączące gabapentynę z poważną, zagrażającą życiu lub śmiertelną depresją oddechową w przypadku jednoczesnego podawania z lekami hamującymi OUN, w tym opioidami, lub w przypadku współistniejących zaburzeń oddechowych. Kiedy zostanie podjęta decyzja o przepisaniu NEURONTIN 100 mg z innym lekiem hamującym czynność ośrodkowego układu nerwowego, zwłaszcza opioidem, lub przepisanie NEURONTIN 100 mg pacjentom z podstawowymi zaburzeniami oddychania, należy monitorować pacjentów pod kątem objawów depresji oddechowej i sedacji oraz rozważyć rozpoczęcie stosowania NEURONTIN w małej dawce . Postępowanie w depresji oddechowej może obejmować ścisłą obserwację, środki wspomagające oraz zmniejszenie lub odstawienie leków depresyjnych na OUN (w tym NEURONTIN).
Neuropsychiatryczne reakcje niepożądane (pacjenci pediatryczni w wieku od 3 do 12 lat)
Stosowanie gabapentyny u dzieci i młodzieży z padaczką w wieku od 3 do 12 lat wiąże się z występowaniem działań niepożądanych związanych z ośrodkowym układem nerwowym. Najistotniejsze z nich można podzielić na następujące kategorie: 1) labilność emocjonalna (głównie problemy behawioralne), 2) wrogość, w tym zachowania agresywne, 3) zaburzenia myślenia, w tym problemy z koncentracją i zmiany wyników w szkole oraz 4) hiperkinezja ( przede wszystkim niepokój i nadpobudliwość). Wśród pacjentów leczonych gabapentyną większość reakcji miała nasilenie łagodne do umiarkowanego.
kontrolowanych badaniach klinicznych dotyczących padaczki u dzieci w wieku od 3 do 12 lat częstość występowania tych działań niepożądanych wynosiła: chwiejność emocjonalna 6% (pacjenci leczeni gabapentyną) w porównaniu do 1,3% (pacjenci leczeni placebo); wrogość 5,2% wobec 1,3%; hiperkinezja 4,7% w porównaniu z 2,9%; i zaburzenia myśli 1,7% w porównaniu do 0%. Jedną z tych reakcji, doniesienie o wrogości, uznano za poważną. Przerwanie leczenia gabapentyną wystąpiło u 1,3% pacjentów zgłaszających labilność emocjonalną i hiperkinezę oraz u 0,9% pacjentów leczonych gabapentyną zgłaszających wrogość i zaburzenia myślenia. Jeden pacjent otrzymujący placebo (0,4%) wycofał się z powodu chwiejności emocjonalnej.
Potencjał rakotwórczy
W badaniu rakotwórczości jamy ustnej gabapentyna zwiększała częstość występowania nowotworów z komórek groniastych trzustki u szczurów [patrz Toksykologia niekliniczna ]. Kliniczne znaczenie tego odkrycia nie jest znane. Doświadczenie kliniczne z okresu przed wprowadzeniem do obrotu gabapentyny nie dostarcza żadnych bezpośrednich środków do oceny jej potencjału do wywoływania nowotworów u ludzi.
W badaniach klinicznych dotyczących terapii wspomagającej w padaczce, obejmujących 2085 pacjento-lat ekspozycji u pacjentów w wieku >12 lat, nowe nowotwory zgłoszono u 10 pacjentów (2 piersi, 3 mózgu, 2 płuca, 1 nadnercza, 1 nieziarnicze; s chłoniak, 1 rak endometrium in situ) i istniejące wcześniej nowotwory pogorszyły się u 11 pacjentów (9 mózgów, 1 pierś, 1 prostata) w czasie lub do 2 lat po odstawieniu leku NEURONTIN. Bez znajomości podstawowej zachorowalności i nawrotów w podobnej populacji nieleczonej NEURONTIN 100 mg, nie jest możliwe ustalenie, czy leczenie ma wpływ na częstość występowania obserwowaną w tej kohorcie.
Nagła i niewyjaśniona śmierć u pacjentów z padaczką
trakcie opracowywania produktu NEURONTIN 400 mg przed wprowadzeniem do obrotu zarejestrowano 8 nagłych i niewyjaśnionych zgonów w kohorcie 2203 pacjentów z padaczką leczonych (2103 pacjento-lat ekspozycji) na NEURONTIN.
Niektóre z nich mogą reprezentować zgony związane z napadami, w których napad nie był obserwowany, np. w nocy. Odpowiada to częstości zgonów 0,0038 na pacjentorok. Chociaż wskaźnik ten przekracza oczekiwany w zdrowej populacji dobranej pod względem wieku i płci, mieści się w zakresie szacowanej częstości występowania nagłych niewyjaśnionych zgonów u pacjentów z padaczką nieotrzymujących NEURONTIN (od 0,0005 dla ogólnej populacji chorych na padaczkę do 0,003 dla populacja badań klinicznych podobna do tej w programie NEURONTIN, do 0,005 dla pacjentów z padaczką oporną na leczenie). W związku z tym to, czy liczby te są uspokajające, czy też budzą dalsze obawy, zależy od porównywalności populacji zgłoszonych do kohorty NEURONTIN i dokładności przedstawionych szacunków.
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( Przewodnik po lekach ).
Informacje administracyjne
Należy poinformować pacjentów, że NEURONTIN jest przyjmowany doustnie z jedzeniem lub bez jedzenia. Należy poinformować pacjentów, że jeśli podzielą podzieloną tabletkę 600 mg lub 800 mg w celu podania połowy tabletki, powinni przyjąć niewykorzystaną połowę tabletki jako kolejną dawkę. Należy doradzić pacjentom, aby wyrzucili połówki tabletek, które nie zostały zużyte w ciągu 28 dni od podzielenia tabletki z linią podziału.
Reakcja polekowa z eozynofilią i objawami ogólnoustrojowymi (DRESS)/nadwrażliwość wielonarządowa
Przed rozpoczęciem leczenia preparatem NEURONTIN należy poinstruować pacjentów, że wysypka lub inne oznaki lub objawy nadwrażliwości (takie jak gorączka lub powiększenie węzłów chłonnych) mogą zwiastować poważne zdarzenie medyczne i że pacjent powinien niezwłocznie zgłosić to lekarzowi [patrz OSTRZEŻENIA I ŚRODKI ].
Anafilaksja i obrzęk naczynioruchowy
Należy doradzić pacjentom, aby przerwali stosowanie leku NEURONTIN 300 mg i zgłosili się do lekarza, jeśli wystąpią u nich objawy anafilaksji lub obrzęku naczynioruchowego [patrz OSTRZEŻENIA I ŚRODKI ].
Zawroty głowy i senność oraz wpływ na prowadzenie i obsługę ciężkich maszyn
Poinformuj pacjentów, że NEURONTIN 100 mg może powodować zawroty głowy, senność oraz inne objawy i oznaki depresji ośrodkowego układu nerwowego. Inne leki o właściwościach uspokajających mogą nasilać te objawy. W związku z tym, chociaż pacjenci zdolność do określenia poziomu upośledzenia może być niewiarygodna, należy odradzać prowadzenie samochodu ani obsługiwanie innych skomplikowanych maszyn, dopóki nie zdobędą wystarczającego doświadczenia w stosowaniu leku NEURONTIN, aby ocenić, czy wpływa to niekorzystnie na ich sprawność umysłową i/lub motoryczną. Poinformuj pacjentów, że nie wiadomo, jak długo utrzymuje się ten efekt [patrz OSTRZEŻENIA I ŚRODKI oraz OSTRZEŻENIA I ŚRODKI ].
Myślenie i zachowanie samobójcze
Poinformuj pacjenta, jego opiekunów i rodziny, że leki przeciwpadaczkowe, w tym NEURONTIN, mogą zwiększać ryzyko myśli i zachowań samobójczych. Poinformuj pacjentów o potrzebie zachowania czujności w przypadku pojawienia się lub nasilenia objawów depresji, wszelkich nietypowych zmian nastroju lub zachowania lub pojawienia się myśli, zachowań samobójczych lub myśli o samookaleczeniu. Poinstruuj pacjentów, aby natychmiast zgłaszali niepokojące zachowania świadczeniodawcom opieki zdrowotnej [patrz OSTRZEŻENIA I ŚRODKI ].
Niewydolność oddechowa
Poinformuj pacjentów o ryzyku wystąpienia depresji oddechowej. Uwzględnij informację, że ryzyko jest największe w przypadku osób stosujących jednocześnie leki działające depresyjnie na ośrodkowy układ nerwowy (takie jak opioidowe leki przeciwbólowe) lub osoby z podstawowymi zaburzeniami oddychania. Naucz pacjentów, jak rozpoznawać depresję oddechową i doradzaj im, aby natychmiast zwrócili się o pomoc lekarską, jeśli się pojawi [patrz OSTRZEŻENIA I ŚRODKI ].
Użyj w ciąży
Należy poinstruować pacjentki, aby powiadomiły lekarza, jeśli zajdą w ciążę lub zamierzają zajść w ciążę w trakcie terapii, oraz powiadomiły lekarza, jeśli karmią piersią lub zamierzają karmić piersią w trakcie leczenia [patrz Używaj w określonych populacjach ].
Zachęć pacjentki do zapisania się do rejestru ciąż NAAED, jeśli zajdą w ciążę. Rejestr ten gromadzi informacje o bezpieczeństwie leków przeciwpadaczkowych w czasie ciąży. Aby się zapisać, pacjenci mogą zadzwonić pod bezpłatny numer 1-888-233-2334 [patrz Używaj w określonych populacjach ].
Etykieta tego produktu mogła zostać zaktualizowana. Najnowsze informacje na temat przepisywania leków można znaleźć na stronie www.pfizer.com.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Karcynogeneza
Gabapentyna podawano doustnie myszom i szczurom w 2-letnich badaniach rakotwórczości. Nie zaobserwowano dowodów na rakotwórczość związaną z lekiem u myszy leczonych dawkami do 2000 mg/kg/dobę. Przy 2000 mg/kg ekspozycja na gabapentynę w osoczu (AUC) u myszy była około 2 razy większa niż u ludzi przy MRHD 3600 mg/dobę. U szczurów stwierdzono zwiększenie częstości występowania gruczolaka i raka komórek zrazikowych trzustki u samców szczurów otrzymujących najwyższą dawkę (2000 mg/kg), ale nie w dawkach 250 lub 1000 mg/kg/dobę. Przy dawce 1000 mg/kg ekspozycja na gabapentynę w osoczu (AUC) u szczurów była około 5 razy większa niż u ludzi przy MRHD.
Badania zaprojektowane w celu zbadania mechanizmu indukowanej przez gabapentynę karcynogenezy trzustki u szczurów wskazują, że gabapentyna stymuluje syntezę DNA w szczurzych komórkach groniastych trzustki in vitro, a zatem może działać jako promotor nowotworu poprzez wzmacnianie aktywności mitogennej. Nie wiadomo, czy gabapentyna ma zdolność zwiększania proliferacji komórek w innych typach komórek lub u innych gatunków, w tym u ludzi.
Mutageneza
Gabapentyna nie wykazywała potencjału mutagennego ani genotoksycznego in vitro (test Amesa, test postępującej mutacji HGPRT w komórkach płuc chomika chińskiego) i in vivo (aberracje chromosomowe i test mikrojądrowy w szpiku kostnym chomika chińskiego, mikrojądra myszy, nieplanowana synteza DNA w hepatocytach szczura) testy.
Upośledzenie płodności
Nie zaobserwowano niekorzystnego wpływu na płodność lub reprodukcję u szczurów przy dawkach do 2000 mg/kg. Przy 2000 mg/kg ekspozycja na gabapentynę w osoczu (AUC) u szczurów jest około 8 razy większa niż u ludzi przy MRHD.
Używaj w określonych populacjach
Ciąża
Rejestr ekspozycji w ciąży
Istnieje rejestr ekspozycji w czasie ciąży, który monitoruje przebieg ciąży u kobiet narażonych w czasie ciąży na leki przeciwpadaczkowe (LPP), takie jak NEURONTIN 300 mg. Zachęć kobiety przyjmujące NEURONTIN w czasie ciąży do zapisania się do Rejestru Ciąży Północnoamerykańskich Leków Przeciwpadaczkowych (NAAED), dzwoniąc pod bezpłatny numer 1-888-233-2334 lub odwiedzając stronę http://www.aedpregnancyregistry.org/.
Podsumowanie ryzyka
Brak odpowiednich danych dotyczących ryzyka rozwojowego związanego ze stosowaniem preparatu NEURONTIN u kobiet w ciąży. W badaniach nieklinicznych na myszach, szczurach i królikach gabapentyna podawana ciężarnym zwierzętom w dawkach podobnych lub mniejszych niż dawki stosowane klinicznie, była toksyczna dla rozwoju (zwiększone nieprawidłowości szkieletowe i trzewne płodu oraz zwiększona śmiertelność zarodków i płodów). Dane ].
ogólnej populacji USA szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2 do 4% i 15 do 20%. Podstawowe ryzyko poważnych wad wrodzonych i poronienia dla wskazanej populacji jest nieznane.
Dane
Dane zwierząt
Gdy ciężarne myszy otrzymywały doustne dawki gabapentyny (500, 1000 lub 3000 mg/kg/dobę) w okresie organogenezy, toksyczność dla zarodka i płodu (zwiększona częstość występowania zmienności kośćca) obserwowano przy dwóch najwyższych dawkach. Dawka niepowodująca toksycznego wpływu na rozwój zarodka i płodu u myszy (500 mg/kg/dobę) jest mniejsza niż maksymalna zalecana dawka dla człowieka (MRHD) wynosząca 3600 mg na powierzchnię ciała (mg/m²).
W badaniach, w których szczury otrzymywały doustne dawki gabapentyny (500 do 2000 mg/kg/dobę) w czasie ciąży, we wszystkich dawkach obserwowano niekorzystny wpływ na rozwój potomstwa (zwiększona częstość występowania wodniaka moczowodowego i (lub) wodonercza). Najniższa testowana dawka jest podobna do MRHD na podstawie mg/m².
Gdy ciężarne króliki były leczone gabapentyną w okresie organogenezy, obserwowano wzrost śmiertelności zarodków i płodów we wszystkich badanych dawkach (60, 300 lub 1500 mg/kg). Najniższa testowana dawka jest mniejsza niż MRHD na podstawie mg/m².
W opublikowanym badaniu gabapentynę (400 mg/kg/dobę) podawano we wstrzyknięciu dootrzewnowym noworodkom myszy w pierwszym tygodniu po urodzeniu, okresie synaptogenezy u gryzoni (odpowiadającym ostatniemu trymestrowi ciąży u ludzi). Gabapentyna powodowała znaczne zmniejszenie tworzenia się synaps neuronalnych w mózgach nienaruszonych myszy i nieprawidłowe tworzenie synaps neuronalnych w mysim modelu naprawy synaptycznej. Wykazano in vitro, że gabapentyna wpływa na aktywność podjednostki α2δ kanałów wapniowych aktywowanych napięciem, receptora zaangażowanego w synaptogenezę neuronów. Kliniczne znaczenie tych wyników nie jest znane.
Laktacja
Podsumowanie ryzyka
Gabapentyna jest wydzielana do mleka ludzkiego po podaniu doustnym. Wpływ na niemowlę karmione piersią i na produkcję mleka nie jest znany. Należy wziąć pod uwagę korzyści rozwojowe i zdrowotne wynikające z karmienia piersią, a także kliniczne zapotrzebowanie matki na NEURONTIN i wszelkie potencjalne niekorzystne skutki działania NEURONTIN na karmione piersią niemowlę lub wynikające z podstawowej choroby matki.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność NEURONTIN 600 mg w leczeniu neuralgii popółpaścowej u dzieci nie zostały ustalone.
Bezpieczeństwo i skuteczność terapii wspomagającej w leczeniu napadów częściowych u dzieci w wieku poniżej 3 lat nie zostały ustalone [patrz Studia kliniczne ].
Zastosowanie geriatryczne
Całkowita liczba pacjentów leczonych preparatem NEURONTIN w kontrolowanych badaniach klinicznych z udziałem pacjentów z neuralgią popółpaścową wyniosła 336, z czego 102 (30%) było w wieku 65 do 74 lat, a 168 (50%) miało 75 lat i więcej. Efekt leczenia był większy u pacjentów w wieku 75 lat i starszych w porównaniu z młodszymi pacjentami, którzy otrzymali tę samą dawkę. Ponieważ gabapentyna jest prawie wyłącznie wydalana przez nerki, silniejszy efekt leczenia obserwowany u pacjentów w wieku ≥75 lat może być konsekwencją zwiększonej ekspozycji na gabapentynę dla danej dawki, która wynika ze związanego z wiekiem osłabienia czynności nerek. Nie można jednak wykluczyć innych czynników. Rodzaje i częstość występowania działań niepożądanych były podobne we wszystkich grupach wiekowych, z wyjątkiem obrzęków obwodowych i ataksji, których częstość występowania wzrastała wraz z wiekiem.
Badania kliniczne NEURONTIN w padaczce nie obejmowały wystarczającej liczby osób w wieku 65 lat i starszych, aby ustalić, czy reagują oni inaczej niż osoby młodsze. Inne zgłoszone doświadczenia kliniczne nie wykazały różnic w odpowiedziach między pacjentami w podeszłym wieku i młodszymi. Ogólnie rzecz biorąc, dobór dawki u pacjentów w podeszłym wieku powinien być ostrożny, zwykle zaczynając od dolnej granicy zakresu dawkowania, co odzwierciedla większą częstość pogorszenia czynności wątroby, nerek lub serca oraz współistniejących chorób lub innych leków.
Wiadomo, że lek ten jest w znacznym stopniu wydalany przez nerki, a ryzyko reakcji toksycznych na ten lek może być większe u pacjentów z zaburzeniami czynności nerek. Ponieważ u pacjentów w podeszłym wieku istnieje większe prawdopodobieństwo upośledzenia czynności nerek, należy zachować ostrożność przy doborze dawki, a dawkę należy dostosować na podstawie wartości klirensu kreatyniny u tych pacjentów [patrz DAWKOWANIE I SPOSÓB PODAWANIA , DZIAŁANIA NIEPOŻĄDANE , oraz FARMAKOLOGIA KLINICZNA ].
Zaburzenia czynności nerek
Konieczna jest modyfikacja dawkowania u dorosłych pacjentów z zaburzeniami czynności nerek [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz FARMAKOLOGIA KLINICZNA ]. Nie badano pacjentów pediatrycznych z niewydolnością nerek.
Konieczne jest dostosowanie dawki u pacjentów poddawanych hemodializie [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
Objawy ostrej toksyczności u zwierząt obejmowały ataksję, ciężki oddech, opadanie powiek, uspokojenie, hipoaktywność lub pobudzenie.
Zgłaszano przypadki ostrego przedawkowania doustnego preparatu NEURONTIN 300 mg. Objawy obejmowały podwójne widzenie, drżenie, niewyraźną mowę, senność, zaburzenia psychiczne, zawroty głowy, letarg i biegunkę. Po przedawkowaniu 400 mg preparatu NEURONTIN w monoterapii lub w skojarzeniu z innymi lekami działającymi depresyjnie na ośrodkowy układ nerwowy zgłaszano śmiertelną depresję oddechową.
Gabapentyna może być usunięta przez hemodializę.
W przypadku nadmiernego narażenia zadzwoń do centrum kontroli zatruć pod numer 1-800-222-1222.
PRZECIWWSKAZANIA
NEURONTIN jest przeciwwskazany u pacjentów, u których stwierdzono nadwrażliwość na lek lub jego składniki.
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Dokładne mechanizmy działania przeciwbólowego i przeciwpadaczkowego gabapentyny są nieznane. Gabapentyna jest strukturalnie powiązana z neuroprzekaźnikiem kwasu gamma-aminomasłowego (GABA), ale nie ma wpływu na wiązanie, wychwyt lub degradację GABA. Badania in vitro wykazały, że gabapentyna wiąże się z wysokim powinowactwem z podjednostką α2δ kanałów wapniowych aktywowanych napięciem; jednak związek tego wiązania z efektami terapeutycznymi gabapentyny jest nieznany.
Farmakokinetyka
Wszystkie działania farmakologiczne po podaniu gabapentyny wynikają z aktywności związku macierzystego; gabapentyna nie jest w znacznym stopniu metabolizowana u ludzi.
Biodostępność po podaniu doustnym
Dostępność biologiczna gabapentyny nie jest proporcjonalna do dawki; tj. wraz ze wzrostem dawki zmniejsza się biodostępność. Biodostępność gabapentyny wynosi około 60%, 47%, 34%, 33% i 27% po podaniu odpowiednio 900, 1200, 2400, 3600 i 4800 mg/dobę w 3 dawkach podzielonych. Pokarm ma tylko niewielki wpływ na szybkość i stopień wchłaniania gabapentyny (wzrost AUC i Cmax o 14%).
Dystrybucja
Mniej niż 3% gabapentyny krąży w postaci związanej z białkami osocza. Pozorna objętość dystrybucji gabapentyny po podaniu dożylnym 150 mg wynosi 58±6 l (średnia ±SD). U pacjentów z padaczką stężenie gabapentyny w płynie mózgowo-rdzeniowym w stanie stacjonarnym przed podaniem dawki (Cmin) wynosiło około 20% odpowiednich stężeń w osoczu.
Eliminacja
Gabapentyna jest wydalana z krążenia ogólnego przez nerki w postaci niezmienionej. Gabapentyna nie jest w znacznym stopniu metabolizowana u ludzi.
Okres półtrwania gabapentyny w fazie eliminacji wynosi od 5 do 7 godzin i nie zmienia się w zależności od dawki lub po wielokrotnym podaniu. Stała szybkości eliminacji gabapentyny, klirens osoczowy i klirens nerkowy są wprost proporcjonalne do klirensu kreatyniny. U pacjentów w podeszłym wieku oraz u pacjentów z zaburzeniami czynności nerek klirens gabapentyny w osoczu jest zmniejszony. Gabapentyna może być usunięta z osocza za pomocą hemodializy.
Określone populacje
Wiek
Wpływ wieku badano u osób w wieku 20–80 lat. Pozorny klirens doustny (CL/F) gabapentyny zmniejszał się wraz z wiekiem, od około 225 ml/min u osób poniżej 30. roku życia do około 125 ml/min u osób powyżej 70. roku życia. Klirens nerkowy (CLr) i CLr dostosowane do powierzchni ciała również malały wraz z wiekiem; jednakże spadek klirensu nerkowego gabapentyny wraz z wiekiem można w dużej mierze wytłumaczyć pogorszeniem czynności nerek. [Widzieć DAWKOWANIE I SPOSÓB PODAWANIA oraz Używaj w określonych populacjach ].
Płeć
Chociaż nie przeprowadzono formalnych badań w celu porównania farmakokinetyki gabapentyny u mężczyzn i kobiet, wydaje się, że parametry farmakokinetyczne dla mężczyzn i kobiet są podobne i nie ma znaczących różnic między płciami.
Wyścig
Nie badano różnic farmakokinetycznych ze względu na rasę. Ponieważ gabapentyna jest wydalana głównie przez nerki i nie ma istotnych różnic rasowych w klirensie kreatyniny, nie oczekuje się różnic farmakokinetycznych związanych z rasą.
Pediatryczny
Farmakokinetykę gabapentyny określono u 48 pacjentów pediatrycznych w wieku od 1 miesiąca do 12 lat po podaniu dawki około 10 mg/kg. Maksymalne stężenia w osoczu były podobne w całej grupie wiekowej i występowały 2 do 3 godzin po podaniu. Ogólnie rzecz biorąc, dzieci w wieku od 1 miesiąca do
Analizę farmakokinetyki populacyjnej przeprowadzono u 253 pacjentów pediatrycznych w wieku od 1 miesiąca do 13 lat. Pacjenci otrzymywali od 10 do 65 mg/kg/dobę trzy razy dziennie. Pozorny klirens po podaniu doustnym (CL/F) był wprost proporcjonalny do klirensu kreatyniny i zależność ta była podobna po podaniu pojedynczej dawki iw stanie stacjonarnym. Większe wartości klirensu po podaniu doustnym obserwowano u dzieci w wieku
Te dane farmakokinetyczne wskazują, że skuteczna dawka dobowa u dzieci i młodzieży z padaczką w wieku 3 i 4 lat powinna wynosić 40 mg/kg/dobę, aby osiągnąć średnie stężenia w osoczu podobne do uzyskiwanych u pacjentów w wieku 5 lat i starszych otrzymujących gabapentynę w dawce 30 mg/dobę. kg/dzień [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Dorośli pacjenci z zaburzeniami czynności nerek
Osobom (N=60) z zaburzeniami czynności nerek (średni klirens kreatyniny 13–114 ml/min) podawano doustnie pojedynczą dawkę 400 mg gabapentyny. Średni okres półtrwania gabapentyny wahał się od około 6,5 godziny (pacjenci z klirensem kreatyniny >60 ml/min) do 52 godzin (klirens kreatyniny 60 ml/min) grupy) do około 10 ml/min ( DAWKOWANIE I SPOSÓB PODAWANIA oraz Używaj w określonych populacjach ]. Nie badano pacjentów pediatrycznych z niewydolnością nerek.
Hemodializa
badaniu z udziałem dorosłych pacjentów z bezmoczem (N=11) pozorny okres półtrwania w fazie eliminacji gabapentyny w dniach bez dializy wynosił około 132 godziny; podczas dializy pozorny okres półtrwania gabapentyny został skrócony do 3,8 godziny. Hemodializa ma zatem istotny wpływ na eliminację gabapentyny u osób z bezmoczem [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz Używaj w określonych populacjach ].
Choroba wątroby
Ponieważ gabapentyna nie jest metabolizowana, nie przeprowadzono badań u pacjentów z zaburzeniami czynności wątroby.
Interakcje leków
Badania in vitro
Przeprowadzono badania in vitro w celu zbadania potencjału gabapentyny w hamowaniu głównych enzymów cytochromu P450 (CYP1A2, CYP2A6, CYP2C9, CYP2C19, CYP2D6, CYP2E1 i CYP3A4), które pośredniczą w metabolizmie leków i ksenobiotyków, przy użyciu substratów markerów selekcyjnych izoform i preparatów mikrosomalnych wątroby ludzkiej . Jedynie przy najwyższym badanym stężeniu (171 µg/ml; 1 µM) zaobserwowano niewielki stopień zahamowania (14% do 30%) izoformy CYP2A6. Nie zaobserwowano hamowania żadnej z pozostałych badanych izoform przy stężeniach gabapentyny do 171 μg/ml (około 15-krotność Cmax przy 3600 mg/dobę) obserwowanej izoformy CYP2A6. Nie zaobserwowano hamowania żadnej z pozostałych badanych izoform przy stężeniach gabapentyny do 171 µg/ml (około 15-krotność Cmax przy 3600 mg/dobę).
Badania in vivo
Opisane w tym punkcie dane dotyczące interakcji leków uzyskano z badań z udziałem zdrowych osób dorosłych i dorosłych pacjentów z padaczką.
Fenytoina
badaniu z pojedynczą (400 mg) i wielokrotną (400 mg trzy razy na dobę) dawką NEURONTIN 400 mg u pacjentów z padaczką (N=8) utrzymywanych w monoterapii fenytoiną przez co najmniej 2 miesiące, gabapentyna nie miała wpływu na najmniejszą dawkę w stanie stacjonarnym stężenia fenytoiny i fenytoiny w osoczu nie miały wpływu na farmakokinetykę gabapentyny.
Karbamazepina
Równoczesne podawanie gabapentyny (400 mg trzy razy na dobę; N=12) nie miało wpływu na stężenie minimalne karbamazepiny w osoczu i karbamazepiny 10, 11 w stanie stacjonarnym. Podobnie farmakokinetyka gabapentyny nie uległa zmianie po podaniu karbamazepiny.
Kwas walproinowy
Średnie minimalne stężenia kwasu walproinowego w surowicy w stanie stacjonarnym przed i podczas jednoczesnego podawania gabapentyny (400 mg trzy razy na dobę; N=17) nie różniły się, podobnie jak parametry farmakokinetyczne gabapentyny nie miały wpływu na kwas walproinowy.
Fenobarbital
Szacunkowe parametry farmakokinetyczne w stanie stacjonarnym dla fenobarbitalu lub gabapentyny (300 mg trzy razy na dobę; N=12) są identyczne niezależnie od tego, czy leki podaje się osobno, czy razem.
Naproksen
Jednoczesne podawanie (N=18) kapsułek naproksenu sodowego (250 mg) z NEURONTIN (125 mg) wydaje się zwiększać ilość wchłanianej gabapentyny o 12% do 15%. Gabapentyna nie miała wpływu na parametry farmakokinetyczne naproksenu. Dawki te są niższe niż dawki terapeutyczne obu leków. Wielkość interakcji w zalecanych zakresach dawek obu leków nie jest znana.
hydrokodon
Jednoczesne podawanie NEURONTIN (125 do 500 mg; N=48) zmniejsza wartości Cmax i AUC hydrokodonu (10 mg; N=50) w sposób zależny od dawki w stosunku do podawania samego hydrokodonu; Wartości Cmax i AUC są odpowiednio o 3% do 4% mniejsze po podaniu 125 mg NEURONTIN i 21% do 22% mniejsze po podaniu 500 mg NEURONTIN. Mechanizm tej interakcji jest nieznany. Hydrokodon zwiększa wartości AUC gabapentyny o 14%. Wielkość interakcji przy innych dawkach nie jest znana.
Morfina
Artykuł literaturowy donosił, że gdy kapsułka z morfiną o kontrolowanym uwalnianiu 60 mg została podana 2 godziny przed kapsułką 600 mg NEURONTIN (N=12), średnie AUC gabapentyny zwiększyło się o 44% w porównaniu do gabapentyny podawanej bez morfiny. Na wartości parametrów farmakokinetycznych morfiny nie miało wpływu podanie NEURONTIN 2 godziny po podaniu morfiny. Wielkość interakcji przy innych dawkach nie jest znana.
Cymetydyna
obecności cymetydyny w dawce 300 mg cztery razy na dobę (N=12) średni pozorny klirens gabapentyny po podaniu doustnym zmniejszył się o 14%, a klirens kreatyniny o 10%. Tak więc, cymetydyna wydawała się zmieniać wydalanie nerkowe zarówno gabapentyny, jak i kreatyniny, endogennego markera czynności nerek. Nie przewiduje się, aby to niewielkie zmniejszenie wydalania gabapentyny przez cymetydynę miało znaczenie kliniczne. Nie oceniano wpływu gabapentyny na cymetydynę.
Doustnych środków antykoncepcyjnych
Na podstawie AUC i okresu półtrwania, profile farmakokinetyczne wielokrotnych dawek noretyndronu i etynyloestradiolu po podaniu tabletek zawierających 2,5 mg octanu noretyndronu i 50 mcg etynyloestradiolu były podobne przy jednoczesnym podawaniu gabapentyny i bez niego (400 mg trzy razy na dobę; N=13). Cmax noretyndronu był o 13% wyższy, gdy był podawany jednocześnie z gabapentyną; nie oczekuje się, że ta interakcja będzie miała znaczenie kliniczne.
Środek zobojętniający kwas (Maalox®) (wodorotlenek glinu, wodorotlenek magnezu)
Środek zobojętniający kwas (Maalox®) zawierający wodorotlenki magnezu i glinu zmniejszał średnią biodostępność gabapentyny (N=16) o około 20%. Ten spadek biodostępności wyniósł około 10%, gdy gabapentynę podawano 2 godziny po podaniu preparatu Maalox.
Probenecyd
Probenecyd jest blokerem wydzielania kanalików nerkowych. Parametry farmakokinetyczne gabapentyny bez i z probenecydem były porównywalne. Wskazuje to, że gabapentyna nie podlega wydzielaniu w kanalikach nerkowych drogą blokowaną przez probenecyd.
Studia kliniczne
Neuralgia popółpaścowa
NEURONTIN oceniano pod kątem leczenia neuralgii popółpaścowej (PHN) w dwóch wieloośrodkowych, randomizowanych badaniach z podwójnie ślepą próbą, kontrolowanych placebo. Populacja intent-to-treat (ITT) składała się łącznie z 563 pacjentów z bólem przez ponad 3 miesiące po wygojeniu wysypki skórnej z półpaśca (Tabela 6).
TABELA 6. Kontrolowane badania PHN: czas trwania, dawki i liczba pacjentów
Każde badanie obejmowało 7- lub 8-tygodniową fazę podwójnie ślepej próby (3 lub 4 tygodnie miareczkowania i 4 tygodnie stałej dawki). Pacjenci rozpoczynali leczenie od zwiększania dawki do maksymalnie 900 mg/dobę gabapentyny przez 3 dni. Dawki miały być następnie dostosowywane w krokach od 600 do 1200 mg/dobę w odstępach od 3 do 7 dni do dawki docelowej przez 3 do 4 tygodni. Pacjenci zapisywali swój ból w codziennym dzienniczku za pomocą 11-punktowej numerycznej skali oceny bólu w zakresie od 0 (brak bólu) do 10 (najgorszy możliwy ból). Do randomizacji wymagany był średni wynik oceny bólu podczas wizyty początkowej wynoszący co najmniej 4 punkty. Analizy przeprowadzono z wykorzystaniem populacji ITT (wszyscy zrandomizowani pacjenci, którzy otrzymali co najmniej jedną dawkę badanego leku).
Oba badania wykazały skuteczność w porównaniu z placebo we wszystkich testowanych dawkach.
Zmniejszenie średnich tygodniowych wyników oceny bólu zaobserwowano w pierwszym tygodniu w obu badaniach i utrzymywało się do końca leczenia. Porównywalne efekty leczenia zaobserwowano we wszystkich aktywnych ramionach leczenia. Modelowanie farmakokinetyczne/farmakodynamiczne dostarczyło dowodów potwierdzających skuteczność we wszystkich dawkach. Ryciny 1 i 2 przedstawiają wyniki intensywności bólu w czasie w badaniach 1 i 2.
Rycina 1. Średnie tygodniowe wyniki oceny bólu (obserwowane przypadki w populacji ITT): Badanie 1
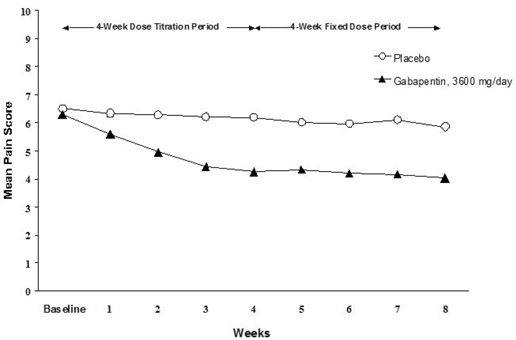
Rycina 2. Średnie tygodniowe wyniki oceny bólu (obserwowane przypadki w populacji ITT): Badanie 2
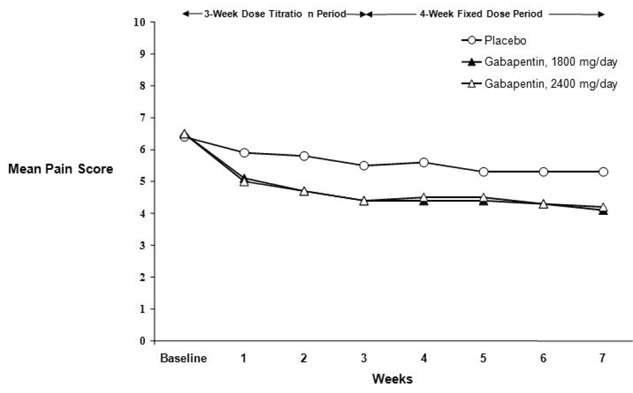
Dla każdego badania obliczono odsetek osób odpowiadających (ci pacjenci zgłaszający co najmniej 50% poprawę w punktacji punktowej oceny bólu w porównaniu z wartością wyjściową) (Rysunek 3).
Rycina 3. Odsetek osób odpowiadających (pacjenci z ≥50% zmniejszeniem wskaźnika bólu) w punkcie końcowym: kontrolowane badania nad PHN
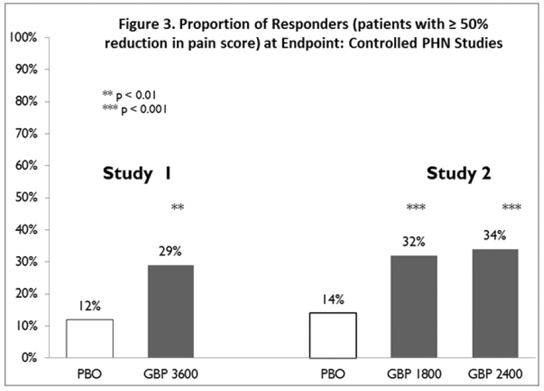
Padaczka w przypadku napadów o częściowym początku (terapia wspomagająca)
Skuteczność preparatu NEURONTIN 400 mg jako terapii wspomagającej (dodanej do innych leków przeciwpadaczkowych) ustalono w wieloośrodkowych, kontrolowanych placebo badaniach klinicznych z podwójnie ślepą próbą, prowadzonych w grupach równoległych u dorosłych i dzieci (w wieku 3 lat i starszych) z opornymi na leczenie napadami częściowymi.
Dowody skuteczności uzyskano w trzech badaniach przeprowadzonych z udziałem 705 pacjentów (w wieku 12 lat i powyżej) oraz w jednym badaniu przeprowadzonym u 247 pacjentów pediatrycznych (w wieku od 3 do 12 lat). Włączeni pacjenci mieli w wywiadzie co najmniej 4 napady częściowe na miesiąc, pomimo otrzymywania jednego lub więcej leków przeciwpadaczkowych w dawkach terapeutycznych i byli obserwowani przy ustalonym schemacie leczenia przeciwpadaczkowego w 12-tygodniowym okresie początkowym (6 tygodni w badaniu pediatrycznym). pacjentów). U pacjentów, u których nadal występują co najmniej 2 (lub 4 w niektórych badaniach) napady w miesiącu, do dotychczasowej terapii w trakcie 12-tygodniowego okresu leczenia dodano NEURONTIN 300 mg lub placebo. Skuteczność oceniano przede wszystkim na podstawie odsetka pacjentów z 50% lub większym zmniejszeniem częstości napadów od wartości początkowej do leczenia („wskaźnik odpowiedzi”) oraz miary pochodnej zwanej współczynnikiem odpowiedzi, miarą zmiany zdefiniowaną jako (T - B)/(T + B), gdzie B jest wyjściową częstością napadów u pacjenta, a T jest częstością napadów u pacjenta podczas leczenia. Współczynnik odpowiedzi rozkłada się w zakresie od -1 do +1. Wartość zero wskazuje na brak zmian, podczas gdy całkowite wyeliminowanie napadów dałoby wartość -1; zwiększone wskaźniki napadów dawałyby wartości dodatnie. Stosunek odpowiedzi wynoszący -0,33 odpowiada 50% zmniejszeniu częstości napadów. Podane poniżej wyniki dotyczą wszystkich napadów częściowych w populacji ITT (wszyscy pacjenci, którzy otrzymali jakiekolwiek dawki leczenia) w każdym badaniu, chyba że wskazano inaczej.
jednym badaniu porównywano NEURONTIN 1200 mg/dobę w trzech podzielonych dawkach z placebo. Wskaźnik odpowiedzi wyniósł 23% (14/61) w grupie NEURONTIN 600 mg i 9% (6/66) w grupie placebo; różnica między grupami była istotna statystycznie. Współczynnik odpowiedzi był również lepszy w grupie NEURONTIN (-0,199) niż w grupie placebo (-0,044), różnica, która również osiągnęła istotność statystyczną.
drugim badaniu porównywano głównie NEURONTIN 1200 mg/dobę w trzech dawkach podzielonych (N=101) z placebo (N=98). Dodatkowe mniejsze grupy dawek 300 mg NEURONTIN (600 mg/dobę, N=53; 1800 mg/dobę, N=54) przebadano również pod kątem informacji dotyczących odpowiedzi na dawkę. Wskaźnik odpowiedzi był wyższy w grupie NEURONTIN 1200 mg/dobę (16%) niż w grupie placebo (8%), ale różnica nie była istotna statystycznie. Wskaźnik odpowiedzi przy 600 mg (17%) również nie był znacząco wyższy niż w grupie placebo, ale wskaźnik odpowiedzi w grupie 1800 mg (26%) był statystycznie istotnie wyższy niż wskaźnik placebo. Współczynnik odpowiedzi był lepszy w grupie NEURONTIN 1200 mg/dzień (-0,103) niż w grupie placebo (-0,022); ale ta różnica również nie była istotna statystycznie (p = 0,224). Lepszą odpowiedź zaobserwowano w grupie NEURONTIN 600 mg/dobę (-0,105) i 1800 mg/dobę (-0,222) niż w grupie 1200 mg/dobę, przy czym grupa 1800 mg/dobę osiągnęła istotność statystyczną w porównaniu z placebo Grupa.
trzecim badaniu porównywano NEURONTIN 900 mg/dobę w trzech dawkach podzielonych (N=111) i placebo (N=109). Dodatkowa grupa dawkująca NEURONTIN 1200 mg/dobę (N=52) dostarczyła danych dotyczących odpowiedzi na dawkę. Statystycznie istotną różnicę we wskaźniku odpowiedzi zaobserwowano w grupie NEURONTIN 900 mg/dobę (22%) w porównaniu z grupą placebo (10%). Wskaźnik odpowiedzi był również statystycznie istotnie lepszy w grupie NEURONTIN 900 mg/dobę (-0,119) w porównaniu z grupą placebo (-0,027), podobnie jak wskaźnik odpowiedzi w grupie 1200 mg/dobę NEURONTIN (-0,184) w porównaniu z placebo.
każdym badaniu przeprowadzono również analizy w celu zbadania wpływu leku NEURONTIN 300 mg na zapobieganie wtórnie uogólnionym napadom toniczno-klonicznym. Do tych analiz włączono pacjentów, u których wystąpiły wtórnie uogólnione napady toniczno-kloniczne w okresie początkowym lub w okresie leczenia we wszystkich trzech badaniach kontrolowanych placebo. Było kilka porównań współczynnika odpowiedzi, które wykazały statystycznie istotną przewagę dla NEURONTIN w porównaniu z placebo i korzystne trendy dla prawie wszystkich porównań.
Analiza wskaźnika odpowiedzi na podstawie połączonych danych ze wszystkich trzech badań i wszystkich dawek (N=162, NEURONTIN; N=89, placebo) również wykazała istotną przewagę NEURONTIN nad placebo w zmniejszaniu częstości wtórnie uogólnionych napadów toniczno-klonicznych.
dwóch z trzech kontrolowanych badań zastosowano więcej niż jedną dawkę NEURONTIN. W każdym badaniu wyniki nie wykazały konsekwentnie zwiększonej odpowiedzi na dawkę. Jednak patrząc na różne badania, widoczna jest tendencja do zwiększania skuteczności wraz ze wzrostem dawki (patrz Rysunek 4).
Rycina 4. Odsetek odpowiedzi u pacjentów otrzymujących NEURONTIN 600 mg wyrażony jako różnica w stosunku do placebo według dawki i badania: badania terapii wspomagającej u pacjentów w wieku ≥12 lat z napadami częściowymi
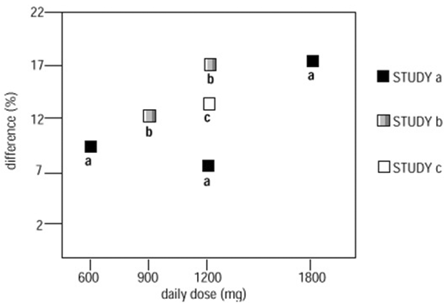
Na wykresie wielkość efektu leczenia, mierzona na osi Y jako różnica w proporcji pacjentów otrzymujących gabapentynę i pacjentów otrzymujących placebo, osiągających 50% lub więcej zmniejszenie częstości napadów w stosunku do wartości początkowej, wykreślono w stosunku do podawanej dziennej dawki gabapentyny. (oś X).
Chociaż nie przeprowadzono formalnej analizy ze względu na płeć, szacunki odpowiedzi (współczynnik odpowiedzi) pochodzące z badań klinicznych (398 mężczyzn, 307 kobiet) wskazują na brak istotnych różnic między płciami. Nie było spójnego wzorca wskazującego, że wiek miał jakikolwiek wpływ na odpowiedź na NEURONTIN. Liczba pacjentów ras innych niż kaukaska była niewystarczająca, aby umożliwić porównanie skuteczności między grupami rasowymi.
W czwartym badaniu z udziałem dzieci i młodzieży w wieku od 3 do 12 lat porównywano dawkę 25 –35 mg/kg/dobę NEURONTIN (N=118) z placebo (N=127). W przypadku wszystkich napadów częściowych w populacji ITT wskaźnik odpowiedzi był statystycznie istotnie lepszy w grupie NEURONTIN (-0,146) niż w grupie placebo (-0,079). W tej samej populacji wskaźnik odpowiedzi na NEURONTIN (21%) nie różnił się istotnie od placebo (18%).
badaniu z udziałem dzieci w wieku od 1 miesiąca do 3 lat porównywano dawkę 40 mg/kg/dobę NEURONTIN (N=38) z placebo (N=38) u pacjentów, którzy otrzymywali co najmniej jeden dostępny na rynku lek przeciwpadaczkowy i mieli przynajmniej jeden napad częściowy podczas okres przesiewowy (w ciągu 2 tygodni przed punktem początkowym). Pacjenci mieli do 48 godzin stanu wyjściowego i do 72 godzin podwójnie ślepego monitorowania wideo EEG w celu rejestrowania i liczenia występowania napadów. Nie było statystycznie istotnych różnic między terapiami ani pod względem wskaźnika odpowiedzi, ani wskaźnika odpowiedzi.
INFORMACJA O PACJENCIE
NEURONTYNA (Neuron tin) (Gabapentyna) Kapsułki, tabletki i roztwór doustny
Jakie są najważniejsze informacje, które powinienem wiedzieć o NEURONTIN?
Nie należy przerywać przyjmowania leku NEURONTIN 300 mg bez wcześniejszej konsultacji z lekarzem.
Nagłe zatrzymanie NEURONTIN może spowodować poważne problemy.
NEURONTIN 400mg może powodować poważne skutki uboczne, w tym:
1. Myśli samobójcze. Podobnie jak inne leki przeciwpadaczkowe, NEURONTIN 100 mg może powodować myśli lub działania samobójcze u bardzo małej liczby osób, około 1 na 500.
Zadzwoń do lekarza natychmiast, jeśli wystąpi którykolwiek z tych objawów, zwłaszcza jeśli są nowe, gorsze lub martwią Cię:
- myśli o samobójstwie lub śmierci
- próby popełnienia samobójstwa
- nowa lub gorsza depresja
- nowy lub gorszy niepokój
- uczucie pobudzenia lub niepokoju
- atak paniki
- kłopoty ze snem (bezsenność)
- nowa lub gorsza drażliwość
- zachowywanie się agresywnie, złość lub przemoc
- działając na niebezpieczne impulsy
- ekstremalny wzrost aktywności i mówienia (mania)
- inne nietypowe zmiany w zachowaniu lub nastroju
Jak mogę obserwować wczesne objawy myśli i działań samobójczych?
- Zwracaj uwagę na wszelkie zmiany, zwłaszcza nagłe zmiany nastroju, zachowań, myśli lub uczuć.
- Utrzymuj wszystkie wizyty kontrolne u swojego lekarza zgodnie z planem.
Zadzwoń do swojego lekarza w razie potrzeby między wizytami, zwłaszcza jeśli martwisz się objawami.
Nie należy przerywać przyjmowania leku NEURONTIN bez uprzedniej konsultacji z lekarzem.
- Nagłe zatrzymanie NEURONTIN 100mg może spowodować poważne problemy. Nagłe zatrzymanie leku napadowego u pacjenta z padaczką może spowodować napady, które nie ustaną (stan padaczkowy).
- Myśli lub działania samobójcze mogą być spowodowane innymi czynnikami niż leki. Jeśli masz myśli lub działania samobójcze, Twój lekarz może sprawdzić inne przyczyny.
2. Zmiany w zachowaniu i myśleniu - Stosowanie NEURONTIN 100mg u dzieci w wieku od 3 do 12 lat może powodować zmiany emocjonalne, agresywne zachowanie, problemy z koncentracją, niepokój, zmiany w wynikach szkolnych oraz nadpobudliwość.
3. NEURONTIN może powodować poważne lub zagrażające życiu reakcje alergiczne które mogą wpływać na skórę lub inne części ciała, takie jak wątroba lub komórki krwi. Może to spowodować hospitalizację lub odstawienie leku NEURONTIN. Możesz mieć wysypkę z reakcją alergiczną wywołaną przez NEURONTIN lub nie. Natychmiast skontaktuj się z lekarzem, jeśli wystąpi którykolwiek z następujących objawów:
- wysypka na skórze
- pokrzywka
- trudności w oddychaniu
- gorączka
- obrzęk gruczołów, które nie znikają
- obrzęk twarzy, ust, gardła lub języka
- zażółcenie skóry lub białek oczu
- nietypowe siniaki lub krwawienie
- silne zmęczenie lub osłabienie
- nieoczekiwany ból mięśni
- częste infekcje
Te objawy mogą być pierwszymi oznakami poważnej reakcji. Pracownik służby zdrowia powinien zbadać pacjenta, aby zdecydować, czy należy kontynuować przyjmowanie leku NEURONTIN.
4. Poważne problemy z oddychaniem. Poważne problemy z oddychaniem mogą wystąpić, gdy NEURONTIN jest przyjmowany z innymi lekami, które mogą powodować ciężką senność lub zmniejszoną świadomość, lub gdy jest przyjmowany przez osobę, która już ma problemy z oddychaniem. Podczas rozpoczynania stosowania leku NEURONTIN 300 mg lub zwiększania dawki należy zwracać uwagę na zwiększoną senność lub spowolnienie oddychania. Natychmiast uzyskaj pomoc, jeśli wystąpią problemy z oddychaniem.
Co to jest NEURONTIN 400mg?
NEURONTIN 400mg to lek na receptę stosowany w leczeniu:
- Ból spowodowany uszkodzeniem nerwów (ból popółpaścowy), który następuje po gojeniu się półpaśca (bolesna wysypka po infekcji półpaśca) u dorosłych.
- Napady częściowe przyjmowane razem z innymi lekami u dorosłych i dzieci w wieku 3 lat i starszych z napadami padaczkowymi.
Kto nie powinien brać NEURONTIN?
Nie stosować leku NEURONTIN, jeśli pacjent ma uczulenie na gabapentynę lub którykolwiek z pozostałych składników leku NEURONTIN. Pełna lista składników NEURONTIN znajduje się na końcu tego Przewodnika po lekach.
czym powinienem powiedzieć lekarzowi przed przyjęciem leku NEURONTIN 300 mg?
Przed przyjęciem leku NEURONTIN 400 mg należy poinformować lekarza, jeśli:
- masz lub miałeś problemy z nerkami lub jesteś poddawany hemodializie
- masz lub miałeś depresję, problemy z nastrojem lub myśli lub zachowania samobójcze;
- mieć cukrzycę
- masz problemy z oddychaniem
- są w ciąży lub planują zajść w ciążę. Nie wiadomo, czy NEURONTIN może zaszkodzić nienarodzonemu dziecku. Należy natychmiast poinformować lekarza, jeśli zajdziesz w ciążę podczas przyjmowania leku NEURONTIN. Ty i Twój lekarz zdecydujecie, czy należy przyjmować NEURONTIN 100 mg podczas ciąży. Rejestr ciąży: Jeśli zajdziesz w ciążę podczas przyjmowania leku NEURONTIN, porozmawiaj ze swoim lekarzem o rejestracji w Północnoamerykańskim Rejestrze Ciąży Leków Przeciwpadaczkowych (NAAED). Celem tego rejestru jest zebranie informacji o bezpieczeństwie leków przeciwpadaczkowych w czasie ciąży. Możesz zarejestrować się w tym rejestrze, dzwoniąc pod numer 1-888-233-2334.
- karmisz piersią lub planujesz karmić piersią. NEURONTIN może przenikać do mleka matki. Ty i Twój lekarz powinniście zdecydować, w jaki sposób będziecie karmić swoje dziecko podczas przyjmowania leku NEURONTIN.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe. W szczególności powiedz swojemu lekarzowi, jeśli zażywasz jakiekolwiek opioidowe leki przeciwbólowe (takie jak oksykodon), jakiekolwiek leki przeciwlękowe (takie jak lorazepam) lub bezsenność (takie jak zolpidem) lub jakiekolwiek leki, które powodują senność.
Jeśli leki te są przyjmowane z lekiem NEURONTIN, możesz mieć większe ryzyko wystąpienia zawrotów głowy, senności lub problemów z oddychaniem.
Przyjmowanie leku NEURONTIN 100 mg z niektórymi innymi lekami może powodować działania niepożądane lub wpływać na ich działanie. Nie rozpoczynaj ani nie przerywaj innych leków bez konsultacji z lekarzem.
Poznaj leki, które przyjmujesz. Zachowaj ich listę i pokaż ją swojemu lekarzowi i farmaceucie, gdy otrzymasz nowy lek.
Jak powinienem przyjmować NEURONTIN 400mg?
- Weź NEURONTIN dokładnie zgodnie z zaleceniami. Twój lekarz poinformuje Cię, jaką dawkę NEURONTIN 600 mg należy przyjąć.
- Nie należy zmieniać dawki leku NEURONTIN bez konsultacji z lekarzem.
- Jeśli pacjent przyjmuje NEURONTIN tabletki i przełamuje tabletkę na pół, niewykorzystaną połowę tabletki należy przyjąć w następnej zaplanowanej dawce. Połówki tabletek, które nie zostały zużyte w ciągu 28 dni od przełamania, należy wyrzucić.
- Kapsułki NEURONTIN należy popić wodą.
- Tabletki NEURONTIN można przyjmować z posiłkiem lub bez posiłku. Jeśli przyjmujesz środki zobojętniające kwasy zawierające aluminium i magnez, takie jak Maalox®, Mylanta®, Gelusil®, Gaviscon® lub Di-Gel®, powinieneś odczekać co najmniej 2 godziny przed przyjęciem kolejnej dawki NEURONTIN. Jeśli zażyjesz zbyt dużo NEURONTIN 600 mg, natychmiast skontaktuj się z lekarzem lub lokalnym Centrum Kontroli Zatruć pod numerem 1-800-222-1222.
Czego powinienem unikać podczas przyjmowania NEURONTIN?
- Podczas przyjmowania leku NEURONTIN nie należy pić alkoholu ani przyjmować innych leków powodujących senność lub zawroty głowy bez uprzedniej konsultacji z lekarzem. Przyjmowanie leku NEURONTIN 600 mg z alkoholem lub lekami, które powodują senność lub zawroty głowy, może pogorszyć senność lub zawroty głowy.
- Nie prowadź samochodu, nie obsługuj ciężkich maszyn ani nie wykonuj innych niebezpiecznych czynności, dopóki nie dowiesz się, jak wpływa na Ciebie NEURONTIN 100mg. NEURONTIN 600mg może spowolnić myślenie i zdolności motoryczne.
Jakie są możliwe skutki uboczne NEURONTIN 300mg?
NEURONTIN 100mg może powodować poważne skutki uboczne, w tym:
Widzieć „Jakie są najważniejsze informacje, które powinienem wiedzieć o NEURONTIN?”
- problemy z jazdą podczas korzystania z NEURONTIN. Zobacz „Czego powinienem unikać podczas przyjmowania Neurontin 600 mg?”
- senność i zawroty głowy, które mogą nasilać występowanie przypadkowych urazów, w tym upadków
- Najczęstsze działania niepożądane NEURONTIN 100mg to:
- brak koordynacji
- Infekcja wirusowa
- czuć się sennym
- nudności i wymioty
- trudności z mówieniem
- drżenie
- obrzęk, zwykle nóg i stóp
- czuć się zmęczonym
- gorączka
- gwałtowne ruchy
- trudności z koordynacją
- podwójne widzenie
- niezwykły ruch gałek ocznych
Poinformuj swojego lekarza, jeśli masz jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe działania niepożądane NEURONTIN. Aby uzyskać więcej informacji, zapytaj swojego lekarza lub farmaceutę.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać NEURONTIN?
- Przechowywać NEURONTIN 400 mg kapsułki i tabletki w temperaturze od 68 do 77 °F (20 °C do 25 °C).
- Przechowywać NEURONTIN 400 mg roztwór doustny w lodówce w temperaturze od 2°C do 8°C (36°F do 46°F).
Przechowuj NEURONTIN 600 mg i wszystkie leki w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu NEURONTIN
Leki są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Nie należy stosować leku NEURONTIN 300 mg na stan, na który nie został przepisany. Nie należy podawać leku NEURONTIN innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić.
Ten przewodnik po lekach podsumowuje najważniejsze informacje o NEURONTIN. Jeśli chcesz uzyskać więcej informacji, porozmawiaj ze swoim lekarzem. Możesz poprosić swojego lekarza lub farmaceutę o informacje o NEURONTIN 100mg, które zostały napisane dla pracowników służby zdrowia.
Aby uzyskać więcej informacji, odwiedź stronę http://www.pfizer.com lub zadzwoń pod numer 1-800-438-1985.
Jakie są składniki NEURONTIN 400mg?
Składnik czynny: gabapentyna
Składniki nieaktywne w kapsułkach: laktoza, skrobia kukurydziana, talk, żelatyna, dwutlenek tytanu i FD&C Blue No. 2.
Otoczka kapsułki 300 mg zawiera również: żółty tlenek żelaza.
Otoczka kapsułki 400 mg zawiera również: czerwony tlenek żelaza i żółty tlenek żelaza.
Składniki nieaktywne w tabletkach: poloksamer 407, kopowidon, skrobia kukurydziana, stearynian magnezu, hydroksypropyloceluloza, talk i wosk kandelila
Składniki nieaktywne w roztworze doustnym: gliceryna, ksylitol, woda oczyszczona i sztuczny aromat.
Ten przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków.
