Imitrex 100mg, 25mg, 50mg Sumatriptan Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Imitrex 25mg i jak się go stosuje?
Imitrex 100mg to lek na receptę stosowany w leczeniu objawów migrenowych bólów głowy i klasterowych bólów głowy. Imitrex może być stosowany samodzielnie lub z innymi lekami.
Imitrex 50mg jest środkiem przeciwmigrenowym, agonistą receptora serotoninowego 5-HT.
Nie wiadomo, czy Imitrex 50 mg jest bezpieczny i skuteczny u dzieci w wieku poniżej 18 lat i nie zaleca się jego stosowania u pacjentów geriatrycznych.
Jakie są możliwe skutki uboczne Imitrexu 50mg?
Imitrex 25mg może powodować poważne skutki uboczne, w tym:
- nagły, silny ból brzucha,
- biegunka z lub bez obecności krwi,
- silny ból w klatce piersiowej,
- ból w szczęce lub ramieniu,
- duszność,
- nieregularne bicie serca,
- drgawki (drgawki),
- kurcze nóg,
- drętwienie lub mrowienie w nogach lub stopach,
- piekący ból w nogach lub stopach,
- uczucie zimna w nogach lub stopach,
- zmiany koloru nóg lub stóp,
- ból biodra,
- mdłości,
- wymioty,
- pocenie się lub dreszcze,
- podniecenie,
- halucynacje,
- gorączka,
- sztywność mięśni,
- utrata koordynacji,
- nagłe drętwienie lub osłabienie jednej strony ciała,
- bełkotliwa wymowa,
- trudności z widzeniem,
- słaba równowaga i
- nagły silny ból głowy
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze działania niepożądane Imitrexu to:
- ból lub ucisk w klatce piersiowej, gardle lub szczęce,
- ucisk w dowolnej części ciała,
- drętwienie lub mrowienie ,
- uczucie gorąca lub zimna,
- zawroty głowy,
- senność,
- słabość,
- nieprzyjemny smak po zastosowaniu leku do nosa,
- ból, pieczenie, drętwienie lub mrowienie w nosie lub gardle po zastosowaniu leku do nosa oraz
- katar lub zatkany nos po zastosowaniu leku do nosa
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie są wszystkie możliwe skutki uboczne Imitrexu. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
IMITREX 50 mg zawiera bursztynian sumatryptanu, selektywnego agonistę receptora 5-HT1B/1D. Bursztynian sumatryptanu jest chemicznie oznaczony jako bursztynian 3-[2-(dimetyloamino)etylo]-N-metylo-indolo-5-metanosulfonamidu (1:1) i ma następującą strukturę:
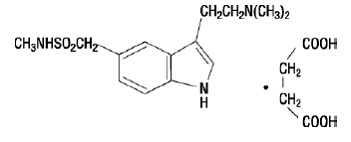
Wzór empiryczny to C14H21N3O2S•C4H6O4, reprezentujący masę cząsteczkową 413,5. Bursztynian sumatryptanu jest proszkiem o barwie od białej do białawej, łatwo rozpuszczalnym w wodzie i soli fizjologicznej.
IMITREX to przejrzysty, bezbarwny do jasnożółtego, sterylny, apirogenny roztwór do wstrzykiwań podskórnych. Każde 0,5 ml roztworu 8 mg/ml IMITREX do wstrzykiwań zawiera 4 mg sumatryptanu (zasady) w postaci bursztynianu i 3,8 mg chlorku sodu, USP w wodzie do wstrzykiwań, USP. Każde 0,5 ml 12 mg/ml roztworu IMITREX do wstrzykiwań zawiera 6 mg sumatryptanu (zasady) w postaci bursztynianu i 3,5 mg chlorku sodu, USP w wodzie do wstrzykiwań, USP. Zakres pH obu roztworów wynosi około 4,2 do 5,3. Osmolalność obu wstrzyknięć wynosi 291 mOsmol.
WSKAZANIA
IMITREX® Injection jest wskazany u dorosłych w (1) ostrym leczeniu migreny, z aurą lub bez, oraz (2) ostrym leczeniu klasterowego bólu głowy.
Ograniczenia użytkowania
- Stosować tylko wtedy, gdy postawiono jednoznaczną diagnozę migreny lub klasterowego bólu głowy. Jeśli pacjent nie reaguje na pierwszy napad migreny lub klasterowego bólu głowy leczony preparatem IMITREX 50 mg do wstrzykiwań, należy ponownie rozważyć diagnozę przed podaniem leku IMITREX do wstrzykiwań w celu leczenia kolejnych napadów.
- IMITREX Injection nie jest wskazany do zapobiegania napadom migreny lub klasterowych bólów głowy.
DAWKOWANIE I SPOSÓB PODAWANIA
Informacje o dawkowaniu
Maksymalna pojedyncza zalecana dawka produktu IMITREX 25 mg do wstrzykiwań dla dorosłych w ostrym leczeniu migreny lub klasterowego bólu głowy wynosi 6 mg we wstrzyknięciu podskórnym. W leczeniu migreny, jeśli działania niepożądane ograniczają dawkę, można zastosować niższe dawki (1 mg do 5 mg) [patrz Studia kliniczne ]. W leczeniu klasterowego bólu głowy nie ustalono skuteczności niższych dawek.
Maksymalna skumulowana dawka, jaką można podać w ciągu 24 godzin, wynosi 12 mg, dwa wstrzyknięcia po 6 mg w odstępie co najmniej 1 godziny. Drugą dawkę 6 mg należy rozważyć tylko w przypadku zaobserwowania pewnej odpowiedzi na pierwsze wstrzyknięcie.
Podawanie za pomocą wstrzykiwacza IMITREX STATdose Pen®
Dostępny jest automatyczny wstrzykiwacz (IMITREX 25 mg STATdose Pen) do stosowania z wkładami 4 mg i 6 mg napełnionych strzykawek. Za pomocą tego urządzenia igła wbija się na około 1/4 cala (5 do 6 mm). Zastrzyk ma być podany podskórnie i należy unikać podawania domięśniowego lub donaczyniowego. Należy poinstruować pacjentów, jak prawidłowo stosować wstrzykiwacz IMITREX 100 mg STATdose Pen i poinstruować ich, aby korzystali z miejsc wstrzyknięcia o odpowiedniej grubości skóry i warstwy podskórnej, aby dostosować się do długości igły.
Podawanie dawek IMITREX innych niż 4 lub 6 mg
pacjentów otrzymujących dawki inne niż 4 mg lub 6 mg należy użyć fiolki jednodawkowej 6 mg; nie należy używać wstrzykiwacza IMITREX 50 mg STATdose Pen. Przed podaniem wzrokowo skontrolować fiolkę pod kątem cząstek stałych i przebarwień. Nie używać, jeśli widoczne są cząstki stałe i przebarwienia.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
- Wstrzykiwanie: 4 mg i 6 mg jednodawkowe wkłady z ampułkostrzykawką do stosowania ze wstrzykiwaczem IMITREX STATdose Pen.
- Wstrzyknięcie: fiolka jednodawkowa 6 mg.
Składowania i stosowania
IMITREX 100 mg do wstrzykiwań zawiera sumatryptan (zasada) w postaci bursztynianu i jest dostarczany jako przejrzysty, bezbarwny do jasnożółtego, sterylny, niepirogenny roztwór w następujący sposób:
Wstępnie napełniona strzykawka i/lub automatyczny wstrzykiwacz
Każde opakowanie zawiera ulotkę z informacjami dla pacjenta i instrukcją użycia.
IMITREX 100 mg STATdose System®, 4 mg , zawierający 1 wstrzykiwacz IMITREX 25 mg STATdose Pen, 2 napełnione jednodawkowe wkłady strzykawki i 1 futerał do przenoszenia ( NDC 0173-0739-00).
IMITREX 100 mg STATdose System, 6 mg zawierający 1 wstrzykiwacz IMITREX STATdose Pen, 2 napełnione jednodawkowe wkłady strzykawki i 1 futerał do przenoszenia ( NDC 0173-0479-00).
Dwie ampułko-strzykawki zawierające pojedynczą dawkę 4 mg wkłady do stosowania z systemem IMITREX STATdose ( NDC 0173-0739-02).
Dwie ampułko-strzykawki z pojedynczą dawką 6 mg wkłady do stosowania z systemem IMITREX 25 mg STATdose ( NDC 0173-0478-00).
Fiolka jednodawkowa
IMITREX 25 mg Fiolka do wstrzykiwań z pojedynczą dawką (6 mg/0,5 ml) w kartonikach zawierających 5 fiolek ( NDC 01730449-02).
Przechowywać w temperaturze od 2° do 30°C (36° do 86°F). Chronić przed światłem.
GlaxoSmithKline, Research Triangle Park, NC 27709
SKUTKI UBOCZNE
Poniżej oraz w innych miejscach na etykiecie opisano następujące poważne działania niepożądane:
- Niedokrwienie mięśnia sercowego, zawał mięśnia sercowego i dławica Prinzmetala [patrz OSTRZEŻENIA I ŚRODKI ]
- Arytmie [patrz OSTRZEŻENIA I ŚRODKI ]
- Ból/ucisk/ucisk w klatce piersiowej, gardle, szyi i/lub żuchwie [patrz OSTRZEŻENIA I ŚRODKI ]
- Incydenty mózgowo-naczyniowe [patrz OSTRZEŻENIA I ŚRODKI ]
- Inne reakcje skurczu naczyń [patrz OSTRZEŻENIA I ŚRODKI ]
- Ból głowy spowodowany nadużywaniem leków [patrz OSTRZEŻENIA I ŚRODKI ]
- Zespół serotoninowy [patrz OSTRZEŻENIA I ŚRODKI ]
- Wzrost ciśnienia krwi [patrz OSTRZEŻENIA I ŚRODKI ]
- Reakcje nadwrażliwości [patrz PRZECIWWSKAZANIA , OSTRZEŻENIA I ŚRODKI ]
- Napady [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Migrena
W Tabeli 1 wymieniono działania niepożądane, które wystąpiły w 2 amerykańskich badaniach klinicznych kontrolowanych placebo u pacjentów z migreną (Badania 2 i 3) po podaniu pojedynczej dawki 6 mg IMITREX 100 mg do wstrzykiwań lub placebo. W Tabeli 1 uwzględniono tylko reakcje, które wystąpiły z częstością 2% lub więcej w grupach leczonych IMITREX 6 mg i które wystąpiły z częstością większą niż w grupie placebo.
Płeć ani wiek pacjentów nie miały wpływu na częstość występowania działań niepożądanych w kontrolowanych badaniach klinicznych. Nie było wystarczających danych, aby ocenić wpływ rasy na częstość występowania działań niepożądanych.
Klasterowy ból głowy
W kontrolowanych badaniach klinicznych oceniających skuteczność IMITREX 50 mg do wstrzykiwań w leczeniu klasterowych bólów głowy (Badania 4 i 5), nie wykryto nowych istotnych działań niepożądanych, które nie zostały już zidentyfikowane w badaniach IMITREX 100 mg u pacjentów z migreną.
Ogólnie częstość działań niepożądanych zgłaszanych w badaniach klasterowego bólu głowy była generalnie niższa niż w badaniach dotyczących migreny. Wyjątkiem są doniesienia o parestezji (5% IMITREX, 0% placebo), nudnościach i wymiotach (4% IMITREX, 0% placebo) i skurczu oskrzeli (1% IMITREX 50 mg, 0% placebo).
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane po zatwierdzeniu stosowania tabletek IMITREX 50 mg, aerozolu do nosa IMITREX i IMITREX 50 mg do wstrzykiwań. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Układ sercowo-naczyniowy
Niedociśnienie, kołatanie serca.
Neurologiczna
Dystonia, drżenie.
INTERAKCJE Z LEKAMI
Leki zawierające ergot
Istnieją doniesienia, że leki zawierające sporysz powodują przedłużone reakcje naczynioskurczowe. Ponieważ te działania mogą się sumować, przeciwwskazane jest stosowanie leków zawierających ergotaminę lub typu sporyszu (takich jak dihydroergotamina lub metysergid) oraz IMITREX 25 mg do wstrzykiwań w odstępie 24 godzin.
Inhibitory monoaminooksydazy-A
Inhibitory MAO-A dwukrotnie zwiększają ekspozycję ogólnoustrojową. Dlatego stosowanie IMITREX-u u pacjentów otrzymujących inhibitory MAO-A jest przeciwwskazane [patrz FARMAKOLOGIA KLINICZNA ].
Inni agoniści 5-HT1
Ponieważ ich działanie naczynioskurczowe może się sumować, przeciwwskazane jest jednoczesne podawanie produktu IMITREX i innych agonistów receptora 5-HT1 (np. tryptanów) w ciągu 24 godzin.
Selektywne inhibitory wychwytu zwrotnego serotoniny/inhibitory wychwytu zwrotnego serotoniny norepinefryny i zespół serotoninowy
Zgłaszano przypadki zespołu serotoninowego podczas jednoczesnego podawania tryptanów i SSRI, SNRI, TCA i inhibitorów MAO [patrz OSTRZEŻENIA I ŚRODKI ].
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
niedokrwienie mięśnia sercowego, zawał mięśnia sercowego i dławica piersiowa Prinzmetala
Stosowanie leku IMITREX Injection jest przeciwwskazane u pacjentów z CAD z niedokrwieniem lub skurczem naczyń. Odnotowano rzadkie przypadki poważnych działań niepożądanych ze strony serca, w tym ostrego zawału mięśnia sercowego, występujących w ciągu kilku godzin po podaniu produktu IMITREX. Niektóre z tych reakcji wystąpiły u pacjentów bez rozpoznanej CAD. IMITREX 100 mg Iniekcja może powodować skurcz naczyń wieńcowych (dławica Prinzmetala), nawet u pacjentów bez choroby wieńcowej w wywiadzie.
Wykonać ocenę układu krążenia u pacjentów nieleczonych wcześniej tryptanem, u których występuje wiele czynników ryzyka sercowo-naczyniowego (np. podeszły wiek, cukrzyca, nadciśnienie, palenie tytoniu, otyłość, silny wywiad rodzinny w kierunku CAD) przed otrzymaniem IMITREX Injection. Jeśli istnieją dowody na CAD lub skurcz naczyń wieńcowych, przeciwwskazane jest stosowanie preparatu IMITREX 100 mg do wstrzykiwań. W przypadku pacjentów z wieloma czynnikami ryzyka sercowo-naczyniowego, u których ocena sercowo-naczyniowa jest ujemna, należy rozważyć podanie pierwszej dawki IMITREX w warunkach nadzorowanych przez personel medyczny i wykonanie elektrokardiogramu (EKG) natychmiast po podaniu IMITREX. W przypadku takich pacjentów należy rozważyć okresową ocenę układu sercowo-naczyniowego u okresowych, długotrwałych użytkowników IMITREX 100 mg do wstrzykiwań.
arytmie
ciągu kilku godzin po podaniu agonistów receptora 5-HT1 zgłaszano zagrażające życiu zaburzenia rytmu serca, w tym częstoskurcz komorowy i migotanie komór prowadzące do zgonu. W przypadku wystąpienia tych zaburzeń należy przerwać wstrzykiwanie leku IMITREX. IMITREX jest przeciwwskazany u pacjentów z zespołem Wolffa-Parkinsona-White'a lub zaburzeniami rytmu serca związanymi z innymi zaburzeniami dodatkowej drogi przewodzenia serca.
Ból w klatce piersiowej, gardle, szyi i/lub żuchwie/ucisk/ucisk
Uczucie ucisku, bólu, ucisku i ciężkości w okolicy przedsercowej, gardle, szyi i szczęce często występuje po leczeniu lekiem IMITREX do wstrzykiwań i zwykle nie ma pochodzenia sercowego. Należy jednak przeprowadzić ocenę kardiologiczną, jeśli u tych pacjentów występuje wysokie ryzyko kardiologiczne. Stosowanie produktu IMITREX Injection jest przeciwwskazane u pacjentów z CAD i dławicą piersiową typu Prinzmetala.
Zdarzenia mózgowo-naczyniowe
Krwotok mózgowy, krwotok podpajęczynówkowy i udar mózgu występowały u pacjentów leczonych agonistami 5-HT1, a niektóre zakończyły się zgonem. W wielu przypadkach wydaje się możliwe, że zdarzenia naczyniowo-mózgowe były pierwotne, agonista receptora 5-HT1 został podany w błędnym przekonaniu, że doświadczane objawy były konsekwencją migreny, gdy tak nie było. Ponadto pacjenci z migreną mogą być narażeni na zwiększone ryzyko wystąpienia pewnych zdarzeń naczyniowo-mózgowych (np. udaru, krwotoku, TIA). W przypadku wystąpienia incydentu naczyniowo-mózgowego należy przerwać wstrzykiwanie leku IMITREX.
Przed leczeniem bólów głowy u pacjentów, u których wcześniej nie zdiagnozowano migreny lub klasterowych bólów głowy lub u pacjentów z nietypowymi objawami, należy wykluczyć inne potencjalnie poważne schorzenia neurologiczne. IMITREX jest przeciwwskazany u pacjentów z udarem lub TIA w wywiadzie.
Inne reakcje skurczu naczyń
IMITREX 25 mg może powodować reakcje naczynioskurczowe inne niż wieńcowe, takie jak niedokrwienie naczyń obwodowych, niedokrwienie naczyń żołądkowo-jelitowych i zawał (objawiający się bólem brzucha i krwawą biegunką), zawał śledziony i zespół Raynauda. U pacjentów, u których po zastosowaniu dowolnego agonisty receptora 5-HT1 wystąpią objawy lub oznaki sugerujące niewieńcową reakcję skurczu naczyń, należy wykluczyć reakcję skurczu naczyń przed podaniem dodatkowych wstrzyknięć produktu IMITREX.
Zgłaszano przypadki przejściowej i trwałej ślepoty oraz znacznej częściowej utraty wzroku po zastosowaniu agonistów 5-HT1. Ponieważ zaburzenia widzenia mogą być częścią napadu migreny, związek przyczynowy między tymi zdarzeniami a stosowaniem agonistów 5-HT1 nie został jasno ustalony.
Ból głowy spowodowany nadużywaniem leków
Nadużywanie ostrych leków migrenowych (np. ergotaminy, tryptanów, opioidów lub kombinacji tych leków przez 10 lub więcej dni w miesiącu) może prowadzić do zaostrzenia bólu głowy (ból głowy spowodowany nadużywaniem leków). Ból głowy spowodowany nadużywaniem leków może objawiać się jako codzienne bóle głowy przypominające migrenę lub jako znaczny wzrost częstości napadów migreny. Konieczna może być detoksykacja pacjentów, w tym odstawienie nadużywanych leków oraz leczenie objawów odstawienia (które często obejmuje przemijające nasilenie bólu głowy).
Zespół serotoninowy
Zespół serotoninowy może wystąpić po wstrzyknięciu produktu IMITREX, szczególnie podczas jednoczesnego podawania z selektywnymi inhibitorami wychwytu zwrotnego serotoniny (SSRI), inhibitorami wychwytu zwrotnego serotoniny i noradrenaliny (SNRI), trójpierścieniowymi lekami przeciwdepresyjnymi (TCA) i inhibitorami MAO [patrz INTERAKCJE Z LEKAMI ]. Objawy zespołu serotoninowego mogą obejmować zmiany stanu psychicznego (np. pobudzenie, halucynacje, śpiączka), niestabilność autonomiczną (np. tachykardia, niestabilne ciśnienie krwi, hipertermia), aberracje nerwowo-mięśniowe (np. hiperrefleksja, brak koordynacji) i/lub objawy żołądkowo-jelitowe (np. nudności, wymioty, biegunka). Początek objawów zwykle występuje w ciągu kilku minut do kilku godzin po otrzymaniu nowej lub większej dawki leku serotoninergicznego. W przypadku podejrzenia zespołu serotoninowego należy przerwać stosowanie leku IMITREX.
Wzrost ciśnienia krwi
U pacjentów leczonych agonistami receptorów 5-HT1, w tym u pacjentów bez nadciśnienia w wywiadzie, w rzadkich przypadkach zgłaszano znaczne podwyższenie ciśnienia krwi, w tym przełom nadciśnieniowy z ostrą niewydolnością układów narządów. Monitoruj ciśnienie krwi u pacjentów leczonych preparatem IMITREX. IMITREX jest przeciwwskazany u pacjentów z niekontrolowanym nadciśnieniem tętniczym.
Reakcje anafilaktyczne/rzekomoanafilaktyczne
pacjentów otrzymujących IMITREX występowały reakcje anafilaktyczne/rzekomoanafilaktyczne. Takie reakcje mogą zagrażać życiu lub być śmiertelne. Ogólnie rzecz biorąc, reakcje anafilaktyczne na leki są bardziej prawdopodobne u osób z historią wrażliwości na wiele alergenów. IMITREX 50 mg do wstrzykiwań jest przeciwwskazany u pacjentów z reakcją nadwrażliwości na IMITREX w wywiadzie.
Napady padaczkowe
Po podaniu produktu IMITREX zgłaszano napady padaczkowe. Niektóre z nich wystąpiły u pacjentów z napadami w wywiadzie lub współistniejącymi stanami predysponującymi do napadów. Istnieją również doniesienia o pacjentach, u których takie czynniki predysponujące nie są widoczne. IMITREX należy stosować ostrożnie u pacjentów z padaczką w wywiadzie lub stanami związanymi z obniżonym progiem drgawkowym.
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( INFORMACJE DLA PACJENTA i instrukcje użytkowania ).
Ryzyko niedokrwienia i/lub zawału mięśnia sercowego, dławicy Prinzmetala, innych zdarzeń związanych ze skurczem naczyń, zaburzeń rytmu serca i zdarzeń naczyniowo-mózgowych
Należy poinformować pacjentów, że IMITREX 50 mg w postaci wstrzykiwań może powodować poważne skutki uboczne ze strony układu krążenia, takie jak zawał mięśnia sercowego lub udar. Chociaż poważne zdarzenia sercowo-naczyniowe mogą wystąpić bez objawów ostrzegawczych, pacjenci powinni być wyczuleni na oznaki i objawy bólu w klatce piersiowej, duszności, nieregularnego bicia serca, znacznego wzrostu ciśnienia krwi, osłabienia i niewyraźnej mowy, a jeśli obserwuje się wszelkie oznaki lub objawy wskazujące. Poinformuj pacjentów o znaczeniu tej obserwacji [patrz OSTRZEŻENIA I ŚRODKI ].
Reakcje anafilaktyczne/rzekomoanafilaktyczne
Należy poinformować pacjentów, że u pacjentów otrzymujących IMITREX 100 mg do wstrzykiwań wystąpiły reakcje anafilaktyczne/rzekomoanafilaktyczne. Takie reakcje mogą zagrażać życiu lub być śmiertelne. Ogólnie rzecz biorąc, reakcje anafilaktyczne na leki są bardziej prawdopodobne u osób z historią wrażliwości na wiele alergenów [patrz PRZECIWWSKAZANIA , OSTRZEŻENIA I ŚRODKI ].
Jednoczesne stosowanie z innymi tryptanami lub lekami sporyszu
Poinformuj pacjentów, że stosowanie leku IMITREX 50 mg w ciągu 24 godzin po podaniu innego tryptanu lub leku sporyszowego (w tym dihydroergotaminy lub metysergidu) jest przeciwwskazane [patrz PRZECIWWSKAZANIA , INTERAKCJE Z LEKAMI ].
Zespół serotoninowy
Przestrzegać pacjentów o ryzyku wystąpienia zespołu serotoninowego przy stosowaniu IMITREX-u lub innych tryptanów, szczególnie podczas skojarzonego stosowania z SSRI, SNRI, TCA i inhibitorami MAO [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI ].
Ból głowy spowodowany nadużywaniem leków
Poinformuj pacjentów, że stosowanie ostrych leków migrenowych przez 10 lub więcej dni w miesiącu może prowadzić do zaostrzenia bólu głowy i zachęć pacjentów do zapisywania częstotliwości bólu głowy i zażywania leków (np. poprzez prowadzenie dziennika bólu głowy) [patrz OSTRZEŻENIA I ŚRODKI ].
Ciąża
Należy poinformować pacjentki, że IMITREX 25 mg nie powinien być stosowany w okresie ciąży, chyba że potencjalne korzyści uzasadniają potencjalne ryzyko dla płodu [patrz Używaj w określonych populacjach ].
Matki karmiące
Doradź pacjentom, aby powiadomili swojego lekarza, jeśli karmią piersią lub planują karmić piersią [patrz Stosowanie w określonych populacjach ].
Umiejętność wykonywania złożonych zadań
Leczenie preparatem IMITREX 25 mg do wstrzykiwań może powodować senność i zawroty głowy; poinstruować pacjentów, aby ocenili ich zdolność do wykonywania złożonych zadań po podaniu IMITREX 25 mg do wstrzykiwań.
Jak stosować IMITREX 100 mg do wstrzykiwań
Należy zapewnić pacjentom instrukcje dotyczące prawidłowego stosowania IMITREX 100 mg do wstrzykiwań, jeśli są w stanie samodzielnie podawać IMITREX 50 mg do wstrzykiwań w sytuacjach bez nadzoru medycznego.
Należy poinformować pacjentów, że igła wstrzykiwacza IMITREX STATdose Pen wbija się na około 1/4 cala (5 do 6 mm). Należy poinformować pacjentów, że wstrzyknięcie ma być wykonane podskórnie i należy unikać podawania domięśniowego lub donaczyniowego. Należy poinstruować pacjentów, aby stosowali miejsca wstrzyknięcia o odpowiedniej grubości skóry i warstwy podskórnej, aby dopasować długość igły.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Karcynogeneza
badaniach rakotwórczości u myszy i szczurów, którym sumatryptan podawano doustnie przez odpowiednio 78 i 104 tygodnie w dawkach do 160 mg/kg/dobę (największa dawka u szczura została zmniejszona z 360 mg/kg/dobę w 21. tygodniu). ). Najwyższa dawka dla myszy i szczurów wynosiła około 130 i 260-krotność pojedynczej dawki MRHD wynoszącej 6 mg podawanej podskórnie w przeliczeniu na mg/m². U żadnego z gatunków nie było dowodów na wzrost guzów związanych z podawaniem sumatryptanu.
Mutageneza
Sumatryptan dał wynik ujemny in vitro (mutacja odwrotna bakteryjna [Ames], mutacja komórek genowych V79/HGPRT u chomika chińskiego, aberracja chromosomowa w ludzkich limfocytach) i in vivo (mikrojądra szczura).
Upośledzenie płodności
Gdy sumatryptan podawano we wstrzyknięciu podskórnym samcom i samicom szczurów przed i przez okres kojarzenia, nie stwierdzono zaburzeń płodności w dawkach do 60 mg/kg/dobę lub około 100-krotności pojedynczej dawki 6 mg stosowanej u ludzi na mg/m² podstawy. Gdy sumatryptan (5, 50, 500 mg/kg/dobę) podawano doustnie samcom i samicom szczurów przed i przez okres krycia, wystąpił związany z leczeniem spadek płodności wtórny do zmniejszenia krycia u zwierząt leczonych dawkami powyżej 5 mg/kg/dzień. Nie jest jasne, czy to odkrycie było spowodowane wpływem na samce, samice, czy na jedno i drugie.
Używaj w określonych populacjach
Ciąża
Ciąża Kategoria C
Nie ma odpowiednich i dobrze kontrolowanych badań IMITREX 50 mg do wstrzykiwań u kobiet w ciąży. W badaniach toksyczności rozwojowej u szczurów i królików doustne podawanie sumatryptanu ciężarnym zwierzętom wiązało się ze śmiertelnością zarodków, nieprawidłowościami płodów i śmiertelnością młodych. Sumatryptan podawany dożylnie ciężarnym królikom powodował śmierć zarodków. IMITREX 100 mg do wstrzykiwań należy stosować w czasie ciąży tylko wtedy, gdy potencjalna korzyść uzasadnia potencjalne ryzyko dla płodu.
Doustne podawanie sumatryptanu ciężarnym samicom szczurów w okresie organogenezy powodowało zwiększoną częstość występowania nieprawidłowości naczyń krwionośnych płodu (piersiowo-piersiowych i pępowinowych). Najwyższa dawka nie powodująca toksycznego wpływu na rozwój zarodka i płodu w częstości wynosiła 60 mg/kg/dobę lub około 100-krotność pojedynczej maksymalnej zalecanej dawki dla ludzi (MRHD) wynoszącej 6 mg podawanej podskórnie w przeliczeniu na mg/m². Doustne podawanie sumatryptanu ciężarnym samicom królików w okresie organogenezy powodowało zwiększoną częstość występowania śmiertelności zarodków oraz nieprawidłowości naczyń i szkieletu w odcinku szyjno-piersiowym płodu. Dożylne podawanie sumatryptanu ciężarnym królikom w okresie organogenezy powodowało zwiększoną częstość śmiertelności zarodków. Najwyższe doustne i dożylne dawki nie powodujące toksycznego wpływu na rozwój u królików wynosiły odpowiednio 15 i 0,75 mg/kg/dobę lub około 50 i 2 razy więcej niż pojedyncza MRHD w wysokości 6 mg podawana podskórnie w przeliczeniu na mg/m2.
Doustne podawanie sumatryptanu szczurom przed i podczas ciąży powodowało toksyczne działanie na zarodek i płód (zmniejszenie masy ciała, zmniejszenie kostnienia, zwiększona częstość występowania nieprawidłowości szkieletowych). Najwyższa dawka niepowodująca efektu wynosiła 50 mg/kg/dobę, czyli około 80-krotność pojedynczej dawki MRHD wynoszącej 6 mg podawanej podskórnie w przeliczeniu na mg/m². U potomstwa ciężarnych szczurów, którym podano doustnie sumatryptan podczas organogenezy, zaobserwowano zmniejszenie przeżywalności młodych. Najwyższa dawka niepowodująca tego efektu wynosiła 60 mg/kg/dobę, czyli około 100-krotność pojedynczej dawki MRHD wynoszącej 6 mg podawanej podskórnie w przeliczeniu na mg/m². Doustne podawanie ciężarnym samicom szczurów sumatryptanem w drugiej fazie ciąży i podczas laktacji spowodowało zmniejszenie przeżywalności młodych. Najwyższa dawka niepowodująca tego efektu wynosiła 100 mg/kg/dobę, czyli około 160-krotność pojedynczej dawki MRHD wynoszącej 6 mg podawanej podskórnie w przeliczeniu na mg/m².
Matki karmiące
Sumatryptan przenika do mleka ludzkiego po podaniu podskórnym. Narażenie niemowląt na sumatryptan można zminimalizować, unikając karmienia piersią przez 12 godzin po podaniu IMITREX 50 mg do wstrzykiwań.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność u pacjentów pediatrycznych nie zostały ustalone. IMITREX 100 mg do wstrzykiwań nie jest zalecany do stosowania u pacjentów w wieku poniżej 18 lat.
W dwóch kontrolowanych badaniach klinicznych oceniano preparat IMITREX w aerozolu do nosa (5 do 20 mg) z udziałem 1248 dzieci z migreną w wieku od 12 do 17 lat, które leczyły pojedynczy napad. W badaniach nie ustalono skuteczności preparatu IMITREX aerozol do nosa w porównaniu z placebo w leczeniu migreny u dzieci. Działania niepożądane obserwowane w tych badaniach klinicznych miały podobny charakter do tych zgłaszanych w badaniach klinicznych u dorosłych.
Do pięciu kontrolowanych badań klinicznych (2 badania z pojedynczym atakiem, 3 badania z wieloma atakami) oceniających doustny IMITREX (25 do 100 mg) u dzieci w wieku od 12 do 17 lat włączono w sumie 701 dzieci z migreną. W badaniach tych nie ustalono skuteczności doustnego preparatu IMITREX 25 mg w porównaniu z placebo w leczeniu migreny u dzieci. Działania niepożądane obserwowane w tych badaniach klinicznych miały podobny charakter do tych zgłaszanych w badaniach klinicznych u dorosłych. Częstość występowania wszystkich działań niepożądanych u tych pacjentów wydawała się być zależna zarówno od dawki, jak i wieku, przy czym młodsi pacjenci zgłaszali reakcje częściej niż starsi pacjenci pediatryczni.
Doświadczenia po wprowadzeniu produktu do obrotu potwierdzają, że w populacji pediatrycznej wystąpiły poważne działania niepożądane po podaniu podskórnym, doustnym i (lub) donosowym IMITREX. Zgłoszenia te obejmują reakcje o podobnym charakterze do rzadko zgłaszanych u dorosłych, w tym udar, utratę wzroku i zgon. Zawał mięśnia sercowego został zgłoszony u 14-letniego mężczyzny po zastosowaniu doustnego IMITREX; objawy kliniczne wystąpiły w ciągu 1 dnia od podania leku. Obecnie nie są dostępne dane kliniczne pozwalające określić częstość występowania ciężkich działań niepożądanych u dzieci i młodzieży, które mogą otrzymać IMITREX podskórnie, doustnie lub donosowo.
Zastosowanie geriatryczne
Badania kliniczne preparatu IMITREX 100 mg do wstrzykiwań nie obejmowały wystarczającej liczby pacjentów w wieku 65 lat i starszych, aby określić, czy reagują oni inaczej niż pacjenci młodsi. Inne zgłoszone doświadczenia kliniczne nie wykazały różnic w odpowiedziach między pacjentami w podeszłym wieku i młodszymi. Ogólnie rzecz biorąc, dobór dawki u pacjentów w podeszłym wieku powinien być ostrożny, zwykle zaczynając od dolnej granicy zakresu dawkowania, co odzwierciedla większą częstość pogorszenia czynności wątroby, nerek lub serca oraz współistniejących chorób lub innych leków.
U pacjentów geriatrycznych, u których występują inne czynniki ryzyka sercowo-naczyniowego (np. cukrzyca, nadciśnienie, palenie tytoniu, otyłość, ciężki wywiad rodzinny w kierunku CAD) zaleca się ocenę układu krążenia [patrz OSTRZEŻENIA I ŚRODKI ].
PRZEDAWKOWAĆ
Po dożylnym podaniu produktu IMITREX 50 mg do wstrzykiwań obserwowano skurcz naczyń wieńcowych [patrz PRZECIWWSKAZANIA ]. Na podstawie danych na zwierzętach można się spodziewać, że przedawkowanie (psy 0,1 g/kg, szczury 2 g/kg) może spowodować drgawki, drżenie, brak aktywności, rumień kończyn, zmniejszoną częstość oddechów, sinicę, ataksję, rozszerzenie źrenic, reakcje w miejscu wstrzyknięcia ( łuszczenie, wypadanie włosów i tworzenie strupów) i paraliż.
Okres półtrwania sumatryptanu w fazie eliminacji wynosi około 2 godzin [patrz FARMAKOLOGIA KLINICZNA ]; dlatego monitorowanie pacjentów po przedawkowaniu produktu leczniczego IMITREX IMITREX należy kontynuować przez co najmniej 10 godzin lub do czasu utrzymywania się objawów podmiotowych lub przedmiotowych.
Nie wiadomo, jaki wpływ ma hemodializa lub dializa otrzewnowa na stężenia sumatryptanu w surowicy.
PRZECIWWSKAZANIA
IMITREX jest przeciwwskazany u pacjentów z:
- Choroba niedokrwienna tętnic wieńcowych (CAD) (dławica piersiowa, przebyty zawał mięśnia sercowego lub udokumentowane nieme niedokrwienie) lub skurcz tętnic wieńcowych, w tym dławica Prinzmetala [patrz OSTRZEŻENIA I ŚRODKI ].
- Zespół Wolffa-Parkinsona-White'a lub arytmie związane z innymi zaburzeniami dodatkowej drogi przewodzenia serca [patrz OSTRZEŻENIA I ŚRODKI ].
- Przebyty udar mózgu lub przemijający napad niedokrwienny (TIA) lub migrena połowiczna lub podstawna, ponieważ ci pacjenci są bardziej narażeni na udar mózgu [patrz OSTRZEŻENIA I ŚRODKI ].
- Choroba naczyń obwodowych [patrz OSTRZEŻENIA I ŚRODKI ].
- Choroba niedokrwienna jelit [patrz OSTRZEŻENIA I ŚRODKI ].
- Niekontrolowane nadciśnienie [patrz OSTRZEŻENIA I ŚRODKI ].
- Niedawne użycie (tj. w ciągu 24 godzin) leków zawierających ergotaminę, leków typu sporyszu (takich jak dihydroergotamina lub metysergid) lub innego agonisty 5-hydroksytryptaminy1 (5-HT1) [patrz INTERAKCJE Z LEKAMI ].
- Jednoczesne podawanie inhibitora monoaminooksydazy (MAO)-A lub niedawne (w ciągu 2 tygodni) stosowanie inhibitora MAO-A [patrz INTERAKCJE Z LEKAMI , FARMAKOLOGIA KLINICZNA ].
- Nadwrażliwość na IMITREX (obserwowany obrzęk naczynioruchowy i anafilaksja) [patrz OSTRZEŻENIA I ŚRODKI ].
- Ciężkie zaburzenia czynności wątroby [patrz FARMAKOLOGIA KLINICZNA ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Sumatryptan wiąże się z wysokim powinowactwem z ludzkimi sklonowanymi receptorami 5-HT1B/1D. Sumatryptan prawdopodobnie wywiera działanie terapeutyczne w leczeniu migreny i klasterowych bólów głowy poprzez działanie agonistyczne na receptory 5-HT1B/1D na wewnątrzczaszkowe naczynia krwionośne i nerwy czuciowe układu trójdzielnego, co powoduje zwężenie naczyń czaszkowych i hamowanie prozapalnego neuropeptydu wydanie.
Farmakodynamika
Ciśnienie krwi
Znaczące podwyższenie ciśnienia krwi, w tym przełom nadciśnieniowy, odnotowano u pacjentów z nadciśnieniem w wywiadzie i bez nadciśnienia [patrz OSTRZEŻENIA I ŚRODKI ].
Tętnice obwodowe (małe)
U zdrowych ochotników (N = 18) badanie oceniające wpływ sumatryptanu na reaktywność tętnic obwodowych (małych naczyń) nie wykazało klinicznie istotnego wzrostu oporu obwodowego.
Tętno
Przemijającemu wzrostowi ciśnienia krwi obserwowanemu u niektórych pacjentów w badaniach klinicznych przeprowadzonych podczas rozwoju sumatryptanu w leczeniu migreny nie towarzyszyły żadne klinicznie istotne zmiany częstości akcji serca.
Farmakokinetyka
Wchłanianie i biodostępność
Biodostępność sumatryptanu we wstrzyknięciu podskórnym u 18 zdrowych mężczyzn wynosiła 97% ± 16% tej uzyskanej po wstrzyknięciu dożylnym.
Po pojedynczym podskórnym, manualnym wstrzyknięciu 6 mg w okolicę mięśnia naramiennego u 18 zdrowych mężczyzn (wiek: 24 ± 6 lat, masa ciała: 70 kg), maksymalne stężenie sumatryptanu w surowicy (Cmax) wynosiło (średnia ± odchylenie standardowe) 74 ± 15 ng/ml, a czas do osiągnięcia maksymalnego stężenia (Tmax) wynosił 12 minut po wstrzyknięciu (zakres: 5 do 20 minut). W tym badaniu ta sama dawka wstrzyknięta podskórnie w udo dawała Cmax 61 ± 15 ng/ml przy wstrzyknięciu ręcznym w porównaniu z 52 ± 15 ng/ml przy użyciu techniki automatycznego wstrzykiwania. Tmax lub wchłonięta ilość nie uległy znaczącej zmianie ani w miejscu, ani w technice wstrzyknięcia.
Dystrybucja
Wiązanie z białkami, określone przez dializę równowagową w zakresie stężeń od 10 do 1000 ng/ml jest niskie, około 14% do 21%. Nie oceniano wpływu sumatryptanu na wiązanie innych leków z białkami.
Po wstrzyknięciu podskórnym 6 mg w okolicę mięśnia naramiennego u 9 mężczyzn (średni wiek: 33 lata, średnia masa ciała: 77 kg) objętość centralnego kompartmentu dystrybucji sumatryptanu wynosiła 50 ± 8 litrów, a okres półtrwania dystrybucji wynosił 15 ± 2 minuty.
Metabolizm
Badania in vitro na ludzkich mikrosomach sugerują, że sumatryptan jest metabolizowany przez MAO, głównie izoenzym A. Większość znakowanej radioaktywnie dawki sumatryptanu wydalanego z moczem to główny metabolit kwasu indolooctowego (IAA) lub glukuronid IAA, które są nieaktywne.
Eliminacja
Po podaniu pojedynczej dawki podskórnej 6 mg, 22% ± 4% było wydalane z moczem w postaci niezmienionego sumatryptanu, a 38% ± 7% jako metabolit IAA.
Po wstrzyknięciu podskórnym 6 mg w okolicę mięśnia naramiennego klirens ogólnoustrojowy sumatryptanu wynosił 1194 ± 149 ml/min, a końcowy okres półtrwania 115 ± 19 minut.
Określone populacje
Wiek
Farmakokinetyka sumatryptanu u osób w podeszłym wieku (średnia wieku: 72 lata, 2 mężczyzn i 4 kobiety) oraz u osób z migreną (średnia wieku: 38 lat, 25 mężczyzn i 155 kobiet) była podobna jak u zdrowych mężczyzn (średni wiek: 30 lat).
Niewydolność wątroby
Oceniono wpływ łagodnej do umiarkowanej choroby wątroby na farmakokinetykę sumatryptanu podawanego podskórnie. Nie było istotnych różnic w farmakokinetyce podskórnie podawanego sumatryptanu u osób z umiarkowanymi zaburzeniami czynności wątroby w porównaniu ze zdrowymi osobami z grupy kontrolnej. Nie badano farmakokinetyki sumatryptanu podawanego podskórnie u pacjentów z ciężkimi zaburzeniami czynności wątroby. Stosowanie leku IMITREX w tej populacji jest przeciwwskazane [patrz PRZECIWWSKAZANIA ].
Wyścig
Klirens ogólnoustrojowy i Cmax sumatryptanu podawanego podskórnie były podobne u zdrowych mężczyzn rasy czarnej (n = 34) i rasy kaukaskiej (n = 38).
Badania interakcji leków
Inhibitory monoaminooksydazy-A
badaniu z udziałem 14 zdrowych kobiet wstępne leczenie inhibitorem MAO-A zmniejszyło klirens podskórnego sumatryptanu, powodując dwukrotne zwiększenie powierzchni pod krzywą zależności stężenia sumatryptanu w osoczu od czasu (AUC), co odpowiada 40% wzrostowi w okresie półtrwania eliminacji.
Toksykologia i/lub farmakologia zwierząt
Zmętnienia rogówki
U psów otrzymujących doustnie sumatryptan wystąpiły zmętnienia rogówki i ubytki nabłonka rogówki. Zmętnienia rogówki zaobserwowano przy najniższej badanej dawce, 2 mg/kg/dobę, i były one obecne po 1 miesiącu leczenia. W 60-tygodniowym badaniu odnotowano wady nabłonka rogówki. Nie przeprowadzono wcześniejszych badań pod kątem tych toksyczności i nie ustalono dawek niepowodujących efektów; jednak względna ekspozycja w osoczu przy najniższej badanej dawce była około 3 razy większa niż ekspozycja u ludzi po podaniu dawki podskórnej 6 mg.
Studia kliniczne
Migrena
kontrolowanych badaniach klinicznych obejmujących ponad 1000 pacjentów z napadami migreny, którzy odczuwali umiarkowany lub silny ból i co najmniej 1 z objawów wymienionych w Tabeli 3, ulga zaczęła się pojawiać już po 10 minutach od wstrzyknięcia 6 mg IMITREX 50 mg. Niższe dawki preparatu IMITREX 100 mg do wstrzykiwań mogą również okazać się skuteczne, chociaż odsetek pacjentów otrzymujących odpowiednią ulgę został zmniejszony, a opóźnienie do tej ulgi jest większe przy niższych dawkach.
W badaniu 1 6 różnych dawek IMITREX 100 mg do wstrzykiwań (n = 30 w każdej grupie) porównano z placebo (n = 62). w tabeli 2.
2 randomizowanych, kontrolowanych placebo badaniach klinicznych IMITREX 25 mg do wstrzykiwań 6 mg u 1104 pacjentów z umiarkowanym lub ciężkim bólem migrenowym (Badania 2 i 3), początek ulgi był krótszy niż 10 minut. Złagodzenie bólu głowy, zdefiniowane jako zmniejszenie bólu od silnego lub umiarkowanie silnego do łagodnego lub bez bólu głowy, osiągnięto u 70% pacjentów w ciągu 1 godziny po podaniu pojedynczej dawki podskórnej 6 mg produktu IMITREX do wstrzykiwań. U około 82% i 65% pacjentów leczonych produktem IMITREX 6 mg wystąpiło ustąpienie bólu głowy i brak bólu w ciągu 2 godzin.
Tabela 3 przedstawia wyniki skuteczności po 1 i 2 godzinach IMITREX 6 mg w badaniach 2 i 3.
IMITREX 100 mg zastrzyk również łagodził światłowstręt, fonofobię (wrażliwość na dźwięk), nudności i wymioty związane z napadami migreny. Podobną skuteczność zaobserwowano, gdy pacjenci samodzielnie podawali IMITREX 50 mg do wstrzykiwań przy użyciu wstrzykiwacza IMITREX 100 mg STATdose Pen.
Na skuteczność produktu IMITREX Injection nie miało wpływu to, czy migrena była związana z aurą, czasem trwania napadu, płcią lub wiekiem pacjenta, ani równoczesnym stosowaniem powszechnie stosowanych leków w profilaktyce migreny (np. beta-adrenolityków).
Klasterowy ból głowy
Skuteczność IMITREX Injection w ostrym leczeniu klasterowych bólów głowy wykazano w 2 randomizowanych, podwójnie zaślepionych, kontrolowanych placebo, 2-okresowych badaniach krzyżowych (Badania 4 i 5). Do badania włączono pacjentów w wieku od 21 do 65 lat, których poinstruowano, aby leczyli ból głowy o nasileniu od umiarkowanego do bardzo silnego w ciągu 10 minut od wystąpienia. Ustąpienie bólu głowy zdefiniowano jako zmniejszenie nasilenia bólu głowy do łagodnego bólu lub jego braku. W obu badaniach odsetek osób, które odczuwały ulgę po 10 lub 15 minutach, był znacząco większy wśród pacjentów otrzymujących 6 mg IMITREX Injection w porównaniu z tymi, którzy otrzymywali placebo (patrz Tabela 4).
Oszacowanie skumulowanego prawdopodobieństwa uzyskania ulgi u pacjenta z klasterowym bólem głowy po leczeniu preparatem IMITREX 25 mg do wstrzykiwań lub placebo przedstawiono na Rycinie 1.
Rysunek 1: Czas do złagodzenia klasterowego bólu głowy od czasu wstrzyknięciaa 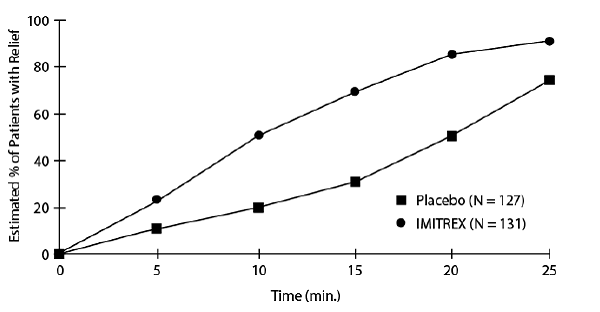
a Rysunek wykorzystuje wykres przetrwania Kaplana-Meiera (limit produktu). Pacjenci przyjmujący leki ratunkowe zostali ocenzurowani po 15 minutach.
Wykres został skonstruowany z danych od pacjentów, którzy albo doświadczyli ulgi, albo nie wymagali (żądania) leków ratunkowych w okresie 2 godzin po leczeniu. W konsekwencji dane na wykresie pochodzą tylko z podzbioru 258 leczonych bólów głowy (leczenie ratunkowe było wymagane w przypadku 52 ze 127 bólów głowy leczonych placebo i 18 ze 131 bólów głowy leczonych IMITREX 50mg Injection).
Inne dane sugerują, że leczenie preparatem IMITREX 25 mg nie wiąże się ze wzrostem wczesnych nawrotów bólu głowy i ma niewielki wpływ na częstość występowania późniejszych bólów głowy (tj. tych występujących po 2, ale przed 18 lub 24 godzinami).
INFORMACJA O PACJENCIE
IMITREX® (IM-i-trex) (bursztynian sumatryptanu) Iniekcja
Przeczytaj tę Informację dla Pacjenta przed rozpoczęciem przyjmowania leku IMITREX i za każdym razem, gdy otrzymasz uzupełnienie. Mogą pojawić się nowe informacje. Informacje te nie zastępują rozmowy z lekarzem o stanie zdrowia lub leczeniu.
Jakie są najważniejsze informacje, które powinienem wiedzieć o IMITREX?
IMITREX może powodować poważne skutki uboczne, w tym:
Zawał serca i inne problemy z sercem. Problemy z sercem mogą prowadzić do śmierci.
Przestań przyjmować IMITREX 25 mg i natychmiast uzyskaj pomoc medyczną w nagłych wypadkach, jeśli wystąpi którykolwiek z następujących objawów zawału serca:
- dyskomfort w środku klatki piersiowej, który trwa dłużej niż kilka minut lub który ustępuje i powraca
- silny ucisk, ból, ucisk lub ciężkość w klatce piersiowej, gardle, szyi lub szczęce
- ból lub dyskomfort w ramionach, plecach, szyi, szczęce lub brzuchu
- duszność z lub bez dyskomfortu w klatce piersiowej
- wylewając się z zimnego potu
- nudności lub wymioty
- uczucie oszołomienia
IMITREX nie jest przeznaczony dla osób z czynnikami ryzyka chorób serca, chyba że zostanie wykonane badanie serca i nie wykaże on problemu. Masz większe ryzyko chorób serca, jeśli:
- mieć wysokie ciśnienie krwi
- mają wysoki poziom cholesterolu
- palić
- mają nadwagę
- mieć cukrzycę
- mieć rodzinną historię chorób serca
Co to jest IMITREX?
IMITREX Injection to lek na receptę stosowany w leczeniu ostrych migrenowych bólów głowy z aurą lub bez aury oraz ostrych klasterowych bólów głowy u osób dorosłych, u których zdiagnozowano migrenę lub klasterowe bóle głowy.
IMITREX 50 mg nie jest stosowany w leczeniu innych rodzajów bólów głowy, takich jak migreny połowiczne (uniemożliwiające poruszanie się po jednej stronie ciała) lub migreny podstawne (rzadka postać migreny z aurą).
IMITREX 100 mg nie jest stosowany w celu zapobiegania lub zmniejszania liczby migrenowych lub klasterowych bólów głowy.
Nie wiadomo, czy IMITREX 100mg jest bezpieczny i skuteczny u dzieci poniżej 18 roku życia.
Kto nie powinien przyjmować IMITREX 100mg?
Nie należy przyjmować leku IMITREX 50 mg, jeśli u pacjenta występuje:
- problemy z sercem lub historia problemów z sercem
- zwężenie naczyń krwionośnych w nogach, ramionach, żołądku lub nerkach (choroba naczyń obwodowych)
- niekontrolowane wysokie ciśnienie krwi
- poważne problemy z wątrobą
- migreny hemiplegiczne lub migreny podstawne. Jeśli nie masz pewności, czy masz tego typu migreny, zapytaj swojego lekarza.
- miał udar, przemijające napady niedokrwienne (TIA) lub problemy z krążeniem krwi;
- przyjmował którykolwiek z następujących leków w ciągu ostatnich 24 godzin:
- almotryptan (AXERT®)
- eletryptan (RELPAX®)
- frowatryptan (FROVA®)
- naratryptan (AMERGE®)
- ryzatryptan (MAXALT®, MAXALT-MLT®)
- sumatryptan i naproksen (TREXIMET®)
- ergotaminy (CAFERGOT®, ERGOMAR®, MIGERGOT®)
- dihydroergotamina (DHE 45®, MIGRANAL®) Zapytaj swojego lekarza, jeśli nie masz pewności, czy Twój lek znajduje się na powyższej liście.
- uczulenie na sumatryptan lub którykolwiek ze składników leku IMITREX. Pełna lista składników leku IMITREX znajduje się na końcu tej ulotki.
O czym powinienem powiedzieć lekarzowi przed przyjęciem IMITREX?
Przed przyjęciem leku IMITREX należy poinformować lekarza o wszystkich swoich schorzeniach, w tym o:
- mieć wysokie ciśnienie krwi
- mieć wysoki poziom cholesterolu
- mieć cukrzycę
- palić
- mają nadwagę
- masz problemy z sercem lub w rodzinie występowały problemy z sercem lub udar mózgu
- masz problemy z nerkami
- masz problemy z wątrobą
- miałeś epilepsję lub drgawki
- nie stosuje skutecznej kontroli urodzeń
- zajść w ciążę podczas przyjmowania leku IMITREX
- karmisz piersią lub planujesz karmić piersią. IMITREX 25 mg przenika do mleka matki i może zaszkodzić dziecku. Porozmawiaj ze swoim lekarzem o najlepszym sposobie karmienia dziecka, jeśli przyjmujesz IMITREX.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe.
IMITREX i niektóre inne leki mogą wzajemnie na siebie wpływać, powodując poważne działania niepożądane.
Szczególnie powiedz swojemu lekarzowi, jeśli: przyjmujesz leki przeciwdepresyjne zwane:
- selektywne inhibitory wychwytu zwrotnego serotoniny (SSRI)
- inhibitory wychwytu zwrotnego serotoniny i noradrenaliny (SNRI)
- trójpierścieniowe leki przeciwdepresyjne (TCA)
- inhibitory monoaminooksydazy (IMAO)
Zapytaj swojego lekarza lub farmaceutę o listę tych leków, jeśli nie masz pewności.
Poznaj leki, które przyjmujesz. Zachowaj ich listę, aby pokazać swojemu lekarzowi lub farmaceucie, gdy otrzymasz nowy lek.
Jak powinienem przyjmować IMITREX 100mg?
- Niektóre osoby powinny przyjąć pierwszą dawkę IMITREX 25 mg w gabinecie lekarza lub w innym miejscu medycznym. Zapytaj swojego lekarza, czy powinieneś przyjąć pierwszą dawkę w warunkach medycznych.
- Używaj IMITREX 50 mg dokładnie tak, jak zalecił go Twój lekarz.
- Twój lekarz może zmienić dawkę. Nie zmieniaj dawki bez wcześniejszej rozmowy z lekarzem.
- W przypadku osób dorosłych zwykle stosowana dawka to pojedyncze wstrzyknięcie podane tuż pod skórę.
- Zastrzyk należy wykonać, gdy tylko pojawią się objawy bólu głowy, ale można go podać w dowolnym momencie podczas napadu migreny lub klasterowego bólu głowy.
- Jeśli po pierwszym wstrzyknięciu nie wystąpiła ulga, nie należy wykonywać drugiego wstrzyknięcia bez wcześniejszej konsultacji z lekarzem.
- Jeśli ból głowy powróci lub poczujesz ulgę dopiero po pierwszym wstrzyknięciu, możesz przyjąć drugie wstrzyknięcie 1 godzinę po pierwszym wstrzyknięciu, ale nie wcześniej.
- Nie należy przyjmować więcej niż 12 mg w ciągu 24 godzin.
- Jeśli użyjesz zbyt dużej ilości IMITREX 25mg, skontaktuj się z lekarzem lub natychmiast udaj się na pogotowie ratunkowe najbliższego szpitala.
- Powinieneś zanotować, kiedy masz bóle głowy i kiedy przyjmujesz IMITREX, aby móc porozmawiać z lekarzem o tym, jak IMITREX 25 mg działa na Ciebie.
Czego powinienem unikać podczas przyjmowania IMITREX?
IMITREX może powodować zawroty głowy, osłabienie lub senność. Jeśli masz te objawy, nie prowadź samochodu, nie używaj maszyn ani nie rób niczego, co wymaga czujności.
Jakie są możliwe skutki uboczne IMITREX 25mg?
IMITREX może powodować poważne skutki uboczne. Zobacz „Jakie są najważniejsze informacje, które powinienem wiedzieć o IMITREX?”
Te poważne skutki uboczne obejmują:
- zmiany koloru lub czucia w palcach rąk i nóg (zespół Raynauda)
- problemy żołądkowe i jelitowe (przypadki niedokrwienia przewodu pokarmowego i okrężnicy). Do objawów niedokrwienia przewodu pokarmowego i okrężnicy należą:
- nagły lub silny ból brzucha
- ból brzucha po posiłkach
- utrata wagi
- nudności lub wymioty
- zaparcia lub biegunka
- krwawa biegunka
- gorączka
- problemy z krążeniem krwi w nogach i stopach (niedokrwienie naczyń obwodowych). Objawy niedokrwienia naczyń obwodowych obejmują:
- skurcze i ból w nogach lub biodrach
- uczucie ciężkości lub napięcia mięśni nóg
- pieczenie lub ból w stopach lub palcach podczas odpoczynku
- drętwienie, mrowienie lub osłabienie nóg
- uczucie zimna lub zmiany koloru w jednej lub obu nogach lub stopach
- pokrzywka (swędzące guzki); obrzęk języka, ust lub gardła
- nadużywanie leków bóle głowy. Niektóre osoby, które stosują zbyt wiele zastrzyków IMITREX 100 mg, mogą mieć gorsze bóle głowy (ból głowy spowodowany nadużywaniem leków). Jeśli bóle głowy nasilą się, lekarz może zdecydować o przerwaniu leczenia lekiem IMITREX.
- zespół serotoninowy. Zespół serotoninowy jest rzadkim, ale poważnym problemem, który może wystąpić u osób stosujących IMITREX, zwłaszcza jeśli IMITREX 50 mg jest stosowany z lekami przeciwdepresyjnymi zwanymi SSRI lub SNRI. Zadzwoń do swojego lekarza od razu, jeśli masz którykolwiek z następujących objawów zespołu serotoninowego:
- zmiany psychiczne, takie jak widzenie rzeczy, których nie ma (omamy), pobudzenie lub śpiączka
- szybkie bicie serca
- zmiany ciśnienia krwi
- wysoka temperatura ciała
- napięte mięśnie
- kłopoty z chodzeniem
- drgawki. Napady zdarzały się u osób przyjmujących IMITREX, które nigdy wcześniej nie miały napadów. Porozmawiaj ze swoim lekarzem o możliwości wystąpienia drgawek podczas przyjmowania leku IMITREX.
Najczęstsze działania niepożądane IMITREX 50mg Injection obejmują:
- ból lub zaczerwienienie w miejscu wstrzyknięcia
- mrowienie lub drętwienie palców rąk i nóg
- zawroty głowy
- uczucie ciepła, gorąca, pieczenia na twarzy (zaczerwienienie twarzy)
- dyskomfort lub sztywność szyi
- uczucie osłabienia, senności lub zmęczenia
Poinformuj swojego lekarza, jeśli masz jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne IMITREX-u. Aby uzyskać więcej informacji, zapytaj swojego lekarza lub farmaceutę.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać lek IMITREX Injection?
- Przechowywać IMITREX w temperaturze od 36°F do 86°F (2°C do 30°C).
- Lek należy przechowywać z dala od światła.
- Lek należy przechowywać w dołączonym do niego opakowaniu lub futerale.
Przechowywać IMITREX i wszystkie leki w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu IMITREX
Leki są czasami przepisywane do celów innych niż wymienione w ulotkach dla pacjenta. Nie należy stosować leku IMITREX w stanach, na które nie został przepisany. Nie należy podawać leku IMITREX 25 mg innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić.
Niniejsza ulotka z informacjami dla pacjenta podsumowuje najważniejsze informacje dotyczące preparatu IMITREX. Jeśli chcesz uzyskać więcej informacji, porozmawiaj ze swoim lekarzem. Możesz poprosić swojego lekarza lub farmaceutę o informacje o IMITREX, które są przeznaczone dla pracowników służby zdrowia.
Aby uzyskać więcej informacji, odwiedź stronę www.gsk.com lub zadzwoń pod numer 1-888-825-5249.
Jakie są składniki IMITREX Injection?
Składnik aktywny: bursztynian sumatryptanu
Składniki nieaktywne: chlorek sodu, woda do wstrzykiwań
Niniejsze informacje dla pacjenta i instrukcje użytkowania zostały zatwierdzone przez amerykańską Agencję ds. Żywności i Leków.
Instrukcja użytkowania dla pacjenta
System dozowania IMITREX STAT
Przed rozpoczęciem stosowania systemu IMITREX STATdose należy zapoznać się z niniejszą Instrukcją dla pacjenta. Mogą pojawić się nowe informacje. Informacje te nie zastępują rozmowy z lekarzem o stanie zdrowia lub leczeniu. Ty i Twój lekarz powinniście porozmawiać o IMITREX 25mg Injection, kiedy zaczniecie go przyjmować i podczas regularnych kontroli.
System dawkowania IMITREX STAT należy przechowywać w miejscu niedostępnym dla dzieci.
Przed użyciem systemu dawkowania IMITREX STAT
Kiedy po raz pierwszy otworzysz pudełko z systemem IMITREX 25 mg STATdose System, dla Twojej wygody opakowanie wkładu i IMITREX STATdose Pen® znajdują się już w futerale.
Szary i niebieski Pokrowiec służy do przechowywania rozładowanego wstrzykiwacza i zestawu wkładów, gdy nie są używane.
The Pakiet wkładów posiada 2 indywidualnie zapieczętowane Wkłady strzykawkowe Każdy wkład strzykawki zawiera 1 dawkę IMITREX® (bursztynianu sumatryptanu) do wstrzykiwań. Opakowanie wkładu dla mocy 4 mg tego leku jest żółte, a opakowanie wkładu dla mocy 6 mg jest niebieskie (jak pokazano). Dostępne są wkłady uzupełniające.
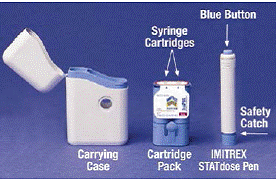
Szary i niebieski Długopis służy do automatycznego wstrzyknięcia 1 dawki leku z wkładu strzykawki. Nie dotykaj Niebieski przycisk do momentu przyciśnięcia wstrzykiwacza do skóry w celu podania dawki. Jeśli naciśniesz go w dowolnym innym momencie, możesz stracić dawkę. The Zapadka zabezpieczająca zapobiega przypadkowemu uruchomieniu pióra, dopóki nie będziesz gotowy. Pióro będzie działać tylko wtedy, gdy zsuniesz szarą część tulei do niebieskiej. Przed włożeniem nowego wkładu strzykawki należy zawsze sprawdzić, czy biały pręt zalewania nie wystaje z końca wstrzykiwacza (jak pokazano na Rysunku B). Jeśli wystaje, stracisz tę dawkę.
Jak załadować wstrzykiwacz IMITREX STATdose Pen?
Nie wkładać wstrzykiwacza, dopóki nie będziesz gotowy do samodzielnego wykonania wstrzyknięcia. Nie dotykaj niebieskiego przycisku na górze pióra (patrz Rysunek A) podczas ładowania pióra.
Rysunek A 
Rysunek B 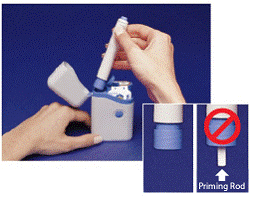
1. Otwórz pokrywę torby transportowej. Plomby zabezpieczające 2 wkłady strzykawkowe są oznaczone literami „A” i „B” (patrz Rysunek A wstawka ).
Zawsze używaj wkładu strzykawki oznaczonego „A” przed wkładem oznaczonym „B”, aby ułatwić sobie śledzenie dawek. Nie używać, jeśli którakolwiek plomba jest uszkodzona lub jej brakuje przy pierwszym otwarciu futerału.
2. Oderwij jedną z plomb gwarancyjnych (patrz Rysunek A ). Wyrzuć pieczęć. Otwórz pokrywę nad wkładem strzykawki.
3. Trzymaj wstrzykiwacz za krawędzie u góry. Wyjmij pióro z futerału (patrz Rysunek B ).
Sprawdź, czy biały pręt zalewania nie wystaje z dolnego końca wstrzykiwacza (patrz Rysunek B wstawka ). Jeśli wystaje, włóż wstrzykiwacz z powrotem do futerału i mocno dociśnij, aż poczujesz kliknięcie. Wyjmij pióro z futerału.
Rysunek C 
4. Umieść wstrzykiwacz w opakowaniu wkładu. Obróć go w prawo (zgodnie z ruchem wskazówek zegara), aż przestanie się obracać (około pół obrotu) (patrz Rysunek C ).
5. Chwyć załadowany wstrzykiwacz za krawędzie i wyciągnij go prosto (patrz Rysunek D ). Być może trzeba będzie mocno pociągnąć za pióro, ale jest to normalne. Nie naciskaj jeszcze niebieskiego przycisku.
Rysunek D 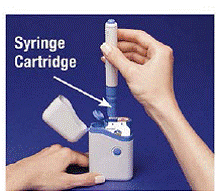
Pióro jest teraz gotowe do użycia. Nie rób włóż załadowany wstrzykiwacz z powrotem do futerału, ponieważ spowoduje to uszkodzenie igły.
Jak stosować wstrzykiwacz IMITREX STAT do zażywania leku?
Przed wstrzyknięciem leku należy wybrać obszar z warstwą tkanki tłuszczowej (patrz Rysunek E lub Rysunek F). Zapytaj swojego lekarza, jeśli masz pytanie, gdzie wstrzyknąć lek.
celu przygotowania obszaru skóry, w który ma zostać wstrzyknięty IMITREX, przetrzeć miejsce wstrzyknięcia gazikiem nasączonym alkoholem. Nie dotykać ponownie tego obszaru przed wykonaniem wstrzyknięcia.
Rysunek E lub Rysunek F Rysunek G 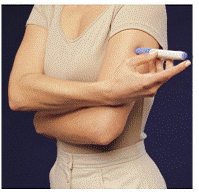
6. Bez naciskania niebieskiego przycisku, mocno dociśnij załadowany wstrzykiwacz do skóry tak, aby szary korpus zsunął się w kierunku niebieskiej części, w której znajduje się wkład strzykawki (patrz Rysunek D ). (To zwalnia blokadę bezpieczeństwa, która zapobiega przypadkowemu uruchomieniu pióra, dopóki nie będziesz gotowy).
7. Naciśnij niebieski przycisk. Trzymaj długopis nieruchomo przez co najmniej 5 sekund . Jeśli wstrzykiwacz zostanie zbyt szybko oderwany od skóry, nie cały lek zostanie usunięty.
8 Po 5 sekundach , ostrożnie zdjąć wstrzykiwacz ze skóry. Igła pokaże (patrz Rysunek G ). Nie dotykaj igły.
Jak rozładować wstrzykiwacz dawki IMITREX STAT po zażyciu leku?
Zaraz po przyjęciu dawki za pomocą wstrzykiwacza należy zwrócić zużyty wkład strzykawki do opakowania wkładu.
Rysunek H Rysunek I i rysunek J 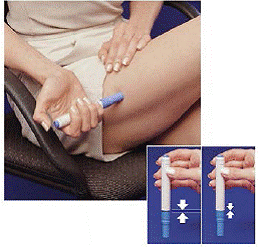
9. Wciśnij wstrzykiwacz w pustą stronę wkładu do oporu (patrz Rysunek H ).
10. Obróć wstrzykiwacz w lewo (przeciwnie do ruchu wskazówek zegara) o około pół obrotu, aż zostanie zwolniony z wkładu strzykawki (patrz Rysunek I ).
11. Wyciągnij pusty wstrzykiwacz z opakowania wkładu (patrz Rysunek J ).
Ponieważ pisak został już użyty, biały pręt zalewania będzie wystawał z dolnego końca pisaka (patrz Rysunek J ).
12. Zamknij pokrywę pojemnika na zużyty wkład strzykawki. Po prawidłowym włożeniu zużytych wkładów strzykawek opakowanie z wkładem stanowi jednorazowe opakowanie ochronne, które pomaga uniknąć ukłucia się igłą i prawidłowego używania strzykawek.
13. Włóż wstrzykiwacz z powrotem do futerału i mocno dociśnij, aż poczujesz kliknięcie. Zamknij pokrywę futerału. Dzięki temu pióro jest gotowe do następnego użycia.
Jeśli pokrywa się nie zamyka, wciśnij wstrzykiwacz, aż poczujesz kliknięcie. Następnie zamknij pokrywę.
Jak wyjąć zużyty zestaw wkładów?
Po użyciu obu wkładów strzykawek wyjmij opakowanie wkładu z futerału. Nigdy nie używaj ponownie ani nie poddaj recyklingowi wkładu strzykawki.
Rysunek K Rysunek L 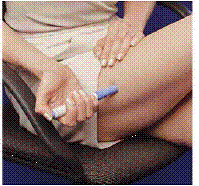
14. Otwórz pokrywę torby transportowej.
15. Przytrzymaj jedną ręką futerał i naciśnij 2 przyciski po obu stronach futerału (patrz Rysunek K ).
16. Drugą ręką delikatnie wyciągnij kasetę (patrz Rysunek L ).
17. Wyrzuć opakowanie z wkładem lub wyrzuć go zgodnie z instrukcjami lekarza. Mogą obowiązywać specjalne przepisy stanowe i lokalne dotyczące usuwania zużytych igieł i strzykawek. Zawsze przechowywać poza zasięgiem dzieci.
Jak włożyć nowy zestaw wkładów
Rysunek M Rysunek N i Rysunek O 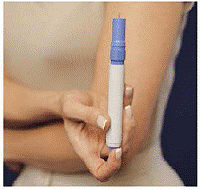
18. Wyjmij nowe opakowanie kasety z pudełka. Nie zdejmuj plomb gwarancyjnych (patrz Rysunek M).
19. Włóż kasetę do futerału. Przesuń go płynnie w dół (patrz Rysunek N ).
20. Zestaw wkładów zatrzaśnie się na swoim miejscu, gdy 2 przyciski przejdą przez otwory w futerale (patrz Postać O ). Zamknij pokrywę.
Niniejsze informacje dla pacjenta i instrukcje użytkowania zostały zatwierdzone przez amerykańską Agencję ds. Żywności i Leków.
