Naprelan 250mg, 500mg Naproxen Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Naprelan i jak się go stosuje?
Naprelan to lek na receptę stosowany w leczeniu objawów reumatoidalnego zapalenia stawów, choroby zwyrodnieniowej stawów, zesztywniającego zapalenia stawów kręgosłupa, bolesnego miesiączkowania, ostrej dny moczanowej i bólu. Naprelan można stosować samodzielnie lub z innymi lekami.
Naprelan należy do klasy leków zwanych NLPZ.
Nie wiadomo, czy Naprelan 250 mg jest bezpieczny i skuteczny u dzieci w wieku poniżej 2 lat.
Jakie są możliwe skutki uboczne leku Naprelan 500mg?
Naprelan może powodować poważne działania niepożądane, w tym:
- pokrzywka,
- trudności w oddychaniu,
- obrzęk twarzy, warg, języka lub gardła,
- łatwość powstawania siniaków lub krwawień,
- trudne lub bolesne połykanie,
- dzwonienie w uszach,
- zmiany nastroju,
- zmiany ilości moczu,
- niewyjaśniony sztywny kark,
- zmiany widzenia,
- obrzęk kostek i stóp,
- niezwykłe zmęczenie,
- nietypowy i nagły przyrost masy ciała,
- ciemny mocz,
- uporczywe nudności lub wymioty,
- utrata apetytu,
- ból brzucha,
- zażółcenie oczu lub skóry (żółtaczka) oraz
- silne zawroty głowy
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze działania niepożądane leku Naprelan to:
- rozstrój żołądka,
- mdłości,
- zgaga,
- ból głowy,
- podwyższone ciśnienie krwi
- senność i
- zawroty głowy
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe działania niepożądane leku Naprelan. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OSTRZEŻENIE
RYZYKO POWAŻNYCH ZDARZEŃ SERCOWO-NACZYNIOWYCH I PRZEWODOWYCH
Zdarzenia zakrzepowo-sercowe
- Niesteroidowe leki przeciwzapalne (NLPZ) zwiększają ryzyko poważnych incydentów zakrzepowych układu krążenia, w tym zawału mięśnia sercowego i udaru mózgu, które mogą być śmiertelne. Ryzyko to może wystąpić na początku leczenia i może narastać wraz z czasem stosowania [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
- NAPRELAN jest przeciwwskazany w przypadku operacji pomostowania aortalno-wieńcowego (CABG) [patrz PRZECIWWSKAZANIA i OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
Krwawienie z przewodu pokarmowego, owrzodzenie i perforacja
- NLPZ powodują zwiększone ryzyko poważnych działań niepożądanych ze strony przewodu pokarmowego (GI), w tym krwawienia, owrzodzenia i perforacji żołądka lub jelit, które mogą być śmiertelne. Zdarzenia te mogą wystąpić w dowolnym momencie podczas użytkowania i bez objawów ostrzegawczych. Pacjenci w podeszłym wieku oraz pacjenci z chorobą wrzodową i/lub krwawieniem z przewodu pokarmowego w wywiadzie są narażeni na większe ryzyko poważnych zdarzeń żołądkowo-jelitowych [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
OPIS
NAPRELAN (naproksen sodu) Controlled-Release Tablets to niesteroidowy lek przeciwzapalny, dostępny w postaci tabletek o kontrolowanym uwalnianiu o mocy 375 mg, 500 mg i 750 mg do podawania doustnego. Nazwa chemiczna to sól 6-metoksy-α-metylo-sodowa kwasu 2-naftalenooctowego, (S)-. Masa cząsteczkowa wynosi 252,24. Jego wzór cząsteczkowy to C14H13NaO3 i ma następującą strukturę chemiczną.
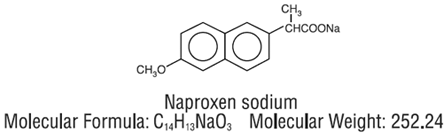
Naproksen sodu jest bezwonnym krystalicznym proszkiem o barwie od białej do kremowej. Jest rozpuszczalny w metanolu i wodzie. Tabletki NAPRELAN 250 mg zawierają 412,5 mg, 550 mg lub 825 mg naproksenu sodu, co odpowiada odpowiednio 375 mg, 500 mg i 750 mg naproksenu oraz 37,5 mg, 50 mg i 75 mg sodu. Każda tabletka NAPRELAN 250 mg zawiera również następujące nieaktywne składniki: kopolimer metakrylanu amoniowego typu A, kopolimer etakrylanu amoniowego typu B, kwas cytrynowy, krospowidon, stearynian magnezu, kopolimer kwasu metakrylowego typu A, celuloza mikrokrystaliczna, powidon i talk. Otoczka tabletki zawiera hydroksypropylometylocelulozę, glikol polietylenowy i dwutlenek tytanu.
WSKAZANIA
NAPRELAN 250mg Tabletki są wskazane w leczeniu:
- reumatoidalne zapalenie stawów (RZS)
- choroba zwyrodnieniowa stawów (OA)
- zesztywniające zapalenie stawów kręgosłupa (AS)
- zapalenie ścięgna, zapalenie kaletki
- ostra dna moczanowa
- pierwotne bolesne miesiączkowanie (PD)
- łagodzenie bólu o nasileniu od łagodnego do umiarkowanego
 [patrz OSTRZEŻENIA I ŚRODKI ].
DAWKOWANIE I SPOSÓB PODAWANIA
Ogólne instrukcje dozowania
Przed podjęciem decyzji o zastosowaniu NAPRELANU należy dokładnie rozważyć potencjalne korzyści i zagrożenia związane z NAPRELANEM i innymi opcjami leczenia. Stosuj najniższą skuteczną dawkę przez najkrótszy czas, zgodnie z indywidualnymi celami leczenia pacjenta [patrz OSTRZEŻENIA I ŚRODKI ].
Po zaobserwowaniu odpowiedzi na wstępną terapię NAPRELANEM należy dostosować dawkę i częstotliwość do indywidualnych potrzeb pacjenta.
Reumatoidalne zapalenie stawów, choroba zwyrodnieniowa stawów i zesztywniające zapalenie stawów kręgosłupa
Zalecana dawka początkowa tabletek NAPRELAN u dorosłych to dwie tabletki NAPRELAN 375 mg (750 mg) raz na dobę, jedna tabletka NAPRELAN 750 mg (750 mg) raz na dobę lub dwie tabletki NAPRELAN 500 mg (1000 mg) raz na dobę. U pacjentów przyjmujących już 250 mg, 375 mg lub 500 mg naproksenu dwa razy na dobę (rano i wieczorem) całkowitą dawkę dobową można zastąpić tabletkami NAPRELAN 500 mg w pojedynczej dawce dobowej.
Podczas długotrwałego podawania dawki leku NAPRELAN 250 mg tabletki można zwiększać lub zmniejszać w zależności od odpowiedzi klinicznej pacjenta. U pacjentów, którzy dobrze tolerują niższe dawki tabletek NAPRELANU, dawkę można zwiększyć do dwóch tabletek NAPRELAN 750 mg (1500 mg) lub trzech tabletek NAPRELAN 500 mg (1500 mg) raz dziennie przez ograniczony okres czasu, gdy wyższy poziom działania przeciwzapalnego / wymagane jest działanie przeciwbólowe. Podczas leczenia pacjentów, zwłaszcza przy wyższych dawkach, lekarz powinien obserwować wystarczająco zwiększone korzyści kliniczne, aby zrównoważyć potencjalne zwiększone ryzyko [patrz FARMAKOLOGIA KLINICZNA ]. U każdego pacjenta należy poszukiwać i stosować najniższą skuteczną dawkę. Objawowa poprawa zapalenia stawów zwykle rozpoczyna się w ciągu jednego tygodnia; jednak do osiągnięcia korzyści terapeutycznych może być wymagane leczenie przez dwa tygodnie.
Leczenie bólu, pierwotnego bolesnego miesiączkowania oraz ostrego zapalenia ścięgna i zapalenia kaletki
Zalecana dawka początkowa to dwie tabletki NAPRELAN 500 mg (1000 mg) raz na dobę. W przypadku pacjentów wymagających większych korzyści przeciwbólowych można przez ograniczony okres stosować dwie tabletki NAPRELAN 750 mg (1500 mg) lub trzy tabletki NAPRELAN 500 mg (1500 mg). Następnie całkowita dawka dobowa nie powinna przekraczać dwóch tabletek NAPRELAN 500 mg (1000 mg).
Ostra dna moczanowa
Zalecana dawka pierwszego dnia to dwie do trzech tabletek NAPRELAN 500 mg (1000 do 1500 mg) raz na dobę, a następnie dwie tabletki NAPRELAN 500 mg (1000 mg) raz na dobę, aż do ustąpienia napadu.
Dostosowanie dawkowania u pacjentów z niewydolnością wątroby
Mniejszą dawkę należy rozważyć u pacjentów z zaburzeniami czynności nerek lub wątroby lub u pacjentów w podeszłym wieku [patrz OSTRZEŻENIA I ŚRODKI ]. Badania wskazują, że chociaż całkowite stężenie naproksenu w osoczu pozostaje niezmienione, niezwiązana frakcja naproksenu w osoczu jest zwiększona u osób w podeszłym wieku. Zaleca się ostrożność, gdy wymagane są duże dawki, a u pacjentów w podeszłym wieku może być konieczne pewne dostosowanie dawki. Podobnie jak w przypadku innych leków stosowanych u osób starszych, rozsądnie jest stosować najmniejszą skuteczną dawkę.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Tabletki o kontrolowanym uwalnianiu NAPRELAN (naproksen sodu) są dostępne w następujący sposób:
- NAPRELAN 375: biała tabletka w kształcie kapsułki z literą „N” po jednej stronie i „375” na odwrocie. Każda tabletka zawiera 412,5 mg naproksenu sodu, co odpowiada 375 mg naproksenu.
- NAPRELAN 500: biała tabletka w kształcie kapsułki z literą „N” po jednej stronie i „500” po drugiej stronie. Każda tabletka zawiera 550 mg naproksenu sodowego, co odpowiada 500 mg naproksenu.
- NAPRELAN 750: biała tabletka w kształcie kapsułki z literą „N” po jednej stronie i „750” na odwrocie. Każda tabletka zawiera 825 mg naproksenu sodowego, co odpowiada 750 mg naproksenu.
Składowania i stosowania
NAPRELAN (naproksen sodu) 375 mg, 500 mg i 750 mg to tabletki o kontrolowanym uwalnianiu dostarczane jako:
NAPRELAN 375 : biała tabletka w kształcie kapsułki z literą „N” po jednej stronie i „375” po drugiej stronie; w butelkach po 100 sztuk; NDC 52427-272-01. Każda tabletka zawiera 412,5 mg naproksenu sodu, co odpowiada 375 mg naproksenu.
NAPRELAN 500 : biała tabletka w kształcie kapsułki z literą „N” po jednej stronie i „500” po drugiej stronie; w butelkach po 75 sztuk; NDC 52427-273-75. Każda tabletka zawiera 550 mg naproksenu sodowego, co odpowiada 500 mg naproksenu.
NAPRELAN 750 : biała tabletka w kształcie kapsułki z literą „N” po jednej stronie i „750” na odwrocie; w butelkach po 30 sztuk; NDC 52427-274-30. Każda tabletka zawiera 825 mg naproksenu sodowego, co odpowiada 750 mg naproksenu.
Magazynowanie
Przechowywać w temperaturze pokojowej, 20° do 25°C (68° do 77°F), dopuszczalne odchylenia od 15° do 30°C (59° do 86°F) [patrz Kontrolowana temperatura pokojowa USP]. APTEKA: Dozować w dobrze zamkniętym pojemniku.
Dystrybutor: Almatica Pharma, Inc. Morristown, NJ 07960 USA. Poprawiono: kwiecień 2021
SKUTKI UBOCZNE
Następujące działania niepożądane omówiono bardziej szczegółowo w innych punktach oznakowania:
- Sercowo-naczyniowe zdarzenia zakrzepowe [patrz OSTRZEŻENIA I ŚRODKI ]
- Krwawienie, owrzodzenie i perforacja przewodu pokarmowego [patrz OSTRZEŻENIA I ŚRODKI ]
- Hepatotoksyczność [patrz OSTRZEŻENIA I ŚRODKI ]
- Nadciśnienie [patrz OSTRZEŻENIA I ŚRODKI ]
- Niewydolność serca i obrzęk [patrz OSTRZEŻENIA I ŚRODKI ]
- Toksyczność nerek i hiperkaliemia [patrz OSTRZEŻENIA I ŚRODKI ]
- Reakcje anafilaktyczne [patrz OSTRZEŻENIA I ŚRODKI ]
- Poważne reakcje skórne [patrz OSTRZEŻENIA I ŚRODKI ]
- Toksyczność hematologiczna [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Podobnie jak w przypadku wszystkich leków z tej klasy, częstość i nasilenie zdarzeń niepożądanych zależy od kilku czynników: dawki leku i czasu trwania leczenia; wiek, płeć, stan fizyczny pacjenta; wszelkie współistniejące diagnozy medyczne lub indywidualne czynniki ryzyka. Poniższe działania niepożądane podzielono na trzy części w zależności od częstości występowania oraz tego, czy istnieje możliwość związku przyczynowego między stosowaniem leku a tymi zdarzeniami niepożądanymi. W przypadku reakcji wymienionych jako „Prawdopodobny związek przyczynowy” istnieje co najmniej jeden przypadek dla każdego działania niepożądanego, w którym istnieją dowody sugerujące, że istnieje związek przyczynowy między stosowaniem leku a zgłaszanym zdarzeniem. Zgłaszane działania niepożądane oparto na wynikach dwóch kontrolowanych badań klinicznych z podwójnie ślepą próbą, trwających trzy miesiące, z dodatkowym dziewięciomiesięcznym przedłużeniem otwartej próby. Łącznie 542 pacjentów otrzymało tabletki NAPRELAN albo w okresie podwójnie ślepej próby, albo w dziewięciomiesięcznym przedłużeniu otwartej próby. Spośród tych 542 pacjentów, 232 otrzymało tabletki NAPRELAN, 167 było początkowo leczonych Naprosynem®, a 143 było początkowo leczonych placebo. Działania niepożądane zgłaszane przez pacjentów, którzy otrzymywali tabletki NAPRELAN 500 mg, są przedstawiane w układzie narządu. Te działania niepożądane obserwowane podczas stosowania naproksenu, ale nie zgłoszone w kontrolowanych badaniach dotyczących tabletek NAPRELAN, są oznaczone kursywą.
Najczęstszymi zdarzeniami niepożądanymi z podwójnie ślepych i otwartych badań klinicznych były bóle głowy (15%), a następnie niestrawność (14%) i zespół grypowy (10%). Częstość występowania innych zdarzeń niepożądanych występujących u 3% do 9% pacjentów zaznaczono gwiazdką.
Reakcje występujące u mniej niż 3% pacjentów są nieoznaczone.
Częstość występowania większa niż 1% (prawdopodobny związek przyczynowy)
Ciało jako całość - Ból (plecy)*, ból*, infekcja*, gorączka, uraz (wypadek), astenia, ból w klatce piersiowej, ból głowy (15%), zespół grypowy (10%).
Przewód pokarmowy - Nudności*, biegunka*, zaparcia*, ból brzucha*, wzdęcia, zapalenie żołądka, wymioty, dysfagia, niestrawność (14%), zgaga*, zapalenie jamy ustnej.
Hematologiczny - Anemia, wybroczyny.
Układ oddechowy - Zapalenie gardła*, nieżyt nosa*, zapalenie zatok*, zapalenie oskrzeli, nasilony kaszel.
nerki - Zakażenie dróg moczowych*, zapalenie pęcherza moczowego.
Dermatologiczne - Wysypka*, wykwity skórne*, wybroczyny*, plamica.
Metabolizm i odżywianie - Obrzęki obwodowe, hiperglikemia.
Ośrodkowy układ nerwowy - Zawroty głowy, parestezje, bezsenność, senność*, oszołomienie.
Układ sercowo-naczyniowy - Nadciśnienie, obrzęk*, duszność*, kołatanie serca.
Układ mięśniowo-szkieletowy - Skurcze (nogi), bóle mięśni, bóle stawów, zaburzenia stawów, zaburzenia ścięgien.
Zmysły specjalne - Szumy uszne*, zaburzenia słuchu, zaburzenia widzenia.
Ogólny - Pragnienie.
Częstość występowania mniej niż 1% (prawdopodobny związek przyczynowy)
Ciało jako całość - Ropień, monilia, sztywność karku, ból szyi, powiększenie brzucha, rak, zapalenie tkanki łącznej, obrzęk ogólny, zespół LE, złe samopoczucie, zaburzenia błony śluzowej, reakcja alergiczna, ból miednicy.
Przewód pokarmowy - Anoreksja, zapalenie pęcherzyka żółciowego, kamica żółciowa, odbijanie się, krwotok z przewodu pokarmowego, krwotok z odbytu, aftowe zapalenie jamy ustnej, wrzód jamy ustnej, wrzód jamy ustnej, wrzód żołądka, ropień przyzębia, skurcz serca, zapalenie okrężnicy, zapalenie przełyku, zapalenie żołądka i jelit, nieprawidłowości, smoliste stolce, wrzód przełyku, krwawe wymioty, żółtaczka, zapalenie trzustki, martwica.
nerki - Bolesne miesiączkowanie, bolesne oddawanie moczu, zaburzenia czynności nerek, nokturia, zaburzenia prostaty, odmiedniczkowe zapalenie nerek, rak piersi, nietrzymanie moczu, kamień nerkowy, niewydolność nerek, krwotok miesiączkowy, krwotok maciczny, nowotwór piersi, miażdżyca nerek, krwiomocz, ból nerek, ropomocz, nieprawidłowe oddawanie moczu, częste oddawanie moczu zatrzymanie, skurcz macicy, zapalenie pochwy, kłębuszkowe zapalenie nerek, hiperkaliemia, śródmiąższowe zapalenie nerek, zespół nerczycowy, choroba nerek, niewydolność nerek, martwica brodawek nerkowych.
Hematologiczny - Leukopenia, wydłużenie czasu krwawienia, eozynofilia, nieprawidłowe RBC, nieprawidłowe WBC, trombocytopenia, agranulocytoza, granulocytopenia.
Ośrodkowy układ nerwowy - Depresja, lęk, hipertonia, nerwowość, nerwoból, zapalenie nerwu, zawroty głowy, amnezja, splątanie, koordynacja, nieprawidłowe podwójne widzenie, labilność emocjonalna, krwiak podtwardówkowy, porażenie, zaburzenia snu, niemożność koncentracji, osłabienie mięśni.
Dermatologiczne: Angiodermatitis, opryszczka zwykła, suchość skóry, pocenie się, owrzodzenie skóry, trądzik, łysienie, kontaktowe zapalenie skóry, egzema, półpasiec, zaburzenia paznokci, martwica skóry, guzek podskórny, świąd, pokrzywka, nowotwory skóry, światłoczułe zapalenie skóry, reakcje nadwrażliwości na światło przypominające porfirię skórną , pęcherzowe oddzielanie się naskórka.
Zmysły specjalne - Niedowidzenie, zapalenie twardówki, zaćma, zapalenie spojówek, głuchota, zaburzenia ucha, zapalenie rogówki i spojówki, zaburzenia łzawienia, zapalenie ucha środkowego, ból oka.
Układ sercowo-naczyniowy - Dławica piersiowa, choroba wieńcowa, zawał mięśnia sercowego, zakrzepowe zapalenie żył głębokich, rozszerzenie naczyń, anomalia naczyniowa, arytmia, blok odnogi pęczka Hisa, nieprawidłowy zapis EKG, niewydolność prawostronna, krwotok, migrena, zwężenie aorty, omdlenie, tachykardia, zastoinowa niewydolność serca.
Układ oddechowy - Astma, duszność, obrzęk płuc, zapalenie krtani, zaburzenia płuc, krwawienie z nosa, zapalenie płuc, niewydolność oddechowa, zaburzenia oddechowe, eozynofilowe zapalenie płuc.
Układ mięśniowo-szkieletowy - Miastenia, choroba kości, samoistne złamanie kości, zapalenie ścięgna, ból kości, opadanie powiek, ogólny skurcz, zapalenie kaletki.
Metabolizm i odżywianie - Wzrost kreatyniny, cukromocz, hipercholesterolemia, albuminuria, zasadowica, podwyższenie BUN, odwodnienie, obrzęk, zmniejszenie tolerancji glukozy, hiperurykemia, hipokaliemia, wzrost SGOT, wzrost SGPT, zmniejszenie masy ciała.
Ogólny - Reakcje rzekomoanafilaktyczne, obrzęk naczynioruchowy, zaburzenia miesiączkowania, hipoglikemia, gorączka (dreszcze i gorączka).
Częstość występowania mniej niż 1% (związek przyczynowy nieznany)
Inne działania niepożądane wymienione na etykiecie opakowania naproksenu, ale nie zgłoszone przez osoby, które otrzymały tabletki NAPRELAN, są oznaczone kursywą. Obserwacje te są wymieniane jako informacje alarmujące dla lekarza.
Hematologiczny - Niedokrwistość aplastyczna, niedokrwistość hemolityczna.
Ośrodkowy układ nerwowy - Aseptyczne zapalenie opon mózgowych, zaburzenia funkcji poznawczych.
Dermatologiczne - Martwica naskórka, rumień wielopostaciowy, zespół Stevensa-Johnsona.
Przewód pokarmowy - Niestrawne owrzodzenie przewodu pokarmowego, wrzodziejące zapalenie jamy ustnej.
Układ sercowo-naczyniowy - Zapalenie naczyń.
INTERAKCJE Z LEKAMI
W Tabeli 1 przedstawiono klinicznie istotne interakcje leków z naproksenem.
Interakcje leków/testów laboratoryjnych
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Zdarzenia zakrzepowo-sercowe
Badania kliniczne kilku selektywnych i nieselektywnych NLPZ COX-2 trwające do trzech lat wykazały zwiększone ryzyko poważnych zakrzepowych zdarzeń sercowo-naczyniowych (CV), w tym zawału mięśnia sercowego (MI) i udaru mózgu, które mogą być śmiertelne. Na podstawie dostępnych danych nie jest jasne, czy ryzyko wystąpienia incydentów zakrzepowych w układzie sercowo-naczyniowym jest podobne w przypadku wszystkich NLPZ. Względny wzrost częstości występowania poważnych incydentów zakrzepowych w układzie sercowo-naczyniowym w porównaniu z wartościami wyjściowymi spowodowany stosowaniem NLPZ wydaje się być podobny u osób z rozpoznaną chorobą sercowo-naczyniową lub czynnikami ryzyka choroby sercowo-naczyniowej lub bez nich. Jednak pacjenci z rozpoznaną chorobą sercowo-naczyniową lub czynnikami ryzyka mieli większą bezwzględną częstość występowania poważnych incydentów zakrzepowych sercowo-naczyniowych ze względu na ich zwiększoną wyjściową częstość występowania. Niektóre badania obserwacyjne wykazały, że to zwiększone ryzyko poważnych incydentów zakrzepowych układu sercowo-naczyniowego rozpoczęło się już w pierwszych tygodniach leczenia. Wzrost ryzyka zakrzepicy sercowo-naczyniowej był najbardziej konsekwentnie obserwowany przy wyższych dawkach.
Aby zminimalizować potencjalne ryzyko wystąpienia niepożądanego zdarzenia sercowo-naczyniowego u pacjentów leczonych NLPZ, należy stosować najniższą skuteczną dawkę przez możliwie najkrótszy czas. Lekarze i pacjenci powinni zachować czujność na rozwój takich zdarzeń przez cały cykl leczenia, nawet przy braku wcześniejszych objawów sercowo-naczyniowych. Pacjentów należy poinformować o objawach poważnych zdarzeń sercowo-naczyniowych oraz o krokach, jakie należy podjąć w przypadku ich wystąpienia.
Nie ma spójnych dowodów na to, że jednoczesne stosowanie aspiryny łagodzi zwiększone ryzyko poważnych incydentów zakrzepicy sercowo-naczyniowej związane ze stosowaniem NLPZ. Jednoczesne stosowanie aspiryny i NLPZ, takich jak naproksen, zwiększa ryzyko poważnych zdarzeń żołądkowo-jelitowych (GI) [patrz OSTRZEŻENIA I ŚRODKI ].
Stan po zabiegu pomostowania tętnic wieńcowych (CABG)
Dwa duże, kontrolowane badania kliniczne NLPZ selektywnego wobec COX-2 w leczeniu bólu w ciągu pierwszych 10-14 dni po operacji CABG wykazały zwiększoną częstość występowania zawału mięśnia sercowego i udaru mózgu. NLPZ są przeciwwskazane w CABG [patrz PRZECIWWSKAZANIA ].
Pacjenci po MI
Badania obserwacyjne przeprowadzone w Duńskim Krajowym Rejestrze wykazały, że pacjenci leczeni NLPZ w okresie po MI byli narażeni na zwiększone ryzyko ponownego zawału, zgonów z przyczyn sercowo-naczyniowych i śmiertelności z jakiejkolwiek przyczyny, począwszy od pierwszego tygodnia leczenia. W tej samej kohorcie częstość zgonów w pierwszym roku po MI wynosiła 20 na 100 osobolat u pacjentów leczonych NLPZ w porównaniu z 12 na 100 osobolat u pacjentów nie narażonych na NLPZ. Chociaż bezwzględny wskaźnik zgonów zmniejszył się nieco po pierwszym roku po MI, zwiększone względne ryzyko zgonu u osób stosujących NLPZ utrzymywało się przez co najmniej kolejne cztery lata obserwacji.
Należy unikać stosowania leku NAPRELAN 250 mg u pacjentów po niedawno przebytym zawale serca, chyba że oczekuje się, że korzyści przewyższą ryzyko nawrotów zakrzepicy sercowo-naczyniowej. Jeśli NAPRELAN jest stosowany u pacjentów po niedawno przebytym MI, należy monitorować pacjentów pod kątem objawów niedokrwienia serca.
Krwawienie z przewodu pokarmowego, owrzodzenie i perforacja
NLPZ, w tym naproksen, powodują poważne zdarzenia niepożądane ze strony przewodu pokarmowego (GI), w tym zapalenie, krwawienie, owrzodzenie i perforację przełyku, żołądka, jelita cienkiego lub grubego, które mogą być śmiertelne. Te poważne zdarzenia niepożądane mogą wystąpić w dowolnym momencie, z objawami ostrzegawczymi lub bez, u pacjentów leczonych NLPZ. Tylko jeden na pięciu pacjentów, u których wystąpiło poważne zdarzenie niepożądane w górnym odcinku przewodu pokarmowego podczas leczenia NLPZ, ma charakter objawowy. Owrzodzenia górnego odcinka przewodu pokarmowego, duże krwawienia lub perforacje spowodowane przez NLPZ wystąpiły u około 1% pacjentów leczonych przez 3 do 6 miesięcy i u około 2% do 4% pacjentów leczonych przez jeden rok. Jednak nawet krótkotrwała terapia NLPZ nie jest pozbawiona ryzyka.
Czynniki ryzyka krwawienia z przewodu pokarmowego, owrzodzeń i perforacji
Pacjenci z chorobą wrzodową w wywiadzie i/lub krwawieniem z przewodu pokarmowego, którzy stosowali NLPZ, mieli ponad 10-krotnie większe ryzyko wystąpienia krwawienia z przewodu pokarmowego w porównaniu z pacjentami bez tych czynników ryzyka. Inne czynniki zwiększające ryzyko krwawienia z przewodu pokarmowego u pacjentów leczonych NLPZ obejmują dłuższy czas leczenia NLPZ; jednoczesne stosowanie doustnych kortykosteroidów, aspiryny, antykoagulantów lub selektywnych inhibitorów wychwytu zwrotnego serotoniny (SSRI); palenie; używanie alkoholu; starszy wiek; i zły ogólny stan zdrowia. Większość zgłoszeń po wprowadzeniu do obrotu śmiertelnych zdarzeń ze strony przewodu pokarmowego dotyczyła pacjentów w podeszłym wieku lub osłabionych. Ponadto pacjenci z zaawansowaną chorobą wątroby i/lub koagulopatią są narażeni na zwiększone ryzyko krwawienia z przewodu pokarmowego.
Strategie minimalizacji ryzyka przewodu pokarmowego u pacjentów leczonych NLPZ
- Użyj najniższej skutecznej dawki przez możliwie najkrótszy czas.
- Unikaj jednoczesnego podawania więcej niż jednego NLPZ.
- Należy unikać stosowania u pacjentów z grupy podwyższonego ryzyka, chyba że spodziewane korzyści przewyższają zwiększone ryzyko krwawienia. W przypadku takich pacjentów, a także tych z aktywnym krwawieniem z przewodu pokarmowego, należy rozważyć alternatywne terapie inne niż NLPZ.
- Zachowaj czujność na oznaki i objawy owrzodzenia przewodu pokarmowego i krwawienia podczas leczenia NLPZ.
- przypadku podejrzenia poważnego zdarzenia niepożądanego ze strony przewodu pokarmowego należy niezwłocznie rozpocząć ocenę i leczenie, a następnie odstawić NAPRELAN 250 mg do czasu wykluczenia poważnego zdarzenia niepożądanego ze strony przewodu pokarmowego.
- W przypadku jednoczesnego stosowania małej dawki aspiryny w profilaktyce kardiologicznej należy uważniej monitorować pacjentów pod kątem krwawienia z przewodu pokarmowego [patrz INTERAKCJE Z LEKAMI ].
Hepatotoksyczność
W badaniach klinicznych u około 1% pacjentów leczonych NLPZ zgłaszano zwiększenie aktywności AlAT lub AspAT (trzy lub więcej razy powyżej górnej granicy normy [GGN]). Ponadto zgłaszano rzadkie, czasami śmiertelne przypadki ciężkiego uszkodzenia wątroby, w tym piorunującego zapalenia wątroby, martwicy wątroby i niewydolności wątroby.
Podwyższenie aktywności AlAT lub AspAT (mniej niż trzykrotność GGN) może wystąpić nawet u 15% pacjentów leczonych NLPZ, w tym naproksenem.
Należy poinformować pacjentów o oznakach i objawach ostrzegawczych hepatotoksyczności (np. nudności, zmęczenie, letarg, biegunka, świąd, żółtaczka, tkliwość w prawym górnym kwadrancie i objawy grypopodobne). Jeśli pojawią się objawy kliniczne wskazujące na chorobę wątroby lub jeśli wystąpią objawy ogólnoustrojowe (np. eozynofilia, wysypka itp.), należy natychmiast przerwać podawanie leku NAPRELAN 500 mg i przeprowadzić ocenę kliniczną pacjenta.
Nadciśnienie
NLPZ, w tym NAPRELAN, mogą prowadzić do nowego początku lub pogorszenia istniejącego nadciśnienia, co może przyczynić się do zwiększonej częstości występowania incydentów sercowo-naczyniowych. Pacjenci przyjmujący inhibitory konwertazy angiotensyny (ACE), diuretyki tiazydowe lub diuretyki pętlowe mogą mieć osłabioną odpowiedź na te terapie podczas przyjmowania NLPZ [patrz INTERAKCJE Z LEKAMI ].
Monitorować ciśnienie krwi (BP) podczas rozpoczynania leczenia NLPZ oraz w trakcie leczenia.
Niewydolność serca i obrzęk
Metaanaliza randomizowanych badań kontrolowanych Coxib and traditional NSAID Trialists' Collaboration wykazała około dwukrotny wzrost liczby hospitalizacji z powodu niewydolności serca u pacjentów leczonych selektywnie COX-2 i nieselektywnych NLPZ w porównaniu z pacjentami otrzymującymi placebo. W badaniu duńskiego krajowego rejestru pacjentów z niewydolnością serca stosowanie NLPZ zwiększało ryzyko zawału serca, hospitalizacji z powodu niewydolności serca i zgonu.
Ponadto u niektórych pacjentów leczonych NLPZ obserwowano zatrzymanie płynów i obrzęki. Stosowanie naproksenu może osłabić wpływ na CV kilku środków terapeutycznych stosowanych w leczeniu tych schorzeń (np. diuretyków, inhibitorów ACE lub blokerów receptora angiotensyny [ARB]) [patrz INTERAKCJE Z LEKAMI ].
Należy unikać stosowania leku NAPRELAN 250 mg u pacjentów z ciężką niewydolnością serca, chyba że spodziewane korzyści przewyższają ryzyko pogorszenia niewydolności serca. Jeśli NAPRELAN jest stosowany u pacjentów z ciężką niewydolnością serca, należy monitorować pacjentów pod kątem objawów pogorszenia niewydolności serca.
Toksyczność nerek i hiperkaliemia
Toksyczność nerek
Długotrwałe podawanie NLPZ spowodowało martwicę brodawek nerkowych i inne uszkodzenie nerek.
Toksyczny wpływ na nerki obserwowano również u pacjentów, u których prostaglandyny nerkowe pełnią funkcję kompensacyjną w utrzymaniu perfuzji nerek. U tych pacjentów podawanie NLPZ może powodować zależne od dawki zmniejszenie wytwarzania prostaglandyn i, wtórnie, nerkowego przepływu krwi, co może przyspieszyć jawną dekompensację nerek. Największe ryzyko wystąpienia tej reakcji to pacjenci z zaburzeniami czynności nerek, odwodnieniem, hipowolemią, niewydolnością serca, zaburzeniami czynności wątroby, przyjmujący leki moczopędne i inhibitory ACE lub ARB oraz osoby starsze. Po przerwaniu leczenia NLPZ następuje zazwyczaj powrót do stanu sprzed leczenia.
Brak informacji z kontrolowanych badań klinicznych dotyczących stosowania preparatu NAPRELAN u pacjentów z zaawansowaną chorobą nerek. Działanie leku NAPRELAN 250 mg na nerki może przyspieszyć postęp zaburzeń czynności nerek u pacjentów z istniejącą wcześniej chorobą nerek.
Prawidłowy stan objętości u pacjentów odwodnionych lub z hipowolemią przed rozpoczęciem leczenia NAPRELAN. Monitorować czynność nerek u pacjentów z zaburzeniami czynności nerek lub wątroby, niewydolnością serca, odwodnieniem lub hipowolemią podczas stosowania leku NAPRELAN [patrz INTERAKCJE Z LEKAMI ]. Należy unikać stosowania leku NAPRELAN 500 mg u pacjentów z zaawansowaną chorobą nerek, chyba że spodziewane korzyści przewyższają ryzyko pogorszenia czynności nerek. Jeśli NAPRELAN jest stosowany u pacjentów z zaawansowaną chorobą nerek, należy monitorować pacjentów pod kątem objawów pogorszenia czynności nerek.
Hiperkaliemia
Podczas stosowania NLPZ zgłaszano zwiększenie stężenia potasu w surowicy, w tym hiperkaliemię, nawet u niektórych pacjentów bez zaburzeń czynności nerek. U pacjentów z prawidłową czynnością nerek działania te przypisano stanowi hiporeninemii i hipoaldosteronizmu.
Reakcje anafilaktyczne
Naproksen był związany z reakcjami anafilaktycznymi u pacjentów z nadwrażliwością na naproksen i bez znanej nadwrażliwości na naproksen oraz u pacjentów z astmą wrażliwą na aspirynę [patrz PRZECIWWSKAZANIA oraz OSTRZEŻENIA I ŚRODKI ].
Poszukaj pomocy w nagłych wypadkach, jeśli wystąpi reakcja anafilaktyczna.
Zaostrzenie astmy związane z wrażliwością na aspirynę
Subpopulacja pacjentów z astmą może mieć astmę wrażliwą na aspirynę, która może obejmować przewlekłe zapalenie zatok przynosowych powikłane polipami nosa; ciężki, potencjalnie śmiertelny skurcz oskrzeli; i/lub nietolerancja aspiryny i innych NLPZ. Ponieważ u takich pacjentów wrażliwych na aspirynę odnotowano reakcję krzyżową między aspiryną a innymi NLPZ, NAPRELAN 250 mg jest przeciwwskazany u pacjentów z tą formą wrażliwości na aspirynę [patrz PRZECIWWSKAZANIA ]. Gdy NAPRELAN jest stosowany u pacjentów z istniejącą wcześniej astmą (bez znanej wrażliwości na aspirynę), należy monitorować pacjentów pod kątem zmian w objawach przedmiotowych i podmiotowych astmy.
Poważne reakcje skórne
NLPZ, w tym naproksen, mogą powodować poważne reakcje skórne, takie jak złuszczające zapalenie skóry, zespół Stevensa-Johnsona (SJS) i toksyczna nekroliza naskórka (TEN), które mogą być śmiertelne. Te poważne zdarzenia mogą wystąpić bez ostrzeżenia. Należy poinformować pacjentów o objawach przedmiotowych i podmiotowych ciężkich reakcji skórnych oraz o zaprzestaniu stosowania leku NAPRELAN 500 mg w przypadku pojawienia się pierwszych objawów wysypki skórnej lub jakichkolwiek innych objawów nadwrażliwości.
NAPRELAN jest przeciwwskazany u pacjentów z wcześniejszymi ciężkimi reakcjami skórnymi na NLPZ [patrz PRZECIWWSKAZANIA ].
Reakcja lekowa z eozynofilią i objawami ogólnoustrojowymi (DRESS)
pacjentów przyjmujących NLPZ, takie jak NAPRELAN, zgłaszano reakcje polekowe z eozynofilią i objawami ogólnoustrojowymi (DRESS). Niektóre z tych zdarzeń były śmiertelne lub zagrażały życiu. SUKIENKA zazwyczaj, choć nie wyłącznie, objawia się gorączką, wysypką, powiększeniem węzłów chłonnych i/lub obrzękiem twarzy. Inne objawy kliniczne mogą obejmować zapalenie wątroby, zapalenie nerek, nieprawidłowości hematologiczne, zapalenie mięśnia sercowego lub zapalenie mięśni. Czasami objawy DRESS mogą przypominać ostrą infekcję wirusową. Często występuje eozynofilia. Ponieważ zaburzenie to ma zmienną prezentację, mogą być zaangażowane inne układy narządów nie wymienione tutaj. Należy zauważyć, że wczesne objawy nadwrażliwości, takie jak gorączka lub powiększenie węzłów chłonnych, mogą być obecne, nawet jeśli wysypka nie jest widoczna. Jeśli takie oznaki lub objawy są obecne, należy przerwać stosowanie leku NAPRELAN i natychmiast ocenić stan pacjenta.
Toksyczność płodu
Przedwczesne zamknięcie przewodu tętniczego płodu
Unikaj stosowania NLPZ, w tym NAPRELANU, u kobiet w ciąży około 30 tygodnia ciąży i później. NLPZ, w tym NAPRELAN, zwiększają ryzyko przedwczesnego zamknięcia przewodu tętniczego płodu mniej więcej w tym wieku ciążowym.
Małowodzie/niewydolność nerek noworodka
Stosowanie NLPZ, w tym NAPRELAN 500 mg, w około 20. tygodniu ciąży lub później w ciąży może powodować zaburzenia czynności nerek płodu prowadzące do małowodzia, a w niektórych przypadkach do zaburzeń czynności nerek u noworodków. Te działania niepożądane obserwuje się średnio po dniach lub tygodniach leczenia, chociaż małowodzie zgłaszano rzadko już po 48 godzinach od rozpoczęcia leczenia NLPZ. Małowodzie jest często, ale nie zawsze, odwracalne po przerwaniu leczenia. Powikłania przedłużonego małowodzia mogą na przykład obejmować przykurcze kończyn i opóźnione dojrzewanie płuc. W niektórych przypadkach zaburzeń czynności nerek noworodków po wprowadzeniu do obrotu konieczne były procedury inwazyjne, takie jak transfuzja wymienna lub dializa.
Jeśli leczenie NLPZ jest konieczne między około 20 tygodniem a 30 tygodniem ciąży, należy ograniczyć stosowanie NAPRELAN 500 mg do najniższej skutecznej dawki i możliwie najkrótszego czasu trwania. Rozważ monitorowanie ultrasonograficzne płynu owodniowego, jeśli leczenie NAPRELANEM trwa dłużej niż 48 godzin. W przypadku wystąpienia małowodzia należy przerwać stosowanie leku NAPRELAN i postępować zgodnie z praktyką kliniczną [patrz Używaj w określonych populacjach ].
Toksyczność hematologiczna
U pacjentów leczonych NLPZ wystąpiła niedokrwistość. Może to być spowodowane utajoną lub znaczną utratą krwi, zatrzymaniem płynów lub niekompletnie opisanym wpływem na erytropoezę. Jeśli pacjent leczony preparatem NAPRELAN 500mg ma jakiekolwiek oznaki lub objawy niedokrwistości, należy monitorować poziom hemoglobiny lub hematokrytu.
NLPZ, w tym NAPRELAN, mogą zwiększać ryzyko krwawień. Choroby współistniejące, takie jak zaburzenia krzepnięcia, jednoczesne stosowanie warfaryny, innych leków przeciwzakrzepowych, leków przeciwpłytkowych (np. aspiryna), inhibitorów wychwytu zwrotnego serotoniny (SSRI) i inhibitorów wychwytu zwrotnego serotoniny i noradrenaliny (SNRI) mogą zwiększać to ryzyko. Monitoruj tych pacjentów pod kątem oznak krwawienia [patrz INTERAKCJE Z LEKAMI ].
Maskowanie stanu zapalnego i gorączki
Aktywność farmakologiczna NAPRELAN 250mg w zmniejszaniu stanu zapalnego i ewentualnie gorączki może zmniejszyć użyteczność oznak diagnostycznych w wykrywaniu infekcji.

Monitoring laboratoryjny
Ponieważ poważne krwawienie z przewodu pokarmowego, hepatotoksyczność i uszkodzenie nerek mogą wystąpić bez objawów lub oznak ostrzegawczych, należy rozważyć okresowe monitorowanie pacjentów długotrwale leczonych NLPZ za pomocą CBC i profilu chemicznego [patrz OSTRZEŻENIA I ŚRODKI ].
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( Przewodnik po lekach ), która towarzyszy każdej zrealizowanej recepcie. Należy poinformować pacjentów, rodziny lub ich opiekunów o następujących informacjach przed rozpoczęciem leczenia NAPRELAN 500mg oraz okresowo w trakcie trwającej terapii.
Zdarzenia zakrzepowo-sercowe
Należy doradzić pacjentom, aby zwracali uwagę na objawy zakrzepicy sercowo-naczyniowej, w tym ból w klatce piersiowej, duszność, osłabienie lub niewyraźną mowę, i natychmiast zgłaszali każdy z tych objawów swojemu lekarzowi [patrz OSTRZEŻENIA I ŚRODKI ].
Krwawienie z przewodu pokarmowego, owrzodzenie i perforacja
NAPRELAN 500 mg, podobnie jak inne NLPZ, może powodować dyskomfort ze strony przewodu pokarmowego i rzadko poważne skutki uboczne, takie jak wrzody i krwawienie, które mogą skutkować hospitalizacją, a nawet śmiercią. Poradź pacjentom, aby zgłaszali swojemu lekarzowi objawy owrzodzeń i krwawień, w tym ból w nadbrzuszu, niestrawność, smoliste stolce i krwawe wymioty. W przypadku jednoczesnego stosowania aspiryny w małych dawkach w profilaktyce kardiologicznej należy poinformować pacjentów o zwiększonym ryzyku wystąpienia krwawienia z przewodu pokarmowego [patrz OSTRZEŻENIA I ŚRODKI ].
Hepatotoksyczność
Należy poinformować pacjentów o oznakach i objawach ostrzegawczych hepatotoksyczności (np. nudności, zmęczenie, letarg, świąd, biegunka, żółtaczka, tkliwość w prawym górnym kwadrancie i objawy grypopodobne). W takim przypadku należy poinstruować pacjentów, aby odstawili NAPRELAN i natychmiast poszukali leczenia [patrz OSTRZEŻENIA I ŚRODKI ].
Niewydolność serca i obrzęk
Należy doradzić pacjentom, aby zwracali uwagę na objawy zastoinowej niewydolności serca, w tym duszność, niewyjaśniony przyrost masy ciała lub obrzęki, i skontaktowali się z lekarzem, jeśli takie objawy wystąpią [patrz OSTRZEŻENIA I ŚRODKI ].
Reakcje anafilaktyczne
Poinformuj pacjentów o objawach reakcji anafilaktycznej (np. trudności w oddychaniu, obrzęk twarzy lub gardła). Należy poinstruować pacjentów, aby w razie ich wystąpienia szukali natychmiastowej pomocy w nagłych wypadkach [patrz PRZECIWWSKAZANIA oraz OSTRZEŻENIA I ŚRODKI ].
Poważne reakcje skórne, w tym SUKIENKA
NAPRELAN 500 mg, podobnie jak inne NLPZ, może powodować poważne skutki uboczne dla skóry, takie jak złuszczające zapalenie skóry, SJS i TEN, które mogą skutkować hospitalizacją, a nawet śmiercią. Należy doradzić pacjentom, aby w przypadku wystąpienia jakiejkolwiek wysypki lub gorączki natychmiast przerwali przyjmowanie leku NAPRELAN i jak najszybciej skontaktowali się z lekarzem [patrz OSTRZEŻENIA I ŚRODKI ].
Płodność kobiet
Poinformuj kobiety w wieku rozrodczym, które pragną zajść w ciążę, że NLPZ, w tym NAPRELAN 250 mg, mogą być związane z odwracalnym opóźnieniem owulacji [patrz Używaj w określonych populacjach ].
Toksyczność płodu
Poinformuj kobiety w ciąży, aby unikały stosowania leku NAPRELAN 500 mg i innych NLPZ po 30. tygodniu ciąży ze względu na ryzyko przedwczesnego zamknięcia przewodu tętniczego płodu. Jeśli leczenie preparatem NAPRELAN 500 mg jest konieczne dla kobiety w ciąży między około 20. a 30. tygodniem ciąży, należy poinformować ją, że może być konieczne monitorowanie pod kątem małowodzia, jeśli leczenie trwa dłużej niż 48 godzin [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
Unikaj jednoczesnego stosowania NLPZ
Należy poinformować pacjentów, że jednoczesne stosowanie preparatu NAPRELAN z innymi NLPZ lub salicylanami (np. diflunisalem, salsalatem) nie jest zalecane ze względu na zwiększone ryzyko toksyczności żołądkowo-jelitowej oraz niewielki lub żaden wzrost skuteczności [patrz OSTRZEŻENIA I ŚRODKI oraz INTERAKCJE Z LEKAMI ]. Ostrzegaj pacjentów, że NLPZ mogą być obecne w lekach „bez recepty” stosowanych w leczeniu przeziębienia, gorączki lub bezsenności.
Stosowanie NLPZ i aspiryny w niskich dawkach
Poinformuj pacjentów, aby nie stosowali małych dawek aspiryny jednocześnie z NAPRELAN 250mg, dopóki nie porozmawiają ze swoim lekarzem [patrz INTERAKCJE Z LEKAMI ].
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Karcynogeneza
Przeprowadzono dwuletnie badanie na szczurach w celu oceny potencjału rakotwórczego naproksenu w dawkach 8 mg/kg/dobę, 16 mg/kg/dobę i 24 mg/kg/dobę (0,05, 0,1 i 0,16-krotność maksymalnej zalecanej dawki). dawka dobowa u ludzi wynosząca 1500 mg/dobę na podstawie porównania powierzchni ciała). Nie znaleziono dowodów na rakotwórczość.
Mutageneza
Badania mające na celu ocenę potencjału mutagennego zawiesiny Naprosyn nie zostały zakończone.
Upośledzenie płodności
Nie ukończono badań oceniających wpływ naproksenu na płodność mężczyzn lub kobiet.
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
Stosowanie NLPZ, w tym NAPRELAN 500 mg, może spowodować przedwczesne zamknięcie przewodu tętniczego płodu i dysfunkcję nerek płodu prowadzącą do małowodzia, a w niektórych przypadkach do niewydolności nerek u noworodków. Ze względu na te zagrożenia należy ograniczyć dawkę i czas stosowania NAPRELAN 500 mg między około 20 a 30 tygodniem ciąży oraz unikać stosowania NAPRELAN 500 mg około 30 tygodnia ciąży i później (patrz Rozważania kliniczne , Dane ).
Przedwczesne zamknięcie przewodu tętniczego płodu
Stosowanie NLPZ, w tym NAPRELAN 500mg, około 30 tygodnia ciąży lub później zwiększa ryzyko przedwczesnego zamknięcia przewodu tętniczego płodu.
Małowodzie/niewydolność nerek noworodka
Stosowanie NLPZ w około 20. tygodniu ciąży lub później w ciąży wiązało się z przypadkami dysfunkcji nerek płodu prowadzącej do małowodzia, a w niektórych przypadkach do niewydolności nerek u noworodków.
Dane z badań obserwacyjnych dotyczące innych potencjalnych zagrożeń dla zarodka i płodu związanych ze stosowaniem NLPZ u kobiet w pierwszym lub drugim trymestrze ciąży są niejednoznaczne. W badaniach na szczurach, królikach i myszach dotyczących reprodukcji na zwierzętach nie stwierdzono działania teratogennego ani uszkodzenia płodu, gdy naproksen był podawany w okresie organogenezy w dawkach odpowiednio 0,13, 0,26 i 0,6 razy większych od maksymalnej zalecanej dawki dobowej u ludzi wynoszącej 1500 mg/dobę. Na podstawie danych na zwierzętach wykazano, że prostaglandyny odgrywają ważną rolę w przepuszczalności naczyń endometrium, implantacji blastocysty i decydualizacji. W badaniach na zwierzętach podawanie inhibitorów syntezy prostaglandyn, takich jak naproksen, powodowało zwiększoną utratę przed i po implantacji. Wykazano również, że prostaglandyny odgrywają ważną rolę w rozwoju nerek płodu. W opublikowanych badaniach na zwierzętach donoszono, że inhibitory syntezy prostaglandyn, podawane w klinicznie istotnych dawkach, zaburzają rozwój nerek.
Szacowane ryzyko tła poważnych wad wrodzonych i poronienia dla wskazanej populacji jest nieznane. Wszystkie ciąże wiążą się z ryzykiem wady wrodzonej, utraty lub innych niekorzystnych skutków. W ogólnej populacji Stanów Zjednoczonych szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2% do 4% i 15% do 20%.
Rozważania kliniczne
Działania niepożądane u płodu/noworodka
Przedwczesne zamknięcie przewodu tętniczego płodu: Należy unikać stosowania NLPZ u kobiet w około 30. tygodniu ciąży i później w ciąży, ponieważ NLPZ, w tym NAPRELAN, mogą spowodować przedwczesne zamknięcie przewodu tętniczego płodu (patrz Dane ).
Małowodzie/niewydolność nerek noworodka: Jeśli NLPZ jest konieczne w około 20. tygodniu ciąży lub później, ogranicz stosowanie do najniższej skutecznej dawki i możliwie najkrótszego czasu trwania. Jeśli leczenie NAPRELAN 500 mg trwa dłużej niż 48 godzin, rozważ monitorowanie ultrasonograficzne pod kątem małowodzia. W przypadku wystąpienia małowodzia należy odstawić NAPRELAN 500 mg i postępować zgodnie z praktyką kliniczną (patrz Dane ).
Praca lub dostawa
Nie ma badań dotyczących wpływu NAPRELAN 500mg podczas porodu lub porodu. W badaniach na zwierzętach NLPZ, w tym sól sodowa naproksenu, hamują syntezę prostaglandyn, powodują opóźniony poród, zwiększają częstość występowania dystocji i urodzeń martwych.
Dane
Dane ludzkie
Istnieją dowody sugerujące, że stosowanie inhibitorów syntezy prostaglandyn w celu opóźnienia porodu przedwczesnego zwiększa ryzyko powikłań noworodkowych, takich jak martwicze zapalenie jelit, przetrwały przewód tętniczy i krwotok śródczaszkowy. Leczenie naproksenem podawane w późnej ciąży w celu opóźnienia porodu wiąże się z utrzymującym się nadciśnieniem płucnym, dysfunkcją nerek i nieprawidłowym stężeniem prostaglandyny E u wcześniaków. Ze względu na znany wpływ leków tej klasy na układ sercowo-naczyniowy płodu ludzkiego (zamknięcie przewodu tętniczego), należy unikać ich stosowania w trzecim trymestrze ciąży.
Przedwczesne zamknięcie przewodu tętniczego płodu
Z opublikowanego piśmiennictwa wynika, że stosowanie NLPZ w około 30. tygodniu ciąży i później w ciąży może spowodować przedwczesne zamknięcie przewodu tętniczego płodu.
Małowodzie/niewydolność nerek noworodka
Opublikowane badania i raporty postmarketingowe opisują stosowanie NLPZ przez matki w około 20. tygodniu ciąży lub później w związku z zaburzeniami czynności nerek płodu prowadzącymi do małowodzia, a w niektórych przypadkach z zaburzeniami czynności nerek u noworodków. Te działania niepożądane obserwuje się średnio po dniach lub tygodniach leczenia, chociaż małowodzie zgłaszano rzadko już po 48 godzinach od rozpoczęcia leczenia NLPZ. W wielu przypadkach, ale nie we wszystkich, spadek płynu owodniowego był przemijający i odwracalny wraz z odstawieniem leku. Istnieje ograniczona liczba opisów przypadków stosowania NLPZ u matek i zaburzeń czynności nerek u noworodków bez małowodzia, z których niektóre były nieodwracalne. Niektóre przypadki dysfunkcji nerek noworodków wymagały leczenia za pomocą procedur inwazyjnych, takich jak transfuzja wymienna lub dializa.
Ograniczenia metodologiczne tych badań i raportów postmarketingowych obejmują brak grupy kontrolnej; ograniczone informacje dotyczące dawki, czasu trwania i czasu ekspozycji na lek; i jednoczesne stosowanie innych leków. Ograniczenia te uniemożliwiają ustalenie wiarygodnego oszacowania ryzyka niekorzystnych wyników dla płodu i noworodka przy stosowaniu NLPZ u matki. Ponieważ opublikowane dane dotyczące bezpieczeństwa u noworodków dotyczyły głównie wcześniaków, możliwość uogólnienia niektórych zgłoszonych zagrożeń dla urodzonego w terminie niemowlęcia narażonego na NLPZ poprzez stosowanie przez matkę jest niepewna.
Dane zwierząt
Badania nad reprodukcją przeprowadzono na szczurach przy dawce 20 mg/kg/dobę (0,13-krotność maksymalnej zalecanej dawki dobowej dla ludzi wynoszącej 1500 mg/dobę na podstawie porównania powierzchni ciała) królikach przy dawce 20 mg/kg/dobę (0,26-krotność maksymalnej zalecanej dawki u ludzi dawka dobowa, na podstawie porównania powierzchni ciała) i myszy w dawce 170 mg/kg/dobę (0,6-krotność maksymalnej zalecanej dawki dobowej u ludzi na podstawie porównania powierzchni ciała) bez dowodów na upośledzenie płodności lub uszkodzenie płodu z powodu lek. Na podstawie danych na zwierzętach wykazano, że prostaglandyny odgrywają ważną rolę w przepuszczalności naczyń endometrium, implantacji blastocysty i decydualizacji. W badaniach na zwierzętach podawanie inhibitorów syntezy prostaglandyn, takich jak sól sodowa naproksenu, powodowało zwiększenie poronień przed i po implantacji.
Laktacja
Podsumowanie ryzyka
Anion naproksenu wykryto w mleku kobiet karmiących piersią w stężeniu około 1% stężenia w osoczu. Należy wziąć pod uwagę korzyści rozwojowe i zdrowotne wynikające z karmienia piersią, a także kliniczne zapotrzebowanie matki na NAPRELAN oraz wszelkie potencjalne niekorzystne skutki działania NAPRELANU na niemowlę karmione piersią lub wynikające z tego schorzenia matki.
Kobiety i mężczyźni o potencjale rozrodczym
Bezpłodność
Kobiety
oparciu o mechanizm działania, stosowanie NLPZ, w których pośredniczą prostaglandyny, w tym NAPRELAN, może opóźnić lub zapobiec pęknięciu pęcherzyków jajnikowych, które u niektórych kobiet jest związane z odwracalną niepłodnością. Opublikowane badania na zwierzętach wykazały, że podawanie inhibitorów syntezy prostaglandyn może zaburzać pośredniczone przez prostaglandyny pęknięcie pęcherzyka wymagane do owulacji. Niewielkie badania u kobiet leczonych NLPZ wykazały również odwracalne opóźnienie owulacji. Rozważ odstawienie NLPZ, w tym NAPRELAN 250 mg, u kobiet, które mają trudności z zajściem w ciążę lub są w trakcie badania niepłodności.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność preparatu NAPRELAN 500mg w populacji pediatrycznej nie zostały ustalone.
Zastosowanie geriatryczne
Pacjenci w podeszłym wieku, w porównaniu z młodszymi pacjentami, są narażeni na większe ryzyko poważnych działań niepożądanych ze strony układu krążenia, przewodu pokarmowego i (lub) nerek związanych z NLPZ. Jeśli przewidywane korzyści dla pacjenta w podeszłym wieku przewyższają potencjalne ryzyko, należy rozpocząć dawkowanie od dolnej granicy zakresu dawkowania i monitorować pacjentów pod kątem działań niepożądanych [patrz OSTRZEŻENIA I ŚRODKI ].
Wiadomo, że naproksen i jego metabolity są w znacznym stopniu wydalane przez nerki, a ryzyko działań niepożądanych tego leku może być większe u pacjentów z zaburzeniami czynności nerek. Ponieważ u pacjentów w podeszłym wieku istnieje większe prawdopodobieństwo upośledzenia czynności nerek, należy zachować ostrożność w tej populacji pacjentów i może być przydatne monitorowanie czynności nerek [patrz FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
Objawy występujące po ostrym przedawkowaniu NLPZ były zazwyczaj ograniczone do letargu, senności, nudności, wymiotów i bólu w nadbrzuszu, które na ogół ustępowały po zastosowaniu leczenia wspomagającego. Wystąpiło krwawienie z przewodu pokarmowego. Wystąpiło nadciśnienie, ostra niewydolność nerek, depresja oddechowa i śpiączka, ale występowały one rzadko [patrz OSTRZEŻENIA I ŚRODKI ].
Kilku pacjentów doświadczyło napadów, ale nie jest jasne, czy były one związane z lekiem. Nie wiadomo, jaka dawka leku zagrażałaby życiu.
Prowadź pacjentów z opieką objawową i podtrzymującą po przedawkowaniu NLPZ. Nie ma swoistych odtrutek. Hemodializa nie zmniejsza stężenia naproksenu w osoczu ze względu na wysoki stopień jego wiązania z białkami. Rozważyć wymioty i/lub węgiel aktywowany (60 do 100 gramów u dorosłych, 1 do 2 gramów na kg masy ciała u dzieci) i/lub osmotyczne przeczyszczanie u pacjentów z objawami obserwowanymi w ciągu czterech godzin od spożycia lub u pacjentów z dużym przedawkowaniem ( 5 do 10 razy więcej niż zalecana dawka). Wymuszona diureza, alkalizacja moczu, hemodializa lub hemoperfuzja mogą nie być przydatne ze względu na wysokie wiązanie z białkami.
Aby uzyskać dodatkowe informacje na temat leczenia przedawkowania, skontaktuj się z centrum kontroli zatruć (1-800-222-1222).
PRZECIWWSKAZANIA
NAPRELAN 500mg jest przeciwwskazany u następujących pacjentów:
Znana nadwrażliwość (np. reakcje anafilaktyczne i poważne reakcje skórne) na naproksen lub którykolwiek ze składników produktu leczniczego [patrz OSTRZEŻENIA I ŚRODKI ]
Historia astmy, pokrzywki lub innych reakcji alergicznych po przyjęciu aspiryny lub innych NLPZ. U takich pacjentów zgłaszano ciężkie, czasami prowadzące do zgonu reakcje anafilaktyczne na NLPZ [patrz OSTRZEŻENIA I ŚRODKI ]
przypadku operacji pomostowania aortalno-wieńcowego (CABG) [patrz OSTRZEŻENIA I ŚRODKI ]
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Naproksen ma właściwości przeciwbólowe, przeciwzapalne i przeciwgorączkowe.
Mechanizm działania NAPRELAN, podobnie jak innych NLPZ, nie jest w pełni poznany, ale obejmuje hamowanie cyklooksygenazy (COX-1 i COX-2).
Naproksen sodu jest silnym inhibitorem syntezy prostaglandyn in vitro. Stężenia sodu naproksenu osiągnięte podczas terapii wywoływały efekty in vivo. Prostaglandyny uwrażliwiają nerwy doprowadzające i nasilają działanie bradykininy w wywoływaniu bólu w modelach zwierzęcych.
Prostaglandyny są mediatorami stanu zapalnego. Ponieważ naproksen sodowy jest inhibitorem syntezy prostaglandyn, jego mechanizm działania może wynikać ze zmniejszenia stężenia prostaglandyn w tkankach obwodowych.
Farmakodynamika
badaniu na zdrowych ochotnikach, 10 dni jednoczesnego podawania naproksenu 220 mg raz na dobę z małą dawką kwasu acetylosalicylowego o natychmiastowym uwalnianiu (81 mg) wykazało interakcję z działaniem przeciwpłytkowym aspiryny, mierzonym jako % hamowania tromboksanu B2 w surowicy po 24 godzinach po dawce 10 dnia [98,7% (sama aspiryna) vs 93,1% (naproksen i aspiryna)]. Interakcję zaobserwowano nawet po odstawieniu naproksenu w dniu 11 (podczas kontynuowania dawki aspiryny), ale normalizacja nastąpiła w dniu 13. W tym samym badaniu interakcja była większa, gdy naproksen był podawany 30 minut przed aspiryną [98,7% vs 87,7%]. i minimalny, gdy aspirynę podawano 30 minut przed naproksenem [98,7% vs 95,4%].
Po podaniu naproksenu 220 mg dwa razy dziennie z małą dawką aspiryny o natychmiastowym uwalnianiu (pierwsza dawka naproksenu podana 30 minut przed aspiryną), interakcja była minimalna po 24 godzinach od dawki 10 dnia [98,7% vs 95,7%]. Jednak interakcja była bardziej widoczna po odstawieniu naproksenu (wypłukanie) w dniu 11. [98,7% vs 84,3%] i nie uległa całkowitej normalizacji do dnia 13 [98,5% vs 90,7%]. [Widzieć INTERAKCJE Z LEKAMI ].
Farmakokinetyka
Chociaż sam naproksen jest dobrze wchłaniany, postać soli sodowej jest wchłaniana szybciej, co skutkuje wyższymi maksymalnymi stężeniami w osoczu dla danej dawki. Około 30% całkowitej dawki naproksenu sodowego w tabletkach NAPRELAN 500 mg występuje w postaci dawkowania jako składnik o natychmiastowym uwalnianiu. Pozostała sól sodowa naproksenu jest powlekana w postaci mikrocząstek, aby zapewnić właściwości przedłużonego uwalniania. Po podaniu doustnym stężenie naproksenu w osoczu jest wykrywane w ciągu 30 minut od podania, przy czym maksymalne stężenie w osoczu występuje około 5 godzin po podaniu. Obserwowany okres półtrwania w końcowej fazie eliminacji naproksenu z tabletek naproksenu sodowego o natychmiastowym uwalnianiu i tabletek NAPRELAN wynosi około 15 godzin. Poziomy stanu stacjonarnego naproksenu są osiągane w ciągu 3 dni i stopień akumulacji naproksenu we krwi jest z tym zgodny.
Stężenia naproksenu w osoczu Średnia 24 pacjentów (+/-2 SD) (stan stacjonarny, dzień 5)
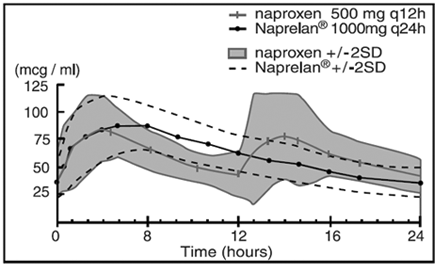
Parametry farmakokinetyczne w 5. dniu stanu stacjonarnego (średnia z 24 pacjentów)
Wchłanianie
Sam naproksen jest szybko i całkowicie wchłaniany z przewodu pokarmowego z biodostępnością in vivo na poziomie 95%. W oparciu o profil farmakokinetyczny faza wchłaniania tabletek NAPRELAN 250 mg następuje w ciągu pierwszych 4 do 6 godzin po podaniu. Zbiega się to z rozpadem tabletki w żołądku, przejściem mikrocząstek o przedłużonym uwalnianiu przez jelito cienkie do proksymalnego jelita grubego. Przeprowadzono badanie obrazowania in vivo na zdrowych ochotnikach, które potwierdza szybki rozpad matrycy tabletki i dyspersję mikrocząstek.
Szybkość wchłaniania składnika w postaci cząstek o przedłużonym uwalnianiu w tabletkach NAPRELAN jest wolniejsza niż w przypadku konwencjonalnych tabletek naproksenu sodowego. To właśnie wydłużenie procesów wchłaniania leku utrzymuje poziom w osoczu i pozwala na dawkowanie raz dziennie.
Efekty żywności
Nie zaobserwowano żadnych znaczących efektów pokarmowych, gdy dwudziestu czterem pacjentom podano pojedynczą dawkę 500 mg tabletki NAPRELAN po całonocnym poście lub 30 minut po posiłku. Podobnie jak w przypadku konwencjonalnych preparatów naproksenu i naproksenu sodu, pożywienie powoduje nieznaczne zmniejszenie szybkości wchłaniania naproksenu po podaniu tabletek NAPRELAN 250 mg.
Dystrybucja
Objętość dystrybucji naproksenu wynosi 0,16 l/kg. Na poziomie terapeutycznym naproksen wiąże się w ponad 99% z albuminą. Przy dawkach naproksenu większych niż 500 mg/dobę występuje mniej niż proporcjonalny wzrost stężenia w osoczu z powodu zwiększenia klirensu spowodowanego wysyceniem wiązania z białkami osocza przy wyższych dawkach. Jednak stężenie niezwiązanego naproksenu nadal wzrasta proporcjonalnie do dawki. Tabletki NAPRELAN wykazują podobną charakterystykę proporcjonalną do dawki.
Eliminacja
Metabolizm
Naproksen jest intensywnie metabolizowany do 6-0-desmetylonaproksenu i zarówno macierzysty, jak i metabolity nie indukują enzymów metabolizujących.
Wydalanie
Okres półtrwania w fazie eliminacji tabletek NAPRELAN 500 mg i konwencjonalnego naproksenu wynosi około 15 godzin. Stan stacjonarny osiągany jest po 2-3 dawkach tabletek NAPRELAN. Większość leku jest wydalana z moczem, głównie w postaci niezmienionego naproksenu (mniej niż 1%), 6-0-desmetylonaproksenu (mniej niż 1%) oraz ich glukuronidów lub innych koniugatów (66 do 92%). Niewielka ilość (
Określone populacje
Pediatryczny
Nie przeprowadzono badań pediatrycznych z preparatem NAPRELAN 500 mg tabletki, dlatego bezpieczeństwo stosowania NAPRELAN 500 mg tabletki w populacji pediatrycznej nie zostało ustalone.
Niewydolność wątroby
Przewlekła alkoholowa choroba wątroby i prawdopodobnie inne choroby ze zmniejszonymi lub nieprawidłowymi białkami osocza (albuminą) zmniejszają całkowite stężenie naproksenu w osoczu, ale stężenie niezwiązanego naproksenu w osoczu jest zwiększone. Zaleca się ostrożność, gdy wymagane są duże dawki, a u tych pacjentów może być konieczne pewne dostosowanie dawki. Rozsądnie jest stosować najmniejszą skuteczną dawkę.
Zaburzenia czynności nerek
Nie określono farmakokinetyki naproksenu u osób z niewydolnością nerek. Biorąc pod uwagę, że naproksen jest metabolizowany, a koniugaty są głównie wydalane przez nerki, istnieje możliwość kumulacji metabolitów naproksenu w przypadku niewydolności nerek. Eliminacja naproksenu jest zmniejszona u pacjentów z ciężkimi zaburzeniami czynności nerek. Produkty zawierające naproksen nie są zalecane do stosowania u pacjentów z umiarkowanymi do ciężkich i ciężkimi zaburzeniami czynności nerek (klirens kreatyniny OSTRZEŻENIA I ŚRODKI ].
Badania interakcji leków
Aspiryna
Gdy NLPZ podawano z aspiryną, wiązanie NLPZ z białkami było zmniejszone, chociaż klirens wolnego NLPZ nie uległ zmianie. Kliniczne znaczenie tej interakcji nie jest znane. W Tabeli 1 przedstawiono klinicznie istotne interakcje leków NLPZ z aspiryną [patrz INTERAKCJE Z LEKAMI ].
Studia kliniczne
Reumatyzm
Stosowanie tabletek NAPRELAN 500 mg w leczeniu objawów przedmiotowych i podmiotowych reumatoidalnego zapalenia stawów zostało ocenione w 12-tygodniowym podwójnie zaślepionym, randomizowanym, kontrolowanym placebo i aktywnym badaniu z udziałem 348 pacjentów. Dwie tabletki NAPRELAN 500 mg (1000 mg) raz na dobę i tabletki naproksenu 500 mg dwa razy na dobę (1000 mg) były bardziej skuteczne niż placebo. Skuteczność kliniczną wykazano po jednym tygodniu i utrzymywano przez cały czas trwania badania.
Zapalenie kości i stawów
Stosowanie tabletek NAPRELAN w leczeniu oznak i objawów choroby zwyrodnieniowej stawu kolanowego zostało ocenione w 12-tygodniowym badaniu z podwójnie ślepą próbą, placebo i aktywną kontrolą z udziałem 347 pacjentów. Dwie tabletki NAPRELAN 500 mg (1000 mg) raz na dobę i tabletki naproksenu 500 mg dwa razy na dobę (1000 mg) były bardziej skuteczne niż placebo. Skuteczność kliniczną wykazano po jednym tygodniu i utrzymywano przez cały czas trwania badania.
Znieczulenie
Początek działania przeciwbólowego produktu NAPRELAN tabletki obserwowano w ciągu 30 minut w badaniu farmakokinetycznym/farmakodynamicznym u pacjentów z bólem po zabiegu chirurgicznym jamy ustnej. W kontrolowanych badaniach klinicznych naproksen stosowano w połączeniu ze złotem, D-penicylaminą, metotreksatem i kortykosteroidami. Jego stosowanie w połączeniu z salicylanami nie jest zalecane, ponieważ istnieją dowody na to, że aspiryna zwiększa szybkość wydalania naproksenu, a dane są niewystarczające, aby wykazać, że naproksen i aspiryna dają większą poprawę w porównaniu z samą aspiryną. Ponadto, podobnie jak w przypadku innych NLPZ, połączenie może powodować częstsze występowanie zdarzeń niepożądanych niż wykazano dla każdego produktu osobno.
Studia specjalne
randomizowanym badaniu z podwójnie ślepą próbą, prowadzonym w grupach równoległych, 19 pacjentów otrzymywało dwie tabletki NAPRELAN 500 mg (1000 mg) raz na dobę lub tabletki naproksenu 500 mg (1000 mg) dwa razy na dobę przez 7 dni. Wyniki biopsji śluzówki i wyniki endoskopii były niższe u pacjentów, którzy otrzymywali tabletki NAPRELAN. W innym, podwójnie ślepym, randomizowanym badaniu krzyżowym, 23 osoby otrzymywały dwie tabletki NAPRELAN 500 mg (1000 mg) raz na dobę, tabletki naproksenu 500 mg (1000 mg) dwa razy na dobę i aspirynę 650 mg cztery razy na dobę (2600 mg) przez 7 dni każdy. W przypadku tabletek NAPRELAN zaobserwowano znacznie mniej nadżerek dwunastnicy niż w przypadku naproksenu lub aspiryny. W przypadku tabletek NAPRELAN i naproksenu wystąpiło znacznie mniej nadżerek żołądka niż w przypadku aspiryny. Kliniczne znaczenie tych wyników nie jest znane.
INFORMACJA O PACJENCIE
Przewodnik po lekach dla niesteroidowych leków przeciwzapalnych (NLPZ)
Jakie są najważniejsze informacje, które powinienem wiedzieć o lekach zwanych niesteroidowymi lekami przeciwzapalnymi (NLPZ)?
NLPZ mogą powodować poważne skutki uboczne, w tym:
- Zwiększone ryzyko zawału serca lub udaru mózgu, które mogą prowadzić do śmierci. Ryzyko to może wystąpić na początku leczenia i może wzrosnąć:
- ze wzrastającymi dawkami NLPZ
- przy dłuższym stosowaniu NLPZ
Nie przyjmuj NLPZ bezpośrednio przed lub po operacji serca, zwanej „pomostowaniem aortalno-wieńcowym (CABG).“ Unikaj przyjmowania NLPZ po niedawnym zawale serca, chyba że tak zaleci lekarz. Możesz mieć zwiększone ryzyko kolejnego zawału serca, jeśli przyjmujesz NLPZ po niedawnym zawale serca.
- Zwiększone ryzyko krwawienia, owrzodzeń i pęknięć (perforacji) przełyku (przewodu prowadzącego z jamy ustnej do żołądka), żołądka i jelit:
- w dowolnym momencie podczas użytkowania
- bez objawów ostrzegawczych
- które mogą spowodować śmierć
Ryzyko owrzodzenia lub krwawienia wzrasta wraz z:
- wrzody żołądka w przeszłości lub krwawienie z żołądka lub jelit po zastosowaniu NLPZ
- przyjmowanie leków zwanych „kortykosteroidami”, „antykoagulantami”, „SSRI” lub „SNRI”
- rosnące dawki NLPZ
- starszy wiek
- dłuższe stosowanie NLPZ
- słabe zdrowie
- palenie
- zaawansowana choroba wątroby
- picie alkoholu
- problemy z krwawieniem
NLPZ powinny być stosowane wyłącznie:
- dokładnie zgodnie z zaleceniami
- w najniższej możliwej dawce dla twojego leczenia
- na jak najkrótszy czas
Co to są NLPZ?
NLPZ są stosowane w leczeniu bólu i zaczerwienienia, obrzęku i gorąca (zapalenia) z powodu schorzeń, takich jak różne rodzaje zapalenia stawów, skurcze menstruacyjne i inne rodzaje krótkotrwałego bólu.
Kto nie powinien brać NLPZ?
Nie przyjmuj NLPZ:
- jeśli u pacjenta wystąpił atak astmy, pokrzywka lub inna reakcja alergiczna na aspirynę lub inne NLPZ.
- tuż przed lub po operacji pomostowania aortalno-wieńcowego.
Przed zażyciem NLPZ poinformuj swojego lekarza o wszystkich swoich schorzeniach, w tym jeśli:
- masz problemy z wątrobą lub nerkami
- mieć wysokie ciśnienie krwi
- mieć astmę
- są w ciąży lub planują zajść w ciążę. Przyjmowanie NLPZ w około 20. tygodniu ciąży lub później może zaszkodzić nienarodzonemu dziecku. Jeśli musisz zażywać NLPZ przez ponad 2 dni między 20. a 30. tygodniem ciąży, Twój lekarz może być zmuszony do monitorowania ilości płynu w macicy wokół Twojego dziecka. Nie powinieneś brać NLPZ po około 30 tygodniu ciąży.
- karmisz piersią lub planujesz karmić piersią.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym o lekach na receptę lub dostępnych bez recepty, witaminach lub suplementach ziołowych. NLPZ i niektóre inne leki mogą wchodzić ze sobą w interakcje i powodować poważne skutki uboczne. Nie rozpoczynaj przyjmowania nowych leków bez uprzedniej konsultacji z lekarzem.
Jakie są możliwe skutki uboczne NLPZ?
NLPZ mogą powodować poważne skutki uboczne, w tym:
Zobacz „Jakie są najważniejsze informacje, które powinienem wiedzieć o lekach zwanych niesteroidowymi lekami przeciwzapalnymi (NLPZ)?
- nowe lub gorsze wysokie ciśnienie krwi
- niewydolność serca
- problemy z wątrobą, w tym niewydolność wątroby
- problemy z nerkami, w tym niewydolność nerek
- niski poziom czerwonych krwinek (niedokrwistość)
- zagrażające życiu reakcje skórne
- zagrażające życiu reakcje alergiczne
Inne skutki uboczne NLPZ obejmują: ból brzucha, zaparcia, biegunka, gazy, zgaga, nudności, wymioty i zawroty głowy.
Natychmiast uzyskaj pomoc w nagłych wypadkach, jeśli wystąpi którykolwiek z następujących objawów:
- duszność lub trudności w oddychaniu
- bełkotliwa wymowa
- ból w klatce piersiowej
- obrzęk twarzy lub gardła
- osłabienie w jednej części lub boku ciała
Przestań brać NLPZ i natychmiast skontaktuj się z lekarzem, jeśli wystąpi którykolwiek z następujących objawów:
- mdłości
- krew wymiotów
- bardziej zmęczony lub słabszy niż zwykle
- w wypróżnieniach pojawia się krew lub jest czarna i lepka jak smoła
- biegunka
- swędzący
- nietypowy przyrost masy ciała
- Twoja skóra lub oczy wyglądają na żółte
- wysypka skórna lub pęcherze z gorączką
- niestrawność lub ból brzucha
- obrzęk ramion, nóg, dłoni i stóp
- objawy grypopodobne
Jeśli zażyjesz zbyt dużo NLPZ, skontaktuj się z lekarzem lub natychmiast uzyskaj pomoc medyczną.
To nie wszystkie możliwe skutki uboczne NLPZ. Aby uzyskać więcej informacji, zapytaj swojego lekarza lub farmaceutę o NLPZ.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Inne informacje o NLPZ
- Aspiryna jest NLPZ, ale nie zwiększa ryzyka zawału serca. Aspiryna może powodować krwawienie w mózgu, żołądku i jelitach. Aspiryna może również powodować wrzody żołądka i jelit.
- Niektóre NLPZ są sprzedawane w mniejszych dawkach bez recepty (bez recepty). Porozmawiaj ze swoim lekarzem przed użyciem NLPZ dostępnych bez recepty przez ponad 10 dni.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu NLPZ
Leki są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Nie należy stosować NLPZ w stanie, na który nie został przepisany. Nie podawaj NLPZ innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić.
Jeśli chcesz uzyskać więcej informacji na temat NLPZ, porozmawiaj ze swoim lekarzem. Możesz poprosić farmaceutę lub pracownika służby zdrowia o informacje na temat NLPZ, które są przeznaczone dla pracowników służby zdrowia.
Ten przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków.
