Leczenie bólu: Lioresal 10mg, 25mg Baclofen Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Lioresal 10mg Intrathecal i jak się go stosuje?
Lioresal Intrathecal to lek na receptę stosowany w leczeniu objawów spastyczności. Lioresal Intrathecal może być stosowany samodzielnie lub z innymi lekami.
Lioresal Intrathecal należy do klasy leków zwanych środkami zwiotczającymi mięśnie szkieletowe.
Nie wiadomo, czy Lioresal Intrathecal jest bezpieczny i skuteczny u dzieci w wieku poniżej 12 lat.
Jakie są możliwe skutki uboczne Lioresal 25mg Intrathecal?
Lioresal 10mg Intrathecal może powodować poważne działania niepożądane, w tym:
- pokrzywka,
- trudności w oddychaniu,
- obrzęk twarzy, warg, języka lub gardła,
- silna senność,
- słaby lub płytki oddech,
- dezorientacja,
- halucynacje,
- swędzenie, mrowienie lub drganie w dłoniach, ramionach, stopach lub nogach,
- gorączka i
- konfiskata
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze działania niepożądane Lioresal 25mg Intrathecal to:
- senność,
- zawroty głowy,
- słabość,
- zmęczenie,
- ból głowy,
- problemy ze snem (bezsenność),
- mdłości,
- zaparcia i
- oddawanie moczu częściej niż zwykle
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Lioresal Intrathecal. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Nagłe odstawienie baklofenu dooponowego, niezależnie od przyczyny, spowodowało następstwa, które obejmują wysoką gorączkę, zmiany stanu psychicznego, nadmierną spastyczność z odbicia i sztywność mięśni, które w rzadkich przypadkach prowadziły do rabdomiolizy, niewydolności wielonarządowej i zgonu.
Zapobieganie nagłemu odstawieniu baklofenu dooponowego wymaga szczególnej uwagi podczas programowania i monitorowania systemu infuzyjnego, planowania i procedur ponownego napełniania oraz alarmów pompy. Pacjenci i opiekunowie powinni być poinformowani o znaczeniu regularnych wizyt uzupełniających i powinni być pouczeni o wczesnych objawach odstawienia baklofenu. Szczególną uwagę należy zwrócić na pacjentów z widocznym ryzykiem (np. urazy rdzenia kręgowego w stopniu T-6 lub wyższym, trudności w komunikacji, objawy odstawienia po podaniu doustnym lub dooponowym baklofenu w wywiadzie). Zapoznać się z instrukcją techniczną wszczepialnego systemu infuzyjnego, aby uzyskać dodatkowe informacje dla lekarzy po implantacji i dla pacjenta (patrz OSTRZEŻENIA ).
OPIS
LIORESAL INTRATHECAL (wstrzyknięcie baklofenu) jest środkiem zwiotczającym mięśnie i przeciwskurczowym. Jego nazwa chemiczna to kwas 4-amino-3-(4-chlorofenylo)butanowy, a jej wzór strukturalny to:
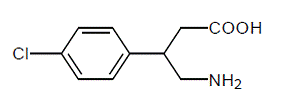
Baklofen jest białym lub prawie białym, bezwonnym lub praktycznie bezwonnym krystalicznym proszkiem o masie cząsteczkowej 213,66. Jest słabo rozpuszczalny w wodzie, bardzo słabo rozpuszczalny w metanolu i nierozpuszczalny w chloroformie.
LIORESAL INTRATHECAL to sterylny, wolny od pirogenów, izotoniczny roztwór wolny od przeciwutleniaczy, konserwantów i innych potencjalnie neurotoksycznych dodatków wskazanych wyłącznie do podawania dooponowego. Lek jest stabilny w roztworze w 37°C i kompatybilny z płynem mózgowo-rdzeniowym. Każdy mililitr LIORESAL INTRATHECAL zawiera baklofen USP 50 mcg, 500 mcg lub 2000 mcg i chlorek sodu 9 mg w wodzie do wstrzykiwań; Zakres pH wynosi 5,0 - 7,0. Każda ampułka jest przeznaczona WYŁĄCZNIE DO JEDNORAZOWEGO UŻYCIA. Wyrzuć niewykorzystaną część. NIE WOLNO AUTOKLAWOWAĆ.
WSKAZANIA
LIORESAL 10 mg INTRATHECAL (wstrzyknięcie baklofenu) jest wskazany do stosowania w leczeniu ciężkiej spastyczności. Pacjenci powinni najpierw zareagować na przesiewową dawkę baklofenu dooponowego przed rozważeniem długoterminowej infuzji za pomocą wszczepionej pompy. W przypadku spastyczności pochodzenia rdzeniowego, przewlekły wlew preparatu LIORESAL INTRATHECAL przez wszczepialną pompę powinien być zarezerwowany dla pacjentów niereagujących na doustną terapię baklofenem lub dla tych, u których występują nie tolerowane działania niepożądane ośrodkowego układu nerwowego przy skutecznych dawkach. Pacjenci ze spastycznością spowodowaną urazowym uszkodzeniem mózgu powinni odczekać co najmniej rok po urazie przed rozważeniem długoterminowej terapii dooponowej baklofenem. LIORESAL INTRATHECAL jest przeznaczony do stosowania drogą dooponową w pojedynczych dawkach testowych bolusa (przez cewnik rdzeniowy lub nakłucie lędźwiowe) oraz, do stosowania przewlekłego, wyłącznie w pompach wszczepialnych zatwierdzonych przez FDA specjalnie do podawania produktu LIORESAL INTRATHECAL do przestrzeni dooponowej.
Spastyczność pochodzenia rdzenia kręgowego
Dowody potwierdzające skuteczność preparatu LIORESAL INTRATHECAL uzyskano w randomizowanych, kontrolowanych badaniach, w których porównywano wpływ pojedynczej dawki dooponowej lub trzydniowego wlewu dooponowego preparatu LIORESAL INTRATHECAL z placebo u pacjentów z ciężką spastycznością i skurczami spowodowanymi urazem rdzenia kręgowego lub wielokrotnym skleroza. LIORESAL 10 mg INTRATHECAL był lepszy od placebo pod względem obu głównych zastosowanych miar wyników: zmiany od wartości wyjściowej w ocenie spastyczności według Ashwortha i częstości napadów.
Spastyczność pochodzenia mózgowego
Skuteczność preparatu LIORESAL INTRATHECAL badano w trzech kontrolowanych badaniach klinicznych; dwóch włączonych pacjentów z mózgowym porażeniem dziecięcym i jeden włączony pacjent ze spastycznością z powodu wcześniejszego uszkodzenia mózgu. Pierwsze badanie, randomizowane kontrolowane badanie krzyżowe obejmujące 51 pacjentów z mózgowym porażeniem dziecięcym, dostarczyło silnych, statystycznie istotnych wyników; LIORESAL INTRATHECAL okazał się skuteczniejszy od placebo w zmniejszaniu spastyczności mierzonej za pomocą Skali Ashwortha. Drugie badanie krzyżowe przeprowadzono u 11 pacjentów ze spastycznością wynikającą z uszkodzenia mózgu. Pomimo małej liczebności próby badanie przyniosło prawie istotną statystykę testową (p=0,066) i dostarczyło kierunkowo korzystnych wyników. Ostatnie badanie nie dostarczyło jednak danych, które można by rzetelnie przeanalizować.
Terapię LIORESAL 10mg INTRATHECAL można uznać za alternatywę dla destrukcyjnych zabiegów neurochirurgicznych. Przed wszczepieniem urządzenia do przewlekłego wlewu dooponowego produktu LIORESAL 10 mg INTRATHECAL pacjenci muszą wykazać odpowiedź na lek LIORESAL 10 mg INTRATHECAL w badaniu przesiewowym (patrz DAWKOWANIE I SPOSÓB PODAWANIA ).
DAWKOWANIE I SPOSÓB PODAWANIA
Szczegółowe instrukcje i środki ostrożności dotyczące programowania pompy i/lub ponownego napełniania zbiornika można znaleźć w instrukcji producenta pompy wszczepialnej zatwierdzonej do infuzji dooponowej. Istnieją różne pompy o różnej pojemności zbiornika i dostępne są różne zestawy do napełniania. Ważne jest, aby zapoznać się ze wszystkimi tymi produktami, aby wybrać odpowiedni zestaw do napełniania dla konkretnej używanej pompy.
Faza przesiewowa
Przed wszczepieniem pompy i rozpoczęciem długotrwałego wlewu produktu LIORESAL INTRATHECAL (wstrzyknięcie baklofenu) pacjenci muszą wykazać pozytywną odpowiedź kliniczną na dawkę LIORESAL INTRATHECAL w bolusie podawaną dooponowo w badaniu przesiewowym. W badaniu przesiewowym zastosowano LIORESAL INTRATHECAL w stężeniu 50 µg/ml. Ampułka 1 ml (50 mcg/ml) jest dostępna do użycia w badaniu przesiewowym. Procedura przesiewowa jest następująca. Początkowy bolus zawierający 50 mikrogramów w objętości 1 mililitra podaje się do przestrzeni dooponowej przez barbotaż w czasie nie krótszym niż jedna minuta. Pacjent jest obserwowany przez kolejne 4-8 godzin. Na pozytywną odpowiedź składa się znaczne zmniejszenie napięcia mięśniowego i/lub częstotliwości i/lub nasilenia skurczów. Jeśli początkowa odpowiedź jest mniejsza niż pożądana, drugie wstrzyknięcie w bolusie można podać 24 godziny po pierwszym. Druga przesiewowa dawka bolusa to 75 mikrogramów w 1,5 mililitra. Ponownie pacjent powinien być obserwowany przez okres od 4 do 8 godzin. Jeśli odpowiedź jest nadal niewystarczająca, ostateczną dawkę przesiewową w bolusie 100 mikrogramów w 2 mililitrach można podać 24 godziny później.
Pacjenci pediatryczni
Początkowa dawka przesiewowa dla pacjentów pediatrycznych jest taka sama jak u pacjentów dorosłych, tj. 50 mcg. Jednak w przypadku bardzo małych pacjentów można najpierw wypróbować dawkę przesiewową 25 mcg. Pacjenci, którzy nie reagują na bolus dooponowy 100 mcg, nie powinni być uważani za kandydatów do wszczepionej pompy do przewlekłego wlewu.
Okres miareczkowania dawki po implantacji
Aby określić początkową całkowitą dawkę dobową preparatu LIORESAL INTRATHECAL po wszczepieniu implantu, dawkę przesiewową, która dała pozytywny efekt, należy podwoić i podawać przez okres 24 godzin, chyba że skuteczność dawki bolusa utrzymywała się przez ponad 8 godzin, w których W takim przypadku początkowa dawka dobowa powinna być dawką przesiewową dostarczaną w ciągu 24 godzin. Nie należy zwiększać dawki w ciągu pierwszych 24 godzin (tj. do osiągnięcia stanu stacjonarnego).
Dorośli pacjenci ze spastycznością pochodzenia rdzenia kręgowego
Po pierwszych 24 godzinach u dorosłych pacjentów dawkę dobową należy zwiększać powoli o 10-30% i tylko raz na 24 godziny, aż do uzyskania pożądanego efektu klinicznego.
Dorośli pacjenci ze spastycznością pochodzenia mózgowego
Po pierwszych 24 godzinach dawkę dobową należy powoli zwiększać o 5-15% tylko raz na 24 godziny, aż do uzyskania pożądanego efektu klinicznego.
Pacjenci pediatryczni
Po pierwszych 24 godzinach dawkę dobową należy powoli zwiększać o 5-15% tylko raz na 24 godziny, aż do uzyskania pożądanego efektu klinicznego. Jeśli nie ma istotnej odpowiedzi klinicznej na zwiększenie dawki dobowej, należy sprawdzić prawidłowe działanie pompy i drożność cewnika. Pacjenci muszą być ściśle monitorowani w pełni wyposażonym i obsadzonym personelem środowisku podczas fazy przesiewowej i okresu miareczkowania dawki bezpośrednio po implantacji. Sprzęt do resuscytacji powinien być natychmiast dostępny do użycia w przypadku wystąpienia zagrażających życiu lub niedopuszczalnych skutków ubocznych.
Terapia podtrzymująca
Spastyczność pacjentów z rdzeniem kręgowym
Celem klinicznym jest utrzymanie napięcia mięśniowego jak najbardziej zbliżonego do normalnego oraz zminimalizowanie częstotliwości i nasilenia skurczów w możliwie największym stopniu, bez wywoływania niedopuszczalnych skutków ubocznych. Bardzo często dawka podtrzymująca wymaga dostosowania w ciągu pierwszych kilku miesięcy terapii, podczas gdy pacjenci przystosowują się do zmian stylu życia ze względu na złagodzenie spastyczności. Podczas okresowego uzupełniania pompy dawkę dzienną można zwiększyć o 10-40%, ale nie więcej niż 40%, aby utrzymać odpowiednią kontrolę objawów. Dzienna dawka może zostać zmniejszona o 10-20%, jeśli u pacjenta wystąpią działania niepożądane. Większość pacjentów wymaga stopniowego zwiększania dawki w czasie, aby utrzymać optymalną odpowiedź podczas przewlekłej terapii. Nagłe, duże zapotrzebowanie na zwiększenie dawki sugeruje powikłanie cewnika (tj. załamanie lub przemieszczenie cewnika).
Dawka podtrzymująca przy długotrwałym ciągłym wlewie preparatu LIORESAL 10 mg INTRATHECAL (wstrzyknięcie baklofenu) wahała się od 12 mikrogramów/dobę do 2003 mikrogramów/dobę, przy czym u większości pacjentów odpowiednio utrzymywano dawkę od 300 do 800 mikrogramów na dobę. Doświadczenie z dawkami dobowymi większymi niż 1000 mcg/dobę jest ograniczone. Ustalenie optymalnej dawki preparatu LIORESAL INTRATHECAL wymaga indywidualnego dostosowania dawki. Należy stosować najniższą dawkę z optymalną odpowiedzią.
Pacjenci ze spastycznością pochodzenia mózgowego
Celem klinicznym jest utrzymanie napięcia mięśniowego jak najbardziej zbliżonego do normalnego oraz zminimalizowanie częstotliwości i nasilenia skurczów w możliwie największym stopniu, bez wywoływania nietolerowanych działań niepożądanych, lub dostosowanie dawki do pożądanego stopnia napięcia mięśniowego w celu uzyskania optymalnych funkcji. Bardzo często dawka podtrzymująca wymaga dostosowania w ciągu pierwszych kilku miesięcy terapii, podczas gdy pacjenci przystosowują się do zmian stylu życia ze względu na złagodzenie spastyczności. Podczas okresowego uzupełniania pompy dawkę dobową można zwiększyć o 5-20%, ale nie więcej niż o 20%, aby utrzymać odpowiednią kontrolę objawów. Dzienna dawka może zostać zmniejszona o 10-20%, jeśli u pacjenta wystąpią działania niepożądane. Wielu pacjentów wymaga stopniowego zwiększania dawki w czasie, aby utrzymać optymalną odpowiedź podczas przewlekłej terapii. Nagłe, duże zapotrzebowanie na zwiększenie dawki sugeruje powikłanie cewnika (tj. załamanie lub przemieszczenie cewnika).
Dawka podtrzymująca w przypadku długotrwałej ciągłej infuzji produktu leczniczego Lioresal 25 mg INTRATHECAL (wstrzyknięcie baklofenu) wahała się od 22 mikrogramów/dobę do 1400 mikrogramów/dobę, przy czym u większości pacjentów odpowiednio utrzymywała się dawka od 90 do 703 mikrogramów na dobę. W badaniach klinicznych tylko 3 ze 150 pacjentów wymagało dawek dobowych większych niż 1000 mcg/dobę.
Pacjenci pediatryczni
Należy stosować te same zalecenia dotyczące dawkowania u pacjentów ze spastycznością pochodzenia mózgowego. W badaniach klinicznych wydawało się, że pacjenci pediatryczni w wieku poniżej 12 lat wymagają mniejszej dawki dobowej. Średnia dzienna dawka dla pacjentów w wieku poniżej 12 lat wynosiła 274 mcg/dobę, w zakresie od 24 do 1199 mcg/dobę. Wydaje się, że wymagania dotyczące dawkowania u dzieci w wieku powyżej 12 lat nie różnią się od wymagań u pacjentów dorosłych. Ustalenie optymalnej dawki preparatu LIORESAL INTRATHECAL wymaga indywidualnego dostosowania dawki. Należy stosować najniższą dawkę z optymalną odpowiedzią.
Potencjalna potrzeba dostosowania dawki w przypadku długotrwałego stosowania
Podczas długotrwałego leczenia około 5% (28/627) pacjentów staje się opornych na wzrastające dawki. Nie ma wystarczającego doświadczenia, aby sformułować jednoznaczne zalecenia dotyczące leczenia tolerancji; jednak ta „tolerancja” była czasami leczona w szpitalu przez „wakacje od narkotyków” polegające na stopniowym zmniejszaniu dawki LIORESAL 25 mg INTRATHECAL w okresie od 2 do 4 tygodni i przejściu na alternatywne metody leczenia spastyczności. Po przerwie od przyjmowania leku LIORESAL INTRATHECAL można wznowić w początkowej ciągłej dawce wlewu.
Stabilność
Produkty lecznicze do podawania pozajelitowego należy przed podaniem sprawdzić pod kątem obecności cząstek stałych i przebarwień, o ile pozwala na to roztwór i pojemnik.
Specyfikacja dostawy
Konkretne stężenie, które należy zastosować, zależy od całkowitej wymaganej dawki dziennej, a także od szybkości podawania pompy. LIORESAL 10 mg INTRATHECAL może wymagać rozcieńczenia w przypadku stosowania z niektórymi wszczepialnymi pompami. Szczegółowe zalecenia można znaleźć w instrukcji producenta.
Instrukcja przygotowania
Ekranizacja
Do wstrzyknięcia bolusa do przestrzeni podpajęczynówkowej należy używać wyłącznie ampułki przesiewowej o pojemności 1 ml (50 μg/ml). W przypadku dawki bolusa 50 mcg należy użyć 1 ml ampułki przesiewowej. Użyj 1,5 ml zastrzyku 50 mcg/ml baklofenu dla dawki 75 mcg w bolusie. W celu uzyskania maksymalnej dawki przesiewowej 100 mcg należy użyć 2 ml wstrzyknięcia baklofenu 50 mcg/ml (2 ampułki przesiewowe).
Konserwacja
Dla pacjentów, którzy wymagają stężeń innych niż 500 μg/ml lub 2000 μg/ml, LIORESAL INTRATHECAL musi być rozcieńczony .
LIORESAL 10 mg DOKANAŁOWY musi być rozcieńczony ze sterylnym chlorkiem sodu do wstrzykiwań bez konserwantów, USP
Schemat dostawy
LIORESAL 10 mg INTRATHECAL jest najczęściej podawany we wlewie ciągłym bezpośrednio po wszczepieniu. W przypadku pacjentów z wszczepionymi programowalnymi pompami, którzy uzyskali względnie zadowalającą kontrolę podczas wlewu ciągłego, dalsze korzyści można osiągnąć, stosując bardziej złożone schematy podawania LIORESAL INTRATHECAL. Na przykład pacjenci, u których w nocy występują nasilone skurcze, mogą wymagać 20% zwiększenia szybkości infuzji na godzinę. Zmiany szybkości przepływu należy zaprogramować tak, aby rozpoczynały się na dwie godziny przed pożądanym efektem klinicznym.
JAK DOSTARCZONE
LIORESAL INTRATHECAL (wstrzyknięcie baklofenu) jest pakowany w jednorazowych ampułkach zawierających 0,05 mg/1 ml (50 mcg/ml), 10 mg/20 ml (500 mcg/ml), 10 mg/5 ml (2000 mcg/ml) lub 40 mg/20 ml ( 2000 mcg/ml) dostarczane w następujący sposób:
Dawka przesiewowa (Model 8563s): pięć ampułek, każda zawierająca 0,05 mg/1 ml (50 mcg/ml) ( NDC 70257-562-55).
LIORESAL INTRATHECAL (wstrzyknięcie baklofenu) Zestawy uzupełniające Każdy zestaw uzupełniający zawiera wskazaną ilość LIORESAL INTRATHECAL, zestaw do przygotowania leku, zestaw do napełniania pompy z akcesoriami zgodnymi z systemami infuzyjnymi Medtronic SynchroMed® oraz powiązane instrukcje.
Model 8561 : jedna ampułka zawierająca 10 mg/20 ml (500 mcg/ml) ( NDC 70257-560-01).
Model 8562 : dwie ampułki, każda zawiera 10 mg/5 ml (2000 mcg/ml) ( NDC 70257-561-02).
Model 8564 : jedna ampułka zawierająca 40 mg/20 ml (2000 mcg/ml) ( NDC 70257-563-01).
Model 8565 : dwie ampułki, każda zawiera 10 mg/20 ml (500 mcg/ml) ( NDC 70257-560-02).
Model 8566 : dwie ampułki, każda zawiera 40 mg/20 ml (2000 mcg/ml) ( NDC 70257-563-02).
Magazynowanie
Nie wymaga chłodzenia.
Nie przechowywać w temperaturze powyżej 86 ° F (30 ° C).
Nie zamrażać.
Nie sterylizować termicznie.
Dystrybutor: Saol Therapeutics Inc. Saol Therapeutics Inc., Roswell, GA 30076. Aktualizacja: styczeń 2019 r.
SKUTKI UBOCZNE
Spastyczność pochodzenia rdzenia kręgowego - badania kliniczne
Powszechnie obserwowane u pacjentów ze spastycznością pochodzenia rdzeniowego
W badaniach klinicznych przed wprowadzeniem do obrotu i po wprowadzeniu do obrotu najczęściej obserwowanymi zdarzeniami niepożądanymi związanymi ze stosowaniem produktu LIORESAL 25 mg INTRATHECAL (wstrzyknięcie baklofenu), które nie występowały z taką samą częstością wśród pacjentów otrzymujących placebo, były: senność, zawroty głowy, nudności, niedociśnienie, ból głowy, drgawki i hipotonia.
Związane z przerwaniem leczenia
8/474 pacjentów ze spastycznością pochodzenia rdzeniowego otrzymujących długotrwałą infuzję produktu LIORESAL 25 mg INTRATHECAL w badaniach klinicznych prowadzonych przed i po wprowadzeniu do obrotu w USA przerwało leczenie z powodu działań niepożądanych. Należą do nich: infekcje kieszonki pompy (3), zapalenie opon mózgowo-rdzeniowych (2), rozejście się rany (1), włókniaki ginekologiczne (1) i nadciśnienie pompy (1) z nieznanymi, jeśli występują, następstwami. Jedenastu pacjentów, u których rozwinęła się śpiączka wtórna do przedawkowania, tymczasowo zawieszono leczenie, ale wszyscy zostali następnie wznowieni i dlatego nie uznano ich za rzeczywiste przerwanie leczenia.
Ofiary śmiertelne
Widzieć OSTRZEŻENIA .
Przypadki w kontrolowanych badaniach
Doświadczenie ze stosowaniem preparatu LIORESAL INTRATHECAL (wstrzyknięcie baklofenu) uzyskane w równoległych, randomizowanych badaniach kontrolowanych placebo dostarcza jedynie ograniczonej podstawy do oszacowania częstości występowania zdarzeń niepożądanych, ponieważ badania trwały bardzo krótko (do trzech dni wlewu) i obejmowały tylko łącznie 63 pacjentów. Następujące zdarzenia wystąpiły wśród 31 pacjentów otrzymujących LIORESAL INTRATHECAL (wstrzyknięcie baklofenu) w dwóch randomizowanych, kontrolowanych placebo badaniach: niedociśnienie (2), zawroty głowy (2), ból głowy (2), duszność (1). W badaniach tych nie zgłoszono żadnych działań niepożądanych wśród 32 pacjentów otrzymujących placebo.
Zdarzenia obserwowane podczas oceny preparatu LIORESAL INTRATHECAL przed i po wprowadzeniu do obrotu
Zdarzenia niepożądane związane ze stosowaniem preparatu LIORESAL 25 mg INTRATHECAL odzwierciedlają doświadczenie zdobyte u 576 pacjentów obserwowanych prospektywnie w Stanach Zjednoczonych. Otrzymywali LIORESAL INTRATHECAL przez okres od jednego dnia (badania przesiewowe) (N = 576) do ponad ośmiu lat (podtrzymanie) (N = 10). Zazwyczaj przesiewowa dawka bolusa podawana przed wszczepieniem pompy w tych badaniach wynosiła zazwyczaj 50 mcg. Dawka podtrzymująca wahała się od 12 mcg do 2003 mcg dziennie. Ze względu na otwarty, niekontrolowany charakter doświadczenia, w wielu przypadkach nie można wiarygodnie ocenić związku przyczynowego między zaobserwowanymi zdarzeniami a podawaniem produktu LIORESAL INTRATHECAL, a wiele ze zgłoszonych zdarzeń niepożądanych występuje w związku z leczonymi chorobami podstawowymi. Niemniej jednak wiele częściej zgłaszanych reakcji – hipotonia, senność, zawroty głowy, parestezje, nudności/wymioty i ból głowy – wydaje się wyraźnie związanych z lekiem.
Działania niepożądane zgłaszane podczas wszystkich badań w USA (zarówno kontrolowanych, jak i niekontrolowanych) przedstawiono w poniższej tabeli. Ośmiu z 474 pacjentów, którzy otrzymywali przewlekłą infuzję za pomocą wszczepionych pomp, doświadczyło działań niepożądanych, które doprowadziły do przerwania długoterminowego leczenia w badaniach przed wprowadzeniem do obrotu i po wprowadzeniu do obrotu.
WYSTĘPOWANIE NAJCZĘSTSZYCH (≥1%) ZDARZEŃ NIEPOŻĄDANYCH U PACJENTÓW ZE SPASTYCZNOŚCIĄ POCHODZENIA KRĘGOSŁUPA W PROSPEKTYWNIE MONITOROWANYCH BADANIACH KLINICZNYCH
Poza częstszymi (1% lub więcej) zdarzeniami niepożądanymi zgłoszonymi u prospektywnie obserwowanych 576 pacjentów krajowych w badaniach przed wprowadzeniem i po wprowadzeniu produktu do obrotu, doświadczenie dodatkowych 194 pacjentów poddanych ekspozycji na produkt leczniczy LIORESAL 25 mg INTRATHECAL (wstrzyknięcie baklofenu) z badań zagranicznych zostały zgłoszone. Zgłoszono następujące zdarzenia niepożądane, nieopisane w tabeli, uporządkowane według częstości występowania i sklasyfikowane według układu organizmu:
System nerwowy: Nieprawidłowy chód, nieprawidłowe myślenie, drżenie, amnezja, drżenie, rozszerzenie naczyń, udar naczyniowy mózgu, oczopląs, zaburzenia osobowości, depresja psychotyczna, niedokrwienie mózgu, labilność emocjonalna, euforia, hipertonia, niedrożność jelit, uzależnienie od leków, brak koordynacji, reakcja paranoidalna i opadanie powiek.
Układ trawienny: Wzdęcia, dysfagia, niestrawność i zapalenie żołądka i jelit.
Układ sercowo-naczyniowy: Niedociśnienie ortostatyczne, bradykardia, kołatanie serca, omdlenia, arytmia komorowa, zakrzepowe zapalenie żył głębokich, bladość i tachykardia.
Oddechowy: Zaburzenia oddechowe, zachłystowe zapalenie płuc, hiperwentylacja, zator płucny i nieżyt nosa.
Układ moczowo-płciowy: Krwiomocz i niewydolność nerek.
Skóra i przydatki: Łysienie i pocenie się.
Zaburzenia metabolizmu i odżywiania: Utrata masy ciała, albuminuria, odwodnienie i hiperglikemia.
Zmysły specjalne: Zaburzenia widzenia, zaburzenia akomodacji, światłowstręt, utrata smaku i szumy uszne.
Ciało jako całość: Samobójstwo, brak działania leku, ból brzucha, hipotermia, sztywność karku, ból w klatce piersiowej, dreszcze, obrzęk twarzy, zespół grypowy i przedawkowanie.
Układ hemiczny i limfatyczny: Niedokrwistość.
Spastyczność pochodzenia mózgowego - badania kliniczne
Powszechnie obserwowane
W badaniach klinicznych przed wprowadzeniem do obrotu najczęściej obserwowanymi zdarzeniami niepożądanymi związanymi ze stosowaniem produktu leczniczego LIORESAL INTRATHECAL 25 mg (wstrzyknięcie baklofenu), które nie były obserwowane z równą częstością wśród pacjentów otrzymujących placebo, były: pobudzenie, zaparcia, senność, leukocytoza, dreszcze, oddawanie moczu zatrzymanie i hipotonia.
Związane z przerwaniem leczenia
Dziewięciu z 211 pacjentów otrzymujących LIORESAL INTRATHECAL w badaniach klinicznych przed wprowadzeniem do obrotu w Stanach Zjednoczonych przerwało długotrwałą infuzję z powodu działań niepożądanych związanych z terapią dooponową.
Dziewięcioma zdarzeniami niepożądanymi prowadzącymi do przerwania leczenia były: infekcja (3), wyciek płynu mózgowo-rdzeniowego (2), zapalenie opon mózgowo-rdzeniowych (2), drenaż (1) i niekontrolowana kontrola tułowia (1).
Ofiary śmiertelne
W badaniach klinicznych z udziałem pacjentów ze spastycznością pochodzenia mózgowego zgłoszono trzy zgony, z których żaden nie był przypisany do produktu LIORESAL 10 mg INTRATHECAL. Widzieć Ostrzeżenia dotyczące innych zgonów zgłaszanych u pacjentów ze spastycznością kręgosłupa .
Przypadki w kontrolowanych badaniach
Doświadczenie ze stosowaniem preparatu LIORESAL INTRATHECAL (wstrzyknięcie baklofenu) uzyskane w równoległych, randomizowanych badaniach kontrolowanych placebo dostarcza jedynie ograniczonej podstawy do oszacowania częstości występowania zdarzeń niepożądanych, ponieważ badania obejmowały łącznie 62 pacjentów, którym podano pojedynczy bolus dooponowy 50 µg. Następujące zdarzenia wystąpiły u 62 pacjentów otrzymujących lek Lioresal 10 mg INTRATHECAL w dwóch randomizowanych, kontrolowanych placebo badaniach obejmujących pacjentów z porażeniem mózgowym i urazami głowy, odpowiednio: pobudzenie, zaparcia, senność, leukocytoza, nudności, wymioty, oczopląs, dreszcze, zatrzymanie moczu i hipotonia.
Zdarzenia obserwowane podczas oceny leku LIORESAL 25 mg INTRATHECAL przed wprowadzeniem do obrotu
Zdarzenia niepożądane związane ze stosowaniem preparatu LIORESAL INTRATHECAL odzwierciedlają doświadczenie zdobyte łącznie z 211 pacjentami ze Stanów Zjednoczonych ze spastycznością pochodzenia mózgowego, z których 112 było pacjentami pediatrycznymi (w momencie włączenia do badania poniżej 16 roku życia). Otrzymywali LIORESAL INTRATHECAL przez okres od jednego dnia (badania przesiewowe) (N=211) do 84 miesięcy (podtrzymanie) (N=1). Zazwyczaj przesiewowa dawka bolusa podawana przed wszczepieniem pompy w tych badaniach wynosiła 50-75 mcg. Dawka podtrzymująca wahała się od 22 mcg do 1400 mcg dziennie. Dawki stosowane w tej populacji pacjentów do długotrwałej infuzji są na ogół niższe niż dawki wymagane u pacjentów ze spastycznością pochodzenia rdzenia kręgowego.
Ze względu na otwarty, niekontrolowany charakter doświadczenia, w wielu przypadkach nie można wiarygodnie ocenić związku przyczynowego między zaobserwowanymi zdarzeniami a podawaniem produktu LIORESAL INTRATHECAL. Niemniej jednak wiele częściej zgłaszanych reakcji – senność, zawroty głowy, ból głowy, nudności, niedociśnienie, hipotonia i śpiączka – wydaje się wyraźnie związanych z lekiem.
W poniższej tabeli przedstawiono najczęstsze (≥1%) zdarzenia niepożądane zgłaszane podczas wszystkich badań klinicznych. Dziewięciu pacjentów przerwało długoterminowe leczenie z powodu działań niepożądanych.
WYSTĘPOWANIE NAJCZĘSTSZE (≥ 1%) ZDARZEŃ NIEPOŻĄDANYCH U PACJENTÓW ZE SPASTYCZNOŚCIĄ POCHODZENIA MÓZGOWEGO W PROSPEKTYWNIE MONITOROWANYCH BADANIACH KLINICZNYCH
Zgłoszono częstsze (1% lub więcej) zdarzenia niepożądane zgłaszane u prospektywnie obserwowanych 211 pacjentów poddanych ekspozycji na produkt leczniczy Lioresal 25 mg INTRATHECAL (wstrzyknięcie baklofenu). W całej kohorcie zgłoszono następujące zdarzenia niepożądane, nieopisane w tabeli, uporządkowane według częstości występowania i sklasyfikowane według układu organizmu:
System nerwowy: Akatyzja, ataksja, splątanie, depresja, opistotonos, amnezja, lęk, halucynacje, histeria, bezsenność, oczopląs, zaburzenia osobowości, osłabienie odruchów i rozszerzenie naczyń.
Układ trawienny: Dysfagia, nietrzymanie stolca, krwotok z przewodu pokarmowego i zaburzenia języka.
Układ sercowo-naczyniowy: Bradykardia.
Oddechowy: Bezdech, duszność i hiperwentylacja.
Układ moczowo-płciowy: Nieprawidłowy wytrysk, kamień nerkowy, skąpomocz i zapalenie pochwy.
Skóra i przydatki: Wysypka, pocenie się, łysienie, kontaktowe zapalenie skóry i owrzodzenie skóry.
Zmysły specjalne: Nieprawidłowość zakwaterowania.
Ciało jako całość: Śmierć, gorączka, ból brzucha, rak, złe samopoczucie i hipotermia.
Układ hemiczny i limfatyczny: Leukocytoza i wysypka wybroczynowa.
Doświadczenie postmarketingowe
Następujące działania niepożądane zgłaszano po dopuszczeniu produktu LIORESAL INTRATHECAL do obrotu. Ponieważ zdarzenia te są zgłaszane dobrowolnie z populacji o niepewnej wielkości, nie jest możliwe wiarygodne oszacowanie ich częstotliwości.
Układ mięśniowo-szkieletowy
Zgłaszano początek skoliozy lub pogorszenie już istniejącej skoliozy.
Układ moczowo-płciowy
Zgłaszano zaburzenia seksualne u mężczyzn i kobiet, w tym zmniejszenie libido i zaburzenia orgazmu. Zgłaszano również zaburzenia erekcji u mężczyzn. Po odstawieniu baklofenu zgłaszano priapizm.
INTERAKCJE Z LEKAMI
Nie ma wystarczającego systematycznego doświadczenia ze stosowaniem preparatu LIORESAL INTRATHECAL w skojarzeniu z innymi lekami w celu przewidzenia określonych interakcji lekowych. Interakcje przypisywane skojarzonemu stosowaniu LIORESAL INTRATHECAL i morfiny zewnątrzoponowej obejmują niedociśnienie i duszność.
OSTRZEŻENIA
LIORESAL INTRATHECAL jest przeznaczony do stosowania w pojedynczych wstrzyknięciach dooponowych w bolusie (przez cewnik umieszczony w przestrzeni lędźwiowej dooponowej lub wstrzyknięcie przez nakłucie lędźwiowe) oraz w wszczepialnych pompach zatwierdzonych przez FDA specjalnie do dooponowego podawania baklofenu. Ze względu na możliwość wystąpienia potencjalnie zagrażającej życiu depresji ośrodkowego układu nerwowego, zapaści sercowo-naczyniowej i (lub) niewydolności oddechowej, lekarze muszą być odpowiednio przeszkoleni i przeszkoleni w zakresie przewlekłego leczenia wlewem dooponowym.
Systemu pompy nie należy wszczepiać do czasu odpowiedniej oceny odpowiedzi pacjenta na bolus LIORESAL 10 mg INTRATHECAL. Ocena (składająca się z procedury przesiewowej: patrz DAWKOWANIE I SPOSÓB PODAWANIA wymaga podania leku LIORESAL 25 mg INTRATHECAL do przestrzeni dooponowej przez cewnik lub nakłucie lędźwiowe. Ze względu na ryzyko związane z badaniem przesiewowym i dostosowaniem dawkowania po wszczepieniu pompy, fazy te należy przeprowadzać w środowisku nadzorowanym przez personel medyczny i odpowiednio wyposażonym, zgodnie z instrukcjami podanymi w rozdziale „Dawkowanie i podawanie”.
Sprzęt do resuscytacji powinien być dostępny.
Po chirurgicznym wszczepieniu pompy, szczególnie w początkowych fazach używania pompy, pacjenta należy ściśle monitorować do momentu upewnienia się, że odpowiedź pacjenta na infuzję jest akceptowalna i względnie stabilna.
Za każdym razem, gdy szybkość dawkowania pompy i (lub) stężenie preparatu LIORESAL INTRATHECAL (wstrzyknięcie baklofenu) w zbiorniku jest dostosowywana, wymagana jest ścisła obserwacja lekarska do czasu upewnienia się, że reakcja pacjenta na infuzję jest akceptowalna i względnie stabilna.
Obowiązkowe jest, aby pacjent, wszyscy opiekunowie pacjenta oraz lekarze odpowiedzialni za pacjenta otrzymywali odpowiednie informacje dotyczące zagrożeń związanych z tym sposobem leczenia. Cały personel medyczny i opiekunowie powinni zostać poinstruowani w zakresie 1) oznak i objawów przedawkowania, 2) procedur postępowania w przypadku przedawkowania oraz 3) właściwej domowej pielęgnacji pompy i miejsca wprowadzenia.
Przedawkować
Oznaki przedawkowania mogą pojawić się nagle lub podstępnie. Ostre, masowe przedawkowanie może objawiać się śpiączką. Mniej nagłe i (lub) mniej nasilone postacie przedawkowania mogą objawiać się objawami senności, zawrotów głowy, zawrotów głowy, senności, depresji oddechowej, drgawek, progralnej progresji hipotonii i utraty przytomności prowadzącej do śpiączki. Jeśli prawdopodobne jest przedawkowanie, pacjenta należy natychmiast zabrać do szpitala w celu oceny i opróżnienia zbiornika pompy. W dotychczas zgłoszonych przypadkach przedawkowanie było na ogół związane z nieprawidłowym działaniem pompy, niezamierzonym wstrzyknięciem podskórnym lub błędem dawkowania. (Widzieć Objawy i leczenie przedawkowania leków .)
Podczas napełniania wszczepialnej pompy zatwierdzonej przez FDA należy zachować szczególną ostrożność. Takie pompy powinny być uzupełniane tylko przez przegrodę do napełniania zbiornika. Nieumyślne wstrzyknięcie do tkanki podskórnej może nastąpić, jeśli przegroda napełniania zbiornika nie jest prawidłowo dostępna. Niektóre pompy są również wyposażone w port dostępu do cewnika, który umożliwia bezpośredni dostęp do cewnika dooponowego. Bezpośrednie wstrzyknięcie do tego portu dostępu cewnika lub nieumyślne wstrzyknięcie do tkanki podskórnej może spowodować zagrażające życiu przedawkowanie.
Wycofanie
Nagłe odstawienie baklofenu dooponowego, niezależnie od przyczyny, spowodowało następstwa, które obejmowały wysoką gorączkę, zmiany stanu psychicznego, nadmierną spastyczność z odbicia i sztywność mięśni, która w rzadkich przypadkach prowadziła do rabdomiolizy, niewydolności wielonarządowej i zgonu. W ciągu pierwszych 9 lat doświadczenia po wprowadzeniu do obrotu zgłoszono 27 przypadków odstawienia czasowo związanych z zaprzestaniem leczenia baklofenem; zmarło sześciu pacjentów. W większości przypadków objawy odstawienia pojawiały się w ciągu kilku godzin do kilku dni po przerwaniu terapii baklofenem. Najczęstszymi przyczynami nagłego przerwania dooponowej terapii baklofenem były nieprawidłowe działanie cewnika (zwłaszcza odłączenie), mała objętość zbiornika pompy i koniec żywotności baterii pompy; W niektórych przypadkach błąd ludzki mógł odgrywać rolę przyczynową lub przyczyniającą się do tego. Zgłaszano również przypadki nacieku dooponowego na końcu wszczepionego cewnika prowadzące do objawów odstawienia, większość z nich dotyczyła domieszek przeciwbólowych przygotowywanych przez farmację (patrz ŚRODKI OSTROŻNOŚCI ).
Zapobieganie nagłemu odstawieniu baklofenu dooponowego wymaga szczególnej uwagi podczas programowania i monitorowania systemu infuzyjnego, planowania i procedur ponownego napełniania oraz alarmów pompy. Pacjenci i opiekunowie powinni być poinformowani o znaczeniu regularnych wizyt uzupełniających i powinni być pouczeni o wczesnych objawach odstawienia baklofenu.
Wszyscy pacjenci otrzymujący dooponową terapię baklofenem są potencjalnie narażeni na ryzyko odstawienia. Wczesne objawy odstawienia baklofenu mogą obejmować powrót spastyczności, świąd, niedociśnienie i parestezje. Priapizm może rozwinąć się lub nawrócić, jeśli leczenie dooponowym baklofenem zostanie przerwane. Niektóre cechy kliniczne zaawansowanego dooponowego zespołu odstawienia baklofenu mogą przypominać autonomiczną dysrefleksję, infekcję (sepsę), hipertermię złośliwą, złośliwy zespół neuroleptyczny lub inne stany związane ze stanem hipermetabolicznym lub rozległą rabdomiolizą.
Szybka, dokładna diagnoza i leczenie na izbie przyjęć lub na oddziale intensywnej terapii są ważne, aby zapobiec potencjalnie zagrażającemu życiu ośrodkowemu układowi nerwowemu i ogólnoustrojowym skutkom odstawienia baklofenu dooponowego. Sugerowanym sposobem leczenia dooponowego odstawienia baklofenu jest przywrócenie baklofenu podawanego dooponowo w takiej samej dawce lub zbliżonej do tej, jaka była przed przerwaniem terapii. Jednakże, jeśli przywrócenie dooponowego dostarczania jest opóźnione, leczenie agonistami receptorów GABA-ergicznych, takimi jak doustny lub dojelitowy baklofen, albo doustne, dojelitowe lub dożylne benzodiazepiny może zapobiec potencjalnie śmiertelnym następstwom. Sam baklofen podawany doustnie lub dojelitowo nie powinien hamować postępu odstawienia baklofenu dooponowego.
Napady drgawkowe zgłaszano podczas przedawkowania i po odstawieniu produktu LIORESAL INTRATHECAL 25 mg, jak również u pacjentów, u których stosowano dawki terapeutyczne produktu LIORESAL INTRATHECAL.
Ofiary śmiertelne
Spastyczność pochodzenia rdzenia kręgowego
Odnotowano 16 zgonów wśród 576 pacjentów w USA leczonych produktem leczniczym LIORESAL 10 mg INTRATHECAL (wstrzyknięcie baklofenu) w badaniach przed i po wprowadzeniu do obrotu ocenianych w grudniu 1992 roku. Ponieważ pacjenci ci byli leczeni w niekontrolowanych warunkach klinicznych, nie jest możliwe ostateczne ustalenie, co Rola, jeśli w ogóle, odegrała LIORESAL INTRATHECAL w ich śmierci.
Jako grupa pacjenci, którzy zmarli, byli stosunkowo młodzi (średnia wieku 47 lat z przedziałem od 25 do 63 lat), ale większość cierpiała na ciężką spastyczność, trwającą wiele lat, nie poruszała się, miała różne powikłania medyczne, takie jak zapalenie płuc, dróg moczowych infekcje i odleżyny i/lub otrzymywał jednocześnie wiele leków. Indywidualny przegląd przebiegu klinicznego 16 pacjentów, którzy zmarli, nie ujawnił żadnych unikalnych oznak, objawów ani wyników badań laboratoryjnych, które sugerowałyby, że leczenie preparatem LIORESAL INTRATHECAL spowodowało ich zgon. Dwóch pacjentów doznało jednak nagłej i nieoczekiwanej śmierci w ciągu 2 tygodni od implantacji pompy, a jeden pacjent zmarł niespodziewanie po badaniu przesiewowym.
Jeden pacjent, 44-letni mężczyzna ze stwardnieniem rozsianym, zmarł w szpitalu drugiego dnia po wszczepieniu pompy. Sekcja zwłok wykazała silne zwłóknienie układu przewodzenia wieńcowego. Drugi pacjent, 52-letnia kobieta ze stwardnieniem rozsianym i przebytym zawałem mięśnia sercowego dolnej ściany, został znaleziony martwy w łóżku 12 dni po wszczepieniu pompy, 2 godziny po udokumentowaniu normalnych parametrów życiowych. Sekcja zwłok wykazała przekrwienie płuc i obustronny wysięk opłucnowy. Nie można ustalić, czy LIORESAL INTRATHECAL przyczynił się do tych zgonów. Trzeci pacjent przeszedł trzy badania przesiewowe z użyciem baklofenu. Jego historia medyczna obejmowała SCI, zachłystowe zapalenie płuc, wstrząs septyczny, rozsianą koagulopatię wewnątrznaczyniową, ciężką kwasicę metaboliczną, toksyczność wątrobową i stan padaczkowy. Dwanaście dni po badaniu przesiewowym (nie wszczepiono mu implantu) ponownie doświadczył stanu padaczkowego z późniejszym znacznym pogorszeniem stanu neurologicznego. Na podstawie wcześniejszych instrukcji nie podjęto nadzwyczajnych środków resuscytacyjnych i pacjent zmarł.
Spastyczność pochodzenia mózgowego
Spośród 211 pacjentów leczonych produktem LIORESAL INTRATHECAL w badaniach przed wprowadzeniem do obrotu w marcu 1996 r. wystąpiły trzy zgony. Zgony te nie były przypisywane terapii.
Nadmierna infuzja
Podanie większej ilości leku niż zaprogramowana szybkość (nadmierna infuzja) może spowodować nieoczekiwane przedawkowanie lub wycofanie spowodowane wczesnym opróżnieniem zbiornika pompy. Zapoznaj się z instrukcją producenta pompy i instrukcjami ponownego napełniania zbiornika.
ŚRODKI OSTROŻNOŚCI
Dzieci powinny mieć wystarczającą masę ciała, aby pomieścić wszczepialną pompę do przewlekłej infuzji. Szczegółowe zalecenia można znaleźć w instrukcji producenta pompy.
Bezpieczeństwo i skuteczność u dzieci w wieku poniżej 4 lat nie zostały ustalone.
Ekranizacja
Pacjenci powinni być wolni od infekcji przed badaniem przesiewowym z zastosowaniem LIORESAL INTRATHECAL (wstrzyknięcie baklofenu), ponieważ obecność infekcji ogólnoustrojowej może zakłócać ocenę odpowiedzi pacjenta na bolus LIORESAL INTRATHECAL 10 mg.
Implantacja pompy
Pacjenci powinni być wolni od infekcji przed implantacją pompy, ponieważ obecność infekcji może zwiększać ryzyko powikłań chirurgicznych. Ponadto infekcja ogólnoustrojowa może skomplikować dawkowanie.
Regulacja i miareczkowanie dawki pompy
U większości pacjentów konieczne będzie stopniowe zwiększanie dawki w czasie w celu utrzymania skuteczności; nagłe zapotrzebowanie na znaczne zwiększenie dawki zazwyczaj wskazuje na powikłanie cewnika (tj. załamanie lub przemieszczenie cewnika).
Napełnianie zbiornika musi być wykonywane przez w pełni przeszkolony i wykwalifikowany personel, zgodnie z instrukcjami dostarczonymi przez producenta pompy. Nieumyślne wstrzyknięcie do tkanki podskórnej może nastąpić, jeśli przegroda napełniania zbiornika nie jest prawidłowo dostępna. Wstrzyknięcie podskórne może spowodować objawy ogólnoustrojowego przedawkowania lub wczesne wyczerpanie zbiornika. Okresy między kolejnymi napełnianiami powinny być dokładnie obliczone, aby zapobiec wyczerpaniu zbiornika, ponieważ mogłoby to spowodować nawrót ostrej spastyczności i ewentualnie objawów odstawienia.
Wymagana jest ścisła aseptyczna technika napełniania, aby uniknąć skażenia bakteryjnego i poważnej infekcji. Po każdym ponownym napełnieniu lub manipulacji zbiornikiem leku powinien następować okres obserwacji odpowiedni do sytuacji klinicznej.
Należy zachować szczególną ostrożność podczas napełniania wszczepialnej pompy zatwierdzonej przez FDA wyposażonej w port iniekcyjny, który umożliwia bezpośredni dostęp do cewnika dooponowego. Bezpośrednie wstrzyknięcie do cewnika przez port dostępu cewnika może spowodować zagrażające życiu przedawkowanie.
Dodatkowe uwagi dotyczące dostosowania dawki
Może być ważne dostosowanie dawki w celu utrzymania odpowiedniego napięcia mięśniowego i umożliwienia sporadycznych skurczów, aby: 1) wspomóc funkcjonowanie układu krążenia, 2) ewentualnie zapobiec powstawaniu zakrzepicy żył głębokich, 3) zoptymalizować codzienne czynności i ułatwić pielęgnację .
Z wyjątkiem nagłych przypadków związanych z przedawkowaniem, dawkę produktu leczniczego Lioresal 25 mg INTRATHECAL należy zwykle zmniejszać powoli, jeśli lek zostanie przerwany z jakiegokolwiek powodu.
Należy podjąć próbę odstawienia jednocześnie podawanych doustnych leków przeciwspastycznych, aby uniknąć możliwego przedawkowania lub niepożądanych interakcji leków, przed badaniem przesiewowym lub po wszczepieniu implantu i rozpoczęciu przewlekłej infuzji produktu Lioresal INTRATHECAL. Zmniejszenie dawki i odstawienie doustnych leków przeciwskurczowych powinno odbywać się powoli i pod ścisłą kontrolą lekarza. Należy unikać nagłego zmniejszenia dawki lub odstawienia jednocześnie stosowanych leków przeciwskurczowych.
Senność
Senność była zgłaszana u pacjentów stosujących LIORESAL INTRATHECAL. Pacjentów należy ostrzec o obsłudze samochodów lub innych niebezpiecznych maszyn oraz czynnościach, które są niebezpieczne z powodu obniżonej czujności. Należy również ostrzec pacjentów, że działanie depresyjne na ośrodkowy układ nerwowy produktu LIORESAL INTRATHECAL (wstrzyknięcie baklofenu) może się sumować z działaniem alkoholu i innych leków depresyjnych na ośrodkowy układ nerwowy.
Masa dooponowa
Zgłaszano przypadki nacieku wewnątrzkanałowego na końcu wszczepionego cewnika, w większości przypadków domieszek przeciwbólowych skomponowanych w farmacji. Najczęstsze objawy związane z naciekiem dooponowym to: 1) zmniejszona odpowiedź terapeutyczna (pogorszenie spastyczności, nawrót spastyczności przy wcześniej dobrze kontrolowanej, objawy odstawienia, słaba reakcja na rosnące dawki lub częste lub duże zwiększanie dawki), 2) ból, 3) deficyt/dysfunkcja neurologiczna. Klinicyści powinni uważnie monitorować pacjentów leczonych dordzeniowo pod kątem nowych oznak lub objawów neurologicznych. U pacjentów z nowymi objawami lub objawami neurologicznymi sugerującymi naciek dooponowy należy rozważyć konsultację neurochirurgiczną, ponieważ wiele objawów nacieku zapalnego nie różni się od objawów, których doświadczają pacjenci z ciężką spastycznością spowodowaną chorobą. W niektórych przypadkach wykonanie procedury obrazowania może być właściwe w celu potwierdzenia lub wykluczenia diagnozy guza wewnątrzoponowego.
Środki ostrożności w specjalnych populacjach pacjentów
Ostrożne dostosowywanie dawki produktu leczniczego Lioresal 10 mg INTRATHECAL jest konieczne, gdy spastyczność jest konieczna do utrzymania wyprostowanej postawy i równowagi podczas poruszania się lub gdy spastyczność jest stosowana w celu uzyskania optymalnego funkcjonowania i opieki.
Pacjenci cierpiący na zaburzenia psychotyczne, schizofrenię lub stany splątania powinni być ostrożnie leczeni produktem LIORESAL INTRATHECAL i pozostawać pod ścisłą obserwacją, ponieważ zaostrzenia tych stanów obserwowano po podaniu doustnym.
LIORESAL INTRATHECAL należy stosować ostrożnie u pacjentów z dysrefleksją autonomiczną w wywiadzie. Obecność bodźców nocyceptywnych lub nagłe odstawienie produktu Lioresal 10 mg INTRATHECAL (wstrzyknięcie baklofenu) może spowodować epizod autonomicznej dysrefleksji.
Ponieważ LIORESAL jest wydalany głównie w postaci niezmienionej przez nerki, należy go podawać ostrożnie pacjentom z zaburzeniami czynności nerek i może być konieczne zmniejszenie dawki.
Testy laboratoryjne
Żadne specjalne testy laboratoryjne nie są uważane za niezbędne do leczenia pacjentów stosujących LIORESAL INTRATHECAL.
Karcynogeneza, mutageneza i upośledzenie płodności
Nie zaobserwowano wzrostu guzów u szczurów otrzymujących doustnie baklofen przez dwa lata. Nie przeprowadzono odpowiednich testów genotoksyczności baklofenu.
Ciąża
Nie ma odpowiednich i dobrze kontrolowanych badań u kobiet w ciąży. W badaniach na zwierzętach baklofen miał niekorzystny wpływ na rozwój zarodka i płodu, gdy był podawany doustnie ciężarnym szczurom. LIORESAL 25 mg INTRATHECAL należy stosować w okresie ciąży tylko wtedy, gdy potencjalna korzyść przewyższa potencjalne ryzyko dla płodu.
Baklofen podawany doustnie zwiększał częstość występowania nieprawidłowości strukturalnych płodu (pęcherzyki pępowinowe) u szczurów. U matek zaobserwowano zmniejszenie spożycia pokarmu i przyrostu masy ciała. Nieprawidłowości strukturalne płodu nie obserwowano u myszy ani królików
Matki karmiące
matek leczonych doustnie LIORESALEM (baklofen USP) w dawkach terapeutycznych substancja czynna przenika do mleka. Nie wiadomo, czy w mleku karmiących matek otrzymujących LIORESAL 25 mg INTRATHECAL obecne są wykrywalne poziomy leku. Zasadniczo karmienie piersią należy podejmować w czasie, gdy pacjent otrzymuje produkt leczniczy Lioresal 25 mg INTRATHECAL tylko wtedy, gdy potencjalna korzyść uzasadnia potencjalne ryzyko dla niemowlęcia.
Zastosowanie pediatryczne
Dzieci powinny mieć wystarczającą masę ciała, aby pomieścić wszczepialną pompę do przewlekłej infuzji. Szczegółowe zalecenia można znaleźć w instrukcji producenta pompy.
Bezpieczeństwo i skuteczność u dzieci w wieku poniżej 4 lat nie zostały ustalone.
Rozważania oparte na doświadczeniu z doustnym preparatem LIORESAL (baklofen USP)
U samic szczurów leczonych przewlekle doustnym produktem leczniczym Lioresal zaobserwowano zależne od dawki zwiększenie częstości występowania torbieli jajników. Torbiele jajników wykryto przez badanie dotykowe u około 4% pacjentów ze stwardnieniem rozsianym, którzy byli leczeni doustnym lekiem LIORESAL 25 mg przez okres do jednego roku. W większości przypadków torbiele te znikały samoistnie, podczas gdy pacjenci kontynuowali przyjmowanie leku. Szacuje się, że torbiele jajników występują spontanicznie u około 1% do 5% normalnej populacji kobiet.
PRZEDAWKOWAĆ
Szczególną uwagę należy zwrócić na rozpoznanie oznak i objawów przedawkowania, zwłaszcza w początkowej fazie badania przesiewowego i miareczkowania dawki leczenia, a także podczas ponownego wprowadzania produktu LIORESAL INTRATHECAL po okresie przerwy w leczeniu.
Objawy przedawkowania LIORESAL DOKANAŁOWEGO
Senność, zawroty głowy, zawroty głowy, senność, depresja oddechowa, hipotermia, drgawki, progresja hipotonii rostralnej i utrata przytomności przechodząca w śpiączkę trwającą do 72 godzin. Trwanie. W większości zgłoszonych przypadków śpiączka ustępowała bez następstw po odstawieniu leku. Objawy przedawkowania produktu Lioresal 25 mg INTRATHECAL zgłoszono u wrażliwego dorosłego pacjenta po otrzymaniu 25 mikrogramów w bolusie dooponowym.
Zalecenia dotyczące leczenia przedawkowania
Nie ma swoistego antidotum w przypadku przedawkowania preparatu LIORESAL INTRATHECAL (wstrzyknięcie baklofenu); jednak zwykle należy podjąć następujące kroki:
Jeśli nakłucie lędźwiowe nie jest przeciwwskazane, należy rozważyć pobranie 30-40 ml płynu mózgowo-rdzeniowego w celu zmniejszenia stężenia baklofenu w płynie mózgowo-rdzeniowym.
PRZECIWWSKAZANIA
Nadwrażliwość na baklofen. LIORESAL INTRATHECAL nie jest zalecany do podawania dożylnego, domięśniowego, podskórnego lub nadtwardówkowego.
FARMAKOLOGIA KLINICZNA
Dokładny mechanizm działania baklofenu jako środka zwiotczającego mięśnie i przeciwskurczowego nie jest w pełni poznany. Baklofen hamuje zarówno odruchy monosynaptyczne, jak i polisynaptyczne na poziomie rdzenia kręgowego, prawdopodobnie poprzez zmniejszenie uwalniania neuroprzekaźników pobudzających z pierwotnych zakończeń doprowadzających, chociaż działania w miejscach nadrdzeniowych mogą również wystąpić i przyczynić się do jego działania klinicznego. Baklofen jest strukturalnym analogiem hamującego neuroprzekaźnika kwasu gamma-aminomasłowego (GABA) i może wywierać swoje działanie poprzez stymulację podtypu receptora GABAB.
LIORESAL INTRATHECAL po wprowadzeniu bezpośrednio do przestrzeni dooponowej pozwala na osiągnięcie skutecznych stężeń płynu mózgowo-rdzeniowego, przy czym wynikowe stężenia w osoczu są 100 razy mniejsze niż te występujące przy podawaniu doustnym.
ludzi, jak również u zwierząt wykazano, że baklofen ma ogólne właściwości hamujące ośrodkowy układ nerwowy, na co wskazuje sedacja z tolerancją, senność, ataksja oraz depresja oddechowa i sercowo-naczyniowa.
Farmakodynamika LIORESAL INTRATHECAL
Bolus dooponowy
Pacjenci dorośli
Początek działania to zazwyczaj od pół godziny do godziny po podaniu bolusa dooponowego. Szczytowe działanie spazmolityczne obserwuje się po około czterech godzinach po podaniu, a efekty mogą trwać od czterech do ośmiu godzin. Początek, szczytowa odpowiedź i czas trwania działania mogą się różnić u poszczególnych pacjentów w zależności od dawki i nasilenia objawów.
Pacjenci pediatryczni
Początek, szczytowa odpowiedź i czas działania są podobne do obserwowanych u dorosłych pacjentów.
Ciągła infuzja
Działanie przeciwskurczowe preparatu LIORESAL 25 mg INTRATHECAL jest po raz pierwszy widoczne po 6 do 8 godzinach od rozpoczęcia ciągłej infuzji. Maksymalną aktywność obserwuje się w ciągu 24 do 48 godzin.
Ciągła infuzja
Brak dodatkowych informacji dla pacjentów pediatrycznych.
Farmakokinetyka LIORESAL 25 mg DOKANA
Farmakokinetyka klirensu płynu mózgowo-rdzeniowego produktu LIORESAL 25 mg INTRATHECAL, obliczona na podstawie badań bolusa dooponowego lub ciągłej infuzji, jest zbliżona do obrotu płynu mózgowo-rdzeniowego, co sugeruje, że eliminacja odbywa się przez usuwanie płynu mózgowo-rdzeniowego w dużych ilościach.
Bolus dooponowy
Po wstrzyknięciu w bolusie lędźwiowym 50 lub 100 µg produktu LIORESAL 10 mg INTRATHECAL u siedmiu pacjentów, średni okres półtrwania w fazie eliminacji z płynu mózgowo-rdzeniowego wynosił 1,51 godziny w ciągu pierwszych czterech godzin, a średni klirens płynu mózgowo-rdzeniowego wynosił około 30 ml/godzinę.
Ciągła infuzja
Średni klirens płynu mózgowo-rdzeniowego produktu LIORESAL 10 mg INTRATHECAL (wstrzyknięcie baklofenu) wynosił około 30 ml/godzinę w badaniu z udziałem dziesięciu pacjentów otrzymujących ciągłą infuzję dooponową. Oczekuje się, że jednoczesne stężenia baklofenu w osoczu podczas podawania dooponowego będą niskie (0-5 ng/ml).
Ograniczone dane farmakokinetyczne sugerują, że gradient stężenia w odcinku lędźwiowo-cyrkowym wynosi około 4:1 wzdłuż neuroosi podczas infuzji baklofenu. Opiera się to na równoczesnym pobieraniu próbek płynu mózgowo-rdzeniowego przez nakłucie zbiornika i lędźwi u 5 pacjentów otrzymujących ciągły wlew baklofenu na poziomie lędźwiowym w dawkach związanych ze skutecznością terapeutyczną; zmienność między pacjentami była duża. Gradient nie został zmieniony przez położenie.
Sześciu pacjentów pediatrycznych (w wieku 8-18 lat) otrzymujących ciągłą dooponową infuzję baklofenu w dawkach 77-400 µg/dobę miało poziom baklofenu w osoczu bliski lub niższy niż 10 ng/ml.
INFORMACJA O PACJENCIE
PrLIORESAL dokanałowe (baklofen) Iniekcja 0,05 mg/ml, 0,5 mg/ml i 2 mg/ml
Wyłącznie do wstrzykiwań dooponowych i infuzji
Niniejsza ulotka jest częścią III trzyczęściowej „Monografii produktu” opublikowanej po dopuszczeniu do sprzedaży w Kanadzie produktu LIORESAL IT i jest przeznaczona specjalnie dla konsumentów. Ta ulotka jest streszczeniem i nie powie Ci wszystkiego o LIORESAL 10mg IT. Skontaktuj się z lekarzem lub farmaceutą, jeśli masz jakiekolwiek pytania dotyczące leku.
O TYM LEKU
Do czego służy lek:
LIORESAL 25mg Intrathecal należy do grupy leków zwanych środkami zwiotczającymi mięśnie. Stosuje się go w celu zmniejszenia i łagodzenia nadmiernej sztywności i/lub skurczów występujących w różnych schorzeniach, takich jak np. stwardnienie rozsiane, choroby lub urazy rdzenia kręgowego oraz niektóre schorzenia mózgu.
Co to robi:
Roztwór jest wstrzykiwany lub podawany do przestrzeni płynowej wokół rdzenia kręgowego za pomocą specjalnej pompy, która jest wszczepiana pod skórę brzucha. Z pompy przez maleńką rurkę do przestrzeni płynowej wokół rdzenia kręgowego dostarczana jest stała ilość roztworu.
Ze względu na korzystny wpływ na skurcze mięśni i w konsekwencji łagodzenie bólu, LIORESAL Intrathecal poprawia Twoją mobilność i zdolność do samodzielnego wykonywania codziennych czynności. LIORESAL 25mg pomaga również czerpać większe korzyści z fizjoterapii.
Kiedy nie należy go używać:
Nie należy stosować leku LIORESALIT, jeśli:
- jeśli pacjent ma uczulenie (nadwrażliwość) na LIORESAL 25 mg Intrathecal lub którykolwiek z pozostałych składników leku LIORESAL 10 mg Intrathecal wymienionych poniżej.
Co to jest składnik leczniczy:
baklofen.
Jakie są składniki nielecznicze:
LIORESAL 25mg IT zawiera: chlorek sodu i wodę do wstrzykiwań
Jakie postacie dawkowania, w jakich się znajduje:
LIORESAL 25 mg dooponowo (wstrzyknięcie baklofenu) 0,05 mg/ml: Każda 1 ml ampułka zawiera 0,05 mg baklofenu do podania dooponowego.
LIORESAL Intrathecal (wstrzyknięcie baklofenu) 0,5 mg/ml: Każda ampułka 20 ml zawiera 10 mg baklofenu do podania dooponowego.
LIORESAL 25 mg Intrathecal (wstrzyknięcie baklofenu) 2 mg/ml: Każda ampułka 5 ml zawiera 10 mg baklofenu do podania dooponowego.
OSTRZEŻENIA I ŚRODKI
LIORESAL 10mg Intrathecal jest odpowiedni dla wielu, ale nie dla wszystkich pacjentów ze skurczami mięśni.
PRZED zastosowaniem leku Lioresal 25mgIT należy porozmawiać z lekarzem lub farmaceutą, jeśli:
- mieć jakąkolwiek infekcję
- masz chorobę Parkinsona lub niektóre choroby psychiczne, którym towarzyszy splątanie;
- mieć epilepsję (drgawki)
- mieć cukrzycę
- kiedykolwiek miałeś problemy z sercem
- kiedykolwiek miałeś problemy z nerkami
- masz problemy z oddychaniem
- masz ostry ból żołądka lub jelit;
- masz zaburzone krążenie krwi w mózgu
- kiedykolwiek wystąpiły nagłe epizody wysokiego ciśnienia krwi, lęku, nadmiernego pocenia się, „gęsiej skórki”, pulsującego bólu głowy i niezwykle wolnego bicia serca z powodu nadmiernej reakcji układu nerwowego na bodźce, takie jak wzdęcie pęcherza i jelit, podrażnienie i ból skóry
Jeśli którakolwiek z powyższych sytuacji dotyczy pacjenta, lekarz może nie chcieć podawać tego leku lub może chcieć podjąć specjalne środki ostrożności. Jeśli pacjent nie poinformował lekarza o żadnej z tych kwestii, należy powiedzieć mu o tym przed rozpoczęciem leczenia lekiem LIORESAL 25 mg Intrathecal.
Jeśli uważasz, że możesz być uczulony, poproś lekarza o poradę.
Prowadzenie i obsługa maszyn: LIORESAL Intrathecal może powodować senność lub zawroty głowy. Zachowaj ostrożność podczas prowadzenia samochodu lub obsługiwania maszyn lub robienia rzeczy, które wymagają szczególnej uwagi, dopóki nie poczujesz się normalnie.
INTERAKCJE Z TYM LEKIEM
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje lub ostatnio przyjmował jakiekolwiek inne leki, w tym leki ziołowe i leki wydawane bez recepty (bez recepty). Niektóre inne leki mogą wchodzić w interakcje z lekiem Lioresal 10mgIT. Lekarz może zmienić dawkowanie lub czasami odstawić jeden z leków. Jest to szczególnie ważne w przypadku następujących leków:
- inne leki na stan spastyczny
- leki na chorobę Parkinsona
- leki na padaczkę
- leki stosowane w leczeniu zaburzeń nastroju, takie jak leki przeciwdepresyjne i lit;
- leki na nadciśnienie
- inne leki działające na nerki, np. ibuprofen
- opiaty łagodzące ból
- leki nasenne lub uspokajające
- leki spowalniające centralny układ nerwowy, np. leki przeciwhistaminowe i uspokajające (niektóre z nich można kupić bez recepty)
Zawsze informuj swojego lekarza lub pielęgniarkę o wszystkich przyjmowanych lekach. Oznacza to leki, które kupiłeś sam, a także leki na receptę od lekarza.
Należy zachować ostrożność podczas picia napojów alkoholowych podczas leczenia lekiem LIORESAL 25 mg Intrathecal, ponieważ może to spowodować większą niż zwykle senność lub zawroty głowy.
WŁAŚCIWE STOSOWANIE TEGO LEKU
Zwykła dawka
LIORESAL Intrathecal może być podawany wyłącznie przez doświadczonych lekarzy przy użyciu specjalnego sprzętu medycznego. Będziesz musiał pozostać w szpitalu przynajmniej na początku leczenia.
Lekarz wstrzyknie niewielką ilość leku LIORESAL Intrathecal do rdzenia kręgowego, aby sprawdzić, czy łagodzi on skurcze mięśni. Jeśli tak, to pod Twoją skórę zostanie wszczepiona specjalna pompka. Pompa będzie podawała przez cały czas niewielką ilość leku.
Ustalenie odpowiedniej dawki leku może potrwać kilka dni, w tym czasie lekarz będzie Cię uważnie obserwował.
Następnie lekarz nadal będzie chciał Cię regularnie odwiedzać, aby sprawdzić postępy i upewnić się, że pompa działa prawidłowo.
NAJWAŻNIEJSZE JEST, ABY PRZECHOWYWAĆ TERMINY NA NAPEŁNIANIE POMPY, W PRZECIWNYM PRZYPADKU MOGĄ POWRÓCIĆ SIĘ SPAZMY, PONIEWAŻ NIE PRZYJMUJESZ WYSTARCZAJĄCEJ DAWKI LIORESAL DOKANEJ. W WYNIKU SPASTY MIĘŚNI MOŻE NIE POPRAWIAĆ LUB POGORSZYĆ.
Jeśli spastyczność mięśni nie ulega poprawie lub jeśli ponownie zaczniesz mieć skurcze, stopniowo lub nagle, natychmiast skontaktuj się z lekarzem.
Należy zapoznać się z literaturą producenta pompy, aby uzyskać informacje dotyczące właściwej pielęgnacji pompy i miejsca jej założenia w domu.
Monitorowanie podczas leczenia lekiem LIORESAL 10 mg Intrathecal
Będziesz ściśle monitorowany w pełni wyposażonym i obsadzonym personelem środowisku podczas fazy przesiewowej i okresu miareczkowania dawki bezpośrednio po wszczepieniu pompy. Będziesz regularnie oceniany pod kątem wymagań dotyczących dawkowania, możliwych skutków ubocznych lub dowodów infekcji. Sprawdzane będzie również funkcjonowanie systemu dostaw.
Ciąża i karmienie piersią
Należy poinformować lekarza, jeśli pacjentka jest w ciąży lub planuje zajść w ciążę, ponieważ leku Lioresal 25 mg Intrathecal nie należy stosować w okresie ciąży lub karmienia piersią. Przed zażyciem jakiegokolwiek leku należy zasięgnąć porady lekarza lub farmaceuty.
Lekarz omówi z pacjentką potencjalne ryzyko związane ze stosowaniem leku Lioresal 25 mg Intrathecal podczas ciąży.
Lekarz zadecyduje, czy w tych szczególnych sytuacjach pacjentka może otrzymać LIORESAL 10 mg Intrathecal. Tylko bardzo małe ilości leku Lioresal 10 mg przenikają do mleka matki. Zapytaj lekarza, czy chcesz karmić piersią.
Przedawkować
W przypadku przedawkowania narkotyków należy natychmiast skontaktować się z lekarzem, szpitalnym oddziałem ratunkowym lub regionalnym Centrum Kontroli Zatruć, nawet jeśli nie występują żadne objawy.
Oznaki przedawkowania mogą pojawić się nagle lub podstępnie, np. w wyniku nieprawidłowego działania pompy. Bardzo ważne jest, abyś Ty i osoby opiekujące się Tobą rozpoznały oznaki przedawkowania. Jeśli wystąpi którykolwiek z poniższych objawów lub ich kombinacja, należy niezwłocznie poinformować lekarza, ponieważ ilość przyjmowanego leku może być zbyt duża:
- nietypowe osłabienie mięśni (zbyt małe napięcie mięśniowe)
- senność
- zawroty głowy lub zawroty głowy
- nadmierne ślinienie
- nudności lub wymioty
- trudności w oddychaniu, drgawki lub utrata przytomności
- nienormalnie niska temperatura ciała
Pominięta dawka
Nagłe odstawienie leku Lioresal 10 mg Intrathecal może spowodować poważne problemy zdrowotne, a w rzadkich przypadkach może doprowadzić do zgonu.
Oznaki, że pompa nie działa prawidłowo lub nie dostarcza odpowiedniej ilości leków, obejmują zwiększenie lub nawrót spastyczności, swędzenie, niskie ciśnienie krwi, zawroty głowy, uczucie mrowienia, wysoką gorączkę, zmieniony stan psychiczny i sztywność mięśni lub nowe osłabienie lub paraliż mięśni. Ważne jest, aby natychmiast poinformować lekarza, jeśli wystąpi którykolwiek z powyższych objawów.
SKUTKI UBOCZNE I CO Z NIM ZROBIĆ
Podobnie jak w przypadku wszystkich leków, u pacjentów leczonych lekiem LIORESAL 25 mg Intrathecal mogą wystąpić pewne działania niepożądane, chociaż nie u każdego one wystąpią. Występują one częściej na początku leczenia podczas pobytu w szpitalu, ale mogą również wystąpić później i należy je skonsultować z lekarzem.
Bardzo powszechne: Senność, osłabienie mięśni
Wspólny: Uczucie niepokoju, uspokojenie polekowe i znużenie (wyczerpanie), osłabienie nóg, sztywność mięśni, zawroty głowy, bóle głowy, senność, nudności i (lub) wymioty, mrowienie w dłoniach i stopach, bezsenność, niewyraźna mowa, zapalenie płuc osłabienie, dreszcze, zmęczenie, ból, suchość w ustach, wysypka skórna i (lub) swędzenie, obrzęk kostek, stóp lub podudzi, opuchnięta twarz, niezwykła nerwowość lub niepokój, splątanie/dezorientacja, zaparcia, biegunka, zmniejszony apetyt, nadmierny ślinotok, gorączka/dreszcze, problemy z oddawaniem moczu, trudności seksualne.
Niezwykły: Zmiany nastroju lub umysłowe, paranoja, uczucie skrajnego szczęścia (euforia), utrata koordynacji mięśni (ataksja), nienormalnie niska temperatura ciała, utrata pamięci, ciągłe niekontrolowane ruchy gałek ocznych, zmniejszone poczucie smaku, trudności w przełykaniu, ból brzucha, wypadanie włosów, nadmierne pocenie.
Rzadki: Niepokój, nienormalnie wolne tempo oddychania.
Jeśli zauważysz jakikolwiek inny efekt, poinformuj o tym lekarza. Niektóre skutki uboczne mogą być związane z systemem dostarczania.
POWAŻNE SKUTKI UBOCZNE, JAK CZĘSTO SIĘ DZIEJĄ I CO Z NIM ZROBIĆ
To nie jest pełna lista skutków ubocznych. W przypadku wystąpienia nieoczekiwanych efektów podczas stosowania leku LIORESAL IT należy skontaktować się z lekarzem lub farmaceutą.
JAK TO PRZECHOWYWAĆ?
Ampułki LIORESAL 10mg IT przechowywać w temperaturze 15-30°C (chronić przed wysoką temperaturą). Nie zamrażać. Nie sterylizować termicznie.
Wszystkie leki przechowywać w miejscu niedostępnym i niewidocznym dla dzieci.
Ten lek jest przepisywany na konkretny problem medyczny i wyłącznie do użytku własnego. Nie dawaj innym.
Nie używaj przestarzałych leków. Wyrzuć je w bezpieczny sposób poza zasięgiem dzieci lub zanieś je do apteki, która wyrzuci je dla Ciebie.
ZGŁASZANIE PODEJRZEWANYCH SKUTKÓW UBOCZNYCH
Wszelkie podejrzewane działania niepożądane związane ze stosowaniem produktów zdrowotnych można zgłaszać do Kanadyjskiego Programu Czuwania na jeden z trzech poniższych sposobów:
- Zgłoś online na www.healthcanada.gc.ca/medeffect
- Zadzwoń pod bezpłatny numer 1-866-234-2345
- Wypełnij formularz zgłoszeniowy Canada Vigilance Reporting i:
- Faks bezpłatny pod numer 1-866-678-6789 lub
- Wyślij e-mail na adres: Canada Vigilance Program, Health Canada, Postal Locator 0701E, Ottawa, Ontario, K1A 0K9
Płatne etykiety pocztowe, formularz zgłoszeniowy Canada Vigilance Reporting oraz wytyczne dotyczące zgłaszania działań niepożądanych są dostępne w kanadyjskiej witrynie internetowej MedEffect™ pod adresem www.healthcanada.gc.ca/medeffect.
NOTATKA: Jeśli potrzebujesz informacji związanych z zarządzaniem skutkami ubocznymi, skontaktuj się z lekarzem. Kanadyjski Program Czujności nie zapewnia porad medycznych.
WIĘCEJ INFORMACJI
Ten dokument oraz pełna monografia produktu, przygotowana dla pracowników służby zdrowia, można znaleźć pod adresem: http://www.novartis.ca lub kontaktując się ze sponsorem, Novartis Pharmaceuticals Canada Inc, pod adresem: 1-800-363-8883
