Abilify 10mg, 15mg, 20mg Aripiprazole Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.

Co to jest Abilify 20mg i jak się go stosuje?
Abilify to lek na receptę stosowany w leczeniu objawów schizofrenii, choroby afektywnej dwubiegunowej typu I (depresji maniakalnej) i ciężkiej depresji. Abilify 10mg może być stosowany samodzielnie lub z innymi lekami. Abilify to środek przeciwpsychotyczny, przeciwmaniakalny.
- Nie wiadomo, czy Abilify jest bezpieczny i skuteczny u dzieci w wieku poniżej 6 lat.
Jakie są możliwe skutki uboczne Abilify 15mg?
Abilify 15mg może powodować poważne skutki uboczne, w tym:
- silne pobudzenie lub stres,
- uczucie niepokoju,
- drżenie lub niekontrolowane ruchy oczu, ust, języka, twarzy, rąk lub nóg,
- maskowaty wygląd twarzy,
- kłopoty z połykaniem,
- problemy z mową,
- drgawki (drgawki),
- myśli samobójcze lub samookaleczenia,
- sztywne lub sztywne mięśnie,
- wysoka gorączka,
- wyzysk,
- dezorientacja,
- szybkie lub nierówne bicie serca,
- drżenie (drżenie),
- uczucie oszołomienia,
- dreszcze,
- ból gardła,
- owrzodzenia jamy ustnej,
- owrzodzenia skóry,
- kaszel,
- trudności w oddychaniu,
- zwiększone pragnienie,
- zwiększone oddawanie moczu,
- suchość w ustach i
- owocowy zapach oddechu
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Abilify 20mg to:
- niekontrolowane ruchy mięśni,
- lęk,
- uczucie niepokoju,
- przybranie na wadze,
- mdłości,
- wymioty,
- zaparcie,
- zwiększony apetyt,
- ból głowy,
- zawroty głowy,
- senność,
- czuć się zmęczonym,
- problemy ze snem (bezsenność),
- zatkany nos i
- ból gardła
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Abilify. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OSTRZEŻENIE
ZWIĘKSZONA ŚMIERTELNOŚĆ U PACJENTÓW W STARSZYM WIEKU Z PSYCHOZĄ ZWIĄZANĄ Z DEMENCJAMI ORAZ MYŚLAMI I ZACHOWANIAMI SAMOBÓJCZYMI Z LEKAMI PRZECIWDEPRESYJNYMI
Pacjenci w podeszłym wieku z psychozą otępienną leczeni lekami przeciwpsychotycznymi są narażeni na zwiększone ryzyko zgonu. ABILIFY 20mg nie jest zatwierdzony do leczenia pacjentów z psychozą związaną z otępieniem [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
badaniach krótkoterminowych leki przeciwdepresyjne zwiększały ryzyko myśli i zachowań samobójczych u dzieci, młodzieży i młodych dorosłych. Badania te nie wykazały wzrostu ryzyka myśli i zachowań samobójczych podczas stosowania leków przeciwdepresyjnych u pacjentów w wieku powyżej 24 lat; wystąpiło zmniejszenie ryzyka przy stosowaniu leków przeciwdepresyjnych u pacjentów w wieku 65 lat i starszych [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
U pacjentów w każdym wieku, którzy rozpoczęli terapię przeciwdepresyjną, należy uważnie monitorować pogorszenie oraz pojawienie się myśli i zachowań samobójczych. Poinformuj rodziny i opiekunów o potrzebie ścisłej obserwacji i komunikacji z lekarzem [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
OPIS
Arypiprazol jest lekiem psychotropowym, który jest dostępny jako tabletki ABILIFY® (arypiprazol), ABILIFY DISCMELT® (arypiprazol) tabletki rozpadające się doustnie, ABILIFY® (arypiprazol) roztwór doustny oraz ABILIFY® (arypiprazol) do wstrzykiwań, roztwór do wstrzykiwań domięśniowych. Arypiprazol to 7-[4-[4-(2,3dichlorofenylo)-1-piperazynylo]butoksy]-3,4-dihydrokarbostyryl. Wzór empiryczny to C23H27Cl2N3O2, a jego masa cząsteczkowa to 448,38. Struktura chemiczna to:
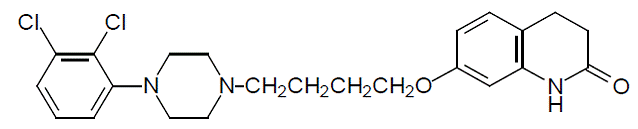
Tabletki ABILIFY są dostępne w mocach 2 mg, 5 mg, 10 mg, 15 mg, 20 mg i 30 mg. Składniki nieaktywne obejmują skrobię kukurydzianą, hydroksypropylocelulozę, monohydrat laktozy, stearynian magnezu i celulozę mikrokrystaliczną. Barwniki obejmują tlenek żelaza (żółty lub czerwony) i FD&C Blue No. 2 Aluminium Lake.
Tabletki ulegające rozpadowi w jamie ustnej ABILIFY 20 mg DISCMELT są dostępne w mocach 10 mg i 15 mg. Nieaktywne składniki to acesulfam potasu, aspartam, krzemian wapnia, kroskarmeloza sodowa, krospowidon, krem waniliowy (naturalne i sztuczne aromaty), stearynian magnezu, celuloza mikrokrystaliczna, dwutlenek krzemu, kwas winowy i ksylitol. Barwniki obejmują tlenek żelaza (żółty lub czerwony) i FD&C Blue No. 2 Aluminium Lake.
ABILIFY Oral Solution to przezroczysty, bezbarwny do jasnożółtego roztwór dostępny w stężeniu 1 mg/ml. Nieaktywne składniki tego roztworu obejmują wersenian disodowy, fruktozę, glicerynę, kwas dl-mlekowy, metyloparaben, glikol propylenowy, propyloparaben, wodorotlenek sodu, sacharozę i wodę oczyszczoną. Roztwór doustny jest aromatyzowany naturalnym pomarańczowym kremem i innymi naturalnymi aromatami.
ABILIFY do wstrzykiwań jest dostępny w fiolkach jednodawkowych jako gotowy do użycia, przejrzysty, bezbarwny, jałowy roztwór wodny o stężeniu 9,75 mg/1,3 ml (7,5 mg/ml) wyłącznie do podania domięśniowego. Nieaktywne składniki tego roztworu obejmują 199,5 mg eteru sulfobutylowego β-cyklodekstryny (SBECD), 10,4 mg kwasu winowego, qs do pH 4,3 wodorotlenku sodu i qs do 1,33 ml wody do wstrzykiwań.
WSKAZANIA
ABILIFY Tabletki doustne, tabletki ulegające rozpadowi w jamie ustnej i roztwór doustny są wskazane w leczeniu:
- Schizofrenia [patrz Studia kliniczne ]
- Ostre leczenie epizodów maniakalnych i mieszanych związanych z zaburzeniem afektywnym dwubiegunowym typu I [patrz Studia kliniczne ]
- Leczenie wspomagające dużych zaburzeń depresyjnych [patrz Studia kliniczne ]
- Drażliwość związana z zaburzeniami autystycznymi [patrz Studia kliniczne ]
- Leczenie zaburzenia Tourette'a [patrz Studia kliniczne ]
ABILIFY Wstrzyknięcie jest wskazane w leczeniu:
- Pobudzenie związane ze schizofrenią lub manią dwubiegunową [patrz Studia kliniczne ]
DAWKOWANIE I SPOSÓB PODAWANIA
Schizofrenia
Dorośli ludzie
Zalecana dawka początkowa i docelowa preparatu ABILIFY to 10 lub 15 mg/dobę podawane w schemacie raz na dobę, niezależnie od posiłków. ABILIFY był systematycznie oceniany i wykazano, że jest skuteczny w zakresie dawek od 10 do 30 mg/dzień, przy podawaniu w postaci tabletki; jednakże dawki wyższe niż 10 lub 15 mg/dzień nie były bardziej skuteczne niż 10 lub 15 mg/dzień. Zasadniczo nie należy zwiększać dawki przed upływem 2 tygodni, czasu potrzebnego do osiągnięcia stanu stacjonarnego [patrz Studia kliniczne ].
Leczenie podtrzymujące: Utrzymanie skuteczności w schizofrenii wykazano w badaniu obejmującym pacjentów ze schizofrenią, u których objawy były stabilne, przyjmując inne leki przeciwpsychotyczne przez okres 3 miesięcy lub dłuższy. Pacjenci ci zostali odstawieni od tych leków i przydzieleni losowo do grupy ABILIFY 15 mg/dobę lub placebo i obserwowani pod kątem nawrotu [patrz Studia kliniczne ]. Pacjenci powinni być okresowo poddawani ponownej ocenie w celu ustalenia dalszej potrzeby leczenia podtrzymującego.
Młodzież
Zalecana dawka docelowa ABILIFY wynosi 10 mg/dobę. Arypiprazol badano u młodzieży w wieku od 13 do 17 lat ze schizofrenią w dawkach dobowych 10 mg i 30 mg. Początkowa dawka dobowa postaci tabletki u tych pacjentów wynosiła 2 mg, którą zwiększano do 5 mg po 2 dniach i do dawki docelowej 10 mg po 2 dodatkowych dniach. Kolejne zwiększanie dawki należy podawać w odstępach co 5 mg. Nie wykazano, aby dawka 30 mg/dobę była bardziej skuteczna niż dawka 10 mg/dobę. ABILIFY można podawać niezależnie od posiłków [patrz Studia kliniczne ]. Pacjenci powinni być okresowo poddawani ponownej ocenie w celu ustalenia potrzeby leczenia podtrzymującego.
Przejście z innych leków przeciwpsychotycznych
Nie ma systematycznie gromadzonych danych dotyczących konkretnie zmiany leczenia pacjentów ze schizofrenią z innych leków przeciwpsychotycznych na ABILIFY 20 mg lub dotyczących jednoczesnego podawania z innymi lekami przeciwpsychotycznymi. O ile natychmiastowe przerwanie wcześniejszego leczenia przeciwpsychotycznego może być akceptowalne dla niektórych pacjentów ze schizofrenią, o tyle bardziej odpowiednie może być odstawienie bardziej stopniowe dla innych. We wszystkich przypadkach należy zminimalizować okres nakładania się leków przeciwpsychotycznych.
Zaburzenie dwubiegunowe typu I
Ostre leczenie epizodów maniakalnych i mieszanych
Dorośli ludzie
Zalecana dawka początkowa u dorosłych to 15 mg raz na dobę w monoterapii i 10 do 15 mg raz na dobę w terapii wspomagającej z litem lub walproinianem. ABILIFY 10mg można podawać niezależnie od posiłków. Zalecana dawka docelowa ABILIFY to 15 mg/dobę, w monoterapii lub jako terapia wspomagająca z litem lub walproinianem. Dawkę można zwiększyć do 30 mg/dobę w zależności od odpowiedzi klinicznej. Bezpieczeństwo dawek powyżej 30 mg/dobę nie było oceniane w badaniach klinicznych.
Pediatria
Zalecana dawka początkowa u pacjentów pediatrycznych (10 do 17 lat) w monoterapii wynosi 2 mg/dobę, ze zwiększaniem dawki do 5 mg/dobę po 2 dniach i dawką docelową 10 mg/dobę po 2 dodatkowych dniach. Zalecane dawkowanie w terapii wspomagającej z litem lub walproinianem jest takie samo. Kolejne zwiększanie dawki, w razie potrzeby, należy podawać w odstępach co 5 mg/dobę. ABILIFY można podawać niezależnie od posiłków [patrz Studia kliniczne ].
Leczenie wspomagające ciężkiego zaburzenia depresyjnego
Dorośli ludzie
Zalecana dawka początkowa preparatu ABILIFY jako leczenia wspomagającego u pacjentów już przyjmujących lek przeciwdepresyjny wynosi od 2 do 5 mg/dobę. Zalecany zakres dawkowania wynosi od 2 do 15 mg/dzień. Dostosowanie dawki do 5 mg/dobę powinno następować stopniowo, w odstępach nie krótszych niż 1 tydzień [patrz Studia kliniczne ]. Pacjenci powinni być okresowo poddawani ponownej ocenie w celu ustalenia dalszej potrzeby leczenia podtrzymującego.
Drażliwość związana z zaburzeniami autystycznymi
Pacjenci pediatryczni (6 do 17 lat)
Zalecany zakres dawkowania w leczeniu pacjentów pediatrycznych z drażliwością związaną z zaburzeniami autystycznymi wynosi od 5 do 15 mg/dobę.
Dawkowanie należy rozpocząć od 2 mg/dobę. Dawkę należy zwiększyć do 5 mg/dobę, a następnie w razie potrzeby zwiększyć do 10 lub 15 mg/dobę. Dostosowanie dawki do 5 mg/dobę powinno następować stopniowo, w odstępach nie krótszych niż 1 tydzień [patrz Studia kliniczne ]. Pacjenci powinni być okresowo poddawani ponownej ocenie w celu ustalenia dalszej potrzeby leczenia podtrzymującego.
Zaburzenie Tourette'a
Pacjenci pediatryczni (6 do 18 lat)
Zalecany zakres dawkowania w przypadku zaburzenia Tourette'a wynosi od 5 do 20 mg/dzień.
W przypadku pacjentów o masie ciała poniżej 50 kg dawkowanie należy rozpocząć od 2 mg/dobę, a po 2 dniach dawkę docelową 5 mg/dobę. U pacjentów, u których nie uzyskano optymalnej kontroli tików, dawkę można zwiększyć do 10 mg/dobę. Dostosowanie dawkowania powinno następować stopniowo w odstępach nie krótszych niż 1 tydzień.
U pacjentów o masie ciała 50 kg lub większej dawkę należy rozpocząć od 2 mg/dobę przez 2 dni, a następnie zwiększać do 5 mg/dobę przez 5 dni, przy czym w 8. dniu dawka docelowa powinna wynosić 10 mg/dobę. zwiększone do 20 mg/dobę u pacjentów, którzy nie osiągają optymalnej kontroli tików. Dostosowanie dawkowania powinno następować stopniowo, w przyrostach o 5 mg/dobę w odstępach nie krótszych niż 1 tydzień. [Widzieć Studia kliniczne ].
Pacjenci powinni być okresowo poddawani ponownej ocenie w celu ustalenia dalszej potrzeby leczenia podtrzymującego.
Pobudzenie związane ze schizofrenią lub manią dwubiegunową (wstrzyknięcie domięśniowe)
Dorośli ludzie
Zalecana dawka u tych pacjentów wynosi 9,75 mg. Zalecany zakres dawkowania to 5,25 do 15 mg. Nie wykazano dodatkowych korzyści dla 15 mg w porównaniu do 9,75 mg. Można rozważyć mniejszą dawkę 5,25 mg, jeśli uzasadniają to czynniki kliniczne. Jeśli pobudzenie, które wymaga podania drugiej dawki, utrzymuje się po podaniu dawki początkowej, można podać dawki skumulowane do 30 mg/dobę. Jednak skuteczność powtarzanych dawek ABILIFY 10 mg do wstrzykiwań u pobudzonych pacjentów nie była systematycznie oceniana w kontrolowanych badaniach klinicznych. Bezpieczeństwo całkowitych dawek dobowych większych niż 30 mg lub wstrzyknięć podawanych częściej niż co 2 godziny nie zostało odpowiednio ocenione w badaniach klinicznych [patrz Studia kliniczne ].
Jeśli trwające leczenie ABILIFY jest wskazane klinicznie, doustny ABILIFY w zakresie od 10 do 30 mg/dobę powinien jak najszybciej zastąpić wstrzyknięcie ABILIFY [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Podawanie wstrzyknięcia ABILIFY
Aby podać ABILIFY 10 mg do wstrzykiwań, pobrać wymaganą objętość roztworu do strzykawki, jak pokazano w Tabeli 1. Wszelkie niewykorzystane części należy wyrzucić.
ABILIFY Injection jest przeznaczony wyłącznie do podawania domięśniowego. Nie podawać dożylnie ani podskórnie. Wstrzykiwać powoli, głęboko w masę mięśniową.
Produkty lecznicze do podawania pozajelitowego należy przed podaniem skontrolować wzrokowo pod kątem obecności cząstek stałych i przebarwień, o ile pozwala na to roztwór i pojemnik.
Dostosowanie dawkowania dla rozważań dotyczących cytochromu P450
Dostosowanie dawkowania jest zalecane u pacjentów, u których wiadomo, że słabo metabolizują CYP2D6 oraz u pacjentów przyjmujących jednocześnie inhibitory CYP3A4 lub inhibitory CYP2D6 lub silne induktory CYP3A4 (patrz Tabela 2). Gdy jednocześnie podawany lek zostanie wycofany z terapii skojarzonej, dawkę ABILIFY 10 mg należy dostosować do pierwotnego poziomu. Po odstawieniu jednocześnie podawanego induktora CYP3A4 dawkę ABILIFY należy zmniejszyć do pierwotnego poziomu w ciągu 1 do 2 tygodni. Pacjenci, którzy mogą otrzymywać połączenie silnych, umiarkowanych i słabych inhibitorów CYP3A4 i CYP2D6 (np. silny inhibitor CYP3A4 i umiarkowany inhibitor CYP2D6 lub umiarkowany inhibitor CYP3A4 z umiarkowanym inhibitorem CYP2D6), dawkowanie można zmniejszyć do jednego – początkowo ćwierć (25%) zwykle stosowanej dawki, a następnie dostosowywać w celu uzyskania korzystnej odpowiedzi klinicznej.
Jeśli wspomagająco podaje się ABILIFY pacjentom z ciężkimi zaburzeniami depresyjnymi, ABILIFY 10 mg należy podawać bez zmiany dawkowania, jak określono w Dawkowanie i sposób podawania (2.3).
Dawkowanie roztworu doustnego
Roztwór doustny można zastąpić tabletkami w ilości mg na mg do poziomu dawki 25 mg. Pacjenci otrzymujący tabletki 30 mg powinni otrzymać 25 mg roztworu [patrz FARMAKOLOGIA KLINICZNA ].
Dawkowanie tabletek rozpadających się w jamie ustnej
Dawkowanie ABILIFY 10 mg tabletki ulegające rozpadowi w jamie ustnej jest takie samo jak w przypadku tabletek doustnych [patrz powyżej Sekcje ].
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Tabletki ABILIFY® (arypiprazol) są dostępne jak opisano w Tabeli 3.
Tabletki ABILIFY DISCMELT® (arypiprazol) ulegające rozpadowi w jamie ustnej są dostępne zgodnie z opisem w Tabeli 4.
ABILIFY® (arypiprazol) roztwór doustny (1 mg/ml) jest przezroczystym, bezbarwnym do jasnożółtego roztworem, dostarczanym w butelkach zabezpieczonych przed dostępem dzieci wraz ze skalibrowanym doustnym kubkiem dozującym.
ABILIFY® (arypiprazol) do wstrzykiwań domięśniowych jest przezroczystym, bezbarwnym roztworem dostępnym jako gotowy do użycia roztwór o stężeniu 9,75 mg/1,3 ml (7,5 mg/ml) w przezroczystych fiolkach ze szkła typu 1.
Składowania i stosowania
ABILIFY® (arypiprazol) Tabletki posiadają oznaczenia z jednej strony i są dostępne w wytrzymałościach i opakowaniach wymienionych w Tabeli 32.
ABILIFY 15mg DISCMELT® (arypiprazol) tabletki rozpadające się w jamie ustnej to okrągłe tabletki z oznaczeniami po obu stronach. ABILIFY 15mg DISCMELT jest dostępny w mocach i opakowaniach wymienionych w Tabeli 33.
ABILIFY® (arypiprazol) roztwór doustny (1 mg/ml) jest dostarczany w butelkach zabezpieczonych przed dostępem dzieci wraz ze skalibrowanym doustnym kubkiem dozującym. ABILIFY 20 mg roztwór doustny jest dostępny w następujący sposób:
Butelka 150 ml NDC 59148-013-15
ABILIFY® (arypiprazol) do wstrzykiwań domięśniowych jest dostępny jako gotowy do użycia roztwór o stężeniu 9,75 mg/1,3 ml (7,5 mg/ml) w przezroczystych fiolkach ze szkła typu 1 w następujący sposób:
Fiolka jednodawkowa 9,75 mg/1,3 ml NDC 59148-016-65
Magazynowanie
Tablety
Przechowywać w 25°C (77°F); dopuszczalne odchylenia od 15°C do 30°C (59°F do 86°F) [patrz Temperatura pokojowa kontrolowana przez USP ].
Rozwiązanie doustne
Przechowywać w 25°C (77°F); dopuszczalne odchylenia od 15°C do 30°C (59°F do 86°F) [patrz Temperatura pokojowa kontrolowana przez USP ]. Otwarte butelki ABILIFY roztwór doustny mogą być używane przez okres do 6 miesięcy po otwarciu, ale nie po upływie daty ważności podanej na butelce. Butelkę i jej zawartość należy wyrzucić po upływie terminu ważności.
Zastrzyk
Przechowywać w 25°C (77°F); dopuszczalne odchylenia od 15°C do 30°C (59°F do 86°F) [patrz Temperatura pokojowa kontrolowana przez USP ]. Chronić przed światłem przechowując w oryginalnym pojemniku. Przechowywać w kartoniku do czasu użycia.
Dystrybucją i sprzedażą zajmuje się Otsuka America Pharmaceutical, Inc., Rockville, MD 20850 USA. Otsuka America Pharmaceutical, Inc. Wersja sie 2019
SKUTKI UBOCZNE
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Następujące działania niepożądane omówiono bardziej szczegółowo w innych punktach oznakowania:
- Zwiększona śmiertelność u starszych pacjentów z psychozą związaną z demencją [patrz OSTRZEŻENIE W PUDEŁKU oraz OSTRZEŻENIA I ŚRODKI ]
- Zdarzenia niepożądane naczyniowo-mózgowe, w tym udar [patrz OSTRZEŻENIA I ŚRODKI ]
- Myśli i zachowania samobójcze u dzieci, młodzieży i młodych dorosłych [zobacz OSTRZEŻENIE W PUDEŁKU oraz OSTRZEŻENIA I ŚRODKI ]
- Złośliwy Zespół Neuroleptyczny (NMS) [patrz OSTRZEŻENIA I ŚRODKI ]
- Późne dyskinezy [patrz OSTRZEŻENIA I ŚRODKI ]
- Zmiany metaboliczne [patrz OSTRZEŻENIA I ŚRODKI ]
- Patologiczny hazard i inne kompulsywne zachowania [zobacz OSTRZEŻENIA I ŚRODKI ]
- Niedociśnienie ortostatyczne [patrz OSTRZEŻENIA I ŚRODKI ]
- Upadki [patrz OSTRZEŻENIA I ŚRODKI ]
- leukopenia, neutropenia i agranulocytoza [patrz OSTRZEŻENIA I ŚRODKI ]
- Drgawki/konwulsje [patrz OSTRZEŻENIA I ŚRODKI ]
- Potencjał upośledzenia funkcji poznawczych i motorycznych [patrz OSTRZEŻENIA I ŚRODKI ]
- Regulacja temperatury ciała [patrz OSTRZEŻENIA I ŚRODKI ]
- samobójstwo [patrz OSTRZEŻENIA I ŚRODKI ]
- Dysfagia [patrz OSTRZEŻENIA I ŚRODKI ]
Najczęstszymi działaniami niepożądanymi u dorosłych pacjentów w badaniach klinicznych (≥10%) były nudności, wymioty, zaparcia, ból głowy, zawroty głowy, akatyzja, lęk, bezsenność i niepokój.
Najczęstszymi działaniami niepożądanymi w pediatrycznych badaniach klinicznych (≥10%) były senność, ból głowy, wymioty, zaburzenia pozapiramidowe, zmęczenie, zwiększony apetyt, bezsenność, nudności, zapalenie nosogardzieli i zwiększenie masy ciała.
ABILIFY oceniano pod kątem bezpieczeństwa u 13 543 dorosłych pacjentów, którzy uczestniczyli w badaniach klinicznych po podaniu wielokrotnym w schizofrenii, chorobie afektywnej dwubiegunowej, dużej depresji, otępieniu typu Alzheimera, chorobie Parkinsona i alkoholizmie, i którzy mieli około 7619 pacjentolat ekspozycja na doustny ABILIFY 10 mg i 749 pacjentów z ekspozycją na wstrzyknięcie ABILIFY. Łącznie 3390 pacjentów było leczonych doustnym ABILIFY przez co najmniej 180 dni, a 1933 pacjentów leczonych doustnym ABILIFY miało co najmniej 1 rok ekspozycji.
Bezpieczeństwo ABILIFY 15 mg zostało ocenione pod kątem bezpieczeństwa u 1686 pacjentów (od 6 do 18 lat), którzy uczestniczyli w badaniach klinicznych z wielokrotnymi dawkami w schizofrenii, mania dwubiegunowej, zaburzeniach autystycznych lub zaburzeniu Tourette'a i którzy mieli około 1342 pacjento-lat ekspozycji na doustny ABILIFY . Łącznie 959 pacjentów pediatrycznych było leczonych doustnie ABILIFY przez co najmniej 180 dni, a 556 pacjentów pediatrycznych leczonych doustną ABILIFY 10 mg miało co najmniej 1 rok ekspozycji.
Warunki i czas trwania leczenia ABILIFY (monoterapia i terapia wspomagająca lekami przeciwdepresyjnymi lub lekami stabilizującymi nastrój) obejmowały (w nakładających się kategoriach) podwójnie ślepe, porównawcze i nieporównawcze badania otwarte, badania szpitalne i ambulatoryjne, badania z zastosowaniem stałej i elastycznej dawki, oraz ekspozycja krótko- i długoterminowa.
Doświadczenie w badaniach klinicznych
Dorośli pacjenci ze schizofrenią
Poniższe wyniki są oparte na puli pięciu badań kontrolowanych placebo (cztery 4-tygodniowe i jedno 6-tygodniowe), w których ABILIFY 15 mg podawano doustnie w dawkach od 2 do 30 mg/dobę.
Powszechnie obserwowane działania niepożądane
Jedynym często obserwowanym działaniem niepożądanym związanym ze stosowaniem ABILIFY 20 mg u pacjentów ze schizofrenią (zapadalność 5% lub większa i częstość występowania ABILIFY co najmniej dwukrotnie większa niż w przypadku placebo) była akatyzja (ABILIFY 8%; placebo 4%).
Dorośli pacjenci z manią afektywną dwubiegunową
Monoterapia
Poniższe wyniki są oparte na puli 3-tygodniowych, kontrolowanych placebo badań klinicznych dotyczących manii dwubiegunowej, w których ABILIFY 15 mg podawano doustnie w dawkach 15 lub 30 mg/dobę.
Powszechnie obserwowane działania niepożądane
Często obserwowane działania niepożądane związane ze stosowaniem ABILIFY u pacjentów z manią afektywną dwubiegunową (częstość występowania 5% lub większa i częstość występowania ABILIFY 15 mg co najmniej dwukrotnie większa niż w przypadku placebo) przedstawiono w Tabeli 16.
Mniej częste działania niepożądane u dorosłych
W Tabeli 17 wymieniono łączną częstość występowania, zaokrągloną do najbliższego procentu, działań niepożądanych, które wystąpiły podczas ostrej terapii (do 6 tygodni w schizofrenii i do 3 tygodni w manii dwubiegunowej), w tym tylko te reakcje, które wystąpiły w 2% lub więcej przypadków pacjentów leczonych ABILIFY (dawki ≥2 mg/dobę) i dla których częstość występowania u pacjentów leczonych ABILIFY 20 mg była większa niż częstość występowania u pacjentów otrzymujących placebo w połączonym zestawie danych.
Badanie podgrup populacji nie ujawniło żadnych wyraźnych dowodów na występowanie zróżnicowanej częstości występowania działań niepożądanych ze względu na wiek, płeć lub rasę.
Dorośli pacjenci z terapią wspomagającą z dwubiegunową manią
Poniższe wyniki są oparte na badaniu kontrolowanym placebo z udziałem dorosłych pacjentów z chorobą afektywną dwubiegunową, w którym ABILIFY 15 mg podawano w dawkach 15 lub 30 mg/dobę jako terapia wspomagająca z litem lub walproinianem.
Działania niepożądane związane z przerwaniem leczenia
W badaniu z udziałem pacjentów, którzy już tolerowali lit lub walproinian w monoterapii, częstość przerwania leczenia z powodu działań niepożądanych wyniosła 12% u pacjentów leczonych wspomagającym ABILIFY w porównaniu do 6% u pacjentów otrzymujących uzupełniające placebo. Najczęstszymi działaniami niepożądanymi związanymi z przerwaniem leczenia w leczeniu uzupełniającym ABILIFY w porównaniu z pacjentami otrzymującymi placebo były akatyzja (odpowiednio 5% i 1%) i drżenie (odpowiednio 2% i 1%).
Powszechnie obserwowane działania niepożądane
Często obserwowanymi działaniami niepożądanymi związanymi ze skojarzonym stosowaniem ABILIFY i litu lub walproinianu u pacjentów z manią afektywną dwubiegunową (częstość występowania 5% lub większa i częstość co najmniej dwukrotnie większa niż w przypadku dodatkowego placebo) to: akatyzja, bezsenność i zaburzenia pozapiramidowe.
Mniej częste działania niepożądane u dorosłych pacjentów leczonych terapią wspomagającą w chorobie afektywnej dwubiegunowej
W tabeli 18 wymieniono częstość występowania, zaokrągloną do najbliższego procentu, działań niepożądanych, które wystąpiły podczas ostrego leczenia (do 6 tygodni), w tym tylko te reakcje, które wystąpiły u 2% lub więcej pacjentów leczonych wspomagającym ABILIFY (dawki 15 lub 30 mg/dobę) i litu lub walproinianu i dla których częstość występowania u pacjentów leczonych tą kombinacją była większa niż częstość występowania u pacjentów otrzymujących placebo z litem lub walproinianem.
Pacjenci pediatryczni (od 13 do 17 lat) ze schizofrenią
Poniższe wyniki są oparte na jednym 6-tygodniowym badaniu kontrolowanym placebo, w którym ABILIFY podawano doustnie w dawkach od 2 do 30 mg/dobę.
Działania niepożądane związane z przerwaniem leczenia
Częstość przerwania leczenia z powodu działań niepożądanych pomiędzy pacjentami pediatrycznymi leczonymi ABILIFY i placebo (13 do 17 lat) wynosiła odpowiednio 5% i 2%.
Powszechnie obserwowane działania niepożądane
Często obserwowanymi działaniami niepożądanymi związanymi ze stosowaniem ABILIFY 10 mg u nastoletnich pacjentów ze schizofrenią (częstość występowania 5% lub większa i częstość występowania ABILIFY co najmniej dwukrotnie większa niż w przypadku placebo) to zaburzenia pozapiramidowe, senność i drżenie.
Pacjenci pediatryczni (od 10 do 17 lat) z manią afektywną dwubiegunową
Poniższe wyniki są oparte na jednym 4-tygodniowym badaniu kontrolowanym placebo, w którym ABILIFY podawano doustnie w dawkach 10 lub 30 mg/dobę.
Działania niepożądane związane z przerwaniem leczenia
Częstość przerwania leczenia z powodu działań niepożądanych pomiędzy pacjentami pediatrycznymi (od 10 do 17 lat) leczonymi ABILIFY i placebo wynosiła odpowiednio 7% i 2%.
Powszechnie obserwowane działania niepożądane
Często obserwowane działania niepożądane związane ze stosowaniem ABILIFY 20 mg u dzieci z manią afektywną dwubiegunową (częstość występowania 5% lub większa i częstość występowania ABILIFY co najmniej dwukrotnie większa niż w przypadku placebo) przedstawiono w Tabeli 19.
Pacjenci pediatryczni (od 6 do 17 lat) z zaburzeniami autystycznymi
Poniższe wyniki oparte są na dwóch 8-tygodniowych badaniach kontrolowanych placebo, w których ABILIFY 20 mg podawano doustnie w dawkach od 2 do 15 mg/dobę.
Działania niepożądane związane z przerwaniem leczenia
Częstość przerwania leczenia z powodu działań niepożądanych pomiędzy pacjentami pediatrycznymi (od 6 do 17 lat) leczonymi ABILIFY i placebo wynosiła odpowiednio 10% i 8%.
Powszechnie obserwowane działania niepożądane
Często obserwowane działania niepożądane związane ze stosowaniem ABILIFY u pacjentów pediatrycznych z zaburzeniami autystycznymi (częstość występowania 5% lub większa i częstość występowania ABILIFY 10 mg co najmniej dwukrotnie większa niż w przypadku placebo) przedstawiono w Tabeli 20.
Pacjenci pediatryczni (od 6 do 18 lat) z chorobą Tourette'a
Poniższe wyniki są oparte na jednym 8-tygodniowym i jednym 10-tygodniowym badaniu kontrolowanym placebo, w którym ABILIFY 15 mg podawano doustnie w dawkach od 2 do 20 mg/dobę.
Działania niepożądane związane z przerwaniem leczenia
Częstość przerwania leczenia z powodu działań niepożądanych pomiędzy pacjentami pediatrycznymi (od 6 do 18 lat) leczonymi ABILIFY i placebo wynosiła odpowiednio 7% i 1%.
Powszechnie obserwowane działania niepożądane
Często obserwowane działania niepożądane związane ze stosowaniem ABILIFY u pacjentów pediatrycznych z zespołem Tourette'a (częstość występowania 5% lub większa i częstość występowania ABILIFY 10 mg co najmniej dwukrotnie większa niż w przypadku placebo) przedstawiono w Tabeli 21.
Mniej częste działania niepożądane u pacjentów pediatrycznych (6-18 lat) ze schizofrenią, manią dwubiegunową, zaburzeniem autystycznym lub zaburzeniem Tourette'a
tabeli 22 wymieniono łączną częstość występowania, zaokrągloną do najbliższego procentu, działań niepożądanych, które wystąpiły podczas ostrej terapii (do 6 tygodni w schizofrenii, do 4 tygodni w maniach dwubiegunowych, do 8 tygodni w zaburzeniu autystycznym i do 10 tygodni w zaburzeniu Tourette'a), w tym tylko te reakcje, które wystąpiły u 2% lub więcej pacjentów pediatrycznych leczonych ABILIFY (dawki ≥2 mg/dobę) i dla których częstość występowania u pacjentów leczonych ABILIFY 10 mg była większa niż częstość występowania u pacjentów leczonych placebo.
Dorośli pacjenci otrzymujący ABILIFY jako leczenie wspomagające ciężkiego zaburzenia depresyjnego
Poniższe wyniki są oparte na puli dwóch kontrolowanych placebo badań pacjentów z ciężkimi zaburzeniami depresyjnymi, w których ABILIFY 20 mg podawano w dawkach od 2 mg do 20 mg jako leczenie uzupełniające do kontynuowanej terapii przeciwdepresyjnej.
Działania niepożądane związane z przerwaniem leczenia
Częstość przerwania leczenia z powodu działań niepożądanych wynosiła 6% u pacjentów otrzymujących dodatkowo ABILIFY i 2% u pacjentów otrzymujących dodatkowo placebo.
Powszechnie obserwowane działania niepożądane
Często obserwowanymi działaniami niepożądanymi związanymi ze stosowaniem uzupełniającego leku ABILIFY 15 mg u pacjentów z ciężkimi zaburzeniami depresyjnymi (częstość występowania 5% lub większa i częstość występowania ABILIFY 15 mg co najmniej dwukrotnie większa niż w przypadku placebo) to: akatyzja, niepokój, bezsenność, zaparcia, zmęczenie i rozmazany obraz.
Mniej częste działania niepożądane u dorosłych pacjentów z dużym zaburzeniem depresyjnym
Tabeli 23 wymieniono łączną częstość występowania, zaokrągloną do najbliższego procentu, działań niepożądanych, które wystąpiły podczas ostrej terapii (do 6 tygodni), w tym tylko te działania niepożądane, które wystąpiły u 2% lub więcej pacjentów leczonych wspomagającym leczeniem ABILIFY (dawki ≥2 mg/dobę) i dla których częstość występowania u pacjentów leczonych uzupełniającym preparatem ABILIFY 10 mg była większa niż częstość występowania u pacjentów leczonych uzupełniającym placebo w połączonym zbiorze danych.
Pacjenci z pobudzeniem związanym ze schizofrenią lub manią dwubiegunową (wstrzyknięcie domięśniowe)
Poniższe wyniki są oparte na puli trzech kontrolowanych placebo badań pacjentów z pobudzeniem związanym ze schizofrenią lub manią afektywną dwubiegunową, w których ABILIFY 20 mg podawano w dawkach od 5,25 mg do 15 mg.
Powszechnie obserwowane działania niepożądane
Wystąpiło jedno często obserwowane działanie niepożądane (nudności) związane ze stosowaniem ABILIFY 10 mg do wstrzykiwań u pacjentów z pobudzeniem związanym ze schizofrenią i manią afektywną dwubiegunową (częstość występowania 5% lub większa i częstość występowania ABILIFY 20 mg co najmniej dwukrotnie większa niż w przypadku placebo).
Mniej częste działania niepożądane u pacjentów z pobudzeniem związanym ze schizofrenią lub manią dwubiegunową
W Tabeli 24 wymieniono łączną częstość występowania, zaokrągloną do najbliższego procentu, działań niepożądanych, które wystąpiły podczas ostrej terapii (24-godzinnej), w tym tylko te działania niepożądane, które wystąpiły u 2% lub więcej pacjentów leczonych wstrzyknięciem ABILIFY (dawki ≥5,25 mg /dzień) i dla których częstość występowania u pacjentów leczonych preparatem ABILIFY 15 mg do wstrzykiwań była większa niż częstość występowania u pacjentów leczonych placebo w połączonym zbiorze danych.
Działania niepożądane związane z dawką
Schizofrenia
Zależności od dawki dla częstości występowania zdarzeń niepożądanych związanych z leczeniem oceniano w czterech badaniach u dorosłych pacjentów ze schizofrenią, porównując różne stałe dawki (2, 5, 10, 15, 20 i 30 mg/dobę) doustnego ABILIFY z placebo. Ta analiza, stratyfikowana według badania, wykazała, że jedynym działaniem niepożądanym, które może mieć związek z dawką odpowiedzi, a następnie najbardziej widocznym tylko przy dawce 30 mg, była senność [w tym sedacja]; (częstość występowania to placebo, 7,1%; 10 mg, 8,5%; 15 mg, 8,7%; 20 mg, 7,5%; 30 mg, 12,6%).
W badaniu pacjentów pediatrycznych (w wieku od 13 do 17 lat) ze schizofrenią trzy częste działania niepożądane wydawały się mieć możliwą zależność od dawki: zaburzenia pozapiramidowe (częstość występowania to placebo 5,0%; 10 mg 13,0%; 30 mg 21,6 %); senność (częstość występowania to placebo, 6,0%; 10 mg, 11,0%; 30 mg, 21,6%); i drżenie (częstość występowania to placebo 2,0%; 10 mg 2,0%; 30 mg 11,8%).
Mania dwubiegunowa
badaniu pacjentów pediatrycznych (w wieku 10 do 17 lat) z manią afektywną dwubiegunową cztery częste działania niepożądane miały możliwą zależność od dawki po 4 tygodniach; zaburzenia pozapiramidowe (częstość występowania to placebo, 3,1%; 10 mg, 12,2%; 30 mg, 27,3%); senność (częstość występowania to placebo 3,1%; 10 mg 19,4%; 30 mg 26,3%); akatyzja (częstość występowania to placebo, 2,1%; 10 mg, 8,2%; 30 mg, 11,1%); oraz nadmierne wydzielanie śliny (częstość występowania to placebo, 0%; 10 mg, 3,1%; 30 mg, 8,1%).
Zaburzenie autystyczne
W badaniu pacjentów pediatrycznych (w wieku od 6 do 17 lat) z zaburzeniami autystycznymi, jedno częste działanie niepożądane miało możliwą zależność od dawki: zmęczenie (częstość występowania to placebo 0%; 5 mg 3,8%; 10 mg 22,0%; 15 mg, 18,5%).
Zaburzenie Tourette'a
W badaniu pacjentów pediatrycznych (w wieku od 7 do 17 lat) z zespołem Tourette'a, żadne częste działanie niepożądane nie miało związku z odpowiedzią na dawkę.
Objawy pozapiramidowe
Schizofrenia
krótkoterminowych, kontrolowanych placebo badaniach dotyczących schizofrenii u dorosłych, częstość zgłaszanych zdarzeń związanych z EPS, z wyłączeniem zdarzeń związanych z akatyzją, u pacjentów leczonych ABILIFY wynosiła 13% w porównaniu do 12% w przypadku placebo; a częstość występowania zdarzeń związanych z akatyzją u pacjentów leczonych ABILIFY wynosiła 8% w porównaniu z 4% dla placebo. W krótkoterminowym, kontrolowanym placebo badaniu schizofrenii u pacjentów pediatrycznych (13 do 17 lat), częstość zgłoszonych zdarzeń związanych z EPS, z wyłączeniem zdarzeń związanych z akatyzją, u pacjentów leczonych ABILIFY wynosiła 25% w porównaniu z 7% placebo; a częstość występowania zdarzeń związanych z akatyzją u pacjentów leczonych ABILIFY wynosiła 9% w porównaniu z 6% dla placebo.
Obiektywnie zebrane dane z tych prób zostały zebrane w Skali Oceny Simpson Angus (dla EPS), Skali Akatyzji Barnesa (dla akatyzji) oraz Skalach Oceny Ruchu Mimowolnego (dla dyskinez). W badaniach dotyczących schizofrenii dorosłych obiektywnie zebrane dane nie wykazały różnicy między ABILIFY 10 mg a placebo, z wyjątkiem Skali Akatyzji Barnesa (ABILIFY 20 mg, 0,08; placebo, -0,05). W badaniu pediatrycznym (13 do 17 lat) dotyczącym schizofrenii obiektywnie zebrane dane nie wykazały różnicy między ABILIFY 20 mg a placebo, z wyjątkiem Skali Simpson Angus Rating Scale (ABILIFY 20 mg, 0,24; placebo, -0,29).
Podobnie w długoterminowym (26-tygodniowym), kontrolowanym placebo badaniu schizofrenii u dorosłych, obiektywnie zebrano dane na podstawie Skali Simpson Angus Rating Scale (dla EPS), Skali Akatyzji Barnesa (dla akatyzji) oraz Oceny Niedobrowolnej Skale Ruchu (dla dyskinez) nie wykazały różnicy między ABILIFY a placebo.
Mania dwubiegunowa
krótkoterminowych, kontrolowanych placebo badaniach dotyczących manii w chorobie afektywnej dwubiegunowej u dorosłych, częstość zgłaszanych zdarzeń związanych z EPS, z wyłączeniem zdarzeń związanych z akatyzją, u pacjentów leczonych ABILIFY w monoterapii wynosiła 16% w porównaniu do 8% w przypadku placebo, a częstość występowania zdarzenia związane z akatyzją u pacjentów leczonych ABILIFY w monoterapii wynosiły 13% w porównaniu do 4% w przypadku placebo. W 6-tygodniowym, kontrolowanym placebo badaniu w chorobie afektywnej dwubiegunowej w leczeniu skojarzonym z litem lub walproinianem, częstość zgłaszanych zdarzeń związanych z EPS, z wyłączeniem zdarzeń związanych z akatyzją u pacjentów otrzymujących skojarzone leczenie ABILIFY wynosiła 15% w porównaniu z 8% w przypadku skojarzonego leczenia. placebo, a częstość występowania zdarzeń związanych z akatyzją u pacjentów leczonych dodatkowo preparatem ABILIFY wynosiła 19% w porównaniu z 5% w przypadku uzupełniającego placebo. W krótkoterminowym badaniu kontrolowanym placebo u pacjentów z manią afektywną dwubiegunową u dzieci (10 do 17 lat) częstość zgłaszanych zdarzeń związanych z EPS, z wyłączeniem zdarzeń związanych z akatyzją, u pacjentów leczonych ABILIFY wynosiła 26% w porównaniu z 5% dla placebo, a częstość występowania zdarzeń związanych z akatyzją u pacjentów leczonych ABILIFY wynosiła 10% w porównaniu do 2% dla placebo.
badaniach maniaków dwubiegunowych u dorosłych z monoterapią ABILIFY, Skala Simpson Angus Rating Scale i Skala Akatyzji Barnesa wykazały istotną różnicę między ABILIFY 15 mg a placebo (ABILIFY 0,50; placebo -0,01 i ABILIFY 10 mg, 0,21; placebo -0,05). Zmiany w Skalach Oceny Ruchów Mimowolnych były podobne dla grup ABILIFY 15 mg i placebo. W badaniach klinicznych dotyczących manii afektywnej dwubiegunowej z zastosowaniem ABILIFY 20 mg jako terapii wspomagającej z litem lub walproinianem, Skala Oceny Simpson Angus i Skala Akatyzji Barnesa wykazała istotną różnicę pomiędzy wspomagającym ABILIFY i uzupełniającym placebo (ABILIFY 20 mg, 0,73; placebo, 0,07 i ABILIFY 10 mg, 0,30; placebo, 0,11). Zmiany w Skalach Oceny Ruchów Mimowolnych były podobne dla wspomagającego ABILIFY 20 mg i wspomagającego placebo. W pediatrycznym (10 do 17 lat), krótkoterminowym badaniu maniaków dwubiegunowych, Skala Simpson Angus Rating Scale wykazała istotną różnicę między ABILIFY 10 mg a placebo (ABILIFY 15 mg, 0,90; placebo, -0,05). Zmiany w Skali Akatyzji Barnesa i Skalach Oceny Ruchów Mimowolnych były podobne dla grup ABILIFY 20 mg i placebo.
Ciężkie zaburzenie depresyjne
W krótkoterminowych, kontrolowanych placebo badaniach dotyczących dużego zaburzenia depresyjnego, częstość zgłaszanych zdarzeń związanych z EPS, z wyłączeniem zdarzeń związanych z akatyzją, u pacjentów leczonych dodatkowo ABILIFY wynosiła 8% w porównaniu do 5% u pacjentów otrzymujących dodatkowo placebo; a częstość występowania zdarzeń związanych z akatyzją u pacjentów otrzymujących dodatkowo ABILIFY wynosiła 25% w porównaniu do 4% u pacjentów otrzymujących dodatkowo placebo.
W głównych badaniach zaburzeń depresyjnych Skala Simpson Angus Rating Scale i Skala Akatyzji Barnesa wykazały istotną różnicę między dołączanym ABILIFY i dołączanym placebo (ABILIFY 10 mg 0,31; placebo 0,03 i ABILIFY 0,22; placebo 0,02). Zmiany w Skalach Oceny Ruchu Mimowolnego były podobne w przypadku leczenia uzupełniającego ABILIFY i placebo.
Zaburzenie autystyczne
krótkoterminowych badaniach kontrolowanych placebo dotyczących zaburzeń autystycznych u pacjentów pediatrycznych (6 do 17 lat), częstość zgłaszanych zdarzeń związanych z EPS, z wyłączeniem zdarzeń związanych z akatyzją, u pacjentów leczonych ABILIFY wynosiła 18% w porównaniu do 2% dla placebo, a częstość występowania zdarzeń związanych z akatyzją u pacjentów leczonych ABILIFY wynosiła 3% w porównaniu do 9% dla placebo.
W badaniach klinicznych u dzieci (6 do 17 lat) z krótkotrwałymi zaburzeniami autystycznymi, Skala Simpson Angus Rating Scale wykazała istotną różnicę między ABILIFY a placebo (ABILIFY 20 mg, 0,1; placebo, -0,4). Zmiany w Skali Akatyzji Barnesa i Skalach Oceny Ruchów Mimowolnych były podobne dla grup ABILIFY 10 mg i placebo.
Zaburzenie Tourette'a
krótkoterminowych, kontrolowanych placebo badaniach dotyczących zaburzenia Tourette'a u pacjentów pediatrycznych (6 do 18 lat), częstość zgłoszonych zdarzeń związanych z EPS, z wyłączeniem zdarzeń związanych z akatyzją, u pacjentów leczonych ABILIFY wynosiła 7% w porównaniu z 6% dla placebo, a częstość występowania zdarzeń związanych z akatyzją u pacjentów leczonych ABILIFY wynosiła 4% w porównaniu do 6% dla placebo.
W krótkoterminowych badaniach Tourette'a z udziałem dzieci (6-18 lat) zmiany w Skali Oceny Angusa Simpsona, Skali Akatyzji Barnesa i Skali Oceny Ruchów Mimowolnych nie różniły się istotnie klinicznie dla preparatu ABILIFY 15 mg i placebo.
Pobudzenie związane ze schizofrenią lub manią dwubiegunową
badaniach kontrolowanych placebo u pacjentów z pobudzeniem związanym ze schizofrenią lub manią dwubiegunową, częstość zgłoszonych zdarzeń związanych z EPS z wyłączeniem zdarzeń związanych z akatyzją u pacjentów leczonych ABILIFY wynosiła 2% w porównaniu z 2% w przypadku placebo, a częstość występowania akatyzji- powiązanych zdarzeń u pacjentów leczonych ABILIFY wynosił 2% w porównaniu do 0% w przypadku placebo. Obiektywnie zebrane dane w Skali Oceny Simpson Angus (dla EPS) i Skali Akatyzji Barnesa (dla akatyzji) dla wszystkich leczonych grup nie wykazały różnicy między ABILIFY 10mg a placebo.
Dystonia
Objawy dystonii, przedłużające się nieprawidłowe skurcze grup mięśni, mogą wystąpić u osób podatnych w ciągu pierwszych kilku dni leczenia. Objawy dystoniczne obejmują: skurcz mięśni szyi, czasami przechodzący w ucisk w gardle, trudności w połykaniu, trudności w oddychaniu i (lub) wysunięcie języka. Chociaż objawy te mogą wystąpić przy niskich dawkach, występują częściej i z większym nasileniem przy dużej sile działania i przy wyższych dawkach leków przeciwpsychotycznych pierwszej generacji. Podwyższone ryzyko ostrej dystonii obserwuje się u mężczyzn i młodszych grup wiekowych.
Dodatkowe wyniki obserwowane w badaniach klinicznych
Działania niepożądane w długotrwałych, podwójnie ślepych, kontrolowanych placebo badaniach
Działania niepożądane zgłaszane w 26-tygodniowym, podwójnie zaślepionym badaniu porównującym doustny ABILIFY 10 mg i placebo u pacjentów ze schizofrenią były zasadniczo zgodne z tymi zgłaszanymi w krótkoterminowych badaniach kontrolowanych placebo, z wyjątkiem większej częstości występowania drżenia [8]. % (12/153) dla ABILIFY 20mg vs. 2% (3/153) dla placebo]. W tym badaniu większość przypadków drżenia miała łagodne nasilenie (8/12 łagodne i 4/12 umiarkowane), wystąpiła na początku leczenia (9/12 ≤49 dni) i miała ograniczony czas trwania (7/12 ≤ 10 dni). Drżenie rzadko prowadziło do przerwania (
Inne działania niepożądane obserwowane podczas oceny preparatu ABILIFY przed wprowadzeniem do obrotu
Poniższy wykaz nie obejmuje reakcji: 1) już wymienionych w poprzednich tabelach lub w innych miejscach na etykiecie, 2) dla których przyczyna leku była odległa, 3) które były tak ogólne, że nie dostarczały informacji, 4) które nie zostały uznane za istotne implikacje kliniczne lub 5), które wystąpiły z częstością równą lub mniejszą niż placebo.
Reakcje są klasyfikowane według układu organizmu zgodnie z następującymi definicjami: częste działania niepożądane to te, które występują u co najmniej 1/100 pacjentów; rzadkie reakcje niepożądane występują u 1/100 do 1/1000 pacjentów; rzadkie reakcje to te występujące u mniej niż 1/1000 pacjentów:
Dorośli – podanie doustne
Zaburzenia krwi i układu chłonnego: rzadko - małopłytkowość
Zaburzenia serca: rzadko - bradykardia, kołatanie serca, rzadko - trzepotanie przedsionków, zatrzymanie krążenia i oddychania, blok przedsionkowo-komorowy, migotanie przedsionków, dusznica bolesna, niedokrwienie mięśnia sercowego, zawał mięśnia sercowego, niewydolność krążeniowo-oddechowa
Zaburzenia oka: rzadko - światłowstręt; rzadki - podwójne widzenie
Zaburzenia żołądkowo-jelitowe: rzadko - choroba refluksowa przełyku
Ogólne Zaburzenia i Warunki Miejsca Administracji: często - astenia; rzadko - obrzęk obwodowy, ból w klatce piersiowej; rzadki - obrzęk twarzy
Zaburzenia wątroby i dróg żółciowych: rzadko - zapalenie wątroby, żółtaczka
Zaburzenia układu immunologicznego : rzadko - nadwrażliwość
Urazy, zatrucia i powikłania po zabiegach: rzadko - upadek; rzadki - udar cieplny
Dochodzenia: częste - zmniejszenie masy ciała, rzadkie - zwiększenie aktywności enzymów wątrobowych, zwiększenie stężenia glukozy we krwi, zwiększenie aktywności dehydrogenazy mleczanowej we krwi, zwiększenie aktywności transferazy gamma-glutamylowej; rzadko - zwiększenie stężenia prolaktyny we krwi, zwiększenie stężenia mocznika we krwi, zwiększenie stężenia kreatyniny we krwi, zwiększenie stężenia bilirubiny we krwi, wydłużenie odstępu QT w elektrokardiogramie, zwiększenie stężenia hemoglobiny glikozylowanej
Zaburzenia metabolizmu i odżywiania: częste - anoreksja; rzadko - hipokaliemia, hiponatremia, hipoglikemia
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej: rzadko - osłabienie mięśni, napięcie mięśni; rzadko - rabdomioliza, zmniejszona ruchliwość
Zaburzenia układu nerwowego: rzadko - parkinsonizm, upośledzenie pamięci, sztywność koła zębatego, hipokinezja, bradykinezja; rzadko - akinezja, mioklonie, nieprawidłowa koordynacja, zaburzenia mowy, drgawki Grand Mal;
Zaburzenia psychiczne: rzadko - agresja, utrata libido, majaczenie; rzadko - zwiększone libido, anorgazmia, tiki, myśli mordercze, katatonia, lunatyka
Zaburzenia nerek i dróg moczowych: rzadko - zatrzymanie moczu, nokturia
Zaburzenia układu rozrodczego i piersi: rzadko - zaburzenia erekcji; rzadko - ginekomastia, nieregularne miesiączki, brak miesiączki, ból piersi, priapizm
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia: rzadko - zatkany nos, duszność
Zaburzenia skóry i tkanki podskórnej: rzadko - wysypka, nadmierne pocenie się, świąd, reakcja nadwrażliwości na światło, łysienie; rzadko - pokrzywka
Zaburzenia naczyniowe: rzadko - niedociśnienie, nadciśnienie
Pacjenci pediatryczni — podawanie doustne
Większość zdarzeń niepożądanych obserwowanych w zbiorczej bazie danych 1686 pacjentów pediatrycznych w wieku od 6 do 18 lat zaobserwowano również w populacji osób dorosłych. Poniżej wymieniono dodatkowe działania niepożądane obserwowane w populacji pediatrycznej.
Zaburzenia oka nieczęsty - kryzys okulistyki
Zaburzenia żołądkowo-jelitowe: rzadko - suchość języka, skurcz języka
Dochodzenia: często - podwyższona insulina we krwi
Zaburzenia układu nerwowego: rzadkie - mówienie przez sen
Zaburzenia nerek i dróg moczowych częste - moczenie nocne
Zaburzenia skóry i tkanki podskórnej: rzadko - hirsutyzm
Dorośli – wstrzyknięcie domięśniowe
Większość działań niepożądanych obserwowanych w zbiorczej bazie danych 749 dorosłych pacjentów leczonych preparatem ABILIFY w postaci wstrzyknięć obserwowano również w populacji dorosłych leczonych preparatem ABILIFY doustnie. Poniżej wymieniono dodatkowe działania niepożądane obserwowane w populacji pacjentów otrzymujących ABILIFY.
Ogólne Zaburzenia i Warunki Miejsca Administracji: ≥1/100 pacjentów - reakcja w miejscu wstrzyknięcia; ≥1/1000 pacjentów i
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane po zatwierdzeniu stosowania ABILIFY. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe ustalenie związku przyczynowego z ekspozycją na lek: wystąpienie reakcji alergicznej (reakcja anafilaktyczna, obrzęk naczynioruchowy, skurcz krtani, świąd/pokrzywka lub skurcz jamy ustnej i gardła), hazard patologiczny , czkawka i wahania poziomu glukozy we krwi.
INTERAKCJE Z LEKAMI
Leki mające klinicznie istotne interakcje z ABILIFY
Leki nie mające klinicznie istotnych interakcji z ABILIFY
Na podstawie badań farmakokinetycznych nie ma konieczności dostosowania dawki ABILIFY w przypadku jednoczesnego podawania z famotydyną, walproinianem, litem, lorazepamem.
Ponadto nie jest konieczne dostosowanie dawki dla substratów CYP2D6 (np. dekstrometorfan, fluoksetyna, paroksetyna lub wenlafaksyna), CYP2C9 (np. warfaryna), CYP2C19 (np. omeprazol, warfaryna, escitalopram) lub CYP3A4 (np. dekstrometorfan) przy jednoczesnym podawaniu z ABILIFY. Ponadto nie ma konieczności dostosowania dawkowania walproinianu, litu, lamotryginy, lorazepamu lub sertraliny, gdy są one podawane jednocześnie z ABILIFY [patrz FARMAKOLOGIA KLINICZNA ].
Nadużywanie i uzależnienie od narkotyków
Substancja kontrolowana
ABILIFY nie jest substancją kontrolowaną.
Nadużywać
ABILIFY nie był systematycznie badany u ludzi pod kątem możliwości nadużywania, tolerancji lub uzależnienia fizycznego. W związku z tym pacjentów należy dokładnie zbadać pod kątem historii nadużywania leków i takich pacjentów należy uważnie obserwować pod kątem oznak niewłaściwego stosowania lub nadużywania leku ABILIFY 20 mg (np. rozwój tolerancji, zwiększenie dawki, poszukiwanie leku).
Zależność
W badaniach uzależnienia fizycznego u małp objawy odstawienia obserwowano po nagłym zaprzestaniu dawkowania. Chociaż badania kliniczne nie wykazały żadnej tendencji do jakichkolwiek zachowań związanych z poszukiwaniem leku, obserwacje te nie były systematyczne i na podstawie tego ograniczonego doświadczenia nie można przewidzieć, w jakim stopniu lek działający na OUN będzie niewłaściwie stosowany, przekierowywany, i/lub nadużywane po wprowadzeniu do obrotu.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Zwiększona śmiertelność u starszych pacjentów z psychozą związaną z demencją
Zwiększona śmiertelność
Pacjenci w podeszłym wieku z psychozą otępienną leczeni lekami przeciwpsychotycznymi są narażeni na zwiększone ryzyko zgonu. ABILIFY (arypiprazol) nie jest zatwierdzony do leczenia pacjentów z psychozą związaną z otępieniem [patrz OSTRZEŻENIE W RAMCE].
Doświadczenie w zakresie bezpieczeństwa u starszych pacjentów z psychozą związaną z chorobą Alzheimera
W trzech 10-tygodniowych, kontrolowanych placebo badaniach ABILIFY 10 mg u starszych pacjentów z psychozą związaną z chorobą Alzheimera (n=938; średni wiek: 82,4 lat; zakres: 56-99 lat), działania niepożądane, które były zgłaszane z częstością ≥ 3%, a ABILIFY 15 mg z częstością co najmniej dwa razy niż w przypadku placebo były letarg  [placebo 2%, ABILIFY 5%], senność (w tym sedacja) [placebo 3%, ABILIFY 8%] i nietrzymanie moczu (głównie , nietrzymanie moczu) [placebo 1%, ABILIFY 5%], nadmierne ślinienie [placebo 0%, ABILIFY 4%] i zawroty głowy [placebo 1%, ABILIFY 4%].
Bezpieczeństwo i skuteczność ABILIFY 15 mg w leczeniu pacjentów z psychozą związaną z otępieniem nie zostały ustalone. Jeśli lekarz przepisujący zdecyduje się leczyć takich pacjentów preparatem ABILIFY 15 mg, należy ocenić, czy nie występują trudności w połykaniu lub nadmierna senność, które mogą predysponować do przypadkowego urazu lub zachłyśnięcia [patrz OSTRZEŻENIE W PUDEŁKU ].
Zdarzenia niepożądane dotyczące naczyń mózgowych, w tym udar mózgu
W badaniach klinicznych kontrolowanych placebo (dwa badania ze zmienną dawką i jedno badanie z ustaloną dawką) psychozy związanej z otępieniem stwierdzono zwiększoną częstość występowania zdarzeń niepożądanych naczyniowo-mózgowych (np. udar, przemijający napad niedokrwienny), w tym zgonów, u pacjentów leczonych ABILIFY ( średni wiek: 84 lata; zakres: 78-88 lat). W badaniu ze stałą dawką wystąpiła statystycznie istotna zależność dawka-odpowiedź dla mózgowo-naczyniowych zdarzeń niepożądanych u pacjentów leczonych ABILIFY. ABILIFY nie jest zatwierdzony do leczenia pacjentów z psychozą związaną z otępieniem [patrz OSTRZEŻENIE W PUDEŁKU ].
Myśli i zachowania samobójcze u dzieci, młodzieży i młodych dorosłych
Pacjenci z ciężkimi zaburzeniami depresyjnymi (MDD), zarówno dorośli, jak i pediatryczni, mogą doświadczać nasilenia depresji i/lub pojawienia się myśli i zachowań samobójczych (samobójstwa) lub nietypowych zmian w zachowaniu, niezależnie od tego, czy przyjmują leki przeciwdepresyjne, a to ryzyko może utrzymywać się aż do wystąpienia znacznej remisji. Samobójstwo jest znanym ryzykiem depresji i niektórych innych zaburzeń psychicznych, a same te zaburzenia są najsilniejszymi predyktorami samobójstwa. Od dawna istnieje jednak obawa, że leki przeciwdepresyjne mogą odgrywać rolę w wywoływaniu nasilenia depresji i pojawianiu się myśli samobójczych u niektórych pacjentów we wczesnych fazach leczenia. Zbiorcze analizy krótkoterminowych, kontrolowanych placebo badań leków przeciwdepresyjnych (SSRI i inne) wykazały, że leki te zwiększają ryzyko myśli i zachowań samobójczych (samobójstwa) u dzieci, młodzieży i młodych dorosłych (w wieku 18-24 lat) z MDD i inne zaburzenia psychiczne. Badania krótkoterminowe nie wykazały wzrostu ryzyka samobójstw w przypadku stosowania leków przeciwdepresyjnych w porównaniu z placebo u osób dorosłych w wieku powyżej 24 lat; u osób dorosłych w wieku 65 lat i starszych odnotowano zmniejszenie liczby przyjmowanych leków przeciwdepresyjnych w porównaniu z placebo.
Połączone analizy badań kontrolowanych placebo u dzieci i młodzieży z MDD, zaburzeniami obsesyjno-kompulsywnymi (OCD) lub innymi zaburzeniami psychicznymi obejmowały łącznie 24 krótkoterminowe badania 9 leków przeciwdepresyjnych z udziałem ponad 4400 pacjentów. Zbiorcze analizy badań kontrolowanych placebo u dorosłych z MDD lub innymi zaburzeniami psychicznymi obejmowały łącznie 295 krótkoterminowych badań (mediana czasu trwania wynosząca 2 miesiące) 11 leków przeciwdepresyjnych z udziałem ponad 77 000 pacjentów. Istniało znaczne zróżnicowanie ryzyka samobójstwa wśród leków, ale tendencja do wzrostu u młodszych pacjentów w przypadku prawie wszystkich badanych leków. Istniały różnice w bezwzględnym ryzyku samobójstwa w różnych wskazaniach, z największą częstością występowania MDD. Różnice ryzyka (lek vs placebo) były jednak stosunkowo stabilne w obrębie warstw wiekowych i we wskazaniach. Te różnice ryzyka (różnica między lekami a placebo w liczbie przypadków samobójstw na 1000 leczonych pacjentów) przedstawiono w Tabeli 5.
żadnym z badań pediatrycznych nie doszło do samobójstw. W badaniach z udziałem dorosłych zdarzały się samobójstwa, ale liczba ta nie była wystarczająca, aby wyciągnąć jakiekolwiek wnioski na temat wpływu leku na samobójstwo.
Nie wiadomo, czy ryzyko samobójstwa rozciąga się na długotrwałe używanie, tj. dłużej niż kilka miesięcy. Jednak istnieją dowody z kontrolowanych placebo badań podtrzymujących u dorosłych z depresją, że stosowanie leków przeciwdepresyjnych może opóźnić nawrót depresji.
Wszyscy pacjenci leczeni lekami przeciwdepresyjnymi w jakimkolwiek wskazaniu powinni być odpowiednio monitorowani i obserwowani pod kątem pogorszenia stanu klinicznego, skłonności samobójczych i nietypowych zmian w zachowaniu, szczególnie w ciągu pierwszych kilku miesięcy terapii lekowej lub w czasie zmiany dawki, albo zwiększa się lub maleje.
dorosłych i dzieci leczonych lekami przeciwdepresyjnymi z powodu MDD, a także w inne wskazania, zarówno psychiatryczne, jak i niepsychiatryczne. Chociaż nie ustalono związku przyczynowo-skutkowego między pojawieniem się takich objawów a nasileniem depresji i/lub pojawieniem się impulsów samobójczych, istnieje obawa, że takie objawy mogą być prekursorem pojawiania się samobójstw.
Należy rozważyć zmianę schematu leczenia, w tym ewentualnie odstawienie leku, u pacjentów, u których depresja jest stale nasilona lub u których pojawiają się myśli samobójcze lub objawy, które mogą być prekursorami nasilenia depresji lub myśli samobójczych, zwłaszcza jeśli objawy te są ciężkie, nagłe na początku lub nie były częścią objawów występujących u pacjenta.
Rodziny i opiekunowie pacjentów leczonych lekami przeciwdepresyjnymi z powodu dużych zaburzeń depresyjnych lub innych wskazań, zarówno psychiatrycznych, jak i niepsychiatrycznych, powinni być ostrzeżeni o konieczności monitorowania pacjentów pod kątem pojawienia się pobudzenia, drażliwości, nietypowych zmian w zachowaniu i innych objawów opisanych powyżej , a także pojawienia się samobójstw i natychmiastowego zgłaszania takich objawów świadczeniodawcom. Taki monitoring powinien obejmować codzienną obserwację rodzin i opiekunów. Recepty na ABILIFY należy wypisać na najmniejszą ilość tabletek, zgodnie z dobrym postępowaniem z pacjentem, aby zmniejszyć ryzyko przedawkowania.
Badanie przesiewowe pacjentów pod kątem choroby afektywnej dwubiegunowej
Poważny epizod depresyjny może być początkowym objawem choroby afektywnej dwubiegunowej. Powszechnie uważa się (chociaż nie zostało to potwierdzone w badaniach kontrolowanych), że leczenie takiego epizodu samym lekiem przeciwdepresyjnym może zwiększyć prawdopodobieństwo wystąpienia epizodu mieszanego/maniakalnego u pacjentów z ryzykiem choroby afektywnej dwubiegunowej. Nie wiadomo, czy którykolwiek z objawów opisanych powyżej reprezentuje taką konwersję. Jednak przed rozpoczęciem leczenia lekiem przeciwdepresyjnym pacjenci z objawami depresji powinni zostać odpowiednio przebadani w celu ustalenia, czy są oni zagrożeni chorobą afektywną dwubiegunową; takie badania przesiewowe powinny obejmować szczegółowy wywiad psychiatryczny, w tym wywiad rodzinny dotyczący samobójstw, choroby afektywnej dwubiegunowej i depresji.
Należy zauważyć, że ABILIFY 20mg nie jest zatwierdzony do stosowania w leczeniu depresji w populacji pediatrycznej.
Złośliwy Zespół Neuroleptyczny (NMS)
Potencjalnie śmiertelny zespół objawów czasami określany jako złośliwy zespół neuroleptyczny (NMS) może wystąpić po podaniu leków przeciwpsychotycznych, w tym ABILIFY. rzadkie przypadki NMS wystąpiły podczas leczenia ABILIFY 15 mg w ogólnoświatowej klinicznej bazie danych. Objawy kliniczne NMS to hiperpyreksja, sztywność mięśni, zmieniony stan psychiczny i dowody niestabilności autonomicznej (nieregularne tętno lub ciśnienie krwi, tachykardia, pocenie się i arytmia serca). Dodatkowe objawy mogą obejmować podwyższoną aktywność kinazy kreatynowej, mioglobinuria (rabdomioliza) i ostrą niewydolność nerek.
Diagnostyczna ocena pacjentów z tym zespołem jest skomplikowana. Przy ustalaniu diagnozy ważne jest, aby wykluczyć przypadki, w których obraz kliniczny obejmuje zarówno poważną chorobę medyczną (np. zapalenie płuc, zakażenie ogólnoustrojowe), jak i nieleczone lub niewłaściwie leczone objawy pozapiramidowe (EPS). Inne ważne czynniki w diagnostyce różnicowej obejmują ośrodkową toksyczność antycholinergiczną, udar cieplny, gorączkę polekową i pierwotną patologię ośrodkowego układu nerwowego.
Postępowanie w NMS powinno obejmować: 1) natychmiastowe odstawienie leków przeciwpsychotycznych i innych leków, które nie są niezbędne do jednoczesnego leczenia; 2) intensywne leczenie objawowe i monitoring medyczny; oraz 3) leczenie wszelkich współistniejących poważnych problemów medycznych, dla których dostępne są określone metody leczenia. Nie ma ogólnej zgody co do konkretnych schematów leczenia farmakologicznego niepowikłanych NMS.
Jeśli pacjent wymaga leczenia przeciwpsychotycznego po wyzdrowieniu z NMS, należy dokładnie rozważyć możliwość ponownego włączenia terapii lekowej. Pacjenta należy uważnie obserwować, ponieważ zgłaszano nawroty NMS.
Późne dyskinezy
U pacjentów leczonych lekami przeciwpsychotycznymi może rozwinąć się zespół potencjalnie nieodwracalnych, mimowolnych ruchów dyskinetycznych. Chociaż częstość występowania zespołu wydaje się być najwyższa wśród osób starszych, zwłaszcza starszych kobiet, nie można polegać na szacunkach częstości występowania, aby przewidzieć na początku leczenia przeciwpsychotycznego, u których pacjentów prawdopodobnie rozwinie się zespół. Nie wiadomo, czy produkty leków przeciwpsychotycznych różnią się potencjałem wywoływania późnych dyskinez.
Uważa się, że wraz ze wzrostem czasu trwania leczenia i całkowitej skumulowanej dawki leków przeciwpsychotycznych podawanych pacjentowi wzrasta ryzyko wystąpienia dyskinezy późnej i prawdopodobieństwo, że stanie się ona nieodwracalna. Zespół może jednak rozwinąć się, choć znacznie rzadziej, po stosunkowo krótkich okresach leczenia małymi dawkami.
Późne dyskinezy mogą ustąpić, częściowo lub całkowicie, jeśli leczenie przeciwpsychotyczne zostanie przerwane. Jednak samo leczenie przeciwpsychotyczne może tłumić (lub częściowo tłumić) oznaki i objawy zespołu, a tym samym może maskować leżący u podstaw proces. Wpływ supresji objawowej na długotrwały przebieg zespołu jest nieznany.
Biorąc pod uwagę powyższe rozważania, ABILIFY należy przepisywać w sposób, który najprawdopodobniej zminimalizuje występowanie późnych dyskinez. Przewlekłe leczenie przeciwpsychotyczne powinno być generalnie zarezerwowane dla pacjentów cierpiących na przewlekłą chorobę, na którą (1) wiadomo, że reaguje na leki przeciwpsychotyczne i (2) dla których alternatywne, równie skuteczne, ale potencjalnie mniej szkodliwe terapie nie są dostępne lub odpowiednie. U pacjentów, którzy wymagają przewlekłego leczenia, należy dążyć do jak najmniejszej dawki i najkrótszego czasu trwania leczenia dającego zadowalającą odpowiedź kliniczną. Konieczność kontynuacji leczenia powinna być okresowo oceniana.
Jeśli u pacjenta przyjmującego ABILIFY pojawią się objawy przedmiotowe i podmiotowe późnych dyskinez, należy rozważyć odstawienie leku. Jednak niektórzy pacjenci mogą wymagać leczenia ABILIFY 15 mg pomimo obecności zespołu.
Zmiany metaboliczne
Atypowe leki przeciwpsychotyczne powiązano ze zmianami metabolicznymi, które obejmują hiperglikemię/cukrzycę, dyslipidemię i przyrost masy ciała. Chociaż wykazano, że wszystkie leki z tej klasy powodują pewne zmiany metaboliczne, każdy lek ma swój własny profil ryzyka.
Hiperglikemia/cukrzyca
U pacjentów leczonych atypowymi lekami przeciwpsychotycznymi zgłaszano hiperglikemię, w niektórych przypadkach skrajną i związaną z kwasicą ketonową, śpiączką hiperosmolarną lub zgonem. Istnieją doniesienia o hiperglikemii u pacjentów leczonych ABILIFY [patrz DZIAŁANIA NIEPOŻĄDANE ]. Ocenę związku między stosowaniem atypowych leków przeciwpsychotycznych a nieprawidłowościami glikemii komplikuje możliwość zwiększonego podstawowego ryzyka cukrzycy u pacjentów ze schizofrenią oraz wzrastająca częstość występowania cukrzycy w populacji ogólnej. Biorąc pod uwagę te czynniki, związek między stosowaniem atypowych leków przeciwpsychotycznych a zdarzeniami niepożądanymi związanymi z hiperglikemią nie jest w pełni zrozumiały. Jednak badania epidemiologiczne sugerują zwiększone ryzyko działań niepożądanych związanych z hiperglikemią u pacjentów leczonych atypowymi lekami przeciwpsychotycznymi. Ponieważ ABILIFY nie był sprzedawany w momencie przeprowadzania tych badań, nie wiadomo, czy ABILIFY jest związany z tym zwiększonym ryzykiem. Dokładne szacunki ryzyka wystąpienia działań niepożądanych związanych z hiperglikemią u pacjentów leczonych atypowymi lekami przeciwpsychotycznymi nie są dostępne.
Pacjenci z ustalonym rozpoznaniem cukrzycy, którzy rozpoczynają leczenie atypowymi lekami przeciwpsychotycznymi, powinni być regularnie monitorowani pod kątem pogorszenia kontroli glikemii. U pacjentów z czynnikami ryzyka cukrzycy (np. otyłość, cukrzyca w wywiadzie rodzinnym), którzy rozpoczynają leczenie atypowymi lekami przeciwpsychotycznymi, należy wykonać badanie stężenia glukozy we krwi na czczo na początku leczenia oraz okresowo w trakcie leczenia. Każdy pacjent leczony atypowymi lekami przeciwpsychotycznymi powinien być monitorowany pod kątem objawów hiperglikemii, w tym polidypsji, wielomoczu, polifagii i osłabienia. U pacjentów, u których podczas leczenia atypowymi lekami przeciwpsychotycznymi wystąpią objawy hiperglikemii, należy wykonać badanie stężenia glukozy we krwi na czczo. W niektórych przypadkach hiperglikemia ustąpiła po odstawieniu atypowego leku przeciwpsychotycznego; jednak niektórzy pacjenci wymagali kontynuacji leczenia przeciwcukrzycowego pomimo odstawienia podejrzanego leku.
Dorośli ludzie
analizie 13 kontrolowanych placebo badań monoterapii u dorosłych, głównie ze schizofrenią lub chorobą afektywną dwubiegunową, średnia zmiana stężenia glukozy na czczo u pacjentów leczonych ABILIFY (+4,4 mg/dl; mediana ekspozycji 25 dni; N=1057) nie była istotna inne niż u pacjentów otrzymujących placebo (+2,5 mg/dl; mediana ekspozycji 22 dni; N=799). Tabela 6 przedstawia odsetek pacjentów leczonych ABILIFY z normalną i graniczną glikemią na czczo na początku (mediana ekspozycji 25 dni), u których uzyskano wysoki poziom glukozy na czczo związany z leczeniem w porównaniu z pacjentami otrzymującymi placebo (mediana ekspozycji 22 dni).
Po 24 tygodniach średnia zmiana stężenia glukozy na czczo u pacjentów leczonych ABILIFY nie różniła się znacząco niż u pacjentów otrzymujących placebo [odpowiednio +2,2 mg/dl (n=42) i +9,6 mg/dl (n=28)] .
Średnia zmiana stężenia glukozy na czczo u pacjentów z ciężkimi zaburzeniami depresyjnymi leczonych preparatem ABILIFY (+0,7 mg/dl; mediana ekspozycji 42 dni; N=241) nie różniła się znacząco niż u pacjentów otrzymujących placebo (+0,8 mg/dl; mediana ekspozycja 42 dni; N=246). Tabela 7 przedstawia odsetek dorosłych pacjentów ze zmianami stężenia glukozy na czczo w dwóch kontrolowanych placebo badaniach uzupełniających (mediana ekspozycji 42 dni) u pacjentów z dużym zaburzeniem depresyjnym.
Pacjenci pediatryczni i młodzież
W analizie dwóch kontrolowanych placebo badań z udziałem młodzieży ze schizofrenią (13 do 17 lat) i dzieci z chorobą afektywną dwubiegunową (10 do 17 lat), średnia zmiana stężenia glukozy na czczo u pacjentów leczonych ABILIFY (+4,8 mg/dl; z medianą ekspozycji 43 dni; N=259) nie różniła się istotnie niż u pacjentów otrzymujących placebo (+1,7 mg/dl; z medianą ekspozycji 42 dni; N=123).
analizie dwóch kontrolowanych placebo badań u dzieci i młodzieży z drażliwością związaną z zaburzeniami autystycznymi (6 do 17 lat) z medianą ekspozycji 56 dni, średnia zmiana stężenia glukozy na czczo u pacjentów leczonych ABILIFY (- 0,2 mg /dl; N=83) nie różniła się istotnie niż u pacjentów otrzymujących placebo (
W analizie dwóch kontrolowanych placebo badań u dzieci i młodzieży z chorobą Tourette'a (6 do 18 lat) z medianą ekspozycji 57 dni, średnia zmiana stężenia glukozy na czczo u pacjentów leczonych ABILIFY (0,79 mg/dl; N=90) nie różniła się istotnie niż u pacjentów otrzymujących placebo (-1,66 mg/dl; N=58).
tabeli 8 przedstawiono odsetek pacjentów ze zmianami poziomu glukozy na czczo w łącznej grupie młodzieży ze schizofrenią i u dzieci z chorobą afektywną dwubiegunową (mediana ekspozycji 42-43 dni), z dwóch kontrolowanych placebo badań u dzieci (6-17 lat) z drażliwością związaną z zaburzeniami autystycznymi (mediana ekspozycji 56 dni) oraz z dwóch kontrolowanych placebo badań u dzieci (6 do 18 lat) z zespołem Tourette'a (mediana ekspozycji 57 dni).
Po 12 tygodniach w zbiorczych badaniach dotyczących schizofrenii młodzieńczej i dziecięcej choroby afektywnej dwubiegunowej, średnia zmiana stężenia glukozy na czczo u pacjentów leczonych ABILIFY nie różniła się znacząco niż u pacjentów otrzymujących placebo [+2,4 mg/dl (n=81) i +0,1 mg /dL (n=15)].
Dyslipidemia
U pacjentów leczonych atypowymi lekami przeciwpsychotycznymi obserwowano niepożądane zmiany lipidów.
Nie było istotnych różnic pomiędzy pacjentami leczonymi ABILIFY i placebo w proporcji ze zmianami od normalnego do klinicznie istotnego poziomu dla cholesterolu całkowitego na czczo/nie na czczo, triglicerydów na czczo, LDL na czczo i HDL na czczo/nie. Analizy pacjentów z ekspozycją trwającą co najmniej 12 lub 24 tygodnie były ograniczone przez niewielką liczbę pacjentów.
Dorośli ludzie
Tabela 9 przedstawia odsetek dorosłych pacjentów, pochodzących głównie z połączonych badań kontrolowanych placebo dotyczących schizofrenii i choroby afektywnej dwubiegunowej w monoterapii, ze zmianami w całkowitym cholesterolu (zbiorcze z 17 badań; mediana ekspozycji od 21 do 25 dni), trójglicerydami na czczo (zbiorcze z ośmiu badań; mediana ekspozycji 42 dni), stężenie cholesterolu LDL na czczo (zestawione z ośmiu badań; mediana ekspozycji 39 do 45 dni, z wyjątkiem pacjentów otrzymujących placebo z wyjściowymi prawidłowymi pomiarami LDL na czczo, u których badania, mediana ekspozycji 40 do 42 dni).
badaniach monoterapii u dorosłych, odsetek pacjentów w 12. tygodniu i 24. tygodniu ze zmianami od normalnego do wysokiego stężenia cholesterolu całkowitego (na czczo/nie na czczo), trójglicerydów na czczo i cholesterolu LDL na czczo był podobny u pacjentów otrzymujących ABILIFY i placebo: 12 tygodni, całkowity cholesterol (na czczo/nie na czczo), 1/71 (1,4%) vs. 3/74 (4,1%); Trójglicerydy na czczo, 8/62 (12,9%) w porównaniu z 5/37 (13,5%); Cholesterol LDL na czczo, odpowiednio 0/34 (0%) vs. 1/25 (4,0%); a po 24 tygodniach całkowity cholesterol (na czczo/nie na czczo), 1/42 (2,4%) vs. 3/37 (8,1%); Trójglicerydy na czczo, 5/34 (14,7%) w porównaniu do 5/20 (25%); Cholesterol LDL na czczo, odpowiednio 0/22 (0%) vs. 1/18 (5,6%).
Tabela 10 przedstawia odsetek pacjentów ze zmianami cholesterolu całkowitego (na czczo/nie na czczo), trójglicerydów na czczo, cholesterolu LDL na czczo i cholesterolu HDL na czczo z dwóch kontrolowanych placebo badań uzupełniających u dorosłych pacjentów z ciężkimi zaburzeniami depresyjnymi (mediana ekspozycji 42 dni).
Pacjenci pediatryczni i młodzież
Tabela 11 przedstawia odsetek nastolatków ze schizofrenią (13 do 17 lat) i dzieci z chorobą afektywną dwubiegunową (10 do 17 lat) ze zmianami cholesterolu całkowitego i cholesterolu HDL (zbiorcze dane z dwóch badań kontrolowanych placebo; mediana ekspozycji 42 do 43 dni ) i triglicerydy na czczo (zestawione z dwóch badań kontrolowanych placebo; mediana ekspozycji 42 do 44 dni).
badaniach monoterapii młodzieży ze schizofrenią i dzieci z chorobą afektywną dwubiegunową odsetek pacjentów w 12. tygodniu i 24. tygodniu ze zmianami z normalnego do wysokiego stężenia cholesterolu całkowitego (na czczo/nie na czczo), trójglicerydów na czczo i cholesterolu LDL na czczo był podobny w przypadku stosowania preparatu ABILIFY. - i pacjenci leczeni placebo: po 12 tygodniach cholesterol całkowity (na czczo/bez czczo), 0/57 (0%) vs. 0/15 (0%); Trójglicerydy na czczo, odpowiednio 2/72 (2,8%) w porównaniu z 1/14 (7,1%); a po 24 tygodniach całkowity cholesterol (na czczo/nie na czczo), 0/36 (0%) vs. 0/12 (0%); Trójglicerydy na czczo, odpowiednio 1/47 (2,1%) vs. 1/10 (10,0%).
Tabela 12 przedstawia odsetek pacjentów ze zmianami całkowitego cholesterolu (na czczo/nie na czczo) i trójglicerydów na czczo (mediana ekspozycji 56 dni) oraz cholesterolu HDL (mediana ekspozycji 55 do 56 dni) z dwóch kontrolowanych placebo badań z udziałem dzieci (6 do 17 dni) lat) z drażliwością związaną z zaburzeniami autystycznymi.
Tabela 13 przedstawia odsetek pacjentów ze zmianami całkowitego cholesterolu (na czczo/nie na czczo) i trójglicerydów na czczo (mediana ekspozycji 57 dni) i cholesterolu HDL (mediana ekspozycji 57 dni) z dwóch kontrolowanych placebo badań z udziałem dzieci (od 6 do 18 lat) z zespołem Tourette'a.
Przybranie na wadze
Przyrost masy ciała zaobserwowano przy nietypowym stosowaniu leków przeciwpsychotycznych. Zalecane jest kliniczne monitorowanie masy ciała.
Dorośli ludzie
W analizie 13 badań kontrolowanych placebo dotyczących monoterapii, głównie dotyczących schizofrenii zbiorczej i choroby afektywnej dwubiegunowej, z medianą ekspozycji wynoszącą 21 do 25 dni, średnia zmiana masy ciała u pacjentów leczonych ABILIFY wyniosła +0,3 kg (N=1673) w porównaniu do -0,1 kg (N=1100) u pacjentów z grupą kontrolną placebo. Po 24 tygodniach średnia zmiana masy ciała w stosunku do wartości początkowej u pacjentów leczonych ABILIFY wyniosła –1,5 kg (n=73) w porównaniu do –0,2 kg (n=46) u pacjentów otrzymujących placebo.
badaniach, w których dodawano ABILIFY do leków przeciwdepresyjnych, pacjenci otrzymywali najpierw 8 tygodni leczenia przeciwdepresyjnego, a następnie 6 tygodni dodatkowego ABILIFY 10 mg lub placebo w uzupełnieniu do trwającego leczenia przeciwdepresyjnego. Średnia zmiana masy ciała u pacjentów otrzymujących skojarzenie ABILIFY wyniosła +1,7 kg (N=347) w porównaniu do +0,4 kg (N=330) u pacjentów otrzymujących skojarzone placebo.
Tabela 14 przedstawia odsetek dorosłych pacjentów z przyrostem masy ciała o ≥7% masy ciała według wskazań.
Pacjenci pediatryczni i młodzież
W analizie dwóch kontrolowanych placebo badań u młodzieży ze schizofrenią (13 do 17 lat) i dzieci z chorobą afektywną dwubiegunową (10 do 17 lat) z medianą ekspozycji 42 do 43 dni, średnia zmiana masy ciała w grupie leczonej ABILIFY pacjenci ważyli +1,6 kg (N=381) w porównaniu do +0,3 kg (N=187) u pacjentów otrzymujących placebo. Po 24 tygodniach średnia zmiana masy ciała w stosunku do wartości początkowej w
Pacjenci leczeni ABILIFY ważyli +5,8 kg (n=62) w porównaniu do +1,4 kg (n=13) u pacjentów otrzymujących placebo.
dwóch krótkoterminowych badaniach kontrolowanych placebo u pacjentów (6 do 17 lat) z drażliwością związaną z zaburzeniami autystycznymi z medianą ekspozycji wynoszącą 56 dni, średnia zmiana masy ciała u pacjentów leczonych ABILIFY wyniosła +1,6 kg (n=209). ) w porównaniu do +0,4 kg (n=98) u pacjentów otrzymujących placebo.
W dwóch krótkoterminowych badaniach kontrolowanych placebo u pacjentów (6 do 18 lat) z zespołem Tourette'a z medianą ekspozycji wynoszącą 57 dni, średnia zmiana masy ciała u pacjentów leczonych ABILIFY wyniosła +1,5 kg (n=105). ) w porównaniu do +0,4 kg (n=66) u pacjentów otrzymujących placebo.
Tabela 15 przedstawia odsetek pacjentów pediatrycznych i młodzieżowych z przyrostem masy ciała ≥7% masy ciała według wskazań.
otwartym badaniu, do którego włączono pacjentów z dwóch kontrolowanych placebo badań obejmujących młodzież ze schizofrenią (13 do 17 lat) i dzieci z chorobą afektywną dwubiegunową (10 do 17 lat), 73,2% pacjentów (238/325) ukończyło 26 tygodni terapii preparatem ABILIFY. Po 26 tygodniach 32,8% pacjentów przybrało ≥7% masy ciała, nieskorygowanej na normalny wzrost. Aby skorygować normalny wzrost, wyprowadzono z-scores (mierzone w odchyleniach standardowych [SD]), które normalizują naturalny wzrost pacjentów pediatrycznych i młodzieży przez porównanie ze standardami populacji dopasowanymi pod względem wieku i płci. Zmiana z-score
otwartym badaniu, do którego włączono pacjentów z dwóch krótkoterminowych, kontrolowanych placebo badań, pacjentów (6 do 17 lat) z drażliwością związaną z zaburzeniami autystycznymi, jak również pacjentów de novo, 60,3% (199/330) ukończyło jedno badanie. rok terapii preparatem ABILIFY. Średnia zmiana wagi z-score wyniosła 0,26 SD dla pacjentów otrzymujących >9 miesięcy leczenia.
Podczas leczenia pacjentów pediatrycznych z jakiegokolwiek wskazania, przyrost masy ciała należy monitorować i oceniać w stosunku do oczekiwanego dla normalnego wzrostu.
Patologiczny hazard i inne kompulsywne zachowania
Opisy przypadków po wprowadzeniu do obrotu sugerują, że pacjenci mogą odczuwać intensywne popędy, zwłaszcza związane z hazardem, oraz niemożność kontrolowania tych popędów podczas przyjmowania arypiprazolu. Inne kompulsywne popędy, zgłaszane rzadziej, obejmują: popęd seksualny, zakupy, jedzenie lub napadowe objadanie się oraz inne impulsywne lub kompulsywne zachowania. Ponieważ pacjenci mogą nie rozpoznać tych zachowań jako nienormalnych, ważne jest, aby lekarze przepisujący leki pytali pacjentów lub ich opiekunów konkretnie o rozwój nowych lub intensywnych popędów hazardowych, kompulsywnych popędów seksualnych, kompulsywnych zakupów, objadania się lub kompulsywnego jedzenia lub innych popędów podczas leczenia z arypiprazolem. Należy zauważyć, że objawy kontroli impulsów mogą być związane z podstawowym zaburzeniem. W niektórych przypadkach, choć nie we wszystkich, popędy ustały po zmniejszeniu dawki lub odstawieniu leku. Zachowania kompulsywne mogą spowodować krzywdę pacjenta i innych, jeśli nie zostaną rozpoznane. Rozważ zmniejszenie dawki lub odstawienie leku, jeśli u pacjenta wystąpi taka potrzeba.
Niedociśnienie ortostatyczne
ABILIFY 20mg może powodować niedociśnienie ortostatyczne, być może ze względu na antagonizm receptora α1-adrenergicznego. Częstość występowania zdarzeń związanych z niedociśnieniem ortostatycznym w krótkoterminowych, kontrolowanych placebo badaniach dorosłych pacjentów stosujących ABILIFY doustnie (n=2467) obejmowała (częstość występowania ABILIFY 20 mg, częstość występowania placebo) niedociśnienie ortostatyczne (1%, 0,3%), zawroty głowy związane z postawą ciała ( 0,5%, 0,3% i omdlenia (0,5%, 0,4%); pacjentów pediatrycznych w wieku od 6 do 18 lat (n=732) leczonych doustnym preparatem ABILIFY obejmowało niedociśnienie ortostatyczne (0,5%, 0%), zawroty głowy związane ze zmianą pozycji ciała (0,4%, 0%) i omdlenia (0,2%, 0%); oraz pacjentów otrzymujących ABILIFY (n=501) obejmowały niedociśnienie ortostatyczne (0,6%, 0%), zawroty głowy związane z ortostazą (0,2%, 0,5%), i omdlenia (0,4%, 0%) [patrz DZIAŁANIA NIEPOŻĄDANE ].
Częstość występowania istotnej ortostatycznej zmiany ciśnienia krwi (definiowanej jako spadek skurczowego ciśnienia krwi ≥20 mmHg z towarzyszącym wzrostem częstości akcji serca ≥25 uderzeń na minutę przy porównywaniu wartości w pozycji stojącej i leżącej) dla ABILIFY nie różniła się istotnie od placebo (częstość występowania ABILIFY , częstość występowania placebo): u dorosłych pacjentów leczonych doustnie ABILIFY (4%, 2%), u dzieci i młodzieży doustnie
Pacjenci w wieku od 6 do 18 lat leczeni ABILIFY (0,4%, 1%) lub pacjenci leczeni ABILIFY 15 mg we wstrzyknięciach (3%, 2%).
ABILIFY 20 mg należy stosować ostrożnie u pacjentów z rozpoznaną chorobą sercowo-naczyniową (zawał mięśnia sercowego lub choroba niedokrwienna serca w wywiadzie, niewydolność serca lub zaburzenia przewodzenia), choroba naczyń mózgowych lub stany predysponujące pacjentów do niedociśnienia (odwodnienie, hipowolemia i leczenie przeciwnadciśnieniowe leki) [patrz INTERAKCJE Z LEKAMI ].
Jeśli pozajelitowe leczenie benzodiazepinami zostanie uznane za konieczne oprócz leczenia wstrzyknięciami ABILIFY, pacjentów należy monitorować pod kątem nadmiernej sedacji i hipotonii ortostatycznej [patrz INTERAKCJE Z LEKAMI ].
Spada
Leki przeciwpsychotyczne, w tym ABILIFY 10 mg, mogą powodować senność, niedociśnienie ortostatyczne, niestabilność ruchową i czuciową, co może prowadzić do upadków, a w konsekwencji złamań lub innych urazów. W przypadku pacjentów z chorobami, stanami lub lekami, które mogą nasilać te skutki, należy przeprowadzić pełną ocenę ryzyka upadków na początku leczenia przeciwpsychotycznego oraz ponownie w przypadku pacjentów poddawanych długotrwałemu leczeniu przeciwpsychotycznemu.
leukopenia, neutropenia i agranulocytoza
W badaniach klinicznych i (lub) po wprowadzeniu produktu do obrotu zgłaszano przypadki leukopenii i neutropenii związane czasowo ze środkami przeciwpsychotycznymi, w tym ABILIFY. Zgłaszano również agranulocytozę.
Możliwe czynniki ryzyka leukopenii/neutropenii obejmują istniejącą wcześniej małą liczbę białych krwinek (WBC)/bezwzględną liczbę neutrofili (ANC) oraz historię leukopenii/neutropenii polekowej. U pacjentów z klinicznie istotnym niskim WBC/ANC lub polekową leukopenią/neutropenią w ciągu pierwszych kilku miesięcy leczenia należy często wykonywać pełną morfologię krwi (CBC). U takich pacjentów należy rozważyć przerwanie stosowania ABILIFY przy pierwszych objawach klinicznie istotnego zmniejszenia liczby białych krwinek przy braku innych czynników sprawczych.
Monitorować pacjentów z klinicznie istotną neutropenią pod kątem gorączki lub innych objawów lub oznak infekcji i niezwłocznie leczyć, jeśli takie objawy lub oznaki wystąpią. Należy odstawić ABILIFY 20 mg u pacjentów z ciężką neutropenią (bezwzględna liczba neutrofili
Drgawki/konwulsje
krótkoterminowych, kontrolowanych placebo badaniach, pacjenci z napadami drgawkowymi w wywiadzie wykluczali napady/drgawki występujące u 0,1% (3/2467) niezdiagnozowanych dorosłych pacjentów leczonych doustnie ABILIFY 20 mg, u 0,1% (1/732) pacjentów pediatrycznych (6 do 18 lat) oraz u 0,2% (1/501) dorosłych pacjentów leczonych preparatem ABILIFY 15 mg we wstrzyknięciach.
Podobnie jak w przypadku innych leków przeciwpsychotycznych, ABILIFY 15 mg należy stosować ostrożnie u pacjentów z drgawkami w wywiadzie lub ze stanami obniżającymi próg drgawkowy. Stany, które obniżają próg drgawkowy, mogą występować częściej w populacji osób w wieku 65 lat lub starszych.
Możliwość upośledzenia funkcji poznawczych i motorycznych
ABILIFY, podobnie jak inne leki przeciwpsychotyczne, może potencjalnie zaburzać osąd, myślenie lub zdolności motoryczne. Na przykład w krótkoterminowych badaniach kontrolowanych placebo senność (w tym sedację) zgłaszano w następujący sposób (częstość występowania ABILIFY, częstość występowania placebo): u dorosłych pacjentów (n=2467) leczonych doustnie ABILIFY (11%, 6%), u dzieci w wieku od 6 do 17 lat (n=611) (24%, 6%) oraz u pacjentów dorosłych (n=501) przyjmujących ABILIFY Injection (9%, 6%). Senność (w tym sedacja) doprowadziła do przerwania leczenia u 0,3% (8/2467) dorosłych pacjentów i 3% (20/732) dzieci (6 do 18 lat) doustnego ABILIFY 10 mg w krótkotrwałych badaniach kontrolowanych placebo, ale nie doprowadziło do przerwania leczenia przez dorosłych pacjentów przyjmujących ABILIFY Injection.
Pomimo stosunkowo niewielkiego wzrostu częstości występowania tych zdarzeń w porównaniu z placebo, pacjentów należy ostrzec przed obsługą niebezpiecznych maszyn, w tym samochodów, dopóki nie upewnią się, że terapia ABILIFY 15 mg nie wpływa na nich niekorzystnie.
Regulacja temperatury ciała
Zakłócenie zdolności organizmu do obniżania temperatury głębokiej ciała przypisuje się środkom przeciwpsychotycznym. Zaleca się zachowanie odpowiedniej ostrożności podczas przepisywania ABILIFY 10 mg pacjentom, u których wystąpią stany, które mogą przyczyniać się do wzrostu temperatury głębokiej ciała (np. intensywny wysiłek fizyczny, ekspozycja na ekstremalne ciepło, jednoczesne przyjmowanie leków o działaniu antycholinergicznym lub odwodnienie) [Widzieć DZIAŁANIA NIEPOŻĄDANE ].
Samobójstwo
Możliwość próby samobójczej jest nierozerwalnie związana z chorobami psychotycznymi, chorobą dwubiegunową i dużą depresją, a farmakoterapii powinien towarzyszyć ścisły nadzór nad pacjentami wysokiego ryzyka. Recepty na ABILIFY należy wypisać na najmniejszą ilość, zgodną z dobrym postępowaniem z pacjentem, aby zmniejszyć ryzyko przedawkowania [patrz DZIAŁANIA NIEPOŻĄDANE ].
Dysfagia
Zaburzenia motoryki przełyku i aspiracja były związane ze stosowaniem leków przeciwpsychotycznych, w tym ABILIFY. Aspiracyjne zapalenie płuc jest częstą przyczyną zachorowalności i śmiertelności u pacjentów w podeszłym wieku, zwłaszcza z zaawansowaną demencją Alzheimera. ABILIFY i inne leki przeciwpsychotyczne należy stosować ostrożnie u pacjentów z ryzykiem zachłystowego zapalenia płuc [patrz Zwiększona śmiertelność u starszych pacjentów z psychozą związaną z demencją Â i DZIAŁANIA NIEPOŻĄDANE ].
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( Przewodnik po lekach ).
Omów następujące kwestie z pacjentami, którym przepisano ABILIFY:
Kliniczne pogorszenie ryzyka depresji i samobójstwa
Należy zachęcać pacjentów, ich rodziny i ich opiekunów do wyczulenia na pojawienie się lęku, pobudzenia, ataków paniki, bezsenności, drażliwości, wrogości, agresywności, impulsywności, akatyzji (niepokoju psychoruchowego), hipomanii, manii i innych nietypowych zmian w zachowaniu , nasilenie depresji i myśli samobójcze, szczególnie na początku leczenia przeciwdepresyjnego oraz przy zwiększaniu lub zmniejszaniu dawki. Rodzinom i opiekunom pacjentów należy zalecić, aby codziennie zwracali uwagę na pojawienie się takich objawów, ponieważ zmiany mogą być nagłe. Takie objawy należy zgłaszać lekarzowi lub pracownikowi służby zdrowia, zwłaszcza jeśli są one ciężkie, mają nagły początek lub nie były częścią objawów występujących u pacjenta. Takie objawy mogą wiązać się ze zwiększonym ryzykiem myśli i zachowań samobójczych i wskazują na potrzebę bardzo ścisłego monitorowania i ewentualnie zmian w leczeniu [patrz OSTRZEŻENIA I ŚRODKI ].
Lekarze przepisujący lek lub inni pracownicy służby zdrowia powinni informować pacjentów, ich rodziny i ich opiekunów o korzyściach i zagrożeniach związanych z leczeniem preparatem ABILIFY oraz powinni doradzać im w zakresie właściwego jego stosowania. Dla ABILIFY dostępny jest przewodnik po lekach dla pacjenta zawierający informacje na temat „Leków przeciwdepresyjnych, depresji i innych poważnych chorób psychicznych oraz myśli lub działań samobójczych”. Lekarz lub pracownik służby zdrowia powinien poinstruować pacjentów, ich rodziny i ich opiekunów, aby przeczytali Przewodnik po lekach i powinni pomóc im w zrozumieniu jego treści. Pacjenci powinni mieć możliwość omówienia treści Przewodnika po lekach i uzyskania odpowiedzi na wszelkie pytania, jakie mogą mieć. Należy zauważyć, że ABILIFY nie jest zatwierdzony jako pojedynczy środek do leczenia depresji i nie był oceniany w pediatrycznym zaburzeniu depresyjnym.
Patologiczny hazard i inne kompulsywne zachowania
Poinformuj pacjentów i ich opiekunów o możliwości wystąpienia kompulsywnego pragnienia robienia zakupów, intensywnego pragnienia hazardu, kompulsywnego pragnienia seksualnego, napadowego objadania się i/lub innych kompulsywnych pragnień oraz niemożności kontrolowania tych pragnień podczas przyjmowania arypiprazolu. W niektórych przypadkach, ale nie we wszystkich, popędy ustały, gdy dawka została zmniejszona lub zatrzymana [patrz OSTRZEŻENIA I ŚRODKI ].
Stosowanie tabletki rozpadającej się w jamie ustnej
Nie otwierać blistra do czasu podania. W celu usunięcia pojedynczej tabletki należy otworzyć opakowanie i oderwać folię z blistra, aby odsłonić tabletkę. Nie należy przepychać tabletki przez folię, ponieważ może to spowodować jej uszkodzenie. Natychmiast po otwarciu blistra, suchymi rękami, wyjąć tabletkę i umieścić całą tabletkę ulegającą rozpadowi w jamie ustnej ABILIFY DISCMELT na języku. W ślinie rozpad tabletki następuje szybko. Zaleca się przyjmowanie ABILIFY DISCMELT bez płynu. Jednak w razie potrzeby można go popijać płynem. Nie próbuj dzielić tabletu.
Zakłócenia sprawności poznawczej i motorycznej
Ponieważ ABILIFY może potencjalnie zaburzać osąd, myślenie lub zdolności motoryczne, pacjentów należy ostrzec przed obsługą niebezpiecznych maszyn, w tym samochodów, dopóki nie upewnią się, że terapia ABILIFY nie wpływa na nich niekorzystnie [patrz OSTRZEŻENIA I ŚRODKI ].
Leki towarzyszące
Pacjentom należy doradzić, aby informowali swoich lekarzy o przyjmowaniu lub planowaniu przyjmowania jakichkolwiek leków na receptę lub leków dostępnych bez recepty, ponieważ istnieje możliwość interakcji [patrz INTERAKCJE Z LEKAMI ].
Ekspozycja na ciepło i odwodnienie
Pacjentów należy pouczyć o zachowaniu odpowiedniej ostrożności w celu uniknięcia przegrzania i odwodnienia [patrz OSTRZEŻENIA I ŚRODKI ].
Zawartość cukru
Należy poinformować pacjentów, że każdy mililitr ABILIFY 10 mg roztworu doustnego zawiera 400 mg sacharozy i 200 mg fruktozy.
Ciąża
Należy doradzić pacjentkom, aby powiadomiły swojego lekarza, jeśli zajdą w ciążę lub zamierzają zajść w ciążę podczas leczenia lekiem ABILIFY. Należy poinformować pacjentów, że ABILIFY 20 mg może powodować objawy pozapiramidowe i/lub objawy odstawienia (pobudzenie, hipertonia, hipotonia, drżenie, senność, niewydolność oddechowa i zaburzenia odżywiania) u noworodka. Poinformuj pacjentki, że istnieje rejestr ciąż, który monitoruje przebieg ciąży u kobiet narażonych na działanie ABILIFY 15 mg podczas ciąży [patrz Używaj w określonych populacjach ].
Fenyloketonuryka
Fenyloalanina jest składnikiem aspartamu. Każda tabletka ulegająca rozpadowi w jamie ustnej ABILIFY DISCMELT zawiera następujące ilości: 10 mg, 1,12 mg fenyloalaniny i 15 mg, 1,68 mg fenyloalaniny.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Karcynogeneza
Badania rakotwórczości w ciągu całego życia przeprowadzono na myszach ICR, szczurach F344 i szczurach Sprague-Dawley (SD). Arypiprazol podawano przez 2 lata w diecie w dawkach 1, 3, 10 i 30 mg/kg/dzień myszom ICR oraz 1, 3 i 10 mg/kg/dzień szczurom F344 (0,2, 0,5, 2 i 5 razy i 0,3, 1 i 3 razy MRHD 30 mg/dobę na podstawie, odpowiednio, mg/m2 powierzchni ciała). Ponadto szczurom SD podawano doustnie przez 2 lata dawki 10, 20, 40 i 60 mg/kg/dobę, co stanowi 3, 6, 13 i 19-krotność MRHD na podstawie mg/m2 powierzchni ciała. Arypiprazol nie wywoływał nowotworów u samców myszy ani samców szczurów. U samic myszy częstość występowania gruczolaków przysadki oraz gruczolakoraków i gruczolakoraków gruczołu sutkowego była zwiększona przy dawkach dietetycznych od 3 do 30 mg/kg/dobę (od 0,5 do 5 razy większa od MRHD). U samic szczurów częstość występowania gruczolakowłókniaków gruczołu sutkowego była zwiększona po podaniu dawki pokarmowej 10 mg/kg/dobę (3-krotność MRHD); a częstość występowania raków kory nadnerczy i połączonych gruczolaków/raków kory nadnerczy wzrosła przy dawce doustnej 60 mg/kg/dzień (19-krotność MRHD).
gryzoni po długotrwałym podawaniu innych leków przeciwpsychotycznych stwierdzano wzrost liczby nowotworów sutka, przysadki i trzustki. Prolaktyny w surowicy nie mierzono w badaniach rakotwórczości arypiprazolu. Jednak wzrost poziomu prolaktyny w surowicy zaobserwowano u samic myszy w 13-tygodniowym badaniu żywieniowym przy dawkach związanych z guzami gruczołu sutkowego i przysadki. Prolaktyna w surowicy nie była zwiększona u samic szczurów w 4-tygodniowych i 13-tygodniowych badaniach żywieniowych w dawkach związanych z guzami gruczołu sutkowego. Znaczenie guzów endokrynnych zależnych od prolaktyny u gryzoni dla ryzyka u ludzi jest niejasne.
Mutageneza
Potencjał mutagenny arypiprazolu badano w teście odwrotnej mutacji bakteryjnej in vitro, teście naprawy bakteryjnego DNA in vitro, teście postępującej mutacji genowej in vitro w komórkach chłoniaka myszy, teście aberracji chromosomowych in vitro w płucu chomika chińskiego (CHL). komórek, test mikrojądrowy in vivo u myszy oraz test nieplanowej syntezy DNA u szczurów. Arypiprazol i jego metabolit (2,3-DCPP) były klastogenne w teście aberracji chromosomowych in vitro w komórkach CHL z aktywacją metaboliczną lub bez niej. Metabolit, 2,3DCPP, zwiększył aberracje liczbowe w teście in vitro w komórkach CHL przy braku aktywacji metabolicznej. Pozytywną odpowiedź uzyskano w teście mikrojądrowym in vivo u myszy; jednak odpowiedź była spowodowana mechanizmem, który nie jest uważany za istotny dla ludzi.
Upośledzenie płodności
Samicom szczurów podawano doustnie arypiprazol od 2 tygodni przed kryciem do 7 dnia ciąży w dawkach 2, 6 i 20 mg/kg/dobę, co stanowi 0,6, 2 i 6 razy MRHD wynoszące 30 mg/dobę na podstawie mg/m² powierzchni ciała. We wszystkich dawkach obserwowano nieprawidłowości cyklu rui i zwiększenie liczby ciałek żółtych, ale nie zaobserwowano zaburzeń płodności. Zwiększona utrata przed implantacją była obserwowana przy 2 i 6 krotności MRHD, a zmniejszona masa płodu była obserwowana przy 6 krotności MRHD.
Samcom szczurów podawano doustnie arypiprazol od 9 tygodni przed kryciem poprzez krycie w dawkach 20, 40 i 60 mg/kg/dobę, co stanowi 6, 13 i 19-krotność MRHD 30 mg/dobę w przeliczeniu na mg/ m² powierzchni ciała. Zaburzenia spermatogenezy były obserwowane przy 19-krotności MRHD, a atrofia prostaty była obserwowana przy 13 i 19-krotnie MRHD bez upośledzenia płodności.
Używaj w określonych populacjach
Ciąża
Rejestr ekspozycji w ciąży
Istnieje rejestr ekspozycji w czasie ciąży, który monitoruje przebieg ciąży u kobiet narażonych w czasie ciąży na atypowe leki przeciwpsychotyczne, w tym ABILIFY. Zachęcamy świadczeniodawców do rejestrowania pacjentów, kontaktując się z Krajowym Rejestrem Ciąży dla Atypowych Leków Przeciwpsychotycznych pod numerem 1-866-961-2388 lub odwiedzając stronę http://womensmentalhealth.org/clinical-and-researchprograms/pregnancyregistry/.
Podsumowanie ryzyka
Noworodki narażone w trzecim trymestrze ciąży na leki przeciwpsychotyczne, w tym ABILIFY 20 mg, są narażone na wystąpienie objawów pozapiramidowych i/lub objawów odstawienia po porodzie (patrz Rozważania kliniczne ). Ogólne dostępne dane z opublikowanych badań epidemiologicznych kobiet w ciąży narażonych na arypiprazol nie wykazały związanego z lekiem ryzyka wystąpienia poważnych wad wrodzonych, poronienia lub niekorzystnych skutków dla matki lub płodu (patrz Dane ). Istnieje ryzyko dla matki związane z nieleczoną schizofrenią, zaburzeniem afektywnym dwubiegunowym typu I lub ciężką depresją oraz z ekspozycją na leki przeciwpsychotyczne, w tym ABILIFY, w czasie ciąży (patrz Rozważania kliniczne ).
W badaniach reprodukcji na zwierzętach, doustne i dożylne podawanie arypiprazolu podczas organogenezy szczurom i (lub) królikom w dawkach, odpowiednio, 10 i 19-krotnych, wytworzyło maksymalną zalecaną dawkę u ludzi (MRHD) wynoszącą 30 mg/dobę na podstawie mg/m2 śmierć płodu, zmniejszona masa płodu, niezstąpione jądra, opóźnione kostnienie szkieletu, nieprawidłowości szkieletu i przepuklina przeponowa. Doustne i dożylne podawanie arypiprazolu szczurom w okresie przed- i pourodzeniowym w dawkach 10 razy większych niż MRHD na podstawie mg/m2 powierzchni ciała powodowało wydłużenie ciąży, martwe urodzenia, zmniejszenie masy ciała i skrócenie przeżycia młodych (patrz Dane ).
Szacowane ryzyko tła poważnych wad wrodzonych i poronienia dla wskazanej populacji jest nieznane. Wszystkie ciąże wiążą się z ryzykiem wady wrodzonej, utraty lub innych niekorzystnych skutków. W ogólnej populacji USA szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2-4% i 15-20%.
Rozważania kliniczne
Ryzyko związane z chorobą u matki i/lub zarodka/płodu
Istnieje ryzyko dla matki z powodu nieleczonej schizofrenii lub choroby afektywnej dwubiegunowej typu I, w tym zwiększone ryzyko nawrotu, hospitalizacji i samobójstwa. Schizofrenia i choroba afektywna dwubiegunowa typu I wiążą się z częstszymi niekorzystnymi następstwami okołoporodowymi, w tym przedwczesnym porodem. Nie wiadomo, czy jest to bezpośredni skutek choroby, czy innych współistniejących czynników.
Prospektywne, podłużne badanie objęło 201 ciężarnych kobiet z wywiadem poważnych zaburzeń depresyjnych, które były w stanie eutymii i przyjmowały leki przeciwdepresyjne na początku ciąży. Kobiety, które odstawiły leki przeciwdepresyjne w czasie ciąży, częściej doświadczały nawrotu ciężkiej depresji niż kobiety, które kontynuowały przyjmowanie leków przeciwdepresyjnych. Rozważ ryzyko nieleczonej depresji, przerywając lub zmieniając leczenie lekami przeciwdepresyjnymi w czasie ciąży i połogu.
Działania niepożądane u płodu/noworodka
noworodków narażonych na leki przeciwpsychotyczne (w tym ABILIFY) w trzecim trymestrze ciąży zgłaszano objawy pozapiramidowe i (lub) odstawienia, w tym pobudzenie, hipertonię, hipotonię, drżenie, senność, niewydolność oddechową i zaburzenia odżywiania. Objawy te miały różne nasilenie. Monitoruj noworodki pod kątem objawów pozapiramidowych i/lub objawów odstawienia i odpowiednio zarządzaj objawami. Niektóre noworodki wyzdrowiały w ciągu kilku godzin lub dni bez specjalnego leczenia; inne wymagały przedłużonej hospitalizacji.
Dane
Dane ludzkie
Opublikowane dane z badań obserwacyjnych, rejestrów urodzeń i opisów przypadków stosowania atypowych leków przeciwpsychotycznych podczas ciąży nie wykazują wyraźnego związku z lekami przeciwpsychotycznymi i poważnymi wadami wrodzonymi. Badanie retrospektywne z bazy danych Medicaid obejmującej 9258 kobiet narażonych na leki przeciwpsychotyczne w czasie ciąży nie wykazało ogólnego zwiększonego ryzyka poważnych wad wrodzonych.
Dane zwierząt
badaniach na zwierzętach arypiprazol wykazał toksyczny wpływ na rozwój, w tym możliwe działanie teratogenne u szczurów i królików.
ciężarnych szczurów leczonych doustnie arypiprazolem podczas organogenezy w dawkach 3, 10 i 30 mg/kg/dobę, co stanowi około 1, 3 i 10 razy MRHD wynoszącą 30 mg/dobę w przeliczeniu na mg/m2 powierzchni ciała, Niewielkie wydłużenie ciąży i opóźnienie rozwoju płodu, o czym świadczy zmniejszona masa płodu i niezstąpione jądra, obserwowano przy 10-krotnej MRHD. Opóźnione kostnienie szkieletu obserwowano przy 3 i 10 krotności MRHD. Urodzone potomstwo miało zwiększoną częstość występowania guzków wątrobowo-przeponowych, a przepuklinę przeponową obserwowano przy 10-krotnej MRHD (inne grupy dawek nie były badane pod kątem tych wyników). Po urodzeniu, opóźnione otwarcie pochwy było obserwowane przy 3 i 10 krotności MRHD. Zaburzenie zdolności rozrodczych (zmniejszony wskaźnik płodności, ciałka żółte, implanty, żywe płody i zwiększona utrata po implantacji, prawdopodobnie pośredniczona przez wpływ na potomstwo płci żeńskiej) obserwowano przy 10-krotnej MRHD; jednak nie było dowodów sugerujących, że te skutki rozwojowe były wtórne do toksyczności matczynej.
ciężarnych szczurów, którym w trakcie organogenezy wstrzyknięto dożylnie arypiprazol w dawkach 3, 9 i 27 mg/kg/dobę, co stanowi 1, 3 i 9-krotność MRHD wynoszącą 30 mg/dobę w przeliczeniu na mg/m2 powierzchni ciała masę płodu i opóźnione kostnienie szkieletu obserwowano przy 9-krotności MRHD; dawka ta powodowała również toksyczność u matek.
U ciężarnych królików leczonych doustnie arypiprazolem podczas organogenezy w dawkach 10, 30 i 100 mg/kg/dobę, które są 6, 19 i 65 razy większe od MRHD 30 mg/dobę w przeliczeniu na mg/m2 powierzchni ciała, zmniejszenie spożycie pokarmu i zwiększone aborcje, a także zwiększoną śmiertelność płodów zaobserwowano przy 65-krotności MHRD. Zmniejszoną masę płodu i zwiększoną częstość występowania zrośniętych mostków mostkowych obserwowano przy 19 i 65-krotności MRHD.
ciężarnych królików, którym podano dożylnie arypiprazol podczas organogenezy w dawkach 3, 10 i 30 mg/kg/dobę, co stanowi 2, 6 i 19-krotność MRHD 30 mg/dobę w przeliczeniu na mg/m2 powierzchni ciała masa płodu, zwiększone nieprawidłowości płodu (głównie szkieletowe) i zmniejszone kostnienie szkieletu płodu obserwowano przy 19-krotności MRHD; dawka ta powodowała również toksyczność u matek. Płodowa dawka niepowodująca efektu wynosiła 10 mg/kg/dobę, co jest sześciokrotnością MRHD.
U szczurów leczonych doustnie arypiprazolem około- i pourodzeniowym od 17. dnia ciąży do 21. dnia poporodowego w dawkach 3, 10 i 30 mg/kg/dobę, które są 1, 3 i 10 razy większe niż MRHD wynoszące 30 mg/dobę na podstawie mg/m2 powierzchni ciała zaobserwowano nieznaczną toksyczność u matki i nieznaczne wydłużenie ciąży przy 10-krotności MHRD. Przy tej dawce zaobserwowano również wzrost liczby martwych urodzeń oraz zmniejszenie masy młodych (utrzymujących się do dorosłości) i przeżywalności.
szczurów, którym wstrzyknięto dożylnie arypiprazol od 6. dnia ciąży do 20. dnia laktacji w dawkach 3, 8 i 20 mg/kg/dobę, co stanowi 1, 3 i 6 razy MRHD 30 mg/dobę w przeliczeniu na mg/m² powierzchnia ciała, zaobserwowano zwiększoną liczbę martwych urodzeń przy 3 i 6 krotności MRHD; a zmniejszenie masy ciała i przeżycia we wczesnym okresie poporodowym było obserwowane przy 6-krotności MRHD; dawki te powodowały również pewną toksyczność dla matki. Nie stwierdzono wpływu na rozwój behawioralny i reprodukcyjny po urodzeniu.
Laktacja
Podsumowanie ryzyka
Ograniczone dane z opublikowanego piśmiennictwa wskazują na obecność arypiprazolu w mleku kobiecym we względnych dawkach dla niemowląt w zakresie od 0,7% do 8,3% dawki dostosowanej do masy ciała matki. Istnieją doniesienia o słabym przybieraniu na wadze u niemowląt karmionych piersią narażonych na arypiprazol oraz o niedostatecznej podaży mleka u kobiet karmiących piersią przyjmujących arypiprazol.
Należy wziąć pod uwagę korzyści rozwojowe i zdrowotne wynikające z karmienia piersią, a także kliniczne zapotrzebowanie matki na ABILIFY i wszelkie potencjalne niekorzystne skutki ABILIFY u karmionego piersią dziecka lub wynikające z tego schorzenia matki.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność u dzieci i młodzieży z ciężkimi zaburzeniami depresyjnymi lub pobudzeniem związanym ze schizofrenią lub manią dwubiegunową nie zostały ustalone.
Farmakokinetyka arypiprazolu i dehydroarypiprazolu u dzieci w wieku od 10 do 17 lat była podobna do farmakokinetyki u dorosłych po uwzględnieniu różnic w masie ciała [patrz FARMAKOLOGIA KLINICZNA ].
Schizofrenia
Bezpieczeństwo i skuteczność u pacjentów pediatrycznych ze schizofrenią ustalono w 6-tygodniowym badaniu klinicznym kontrolowanym placebo z udziałem 202 pacjentów pediatrycznych w wieku od 13 do 17 lat [patrz DAWKOWANIE I SPOSÓB PODAWANIA , DZIAŁANIA NIEPOŻĄDANE , oraz Studia kliniczne ]. Chociaż skuteczność leczenia podtrzymującego u dzieci nie była systematycznie oceniana, skuteczność leczenia podtrzymującego można ekstrapolować na podstawie danych dotyczących dorosłych wraz z porównaniami parametrów farmakokinetycznych arypiprazolu u pacjentów dorosłych i dzieci.
Zaburzenie dwubiegunowe typu I
Bezpieczeństwo i skuteczność u pacjentów pediatrycznych z manią afektywną dwubiegunową ustalono w 4-tygodniowym, kontrolowanym placebo badaniu klinicznym z udziałem 197 pacjentów pediatrycznych w wieku od 10 do 17 lat [patrz DAWKOWANIE I SPOSÓB PODAWANIA , DZIAŁANIA NIEPOŻĄDANE , oraz Studia kliniczne ]. Chociaż skuteczność leczenia podtrzymującego u dzieci nie była systematycznie oceniana, skuteczność leczenia podtrzymującego można ekstrapolować na podstawie danych dotyczących dorosłych wraz z porównaniami parametrów farmakokinetycznych arypiprazolu u pacjentów dorosłych i dzieci.
Skuteczność wspomagającego stosowania ABILIFY 10 mg z litem lub walproinianem w leczeniu epizodów maniakalnych lub mieszanych u dzieci nie była systematycznie oceniana. Jednak taką skuteczność i brak interakcji farmakokinetycznych między arypiprazolem a litem lub walproinianem można ekstrapolować na podstawie danych dotyczących dorosłych, wraz z porównaniami parametrów farmakokinetycznych arypiprazolu u pacjentów dorosłych i dzieci.
Drażliwość związana z zaburzeniami autystycznymi
Bezpieczeństwo i skuteczność u pacjentów pediatrycznych wykazujących drażliwość związaną z zaburzeniami autystycznymi ustalono w dwóch 8-tygodniowych badaniach klinicznych kontrolowanych placebo z udziałem 212 pacjentów pediatrycznych w wieku od 6 do 17 lat [patrz WSKAZANIA I ZASTOSOWANIE , DAWKOWANIE I SPOSÓB PODAWANIA , DZIAŁANIA NIEPOŻĄDANE , oraz Studia kliniczne ]. Badanie podtrzymujące przeprowadzono u pacjentów pediatrycznych (w wieku 6 do 17 lat) z drażliwością związaną z zaburzeniami autystycznymi. Pierwsza faza tego badania była fazą otwartą, elastycznie dawkowaną (arypiprazol od 2 do 15 mg/dobę), w której pacjenci byli ustabilizowani (zdefiniowana jako > 25% poprawa w podskali ABC-I oraz ocena CGI-I na poziomie „znacznie ulepszony” lub „bardzo poprawiony”) w ABILIFY przez 12 kolejnych tygodni. W sumie 85 pacjentów zostało ustabilizowanych i weszło do drugiej, 16-tygodniowej fazy podwójnie ślepej próby, w której zostali losowo przydzieleni do kontynuacji leczenia ABILIFY lub przejścia na placebo. W tym badaniu nie ustalono skuteczności ABILIFY w leczeniu podtrzymującym drażliwości związanej z zaburzeniami autystycznymi.
Zaburzenie Tourette'a
Bezpieczeństwo i skuteczność arypiprazolu u pacjentów pediatrycznych z zespołem Tourette'a ustalono w jednym 8-tygodniowym (w wieku od 7 do 17 lat) i jednym 10-tygodniowym badaniu (w wieku od 6 do 18 lat) z udziałem 194 pacjentów pediatrycznych [patrz DAWKOWANIE I SPOSÓB PODAWANIA , DZIAŁANIA NIEPOŻĄDANE , oraz Studia kliniczne ]. Skuteczność podtrzymująca u dzieci i młodzieży nie była systematycznie oceniana.
Badania nad młodymi zwierzętami
Arypiprazol podawany młodym szczurom w dawkach doustnych 10, 20, 40 mg/kg/dobę od odsadzenia (21 dni) do dojrzałości (80 dni) powodował śmiertelność, objawy kliniczne ze strony OUN, zaburzenia pamięci i uczenia się oraz opóźnione dojrzewanie płciowe. . Przy dawce 40 mg/kg/dobę u obu płci zaobserwowano śmiertelność, zmniejszoną aktywność, rozchylone tylne kończyny, zgarbioną postawę, ataksję, drżenie i inne objawy ze strony ośrodkowego układu nerwowego. Ponadto u samców zaobserwowano opóźnione dojrzewanie płciowe. Przy wszystkich dawkach i w sposób zależny od dawki, zaburzenia pamięci i uczenia się, zwiększona aktywność ruchowa i zmiany histopatologiczne w przysadce mózgowej (atrofia), nadnerczach (przerost kory nadnerczy), gruczołach sutkowych (hiperplazja i zwiększone wydzielanie) i żeńskich narządach rozrodczych ( zaobserwowano występowanie śluzu pochwy, zanik endometrium, zmniejszenie liczby ciałek żółtych jajników). Zmiany w żeńskich narządach rodnych uznano za wtórne do wzrostu stężenia prolaktyny w surowicy. Nie można było określić poziomu, przy którym nie obserwuje się szkodliwych zmian (NOAEL), a przy najniższej badanej dawce wynoszącej 10 mg/kg/dobę nie ma marginesu bezpieczeństwa w stosunku do ekspozycji ogólnoustrojowych (AUC0-24) dla arypiprazolu lub jego głównego aktywnego metabolitu u młodzieży przy maksymalnej zalecanej dawce pediatrycznej wynoszącej 15 mg/dobę. Wszystkie działania związane z lekiem były odwracalne po 2-miesięcznym okresie rekonwalescencji, a większość skutków działania leku u młodych szczurów zaobserwowano również u dorosłych szczurów z wcześniej przeprowadzonych badań.
Arypiprazol u młodych psów (w wieku 2 miesięcy) powodował kliniczne objawy ośrodkowego układu nerwowego w postaci drżenia, hipoaktywności, ataksji, leżenia i ograniczonego używania kończyn tylnych, gdy był podawany doustnie przez 6 miesięcy w dawkach 3, 10, 30 mg/kg/dzień. Średnia masa ciała i przyrost masy ciała zmniejszyły się do 18% u kobiet we wszystkich grupach leków w stosunku do wartości kontrolnych. Nie można było określić NOAEL, a przy najniższej badanej dawce 3 mg/kg/dobę nie ma marginesu bezpieczeństwa w stosunku do ekspozycji ogólnoustrojowych (AUC0-24) dla arypiprazolu lub jego głównego aktywnego metabolitu u młodzieży przy maksymalnej zalecanej dawce pediatrycznej dawka 15 mg/dobę. Wszystkie efekty związane z lekiem były odwracalne po 2-miesięcznym okresie rekonwalescencji.
Zastosowanie geriatryczne
Nie zaleca się dostosowywania dawki u pacjentów w podeszłym wieku [patrz OSTRZEŻENIE W PUDEŁKU , OSTRZEŻENIA I ŚRODKI , oraz FARMAKOLOGIA KLINICZNA ].
Spośród 13 543 pacjentów leczonych doustnie ABILIFY 15 mg w badaniach klinicznych, 1073 (8%) było w wieku ≥65 lat, a 799 (6%) miało ≥75 lat. Kontrolowane placebo badania doustnego ABILIFY 10 mg w schizofrenii, dwubiegunowej manii lub zaburzeniu depresyjnym nie obejmowały wystarczającej liczby osób w wieku 65 lat i starszych, aby ustalić, czy reagują oni inaczej niż osoby młodsze.
Spośród 749 pacjentów leczonych preparatem ABILIFY w badaniach klinicznych 99 (13%) miało ≥65 lat, a 78 (10%) miało ≥75 lat. Kontrolowane placebo badania nad wstrzyknięciem ABILIFY u pacjentów z pobudzeniem związanym ze schizofrenią lub manią afektywną dwubiegunową nie obejmowały wystarczającej liczby osób w wieku 65 lat i starszych, aby ustalić, czy reagują oni inaczej niż osoby młodsze.
ABILIFY 15mg nie jest zatwierdzony do leczenia pacjentów z psychozą związaną z chorobą Alzheimera [patrz OSTRZEŻENIE W PUDEŁKU oraz OSTRZEŻENIA I ŚRODKI ].
Słabe metabolizmy CYP2D6
Ze względu na wysokie stężenia arypiprazolu zaleca się dostosowanie dawkowania u pacjentów ze znanym słabym metabolizmem CYP2D6. Około 8% rasy białej i 3–8% czarnoskórych/Afroamerykanów nie może metabolizować substratów CYP2D6 i są klasyfikowani jako słabo metabolizujący (PM) [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz FARMAKOLOGIA KLINICZNA ].
Zaburzenia wątroby i nerek
Nie jest wymagane dostosowanie dawki ABILIFY ze względu na czynność wątroby pacjenta (łagodne do ciężkiego zaburzenia czynności wątroby, wynik w skali Child-Pugh od 5 do 15) lub czynność nerek (łagodne do ciężkiego zaburzenia czynności nerek, współczynnik przesączania kłębuszkowego między 15 i 90 ml/minutę) [patrz FARMAKOLOGIA KLINICZNA ].
Inne specyficzne populacje
Nie jest wymagane dostosowanie dawki preparatu ABILIFY ze względu na płeć pacjenta, rasę lub palenie tytoniu [patrz FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
Do klasyfikacji działań niepożądanych zastosowano terminologię MedDRA.
Ludzkie doświadczenie
badaniach klinicznych i po wprowadzeniu produktu do obrotu na całym świecie zgłaszano działania niepożądane zamierzonego lub przypadkowego przedawkowania doustnego ABILIFY. Obejmują one przedawkowanie samego doustnego ABILIFY 20mg oraz w połączeniu z innymi substancjami. Nie zgłoszono żadnego zgonu w przypadku samego ABILIFY. Największa znana dawka o znanym wyniku obejmowała ostre przyjęcie 1260 mg doustnego ABILIFY (42-krotność maksymalnej zalecanej dawki dobowej) przez pacjenta, który w pełni wyzdrowiał. Zamierzone lub przypadkowe przedawkowanie było również zgłaszane u dzieci (w wieku 12 lat i młodszych) po doustnym połknięciu ABILIFY 10 mg do 195 mg bez zgonów.
Częste działania niepożądane (zgłaszane w co najmniej 5% wszystkich przypadków przedawkowania) zgłaszane po doustnym przedawkowaniu ABILIFY (samego lub w połączeniu z innymi substancjami) obejmują wymioty, senność i drżenie. Inne klinicznie istotne objawy przedmiotowe i podmiotowe obserwowane u jednego lub więcej pacjentów z przedawkowaniem ABILIFY (samego lub z innymi substancjami) obejmują kwasicę, agresję, zwiększenie aktywności aminotransferazy asparaginianowej, migotanie przedsionków, bradykardię, śpiączkę, stan splątania, drgawki, zwiększenie aktywności kinazy kreatynowej we krwi, obniżenie poziomu świadomości, nadciśnienie, hipokaliemia, niedociśnienie, letarg, utrata przytomności, wydłużenie zespołu QRS, wydłużenie odstępu QT, zachłystowe zapalenie płuc, zatrzymanie oddechu, stan padaczkowy i tachykardia.
Zarządzanie przedawkowaniem
Brak szczegółowych informacji dotyczących leczenia przedawkowania ABILIFY. W przypadku przedawkowania należy wykonać elektrokardiogram, a jeśli występuje wydłużenie odstępu QT, należy rozpocząć monitorowanie pracy serca. W przeciwnym razie postępowanie w przypadku przedawkowania powinno koncentrować się na leczeniu podtrzymującym, utrzymaniu odpowiednich dróg oddechowych, natlenieniu i wentylacji oraz opanowaniu objawów. Ścisły nadzór lekarski i monitorowanie powinny być kontynuowane do czasu wyzdrowienia pacjenta.
Węgiel drzewny
W przypadku przedawkowania ABILIFY 10 mg, wczesne podanie węgla może być przydatne w częściowym zapobieganiu wchłaniania arypiprazolu. Podanie 50 g węgla aktywowanego godzinę po podaniu pojedynczej dawki doustnej 15 mg ABILIFY zmniejszyło średnią wartość AUC i Cmax arypiprazolu o 50%.
Hemodializa
Chociaż nie ma informacji na temat wpływu hemodializy na leczenie przedawkowania preparatu ABILIFY, jest mało prawdopodobne, aby hemodializa była użyteczna w leczeniu przedawkowania, ponieważ arypiprazol silnie wiąże się z białkami osocza.
PRZECIWWSKAZANIA
ABILIFY 15 mg jest przeciwwskazany u pacjentów z reakcją nadwrażliwości na arypiprazol w wywiadzie. Reakcje wahały się od świądu/pokrzywki do anafilaksji [patrz DZIAŁANIA NIEPOŻĄDANE ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Mechanizm działania arypiprazolu w schizofrenii lub manii dwubiegunowej jest niejasny. Jednak w skuteczności arypiprazolu w wymienionych wskazaniach może pośredniczyć połączenie częściowego działania agonistycznego na receptory D2 i 5-HT1A oraz działania antagonistycznego na receptory 5-HT2A.
Farmakodynamika
Arypiprazol wykazuje wysokie powinowactwo do receptorów dopaminy D2 i D3, serotoniny 5-HT1A i 5-HT2A (wartości Ki odpowiednio 0,34 nM, 0,8 nM, 1,7 nM i 3,4 nM), umiarkowane powinowactwo do dopaminy D4, serotoniny 5-HT2C i receptory 5-HT7, alfa1-adrenergiczne i histaminowe H1 (wartości Ki odpowiednio 44 nM, 15 nM, 39 nM, 57 nM i 61 nM) oraz umiarkowane powinowactwo do miejsca wychwytu zwrotnego serotoniny (Ki=98 nM). Arypiprazol nie wykazuje znaczącego powinowactwa do cholinergicznych receptorów muskarynowych (IC50>1000 nM).
Farmakokinetyka
Aktywność ABILIFY jest prawdopodobnie spowodowana głównie lekiem macierzystym, aripiprazolem, oraz, w mniejszym stopniu, jego głównym metabolitem, dehydroarypiprazolem, który, jak wykazano, ma powinowactwo do receptorów D2 podobne do leku macierzystego i stanowi 40% macierzystego leku. ekspozycja na lek w osoczu. Średnie okresy półtrwania w fazie eliminacji wynoszą odpowiednio około 75 godzin i 94 godziny dla arypiprazolu i dehydroarypiprazolu. Stężenia w stanie stacjonarnym są osiągane w ciągu 14 dni od podania dla obu aktywnych cząsteczek. Akumulację arypiprazolu można przewidzieć na podstawie farmakokinetyki pojedynczej dawki. W stanie stacjonarnym farmakokinetyka arypiprazolu jest proporcjonalna do dawki. Eliminacja arypiprazolu odbywa się głównie poprzez metabolizm wątrobowy z udziałem dwóch izoenzymów P450: CYP2D6 i CYP3A4. W przypadku osób słabo metabolizujących z udziałem CYP2D6 średni okres półtrwania w fazie eliminacji arypiprazolu wynosi około 146 godzin.
Badania farmakokinetyczne wykazały, że tabletki ulegające rozpadowi w jamie ustnej ABILIFY 10 mg DISCMELT są biorównoważne z tabletkami ABILIFY 15 mg.
Administracja ustna
Wchłanianie
Tabletka: Arypiprazol jest dobrze wchłaniany po podaniu tabletki, osiągając maksymalne stężenie w osoczu w ciągu 3 do 5 godzin; bezwzględna biodostępność po podaniu doustnym postaci tabletki wynosi 87%. ABILIFY 10 mg można podawać z posiłkiem lub bez posiłku. Podawanie tabletki 15 mg ABILIFY ze standardowym posiłkiem wysokotłuszczowym nie miało istotnego wpływu na Cmax lub AUC arypiprazolu lub jego aktywnego metabolitu, dehydroarypiprazolu, ale opóźniło Tmax o 3 godziny w przypadku arypiprazolu i 12 godzin w przypadku dehydroarypiprazolu.
Roztwór doustny: Arypiprazol dobrze się wchłania po podaniu doustnym w postaci roztworu. W równoważnych dawkach stężenia arypiprazolu w osoczu z roztworu były wyższe niż w postaci tabletki. W badaniu względnej biodostępności porównującym farmakokinetykę 30 mg arypiprazolu w postaci roztworu doustnego z 30 mg arypiprazolu w tabletkach u zdrowych osób, stosunek roztworu do tabletki średniej geometrycznej wartości Cmax i AUC wynosił odpowiednio 122% i 114% [patrz DAWKOWANIE I SPOSÓB PODAWANIA ]. Farmakokinetyka pojedynczej dawki arypiprazolu była liniowa i proporcjonalna do dawki pomiędzy dawkami od 5 mg do 30 mg.
Dystrybucja
Objętość dystrybucji arypiprazolu w stanie stacjonarnym po podaniu dożylnym jest duża (404 l lub 4,9 l/kg), co wskazuje na rozległą dystrybucję pozanaczyniową. W stężeniach terapeutycznych arypiprazol i jego główny metabolit wiążą się w ponad 99% z białkami surowicy, głównie z albuminami. U zdrowych ochotników, którym podawano arypiprazol w dawce 0,5 do 30 mg/dobę przez 14 dni, występowało zależne od dawki wysycenie receptora D2, co wskazuje na przenikanie arypiprazolu do mózgu u ludzi.
Metabolizm i eliminacja
Arypiprazol jest metabolizowany głównie przez trzy szlaki biotransformacji: dehydrogenację, hydroksylację i N-dealkilację. Na podstawie badań in vitro stwierdzono, że enzymy CYP3A4 i CYP2D6 są odpowiedzialne za odwodornienie i hydroksylację arypiprazolu, a N-dealkilacja jest katalizowana przez CYP3A4. Arypiprazol jest dominującą cząsteczką leku w krążeniu ogólnoustrojowym. W stanie stacjonarnym, dehydroarypiprazol, aktywny metabolit, stanowi około 40% AUC arypiprazolu w osoczu.
Po podaniu pojedynczej dawki doustnej arypiprazolu znakowanego [14C] około 25% i 55% podanej radioaktywności odzyskano odpowiednio w moczu i kale. Mniej niż 1% niezmienionego arypiprazolu było wydalane z moczem, a około 18% dawki doustnej zostało wydalone w postaci niezmienionej z kałem.
Badania interakcji leków
Wpływ innych leków na ekspozycję arypiprazolu i dehydroarypiprazolu podsumowano odpowiednio na Rysunku 1 i Rysunku 2. Na podstawie symulacji oczekuje się 4,5-krotnego wzrostu średnich wartości Cmax i AUC w stanie stacjonarnym, gdy osoby intensywnie metabolizujące CYP2D6 podawane są z silnymi inhibitorami CYP2D6 i CYP3A4. Oczekuje się 3-krotnego wzrostu średnich wartości Cmax i AUC w stanie stacjonarnym u osób słabo metabolizujących CYP2D6, którym podawano silne inhibitory CYP3A4.
Rysunek 1: Wpływ innych leków na farmakokinetykę arypiprazolu 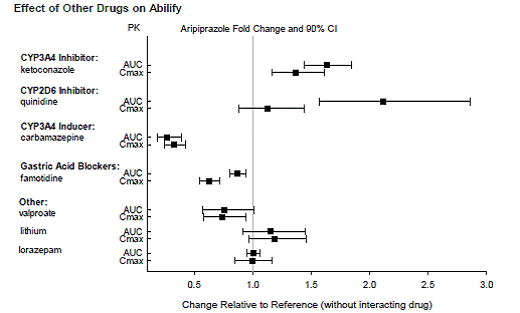
Rysunek 2: Wpływ innych leków na farmakokinetykę dehydroarypiprazolu 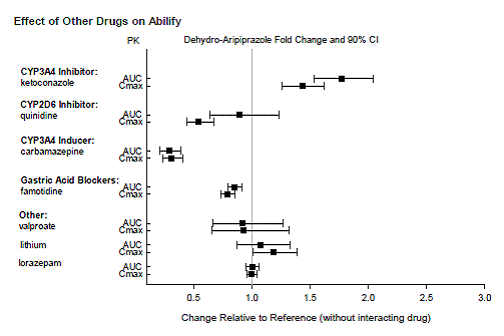
Wpływ ABILIFY 15 mg na ekspozycję na inne leki podsumowano na Rycinie 3. Analiza farmakokinetyki populacyjnej u pacjentów z ciężkimi zaburzeniami depresyjnymi nie wykazała istotnych zmian w stężeniach fluoksetyny w osoczu (20 lub 40 mg/dobę), paroksetyny CR (37,5 lub 50 mg/dobę) lub sertralina (100 lub 150 mg/dobę) podawane do stanu stacjonarnego. Stężenia fluoksetyny i norfluoksetyny w osoczu w stanie stacjonarnym wzrosły odpowiednio o około 18% i 36%, a stężenia paroksetyny zmniejszyły się o około 27%. Stężenia sertraliny i desmetylosertraliny w osoczu w stanie stacjonarnym nie zmieniały się znacząco, gdy te leki przeciwdepresyjne podawano jednocześnie z arypiprazolem.
Rysunek 3: Wpływ ABILIFY 15 mg na farmakokinetykę innych leków 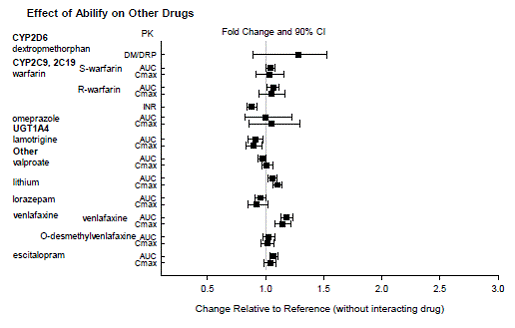
Badania w określonych populacjach
Ekspozycje na arypiprazol i dehydroarypiprazol w określonych populacjach podsumowano odpowiednio na Figurze 4 i Figurze 5. Ponadto u pacjentów pediatrycznych (w wieku 10 do 17 lat) otrzymujących produkt ABILIFY (20 mg do 30 mg) klirens arypiprazolu skorygowany o masę ciała był podobny jak u dorosłych.
Rysunek 4: Wpływ czynników wewnętrznych na farmakokinetykę arypiprazolu 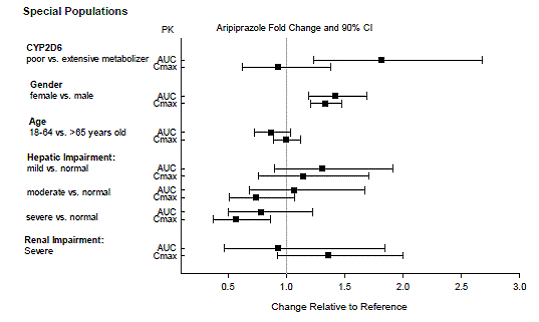
Rysunek 5: Wpływ czynników wewnętrznych na farmakokinetykę dehydroarypiprazolu 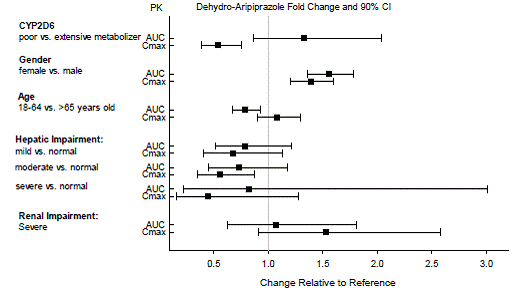
Podawanie domięśniowe
dwóch badaniach farmakokinetycznych arypiprazolu podawanego domięśniowo zdrowym ochotnikom mediana czasu do osiągnięcia maksymalnych stężeń w osoczu wynosiła 1 godzinę i 3 godziny. Domięśniowe wstrzyknięcie 5 mg arypiprazolu miało całkowitą biodostępność 100%. Średnia geometryczna maksymalnego stężenia osiąganego po podaniu domięśniowym była średnio o 19% wyższa niż Cmax tabletki doustnej. Chociaż ekspozycja ogólnoustrojowa w ciągu 24 godzin była zasadniczo podobna w przypadku wstrzyknięcia domięśniowego arypiprazolu i po podaniu doustnym tabletki, AUC arypiprazolu w ciągu pierwszych 2 godzin po wstrzyknięciu domięśniowym było o 90% większe niż AUC po tej samej dawce co tabletka. U stabilnych pacjentów ze schizofrenią lub zaburzeniem schizoafektywnym farmakokinetyka arypiprazolu po podaniu domięśniowym była liniowa w zakresie dawek od 1 mg do 45 mg. Chociaż metabolizm iniekcji arypiprazolu nie był systematycznie oceniany, nie oczekuje się, że domięśniowa droga podania zmieni szlaki metaboliczne.
Toksykologia i/lub farmakologia zwierząt
Arypiprazol powodował zwyrodnienie siatkówki u szczurów albinosów w 26-tygodniowym badaniu toksyczności przewlekłej przy dawce 60 mg/kg/dobę oraz w 2-letnim badaniu rakotwórczości przy dawkach 40 i 60 mg/kg/dobę, które były 13 i 19 razy MRHD 30 mg/dobę na podstawie mg/m2 powierzchni ciała. Ocena siatkówek myszy albinosów i małp nie ujawniła dowodów na zwyrodnienie siatkówki. Nie przeprowadzono dodatkowych badań w celu dalszej oceny mechanizmu. Znaczenie tego odkrycia dla ryzyka dla ludzi nie jest znane.
Studia kliniczne
Skuteczność preparatów doustnych ABILIFY (arypiprazol) została ustalona w następujących odpowiednich i dobrze kontrolowanych badaniach:
- Cztery badania krótkoterminowe i jedno badanie podtrzymujące u dorosłych pacjentów i jedno badanie krótkoterminowe u młodzieży (w wieku 13-17 lat) ze schizofrenią [patrz Studia kliniczne ]
- Cztery krótkoterminowe badania dotyczące monoterapii i jedno 6-tygodniowe badanie uzupełniające u pacjentów dorosłych i jedno badanie krótkoterminowej monoterapii u dzieci (w wieku 1017) z epizodami maniakalnymi lub mieszanymi [patrz Studia kliniczne ]
- Jedno badanie dotyczące monoterapii podtrzymującej i jedno badanie uzupełniające leczenie podtrzymujące u dorosłych pacjentów z chorobą afektywną dwubiegunową typu I [patrz Studia kliniczne ]
- Dwa krótkoterminowe badania z udziałem dorosłych pacjentów z MDD, którzy mieli niewystarczającą odpowiedź na leczenie przeciwdepresyjne podczas obecnego epizodu [patrz Studia kliniczne ]
- Dwa krótkoterminowe badania u pacjentów pediatrycznych (w wieku 6-17 lat) dotyczące leczenia drażliwości związanej z zaburzeniami autystycznymi [patrz Studia kliniczne ]
- Dwa krótkoterminowe badania u pacjentów pediatrycznych (w wieku 6-18 lat) z chorobą Tourette'a [patrz Studia kliniczne ]
Skuteczność preparatu ABILIFY (arypiprazol) do wstrzykiwań ustalono w następujących odpowiednich i dobrze kontrolowanych badaniach:
- Trzy 24-godzinne badania z udziałem pobudzonych dorosłych pacjentów ze schizofrenią lub maniakalnymi/mieszanymi epizodami choroby afektywnej dwubiegunowej typu I [patrz Studia kliniczne ]
Schizofrenia
Dorośli ludzie
Skuteczność ABILIFY 15 mg w leczeniu schizofrenii oceniano w pięciu krótkoterminowych (4-tygodniowych i 6-tygodniowych), kontrolowanych placebo badaniach klinicznych z udziałem pacjentów hospitalizowanych z ostrym nawrotem, którzy w przeważającej mierze spełniali kryteria DSM-III/IV dla schizofrenii. W czterech z pięciu badań udało się odróżnić ABILIFY od placebo, ale jedno badanie, najmniejsze, nie. Trzy z tych badań obejmowały również aktywną grupę kontrolną składającą się z risperidonu (jedno badanie) lub haloperidolu (dwa badania), ale nie zostały one zaprojektowane tak, aby umożliwić porównanie ABILIFY 20 mg z aktywnymi lekami porównawczymi.
czterech pozytywnych próbach dla ABILIFY 10 mg zastosowano cztery podstawowe miary do oceny objawów psychiatrycznych. Skuteczność oceniano za pomocą łącznej punktacji w Skali Zespołów Pozytywnych i Negatywnych (PANSS). PANSS to 30-elementowa skala, która mierzy pozytywne objawy schizofrenii (7 pozycji), negatywne objawy schizofrenii (7 pozycji) i ogólną psychopatologię (16 pozycji), każda oceniana w skali od 1 (brak) do 7 (skrajne). ; całkowite wyniki PANSS wahają się od 30 do 210. Ocena Clinical Global Impression (CGI) odzwierciedla wrażenie wykwalifikowanego obserwatora, w pełni zaznajomionego z objawami schizofrenii, na temat ogólnego stanu klinicznego pacjenta.
4-tygodniowym badaniu (n=414) porównującym dwie stałe dawki ABILIFY (15 lub 30 mg/dobę) z placebo, obie dawki ABILIFY 10 mg były lepsze od placebo w całkowitym wyniku PANSS (Badanie 1 w Tabeli 26). Podskala pozytywna PANSS i wynik CGI-severity. Ponadto dawka 15 mg była lepsza niż placebo w podskali negatywnej PANSS.
W 4-tygodniowym badaniu (n=404) porównującym dwie stałe dawki ABILIFY (20 lub 30 mg/dobę) z placebo, obie dawki ABILIFY były lepsze od placebo w całkowitym wyniku PANSS (Badanie 2 w Tabeli 26), PANSS podskala dodatnia, podskala ujemna PANSS i wynik CGI-severity.
W 6-tygodniowym badaniu (n=420) porównującym trzy stałe dawki ABILIFY (10, 15 lub 20 mg/dobę) z placebo, wszystkie trzy dawki ABILIFY były lepsze od placebo w całkowitym wyniku PANSS (Badanie 3 w Tabeli 26), podskala dodatnia PANSS i podskala ujemna PANSS.
6-tygodniowym badaniu (n=367) porównującym trzy stałe dawki ABILIFY (2, 5 lub 10 mg/dobę) z placebo, dawka 10 mg ABILIFY była lepsza od placebo w całkowitej punktacji PANSS (Badanie 4 w Tabela 26), główny punkt końcowy badania. Dawki 2 i 5 mg nie wykazały wyższości nad placebo pod względem pierwszorzędowego punktu końcowego.
Tak więc skuteczność dawek dziennych 10, 15, 20 i 30 mg ustalono w dwóch badaniach dla każdej dawki. Wśród tych dawek nie było dowodów na to, że grupy z wyższą dawką oferowały jakąkolwiek przewagę nad grupą o najniższej dawce w tych badaniach.
Badanie podgrup populacji nie ujawniło żadnych wyraźnych dowodów na zróżnicowaną reaktywność ze względu na wiek, płeć lub rasę.
Do badania długoterminowego włączono 310 pacjentów hospitalizowanych lub ambulatoryjnych spełniających kryteria DSM-IV dla schizofrenii, u których w wywiadzie utrzymywały się objawy stabilne pod wpływem innych leków przeciwpsychotycznych przez okres 3 miesięcy lub dłuższy. Pacjenci ci zostali odstawieni od leków przeciwpsychotycznych i przydzieleni losowo do grupy ABILIFY 15 mg/dobę lub placebo na okres do 26 tygodni obserwacji pod kątem nawrotu. Nawrót podczas fazy podwójnie ślepej próby zdefiniowano jako wynik poprawy w skali CGI ≥5 (co najmniej gorszy), wynik ≥5 (umiarkowanie ciężki) w elementach wrogości lub braku współpracy w PANSS lub ≥20% wzrost całkowitego wyniku PANSS. Pacjenci otrzymujący ABILIFY 15 mg/dobę doświadczyli znacznie dłuższego czasu do nawrotu w ciągu kolejnych 26 tygodni w porównaniu do pacjentów otrzymujących placebo (Badanie 5 na Rycinie 6).
Pacjenci pediatryczni
Skuteczność ABILIFY (arypiprazol) w leczeniu schizofrenii u pacjentów pediatrycznych (w wieku od 13 do 17 lat) oceniano w jednym 6-tygodniowym badaniu kontrolowanym placebo u pacjentów ambulatoryjnych, którzy spełniali kryteria DSM-IV dla schizofrenii i uzyskali wynik w skali PANSS ≥70 na początku. W tym badaniu (n=302) porównującym dwie stałe dawki ABILIFY (10 lub 30 mg/dobę) z placebo, ABILIFY 15 mg miareczkowano zaczynając od 2 mg/dobę do dawki docelowej w ciągu 5 dni w grupie leczonej 10 mg/dobę oraz po 11 dniach w grupie leczonej 30 mg/dobę. Obie dawki ABILIFY były lepsze niż placebo w całkowitym wyniku PANSS (Badanie 6 w Tabeli 26), głównym punkcie końcowym badania. Nie wykazano, aby dawka 30 mg/dzień była bardziej skuteczna niż dawka 10 mg/dzień. Chociaż skuteczność leczenia podtrzymującego u dzieci nie była systematycznie oceniana, skuteczność leczenia podtrzymującego można ekstrapolować na podstawie danych dotyczących dorosłych wraz z porównaniami parametrów farmakokinetycznych arypiprazolu u pacjentów dorosłych i dzieci.
Rycina 6: Oszacowanie Kaplana-Meiera skumulowanego odsetka pacjentów z nawrotem (badanie 5 dotyczące schizofrenii) 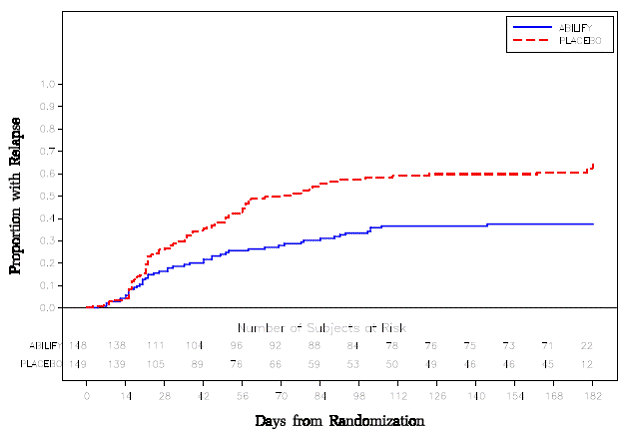
Zaburzenie afektywne dwubiegunowe
Ostre leczenie epizodów maniakalnych i mieszanych
Dorośli ludzie
Monoterapia
Skuteczność ABILIFY 10 mg w monoterapii w ostrym leczeniu epizodów maniakalnych została ustalona w czterech 3-tygodniowych badaniach kontrolowanych placebo u hospitalizowanych pacjentów spełniających kryteria DSM-IV dla zaburzenia afektywnego dwubiegunowego typu I z epizodami maniakalnymi lub mieszanymi. Badania te obejmowały pacjentów z objawami psychotycznymi lub bez nich, a dwa z nich obejmowały również pacjentów z lub bez kursu szybkiego cyklu.
Podstawowym instrumentem używanym do oceny objawów maniakalnych była Skala Oceny Młodej Manii (Y-MRS), 11-punktowa skala oceniana przez klinicystę tradycyjnie stosowana do oceny stopnia symptomatologii maniakalnej w zakresie od 0 (brak cech manii) do 60 ( maksymalny wynik). Kluczowym instrumentem drugorzędnym była skala Clinical Global Impression-Bipolar (CGI-BP).
czterech pozytywnych, 3-tygodniowych, kontrolowanych placebo badaniach (n=268; n=248; n=480; n=485), w których oceniano ABILIFY w zakresie od 15 mg do 30 mg raz na dobę (z dawką początkową 30 mg/dobę w dwóch badaniach i 15 mg/dobę w dwóch badaniach), ABILIFY 20 mg był skuteczniejszy niż placebo pod względem redukcji całkowitego wyniku Y-MRS (Badania 1-4 w Tabeli 27) i CGI-BP ciężkości choroby (mania). W dwóch badaniach z dawką początkową 15 mg/dobę 48% i 44% pacjentów otrzymywało 15 mg/dobę w punkcie końcowym. W dwóch badaniach z dawką początkową 30 mg/dobę 86% i 85% pacjentów przyjmowało w punkcie końcowym dawkę 30 mg/dobę.
Terapia wspomagająca
Skuteczność wspomagającego stosowania ABILIFY z litem lub walproinianem w leczeniu epizodów maniakalnych lub mieszanych została potwierdzona w 6-tygodniowym badaniu kontrolowanym placebo (n=384) z 2-tygodniową wstępną fazą monoterapii lekiem normotymicznym u dorosłych pacjentów którzy spełnili kryteria DSM-IV dla zaburzenia afektywnego dwubiegunowego typu I. Badanie to obejmowało pacjentów z epizodami maniakalnymi lub mieszanymi oraz z cechami psychotycznymi lub bez.
Pacjenci byli początkowo leczeni litem (0,6 do 1,0 mEq/l) lub walproinianem (50 do 125 μg/ml) w stężeniach terapeutycznych w surowicy i pozostawali przy stałych dawkach przez 2 tygodnie. Pod koniec 2 tygodni pacjenci z niewystarczającą odpowiedzią (całkowity wynik YMRS ≥16 i ≤25% poprawa w całkowitym wyniku Y-MRS) na lit lub walproinian zostali losowo przydzieleni do grupy otrzymującej ABILIFY (15 mg/dobę lub zwiększenie do 30 mg/dobę już w 7. dniu lub placebo jako terapia wspomagająca z otwartym litem lub walproinianem. W 6-tygodniowej fazie kontrolowanej placebo, wspomagający ABILIFY rozpoczynający się od 15 mg/dobę z litem lub walproinianem (w zakresie terapeutycznym odpowiednio 0,6 do 1,0 mEq/l lub 50 do 125 μg/ml) był lepszy niż lit lub walproinian z dodatkowym placebo w zmniejszeniu całkowitego wyniku YMRS (badanie 5 w tabeli 27) i wyniku nasilenia choroby (mania) w skali CGI-BP. Siedemdziesiąt jeden procent pacjentów otrzymywało jednocześnie walproinian, a 62% pacjentów otrzymywało lit w dawce 15 mg/dobę w punkcie końcowym po 6 tygodniach.
Pacjenci pediatryczni
Skuteczność ABILIFY 15 mg w leczeniu zaburzenia afektywnego dwubiegunowego typu I u dzieci (w wieku od 10 do 17 lat) oceniano w jednym 4-tygodniowym badaniu kontrolowanym placebo (n=296) z udziałem pacjentów ambulatoryjnych spełniających kryteria DSM-IV dla choroby afektywnej dwubiegunowej Zaburzenie maniakalne lub epizody mieszane z objawami psychotycznymi lub bez nich i wyjściowo uzyskał wynik w skali Y-MRS ≥20. W tym podwójnie ślepym badaniu kontrolowanym placebo porównano dwie stałe dawki ABILIFY (10 lub 30 mg/dobę) z placebo. Dawkę ABILIFY 20 mg rozpoczęto od 2 mg/dobę, którą zwiększono do 5 mg/dobę po 2 dniach, a do dawki docelowej po 5 dniach w grupie 10 mg/dobę i po 13 dniach w grupie 30 mg/dobę. ramię leczenia dziennego. Obie dawki preparatu ABILIFY 10 mg przewyższały placebo pod względem zmiany od wartości początkowej do tygodnia 4 w całkowitym wyniku Y-MRS (Badanie 6 w Tabeli 27).
Leczenie podtrzymujące choroby afektywnej dwubiegunowej I
Monoterapia Terapia podtrzymująca
Przeprowadzono badanie podtrzymujące u dorosłych pacjentów spełniających kryteria DSM-IV dla zaburzenia afektywnego dwubiegunowego typu I z niedawnym epizodem maniakalnym lub mieszanym, ustabilizowanych za pomocą otwartej próby ABILIFY 20 mg i u których odpowiedź kliniczna utrzymywała się przez co najmniej 6 tygodni. Pierwszą fazą tego badania był otwarty okres stabilizacji, w którym pacjenci hospitalizowani i ambulatoryjny byli klinicznie ustabilizowani, a następnie utrzymywani w otwartym badaniu ABILIFY (15 lub 30 mg/dobę, z dawką początkową 30 mg/dobę) przez co najmniej 6 kolejnych tygodni. Następnie stu sześćdziesięciu jeden pacjentów ambulatoryjnych zostało losowo przydzielonych metodą podwójnie ślepej próby, albo do tej samej dawki ABILIFY, którą otrzymywali pod koniec okresu stabilizacji i podtrzymywania, albo do placebo, a następnie monitorowano pod kątem nawrotu maniakalnego lub depresyjnego. Podczas fazy randomizacji ABILIFY przewyższał placebo w czasie w stosunku do liczby połączonych nawrotów afektywnych (maniakalnych i depresyjnych), będących głównym punktem końcowym tego badania (Badanie 7 na Rycinie 7). Podczas fazy leczenia metodą podwójnie ślepej próby zaobserwowano łącznie 55 zdarzeń związanych z nastrojem. Dziewiętnastu było z grupy ABILIFY, a 36 z grupy placebo. Liczba obserwowanych epizodów maniakalnych w grupie ABILIFY 15 mg (6) była mniejsza niż w grupie placebo (19), natomiast liczba epizodów depresyjnych w grupie ABILIFY (9) była podobna do tej w grupie placebo (11) .
Badanie podgrup populacji nie ujawniło żadnych wyraźnych dowodów na zróżnicowaną reaktywność w zależności od wieku i płci; jednak liczba pacjentów w każdej z grup etnicznych była niewystarczająca, aby odpowiednio ocenić różnice między grupami.
Rycina 7: Oszacowanie Kaplana-Meiera skumulowanego odsetka pacjentów z nawrotem (badanie dwubiegunowe 7) 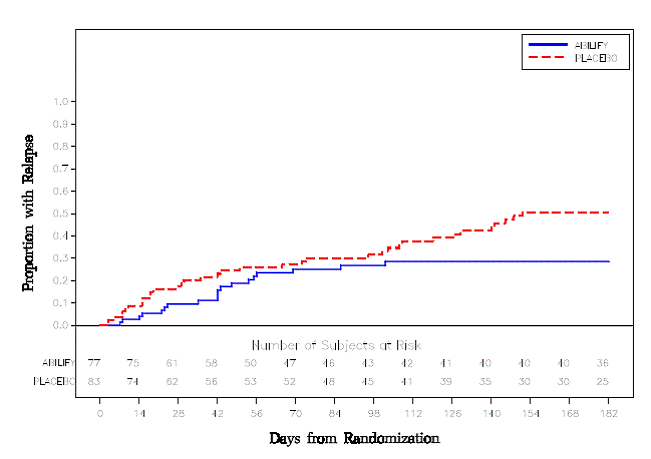
Uzupełniająca terapia podtrzymująca
Przeprowadzono badanie dotyczące leczenia wspomagającego u dorosłych pacjentów spełniających kryteria DSMIV dla choroby afektywnej dwubiegunowej typu I z niedawnym epizodem maniakalnym lub mieszanym. Pacjenci byli początkowo leczeni litem (0,6 do 1,0 mEq/l) lub walproinianem (50 do 125 μg/ml) w stężeniach terapeutycznych w surowicy i pozostawali przy stałych dawkach przez 2 tygodnie. Pod koniec 2 tygodni pacjenci wykazujący niewystarczającą odpowiedź (całkowity wynik Y-MRS ≥16 i ≤35% poprawa wyniku całkowitego Y-MRS) na lit lub walproinian otrzymywali ABILIFY w dawce początkowej 15 mg/dobę z opcją zwiększenie do 30 mg lub zmniejszenie do 10 mg już w 4. dniu w ramach terapii wspomagającej z zastosowaniem otwartej próby litu lub walproinianu. Przed randomizacją pacjenci otrzymujący skojarzenie podwójnie ślepej próby ABILIFY i litu lub walproinianu musieli utrzymać stabilność (łączne wyniki Y-MRS i MADRS ≤12) przez 12 kolejnych tygodni. Następnie trzystu trzydziestu siedmiu pacjentów zostało losowo przydzielonych metodą podwójnie ślepej próby, albo do tej samej dawki ABILIFY 20 mg, którą otrzymywali pod koniec okresu stabilizacji, albo do placebo i litu lub walproinianu, a następnie byli monitorowani pod kątem manii, mieszanej lub nawrót depresji trwający maksymalnie 52 tygodnie. ABILIFY 15 mg był lepszy od placebo pod względem pierwszorzędowego punktu końcowego, czasu od randomizacji do nawrotu do dowolnego zdarzenia związanego z nastrojem (Badanie 8 na Ryc. 8). Zdarzenie nastroju zdefiniowano jako hospitalizację z powodu epizodu maniakalnego, mieszanego lub depresyjnego, przerwanie badania z powodu braku skuteczności z towarzyszącym wynikiem Y-MRS >16 i/lub MADRS >16 lub SAE pogorszenia choroby z towarzyszącym Y- wynik MRS >16 i/lub MADRS >16. Podczas fazy leczenia metodą podwójnie ślepej próby zaobserwowano łącznie 68 zdarzeń związanych z nastrojem. Dwudziestu pięciu było z grupy ABILIFY 20mg, a 43 z grupy placebo. Liczba obserwowanych epizodów maniakalnych w grupie ABILIFY 15 mg (7) była mniejsza niż w grupie placebo (19), podczas gdy liczba epizodów depresyjnych w grupie ABILIFY (14) była podobna do tej w grupie placebo (18) . Krzywe Kaplana-Meiera dla czasu od randomizacji do nawrotu do dowolnego zdarzenia związanego z nastrojem podczas 52-tygodniowej fazy leczenia metodą podwójnie ślepej próby dla grup ABILIFY 10 mg i placebo przedstawiono na Rycinie 8.
Rycina 8: Oszacowanie Kaplana-Meiera skumulowanego odsetka pacjentów z nawrotem do dowolnego zdarzenia związanego z nastrojem (badanie dwubiegunowe 8) 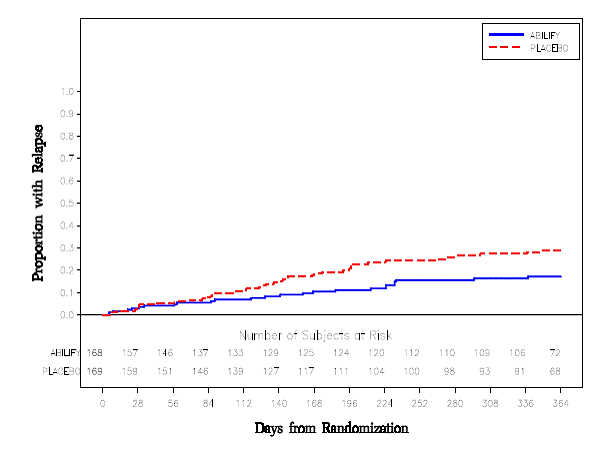
Badanie podgrup populacji nie ujawniło żadnych wyraźnych dowodów na zróżnicowaną reaktywność w zależności od wieku i płci; jednak liczba pacjentów w każdej z grup etnicznych była niewystarczająca, aby odpowiednio ocenić różnice między grupami.
Leczenie wspomagające ciężkiego zaburzenia depresyjnego
Dorośli ludzie
Skuteczność preparatu ABILIFY 15 mg w leczeniu wspomagającym ciężkiego zaburzenia depresyjnego (MDD) wykazano w dwóch krótkoterminowych (6-tygodniowych) badaniach kontrolowanych placebo u dorosłych pacjentów spełniających kryteria DSM-IV dla MDD, u których wystąpiła niewystarczająca odpowiedź na wcześniejszą terapię przeciwdepresyjną (1 do 3 kursów) w bieżącym epizodzie i u których również wykazano niewystarczającą odpowiedź na 8 tygodni prospektywnego leczenia przeciwdepresyjnego (paroksetyny o kontrolowanym uwalnianiu, wenlafaksyny o przedłużonym uwalnianiu, fluoksetyny, escitalopramu lub sertraliny). Nieodpowiednią odpowiedź na leczenie prospektywne zdefiniowano jako mniej niż 50% poprawę w 17-punktowej wersji Skali Oceny Depresji Hamiltona (HAMD17), minimalny wynik w skali HAMD17 wynoszący 14 oraz ocenę poprawy w skali Clinical Global Impressions nie lepszą niż minimalna. Nieodpowiednią odpowiedź na wcześniejsze leczenie zdefiniowano jako poprawę o mniej niż 50% odczuwaną przez pacjenta po co najmniej 6 tygodniach leczenia przeciwdepresyjnego w dawce minimalnej skutecznej lub większej.
Podstawowym instrumentem używanym do oceny objawów depresji była Skala Oceny Depresji Montgomery-Asberg (MADRS), 10-punktowa skala oceniana przez klinicystów, służąca do oceny stopnia symptomatologii depresji. Kluczowym instrumentem drugorzędnym była Skala Niepełnosprawności Sheehana (SDS), 3-punktowe narzędzie samooceny stosowane do oceny wpływu depresji na trzy domeny funkcjonowania, przy czym każda pozycja została oceniona od 0 (wcale) do 10 (skrajne).
W dwóch badaniach (n=381, n=362) ABILIFY 15 mg był skuteczniejszy niż placebo pod względem zmniejszenia średnich całkowitych wyników MADRS (Badania 1, 2 w Tabeli 28). W jednym badaniu ABILIFY był również lepszy od placebo pod względem zmniejszania średniego wyniku SDS.
obu badaniach pacjenci otrzymywali ABILIFY 15 mg w połączeniu z lekami przeciwdepresyjnymi w dawce 5 mg/dobę. W oparciu o tolerancję i skuteczność dawki można było dostosowywać w odstępach co 5 mg w odstępie tygodnia. Dopuszczalne dawki wynosiły: 2, 5, 10, 15 mg/dobę, a dla pacjentów, którzy nie przyjmowali silnych inhibitorów CYP2D6, fluoksetyny i paroksetyny, 20 mg/dobę. Średnia końcowa dawka w punkcie końcowym obu badań wynosiła 10,7 i 11,4 mg/dobę.
Badanie podgrup populacji nie ujawniło dowodów na zróżnicowaną odpowiedź w zależności od wieku, wyboru przyszłego leku przeciwdepresyjnego lub rasy. W odniesieniu do płci, mniejsze średnie obniżenie całkowitego wyniku MADRS zaobserwowano u mężczyzn niż u kobiet.
Drażliwość związana z zaburzeniami autystycznymi
Pacjenci pediatryczni
Skuteczność ABILIFY (arypiprazol) w leczeniu drażliwości związanej z zaburzeniami autystycznymi została potwierdzona w dwóch 8-tygodniowych badaniach kontrolowanych placebo u pacjentów pediatrycznych (w wieku od 6 do 17 lat), którzy spełniali kryteria DSM-IV dla zaburzeń autystycznych i wykazali zachowania, takie jak napady złości, agresja, zachowania samookaleczenia lub połączenie tych problemów. Ponad 75% tych osób miało mniej niż 13 lat.
Skuteczność oceniano za pomocą dwóch skal oceny: Aberrant Behaviour Checklist (ABC) oraz Clinical Global Impression-Poprawa (CGI-I). Pierwszorzędowym punktem końcowym w obu badaniach była zmiana od punktu początkowego do punktu końcowego w podskali Drażliwość ABC (ABC-I). Podskala ABC-I mierzyła objawy drażliwości w zaburzeniu autystycznym.
Wyniki tych prób są następujące:
jednym z 8-tygodniowych badań kontrolowanych placebo dzieci i młodzież z zaburzeniami autystycznymi (n=98) w wieku od 6 do 17 lat otrzymywały dobowe dawki placebo lub ABILIFY od 2 do 15 mg/dobę. ABILIFY, począwszy od 2 mg/dobę, ze wzrostem dozwolonym do 15 mg/dobę w oparciu o odpowiedź kliniczną, znacząco poprawił wyniki w podskali ABC-I oraz w skali CGI-I w porównaniu z placebo. Średnia dzienna dawka ABILIFY 10 mg pod koniec 8-tygodniowego leczenia wynosiła 8,6 mg/dobę (Badanie 1 w Tabeli 29).
innym 8-tygodniowym badaniu kontrolowanym placebo u dzieci i młodzieży z zaburzeniami autystycznymi (n=218) w wieku od 6 do 17 lat trzy stałe dawki preparatu ABILIFY (5 mg/dobę, 10 mg/dobę lub 15 mg/dobę) dnia) porównano z placebo. Dawkowanie ABILIFY rozpoczęto od 2 mg/dobę i zwiększono do 5 mg/dobę po tygodniu. Po drugim tygodniu zwiększono ją do 10 mg/dobę u pacjentów w grupie dawki 10 i 15 mg, a po trzecim tygodniu zwiększono ją do 15 mg/dobę w grupie leczonej 15 mg/dobę (Badanie 2 w Tabela 29). Wszystkie trzy dawki ABILIFY znacząco poprawiły wyniki w podskali ABC-I w porównaniu z placebo.
Zaburzenie Tourette'a
Pacjenci pediatryczni
Skuteczność ABILIFY (arypiprazol) w leczeniu zaburzenia Tourette'a ustalono w jednym 8-tygodniowym (w wieku 7 do 17 lat) i jednym 10-tygodniowym (w wieku 6 do 18 lat) kontrolowanych placebo badaniach w pacjenci pediatryczni (w wieku od 6 do 18 lat), którzy spełniali kryteria DSM-IV dla zaburzenia Tourette'a i mieli całkowity wynik tików (TTS) ≥ 20-22 w skali Yale Global Tic Severity Scale (YGTSS). YGTSS to w pełni zwalidowana skala zaprojektowana do pomiaru aktualnego nasilenia tików. Skuteczność oceniano za pomocą dwóch skal oceny: 1) skali całkowitego tika (TTS) YGTSS oraz 2) skali Clinical Global Impressions Scale for Tourette's Syndrome (CGI-TS), sumarycznej miary ustalonej przez lekarza, która uwzględnia wszystkie dostępne informacje o pacjencie. Ponad 65% tych pacjentów było w wieku poniżej 13 lat.
Pierwszorzędową miarą wyniku w obu badaniach była zmiana od punktu początkowego do punktu końcowego w TTS skali YGTSS. Oceny TTS są dokonywane w 5 różnych wymiarach w skali od 0 do 5 dla tików ruchowych i głosowych. Suma tych 10 wyników daje TTS (tj. 0-50).
Wyniki tych prób są następujące:
8-tygodniowym, kontrolowanym placebo badaniu ze stałą dawką, dzieci i młodzież z chorobą Tourette'a (n=133), w wieku od 7 do 17 lat, zostali losowo przydzieleni w stosunku 1:1:1 do małej dawki ABILIFY, dużej dawki ABILIFY 15 mg lub placebo. Docelowe dawki dla grup otrzymujących niską i wysoką dawkę ABILIFY 10 mg były oparte na wadze. Pacjenci o masie
Rysunek 9: Średnie najmniejszych kwadratów zmian od wartości wyjściowych w YGTSS TTS według tygodnia (badanie zaburzeń Tourette'a 1) 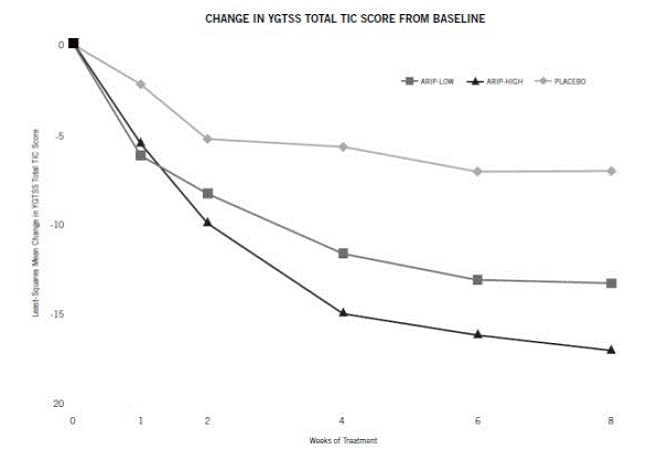
W 10-tygodniowym, kontrolowanym placebo badaniu ze zmienną dawką u dzieci i młodzieży z chorobą Tourette'a (n=61), w wieku od 6 do 18 lat, pacjenci otrzymywali dobowe dawki placebo lub ABILIFY, zaczynając od 2 mg/ dzień ze wzrostem dozwolonym do 20 mg/dobę w oparciu o odpowiedź kliniczną. ABILIFY wykazał statystycznie znamienną poprawę wyników w skali YGTSS TTS w porównaniu z placebo (Badanie 2 w Tabeli 30). Średnia dzienna dawka ABILIFY pod koniec 10-tygodniowego leczenia wynosiła 6,54 mg/dobę.
Pobudzenie związane ze schizofrenią lub manią dwubiegunową
Skuteczność domięśniowego ABILIFY do wstrzykiwań w leczeniu pobudzenia została potwierdzona w trzech krótkoterminowych (24-godzinnych), kontrolowanych placebo badaniach klinicznych u pacjentów z pobudzeniem z dwóch grup diagnostycznych: schizofrenii i zaburzenia afektywnego dwubiegunowego typu I (epizody maniakalne lub mieszane, z lub bez cech psychotycznych). Każde z badań obejmowało pojedyncze aktywne ramię leczenia porównawczego, polegające na wstrzyknięciu haloperidolu (badania nad schizofrenią) lub wstrzyknięciu lorazepamu (badanie dwubiegunowej manii). Pacjenci mogli otrzymać do trzech wstrzyknięć podczas 24-godzinnych okresów leczenia; jednak pacjenci nie mogli otrzymać drugiego wstrzyknięcia przed upływem początkowego 2 godzinnego okresu, kiedy oceniano główny miernik skuteczności. Pacjenci włączeni do badań musieli być: (1) ocenieni przez badaczy klinicznych jako klinicznie pobudzeni i klinicznie odpowiedni kandydaci do leczenia lekami domięśniowymi oraz (2) wykazywać poziom pobudzenia, który osiągnął lub przekroczył próg wyniku ≥15 w dniu pięć pozycji składających się na komponent podekscytowany Skali Zespołów Pozytywnych i Negatywnych (PANSS) (tj. słaba kontrola impulsów, napięcie, wrogość, brak współpracy i podniecenie) z co najmniej dwoma punktami poszczególnych pozycji ≥4 przy użyciu systemu punktacji 1-7 (1 = nieobecny, 4 = umiarkowany, 7 = skrajny). W badaniach średni wyjściowy wynik komponentu wzbudzonego PANSS wynosił 19, z punktacją w zakresie od 15 do 34 (z maksymalnej liczby 35), co sugeruje głównie umiarkowane poziomy pobudzenia, a niektórzy pacjenci doświadczają łagodnego lub ciężkiego poziomu pobudzenia. Główną miarą skuteczności stosowaną do oceny oznak i objawów pobudzenia w tych badaniach była zmiana w stosunku do wartości wyjściowej w składniku wzbudzonym PANSS w 2 godziny po wstrzyknięciu. Kluczową miarą drugorzędową była skala klinicznego ogólnego wrażenia poprawy (CGI-I). Wyniki prób są następujące:
badaniu kontrolowanym placebo u pacjentów hospitalizowanych z pobudzeniem, spełniających głównie kryteria DSM-IV dla schizofrenii (n=350), oceniono cztery stałe dawki iniekcyjne ABILIFY 20 mg: 1 mg, 5,25 mg, 9,75 mg i 15 mg. W 2 godziny po wstrzyknięciu dawki 5,25 mg, 9,75 mg i 15 mg były statystycznie lepsze niż placebo w komponencie wzbudzonym PANSS (badanie 1 w tabeli 31) oraz w skali CGII.
W drugim badaniu z grupą kontrolną otrzymującą placebo z udziałem pobudzonych pacjentów hospitalizowanych, w większości spełniających kryteria DSM-IV dla schizofrenii (n=445), oceniano jedno stałe wstrzyknięcie ABILIFY 15 mg w dawce 9,75 mg. W 2 godziny po wstrzyknięciu ABILIFY do wstrzykiwań był statystycznie lepszy od placebo w składniku wzbudzonym PANSS (badanie 2 w tabeli 31) oraz w skali CGI-I.
badaniu kontrolowanym placebo z udziałem pobudzonych pacjentów hospitalizowanych spełniających kryteria DSMIV dla zaburzenia afektywnego dwubiegunowego typu I (maniakalnego lub mieszanego) (n=291), oceniono dwie stałe dawki do wstrzykiwań ABILIFY 10 mg wynoszące 9,75 mg i 15 mg. W 2 godziny po wstrzyknięciu obie dawki były statystycznie lepsze niż placebo w składniku wzbudzonym PANSS (Badanie 3 w Tabeli 31).
Badanie podzbiorów populacji (wiek, rasa i płeć) nie ujawniło żadnej zróżnicowanej reakcji na podstawie tych podgrup.
INFORMACJA O PACJENCIE
ABILIFY® (arypiprazol) Tabletki
ABILIFY DISCMELT® (arypiprazol) tabletki rozpadające się w jamie ustnej
ABILIFY® (arypiprazol) roztwór doustny
ABILIFY® (arypiprazol) do wstrzykiwań wyłącznie do stosowania domięśniowego
Jakie są najważniejsze informacje, które powinienem wiedzieć o ABILIFY 20mg?
(Aby uzyskać informacje o innych działaniach niepożądanych, zobacz również „Jakie są możliwe skutki uboczne ABILIFY?”)
Podczas przyjmowania leku ABILIFY mogą wystąpić poważne działania niepożądane, w tym:
- Zwiększone ryzyko zgonu u pacjentów w podeszłym wieku z psychozą związaną z otępieniem: Leki takie jak ABILIFY 10mg mogą zwiększać ryzyko śmierci u osób starszych, które utraciły kontakt z rzeczywistością (psychoza) z powodu splątania i utraty pamięci (demencja). ABILIFY nie jest zatwierdzony do leczenia pacjentów z psychozą związaną z otępieniem.
- Ryzyko myśli lub działań samobójczych: Leki przeciwdepresyjne, depresja i inne poważne choroby psychiczne oraz myśli lub działania samobójcze:
1. Leki przeciwdepresyjne mogą nasilać myśli lub działania samobójcze u niektórych dzieci, nastolatków i młodych dorosłych w ciągu pierwszych kilku miesięcy leczenia.
2. Depresja i inne poważne choroby psychiczne są najważniejszymi przyczynami myśli i działań samobójczych. Niektóre osoby mogą być szczególnie narażone na myśli lub działania samobójcze. Należą do nich osoby, które mają (lub mają w rodzinie) chorobę afektywną dwubiegunową (zwaną również chorobą maniakalno-depresyjną) lub myśli lub działania samobójcze.
3. Jak mogę obserwować i starać się zapobiegać myślom i działaniom samobójczym u siebie lub członka rodziny?
- Zwróć szczególną uwagę na wszelkie zmiany, zwłaszcza nagłe zmiany nastroju, zachowań, myśli lub uczuć. Jest to bardzo ważne w przypadku rozpoczęcia przyjmowania leku przeciwdepresyjnego lub zmiany dawki.
- Natychmiast zadzwoń do lekarza, aby zgłosić nowe lub nagłe zmiany nastroju, zachowania, myśli lub uczuć.
- Zachowaj wszystkie wizyty kontrolne u lekarza zgodnie z planem. Zadzwoń do lekarza między wizytami w razie potrzeby, zwłaszcza jeśli masz obawy dotyczące objawów.
Zadzwoń do lekarza natychmiast, jeśli ty lub członek twojej rodziny ma którykolwiek z poniższych objawów, zwłaszcza jeśli są nowe, gorsze lub martwią cię:
- myśli o samobójstwie lub śmierci
- próby popełnienia samobójstwa
- nowa lub gorsza depresja
- nowy lub gorszy niepokój
- czuję się bardzo poruszony lub niespokojny
- atak paniki
- kłopoty ze snem (bezsenność)
- nowa lub gorsza drażliwość
- zachowywanie się agresywnie, złość lub przemoc
- działając na niebezpieczne impulsy
- ekstremalny wzrost aktywności i mówienia (mania)
- inne nietypowe zmiany w zachowaniu lub nastroju
Co jeszcze muszę wiedzieć o lekach przeciwdepresyjnych?
- Nigdy nie odstawiaj leku przeciwdepresyjnego bez uprzedniej rozmowy z lekarzem. Nagłe zatrzymanie leku przeciwdepresyjnego może spowodować inne objawy.
- Antydepresanty to leki stosowane w leczeniu depresji i innych chorób. Ważne jest omówienie wszystkich zagrożeń związanych z leczeniem depresji, a także zagrożeń związanych z jej nieleczeniem. Pacjenci i ich rodziny lub inni opiekunowie powinni omówić z lekarzem wszystkie opcje leczenia, a nie tylko stosowanie leków przeciwdepresyjnych.
- Leki przeciwdepresyjne mają inne skutki uboczne. Porozmawiaj z lekarzem o skutkach ubocznych leku przepisanego Tobie lub członkowi Twojej rodziny.
- Leki przeciwdepresyjne mogą wchodzić w interakcje z innymi lekami. Poznaj wszystkie leki, które przyjmujesz Ty lub członek Twojej rodziny. Zachowaj listę wszystkich leków, aby pokazać je lekarzowi. Nie rozpoczynaj nowych leków bez uprzedniej konsultacji z lekarzem.
- Nie wszystkie leki przeciwdepresyjne przepisywane dzieciom są zatwierdzone przez FDA do stosowania u dzieci. Porozmawiaj z lekarzem swojego dziecka, aby uzyskać więcej informacji.
Co to jest ABILIFY?
- ABILIFY 20 mg tabletki doustne, tabletki ulegające rozpadowi w jamie ustnej i roztwór doustny to leki na receptę stosowane w leczeniu:
- Schizofrenia
- epizody maniakalne lub mieszane, które występują w chorobie afektywnej dwubiegunowej typu I
- ciężkie zaburzenie depresyjne (MDD), gdy ABILIFY 20 mg jest stosowany z lekami przeciwdepresyjnymi
- drażliwość związana z zaburzeniami autystycznymi
- Zaburzenie Tourette'a
- ABILIFY Injection to lek na receptę stosowany w leczeniu:
- pobudzenie związane ze schizofrenią lub manią dwubiegunową
Nie wiadomo, czy ABILIFY 10 mg jest bezpieczny lub skuteczny u dzieci:
- poniżej 13 roku życia ze schizofrenią
- poniżej 10 roku życia z chorobą afektywną dwubiegunową typu I
- poniżej 6 roku życia z drażliwością związaną z zaburzeniami autystycznymi
- poniżej 6 roku życia z chorobą Tourette'a
Nie należy przyjmować leku ABILIFY 20 mg, jeśli: jesteś uczulony na arypiprazol lub którykolwiek ze składników leku ABILIFY. Pełna lista składników ABILIFY znajduje się na końcu niniejszego Przewodnika po lekach.
Przed zażyciem ABILIFY 15mg, poinformuj swojego lekarza o wszystkich swoich schorzeniach, w tym o tym, czy masz lub miałeś:
- cukrzyca lub wysoki poziom cukru we krwi u Ciebie lub Twojej rodziny; Twój lekarz powinien sprawdzić poziom cukru we krwi przed rozpoczęciem stosowania leku ABILIFY 10 mg, a także w trakcie leczenia.
- drgawki (konwulsje).
- niskie lub wysokie ciśnienie krwi.
- problemy z sercem lub udar.
- ciąża lub plany zajścia w ciążę. Nie wiadomo, czy ABILIFY zaszkodzi nienarodzonemu dziecku.
- Jeśli zajdziesz w ciążę podczas przyjmowania leku ABILIFY 10 mg, porozmawiaj ze swoim lekarzem o zarejestrowaniu się w Krajowym Rejestrze Ciąży dla atypowych leków przeciwpsychotycznych. Możesz zarejestrować się dzwoniąc pod numer 1-866-961-2388 lub wejdź na http://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/
- karmienie piersią lub plany karmienia piersią. ABILIFY przenika do mleka matki. Porozmawiaj ze swoim lekarzem o najlepszym sposobie karmienia dziecka, jeśli otrzymasz ABILIFY.
- mała liczba białych krwinek.
- fenyloketonuria. ABILIFY DISCMELT Tabletki ulegające rozpadowi w jamie ustnej zawierają fenyloalaninę.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe.
ABILIFY i inne leki mogą wzajemnie na siebie wpływać, powodując możliwe poważne działania niepożądane. ABILIFY może wpływać na działanie innych leków, a inne leki mogą wpływać na działanie ABILIFY.
Twój lekarz może poinformować Cię, czy przyjmowanie ABILIFY z innymi lekami jest bezpieczne. Nie należy rozpoczynać ani przerywać przyjmowania jakichkolwiek leków podczas przyjmowania leku ABILIFY bez uprzedniej konsultacji z lekarzem. Poznaj leki, które przyjmujesz. Zachowaj listę swoich leków, aby pokazać swojemu lekarzowi i farmaceucie, kiedy otrzymasz nowy lek.
Jak powinienem przyjmować ABILIFY 20mg?
- Weź ABILIFY 10 mg dokładnie tak, jak zalecił Ci lekarz. Nie należy zmieniać dawki ani samodzielnie przerywać przyjmowania leku ABILIFY.
- ABILIFY 20 mg można przyjmować z posiłkiem lub bez posiłku.
- Tabletki ABILIFY należy połykać w całości.
- W przypadku pominięcia dawki leku ABILIFY 20 mg, należy przyjąć pominiętą dawkę, gdy tylko sobie o tym przypomni. Jeśli zbliża się pora przyjęcia następnej dawki, po prostu pomiń pominiętą dawkę i weź kolejną dawkę o zwykłej porze. Nie należy przyjmować dwóch dawek ABILIFY 10mg w tym samym czasie.
- Jeśli przepisano ABILIFY DISCMELT, należy go przyjmować w następujący sposób:
- Nie otwierać blistra do czasu przyjęcia tabletki DISCMELT.
- Aby wyjąć jedną tabletkę DISCMELT, należy otworzyć opakowanie i oderwać folię z blistra, aby odsłonić tabletkę.
- Nie należy przepychać tabletki przez folię, ponieważ może to spowodować jej uszkodzenie.
- Natychmiast po otwarciu blistra, suchymi rękami, wyjąć tabletkę i umieścić całą tabletkę ulegającą rozpadowi w jamie ustnej ABILIFY DISCMELT na języku.
- ślinie rozpad tabletki następuje szybko. Zaleca się przyjmowanie ABILIFY 10mg DISCMELT bez płynu. Jednak w razie potrzeby można go popijać płynem.
- Nie próbuj dzielić tabletu DISCMELT.
- Jeśli zażyjesz zbyt dużo ABILIFY, natychmiast zadzwoń do swojego lekarza lub centrum kontroli zatruć pod numer 1-800-222-1222 lub udaj się na pogotowie ratunkowe najbliższego szpitala.
Czego powinienem unikać podczas przyjmowania ABILIFY 10mg?
- Nie prowadź pojazdów, nie obsługuj ciężkich maszyn ani nie wykonuj innych niebezpiecznych czynności, dopóki nie dowiesz się, jak ABILIFY 10mg wpływa na Ciebie. ABILIFY 20mg może powodować senność.
- Unikaj przegrzania lub odwodnienia.
- Nie przesadzaj.
- W czasie upałów pozostań w chłodnym miejscu, jeśli to możliwe.
- Trzymaj się z dala od słońca. Nie noś zbyt dużej lub ciężkiej odzieży.
- Pić dużo wody.
Jakie są możliwe skutki uboczne ABILIFY?
ABILIFY 10mg może powodować poważne skutki uboczne, w tym:
- Zobacz „Jakie są najważniejsze informacje, które powinienem wiedzieć o ABILIFY 10mg?”
- Udar mózgu u osób starszych (problemy naczyniowo-mózgowe), który może prowadzić do śmierci
- Złośliwy zespół neuroleptyczny (NMS). Należy natychmiast poinformować lekarza, jeśli wystąpią niektóre lub wszystkie z następujących objawów: wysoka gorączka, sztywność mięśni, dezorientacja, pocenie się, zmiany tętna, tętna i ciśnienia krwi. Mogą to być objawy rzadkiego i poważnego stanu, który może prowadzić do śmierci. Zadzwoń do swojego lekarza natychmiast, jeśli wystąpi którykolwiek z tych objawów.
- Niekontrolowane ruchy ciała (późna dyskineza). ABILIFY może powodować ruchy twarzy, języka lub innych części ciała, których nie możesz kontrolować. Późna dyskineza może nie ustąpić, nawet jeśli przestaniesz otrzymywać ABILIFY. Późna dyskineza może również rozpocząć się po zaprzestaniu przyjmowania ABILIFY.
- Problemy z metabolizmem, takie jak:
- Wysoki poziom cukru we krwi (hiperglikemia) i cukrzyca. niektórych osób przyjmujących ABILIFY może wystąpić podwyższenie poziomu cukru we krwi. Niezwykle wysoki poziom cukru we krwi może prowadzić do śpiączki lub śmierci. Jeśli masz cukrzycę lub czynniki ryzyka cukrzycy (takie jak nadwaga lub cukrzyca w wywiadzie rodzinnym), Twój lekarz powinien sprawdzić poziom cukru we krwi przed rozpoczęciem stosowania ABILIFY i podczas leczenia.
Zadzwoń do swojego lekarza, jeśli wystąpi którykolwiek z tych objawów wysokiego poziomu cukru we krwi podczas przyjmowania ABILIFY:
- czuję się bardzo spragniony
- trzeba oddawać mocz częściej niż zwykle
- czuć się bardzo głodnym
- czuć się słabym lub zmęczonym
- czujesz się chory na żołądek
- czujesz się zdezorientowany lub twój oddech pachnie owocowo
- Podwyższony poziom tłuszczów (cholesterolu i trójglicerydów) we krwi.
- Przybranie na wadze. Ty i Twój lekarz powinniście regularnie sprawdzać swoją wagę.
- Niezwykłe popędy. Niektóre osoby przyjmujące ABILIFY 15 mg miały nietypowe potrzeby, takie jak hazard, napady objadania się lub jedzenie, których nie można kontrolować (kompulsywne), kompulsywne zakupy i popęd seksualny. Jeśli Ty lub członkowie Twojej rodziny zauważycie, że odczuwacie nietypowe pragnienia lub zachowania, porozmawiajcie ze swoim lekarzem.
- Niedociśnienie ortostatyczne (obniżone ciśnienie krwi). Zawroty głowy lub omdlenia mogą wystąpić, gdy zbyt szybko wstajemy z pozycji siedzącej lub leżącej.
- Spada. ABILIFY może powodować senność lub zawroty głowy, może powodować obniżenie ciśnienia krwi podczas zmiany pozycji i może spowolnić myślenie i motorykę, co może prowadzić do upadków, które mogą spowodować złamania lub inne urazy.
- Niska liczba białych krwinek
- Drgawki (konwulsje)
- Problemy z kontrolą temperatury ciała, zwłaszcza gdy dużo ćwiczysz lub przebywasz w bardzo gorącym miejscu. Ważne jest, aby pić wodę, aby uniknąć odwodnienia. Zobacz „Czego powinienem unikać podczas otrzymywania ABILIFY 15mg?”
- Trudności w połykaniu, które mogą spowodować dostanie się pokarmu lub płynu do płuc.
Najczęstsze działania niepożądane ABILIFY 10mg u dorosłych to:
- Mdłości
- zawroty głowy
- wymioty
- lęk
- zaparcie
- bezsenność
- ból głowy
- niepokój
- rozmazany obraz
- choroba górnych dróg oddechowych
- wewnętrzne poczucie niepokoju/potrzeby ruchu (akatyzja)
Najczęstsze działania niepożądane ABILIFY u dzieci obejmują:
- czuje się senny
- bezsenność
- ból głowy
- mdłości
- wymioty
- zatkany nos
- zmęczenie
- przybranie na wadze
- zwiększony lub zmniejszony apetyt
- niekontrolowany ruch, taki jak niepokój, drżenie
- zwiększona ślina lub ślinotok
- sztywność mięśni
To nie wszystkie możliwe skutki uboczne ABILIFY.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać ABILIFY?
- Przechowywać ABILIFY 15mg w temperaturze pokojowej, między 68 ° F do 77 ° F (20 ° C do 25 ° C).
- Otwarte butelki ABILIFY 10 mg roztwór doustny mogą być używane przez okres do 6 miesięcy po otwarciu, ale nie po upływie daty ważności podanej na butelce.
ABILIFY i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu ABILIFY
Leki są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Nie należy stosować ABILIFY 20mg w przypadku schorzenia, na które nie został przepisany. Nie należy podawać ABILIFY 20mg innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić. Możesz poprosić swojego lekarza lub farmaceutę o informacje na temat ABILIFY 10mg, który został napisany dla pracowników służby zdrowia.
Jakie są składniki ABILIFY?
Składnik czynny: arypiprazol
Nieaktywne składniki:
skrobia kukurydziana, hydroksypropyloceluloza, monohydrat laktozy, stearynian magnezu i celuloza mikrokrystaliczna. Barwniki obejmują tlenek żelaza (żółty lub czerwony) i FD&C Blue No. 2 Aluminium Lake
ABILIFY 10 mg DISCMELT Tabletki rozpadające się w jamie ustnej: acesulfam potasu, aspartam (zawierający fenyloalaninę), krzemian wapnia, kroskarmeloza sodowa, krospowidon, krem waniliowy (naturalne i sztuczne aromaty), stearynian magnezu, celuloza mikrokrystaliczna, dwutlenek krzemu, kwas winowy i ksylitol. Barwniki obejmują tlenek żelaza (żółty lub czerwony) i FD&C Blue No. 2 Aluminium Lake
ABILIFY roztwór doustny: wersenian disodowy, fruktoza (200 mg na ml), gliceryna, kwas dl-mlekowy, metyloparaben, glikol propylenowy, propyloparaben, wodorotlenek sodu, sacharoza (400 mg na ml) i woda oczyszczona. Roztwór doustny jest aromatyzowany naturalnym pomarańczowym kremem i innymi naturalnymi aromatami
Aby uzyskać więcej informacji o ABILIFY, odwiedź stronę www.abilify.com lub zadzwoń pod numer 1-800-438-6055.
Ten przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków
