Wellbutrin 150mg, 300mg Bupropion Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Wellbutrin 150mg i jak się go stosuje?
Wellbutrin 150mg to lek na receptę stosowany w leczeniu objawów dużej depresji i sezonowych zaburzeń afektywnych. Wellbutrin 150mg może być stosowany samodzielnie lub z innymi lekami.
Wellbutrin 150mg należy do klasy leków zwanych antydepresantami, inhibitorami wychwytu zwrotnego dopaminy, antydepresantami, innymi, pomocami w rzucaniu palenia.
Jakie są możliwe skutki uboczne Wellbutrin 150mg?
Wellbutrin może powodować poważne skutki uboczne, w tym:
- drgawki (drgawki),
- dezorientacja,
- nietypowe zmiany nastroju lub zachowania,
- rozmazany obraz,
- widzenie tunelowe,
- ból lub obrzęk oka,
- widząc aureole wokół świateł,
- szybkie lub nieregularne bicie serca,
- goniące myśli,
- zwiększona energia,
- lekkomyślne zachowanie,
- uczucie skrajnego szczęścia lub rozdrażnienia,
- mówić więcej niż zwykle i
- poważne problemy ze snem
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Wellbutrin to:
- suchość w ustach,
- zatkany nos,
- Problemy ze wzrokiem,
- problemy ze słuchem,
- mdłości,
- wymioty,
- zaparcie,
- problemy ze snem (bezsenność),
- drżenia,
- wyzysk,
- uczucie niepokoju lub zdenerwowania,
- szybkie bicie serca,
- dezorientacja,
- podniecenie,
- wrogość,
- wysypka,
- ból głowy,
- zawroty głowy i
- ból stawu
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Wellbutrin. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088
OSTRZEŻENIE
MYŚLI I ZACHOWANIA SAMOBÓJCZE
SAMOBÓJSTWO I NARKOTYKI PRZECIWDEPRESYJNE
Leki przeciwdepresyjne zwiększały ryzyko myśli i zachowań samobójczych u dzieci, młodzieży i młodych dorosłych w badaniach krótkoterminowych. Badania te nie wykazały wzrostu ryzyka myśli i zachowań samobójczych podczas stosowania leków przeciwdepresyjnych u osób w wieku powyżej 24 lat; wystąpiło zmniejszenie ryzyka przy stosowaniu leków przeciwdepresyjnych u osób w wieku 65 lat i starszych [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
pacjentów w każdym wieku, którzy rozpoczęli terapię przeciwdepresyjną, należy uważnie monitorować pogorszenie i pojawienie się myśli i zachowań samobójczych. Poinformuj rodziny i opiekunów o potrzebie ścisłej obserwacji i komunikacji z lekarzem [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI].
OPIS
WELLBUTRIN (chlorowodorek bupropionu), lek przeciwdepresyjny z klasy aminoketonów, nie jest chemicznie spokrewniony z tricyklicznym, tetracyklicznym, selektywnym inhibitorem wychwytu zwrotnego serotoniny ani innymi znanymi środkami przeciwdepresyjnymi. Jego struktura bardzo przypomina strukturę dietylopropionu; jest związany z fenyloetyloaminami. Jest on oznaczony jako chlorowodorek (±)-1-(3-chlorofenylo)-2-[(1,1-dimetyloetylo)amino]-1-propanonu. Masa cząsteczkowa wynosi 276,2. Wzór cząsteczkowy to C13H18ClNO•HCl. Proszek chlorowodorku bupropionu jest biały, krystaliczny i dobrze rozpuszczalny w wodzie. Ma gorzki smak i wywołuje uczucie znieczulenia miejscowego na błonie śluzowej jamy ustnej. Wzór strukturalny to:
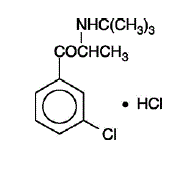
WELLBUTRIN jest dostarczany do podawania doustnego w postaci tabletek powlekanych 75 mg (żółto-złota) i 100 mg (czerwona). Każda tabletka zawiera oznaczoną ilość chlorowodorku bupropionu oraz składniki nieaktywne: tabletka 75 mg – D&C Yellow No. 10 Lake, FD&C Yellow No. 6 Lake, hydroksypropyloceluloza, hypromeloza, mikrokrystaliczna celuloza, glikol polietylenowy, talk i dwutlenek tytanu; Tabletka 100 mg – FD&C Red No. 40 Lake, FD&C Yellow No. 6 Lake, hydroksypropyloceluloza, hypromeloza, celuloza mikrokrystaliczna, glikol polietylenowy, talk i dwutlenek tytanu.
WSKAZANIA
WELLBUTRIN (chlorowodorek bupropionu) jest wskazany w leczeniu dużych zaburzeń depresyjnych (MDD), zgodnie z definicją w podręczniku Diagnostic and Statistical Manual (DSM).
Skuteczność preparatu WELLBUTRIN 300 mg w leczeniu dużego epizodu depresyjnego ustalono w dwóch 4-tygodniowych kontrolowanych badaniach ambulatoryjnych i jednym 6-tygodniowym kontrolowanym badaniu ambulatoryjnym z udziałem dorosłych pacjentów z MDD [patrz Studia kliniczne ].
DAWKOWANIE I SPOSÓB PODAWANIA
Ogólne instrukcje użytkowania
Aby zminimalizować ryzyko napadu, stopniowo zwiększaj dawkę [patrz OSTRZEŻENIA I ŚRODKI ]. Zwiększenie dawki nie powinno przekraczać 100 mg/dobę w okresie 3 dni. Tabletki WELLBUTRIN należy połykać w całości, nie rozkruszać, dzielić ani nie żuć. WELLBUTRIN 300 mg można przyjmować z posiłkiem lub bez posiłku.
Zalecana dawka początkowa to 200 mg/dobę, podawana jako 100 mg dwa razy na dobę. Po 3 dniach dawkowania dawkę można zwiększyć do 300 mg/dobę, podawana jako 100 mg 3 razy na dobę, zachowując co najmniej 6 godzin przerwy między kolejnymi dawkami. Dawkowanie powyżej 300 mg/dobę można osiągnąć stosując tabletki 75 lub 100 mg.
Maksymalnie 450 mg/dobę, podawane w podzielonych dawkach nie większych niż 150 mg każda, można rozważyć u pacjentów, którzy nie wykazują klinicznej poprawy po kilku tygodniach leczenia 300 mg/dobę. Podawać tabletkę 100 mg 4 razy dziennie, aby nie przekroczyć limitu 150 mg w pojedynczej dawce.
Powszechnie uważa się, że ostre epizody depresji wymagają kilkumiesięcznego lub dłuższego leczenia lekami przeciwdepresyjnymi poza odpowiedzią w ostrym epizodzie. Nie wiadomo, czy dawka preparatu WELLBUTRIN potrzebna do leczenia podtrzymującego jest identyczna z dawką, która zapewniła początkową odpowiedź. Okresowo oceniaj potrzebę leczenia podtrzymującego i odpowiednią dawkę do takiego leczenia.
Dostosowanie dawki u pacjentów z niewydolnością wątroby
U pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby (wskaźnik Child-Pugh: 7 do 15) maksymalna dawka preparatu WELLBUTRIN 150 mg wynosi 75 mg/dobę. U pacjentów z łagodnymi zaburzeniami czynności wątroby (punktacja Child-Pugh: 5 do 6), należy rozważyć zmniejszenie dawki i (lub) częstość dawkowania [patrz Używaj w określonych populacjach , FARMAKOLOGIA KLINICZNA ].
Dostosowanie dawki u pacjentów z zaburzeniami czynności nerek
Należy rozważyć zmniejszenie dawki i (lub) częstości podawania produktu WELLBUTRIN 150 mg u pacjentów z zaburzeniami czynności nerek (wskaźnik przesączania kłębuszkowego poniżej 90 ml/min) [patrz Używaj w określonych populacjach , FARMAKOLOGIA KLINICZNA ].
Zmiana pacjenta na lek przeciwdepresyjny będący inhibitorem monoaminooksydazy (MAOI)
Pomiędzy odstawieniem MAOI przeznaczonego do leczenia depresji a rozpoczęciem leczenia preparatem WELLBUTRIN powinno upłynąć co najmniej 14 dni. Odwrotnie, należy odczekać co najmniej 14 dni po odstawieniu preparatu WELLBUTRIN przed rozpoczęciem leczenia przeciwdepresyjnego MAOI [patrz PRZECIWWSKAZANIA , INTERAKCJE Z LEKAMI ].
Stosowanie WELLBUTRIN z odwracalnymi MAOI, takimi jak linezolid lub błękit metylenowy
Nie należy rozpoczynać podawania leku WELLBUTRIN 300 mg u pacjenta, który jest leczony odwracalnym MAOI, takim jak linezolid lub dożylny błękit metylenowy. Interakcje leków mogą zwiększać ryzyko reakcji nadciśnieniowych. U chorego wymagającego pilniejszego leczenia schorzenia psychicznego należy rozważyć interwencje niefarmakologiczne, w tym hospitalizację [zob. PRZECIWWSKAZANIA , INTERAKCJE Z LEKAMI ].
niektórych przypadkach pacjent już otrzymujący lek WELLBUTRIN może wymagać pilnego leczenia linezolidem lub dożylnym błękitem metylenowym. Jeśli akceptowalne alternatywy dla linezolidu lub dożylnego leczenia błękitem metylenowym nie są dostępne, a potencjalne korzyści z leczenia linezolidem lub dożylnym błękitem metylenowym są oceniane jako przewyższające ryzyko wystąpienia reakcji nadciśnieniowych u konkretnego pacjenta, należy natychmiast przerwać podawanie preparatu WELLBUTRIN 300 mg, a linezolid lub dożylny preparat metylenowy niebieski można podawać. Pacjenta należy monitorować przez 2 tygodnie lub do 24 godzin po podaniu ostatniej dawki linezolidu lub dożylnego błękitu metylenowego, w zależności od tego, co nastąpi wcześniej. Leczenie preparatem WELLBUTRIN 300 mg można wznowić po 24 godzinach od podania ostatniej dawki linezolidu lub dożylnego błękitu metylenowego.
Ryzyko podawania błękitu metylenowego drogami nie dożylnymi (takimi jak tabletki doustne lub miejscowe wstrzyknięcia) lub w dawkach dożylnych znacznie niższych niż 1 mg/kg z preparatem WELLBUTRIN 300 mg jest niejasne. Jednak klinicysta powinien być świadomy możliwości interakcji leku z takim stosowaniem [patrz PRZECIWWSKAZANIA , INTERAKCJE Z LEKAMI ].
JAK DOSTARCZONE
Formy dawkowania i mocne strony
- 75 mg – żółto-złote, okrągłe, dwuwypukłe tabletki z nadrukiem „WELLBUTRIN 75”.
- 100 mg – czerwone, okrągłe, obustronnie wypukłe tabletki z nadrukiem „WELLBUTRIN 100”.
Składowania i stosowania
Tabletki WELLBUTRIN 150 mg, 75 mg chlorowodorku bupropionu, to żółto-złote, okrągłe, obustronnie wypukłe tabletki z nadrukiem „WELLBUTRIN 75” w butelkach po 100 ( NDC 0173-0177-55).
Tabletki WELLBUTRIN, 100 mg chlorowodorku bupropionu, to czerwone, okrągłe, obustronnie wypukłe tabletki z nadrukiem „WELLBUTRIN 100” w butelkach po 100 ( NDC 0173-0178-55).
Przechowywać w temperaturze pokojowej, 20° do 25°C (68° do 77°F); wycieczki dozwolone między 15°C a 30°C (59°F i 86°F) [Patrz Temperatura pokojowa kontrolowana przez USP ]. Chronić przed światłem i wilgocią.
Wyprodukowano dla: GlaxoSmithKline, Research Triangle Park. Aktualizacja: listopad 2019 r.
SKUTKI UBOCZNE
Następujące działania niepożądane omówiono bardziej szczegółowo w innych punktach oznakowania:
- Myśli i zachowania samobójcze u nastolatków i młodych dorosłych [patrz OSTRZEŻENIE W PUDEŁKU , OSTRZEŻENIA I ŚRODKI ]
- Objawy neuropsychiatryczne i ryzyko samobójstwa w leczeniu rzucania palenia [patrz OSTRZEŻENIA I ŚRODKI ]
- Napad [patrz OSTRZEŻENIA I ŚRODKI ]
- Nadciśnienie [patrz OSTRZEŻENIA I ŚRODKI ]
- Aktywacja manii lub hipomanii [patrz OSTRZEŻENIA I ŚRODKI ]
- Psychoza i inne reakcje neuropsychiatryczne [patrz OSTRZEŻENIA I ŚRODKI ]
- Jaskra zamykającego się kąta [patrz OSTRZEŻENIA I ŚRODKI ]
- Reakcje nadwrażliwości [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce klinicznej.
Działania niepożądane prowadzące do przerwania leczenia
Działania niepożądane były na tyle uciążliwe, że spowodowały przerwanie leczenia produktem WELLBUTRIN u około 10% z 2400 pacjentów i zdrowych ochotników, którzy uczestniczyli w badaniach klinicznych podczas początkowego opracowywania produktu. Do częstszych zdarzeń powodujących przerwanie leczenia należą zaburzenia neuropsychiatryczne (3,0%), przede wszystkim pobudzenie i zaburzenia stanu psychicznego; zaburzenia żołądkowo-jelitowe (2,1%), głównie nudności i wymioty; zaburzenia neurologiczne (1,7%), głównie drgawki, bóle głowy i zaburzenia snu; oraz problemy dermatologiczne (1,4%), głównie wysypki. Należy jednak zauważyć, że wiele z tych zdarzeń wystąpiło przy dawkach przekraczających zalecaną dawkę dzienną.
Powszechnie obserwowane działania niepożądane
Działania niepożądane często spotykane u osób leczonych preparatem WELLBUTRIN to pobudzenie, suchość w ustach, bezsenność, ból głowy/migrena, nudności/wymioty, zaparcia, drżenie, zawroty głowy, nadmierne pocenie się, niewyraźne widzenie, tachykardia, splątanie, wysypka, wrogość, arytmia serca i słuch niepokojenie.
W Tabeli 2 zestawiono działania niepożądane, które wystąpiły w badaniach kontrolowanych placebo z częstością występowania co najmniej 1% pacjentów otrzymujących WELLBUTRIN 150 mg i częściej u tych pacjentów niż w grupie placebo.
Inne działania niepożądane obserwowane podczas rozwoju klinicznego WELLBUTRIN®
Warunki i czas trwania ekspozycji na WELLBUTRIN były bardzo zróżnicowane, a znaczną część doświadczenia uzyskano w otwartych i niekontrolowanych warunkach klinicznych. Podczas tego doświadczenia zgłoszono liczne zdarzenia niepożądane; jednak bez odpowiednich kontroli nie jest możliwe ustalenie z całą pewnością, które zdarzenia były lub nie były spowodowane przez WELLBUTRIN. Poniższe wyliczenie jest uporządkowane według układu narządów i opisuje zdarzenia pod względem ich względnej częstotliwości raportowania w bazie danych.
Stosuje się następujące definicje częstości: Częste działania niepożądane zdefiniowano jako występujące u co najmniej 1/100 pacjentów. Rzadkie działania niepożądane to te, które występują u 1/100 do 1/1000 pacjentów, natomiast rzadkie zdarzenia to te, które występują u mniej niż 1/1000 pacjentów.
Układ sercowo-naczyniowy Częsty był obrzęk; rzadko występował ból w klatce piersiowej, nieprawidłowości w elektrokardiogramie (EKG) (przedwczesne pobudzenia i niespecyficzne zmiany odcinka ST-T) oraz duszność/duszność; rzadko były uderzenia gorąca i zawał mięśnia sercowego.
Dermatologiczne: Rzadko zdarzało się łysienie.
Wewnątrzwydzielniczy: Nieczęsta była ginekomastia; rzadka była glikozuria.
Przewód pokarmowy: Rzadkie były dysfagia, zaburzenia pragnienia i uszkodzenie wątroby/żółtaczka; rzadko występowała perforacja jelit.
Układ moczowo-płciowy: Częsta była nokturia; rzadko występowały podrażnienie pochwy, obrzęk jąder, infekcja dróg moczowych, bolesna erekcja i opóźniony wytrysk; rzadkie były moczenie i nietrzymanie moczu.
Neurologiczna: Częste były ataksja/brak koordynacji, drgawki, mioklonie, dyskineza i dystonia; rzadkie były rozszerzenie źrenic, zawroty głowy i dyzartria; rzadko występowały nieprawidłowości w elektroencefalogramie (EEG) i zaburzenia uwagi.
Neuropsychiatryczny: Częste były mania/hipomania, zwiększone libido, halucynacje, osłabienie funkcji seksualnych i depresja; rzadkie były zaburzenia pamięci, depersonalizacja, psychoza, dysforia, niestabilność nastroju, paranoja i formalne zaburzenie myślenia; rzadko zdarzały się myśli samobójcze.
Skargi ustne: Częste było zapalenie jamy ustnej; rzadko występowały bóle zębów, bruksizm, podrażnienie dziąseł i obrzęk jamy ustnej.
Oddechowy: Rzadkie były zapalenie oskrzeli i duszność/duszność; rzadko występował zator płucny.
Zmysły specjalne: Rzadkie były zaburzenia widzenia; rzadkie było podwójne widzenie.
Niespecyficzne: Częste były objawy grypopodobne; rzadki był niespecyficzny ból; rzadkie było przedawkowanie.
Zmieniony apetyt i waga
Utrata masy ciała większa niż 5 funtów. wystąpiło u 28% osób otrzymujących WELLBUTRIN. Częstość ta jest w przybliżeniu dwukrotnie wyższa niż u porównywalnych osób leczonych tricyklicznymi lub placebo. Ponadto, podczas gdy 35% osób otrzymujących trójpierścieniowe leki przeciwdepresyjne przybrało na wadze, tylko 9,4% osób leczonych preparatem WELLBUTRIN zrobiło to. W związku z tym, jeśli utrata masy ciała jest głównym objawem choroby depresyjnej pacjenta, należy wziąć pod uwagę potencjał anorektyczny i/lub redukujący masę ciała WELLBUTRIN.
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania produktu WELLBUTRIN po dopuszczeniu do obrotu i nie zostały opisane w innym miejscu na etykiecie. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Ciało (ogólne)
Ból stawów, ból mięśni i gorączka z wysypką i innymi objawami sugerującymi nadwrażliwość opóźnioną. Objawy te mogą przypominać chorobę posurowiczą [patrz OSTRZEŻENIA I ŚRODKI ].
Układ sercowo-naczyniowy
Nadciśnienie (w niektórych przypadkach ciężkie), niedociśnienie ortostatyczne, blok serca trzeciego stopnia.
Wewnątrzwydzielniczy
Hiponatremia, zespół nieprawidłowego wydzielania hormonu antydiuretycznego, hiperglikemia, hipoglikemia.
Przewód pokarmowy
Zapalenie przełyku, zapalenie wątroby.
Hemiczny i limfatyczny
Wybroczyny, leukocytoza, leukopenia, małopłytkowość. Zmieniony PT i/lub INR, rzadko związany z powikłaniami krwotocznymi lub zakrzepowymi, obserwowano podczas jednoczesnego podawania bupropionu z warfaryną.
Układ mięśniowo-szkieletowy
Sztywność mięśni/gorączka/rabdomioliza, osłabienie mięśni.
System nerwowy
Agresja, śpiączka, dokonane samobójstwo, majaczenie, zaburzenia snu, myśli paranoidalne, parestezje, parkinsonizm, niepokój ruchowy, próby samobójcze, demaskowanie późnych dyskinez.
Skóra i przydatki
Zespół Stevensa-Johnsona, obrzęk naczynioruchowy, złuszczające zapalenie skóry, pokrzywka.
Specjalne zmysły
Szum w uszach, zwiększone ciśnienie wewnątrzgałkowe.
INTERAKCJE Z LEKAMI
Potencjał innych leków wpływających na WELLBUTRIN
Bupropion jest metabolizowany głównie do hydroksybupropionu przez CYP2B6. W związku z tym istnieje możliwość interakcji między lekiem WELLBUTRIN a lekami będącymi inhibitorami lub induktorami CYP2B6.
Inhibitory CYP2B6
Tiklopidyna i klopidogrel
Jednoczesne leczenie tymi lekami może zwiększać ekspozycję na bupropion, ale zmniejszać ekspozycję na hydroksybupropion. W oparciu o odpowiedź kliniczną może być konieczne dostosowanie dawki preparatu WELLBUTRIN w przypadku jednoczesnego podawania z inhibitorami CYP2B6 (np. tyklopidyną lub klopidogrelem) [patrz FARMAKOLOGIA KLINICZNA ].
Induktory CYP2B6
Rytonawir, Lopinawir i Efawirenz
Jednoczesne leczenie tymi lekami może zmniejszyć ekspozycję na bupropion i hydroksybupropion. Może być konieczne zwiększenie dawki produktu WELLBUTRIN w przypadku jednoczesnego podawania z rytonawirem, lopinawirem lub efawirenzem [patrz FARMAKOLOGIA KLINICZNA ], ale nie powinna przekraczać maksymalnej zalecanej dawki.
Karbamazepina, Fenobarbital, Fenytoina
Chociaż nie są one systematycznie badane, leki te mogą indukować metabolizm bupropionu i zmniejszać ekspozycję na bupropion [patrz FARMAKOLOGIA KLINICZNA ]. Jeśli bupropion jest stosowany jednocześnie z induktorem CYP, może być konieczne zwiększenie dawki bupropionu, ale nie należy przekraczać maksymalnej zalecanej dawki.
Potencjał WELLBUTRIN 300 mg na inne leki
Leki metabolizowane przez CYP2D6
Bupropion i jego metabolity (erytrohydrobupropion, treohydrobupropion, hydroksybupropion) są inhibitorami CYP2D6. Dlatego jednoczesne podawanie produktu WELLBUTRIN z lekami metabolizowanymi przez CYP2D6 może zwiększać ekspozycję na leki będące substratami CYP2D6. Takie leki obejmują niektóre leki przeciwdepresyjne (np. wenlafaksyna, nortryptylina, imipramina, dezypramina, paroksetyna, fluoksetyna i sertralina), leki przeciwpsychotyczne (np. haloperidol, risperidon, tiorydazyna), beta-blokery (np. metoprolol) i leki przeciwarytmiczne typu 1C ( , propafenon i flekainid). W przypadku jednoczesnego stosowania z preparatem WELLBUTRIN może być konieczne zmniejszenie dawki tych substratów CYP2D6, szczególnie w przypadku leków o wąskim indeksie terapeutycznym.
Leki, które wymagają aktywacji metabolicznej przez CYP2D6, aby były skuteczne (np. tamoksyfen), teoretycznie mogą mieć zmniejszoną skuteczność, gdy są podawane jednocześnie z inhibitorami CYP2D6, takimi jak bupropion. Pacjenci leczeni jednocześnie preparatem WELLBUTRIN i takimi lekami mogą wymagać zwiększonych dawek leku [patrz FARMAKOLOGIA KLINICZNA ].
Digoksyna
Jednoczesne podawanie produktu WELLBUTRIN z digoksyną może zmniejszać stężenie digoksyny w osoczu. Monitorować stężenie digoksyny w osoczu u pacjentów leczonych jednocześnie produktem WELLBUTRIN i digoksyną [patrz FARMAKOLOGIA KLINICZNA ].
Leki obniżające próg napadów
Należy zachować szczególną ostrożność podczas jednoczesnego podawania preparatu WELLBUTRIN z innymi lekami obniżającymi próg drgawkowy (np. innymi produktami bupropionowymi, lekami przeciwpsychotycznymi, lekami przeciwdepresyjnymi, teofiliną lub kortykosteroidami ogólnoustrojowymi). Stosuj niskie dawki początkowe i stopniowo zwiększaj dawkę [patrz PRZECIWWSKAZANIA , OSTRZEŻENIA I ŚRODKI ].
Leki dopaminergiczne (lewodopa i amantadyna)
Bupropion, lewodopa i amantadyna mają działanie agonistyczne dopaminy. Donoszono o toksycznym działaniu na OUN, gdy bupropion podawano jednocześnie z lewodopą lub amantadyną. Działania niepożądane obejmowały niepokój, pobudzenie, drżenie, ataksję, zaburzenia chodu, zawroty głowy i zawroty głowy. Przypuszcza się, że toksyczność wynika ze skumulowanego działania agonisty dopaminy. Należy zachować ostrożność podając WELLBUTRIN 150 mg jednocześnie z tymi lekami.
Używaj z alkoholem
Po wprowadzeniu produktu do obrotu rzadko zgłaszano niepożądane zdarzenia neuropsychiatryczne lub zmniejszoną tolerancję alkoholu u pacjentów, którzy pili alkohol podczas leczenia preparatem WELLBUTRIN. Należy ograniczyć do minimum lub unikać spożywania alkoholu podczas leczenia preparatem WELLBUTRIN.
Inhibitory MAO
Bupropion hamuje wychwyt zwrotny dopaminy i noradrenaliny. Jednoczesne stosowanie MAOI i bupropionu jest przeciwwskazane, ponieważ istnieje zwiększone ryzyko wystąpienia reakcji nadciśnieniowych, jeśli bupropion jest stosowany jednocześnie z MAOI. Badania na zwierzętach wykazują, że ostra toksyczność bupropionu jest wzmacniana przez inhibitor MAO, fenelzynę. Pomiędzy odstawieniem MAOI przeznaczonego do leczenia depresji a rozpoczęciem leczenia preparatem WELLBUTRIN powinno upłynąć co najmniej 14 dni. Odwrotnie, należy odczekać co najmniej 14 dni po odstawieniu leku WELLBUTRIN 150mg przed rozpoczęciem leczenia przeciwdepresyjnego MAOI [patrz DAWKOWANIE I SPOSÓB PODAWANIA , PRZECIWWSKAZANIA ].
Interakcje lekowo-laboratoryjne
U pacjentów przyjmujących bupropion zgłaszano fałszywie dodatnie testy przesiewowe moczu na obecność amfetaminy. Wynika to z braku specyficzności niektórych badań przesiewowych. Fałszywie dodatnie wyniki testu mogą być wynikiem nawet po przerwaniu leczenia bupropionem. Testy potwierdzające, takie jak chromatografia gazowa/spektrometria mas, pozwolą odróżnić bupropion od amfetamin.
Nadużywanie i uzależnienie od narkotyków
Substancja kontrolowana
Bupropion nie jest substancją kontrolowaną.
Nadużywać
Ludzie
Kontrolowane badania kliniczne przeprowadzone na zdrowych ochotnikach, na osobach z historią nadużywania wielu leków oraz na osobach z depresją wykazały pewien wzrost aktywności motorycznej i pobudzenia/podniecenia, często typowego dla ośrodkowej aktywności pobudzającej.
W populacji osób doświadczających nadużywania narkotyków pojedyncza doustna dawka 400 mg bupropionu wywoływała łagodną aktywność podobną do amfetaminy w porównaniu z placebo w podskali Morfina-Benzedryna z Inwentaryzacji Centrum Badań Uzależnień (ARCI) i wynik wyższy niż placebo, ale mniej niż 15 mg dekstroamfetaminy stymulującej według Schedule II w skali sympatii ARCI. Skale te mierzą ogólne odczucia euforii i upodobania do narkotyków, które często wiążą się z możliwością nadużywania.
Nie wiadomo jednak, jak wyniki badań klinicznych pozwalają wiarygodnie przewidzieć potencjalne nadużywanie leków. Niemniej jednak dowody z badań z pojedynczą dawką sugerują, że zalecana dzienna dawka bupropionu podawanego doustnie w dawkach podzielonych prawdopodobnie nie będzie znacząco wzmacniać działania amfetaminy lub stymulantów ośrodkowego układu nerwowego. Jednak wyższe dawki (które nie mogły zostać przetestowane ze względu na ryzyko napadu) mogą być umiarkowanie atrakcyjne dla osób nadużywających leków pobudzających OUN.
WELLBUTRIN jest przeznaczony wyłącznie do stosowania doustnego. Zgłaszano wdychanie rozkruszonych tabletek lub wstrzykiwanie rozpuszczonego bupropionu. Zgłaszano drgawki i (lub) przypadki zgonu po podaniu bupropionu donosowo lub pozajelitowo.
Zwierząt
Badania na gryzoniach i naczelnych wykazały, że bupropion wykazuje pewne działania farmakologiczne wspólne dla psychostymulantów. Wykazano, że u gryzoni zwiększa aktywność lokomotoryczną, wywołuje łagodną, stereotypową reakcję behawioralną i zwiększa odsetek odpowiedzi w kilku paradygmatach zachowań kontrolowanych harmonogramem. W modelach naczelnych oceniających pozytywny, wzmacniający wpływ leków psychoaktywnych bupropion podawano samodzielnie dożylnie. U szczurów bupropion powodował dyskryminacyjne efekty bodźca podobne do amfetaminy i kokainy w paradygmatach dyskryminacji narkotyków stosowanych do scharakteryzowania subiektywnych skutków leków psychoaktywnych.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Myśli i zachowania samobójcze u dzieci, młodzieży i młodych dorosłych
Pacjenci z MDD, zarówno dorośli, jak i pediatryczni, mogą doświadczać nasilenia depresji i/lub pojawienia się myśli i zachowań samobójczych (samobójstwa) lub niezwykłych zmian w zachowaniu, niezależnie od tego, czy przyjmują leki przeciwdepresyjne, a ryzyko to może utrzymywać się do znaczącego następuje remisja. Samobójstwo jest znanym ryzykiem depresji i niektórych innych zaburzeń psychicznych, a same te zaburzenia są najsilniejszymi predyktorami samobójstwa. Od dawna istnieje obawa, że leki przeciwdepresyjne mogą odgrywać rolę w wywoływaniu nasilenia depresji i pojawianiu się samobójstw u niektórych pacjentów we wczesnych fazach leczenia.
Zbiorcze analizy krótkoterminowych, kontrolowanych placebo badań leków przeciwdepresyjnych (selektywnych inhibitorów wychwytu zwrotnego serotoniny [SSRI] i innych) pokazują, że leki te zwiększają ryzyko myśli i zachowań samobójczych (samobójczych) u dzieci, młodzieży i młodych dorosłych (w wieku 18 lat). do 24) z MDD i innymi zaburzeniami psychicznymi. Krótkoterminowe badania kliniczne nie wykazały wzrostu ryzyka samobójstw w przypadku stosowania leków przeciwdepresyjnych w porównaniu z placebo u osób dorosłych w wieku powyżej 24 lat; u osób dorosłych w wieku 65 lat i starszych odnotowano zmniejszenie liczby leków przeciwdepresyjnych w porównaniu z placebo.
Zbiorcze analizy badań kontrolowanych placebo u dzieci i młodzieży z MDD, zaburzeniami obsesyjno-kompulsywnymi (OCD) lub innymi zaburzeniami psychicznymi obejmowały łącznie 24 krótkoterminowe badania 9 leków przeciwdepresyjnych z udziałem ponad 4400 osób. Zbiorcze analizy badań kontrolowanych placebo u dorosłych z MDD lub innymi zaburzeniami psychicznymi obejmowały łącznie 295 krótkoterminowych badań (mediana czasu trwania wynosząca 2 miesiące) 11 leków przeciwdepresyjnych z udziałem ponad 77 000 pacjentów. Istniało znaczne zróżnicowanie w ryzyku samobójstwa wśród leków, ale tendencja do wzrostu wśród młodszych osób w przypadku prawie wszystkich badanych leków. Istniały różnice w bezwzględnym ryzyku samobójstwa w różnych wskazaniach, z największą częstością występowania MDD. Różnice ryzyka (lek vs placebo) były jednak stosunkowo stabilne w obrębie warstw wiekowych i we wskazaniach. Te różnice w ryzyku (różnica między lekami a placebo w liczbie przypadków samobójstw na 1000 leczonych pacjentów) przedstawiono w Tabeli 1.
żadnym z badań pediatrycznych nie doszło do samobójstw. W badaniach z udziałem dorosłych zdarzały się samobójstwa, ale liczba ta nie była wystarczająca, aby wyciągnąć jakiekolwiek wnioski na temat wpływu leku na samobójstwo.
Nie wiadomo, czy ryzyko samobójstwa rozciąga się na długotrwałe używanie, tj. dłużej niż kilka miesięcy. Jednak istnieją dowody z kontrolowanych placebo badań podtrzymujących u dorosłych z depresją, że stosowanie leków przeciwdepresyjnych może opóźnić nawrót depresji.
Wszyscy pacjenci leczeni lekami przeciwdepresyjnymi w jakimkolwiek wskazaniu powinni być odpowiednio monitorowani i obserwowani pod kątem pogorszenia stanu klinicznego, skłonności samobójczych i nietypowych zmian w zachowaniu, szczególnie w ciągu pierwszych kilku miesięcy terapii lekowej lub w czasie zmiany dawki, albo zwiększa się lub maleje [patrz OSTRZEŻENIE W RAMCE].
Następujące objawy: lęk, pobudzenie, ataki paniki, bezsenność, drażliwość, wrogość, agresywność, impulsywność, akatyzję (niepokój psychoruchowy), hipomanię i manię zgłaszano również u dorosłych i dzieci leczonych lekami przeciwdepresyjnymi z powodu dużych zaburzeń depresyjnych. co do innych wskazań, zarówno psychiatrycznych, jak i niepsychiatrycznych. Chociaż nie ustalono związku przyczynowo-skutkowego między pojawieniem się takich objawów a nasileniem depresji i/lub pojawieniem się impulsów samobójczych, istnieje obawa, że takie objawy mogą być prekursorem pojawiania się samobójstw.
Należy rozważyć zmianę schematu leczenia, w tym ewentualnie odstawienie leku, u pacjentów, u których depresja jest stale nasilona lub u których pojawiają się myśli samobójcze lub objawy, które mogą być prekursorami nasilenia depresji lub myśli samobójczych, zwłaszcza jeśli objawy te są ciężkie, nagłe na początku lub nie były częścią objawów występujących u pacjenta.
Rodziny i opiekunowie pacjentów leczonych lekami przeciwdepresyjnymi z powodu MDD lub innych wskazań, zarówno psychiatrycznych, jak i niepsychiatrycznych, powinni być ostrzeżeni o konieczności monitorowania pacjentów pod kątem pojawienia się pobudzenia, drażliwości, nietypowych zmian w zachowaniu i innych objawów opisanych powyżej, ponieważ a także pojawienia się samobójstw i natychmiastowego zgłaszania takich objawów świadczeniodawcom. Taki monitoring powinien obejmować codzienną obserwację rodzin i opiekunów. Recepty na WELLBUTRIN 150mg należy wypisać na najmniejszą ilość tabletek zgodnie z dobrym postępowaniem z pacjentem, aby zmniejszyć ryzyko przedawkowania.
Neuropsychiatryczne zdarzenia niepożądane i ryzyko samobójstwa w leczeniu rzucania palenia
WELLBUTRIN nie jest zatwierdzony do leczenia zaprzestania palenia; zawiera jednak tę samą substancję czynną, co lek na rzucenie palenia ZYBAN. U pacjentów przyjmujących bupropion w celu zaprzestania palenia zgłaszano poważne neuropsychiatryczne zdarzenia niepożądane. Te doniesienia po wprowadzeniu do obrotu obejmowały zmiany nastroju (w tym depresję i manię), psychozy, halucynacje, paranoję, urojenia, myśli mordercze, agresję, wrogość, pobudzenie, lęk i panikę, a także myśli samobójcze, próby samobójcze i zakończone samobójstwa [ Widzieć DZIAŁANIA NIEPOŻĄDANE ]. Niektórzy pacjenci, którzy rzucili palenie, mogli odczuwać objawy odstawienia nikotyny, w tym obniżony nastrój. Depresję, rzadko obejmującą myśli samobójcze, zgłaszano u palaczy podejmujących próbę zaprzestania palenia bez leków. Jednak niektóre z tych działań niepożądanych wystąpiły u pacjentów przyjmujących bupropion, którzy nadal palili.
Neuropsychiatryczne zdarzenia niepożądane wystąpiły u pacjentów bez lub z istniejącą wcześniej chorobą psychiczną; niektórzy pacjenci doświadczyli pogorszenia swoich chorób psychicznych. Obserwować pacjentów pod kątem występowania neuropsychiatrycznych zdarzeń niepożądanych. Należy poinformować pacjentów i opiekunów, że pacjent powinien przerwać przyjmowanie leku WELLBUTRIN 300 mg i niezwłocznie skontaktować się z lekarzem, jeśli wystąpi pobudzenie, obniżony nastrój lub zmiany w zachowaniu lub myśleniu, które nie są typowe dla pacjenta, lub jeśli u pacjenta wystąpią myśli samobójcze lub zachowania samobójcze . W wielu przypadkach po wprowadzeniu do obrotu zgłaszano ustąpienie objawów po odstawieniu bupropionu. Jednak w niektórych przypadkach objawy utrzymywały się; dlatego należy zapewnić stałe monitorowanie i leczenie podtrzymujące do czasu ustąpienia objawów.
Konfiskata
WELLBUTRIN 300mg może powodować drgawki. Ryzyko napadu jest zależne od dawki. Dawka nie powinna przekraczać 450 mg/dobę. Zwiększaj dawkę stopniowo. Przerwać WELLBUTRIN 150 mg i nie wznawiać leczenia, jeśli u pacjenta wystąpi napad drgawkowy.
Ryzyko napadów jest również związane z czynnikami pacjenta, sytuacjami klinicznymi i przyjmowanymi jednocześnie lekami obniżającymi próg drgawkowy. Rozważ te zagrożenia przed rozpoczęciem leczenia preparatem WELLBUTRIN. WELLBUTRIN 300 mg jest przeciwwskazany u pacjentów z napadami padaczkowymi, z obecnym lub wcześniejszym rozpoznaniem jadłowstrętu psychicznego lub bulimii, lub u pacjentów po nagłym odstawieniu alkoholu, benzodiazepin, barbituranów i leków przeciwpadaczkowych [patrz PRZECIWWSKAZANIA , INTERAKCJE Z LEKAMI ]. Następujące stany mogą również zwiększać ryzyko napadu: ciężki uraz głowy; malformacja tętniczo-żylna; guz OUN lub infekcja OUN; ciężki udar; jednoczesne stosowanie innych leków obniżających próg drgawkowy (np. innych produktów bupropionowych, leków przeciwpsychotycznych, trójpierścieniowych leków przeciwdepresyjnych, teofiliny i kortykosteroidów ogólnoustrojowych); zaburzenia metaboliczne (np. hipoglikemia, hiponatremia, ciężkie zaburzenia czynności wątroby i niedotlenienie); zażywanie nielegalnych narkotyków (np. kokainy); lub nadużywanie lub niewłaściwe stosowanie leków na receptę, takich jak środki pobudzające ośrodkowy układ nerwowy. Dodatkowe stany predysponujące obejmują cukrzycę leczoną doustnymi lekami hipoglikemizującymi lub insuliną; stosowanie leków anorektycznych; nadużywanie alkoholu, benzodiazepin, środków uspokajających/nasennych lub opiatów.
Przypadki napadów przy użyciu bupropionu
Bupropion wiąże się z drgawkami u około 0,4% (4/1000) pacjentów leczonych dawkami do 450 mg/dobę. Szacowana częstość występowania napadów w przypadku WELLBUTRIN wzrasta prawie 10-krotnie między 450 a 600 mg/dzień.
Ryzyko drgawek można zmniejszyć, jeśli dawka preparatu WELLBUTRIN 300 mg nie przekracza 450 mg/dobę, podawana w dawce 150 mg 3 razy na dobę, a tempo zwiększania dawki jest stopniowe.
Nadciśnienie
Leczenie preparatem WELLBUTRIN może powodować podwyższone ciśnienie krwi i nadciśnienie. Ocenić ciśnienie krwi przed rozpoczęciem leczenia preparatem WELLBUTRIN 150mg i okresowo monitorować w trakcie leczenia. Ryzyko nadciśnienia jest zwiększone, jeśli WELLBUTRIN 150 mg jest stosowany jednocześnie z IMAO lub innymi lekami zwiększającymi aktywność dopaminergiczną lub noradrenergiczną [patrz PRZECIWWSKAZANIA ].
Dane z badania porównawczego preparatu bupropionu o przedłużonym uwalnianiu, nikotynowego systemu transdermalnego (NTS), połączenia bupropionu o przedłużonym uwalnianiu z NTS i placebo jako środka wspomagającego rzucenie palenia sugerują częstsze występowanie nadciśnienia tętniczego związanego z leczeniem u pacjenci leczeni kombinacją bupropionu o przedłużonym uwalnianiu i NTS. W tym badaniu u 6,1% pacjentów leczonych skojarzeniem bupropionu o przedłużonym uwalnianiu i NTS wystąpiło nadciśnienie związane z leczeniem w porównaniu z odpowiednio 2,5%, 1,6% i 3,1% pacjentów leczonych bupropionem o przedłużonym uwalnianiu, NTS i placebo. . Większość z tych osób miała dowody na wcześniejsze nadciśnienie. U trzech pacjentów (1,2%) leczonych kombinacją bupropionu o przedłużonym uwalnianiu i NTS oraz 1 pacjenta (0,4%) leczonego NTS odstawiono badany lek z powodu nadciśnienia, w porównaniu z żadnym z pacjentów leczonych bupropionem o przedłużonym uwalnianiu lub placebo. Zaleca się monitorowanie ciśnienia krwi u pacjentów otrzymujących połączenie bupropionu i substytucji nikotyny.
badaniu klinicznym bupropionu o natychmiastowym uwalnianiu u pacjentów z MDD ze stabilną zastoinową niewydolnością serca (n = 36), bupropion wiązał się z zaostrzeniem istniejącego wcześniej nadciśnienia u 2 pacjentów, co prowadziło do przerwania leczenia bupropionem. Nie ma kontrolowanych badań oceniających bezpieczeństwo bupropionu u pacjentów z niedawno przebytym zawałem mięśnia sercowego lub niestabilną chorobą serca.
Aktywacja manii/hipomanii
Leczenie przeciwdepresyjne może wywołać epizod maniakalny, mieszany lub hipomaniakalny. Ryzyko wydaje się być zwiększone u pacjentów z chorobą afektywną dwubiegunową lub z czynnikami ryzyka choroby afektywnej dwubiegunowej. Przed rozpoczęciem leczenia WELLBUTRIN należy przebadać pacjentów pod kątem choroby afektywnej dwubiegunowej w wywiadzie i obecności czynników ryzyka choroby afektywnej dwubiegunowej (np. wywiad rodzinny w kierunku choroby afektywnej dwubiegunowej, samobójstwa lub depresji). WELLBUTRIN 150mg nie jest zatwierdzony do stosowania w leczeniu depresji afektywnej dwubiegunowej.
Psychoza i inne reakcje neuropsychiatryczne
pacjentów z depresją leczonych preparatem WELLBUTRIN występowały różne neuropsychiatryczne objawy przedmiotowe i podmiotowe, w tym urojenia, halucynacje, psychozy, zaburzenia koncentracji, paranoja i splątanie. U niektórych z tych pacjentów rozpoznano chorobę afektywną dwubiegunową. W niektórych przypadkach objawy te ustępowały po zmniejszeniu dawki i/lub zaprzestaniu leczenia. Należy poinstruować pacjentów, aby w przypadku wystąpienia takich reakcji skontaktowali się z pracownikiem służby zdrowia.
Jaskra zamykającego się kąta
Rozszerzenie źrenic, które występuje po zastosowaniu wielu leków przeciwdepresyjnych, w tym WELLBUTRIN 300 mg, może wywołać atak zamykającego się kąta u pacjenta z anatomicznie wąskim kątem, który nie ma drożnej irydektomii.
Reakcje nadwrażliwości
Podczas badań klinicznych bupropionu występowały reakcje rzekomoanafilaktyczne/anafilaktyczne. Reakcje charakteryzowały się świądem, pokrzywką, obrzękiem naczynioruchowym i dusznością wymagającą leczenia. Ponadto po wprowadzeniu do obrotu rzadko zgłaszano spontaniczne zgłoszenia rumienia wielopostaciowego, zespołu Stevensa-Johnsona i wstrząsu anafilaktycznego związanego z bupropionem. Należy poinstruować pacjentów, aby przerwali przyjmowanie preparatu WELLBUTRIN 150 mg i skonsultowali się z lekarzem, jeśli podczas leczenia wystąpią u nich reakcje alergiczne lub anafilaktoidalne/anafilaktyczne (np. wysypka skórna, świąd, pokrzywka, ból w klatce piersiowej, obrzęk i duszność).
Istnieją doniesienia o bólach stawów, bólach mięśni, gorączce z wysypką i innych objawach podobnych do choroby posurowiczej sugerujących nadwrażliwość opóźnioną.
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( Przewodnik po lekach ).
Myśli i zachowania samobójcze
Poinstruuj pacjentów, ich rodziny i/lub ich opiekunów, aby byli wyczuleni na pojawienie się lęku, pobudzenia, ataków paniki, bezsenności, drażliwości, wrogości, agresywności, impulsywności, akatyzji (niepokoju psychoruchowego), hipomanii, manii, innych nietypowych zmian w zachowaniu , nasilenie depresji i myśli samobójcze, szczególnie na początku leczenia przeciwdepresyjnego oraz przy zwiększaniu lub zmniejszaniu dawki. Doradź rodzinom i opiekunom pacjentów, aby codziennie obserwowali pojawienie się takich objawów, ponieważ zmiany mogą być nagłe. Takie objawy należy zgłaszać lekarzowi przepisującemu pacjentowi lub pracownikowi służby zdrowia, zwłaszcza jeśli są one ciężkie, mają nagły początek lub nie były częścią objawów występujących u pacjenta. Takie objawy mogą wiązać się ze zwiększonym ryzykiem myśli i zachowań samobójczych i wskazują na potrzebę bardzo ścisłego monitorowania i ewentualnie zmian w leczeniu.
Neuropsychiatryczne zdarzenia niepożądane i ryzyko samobójstwa w leczeniu rzucania palenia
Chociaż WELLBUTRIN 150mg nie jest wskazany do leczenia rzucania palenia, zawiera ten sam składnik aktywny co ZYBAN, który jest dopuszczony do tego zastosowania. Poinformuj pacjentów, że niektórzy pacjenci doświadczyli zmian nastroju (w tym depresji i manii), psychozy, halucynacji, paranoi, urojeń, myśli morderczych, agresji, wrogości, pobudzenia, lęku i paniki, a także myśli samobójczych i samobójstwa podczas próby rzucenia palenia palenie podczas przyjmowania bupropionu. Należy poinstruować pacjentów, aby odstawili bupropion i skontaktowali się z pracownikiem służby zdrowia, jeśli wystąpią takie objawy [patrz OSTRZEŻENIA I ŚRODKI , DZIAŁANIA NIEPOŻĄDANE ].
Ciężkie reakcje alergiczne
Edukować pacjentów w zakresie objawów nadwrażliwości i zaprzestać przyjmowania preparatu WELLBUTRIN 300mg, jeśli wystąpią u nich ciężka reakcja alergiczna.
Konfiskata
Należy poinstruować pacjentów, aby przerwali leczenie i nie wznawiali WELLBUTRIN, jeśli wystąpią napady drgawkowe podczas leczenia. Poinformuj pacjentów, że nadmierne spożycie lub nagłe odstawienie alkoholu, benzodiazepin, leków przeciwpadaczkowych lub środków uspokajających/nasennych może zwiększyć ryzyko napadu drgawkowego. Doradź pacjentom, aby minimalizowali lub unikali spożywania alkoholu.
Jaskra zamykającego się kąta
Należy poinformować pacjentów, że przyjmowanie leku WELLBUTRIN 150 mg może powodować łagodne rozszerzenie źrenic, które u osób podatnych może prowadzić do epizodu jaskry zamykającego się kąta. Wcześniej istniejąca jaskra jest prawie zawsze jaskrą otwartego kąta, ponieważ jaskra zamkniętego kąta, po zdiagnozowaniu, może być ostatecznie leczona za pomocą irydektomii. Jaskra otwartego kąta nie jest czynnikiem ryzyka jaskry zamykającego się kąta. Pacjenci mogą chcieć zostać przebadani w celu ustalenia, czy są podatni na zamknięcie kąta i przejść zabieg profilaktyczny (np. irydektomia), jeśli są podatni [patrz OSTRZEŻENIA I ŚRODKI ].
Produkty zawierające bupropion
Należy pouczyć pacjentów, że WELLBUTRIN 150 mg zawiera tę samą substancję czynną (chlorowodorek bupropionu), co ZYBAN, który jest stosowany jako pomoc w leczeniu rzucania palenia, oraz że WELLBUTRIN 150 mg nie powinien być stosowany w połączeniu z ZYBAN lub jakimikolwiek innymi lekami zawierającymi bupropion (np. jako WELLBUTRIN 150 mg SR, preparat o przedłużonym uwalnianiu i WELLBUTRIN XL lub FORFIVO XL, preparaty o przedłużonym uwalnianiu oraz APLENZIN, preparat o przedłużonym uwalnianiu bromowodorku bupropionu). Ponadto istnieje szereg generycznych produktów chlorowodorku bupropionu do preparatów o natychmiastowym, przedłużonym i przedłużonym uwalnianiu.
Możliwość upośledzenia funkcji poznawczych i motorycznych
Poinformuj pacjentów, że jakikolwiek lek działający na OUN, taki jak WELLBUTRIN, może osłabiać ich zdolność do wykonywania zadań wymagających oceny lub zdolności motorycznych i poznawczych. Poinformuj pacjentów, że dopóki nie będą mieć wystarczającej pewności, że WELLBUTRIN 300 mg nie wpływa negatywnie na ich wydajność, powinni powstrzymać się od prowadzenia samochodu lub obsługi skomplikowanych, niebezpiecznych maszyn. WELLBUTRIN 150mg może prowadzić do zmniejszenia tolerancji na alkohol.
Leki towarzyszące
Poradź pacjentom, aby powiadomili swojego lekarza, jeśli przyjmują lub planują przyjmować leki na receptę lub leki dostępne bez recepty, ponieważ WELLBUTRIN 150 mg i inne leki mogą wpływać na metabolizm innych.
Ciąża
Należy doradzić pacjentkom, aby powiadomiły swojego lekarza, jeśli zajdą w ciążę lub zamierzają zajść w ciążę podczas leczenia preparatem WELLBUTRIN. Poinformuj pacjentki, że istnieje rejestr ekspozycji na ciążę, który monitoruje przebieg ciąży u kobiet narażonych na działanie preparatu WELLBUTRIN 150 mg podczas ciąży [patrz Używaj w określonych populacjach ].
Informacje o przechowywaniu
Należy poinstruować pacjentów, aby przechowywali WELLBUTRIN w temperaturze pokojowej, między 68 ° F a 77 ° F (20 ° C do 25 ° C) i trzymały tabletki w suchym miejscu i poza zasięgiem światła.
Informacje administracyjne
Należy poinstruować pacjentów, aby przyjmowali WELLBUTRIN w równych dawkach podzielonych 3 lub 4 razy na dobę, w odstępie co najmniej 6 godzin, aby zminimalizować ryzyko napadu drgawkowego. Należy poinstruować pacjentów, aby w przypadku pominięcia dawki nie przyjmowali dodatkowej tabletki w celu uzupełnienia pominiętej dawki, a następną tabletkę przyjmowali o zwykłej porze ze względu na zależne od dawki ryzyko napadu drgawkowego. Należy poinstruować pacjentów, że tabletki WELLBUTRIN należy połykać w całości, a nie kruszyć, dzielić ani żuć. WELLBUTRIN można przyjmować z jedzeniem lub bez jedzenia.
WELLBUTRIN, WELLBUTRIN SR, WELLBUTRIN 150mg XL i ZYBAN są znakami towarowymi należącymi do lub licencjonowanymi przez grupę firm GSK. Inne wymienione marki są znakami towarowymi należącymi do ich odpowiednich właścicieli lub licencjonowanymi przez nich i nie są własnością ani nie są licencjonowane przez grupę spółek GSK. Twórcy tych marek nie są związani i nie popierają grupy firm GSK ani jej produktów.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Badania rakotwórczości w ciągu całego życia przeprowadzono na szczurach i myszach przy dawkach bupropionu odpowiednio do 300 i 150 mg/kg/dobę. Dawki te są odpowiednio około 6 i 2 razy większe od MRHD w przeliczeniu na mg/m2. W badaniu na szczurach zaobserwowano wzrost guzkowatych zmian proliferacyjnych wątroby po dawkach od 100 do 300 mg/kg/dobę (około 2 do 6 razy więcej niż MRHD w przeliczeniu na mg/m2); mniejsze dawki nie były testowane. Pytanie, czy takie zmiany mogą być prekursorami nowotworów wątroby, jest obecnie nierozstrzygnięte. W badaniu na myszach nie zaobserwowano podobnych zmian w wątrobie, aw żadnym z badań nie zaobserwowano wzrostu złośliwych guzów wątroby i innych narządów.
Bupropion wywołał pozytywną odpowiedź (2 do 3 razy większą częstość mutacji kontrolnych) w 2 z 5 szczepów w teście mutagenności bakteryjnej Amesa. Bupropion powodował wzrost aberracji chromosomowych w 1 z 3 badań cytogenetycznych szpiku kostnego szczurów in vivo.
Nie stwierdzono wpływu na płodność samców i samic, gdy szczurom podawano doustnie dawki bupropionu do 300 mg/kg/dobę (około 6 razy większe niż MRHD w przeliczeniu na mg/m2) samicom przed kryciem i do 13. dnia ciąży lub przez laktację, a samcom przez 60 dni przed i po kryciu. Jednak dawki 200 mg/kg/dobę (około 4-krotność MRHD w przeliczeniu na mg/m2) lub większe powodowały przejściową ataksję lub zmiany behawioralne u dorosłych samic szczurów. Nie stwierdzono również niekorzystnego wpływu na płodność, reprodukcję ani wzrost i rozwój potomstwa płci męskiej lub żeńskiej.
Używaj w określonych populacjach
Ciąża
Rejestr ekspozycji w ciąży
Istnieje niezależny rejestr ekspozycji w czasie ciąży, który monitoruje przebieg ciąży u kobiet narażonych w czasie ciąży na jakiekolwiek leki przeciwdepresyjne. Zachęcamy świadczeniodawców do rejestrowania pacjentów, dzwoniąc do Krajowego Rejestru Ciąży dla Antydepresantów pod numer 1-844-4056185 lub odwiedzając stronę internetową https://womensmentalhealth.org/clinical-and-researchprograms/pregnancyregistry/antidepressants.
Podsumowanie ryzyka
Dane z badań epidemiologicznych kobiet ciężarnych narażonych na bupropion w pierwszym trymestrze nie wykazały ogólnego zwiększonego ryzyka wad wrodzonych (patrz Dane ). Istnieje ryzyko dla matki związane z nieleczoną depresją w czasie ciąży (patrz Rozważania kliniczne ). Gdy bupropion podawano ciężarnym samicom szczurów w trakcie organogenezy, nie było dowodów na wady rozwojowe płodu w dawkach do około 10 razy większych od maksymalnej zalecanej dawki u ludzi (MRHD) wynoszącej 450 mg/dobę. Po podaniu ciężarnym samicom królików w trakcie organogenezy, obserwowano niezwiązane z dawką zwiększenie częstości występowania wad rozwojowych płodu i zmienności szkieletu po dawkach w przybliżeniu równych MRHD i większych. Zmniejszenie masy ciała płodu obserwowano przy dawkach dwukrotnie większych niż MRHD i większych (patrz Dane zwierząt ).
Szacowane ryzyko tła poważnych wad wrodzonych i poronienia jest nieznane dla wskazanej populacji. Wszystkie ciąże wiążą się z ryzykiem wady wrodzonej, utraty lub innych niekorzystnych skutków. W ogólnej populacji Stanów Zjednoczonych szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2% do 4% i 15% do 20%.
Rozważania kliniczne
Ryzyko związane z chorobą u matki i/lub zarodka/płodu
Prospektywne, podłużne badanie objęło 201 ciężarnych kobiet z wywiadem poważnych zaburzeń depresyjnych, które były w stanie eutymii i przyjmowały leki przeciwdepresyjne podczas ciąży na początku ciąży. Kobiety, które odstawiły leki przeciwdepresyjne w czasie ciąży, częściej doświadczały nawrotu ciężkiej depresji niż kobiety, które kontynuowały przyjmowanie leków przeciwdepresyjnych. Rozważ ryzyko dla matki nieleczonej depresji i potencjalny wpływ na płód w przypadku przerwania lub zmiany leczenia lekami przeciwdepresyjnymi w czasie ciąży i połogu.
Dane
Dane ludzkie
Dane z międzynarodowego rejestru ciąży na bupropion (675 ekspozycji w pierwszym trymestrze) oraz retrospektywne badanie kohortowe z wykorzystaniem bazy danych United Healthcare (1213 ekspozycji w pierwszym trymestrze) nie wykazały zwiększonego ryzyka wystąpienia wad rozwojowych. Rejestr nie został zaprojektowany ani przystosowany do oceny konkretnych wad, ale sugerował możliwy wzrost wad rozwojowych serca.
Nie zaobserwowano ogólnego zwiększonego ryzyka wad rozwojowych układu sercowo-naczyniowego po ekspozycji na bupropion w pierwszym trymestrze ciąży. Prospektywnie obserwowany odsetek wad rozwojowych układu sercowo-naczyniowego w ciążach z ekspozycją na bupropion w pierwszym trymestrze z międzynarodowego rejestru ciąż wynosił 1,3% (9 wad rozwojowych układu sercowo-naczyniowego/675 ekspozycji na bupropion u matki w pierwszym trymestrze), co jest podobne do częstości występowania wad rozwojowych układu sercowo-naczyniowego (w przybliżeniu). 1%). Dane z bazy danych United Healthcare, która obejmowała ograniczoną liczbę narażonych przypadków z wadami rozwojowymi układu sercowo-naczyniowego oraz badanie kliniczno-kontrolne (6853 niemowlęta z wadami rozwojowymi układu sercowo-naczyniowego i 5763 z wadami rozwojowymi innymi niż układ sercowo-naczyniowy) dotyczące stosowania bupropionu zgłoszonego przez samych pacjentów z National Birth Defects Badanie dotyczące zapobiegania (NBDPS) nie wykazało ogólnego zwiększonego ryzyka wad rozwojowych układu sercowo-naczyniowego po ekspozycji na bupropion w pierwszym trymestrze ciąży.
Wyniki badań dotyczące ekspozycji na bupropion w pierwszym trymestrze ciąży i ryzyka wystąpienia zwężenia drogi odpływu lewej komory (LVOTO) są niespójne i nie pozwalają na wyciągnięcie wniosków dotyczących możliwego związku. Baza danych United Healthcare nie miała wystarczającej mocy, aby ocenić to powiązanie; NBDPS wykazało zwiększone ryzyko LVOTO (n = 10; skorygowany OR = 2,6; 95% CI: 1,2, 5,7), a badanie kontrolne Slone Epidemiology nie wykazało zwiększonego ryzyka LVOTO.
Wyniki badań dotyczące ekspozycji na bupropion w pierwszym trymestrze ciąży i ryzyka wystąpienia ubytku w przegrodzie międzykomorowej (VSD) są niespójne i nie pozwalają na wyciągnięcie wniosków dotyczących możliwego związku. Slone Epidemiology Study wykazało zwiększone ryzyko VSD po ekspozycji matki na bupropion w pierwszym trymestrze (n = 17; skorygowany OR = 2,5; 95% CI: 1,3, 5,0), ale nie wykazało zwiększonego ryzyka innych badanych wad rozwojowych układu sercowo-naczyniowego (w tym LVOTO jako nad). W badaniu baz danych NBDPS i United Healthcare nie znaleziono związku między ekspozycją matki na bupropion w pierwszym trymestrze ciąży a VSD.
W przypadku wyników LVOTO i VSD badania były ograniczone niewielką liczbą ujawnionych przypadków, niespójnymi wynikami między badaniami oraz możliwością przypadkowych wyników wielokrotnych porównań w badaniach kontrolnych przypadków.
Dane zwierząt
badaniach przeprowadzonych na ciężarnych szczurach i królikach bupropion podawano doustnie w okresie organogenezy w dawkach odpowiednio do 450 i 150 mg/kg/dobę (odpowiednio około 10 i 6 razy większe niż MRHD w przeliczeniu na mg/m2) ). Nie było dowodów wad rozwojowych płodu u szczurów. Po podaniu ciężarnym królikom podczas organogenezy, zaobserwowano niezwiązane z dawką zwiększenie częstości występowania wad rozwojowych płodu i zmian szkieletowych przy najniższej badanej dawce (25 mg/kg/dobę, w przybliżeniu równe MRHD w przeliczeniu na mg/m2). i większe. Zmniejszoną masę ciała płodów obserwowano przy dawkach 50 mg/kg/dobę (w przybliżeniu 2-krotność MRHD w przeliczeniu na mg/m2) i większych. Nie stwierdzono toksyczności matczynej przy dawkach 50 mg/kg/dobę lub mniejszych.
badaniu rozwoju przed- i pourodzeniowego bupropion podawany doustnie ciężarnym samicom szczurów w dawkach do 150 mg/kg/dobę (około 3-krotność MRHD w przeliczeniu na mg/m2) od implantacji zarodka do laktacji nie miał wpływu na wzrost potomstwa lub rozwoju.
Laktacja
Podsumowanie ryzyka
Dane z opublikowanej literatury wskazują na obecność bupropionu i jego metabolitów w mleku ludzkim (patrz Dane ). Brak danych dotyczących wpływu bupropionu lub jego metabolitów na produkcję mleka. Ograniczone dane ze zgłoszeń po wprowadzeniu produktu do obrotu nie wykazały wyraźnego związku działań niepożądanych u niemowląt karmionych piersią. Należy wziąć pod uwagę korzyści rozwojowe i zdrowotne wynikające z karmienia piersią wraz z klinicznym zapotrzebowaniem matki na WELLBUTRIN oraz wszelkimi potencjalnymi niekorzystnymi skutkami stosowania WELLBUTRIN na karmione piersią dziecko lub wynikającymi z tego schorzenia matki.
Dane
badaniu laktacyjnym z udziałem 10 kobiet mierzono poziomy bupropionu podawanego doustnie i jego aktywnych metabolitów w odciągniętym mleku. Średnia dzienna ekspozycja niemowlęcia (przy założeniu 150 ml/kg dziennego spożycia) na bupropion i jego aktywne metabolity wynosiła 2% dawki dostosowanej do masy ciała matki. W raportach po wprowadzeniu produktu do obrotu opisano napady padaczkowe u niemowląt karmionych piersią. Związek między ekspozycją na bupropion a tymi napadami jest niejasny.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność w populacji pediatrycznej nie zostały ustalone [patrz OSTRZEŻENIE W PUDEŁKU , OSTRZEŻENIA I ŚRODKI ].
Zastosowanie geriatryczne
Spośród około 6000 osób, które uczestniczyły w badaniach klinicznych z bupropionem w postaci tabletek o przedłużonym uwalnianiu (badania dotyczące depresji i rzucania palenia), 275 było w wieku ≥65 lat, a 47 było w wieku ≥75 lat. Ponadto kilkaset osób w wieku ≥65 lat uczestniczyło w badaniach klinicznych z użyciem bupropionu o natychmiastowym uwalnianiu (badania dotyczące depresji). Nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między tymi osobami a młodszymi osobami. Zgłoszone doświadczenie kliniczne nie wykazało różnic w odpowiedziach między pacjentami w podeszłym wieku i młodszymi, ale nie można wykluczyć większej wrażliwości niektórych osób starszych.
Bupropion jest intensywnie metabolizowany w wątrobie do aktywnych metabolitów, które są dalej metabolizowane i wydalane przez nerki. Ryzyko działań niepożądanych może być większe u pacjentów z zaburzeniami czynności nerek. Ponieważ pacjenci w podeszłym wieku są bardziej narażeni na zaburzenia czynności nerek, może być konieczne uwzględnienie tego czynnika przy doborze dawki; przydatne może być monitorowanie czynności nerek [patrz DAWKOWANIE I SPOSÓB PODAWANIA , Używaj w określonych populacjach , FARMAKOLOGIA KLINICZNA ].
Zaburzenia czynności nerek
Należy rozważyć zmniejszenie dawki i (lub) częstości podawania produktu WELLBUTRIN u pacjentów z zaburzeniami czynności nerek (wskaźnik filtracji kłębuszkowej: poniżej 90 ml/min). Bupropion i jego metabolity są usuwane przez nerki i mogą się kumulować u tych pacjentów w większym niż zwykle stopniu. Uważnie monitorować reakcje niepożądane, które mogą wskazywać na wysokie narażenie na bupropion lub metabolity [patrz DAWKOWANIE I SPOSÓB PODAWANIA , FARMAKOLOGIA KLINICZNA ].
Niewydolność wątroby
pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności wątroby (wskaźnik Child-Pugh: 7 do 15) maksymalna dawka preparatu WELLBUTRIN 150 mg wynosi 75 mg na dobę. U pacjentów z łagodnymi zaburzeniami czynności wątroby (punktacja Child-Pugh: 5 do 6), należy rozważyć zmniejszenie dawki i (lub) częstość dawkowania [patrz DAWKOWANIE I SPOSÓB PODAWANIA , FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
Doświadczenie przedawkowania u ludzi
Zgłaszano przypadki przedawkowania bupropionu do 30 gramów lub więcej. Napad padaczkowy został zgłoszony w około jednej trzeciej wszystkich przypadków. Inne ciężkie reakcje zgłaszane po przedawkowaniu samego bupropionu obejmowały omamy, utratę przytomności, częstoskurcz zatokowy i zmiany w zapisie EKG, takie jak zaburzenia przewodzenia (w tym wydłużenie zespołu QRS) lub arytmie. Gorączka, sztywność mięśni, rabdomioliza, niedociśnienie, otępienie, śpiączka i niewydolność oddechowa były zgłaszane głównie wtedy, gdy bupropion był częścią przedawkowania wielu leków.
Chociaż większość pacjentów wyzdrowiała bez następstw, zgony związane z przedawkowaniem samego bupropionu odnotowano u pacjentów przyjmujących duże dawki leku. U tych pacjentów zgłaszano liczne niekontrolowane drgawki, bradykardię, niewydolność serca i zatrzymanie akcji serca przed śmiercią.
Zarządzanie przedawkowaniem
Skonsultuj się z Certyfikowanym Centrum Kontroli Zatruć, aby uzyskać aktualne wskazówki i porady. Numery telefonów do certyfikowanych ośrodków kontroli zatruć są wymienione w Physician's Desk Reference (PDR). Zadzwoń pod numer 1-800-222-1222 lub odwiedź www.poison.org.
Nie jest znane antidotum na bupropion. W przypadku przedawkowania należy zapewnić opiekę podtrzymującą, w tym ścisły nadzór i monitorowanie lekarskie. Rozważ możliwość wielokrotnego przedawkowania leków. Zapewnić odpowiednie drogi oddechowe, natlenienie i wentylację. Monitoruj rytm serca i parametry życiowe. Nie zaleca się wywoływania wymiotów.
PRZECIWWSKAZANIA
- WELLBUTRIN 150mg jest przeciwwskazany u pacjentów z zaburzeniami napadowymi.
- WELLBUTRIN jest przeciwwskazany u pacjentów z aktualnym lub wcześniejszym rozpoznaniem bulimii lub jadłowstrętu psychicznego, ponieważ u takich pacjentów leczonych produktem WELLBUTRIN obserwowano większą częstość występowania drgawek [patrz OSTRZEŻENIA I ŚRODKI ].
- WELLBUTRIN 300mg jest przeciwwskazany u pacjentów poddawanych nagłemu odstawieniu alkoholu, benzodiazepin, barbituranów i leków przeciwpadaczkowych [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI ].
- Stosowanie IMAO (przeznaczonych do leczenia zaburzeń psychicznych) jednocześnie z preparatem WELLBUTRIN 300 mg lub w ciągu 14 dni od zaprzestania leczenia preparatem WELLBUTRIN 150 mg jest przeciwwskazane. Istnieje zwiększone ryzyko wystąpienia reakcji nadciśnieniowych, gdy WELLBUTRIN jest stosowany jednocześnie z IMAO. Stosowanie preparatu WELLBUTRIN w ciągu 14 dni od zaprzestania leczenia IMAO jest również przeciwwskazane. Rozpoczęcie leczenia preparatem WELLBUTRIN 150 mg u pacjenta leczonego odwracalnymi inhibitorami MAO, takimi jak linezolid lub dożylnie błękit metylenowy, jest przeciwwskazane [patrz DAWKOWANIE I SPOSÓB PODAWANIA , OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI ].
- WELLBUTRIN jest przeciwwskazany u pacjentów ze stwierdzoną nadwrażliwością na bupropion lub inne składniki leku WELLBUTRIN. Zgłaszano reakcje rzekomoanafilaktyczne/anafilaktyczne i zespół Stevensa-Johnsona [patrz OSTRZEŻENIA I ŚRODKI ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Dokładny mechanizm przeciwdepresyjnego działania bupropionu nie jest znany, ale przypuszcza się, że jest związany z mechanizmami noradrenergicznymi i (lub) dopaminergicznymi. Bupropion jest stosunkowo słabym inhibitorem neuronalnego wychwytu zwrotnego norepinefryny i dopaminy i nie hamuje wychwytu zwrotnego serotoniny. Bupropion nie hamuje oksydazy monoaminowej.
Farmakokinetyka
Bupropion jest mieszaniną racemiczną. Nie badano aktywności farmakologicznej i farmakokinetyki poszczególnych enancjomerów. Średni okres półtrwania w fazie eliminacji (±SD) bupropionu po długotrwałym podawaniu wynosi 21 (±9) godzin, a stężenie bupropionu w osoczu w stanie stacjonarnym jest osiągane w ciągu 8 dni.
Wchłanianie
Całkowita biodostępność preparatu WELLBUTRIN u ludzi nie została określona, ponieważ preparat dożylny do stosowania u ludzi nie jest dostępny. Wydaje się jednak prawdopodobne, że tylko niewielka część podanej doustnie dawki dociera do krążenia systemowego w stanie nienaruszonym. W badaniach na szczurach i psach biodostępność bupropionu wahała się od 5% do 20%.
U ludzi, po podaniu doustnym produktu WELLBUTRIN 300 mg, maksymalne stężenie bupropionu w osoczu jest zwykle osiągane w ciągu 2 godzin. Stężenia bupropionu w osoczu są proporcjonalne do dawki po podaniu pojedynczych dawek od 100 do 250 mg; jednak nie wiadomo, czy proporcjonalność między dawką a poziomem w osoczu jest zachowana przy długotrwałym stosowaniu.
Dystrybucja
Badania in vitro wykazały, że bupropion w 84% wiąże się z białkami osocza ludzkiego w stężeniach do 200 mcg/ml. Stopień wiązania metabolitu hydroksybupropionu z białkami jest podobny do wiązania bupropionu, natomiast stopień wiązania metabolitu treohydrobupropionu z białkami jest o połowę mniejszy niż w przypadku bupropionu.
Metabolizm
Bupropion jest intensywnie metabolizowany u ludzi. Aktywne są trzy metabolity: hydroksybupropion, który powstaje w wyniku hydroksylacji grupy tert-butylowej bupropionu oraz izomery aminoalkoholowe treohydrobupropion i erytrohydrobupropion, które powstają w wyniku redukcji grupy karbonylowej. Wyniki badań in vitro sugerują, że CYP2B6 jest głównym izoenzymem biorącym udział w tworzeniu hydroksybupropionu, podczas gdy enzymy cytochromu P450 nie biorą udziału w tworzeniu treohydrobupropionu. Utlenianie łańcucha bocznego bupropionu powoduje powstanie koniugatu glicyny z kwasem meta-chlorobenzoesowym, który jest następnie wydalany jako główny metabolit z moczem. Moc i toksyczność metabolitów w stosunku do bupropionu nie zostały w pełni scharakteryzowane. Jednak w badaniach przesiewowych leków przeciwdepresyjnych na myszach wykazano, że hydroksybupropion jest o połowę silniejszy niż bupropion, podczas gdy treohydrobupropion i erytrohydrobupropion są 5-krotnie słabsze niż bupropion. Może to mieć znaczenie kliniczne, ponieważ stężenia metabolitów w osoczu są tak samo wysokie lub wyższe niż bupropionu.
Po podaniu pojedynczej dawki u ludzi maksymalne stężenie hydroksybupropionu w osoczu występuje po około 3 godzinach od podania produktu WELLBUTRIN i jest około 10 razy większe od maksymalnego stężenia leku macierzystego w stanie stacjonarnym. Okres półtrwania hydroksybupropionu w fazie eliminacji wynosi około 20 (±5) godzin, a jego AUC w stanie stacjonarnym jest około 17 razy większe niż bupropionu. Czasy do osiągnięcia maksymalnych stężeń metabolitów erytrohydrobupropionu i treohydrobupropionu są podobne do czasów metabolitu hydroksybupropionu. Jednak ich okresy półtrwania w fazie eliminacji są dłuższe, odpowiednio 33 (±10) i 37 (±13) godzin, a AUC w stanie stacjonarnym są odpowiednio 1,5 i 7 razy większe niż w przypadku bupropionu.
Bupropion i jego metabolity wykazują kinetykę liniową po długotrwałym podawaniu 300 do 450 mg/dobę.
Eliminacja
Po podaniu doustnym 200 mg 14C-bupropionu ludziom, 87% i 10% radioaktywnej dawki wykryto odpowiednio w moczu i kale. Tylko 0,5% dawki doustnej było wydalane w postaci niezmienionego bupropionu.
Określone populacje
Można oczekiwać, że czynniki lub stany zmieniające zdolność metaboliczną (np. choroba wątroby, zastoinowa niewydolność serca [CHF], wiek, przyjmowane jednocześnie leki itp.) lub wydalanie mogą wpływać na stopień i zakres akumulacji aktywnych metabolitów bupropionu. Eliminacja głównych metabolitów bupropionu może zależeć od upośledzenia czynności nerek lub wątroby, ponieważ są to związki umiarkowanie polarne i prawdopodobnie ulegną dalszemu metabolizmowi lub sprzężeniu w wątrobie przed wydaleniem z moczem.
Pacjenci z niewydolnością nerek
Dane dotyczące farmakokinetyki bupropionu u pacjentów z zaburzeniami czynności nerek są ograniczone. Porównanie między próbami zdrowych osób i osób ze schyłkową niewydolnością nerek wykazało, że wartości Cmax i AUC leku macierzystego były porównywalne w obu grupach, podczas gdy metabolity hydroksybupropion i treohydrobupropion miały odpowiednio 2,3-krotny i 2,8-krotny wzrost. w AUC dla osób ze schyłkową niewydolnością nerek. Drugie badanie porównujące osoby zdrowe i osoby z umiarkowanymi do ciężkich zaburzeniami czynności nerek (GFR 30,9 ± 10,8 ml/min) wykazało, że po podaniu pojedynczej dawki 150 mg bupropionu o przedłużonym uwalnianiu ekspozycja na bupropion była około 2-krotnie większa u pacjentów z zaburzeniami czynności nerek, natomiast stężenia hydroksybupropionu i metabolitów treo/erytrohydrobupropionu (połączonych) były podobne w obu grupach. Bupropion jest intensywnie metabolizowany w wątrobie do aktywnych metabolitów, które są dalej metabolizowane, a następnie wydalane przez nerki. Eliminacja głównych metabolitów bupropionu może być zmniejszona przez zaburzenia czynności nerek. WELLBUTRIN należy stosować ostrożnie u pacjentów z zaburzeniami czynności nerek i rozważyć zmniejszenie częstości i (lub) dawki [patrz Używaj w określonych populacjach ].
Pacjenci z niewydolnością wątroby
Wpływ zaburzeń czynności wątroby na farmakokinetykę bupropionu scharakteryzowano w 2 badaniach z pojedynczą dawką, jednym z udziałem pacjentów z alkoholową chorobą wątroby i jednym z udziałem pacjentów z lekką do ciężkiej marskością wątroby. Pierwsze badanie wykazało, że okres półtrwania hydroksybupropionu był znacznie dłuższy u 8 pacjentów z alkoholową chorobą wątroby niż u 8 zdrowych ochotników (odpowiednio 32 ± 14 godzin w porównaniu z 21 ± 5 godzin). Chociaż nie jest to statystycznie istotne, wartości AUC dla bupropionu i hydroksybupropionu były bardziej zmienne i zwykle większe (o 53% do 57%) u ochotników z alkoholową chorobą wątroby. Różnice w okresie półtrwania bupropionu i innych metabolitów w 2 grupach były minimalne.
Drugie badanie nie wykazało statystycznie istotnych różnic w farmakokinetyce bupropionu i jego aktywnych metabolitów u 9 pacjentów z łagodną do umiarkowanej marskością wątroby w porównaniu z 8 zdrowymi ochotnikami. Jednak u pacjentów z lekką lub umiarkowaną marskością wątroby zaobserwowano większą zmienność niektórych parametrów farmakokinetycznych bupropionu (AUC, Cmax i Tmax) oraz jego aktywnych metabolitów (t½). U osób z ciężką marskością wątroby zaobserwowano istotne zmiany w farmakokinetyce bupropionu i jego metabolitów (Tabela 3).
Pacjenci z dysfunkcją lewej komory
Podczas długotrwałego badania dawkowania bupropionu u 14 pacjentów z depresją z dysfunkcją lewej komory (wywiad CHF lub powiększenie serca w badaniu rentgenowskim) nie stwierdzono widocznego wpływu na farmakokinetykę bupropionu lub jego metabolitów w porównaniu ze zdrowymi ochotnikami.
Wiek
Wpływ wieku na farmakokinetykę bupropionu i jego metabolitów nie został w pełni scharakteryzowany, ale badanie stężeń bupropionu w stanie stacjonarnym z kilku badań skuteczności w leczeniu depresji z udziałem osób otrzymujących dawki w zakresie od 300 do 750 mg/dobę, w raz dziennie, nie wykazał związku między wiekiem (18 do 83 lat) a stężeniem bupropionu w osoczu. Badanie farmakokinetyczne pojedynczej dawki wykazało, że dystrybucja bupropionu i jego metabolitów u osób w podeszłym wieku była podobna do dystrybucji u osób młodszych. Dane te sugerują, że wiek nie ma znaczącego wpływu na stężenie bupropionu; jednak inne badanie farmakokinetyczne z pojedynczą i wielokrotną dawką sugerowało, że osoby w podeszłym wieku są bardziej narażone na akumulację bupropionu i jego metabolitów [patrz Używaj w określonych populacjach ].
Pacjenci płci męskiej i żeńskiej
Zbiorcza analiza danych farmakokinetycznych bupropionu pochodzących od 90 zdrowych mężczyzn i 90 zdrowych ochotniczek nie wykazała związanych z płcią różnic w maksymalnych stężeniach bupropionu w osoczu. Średnia ekspozycja ogólnoustrojowa (AUC) była o około 13% większa u ochotników płci męskiej w porównaniu z ochotnikami płci żeńskiej. Kliniczne znaczenie tego odkrycia nie jest znane.
Palacze
Wpływ palenia papierosów na farmakokinetykę bupropionu zbadano u 34 zdrowych ochotników płci męskiej i żeńskiej; 17 było nałogowymi palaczami papierosów, a 17 było niepalącymi. Po podaniu doustnym pojedynczej dawki 150 mg bupropionu nie było statystycznie istotnych różnic w Cmax, okresie półtrwania, Tmax, AUC lub klirensie bupropionu lub jego aktywnych metabolitów między palaczami a osobami niepalącymi.
Badania interakcji leków
Potencjał innych leków wpływających na WELLBUTRIN
Badania in vitro wskazują, że bupropion jest metabolizowany głównie do hydroksybupropionu przez CYP2B6. W związku z tym istnieje możliwość interakcji między lekiem WELLBUTRIN a lekami będącymi inhibitorami lub induktorami CYP2B6. Ponadto badania in vitro sugerują, że paroksetyna, sertralina, norfluoksetyna, fluwoksamina i nelfinawir hamują hydroksylację bupropionu.
Inhibitory CYP2B6
Tiklopidyna, klopidogrel: W badaniu z udziałem zdrowych ochotników płci męskiej klopidogrel 75 mg raz na dobę lub 250 mg tiklopidyny dwa razy na dobę zwiększały ekspozycję (Cmax i AUC) na bupropion o 40% i 60% dla klopidogrelu oraz o 38% i 85% dla tyklopidyny , odpowiednio. Ekspozycja (Cmax i AUC) na hydroksybupropion zmniejszyła się odpowiednio o 50% i 52% przez klopidogrel oraz odpowiednio o 78% i 84% przez tiklopidynę. Uważa się, że efekt ten jest spowodowany hamowaniem hydroksylacji bupropionu katalizowanej przez CYP2B6.
Prasugrel: Prasugrel jest słabym inhibitorem CYP2B6. U zdrowych osób prasugrel zwiększał wartości Cmax i AUC bupropionu odpowiednio o 14% i 18% oraz zmniejszał wartości Cmax i AUC hydroksybupropionu, aktywnego metabolitu bupropionu, odpowiednio o 32% i 24%.
Cymetydyna: metabolit bupropionu, treohydrobupropion, nie wydaje się być wytwarzany przez enzymy cytochromu P450. Wpływ równoczesnego podawania cymetydyny na farmakokinetykę bupropionu i jego aktywnych metabolitów badano u 24 zdrowych młodych ochotników płci męskiej. Po podaniu doustnym bupropionu 300 mg z cymetydyną 800 mg lub bez, farmakokinetyka bupropionu i hydroksybupropionu nie uległa zmianie. Jednak stwierdzono odpowiednio 16% i 32% wzrost AUC i Cmax połączonych grup treohydrobupropionu i erytrohydrobupropionu.
Citalopram: Citalopram nie wpływał na farmakokinetykę bupropionu i jego trzech metabolitów.
Induktory CYP2B6
Rytonawir i Lopinawir: W badaniu przeprowadzonym na zdrowych ochotnikach rytonawir w dawce 100 mg dwa razy na dobę zmniejszał AUC i Cmax bupropionu odpowiednio o 22% i 21%. Ekspozycja na metabolit hydroksybupropion zmniejszyła się o 23%, treohydrobupropion o 38%, a erytrohydrobupropion o 48%.
W drugim badaniu z udziałem zdrowych ochotników rytonawir w dawce 600 mg dwa razy na dobę zmniejszał AUC i Cmax bupropionu odpowiednio o 66% i 62%. Ekspozycja na metabolit hydroksybupropion zmniejszyła się o 78%, treohydrobupropion o 50%, a erytrohydrobupropion o 68%.
W innym badaniu z udziałem zdrowych ochotników lopinawir 400 mg/rytonawir 100 mg dwa razy na dobę zmniejszał AUC i Cmax bupropionu o 57%. AUC i Cmax hydroksybupropionu zmniejszyły się odpowiednio o 50% i 31%.
Efawirenz: W badaniu na zdrowych ochotnikach efawirenz w dawce 600 mg raz na dobę przez 2 tygodnie zmniejszał AUC i Cmax bupropionu odpowiednio o około 55% i 34%. AUC hydroksybupropionu pozostało niezmienione, natomiast Cmax hydroksybupropionu było zwiększone o 50%.
Karbamazepina, fenobarbital, fenytoina: chociaż nie są one systematycznie badane, leki te mogą indukować metabolizm bupropionu.
Potencjał WELLBUTRIN do wpływania na inne leki
Dane na zwierzętach wskazują, że bupropion może być induktorem enzymów metabolizujących leki u ludzi. W jednym badaniu, po długotrwałym podawaniu bupropionu 100 mg trzy razy dziennie 8 zdrowym ochotnikom płci męskiej przez 14 dni, nie stwierdzono dowodów na indukcję własnego metabolizmu bupropionu. Niemniej jednak, mogą wystąpić klinicznie istotne zmiany stężeń jednocześnie podawanych leków we krwi.
Leki metabolizowane przez CYP2D6
In vitro bupropion i jego metabolity (erytrohydrobupropion, treohydrobupropion, hydroksybupropion) są inhibitorami CYP2D6. W badaniu klinicznym z udziałem 15 mężczyzn (w wieku od 19 do 35 lat), którzy intensywnie metabolizowali CYP2D6, bupropion w dawce 300 mg/dobę, a następnie pojedyncza dawka 50 mg dezypraminy zwiększał Cmax, AUC i t½ dezypraminy średnio o w przybliżeniu odpowiednio 2-, 5- i 2-krotnie. Efekt utrzymywał się przez co najmniej 7 dni po ostatniej dawce bupropionu. Jednoczesne stosowanie bupropionu z innymi lekami metabolizowanymi przez CYP2D6 nie było formalnie badane.
Citalopram: Chociaż cytalopram nie jest metabolizowany głównie przez CYP2D6, w jednym badaniu bupropion zwiększał Cmax i AUC cytalopramu odpowiednio o 30% i 40%.
Lamotrygina: Wielokrotne doustne dawki bupropionu nie miały statystycznie istotnego wpływu na farmakokinetykę pojedynczej dawki lamotryginy u 12 zdrowych ochotników.
Digoksyna: Dane z piśmiennictwa wykazały, że ekspozycja na digoksynę była zmniejszona, gdy pojedynczą doustną dawkę 0,5 mg digoksyny podano zdrowym ochotnikom 24 godziny po doustnym podaniu pojedynczej dawki 150 mg bupropionu o przedłużonym uwalnianiu.
Studia kliniczne
Skuteczność preparatu WELLBUTRIN 150 mg w leczeniu dużych zaburzeń depresyjnych potwierdzono w dwóch 4-tygodniowych badaniach kontrolowanych placebo u dorosłych pacjentów hospitalizowanych z powodu MDD (Badania 1 i 2 w Tabeli 4) oraz w jednym 6-tygodniowym badaniu kontrolowanym placebo u pacjentów z MDD. dorosłych pacjentów ambulatoryjnych z MDD (badanie 3 w tabeli 4). W pierwszym badaniu zakres dawek preparatu WELLBUTRIN 300 mg wynosił od 300 mg do 600 mg/dobę podawanych w 3 dawkach podzielonych; 78% badanych otrzymywało dawki od 300 mg do 450 mg/dobę. Badanie wykazało skuteczność preparatu WELLBUTRIN 300 mg, mierzoną za pomocą całkowitego wyniku w Skali Oceny Depresji Hamiltona (HDRS), elementu nastroju depresyjnego HDRS (punkt 1) oraz wskaźnika klinicznego nasilenia globalnych wrażeń (CGI-S). Drugie badanie obejmowało 2 dawki preparatu WELLBUTRIN (300 i 450 mg/dobę) oraz placebo. To badanie wykazało skuteczność WELLBUTRIN 150 mg tylko przy dawce 450 mg/dzień. Wyniki skuteczności były statystycznie istotne dla całkowitej punktacji HDRS i punktacji CGI-S, ale nie dla punktacji 1 HDRS. W trzecim badaniu pacjenci ambulatoryjni otrzymywali 300 mg/dobę preparatu WELLBUTRIN. Badanie to wykazało skuteczność WELLBUTRIN 150 mg mierzoną za pomocą całkowitego wyniku HDRS, HDRS Punkt 1, Skali Oceny Depresji Montgomery-Asberg (MADRS), wyniku CGI-S i Skali Poprawy CGI (CGI-I) . Skuteczność preparatu WELLBUTRIN 300mg przy długotrwałym stosowaniu, czyli przez ponad 6 tygodni, nie była systematycznie oceniana w kontrolowanych badaniach.
INFORMACJA O PACJENCIE
WELLBUTRIN (Dobrze byu-trin) (chlorowodorek bupropionu) Tabletki
WAŻNE: Koniecznie przeczytaj trzy sekcje niniejszego Przewodnika po lekach. Pierwsza część dotyczy ryzyka myśli i działań samobójczych związanych z lekami przeciwdepresyjnymi; druga część dotyczy ryzyka zmian w myśleniu i zachowaniu, depresji i myśli samobójczych lub działań związanych z rzucaniem palenia; a trzecia część jest zatytułowana „Jakie inne ważne informacje powinienem wiedzieć o WELLBUTRIN 150mg?”
Leki przeciwdepresyjne, depresja i inne poważne choroby psychiczne oraz myśli lub działania samobójcze
Ta część Przewodnika po lekach dotyczy wyłącznie ryzyka myśli i działań samobójczych związanych z lekami przeciwdepresyjnymi.
Jakie są najważniejsze informacje, które powinienem wiedzieć o lekach przeciwdepresyjnych, depresji i innych poważnych chorobach psychicznych oraz myślach i działaniach samobójczych?
1. Leki przeciwdepresyjne mogą zwiększać ryzyko myśli lub działań samobójczych u niektórych dzieci, nastolatków lub młodych dorosłych w ciągu pierwszych kilku miesięcy leczenia.
2. Depresja lub inne poważne choroby psychiczne są najważniejszymi przyczynami myśli i działań samobójczych. Niektóre osoby mogą być szczególnie narażone na myśli lub działania samobójcze. Należą do nich osoby, które mają (lub mają w rodzinie) chorobę afektywną dwubiegunową (zwaną również chorobą maniakalno-depresyjną) lub myśli lub działania samobójcze.
3. Jak mogę obserwować i starać się zapobiegać myślom i działaniom samobójczym u siebie lub członka rodziny?
- Zwróć szczególną uwagę na wszelkie zmiany, zwłaszcza nagłe zmiany nastroju, zachowań, myśli lub uczuć. Jest to bardzo ważne w przypadku rozpoczęcia przyjmowania leku przeciwdepresyjnego lub zmiany dawki.
- Zadzwoń natychmiast do swojego lekarza, aby zgłosić nowe lub nagłe zmiany nastroju, zachowania, myśli lub uczuć.
- Utrzymuj wszystkie wizyty kontrolne u swojego lekarza zgodnie z planem. Zadzwoń do lekarza między wizytami w razie potrzeby, zwłaszcza jeśli masz obawy dotyczące objawów.
Zadzwoń natychmiast do swojego lekarza, jeśli Ty lub członek Twojej rodziny macie którykolwiek z poniższych objawów, zwłaszcza jeśli są nowe, gorsze lub martwią Cię:
- myśli o samobójstwie lub śmierci
- próby popełnienia samobójstwa
- nowa lub gorsza depresja
- nowy lub gorszy niepokój
- czuję się bardzo poruszony lub niespokojny
- atak paniki
- kłopoty ze snem (bezsenność)
- nowa lub gorsza drażliwość
- zachowywanie się agresywnie, złość lub przemoc
- działając na niebezpieczne impulsy
- ekstremalny wzrost aktywności i mówienia (mania)
- inne nietypowe zmiany w zachowaniu lub nastroju
Co jeszcze muszę wiedzieć o lekach przeciwdepresyjnych?
- Nigdy nie odstawiaj leku przeciwdepresyjnego bez uprzedniej rozmowy z lekarzem. Nagłe zatrzymanie leku przeciwdepresyjnego może spowodować inne objawy.
- Antydepresanty to leki stosowane w leczeniu depresji i innych chorób. Ważne jest omówienie wszystkich zagrożeń związanych z leczeniem depresji, a także zagrożeń związanych z jej nieleczeniem. Pacjenci i ich rodziny lub inni opiekunowie powinni omówić z lekarzem wszystkie opcje leczenia, a nie tylko stosowanie leków przeciwdepresyjnych.
- Leki przeciwdepresyjne mają inne skutki uboczne. Porozmawiaj z lekarzem o skutkach ubocznych leku przepisanego Tobie lub członkowi Twojej rodziny.
- Leki przeciwdepresyjne mogą wchodzić w interakcje z innymi lekami. Poznaj wszystkie leki, które przyjmujesz Ty lub członek Twojej rodziny. Zachowaj listę wszystkich leków, aby pokazać je lekarzowi. Nie rozpoczynaj nowych leków bez uprzedniej konsultacji z lekarzem.
Nie wiadomo, czy WELLBUTRIN jest bezpieczny i skuteczny u dzieci poniżej 18 roku życia.
Rzucenie palenia, leki na rzucenie palenia, zmiany w myśleniu i zachowaniu, depresja oraz myśli lub działania samobójcze
Ta część Przewodnika po lekach dotyczy wyłącznie ryzyka zmian w myśleniu i zachowaniu, depresji i myśli samobójczych lub działań związanych z lekami stosowanymi w celu rzucenia palenia. Chociaż WELLBUTRIN nie jest lekiem na rzucenie palenia, zawiera tę samą substancję czynną (chlorowodorek bupropionu) co ZYBAN, który pomaga pacjentom rzucić palenie.
Porozmawiaj ze swoim lekarzem lub lekarzem członka Twojej rodziny o:
- wszystkie zagrożenia i korzyści związane z lekami rzucającymi palenie.
- wszystkie opcje leczenia w celu rzucenia palenia.
Kiedy próbujesz rzucić palenie, z bupropionem lub bez, możesz mieć objawy, które mogą być spowodowane odstawieniem nikotyny, w tym:
- Zachęcam do palenia
- udaremnienie
- niepokój
- depresyjny nastrój
- gniew
- zmniejszone tętno
- problemy ze snem
- czuję się niespokojny
- zwiększony apetyt
- drażliwość
- Trudności z koncentracją
- przybranie na wadze
Niektórzy ludzie doświadczają nawet myśli samobójczych, gdy próbują rzucić palenie bez leków.
Czasami rzucenie palenia może prowadzić do pogorszenia problemów ze zdrowiem psychicznym, które już masz, takich jak depresja.
Niektóre osoby miały poważne skutki uboczne podczas przyjmowania bupropionu, aby pomóc im rzucić palenie, w tym: Nowe lub gorsze problemy ze zdrowiem psychicznym, takie jak zmiany w zachowaniu lub myśleniu, agresja, wrogość, pobudzenie, depresja lub myśli lub działania samobójcze. Niektóre osoby miały te objawy, gdy rozpoczęły przyjmowanie bupropionu, a inne rozwinęły je po kilku tygodniach leczenia lub po odstawieniu bupropionu. Objawy te występowały częściej u osób, które miały problemy ze zdrowiem psychicznym przed przyjęciem bupropionu niż u osób bez historii problemów ze zdrowiem psychicznym.
Przestań zażywać WELLBUTRIN i natychmiast skontaktuj się z lekarzem, jeśli Ty, Twoja rodzina lub opiekun zauważycie którykolwiek z tych objawów. Skontaktuj się z lekarzem, aby zdecydować, czy powinieneś kontynuować przyjmowanie leku WELLBUTRIN. U wielu osób objawy te ustąpiły po odstawieniu preparatu WELLBUTRIN 300 mg, ale u niektórych objawy utrzymywały się po odstawieniu preparatu WELLBUTRIN. Ważne jest, aby skontaktować się z lekarzem, aż objawy ustąpią. Przed przyjęciem leku WELLBUTRIN 150 mg należy poinformować lekarza, jeśli kiedykolwiek miałeś depresję lub inne problemy ze zdrowiem psychicznym. Powinieneś również poinformować swojego lekarza o wszelkich objawach, które wystąpiły podczas innych prób rzucenia palenia, z bupropionem lub bez.
Jakie inne ważne informacje powinienem wiedzieć o WELLBUTRIN?
- Drgawki: Istnieje ryzyko wystąpienia drgawek (drgawki, napad) przy stosowaniu WELLBUTRIN 150 mg, szczególnie u osób:
- z pewnymi problemami medycznymi.
- którzy przyjmują niektóre leki. Szansa na drgawki wzrasta wraz z wyższymi dawkami WELLBUTRIN. Więcej informacji można znaleźć w rozdziałach „Kto nie powinien przyjmować leku WELLBUTRIN?” oraz „O czym powinienem powiedzieć lekarzowi przed przyjęciem leku WELLBUTRIN 300 mg?” Poinformuj swojego lekarza o wszystkich swoich schorzeniach i wszystkich przyjmowanych lekach. Nie należy przyjmować żadnych innych leków podczas przyjmowania leku WELLBUTRIN 150 mg, chyba że lekarz stwierdzi, że można je przyjmować. W przypadku wystąpienia drgawek podczas przyjmowania leku WELLBUTRIN należy zaprzestać przyjmowania tabletek i natychmiast skontaktować się z lekarzem. Nie należy ponownie przyjmować leku WELLBUTRIN 150 mg, jeśli wystąpi napad drgawkowy.
- Wysokie ciśnienie krwi (nadciśnienie). U niektórych osób podczas przyjmowania leku WELLBUTRIN dochodzi do wysokiego ciśnienia krwi, które może być ciężkie. Szansa na nadciśnienie może być większa, jeśli stosujesz również nikotynową terapię zastępczą (taką jak plaster nikotynowy), aby pomóc ci rzucić palenie (patrz rozdział tego Przewodnika po lekach zatytułowany „Jak powinienem przyjmować WELLBUTRIN 150 mg?”).
- Epizody maniakalne. Niektóre osoby mogą mieć okresy manii podczas przyjmowania leku WELLBUTRIN 300 mg, w tym:
- Znacznie zwiększona energia
- Poważne problemy ze snem
- Wyścigi myśli
- Lekkomyślne zachowanie
- Niezwykle wielkie pomysły
- Nadmierne szczęście lub drażliwość
- Mówienie więcej lub szybciej niż zwykle Jeśli masz którykolwiek z powyższych objawów manii, zadzwoń do swojego lekarza.
- Niezwykłe myśli lub zachowania. Niektórzy pacjenci mają nietypowe myśli lub zachowania podczas przyjmowania leku WELLBUTRIN, w tym urojenia (wierzenie, że jesteś kimś innym), halucynacje (widzenie lub słyszenie rzeczy, których nie ma), paranoję (poczucie, że ludzie są przeciwko tobie) lub poczucie dezorientacji. Jeśli tak się stanie, zadzwoń do swojego lekarza.
- Problemy wizualne.
- ból oka
- zmiany w wizji
- obrzęk lub zaczerwienienie oka lub wokół oka Tylko niektóre osoby są narażone na te problemy. Możesz chcieć przejść badanie wzroku, aby sprawdzić, czy jesteś zagrożony i otrzymać leczenie zapobiegawcze, jeśli tak.
- Ciężkie reakcje alergiczne. Niektórzy ludzie mogą mieć ciężkie reakcje alergiczne na WELLBUTRIN. Przestań zażywać WELLBUTRIN 300mg i natychmiast skontaktuj się z lekarzem jeśli u pacjenta wystąpi wysypka, swędzenie, pokrzywka, gorączka, obrzęk węzłów chłonnych, bolesne owrzodzenia w jamie ustnej lub wokół oczu, obrzęk warg lub języka, ból w klatce piersiowej lub trudności w oddychaniu. Mogą to być objawy poważnej reakcji alergicznej.
Co to jest WELLBUTRIN?
WELLBUTRIN to lek na receptę stosowany w leczeniu osób dorosłych z pewnym rodzajem depresji, zwanym zaburzeniem depresyjnym.
Kto nie powinien brać WELLBUTRIN 150mg?
Nie należy przyjmować leku WELLBUTRIN, jeśli:
- masz lub miałeś napady padaczkowe lub epilepsję.
- masz lub miałeś zaburzenia odżywiania, takie jak jadłowstręt psychiczny lub bulimia.
- pacjent przyjmuje jakiekolwiek inne leki zawierające bupropion, w tym ZYBAN (stosowany w rzuceniu palenia), WELLBUTRIN 300 mg SR, WELLBUTRIN 150 mg XL, APLENZIN lub FORFIVO XL. Bupropion to ten sam składnik aktywny, który znajduje się w WELLBUTRIN.
- pić dużo alkoholu i nagle przestać pić lub stosować leki zwane uspokajającymi (które powodują senność), benzodiazepiny lub leki przeciwpadaczkowe i nagle przestajesz ich używać.
- weź inhibitor monoaminooksydazy (MAOI). Zapytaj swojego lekarza lub farmaceutę, jeśli nie jesteś pewien, czy przyjmujesz IMAO, w tym antybiotyk linezolid.
- nie należy przyjmować MAOI w ciągu 2 tygodni od odstawienia leku WELLBUTRIN, chyba że zaleci to lekarz.
- nie należy rozpoczynać przyjmowania leku WELLBUTRIN 150 mg, jeśli zaprzestano przyjmowania MAOI w ciągu ostatnich 2 tygodni, chyba że zalecił to lekarz.
- jesteś uczulony na substancję czynną preparatu WELLBUTRIN 300mg, bupropion lub którykolwiek z nieaktywnych składników. Pełna lista składników WELLBUTRIN znajduje się na końcu niniejszego Przewodnika po lekach.
O czym powinienem powiedzieć lekarzowi przed przyjęciem leku WELLBUTRIN?
Poinformuj swojego lekarza, jeśli kiedykolwiek miałeś depresję, myśli lub działania samobójcze lub inne problemy ze zdrowiem psychicznym. Zobacz „Leki przeciwdepresyjne, depresja i inne poważne choroby psychiczne oraz myśli i działania samobójcze”.
- Poinformuj swojego dostawcę opieki zdrowotnej o innych schorzeniach, w tym jeśli:
- mają problemy z wątrobą, zwłaszcza marskość wątroby.
- mają problemy z nerkami.
- masz lub miałeś zaburzenia odżywiania, takie jak jadłowstręt psychiczny lub bulimia.
- miał uraz głowy.
- miał napad drgawkowy (drgawki, napad).
- masz guza w układzie nerwowym (mózgu lub kręgosłupie).
- miał zawał serca, problemy z sercem lub wysokie ciśnienie krwi.
- jesteś cukrzykiem przyjmującym insulinę lub inne leki w celu kontrolowania poziomu cukru we krwi.
- pić alkohol.
- nadużywać leków na receptę lub narkotyków.
- są w ciąży lub planują zajść w ciążę. Porozmawiaj z lekarzem o ryzyku dla nienarodzonego dziecka, jeśli zażywasz WELLBUTRIN 300 mg w czasie ciąży.
- Należy poinformować lekarza o zajściu w ciążę lub podejrzeniu ciąży podczas leczenia lekiem WELLBUTRIN.
- Jeśli zajdziesz w ciążę podczas leczenia lekiem WELLBUTRIN, porozmawiaj ze swoim lekarzem o rejestracji w Krajowym Rejestrze Ciąży dla Antydepresantów. Możesz zarejestrować się dzwoniąc pod numer 1-844-405-6185.
- karmisz piersią lub planujesz karmić piersią podczas leczenia lekiem WELLBUTRIN. WELLBUTRIN przenika do mleka. Porozmawiaj z lekarzem o najlepszym sposobie karmienia dziecka podczas leczenia preparatem WELLBUTRIN.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę, leki dostępne bez recepty, witaminy i suplementy ziołowe. Wiele leków zwiększa ryzyko wystąpienia drgawek lub innych poważnych działań niepożądanych, jeśli są przyjmowane podczas przyjmowania leku WELLBUTRIN.
Jak powinienem przyjmować WELLBUTRIN 300mg?
- Weź WELLBUTRIN 300mg dokładnie zgodnie z zaleceniami lekarza. Nie należy zmieniać dawki ani przerywać przyjmowania leku WELLBUTRIN bez uprzedniej konsultacji z lekarzem.
- Tabletki WELLBUTRIN należy połknąć w całości. Nie żuć, nie ciąć ani nie kruszyć tabletek WELLBUTRIN 300mg.
- Przyjmuj WELLBUTRIN 300mg o tej samej porze każdego dnia.
- Dawki leku WELLBUTRIN 300 mg należy przyjmować w odstępach co najmniej 6 godzin.
- Lek WELLBUTRIN można przyjmować z posiłkiem lub bez posiłku.
- przypadku pominięcia dawki nie należy przyjmować dodatkowej dawki w celu uzupełnienia pominiętej dawki. Poczekaj i weź kolejną dawkę o zwykłej porze. To jest bardzo ważne. Zbyt dużo WELLBUTRIN może zwiększyć prawdopodobieństwo wystąpienia napadu.
- Jeśli zażyjesz zbyt dużo leku WELLBUTRIN lub przedawkujesz, natychmiast skontaktuj się z pogotowiem lub centrum kontroli zatruć.
- Nie należy przyjmować żadnych innych leków podczas przyjmowania leku WELLBUTRIN 300 mg, chyba że lekarz powiedział, że jest to w porządku.
- Jeśli pacjent przyjmuje lek WELLBUTRIN 150 mg w leczeniu dużych zaburzeń depresyjnych, może upłynąć kilka tygodni, zanim poczuje się, że lek WELLBUTRIN 150 mg działa. Gdy poczujesz się lepiej, ważne jest, aby kontynuować przyjmowanie leku WELLBUTRIN zgodnie z zaleceniami lekarza. Zadzwoń do swojego lekarza, jeśli nie czujesz, że WELLBUTRIN pracuje dla Ciebie.
Czego powinienem unikać biorąc WELLBUTRIN 300mg?
- Ogranicz lub unikaj spożywania alkoholu podczas leczenia preparatem WELLBUTRIN. Jeśli zwykle pijesz dużo alkoholu, porozmawiaj ze swoim lekarzem, zanim nagle przestaniesz. Jeśli nagle przestaniesz pić alkohol, możesz zwiększyć ryzyko wystąpienia drgawek.
- Nie prowadź samochodu ani nie używaj ciężkich maszyn, dopóki nie dowiesz się, jak wpływa na Ciebie WELLBUTRIN 150mg. WELLBUTRIN może wpłynąć na twoją zdolność do bezpiecznego wykonywania tych czynności.
Jakie są możliwe skutki uboczne WELLBUTRIN 300mg?
WELLBUTRIN może powodować poważne skutki uboczne. Informacje o poważnych skutkach ubocznych leku WELLBUTRIN znajdują się w rozdziałach na początku niniejszego Przewodnika po lekach.
Najczęstsze skutki uboczne WELLBUTRIN to:
- nerwowość
- silne pocenie się
- suchość w ustach
- drżenie (drżenie)
- zaparcie
- problemy ze snem
- ból głowy
- rozmazany obraz
- nudności lub wymioty
- szybkie bicie serca
- zawroty głowy
Jeśli masz nudności, zażywaj lek z jedzeniem. Jeśli masz problemy ze snem, nie zażywaj leku zbyt blisko pory snu.
Natychmiast poinformuj swojego lekarza o wszelkich skutkach ubocznych, które Cię niepokoją.
To nie wszystkie możliwe skutki uboczne WELLBUTRIN. Aby uzyskać więcej informacji, zapytaj swojego lekarza lub farmaceutę.
Zadzwoń do swojego lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Możesz również zgłosić skutki uboczne do GlaxoSmithKline pod numerem 1-888-825-5249.
Jak przechowywać WELLBUTRIN 300mg?
- Przechowywać WELLBUTRIN w temperaturze pokojowej między 68 ° F a 77 ° F (20 ° C do 25 ° C).
- Tabletki WELLBUTRIN należy przechowywać w suchym miejscu, z dala od światła.
Lek WELLBUTRIN i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu WELLBUTRIN.
Leki są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Nie należy stosować preparatu WELLBUTRIN 300 mg w przypadku schorzenia, na które nie został przepisany. Nie należy podawać leku WELLBUTRIN innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić.
Jeśli wykonasz test przesiewowy moczu na obecność narkotyków, WELLBUTRIN może sprawić, że wynik testu będzie pozytywny na obecność amfetaminy. Jeśli powiesz osobie wykonującej test przesiewowy na obecność narkotyków, że przyjmujesz WELLBUTRIN 300 mg, może ona wykonać bardziej szczegółowe badanie przesiewowe na obecność narkotyków, które nie powinno mieć tego problemu.
Niniejszy przewodnik po lekach podsumowuje ważne informacje dotyczące preparatu WELLBUTRIN. Jeśli chcesz uzyskać więcej informacji, porozmawiaj ze swoim lekarzem. Możesz poprosić swojego lekarza lub farmaceutę o informacje o WELLBUTRIN, które są przeznaczone dla pracowników służby zdrowia.
Aby uzyskać więcej informacji o WELLBUTRIN, zadzwoń pod numer 1-888-825-5249.
Jakie są składniki WELLBUTRIN 300mg?
Składnik aktywny: chlorowodorek bupropionu.
Składniki nieaktywne: tabletka 75 mg – D&C Yellow No. 10 Lake, FD&C Yellow No. 6 Lake, hydroksypropyloceluloza, hypromeloza, celuloza mikrokrystaliczna, glikol polietylenowy, talk i dwutlenek tytanu; Tabletka 100 mg – FD&C Red No. 40 Lake, FD&C Yellow No. 6 Lake, hydroksypropyloceluloza, hypromeloza, celuloza mikrokrystaliczna, glikol polietylenowy, talk i dwutlenek tytanu.
Ten przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków.
