Paxil 10mg, 20mg, 30mg, 40mg Paroxetine Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Paxil i jak się go stosuje?
Paxil 20mg to lek na receptę stosowany w leczeniu objawów depresji, zaburzeń obsesyjno-kompulsywnych (OCD), lęku napadowego, fobii społecznej, zespołu lęku uogólnionego, zespołu stresu pourazowego (PTSD) i przedmiesiączkowych zaburzeń dysohoricznych (PMDD). Paxil może być stosowany samodzielnie lub z innymi lekami.
- Paxil 40mg należy do klasy leków zwanych antydepresantami, SSRI.
- Nie wiadomo, czy Paxil jest bezpieczny i skuteczny u dzieci.
Jakie są możliwe skutki uboczne Paxil 30mg?
Paxil 10mg może powodować poważne skutki uboczne, w tym:
- goniące myśli,
- zmniejszone zapotrzebowanie na sen,
- nietypowe zachowanie ryzykowne,
- uczucia skrajnego szczęścia lub smutku,
- bycie bardziej rozmownym niż zwykle,
- rozmazany obraz,
- widzenie tunelowe,
- ból lub obrzęk oka,
- widząc aureole wokół świateł,
- nietypowy ból lub tkliwość kości, obrzęk lub zasinienie,
- zmiany wagi,
- zmiany apetytu,
- łatwe siniaki,
- nietypowe krwawienie z nosa, ust, pochwy lub odbytnicy,
- kaszel krwią,
- bardzo sztywne lub sztywne mięśnie,
- wysoka gorączka,
- wyzysk,
- dezorientacja,
- szybkie lub nierówne bicie serca,
- drżenia,
- półomdlały,
- ból głowy,
- dezorientacja,
- bełkotliwa wymowa,
- silne osłabienie,
- utrata koordynacji oraz
- czuć się niepewnie
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Paxil 30mg to:
- zmiany widzenia,
- słabość,
- senność,
- zawroty głowy,
- zmęczenie,
- wyzysk,
- lęk,
- drżący,
- problemy ze snem (bezsenność),
- utrata apetytu,
- mdłości,
- wymioty,
- biegunka,
- zaparcie,
- suchość w ustach,
- infekcja,
- ból głowy,
- zmniejszony popęd płciowy,
- impotencja,
- nieprawidłowy wytrysk i
- trudności z orgazmem
Samobójstwa i leki przeciwdepresyjne
Leki przeciwdepresyjne zwiększały w porównaniu z placebo ryzyko myśli i zachowań samobójczych (samobójstwa) u dzieci, młodzieży i młodych dorosłych w krótkoterminowych badaniach nad ciężkimi zaburzeniami depresyjnymi (MDD) i innymi zaburzeniami psychicznymi. Każdy, kto rozważa zastosowanie PAXIL 40 mg lub innego leku przeciwdepresyjnego u dzieci, młodzieży lub młodych dorosłych, musi zrównoważyć to ryzyko z potrzebą kliniczną. Badania krótkoterminowe nie wykazały wzrostu ryzyka samobójstw w przypadku stosowania leków przeciwdepresyjnych w porównaniu z placebo u osób dorosłych w wieku powyżej 24 lat; wystąpiło zmniejszenie ryzyka w przypadku stosowania leków przeciwdepresyjnych w porównaniu z placebo u osób dorosłych w wieku 65 lat i starszych. Depresja i niektóre inne zaburzenia psychiczne same w sobie wiążą się ze wzrostem ryzyka samobójstwa. Pacjenci w każdym wieku, którzy rozpoczynają leczenie lekami przeciwdepresyjnymi, powinni być odpowiednio monitorowani i ściśle obserwowani pod kątem pogorszenia stanu klinicznego, skłonności samobójczych lub nietypowych zmian w zachowaniu. Rodziny i opiekunowie powinni być poinformowani o potrzebie ścisłej obserwacji i komunikacji z lekarzem. PAXIL 30mg nie jest zatwierdzony do stosowania u dzieci. (Patrz OSTRZEŻENIA: Pogorszenie stanu klinicznego i ryzyko samobójstwa, INFORMACJE DLA PACJENTA i ŚRODKI OSTROŻNOŚCI: Stosowanie u dzieci).
OPIS
PAXIL (chlorowodorek paroksetyny) jest doustnym lekiem psychotropowym. Jest to chlorowodorek związku fenylopiperydyny zidentyfikowany chemicznie jako półwodzian chlorowodorku (-)-trans-4R-(4'fluorofenylo)-3S-[(3',4'-metylenodioksyfenoksy)metylo]piperydyny oraz ma wzór empiryczny C19H20FNO3•HCl•½H2O. Masa cząsteczkowa wynosi 374,8 (329,4 w postaci wolnej zasady). Wzór strukturalny chlorowodorku paroksetyny to:
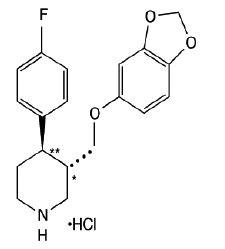
Chlorowodorek paroksetyny jest bezwonnym, białawym proszkiem o temperaturze topnienia w zakresie 120° do 138°C i rozpuszczalności 5,4 mg/ml w wodzie.
Każda tabletka powlekana zawiera chlorowodorek paroksetyny odpowiadający paroksetyny w następujący sposób: 10 mg-żółty (z rowkiem dzielącym); 20 mg-różowy (punktowany); 30 mg-niebieski, 40 mg-zielony. Składniki nieaktywne składają się z dwuwodnego fosforanu wapnia, hypromelozy, stearynianu magnezu, glikoli polietylenowych, polisorbatu 80, glikolanu sodowego skrobi, dwutlenku tytanu i co najmniej jednego z następujących składników: lak glinowy czerwony D&C nr 30, lak glinowy żółty D&C nr 10 , FD&C Blue nr 2 lak aluminiowy, FD&C Yellow nr 6 lak aluminiowy.
Zawieszenie w przypadku podania doustnego
Każde 5 ml pomarańczowego płynu o pomarańczowym smaku zawiera 10 mg chlorowodorku paroksetyny w ilości odpowiadającej paroksetyny. Składniki nieaktywne to polakrylina potasowa, celuloza mikrokrystaliczna, glikol propylenowy, gliceryna, sorbitol, metyloparaben, propyloparaben, dwuwodny cytrynian sodu, bezwodny kwas cytrynowy, sacharyna sodowa, aromaty, lak aluminiowy FD&C Yellow nr 6 i emulsja simetikonowa, USP.
WSKAZANIA
PAXIL 20mg jest wskazany u dorosłych w leczeniu:
- Duże zaburzenie depresyjne (MDD)
- Zaburzenie obsesyjno-kompulsywne (OCD)
- Lęk napadowy (PD)
- Fobia społeczna (SAD)
- Uogólnione zaburzenie lękowe (GAD)
- Zespół stresu pourazowego (PTSD)
DAWKOWANIE I SPOSÓB PODAWANIA
Informacje administracyjne
Podawać PAXIL jako pojedynczą dawkę dobową rano, z jedzeniem lub bez.
Przed podaniem dobrze wstrząsnąć zawiesiną doustną.
Zalecane dawkowanie w przypadku MDD, OCD, PD i PTSD
Zalecane dawki początkowe i maksymalne dawki PAXIL 20 mg u pacjentów z MDD, OCD, PD i PTSD przedstawiono w Tabeli 1.
U pacjentów z niewystarczającą odpowiedzią należy zwiększać dawkę o 10 mg na dobę w odstępach co najmniej 1 tygodnia, w zależności od tolerancji.
Zalecane dawkowanie w przypadku SAD i GAD
SMUTNY
Dawka początkowa i zalecana u pacjentów z SAD wynosi 20 mg na dobę. W badaniach klinicznych skuteczność PAXIL 30 mg wykazano u pacjentów w dawkach od 20 mg do 60 mg na dobę. Chociaż bezpieczeństwo PAXIL oceniano u pacjentów z SAD w dawkach do 60 mg na dobę, dostępne informacje nie sugerują żadnych dodatkowych korzyści przy dawkach powyżej 20 mg na dobę [patrz Studia kliniczne ].
GAD
Dawka początkowa i zalecana u pacjentów z GAD wynosi 20 mg na dobę. W badaniach klinicznych skuteczność PAXIL 10 mg w GAD wykazano u pacjentów w dawkach od 20 mg do 50 mg na dobę. Nie ma wystarczających dowodów, aby sugerować większą korzyść ze stosowania dawek większych niż 20 mg na dobę [patrz Studia kliniczne ].
U pacjentów z niewystarczającą odpowiedzią należy zwiększać dawkę o 10 mg na dobę w odstępach co najmniej 1 tygodnia, w zależności od tolerancji.
Badanie przesiewowe w kierunku choroby afektywnej dwubiegunowej przed rozpoczęciem stosowania PAXIL
Przed rozpoczęciem leczenia PAXIL 10 mg lub innym lekiem przeciwdepresyjnym należy przebadać pacjentów pod kątem osobistej lub rodzinnej historii choroby afektywnej dwubiegunowej, manii lub hipomanii [patrz OSTRZEŻENIA I ŚRODKI ].
Zalecane dawkowanie dla pacjentów w podeszłym wieku, pacjentów z ciężką niewydolnością nerek i pacjentów z ciężką niewydolnością wątroby
Zalecana dawka początkowa wynosi 10 mg na dobę dla pacjentów w podeszłym wieku, pacjentów z ciężkimi zaburzeniami czynności nerek oraz pacjentów z ciężkimi zaburzeniami czynności wątroby. Dawkowanie nie powinno przekraczać 40 mg/dobę.
Przełączanie pacjentów na lub z inhibitora monoaminooksydazy (MAOI)
Pomiędzy odstawieniem inhibitora monoaminooksydazy (MAOI a rozpoczęciem leczenia PAXIL) musi upłynąć co najmniej 14 dni. Ponadto po odstawieniu PAXIL musi upłynąć co najmniej 14 dni przed rozpoczęciem stosowania leku przeciwdepresyjnego z grupy MAOI [patrz PRZECIWWSKAZANIA , OSTRZEŻENIA I ŚRODKI ].
Przerwanie leczenia PAXIL
Działania niepożądane mogą wystąpić po odstawieniu PAXIL [patrz OSTRZEŻENIA I ŚRODKI ]. Stopniowo zmniejszaj dawkowanie, zamiast nagle odstawiać PAXIL, gdy tylko jest to możliwe.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Tabletki PAXIL są dostępne jako:
- 10 mg żółta tabletka z linią podziału z wytłoczonym napisem „PAXIL” i z tyłu „10”.
- 20 mg różowa tabletka z linią podziału z wytłoczonym napisem „PAXIL” i z tyłu „20”.
- Niebieska tabletka 30 mg z wytłoczonym napisem „PAXIL” z przodu iz tyłu „30”.
- Zielona tabletka 40 mg z wytłoczonym napisem „PAXIL” z przodu iz tyłu „40”.
PAXIL 20 mg zawiesina doustna jest dostępny jako:
- 10 mg/5 ml pomarańczowej zawiesiny o smaku pomarańczowym w butelkach zawierających 250 ml.
Składowania i stosowania
Tabletki PAXIL (paroksetyna) to owalne tabletki dostarczane jako:
Tabletki należy przechowywać w temperaturze od 15° do 30°C (59° i 86°F).
PAXIL (paroksetyna) zawiesina doustna jest dostarczany jako:
Przechowywać zawiesinę w temperaturze 25°C (77°F) lub niższej
Producent: Apotex Inc., Toronto, Ontario, Kanada M9L 1T9. Poprawiono: luty 2021
SKUTKI UBOCZNE
Następujące działania niepożądane są bardziej szczegółowo opisane w innych punktach informacji o przepisaniu leku:
- Reakcje nadwrażliwości na paroksetynę [patrz PRZECIWWSKAZANIA ]
- Myśli i zachowania samobójcze [zobacz OSTRZEŻENIA I ŚRODKI ]
- Zespół serotoninowy [patrz OSTRZEŻENIA I ŚRODKI ]
- Toksyczność dla płodu i noworodka [patrz OSTRZEŻENIA I ŚRODKI ]
- Zwiększone ryzyko krwawienia [patrz OSTRZEŻENIA I ŚRODKI ]
- Aktywacja manii/hipomanii [patrz OSTRZEŻENIA I ŚRODKI ]
- Syndrom odstawienia [patrz OSTRZEŻENIA I ŚRODKI ]
- Napady [patrz OSTRZEŻENIA I ŚRODKI ]
- Jaskra zamykającego się kąta [patrz OSTRZEŻENIA I ŚRODKI ]
- Hiponatremia [patrz OSTRZEŻENIA I ŚRODKI ]
- Złamanie kości [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Dane dotyczące bezpieczeństwa PAXIL pochodzą z:
- 6-tygodniowe badania kliniczne u pacjentów z MDD, którzy otrzymywali PAXIL od 20 mg do 50 mg raz na dobę
- 12-tygodniowe badania kliniczne u pacjentów z OCD, którzy otrzymywali PAXIL od 20 mg do 60 mg raz na dobę
- 10- do 12-tygodniowe badania kliniczne u pacjentów z ChP, którzy otrzymywali PAXIL w dawce 10 mg do 60 mg raz na dobę
- 12-tygodniowe badania kliniczne u pacjentów z SAD, którzy otrzymywali PAXIL od 20 mg do 50 mg raz na dobę
- 8-tygodniowe badania kliniczne u pacjentów z GAD, którzy otrzymywali PAXIL od 10 mg do 50 mg raz na dobę
- 12-tygodniowe badania kliniczne u pacjentów z PTSD, którzy otrzymywali PAXIL od 20 mg do 50 mg raz na dobę
Działania niepożądane prowadzące do zaprzestania leczenia
Dwadzieścia procent (1199/6145) pacjentów leczonych PAXIL w badaniach klinicznych w MDD i 16,1% (84/522), 11,8% (64/542), 9,4% (44/469), 10,7% (79/735), i 11,7% (79/676) pacjentów leczonych PAXIL w badaniach klinicznych dotyczących odpowiednio SAD, OCD, PD, GAD i PTSD przerwało leczenie z powodu działania niepożądanego. Najczęstsze działania niepożądane (≥1%) związane z przerwaniem leczenia (tj. te działania niepożądane związane z odstawieniem produktu leczniczego PAXIL 10 mg z częstością około dwukrotnie lub większą niż w przypadku placebo) przedstawiono w Tabeli 3:
Najczęstsze działania niepożądane
Najczęściej obserwowanymi działaniami niepożądanymi związanymi ze stosowaniem PAXIL (częstość występowania 5% lub większa i co najmniej dwukrotnie większa niż w przypadku placebo) były:
MDD
Astenia, pocenie się, nudności, zmniejszony apetyt, senność, zawroty głowy, bezsenność, drżenie, nerwowość, zaburzenia wytrysku i inne zaburzenia męskich narządów płciowych.
OCD
Nudności, suchość w ustach, zmniejszony apetyt, zaparcia, zawroty głowy, senność, drżenie, pocenie się, impotencja i nieprawidłowy wytrysk.
PD
Astenia, pocenie się, zmniejszenie apetytu, zmniejszenie libido, drżenie, nieprawidłowy wytrysk, zaburzenia żeńskich narządów płciowych i impotencja.
SMUTNY
Pocenie się, nudności, suchość w ustach, zaparcia, zmniejszony apetyt, senność, drżenie, zmniejszenie libido, ziewanie, nieprawidłowy wytrysk, zaburzenia żeńskich narządów płciowych i impotencja.
GAD
Astenia, infekcja, zaparcia, zmniejszony apetyt, suchość w ustach, nudności, zmniejszenie libido, senność, drżenie, pocenie się i nieprawidłowy wytrysk.
PTSD
Astenia, pocenie się, nudności, suchość w ustach, biegunka, zmniejszony apetyt, senność, obniżone libido, nieprawidłowy wytrysk, zaburzenia żeńskich narządów płciowych i impotencja.
Działania niepożądane u pacjentów z MDD
Tabela 4 przedstawia działania niepożądane, które wystąpiły z częstością 1% lub większą i większą niż w przypadku placebo w badaniach klinicznych pacjentów z MDD leczonych PAXIL.
Działania niepożądane u pacjentów z OCD, PD i SAD
Tabela 5 przedstawia działania niepożądane, które wystąpiły z częstością 2% lub więcej w badaniach klinicznych u pacjentów z OCD, PD i SAD.
Działania niepożądane u pacjentów z GAD i PTSD
Tabela 6 przedstawia działania niepożądane, które wystąpiły z częstością 2% lub więcej w badaniach klinicznych u pacjentów z GAD i PTSD.
Działania niepożądane zależne od dawki
MDD
Porównanie częstości występowania działań niepożądanych w badaniu ze stałą dawką porównującym PAXIL 10 mg, 20 mg, 30 mg i 40 mg raz na dobę z placebo w leczeniu MDD ujawniło działania niepożądane zależne od dawki, jak pokazano w Tabeli 7:
OCD
W badaniu ze stałą dawką porównującym placebo i PAXIL 20 mg, 40 mg i 60 mg w leczeniu OCD, nie było wyraźnego związku między działaniami niepożądanymi a dawką PAXIL 30 mg, do której przydzielono pacjentów.
PD
badaniu ze stałą dawką porównującym placebo i PAXIL 10 mg, 20 mg i 40 mg w leczeniu PD, następujące działania niepożądane okazały się zależne od dawki: astenia, suchość w ustach, lęk, zmniejszenie libido, drżenie i nieprawidłowy wytrysk.
SMUTNY
W badaniu ze stałą dawką porównującym placebo i PAXIL 20 mg, 40 mg i 60 mg w leczeniu SAD, w przypadku większości działań niepożądanych, nie było wyraźnego związku między działaniami niepożądanymi a dawką PAXIL 10 mg, do której przydzielono pacjentów .
GAD
W badaniu ze stałą dawką porównującym placebo i PAXIL 20 mg i 40 mg w leczeniu GAD wykazano, że następujące działania niepożądane były zależne od dawki: astenia, zaparcia i nieprawidłowy wytrysk.
PTSD
W badaniu ze stałą dawką porównującym placebo i PAXIL 20 mg i 40 mg w leczeniu zespołu stresu pourazowego wykazano, że następujące działania niepożądane były zależne od dawki: impotencja i nieprawidłowy wytrysk.
Zaburzenia seksualne u mężczyzn i kobiet
Chociaż zmiany w pożądaniu seksualnym, sprawności seksualnej i satysfakcji seksualnej często pojawiają się jako przejawy zaburzeń psychicznych, mogą być również konsekwencją leczenia SSRI. Jednak trudno jest uzyskać wiarygodne szacunki częstości i nasilenia niepożądanych doświadczeń związanych z pożądaniem seksualnym, sprawnością i satysfakcją, częściowo dlatego, że pacjenci i pracownicy służby zdrowia mogą niechętnie o nich mówić. W związku z tym przytaczane w etykietowaniu szacunki częstości występowania nieprzewidzianych doświadczeń seksualnych i wydajności seksualnej mogą zaniżać ich rzeczywistą częstość występowania.
Odsetek pacjentów zgłaszających objawy dysfunkcji seksualnej u mężczyzn i kobiet z MDD, OCD, PD, SAD, GAD i PTSD przedstawiono w tabeli 8.
Leczenie PAXIL 20mg było związane z kilkoma przypadkami priapizmu. W przypadkach o znanym wyniku pacjenci wracali do zdrowia bez następstw.
Halucynacje
zbiorczych badaniach klinicznych PAXIL halucynacje obserwowano u 0,2% pacjentów leczonych PAXIL w porównaniu z 0,1% pacjentów otrzymujących placebo.
Mniej częste działania niepożądane
Następujące działania niepożądane wystąpiły podczas badań klinicznych produktu PAXIL i nie zostały wymienione w innym miejscu na etykiecie.
Działania niepożądane są podzielone na kategorie według układów organizmu i wymienione w kolejności malejącej częstości zgodnie z następującymi definicjami: Częste działania niepożądane to te, które występują 1 lub więcej razy u co najmniej 1/100 pacjentów; rzadkie działania niepożądane to te występujące u 1/100 do 1/1000 pacjentów; rzadkie działania niepożądane to te występujące u mniej niż 1/1000 pacjentów.
Ciało jako całość
Rzadko: Reakcja alergiczna, dreszcze, obrzęk twarzy, złe samopoczucie, ból szyi; rzadko: zespół adrenergiczny, zapalenie tkanki łącznej, drożdżyca, sztywność karku, ból miednicy, zapalenie otrzewnej, posocznica, wrzód.
Układu sercowo-naczyniowego
Częste: nadciśnienie, tachykardia; rzadko: bradykardia, krwiak, niedociśnienie, migrena, niedociśnienie ortostatyczne, omdlenia; rzadko: dławica piersiowa, arytmia węzłowa, migotanie przedsionków, blok odnogi pęczka Hisa, niedokrwienie mózgu, udar naczyniowo-mózgowy, zastoinowa niewydolność serca, blok serca, mała pojemność minutowa serca, zawał mięśnia sercowego, niedokrwienie mięśnia sercowego, bladość, zapalenie żył, zator tętnicy płucnej, zakrzepica nadkomorowa, zakrzepica, żylaki, naczyniowy ból głowy, dodatkowe skurcze komorowe.
Układ trawienny
Rzadko: bruksizm, zapalenie okrężnicy, dysfagia, odbijanie się, zapalenie żołądka, zapalenie żołądka i jelit, zapalenie dziąseł, zapalenie języka, zwiększone wydzielanie śliny, nieprawidłowe wyniki testów czynności wątroby, krwotok z odbytu, wrzodziejące zapalenie jamy ustnej; rzadko: aftowe zapalenie jamy ustnej, krwawa biegunka, bulimia, skurcz serca, kamica żółciowa, zapalenie dwunastnicy, zapalenie jelit, zapalenie przełyku, zator kałowy, nietrzymanie stolca, krwotok z dziąseł, krwawe wymioty, zapalenie wątroby, zapalenie jelita krętego, niedrożność jelit, niedrożność jelit, żółtaczka, melena, owrzodzenie jamy ustnej, owrzodzenie jamy ustnej, powiększenie gruczołów ślinowych, zapalenie sialadenitis, wrzód żołądka, zapalenie jamy ustnej, przebarwienia języka, obrzęk języka, próchnica zębów.
Układ hormonalny
Rzadko: cukrzyca, wole, nadczynność tarczycy, niedoczynność tarczycy, zapalenie tarczycy.
Układy hemiczne i limfatyczne
Rzadko: niedokrwistość, leukopenia, powiększenie węzłów chłonnych, plamica; rzadko: nieprawidłowe erytrocyty, bazofilia, wydłużenie czasu krwawienia, eozynofilia, niedokrwistość hipochromiczna, niedokrwistość z niedoboru żelaza, leukocytoza, obrzęk limfatyczny, nieprawidłowe limfocyty, limfocytoza, niedokrwistość mikrocytarna, monocytoza, niedokrwistość normocytarna, nadpłytkowość, małopłytkowość.
Metaboliczne i odżywcze
Częste: Przyrost masy ciała; rzadko: obrzęk, obrzęk obwodowy, zwiększony SGOT, zwiększony SGPT, pragnienie, utrata masy ciała; Rzadko: zwiększenie aktywności fosfatazy alkalicznej, bilirubinemia, zwiększenie stężenia BUN, zwiększenie aktywności fosfokinazy kreatyninowej, odwodnienie, zwiększenie aktywności gamma globulin, dna moczanowa, hiperkalcemia, hipercholesterolemia, hiperglikemia, hiperkaliemia, hiperfosfatemia, hipokalcemia, hipoglikemia, hipokaliemia, hiponatremia, niehydrogeneza, zwiększenie stężenia kwasu mlekowego wzrost azotu (NPN).
Układ mięśniowo-szkieletowy
Częste: bóle stawów; rzadko: zapalenie stawów, choroba zwyrodnieniowa stawów; rzadko: zapalenie kaletki, zapalenie mięśni, osteoporoza, uogólniony skurcz, zapalenie pochewki ścięgna, tężyczka.
System nerwowy
Częste: chwiejność emocjonalna, zawroty głowy; rzadko: zaburzenia myślenia, nadużywanie alkoholu, ataksja, dystonia, dyskineza, euforia, wrogość, hipertonia, niedoczulica, hipokineza, brak koordynacji, brak emocji, zwiększone libido, reakcja maniakalna, nerwica, paraliż, reakcja paranoidalna; rzadko: zaburzenia chodu, akinezja, reakcja antyspołeczna, afazja, choreoatetoza, parestezje okołoustne, drgawki, majaczenie, urojenia, podwójne widzenie, uzależnienie od leków, dyzartria, zespół pozapiramidowy, drgawki, drgawki typu grand mal, przeczulica bólowa, histeria, zapalenie maniakalno-depresyjne, reakcje meningowe zapalenie rdzenia kręgowego, nerwoból, neuropatia, oczopląs, zapalenie nerwów obwodowych, depresja psychotyczna, psychoza, osłabienie odruchów, nasilenie odruchów, otępienie, kręcz szyi, szczękościsk, zespół odstawienia.
Układ oddechowy
Rzadko: astma, zapalenie oskrzeli, duszność, krwawienie z nosa, hiperwentylacja, zapalenie płuc, grypa oddechowa; rzadko: rozedma, krwioplucie, czkawka, zwłóknienie płuc, obrzęk płuc, zwiększona ilość plwociny, stridor, zmiana głosu.
Skóra i przydatki
Częste: świąd; rzadko: Trądzik, łysienie, kontaktowe zapalenie skóry, suchość skóry, wybroczyny, egzema, opryszczka zwykła, nadwrażliwość na światło, pokrzywka; rzadko: obrzęk naczynioruchowy, rumień guzowaty, rumień wielopostaciowy, złuszczające zapalenie skóry, grzybicze zapalenie skóry, czyraczność; półpasiec, hirsutyzm, wysypka plamkowo-grudkowa, łojotok, przebarwienia skóry, przerost skóry, owrzodzenie skóry, zmniejszenie pocenia się, wysypka pęcherzykowo-pęcherzowa.
Specjalne zmysły
Częste: szum w uszach; rzadko: zaburzenia akomodacji, zapalenie spojówek, ból ucha, ból oka, zapalenie rogówki i spojówki, rozszerzenie źrenic, zapalenie ucha środkowego; rzadko: niedowidzenie, anizokoria, zapalenie powiek, zaćma, obrzęk spojówek, owrzodzenie rogówki, głuchota, wytrzeszcz, krwotok do oczu, jaskra, hiperakustyka, ślepota nocna, zapalenie ucha zewnętrznego, węch węchu, światłowstręt, opadanie powiek, krwotok siatkówkowy, ubytek pola widzenia.
Układ moczowo-płciowy
Rzadko: brak miesiączki, ból piersi, zapalenie pęcherza moczowego, bolesne oddawanie moczu, krwiomocz, krwotok miesiączkowy, nokturia, wielomocz, ropomocz, nietrzymanie moczu, zatrzymanie moczu, parcie na mocz, zapalenie pochwy; rzadko: aborcja, atrofia piersi, powiększenie piersi, zaburzenia endometrium, zapalenie najądrza, laktacja u kobiet, włóknienie piersi, kamień nerkowy, ból nerek, leukorrhea, zapalenie sutka, krwotok maciczny, zapalenie nerek, skąpomocz, zapalenie jajowodów, zapalenie cewki moczowej, wałeczki moczowe, skurcze macicy, skurcze pochwy, pęcherze moczowe krwotok, monilioza pochwy.
Doświadczenie postmarketingowe
Następujące reakcje zostały zidentyfikowane podczas stosowania produktu PAXIL po dopuszczeniu do obrotu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o nieznanej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Ostre zapalenie trzustki, podwyższone wyniki testów czynnościowych wątroby (najcięższe przypadki to zgony z powodu martwicy wątroby i rażąco podwyższona aktywność aminotransferaz związana z ciężkimi zaburzeniami czynności wątroby), zespół Guillain-Barré, zespół Stevensa-Johnsona, martwica toksyczno-rozpływna naskórka, zespół nieprawidłowego wydzielania ADH, prolaktynemia i mlekotok; objawy pozapiramidowe, które obejmowały akatyzję, spowolnienie ruchowe, sztywność koła zębatego, przełom w okulistyce, który był związany z jednoczesnym stosowaniem pimozydu; stan padaczkowy, ostra niewydolność nerek, nadciśnienie płucne, alergiczne zapalenie pęcherzyków płucnych, anafilaksja, rzucawka, krtani, zapalenie nerwu wzrokowego, porfiria, zespół niespokojnych nóg (RLS), migotanie komór, częstoskurcz komorowy (w tym torsade de pointes), niedokrwistość hemolityczna, zdarzenia związane z zaburzeniami hematopoeza (w tym niedokrwistość aplastyczna, pancytopenia, aplazja szpiku kostnego i agranulocytoza), zespoły naczyniowe (takie jak plamica Henocha-Schönleina) i przedwczesne porody u kobiet w ciąży. Opisano przypadek ciężkiego niedociśnienia, gdy PAXIL 20 mg został dodany do przewlekłego leczenia metoprololem.
INTERAKCJE Z LEKAMI
Tabela 9 przedstawia klinicznie istotne interakcje leków z PAXIL.
OSTRZEŻENIA
Zawarte jako część "ŚRODKI OSTROŻNOŚCI" Sekcja
ŚRODKI OSTROŻNOŚCI
Myśli i zachowania samobójcze u nastolatków i młodych dorosłych
W zbiorczych analizach kontrolowanych placebo badań leków przeciwdepresyjnych (SSRI i innych klas leków przeciwdepresyjnych), obejmujących około 77 000 pacjentów dorosłych i 4 500 pacjentów pediatrycznych, częstość występowania myśli i zachowań samobójczych u pacjentów w wieku 24 lat i młodszych leczonych lekami przeciwdepresyjnymi była większa niż w pacjentów otrzymujących placebo. Istniało znaczne zróżnicowanie ryzyka myśli i zachowań samobójczych wśród leków, ale w przypadku większości badanych leków stwierdzono zwiększone ryzyko u młodych pacjentów. Istniały różnice w bezwzględnym ryzyku myśli i zachowań samobójczych w różnych wskazaniach, z największą częstością występowania u pacjentów z MDD. Różnice między lekami a placebo w liczbie przypadków myśli i zachowań samobójczych na 1000 leczonych pacjentów przedstawiono w tabeli 2.
PAXIL 30mg nie jest zatwierdzony do stosowania u dzieci.
Nie wiadomo, czy ryzyko myśli i zachowań samobójczych u dzieci, młodzieży i młodych dorosłych rozciąga się na dłuższe stosowanie, tj. powyżej czterech miesięcy. Jednak istnieją dowody z kontrolowanych placebo badań podtrzymujących u dorosłych z MDD, że leki przeciwdepresyjne opóźniają nawrót depresji i że sama depresja jest czynnikiem ryzyka myśli i zachowań samobójczych.
Należy monitorować wszystkich pacjentów leczonych lekami przeciwdepresyjnymi pod kątem oznak pogorszenia stanu klinicznego i pojawienia się myśli i zachowań samobójczych, zwłaszcza podczas pierwszych kilku miesięcy terapii lekowej oraz w czasie zmiany dawkowania. Poradzić członkom rodziny lub opiekunom pacjentów, aby monitorowali zmiany w zachowaniu i ostrzegali świadczeniodawcę. Rozważ zmianę schematu leczenia, w tym ewentualnie odstawienie PAXIL, u pacjentów, u których depresja stale się nasila lub którzy doświadczają pojawiających się myśli lub zachowań samobójczych.
Zespół serotoninowy
SSRI, w tym PAXIL, mogą wywołać zespół serotoninowy, stan potencjalnie zagrażający życiu. Ryzyko zwiększa się w przypadku jednoczesnego stosowania innych leków serotoninergicznych (w tym tryptanów, trójpierścieniowych leków przeciwdepresyjnych, fentanylu, litu, tramadolu, tryptofanu, buspironu, amfetaminy i dziurawca) oraz leków zaburzających metabolizm serotoniny, tj. MAOI [patrz PRZECIWWSKAZANIA , INTERAKCJE Z LEKAMI ]. Zespół serotoninowy może również wystąpić, gdy leki te są stosowane samodzielnie.
Objawy zespołu serotoninowego mogą obejmować zmiany stanu psychicznego (np. pobudzenie, halucynacje, majaczenie i śpiączka), niestabilność autonomiczną (np. tachykardia, niestabilne ciśnienie krwi, zawroty głowy, pocenie się, uderzenia gorąca, hipertermia), objawy nerwowo-mięśniowe (np. drżenie, sztywność, mioklonie, hiperrefleksja, brak koordynacji), drgawki i/lub objawy żołądkowo-jelitowe (np. nudności, wymioty, biegunka).
Jednoczesne stosowanie PAXIL z IMAO jest przeciwwskazane. Ponadto nie należy rozpoczynać stosowania PAXIL 30 mg u pacjenta leczonego inhibitorami MAO, takimi jak linezolid lub dożylnie błękit metylenowy. Żadne doniesienia nie dotyczyły podawania błękitu metylenowego innymi drogami (takimi jak tabletki doustne lub miejscowe wstrzyknięcie do tkanek) lub w niższych dawkach. Jeśli konieczne jest rozpoczęcie leczenia inhibitorami MAO, takimi jak linezolid lub dożylny błękit metylenowy u pacjenta przyjmującego PAXIL w dawce 10 mg, należy przerwać stosowanie leku PAXIL w dawce 40 mg przed rozpoczęciem leczenia IMAO [patrz PRZECIWWSKAZANIA , INTERAKCJE Z LEKAMI ].
Monitoruj wszystkich pacjentów przyjmujących PAXIL 20mg pod kątem wystąpienia zespołu serotoninowego. W przypadku wystąpienia powyższych objawów należy natychmiast przerwać leczenie produktem PAXIL 20 mg i innymi jednocześnie stosowanymi środkami serotoninergicznymi i rozpocząć leczenie objawowe wspomagające. Jeśli jednoczesne stosowanie produktu PAXIL z innymi lekami serotoninergicznymi jest klinicznie uzasadnione, należy poinformować pacjentów o zwiększonym ryzyku wystąpienia zespołu serotoninowego i monitorować objawy.
Interakcje leków prowadzące do wydłużenia odstępu QT
Właściwości hamujące CYP2D6 paroksetyny mogą zwiększać stężenie tiorydazyny i pimozydu w osoczu. Ponieważ podawane same tiorydazyna i pimozyd powodują wydłużenie odstępu QTc i zwiększają ryzyko poważnych arytmii komorowych, stosowanie PAXIL 40 mg jest przeciwwskazane w połączeniu z tiorydazyną i pimozydem [patrz PRZECIWWSKAZANIA , INTERAKCJE Z LEKAMI , FARMAKOLOGIA KLINICZNA ].
Toksyczność zarodkowo-płodowa i noworodkowa
PAXIL może spowodować uszkodzenie płodu, jeśli zostanie podany kobiecie w ciąży. Badania epidemiologiczne wykazały, że niemowlęta narażone na paroksetynę w pierwszym trymestrze ciąży mają zwiększone ryzyko wad rozwojowych układu sercowo-naczyniowego. Ekspozycja na paroksetynę w późnej ciąży może prowadzić do zwiększonego ryzyka przetrwałego nadciśnienia płucnego noworodków (PPNH) i/lub powikłań noworodkowych wymagających przedłużonej hospitalizacji, wspomagania oddychania i karmienia przez sondę.
Jeśli PAXIL 20 mg jest stosowany w czasie ciąży lub jeśli pacjentka zajdzie w ciążę podczas przyjmowania PAXIL 30 mg, pacjentkę należy poinformować o potencjalnym zagrożeniu dla płodu [patrz Używaj w określonych populacjach ].
Zwiększone ryzyko krwawienia
Leki, które zakłócają hamowanie wychwytu zwrotnego serotoniny, w tym PAXIL 40 mg, zwiększają ryzyko wystąpienia krwawień. Jednoczesne stosowanie aspiryny, niesteroidowych leków przeciwzapalnych (NLPZ), innych leków przeciwpłytkowych, warfaryny i innych antykoagulantów może zwiększać to ryzyko. Opisy przypadków i badania epidemiologiczne (kontrola przypadków i projekt kohortowy) wykazały związek między stosowaniem leków zakłócających wychwyt zwrotny serotoniny a występowaniem krwawienia z przewodu pokarmowego. Krwawienia związane z lekami, które zakłócają wychwyt zwrotny serotoniny, wahały się od wybroczyn, krwiaków, krwawienia z nosa i wybroczyn po zagrażające życiu krwotoki.
Należy poinformować pacjentów o zwiększonym ryzyku krwawienia związanym z jednoczesnym stosowaniem PAXIL 20 mg i leków przeciwpłytkowych lub przeciwzakrzepowych. W przypadku pacjentów przyjmujących warfarynę należy uważnie monitorować międzynarodowy współczynnik znormalizowany.
Aktywacja manii lub hipomanii
U pacjentów z chorobą afektywną dwubiegunową leczenie epizodu depresji za pomocą PAXIL 30 mg lub innego leku przeciwdepresyjnego może wywołać epizod mieszany/maniakalny. Podczas kontrolowanych badań klinicznych produktu PAXIL hipomania lub mania wystąpiły u około 1% pacjentów z chorobą jednobiegunową leczonych PAXIL w porównaniu z 1,1% grupy aktywnej grupy kontrolnej i 0,3% pacjentów z chorobą jednobiegunową otrzymujących placebo. Przed rozpoczęciem leczenia PAXIL 20mg należy przebadać pacjentów pod kątem jakiejkolwiek osobistej lub rodzinnej historii choroby afektywnej dwubiegunowej, manii lub hipomanii.
Zespół odstawienia
Działania niepożądane po odstawieniu serotoninergicznych leków przeciwdepresyjnych, szczególnie po nagłym odstawieniu, obejmują: nudności, pocenie się, nastrój dysforyczny, drażliwość, pobudzenie, zawroty głowy, zaburzenia czucia (np. parestezje, takie jak uczucie wstrząsu elektrycznego), drżenie, lęk, splątanie, ból głowy, letarg, labilność emocjonalna, bezsenność, hipomania, szumy uszne i drgawki. Jeśli to możliwe, zaleca się stopniowe zmniejszanie dawki zamiast nagłego jej zaprzestania [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Podczas badań klinicznych nad GAD i PTSD przed przerwaniem leczenia stosowano stopniowe zmniejszanie dawki dobowej o 10 mg/dobę w odstępach tygodniowych, a następnie 1 tydzień w dawce 20 mg/dobę. Następujące działania niepożądane zgłaszano z częstością 2% lub większą w przypadku produktu PAXIL 20 mg i były one co najmniej dwukrotnie większe niż w przypadku placebo: Nieprawidłowe sny, parestezje i zawroty głowy Działania niepożądane zgłaszano po przerwaniu leczenia produktem PAXIL u dzieci i młodzieży. Bezpieczeństwo i skuteczność PAXIL u pacjentów pediatrycznych nie zostały ustalone [patrz OSTRZEŻENIE W PUDEŁKU , Myśli i zachowania samobójcze u nastolatków i młodych dorosłych , Używaj w określonych populacjach ].
Napady padaczkowe
Tabletki PAXIL 10 mg i zawiesina doustna nie były systematycznie oceniane u pacjentów z zaburzeniami drgawkowymi. Pacjenci z napadami drgawkowymi w wywiadzie byli wykluczeni z badań klinicznych. Podczas badań klinicznych drgawki wystąpiły u 0,1% pacjentów leczonych produktem PAXIL. PAXIL należy przepisywać ostrożnie pacjentom z napadami drgawkowymi. Należy odstawić PAXIL 30 mg u każdego pacjenta, u którego wystąpią drgawki.
Jaskra zamykającego się kąta
Rozszerzenie źrenic, które występuje po zastosowaniu wielu leków przeciwdepresyjnych, w tym PAXIL, może wywołać atak zamykania kąta u pacjenta z anatomicznie wąskim kątem, który nie ma drożnej tęczówki. Zgłaszano przypadki jaskry zamykającego się kąta związane ze stosowaniem produktu PAXIL 40 mg. Unikaj stosowania leków przeciwdepresyjnych, w tym PAXIL, u pacjentów z nieleczonymi anatomicznie wąskimi kątami.
Hiponatremia
Hiponatremia może wystąpić w wyniku leczenia SSRI, w tym PAXIL. Zgłaszano przypadki ze stężeniem sodu w surowicy poniżej 110 mmol/l. Oznaki i objawy hiponatremii obejmują ból głowy, trudności z koncentracją, zaburzenia pamięci, splątanie, osłabienie i chwiejność, które mogą prowadzić do upadków. Oznaki i objawy związane z cięższymi i/lub ostrymi przypadkami obejmowały halucynacje, omdlenia, drgawki, śpiączkę, zatrzymanie oddechu i śmierć. W wielu przypadkach ta hiponatremia wydaje się być wynikiem zespołu nieprawidłowego wydzielania hormonu antydiuretycznego (SIADH).
pacjentów z objawową hiponatremią należy odstawić PAXIL i zastosować odpowiednią interwencję medyczną. Pacjenci w podeszłym wieku, pacjenci przyjmujący leki moczopędne i osoby odwodnione mogą być narażeni na większe ryzyko rozwoju hiponatremii po podaniu SSRI [patrz Używaj w określonych populacjach ].
Zmniejszenie skuteczności tamoksyfenu
Niektóre badania wykazały, że skuteczność tamoksyfenu, mierzona ryzykiem nawrotu/śmiertelności raka piersi, może być zmniejszona podczas jednoczesnego stosowania PAXIL w wyniku nieodwracalnego hamowania przez paroksetyny CYP2D6 i obniżenia poziomu tamoksyfenu we krwi [patrz INTERAKCJE Z LEKAMI ]. Jedno z badań sugeruje, że ryzyko może wzrastać wraz z dłuższym czasem jednoczesnego podawania. Jednak inne badania nie wykazały takiego ryzyka. Gdy tamoksyfen jest stosowany w leczeniu lub profilaktyce raka piersi, lekarze przepisujący lek powinni rozważyć zastosowanie alternatywnego leku przeciwdepresyjnego o niewielkim lub zerowym hamowaniu CYP2D6.
Struktura kości
Badania epidemiologiczne dotyczące ryzyka złamań kości podczas ekspozycji na niektóre leki przeciwdepresyjne, w tym SSRI, wykazały związek między leczeniem przeciwdepresyjnym a złamaniami. Istnieje wiele możliwych przyczyn tej obserwacji i nie wiadomo, w jakim stopniu ryzyko złamań jest bezpośrednio związane z leczeniem SSRI.
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( Przewodnik po lekach ).
Myśli i zachowania samobójcze
Należy doradzić pacjentom i opiekunom, aby zwracali uwagę na występowanie samobójstw, zwłaszcza na wczesnym etapie leczenia i gdy dawkowanie jest zwiększane lub zmniejszane, oraz poinstruować ich, aby zgłaszali takie objawy lekarzowi [zob. OSTRZEŻENIE W PUDEŁKU oraz OSTRZEŻENIA I ŚRODKI ].
Zespół serotoninowy
Należy zwrócić uwagę pacjentów na ryzyko wystąpienia zespołu serotoninowego, szczególnie w przypadku jednoczesnego stosowania produktu PAXIL z innymi lekami serotoninergicznymi, w tym tryptanami, trójpierścieniowymi lekami przeciwdepresyjnymi, fentanylem, litem, tramadolem, tryptofanem, buspironem, amfetaminami, zielem dziurawca oraz lekami zaburzającymi metabolizm serotonina (w szczególności MAOI, zarówno te przeznaczone do leczenia zaburzeń psychicznych, jak i inne, np. linezolid). Poinstruuj pacjentów, aby skontaktowali się z lekarzem lub zgłosili się na pogotowie, jeśli wystąpią objawy zespołu serotoninowego [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI ].
Leki towarzyszące
Doradź pacjentom, aby informowali swojego lekarza, jeśli przyjmują lub planują przyjmować leki na receptę lub leki dostępne bez recepty, ponieważ istnieje możliwość interakcji między lekami [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI , INTERAKCJE Z LEKAMI ].
Zwiększone ryzyko krwawienia
Należy poinformować pacjentów o jednoczesnym stosowaniu PAXIL z aspiryną, NLPZ, innymi lekami przeciwpłytkowymi, warfaryną lub innymi lekami przeciwzakrzepowymi, ponieważ łączne stosowanie wiąże się ze zwiększonym ryzykiem krwawienia. Doradź pacjentom, aby informowali swoich lekarzy o przyjmowaniu lub planowaniu przyjmowania jakichkolwiek leków na receptę lub bez recepty, które zwiększają ryzyko krwawienia [patrz OSTRZEŻENIA I ŚRODKI ].
Aktywacja manii/hipomanii
Poradź pacjentom i ich opiekunom, aby obserwowali oznaki aktywacji manii/hipomanii i poinstruuj ich, aby zgłaszali takie objawy lekarzowi [patrz OSTRZEŻENIA I ŚRODKI ].
Zespół odstawienia
Doradź pacjentom, aby nie przerywali nagle leczenia PAXIL 40 mg i omówili z lekarzem wszelkie zmniejszane dawki. Należy poinformować pacjentów, że po odstawieniu produktu PAXIL mogą wystąpić działania niepożądane [patrz OSTRZEŻENIA I ŚRODKI ].
Informacje administracyjne dotyczące zawieszenia ustnego
Należy poinstruować pacjentów, aby dobrze wstrząsnęli zawiesiną doustną przed podaniem [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Reakcje alergiczne
Doradź pacjentom, aby powiadomili swojego lekarza, jeśli wystąpią u nich reakcje alergiczne, takie jak wysypka, pokrzywka, obrzęk lub trudności w oddychaniu [patrz DZIAŁANIA NIEPOŻĄDANE ].
Toksyczność zarodkowo-płodowa
Poinformuj kobiety o potencjalnym ryzyku dla płodu [patrz OSTRZEŻENIA I ŚRODKI , Używaj w określonych populacjach ]. Należy doradzić pacjentkom, aby powiadomiły swojego lekarza, jeśli zajdą w ciążę lub zamierzają zajść w ciążę w trakcie leczenia ze względu na ryzyko dla płodu.
Pielęgniarstwo
Doradź kobietom, aby powiadomiły swojego lekarza, jeśli karmią piersią niemowlę [patrz Używaj w określonych populacjach ].
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Karcynogeneza
Przeprowadzono dwuletnie badania rakotwórczości na gryzoniach, którym podawano paroksetynę w diecie w dawce 1, 5 i 25 mg/kg/dobę (myszy) oraz 1, 5 i 20 mg/kg/dobę (szczury). Te dawki są do 2,0 (mysz) i 3,2 (szczur) razy większe od MRHD 75 mg w przeliczeniu na mg/m2. W grupie otrzymującej wysoką dawkę stwierdzono znacznie większą liczbę samców szczurów z mięsakami komórek retikulum (1/100, 0/50, 0/50 i 4/50 w grupach kontrolnych, z niską, średnią i wysoką dawką , odpowiednio) i znacząco zwiększony trend liniowy w grupach dawek dla występowania guzów limforetikularnych u samców szczurów. Nie dotyczyło to samic szczurów. Chociaż nastąpił związany z dawką wzrost liczby guzów u myszy, nie zaobserwowano związanego z lekiem wzrostu liczby myszy z guzami. Znaczenie tych wyników dla ludzi nie jest znane.

Mutageneza
Paroksetyna nie powodowała działania genotoksycznego w zestawie 5 testów in vitro i 2 in vivo, które obejmowały: test mutacji bakteryjnych, test mutacji chłoniaka myszy, test nieplanowej syntezy DNA oraz testy aberracji cytogenetycznych in vivo w szpiku kostnym myszy i in vitro w ludzkich limfocytach oraz w dominującym teście letalnym u szczurów.
Upośledzenie płodności
Niektóre badania kliniczne wykazały, że SSRI (w tym paroksetyna) mogą wpływać na jakość nasienia podczas leczenia SSRI, co może wpływać na płodność u niektórych mężczyzn.
badaniach rozrodczości u szczurów, którym podawano paroksetynę w dawce 15 mg/kg/dobę, co stanowi 2,4-krotność MRHD wynoszącej 75 mg w przeliczeniu na mg/m2, stwierdzono zmniejszony wskaźnik ciąż. Nieodwracalne zmiany wystąpiły w układzie rozrodczym samców szczurów po dawkowaniu w badaniach toksyczności przez 2 do 52 tygodni. Zmiany te polegały na wakuolizacji nabłonka kanalików najądrza przy dawce 50 mg/kg/dzień oraz zmianach zanikowych w kanalikach nasiennych jąder z zatrzymaniem spermatogenezy przy dawce 25 mg/kg/dzień (8,2 i 4,1 razy MRHD 75 mg na mg/dzień). m2 podstawy).
Używaj w określonych populacjach
Ciąża
Ciąża Kategoria D [Patrz OSTRZEŻENIA I ŚRODKI ]
Badania epidemiologiczne wykazały, że niemowlęta narażone na paroksetynę w pierwszym trymestrze ciąży mają zwiększone ryzyko wad wrodzonych, szczególnie wad rozwojowych układu krążenia. Jeśli paroksetyna jest stosowana w czasie ciąży lub jeśli pacjentka zajdzie w ciążę podczas przyjmowania paroksetyny, należy poinformować pacjentkę o potencjalnym zagrożeniu dla płodu.
Rozważania kliniczne
ile korzyści z paroksetyny dla matki nie uzasadniają kontynuacji leczenia, należy rozważyć przerwanie leczenia paroksetyną lub przejście na inny lek przeciwdepresyjny [patrz OSTRZEŻENIA I ŚRODKI ]. Do
- Badanie oparte na danych z krajowego rejestru szwedzkiego wykazało, że niemowlęta narażone na paroksetynę podczas ciąży (n = 815) miały zwiększone ryzyko wad rozwojowych układu sercowo-naczyniowego (ryzyko 2% u niemowląt eksponowanych na paroksetynę) w porównaniu z całą populacją rejestru (ryzyko 1%). dla ilorazu szans (OR) 1,8 (95% przedział ufności 1,1 do 2,8). Nie zaobserwowano wzrostu ryzyka ogólnych wad wrodzonych u niemowląt narażonych na działanie paroksetyny. Wady rozwojowe serca u niemowląt eksponowanych na paroksetynę to przede wszystkim wady przegrody międzykomorowej (VSD) i wady przegrody międzyprzedsionkowej (ASD). Wady przegrody mają różne nasilenie, od tych, które ustępują samoistnie, do tych, które wymagają operacji.
- oddzielnym retrospektywnym badaniu kohortowym ze Stanów Zjednoczonych (dane United Healthcare) oceniono 5956 niemowląt matek, które podawały leki przeciwdepresyjne w pierwszym trymestrze ciąży (n = 815 dla paroksetyny). Badanie to wykazało tendencję do zwiększonego ryzyka wad rozwojowych układu sercowo-naczyniowego dla paroksetyny (ryzyko 1,5%) w porównaniu z innymi lekami przeciwdepresyjnymi (ryzyko 1%), dla OR 1,5 (95% przedział ufności 0,8 do 2,9). Spośród 12 niemowląt wystawionych na działanie paroksetyny z wadami rozwojowymi układu sercowo-naczyniowego, 9 miało VSD. Badanie to sugerowało również zwiększone ryzyko ogólnych poważnych wad wrodzonych, w tym wad sercowo-naczyniowych dla paroksetyny (ryzyko 4%) w porównaniu z innymi lekami przeciwdepresyjnymi (ryzyko 2%) (OR 1,8; przedział ufności 95% 1,2 do 2,8).
- Dwa duże badania kliniczno-kontrolne z wykorzystaniem oddzielnych baz danych, z których każda zawierała >9000 przypadków wad wrodzonych i >4000 przypadków kontrolnych, wykazały, że stosowanie paroksetyny przez matkę w pierwszym trymestrze ciąży wiązało się z 2-3-krotnym zwiększeniem ryzyka odpływu z prawej komory przeszkody na drogach. W jednym badaniu OR wynosił 2,5 (95% przedział ufności, 1,0 do 6,0, 7 narażonych niemowląt), a w drugim badaniu OR wynosił 3,3 (95% przedział ufności, 1,3 do 8,8, 6 narażonych niemowląt).
Inne badania wykazały różne wyniki dotyczące tego, czy istnieje zwiększone ryzyko ogólnych, sercowo-naczyniowych lub specyficznych wad wrodzonych. Metaanaliza danych epidemiologicznych z okresu 16 lat (1992-2008) dotyczących stosowania paroksetyny w pierwszym trymestrze ciąży i wad wrodzonych obejmowała, oprócz innych, wyżej wymienione badania (n = 17 badań, które obejmowały wady ogólne, a n = 14 badań, które obejmowały wady rozwojowe układu sercowo-naczyniowego; n = 20 odrębnych badań). Chociaż podlega ona ograniczeniom, ta metaanaliza sugeruje zwiększoną częstość występowania wad rozwojowych układu sercowo-naczyniowego (iloraz szans [POR] 1,5; 95% przedział ufności 1,2 do 1,9) i ogólnych wad rozwojowych (POR 1,2; 95% przedział ufności 1,1 do 1,4) w przypadku paroksetyny stosować w pierwszym trymestrze. W tej metaanalizie nie było możliwe określenie stopnia, w jakim obserwowana częstość występowania wad rozwojowych układu sercowo-naczyniowego mogła przyczynić się do występowania wad ogólnych, ani też nie było możliwe ustalenie, czy do obserwowanej częstości mogły przyczynić się jakieś określone typy wad rozwojowych układu sercowo-naczyniowego. wszystkich wad rozwojowych układu sercowo-naczyniowego.
ile korzyści z paroksetyny dla matki nie uzasadniają kontynuacji leczenia, należy rozważyć przerwanie leczenia paroksetyną lub przejście na inny lek przeciwdepresyjny [patrz OSTRZEŻENIA I ŚRODKI ]. W przypadku kobiet, które zamierzają zajść w ciążę lub są w pierwszym trymestrze ciąży, paroksetynę należy rozpoczynać wyłącznie po rozważeniu innych dostępnych opcji leczenia [patrz OSTRZEŻENIA I ŚRODKI ].
Leczenie kobiet w ciąży w trzecim trymestrze
noworodków narażonych na SSRI lub inhibitory wychwytu zwrotnego serotoniny i noradrenaliny (SNRI), w tym PAXIL 40 mg, pod koniec trzeciego trymestru wystąpiły powikłania wymagające długotrwałej hospitalizacji, wspomagania oddychania i karmienia przez sondę. Takie komplikacje mogą pojawić się natychmiast po porodzie. Zgłaszane objawy kliniczne obejmowały niewydolność oddechową, sinicę, bezdech, drgawki, niestabilność temperatury, trudności w karmieniu, wymioty, hipoglikemię, hipotonię, hipertonię, hiperrefleksję, drżenie, drżenie, drażliwość i ciągły płacz. Cechy te są zgodne albo z bezpośrednim toksycznym działaniem SSRI i SNRI, albo ewentualnie z zespołem odstawienia leku. Należy zauważyć, że w niektórych przypadkach obraz kliniczny jest zgodny z zespołem serotoninowym [patrz OSTRZEŻENIA I ŚRODKI ].
Narażenie na SSRI w późnej ciąży może wiązać się ze zwiększonym ryzykiem przetrwałego nadciśnienia płucnego u noworodków (PPHN). PPHN występuje w 1 – 2 przypadkach na 1000 żywych urodzeń w populacji ogólnej i wiąże się ze znaczną zachorowalnością i śmiertelnością noworodków. W retrospektywnym badaniu kliniczno-kontrolnym obejmującym 377 kobiet, których niemowlęta urodziły się z PPHN i 836 kobiet, których niemowlęta urodziły się zdrowe, ryzyko rozwoju PPHN było około sześciokrotnie wyższe u niemowląt narażonych na SSRI po 20. tygodniu ciąży w porównaniu z niemowlętami które nie były narażone na leki przeciwdepresyjne w czasie ciąży.
Istnieją również doniesienia postmarketingowe o przedwczesnych porodach u kobiet w ciąży narażonych na paroksetynę lub inne SSRI.
Podczas leczenia kobiety ciężarnej paroksetyną w trzecim trymestrze lekarz powinien dokładnie rozważyć zarówno potencjalne ryzyko, jak i korzyści leczenia. Prospektywne badanie podłużne 201 kobiet z historią ciężkiej depresji, które były w stanie eutymii na początku ciąży. Kobiety, które odstawiły leki przeciwdepresyjne w czasie ciąży, częściej doświadczały nawrotu ciężkiej depresji niż kobiety, które kontynuowały przyjmowanie leków przeciwdepresyjnych.
Znaleziska zwierząt
Badania nad reprodukcją przeprowadzono przy dawkach do 50 mg/kg/dobę u szczurów i 6 mg/kg/dobę u królików podawanych podczas organogenezy. Dawki te są około 6 (szczur) i mniej niż 2 (królik) razy większe od maksymalnej zalecanej dawki dla człowieka (MRHD – 75 mg) w przeliczeniu na mg/m2. Badania te nie wykazały żadnych dowodów na efekty rozwojowe. Jednak u szczurów zaobserwowano wzrost śmiertelności młodych w ciągu pierwszych 4 dni laktacji, gdy dawkowanie nastąpiło w ostatnim trymestrze ciąży i było kontynuowane przez całą laktację. Efekt ten wystąpił przy dawce 1 mg/kg/dzień, która jest równa MRHD w przeliczeniu na mg/m2. Nie ustalono dawki niepowodującej wpływu na śmiertelność młodych szczurów. Przyczyna tych zgonów nie jest znana.
Matki karmiące
Podobnie jak wiele innych leków, paroksetyna jest wydzielana do mleka ludzkiego. Ze względu na możliwość wystąpienia poważnych działań niepożądanych u niemowląt karmionych PAXIL 20mg, należy podjąć decyzję, czy przerwać karmienie niemowląt, czy przerwać stosowanie leku, biorąc pod uwagę znaczenie leku dla matki.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność PAXIL u pacjentów pediatrycznych nie zostały ustalone [patrz PUDEŁKO OSTRZEŻENIE ]. Skuteczność nie została wykazana w trzech badaniach kontrolowanych placebo z udziałem 752 pacjentów pediatrycznych z MDD leczonych PAXIL.
Leki przeciwdepresyjne zwiększają ryzyko myśli i zachowań samobójczych u pacjentów pediatrycznych [patrz OSTRZEŻENIE W PUDEŁKU , OSTRZEŻENIA I ŚRODKI ]. W związku ze stosowaniem SSRI zaobserwowano zmniejszenie apetytu i utratę masy ciała.
kontrolowanych placebo badaniach klinicznych przeprowadzonych z udziałem dzieci, następujące działania niepożądane zgłoszono u co najmniej 2% dzieci leczonych produktem PAXIL i występowały z częstością co najmniej dwukrotnie większą niż u dzieci i młodzieży otrzymujących placebo: chwiejność emocjonalna (w tym samookaleczenie myśli samobójcze, próby samobójcze, płacz i wahania nastroju), wrogość, zmniejszony apetyt, drżenie, pocenie się, hiperkineza i pobudzenie.
Działania niepożądane po przerwaniu leczenia produktem PAXIL w pediatrycznych badaniach klinicznych obejmujących fazę stopniowego zmniejszania dawki, które wystąpiły u co najmniej 2% pacjentów i z częstością co najmniej dwukrotnie większą niż placebo, to: chwiejność emocjonalna (w tym myśli samobójcze, samobójstwa próba, zmiany nastroju i płaczliwość), nerwowość, zawroty głowy, nudności i ból brzucha.
Zastosowanie geriatryczne
badaniach klinicznych przed wprowadzeniem do obrotu produktu PAXIL 10 mg 17% pacjentów leczonych produktem PAXIL (około 700) było w wieku 65 lat lub starszych. Badania farmakokinetyczne wykazały zmniejszony klirens u osób w podeszłym wieku i zalecana jest niższa dawka początkowa; jednak nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między pacjentami w podeszłym wieku i młodszymi [patrz DAWKOWANIE I SPOSÓB PODAWANIA , FARMAKOLOGIA KLINICZNA ].
SSRI, w tym PAXIL, były związane z przypadkami klinicznie istotnej hiponatremii u pacjentów w podeszłym wieku, którzy mogą być bardziej narażeni na to działanie niepożądane [patrz OSTRZEŻENIA I ŚRODKI ].
Zaburzenia nerek i wątroby
U pacjentów z zaburzeniami czynności nerek i wątroby występuje zwiększone stężenie paroksetyny w osoczu. Początkową dawkę produktu PAXIL należy zmniejszyć u pacjentów z ciężkimi zaburzeniami czynności nerek oraz u pacjentów z ciężkimi zaburzeniami czynności wątroby [patrz DAWKOWANIE I SPOSÓB PODAWANIA , FARMAKOLOGIA KLINICZNA ].
PRZEDAWKOWAĆ
Ludzkie doświadczenie
Od czasu wprowadzenia PAXIL 30 mg w Stanach Zjednoczonych, na całym świecie zgłaszano spontaniczne przypadki celowego lub przypadkowego przedawkowania podczas leczenia paroksetyną. Obejmują one przedawkowanie samej paroksetyny oraz w połączeniu z innymi substancjami. Istnieją doniesienia o zgonach, które wydają się dotyczyć samej paroksetyny.
Często zgłaszane działania niepożądane związane z przedawkowaniem paroksetyny obejmują senność, śpiączkę, nudności, drżenie, tachykardię, splątanie, wymioty i zawroty głowy. Inne godne uwagi oznaki i objawy obserwowane po przedawkowaniu paroksetyny (sam lub z innymi substancjami) obejmują rozszerzenie źrenic, drgawki (w tym stan padaczkowy), arytmie komorowe (w tym torsade de pointes), nadciśnienie, reakcje agresywne, omdlenie, niedociśnienie, otępienie, bradykardię, dystonię rabdomioliza, objawy dysfunkcji wątroby (w tym niewydolność wątroby, martwica wątroby, żółtaczka, zapalenie wątroby i stłuszczenie wątroby), zespół serotoninowy, reakcje maniakalne, mioklonie, ostra niewydolność nerek i zatrzymanie moczu.
Zarządzanie przedawkowaniem
Nie są znane żadne specyficzne antidota na PAXIL. Jeśli wystąpi przedawkowanie, zadzwoń do centrum kontroli zatruć pod numer 1-800-222-1222, aby uzyskać najnowsze zalecenia.
PRZECIWWSKAZANIA
PAXIL jest przeciwwskazany u pacjentów:
- Przyjmowanie lub w ciągu 14 dni od odstawienia IMAO (w tym IMAO linezolid i błękit metylenowy dożylnie) z powodu zwiększonego ryzyka wystąpienia zespołu serotoninowego [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI ].
- Przyjmowanie tiorydazyny z powodu ryzyka wydłużenia odstępu QT [patrz OSTRZEŻENIA I ŚRODKI oraz INTERAKCJE Z LEKAMI ]
- Przyjmowanie pimozydu z powodu ryzyka wydłużenia odstępu QT [patrz OSTRZEŻENIA I ŚRODKI , INTERAKCJE Z LEKAMI ].
- Ze stwierdzoną nadwrażliwością (np. anafilaksją, obrzękiem naczynioruchowym, zespołem Stevensa-Johnsona) na paroksetynę lub którykolwiek z nieaktywnych składników PAXIL [patrz DZIAŁANIA NIEPOŻĄDANE ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Mechanizm działania PAXIL w leczeniu MDD, SAD, OCD\, PD, GAD i PTSD jest nieznany, ale przypuszcza się, że jest powiązany z nasileniem aktywności serotoninergicznej w ośrodkowym układzie nerwowym w wyniku hamowania neuronalnego wychwytu zwrotnego serotoniny (5-hydroksytryptamina, 5-HT).
Farmakodynamika
Badania z klinicznie istotnymi dawkami u ludzi wykazały, że paroksetyna blokuje wychwyt serotoniny przez ludzkie płytki krwi. Badania in vitro na zwierzętach sugerują również, że paroksetyna jest silnym i wysoce selektywnym inhibitorem wychwytu zwrotnego serotoniny w neuronach (SSRI) i ma tylko bardzo słaby wpływ na wychwyt zwrotny norepinefryny i dopaminy w neuronach.
Farmakokinetyka
Nieliniowość farmakokinetyki obserwuje się wraz ze wzrostem dawek produktu PAXIL.
W metaanalizie paroksetyny z 4 badań przeprowadzonych na zdrowych ochotnikach po wielokrotnych dawkach od 20 mg/dobę do 40 mg/dobę, mężczyźni nie wykazywali znacząco niższego Cmax lub AUC niż kobiety.
Wchłanianie
Chlorowodorek paroksetyny jest całkowicie wchłaniany po podaniu doustnym roztworu soli chlorowodorkowej. W badaniu, w którym normalni mężczyźni (n = 15) otrzymywali tabletki 30 mg na dobę przez 30 dni, stężenie paroksetyny w stanie stacjonarnym osiągano u większości pacjentów po około 10 dniach, chociaż u niektórych pacjentów może to trwać znacznie dłużej. W stanie stacjonarnym średnie wartości Cmax, Tmax, Cmin i T½ wynosiły 61,7 ng/ml (CV 45%), 5,2 godz. (CV 10%), 30,7 ng/ml (CV 67%) i 21,0 godzin (CV 32%). Wartości Cmax i Cmin w stanie stacjonarnym były około 6 i 14 razy większe niż przewidywane w badaniach z pojedynczą dawką. Ekspozycja na lek w stanie stacjonarnym na podstawie AUC0-24 była około 8 razy większa niż można by było przewidzieć na podstawie danych dotyczących pojedynczej dawki u tych osób. Nadmierna akumulacja jest konsekwencją faktu, że jeden z enzymów metabolizujących paroksetynę łatwo ulega wysyceniu.
Paroksetyna jest równie biodostępna z zawiesiny doustnej i tabletki.
Wpływ jedzenia
Wpływ pokarmu na biodostępność paroksetyny badano u osób, którym podawano pojedynczą dawkę z pokarmem i bez pokarmu. AUC zwiększyło się tylko nieznacznie (6%), gdy lek podawano z pokarmem, ale Cmax było o 29% większe, podczas gdy czas do osiągnięcia maksymalnego stężenia w osoczu zmniejszył się z 6,4 godziny po podaniu do 4,9 godziny.
Dystrybucja
Paroksetyna rozprowadza się po całym ciele, w tym w OUN, przy czym w osoczu pozostaje tylko 1%.
Około 95% i 93% paroksetyny wiąże się z białkami osocza odpowiednio przy 100 ng/ml i 400 ng/ml. W warunkach klinicznych stężenia paroksetyny normalnie byłyby mniejsze niż 400 ng/ml. Paroksetyna nie zmienia in vitro wiązania fenytoiny lub warfaryny z białkami.
Eliminacja
Metabolizm
Średni okres półtrwania w fazie eliminacji wynosi około 21 godzin (CV 32%) po podaniu doustnym tabletek 30 mg na dobę przez 30 dni produktu PAXIL.
badaniach proporcjonalności dawki w stanie stacjonarnym z udziałem pacjentów w podeszłym wieku i pacjentów w podeszłym wieku, przy dawkach od 20 mg do 40 mg na dobę dla osób w podeszłym wieku i od 20 mg do 50 mg na dobę dla osób innych niż osoby w podeszłym wieku, zaobserwowano pewną nieliniowość w obu populacjach, ponownie odzwierciedlającą wysycony szlak metaboliczny. . W porównaniu z wartościami Cmin po 20 mg dziennie, wartości po 40 mg dziennie były tylko około 2 do 3 razy większe niż dwukrotnie.
Paroksetyna jest intensywnie metabolizowana po podaniu doustnym. Główne metabolity to polarne i skoniugowane produkty utleniania i metylacji, które są łatwo usuwane. Przeważają koniugaty z kwasem glukuronowym i siarczanem, a główne metabolity zostały wyizolowane i zidentyfikowane. Dane wskazują, że metabolity mają nie więcej niż 1/50 siły związku macierzystego w hamowaniu wychwytu serotoniny. Metabolizm paroksetyny odbywa się częściowo przez CYP2D6. Wydaje się, że wysycenie tego enzymu w dawkach klinicznych odpowiada za nieliniowość kinetyki paroksetyny wraz ze wzrostem dawki i wydłużeniem czasu leczenia. Rola tego enzymu w metabolizmie paroksetyny sugeruje również potencjalne interakcje lekowe [patrz INTERAKCJE Z LEKAMI ]. Zachowanie farmakokinetyczne paroksetyny nie zostało ocenione u osób z niedoborem CYP2D6 (słabo metabolizujących).
Wydalanie
Około 64% dawki 30 mg paroksetyny w postaci roztworu doustnego zostało wydalone z moczem, przy czym 2% jako związek macierzysty i 62% jako metabolity w ciągu 10 dni po podaniu. Około 36% zostało wydalone z kałem (prawdopodobnie przez żółć), głównie jako metabolity i mniej niż 1% jako związek macierzysty w ciągu 10 dni po podaniu.
Badania interakcji leków
Istnieją klinicznie istotne, znane interakcje między paroksetyną a innymi lekami [patrz INTERAKCJE Z LEKAMI ].
Rycina 1. Wpływ paroksetyny na farmakokinetykę jednocześnie podawanych leków (skala logarytmiczna)
Rycina 2. Wpływ jednocześnie podawanych leków na farmakokinetykę paroksetyny
Teofilina
Zgłaszano doniesienia o podwyższonych poziomach teofiliny związanych z leczeniem PAXIL. Chociaż ta interakcja nie była formalnie badana, zaleca się monitorowanie stężenia teofiliny podczas jednoczesnego podawania tych leków.
Leki metabolizowane przez cytochrom CYP3A4
Badanie interakcji in vivo obejmujące równoczesne podawanie w stanie stacjonarnym paroksetyny i terfenadyny, substratu CYP3A4, nie wykazało wpływu paroksetyny na farmakokinetykę terfenadyny. Ponadto badania in vitro wykazały, że ketokonazol, silny inhibitor aktywności CYP3A4, jest co najmniej 100 razy silniejszy niż paroksetyna jako inhibitor metabolizmu kilku substratów tego enzymu, w tym terfenadyny, astemizolu, cyzaprydu, triazolamu i cyklosporyna. Oczekuje się, że stopień hamowania aktywności CYP3A4 przez paroksetynę nie będzie miał znaczenia klinicznego.
Określone populacje
Wpływ określonych populacji na farmakokinetykę paroksetyny przedstawiono na rycinie 3.
Zalecana dawka początkowa i maksymalna dawka produktu PAXIL są zmniejszone u pacjentów w podeszłym wieku, pacjentów z ciężkimi zaburzeniami czynności nerek oraz pacjentów z ciężkimi zaburzeniami czynności wątroby [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Rycina 3. Wpływ określonej populacji na farmakokinetykę paroksetyny (skala logarytmiczna)
Studia kliniczne
Ciężkie zaburzenie depresyjne
Skuteczność produktu PAXIL w leczeniu dużych zaburzeń depresyjnych (MDD) została potwierdzona w 6 badaniach kontrolowanych placebo u pacjentów z MDD (w wieku od 18 do 73 lat). W badaniach tych wykazano, że PAXIL jest istotnie statystycznie skuteczniejszy niż placebo w leczeniu MDD, co najmniej za pomocą 2 z następujących wskaźników: Skala Oceny Depresji Hamiltona (HDRS), pozycja dotycząca nastroju depresyjnego Hamiltona oraz Globalna ocena kliniczna (CGI) – Ciężkość choroby. PAXIL był statystycznie istotnie lepszy niż placebo pod względem poprawy wyników sub-czynnikowych HDRS, w tym elementu nastroju depresyjnego, czynnika zaburzeń snu i czynnika lękowego.
randomizowanym badaniu dotyczącym wycofania wykazano długoterminową skuteczność PAXIL 10 mg w leczeniu MDD u pacjentów ambulatoryjnych. Pacjenci, którzy odpowiedzieli na PAXIL (całkowity wynik HDRS
Zaburzenie obsesyjno-kompulsyjne
Skuteczność produktu PAXIL w leczeniu zaburzeń obsesyjno-kompulsywnych (OCD) wykazano w dwóch 12-tygodniowych wieloośrodkowych, kontrolowanych placebo badaniach dorosłych pacjentów ambulatoryjnych (Badania 1 i 2). Pacjenci mieli umiarkowany do ciężkiego OCD (DSM-IIIR) ze średnimi wyjściowymi ocenami w skali Yale Brown Obsessive Compulsive Scale (YBOCS) w zakresie od 23 do 26. W badaniu 1, badaniu ustalającym zakres dawek, pacjenci otrzymywali stałe dawki dobowe wynoszące PAXIL 20 mg, 40 mg lub 60 mg. Badanie 1 wykazało, że dzienne dawki PAXIL 40 mg i 60 mg są skuteczne w leczeniu OCD. U pacjentów otrzymujących dawki PAXIL 40 mg i 60 mg nastąpiło średnie zmniejszenie o odpowiednio około 6 i 7 punktów całkowitego wyniku YBOCS, które było statystycznie istotnie większe niż w przybliżeniu 4-punktowa redukcja przy 20 mg i 3-punktowa redukcja w pacjentów otrzymujących placebo. Badanie 2 było badaniem ze zmienną dawką porównującym PAXIL 20 mg do 60 mg na dobę z klomipraminą w dawce 25 mg do 250 mg na dobę lub placebo). W tym badaniu pacjenci otrzymujący PAXIL doświadczyli średniej redukcji o około 7 punktów w całkowitym wyniku YBOCS, która była statystycznie istotnie większa niż średnia redukcja o około 4 punkty u pacjentów otrzymujących placebo.
Poniższa tabela przedstawia klasyfikację wyników według grup leczenia według pozycji Globalnej Poprawy skali Clinical Global Impression (CGI) dla Badania 1.
Analizy podgrup nie wykazały różnic w wynikach leczenia w zależności od wieku lub płci.
Długoterminową skuteczność PAXIL w leczeniu OCD ustalono w długoterminowym przedłużeniu badania 1. Pacjenci, u których wystąpiła odpowiedź na PAXIL podczas 3-miesięcznej fazy podwójnie ślepej próby i 6-miesięcznego przedłużenia otwartej próby PAXIL 20 Dawki od mg do 60 mg na dobę przydzielono losowo do grupy PAXIL 10 mg lub placebo w 6-miesięcznej fazie zapobiegania nawrotom z podwójnie ślepą próbą. Pacjenci przydzieleni losowo do grupy PAXIL mieli statystycznie istotnie mniejsze prawdopodobieństwo nawrotu choroby niż pacjenci otrzymujący placebo.
Zaburzenie lękowe
Skuteczność PAXIL 20 mg w leczeniu lęku napadowego (PD) wykazano w trzech trwających od 10 do 12 tygodni wieloośrodkowych, kontrolowanych placebo badaniach dorosłych pacjentów ambulatoryjnych (Badania 1, 2 i 3). Pacjenci mieli PD (DSM-IIIR), z agorafobią lub bez agorafobii. W badaniach tych wykazano, że PAXIL jest istotnie statystycznie skuteczniejszy niż placebo w leczeniu PD w co najmniej 2 z 3 miar częstości napadów paniki oraz w skali Clinical Global Impression Severity of Illness.
Badanie 1 było 10-tygodniowym badaniem mającym na celu ustalenie zakresu dawki; pacjenci otrzymywali stałe dawki PAXIL 10 mg, 20 mg lub 40 mg na dobę lub placebo. Statystycznie istotną różnicę w porównaniu z placebo zaobserwowano tylko w grupie PAXIL 40 mg na dobę. W punkcie końcowym 76% pacjentów otrzymujących PAXIL w dawce 40 mg na dobę było wolnych od ataków paniki w porównaniu z 44% pacjentów otrzymujących placebo.
Badanie 2 było 12-tygodniowym badaniem ze zmienną dawką, porównującym PAXIL 10 mg do 60 mg na dobę i placebo. W punkcie końcowym 51% pacjentów leczonych PAXIL było wolnych od ataków paniki w porównaniu z 32% pacjentów otrzymujących placebo.
Badanie 3 było 12-tygodniowym badaniem ze zmienną dawką, porównującym PAXIL 10 mg do 60 mg na dobę z placebo u pacjentów jednocześnie otrzymujących standaryzowaną terapię poznawczo-behawioralną. W punkcie końcowym 33% pacjentów leczonych PAXIL wykazało redukcję do 0 lub 1 napadów paniki w porównaniu do 14% pacjentów otrzymujących placebo.
W badaniach 2 i 3 średnia dawka PAXIL dla osób, które ukończyły leczenie w punkcie końcowym, wynosiła około 40 mg na dobę.
Długoterminową skuteczność PAXIL 10 mg w chP wykazano w rozszerzeniu badania 1. Pacjenci, którzy odpowiedzieli na PAXIL 20 mg podczas 10-tygodniowej fazy podwójnie ślepej próby i podczas 3-miesięcznej fazy przedłużonej podwójnie ślepej próby, zostali losowo przydzieleni do jednej z grup PAXIL 10 mg, 20 mg lub 40 mg na dobę lub placebo w 3-miesięcznej fazie zapobiegania nawrotom z podwójnie ślepą próbą. Pacjenci przydzieleni losowo do grupy PAXIL 20 mg mieli statystycznie istotnie mniejsze prawdopodobieństwo nawrotu choroby niż pacjenci otrzymujący placebo.
Analizy podgrup nie wykazały różnic w wynikach leczenia w zależności od wieku lub płci.
Fobia społeczna
Skuteczność PAXIL w leczeniu zespołu lęku społecznego (SAD) wykazano w trzech 12-tygodniowych, wieloośrodkowych, kontrolowanych placebo badaniach (Badania 1, 2 i 3) dorosłych pacjentów ambulatoryjnych z SAD (DSM-IV). W badaniach tych skuteczność PAXIL 30 mg w porównaniu z placebo oceniano na podstawie (1) odsetka osób reagujących na ) oraz (2) zmiana w stosunku do wartości wyjściowej w Skali Lęku Społecznego Liebowitza (LSAS).
Badania 1 i 2 były badaniami ze zmienną dawką, porównującym PAXIL 20 mg do 50 mg na dobę i placebo. PAXIL wykazał statystycznie istotną wyższość nad placebo zarówno pod względem kryterium odpowiedzi na poprawę CGI, jak i Skali Lęku Społecznego Liebowitza (LSAS). W badaniu 1, w przypadku pacjentów, którzy ukończyli leczenie do 12. tygodnia, 69% pacjentów leczonych PAXIL w porównaniu z 29% pacjentów otrzymujących placebo wykazała odpowiedź na poprawę CGI. W badaniu 2, odpowiedź na poprawę CGI wyniosła 77% i 42% odpowiednio dla pacjentów otrzymujących PAXIL i placebo.
Badanie 3 było 12-tygodniowym badaniem porównującym stałe dawki PAXIL 20 mg, 40 mg lub 60 mg na dobę z placebo. PAXIL 20 mg był statystycznie istotnie lepszy od placebo zarówno pod względem całkowitego wyniku LSAS, jak i kryterium odpowiedzi na poprawę CGI; istniały tendencje do wyższości nad placebo w grupach otrzymujących PAXIL 40 mg i 60 mg dawki dobowej. W badaniu tym nie było wskazań na jakąkolwiek dodatkową korzyść przy dawkach większych niż 20 mg na dobę.
Analizy podgrup na ogół nie wskazywały na różnice w wynikach leczenia w zależności od wieku, rasy lub płci.
Uogólnione zaburzenie lękowe
Skuteczność PAXIL w leczeniu zespołu lęku uogólnionego (GAD) wykazano w dwóch 8-tygodniowych, wieloośrodkowych badaniach kontrolowanych placebo (Badania 1 i 2) z udziałem dorosłych pacjentów ambulatoryjnych z GAD (DSM-IV).
Badanie 1 było 8-tygodniowym badaniem porównującym stałe dawki PAXIL 20 mg lub 40 mg na dobę z placebo. Wykazano, że obie dawki PAXIL 20 mg lub 40 mg były statystycznie istotnie lepsze niż placebo w całkowitej punktacji Skali Oceny Lęku Hamiltona (HAM-A).
W tym badaniu nie było wystarczających dowodów, aby sugerować większą korzyść ze stosowania dawki dobowej PAXIL 40 mg w porównaniu z dawką dobową 20 mg.
Badanie 2 było badaniem ze zmienną dawką porównującym PAXIL 20 mg do 50 mg na dobę i placebo. PAXIL wykazał statystycznie istotną przewagę nad placebo w całkowitym wyniku Skali Oceny Lęku Hamiltona (HAM-A).
Trzecie badanie, badanie ze zmienną dawką, porównujące PAXIL 20 mg do 50 mg na dobę z placebo, nie wykazało statystycznie istotnej wyższości PAXIL nad placebo w łącznej punktacji Hamilton Rating Scale for Anxiety (HAM-A), będącej głównym punktem końcowym.
Analizy podgrup nie wykazały różnic w wynikach leczenia w zależności od rasy lub płci. Nie było wystarczającej liczby pacjentów w podeszłym wieku, aby przeprowadzić analizy podgrup na podstawie wieku.
długoterminowym badaniu 566 pacjentów spełniających kryteria DSM-IV dla GAD, u których wystąpiła odpowiedź podczas 8-tygodniowej ostrej fazy leczenia z pojedynczą ślepą próbą z zastosowaniem PAXIL w dawce 20 mg do 50 mg na dobę, zostało losowo przydzielonych do kontynuacji leczenia PAXIL w dawce 30 mg w ich w tej samej dawce lub placebo przez okres do 24 tygodni obserwacji pod kątem nawrotu. Odpowiedź podczas fazy z pojedynczą ślepą próbą była definiowana jako spadek o ≥2 punkty w porównaniu z wartością wyjściową w skali CGI-Severity of Illness, do wyniku ≤3. Nawrót podczas fazy podwójnie ślepej próby zdefiniowano jako wzrost o ≥2 punkty w porównaniu z wartością wyjściową w skali CGI-Severity of Illness do wyniku ≥4 lub wycofanie z powodu braku skuteczności. Pacjenci kontynuujący przyjmowanie PAXIL 40 mg doświadczyli statystycznie istotnie niższego wskaźnika nawrotów w ciągu kolejnych 24 tygodni w porównaniu z pacjentami otrzymującymi placebo.
Zespołu stresu pourazowego
Skuteczność PAXIL 20 mg w leczeniu zespołu stresu pourazowego (PTSD) została wykazana w dwóch 12-tygodniowych, wieloośrodkowych badaniach kontrolowanych placebo (Badania 1 i 2) z udziałem dorosłych pacjentów ambulatoryjnych spełniających kryteria DSM-IV dla PTSD. Średni czas trwania objawów PTSD dla obu połączonych badań wynosił 13 lat (od 0,1 roku do 57 lat). Odsetek pacjentów z wtórnymi zaburzeniami lękowymi MDD lub innymi niż PTSD w połączonych 2 badaniach wyniósł odpowiednio 41% (356 z 858 pacjentów) i 40% (345 z 858 pacjentów). Wynik badania oceniano za pomocą (1) skali Clinical-Administered PTSD Scale Part 2 (CAPS-2) oraz (2) Clinical Global Impression-Global Improvement Scale (CGI-I). CAPS-2 to wielopunktowe narzędzie, które mierzy 3 aspekty PTSD z następującymi grupami objawów: ponowne doświadczanie/wtargnięcie, unikanie/odrętwienie i nadmierne pobudzenie. Dwoma pierwszorzędowymi punktami końcowymi w każdym badaniu były (1) zmiana od punktu początkowego do punktu końcowego w całkowitej punktacji CAPS-2 (17 pozycji) oraz (2) odsetek osób odpowiadających na CGI-I, gdzie osoby odpowiadające zostały zdefiniowane jako pacjenci z wynikiem 1 (bardzo poprawiona) lub 2 (znaczna poprawa).
Badanie 1 było 12-tygodniowym badaniem porównującym stałe dawki PAXIL 20 mg lub 40 mg na dobę z placebo. Wykazano, że dawki PAXIL 20 mg i 40 mg były statystycznie znamiennie lepsze niż placebo pod względem zmiany w stosunku do wartości wyjściowej dla całkowitego wyniku CAPS-2 oraz odsetka osób odpowiadających na leczenie w skali CGI-I. W tym badaniu nie było wystarczających dowodów, aby sugerować większą korzyść dla dawki dobowej 40 mg w porównaniu z dawką dobową 20 mg.
Badanie 2 było 12-tygodniowym badaniem ze zmienną dawką, porównującym PAXIL 20 mg do 50 mg na dobę z placebo. Wykazano, że PAXIL 40 mg był istotnie lepszy od placebo pod względem zmiany od wartości wyjściowej dla całkowitego wyniku CAPS-2 oraz odsetka osób odpowiadających na leczenie w skali CGI-I.
Trzecie badanie, badanie ze zmienną dawką, porównujące PAXIL 20 mg do 50 mg na dobę z placebo, wykazało statystycznie znamienną przewagę PAXIL 20 mg w porównaniu z placebo pod względem zmiany od wartości wyjściowej dla całkowitego wyniku CAPS-2, ale nie pod względem odsetka osób odpowiadających na CGI -I.
Większość pacjentów w tych badaniach stanowiły kobiety (68% kobiet: 377 z 551 pacjentów w badaniu 1 i 66% kobiet: 202 z 303 pacjentów w badaniu 2). Analizy podgrup nie wykazały różnic w wynikach leczenia w funkcji płci. Nie było wystarczającej liczby pacjentów w wieku 65 lat i starszych lub nie rasy kaukaskiej, aby przeprowadzić analizę podgrup odpowiednio na podstawie wieku lub rasy.
INFORMACJA O PACJENCIE
PAXIL® (PAX-il) (paroksetyna) tabletki i zawiesina doustna
Jakie są najważniejsze informacje, które powinienem wiedzieć o PAXIL?
PAXIL może powodować poważne skutki uboczne, w tym:
- Zwiększone ryzyko myśli lub działań samobójczych. PAXIL 10 mg i inne leki przeciwdepresyjne mogą nasilać myśli i działania samobójcze u niektórych osób w wieku 24 lat i młodszych, zwłaszcza w pierwszych kilku miesiącach leczenia lub zmiany dawki. PAXIL nie jest przeznaczony do stosowania u dzieci.
- Depresja lub inne choroby psychiczne są najważniejszymi przyczynami myśli i działań samobójczych.
Jak mogę obserwować i próbować zapobiegać myślom i działaniom samobójczym?
- Zwróć szczególną uwagę na wszelkie zmiany, zwłaszcza nagłe zmiany nastroju, zachowania, myśli lub uczuć lub jeśli pojawią się myśli lub działania samobójcze. Jest to bardzo ważne w przypadku rozpoczęcia przyjmowania leku przeciwdepresyjnego lub zmiany dawki.
- Zadzwoń natychmiast do swojego lekarza, aby zgłosić nowe lub nagłe zmiany nastroju, zachowania, myśli lub uczuć lub jeśli pojawią się myśli lub działania samobójcze.
- Utrzymuj wszystkie wizyty kontrolne u swojego lekarza zgodnie z planem. Zadzwoń do swojego lekarza w razie potrzeby między wizytami, zwłaszcza jeśli masz obawy dotyczące objawów.
Zadzwoń do swojego lekarza lub natychmiast uzyskaj pomoc medyczną w nagłych wypadkach, jeśli wystąpi którykolwiek z poniższych objawów, zwłaszcza jeśli są nowe, gorsze lub martwią Cię:
- próby popełnienia samobójstwa
- zachowywanie się agresywnie lub agresywnie
- nowa lub gorsza depresja
- uczucie pobudzenia, niepokoju, złości lub irytacji
- wzrost aktywności i mówienie więcej niż to, co jest dla Ciebie normalne
- działając na niebezpieczne impulsy
- myśli o samobójstwie lub śmierci
- nowy lub gorszy lęk lub ataki paniki
- problemy ze snem
- inne nietypowe zmiany w zachowaniu lub nastroju
Co to jest PAXIL?
PAXIL 30mg to lek na receptę stosowany u osób dorosłych w leczeniu:
- Pewien rodzaj depresji zwany dużym zaburzeniem depresyjnym (MDD)
- Zaburzenie obsesyjno-kompulsywne (OCD)
- Zaburzenia paniki (PD)
- Zaburzenia lęku społecznego (SAD)
- Uogólnione zaburzenie lękowe (GAD)
- Zespół stresu pourazowego (PTSD)
Nie należy przyjmować leku PAXIL, jeśli:
- weź inhibitor monoaminooksydazy (MAOI)
- przestałeś brać MAOI w ciągu ostatnich 14 dni
- są leczeni antybiotykiem linezolidem lub dożylnym błękitem metylenowym
- biorą pimozyd
- biorą tiorydazynę
- jesteś uczulony na paroksetynę lub którykolwiek ze składników PAXIL. Pełna lista składników PAXIL znajduje się na końcu niniejszego Przewodnika po lekach.
Zapytaj swojego lekarza lub farmaceutę, jeśli nie masz pewności, czy przyjmujesz MAOI lub jeden z tych leków, w tym antybiotyk linezolid lub dożylny błękit metylenowy.
Nie należy rozpoczynać przyjmowania MAOI przez co najmniej 14 dni po zakończeniu leczenia lekiem PAXIL.
Przed przyjęciem leku PAXIL poinformuj swojego lekarza o wszystkich swoich schorzeniach, w tym o:
- masz problemy z sercem
- masz lub miałeś problemy z krwawieniem
- mieć lub mieć w rodzinie chorobę afektywną dwubiegunową, manię lub hipomanię
- masz lub miałeś drgawki lub konwulsje
- masz jaskrę (wysokie ciśnienie w oku)
- masz niski poziom sodu we krwi
- masz problemy z kośćmi
- masz problemy z nerkami lub wątrobą
- są w ciąży lub planują zajść w ciążę. PAXIL 40 mg może zaszkodzić nienarodzonemu dziecku. Porozmawiaj z lekarzem o zagrożeniach dla nienarodzonego dziecka, jeśli pacjentka przyjmuje PAXIL w czasie ciąży. Należy natychmiast poinformować lekarza o zajściu w ciążę lub podejrzeniu ciąży podczas leczenia lekiem PAXIL.
- karmisz piersią lub planujesz karmić piersią. PAXIL przenika do mleka matki. Porozmawiaj z lekarzem o najlepszym sposobie karmienia dziecka podczas leczenia lekiem PAXIL.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe.
PAXIL i niektóre inne leki mogą wzajemnie na siebie oddziaływać, powodując możliwe poważne działania niepożądane. PAXIL 30 mg może wpływać na działanie innych leków, a inne leki mogą wpływać na działanie leku PAXIL.
Szczególnie powiedz swojemu lekarzowi, jeśli bierzesz:
- leki stosowane w leczeniu migrenowych bólów głowy zwane tryptanami
- trójpierścieniowe leki przeciwdepresyjne
- fentanyl
- lit
- tramadol
- tryptofan
- buspiron
- amfetaminy
- ziele dziurawca zwyczajnego
- leki, które mogą wpływać na krzepliwość krwi, takie jak aspiryna, niesteroidowe leki przeciwzapalne (NLPZ), warfaryna
- diuretyki
- tamoksyfen
- leki stosowane w leczeniu nastroju, lęku, zaburzeń psychotycznych lub myśli, w tym selektywny wychwyt zwrotny serotoniny (SSRI) i inhibitory wychwytu zwrotnego serotoniny i noradrenaliny (SNRI)
Zapytaj swojego lekarza, jeśli nie jesteś pewien, czy przyjmujesz którykolwiek z tych leków. Twój lekarz poinformuje Cię, czy przyjmowanie PAXIL 10 mg z innymi lekami jest bezpieczne.
Nie należy rozpoczynać ani przerywać przyjmowania innych leków podczas leczenia lekiem PAXIL bez uprzedniej konsultacji z lekarzem. Nagłe odstawienie leku PAXIL może spowodować poważne skutki uboczne. Widzieć, „Jakie są możliwe skutki uboczne PAXIL 20mg?”
Poznaj leki, które przyjmujesz. Zachowaj ich listę, aby pokazać swojemu lekarzowi i farmaceucie, gdy otrzymasz nowy lek.
Jak zażywać PAXIL?
- PAXIL należy przyjmować dokładnie zgodnie z zaleceniami. Twój lekarz może potrzebować zmienić dawkę PAXIL 30 mg, dopóki nie będzie to odpowiednia dawka dla Ciebie.
- Przyjmuj PAXIL 1 raz dziennie rano.
- PAXIL 30 mg można przyjmować z posiłkiem lub bez posiłku.
- Jeśli pacjent przyjmuje zawiesinę doustną PAXIL, przed przyjęciem należy dobrze wstrząsnąć zawiesiną.
- Jeśli zażyjesz za dużo PAXIL, zadzwoń do centrum kontroli zatruć pod numer 1-800-222-1222 lub natychmiast udaj się na pogotowie do najbliższego szpitala.
Jakie są możliwe skutki uboczne PAXIL 10mg?
PAXIL 40mg może powodować poważne skutki uboczne, w tym:
- Widzieć, „Jakie są najważniejsze informacje, które powinienem wiedzieć o PAXIL?”
- Zespół serotoninowy. Potencjalnie zagrażający życiu problem zwany zespołem serotoninowym może wystąpić podczas przyjmowania leku PAXIL 20 mg z niektórymi innymi lekami. Zobacz: „Kto nie powinien brać PAXIL?” Zadzwoń do swojego lekarza lub natychmiast udaj się do najbliższej szpitalnej izby przyjęć jeśli u pacjenta wystąpi którykolwiek z następujących objawów zespołu serotoninowego:
- podniecenie
- widzenie lub słyszenie rzeczy, które nie są prawdziwe (omamy)
- dezorientacja
- śpiączka
- szybkie bicie serca
- zmiany ciśnienia krwi
- zawroty głowy
- wyzysk
- spłukiwanie
- wysoka temperatura ciała (hipertermia)
- drżenie (drżenia), sztywność mięśni lub drganie mięśni
- utrata koordynacji
- drgawki
- nudności, wymioty, biegunka
- Problemy z oczami (jaskra zamykającego się kąta). PAXIL 10 mg może powodować rodzaj problemu z oczami zwany jaskrą zamykającego się kąta u osób z pewnymi innymi schorzeniami oczu. Możesz chcieć przejść badanie wzroku, aby sprawdzić, czy jesteś zagrożony i otrzymać leczenie zapobiegawcze, jeśli tak. Zadzwoń do swojego lekarza, jeśli masz ból oka, zmiany w widzeniu lub obrzęk lub zaczerwienienie w oku lub wokół niego.
- Interakcje leków. Przyjmowanie PAXIL 20 mg z niektórymi innymi lekami, w tym tiorydazyną i pimozydem, może zwiększać ryzyko wystąpienia poważnej choroby serca zwanej wydłużeniem odstępu QT.
- Drgawki (konwulsje).
- Epizody maniakalne. Epizody maniakalne mogą wystąpić u osób z chorobą afektywną dwubiegunową, które przyjmują PAXIL. Objawy mogą obejmować:
- znacznie zwiększona energia
- wyścigi myśli
- niezwykle wielkie pomysły
- mówisz więcej lub szybciej niż zwykle
- poważne problemy ze snem
- lekkomyślne zachowanie
- nadmierne szczęście lub drażliwość
- Zespół odstawienia. Nagłe odstawienie PAXIL 20mg może spowodować poważne skutki uboczne. Twój lekarz może chcieć powoli zmniejszać dawkę. Objawy mogą obejmować:
- mdłości
- wyzysk
- zmiany nastroju
- drażliwość i pobudzenie
- zawroty głowy
- uczucie porażenia prądem (parestezje)
- drżenie
- lęk
- dezorientacja
- ból głowy
- zmęczenie
- problemy ze snem
- hipomania
- dzwonienie w uszach (szum w uszach)
- drgawki
- Niski poziom sodu we krwi (hiponatremia). Podczas leczenia lekiem PAXIL może wystąpić niskie stężenie sodu we krwi, które może być poważne i spowodować śmierć. Osoby w podeszłym wieku i osoby przyjmujące niektóre leki mogą być bardziej narażone na niski poziom sodu we krwi. Oznaki i objawy mogą obejmować:
- ból głowy
- Trudności z koncentracją
- zmiany pamięci
- dezorientacja
- osłabienie i niestabilność stóp, które mogą prowadzić do upadków
cięższych lub bardziej nagłych przypadkach oznaki i objawy obejmują:
- widzenie lub słyszenie rzeczy, które nie są prawdziwe (omamy)
- półomdlały
- drgawki
- śpiączka
- zatrzymanie oddychania (zatrzymanie oddechu)
- Nieprawidłowe krwawienie. Przyjmowanie PAXIL z aspiryną, NLPZ lub lekami rozrzedzającymi krew może zwiększyć to ryzyko. Poinformuj swojego lekarza o wszelkich nietypowych krwawieniach lub siniakach.
- Pęknięcie kości.
Najczęstsze skutki uboczne PAXIL 10mg to:
- problemy z funkcjami seksualnymi mężczyzn i kobiet
- zaparcie
- biegunka
- suchość w ustach
- problemy ze snem
- nerwowość
- wyzysk
- ziewanie
- osłabienie (astenia)
- zmniejszony apetyt
- zawroty głowy
- infekcja
- mdłości
- senność
- drżenie (drżenie)
To nie wszystkie możliwe skutki uboczne PAXIL.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać PAXIL?
- Przechowuj tabletki PAXIL w temperaturze od 59°F do 86°F (15°C do 30°C).
- Przechowywać PAXIL 10 mg zawiesinę doustną w temperaturze 25°C lub poniżej 77°F.
Przechowuj PAXIL i wszystkie leki w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu PAXIL.
Leki są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Nie należy przyjmować leku PAXIL w stanach, na które nie został przepisany. Nie należy podawać PAXIL innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić. Możesz poprosić swojego lekarza lub farmaceutę o informacje na temat PAXIL, które są przeznaczone dla pracowników służby zdrowia.
Jakie są składniki PAXIL 30mg?
Składnik czynny: chlorowodorek paroksetyny
Nieaktywne składniki:
dwuzasadowy fosforan wapnia dwuwodny, hypromeloza, stearynian magnezu, glikole polietylenowe, polisorbat 80, glikolan sodowy skrobi, dwutlenek tytanu i 1 lub więcej z następujących: D&C czerwony nr 30 lak glinowy, D&C żółty nr 10 lak glinowy, FD&C niebieski nie 2 jezioro aluminiowe, FD&C Yellow nr 6 jezioro aluminiowe
Zawiesina doustna: kwas cytrynowy (bezwodny), żółty FD&C nr 6, aromaty, gliceryna, metyloparaben, celuloza mikrokrystaliczna i karboksymetyloceluloza sodowa, polakrylina potasowa, glikol propylenowy, propyloparaben, woda oczyszczona, sacharyna sodowa, emulsja symetykonu i cytrynian sodu (dihydrat)
Ten przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków.
