Tofranil 25mg, 50mg, 75mg Imipramine Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Tofranil i jak się go stosuje?
Tofranil 50mg jest lekiem na receptę stosowanym w leczeniu objawów depresji. Tofranil 25 mg może być stosowany samodzielnie lub z innymi lekami.
Tofranil należy do klasy leków zwanych antydepresantami, TCA.
Nie wiadomo, czy Tofranil jest bezpieczny i skuteczny u dzieci w wieku poniżej 6 lat.
Jakie są możliwe skutki uboczne Tofranil 50mg?
Tofranil może powodować poważne skutki uboczne, w tym:
- zmiany nastroju lub zachowania,
- lęk,
- atak paniki,
- problemy ze snem,
- zachowanie impulsywne,
- drażliwość,
- podniecenie,
- wrogość,
- agresja,
- niepokój,
- nadpobudliwość (psychiczna lub fizyczna),
- więcej depresji,
- myśli samobójcze,
- rozmazany obraz,
- widzenie tunelowe,
- ból lub obrzęk oka,
- widząc aureole wokół świateł,
- zawroty,
- nowy lub nasilający się ból w klatce piersiowej,
- bicie serca,
- fruwające w piersi,
- nagłe drętwienie lub osłabienie,
- problemy ze wzrokiem, mową lub równowagą,
- gorączka,
- ból gardła,
- dezorientacja,
- halucynacje,
- nietypowe myśli lub zachowanie,
- bolesne lub utrudnione oddawanie moczu,
- drgawki i
- zażółcenie skóry lub oczu (żółtaczka)
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Tofranilu to:
- mrowienie uczucie,
- słabość,
- brak koordynacji,
- suchość w ustach,
- mdłości,
- wymioty,
- zaparcie,
- biegunka,
- zmiany widzenia,
- dzwonienie w uszach,
- poprawa biustu (zarówno mężczyzn jak i kobiet),
- zmniejszony popęd płciowy,
- impotencja i
- trudności z orgazmem
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Tofranilu. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Samobójstwa i leki przeciwdepresyjne
Leki przeciwdepresyjne zwiększały w porównaniu z placebo ryzyko myśli i zachowań samobójczych (samobójstwa) u dzieci, młodzieży i młodych dorosłych w krótkoterminowych badaniach nad ciężkimi zaburzeniami depresyjnymi (MDD) i innymi zaburzeniami psychicznymi. Każdy, kto rozważa zastosowanie chlorowodorku imipraminy lub innego leku przeciwdepresyjnego u dzieci, młodzieży lub młodych dorosłych, musi zrównoważyć to ryzyko z potrzebą kliniczną. Badania krótkoterminowe nie wykazały wzrostu ryzyka samobójstw w przypadku stosowania leków przeciwdepresyjnych w porównaniu z placebo u osób dorosłych w wieku powyżej 24 lat; wystąpiło zmniejszenie ryzyka w przypadku stosowania leków przeciwdepresyjnych w porównaniu z placebo u osób dorosłych w wieku 65 lat i starszych. Depresja i niektóre inne zaburzenia psychiczne same w sobie wiążą się ze wzrostem ryzyka samobójstwa. Pacjenci w każdym wieku, którzy rozpoczynają leczenie lekami przeciwdepresyjnymi, powinni być odpowiednio monitorowani i ściśle obserwowani pod kątem pogorszenia stanu klinicznego, skłonności samobójczych lub nietypowych zmian w zachowaniu. Rodziny i opiekunowie powinni być poinformowani o potrzebie ścisłej obserwacji i komunikacji z lekarzem. Chlorowodorek imipraminy nie jest zatwierdzony do stosowania u dzieci (patrz OSTRZEŻENIA Pogorszenie stanu klinicznego i ryzyko samobójstwa; ŚRODKI OSTROŻNOŚCI Informacje dla Pacjentów; oraz ŚRODKI OSTROŻNOŚCI , zastosowanie pediatryczne).
OPIS
Tofranil™ jest dostarczany w postaci tabletek do podawania doustnego.
Tofranil 75 mg, chlorowodorek imipraminy USP, oryginalny trójpierścieniowy lek przeciwdepresyjny, należy do grupy związków dibenzazepinowych. Jest on oznaczony jako monochlorowodorek 5-3-(dimetyloamino)propylo-10,11-dihydro-5Hdibenz[b,f]-azepiny. Jego wzór strukturalny to:
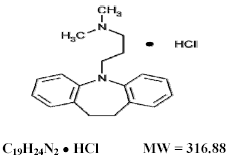
Chlorowodorek imipraminy USP jest białym lub prawie białym, bezwonnym lub praktycznie bezwonnym krystalicznym proszkiem. Jest dobrze rozpuszczalny w wodzie i alkoholu, rozpuszczalny w acetonie, nierozpuszczalny w eterze i benzenie.
Nieaktywne składniki
Fosforan wapnia, związki celulozy, dokuzan sodu, tlenki żelaza, stearynian magnezu, glikol polietylenowy, powidon, glikolan sodowy skrobi, sacharoza, talk i dwutlenek tytanu.
WSKAZANIA
Depresja
Do łagodzenia objawów depresji. Depresja endogenna jest bardziej podatna na złagodzenie niż inne stany depresyjne. Może być potrzebny od jednego do trzech tygodni leczenia, zanim pojawią się optymalne efekty terapeutyczne.
Moczenie dziecięce
Może być przydatny jako doraźna terapia wspomagająca w zmniejszaniu moczenia u dzieci w wieku 6 lat i starszych, po wykluczeniu możliwych przyczyn organicznych odpowiednimi testami. U pacjentów z objawami częstości i parcia naglącego w ciągu dnia badanie powinno obejmować cystouretrografię mikcji i cystoskopię, jeśli to konieczne. Skuteczność leczenia może się zmniejszyć przy dalszym podawaniu leku.
DAWKOWANIE I SPOSÓB PODAWANIA
Depresja
Niższe dawki są zalecane dla pacjentów w podeszłym wieku i młodzieży. Niższe dawki zaleca się również pacjentom ambulatoryjnym w porównaniu z pacjentami hospitalizowanymi, którzy będą pod ścisłym nadzorem. Dawkowanie należy rozpocząć od niskiego poziomu i stopniowo zwiększać, uważnie obserwując odpowiedź kliniczną i wszelkie oznaki nietolerancji. Po remisji mogą być wymagane leki podtrzymujące przez dłuższy czas, w najniższej dawce, która utrzyma remisję.
Zwykła dawka dla dorosłych
Pacjenci hospitalizowani
Początkowo 100 mg/dobę w dawkach podzielonych stopniowo zwiększano do 200 mg/dobę w razie potrzeby. Jeśli nie ma odpowiedzi po dwóch tygodniach, zwiększyć do 250 do 300 mg/dzień.
Ambulatoryjna
Początkowo 75 mg/dzień wzrosła do 150 mg/dzień. Nie zaleca się dawek powyżej 200 mg/dobę. Podtrzymanie, 50 do 150 mg/dzień.
Pacjenci młodociani i geriatryczni
Początkowo od 30 do 40 mg/dzień; na ogół nie jest konieczne przekraczanie 100 mg/dzień.
Moczenie dziecięce
Początkowo u dzieci w wieku 6 lat i starszych należy wypróbować dawkę doustną 25 mg/dobę. Lek należy podać godzinę przed snem. Jeśli zadowalająca odpowiedź nie wystąpi w ciągu tygodnia, należy zwiększyć dawkę do 50 mg na noc u dzieci w wieku poniżej 12 lat; dzieci powyżej 12. roku życia mogą otrzymywać do 75 mg na dobę. Dzienna dawka większa niż 75 mg nie zwiększa skuteczności i ma tendencję do zwiększania skutków ubocznych. Dowody wskazują, że u osób moczących się w nocy lek jest bardziej skuteczny podawany wcześniej iw podzielonych dawkach, tj. 25 mg po południu, powtarzany przed snem. Należy rozważyć wprowadzenie okresu bez leku po odpowiednim badaniu terapeutycznym z pozytywną odpowiedzią. Dawkowanie należy zmniejszać stopniowo, a nie nagle odstawiać; może to zmniejszyć skłonność do nawrotów. Dzieci, które nawracają po odstawieniu leku, nie zawsze reagują na kolejny cykl leczenia.
Nie należy przekraczać dawki 2,5 mg/kg/dobę. Zmiany w zapisie EKG o nieznanym znaczeniu były zgłaszane u pacjentów pediatrycznych przy dawkach dwukrotnie większych.
Nie ustalono bezpieczeństwa i skuteczności Tofranilu jako tymczasowej terapii wspomagającej w przypadku moczenia nocnego u dzieci w wieku poniżej 6 lat.
JAK DOSTARCZONE
Trzy moce Tofranil ™ (chlorowodorek imipraminy USP) są dostępne w następujący sposób:
– trójkątna, dwuwypukła, koralowo-czerwono-brązowa tabletka powlekana cukrem, z nadrukiem z jednej strony i cyfrą „10” w kolorze czarnym.
Butelki 30 NDC 0406-9920-03 Butelki 100 NDC 0406-9920-01
– okrągła, dwuwypukła, koralowo-czerwono-brązowa tabletka powlekana cukrem, z czarnym nadrukiem z jednej strony i „25” z drugiej strony.
Butelki 30 NDC 0406-9921-03 Butelki 100 NDC 0406-9921-01
– okrągła, dwuwypukła, koralowo-czerwono-brązowa tabletka powlekana cukrem, z czarnym nadrukiem z jednej strony i „50” z drugiej strony.
Butelki 30 NDC 0406-9922-03 Butelki 100 NDC 0406-9922-01
Przechowywać w temperaturze 20° do 25°C (68° do 77°F) [patrz Kontrolowana temperatura pokojowa USP].
Dozować w szczelnym pojemniku (USP) z zamknięciem zabezpieczającym przed dostępem dzieci.
Producent: Patheon Inc. Whitby, Ontario, Kanada, L1N 5Z5. Aktualizacja: kwiecień 2017
SKUTKI UBOCZNE
Notatka – Chociaż poniższa lista zawiera kilka działań niepożądanych, które nie zostały zgłoszone w przypadku tego konkretnego leku, podobieństwa farmakologiczne między trójpierścieniowymi lekami przeciwdepresyjnymi wymagają rozważenia każdej z reakcji podczas podawania Tofranilu 25 mg.
Układ sercowo-naczyniowy: Niedociśnienie ortostatyczne, nadciśnienie, tachykardia, kołatanie serca, zawał mięśnia sercowego, zaburzenia rytmu serca, blok serca, zmiany EKG, wystąpienie zastoinowej niewydolności serca, udar.
Psychiatryczny: stany splątania (zwłaszcza u osób starszych) z omamami, dezorientacją, urojeniami; niepokój, niepokój, pobudzenie; bezsenność i koszmary; hipomania; zaostrzenie psychozy.
Neurologiczna: drętwienie, mrowienie, parestezje kończyn; brak koordynacji, ataksja, drżenie; Neuropatia obwodowa; objawy pozapiramidowe; drgawki, zmiany wzorców EEG; szum w uszach.
Antycholinergiczny: Suchość w ustach i, rzadko, towarzyszące podjęzykowe zapalenie węzłów chłonnych; niewyraźne widzenie, zaburzenia akomodacji, rozszerzenie źrenic; zaparcie, porażenna niedrożność jelit; zatrzymanie moczu, opóźnione oddawanie moczu, rozszerzenie dróg moczowych.
Uczulony: Wysypka skórna, wybroczyny, pokrzywka, swędzenie, nadwrażliwość na światło; obrzęk (ogólny lub twarzy i języka); gorączka lekowa; nadwrażliwość krzyżowa z dezypraminą.
Hematologiczny: Depresja szpiku kostnego, w tym agranulocytoza; eozynofilia; plamica; małopłytkowość.
Przewód pokarmowy: Nudności i wymioty, anoreksja, zaburzenia w nadbrzuszu, biegunka; specyficzny smak, zapalenie jamy ustnej, skurcze brzucha, czarny język.
Wewnątrzwydzielniczy: Ginekomastia u mężczyzn; powiększenie piersi i mlekotok u kobiet; zwiększone lub zmniejszone libido, impotencja; obrzęk jąder; podwyższenie lub obniżenie poziomu cukru we krwi; zespół nieprawidłowego wydzielania hormonu antydiuretycznego (ADH).
Inny: Żółtaczka (symulacja obturacyjna); zmieniona czynność wątroby; przyrost lub utrata masy ciała; pot; płukanie; częstotliwość oddawania moczu; senność, zawroty głowy, osłabienie i zmęczenie; ból głowy; obrzęk ślinianki przyusznej; łysienie; skłonność do upadku.
Objawy odstawienia: Chociaż nie wskazuje to na uzależnienie, nagłe przerwanie leczenia po długotrwałej terapii może wywołać nudności, ból głowy i złe samopoczucie.
Notatka – U dzieci z moczeniem moczowym leczonych tofranilem 75 mg najczęstszymi działaniami niepożądanymi były nerwowość, zaburzenia snu, zmęczenie i łagodne zaburzenia żołądkowo-jelitowe. Zwykle ustępują one podczas dalszego podawania leku lub zmniejszania dawki. Inne zgłaszane reakcje to zaparcia, drgawki, lęk, niestabilność emocjonalna, omdlenia i zapaść. Należy wziąć pod uwagę wszystkie działania niepożądane zgłaszane przy stosowaniu przez osoby dorosłe.
INTERAKCJE Z LEKAMI
Leki metabolizowane przez P450 2D6
Aktywność biochemiczna leku metabolizującego izoenzym cytochromu P450 2D6 (hydroksylaza debrizochinowa) jest zmniejszona w podgrupie populacji rasy kaukaskiej (około 7% do 10% osób rasy kaukaskiej to tak zwani „słabo metabolizujący”); wiarygodne szacunki częstości występowania zmniejszonej aktywności izoenzymu 2D6 P450 w populacjach azjatyckich, afrykańskich i innych nie są jeszcze dostępne. Osoby o słabym metabolizmie mają wyższe niż oczekiwane stężenia trójpierścieniowych leków przeciwdepresyjnych (TCA) w osoczu, gdy są podawane w zwykłych dawkach. W zależności od frakcji leku metabolizowanego przez P450 2D6, wzrost stężenia w osoczu może być niewielki lub dość duży (8-krotny wzrost AUC TCA w osoczu).
Ponadto niektóre leki hamują aktywność tego izoenzymu i sprawiają, że osoby normalnie metabolizujące przypominają osoby słabo metabolizujące. Osoba, która jest stabilna na danej dawce TCA, może nagle stać się toksyczne po podaniu jednego z tych leków hamujących w ramach terapii skojarzonej. Leki hamujące cytochrom P450 2D6 obejmują niektóre, które nie są metabolizowane przez enzym (chinidyna; cymetydyna) i wiele, które są substratami dla P450 2D6 (wiele innych leków przeciwdepresyjnych, fenotiazyn oraz leków przeciwarytmicznych typu 1C, propafenonu i flekainidu). Chociaż wszystkie selektywne inhibitory wychwytu zwrotnego serotoniny (SSRI), np. fluoksetyna, sertralina i paroksetyna, hamują P450 2D6, ich stopień hamowania może się różnić. Zakres, w jakim interakcje SSRI-TCA mogą stwarzać problemy kliniczne, będzie zależał od stopnia hamowania i farmakokinetyki zaangażowanych SSRI. Niemniej jednak wskazana jest ostrożność przy jednoczesnym podawaniu TCA z którymkolwiek z SSRI, a także przy przechodzeniu z jednej klasy do drugiej. Szczególnie ważne, biorąc pod uwagę długi okres półtrwania macierzystego i aktywnego metabolitu (może być konieczne co najmniej 5 tygodni), musi upłynąć dostatecznie dużo czasu przed rozpoczęciem leczenia TCA u pacjenta odstawionego od fluoksetyny.
Jednoczesne stosowanie trójpierścieniowych leków przeciwdepresyjnych z lekami, które mogą hamować cytochrom P450 2D6, może wymagać mniejszych dawek niż zwykle przepisywane dla trójpierścieniowych leków przeciwdepresyjnych lub innych leków. Ponadto, ilekroć jeden z tych innych leków zostanie wycofany z terapii skojarzonej, może być wymagana zwiększona dawka trójpierścieniowych leków przeciwdepresyjnych. Pożądane jest monitorowanie poziomu TCA w osoczu za każdym razem, gdy TCA będzie podawany jednocześnie z innym lekiem, o którym wiadomo, że jest inhibitorem P450 2D6.
Stężenie imipraminy w osoczu może wzrosnąć, gdy lek jest podawany jednocześnie z inhibitorami enzymów wątrobowych (np. cymetydyna, fluoksetyna) i zmniejszyć się przy jednoczesnym podawaniu z induktorami enzymów wątrobowych (np. barbiturany, fenytoina), w związku z czym może być dostosowana dawka imipraminy. być niezbędnym.
okazjonalnie wrażliwych pacjentów lub u osób otrzymujących dodatkowo leki przeciwcholinergiczne (w tym leki przeciwparkinsonowskie) działanie podobne do atropiny może być bardziej nasilone (np. porażenna niedrożność jelit). W przypadku jednoczesnego podawania chlorowodorku imipraminy z lekami antycholinergicznymi konieczne jest ścisłe nadzorowanie i staranne dostosowywanie dawki.
Unikaj stosowania preparatów, takich jak leki zmniejszające przekrwienie i środki miejscowo znieczulające, które zawierają jakąkolwiek aminę sympatykomimetyczną (np. epinefrynę, norepinefrynę), ponieważ istnieją doniesienia, że trójpierścieniowe leki przeciwdepresyjne mogą nasilać działanie katecholamin.
Należy zachować ostrożność podczas stosowania imipraminy chlorowodorku z lekami obniżającymi ciśnienie krwi. Chlorowodorek imipraminy może nasilać działanie leków hamujących ośrodkowy układ nerwowy.
Należy ostrzec pacjentów, że chlorowodorek imipraminy może nasilać depresyjne działanie alkoholu na ośrodkowy układ nerwowy (patrz OSTRZEŻENIA ).
OSTRZEŻENIA
Pogorszenie stanu klinicznego i ryzyko samobójstwa
Pacjenci z ciężkimi zaburzeniami depresyjnymi (MDD), zarówno dorośli, jak i pediatryczni, mogą doświadczać nasilenia depresji i/lub pojawienia się myśli i zachowań samobójczych (samobójstwa) lub nietypowych zmian w zachowaniu, niezależnie od tego, czy przyjmują leki przeciwdepresyjne, a to ryzyko może utrzymywać się aż do wystąpienia znacznej remisji. Samobójstwo jest znanym ryzykiem depresji i niektórych innych zaburzeń psychicznych, a same te zaburzenia są najsilniejszymi predyktorami samobójstwa. Od dawna istnieje jednak obawa, że leki przeciwdepresyjne mogą odgrywać rolę w wywoływaniu nasilenia depresji i pojawianiu się myśli samobójczych u niektórych pacjentów we wczesnych fazach leczenia. Zbiorcze analizy krótkoterminowych, kontrolowanych placebo badań leków przeciwdepresyjnych (SSRI i innych) wykazały, że leki te zwiększają ryzyko myśli i zachowań samobójczych (samobójstwa) u dzieci, młodzieży i młodych dorosłych (w wieku od 18 do 24 lat) z ciężką depresją zaburzenia (MDD) i inne zaburzenia psychiczne. Badania krótkoterminowe nie wykazały wzrostu ryzyka samobójstw w przypadku stosowania leków przeciwdepresyjnych w porównaniu z placebo u osób dorosłych w wieku powyżej 24 lat; u osób dorosłych w wieku 65 lat i starszych odnotowano zmniejszenie liczby przyjmowanych leków przeciwdepresyjnych w porównaniu z placebo.
Połączone analizy badań kontrolowanych placebo u dzieci i młodzieży z MDD, zaburzeniami obsesyjno-kompulsywnymi (OCD) lub innymi zaburzeniami psychicznymi obejmowały łącznie 24 krótkoterminowe badania 9 leków przeciwdepresyjnych z udziałem ponad 4400 pacjentów. Zbiorcze analizy badań kontrolowanych placebo u dorosłych z MDD lub innymi zaburzeniami psychicznymi obejmowały łącznie 295 krótkoterminowych badań (mediana czasu trwania wynosząca 2 miesiące) 11 leków przeciwdepresyjnych z udziałem ponad 77 000 pacjentów. Istniało znaczne zróżnicowanie ryzyka samobójstwa wśród leków, ale tendencja do wzrostu u młodszych pacjentów w przypadku prawie wszystkich badanych leków. Istniały różnice w bezwzględnym ryzyku samobójstwa w różnych wskazaniach, z największą częstością występowania MDD. Różnice ryzyka (lek vs placebo) były jednak stosunkowo stabilne w obrębie warstw wiekowych i we wskazaniach. Te różnice w ryzyku (różnica między lekami a placebo w liczbie przypadków samobójstw na 1000 leczonych pacjentów) przedstawiono w Tabeli 1.
żadnym z badań pediatrycznych nie doszło do samobójstw. W badaniach z udziałem dorosłych zdarzały się samobójstwa, ale liczba ta nie była wystarczająca, aby wyciągnąć jakiekolwiek wnioski na temat wpływu leku na samobójstwo.
Nie wiadomo, czy ryzyko samobójstwa rozciąga się na długotrwałe używanie, tj. dłużej niż kilka miesięcy. Jednak istnieją dowody z kontrolowanych placebo badań podtrzymujących u dorosłych z depresją, że stosowanie leków przeciwdepresyjnych może opóźnić nawrót depresji.
Wszyscy pacjenci leczeni lekami przeciwdepresyjnymi w jakimkolwiek wskazaniu powinni być odpowiednio monitorowani i obserwowani pod kątem pogorszenia stanu klinicznego, skłonności samobójczych i nietypowych zmian w zachowaniu, szczególnie w ciągu pierwszych kilku miesięcy terapii lekowej lub w czasie zmiany dawki, albo zwiększa się lub maleje.
Następujące objawy: lęk, pobudzenie, ataki paniki, bezsenność, drażliwość, wrogość, agresywność, impulsywność, akatyzję (niepokój psychoruchowy), hipomanię i manię zgłaszano również u dorosłych i dzieci leczonych lekami przeciwdepresyjnymi z powodu dużych zaburzeń depresyjnych. co do innych wskazań, zarówno psychiatrycznych, jak i niepsychiatrycznych. Chociaż nie ustalono związku przyczynowo-skutkowego między pojawieniem się takich objawów a nasileniem depresji i/lub pojawieniem się impulsów samobójczych, istnieje obawa, że takie objawy mogą być prekursorem pojawiania się samobójstw.
Należy rozważyć zmianę schematu leczenia, w tym ewentualnie odstawienie leku, u pacjentów, u których depresja jest stale nasilona lub u których pojawiają się myśli samobójcze lub objawy, które mogą być prekursorami nasilenia depresji lub myśli samobójczych, zwłaszcza jeśli objawy te są ciężkie, nagłe na początku lub nie były częścią objawów występujących u pacjenta.
Rodziny i opiekunowie pacjentów leczonych lekami przeciwdepresyjnymi z powodu dużych zaburzeń depresyjnych lub innych wskazań, zarówno psychiatrycznych, jak i niepsychiatrycznych, powinni być ostrzeżeni o konieczności monitorowania pacjentów pod kątem pojawienia się pobudzenia, drażliwości, nietypowych zmian w zachowaniu i innych objawów opisanych powyżej , a także pojawienia się samobójstw i natychmiastowego zgłaszania takich objawów świadczeniodawcom. Taki monitoring powinien obejmować codzienną obserwację rodzin i opiekunów. Recepty na chlorowodorek imipraminy należy wypisać na najmniejszą ilość tabletek, zgodnie z dobrym postępowaniem z pacjentem, aby zmniejszyć ryzyko przedawkowania.
Badanie przesiewowe pacjentów pod kątem choroby afektywnej dwubiegunowej
Poważny epizod depresyjny może być początkowym objawem choroby afektywnej dwubiegunowej. Powszechnie uważa się (chociaż nie zostało to potwierdzone w badaniach kontrolowanych), że leczenie takiego epizodu samym lekiem przeciwdepresyjnym może zwiększyć prawdopodobieństwo wystąpienia epizodu mieszanego/maniakalnego u pacjentów z ryzykiem choroby afektywnej dwubiegunowej. Nie wiadomo, czy którykolwiek z objawów opisanych powyżej reprezentuje taką konwersję. Jednak przed rozpoczęciem leczenia lekiem przeciwdepresyjnym pacjenci z objawami depresji powinni zostać odpowiednio przebadani w celu ustalenia, czy są oni zagrożeni chorobą afektywną dwubiegunową; takie badania przesiewowe powinny obejmować szczegółowy wywiad psychiatryczny, w tym wywiad rodzinny dotyczący samobójstw, choroby afektywnej dwubiegunowej i depresji. Należy zauważyć, że chlorowodorek imipraminy nie jest zatwierdzony do stosowania w leczeniu depresji dwubiegunowej.
Jaskra zamykającego się kąta
Rozszerzenie źrenicy, które występuje po zastosowaniu wielu leków przeciwdepresyjnych, w tym Tofranilu, może wywołać atak zamknięcia kąta u pacjenta z anatomicznie wąskim kątem, który nie ma drożnej tęczówki.
Dzieci
W dzieciństwie nie należy przekraczać dawki 2,5 mg/kg/dobę Tofranilu 25 mg. Zmiany w zapisie EKG o nieznanym znaczeniu były zgłaszane u pacjentów pediatrycznych przy dawkach dwukrotnie większych.
Należy zachować szczególną ostrożność przy podawaniu tego leku: pacjentom z chorobami układu krążenia ze względu na możliwość wystąpienia zaburzeń przewodzenia, zaburzeń rytmu serca, zastoinowej niewydolności serca, zawału mięśnia sercowego, udarów i tachykardii. Pacjenci ci wymagają nadzoru kardiologicznego przy wszystkich poziomach dawkowania leku;
pacjenci z historią zatrzymania moczu lub jaskrą z wąskim kątem w wywiadzie ze względu na właściwości antycholinergiczne leku; pacjenci z nadczynnością tarczycy lub przyjmujący leki na tarczycę ze względu na możliwość wystąpienia toksyczności sercowo-naczyniowej;
pacjenci z zaburzeniami napadowymi w wywiadzie, ponieważ wykazano, że lek ten obniża próg drgawkowy;
pacjenci otrzymujący guanetydynę, klonidynę lub podobne środki, ponieważ Tofranil może blokować działanie farmakologiczne tych leków;
pacjentów otrzymujących chlorowodorek metylofenidatu. Ponieważ chlorowodorek metylofenidatu może hamować metabolizm tofranilu 75 mg, może być konieczne zmniejszenie dawki chlorowodorku imipraminy podczas jednoczesnego podawania chlorowodorku metylofenidatu.
Tofranil może nasilać depresyjne działanie alkoholu na OUN. Dlatego należy pamiętać, że niebezpieczeństwa związane z próbą samobójczą lub przypadkowym przedawkowaniem leku mogą być zwiększone u pacjenta spożywającego nadmierne ilości alkoholu (patrz ŚRODKI OSTROŻNOŚCI ).
Ponieważ Tofranil może zaburzać zdolności umysłowe i/lub fizyczne wymagane do wykonywania potencjalnie niebezpiecznych zadań, takich jak prowadzenie samochodu lub maszyn, należy odpowiednio ostrzec pacjenta.
ŚRODKI OSTROŻNOŚCI
Ogólny
Rejestrację EKG należy wykonać przed rozpoczęciem podawania większych niż zwykle dawek tofranilu, a następnie w odpowiednich odstępach czasu, aż do osiągnięcia stanu stacjonarnego. (Pacjenci z jakimikolwiek objawami choroby sercowo-naczyniowej wymagają nadzoru kardiologicznego przy wszystkich poziomach dawkowania leku. Patrz OSTRZEŻENIA .) Pacjenci w podeszłym wieku i pacjenci z chorobami serca lub wcześniejszymi chorobami serca są narażeni na szczególne ryzyko rozwoju nieprawidłowości serca związanych ze stosowaniem Tofranilu.
Należy pamiętać, że prawdopodobieństwo samobójstwa u pacjentów z ciężką depresją jest nieodłączną cechą choroby i może utrzymywać się do czasu wystąpienia znacznej remisji. Tacy pacjenci powinni być uważnie nadzorowani we wczesnej fazie leczenia tofranilem 75 mg i mogą wymagać hospitalizacji. Recepty powinny być wypisane na jak najmniejszą możliwą kwotę. Mogą wystąpić epizody hipomaniakalne lub maniakalne, szczególnie u pacjentów z zaburzeniami cyklicznymi. Takie reakcje mogą wymagać odstawienia leku. W razie potrzeby, Tofranil 75 mg można wznowić w niższej dawce, gdy te epizody zostaną złagodzone.
W opanowaniu takich epizodów pomocne może być podanie środka uspokajającego.
U pacjentów ze schizofrenią można czasami zaobserwować aktywację psychozy, co może wymagać zmniejszenia dawki i dodania fenotiazyny.
Jednoczesne podawanie Tofranilu 50 mg z terapią elektrowstrząsami może zwiększyć ryzyko; takie leczenie powinno być ograniczone do tych pacjentów, dla których jest niezbędne, ponieważ doświadczenie kliniczne jest ograniczone.
Pacjenci przyjmujący chlorowodorek imipraminy powinni unikać nadmiernej ekspozycji na światło słoneczne, ponieważ istnieją doniesienia o fotouczulaniu.
Podczas stosowania chlorowodorku imipraminy zgłaszano zarówno podwyższenie, jak i obniżenie poziomu cukru we krwi.
Chlorowodorek imipraminy należy stosować ostrożnie u pacjentów z istotnymi zaburzeniami czynności nerek lub wątroby.
U pacjentów, u których podczas leczenia chlorowodorkiem imipraminy wystąpi gorączka i ból gardła, należy wykonać badanie leukocytów i rozmazu krwi. Chlorowodorek imipraminy należy odstawić, jeśli istnieją dowody na patologiczną depresję neutrofili.
Przed planowanym zabiegiem chirurgicznym należy odstawić imipraminę chlorowodorek tak długo, jak pozwala na to sytuacja kliniczna.
Informacje dla pacjentów
Lekarze przepisujący lek lub inni pracownicy służby zdrowia powinni informować pacjentów, ich rodziny i ich opiekunów o korzyściach i zagrożeniach związanych z leczeniem chlorowodorkiem imipraminy oraz powinni doradzić im właściwe jego stosowanie. Pacjent Przewodnik po lekach o „Lekach przeciwdepresyjnych, depresji i innych poważnych chorobach psychicznych oraz myślach lub działaniach samobójczych” jest dostępny dla chlorowodorku imipraminy. Lekarz lub pracownik służby zdrowia powinien poinstruować pacjentów, ich rodziny i ich opiekunów, aby przeczytali Przewodnik po lekach i powinni pomóc im w zrozumieniu jego treści. Pacjenci powinni mieć możliwość omówienia treści Przewodnika po lekach i uzyskania odpowiedzi na wszelkie pytania, jakie mogą mieć. Pełny tekst Przewodnika po lekach jest przedrukowany na końcu tego dokumentu.
Pacjentów należy poinformować o następujących kwestiach i poprosić o powiadomienie lekarza przepisującego lek, jeśli wystąpią one podczas przyjmowania imipraminy chlorowodorku.
Należy poinformować pacjentów, że przyjmowanie leku Tofranil może powodować łagodne rozszerzenie źrenic, które u osób podatnych może prowadzić do epizodu jaskry zamykającego się kąta. Wcześniej istniejąca jaskra jest prawie zawsze jaskrą otwartego kąta, ponieważ jaskra zamkniętego kąta, po zdiagnozowaniu, może być ostatecznie leczona za pomocą irydektomii. Jaskra otwartego kąta nie jest czynnikiem ryzyka jaskry zamykającego się kąta. Pacjenci mogą chcieć zostać przebadani w celu określenia, czy są podatni na zamknięcie kąta i przejść zabieg profilaktyczny (np. irydektomię), jeśli są podatni.
Pogorszenie stanu klinicznego i ryzyko samobójstwa
Należy zachęcać pacjentów, ich rodziny i ich opiekunów do wyczulenia na pojawienie się lęku, pobudzenia, ataków paniki, bezsenności, drażliwości, wrogości, agresywności, impulsywności, akatyzji (niepokoju psychoruchowego), hipomanii, manii i innych nietypowych zmian w zachowaniu , nasilenie depresji i myśli samobójcze, szczególnie na początku leczenia przeciwdepresyjnego oraz przy zwiększaniu lub zmniejszaniu dawki. Rodzinom i opiekunom pacjentów należy zalecić, aby codziennie zwracali uwagę na pojawienie się takich objawów, ponieważ zmiany mogą być nagłe. Takie objawy należy zgłaszać lekarzowi lub pracownikowi służby zdrowia, zwłaszcza jeśli są one ciężkie, mają nagły początek lub nie były częścią objawów występujących u pacjenta. Takie objawy mogą wiązać się ze zwiększonym ryzykiem myśli i zachowań samobójczych i wskazują na potrzebę bardzo ścisłego monitorowania i ewentualnie zmian w leczeniu.
Ciąża
Badania reprodukcji na zwierzętach przyniosły niejednoznaczne wyniki (patrz także Farmakologia zwierząt ).
Nie przeprowadzono dobrze kontrolowanych badań z udziałem kobiet w ciąży w celu określenia wpływu Tofranilu na płód. Istnieją jednak doniesienia kliniczne o wadach wrodzonych związanych ze stosowaniem leku. Chociaż nie można było ustalić związku przyczynowego między tymi działaniami a lekiem, nie można wykluczyć ryzyka dla płodu w wyniku spożycia tofranilu przez matkę. Dlatego Tofranil powinien być stosowany u kobiet, które są lub mogą zajść w ciążę tylko wtedy, gdy stan kliniczny wyraźnie uzasadnia potencjalne ryzyko dla płodu.
Matki karmiące
Ograniczone dane sugerują, że tofranil 75 mg prawdopodobnie przenika do mleka ludzkiego. Zasadniczo kobieta przyjmująca lek nie powinna karmić piersią, ponieważ istnieje możliwość, że lek może przenikać do mleka matki i być szkodliwy dla dziecka.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność w populacji pediatrycznej innej niż dzieci i młodzież z moczeniem nocnym nie zostały ustalone (patrz PUDEŁKO OSTRZEŻENIE oraz OSTRZEŻENIA , Pogorszenie stanu klinicznego i ryzyko samobójstwa ). Każdy, kto rozważa zastosowanie chlorowodorku imipraminy u dzieci lub młodzieży, musi zrównoważyć potencjalne ryzyko z potrzebą kliniczną.
Bezpieczeństwo i skuteczność leku jako tymczasowego leczenia wspomagającego w moczeniu nocnym u dzieci w wieku poniżej 6 lat nie zostały ustalone.
Nie ustalono bezpieczeństwa leku do długotrwałego, przewlekłego stosowania jako terapii wspomagającej w przypadku moczenia nocnego u dzieci w wieku 6 lat lub starszych; należy rozważyć wprowadzenie okresu wolnego od leków po odpowiednim badaniu terapeutycznym z pozytywną odpowiedzią.
W dzieciństwie nie należy przekraczać dawki 2,5 mg/kg/dobę. Zmiany w zapisie EKG o nieznanym znaczeniu były zgłaszane u pacjentów pediatrycznych przy dawkach dwukrotnie większych.
Zastosowanie geriatryczne
piśmiennictwie były cztery dobrze kontrolowane, randomizowane, podwójnie zaślepione, równoległe badania kliniczne z porównaniem grup przeprowadzonych z Tofranilem 50 mg w populacji osób starszych. Do tych badań włączono łącznie 651 osób. Badania te nie dały porównania z młodszymi osobami. Nie stwierdzono dodatkowych działań niepożądanych u osób starszych.
Badania kliniczne Tofranilu 75 mg w pierwotnym wniosku nie obejmowały wystarczającej liczby osób w wieku 65 lat i starszych, aby ustalić, czy reagują inaczej niż osoby młodsze. Doświadczenie kliniczne po wprowadzeniu do obrotu nie wykazało różnic w odpowiedziach między osobami w podeszłym wieku i młodszymi. Ogólnie rzecz biorąc, dobór dawki u osób w podeszłym wieku powinien być ostrożny, zwykle zaczynając od dolnej granicy zakresu dawkowania, co odzwierciedla większą częstość pogorszenia czynności wątroby, nerek lub serca oraz współistniejących chorób lub innych leków.
(Zobacz też DAWKOWANIE I SPOSÓB PODAWANIA , Dorastający oraz Pacjenci geriatryczni .)
(Zobacz też ŚRODKI OSTROŻNOŚCI , Ogólny. )
PRZEDAWKOWAĆ
Zgony mogą wystąpić z powodu przedawkowania tej klasy leków. Przyjmowanie wielu leków (w tym alkoholu) jest powszechne w celowym przedawkowaniu trójpierścieniowych leków. Ponieważ postępowanie jest złożone i zmienne, zaleca się, aby lekarz skontaktował się z centrum kontroli zatruć w celu uzyskania aktualnych informacji na temat leczenia. Oznaki i objawy zatrucia rozwijają się szybko po przedawkowaniu tricyklicznym. Dlatego monitorowanie szpitala jest wymagane tak szybko, jak to możliwe.
Zgłaszano, że dzieci są bardziej wrażliwe niż dorośli na ostre przedawkowanie chlorowodorku imipraminy. Ostre przedawkowanie jakiejkolwiek ilości, zwłaszcza u niemowląt lub małych dzieci, należy uznać za poważne i potencjalnie śmiertelne.
Manifestacje
Mogą one mieć różne nasilenie w zależności od takich czynników, jak ilość wchłoniętego leku, wiek pacjenta i odstęp między przyjęciem leku a rozpoczęciem leczenia. Krytyczne objawy przedawkowania obejmują zaburzenia rytmu serca, ciężkie niedociśnienie, drgawki i depresję ośrodkowego układu nerwowego, w tym śpiączkę. Zmiany w elektrokardiogramie, szczególnie w osi lub szerokości QRS, są klinicznie istotnymi wskaźnikami toksyczności trójpierścieniowej.
Inne objawy ze strony OUN mogą obejmować senność, otępienie, ataksję, niepokój, pobudzenie, nadpobudliwość odruchów, sztywność mięśni, ruchy atetoidalne i pląsawicowe.
Nieprawidłowości serca mogą obejmować tachykardię i oznaki niewydolności zastoinowej. Mogą również występować depresja oddechowa, sinica, wstrząs, wymioty, nadmierna gorączka, rozszerzenie źrenic i obfite pocenie.
Kierownictwo
Wykonaj EKG i natychmiast rozpocznij monitorowanie pracy serca. Chronić drogi oddechowe pacjenta, założyć linię dożylną i rozpocząć odkażanie żołądka. Niezbędna jest co najmniej 6 godzinna obserwacja z monitorowaniem pracy serca i obserwacją objawów ośrodkowego układu nerwowego lub depresji oddechowej, niedociśnienia, zaburzeń rytmu serca i/lub blokad przewodzenia oraz drgawek. Jeśli w tym okresie wystąpią oznaki toksyczności, wymagane jest rozszerzone monitorowanie. Istnieją doniesienia o przypadkach pacjentów, u których późno po przedawkowaniu doszło do śmiertelnej arytmii; ci pacjenci mieli kliniczne dowody znacznego zatrucia przed śmiercią, a większość z nich została poddana nieodpowiedniemu odkażaniu przewodu pokarmowego. Monitorowanie stężeń leków w osoczu nie powinno kierować postępowaniem z pacjentem.
Dekontaminacja przewodu pokarmowego
Wszyscy pacjenci z podejrzeniem przedawkowania trójpierścieniowego powinni otrzymać odkażanie przewodu pokarmowego. Powinno to obejmować płukanie żołądka o dużej objętości, a następnie węgiel aktywowany. Jeśli świadomość jest osłabiona, przed płukaniem należy zabezpieczyć drogi oddechowe. Wymioty są przeciwwskazane.
Układ sercowo-naczyniowy
Najlepszym wskaźnikiem ciężkości przedawkowania może być maksymalny czas trwania zespołu QRS odprowadzenia kończyny wynoszący ≥0,10 sekundy. W celu utrzymania pH surowicy w zakresie od 7,45 do 7,55 należy stosować dożylnie wodorowęglan sodu. Jeśli odpowiedź pH jest niewystarczająca, można również zastosować hiperwentylację. Jednoczesne stosowanie hiperwentylacji i wodorowęglanu sodu należy prowadzić z najwyższą ostrożnością, z częstym monitorowaniem pH. Niepożądane jest pH >7,60 lub pCO2
rzadkich przypadkach hemoperfuzja może być korzystna w przypadku ostrej opornej na leczenie niestabilności sercowo-naczyniowej u pacjentów z ostrą toksycznością. Jednak hemodializa, dializa otrzewnowa, transfuzje wymienne i wymuszona diureza ogólnie były zgłaszane jako nieskuteczne w przypadku zatrucia trójpierścieniowego.
CNS
pacjentów z depresją OUN zaleca się wczesną intubację ze względu na możliwość nagłego pogorszenia. Napady padaczkowe należy kontrolować za pomocą benzodiazepin lub, jeśli są nieskuteczne, innych leków przeciwdrgawkowych (np. fenobarbital, fenytoina). Fizostygmina nie jest zalecana, z wyjątkiem leczenia objawów zagrażających życiu, które nie reagowały na inne terapie, i tylko w porozumieniu z centrum kontroli zatruć.
Obserwacja psychiatryczna
Ponieważ przedawkowanie jest często celowe, w fazie zdrowienia pacjenci mogą próbować popełnić samobójstwo innymi sposobami. Wskazane może być skierowanie do psychiatry.
Zarządzanie pediatryczne
Zasady postępowania w przypadku przedawkowania u dzieci i dorosłych są podobne. Zdecydowanie zaleca się, aby lekarz skontaktował się z lokalnym ośrodkiem kontroli zatruć w celu uzyskania określonego leczenia pediatrycznego.
PRZECIWWSKAZANIA
Jednoczesne stosowanie związków hamujących monoaminooksydazę jest przeciwwskazane. U pacjentów otrzymujących takie kombinacje mogą wystąpić przełomy nadgorączkowe lub ciężkie napady drgawkowe. Nasilenie działań niepożądanych może być poważne, a nawet śmiertelne. Gdy pożądane jest zastąpienie Tofranilu u pacjentów otrzymujących inhibitor monoaminooksydazy, powinien upłynąć tak długi odstęp, jak pozwala na to sytuacja kliniczna, wynoszący co najmniej 14 dni. Dawka początkowa powinna być niska, a jej zwiększanie powinno być stopniowe i ostrożnie przepisywane.
Lek jest przeciwwskazany w ostrym okresie rekonwalescencji po zawale mięśnia sercowego. Leku nie należy podawać pacjentom o znanej nadwrażliwości na ten związek. Należy pamiętać o możliwości nadwrażliwości krzyżowej na inne związki dibenzazepinowe.
FARMAKOLOGIA KLINICZNA
Mechanizm działania Tofranil 25mg nie jest do końca poznany. Nie działa jednak przede wszystkim poprzez stymulację ośrodkowego układu nerwowego. Przypuszcza się, że efekt kliniczny jest spowodowany wzmocnieniem synaps adrenergicznych przez blokowanie wychwytu norepinefryny w zakończeniach nerwowych. Uważa się, że mechanizm działania leku w kontrolowaniu moczenia dziecięcego jest niezależny od jego działania przeciwdepresyjnego.
Farmakologia i toksykologia zwierząt
A. Ostre
Zakresy doustnego LD50 są następujące:
Szczur 355 do 682 mg/kg Pies 100 do 215 mg/kg
W zależności od dawki u obu gatunków objawy toksyczne postępowały stopniowo od depresji, nieregularnego oddychania i ataksji do drgawek i śmierci.
B. Rozmnażanie/Teratogenne
Całościową ocenę można podsumować w następujący sposób:
Doustnie: Niezależne badania na trzech gatunkach (szczur, mysz i królik) wykazały, że po podaniu doustnym Tofranilu w dawkach do około 2-1/2-krotności maksymalnej dawki u ludzi w pierwszych 2 gatunkach i do 25-krotności maksymalnej dawki u ludzi dawki u trzeciego gatunku, lek jest zasadniczo wolny od potencjału teratogennego. W trzech badanych gatunkach wystąpił tylko jeden przypadek nieprawidłowości płodu (u królika) i w tym badaniu wystąpiła również nieprawidłowość w grupie kontrolnej. Jednak istnieją dowody z badań na szczurach, że można wykazać pewien potencjał ogólnoustrojowy i embriotoksyczny. Objawia się to zmniejszoną wielkością miotu, niewielkim wzrostem odsetka martwo urodzonych dzieci oraz zmniejszeniem średniej masy urodzeniowej.
