Cipro 1000mg, 250mg, 500mg, 750mg Ciprofloxacin Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Cipro 750mg i jak się go stosuje?
Cipro 500mg to lek na receptę stosowany w leczeniu objawów infekcji bakteryjnych. Cipro może być stosowany samodzielnie lub z innymi lekami.
Cipro należy do klasy leków zwanych fluorochinolonami.
Nie wiadomo, czy Cipro 750 mg jest bezpieczny i skuteczny u dzieci poniżej 1 roku życia.
Jakie są możliwe skutki uboczne Cipro?
Cipro może powodować poważne skutki uboczne, w tym:
- niski poziom cukru we krwi,
- ból głowy,
- głód,
- wyzysk,
- drażliwość,
- zawroty głowy,
- mdłości,
- szybkie tętno,
- uczucie niepokoju lub roztrzęsienia,
- drętwienie rąk, ramion, nóg lub stóp,
- słabość,
- mrowienie lub piekący ból,
- nerwowość,
- dezorientacja,
- podniecenie,
- paranoja,
- halucynacje,
- problemy z pamięcią,
- problemy z koncentracją,
- myśli samobójcze,
- nagły ból,
- obrzęk,
- siniaki,
- czułość,
- sztywność,
- problemy ruchowe,
- zatrzaskiwanie lub wyskakiwanie w dowolnym połączeniu,
- silny lub ciągły ból w klatce piersiowej, brzuchu lub plecach,
- biegunka wodnista lub krwawa,
- fruwające w piersi,
- duszność,
- zawroty,
- wysypka,
- problemy z oddychaniem,
- małe lub brak oddawania moczu,
- zażółcenie skóry lub oczu,
- silny ból głowy,
- dzwonienie w uszach,
- problemy ze wzrokiem i
- ból za oczami
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Cipro 1000mg to:
- mdłości,
- wymioty,
- biegunka,
- ból brzucha,
- swędzenie lub upławy pochwy,
- ból głowy i
- nieprawidłowe testy czynności wątroby
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Cipro. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OSTRZEŻENIE
POWAŻNE REAKCJE NIEPOŻĄDANE W TYM ZAPACHY ŚCIĘGIEN, ZERWANIE ŚCIĘGNA, NEUROPATIA OBWODOWA, DZIAŁANIE NA CENTRALNY UKŁAD NERWOWY ORAZ ZAostrzenie Miastenii Gravis
- Fluorochinolony, w tym Cipro 250mg, były związane z wyłączającymi i potencjalnie nieodwracalnymi poważnymi działaniami niepożądanymi, które występowały razem [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI], w tym:
- Zapalenie ścięgna i zerwanie ścięgna [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI]
- Neuropatia obwodowa [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI]
- Wpływ na centralny układ nerwowy [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI]
Należy natychmiast przerwać stosowanie Cipro 750 mg i unikać stosowania fluorochinolonów, w tym Cipro, u pacjentów, u których wystąpiły którekolwiek z tych ciężkich działań niepożądanych [patrz OSTRZEŻENIA I ŚRODKI ]
- Fluorochinolony, w tym Cipro 750 mg, mogą nasilać osłabienie mięśni u pacjentów z miastenią. Unikaj Cipro u pacjentów ze znaną historią miastenii. [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI]
- Ponieważ fluorochinolony, w tym CIPRO 500 mg, wiązały się z poważnymi działaniami niepożądanymi [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI], należy zachować CIPRO do stosowania u pacjentów, którzy nie mają alternatywnych opcji leczenia niepowikłanych zakażeń dróg moczowych [patrz WSKAZANIA]
OPIS
Cipro (cipro 750 mgfloksacyna*) tabletki o przedłużonym uwalnianiu zawierają cypro 500 mgfloksacyny, syntetyczny środek przeciwbakteryjny do podawania doustnego. Tabletki Cipro 1000 mg to powlekane, dwuwarstwowe tabletki składające się z warstwy o natychmiastowym uwalnianiu i warstwy o kontrolowanym uwalnianiu typu matrycy erozyjnej. Tabletki zawierają połączenie dwóch rodzajów substancji leczniczej cyprofloksacyny, chlorowodorku cyprofloksacyny i betainy cyprofloksacyny (podstawa). Chlorowodorek Cipro 750 mg floksacyny to chlorowodorek kwasu 1-cyklopropylo-6-fluoro-1,4dihydro-4-okso-7-(1-piperazynylo)-3-chinolinokarboksylowego. Jest dostarczany jako mieszanina monohydratu i półtorahydratu. Empiryczny wzór monohydratu to C17H18FN3O3. HCl . H2O, a jego masa cząsteczkowa wynosi 385,8. Empiryczna formuła półtorawodzianu to C17H18FN3O3. HCl . 1,5 H2O, a jego masa cząsteczkowa wynosi 394,8. Substancja lecznicza jest substancją krystaliczną o barwie lekko żółtawej do jasnożółtej. Struktura chemiczna monohydratu jest następująca:
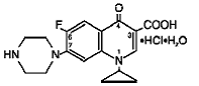
Cipro 1000mgfloksacyna betaina to kwas 1-cyklopropylo-6-fluoro-1,4-dihydro-4-okso-7-(1-piperazynylo)-3-chinolinokarboksylowy. Jako hydrat, jego wzór empiryczny to C17H18FN3O3. 3,5 H2O, a jego masa cząsteczkowa wynosi 394,3. Jest to substancja krystaliczna o barwie jasnożółtawej do jasnożółtej, a jej struktura chemiczna jest następująca:
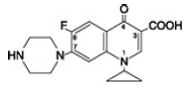
Cipro jest dostępny w tabletkach o mocy 500 mg i 1000 mg (odpowiednik cypro 500 mg floksacyny). Tabletki Cipro to prawie białe do lekko żółtawych, powlekane tabletki o podłużnym kształcie. Każda tabletka Cipro 500 mg zawiera 500 mg cyprofloksacyny w postaci chlorowodorku cyprofloksacyny (287,5 mg w przeliczeniu na cyprofloksacynę w przeliczeniu na suchą masę) i cypro 1000 mg floksacyny† (212,6 mg w przeliczeniu na suchą masę). Każda tabletka Cipro 1000 mg zawiera 1000 mg cyprofloksacyny w postaci chlorowodorku cyprofloksacyny (574,9 mg, w przeliczeniu na cyprofloksacynę w przeliczeniu na suchą masę) i cipro 750 mg floksacyny (425,2 mg, w przeliczeniu na suchą masę). Nieaktywnymi składnikami są krospowidon, hypromeloza, stearynian magnezu, glikol polietylenowy, krzemionka koloidalna bezwodna, kwas bursztynowy i dwutlenek tytanu.
* jako cipro 500mgfloksacyna† i cipro 250mgfloksacyna chlorowodorek† nie spełnia wymagań dotyczących strat w teście suszenia i pozostałości w teście zapłonu monografii USP.
WSKAZANIA
Infekcje skóry i struktury skóry
CIPRO 1000 mg jest wskazany u dorosłych pacjentów w leczeniu zakażeń skóry i struktur skóry wywołanych przez Escherichia coli, Klebsiella pneumoniae, Enterobacter cloacae, Proteus mirabilis, Proteus vulgaris, Providencia stuartii, Morganella morganii, Citrobacter freundii, Pseudomonaceptithic aeruginococcus, meureus wrażliwy na metycylinę Staphylococcus epidermidis lub Streptococcus pyogenes.
Infekcje kości i stawów
CIPRO 750 mg jest wskazany u dorosłych pacjentów w leczeniu zakażeń kości i stawów wywołanych przez Enterobacter cloacae, Serratia marcescens lub Pseudomonas aeruginosa.
Powikłane infekcje w obrębie jamy brzusznej
CIPRO 250 mg jest wskazany u dorosłych pacjentów w leczeniu powikłanych zakażeń w obrębie jamy brzusznej (stosowanych w skojarzeniu z metronidazolem) wywołanych przez Escherichia coli, Pseudomonas aeruginosa, Proteus mirabilis, Klebsiella pneumoniae lub Bacteroides fragilis.
Zakaźna biegunka
CIPRO 500 mg jest wskazany u dorosłych pacjentów w leczeniu biegunki zakaźnej wywołanej przez Escherichia coli (izolaty enterotoksygenne), Campylobacter jejuni, Shigella boydii†, Shigella dysenteriae, Shigella flexneri lub Shigella sonnei†, gdy wskazane jest leczenie przeciwbakteryjne.
†Chociaż leczenie zakażeń wywołanych tym drobnoustrojem w tym układzie narządowym wykazało klinicznie istotny wynik, skuteczność zbadano u mniej niż 10 pacjentów.
Dur brzuszny (gorączka jelitowa)
CIPRO 1000 mg jest wskazany u dorosłych pacjentów w leczeniu duru brzusznego (gorączki jelitowej) wywołanej przez Salmonella typhi. Nie wykazano skuteczności cyprofloksacyny w eradykacji przewlekłego nosicielstwa duru brzusznego.
Nieskomplikowana rzeżączka szyjki macicy i cewki moczowej
CIPRO jest wskazany u dorosłych pacjentów w leczeniu niepowikłanej rzeżączki szyjki macicy i cewki moczowej wywołanej przez Neisseria gonorrhoeae [patrz OSTRZEŻENIA I ŚRODKI ].
Wąglik wziewny (po ekspozycji)
CIPRO 250 mg jest wskazany u dorosłych i dzieci od urodzenia do 17 roku życia w wągliku wziewnym (po ekspozycji) w celu zmniejszenia częstości występowania lub progresji choroby po ekspozycji na aerozol Bacillus anthracis.
Stężenie Cipro 500 mg floksacyny w surowicy osiągnięte u ludzi służyło jako zastępczy punkt końcowy, z rozsądnym prawdopodobieństwem pozwalającym przewidzieć korzyści kliniczne i stanowiło wstępną podstawę do zatwierdzenia tego wskazania.1 Dodatkowe informacje kliniczne dotyczące cyprofloksacyny w profilaktyce poekspozycyjnej wąglika uzyskano podczas ataków bioterroru wąglika w październiku 2001 [patrz Studia kliniczne ].
Plaga
CIPRO 1000 mg jest wskazany do leczenia dżumy, w tym dżumy płucnej i posocznicy, ze względu na Yersinia pestis (Y. pestis) oraz profilaktyki dżumy u dorosłych i dzieci od urodzenia do 17 roku życia. Ze względów wykonalności nie można było przeprowadzić badań skuteczności cipro 250 mgfloksacyny u ludzi z dżumą. Dlatego to wskazanie opiera się na badaniu skuteczności przeprowadzonym wyłącznie na zwierzętach [patrz Studia kliniczne ].
Przewlekłe bakteryjne zapalenie gruczołu krokowego
CIPRO jest wskazany u dorosłych pacjentów w leczeniu przewlekłego bakteryjnego zapalenia gruczołu krokowego wywołanego przez Escherichia coli lub Proteus mirabilis.
Zakażenia dolnych dróg oddechowych
CIPRO 750 mg jest wskazany u dorosłych pacjentów w leczeniu zakażeń dolnych dróg oddechowych wywołanych przez Escherichia coli, Klebsiella pneumoniae, Enterobacter cloacae, Proteus mirabilis, Pseudomonas aeruginosa, Haemophilus influenzae, Haemophilus parainfluenzae lub Streptococcus pneumoniae.
CIPRO nie jest lekiem pierwszego wyboru w leczeniu podejrzenia lub potwierdzenia wtórnego zapalenia płuc wywołanego przez Streptococcus pneumoniae.
CIPRO jest wskazany w leczeniu ostrych zaostrzeń przewlekłego zapalenia oskrzeli (AECB) wywołanych przez Moraxella catarrhalis.
Ponieważ fluorochinolony, w tym CIPRO, były związane z poważnymi działaniami niepożądanymi [patrz OSTRZEŻENIA I ŚRODKI ], aw przypadku niektórych pacjentów AECB ma charakter samoograniczający, należy zarezerwować CIPRO 750 mg do leczenia AECB u pacjentów, którzy nie mają alternatywnych opcji leczenia.
Infekcje dróg moczowych
Zakażenia dróg moczowych u dorosłych
CIPRO 500 mg jest wskazany u dorosłych pacjentów w leczeniu zakażeń dróg moczowych wywołanych przez Escherichia coli, Klebsiella pneumoniae, Enterobacter cloacae, Serratia marcescens, Proteus mirabilis, Providencia rettgeri, Morganella morganii, Citrobacter koseri, Citrobacter freundosa, , Staphylococcus saprophyticus lub Enterococcus faecalis.
Ostre niepowikłane zapalenie pęcherza moczowego
CIPRO 750 mg jest wskazany u dorosłych pacjentek w leczeniu ostrego niepowikłanego zapalenia pęcherza wywołanego przez Escherichia coli lub Staphylococcus saprophyticus.
Ponieważ fluorochinolony, w tym CIPRO, były związane z poważnymi działaniami niepożądanymi [patrz OSTRZEŻENIA I ŚRODKI ], a u niektórych pacjentów ostre niepowikłane zapalenie pęcherza moczowego ustępuje samoistnie, należy zachować CIPRO do leczenia ostrego niepowikłanego zapalenia pęcherza moczowego u pacjentów, którzy nie mają alternatywnych opcji leczenia.
Powikłane zakażenie dróg moczowych i odmiedniczkowe zapalenie nerek u pacjentów pediatrycznych
CIPRO jest wskazany u dzieci w wieku od 1 do 17 lat w leczeniu powikłanych zakażeń dróg moczowych (cUTI) i odmiedniczkowego zapalenia nerek wywołanego przez Escherichia coli [patrz Używaj w określonych populacjach ].
Chociaż jest skuteczny w badaniach klinicznych, CIPRO nie jest lekiem pierwszego wyboru w populacji pediatrycznej ze względu na zwiększoną częstość występowania działań niepożądanych w porównaniu z grupą kontrolną, w tym reakcji związanych ze stawami i (lub) otaczającymi tkankami. CIPRO 250 mg, podobnie jak inne fluorochinolony, wiąże się z artropatią i zmianami histopatologicznymi stawów obciążonych u młodych zwierząt [patrz OSTRZEŻENIA I ŚRODKI , DZIAŁANIA NIEPOŻĄDANE , Używaj w określonych populacjach oraz Toksykologia niekliniczna ].
Ostre zapalenie zatok
CIPRO jest wskazany u dorosłych pacjentów w leczeniu ostrego zapalenia zatok wywołanego przez Haemophilus influenzae, Streptococcus pneumoniae lub Moraxella catarrhalis.
Ponieważ fluorochinolony, w tym CIPRO, były związane z poważnymi działaniami niepożądanymi [patrz OSTRZEŻENIA I ŚRODKI ], a u niektórych pacjentów ostre zapalenie zatok ustępuje samoistnie, należy zachować CIPRO do leczenia ostrego zapalenia zatok u pacjentów, którzy nie mają alternatywnych opcji leczenia.
Stosowanie
Aby ograniczyć rozwój bakterii opornych na leki i utrzymać skuteczność preparatu CIPRO 1000 mg i innych leków przeciwbakteryjnych, preparat CIPRO 500 mg należy stosować wyłącznie w leczeniu lub zapobieganiu zakażeniom, co do których udowodniono, lub co do których istnieje silne podejrzenie, że są wywołane przez wrażliwe bakterie. Gdy dostępne są informacje dotyczące hodowli i wrażliwości, należy je uwzględnić przy wyborze lub modyfikacji terapii przeciwbakteryjnej. W przypadku braku takich danych, lokalna epidemiologia i wzorce podatności mogą przyczynić się do empirycznego doboru terapii.
Jeśli podejrzewa się, że do zakażenia przyczyniają się organizmy beztlenowe, należy zastosować odpowiednią terapię. Przed leczeniem należy przeprowadzić odpowiednie posiewy i testy wrażliwości w celu wyizolowania i identyfikacji drobnoustrojów wywołujących zakażenie oraz określenia ich wrażliwości na cyprofloksacynę. Leczenie preparatem CIPRO można rozpocząć przed poznaniem wyników tych testów; po uzyskaniu wyników należy kontynuować odpowiednią terapię.
Podobnie jak w przypadku innych leków, niektóre izolaty Pseudomonas aeruginosa mogą dość szybko rozwinąć oporność podczas leczenia cipro 1000 mgfloksacyny. Badania posiewów i lekowrażliwości wykonywane okresowo podczas terapii dostarczą informacji nie tylko o działaniu terapeutycznym środka przeciwdrobnoustrojowego, ale także o możliwym pojawieniu się oporności bakterii.
DAWKOWANIE I SPOSÓB PODAWANIA
CIPRO 1000 mg tabletki i zawiesina doustna należy podawać doustnie, jak opisano w odpowiednich tabelach wytycznych dotyczących dawkowania.
Dawkowanie u dorosłych
Ustalenie dawki i czasu trwania dla każdego konkretnego pacjenta musi uwzględniać ciężkość i charakter infekcji, podatność drobnoustrojów wywołujących, integralność mechanizmów obronnych gospodarza pacjenta oraz stan czynności nerek i wątroby . Tabletki CIPRO lub CIPRO do sporządzania zawiesiny doustnej mogą być podawane dorosłym pacjentom, jeśli jest to klinicznie wskazane według uznania lekarza. Podawać CIPRO do zawiesiny doustnej za pomocą dołączonej do opakowania łyżki z podziałką [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Konwersja IV do podawania doustnego u dorosłych
Pacjenci, u których rozpoczęto leczenie preparatem CIPRO IV, mogą zostać zamienieni na CIPRO 750 mg tabletki lub zawiesinę doustną, jeśli jest to klinicznie wskazane według uznania lekarza (Tabela 2) [patrz FARMAKOLOGIA KLINICZNA ].
Dawkowanie u pacjentów pediatrycznych
Dawkowanie i początkowa droga leczenia (tj. IV lub doustna) w przypadku cUTI lub odmiedniczkowego zapalenia nerek powinny być uzależnione od ciężkości zakażenia. CIPRO należy podawać zgodnie z opisem w Tabeli 3. Podawać CIPRO w postaci zawiesiny doustnej za pomocą dołączonej do opakowania łyżki z podziałką [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Modyfikacje dawkowania u pacjentów z niewydolnością nerek
Cipro 250mgfloksacyna jest wydalana głównie przez nerki; jednak lek jest również metabolizowany i częściowo usuwany przez drogi żółciowe wątroby i jelita. Te alternatywne drogi eliminacji leku wydają się kompensować zmniejszone wydalanie nerkowe u pacjentów z zaburzeniami czynności nerek. Niemniej jednak zaleca się pewną modyfikację dawkowania, szczególnie u pacjentów z ciężkimi zaburzeniami czynności nerek. Wytyczne dotyczące dawkowania u pacjentów z zaburzeniami czynności nerek przedstawiono w Tabeli 4.
Gdy znane jest tylko stężenie kreatyniny w surowicy, do oszacowania klirensu kreatyniny można użyć następujących wzorów:
Stężenie kreatyniny w surowicy powinno odzwierciedlać stan stacjonarny czynności nerek.
U pacjentów z ciężkimi zakażeniami i ciężkimi zaburzeniami czynności nerek można podać dawkę jednostkową 750 mg w odstępach podanych powyżej. Pacjenci powinni być uważnie monitorowani.
Pacjenci pediatryczni z umiarkowaną lub ciężką niewydolnością nerek byli wykluczeni z badania klinicznego cUTI i odmiedniczkowego zapalenia nerek. Brak dostępnych informacji na temat konieczności dostosowania dawkowania u dzieci i młodzieży z umiarkowaną lub ciężką niewydolnością nerek (tj. klirens kreatyniny
Ważne instrukcje administracyjne
Z kationami wielowartościowymi
Podawać CIPRO co najmniej 2 godziny przed lub 6 godzin po lekach zobojętniających magnez/glin; polimeryczne środki wiążące fosforany (na przykład sewelamer, węglan lantanu) lub sukralfat; Videx® (dydanozyna) tabletki do żucia/buforowane lub proszek pediatryczny do sporządzania roztworu doustnego; inne silnie zbuforowane leki; lub inne produkty zawierające wapń, żelazo lub cynk.
Z produktami mlecznymi
Należy unikać jednoczesnego podawania preparatu CIPRO 500 mg z produktami mlecznymi (takimi jak mleko lub jogurt) lub samymi sokami wzbogacanymi wapniem, ponieważ możliwe jest zmniejszenie wchłaniania; jednak CIPRO można przyjmować z posiłkiem zawierającym te produkty.
Nawodnienie pacjentów otrzymujących CIPRO
Zapewnić odpowiednie nawodnienie pacjentów otrzymujących CIPRO 1000 mg, aby zapobiec tworzeniu się silnie stężonego moczu. Krystaluria była zgłaszana w przypadku chinolonów.
Należy poinstruować pacjenta o odpowiednim podaniu preparatu CIPRO 1000 mg [patrz Informacje dotyczące poradnictwa dla pacjentów ].
Pominięte dawki
Jeśli pominięto dawkę, należy ją przyjąć w dowolnym momencie, ale nie później niż 6 godzin przed następną zaplanowaną dawką. Jeśli do następnej dawki pozostało mniej niż 6 godzin, nie należy przyjmować pominiętej dawki, a leczenie należy kontynuować zgodnie z zaleceniami z następną zaplanowaną dawką. Nie należy przyjmować podwójnych dawek w celu wyrównania pominiętej dawki.
Dzielenie tabletek CIPRO 1000 mg
Tabletki CIPRO 750 mg, 250 mg i 500 mg to tabletki z funkcjonalną podziałką, które można podzielić na pół na linii z podziałką, aby uzyskać odpowiednio moc 125 mg i 250 mg.
Wskazówki dotyczące rekonstytucji mikrokapsułek CIPRO 500 mg do zawiesiny doustnej
CIPRO 750 mg zawiesina doustna jest dostarczana w stężeniu 5% (5 g cyprofloksacyny w 100 ml) i 10% (10 g cipro 750 mg floksacyny w 100 ml). CIPRO 250 mg zawiesina doustna składa się z dwóch składników (mikrokapsułek i rozcieńczalnika), które należy połączyć przed dozowaniem.
Przygotowanie zawieszenia
Krok 1
Mała butelka zawiera mikrokapsułki, duża butelka zawiera rozcieńczalnik.

Krok 2
Otwórz obie butelki. Nasadka zabezpieczająca przed dziećmi: Naciśnij zgodnie z instrukcjami na nasadce, jednocześnie obracając w lewo.

Krok 3
 Całkowicie wlać mikrokapsułki do większej butelki rozcieńczalnika. Nie dodawaj wody do zawiesiny .
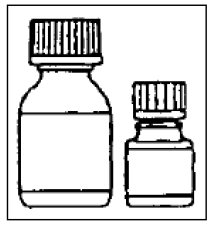
Krok 4
 Zdjąć górną warstwę etykiety butelki z rozcieńczalnikiem (aby odsłonić etykietę CIPRO 1000 mg zawiesiny doustnej). Całkowicie zamknij dużą butelkę zgodnie ze wskazówkami na nakrętce i energicznie potrząsaj przez około 15 sekund. Zawieszenie jest gotowe do użycia.
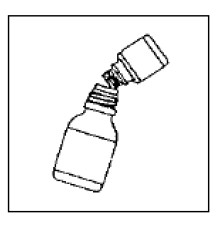
Krok 5
Na etykiecie butelki napisać datę ważności odtworzonej zawiesiny doustnej.
Produkt po rekonstytucji można przechowywać w temperaturze poniżej 30°C (86°F) przez 14 dni. Chronić przed zamarzaniem.
Do zmieszanej końcowej zawiesiny cyprofloksacyny nie należy dodawać żadnych dodatków. CIPRO 1000 mg zawiesina doustna nie powinna być podawana przez sondy do karmienia lub przez sondy NG (nosowo-żołądkowe) ze względu na swoje właściwości fizyczne.
Instrukcje administracyjne dla CIPRO do doustnej zawiesiny po rekonstytucji
- Przed każdym użyciem energicznie wstrząsnąć CIPRO 750 mg zawiesina doustna przez około 15 sekund.
- Podawać zawiesinę doustną CIPRO za pomocą dołączonej do opakowania łyżeczki z podziałką, dostarczonej pacjentowi (patrz Rysunek 1)
Rysunek 1: Dołączona łyżeczka z podziałką o pojemności 5 ml
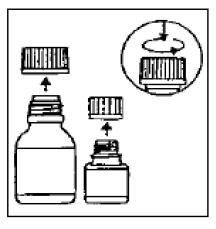
Dołączona jest wyskalowana łyżeczka do herbaty (5 ml) w opakowaniu, z oznaczeniami ½ (2,5 ml) i 1/1 (5 ml)
- Po użyciu umyć łyżeczkę z podziałką pod bieżącą wodą z dodatkiem płynu do mycia naczyń i dokładnie wysuszyć.
- Nie żuć mikrokapsułek zawartych w zawiesinie doustnej CIPRO 250 mg, zamiast tego połykać je w całości.
- Następnie można wziąć wodę.
- Prawidłowo zamknąć butelkę po każdym użyciu, zgodnie z instrukcjami na nakrętce.
- Po zakończeniu leczenia nie należy ponownie stosować CIPRO 1000 mg zawiesiny doustnej.
Dawkowanie CIPRO do zawiesiny doustnej za pomocą dołączonej łyżki u dorosłych i pacjentów pediatrycznych
JAK DOSTARCZONE
Formy dawkowania i mocne strony
Tablety
- 250 mg, lekko żółtawy, powlekany, okrągły, z funkcjonalnym nacięciem, z nadrukiem „BAYER” po jednej stronie i „CIP 250” po drugiej.
- 500 mg, lekko żółtawy, powlekany, w kształcie kapsułki, z funkcjonalnym nacięciem, z nadrukiem „BAYER” po jednej stronie i „CIP 500” po drugiej.
Zawiesina doustna
- 5% zawiesina doustna: 250 mg cipro 750 mgfloksacyny na 5 ml po rekonstytucji
- 10% zawiesina doustna: 500 mg cipro 250 mg floksacyny na 5 ml po rekonstytucji
Składowania i stosowania
Tabletki CIPRO (cipro 750 mg floksacyny chlorowodorku) są dostępne w postaci okrągłych, lekko żółtawych tabletek powlekanych zawierających 250 mg cypro 500 mg floksacyny. Tabletka 250 mg jest zakodowana napisem „BAYER” po jednej stronie oraz funkcjonalnie naciętą i wygrawerowaną literą „CIP 250” po drugiej stronie. CIPRO jest również dostępny w postaci lekko żółtawych tabletek powlekanych w kształcie kapsułki, zawierających 500 mg cyprofloksacyny. Tabletka 500 mg jest zakodowana napisem „BAYER” po jednej stronie oraz funkcjonalnie naciętą i wygrawerowaną literą „CIP 500” po drugiej stronie. CIPRO 250 mg i 500 mg są dostępne w butelkach po 100.
Przechowywać w temperaturze 20° do 25°C (68° do 77°F); wycieczki dozwolone do 15 ° do 30 ° C (59 ° do 86 ° F) [patrz Temperatura pokojowa kontrolowana przez USP ].
Zawiesina doustna CIPRO jest dostarczana w stężeniach 5% i 10%. Produkt leczniczy składa się z dwóch składników (mikrokapsułek zawierających substancję czynną i rozcieńczalnik), które musi wymieszać farmaceuta [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Przechowywać mikrokapsułki i rozcieńczalnik w temperaturze poniżej 25°C (77°F); wycieczki są dozwolone od 15°C do 30°C (59°F do 86°F) [patrz Temperatura pokojowa kontrolowana przez USP ]. Chronić przed zamarzaniem.
Odtworzony produkt można przechowywać w temperaturze 25°C (77°F) przez 14 dni; wycieczki są dozwolone od 15°C do 30°C (59°F do 86°F) [patrz Temperatura pokojowa kontrolowana przez USP ]. Chronić przed zamarzaniem.
Dla pacjenta dostarczana jest łyżeczka z podziałką (5 ml) z oznaczeniami ½ (2,5 ml) i 1/1 (5 ml).
BIBLIOGRAFIA
1. 21 CFR 314.510 (Podczęść H – Przyspieszone zatwierdzanie nowych leków na choroby zagrażające życiu).
2. Friedman J, Polifka J. Teratogenne działanie leków: źródło informacji dla klinicystów (TERIS). Baltimore, Maryland: Johns Hopkins University Press, 2000:149-195.
3. Loebstein R, Addis A, Ho E, et al. Wynik ciąży po ekspozycji ciążowej na fluorochinolony: wieloośrodkowe prospektywne badanie kontrolowane. Środki przeciwdrobnoustrojowe Chemother. 1998;42(6):1336-1339.
Wyprodukowano dla: Bayer HealthCare Pharmaceuticals Inc. Whippany, NJ 07981. Aktualizacja: listopad 2021
SKUTKI UBOCZNE
Następujące poważne i poza tym ważne działania niepożądane leku omówiono bardziej szczegółowo w innych punktach oznakowania:
- Unieruchamiające i potencjalnie nieodwracalne poważne reakcje niepożądane [patrz OSTRZEŻENIA I ŚRODKI ]
- Zapalenie ścięgna i zerwanie ścięgna [patrz OSTRZEŻENIA I ŚRODKI ]
- Neuropatia obwodowa [patrz OSTRZEŻENIA I ŚRODKI ]
- Skutki na ośrodkowy układ nerwowy [patrz OSTRZEŻENIA I ŚRODKI ] Zaostrzenie miastenii Gravis [patrz OSTRZEŻENIA I ŚRODKI ]
- Inne poważne, a czasem śmiertelne reakcje niepożądane [patrz OSTRZEŻENIA I ŚRODKI ]
- Reakcje nadwrażliwości [patrz OSTRZEŻENIA I ŚRODKI ]
- Hepatotoksyczność [patrz OSTRZEŻENIA I ŚRODKI ]
- Ryzyko tętniaka i rozwarstwienia aorty [patrz OSTRZEŻENIA I ŚRODKI ]
- Poważne reakcje niepożądane przy jednoczesnej teofilinie [patrz OSTRZEŻENIA I ŚRODKI ]
- Biegunka związana z Clostridioides difficile [patrz OSTRZEŻENIA I ŚRODKI ]
- Wydłużenie odstępu QT [patrz OSTRZEŻENIA I ŚRODKI ]
- Zaburzenia mięśniowo-szkieletowe u pacjentów pediatrycznych [patrz OSTRZEŻENIA I ŚRODKI ]
- Światłoczułość/Fototoksyczność [patrz OSTRZEŻENIA I ŚRODKI ]
- Rozwój bakterii lekoopornych [patrz OSTRZEŻENIA I ŚRODKI ]
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Pacjenci dorośli
Podczas badań klinicznych z doustnym i pozajelitowym CIPRO 750 mg, 49 038 pacjentów otrzymało kursy tego leku.
Najczęściej zgłaszanymi działaniami niepożądanymi, wynikającymi z badań klinicznych wszystkich postaci, wszystkich dawek, wszystkich czasów trwania terapii lekowej i we wszystkich wskazaniach do leczenia cyprofloksacyną, były nudności (2,5%), biegunka (1,6%), nieprawidłowe wyniki testów czynnościowych wątroby (1,3%). ), wymioty (1%) i wysypka (1%).
W randomizowanych, podwójnie zaślepionych, kontrolowanych badaniach klinicznych porównujących tabletki CIPRO [500 mg dwa razy na dobę (BID)] z aksetylem cefuroksymu (250 mg-500 mg BID) i klarytromycyną (500 mg BID) u pacjentów z zakażeniami dróg oddechowych, CIPRO wykazał profil działań niepożądanych ze strony OUN porównywalny z lekami kontrolnymi.
Pacjenci pediatryczni
Krótkoterminowe (6 tygodni) i długoterminowe (1 rok) bezpieczeństwo mięśniowo-szkieletowe i neurologiczne doustnej/dożylnej cyprofloksacyny porównano z cefalosporyną w leczeniu cUTI lub odmiedniczkowego zapalenia nerek u dzieci w wieku od 1 do 17 lat (średnia wieku 6 ± 4 lata). ) w międzynarodowym badaniu wieloośrodkowym. Czas trwania terapii wynosił od 10 do 21 dni (średni czas trwania leczenia wynosił 11 dni z zakresem od 1 do 88 dni). Do badania włączono łącznie 335 pacjentów leczonych cipro 250 mgfloksacyną i 349 pacjentów leczonych lekiem porównawczym.
Niezależny Komitet ds. Bezpieczeństwa Pediatrycznego (IPSC) dokonał przeglądu wszystkich przypadków działań niepożądanych dotyczących układu mięśniowo-szkieletowego, w tym nieprawidłowego chodu lub nieprawidłowego badania stawów (wyjściowe lub pojawiające się podczas leczenia). W ciągu 6 tygodni od rozpoczęcia leczenia częstość występowania działań niepożądanych dotyczących układu mięśniowo-szkieletowego wyniosła 9,3% (31/335) w grupie leczonej cipro 750 mgfloksacyny w porównaniu do 6% (21/349) w grupie pacjentów leczonych lekiem porównawczym. Wszystkie działania niepożądane dotyczące układu mięśniowo-szkieletowego występujące przed upływem 6 tygodni ustąpiły (ustąpienie objawów klinicznych), zwykle w ciągu 30 dni od zakończenia leczenia. Oceny radiologiczne nie były rutynowo stosowane w celu potwierdzenia ustąpienia działań niepożądanych. Pacjenci leczeni Cipro 500mgfloksacyną częściej zgłaszali więcej niż jedno działanie niepożądane i więcej niż jeden raz w porównaniu z pacjentami z grupy kontrolnej. Częstość występowania działań niepożądanych ze strony układu mięśniowo-szkieletowego była konsekwentnie wyższa w grupie cyprofloksacyny w porównaniu z grupą kontrolną we wszystkich podgrupach wiekowych. Pod koniec 1 roku częstość tych działań niepożądanych zgłoszonych w dowolnym czasie w tym okresie wyniosła 13,7% (46/335) w grupie leczonej cipro 250 mgfloksacyną w porównaniu do 9,5% (33/349) w grupie pacjentów leczonych lekiem porównawczym ( Tabela 9).
Częstość występowania neurologicznych działań niepożądanych w ciągu 6 tygodni od rozpoczęcia leczenia wynosiła 3% (9/335) w grupie CIPRO w porównaniu do 2% (7/349) w grupie porównawczej i obejmowała zawroty głowy, nerwowość, bezsenność i senność.
tym badaniu ogólna częstość występowania działań niepożądanych w ciągu 6 tygodni od rozpoczęcia leczenia wyniosła 41% (138/335) w grupie cypro 250 mgfloksacyny w porównaniu z 31% (109/349) w grupie porównawczej. Najczęstsze działania niepożądane dotyczyły przewodu pokarmowego: 15% (50/335) pacjentów stosujących cyprofloksacynę w porównaniu do 9% (31/349) pacjentów porównawczych. Poważne działania niepożądane zaobserwowano u 7,5% (25/335) pacjentów leczonych cyprofloksacyną w porównaniu z 5,7% (20/349) pacjentów z grupy kontrolnej. Przerwanie leczenia z powodu działania niepożądanego zaobserwowano u 3% (10/335) pacjentów leczonych cyprofloksacyną w porównaniu do 1,4% (5/349) pacjentów porównawczych. Inne działania niepożądane, które wystąpiły u co najmniej 1% pacjentów z ciprofloksacyną to biegunka 4,8%, wymioty 4,8%, ból brzucha 3,3%, niestrawność 2,7%, nudności 2,7%, gorączka 2,1%, astma 1,8% i wysypka 1,8%.
Krótkoterminowe dane dotyczące bezpieczeństwa cipro 1000 mgfloksacyny zostały również zebrane w randomizowanym, podwójnie zaślepionym badaniu klinicznym dotyczącym leczenia ostrych zaostrzeń płucnych u pacjentów z mukowiscydozą (w wieku 5–17 lat). Sześćdziesięciu siedmiu pacjentów otrzymywało CIPRO IV 10 mg/kg/dawkę co 8 godzin przez tydzień, a następnie CIPRO 250 mg tabletki 20 mg/kg/dawkę co 12 godzin w celu zakończenia leczenia przez 10–21 dni, a 62 pacjentów otrzymywało kombinację ceftazydymu w formie dożylnej 50 mg/kg/dawkę co 8 godzin i tobramycynę dożylnie 3 mg/kg/dawkę co 8 godzin przez łącznie 10–21 dni. Okresowe oceny układu mięśniowo-szkieletowego przeprowadzali badacze zaślepieni na leczenie. Pacjenci byli obserwowani przez średnio 23 dni po zakończeniu leczenia (zakres 0-93 dni). Działania niepożądane dotyczące układu mięśniowo-szkieletowego zgłoszono u 22% pacjentów w grupie cyprofloksacyny i 21% w grupie porównawczej. Zmniejszony zakres ruchu odnotowano u 12% badanych w grupie cyprofloksacyny i 16% w grupie porównawczej. Bóle stawów zgłaszano u 10% pacjentów w grupie cipro 500mgfloksacyny i 11% w grupie porównawczej. Inne działania niepożądane miały podobny charakter i częstość w poszczególnych grupach leczenia. Nie ustalono skuteczności CIPRO w leczeniu ostrych zaostrzeń płucnych u dzieci z mukowiscydozą.
Poza działaniami niepożądanymi zgłaszanymi u dzieci w badaniach klinicznych, należy się spodziewać, że działania niepożądane zgłaszane u dorosłych podczas badań klinicznych lub po wprowadzeniu produktu do obrotu mogą również wystąpić u dzieci i młodzieży.
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zgłoszone na podstawie ogólnoświatowych doświadczeń marketingowych dotyczących fluorochinolonów, w tym CIPRO. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek (Tabela 10).
Niekorzystne zmiany laboratoryjne
Zmiany parametrów laboratoryjnych podczas stosowania CIPRO 250mg są wymienione poniżej:
Wątrobiany – podwyższenie ALT (SGPT), AST (SGOT), fosfatazy alkalicznej, LDH, bilirubiny w surowicy.
Hematologiczny –Eozynofilia, leukopenia, zmniejszenie liczby płytek krwi, zwiększenie liczby płytek krwi, pancytopenia.
Nerkowy –Zgłaszano podwyższenie stężenia kreatyniny w surowicy, BUN, krystalurii, cylindrurii i krwiomoczu.
Inne występujące zmiany to: podwyższenie poziomu transferazy gammaglutamylowej w surowicy, podwyższenie poziomu amylazy w surowicy, obniżenie stężenia glukozy we krwi, podwyższony poziom kwasu moczowego, obniżenie stężenia hemoglobiny, niedokrwistość, skaza krwotoczna, wzrost liczby monocytów we krwi i leukocytoza.
INTERAKCJE Z LEKAMI
Cyprofloksacyna jest inhibitorem metabolizmu, w którym pośredniczy ludzki cytochrom P450 1A2 (CYP1A2). Jednoczesne podawanie CIPRO z innymi lekami metabolizowanymi głównie przez CYP1A2 powoduje zwiększenie stężenia tych leków w osoczu i może prowadzić do klinicznie istotnych działań niepożądanych jednocześnie podawanego leku.
OSTRZEŻENIA
Zawarte jako część ŚRODKI OSTROŻNOŚCI Sekcja.
ŚRODKI OSTROŻNOŚCI
Unieruchamiające i potencjalnie nieodwracalne poważne reakcje niepożądane, w tym zapalenie ścięgna i zerwanie ścięgna, neuropatia obwodowa i skutki ośrodkowego układu nerwowego
Fluorochinolony, w tym CIPRO, są związane z uniemożliwiającymi i potencjalnie nieodwracalnymi ciężkimi działaniami niepożądanymi z różnych układów organizmu, które mogą wystąpić razem u tego samego pacjenta. Często obserwowane działania niepożądane obejmują zapalenie ścięgna, zerwanie ścięgna, ból stawów, ból mięśni, neuropatię obwodową i objawy ze strony ośrodkowego układu nerwowego (omamy, lęk, depresja, bezsenność, silne bóle głowy i splątanie). Reakcje te mogą wystąpić w ciągu kilku godzin lub tygodni po rozpoczęciu CIPRO. Te działania niepożądane wystąpiły u pacjentów w każdym wieku lub bez wcześniej istniejących czynników ryzyka [patrz OSTRZEŻENIA I ŚRODKI ].
Należy natychmiast przerwać stosowanie leku CIPRO 250 mg w przypadku wystąpienia pierwszych oznak lub objawów jakiejkolwiek poważnej reakcji niepożądanej. Ponadto należy unikać stosowania fluorochinolonów, w tym CIPRO 500 mg, u pacjentów, u których wystąpiły którekolwiek z tych poważnych działań niepożądanych związanych z fluorochinolonami.
Zapalenie ścięgna i zerwanie ścięgna
Fluorochinolony, w tym CIPRO, są związane ze zwiększonym ryzykiem zapalenia ścięgna i zerwania ścięgna w każdym wieku [patrz OSTRZEŻENIA I ŚRODKI oraz DZIAŁANIA NIEPOŻĄDANE ]. Ta reakcja niepożądana najczęściej dotyczy ścięgna Achillesa i była również zgłaszana w przypadku stożka rotatorów (barku), ręki, bicepsa, kciuka i innych ścięgien. Zapalenie lub zerwanie ścięgna może wystąpić w ciągu kilku godzin lub dni od rozpoczęcia stosowania preparatu CIPRO 500 mg lub nawet kilka miesięcy po zakończeniu leczenia fluorochinolonami. Zapalenie ścięgna i zerwanie ścięgna może wystąpić obustronnie.
Ryzyko rozwoju zapalenia ścięgna związanego z fluorochinolonami i zerwania ścięgna jest zwiększone u pacjentów w wieku powyżej 60 lat, u pacjentów przyjmujących kortykosteroidy oraz u pacjentów po przeszczepieniu nerki, serca lub płuc. Inne czynniki, które mogą niezależnie zwiększać ryzyko zerwania ścięgna, obejmują forsowną aktywność fizyczną, niewydolność nerek i wcześniejsze schorzenia ścięgien, takie jak reumatoidalne zapalenie stawów. Zapalenie ścięgna i zerwanie ścięgna wystąpiły również u pacjentów przyjmujących fluorochinolony, u których nie występują powyższe czynniki ryzyka. Należy natychmiast przerwać stosowanie CIPRO 250 mg, jeśli pacjent odczuwa ból, obrzęk, stan zapalny lub zerwanie ścięgna. Unikaj fluorochinolonów, w tym CIPRO 250 mg, u pacjentów z chorobami ścięgien w wywiadzie lub z zapaleniem ścięgna lub zerwaniem ścięgna [patrz DZIAŁANIA NIEPOŻĄDANE ].
Neuropatia obwodowa
Fluorochinolony, w tym CIPRO, są związane ze zwiększonym ryzykiem neuropatii obwodowej. U pacjentów otrzymujących fluorochinolony, w tym CIPRO, zgłaszano przypadki czuciowej lub czuciowo-ruchowej polineuropatii aksonów obejmującej małe i (lub) duże aksony, powodujące parestezje, niedoczulica, zaburzenia czucia i osłabienie. Objawy mogą wystąpić wkrótce po rozpoczęciu CIPRO i mogą być nieodwracalne u niektórych pacjentów [patrz OSTRZEŻENIA I ŚRODKI oraz DZIAŁANIA NIEPOŻĄDANE ].
Natychmiast przerwij CIPRO, jeśli u pacjenta wystąpią objawy neuropatii obwodowej, w tym ból, pieczenie, mrowienie, drętwienie i/lub osłabienie, lub inne zmiany w odczuciach, w tym lekki dotyk, ból, temperatura, czucie pozycji i wibracje i/lub siła motoryczna w w celu zminimalizowania rozwoju nieodwracalnego stanu. Unikaj fluorochinolonów, w tym CIPRO 500 mg, u pacjentów, u których wcześniej wystąpiła neuropatia obwodowa [patrz DZIAŁANIA NIEPOŻĄDANE ].
Skutki dla centralnego układu nerwowego
Psychiatryczne działania niepożądane
Fluorochinolony, w tym CIPRO, wiązały się ze zwiększonym ryzykiem psychiatrycznych reakcji niepożądanych, w tym: psychozy toksycznej, reakcji psychotycznych przechodzących w myśli/myśli samobójcze, halucynacje lub paranoję; depresja lub samookaleczenia, takie jak usiłowanie lub popełnione samobójstwo; niepokój, pobudzenie lub nerwowość; splątanie, majaczenie, dezorientacja lub zaburzenia uwagi; bezsenność lub koszmary; upośledzenie pamięci. Reakcje te mogą wystąpić po pierwszej dawce. Należy doradzić pacjentom otrzymującym CIPRO natychmiastowe poinformowanie lekarza w przypadku wystąpienia takich reakcji, odstawienie leku i objęcie odpowiednią opieką.
Działania niepożądane ośrodkowego układu nerwowego
Fluorochinolony, w tym CIPRO 750 mg, wiązały się ze zwiększonym ryzykiem napadów padaczkowych (drgawek), zwiększonego ciśnienia śródczaszkowego (guz rzekomy mózgu), zawrotów głowy i drżenia. Wiadomo, że CIPRO, podobnie jak inne fluorochinolony, wywołuje drgawki lub obniża próg drgawkowy. Zgłaszano przypadki stanu padaczkowego. Podobnie jak w przypadku wszystkich fluorochinolonów, należy zachować ostrożność podczas stosowania CIPRO u pacjentów z padaczką oraz pacjentów z rozpoznanymi lub podejrzewanymi zaburzeniami OUN, które mogą predysponować do napadów drgawkowych lub obniżać próg drgawkowy (np. ciężka miażdżyca naczyń mózgowych, drgawki w wywiadzie, zmniejszony przepływ krwi w mózgu, zmiany w mózgu lub udar) lub w obecności innych czynników ryzyka, które mogą predysponować do napadów lub obniżać próg drgawkowy (na przykład niektóre leki, zaburzenia czynności nerek). Jeśli wystąpią drgawki, należy odstawić CIPRO 500 mg i zastosować odpowiednią opiekę [patrz DZIAŁANIA NIEPOŻĄDANE oraz INTERAKCJE Z LEKAMI ].
Zaostrzenie miastenii Gravis
Fluorochinolony, w tym CIPRO, mają działanie blokujące przewodnictwo nerwowo-mięśniowe i mogą nasilać osłabienie mięśni u pacjentów z miastenią. Po wprowadzeniu leku do obrotu stosowanie fluorochinolonów u pacjentów z miastenią było związane z poważnymi działaniami niepożądanymi, w tym zgonami i koniecznością wspomagania wentylacji. Unikaj CIPRO u pacjentów ze znaną historią miastenii [patrz DZIAŁANIA NIEPOŻĄDANE ].
Inne poważne, a czasem śmiertelne reakcje niepożądane
U pacjentów leczonych chinolonami, w tym CIPRO, zgłaszano inne ciężkie i czasami prowadzące do zgonu działania niepożądane, niektóre z powodu nadwrażliwości, a inne z powodu niepewnej etiologii. Zdarzenia te mogą mieć ciężki przebieg i zwykle występują po podaniu wielokrotnych dawek. Objawy kliniczne mogą obejmować jedno lub więcej z następujących:
- Gorączka, wysypka lub ciężkie reakcje dermatologiczne (na przykład martwica toksyczno-rozpływna naskórka, zespół Stevensa-Johnsona);
- zapalenie naczyń; ból stawów; ból mięśni; choroba posurowicza;
- Alergiczne zapalenie płuc;
- śródmiąższowe zapalenie nerek; ostra niewydolność lub niewydolność nerek;
- Zapalenie wątroby; żółtaczka; ostra martwica lub niewydolność wątroby;
- Anemia, w tym hemolityczna i aplastyczna; małopłytkowość, w tym zakrzepowa plamica małopłytkowa; leukopenia; agranulocytoza; pancytopenia; i/lub inne nieprawidłowości hematologiczne.
Należy natychmiast przerwać stosowanie leku CIPRO 500 mg po pierwszym pojawieniu się wysypki skórnej, żółtaczki lub jakichkolwiek innych objawów nadwrażliwości i wdrożonych środków wspomagających [patrz DZIAŁANIA NIEPOŻĄDANE ].
Reakcje nadwrażliwości
pacjentów leczonych fluorochinolonami, w tym CIPRO, zgłaszano ciężkie i czasami prowadzące do zgonu reakcje nadwrażliwości (anafilaktyczne), niektóre po podaniu pierwszej dawki. Niektórym reakcjom towarzyszyły zapaść sercowo-naczyniowa, utrata przytomności, mrowienie, obrzęk gardła lub twarzy, duszność, pokrzywka i swędzenie. Tylko kilku pacjentów miało historię reakcji nadwrażliwości. Poważne reakcje anafilaktyczne wymagają natychmiastowego leczenia epinefryną i innymi środkami resuscytacyjnymi, w tym tlenem, płynami dożylnymi, dożylnymi lekami przeciwhistaminowymi, kortykosteroidami, aminami presyjnymi oraz kontrolą dróg oddechowych, w tym intubacją, zgodnie ze wskazaniami [patrz DZIAŁANIA NIEPOŻĄDANE ].
Hepatotoksyczność
Podczas stosowania CIPRO zgłaszano przypadki ciężkiej hepatotoksyczności, w tym martwicy wątroby, zagrażającej życiu niewydolności wątroby i zgonów. Ostre uszkodzenie wątroby ma szybki początek (zakres 1–39 dni) i często wiąże się z nadwrażliwością. Wzór urazu może być wątrobowokomórkowy, cholestatyczny lub mieszany. Większość pacjentów, u których doszło do zgonu, była w wieku powyżej 55 lat. W przypadku wystąpienia jakichkolwiek oznak i objawów zapalenia wątroby (takich jak anoreksja, żółtaczka, ciemny mocz, świąd lub tkliwość brzucha), należy natychmiast przerwać leczenie.
Może wystąpić przejściowy wzrost aktywności aminotransferaz, fosfatazy alkalicznej lub żółtaczka cholestatyczna, szczególnie u pacjentów z wcześniejszym uszkodzeniem wątroby, leczonych preparatem CIPRO [patrz DZIAŁANIA NIEPOŻĄDANE ].
Ryzyko tętniaka i rozwarstwienia aorty
Badania epidemiologiczne wskazują na zwiększoną częstość występowania tętniaka i rozwarstwienia aorty w ciągu dwóch miesięcy po zastosowaniu fluorochinolonów, szczególnie u pacjentów w podeszłym wieku. Przyczyna zwiększonego ryzyka nie została zidentyfikowana. U pacjentów z rozpoznanym tętniakiem aorty lub u pacjentów z większym ryzykiem wystąpienia tętniaka aorty należy zachować produkt CIPRO 750 mg do stosowania tylko wtedy, gdy nie ma dostępnych alternatywnych metod leczenia przeciwbakteryjnego.
Poważne reakcje niepożądane przy jednoczesnej teofilinie
U pacjentów otrzymujących jednocześnie 250 mg CIPRO i teofilinę zgłaszano ciężkie i śmiertelne reakcje. Reakcje te obejmowały zatrzymanie akcji serca, drgawki, stan padaczkowy i niewydolność oddechową. Zdarzały się również nudności, wymioty, drżenie, drażliwość lub kołatanie serca.
Chociaż podobne ciężkie działania niepożądane zgłaszano u pacjentów otrzymujących samą teofilinę, nie można wyeliminować możliwości ich nasilenia przez CIPRO. Jeśli nie można uniknąć jednoczesnego stosowania, należy monitorować stężenie teofiliny w surowicy i odpowiednio dostosować dawkę [patrz INTERAKCJE Z LEKAMI ].
Biegunka wywołana przez Clostridioides
Przy stosowaniu prawie wszystkich leków przeciwbakteryjnych, w tym CIPRO, zgłaszano występowanie biegunki związanej z Clostridioides difficile (C. difficile) o przebiegu od łagodnej biegunki do zapalenia okrężnicy zakończonego zgonem. Leczenie środkami przeciwbakteryjnymi zmienia normalną florę okrężnicy, prowadząc do przerostu C. difficile.
C. difficile wytwarza toksyny A i B, które przyczyniają się do rozwoju CDAD. Izolaty C. difficile wytwarzające hipertoksyny powodują zwiększoną zachorowalność i śmiertelność, ponieważ zakażenia te mogą być oporne na leczenie przeciwbakteryjne i mogą wymagać kolektomii. CDAD należy rozważyć u wszystkich pacjentów, u których po zastosowaniu leków przeciwbakteryjnych wystąpi biegunka. Konieczna jest staranna historia choroby, ponieważ donoszono, że CDAD występuje w ciągu dwóch miesięcy po podaniu leków przeciwbakteryjnych.
W przypadku podejrzenia lub potwierdzenia CDAD, może być konieczne przerwanie ciągłego stosowania leków przeciwbakteryjnych, które nie są skierowane przeciwko C. difficile. Odpowiednie zarządzanie płynami i elektrolitami, suplementacja białka, leczenie przeciwbakteryjne C. difficile oraz przeprowadzenie oceny chirurgicznej zgodnie ze wskazaniami klinicznymi [patrz DZIAŁANIA NIEPOŻĄDANE ].
Wydłużenie odstępu QT
Niektóre fluorochinolony, w tym CIPRO 750 mg, były związane z wydłużeniem odstępu QT w elektrokardiogramie i przypadkami arytmii. Po wprowadzeniu produktu do obrotu zgłaszano przypadki torsade de pointes u pacjentów otrzymujących fluorochinolony, w tym CIPRO.
Unikaj CIPRO 1000 mg u pacjentów z rozpoznanym wydłużeniem odstępu QT, czynnikami ryzyka wydłużenia odstępu QT lub zaburzeniami typu torsade de pointes (na przykład wrodzony zespół długiego odstępu QT, nieskorygowana nierównowaga elektrolitowa, taka jak hipokaliemia lub hipomagnezemia i choroby serca, takie jak niewydolność serca, mięsień sercowy zawału serca lub bradykardii) oraz pacjentów otrzymujących leki przeciwarytmiczne klasy IA (chinidyna, prokainamid) lub leki przeciwarytmiczne klasy III (amiodaron, sotalol), trójpierścieniowe leki przeciwdepresyjne, makrolidy i leki przeciwpsychotyczne. Pacjenci w podeszłym wieku mogą być również bardziej podatni na wpływ leków na odstęp QT [patrz DZIAŁANIA NIEPOŻĄDANE , Używaj w określonych populacjach ].
Zaburzenia mięśniowo-szkieletowe u pacjentów pediatrycznych i skutki artropatii u zwierząt
CIPRO 250 mg jest wskazany u dzieci i młodzieży (w wieku poniżej 18 lat) wyłącznie w celu zapobiegania wąglikowi wziewnemu (po ekspozycji) i dżumie [patrz WSKAZANIA I ZASTOSOWANIE ]. Zaobserwowano zwiększoną częstość występowania działań niepożądanych w porównaniu z grupą kontrolną, w tym reakcji związanych ze stawami i/lub otaczającymi tkankami [patrz DZIAŁANIA NIEPOŻĄDANE ].
W badaniach przedklinicznych podawanie doustne CIPRO powodowało kulawiznę u niedojrzałych psów. Badanie histopatologiczne obciążonych stawów tych psów ujawniło trwałe uszkodzenia chrząstki. Pokrewne leki z grupy chinolonów powodują również nadżerki chrząstki obciążonych stawów i inne objawy artropatii u niedojrzałych zwierząt różnych gatunków [patrz Używaj w określonych populacjach oraz Toksykologia niekliniczna ].
Światłoczułość/Fototoksyczność
Umiarkowana lub ciężka reakcja nadwrażliwości na światło/fototoksyczność, z których ta ostatnia może objawiać się nadmiernymi reakcjami na oparzenia słoneczne (na przykład pieczenie, rumień, wysięk, pęcherzyki, pęcherze, obrzęk) obejmujące obszary wystawione na światło (zazwyczaj twarz, obszar „V” szyja, prostowniki przedramion, grzbiety dłoni) mogą być związane ze stosowaniem chinolonów, w tym CIPRO, po ekspozycji na słońce lub promieniowanie UV. Dlatego unikaj nadmiernej ekspozycji na te źródła światła. Przerwać CIPRO 250 mg, jeśli wystąpi fototoksyczność [patrz DZIAŁANIA NIEPOŻĄDANE ].
Rozwój bakterii lekoopornych
Przepisywanie CIPRO 250 mg tabletki i CIPRO zawiesina doustna w przypadku braku potwierdzonego lub silnie podejrzewanego zakażenia bakteryjnego lub wskazania profilaktycznego prawdopodobnie nie przyniesie korzyści pacjentowi i zwiększy ryzyko rozwoju bakterii lekoopornych.
Potencjalne zagrożenia związane z jednoczesnym stosowaniem leków metabolizowanych przez enzymy 1A2 cytochromu P450
CIPRO 750 mg jest inhibitorem wątrobowego szlaku enzymatycznego CYP1A2. Jednoczesne podawanie CIPRO i innych leków metabolizowanych głównie przez CYP1A2 (na przykład teofiliny, metyloksantyn, kofeiny, tyzanidyny, ropinirolu, klozapiny, olanzapiny i zolpidemu) powoduje zwiększenie stężenia jednocześnie podawanego leku w osoczu i może prowadzić do klinicznie istotnego farmakodynamiczne działania niepożądane jednocześnie podawanego leku [patrz INTERAKCJE Z LEKAMI oraz FARMAKOLOGIA KLINICZNA ].
Zakłócenia w terminowej diagnozie kiły
Nie wykazano skuteczności CIPRO 1000 mg w leczeniu kiły. Środki przeciwdrobnoustrojowe stosowane w dużych dawkach przez krótki czas w leczeniu rzeżączki mogą maskować lub opóźniać objawy inkubacji kiły. Wykonać badanie serologiczne w kierunku kiły u wszystkich pacjentów z rzeżączką w momencie rozpoznania. Wykonać kontrolne badanie serologiczne w kierunku kiły trzy miesiące po leczeniu CIPRO.
Krystaluria
Kryształy cyprofloksacyny były obserwowane rzadko w moczu ludzi, ale częściej w moczu zwierząt laboratoryjnych, który zwykle ma odczyn zasadowy [patrz Toksykologia niekliniczna ]. Krystaluria związana z CIPRO była zgłaszana rzadko u ludzi, ponieważ ludzki mocz jest zwykle kwaśny. Unikać zasadowości moczu u pacjentów otrzymujących CIPRO. Dobrze nawadniaj pacjentów, aby zapobiec tworzeniu się wysoce stężonego moczu [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Zaburzenia glukozy we krwi
Fluorochinolony, w tym CIPRO, były związane z zaburzeniami stężenia glukozy we krwi, w tym objawową hiperglikemią i hipoglikemią, zwykle u pacjentów z cukrzycą otrzymujących jednocześnie doustny środek hipoglikemizujący (na przykład gliburyd) lub insulinę. U tych pacjentów zaleca się dokładne monitorowanie stężenia glukozy we krwi. Zgłaszano ciężkie przypadki hipoglikemii prowadzące do śpiączki lub zgonu. Jeśli u pacjenta leczonego preparatem CIPRO wystąpi reakcja hipoglikemiczna, należy odstawić preparat CIPRO 750 mg i natychmiast rozpocząć odpowiednie leczenie [patrz DZIAŁANIA NIEPOŻĄDANE , INTERAKCJE Z LEKAMI ].
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( Przewodnik po lekach )
Poważne działania niepożądane
Należy doradzić pacjentom, aby w przypadku wystąpienia działań niepożądanych zaprzestali przyjmowania leku CIPRO 250 mg i skontaktowali się z lekarzem w celu uzyskania porady dotyczącej zakończenia pełnego cyklu leczenia innym lekiem przeciwbakteryjnym.
Należy poinformować pacjentów o następujących ciężkich działaniach niepożądanych, które były związane ze stosowaniem CIPRO lub innych fluorochinolonów:
- Unieruchamiające i potencjalnie nieodwracalne poważne działania niepożądane, które mogą wystąpić łącznie: Należy poinformować pacjentów, że wyłączenie i potencjalnie nieodwracalne poważne działania niepożądane, w tym zapalenie i zerwanie ścięgna, neuropatie obwodowe i wpływ na ośrodkowy układ nerwowy, są związane ze stosowaniem preparatu CIPRO 1000 mg i mogą wystąpić razem u tego samego pacjenta. Należy poinformować pacjentów, aby w przypadku wystąpienia działań niepożądanych natychmiast przerwali przyjmowanie CIPRO i skontaktowali się z lekarzem.
- Zapalenie ścięgna i zerwanie ścięgna: Poinstruuj pacjentów, aby skontaktowali się z lekarzem, jeśli odczuwają ból, obrzęk lub zapalenie ścięgna, osłabienie lub niemożność korzystania z jednego ze stawów; odpocznij i powstrzymaj się od ćwiczeń; i przerwać leczenie CIPRO 750 mg. Objawy mogą być nieodwracalne. Ryzyko wystąpienia ciężkich zaburzeń ścięgien podczas stosowania fluorochinolonów jest wyższe u starszych pacjentów, zwykle powyżej 60. roku życia, u pacjentów przyjmujących kortykosteroidy oraz u pacjentów po przeszczepieniu nerki, serca lub płuc.
- Neuropatie obwodowe: Należy poinformować pacjentów, że neuropatie obwodowe są związane ze stosowaniem cyprofloksacyny, objawy mogą wystąpić wkrótce po rozpoczęciu leczenia i mogą być nieodwracalne. Jeśli wystąpią objawy neuropatii obwodowej, w tym ból, pieczenie, mrowienie, drętwienie i/lub osłabienie, należy natychmiast przerwać stosowanie CIPRO i powiedzieć o skontaktowaniu się z lekarzem.
- Wpływ na ośrodkowy układ nerwowy (na przykład drgawki, zawroty głowy, oszołomienie, podwyższone ciśnienie śródczaszkowe): Należy poinformować pacjentów, że drgawki zgłaszano u pacjentów otrzymujących fluorochinolony, w tym cyprofloksacynę. Poinstruuj pacjentów, aby powiadomili swojego lekarza przed zażyciem tego leku, jeśli mają historię drgawek. Poinformuj pacjentów, że powinni wiedzieć, jak reagują na CIPRO, zanim zaczną obsługiwać samochód lub maszyny lub wykonywać inne czynności wymagające uwagi i koordynacji umysłowej. Poinstruuj pacjentów, aby powiadomili swojego lekarza, jeśli wystąpi uporczywy ból głowy z niewyraźnym widzeniem lub bez niego.
- Zaostrzenie miastenii Gravis: Poinstruuj pacjentów, aby informowali swojego lekarza o historii miastenii. Poinstruuj pacjentów, aby powiadomili swojego lekarza, jeśli wystąpią jakiekolwiek objawy osłabienia mięśni, w tym trudności z oddychaniem.
- Reakcje nadwrażliwości: Należy poinformować pacjentów, że cyprofloksacyna może wywoływać reakcje nadwrażliwości, nawet po podaniu pojedynczej dawki, oraz o odstawieniu leku przy pierwszych objawach wysypki skórnej, pokrzywki lub innych reakcji skórnych, przyspieszonego bicia serca, trudności w połykaniu lub oddychaniu, jakiegokolwiek obrzęku sugerującego obrzęk naczynioruchowy ( na przykład obrzęk warg, języka, twarzy, ucisk w gardle, chrypka) lub inne objawy reakcji alergicznej.
- Hepatotoksyczność: Należy poinformować pacjentów, że u pacjentów przyjmujących CIPRO zgłaszano ciężką hepatotoksyczność (w tym ostre zapalenie wątroby i zdarzenia śmiertelne). Poinstruuj pacjentów, aby poinformowali swojego lekarza, jeśli wystąpią jakiekolwiek oznaki lub objawy uszkodzenia wątroby, w tym: utrata apetytu, nudności, wymioty, gorączka, osłabienie, zmęczenie, tkliwość w prawym górnym kwadrancie, swędzenie, zażółcenie skóry i oczu, jasne wypróżnienia lub ciemny kolor moczu.
- Tętniak aorty i rozwarstwienie: Poinformuj pacjentów, aby szukali pomocy medycznej w nagłych wypadkach, jeśli wystąpią nagły ból w klatce piersiowej, brzuchu lub plecach.
- Biegunka: Biegunka jest częstym problemem powodowanym przez antybiotyki, który zwykle kończy się wraz z odstawieniem antybiotyku. Czasami po rozpoczęciu leczenia antybiotykami u pacjentów mogą pojawić się wodniste i krwawe stolce (ze skurczami żołądka i gorączką lub bez), nawet po dwóch lub więcej miesiącach od przyjęcia ostatniej dawki antybiotyku. W takim przypadku należy poinstruować pacjentów, aby jak najszybciej skontaktowali się z lekarzem.
- Wydłużenie odstępu QT: Poinstruuj pacjentów, aby informowali swojego lekarza o wszelkich osobistych lub rodzinnych wywiadach dotyczących wydłużenia odstępu QT lub stanów proarytmicznych, takich jak hipokaliemia, bradykardia lub niedawne niedokrwienie mięśnia sercowego; jeśli przyjmują jakiekolwiek leki przeciwarytmiczne klasy IA (chinidyna, prokainamid) lub klasy III (amiodaron, sotalol). Poinstruuj pacjentów, aby powiadomili swojego lekarza, jeśli wystąpią jakiekolwiek objawy wydłużenia odstępu QT, w tym przedłużone kołatanie serca lub utrata przytomności.
- Zaburzenia mięśniowo-szkieletowe u pacjentów pediatrycznych: Poinstruuj rodziców, aby przed zażyciem tego leku poinformowali lekarza dziecka, jeśli dziecko ma w przeszłości problemy ze stawami. Poinformuj rodziców pacjentów pediatrycznych, aby powiadomili lekarza dziecka o wszelkich problemach związanych ze stawami, które wystąpią podczas lub po leczeniu cipro 1000 mgfloksacyny [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
- Tyzanidyna: Poinstruuj pacjentów, aby nie stosowali cipro 250 mgfloksacyny, jeśli już przyjmują tyzanidynę. CIPRO zwiększa działanie tyzanidyny (Zanaflex®).
- Teofilina: Należy poinformować pacjentów, że cipro 250 mgfloksacyna CIPRO 1000 mg może nasilać działanie teofiliny. Mogą wystąpić zagrażające życiu objawy ze strony OUN i zaburzenia rytmu serca. Poradź pacjentom, aby natychmiast szukali pomocy medycznej, jeśli wystąpią drgawki, kołatanie serca lub trudności w oddychaniu.
- Kofeina: Należy poinformować pacjentów, że CIPRO 500 mg może nasilać działanie kofeiny. Istnieje możliwość kumulacji kofeiny, gdy produkty zawierające kofeinę są spożywane podczas przyjmowania chinolonów.
- Światłoczułość/Fototoksyczność: Należy poinformować pacjentów, że u pacjentów otrzymujących fluorochinolony zgłaszano nadwrażliwość/fototoksyczność. Poinformuj pacjentów, aby podczas przyjmowania chinolonów zminimalizowali lub unikali ekspozycji na naturalne lub sztuczne światło słoneczne (łóżka opalające lub zabiegi UVA/B). Jeśli pacjenci muszą przebywać na zewnątrz podczas stosowania chinolonów, poinstruuj ich, aby nosili luźne ubrania, które chronią skórę przed ekspozycją na słońce, i przedyskutuj z lekarzem inne środki ochrony przeciwsłonecznej. Jeśli wystąpi reakcja podobna do oparzenia słonecznego lub wykwity skórne, poinstruuj pacjentów, aby skontaktowali się z lekarzem.
- Zaburzenia glukozy we krwi: Należy poinformować pacjentów, że jeśli mają cukrzycę i są leczeni insuliną lub doustnym lekiem hipoglikemizującym i wystąpi reakcja hipoglikemiczna, powinni przerwać stosowanie preparatu CIPRO 250 mg i skonsultować się z lekarzem.
- Laktacja: przypadku wskazań innych niż wąglik wziewny (po ekspozycji), należy poinformować kobietę, że nie zaleca się karmienia piersią podczas leczenia preparatem Cipro oraz przez dodatkowe 2 dni po podaniu ostatniej dawki. Alternatywnie, kobieta może odciągać pokarm i wyrzucać leki podczas leczenia oraz przez dodatkowe 2 dni po przyjęciu ostatniej dawki [patrz Używaj w określonych populacjach ].
Odporność antybakteryjna
Należy poinformować pacjentów, że leki przeciwbakteryjne, w tym tabletki CIPRO 250 mg i zawiesina doustna CIPRO 1000 mg, powinny być stosowane wyłącznie w leczeniu zakażeń bakteryjnych. Nie leczą infekcji wirusowych (np. przeziębienia). Gdy CIPRO 500 mg tabletki i CIPRO 500 mg zawiesina doustna są przepisywane w celu leczenia infekcji bakteryjnej, pacjentom należy poinformować, że chociaż często czuje się lepiej na początku leczenia, lek należy przyjmować dokładnie zgodnie z zaleceniami. Pomijanie dawek lub nieukończenie pełnego cyklu leczenia może (1) zmniejszyć skuteczność natychmiastowego leczenia i (2) zwiększyć prawdopodobieństwo, że bakterie rozwiną się oporność i nie będą mogły być wyleczone za pomocą tabletek CIPRO 500 mg i zawiesiny doustnej CIPRO 250 mg lub innych środków przeciwbakteryjnych narkotyki w przyszłości.
Instrukcje administracyjne
Poinstruuj pacjenta
- Przed każdym użyciem energicznie wstrząsnąć CIPRO zawiesiną doustną przez około 15 sekund.
- Aby zawsze używać dołączonej miarki z podziałką z oznaczeniami ½ (2,5 ml) i 1/1 (5 ml), aby uzyskać dokładną dawkę.
- Po użyciu miarkę należy umyć pod bieżącą wodą z dodatkiem płynu do naczyń i dokładnie wysuszyć.
- Nie żuć mikrokapsułek, ale połykać je w całości.
- Ta woda może być później zabrana.
- Prawidłowo zamknąć butelkę po każdym użyciu, zgodnie z instrukcjami na nakrętce.
- Po zakończeniu leczenia nie należy ponownie stosować CIPRO 1000 mg zawiesiny doustnej.
Należy poinformować pacjentów, że preparat CIPRO 250 mg można przyjmować z posiłkiem lub bez posiłku.
Należy poinformować pacjentów, aby podczas przyjmowania leku CIPRO obficie pili płyny, aby uniknąć tworzenia się silnie stężonego moczu i tworzenia się kryształów w moczu.
Należy poinformować pacjentów, że leki zobojętniające zawierające magnez lub glin, a także sukralfat, kationy metali, takich jak żelazo, oraz preparaty multiwitaminowe z cynkiem lub didanozyną należy przyjmować co najmniej dwie godziny przed lub sześć godzin po podaniu preparatu CIPRO 1000 mg. CIPRO nie powinien być przyjmowany z produktami mlecznymi (takimi jak mleko lub jogurt) lub samymi sokami wzbogacanymi wapniem, ponieważ wchłanianie cyprofloksacyny może być znacznie zmniejszone; jednak CIPRO 500 mg można przyjmować z posiłkiem zawierającym te produkty.
Należy poinformować pacjentów, że w przypadku pominięcia dawki należy ją przyjąć w dowolnym momencie, ale nie później niż 6 godzin przed kolejną zaplanowaną dawką. Jeśli do następnej dawki pozostało mniej niż 6 godzin, nie należy przyjmować pominiętej dawki, a leczenie należy kontynuować zgodnie z zaleceniami z następną zaplanowaną dawką. Nie należy przyjmować podwójnych dawek w celu wyrównania pominiętej dawki.
Należy doradzić pacjentom, że tabletki CIPRO 500 mg (250 mg i 500 mg) są oznaczone punktacją i można je podzielić na pół w linii z podziałką, aby zapewnić odpowiednio moc 125 mg lub 250 mg.
Interakcje leków Doustne leki przeciwcukrzycowe
Poinformuj pacjentów, że podczas jednoczesnego podawania cypro 250 mgfloksacyny i doustnych leków przeciwcukrzycowych zgłaszano przypadki hipoglikemii; jeśli podczas stosowania leku CIPRO 750 mg wystąpi niski poziom cukru we krwi, należy poinstruować ich, aby skonsultowali się z lekarzem i że może być konieczna zmiana leku przeciwbakteryjnego.
Badania wąglika i zarazy
Poinformować pacjentów otrzymujących CIPRO z powodu tych schorzeń, że ze względów wykonalności nie można przeprowadzić badań skuteczności u ludzi. Dlatego zatwierdzenie tych stanów oparto na badaniach skuteczności przeprowadzonych na zwierzętach.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Przeprowadzono osiem testów mutagenności in vitro z użyciem cypro 500mgfloksacyny, a wyniki testów przedstawiono poniżej:
- Test na salmonellę/mikrosom (ujemny)
- Test naprawy DNA E. coli (ujemny)
- Test mutacji do przodu komórek chłoniaka myszy (pozytywny)
- Test HGPRT komórki V79 dla chomika chińskiego (ujemny)
- Test transformacji komórek zarodkowych chomika syryjskiego (ujemny)
- Test mutacji punktowej Saccharomyces cerevisiae (ujemny)
- Saccharomyces cerevisiae Krzyżowanie mitotyczne i test konwersji genów (ujemny)
- Test naprawy hepatocytów szczurzych DNA (pozytywny)
Zatem 2 z 8 testów były pozytywne, ale wyniki następujących 3 systemów testowych in vivo dały wyniki negatywne:
- Test naprawy hepatocytów szczurzych DNA
- Test mikrojądrowy (myszy)
- Dominujący test śmiercionośny (myszy)
Długotrwałe badania rakotwórczości na szczurach i myszach nie wykazały żadnych działań rakotwórczych ani rakotwórczych cypro 500 mgfloksacyny w dziennych dawkach doustnych do 250 mg/kg i 750 mg/kg odpowiednio u szczurów i myszy (około 1,7 i 2,5 razy). najwyższą zalecaną dawkę terapeutyczną na podstawie, odpowiednio, powierzchni ciała).
Wyniki badań fotokorakotwórczości wskazują, że cipro 1000 mgfloksacyna nie skraca czasu do pojawienia się guzów skóry wywołanych promieniowaniem UV w porównaniu z kontrolą z nośnikiem. Myszy bezwłose (Skh-1) eksponowano na światło UVA przez 3,5 godziny pięć razy co dwa tygodnie przez okres do 78 tygodni, jednocześnie otrzymując cyprofloksacynę. Czas do rozwoju pierwszych guzów skóry wynosił 50 tygodni u myszy leczonych jednocześnie UVA i 1000 mg floksacyny cypro (dawka u myszy w przybliżeniu równa maksymalnej zalecanej dawce u ludzi w oparciu o powierzchnię ciała), w przeciwieństwie do 34 tygodni, gdy zwierzęta były leczone jednocześnie UVA i pojazd. Czas do rozwoju guzów skóry wahał się od 16 tygodni do 32 tygodni u myszy leczonych jednocześnie UVA i innymi chinolonami.5
W tym modelu myszy leczone samą cyprofloksacyną nie rozwinęły guzów skóry ani ogólnoustrojowych. Nie ma danych z podobnych modeli wykorzystujących myszy pigmentowane i/lub myszy z pełną sierścią. Kliniczne znaczenie tych wyników dla ludzi nie jest znane.
Badania płodności przeprowadzone na samcach i samicach szczurów, którym podawano doustne dawki cypro 250 mgfloksacyny do 100 mg/kg (około 0,6-krotność największej zalecanej doustnej dawki terapeutycznej w oparciu o powierzchnię ciała) nie wykazały objawów zaburzeń. Samce szczurów otrzymywały doustnie cyprofloksacynę przez 10 tygodni przed kryciem, a samicom przez 3 tygodnie przed kryciem do 7. dnia ciąży.
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
Długotrwałe, kilkudziesięcioletnie doświadczenie ze stosowaniem cypro 1000 mgfloksacyny u kobiet w ciąży, oparte na dostępnych opublikowanych informacjach z opisów przypadków, badań kontrolnych przypadków i badań obserwacyjnych dotyczących cypro 1000 mgfloksacyny podawanego w czasie ciąży, nie wykazało żadnego związanego z lekiem ryzyka wystąpienia poważnych wad wrodzonych, poronienia lub działań niepożądanych. wyniki dla matki lub płodu (patrz Dane ). Doustne podawanie cipro 500 mgfloksacyny podczas organogenezy w dawkach do 100 mg/kg ciężarnym myszom i szczurom oraz do 30 mg/kg ciężarnym królikom nie powodowało wad rozwojowych płodu (patrz Dane ). Dawki te były do 0,3, 0,6 i 0,4 razy większe od maksymalnej zalecanej klinicznej dawki doustnej odpowiednio u myszy, szczurów i królików, w oparciu o powierzchnię ciała. Szacowane ryzyko tła poważnych wad wrodzonych i poronienia dla wskazanej populacji jest nieznane. Wszystkie ciąże wiążą się z ryzykiem wady wrodzonej, utraty lub innych niekorzystnych skutków. W ogólnej populacji USA szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2 do 4% i 15 do 20%.
Dane
Dane ludzkie
Chociaż dostępne badania nie mogą jednoznacznie ustalić braku ryzyka, opublikowane dane z prospektywnych badań obserwacyjnych na przestrzeni kilkudziesięciu lat nie wykazały związku ze stosowaniem cipro 250 mgfloksacyny podczas ciąży i poważnych wad wrodzonych, poronienia lub niekorzystnych wyników dla matki lub płodu. Dostępne badania mają ograniczenia metodologiczne, w tym małą wielkość próby, a niektóre z nich nie są specyficzne dla cyprofloksacyny. Kontrolowane prospektywne badanie obserwacyjne obejmowało 200 kobiet narażonych na fluorochinolony (52,5% narażonych na cipro 250 mgfloksacynę i 68% narażonych na ekspozycję w pierwszym trymestrze ciąży) w czasie ciąży. Narażenie in utero na fluorochinolony podczas embriogenezy nie wiązało się ze zwiększonym ryzykiem poważnych wad rozwojowych. Zgłoszone częstości występowania poważnych wad wrodzonych wynosiły 2,2% w grupie fluorochinolonów i 2,6% w grupie kontrolnej (częstość występowania poważnych wad rozwojowych w tle wynosi 1–5%). Wskaźniki samoistnych poronień, wcześniactwa i niskiej masy urodzeniowej nie różniły się między grupami i nie stwierdzono klinicznie istotnych dysfunkcji układu mięśniowo-szkieletowego do pierwszego roku życia u dzieci narażonych na cipro 500 mgfloksacynę.
innym prospektywnym badaniu obserwacyjnym odnotowano 549 ciąż z ekspozycją na fluorochinolony (93% ekspozycji w pierwszym trymestrze). Było 70 ekspozycji na cipro 500mgfloksacynę, wszystkie w pierwszym trymestrze ciąży. Częstość występowania wad rozwojowych wśród żywo urodzonych dzieci narażonych na działanie cipro 750 mgfloksacyny i fluorochinolony ogólnie mieściła się w podstawowych zakresach częstości występowania. Nie znaleziono konkretnych wzorców wad wrodzonych. W badaniu nie ujawniono żadnych wyraźnych działań niepożądanych związanych z narażeniem in utero na cyprofloksacynę.
Nie zaobserwowano różnic w częstości wcześniactwa, samoistnych poronień ani masy urodzeniowej u kobiet narażonych na cyprofloksacynę w czasie ciąży. Jednak te małe badania epidemiologiczne po wprowadzeniu do obrotu, z których większość doświadczeń pochodzi z krótkoterminowej ekspozycji w pierwszym trymestrze, są niewystarczające do oceny ryzyka rzadszych wad lub do sformułowania wiarygodnych i ostatecznych wniosków dotyczących bezpieczeństwa stosowania cyprofloksacyny u kobiet w ciąży i ich rozwijających się płodów. .
Dane zwierząt
Badania toksykologiczne rozwojowe przeprowadzono z użyciem cipro 500 mgfloksacyny u szczurów, myszy i królików. U szczurów i myszy doustne dawki do 100 mg/kg podawane podczas organogenezy (dni ciąży, GD, 6-17) nie wiązały się z niepożądanymi wynikami rozwojowymi, w tym toksycznym działaniem na zarodek i płód lub wadami rozwojowymi. U szczurów i myszy dawka 100 mg/kg jest w przybliżeniu 0,6 i 0,3 razy większa od maksymalnej dobowej dawki doustnej u ludzi (1500 mg/dobę) w oparciu o powierzchnię ciała, odpowiednio. W serii badań toksykologii rozwojowej królików otrzymywał doustnie lub dożylnie cipro 250 mgfloksacyny przez jeden z następujących 5-dniowych okresów: GD 6 do 10, GD 10 do 14 lub GD 14 do 18, w celu objęcia okresu organogenezy. Była to próba złagodzenia nietolerancji żołądkowo-jelitowej obserwowanej u królików otrzymujących leki przeciwbakteryjne, objawiającej się zmniejszeniem spożycia pokarmu przez matkę i utratą masy ciała, co może prowadzić do resorpcji zarodka i płodu lub samoistnego poronienia. Doustna dawka cypro 750 mg floksacyny wynosząca 100 mg/kg (około 1,3-krotność najwyższej zalecanej klinicznej dawki doustnej w oparciu o powierzchnię ciała) powodowała nadmierną toksyczność matczyną, zakłócając ocenę płodu. Dawka doustna 30 mg/kg (około 0,4 razy większa od najwyższej zalecanej klinicznej dawki doustnej) wiązała się z zahamowaniem przyrostu masy ciała matki i płodu, ale nie zaobserwowano wad rozwojowych płodu. Dożylne podawanie dawek do 20 mg/kg (około 0,3-krotność najwyższej zalecanej klinicznej dawki doustnej w oparciu o powierzchnię ciała) ciężarnym królikom nie było toksyczne dla matki i nie zaobserwowano toksycznego wpływu na zarodek i płód ani wad rozwojowych płodu.
badaniach okołoporodowych i poporodowych szczury otrzymywały 1000 mg floksacyny cypro w dawce do 200 mg/kg/dobę (doustnie) lub do 30 mg/kg/dobę (podskórnie) od 16 do 22 dnia po porodzie. Dawka 200 mg/kg stanowi około 1,3-krotność maksymalnej zalecanej klinicznej dawki doustnej w oparciu o powierzchnię ciała. Nie zaobserwowano toksyczności matczynej ani niekorzystnego wpływu na wzrost i rozwój młodych, w tym nie zaobserwowano oznak artropatii tylnych stawów nóg. Wykazano, że cyprofloksacyna i inne chinolony powodują artropatię u niedojrzałych zwierząt większości badanych gatunków przy bezpośrednim podaniu [patrz OSTRZEŻENIA I ŚRODKI oraz Toksykologia niekliniczna ].
Laktacja
Podsumowanie ryzyka
Z opublikowanego piśmiennictwa wynika, że cypro 1000 mgfloksacyny występuje w mleku ludzkim po podaniu dożylnym i doustnym. Brak informacji dotyczących wpływu CIPRO na produkcję mleka lub niemowlęta karmione piersią. Ze względu na potencjalne ryzyko poważnych działań niepożądanych u niemowląt karmionych piersią, w tym artropatii, wykazanej w badaniach na młodych zwierzętach [patrz Używaj w określonych populacjach (Uwagi kliniczne)], w większości wskazań kobieta karmiąca piersią może rozważyć odciąganie i wyrzucanie mleka matki podczas leczenia preparatem CIPRO 500 mg i dodatkowe dwa dni (pięć okresów półtrwania) po ostatniej dawce. Alternatywnie poinformuj kobietę, że nie zaleca się karmienia piersią podczas leczenia preparatem CIPRO i przez dodatkowe dwa dni (pięć okresów półtrwania) po ostatniej dawce.
Jednak w przypadku wąglika wziewnego (po narażeniu), podczas incydentu skutkującego narażeniem na wąglik, ocena ryzyka i korzyści kontynuacji karmienia piersią w czasie, gdy matka (i potencjalnie niemowlę) jest (są) na CIPRO, może być akceptowalna [patrz DAWKOWANIE I SPOSÓB PODAWANIA , Zastosowanie pediatryczne , oraz Studia kliniczne ]. Należy wziąć pod uwagę korzyści rozwojowe i zdrowotne wynikające z karmienia piersią, a także kliniczne zapotrzebowanie matki na CIPRO oraz wszelkie potencjalne niekorzystne skutki stosowania CIPRO 1000 mg na dziecko karmione piersią lub związane z tym schorzeniem matki.
Rozważania kliniczne
Cipro 1000 mgfloksacyna może powodować zmiany flory jelitowej u niemowląt karmionych piersią. Poradzić kobiecie, aby monitorowała niemowlę karmione piersią pod kątem luźnych lub krwawych stolców i kandydozy (pleśniawki, pieluszkowe).
Zastosowanie pediatryczne
Chociaż skuteczny w badaniach klinicznych, CIPRO 750 mg nie jest lekiem pierwszego wyboru w populacji pediatrycznej ze względu na zwiększoną częstość występowania działań niepożądanych w porównaniu z grupą kontrolną. Chinolony, w tym CIPRO, powodują artropatię (artralgia, zapalenie stawów) u młodych zwierząt [patrz OSTRZEŻENIA I ŚRODKI oraz Toksykologia niekliniczna ].
Powikłane zakażenie dróg moczowych i odmiedniczkowe zapalenie nerek
CIPRO 250 mg jest wskazany w leczeniu cUTI i odmiedniczkowego zapalenia nerek wywołanego przez Escherichia coli u dzieci w wieku od 1 do 17 lat. Chociaż skuteczny w badaniach klinicznych, CIPRO 500 mg nie jest lekiem pierwszego wyboru w populacji pediatrycznej ze względu na zwiększoną częstość występowania działań niepożądanych w porównaniu z grupą kontrolną, w tym zdarzeń związanych ze stawami i/lub otaczającymi tkankami [patrz DZIAŁANIA NIEPOŻĄDANE oraz Studia kliniczne ].
Wąglik wziewny (po ekspozycji)
CIPRO 750 mg jest wskazany do stosowania w wągliku wziewnym u dzieci od urodzenia do 17 roku życia (po ekspozycji). Ocena korzyści i ryzyka wskazuje, że podawanie cyprofloksacyny pacjentom pediatrycznym jest właściwe [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz Studia kliniczne ].
Plaga
CIPRO 500 mg jest wskazany u dzieci od urodzenia do 17 roku życia w leczeniu dżumy, w tym dżumy płucnej i posocznicy wywołanej przez Yersinia pestis (Y. pestis) oraz w profilaktyce dżumy. Ze względów wykonalności nie można było przeprowadzić badań skuteczności CIPRO u ludzi z dżumą płucną. Dlatego zatwierdzenie tego wskazania oparto na badaniu skuteczności przeprowadzonym na zwierzętach. Ocena korzyści i ryzyka wskazuje, że podawanie preparatu CIPRO pacjentom pediatrycznym jest właściwe [patrz WSKAZANIA I ZASTOSOWANIE , DAWKOWANIE I SPOSÓB PODAWANIA oraz Studia kliniczne ].
Zastosowanie geriatryczne
Pacjenci w podeszłym wieku są narażeni na zwiększone ryzyko wystąpienia ciężkich zaburzeń ścięgien, w tym zerwania ścięgna, podczas leczenia fluorochinolonami, takimi jak CIPRO. Ryzyko to jest dodatkowo zwiększone u pacjentów otrzymujących jednocześnie leczenie kortykosteroidami. Zapalenie ścięgna lub zerwanie ścięgna może obejmować Achillesa, rękę, ramię lub inne miejsca ścięgna i może wystąpić podczas lub po zakończeniu terapii; zgłaszano przypadki występujące do kilku miesięcy po leczeniu fluorochinolonem. Należy zachować ostrożność przepisując preparat CIPRO 500 mg pacjentom w podeszłym wieku, zwłaszcza tym, którzy przyjmują kortykosteroidy. Należy poinformować pacjentów o tym potencjalnym działaniu niepożądanym i zalecić im przerwanie stosowania preparatu CIPRO 500 mg i skontaktowanie się z lekarzem w przypadku wystąpienia jakichkolwiek objawów zapalenia ścięgna lub zerwania ścięgna [patrz OSTRZEŻENIE W PUDEŁKU , OSTRZEŻENIA I ŚRODKI , oraz DZIAŁANIA NIEPOŻĄDANE ].
Badania epidemiologiczne donoszą o zwiększonej częstości występowania tętniaka i rozwarstwienia aorty w ciągu dwóch miesięcy po zastosowaniu fluorochinolonów, szczególnie u pacjentów w podeszłym wieku [patrz OSTRZEŻENIA I ŚRODKI ].
retrospektywnej analizie 23 kontrolowanych wielokrotnych badań klinicznych CIPRO, obejmujących ponad 3500 pacjentów leczonych cyprofloksacyną, 25% pacjentów było w wieku co najmniej 65 lat, a 10% było w wieku co najmniej 75 lat. Nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między tymi pacjentami a młodszymi pacjentami, a inne zgłoszone doświadczenia kliniczne nie wykazały różnic w odpowiedziach między pacjentami w podeszłym wieku i młodszymi, ale nie można wykluczyć większej wrażliwości niektórych osób starszych na jakąkolwiek terapię lekową. Wiadomo, że cyprofloksacyna jest w znacznym stopniu wydalana przez nerki, a ryzyko działań niepożądanych może być większe u pacjentów z zaburzeniami czynności nerek. Nie ma konieczności zmiany dawkowania u pacjentów w wieku powyżej 65 lat z prawidłową czynnością nerek. Jednakże, ponieważ niektóre osoby starsze doświadczają upośledzenia czynności nerek z powodu ich zaawansowanego wieku, należy zachować ostrożność przy doborze dawki u pacjentów w podeszłym wieku, a monitorowanie czynności nerek może być przydatne u tych pacjentów [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz FARMAKOLOGIA KLINICZNA ].
Ogólnie rzecz biorąc, pacjenci w podeszłym wieku mogą być bardziej podatni na wpływ leków na odstęp QT. Dlatego należy zachować ostrożność podczas stosowania preparatu CIPRO 500 mg z jednoczesnymi lekami, które mogą powodować wydłużenie odstępu QT (na przykład leki przeciwarytmiczne klasy IA lub klasy III) lub u pacjentów z czynnikami ryzyka torsade de pointes (na przykład znane wydłużenie odstępu QT). , nieskorygowana hipokaliemia) [patrz OSTRZEŻENIA I ŚRODKI ].
Zaburzenia czynności nerek
Cipro 500 mgfloksacyna jest wydalana głównie przez nerki; jednak lek jest również metabolizowany i częściowo usuwany przez drogi żółciowe wątroby i jelita. Te alternatywne drogi eliminacji leku wydają się kompensować zmniejszone wydalanie nerkowe u pacjentów z zaburzeniami czynności nerek. Niemniej jednak zaleca się pewną modyfikację dawkowania, szczególnie u pacjentów z ciężkimi zaburzeniami czynności nerek [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz FARMAKOLOGIA KLINICZNA ].
Niewydolność wątroby
We wstępnych badaniach u pacjentów ze stabilną przewlekłą marskością wątroby nie zaobserwowano istotnych zmian w farmakokinetyce cyprofloksacyny. Nie badano farmakokinetyki cipro 500 mgfloksacyny u pacjentów z ostrą niewydolnością wątroby.
PRZEDAWKOWAĆ
W przypadku ostrego przedawkowania w niektórych przypadkach zgłaszano odwracalną toksyczność nerkową. Opróżnij żołądek przez wywołanie wymiotów lub płukanie żołądka. Uważnie obserwować pacjenta i stosować leczenie wspomagające, w tym monitorować czynność nerek, pH moczu i w razie potrzeby zakwasić, aby zapobiec krystalurii i podawać leki zobojętniające zawierające magnez, glin lub wapń, które mogą zmniejszać wchłanianie cypro 750 mgfloksacyny. Należy utrzymywać odpowiednie nawodnienie. Tylko niewielka ilość cypro 250mgfloksacyny (mniej niż 10%) jest usuwana z organizmu po hemodializie lub dializie otrzewnowej.
PRZECIWWSKAZANIA
Nadwrażliwość
CIPRO 1000mg jest przeciwwskazany u osób z nadwrażliwością na cipro 750mgfloksacynę, którykolwiek z chinolonowych leków przeciwbakteryjnych lub którykolwiek ze składników produktu [patrz OSTRZEŻENIA I ŚRODKI ].
Tyzanidyna
Jednoczesne podawanie z tyzanidyną jest przeciwwskazane [patrz INTERAKCJE Z LEKAMI ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Ciprofloksacyna należy do klasy środków przeciwbakteryjnych fluorochinolonów [patrz Mikrobiologia ].
Farmakokinetyka
Wchłanianie
Całkowita biodostępność cipro 500 mgfloksacyny po podaniu doustnym wynosi około 70%, bez znacznej utraty w wyniku metabolizmu pierwszego przejścia. Maksymalne stężenia cyprofloksacyny w surowicy (Cmax) i pole pod krzywą (AUC) przedstawiono na wykresie dla zakresu dawek od 250 mg do 1000 mg (Tabela 12).
Maksymalne stężenia w surowicy są osiągane 1 do 2 godzin po podaniu doustnym. Średnie stężenia 12 godzin po podaniu 250, 500 lub 750 mg wynoszą odpowiednio 0,1, 0,2 i 0,4 µg/ml. Okres półtrwania w fazie eliminacji z surowicy u osób z prawidłową czynnością nerek wynosi około 4 godziny. Stężenia w surowicy wzrastają proporcjonalnie do dawek do 1000 mg.
Wykazano, że dawka doustna 500 mg podawana co 12 godzin daje wartość AUC równoważną wartości uzyskiwanej po wlewie dożylnym 400 mg CIPRO 1000 mg podawanym przez 60 minut co 12 godzin. Wykazano, że dawka doustna 750 mg podawana co 12 godzin daje AUC w stanie stacjonarnym równoważne wartości uzyskiwanej po wlewie dożylnym 400 mg podawanym przez 60 minut co 8 godzin. Dawka doustna 750 mg daje Cmax podobne do obserwowanego dla dawki dożylnej 400 mg (Tabela 13). Dawka doustna 250 mg podawana co 12 godzin daje wartość AUC odpowiadającą wartości uzyskanej po wlewie 200 mg preparatu CIPRO 1000 mg co 12 godzin.
Żywność
Gdy tabletka CIPRO jest podawana jednocześnie z posiłkiem, następuje opóźnienie wchłaniania leku, co powoduje, że maksymalne stężenia pojawiają się bliżej 2 godzin po podaniu, a nie 1 godziny, podczas gdy nie obserwuje się opóźnienia, gdy CIPRO 750 mg w postaci zawiesiny podaje się z posiłkiem. . Całkowite wchłanianie tabletek CIPRO 1000 mg lub zawiesiny CIPRO 500 mg nie jest jednak znacząco zmienione. Pokarm nie wpływa również na farmakokinetykę cipro 750 mgfloksacyny podawanej w postaci zawiesiny. Należy unikać jednoczesnego podawania preparatu CIPRO z produktami mlecznymi (takimi jak mleko lub jogurt) lub samymi sokami wzbogacanymi wapniem, ponieważ możliwe jest zmniejszenie wchłaniania; jednak CIPRO 1000 mg można przyjmować z posiłkiem zawierającym te produkty
Przy podawaniu doustnym dawka 500 mg podana w postaci 10 ml 5% zawiesiny CIPRO (zawierającej 250 mg cyprofloksacyny/5 ml) jest biorównoważna tabletce 500 mg. Objętość 10 ml 5% zawiesiny CIPRO 1000 mg (zawierającej 250 mg cyprofloksacyny/5 ml) jest biorównoważna objętości 5 ml zawiesiny 10% CIPRO 750 mg (zawierającej 500 mg cyprofloksacyny 1000 mg floksacyny/5 ml).
Dystrybucja
Wiązanie cyprofloksacyny z białkami surowicy wynosi od 20% do 40%, co prawdopodobnie nie jest wystarczająco wysokie, aby powodować znaczące interakcje wiązania białek z innymi lekami.
Po podaniu doustnym cypro 250mgfloksacyna jest szeroko dystrybuowana w całym organizmie. Stężenia w tkankach często przekraczają stężenia w surowicy zarówno u mężczyzn, jak iu kobiet, zwłaszcza w tkance narządów płciowych, w tym w prostacie. Ciprofloksacyna występuje w postaci aktywnej w ślinie, wydzielinie z nosa i oskrzeli, błonie śluzowej zatok, plwocinie, płynie z pęcherzy skórnych, limfie, płynie otrzewnowym, żółci i wydzielinie gruczołu krokowego. Cipro 500 mgfloksacyny wykryto również w płucach, skórze, tłuszczu, mięśniach, chrząstkach i kościach. Lek dyfunduje do płynu mózgowo-rdzeniowego (CSF); jednak stężenia w płynie mózgowo-rdzeniowym są na ogół mniejsze niż 10% maksymalnych stężeń w surowicy. Niskie poziomy leku wykryto w cieczy wodnistej i ciele szklistym oka.
Metabolizm
moczu ludzkim zidentyfikowano cztery metabolity, które łącznie stanowią około 15% dawki doustnej. Metabolity wykazują aktywność przeciwdrobnoustrojową, ale są mniej aktywne niż niezmieniony cipro 500mgfloksacyna. Cipro 500 mgfloksacyna jest inhibitorem metabolizmu, w którym pośredniczy ludzki cytochrom P450 1A2 (CYP1A2). Jednoczesne podawanie cyprofloksacyny z innymi lekami metabolizowanymi głównie przez CYP1A2 powoduje zwiększenie stężenia tych leków w osoczu i może prowadzić do klinicznie istotnych działań niepożądanych jednocześnie podawanego leku [patrz PRZECIWWSKAZANIA , OSTRZEŻENIA I ŚRODKI , oraz INTERAKCJE Z LEKAMI ].
Wydalanie
Okres półtrwania w fazie eliminacji z surowicy u osób z prawidłową czynnością nerek wynosi około 4 godziny. Około 40 do 50% podanej doustnie dawki jest wydalane z moczem w postaci niezmienionej. Po podaniu doustnym 250 mg, stężenie cypro 500 mgfloksacyny w moczu zwykle przekracza 200 µg/ml w ciągu pierwszych dwóch godzin i wynosi około 30 µg/ml w 8 do 12 godzin po podaniu. Wydalanie cyprofloksacyny z moczem jest praktycznie całkowite w ciągu 24 godzin po podaniu. Klirens nerkowy cypro 250 mgfloksacyny, który wynosi około 300 ml/minutę, przekracza normalną szybkość przesączania kłębuszkowego wynoszącą 120 ml/minutę. Wydaje się zatem, że aktywna sekrecja kanalikowa odgrywa istotną rolę w jej eliminacji. Jednoczesne podawanie probenecydu z cyprofloksacyną powoduje około 50% zmniejszenie klirensu nerkowego cyprofloksacyny i 50% zwiększenie jej stężenia w krążeniu ogólnoustrojowym.
Chociaż stężenia cypro 250 mgfloksacyny w żółci są kilkakrotnie wyższe niż stężenia w surowicy po podaniu doustnym, tylko niewielka ilość podanej dawki jest odzyskiwana z żółci w postaci niezmienionej. Dodatkowe 1% do 2% dawki jest odzyskiwane z żółci w postaci metabolitów. Około 20% do 35% dawki doustnej jest wydalane z kału w ciągu 5 dni po podaniu. Może to wynikać z klirensu żółciowego lub wydalania przezjelitowego.
Określone populacje
Osoby starsze
Badania farmakokinetyczne doustnej (pojedyncza dawka) i dożylnej (pojedyncza i wielokrotna dawka) postaci cypro 250 mgfloksacyny wskazują, że stężenie cyprofloksacyny w osoczu jest wyższe u osób w podeszłym wieku (powyżej 65 lat) w porównaniu z młodymi dorosłymi. Chociaż Cmax jest zwiększone o 16% do 40%, wzrost średniej wartości AUC wynosi około 30% i można przynajmniej częściowo przypisać zmniejszeniu klirensu nerkowego u osób w podeszłym wieku. Okres półtrwania w fazie eliminacji jest tylko nieznacznie (~20%) wydłużony u osób starszych. Różnice te nie są uważane za istotne klinicznie [patrz Używaj w określonych populacjach ].
Zaburzenia czynności nerek
U pacjentów z upośledzoną czynnością nerek okres półtrwania cyprofloksacyny jest nieznacznie wydłużony. Może być konieczne dostosowanie dawki [patrz Używaj w określonych populacjach oraz DAWKOWANIE I SPOSÓB PODAWANIA ].
Niewydolność wątroby
We wstępnych badaniach u pacjentów ze stabilną przewlekłą marskością wątroby nie zaobserwowano istotnych zmian w farmakokinetyce cyprofloksacyny. Kinetyka cipro 750 mgfloksacyny u pacjentów z ostrą niewydolnością wątroby nie została w pełni zbadana.
Pediatria
Tabeli 14 zestawiono parametry farmakokinetyczne u dzieci w wieku poniżej 1 do mniej niż 12 lat otrzymujących leczenie dożylne.
Wartości te mieszczą się w zakresie zgłaszanym dla dorosłych w dawkach terapeutycznych. Na podstawie populacyjnej analizy farmakokinetycznej pacjentów pediatrycznych z różnymi zakażeniami przewidywany średni okres półtrwania u dzieci wynosi około 4–5 godzin, a biodostępność zawiesiny doustnej wynosi około 60%.
Interakcje między lekami
Leki zobojętniające sok żołądkowy
Jednoczesne podawanie leków zobojętniających zawierających wodorotlenek magnezu lub wodorotlenek glinu może zmniejszyć biodostępność cipro 500 mgfloksacyny nawet o 90% [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz INTERAKCJE Z LEKAMI ].
Antagoniści receptora histaminowego H2
Wydaje się, że antagoniści receptora histaminowego H2 nie mają znaczącego wpływu na biodostępność cipro 250 mgfloksacyny.
Metronidazol
Stężenia cyprofloksacyny i metronidazolu w surowicy nie uległy zmianie podczas jednoczesnego podawania tych dwóch leków.
Tyzanidyna
badaniu farmakokinetycznym ekspozycja ogólnoustrojowa na tyzanidynę (pojedyncza dawka 4 mg) była znacząco zwiększona (Cmax 7-krotnie, AUC 10-krotnie), gdy lek podawano jednocześnie z CIPRO (500 mg dwa razy na dobę przez 3 dni). Jednoczesne podawanie tyzanidyny i CIPRO jest przeciwwskazane ze względu na nasilenie hipotensyjnego i uspokajającego działania tyzanidyny [patrz PRZECIWWSKAZANIA ].
Ropinirol
W badaniu przeprowadzonym u 12 pacjentów z chorobą Parkinsona, którym podawano 6 mg ropinirolu raz na dobę z 500 mg CIPRO 250 mg dwa razy na dobę, średnie Cmax i średnie AUC ropinirolu wzrosły odpowiednio o 60% i 84%. Zaleca się monitorowanie działań niepożądanych związanych z ropinirolem i odpowiednie dostosowanie dawki ropinirolu podczas i wkrótce po jednoczesnym podaniu z CIPRO [patrz OSTRZEŻENIA I ŚRODKI ].
Klozapina
Po jednoczesnym podaniu 250 mg CIPRO 500 mg z 304 mg klozapiny przez 7 dni, stężenie klozapiny i N-demetyloklozapiny w surowicy zwiększyło się odpowiednio o 29% i 31%. Zaleca się uważne monitorowanie działań niepożądanych związanych z klozapiną i odpowiednie dostosowanie dawki klozapiny podczas i wkrótce po jednoczesnym podaniu z CIPRO.
Sildenafil
Po jednoczesnym podaniu zdrowym osobom pojedynczej dawki doustnej 50 mg syldenafilu i 500 mg CIPRO 1000 mg, średnie Cmax i średnie AUC syldenafilu wzrosły około dwukrotnie. Stosować syldenafil z ostrożnością podczas jednoczesnego podawania z CIPRO 500 mg ze względu na spodziewany dwukrotny wzrost ekspozycji na syldenafil po jednoczesnym podaniu CIPRO.
Duloksetyna
badaniach klinicznych wykazano, że jednoczesne stosowanie duloksetyny z silnymi inhibitorami izoenzymu 1A2 CYP450, takimi jak fluwoksamina, może powodować 5-krotne zwiększenie średniej AUC i 2,5-krotne zwiększenie średniej Cmax duloksetyny.
Lidokaina
W badaniu przeprowadzonym na 9 zdrowych ochotnikach, jednoczesne stosowanie lidokainy w dawce 1,5 mg/kg dożylnie z preparatem CIPRO w dawce 500 mg dwa razy na dobę powodowało zwiększenie Cmax i AUC lidokainy odpowiednio o 12% i 26%. Chociaż leczenie lidokainą było dobrze tolerowane przy tej zwiększonej ekspozycji, możliwe interakcje z CIPRO i nasilenie działań niepożądanych związanych z lidokainą mogą wystąpić po jednoczesnym podaniu.
Metoklopramid
Metoklopramid znacznie przyspiesza wchłanianie cypro 750 mgfloksacyny podawanej doustnie, co powoduje krótszy czas osiągnięcia maksymalnych stężeń w osoczu. Nie zaobserwowano znaczącego wpływu na biodostępność cyprofloksacyny.
Omeprazol
Gdy CIPRO podawano w pojedynczej dawce 1000 mg jednocześnie z omeprazolem (40 mg raz na dobę przez trzy dni) 18 zdrowym ochotnikom, średnie AUC i Cmax cyprofloksacyny zmniejszyły się odpowiednio o 20% i 23%. Kliniczne znaczenie tej interakcji nie zostało określone.
Mikrobiologia
Mechanizm akcji
Działanie bakteriobójcze cipro 750 mgfloksacyny wynika z hamowania enzymów topoizomerazy II (gyraza DNA) i topoizomerazy IV (obie topoizomerazy typu II), które są wymagane do replikacji, transkrypcji, naprawy i rekombinacji DNA bakterii.
Mechanizm oporu
Mechanizm działania fluorochinolonów, w tym cyprofloksacyny, różni się od penicylin, cefalosporyn, aminoglikozydów, makrolidów i tetracyklin; dlatego mikroorganizmy oporne na te klasy leków mogą być wrażliwe na cyprofloksacynę. Oporność na fluorochinolony występuje głównie przez mutacje w gyrazach DNA, zmniejszoną przepuszczalność błony zewnętrznej lub wypływ leków. Oporność in vitro na cyprofloksacynę rozwija się powoli poprzez wielokrotne mutacje etapowe. Oporność na cyprofloksacynę spowodowana spontanicznymi mutacjami występuje z ogólną częstością od
Opór krzyżowy
Nie jest znana oporność krzyżowa między cipro 1000 mgfloksacyny a innymi klasami środków przeciwdrobnoustrojowych.
Wykazano, że cyprofloksacyna działa na większość izolatów następujących bakterii, zarówno in vitro, jak i w zakażeniach klinicznych [patrz WSKAZANIA I ZASTOSOWANIE ].
Bakterie Gram-dodatnie
Bacillus anthracis Enterococcus faecalis Staphylococcus aureus (tylko izolaty wrażliwe na metycylinę) Staphylococcus epidermidis (tylko izolaty wrażliwe na metycylinę) Staphylococcus saprophyticus Streptococcus pneumoniae Streptococcus pyogenes
Bakterie Gram-ujemne
Campylobacter jejuni Citrobacter koseri Citrobacter freundii Enterobacter cloacae Escherichia coli Haemophilus influenza Haemophilus parainfluenzae Klebsiella pneumonia Moraxella catarrhalis Morganella morganii Neisseria gonorrhoeae Proteus mirabilis Proteus vulgaris Providencia rettgeri Providencia stuartii Pseudomonas aeruginosa Salmonella typhi Serratia marcescens Shigella boydii Shigella dysenteriae Shigella flexneri Shigella sonnei Yersinia pestis
Dostępne są następujące dane in vitro, ale ich znaczenie kliniczne nie jest znane. Co najmniej 90 procent następujących bakterii wykazuje in vitro minimalne stężenie hamujące (MIC) mniejsze lub równe wartości granicznej wrażliwości dla cipro 750 mgfloksacyny wobec izolatów podobnego rodzaju lub grupy organizmów. Jednak skuteczność cipro 500 mgfloksacyny w leczeniu zakażeń klinicznych wywołanych przez te bakterie nie została ustalona w odpowiednich i dobrze kontrolowanych badaniach klinicznych.
Bakterie Gram-dodatnie
Staphylococcus haemolyticus (tylko izolaty wrażliwe na metycylinę) Staphylococcus hominis (tylko izolaty wrażliwe na metycylinę)
Bakterie Gram-ujemne
Acinetobacter lwoffi Aeromonas hydrophila Edwardsiella tarda Enterobacter aerogenes Klebsiella oxytoca Legionella pneumophila Pasteurella multocida Salmonella enteritidis Vibrio cholera Vibrio parahaemolyticus Vibrio vulnificus Yersinia enterocolitica
Testy podatności
Szczegółowe informacje dotyczące kryteriów interpretacyjnych testu wrażliwości i powiązanych metod badawczych oraz standardów kontroli jakości uznanych przez FDA dla tego leku można znaleźć na stronie: https://www.fda.gov/STIC.
Studia kliniczne
Powikłane zakażenie dróg moczowych i odmiedniczkowe zapalenie nerek – skuteczność u pacjentów pediatrycznych
CIPRO podawany dożylnie i (lub) doustnie porównywano z cefalosporyną w leczeniu cUTI i odmiedniczkowego zapalenia nerek u dzieci w wieku od 1 do 17 lat (średnia wieku 6 ± 4 lata). Badanie przeprowadzono w USA, Kanadzie, Argentynie, Peru, Kostaryce, Meksyku, RPA i Niemczech. Czas trwania terapii wynosił od 10 do 21 dni (średni czas trwania leczenia wynosił 11 dni z zakresem od 1 do 88 dni). Podstawowym celem badania była ocena bezpieczeństwa układu mięśniowo-szkieletowego i neurologicznego.
Pacjenci byli oceniani pod kątem sukcesu klinicznego i eradykacji bakteriologicznej wyjściowego drobnoustroju(ów) bez nowej infekcji lub nadkażenia w 5 do 9 dni po terapii (test wyleczenia lub TOC). Populacja według protokołu miała organizm(y) sprawczy z określoną w protokole liczbą kolonii na początku badania, bez naruszenia protokołu i bez przedwczesnego przerwania lub utraty obserwacji (wśród innych kryteriów).
Skuteczność kliniczna i wskaźniki eradykacji bakteriologicznej w populacji zgodnej z protokołem były podobne w grupie CIPRO 250 mg i grupie porównawczej, jak pokazano poniżej.
Wąglik wziewny u dorosłych i dzieci
Średnie stężenia cyprofloksacyny w surowicy związane ze statystycznie istotną poprawą przeżycia w modelu wąglika wziewnego małpy rezus są osiągane lub przekraczane u pacjentów dorosłych i dzieci, otrzymujących schematy doustne i dożylne. Farmakokinetykę Cipro 500 mgfloksacyny oceniano w różnych populacjach ludzi. Średnie maksymalne stężenie w surowicy osiągane w stanie stacjonarnym u dorosłych ludzi otrzymujących 500 mg doustnie co 12 godzin wynosi 2,97 μg/ml i 4,56 μg/ml po podaniu 400 mg dożylnie co 12 godzin. Średnie minimalne stężenie w surowicy w stanie stacjonarnym dla obu tych schematów wynosi 0,2 µg/ml. W badaniu z udziałem 10 pacjentów pediatrycznych w wieku od 6 do 16 lat średnie osiągane maksymalne stężenie w osoczu wynosi 8,3 μg/ml, a stężenia minimalne wahają się od 0,09 μg/ml do 0,26 μg/ml, po dwóch 30-minutowych wlewach dożylnych mg/kg podawana w odstępie 12 godzin. Po drugiej infuzji dożylnej pacjenci przestawieni na dawkę 15 mg/kg doustnie co 12 godzin osiągają średnie stężenie maksymalne 3,6 µg/ml po początkowej dawce doustnej. Dane dotyczące długoterminowego bezpieczeństwa, w tym wpływu na chrząstkę, po podaniu preparatu CIPRO pacjentom pediatrycznym są ograniczone. Stężenia Cipro 1000 mg floksacyny w surowicy osiągane u ludzi służą jako zastępczy punkt końcowy, z rozsądnym prawdopodobieństwem pozwalającym przewidzieć korzyści kliniczne i stanowić podstawę tego wskazania.1
Przeprowadzono kontrolowane placebo badanie na małpach rezus, którym podano wziewną średnią dawkę 11 LD50 (~5,5 x 105 zarodników (zakres 5–30 LD50) B. anthracis. Minimalne stężenie hamujące (MIC) cipro 250 mgfloksacyny dla szczep wąglika użyty w tym badaniu wynosił 0,08 µg/ml. U badanych zwierząt średnie stężenie cypro 1000 mgfloksacyny w surowicy osiągane przy spodziewanym Tmax (1 godzina po podaniu) po podaniu doustnym do stanu stacjonarnego wahało się od 0,98 µg/ml do 1,69 Średnie minimalne stężenia w stanie stacjonarnym po 12 godzinach od podania dawki wahały się od 0,12 µg/ml do 0,19 µg/ml.6 Śmiertelność z powodu wąglika u zwierząt, które otrzymały 30-dniowy schemat doustnego podawania cipro 750 mgfloksacyny począwszy od 24 godzin po podaniu - ekspozycja była znacznie niższa (1/9), w porównaniu z grupą placebo (9/10) [p= 0,001].Jedyne zwierzę leczone CIPRO, które zmarło na wąglik, zrobiło to po 30-dniowym okresie podawania leku.7
Zalecono ponad 9300 osobom ukończenie co najmniej 60-dniowej profilaktyki przeciwbakteryjnej przeciwko możliwej ekspozycji wziewnej na B. anthracis w 2001 roku. Większości z nich zalecono CIPRO 250 mg w ramach całości lub części schematu profilaktyki. Niektórym osobom podano również szczepionkę przeciw wąglikowi lub zmieniono leczenie na alternatywne leki przeciwbakteryjne. U nikogo, kto otrzymywał CIPRO 1000 mg lub inne terapie profilaktyczne, nie rozwinął się później wąglik wziewny. Liczba osób, które otrzymały CIPRO jako całość lub część schematu profilaktyki poekspozycyjnej, jest nieznana.
Plaga
Przeprowadzono kontrolowane placebo badanie na afrykańskich małpach zielonych narażonych na wziewną średnią dawkę 110 LD50 (zakres od 92 do 127 LD50) Yersinia pestis (szczep CO92). Minimalne stężenie hamujące (MIC) cyprofloksacyny dla szczepu Y. pestis zastosowanego w tym badaniu wynosiło 0,015 µg/ml. Średnie maksymalne stężenie cyprofloksacyny w surowicy osiągnięte pod koniec pojedynczej 60-minutowej infuzji wyniosło 3,49 ± μg/ml 0,55 μg/ml, 3,91 μg/ml ± 0,58 μg/ml i 4,03 μg/ml ± 1,22 μg/ml w 2. dniu, Dzień 6 i dzień 10 leczenia odpowiednio u afrykańskich małp zielonych Wszystkie stężenia minimalne (dzień 2, dzień 6 i dzień 10) wynosiły
Toksykologia i/lub farmakologia zwierząt
Wykazano, że Cipro 250 mgfloksacyna i inne chinolony powodują artropatię u niedojrzałych zwierząt większości badanych gatunków [patrz OSTRZEŻENIA I ŚRODKI ]. U młodych psów i szczurów zaobserwowano uszkodzenie stawów obciążonych. U młodych psów rasy beagle cyprofloksacyna w dawce 100 mg/kg dziennie przez 4 tygodnie powodowała zmiany zwyrodnieniowe stawu kolanowego. Przy 30 mg/kg wpływ na staw był minimalny. W kolejnym badaniu u młodych psów rasy beagle, doustne dawki cipro 750 mgfloksacyny 30 mg/kg i 90 mg/kg cipro 750 mgfloksacyny (około 1,3-krotność i 3,5-krotność dawki pediatrycznej na podstawie porównawczych AUC w osoczu) podawane codziennie przez 2 tygodnie powodowały zmiany, które nadal były obserwowane w badaniu histopatologicznym po okresie 5 miesięcy bez leczenia. Przy dawce 10 mg/kg (około 0,6-krotność dawki pediatrycznej w oparciu o porównawcze AUC w osoczu) nie zaobserwowano wpływu na stawy. Dawka ta nie była również związana z artrotoksycznością po dodatkowym okresie 5 miesięcy bez leczenia. W innym badaniu usunięcie obciążenia ze stawu zmniejszyło zmiany chorobowe, ale nie zapobiegło im całkowicie.
Krystaluria, czasami związana z wtórną nefropatią, występuje u zwierząt laboratoryjnych, którym podawano cyprofloksacynę. Jest to związane przede wszystkim ze zmniejszoną rozpuszczalnością cyprofloksacyny w warunkach zasadowych, które dominują w moczu badanych zwierząt; u ludzi krystaluria jest rzadka, ponieważ ludzki mocz jest zazwyczaj kwaśny. U małp rezus krystaluria bez nefropatii była obserwowana po pojedynczych dawkach doustnych, tak niskich jak 5 mg/kg. (około 0,07-krotność najwyższej zalecanej dawki terapeutycznej w oparciu o powierzchnię ciała). Po 6 miesiącach dożylnego podawania dawki 10 mg/kg/dobę nie stwierdzono zmian nefropatologicznych; jednak nefropatię obserwowano po podaniu dawki 20 mg/kg/dobę przez taki sam czas trwania (około 0,2-krotność najwyższej zalecanej dawki terapeutycznej w oparciu o powierzchnię ciała).
psów cyprofloksacyna w dawce 3 mg/kg i 10 mg/kg w szybkim wstrzyknięciu dożylnym (15 sek.) powoduje wyraźne działanie hipotensyjne. Uważa się, że te efekty są związane z uwalnianiem histaminy, ponieważ są one częściowo antagonizowane przez pirylaminę, środek przeciwhistaminowy. U małp rezus szybkie wstrzyknięcie dożylne również powoduje niedociśnienie, ale efekt u tego gatunku jest niespójny i mniej wyraźny.
Stwierdzono, że u myszy jednoczesne podawanie niesteroidowych leków przeciwzapalnych, takich jak fenylobutazon i indometacyna, z chinolonami wzmacnia działanie stymulujące ośrodkowy układ nerwowy chinolonów.
U zwierząt leczonych cyprofloksacyną nie obserwowano toksyczności ocznej obserwowanej w przypadku niektórych leków pokrewnych
BIBLIOGRAFIA
1. 21 CFR 314.510 (Podczęść H – Przyspieszone zatwierdzanie nowych leków na choroby zagrażające życiu).
5. Raport przedstawiony na spotkaniu Komitetu Doradczego FDA ds. Leków Przeciwzakaźnych i Leków Dermatologicznych, 31 marca 1993 r., Silver Spring, MD. Raport dostępny w FDA, CDER, Advisors and Consultants Staff, HFD-21, 1901 Chapman Avenue, Room 200, Rockville, MD 20852, USA.
6. Kelly DJ, et al. Stężenia penicyliny, doksycykliny i cyprofloksacyny w surowicy podczas długotrwałej terapii u rezusów. J Infect Dis 1992; 166:1184-7.
7. Friedlander AM i in. Profilaktyka poekspozycyjna przeciwko eksperymentalnemu wąglikowi wziewnemu. J Infect Dis 1993; 167:1239-42.
8. Spotkanie Komitetu Doradczego ds. Leków Przeciwzakaźnych, 3 kwietnia 2012 r. – Skuteczność Ciprofloksacyny w leczeniu dżumy płucnej.
INFORMACJA O PACJENCIE
CIPRO® Tabletki (Sip-row) (chlorowodorek cyprofloksacyny), do stosowania doustnego
CIPRO® (Sip-row) (cipro 1000mgfloksacyna) do zawiesiny doustnej
Przeczytaj ten Przewodnik po lekach przed rozpoczęciem przyjmowania CIPRO 500 mg i za każdym razem, gdy otrzymasz uzupełnienie. Mogą pojawić się nowe informacje. Informacje te nie zastępują rozmowy z lekarzem o stanie zdrowia lub leczeniu.
Jakie są najważniejsze informacje, które powinienem wiedzieć o CIPRO 500mg?
CIPRO, fluorochinolonowy lek przeciwbakteryjny, może powodować poważne skutki uboczne. Niektóre z tych poważnych skutków ubocznych mogą wystąpić w tym samym czasie i mogą spowodować śmierć.
Jeśli podczas przyjmowania leku CIPRO wystąpi którykolwiek z poniższych poważnych działań niepożądanych, należy natychmiast przerwać przyjmowanie leku CIPRO 750 mg i natychmiast uzyskać pomoc medyczną.
1. Zerwanie ścięgna lub obrzęk ścięgna (zapalenie ścięgna).
- Problemy ze ścięgnami mogą wystąpić u osób w każdym wieku, które przyjmują CIPRO. Ścięgna to twarde sznury tkanki, które łączą mięśnie z kośćmi. Objawy problemów ze ścięgnami mogą obejmować:
- ból
- obrzęk
- łzy i obrzęk ścięgien, w tym tylnej części kostki (Achillesa), barku, dłoni, kciuka lub innych miejsc ścięgien.
- Ryzyko wystąpienia problemów ze ścięgnami podczas przyjmowania leku CIPRO jest większe, jeśli:
- ukończyły 60 rok życia
- przyjmujesz sterydy (kortykosteroidy)
- przeszła przeszczep nerki, serca lub płuc.
- Problemy ze ścięgnami mogą wystąpić u osób, które nie mają powyższych czynników ryzyka podczas przyjmowania CIPRO.
- Inne powody, które mogą zwiększać ryzyko problemów ze ścięgnami, mogą obejmować:
- aktywność fizyczna lub ćwiczenia
- niewydolność nerek
- problemy ze ścięgnami w przeszłości, takie jak u osób z reumatoidalnym zapaleniem stawów (RZS).
- Należy natychmiast przerwać przyjmowanie CIPRO i natychmiast uzyskać pomoc medyczną przy pierwszych oznakach bólu, obrzęku lub stanu zapalnego ścięgna. Najczęstszym obszarem bólu i obrzęku jest ścięgno Achillesa z tyłu kostki. Może się to zdarzyć również w przypadku innych ścięgien.
- Zerwanie ścięgna może nastąpić podczas lub po zakończeniu przyjmowania leku CIPRO. Zerwanie ścięgien może nastąpić w ciągu kilku godzin lub dni po zażyciu leku CIPRO i zdarzać się nawet do kilku miesięcy po zakończeniu przyjmowania fluorochinolonów.
- Należy natychmiast przerwać przyjmowanie leku CIPRO 500 mg i natychmiast uzyskać pomoc medyczną, jeśli wystąpi którykolwiek z następujących objawów zerwania ścięgna:
- usłyszeć lub poczuć trzask lub trzask w okolicy ścięgna
- zasinienie zaraz po urazie w okolicy ścięgna
- niezdolny do poruszania się dotkniętym obszarem lub znoszenia ciężaru
Problemy ze ścięgnami mogą być trwałe.
2. Zmiany czucia i możliwe uszkodzenie nerwów (Neuropatia Obwodowa). U osób przyjmujących fluorochinolony, w tym CIPRO, może dojść do uszkodzenia nerwów w ramionach, dłoniach, nogach lub stopach. Należy natychmiast przerwać przyjmowanie leku CIPRO 750 mg i natychmiast skontaktować się z lekarzem, jeśli wystąpi którykolwiek z następujących objawów neuropatii obwodowej w ramionach, dłoniach, nogach lub stopach:
- ból
- drętwienie
- palenie
- słabość
- mrowienie
CIPRO 500mg może wymagać zatrzymania, aby zapobiec trwałemu uszkodzeniu nerwów.
3. Skutki ośrodkowego układu nerwowego (OUN). osób przyjmujących leki przeciwbakteryjne zawierające fluorochinolony, w tym CIPRO, zgłaszano problemy ze zdrowiem psychicznym i drgawki. Przed rozpoczęciem stosowania leku CIPRO należy poinformować lekarza, jeśli w przeszłości występowały napady drgawkowe. Działania niepożądane ze strony OUN mogą wystąpić już po przyjęciu pierwszej dawki leku CIPRO. Należy natychmiast przerwać przyjmowanie CIPRO i natychmiast skontaktować się z lekarzem, jeśli wystąpi którykolwiek z tych działań niepożądanych lub inne zmiany nastroju lub zachowania:
- drgawki
- problemy ze snem
- słyszeć głosy, widzieć lub wyczuwać rzeczy, których nie ma (omamy)
- koszmary
- czuć oszołomienie lub zawroty głowy
- czuć się poruszony
- czuć się bardziej podejrzliwie (paranoja)
- drżenia
- myśli lub czyny samobójcze
- odczuwać niepokój lub zdenerwowanie
- bóle głowy, które nie ustępują, z lub bez
- zamieszanie niewyraźne widzenie
- depresja
- problemy z pamięcią
- zmniejszona świadomość otoczenia
- fałszywe lub dziwne myśli lub przekonania (urojenia)
Zmiany te mogą być trwałe.
4. Nasilenie miastenii (problem powodujący osłabienie mięśni). Fluorochinolony, takie jak CIPRO 500 mg, mogą powodować nasilenie objawów miastenii, w tym osłabienie mięśni i problemy z oddychaniem. Przed rozpoczęciem stosowania leku CIPRO należy poinformować lekarza, jeśli w przeszłości występowała miastenia. Zadzwoń do swojego lekarza natychmiast, jeśli masz jakiekolwiek pogarszające się osłabienie mięśni lub problemy z oddychaniem.
Co to jest CIPRO 750 mg?
CIPRO to fluorochinolonowy lek przeciwbakteryjny stosowany u osób dorosłych w wieku 18 lat i starszych w leczeniu niektórych zakażeń wywołanych przez pewne zarazki zwane bakteriami. Te infekcje bakteryjne obejmują:
-
- zakażenie dróg moczowych
- infekcja kości i stawów
- rzeżączka szyjkowo-cewkowa, nieskomplikowana
- przewlekła infekcja prostaty
- szpitalne zapalenie płuc
- osoby z niską liczbą białych krwinek i gorączką
- infekcja dolnych dróg oddechowych
- zakażenie wewnątrzbrzuszne, powikłane
- wąglik wziewny
- infekcja zatok
- biegunka zakaźna
- plaga
- infekcja skóry
- gorączka tyfusowa (jelitowa)
- Badania nad preparatem CIPRO 1000 mg do stosowania w leczeniu dżumy i wąglika przeprowadzono wyłącznie na zwierzętach, ponieważ dżumy i wąglika nie można było badać u ludzi.
- Preparatu CIPRO 250 mg nie należy stosować u osób z ostrym zaostrzeniem przewlekłego zapalenia oskrzeli, ostrym niepowikłanym zapaleniem pęcherza moczowego i infekcjami zatok, jeśli dostępne są inne opcje leczenia.
- CIPRO 750 mg nie powinien być stosowany jako lek przeciwbakteryjny pierwszego wyboru w leczeniu infekcji dolnych dróg oddechowych wywołanych przez pewien rodzaj bakterii o nazwie Streptococcus pneumoniae.
- CIPRO 1000mg jest również stosowany u dzieci poniżej 18 roku życia w leczeniu powikłanych infekcji dróg moczowych i nerek lub którzy mogli wdychać zarazki wąglika, dżumy lub były narażone na zarazki dżumy.
- Dzieci w wieku poniżej 18 lat mają większe ryzyko wystąpienia problemów kości, stawów lub ścięgien (mięśniowo-szkieletowych), takich jak ból lub obrzęk podczas przyjmowania leku CIPRO. CIPRO 500mg nie powinien być stosowany jako lek przeciwbakteryjny pierwszego wyboru u dzieci poniżej 18 roku życia.
Kto nie powinien brać CIPRO 1000mg?
Nie należy przyjmować leku CIPRO 500 mg, jeśli:
- jeśli kiedykolwiek wystąpiła ciężka reakcja alergiczna na lek przeciwbakteryjny znany jako fluorochinolon lub jesteś uczulony na cipro 500 mg chlorowodorek floksacyny lub którykolwiek ze składników preparatu CIPRO. Pełna lista składników CIPRO znajduje się na końcu tego Przewodnika po lekach.
- należy również przyjmować lek o nazwie tyzanidyna (Zanaflex®). Zapytaj swojego lekarza, jeśli nie jesteś pewien.
O czym powinienem powiedzieć lekarzowi przed zażyciem CIPRO?
Przed przyjęciem CIPRO należy poinformować lekarza o wszystkich swoich schorzeniach, w tym o:
- mieć problemy ze ścięgnami. CIPRO nie powinien być stosowany u osób, które w przeszłości miały problemy ze ścięgnami.
- cierpisz na chorobę, która powoduje osłabienie mięśni (myasthenia gravis). CIPRO nie powinien być stosowany u osób, u których rozpoznano miastenię ciężką.
- masz problemy z wątrobą.
- mają problemy z ośrodkowym układem nerwowym (takie jak padaczka).
- mieć problemy z nerwami. Leku CIPRO 500 mg nie należy stosować u osób, u których w wywiadzie występowały problemy z nerwami zwane neuropatią obwodową lub ktokolwiek z rodziny ma nieregularne bicie serca lub zawał serca, zwłaszcza stan zwany „wydłużeniem odstępu QT”.
- mają niski poziom potasu we krwi (hipokaliemia) lub niski poziom magnezu (hipomagnezemia).
- masz lub miałeś drgawki.
- mają problemy z nerkami. Jeśli nerki nie pracują prawidłowo, może być konieczne zastosowanie mniejszej dawki leku CIPRO 500 mg.
- mieć cukrzycę lub problemy z niskim poziomem cukru we krwi (hipoglikemia).
- mają problemy ze stawami, w tym reumatoidalne zapalenie stawów (RZS).
- mieć problemy z połykaniem tabletek.
- są w ciąży lub planują zajść w ciążę. Nie wiadomo, czy CIPRO 250 mg zaszkodzi nienarodzonemu dziecku.
- karmisz piersią lub planujesz karmić piersią. CIPRO 250 mg przenika do mleka matki.
- Nie należy karmić piersią podczas leczenia lekiem CIPRO 500 mg i przez 2 dni po przyjęciu ostatniej dawki leku CIPRO. Podczas leczenia lekiem CIPRO i przez 2 dni po przyjęciu ostatniej dawki leku CIPRO można odciągać mleko i wyrzucać je.
- Jeśli pacjentka przyjmuje preparat CIPRO w celu leczenia wąglika wziewnego, wraz z lekarzem należy podjąć decyzję, czy można kontynuować karmienie piersią podczas stosowania leku CIPRO.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe.
- CIPRO 1000 mg i inne leki mogą wzajemnie na siebie oddziaływać, powodując działania niepożądane.
- Szczególnie powiedz swojemu lekarzowi, jeśli bierzesz:
- lek steroidowy.
- lek przeciwpsychotyczny.
- trójpierścieniowy lek przeciwdepresyjny.
- pigułka na wodę (diuretyk).
- teofilina (np. Theo-24®, Elixophyllin®, Theochron®, Uniphyl®, Theolair®).
- lek kontrolujący tętno lub rytm serca (leki przeciwarytmiczne).
- doustny lek przeciwcukrzycowy.
- fenytoina (Fosphenytoin Sodium®, Cerebyx®, Dilantin-125®, Dilantin®, Extended Phenytoin Sodium®, Prompt Phenytoin Sodium®, Phenytek®).
- cyklosporyna (Gengraf®, Neoral®, Sandimmune®, Sangcya®).
- rozcieńczalnik krwi (taki jak warfaryna, Coumadin®, Jantoven®).
- metotreksat (Trexall®).
- ropinirol (Requip®).
- klozapina (Clozaril®, Fazaclo® ODT®).
- niesteroidowy lek przeciwzapalny (NLPZ). Wiele popularnych leków przeciwbólowych to NLPZ. Przyjmowanie NLPZ podczas przyjmowania CIPRO 500 mg lub innych fluorochinolonów może zwiększać ryzyko wystąpienia objawów ze strony ośrodkowego układu nerwowego i drgawek.
- sildenafil (Viagra®, Revatio®).
- duloksetyna.
- produkty zawierające kofeinę.
- probenecyd (Probalan®, Col-probenecyd®).
- Niektóre leki mogą uniemożliwiać prawidłowe działanie tabletek CIPRO i zawiesiny doustnej CIPRO. Tabletki CIPRO i zawiesina doustna należy przyjmować 2 godziny przed lub 6 godzin po przyjęciu tych leków, witamin lub suplementów:
- środek zobojętniający kwas, multiwitamina lub inny lek lub suplementy zawierające magnez, wapń, glin, żelazo lub cynk.
- sukralfat (Carafate®).
- didanozyna (Videx®, Videx EC®).
Poproś swojego lekarza o listę tych leków, jeśli nie masz pewności.
Poznaj leki, które przyjmujesz. Zachowaj ich listę, aby pokazać swojemu lekarzowi i farmaceucie, kiedy otrzymasz nowy lek.
Jak powinienem przyjmować CIPRO 500mg?
- Weź CIPRO dokładnie tak, jak zaleci Twój lekarz.
- Twój lekarz poinformuje Cię, ile leku CIPRO należy przyjąć i kiedy.
- CIPRO można przyjmować z jedzeniem lub bez jedzenia.
- CIPRO nie powinien być przyjmowany z produktami mlecznymi (takimi jak mleko lub jogurt) lub samymi sokami wzbogacanymi wapniem, ale można go przyjmować z posiłkiem zawierającym te produkty.
- Pij dużo płynów podczas przyjmowania CIPRO.
- Nie należy pomijać żadnych dawek leku CIPRO ani przerywać jego przyjmowania, nawet jeśli poczujesz się lepiej, aż do zakończenia przepisanego leczenia, chyba że:
- masz problemy ze ścięgnami. Widzieć „Jakie są najważniejsze informacje, które powinienem wiedzieć o CIPRO?”
- masz problemy z nerwami. Widzieć „Jakie są najważniejsze informacje, które powinienem wiedzieć o CIPRO?”
- masz problemy z ośrodkowym układem nerwowym. Widzieć „Jakie są najważniejsze informacje, które powinienem wiedzieć o CIPRO 1000mg?”
- masz poważną reakcję alergiczną. Widzieć „Jakie są możliwe skutki uboczne CIPRO 750mg?”
- Twój lekarz poinformuje Cię o zaprzestaniu przyjmowania CIPRO.
Przyjmowanie wszystkich dawek CIPRO pomoże upewnić się, że wszystkie bakterie zostaną zabite. Przyjmowanie wszystkich dawek CIPRO zmniejszy prawdopodobieństwo, że bakterie staną się oporne na CIPRO. W przypadku uodpornienia się na CIPRO, CIPRO 1000 mg i inne leki przeciwbakteryjne mogą nie działać w przyszłości.
-
Jeśli zażyjesz zbyt dużo CIPRO 750 mg, skontaktuj się z lekarzem lub natychmiast uzyskaj pomoc medyczną.
-
CIPRO jest dostarczany w postaci tabletki z linią podziału (CIPRO 1000 mg tabletki), zawiesiny doustnej (CIPRO 750 mg zawiesina doustna), tabletki o przedłużonym uwalnianiu (CIPRO XR) i zastrzyku do infuzji dożylnej (CIPRO IV). Przeczytaj i postępuj zgodnie z poniższymi instrukcjami dotyczącymi typu CIPRO 500 mg przepisanego przez lekarza.
Tabletki CIPRO:
- Tabletki CIPRO są dostępne w postaci tabletek z linią podziału 250 mg i 500 mg, które można przyjmować w całości lub przełamać na pół na linii z linią podziału. Lekarz poinformuje pacjenta, jaką dawkę leku CIPRO 500 mg tabletki należy przyjąć i czy konieczne będzie przełamanie tabletki CIPRO 1000 mg na pół, aby otrzymać przepisaną dawkę.
- Tabletki CIPRO należy przyjmować rano i wieczorem mniej więcej o tej samej porze każdego dnia. Tabletki nie należy kruszyć ani żuć. Poinformuj swojego lekarza, jeśli nie możesz połknąć tabletki.
- W przypadku pominięcia dawki leku CIPRO 500 mg tabletki, a jest to:
- 6 godzin lub więcej do następnej zaplanowanej dawki, należy natychmiast przyjąć pominiętą dawkę. Następnie przyjmij następną dawkę o zwykłej porze.
- mniej niż 6 godzin do następnej zaplanowanej dawki, nie należy przyjmować pominiętej dawki. Następną dawkę należy przyjąć o zwykłej porze.
- Nie należy przyjmować jednorazowo 2 dawek leku CIPRO 750 mg tabletki w celu uzupełnienia pominiętej dawki. W razie wątpliwości, kiedy przyjąć CIPRO 500 mg tabletki po pominięciu dawki, należy zwrócić się do lekarza lub farmaceuty.
Zawieszenie doustne CIPRO:
- Przyjmuj CIPRO 1000mg zawiesina doustna rano i wieczorem mniej więcej o tej samej porze każdego dnia. Przed każdym użyciem dobrze wstrząsnąć butelką CIPRO 750 mg Oral Suspension przez około 15 sekund, aby upewnić się, że zawiesina jest dobrze wymieszana. Po użyciu całkowicie zamknąć butelkę.
- W przypadku pominięcia dawki leku CIPRO zawiesina doustna, która jest:
- 6 godzin lub więcej do następnej zaplanowanej dawki, należy natychmiast przyjąć pominiętą dawkę. Następnie przyjmij następną dawkę o zwykłej porze.
- mniej niż 6 godzin do następnej zaplanowanej dawki, nie należy przyjmować pominiętej dawki. Następną dawkę należy przyjąć o zwykłej porze.
- Nie należy przyjmować jednorazowo 2 dawek CIPRO 750 mg zawiesina doustna w celu uzupełnienia pominiętej dawki. W razie wątpliwości, kiedy przyjąć CIPRO zawiesinę doustną po pominięciu dawki, należy zwrócić się do lekarza lub farmaceuty.
Czego powinienem unikać podczas przyjmowania CIPRO?
- CIPRO 250mg może wywołać zawroty głowy i oszołomienie. Nie należy prowadzić pojazdów, obsługiwać maszyn ani wykonywać innych czynności wymagających sprawności umysłowej lub koordynacji, dopóki nie dowiesz się, jak CIPRO 250 mg wpływa na Ciebie.
- Unikaj lamp słonecznych, solarium i staraj się ograniczać czas przebywania na słońcu. CIPRO 500 mg może sprawić, że Twoja skóra stanie się wrażliwa na słońce (światłoczułość) oraz światło lamp słonecznych i łóżek opalających. Możesz uzyskać poważne oparzenia słoneczne, pęcherze lub obrzęk skóry. Jeśli wystąpi którykolwiek z tych objawów podczas przyjmowania CIPRO 250 mg, natychmiast skontaktuj się z lekarzem. Powinieneś używać kremu przeciwsłonecznego i nosić czapkę i ubrania zakrywające skórę, jeśli musisz przebywać w słońcu.
Jakie są możliwe skutki uboczne CIPRO?
CIPRO może powodować poważne skutki uboczne, w tym:
- Widzieć „Jakie są najważniejsze informacje, które powinienem wiedzieć o CIPRO?”
- Poważne reakcje alergiczne. Poważne reakcje alergiczne, w tym śmierć, mogą wystąpić u osób przyjmujących fluorochinolony, w tym CIPRO, nawet po 1 dawce. Należy przerwać przyjmowanie CIPRO i natychmiast uzyskać pomoc medyczną w nagłych wypadkach, jeśli wystąpi którykolwiek z następujących objawów ciężkiej reakcji alergicznej:
- pokrzywka
- szybkie bicie serca
- problemy z oddychaniem lub połykaniem
- mdleć
- obrzęk ust, języka, twarzy
- wysypka na skórze
- ucisk w gardle, chrypka
Wysypka skórna może wystąpić u osób przyjmujących CIPRO 1000 mg nawet po 1 dawce. Przestań przyjmować CIPRO 500 mg przy pierwszych oznakach wysypki skórnej i skontaktuj się z lekarzem. Wysypka skórna może być oznaką poważniejszej reakcji na CIPRO.
- Uszkodzenie wątroby (hepatotoksyczność). Hepatotoksyczność może wystąpić u osób przyjmujących CIPRO. Zadzwoń do swojego lekarza natychmiast, jeśli masz niewyjaśnione objawy, takie jak:
- nudności lub wymioty
- niezwykłe zmęczenie
- ból brzucha
- utrata apetytu
- gorączka
- jasne wypróżnienia
- słabość
- ciemny kolor moczu
- ból lub tkliwość brzucha
- zażółcenie skóry i białek oczu
- swędzący
Należy przerwać przyjmowanie leku CIPRO 750 mg i natychmiast poinformować lekarza, jeśli występuje zażółcenie skóry lub białych części oczu lub ciemny mocz. Mogą to być objawy ciężkiej reakcji na CIPRO (problem z wątrobą).
- Tętniak aorty i rozwarstwienie. Poinformuj swojego lekarza, jeśli kiedykolwiek powiedziano Ci, że masz tętniak aorty, obrzęk dużej tętnicy, która przenosi krew z serca do ciała. Natychmiast uzyskaj pomoc medyczną w nagłych wypadkach, jeśli wystąpi nagły ból w klatce piersiowej, brzuchu lub plecach.
- Zakażenie jelit (Clostridioides difficile – biegunka towarzysząca). Biegunka związana z Clostridioides difficile (CDAD) może wystąpić w przypadku wielu leków przeciwbakteryjnych, w tym CIPRO. Natychmiast skontaktuj się z lekarzem, jeśli wystąpi wodnista biegunka, biegunka, która nie ustępuje lub krwawe stolce. Możesz mieć skurcze żołądka i gorączkę. CDAD może wystąpić 2 lub więcej miesięcy po zakończeniu przyjmowania leku przeciwbakteryjnego.
- Poważne zmiany rytmu serca (wydłużenie odstępu QT i torsade de pointes). Poinformuj natychmiast swojego lekarza, jeśli zauważysz zmianę rytmu serca (szybkie lub nieregularne bicie serca) lub jeśli zemdlejesz. CIPRO może powodować rzadką chorobę serca znaną jako wydłużenie odstępu QT. Ten stan może powodować nieprawidłowe bicie serca i może być bardzo niebezpieczny. Szanse na to wydarzenie są większe u osób:
- którzy są w podeszłym wieku.
- z wywiadem rodzinnym wydłużonego odstępu QT.
- z niskim poziomem potasu we krwi (hipokaliemia) lub niskim magnezem (hipomagnezemia).
- którzy przyjmują pewne leki kontrolujące rytm serca (leki przeciwarytmiczne).
- Wspólne problemy. Może wystąpić zwiększone ryzyko problemów ze stawami i tkankami wokół stawów u dzieci poniżej 18 roku życia. Należy poinformować lekarza dziecka, jeśli dziecko ma jakiekolwiek problemy ze stawami w trakcie lub po leczeniu CIPRO.
- Wrażliwość na światło słoneczne (światłoczułość). Zobacz „Czego powinienem unikać podczas przyjmowania CIPRO 250mg?”
- Zmiany poziomu cukru we krwi. Osoby przyjmujące CIPRO i inne leki fluorochinolonowe z doustnymi lekami przeciwcukrzycowymi lub insuliną mogą mieć niski poziom cukru we krwi (hipoglikemia) i wysoki poziom cukru we krwi (hiperglikemia). Postępuj zgodnie z instrukcjami lekarza, jak często sprawdzać poziom cukru we krwi. Jeśli masz cukrzycę i masz niski poziom cukru we krwi podczas przyjmowania CIPRO, przerwij przyjmowanie CIPRO i natychmiast skontaktuj się z lekarzem. Może być konieczna zmiana antybiotyku.
Najczęstsze skutki uboczne CIPRO 750mg to:
- mdłości
- biegunka
- zmiany w testach czynności wątroby
- wymioty
- wysypka
Poinformuj swojego lekarza o wszelkich skutkach ubocznych, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne CIPRO. Aby uzyskać więcej informacji, zapytaj swojego lekarza lub farmaceutę.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać CIPRO?
Tabletki CIPRO 500 mg
- Przechowywać w temperaturze pokojowej między 68 ° F do 77 ° F (20 ° C do 25 ° C).
CIPRO 750 mg zawiesina doustna
- Przechowuj mikrokapsułki i rozcieńczalnik w temperaturze pokojowej do 77 ° F (25 ° C).
- Nie zamrażać.
- Po zakończeniu leczenia CIPRO bezpiecznie wyrzucić niewykorzystaną zawiesinę doustną.
Lek CIPRO 250 mg i wszystkie leki należy przechowywać w miejscu niedostępnym dla dzieci.
Ogólne informacje o bezpiecznym i efektywnym korzystaniu z CIPRO.
Leki są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Nie należy stosować CIPRO w stanach, na które nie jest przepisany. Nie należy podawać CIPRO innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić.
Ten przewodnik po lekach podsumowuje najważniejsze informacje o CIPRO. Jeśli chcesz uzyskać więcej informacji na temat CIPRO, porozmawiaj ze swoim lekarzem. Możesz poprosić swojego lekarza lub farmaceutę o informacje na temat CIPRO 250 mg, które są przeznaczone dla pracowników służby zdrowia.
Jakie są składniki CIPRO 500mg?
Tabletki CIPRO 1000 mg:
- Składnik czynny: cipro 250 mg chlorowodorku floksacyny
- Nieaktywne składniki: skrobia kukurydziana, krospowidon, hypromeloza, stearynian magnezu, celuloza mikrokrystaliczna, glikol polietylenowy, dwutlenek krzemu i dwutlenek tytanu.
Zawieszenie doustne CIPRO:
- Składnik czynny: cyprofloksacyna
- Nieaktywne składniki:
- Mikrokapsułki zawierają: hypromeloza, stearynian magnezu, kopolimer kwasu metakrylowego oraz polisorbat 20 i powidon.
- Rozcieńczalnik zawiera: trójglicerydy średniołańcuchowe, sacharoza, lecytyna sojowa, woda, aromat truskawkowy.
Ten przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków.
