Levaquin 250mg, 500mg, 750mg Levofloxacin Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Levaquin 750mg i jak się go stosuje?
Levaquin to lek na receptę stosowany w leczeniu objawów różnych infekcji bakteryjnych. Levaquin może być stosowany samodzielnie lub z innymi lekami.
Levaquin 500mg należy do klasy leków zwanych Fluorochinolonami.
Nie wiadomo, czy Levaquin jest bezpieczny i skuteczny u dzieci przez okres leczenia powyżej 14 dni.
Jakie są możliwe skutki uboczne Levaquin 500mg?
Levaquin 750mg może powodować poważne skutki uboczne, w tym:
- ból głowy,
- głód,
- wyzysk,
- drażliwość,
- zawroty głowy,
- mdłości,
- szybkie tętno,
- uczucie niepokoju lub roztrzęsienia,
- drętwienie lub mrowienie dłoni, ramion, nóg lub stóp,
- osłabienie ramion, rąk, nóg lub stóp,
- piekący ból ramion, dłoni, nóg lub stóp,
- poważne zmiany nastroju lub zachowania,
- nerwowość,
- dezorientacja,
- podniecenie,
- paranoja,
- halucynacje,
- problemy z pamięcią,
- problemy z koncentracją,
- myśli samobójcze,
- zerwanie ścięgna,
- nagły ból,
- obrzęk,
- siniaki,
- czułość,
- sztywność,
- problemy ruchowe,
- dźwięk trzaskania lub trzaskania w dowolnym stawie,
- silny ból brzucha,
- biegunka wodnista lub krwawa,
- fruwające w piersi,
- duszność,
- wysypka na skórze,
- problemy z oddychaniem,
- drgawki (konwulsje),
- silne bóle głowy,
- Problemy ze wzrokiem,
- ból za oczami,
- ból w górnej części brzucha,
- utrata apetytu,
- ciemny mocz,
- taborety w kolorze gliny i
- zażółcenie skóry lub oczu (żółtaczka)
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Levaquin 250mg to:
- mdłości,
- zaparcie,
- biegunka,
- ból głowy,
- zawroty głowy i
- problemy ze snem
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Levaquin. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OSTRZEŻENIE
POWAŻNE REAKCJE NIEPOŻĄDANE W TYM ZAPACHY ŚCIĘGIEN, ZERWANIE ŚCIĘGNA, NEUROPATIA OBWODOWA, DZIAŁANIE NA CENTRALNY UKŁAD NERWOWY ORAZ ZAostrzenie Miastenii Gravis
- Fluorochinolony, w tym LEVAQUIN®, są związane z uniemożliwiającymi i potencjalnie nieodwracalnymi poważnymi działaniami niepożądanymi, które wystąpiły razem [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI], w tym:
- Zapalenie ścięgna i zerwanie ścięgna [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI]
- Neuropatia obwodowa [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI]
- Wpływ na centralny układ nerwowy [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI]
Natychmiast przerwij stosowanie LEVAQUIN® i unikaj stosowania fluorochinolonów, w tym LEVAQUIN®, u pacjentów, u których wystąpiły którekolwiek z tych poważnych działań niepożądanych [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI]
- Fluorochinolony, w tym LEVAQUIN®, mogą nasilać osłabienie mięśni u pacjentów z miastenią. Unikaj LEVAQUIN® u pacjentów ze znaną historią miastenii [patrz OSTRZEŻENIA I ŚRODKI ].
- Ponieważ fluorochinolony, w tym LEVAQUIN®, były związane z poważnymi działaniami niepożądanymi [patrz OSTRZEŻENIA I ŚRODKI ], należy zarezerwować LEVAQUIN® do stosowania u pacjentów, którzy nie mają alternatywnych możliwości leczenia w następujących wskazaniach:
- Niepowikłane zakażenie dróg moczowych [patrz WSKAZANIA ]
- Ostre bakteryjne zaostrzenie przewlekłego zapalenia oskrzeli [patrz WSKAZANIA ]
- Ostre bakteryjne zapalenie zatok [patrz WSKAZANIA ].
OPIS
LEVAQUIN® Tabletki to syntetyczne środki przeciwbakteryjne do podawania doustnego. Chemicznie, lewofloksacyna, chiralny fluorowany karboksychinolon, jest czystym (-)-(S)-enancjomerem racemicznej substancji leczniczej ofloksacyny. Nazwa chemiczna to (-)-(S)-9-fluoro-2,3-dihydro-3-metylo-10-(4-metylo-1-piperazynylo)-7-okso-7H-pirydo[1,2, Półwodzian kwasu 3-de]-1,4-benzoksazyno-6-karboksylowego.
Rycina 1: Struktura chemiczna lewofloksacyny
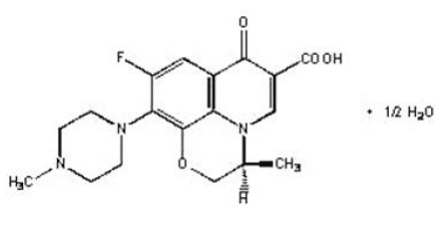
Wzór empiryczny to C18H20FN3O4 · ½ H2O, a masa cząsteczkowa wynosi 370,38. Lewofloksacyna jest kryształem lub proszkiem krystalicznym o barwie jasnożółtawobiałej do żółtobiałej. Cząsteczka występuje jako jon obojnaczy w warunkach pH w jelicie cienkim.
Dane pokazują, że od pH 0,6 do 5,8 rozpuszczalność lewofloksacyny jest zasadniczo stała (około 100 mg/ml). Lewofloksacyna jest uważana za rozpuszczalną lub swobodnie rozpuszczalną w tym zakresie pH, zgodnie z nomenklaturą USP. Powyżej pH 5,8 rozpuszczalność szybko wzrasta do maksimum przy pH 6,7 (272 mg/ml) i jest uważana za swobodnie rozpuszczalną w tym zakresie. Powyżej pH 6,7 rozpuszczalność zmniejsza się i osiąga wartość minimalną (około 50 mg/ml) przy pH około 6,9.
Lewofloksacyna może tworzyć stabilne związki koordynacyjne z wieloma jonami metali. Ten potencjał chelatujący in vitro ma następującą kolejność tworzenia: Al+3>Cu+2>Zn+2>Mg+2>Ca+2.
LEVAQUIN® Tabletki są dostępne w postaci tabletek powlekanych i zawierają następujące nieaktywne składniki:
- 250 mg (wyrażone w postaci bezwodnej): krospowidon, hypromeloza, stearynian magnezu, celuloza mikrokrystaliczna, glikol polietylenowy, polisorbat 80, syntetyczny czerwony tlenek żelaza i dwutlenek tytanu.
- 500 mg (wyrażone w postaci bezwodnej): krospowidon, hypromeloza, stearynian magnezu, celuloza mikrokrystaliczna, glikol polietylenowy, polisorbat 80, syntetyczne czerwone i żółte tlenki żelaza oraz dwutlenek tytanu.
- 750 mg (wyrażone w postaci bezwodnej): krospowidon, hypromeloza, stearynian magnezu, celuloza mikrokrystaliczna, glikol polietylenowy, polisorbat 80, dwutlenek tytanu.
WSKAZANIA
Szpitalne zapalenie płuc
LEVAQUIN® jest wskazany u dorosłych pacjentów w leczeniu szpitalnego zapalenia płuc wywołanego przez wrażliwe na metycylinę Staphylococcus aureus, Pseudomonas aeruginosa, Serratia marcescens, Escherichia coli, Klebsiella pneumoniae, Haemophilus influenzae lub Streptococcus pneumo. Terapia wspomagająca powinna być stosowana zgodnie ze wskazaniami klinicznymi. Gdy Pseudomonas aeruginosa jest udokumentowanym lub przypuszczalnym patogenem, zaleca się terapię skojarzoną z przeciwpseudomonalnym β-laktamem [patrz Studia kliniczne ].
Pozaszpitalne zapalenie płuc
Schemat leczenia od 7 do 14 dni
LEVAQUIN® jest wskazany u dorosłych pacjentów w leczeniu pozaszpitalnego zapalenia płuc wywołanego przez wrażliwe na metycylinę Staphylococcus aureus, Streptococcus pneumoniae (w tym wielolekooporny Streptococcus pneumoniae [MDRSP]), Haemophilus influenzae, Haemophilus parainfluenzae, Haemophilus parainfluenzae, , Chlamydophila pneumoniae, Legionella pneumophila lub Mycoplasma pneumoniae [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz Studia kliniczne ].
Izolaty MDRSP to izolaty oporne na dwa lub więcej z następujących środków przeciwbakteryjnych: penicylinę (MIC ≥2 µg/ml), cefalosporyny II generacji, np. cefuroksym, makrolidy, tetracykliny i trimetoprim/sulfametoksazol.
Pozaszpitalne zapalenie płuc
5-dniowy schemat leczenia
LEVAQUIN® jest wskazany u dorosłych pacjentów w leczeniu pozaszpitalnego zapalenia płuc wywołanego przez Streptococcus pneumoniae (z wyłączeniem izolatów wielolekoopornych [MDRSP]), Haemophilus influenzae, Haemophilus parainfluenzae, Mycoplasma pneumoniae lub Chlamydophila pneumoniae [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz Studia kliniczne ].
Skomplikowane infekcje skóry i struktury skóry
LEVAQUIN® jest wskazany u dorosłych pacjentów w leczeniu powikłanych zakażeń skóry i struktur skóry wywołanych przez wrażliwe na metycylinę Staphylococcus aureus, Enterococcus faecalis, Streptococcus pyogenes lub Proteus mirabilis [patrz Studia kliniczne ].
Nieskomplikowane infekcje skóry i struktury skóry
LEVAQUIN® jest wskazany u dorosłych pacjentów w leczeniu niepowikłanych zakażeń skóry i struktury skóry (łagodnych do umiarkowanych), w tym ropni, zapalenia tkanki łącznej, czyraków, liszajec, ropnego zapalenia skóry, zakażeń ran wywołanych przez wrażliwe na metycylinę Staphylococcus aureus lub Streptococcus pyogenes.
Przewlekłe bakteryjne zapalenie gruczołu krokowego
LEVAQUIN® jest wskazany u dorosłych pacjentów w leczeniu przewlekłego bakteryjnego zapalenia gruczołu krokowego wywołanego przez Escherichia coli, Enterococcus faecalis lub wrażliwego na metycylinę Staphylococcus epidermidis [patrz Studia kliniczne ].
Wąglik wziewny (po ekspozycji)
LEVAQUIN® jest wskazany do wąglika wziewnego (po ekspozycji) w celu zmniejszenia częstości występowania lub progresji choroby po ekspozycji na aerozol Bacillus anthracis u dorosłych i dzieci w wieku 6 miesięcy i starszych [patrz DAWKOWANIE I SPOSÓB PODAWANIA ]. Skuteczność LEVAQUIN® opiera się na stężeniach w osoczu osiąganych u ludzi, zastępczym punkcie końcowym, który może przewidywać korzyści kliniczne.
LEVAQUIN® nie był testowany na ludziach pod kątem zapobiegania wąglikowi inhalacyjnemu po ekspozycji. Nie badano bezpieczeństwa stosowania leku LEVAQUIN® u dorosłych w okresie leczenia dłuższym niż 28 dni lub u pacjentów pediatrycznych w okresie leczenia dłuższym niż 14 dni. Przedłużoną terapię LEVAQUIN® należy stosować tylko wtedy, gdy korzyści przewyższają ryzyko [patrz Studia kliniczne ].
Plaga
LEVAQUIN® jest wskazany do leczenia dżumy, w tym dżumy płucnej i posocznicy, wywołanej przez Yersinia pestis (Y. pestis) oraz profilaktyki dżumy u dorosłych i dzieci w wieku 6 miesięcy i starszych [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Badania skuteczności LEVAQUIN® nie mogły być prowadzone u ludzi z dżumą ze względów etycznych i wykonalności. Dlatego zatwierdzenie tego wskazania oparto na badaniu skuteczności przeprowadzonym na zwierzętach [patrz Studia kliniczne ].
Powikłane infekcje dróg moczowych
5-dniowy schemat leczenia
LEVAQUIN® jest wskazany u dorosłych pacjentów w leczeniu powikłanych zakażeń dróg moczowych wywołanych przez Escherichia coli, Klebsiella pneumoniae lub Proteus mirabilis [patrz Studia kliniczne ].
Powikłane infekcje dróg moczowych
10-dniowy schemat leczenia
LEVAQUIN® jest wskazany u dorosłych pacjentów w leczeniu powikłanych zakażeń dróg moczowych (łagodnych do umiarkowanych) wywołanych przez Enterococcus faecalis, Enterobacter cloacae, Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis lub Pseudomonas aeruginosa [patrz Studia kliniczne ].
Ostre odmiedniczkowe zapalenie nerek
5-dniowy lub 10-dniowy schemat leczenia
LEVAQUIN® jest wskazany u dorosłych pacjentów w leczeniu ostrego odmiedniczkowego zapalenia nerek wywołanego przez Escherichia coli, w tym przypadków ze współistniejącą bakteriemią [patrz Studia kliniczne ].
Nieskomplikowane infekcje dróg moczowych
LEVAQUIN® jest wskazany u dorosłych pacjentów w leczeniu niepowikłanych zakażeń dróg moczowych (łagodnych do umiarkowanych) wywołanych przez Escherichia coli, Klebsiella pneumoniae lub Staphylococcus saprophyticus.
Ponieważ fluorochinolony, w tym LEVAQUIN®, były związane z poważnymi działaniami niepożądanymi [patrz OSTRZEŻENIA I ŚRODKI ], a u niektórych pacjentów niepowikłane zakażenie dróg moczowych ustępuje samoistnie, należy zarezerwować LEVAQUIN® do leczenia niepowikłanych zakażeń dróg moczowych u pacjentów, którzy nie mają alternatywnych opcji leczenia.
Ostre bakteryjne zaostrzenie przewlekłego zapalenia oskrzeli
LEVAQUIN® jest wskazany u dorosłych pacjentów w leczeniu ostrego bakteryjnego zaostrzenia przewlekłego zapalenia oskrzeli (ABECB) wywołanego przez wrażliwe na metycylinę Staphylococcus aureus, Streptococcus pneumoniae, Haemophilus influenzae, Haemophilus parainfluenzae lub Moraxella catarrhalis.
Ponieważ fluorochinolony, w tym LEVAQUIN®, były związane z poważnymi działaniami niepożądanymi [patrz OSTRZEŻENIA I ŚRODKI ], a dla niektórych pacjentów ABECB samoogranicza się, należy zarezerwować LEVAQUIN® do leczenia ABECB u pacjentów, którzy nie mają alternatywnych opcji leczenia.
Ostre bakteryjne zapalenie zatok
5-dniowe i 10-14-dniowe schematy leczenia
LEVAQUIN® jest wskazany u dorosłych pacjentów w leczeniu ostrego bakteryjnego zapalenia zatok (ABS) wywołanego przez Streptococcus pneumoniae, Haemophilus influenzae lub Moraxella catarrhalis [patrz Studia kliniczne ].
Ponieważ fluorochinolony, w tym LEVAQUIN®, były związane z poważnymi działaniami niepożądanymi [patrz OSTRZEŻENIA I ŚRODKI ], au niektórych pacjentów ABS jest samoograniczający, należy zarezerwować LEVAQUIN® do leczenia ABS u pacjentów, którzy nie mają alternatywnych opcji leczenia.
Stosowanie
Aby ograniczyć rozwój bakterii opornych na leki i utrzymać skuteczność LEVAQUIN® i innych leków przeciwbakteryjnych, LEVAQUIN® należy stosować wyłącznie w leczeniu lub zapobieganiu zakażeniom, co do których udowodniono, lub co do których istnieje silne podejrzenie, że są wywołane przez wrażliwe bakterie. Gdy dostępne są informacje dotyczące hodowli i wrażliwości, należy je uwzględnić przy wyborze lub modyfikacji terapii przeciwbakteryjnej. W przypadku braku takich danych, lokalna epidemiologia i wzorce podatności mogą przyczynić się do empirycznego doboru terapii.
Badanie kultury i podatności
Przed leczeniem należy przeprowadzić odpowiednie posiewy i testy wrażliwości w celu wyizolowania i identyfikacji drobnoustrojów powodujących zakażenie oraz określenia ich wrażliwości na lewofloksacynę [patrz Mikrobiologia ]. Terapię lekiem LEVAQUIN® można rozpocząć przed poznaniem wyników tych testów; gdy wyniki staną się dostępne, należy wybrać odpowiednią terapię.
Podobnie jak w przypadku innych leków z tej klasy, niektóre izolaty Pseudomonas aeruginosa mogą dość szybko rozwinąć oporność podczas leczenia LEVAQUIN®. Badania kultur i wrażliwości przeprowadzane okresowo podczas terapii dostarczą informacji o ciągłej wrażliwości patogenów na środek przeciwdrobnoustrojowy, a także o możliwym pojawieniu się oporności bakterii.
DAWKOWANIE I SPOSÓB PODAWANIA
Dawkowanie tabletek LEVAQUIN® u dorosłych pacjentów z klirensem kreatyniny ≥ 50 ml/minutę
Zazwyczaj stosowana dawka leku LEVAQUIN® w tabletkach wynosi 250 mg, 500 mg lub 750 mg podawana doustnie co 24 godziny, zgodnie ze wskazaniami zakażenia i opisanymi w Tabeli 1.
Zalecenia te dotyczą pacjentów z klirensem kreatyniny ≥ 50 ml/min. U pacjentów z klirensem kreatyniny mniejszym niż 50 ml/min konieczna jest modyfikacja schematu dawkowania [patrz Dostosowanie dawkowania u dorosłych z zaburzeniami czynności nerek ].
Dawkowanie tabletek LEVAQUIN® u pacjentów pediatrycznych z wąglikiem lub dżumą wziewną
Dawkowanie tabletek LEVAQUIN® w przypadku wąglika wziewnego (po ekspozycji) i dżumy u dzieci o masie ciała 30 kg lub większej opisano poniżej w Tabeli 2. LEVAQUIN® w tabletkach nie można podawać pacjentom o masie ciała poniżej 30 kg ze względu na ograniczenia dostępnej siły. W przypadku dzieci o masie ciała poniżej 30 kg można rozważyć alternatywne postacie lewofloksacyny.
Dostosowanie dawkowania u dorosłych z zaburzeniami czynności nerek
LEVAQUIN® należy stosować ostrożnie u pacjentów z zaburzeniami czynności nerek. Przed rozpoczęciem leczenia iw trakcie leczenia należy prowadzić dokładną obserwację kliniczną i odpowiednie badania laboratoryjne, ponieważ u tych pacjentów eliminacja lewofloksacyny może być zmniejszona.
U pacjentów z zaburzeniami czynności nerek (klirens kreatyniny mniejszy niż 50 ml/min) konieczna jest modyfikacja dawkowania, aby uniknąć kumulacji lewofloksacyny z powodu zmniejszonego klirensu [patrz Używaj w określonych populacjach ]. Nie ma konieczności dostosowania u pacjentów z klirensem kreatyniny większym lub równym 50 ml/minutę.
Tabela 3 pokazuje, jak dostosować dawkę na podstawie klirensu kreatyniny.
Interakcje leków z czynnikami chelatującymi
Leki zobojętniające sok żołądkowy, sukralfat, kationy metali, multiwitaminy
LEVAQUIN® Tabletki należy podawać co najmniej dwie godziny przed lub dwie godziny po podaniu leków zobojętniających zawierających magnez, glin, a także sukralfat, kationy metali, takich jak żelazo i preparaty multiwitaminowe z cynkiem lub didanozyną w postaci tabletek do żucia/buforowanych lub proszku do sporządzania roztworu doustnego dla dzieci [Widzieć INTERAKCJE Z LEKAMI oraz INFORMACJA O PACJENCIE ].
Instrukcje administracyjne
LEVAQUIN® Tabletki można podawać niezależnie od posiłków.
Nawilżenie dla pacjentów otrzymujących tabletki LEVAQUIN®
Należy utrzymywać odpowiednie nawodnienie pacjentów otrzymujących LEVAQUIN®, aby zapobiec tworzeniu się silnie stężonego moczu. Krystaluria i cylindruria były zgłaszane w przypadku chinolonów [patrz DZIAŁANIA NIEPOŻĄDANE oraz INFORMACJA O PACJENCIE ].
JAK DOSTARCZONE
Formy dawkowania i mocne strony
TABLETKI, powlekane, w kształcie kapsułki
- 250 mg różowe tabletki z terakoty, z nadrukiem „250” po jednej stronie i „LEVAQUIN” po drugiej stronie
- Tabletki brzoskwiniowe 500 mg z nadrukiem „500” po jednej stronie i „LEVAQUIN” po drugiej stronie
- Białe tabletki 750 mg z nadrukiem „750” po jednej stronie i „LEVAQUIN” po drugiej stronie
Składowania i stosowania
Tabletki LEVAQUIN® są dostarczane w postaci tabletek powlekanych w kształcie kapsułki o mocy 250, 500 i 750 mg.
LEVAQUIN® Tabletki pakowane są w butelki w następujących konfiguracjach:
- Tabletki 250 mg są terra cotta w kolorze różowym i mają nadruk „LEVAQUIN®” po jednej stronie i „250” po drugiej stronie
- butelki po 50 ( NDC 50458-920-50)
- Tabletki 500 mg są brzoskwiniowe i mają nadruk „LEVAQUIN®” po jednej stronie i „500” po drugiej stronie
- butelki po 50 ( NDC 50458-925-50)
- Tabletki 750 mg są białe i mają nadruk „LEVAQUIN®” po jednej stronie i „750” po drugiej stronie
- butelki po 20 ( NDC 50458-930-20)
Tabletki LEVAQUIN® należy przechowywać w temperaturze od 15° do 30°C (od 59° do 86°F) w dobrze zamkniętych pojemnikach.
Wyprodukowane przez: Aktywny składnik Wyprodukowano w Japonii. Aktualizacja: lipiec 2018 r.
SKUTKI UBOCZNE
Poważne i poza tym ważne działania niepożądane
Następujące poważne i poza tym ważne działania niepożądane leku omówiono bardziej szczegółowo w innych punktach oznakowania:
- Unieruchamiające i potencjalnie nieodwracalne poważne reakcje niepożądane [patrz OSTRZEŻENIA I ŚRODKI ]
- Zapalenie ścięgna i zerwanie ścięgna [patrz OSTRZEŻENIA I ŚRODKI ]
- Neuropatia obwodowa [patrz OSTRZEŻENIA I ŚRODKI ]
- Skutki na ośrodkowy układ nerwowy [patrz OSTRZEŻENIA I ŚRODKI ]
- Zaostrzenie miastenii Gravis [patrz OSTRZEŻENIA I ŚRODKI ]
- Inne poważne i czasami śmiertelne reakcje [patrz OSTRZEŻENIA I ŚRODKI ]
- Reakcje nadwrażliwości [patrz OSTRZEŻENIA I ŚRODKI ]
- Hepatotoksyczność [patrz OSTRZEŻENIA I ŚRODKI ]
- Biegunka związana z Clostridium difficile [patrz OSTRZEŻENIA I ŚRODKI ]
- Wydłużenie odstępu QT [patrz OSTRZEŻENIA I ŚRODKI ]
- Zaburzenia mięśniowo-szkieletowe u pacjentów pediatrycznych [patrz OSTRZEŻENIA I ŚRODKI ]
- Zaburzenia glukozy we krwi [patrz OSTRZEŻENIA I ŚRODKI ]
- Światłoczułość/Fototoksyczność [patrz OSTRZEŻENIA I ŚRODKI ]
- Rozwój bakterii lekoopornych [patrz OSTRZEŻENIA I ŚRODKI ]
W przypadku chinolonów, w tym LEVAQUIN®, donoszono o krystalurii i cylindrurii. Dlatego należy utrzymywać odpowiednie nawodnienie pacjentów otrzymujących LEVAQUIN®, aby zapobiec tworzeniu się silnie stężonego moczu [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Dane opisane poniżej odzwierciedlają ekspozycję na LEVAQUIN® u 7537 pacjentów w 29 zbiorczych badaniach klinicznych III fazy. Badana populacja miała średni wiek 50 lat (około 74% populacji było w wieku WSKAZANIA ]. Pacjenci otrzymywali dawki LEVAQUIN® 750 mg raz na dobę, 250 mg raz na dobę lub 500 mg raz lub dwa razy na dobę.
Czas trwania leczenia wynosił zwykle 3–14 dni, a średnia liczba dni terapii wynosiła 10 dni.
Ogólna częstość występowania, rodzaj i rozkład działań niepożądanych były podobne u pacjentów otrzymujących LEVAQUIN® w dawkach 750 mg raz na dobę, 250 mg raz na dobę i 500 mg raz lub dwa razy na dobę.
Przerwanie leczenia LEVAQUIN® z powodu działań niepożądanych leku wystąpiło ogółem u 4,3% pacjentów, 3,8% pacjentów leczonych dawkami 250 mg i 500 mg oraz 5,4% pacjentów leczonych dawką 750 mg. Najczęstszymi działaniami niepożądanymi prowadzącymi do przerwania stosowania dawek 250 i 500 mg były zaburzenia żołądkowo-jelitowe (1,4%), głównie nudności (0,6%); wymioty (0,4%); zawroty głowy (0,3%); i ból głowy (0,2%). Najczęstszymi działaniami niepożądanymi prowadzącymi do przerwania stosowania dawki 750 mg były żołądkowo-jelitowe (1,2%), głównie nudności (0,6%), wymioty (0,5%); zawroty głowy (0,3%); i ból głowy (0,3%).
Działania niepożądane występujące u ≥1% pacjentów leczonych LEVAQUIN® i mniej częste działania niepożądane, występujące u 0,1 do
badaniach klinicznych z zastosowaniem terapii wielodawkowej u pacjentów leczonych chinolonami, w tym lekiem LEVAQUIN®, zaobserwowano nieprawidłowości okulistyczne, w tym zaćmę i mnogie punktowe zmętnienia soczewki. Związek leków z tymi wydarzeniami nie jest obecnie ustalony.
Doświadczenie postmarketingowe
W Tabeli 6 wymieniono działania niepożądane, które zostały zidentyfikowane podczas stosowania leku LEVAQUIN® po dopuszczeniu do obrotu. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
INTERAKCJE Z LEKAMI
Środki chelatujące
Leki zobojętniające sok żołądkowy, sukralfat, kationy metali, multiwitaminy
Chociaż chelatacja przez kationy dwuwartościowe jest słabsza niż w przypadku innych fluorochinolonów, jednoczesne podawanie tabletek LEVAQUIN® ze środkami zobojętniającymi zawierającymi magnez lub glin, a także sukralfatem, kationami metali, takimi jak żelazo, oraz preparatami wielowitaminowymi z cynkiem może zakłócać wchłanianie z przewodu pokarmowego lewofloksacyny, co powoduje, że poziomy ogólnoustrojowe są znacznie niższe niż pożądane. Tabletki zawierające środki zobojętniające kwasy zawierające magnez, glin, jak również sukralfat, kationy metali, takich jak żelazo, oraz preparaty multiwitaminowe z cynkiem lub didanozyną mogą znacząco zaburzać wchłanianie lewofloksacyny z przewodu pokarmowego, powodując znacznie niższe poziomy ogólnoustrojowe niż pożądane. Środki te należy przyjmować co najmniej dwie godziny przed lub dwie godziny po podaniu doustnym LEVAQUIN®.
Warfaryna
badaniu klinicznym z udziałem zdrowych ochotników nie wykryto znaczącego wpływu LEVAQUIN® na maksymalne stężenia w osoczu, AUC i inne parametry rozmieszczenia R- i S-warfaryny. Podobnie nie zaobserwowano wyraźnego wpływu warfaryny na wchłanianie i wydalanie lewofloksacyny. Jednakże pojawiły się doniesienia po wprowadzeniu do obrotu u pacjentów, że LEVAQUIN® wzmacnia działanie warfaryny. Wydłużenie czasu protrombinowego w przypadku jednoczesnego stosowania warfaryny i LEVAQUIN® było związane z epizodami krwawienia. Czas protrombinowy, międzynarodowy współczynnik znormalizowany (INR) lub inne odpowiednie testy przeciwzakrzepowe powinny być ściśle monitorowane, jeśli LEVAQUIN® jest podawany jednocześnie z warfaryną. Pacjentów należy również monitorować pod kątem oznak krwawienia [patrz DZIAŁANIA NIEPOŻĄDANE oraz INFORMACJA O PACJENCIE ].
Leki przeciwcukrzycowe
pacjentów leczonych jednocześnie fluorochinolonami i lekiem przeciwcukrzycowym zgłaszano zaburzenia stężenia glukozy we krwi, w tym hiperglikemię i hipoglikemię. Dlatego zaleca się dokładne monitorowanie stężenia glukozy we krwi podczas jednoczesnego podawania tych leków [patrz OSTRZEŻENIA I ŚRODKI , DZIAŁANIA NIEPOŻĄDANE , oraz INFORMACJA O PACJENCIE ].
Niesteroidowe leki przeciwzapalne
Jednoczesne podawanie niesteroidowego leku przeciwzapalnego z fluorochinolonem, w tym LEVAQUIN®, może zwiększać ryzyko pobudzenia ośrodkowego układu nerwowego i napadów drgawkowych [patrz OSTRZEŻENIA I ŚRODKI ].
Teofilina
badaniu klinicznym z udziałem zdrowych ochotników nie wykryto znaczącego wpływu LEVAQUIN® na stężenia w osoczu, AUC i inne parametry rozmieszczenia teofiliny. Podobnie nie zaobserwowano wyraźnego wpływu teofiliny na wchłanianie i wydalanie lewofloksacyny. Jednak jednoczesne podawanie innych fluorochinolonów z teofiliną spowodowało wydłużenie okresu półtrwania w fazie eliminacji, zwiększenie stężenia teofiliny w surowicy, a następnie zwiększenie ryzyka działań niepożądanych związanych z teofiliną w populacji pacjentów. Dlatego podczas jednoczesnego podawania LEVAQUIN® należy ściśle monitorować stężenie teofiliny i odpowiednio dostosowywać dawkowanie. Działania niepożądane, w tym drgawki, mogą wystąpić z podwyższeniem poziomu teofiliny w surowicy lub bez niego [patrz OSTRZEŻENIA I ŚRODKI ].
Cyklosporyna
badaniu klinicznym z udziałem zdrowych ochotników nie wykryto znaczącego wpływu LEVAQUIN® na maksymalne stężenia w osoczu, AUC i inne parametry rozmieszczenia cyklosporyny. Jednak w populacji pacjentów zgłaszano podwyższone stężenie cyklosporyny w surowicy, gdy podawano ją jednocześnie z niektórymi innymi fluorochinolonami. Cmax i ke lewofloksacyny były nieco niższe, podczas gdy Tmax i t1/2 były nieco dłuższe w obecności cyklosporyny niż te obserwowane w innych badaniach bez jednoczesnego leczenia. Różnice nie są jednak uważane za istotne klinicznie. W związku z tym nie jest konieczne dostosowanie dawki dla LEVAQUIN® lub cyklosporyny przy jednoczesnym podawaniu.
Digoksyna
badaniu klinicznym z udziałem zdrowych ochotników nie wykryto znaczącego wpływu LEVAQUIN® na maksymalne stężenia w osoczu, AUC i inne parametry dyspozycji digoksyny. Kinetyka wchłaniania i usuwania lewofloksacyny była podobna w obecności lub nieobecności digoksyny. Dlatego nie ma konieczności dostosowania dawki LEVAQUIN® lub digoksyny przy jednoczesnym podawaniu.
probenecyd i cymetydyna
W badaniu klinicznym z udziałem zdrowych ochotników nie zaobserwowano znaczącego wpływu probenecydu lub cymetydyny na Cmax lewofloksacyny. AUC i t1/2 lewofloksacyny były wyższe, podczas gdy CL/F i CLR były niższe podczas jednoczesnego leczenia LEVAQUIN® z probenecydem lub cymetydyną w porównaniu z samym LEVAQUIN®. Jednak zmiany te nie uzasadniają dostosowania dawki LEVAQUIN® podczas jednoczesnego podawania probenecydu lub cymetydyny.
Interakcje z testami laboratoryjnymi lub diagnostycznymi
Niektóre fluorochinolony, w tym LEVAQUIN®, mogą dawać fałszywie dodatnie wyniki badań przesiewowych moczu na obecność opiatów przy użyciu dostępnych w handlu zestawów do testów immunologicznych. Może być konieczne potwierdzenie pozytywnych badań przesiewowych na obecność opiatów bardziej szczegółowymi metodami.
OSTRZEŻENIA
Zawarte jako część "ŚRODKI OSTROŻNOŚCI" Sekcja
ŚRODKI OSTROŻNOŚCI
Unieruchamiające i potencjalnie nieodwracalne poważne reakcje niepożądane, w tym zapalenie ścięgna i zerwanie ścięgna, neuropatia obwodowa i skutki ośrodkowego układu nerwowego
Fluorochinolony, w tym LEVAQUIN®, są związane z uniemożliwiającymi i potencjalnie nieodwracalnymi poważnymi działaniami niepożądanymi z różnych układów organizmu, które mogą wystąpić razem u tego samego pacjenta. Często obserwowane działania niepożądane obejmują zapalenie ścięgna, zerwanie ścięgna, ból stawów, ból mięśni, neuropatię obwodową i objawy ze strony ośrodkowego układu nerwowego (omamy, lęk, depresja, bezsenność, silne bóle głowy i splątanie). Reakcje te mogą wystąpić w ciągu kilku godzin lub tygodni po rozpoczęciu leczenia LEVAQUIN®. Te działania niepożądane wystąpiły u pacjentów w każdym wieku lub bez wcześniej istniejących czynników ryzyka [patrz Zapalenie ścięgna i zerwanie ścięgna, neuropatia obwodowa, wpływ na ośrodkowy układ nerwowy ].
Należy natychmiast przerwać podawanie LEVAQUIN® przy pierwszych oznakach lub objawach jakiejkolwiek poważnej reakcji niepożądanej. Ponadto należy unikać stosowania fluorochinolonów, w tym LEVAQUIN®, u pacjentów, u których wystąpiły którekolwiek z tych poważnych działań niepożądanych związanych z fluorochinolonami.
Zapalenie ścięgna i zerwanie ścięgna
Fluorochinolony, w tym LEVAQUIN®, są związane ze zwiększonym ryzykiem zapalenia ścięgna i zerwania ścięgna w każdym wieku [patrz Unieruchamiające i potencjalnie nieodwracalne poważne reakcje niepożądane, w tym zapalenie ścięgna i zerwanie ścięgna, neuropatia obwodowa i skutki ośrodkowego układu nerwowego oraz DZIAŁANIA NIEPOŻĄDANE ]. Ta reakcja niepożądana najczęściej dotyczy ścięgna Achillesa i była również zgłaszana w przypadku stożka rotatorów (barku), ręki, bicepsa, kciuka i innych miejsc ścięgna. Zapalenie ścięgna lub zerwanie ścięgna może wystąpić w ciągu kilku godzin lub dni od rozpoczęcia leczenia lekiem LEVAQUIN® lub nawet kilka miesięcy po zakończeniu leczenia fluorochinolonami. Zapalenie ścięgna i zerwanie ścięgna może wystąpić obustronnie.
Ryzyko rozwoju zapalenia ścięgna związanego z fluorochinolonami i zerwania ścięgna jest zwiększone u pacjentów w wieku powyżej 60 lat, u pacjentów przyjmujących kortykosteroidy oraz u pacjentów po przeszczepieniu nerki, serca lub płuc. Inne czynniki, które mogą niezależnie zwiększać ryzyko zerwania ścięgna, obejmują forsowną aktywność fizyczną, niewydolność nerek i wcześniejsze schorzenia ścięgien, takie jak reumatoidalne zapalenie stawów. Zapalenie ścięgna i zerwanie ścięgna zgłaszano u pacjentów przyjmujących fluorochinolony, u których nie występują powyższe czynniki ryzyka. Należy natychmiast przerwać podawanie LEVAQUIN®, jeśli pacjent odczuwa ból, obrzęk, stan zapalny lub zerwanie ścięgna. Pacjentom należy zalecić odpoczynek przy pierwszych objawach zapalenia ścięgna lub zerwania ścięgna oraz skontaktowanie się z lekarzem w sprawie zmiany na lek przeciwdrobnoustrojowy niebędący chinolonami. Unikaj LEVAQUIN® u pacjentów, u których w wywiadzie występowały zaburzenia ścięgna lub zerwanie ścięgna [patrz DZIAŁANIA NIEPOŻĄDANE oraz INFORMACJA O PACJENCIE ].
Neuropatia obwodowa
Fluorochinolony, w tym LEVAQUIN®, są związane ze zwiększonym ryzykiem neuropatii obwodowej. U pacjentów otrzymujących fluorochinolony, w tym LEVAQUIN®, zgłaszano przypadki czuciowej lub czuciowo-ruchowej polineuropatii aksonów obejmującej małe i (lub) duże aksony, powodujące parestezje, niedoczulica, zaburzenia czucia i osłabienie. Objawy mogą wystąpić wkrótce po rozpoczęciu LEVAQUIN® i mogą być nieodwracalne u niektórych pacjentów [patrz Unieruchamiające i potencjalnie nieodwracalne poważne reakcje niepożądane, w tym zapalenie ścięgna i zerwanie ścięgna, neuropatia obwodowa i skutki ośrodkowego układu nerwowego oraz DZIAŁANIA NIEPOŻĄDANE ].
Należy natychmiast przerwać podawanie LEVAQUIN®, jeśli u pacjenta wystąpią objawy neuropatii, w tym ból, pieczenie, mrowienie, drętwienie i/lub osłabienie lub inne zmiany czucia, w tym lekki dotyk, ból, temperatura, czucie pozycji i uczucie wibracji. Unikaj fluorochinolonów, w tym LEVAQUIN® , u pacjentów, u których wcześniej wystąpiła neuropatia obwodowa [patrz DZIAŁANIA NIEPOŻĄDANE oraz INFORMACJA O PACJENCIE ].
Skutki dla centralnego układu nerwowego
Fluorochinolony, w tym LEVAQUIN®, są związane ze zwiększonym ryzykiem wystąpienia działań ośrodkowego układu nerwowego (OUN), w tym drgawek, psychoz toksycznych, zwiększonego ciśnienia śródczaszkowego (w tym guza rzekomego mózgu). Fluorochinolony mogą również powodować stymulację ośrodkowego układu nerwowego, co może prowadzić do drżenia, niepokoju, lęku, zawrotów głowy, dezorientacji, halucynacji, paranoi, depresji, koszmarów sennych i bezsenności. Mogą również wystąpić myśli samobójcze oraz próby samobójcze lub próby samobójcze, zwłaszcza u pacjentów z depresją w wywiadzie lub z podstawowym czynnikiem ryzyka depresji. Reakcje te mogą wystąpić po pierwszej dawce. Jeśli te reakcje wystąpią u pacjentów otrzymujących LEVAQUIN®, należy przerwać podawanie LEVAQUIN® i podjąć odpowiednie działania. Podobnie jak w przypadku innych fluorochinolonów, LEVAQUIN® należy stosować ostrożnie u pacjentów z rozpoznaną lub podejrzewaną chorobą ośrodkowego układu nerwowego (OUN), która może predysponować ich do napadów drgawkowych lub obniżyć próg drgawkowy (np. ciężka miażdżyca naczyń mózgowych, padaczka) lub w przypadku innych czynników ryzyka, które mogą predysponować do napadów drgawkowych lub obniżać próg drgawkowy (np. niektóre leki, zaburzenia czynności nerek). [Widzieć DZIAŁANIA NIEPOŻĄDANE , INTERAKCJE Z LEKAMI , oraz INFORMACJA O PACJENCIE ].
Zaostrzenie miastenii Gravis
Fluorochinolony, w tym LEVAQUIN®, mają działanie blokujące przewodnictwo nerwowo-mięśniowe i mogą nasilać osłabienie mięśni u pacjentów z miastenią. Stosowanie fluorochinolonów u pacjentów z miastenią było związane ze stosowaniem fluorochinolonów po wprowadzeniu do obrotu ciężkich działań niepożądanych, w tym zgonów i konieczności wspomagania wentylacji. Unikaj LEVAQUIN® u pacjentów ze znaną historią miastenii [patrz DZIAŁANIA NIEPOŻĄDANE oraz INFORMACJA O PACJENCIE ].
Inne poważne, a czasem śmiertelne reakcje niepożądane
Inne ciężkie i czasami prowadzące do zgonu działania niepożądane, niektóre z powodu nadwrażliwości, a inne z powodu niepewnej etiologii, były rzadko zgłaszane u pacjentów leczonych fluorochinolonami, w tym LEVAQUIN®. Zdarzenia te mogą mieć ciężki przebieg i zwykle występują po podaniu wielokrotnych dawek. Objawy kliniczne mogą obejmować jedno lub więcej z następujących:
- gorączka, wysypka lub ciężkie reakcje dermatologiczne (np. toksyczna nekroliza naskórka, zespół Stevensa-Johnsona);
- zapalenie naczyń; ból stawów; ból mięśni; choroba posurowicza;
- alergiczne zapalenie płuc;
- śródmiąższowe zapalenie nerek; ostra niewydolność lub niewydolność nerek;
- zapalenie wątroby; żółtaczka; ostra martwica lub niewydolność wątroby;
- anemia, w tym hemolityczna i aplastyczna; małopłytkowość, w tym zakrzepowa plamica małopłytkowa; leukopenia; agranulocytoza; pancytopenia; i/lub inne nieprawidłowości hematologiczne.
Należy natychmiast przerwać stosowanie LEVAQUIN® przy pierwszym pojawieniu się wysypki skórnej, żółtaczki lub jakichkolwiek innych objawów nadwrażliwości i zastosować środki wspomagające [patrz DZIAŁANIA NIEPOŻĄDANE oraz INFORMACJA O PACJENCIE ].
Reakcje nadwrażliwości
pacjentów leczonych fluorochinolonami, w tym LEVAQUIN®, zgłaszano poważną i niekiedy śmiertelną nadwrażliwość i (lub) reakcje anafilaktyczne. Reakcje te często występują po pierwszej dawce. Niektórym reakcjom towarzyszyły zapaść sercowo-naczyniowa, niedociśnienie/wstrząs, drgawki, utrata przytomności, mrowienie, obrzęk naczynioruchowy (w tym obrzęk języka, krtani, gardła lub twarzy), niedrożność dróg oddechowych (w tym skurcz oskrzeli, duszność i ostry oddech ), duszność, pokrzywka, swędzenie i inne poważne reakcje skórne. LEVAQUIN® należy odstawić natychmiast po pierwszym pojawieniu się wysypki skórnej lub jakichkolwiek innych objawów nadwrażliwości. Poważne ostre reakcje nadwrażliwości mogą wymagać leczenia epinefryną i innymi środkami resuscytacyjnymi, w tym tlenem, płynami dożylnymi, lekami przeciwhistaminowymi, kortykosteroidami, aminami presyjnymi i leczeniem dróg oddechowych, zgodnie ze wskazaniami klinicznymi [patrz DZIAŁANIA NIEPOŻĄDANE oraz INFORMACJA O PACJENCIE ].
Hepatotoksyczność
Po wprowadzeniu leku do obrotu otrzymano zgłoszenia ciężkiej hepatotoksyczności (w tym ostrego zapalenia wątroby i zdarzeń śmiertelnych) u pacjentów leczonych lekiem LEVAQUIN®. W badaniach klinicznych z udziałem ponad 7000 pacjentów nie wykryto dowodów na poważną hepatotoksyczność związaną z lekami. Ciężka hepatotoksyczność występowała na ogół w ciągu 14 dni od rozpoczęcia leczenia, a większość przypadków wystąpiła w ciągu 6 dni. Większość przypadków ciężkiej hepatotoksyczności nie była związana z nadwrażliwością [patrz Inne poważne, a czasem śmiertelne reakcje niepożądane ].
Większość zgłoszeń śmiertelnych przypadków hepatotoksyczności wystąpiła u pacjentów w wieku 65 lat lub starszych i większość nie była związana z nadwrażliwością. LEVAQUIN® należy natychmiast odstawić, jeśli u pacjenta wystąpią oznaki i objawy zapalenia wątroby [patrz DZIAŁANIA NIEPOŻĄDANE oraz INFORMACJA O PACJENCIE ].
Biegunka związana z Clostridium Difficile
Biegunkę związaną z Clostridium difficile (CDAD) zgłaszano po zastosowaniu prawie wszystkich środków przeciwbakteryjnych, w tym LEVAQUIN®, a jej nasilenie może wahać się od łagodnej biegunki do śmiertelnego zapalenia okrężnicy. Leczenie środkami przeciwbakteryjnymi zmienia normalną florę okrężnicy, prowadząc do przerostu C. difficile.
C. difficile wytwarza toksyny A i B, które przyczyniają się do rozwoju CDAD. Szczepy C. difficile wytwarzające hipertoksyny powodują zwiększoną zachorowalność i śmiertelność, ponieważ zakażenia te mogą być oporne na leczenie przeciwbakteryjne i mogą wymagać kolektomii. CDAD należy rozważyć u wszystkich pacjentów, u których po zastosowaniu antybiotyków wystąpi biegunka. Konieczna jest staranna historia choroby, ponieważ donoszono, że CDAD występuje w ciągu dwóch miesięcy po podaniu leków przeciwbakteryjnych.
W przypadku podejrzenia lub potwierdzenia CDAD, może być konieczne przerwanie trwającego stosowania antybiotyków, które nie są skierowane przeciwko C. difficile. W zależności od wskazań klinicznych należy wdrożyć odpowiednią gospodarkę wodno-elektrolitową, suplementację białka, antybiotykoterapię C. difficile oraz ocenę chirurgiczną [patrz DZIAŁANIA NIEPOŻĄDANE oraz INFORMACJA O PACJENCIE ].
Wydłużenie odstępu QT
Niektóre fluorochinolony, w tym LEVAQUIN®, były związane z wydłużeniem odstępu QT w elektrokardiogramie i rzadkimi przypadkami arytmii. Rzadkie przypadki torsade de pointes zgłaszano spontanicznie podczas obserwacji po wprowadzeniu do obrotu u pacjentów otrzymujących fluorochinolony, w tym LEVAQUIN®. LEVAQUIN® należy unikać u pacjentów ze stwierdzonym wydłużeniem odstępu QT, pacjentów z niewyrównaną hipokaliemią oraz pacjentów otrzymujących leki przeciwarytmiczne klasy IA (chinidyna, prokainamid) lub klasy III (amiodaron, sotalol). Pacjenci w podeszłym wieku mogą być bardziej podatni na wpływ leków na odstęp QT [patrz DZIAŁANIA NIEPOŻĄDANE , Używaj w określonych populacjach , oraz INFORMACJA O PACJENCIE ].
Zaburzenia mięśniowo-szkieletowe u pacjentów pediatrycznych i skutki artropatii u zwierząt
LEVAQUIN® jest wskazany u pacjentów pediatrycznych (w wieku 6 miesięcy i starszych) wyłącznie w profilaktyce wąglika wziewnego (po ekspozycji) i dżumy [patrz WSKAZANIA ]. U pacjentów pediatrycznych otrzymujących LEVAQUIN® zaobserwowano zwiększoną częstość występowania zaburzeń mięśniowo-szkieletowych (bóle stawów, zapalenie stawów, tendinopatie i zaburzenia chodu) w porównaniu z grupą kontrolną [patrz Używaj w określonych populacjach ].
U niedojrzałych szczurów i psów doustne i dożylne podawanie lewofloksacyny powodowało nasilenie osteochondrozy. Badanie histopatologiczne stawów obciążonych niedojrzałych psów, którym podawano lewofloksacynę, wykazało trwałe uszkodzenia chrząstki. Inne fluorochinolony również powodują podobne nadżerki w stawach obciążonych i inne objawy artropatii u niedojrzałych zwierząt różnych gatunków [patrz Farmakologia zwierząt ].
Zaburzenia glukozy we krwi
Podobnie jak w przypadku innych fluorochinolonów, po zastosowaniu LEVAQUIN® zgłaszano zaburzenia stężenia glukozy we krwi, w tym objawową hiper- i hipoglikemię, zwykle u pacjentów z cukrzycą otrzymujących jednocześnie leczenie doustnym środkiem hipoglikemizującym (np. gliburydem) lub insuliną. U tych pacjentów zaleca się dokładne monitorowanie stężenia glukozy we krwi. Jeśli u pacjenta leczonego lekiem LEVAQUIN® wystąpi reakcja hipoglikemiczna, należy odstawić LEVAQUIN® i natychmiast rozpocząć odpowiednie leczenie [patrz DZIAŁANIA NIEPOŻĄDANE , INTERAKCJE Z LEKAMI oraz INFORMACJA O PACJENCIE ].
Światłoczułość/Fototoksyczność
Umiarkowana lub ciężka reakcja nadwrażliwości na światło/fototoksyczność, z których ta ostatnia może objawiać się nadmiernymi reakcjami na oparzenia słoneczne (np. pieczenie, rumień, wysięk, pęcherzyki, pęcherze, obrzęk) obejmujące obszary wystawione na światło (zazwyczaj twarz, obszar „V” szyi , prostowników powierzchni przedramion, grzbietu dłoni), może wiązać się ze stosowaniem fluorochinolonów po ekspozycji na słońce lub promieniowanie UV. Dlatego należy unikać nadmiernej ekspozycji na te źródła światła. Leczenie farmakologiczne należy przerwać, jeśli wystąpi nadwrażliwość na światło/fototoksyczność [patrz DZIAŁANIA NIEPOŻĄDANE oraz INFORMACJA O PACJENCIE ].
Rozwój bakterii lekoopornych
Przepisywanie LEVAQUIN® w przypadku braku udowodnionego lub silnie podejrzewanego zakażenia bakteryjnego lub wskazania profilaktycznego raczej nie przyniesie korzyści pacjentowi i zwiększy ryzyko rozwoju bakterii lekoopornych [patrz INFORMACJA O PACJENCIE ].
Informacje dotyczące poradnictwa dla pacjentów
Poinformuj pacjenta, aby przeczytał zatwierdzone przez FDA oznakowanie pacjenta ( Przewodnik po lekach ).
Poważne działania niepożądane
Należy doradzić pacjentom, aby zaprzestali przyjmowania leku LEVAQUIN® w przypadku wystąpienia działań niepożądanych i skontaktowali się z lekarzem w celu uzyskania porady dotyczącej zakończenia pełnego cyklu leczenia innym lekiem przeciwbakteryjnym.
Poinformuj pacjentów o następujących ciężkich działaniach niepożądanych, które były związane ze stosowaniem LEVAQUIN® lub innych fluorochinolonów:
- Unieruchamiające i potencjalnie nieodwracalne poważne reakcje niepożądane, które mogą wystąpić razem: Należy poinformować pacjentów, że wyłączenie i potencjalnie nieodwracalne poważne działania niepożądane, w tym zapalenie i zerwanie ścięgna, neuropatie obwodowe i wpływ na ośrodkowy układ nerwowy, są związane ze stosowaniem leku LEVAQUIN® i mogą wystąpić razem u tego samego pacjenta. Należy poinformować pacjentów, aby w przypadku wystąpienia działań niepożądanych natychmiast przerwali przyjmowanie leku LEVAQUIN® i skontaktowali się z lekarzem.
- Zapalenie ścięgna i zerwanie ścięgna: Poinstruuj pacjentów, aby skontaktowali się z lekarzem, jeśli odczuwają ból, obrzęk lub zapalenie ścięgna, osłabienie lub niemożność korzystania z jednego ze stawów; odpocznij i powstrzymaj się od ćwiczeń; i przerwać leczenie LEVAQUIN®. Objawy mogą być nieodwracalne. Ryzyko wystąpienia ciężkich zaburzeń ścięgien podczas stosowania fluorochinolonów jest wyższe u starszych pacjentów, zwykle powyżej 60. roku życia, u pacjentów przyjmujących kortykosteroidy oraz u pacjentów po przeszczepieniu nerki, serca lub płuc.
- Neuropatie obwodowe : Należy poinformować pacjentów, że neuropatie obwodowe są związane ze stosowaniem lewofloksacyny, objawy mogą wystąpić wkrótce po rozpoczęciu leczenia i mogą być nieodwracalne. Jeśli wystąpią objawy neuropatii obwodowej, w tym ból, pieczenie, mrowienie, drętwienie i/lub osłabienie, należy natychmiast odstawić LEVAQUIN® i powiedzieć, aby skontaktował się z lekarzem.
- Skutki dla centralnego układu nerwowego (na przykład drgawki, zawroty głowy, oszołomienie, zwiększone ciśnienie śródczaszkowe): Należy poinformować pacjentów, że drgawki zgłaszano u pacjentów otrzymujących fluorochinolony, w tym lewofloksacynę. Poinstruuj pacjentów, aby powiadomili swojego lekarza przed zażyciem tego leku, jeśli mają historię drgawek. Poinformuj pacjentów, że powinni wiedzieć, jak reagują na LEVAQUIN®, zanim zaczną obsługiwać samochód lub maszyny lub wykonywać inne czynności wymagające uwagi i koordynacji umysłowej. Poinstruuj pacjentów, aby powiadomili swojego lekarza, jeśli wystąpi uporczywy ból głowy z niewyraźnym widzeniem lub bez niego.
- Zaostrzenie miastenii Gravis : Poinstruuj pacjentów, aby informowali swojego lekarza o historii miastenii. Poinstruuj pacjentów, aby powiadomili swojego lekarza, jeśli wystąpią jakiekolwiek objawy osłabienia mięśni, w tym trudności z oddychaniem.
- Reakcje nadwrażliwości : Należy poinformować pacjentów, że lewofloksacyna może powodować reakcje nadwrażliwości, nawet po podaniu pojedynczej dawki, oraz o zaprzestaniu stosowania leku przy pierwszych objawach wysypki skórnej, pokrzywki lub innych reakcji skórnych, przyspieszonego bicia serca, trudności w połykaniu lub oddychaniu, jakiegokolwiek obrzęku sugerującego obrzęk naczynioruchowy ( na przykład obrzęk warg, języka, twarzy, ucisk w gardle, chrypka) lub inne objawy reakcji alergicznej.
- Hepatotoksyczność: Należy poinformować pacjentów, że u pacjentów przyjmujących LEVAQUIN® zgłaszano ciężką hepatotoksyczność (w tym ostre zapalenie wątroby i zdarzenia śmiertelne). Poinstruuj pacjentów, aby poinformowali swojego lekarza, jeśli wystąpią jakiekolwiek oznaki lub objawy uszkodzenia wątroby, w tym: utrata apetytu, nudności, wymioty, gorączka, osłabienie, zmęczenie, tkliwość w prawym górnym kwadrancie, swędzenie, zażółcenie skóry i oczu, jasne wypróżnienia lub ciemny kolor moczu.
- Biegunka: Biegunka jest częstym problemem powodowanym przez antybiotyki, który zwykle kończy się wraz z odstawieniem antybiotyku. Czasami po rozpoczęciu leczenia antybiotykami u pacjentów mogą pojawić się wodniste i krwawe stolce (ze skurczami żołądka i gorączką lub bez), nawet po dwóch lub więcej miesiącach od przyjęcia ostatniej dawki antybiotyku. W takim przypadku należy poinstruować pacjentów, aby jak najszybciej skontaktowali się z lekarzem.
- Wydłużenie odstępu QT: Poinstruuj pacjentów, aby informowali swojego lekarza o wszelkich osobistych lub rodzinnych wywiadach dotyczących wydłużenia odstępu QT lub stanów proarytmicznych, takich jak hipokaliemia, bradykardia lub niedawne niedokrwienie mięśnia sercowego; jeśli przyjmują jakiekolwiek leki przeciwarytmiczne klasy IA (chinidyna, prokainamid) lub klasy III (amiodaron, sotalol). Poinstruuj pacjentów, aby powiadomili swojego lekarza, jeśli wystąpią jakiekolwiek objawy wydłużenia odstępu QT, w tym przedłużone kołatanie serca lub utrata przytomności.
- Zaburzenia mięśniowo-szkieletowe u pacjentów pediatrycznych: Poinstruuj rodziców, aby przed zażyciem tego leku poinformowali lekarza dziecka, jeśli dziecko ma problemy ze stawami w wywiadzie. Poinformuj rodziców pacjentów pediatrycznych, aby powiadomili lekarza dziecka o wszelkich problemach związanych ze stawami, które wystąpią podczas lub po leczeniu lewofloksacyną [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
- Światłoczułość/Fototoksyczność: Należy poinformować pacjentów, że u pacjentów otrzymujących fluorochinolony zgłaszano nadwrażliwość/fototoksyczność. Poinformuj pacjentów, aby podczas przyjmowania fluorochinolonów zminimalizowali lub unikali ekspozycji na naturalne lub sztuczne światło słoneczne (łóżka opalające lub leczenie UVA/B). Jeśli pacjenci muszą przebywać na zewnątrz podczas stosowania fluorochinolonów, poinstruuj ich, aby nosili luźne ubrania, które chronią skórę przed ekspozycją na słońce, i przedyskutuj z lekarzem inne środki ochrony przeciwsłonecznej. Jeśli wystąpi reakcja podobna do oparzenia słonecznego lub wykwity skórne, poinstruuj pacjentów, aby skontaktowali się z lekarzem.
Odporność antybakteryjna
Leki przeciwbakteryjne, w tym LEVAQUIN®, powinny być stosowane wyłącznie w leczeniu zakażeń bakteryjnych. Nie leczą infekcji wirusowych (np. przeziębienia). Kiedy LEVAQUIN® jest przepisywany w celu leczenia infekcji bakteryjnej, pacjentom należy poinformować, że chociaż często zdarza się, że poczują się lepiej na początku leczenia, lek należy przyjmować dokładnie zgodnie z zaleceniami. Pomijanie dawek lub nieukończenie pełnego cyklu terapii może (1) zmniejszyć skuteczność natychmiastowego leczenia i (2) zwiększyć prawdopodobieństwo, że bakterie rozwiną oporność i nie będą mogły być wyleczone za pomocą LEVAQUIN® lub innych leków przeciwbakteryjnych w przyszłości.
Podawanie z żywnością, płynami i towarzyszącymi lekami
Pacjentów należy poinformować, że LEVAQUIN® Tabletki można przyjmować z posiłkiem lub bez posiłku. Tabletki należy przyjmować codziennie o tej samej porze.
Pacjenci powinni pić dużo płynów podczas przyjmowania leku LEVAQUIN®, aby uniknąć tworzenia się silnie stężonego moczu i tworzenia się kryształów w moczu.
Leki zobojętniające sok żołądkowy zawierające magnez lub glin, a także sukralfat, kationy metali takich jak żelazo oraz preparaty multiwitaminowe z cynkiem lub didanozyną należy przyjmować co najmniej dwie godziny przed lub dwie godziny po podaniu doustnym LEVAQUIN®.
Interakcje leków z insuliną, doustnymi środkami hipoglikemicznymi i warfaryną
Pacjentów należy poinformować, że jeśli mają cukrzycę i są leczeni insuliną lub doustnym lekiem hipoglikemizującym i wystąpi reakcja hipoglikemiczna, powinni odstawić LEVAQUIN® i skonsultować się z lekarzem.
Należy poinformować pacjentów, że jednoczesne podawanie warfaryny i LEVAQUIN® wiąże się ze wzrostem międzynarodowego współczynnika znormalizowanego (INR) lub czasu protrombinowego i klinicznymi epizodami krwawienia. Pacjenci powinni powiadomić swojego lekarza, jeśli przyjmują warfarynę, być monitorowani pod kątem oznak krwawienia, a także mieć ściśle monitorowane testy przeciwzakrzepowe podczas jednoczesnego przyjmowania warfaryny.
Badania nad dżumą i wąglikiem
Pacjentów otrzymujących LEVAQUIN® w tych schorzeniach należy poinformować, że badania skuteczności nie mogą być prowadzone na ludziach ze względów etycznych i wykonalności. Dlatego zatwierdzenie tych stanów oparto na badaniach skuteczności przeprowadzonych na zwierzętach.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
biologicznym okresie życia szczurów lewofloksacyna nie wykazywała potencjału rakotwórczego po codziennym podawaniu z dietą przez 2 lata; najwyższa dawka (100 mg/kg/dobę) była 1,4 razy większa od najwyższej zalecanej dawki u ludzi (750 mg) na podstawie względnej powierzchni ciała. Lewofloksacyna nie skróciła czasu do rozwoju guzów skóry wywołanych promieniowaniem UV u bezwłosych myszy albinosów (Skh-1) przy żadnym poziomie dawki lewofloksacyny, a zatem nie była fotorakotwórcza w warunkach tego badania. Stężenia skórne lewofloksacyny u bezwłosych myszy wahały się od 25 do 42 mcg/g przy najwyższym poziomie dawki lewofloksacyny (300 mg/kg/dobę) stosowanym w badaniu fotorakotwórczości. Dla porównania, skórne stężenie lewofloksacyny u ludzi otrzymujących 750 mg LEVAQUIN® wynosiło średnio około 11,8 mcg/g przy Cmax.
Lewofloksacyna nie wykazywała działania mutagennego w następujących testach: test mutacji bakteryjnych Amesa (S. typhimurium i E. coli), test postępującej mutacji CHO/HGPRT, test mikrojądrowy u myszy, test letalnej dominacji myszy, test nieplanowej syntezy DNA u szczura oraz chromatyda siostrzana u myszy test wymiany. Wyniki były pozytywne w testach aberracji chromosomowych in vitro (linia komórkowa CHL) i wymiany chromatyd siostrzanych (linia komórkowa CHL/IU).
Lewofloksacyna nie powodowała upośledzenia płodności ani zdolności rozrodczych szczurów w dawkach doustnych do 360 mg/kg/dobę, co odpowiada 4,2-krotności najwyższej zalecanej dawki u ludzi na podstawie względnej powierzchni ciała i dawek dożylnych do 100 mg/kg/dobę. dzień, co odpowiada 1,2-krotności najwyższej zalecanej dawki u ludzi w oparciu o względną powierzchnię ciała.
Używaj w określonych populacjach
Ciąża
Ciąża Kategoria C
Lewofloksacyna nie wykazywała działania teratogennego u szczurów w dawkach tak wysokich jak 810 mg/kg/dobę, co odpowiada 9,4-krotności najwyższej zalecanej dawki doustnej stosowanej u ludzi w oparciu o względną powierzchnię ciała. Doustna dawka 810 mg/kg/dobę szczurom powodowała zmniejszenie masy ciała płodów i zwiększoną śmiertelność płodów. Nie zaobserwowano działania teratogennego, gdy królikom podawano doustnie tak wysokie dawki jak 50 mg/kg/dobę, co odpowiada 1,1-krotności najwyższej zalecanej dawki doustnej u ludzi w oparciu o względną powierzchnię ciała.
Nie ma jednak odpowiednich i dobrze kontrolowanych badań u kobiet w ciąży. LEVAQUIN® powinien być stosowany w czasie ciąży tylko wtedy, gdy potencjalna korzyść przewyższa potencjalne ryzyko dla płodu.
Matki karmiące
Na podstawie danych dotyczących innych fluorochinolonów i bardzo ograniczonych danych dotyczących LEVAQUIN® można przypuszczać, że lewofloksacyna przenika do mleka ludzkiego. Ze względu na możliwość wystąpienia poważnych działań niepożądanych LEVAQUIN® u niemowląt karmionych piersią, należy podjąć decyzję, czy przerwać karmienie piersią, czy przerwać stosowanie leku, biorąc pod uwagę znaczenie leku dla matki.
Zastosowanie pediatryczne
Chinolony, w tym lewofloksacyna, powodują artropatię i osteochondrozę u młodych zwierząt kilku gatunków. [Widzieć OSTRZEŻENIA I ŚRODKI oraz Farmakologia zwierząt ].
Wąglik wziewny (po ekspozycji)
Lewofloksacyna jest wskazana u dzieci w wieku 6 miesięcy i starszych w wągliku wziewnym (po ekspozycji). Ocena korzyści i ryzyka wskazuje, że podawanie lewofloksacyny pacjentom pediatrycznym jest właściwe. Nie badano bezpieczeństwa stosowania lewofloksacyny u dzieci i młodzieży leczonych przez ponad 14 dni [patrz WSKAZANIA , DAWKOWANIE I SPOSÓB PODAWANIA oraz Studia kliniczne ].
Plaga
Lewofloksacyna jest wskazana u dzieci w wieku 6 miesięcy i starszych w leczeniu dżumy, w tym dżumy płucnej i posocznicy wywołanej przez Yersinia pestis (Y. pestis) oraz w profilaktyce dżumy. Badania skuteczności LEVAQUIN® nie mogły być prowadzone u ludzi z dżumą płucną ze względów etycznych i wykonalności. Dlatego zatwierdzenie tego wskazania oparto na badaniu skuteczności przeprowadzonym na zwierzętach. Ocena korzyści i ryzyka wskazuje, że podawanie lewofloksacyny pacjentom pediatrycznym jest właściwe [patrz WSKAZANIA , DAWKOWANIE I SPOSÓB PODAWANIA oraz Studia kliniczne ].
Bezpieczeństwo i skuteczność LEVAQUIN® u dzieci w wieku poniżej sześciu miesięcy nie zostały ustalone.
Farmakokinetyka po podaniu dożylnym
Farmakokinetykę lewofloksacyny po podaniu pojedynczej dawki dożylnej badano u dzieci w wieku od sześciu miesięcy do 16 lat. Dzieci i młodzież usuwały lewofloksacynę szybciej niż dorośli, co powodowało mniejsze narażenie na osocze niż dorośli dla danej dawki mg/kg [patrz FARMAKOLOGIA KLINICZNA oraz Studia kliniczne ].
Dawkowanie u pacjentów pediatrycznych z wąglikiem lub dżumą wziewną
Zalecane dawkowanie tabletek LEVAQUIN® u pacjentów pediatrycznych z wąglikiem lub dżumą wziewną, patrz DAWKOWANIE I SPOSÓB PODAWANIA . LEVAQUIN® Tabletki nie mogą być podawane pacjentom pediatrycznym o masie ciała poniżej 30 kg ze względu na ograniczenia dostępnych mocy. W przypadku dzieci o masie ciała poniżej 30 kg można rozważyć alternatywne postacie lewofloksacyny.
Działania niepożądane
badaniach klinicznych 1534 pacjentów pediatrycznych (w wieku od 6 miesięcy do 16 lat) leczono lekiem LEVAQUIN® doustnie i dożylnie. Pacjenci pediatryczni w wieku od 6 miesięcy do 5 lat otrzymywali LEVAQUIN® 10 mg/kg dwa razy na dobę, a pacjenci w wieku powyżej 5 lat otrzymywali 10 mg/kg raz na dobę (maksymalnie 500 mg na dobę) przez około 10 dni. LEVAQUIN® Tabletki można podawać wyłącznie pacjentom pediatrycznym z wąglikiem wziewnym (po ekspozycji) lub dżumie, którzy ważą 30 kg lub więcej ze względu na ograniczenia dostępnych mocy [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Podgrupa pacjentów pediatrycznych w badaniach klinicznych (1340 leczonych LEVAQUIN® i 893 nieleczonych fluorochinolonem) włączonych do prospektywnego, długoterminowego badania obserwacyjnego w celu oceny częstości występowania zaburzeń mięśniowo-szkieletowych zdefiniowanych w protokole (bóle stawów, zapalenie stawów, ścięgna, zaburzenia chodu ) w ciągu 60 dni i 1 roku po pierwszej dawce badanego leku. Pacjenci pediatryczni leczeni lekiem LEVAQUIN® mieli znacznie większą częstość występowania zaburzeń mięśniowo-szkieletowych w porównaniu z dziećmi nieleczonymi fluorochinolonami, jak przedstawiono w Tabeli 7. LEVAQUIN® Tabletki można podawać tylko dzieciom z wąglikiem wziewnym (po ekspozycji) lub dżumie którzy mają 30 kg lub więcej ze względu na ograniczenia dostępnych sił [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Ból stawów był najczęściej występującym schorzeniem układu mięśniowo-szkieletowego w obu leczonych grupach. Większość schorzeń układu mięśniowo-szkieletowego w obu grupach dotyczyła wielu obciążonych stawów. Zaburzenia były umiarkowane u 8/46 (17%) dzieci i łagodne u 35/46 (76%) pacjentów pediatrycznych leczonych LEVAQUIN®, a większość z nich była leczona lekami przeciwbólowymi. Mediana czasu do ustąpienia wyniosła 7 dni dla dzieci leczonych LEVAQUIN® i 9 dla dzieci nieleczonych fluorochinolonem (około 80% ustąpiło w ciągu 2 miesięcy w obu grupach). Żaden z pacjentów pediatrycznych nie miał ciężkiego lub poważnego schorzenia, a wszystkie schorzenia układu mięśniowo-szkieletowego ustąpiły bez następstw.
Najczęściej zgłaszanymi działaniami niepożądanymi były wymioty i biegunka, które występowały z podobną częstością u dzieci i młodzieży leczonych LEVAQUIN® i nieleczonych fluorochinolonami.
Poza działaniami niepożądanymi zgłaszanymi u dzieci w badaniach klinicznych, działania niepożądane zgłaszane u dorosłych podczas badań klinicznych lub po wprowadzeniu do obrotu [patrz DZIAŁANIA NIEPOŻĄDANE ] może również wystąpić u pacjentów pediatrycznych.
Zastosowanie geriatryczne
Pacjenci geriatryczni są narażeni na zwiększone ryzyko rozwoju ciężkich zaburzeń ścięgien, w tym zerwania ścięgna, gdy są leczeni fluorochinolonami, takimi jak LEVAQUIN®. Ryzyko to jest dodatkowo zwiększone u pacjentów otrzymujących jednocześnie leczenie kortykosteroidami. Zapalenie ścięgna lub zerwanie ścięgna może obejmować Achillesa, rękę, ramię lub inne miejsca ścięgna i może wystąpić podczas lub po zakończeniu terapii; zgłaszano przypadki występujące do kilku miesięcy po leczeniu fluorochinolonem. Należy zachować ostrożność przepisując LEVAQUIN® pacjentom w podeszłym wieku, zwłaszcza tym, którzy przyjmują kortykosteroidy. Pacjentów należy poinformować o tym potencjalnym działaniu niepożądanym i zalecić im przerwanie leczenia LEVAQUIN® i skontaktowanie się z lekarzem w przypadku wystąpienia jakichkolwiek objawów zapalenia ścięgna lub zerwania ścięgna [patrz PUDEŁKO OSTRZEŻENIE ; OSTRZEŻENIA I ŚRODKI ; oraz DZIAŁANIA NIEPOŻĄDANE ].
badaniach klinicznych III fazy 1945 pacjentów leczonych LEVAQUIN® (26%) było w wieku ≥ 65 lat. Spośród nich 1081 pacjentów (14%) było w wieku od 65 do 74 lat, a 864 pacjentów (12%) miało 75 lat lub więcej. Nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między tymi osobami a młodszymi osobami, ale nie można wykluczyć większej wrażliwości niektórych osób starszych.
Po wprowadzeniu produktu leczniczego LEVAQUIN® do obrotu zgłaszano ciężkie, czasami śmiertelne przypadki hepatotoksyczności. Większość zgłoszeń śmiertelnych przypadków hepatotoksyczności wystąpiła u pacjentów w wieku 65 lat lub starszych i większość nie była związana z nadwrażliwością. LEVAQUIN® należy natychmiast odstawić, jeśli u pacjenta wystąpią oznaki i objawy zapalenia wątroby [patrz OSTRZEŻENIA I ŚRODKI ].
Pacjenci w podeszłym wieku mogą być bardziej podatni na wpływ leku na odstęp QT. Dlatego należy zachować ostrożność stosując LEVAQUIN® jednocześnie z lekami, które mogą powodować wydłużenie odstępu QT (np. leki przeciwarytmiczne klasy IA lub klasy III) lub u pacjentów z czynnikami ryzyka torsade de pointes (np. znane wydłużenie odstępu QT, nieskorygowane hipokaliemia) [patrz OSTRZEŻENIA I ŚRODKI ].
Właściwości farmakokinetyczne lewofloksacyny u młodszych i starszych osób dorosłych nie różnią się istotnie, biorąc pod uwagę klirens kreatyniny. Ponieważ jednak wiadomo, że lek jest w znacznym stopniu wydalany przez nerki, ryzyko wystąpienia reakcji toksycznych na ten lek może być większe u pacjentów z zaburzeniami czynności nerek. Ponieważ u pacjentów w podeszłym wieku istnieje większe prawdopodobieństwo upośledzenia czynności nerek, należy zachować ostrożność przy doborze dawki i może być przydatne monitorowanie czynności nerek [patrz FARMAKOLOGIA KLINICZNA ].
Zaburzenia czynności nerek
pacjentów z zaburzeniami czynności nerek (klirens kreatyniny DAWKOWANIE I SPOSÓB PODAWANIA ].
Niewydolność wątroby
Nie przeprowadzono badań farmakokinetycznych u pacjentów z zaburzeniami czynności wątroby. Ze względu na ograniczony zakres metabolizmu lewofloksacyny nie przewiduje się, aby zaburzenia czynności wątroby miały wpływ na farmakokinetykę lewofloksacyny.
PRZEDAWKOWAĆ
W przypadku ostrego przedawkowania należy opróżnić żołądek. Pacjenta należy obserwować i utrzymywać odpowiednie nawodnienie. Lewofloksacyna nie jest skutecznie usuwana przez hemodializę lub dializę otrzewnową.
LEVAQUIN® wykazuje niski potencjał ostrej toksyczności. Myszy, szczury, psy i małpy wykazywały następujące objawy kliniczne po otrzymaniu pojedynczej dużej dawki LEVAQUIN®: ataksja, opadanie powiek, zmniejszona aktywność ruchowa, duszność, osłabienie, drżenie i drgawki. Dawki przekraczające 1500 mg/kg doustnie i 250 mg/kg IV powodowały znaczną śmiertelność gryzoni.
PRZECIWWSKAZANIA
LEVAQUIN® jest przeciwwskazany u osób ze stwierdzoną nadwrażliwością na lewofloksacynę lub inne chinolonowe leki przeciwbakteryjne [patrz OSTRZEŻENIA I ŚRODKI ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Lewofloksacyna należy do klasy środków przeciwbakteryjnych fluorochinolonów [ patrz Mikrobiologia ].
Farmakokinetyka
Średnie ± SD parametry farmakokinetyczne lewofloksacyny określone w warunkach stanu pojedynczego i stacjonarnego po podaniu tabletek doustnych podsumowano w Tabeli 8.
Farmakokinetyka lewofloksacyny jest liniowa i przewidywalna po pojedynczym i wielokrotnym podaniu doustnym lub dożylnym. Stan stacjonarny osiągany jest w ciągu 48 godzin po podaniu dawki 500 mg lub 750 mg raz na dobę. Średnie ± SD maksymalne i minimalne stężenia w osoczu osiągane po wielokrotnym doustnym schemacie dawkowania raz na dobę wynosiły około 5,7 ± 1,4 i 0,5 ± 0,2 µg/ml po dawkach 500 mg oraz 8,6 ± 1,9 i 1,1 ± 0,4 µg/ml po 750 mg. odpowiednio w dawkach mg. Średnie ± SD maksymalne i minimalne stężenia w osoczu uzyskane po wielu schematach dożylnych raz na dobę wynosiły około 6,4 ± 0,8 i 0,6 ± 0,2 μg/ml po dawkach 500 mg oraz 12,1 ± 4,1 i 1,3 ± 0,71 μg/ml po dawce 750 mg dawki.
Wchłanianie
Lewofloksacyna jest szybko i zasadniczo całkowicie wchłaniana po podaniu doustnym. Maksymalne stężenie w osoczu jest zwykle osiągane po jednej do dwóch godzin po podaniu doustnym. Całkowita biodostępność lewofloksacyny z tabletki 500 mg i tabletki 750 mg LEVAQUIN® wynosi około 99%, co wskazuje na całkowite wchłanianie lewofloksacyny po podaniu doustnym. Po podaniu pojedynczej dawki dożylnej LEVAQUIN® zdrowym ochotnikom, średnie maksymalne stężenie ± SD osiągnięte w osoczu wyniosło 6,2 ± 1,0 µg/ml po dawce 500 mg we wlewie przez 60 minut i 11,5 ± 4,0 µg/ml po podaniu dawki 750 mg przez 90 minut. Doustne podanie dawki 500 mg LEVAQUIN® z jedzeniem wydłuża czas do osiągnięcia maksymalnego stężenia o około 1 godzinę i zmniejsza maksymalne stężenie o około 14% po tabletce i około 25% po podaniu roztworu doustnego. Dlatego LEVAQUIN® Tabletki można podawać niezależnie od posiłków.
Profil stężenia lewofloksacyny w osoczu po podaniu dożylnym jest podobny i porównywalny pod względem stopnia ekspozycji (AUC) do obserwowanego dla tabletek LEVAQUIN®, gdy podaje się równe dawki (mg/mg). W związku z tym doustną i dożylną drogę podawania można uznać za wymienne.
Dystrybucja
Średnia objętość dystrybucji lewofloksacyny na ogół waha się od 74 do 112 l po pojedynczej i wielokrotnej dawce 500 mg lub 750 mg, co wskazuje na rozległą dystrybucję w tkankach organizmu. Szczytowe stężenie lewofloksacyny w tkankach skóry i płynie pęcherzykowym zdrowych osób osiąga około 3 godziny po podaniu. Stosunek biopsji tkanki skóry do AUC osocza wynosi w przybliżeniu 2, a stosunek AUC płynu z pęcherzy do osocza wynosi w przybliżeniu 1 po wielokrotnym podawaniu doustnym raz na dobę dawek odpowiednio 750 mg i 500 mg leku LEVAQUIN® zdrowym osobom. Lewofloksacyna również dobrze przenika do tkanek płucnych. Stężenia w tkance płucnej były zazwyczaj od 2 do 5 razy wyższe niż stężenia w osoczu i wahały się od około 2,4 do 11,3 µg/g w ciągu 24 godzin po podaniu pojedynczej dawki doustnej 500 mg.
In vitro, w klinicznie istotnym zakresie (1 do 10 µg/ml) stężeń lewofloksacyny w surowicy/osoczu, lewofloksacyna wiąże się w około 24 do 38% z białkami surowicy u wszystkich badanych gatunków, co określono metodą dializy równowagowej. U ludzi lewofloksacyna wiąże się głównie z albuminą surowicy. Wiązanie lewofloksacyny z białkami surowicy jest niezależne od stężenia leku.
Eliminacja
Metabolizm
Lewofloksacyna jest stabilna stereochemicznie w osoczu i moczu i nie ulega przemianie metabolicznej do swojego enancjomeru, D-ofloksacyny. U ludzi lewofloksacyna podlega ograniczonemu metabolizmowi i jest wydalana głównie w postaci niezmienionej z moczem. Po podaniu doustnym około 87% podanej dawki zostało wydalone w postaci niezmienionej w moczu w ciągu 48 godzin, podczas gdy mniej niż 4% dawki zostało wydalone w kale w ciągu 72 godzin. Mniej niż 5% podanej dawki zostało wydalone z moczem jako metabolity demetylowe i N-tlenkowe, jedyne metabolity zidentyfikowane u ludzi. Te metabolity mają niewielką istotną aktywność farmakologiczną.
Wydalanie
Lewofloksacyna jest wydalana z moczem głównie w postaci niezmienionej. Średni okres półtrwania lewofloksacyny w końcowej fazie eliminacji z osocza wynosi od około 6 do 8 godzin po podaniu doustnym lub dożylnym pojedynczej lub wielokrotnej dawki lewofloksacyny. Średni pozorny klirens całkowity i nerkowy wahają się odpowiednio od około 144 do 226 ml/min i 96 do 142 ml/min. Klirens nerkowy przekraczający szybkość filtracji kłębuszkowej sugeruje, że oprócz filtracji kłębuszkowej występuje kanalikowe wydzielanie lewofloksacyny. Jednoczesne podawanie cymetydyny lub probenecydu powoduje odpowiednio około 24% i 35% zmniejszenie klirensu nerkowego lewofloksacyny, co wskazuje, że lewofloksacyna jest wydzielana w kanaliku proksymalnym nerki. Nie znaleziono kryształów lewofloksacyny w żadnej z próbek moczu świeżo pobranych od pacjentów otrzymujących LEVAQUIN®.
Określone populacje
Pacjenci geriatryczni
Nie ma znaczących różnic w farmakokinetyce lewofloksacyny między osobami młodymi i starszymi, gdy badani brane są pod uwagę różnice w klirensie kreatyniny. Po podaniu doustnym 500 mg leku LEVAQUIN® zdrowym osobom w podeszłym wieku (66-80 lat) średni okres półtrwania lewofloksacyny w końcowej fazie eliminacji z osocza wynosił około 7,6 godzin, w porównaniu z około 6 godzinami u młodszych dorosłych. Różnicę tę można przypisać zmienności stanu czynności nerek badanych i nie uważano, że ma ona znaczenie kliniczne. Wydaje się, że wiek nie ma wpływu na wchłanianie leku. Nie jest konieczne dostosowanie dawki leku LEVAQUIN® na podstawie samego wieku [patrz Używaj w określonych populacjach ].
Pacjenci pediatryczni
Farmakokinetykę lewofloksacyny po podaniu pojedynczej dawki dożylnej 7 mg/kg badano u dzieci w wieku od 6 miesięcy do 16 lat. Pacjenci pediatryczni wydalali lewofloksacynę szybciej niż dorośli, co skutkowało mniejszą ekspozycją w osoczu niż dorośli dla danej dawki mg/kg. Kolejne analizy farmakokinetyczne przewidywały, że schemat dawkowania 8 mg/kg co 12 godzin (nie przekraczać 250 mg na dawkę) u dzieci w wieku od 6 miesięcy do 17 lat zapewniłby porównywalne ekspozycje w osoczu w stanie stacjonarnym (AUC0-24 i Cmax) do te obserwowane u dorosłych pacjentów, którym podawano 500 mg lewofloksacyny raz na 24 godziny. LEVAQUIN® Tabletki można podawać wyłącznie pacjentom pediatrycznym z wąglikiem wziewnym (po ekspozycji) lub dżumie, którzy ważą 30 kg lub więcej ze względu na ograniczenia dostępnych mocy [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Tematy płci męskiej i żeńskiej
Nie ma znaczących różnic w farmakokinetyce lewofloksacyny między osobnikami płci męskiej i żeńskiej, gdy badani brane są pod uwagę różnice w klirensie kreatyniny. Po podaniu doustnej dawki 500 mg LEVAQUIN® zdrowym mężczyznom średni okres półtrwania lewofloksacyny w końcowej fazie eliminacji z osocza wynosił około 7,5 godziny, w porównaniu z około 6,1 godziny u kobiet. Różnicę tę można przypisać zmienności stanu czynności nerek u mężczyzn i kobiet i nie uważano, aby była ona klinicznie istotna. Wydaje się, że na wchłanianie leku nie ma wpływu płeć badanych. Nie jest konieczne dostosowanie dawki wyłącznie ze względu na płeć.
Grupy rasowe lub etniczne
Wpływ rasy na farmakokinetykę lewofloksacyny zbadano za pomocą analizy współzmiennych przeprowadzonej na danych od 72 pacjentów: 48 rasy białej i 24 rasy innej niż biała. Rasa uczestników nie miała wpływu na pozorny całkowity klirens i pozorną objętość dystrybucji.
Pacjenci z niewydolnością nerek
dorosłych pacjentów z zaburzeniami czynności nerek (klirens kreatyniny DAWKOWANIE I SPOSÓB PODAWANIA oraz Używaj w określonych populacjach ].
Pacjenci z niewydolnością wątroby
Nie przeprowadzono badań farmakokinetycznych u pacjentów z zaburzeniami czynności wątroby. Ze względu na ograniczony zakres metabolizmu lewofloksacyny oczekuje się, że zaburzenia czynności wątroby nie będą miały wpływu na farmakokinetykę lewofloksacyny [patrz Używaj w określonych populacjach ].
Pacjenci z infekcją bakteryjną
Farmakokinetyka lewofloksacyny u pacjentów z ciężkimi pozaszpitalnymi zakażeniami bakteryjnymi jest porównywalna z obserwowanymi u zdrowych osób.
Badania interakcji leków
Oceniono możliwość interakcji farmakokinetycznych między LEVAQUIN® a lekami zobojętniającymi sok żołądkowy, warfaryną, teofiliną, cyklosporyną, digoksyną, probenecydem i cymetydyną [patrz INTERAKCJE Z LEKAMI ].
Mikrobiologia
Mechanizm akcji
Lewofloksacyna jest L-izomerem racematu, ofloksacyny, chinolonowego środka przeciwdrobnoustrojowego. Aktywność przeciwbakteryjna ofloksacyny polega głównie na izomerze L. Mechanizm działania lewofloksacyny i innych fluorochinolonowych środków przeciwdrobnoustrojowych obejmuje hamowanie bakteryjnej topoizomerazy IV i gyrazy DNA (obie to topoizomerazy typu II), enzymów niezbędnych do replikacji, transkrypcji, naprawy i rekombinacji DNA.
Opór
Oporność na fluorochinolony może powstać poprzez mutacje w określonych regionach gyrazy DNA lub topoizomerazy IV, zwanych regionami determinującymi odporność na chinolony (QRDR) lub poprzez zmieniony wypływ.
Fluorochinolony, w tym lewofloksacyna, różnią się budową chemiczną i sposobem działania od aminoglikozydów, makrolidów i antybiotyków β-laktamowych, w tym penicylin. Dlatego fluorochinolony mogą działać na bakterie oporne na te środki przeciwdrobnoustrojowe.
Oporność na lewofloksacynę spowodowana spontaniczną mutacją in vitro występuje rzadko (zakres: 10-9-10-10). Zaobserwowano oporność krzyżową między lewofloksacyną i niektórymi innymi fluorochinolonami, niektóre drobnoustroje oporne na inne fluorochinolony mogą być wrażliwe na lewofloksacynę.
Aktywność przeciwbakteryjna
Lewofloksacyna działa in vitro na bakterie Gram-ujemne i Gram-dodatnie.
Wykazano, że lewofloksacyna działa na większość izolatów następujących bakterii, zarówno in vitro, jak i w zakażeniach klinicznych, jak opisano w WSKAZANIA :
Bakterie tlenowe
Bakterie Gram-dodatnie
Enterococcus faecalisStaphylococcus aureus (izolaty wrażliwe na metycylinę)Staphylococcus epidermidis (izolaty wrażliwe na metycylinę)Staphylococcus saprophyticusStreptococcus pneumoniae (w tym izolaty wielolekooporne [MDRSP]1)Streptococcus pyogenes
Bakterie Gram-ujemne
Enterobacter cloacaeEscherichia coliHaemophilus influenzaeHaemophilus parainfluenzaeKlebsiella pneumoniaeLegionella pneumophilaMoraxella catarrhalisProteus mirabilisPseudomonas aeruginosaSerratia marcescens
Inne mikroorganizmy
Chlamydophila pneumoniaeMycoplasma pneumoniae
Dostępne są następujące dane in vitro, ale ich znaczenie kliniczne nie jest znane: Lewofloksacyna wykazuje in vitro minimalne stężenia hamujące (wartości MIC) wynoszące 2 µg/ml lub mniej w stosunku do większości (≥ 90%) izolatów następujących drobnoustrojów; jednakże bezpieczeństwo i skuteczność LEVAQUIN® w leczeniu infekcji klinicznych wywoływanych przez te bakterie nie zostały ustalone w odpowiednich i dobrze kontrolowanych badaniach klinicznych.
Izolaty MDRSP (Multi-drug resistance Streptococcus pneumoniae) są izolatami opornymi na dwa lub więcej z następujących antybiotyków: penicylinę (MIC ≥2 mcg/ml), cefalosporyny II generacji, np. cefuroksym; makrolidy, tetracykliny i trimetoprim/sulfametoksazol.
Bakterie tlenowe
Bakterie Gram-dodatnie
Staphylococcus haemolyticus Streptococcus beta-hemolizujący (grupa C/F) Streptococcus beta-hemolizujący (grupa G)Streptococcus agalactiaeStreptococcus milleriPaciorkowce z grupy ViridansBacillus anthracis
Bakterie Gram-ujemne
Acinetobacter baumanniiAcinetobacter lwoffiiBordetella pertussisCitrobacter koseriCitrobacter freundiiEnterobacter aerogenesEnterobacter sakazakiiKlebsiella oxytocaMorganella morganiiPantoea agglomeransProteus vulgarisProvidencia rettgeriProvidencia fluorescenis stuart
Bakterie beztlenowe
Bakterie Gram-dodatnie
Clostridium perfringens
Testy podatności
Aby uzyskać szczegółowe informacje dotyczące kryteriów interpretacyjnych testu wrażliwości i powiązanych metod badawczych oraz standardów kontroli jakości uznanych przez FDA dla tego leku, zobacz: https://www.fda.gov/STIC.
Toksykologia i/lub farmakologia zwierząt
Wykazano, że lewofloksacyna i inne chinolony powodują artropatię u niedojrzałych zwierząt większości badanych gatunków [patrz OSTRZEŻENIA I ŚRODKI ]. U niedojrzałych psów (4–5 miesięcy) doustne dawki lewofloksacyny 10 mg/kg/dobę przez 7 dni i dożylne 4 mg/kg/dobę przez 14 dni powodowały zmiany artropatyczne. Podawanie w dawkach doustnych 300 mg/kg/dobę przez 7 dni i dożylnych 60 mg/kg/dobę przez 4 tygodnie powodowało artropatię u młodych szczurów. Trzymiesięczne psy rasy beagle, którym podawano doustnie lewofloksacynę w dawce 40 mg/kg mc./dobę wykazywały klinicznie ciężką artrotoksyczność powodującą zakończenie dawkowania w 8. dniu 14-dniowego schematu dawkowania. Niewielkie efekty kliniczne dotyczące układu mięśniowo-szkieletowego, przy braku poważnych zmian patologicznych lub histopatologicznych, wynikały z najniższego poziomu dawki 2,5 mg/kg/dobę (około 0,2-krotność dawki pediatrycznej na podstawie porównania AUC). Zapalenie błony maziowej i uszkodzenia chrząstki stawowej obserwowano przy dawkach 10 i 40 mg/kg (odpowiednio około 0,7-krotność i 2,4-krotność dawki pediatrycznej, na podstawie porównania AUC). Ogólna patologia i histopatologia chrząstki stawowej utrzymywała się do końca 18-tygodniowego okresu rekonwalescencji u tych psów od poziomów dawek 10 i 40 mg/kg/dobę.
teście biologicznym na obrzęk uszu myszy, lewofloksacyna wykazywała fototoksyczność podobną do ofloksacyny, ale mniejszą fototoksyczność niż inne chinolony.
Podczas gdy w niektórych badaniach dożylnych na szczurach obserwowano krystalurię, kryształy moczu nie tworzą się w pęcherzu, są obecne tylko po oddaniu mikcji i nie są związane z nefrotoksycznością.
U myszy działanie stymulujące ośrodkowy układ nerwowy chinolonów jest wzmacniane przez jednoczesne podawanie niesteroidowych leków przeciwzapalnych.
U psów lewofloksacyna podawana w dawce 6 mg/kg lub wyższej w szybkim wstrzyknięciu dożylnym powodowała działanie hipotensyjne. Uważano, że te efekty są związane z uwalnianiem histaminy.
Badania in vitro i in vivo na zwierzętach wskazują, że lewofloksacyna nie jest ani induktorem, ani inhibitorem enzymów w zakresie stężeń terapeutycznych w ludzkim osoczu; dlatego nie przewiduje się interakcji związanych z enzymami metabolizującymi lek z innymi lekami lub środkami.
Studia kliniczne
Szpitalne zapalenie płuc
Dorośli pacjenci z klinicznie i radiologicznie udokumentowanym szpitalnym zapaleniem płuc zostali włączeni do wieloośrodkowego, randomizowanego, otwartego badania porównującego dożylny LEVAQUIN® (750 mg raz na dobę), a następnie doustny LEVAQUIN® (750 mg raz na dobę) przez łącznie 7–15 dni do imipenemu z cylastatyną dożylnie (500–1000 mg co 6–8 godzin na dobę), a następnie doustnie cyprofloksacyny (750 mg co 12 godzin na dobę) przez 7–15 dni. Pacjenci leczeni LEVAQUIN® otrzymywali średnio 7 dni terapii dożylnej (zakres: 1–16 dni); pacjenci leczeni lekiem porównawczym otrzymywali średnio 8 dni terapii dożylnej (zakres: 1–19 dni).
Ogólnie rzecz biorąc, w populacji ocenianej klinicznie i mikrobiologicznie leczenie wspomagające rozpoczęto empirycznie na początku badania u 56 z 93 (60,2%) pacjentów w ramieniu LEVAQUIN® i 53 z 94 (56,4%) pacjentów w ramieniu porównawczym. Średni czas trwania terapii wspomagającej wynosił 7 dni w ramieniu LEVAQUIN® i 7 dni w grupie porównawczej. U pacjentów ocenianych klinicznie i mikrobiologicznie z udokumentowanym zakażeniem Pseudomonas aeruginosa 15 z 17 (88,2%) otrzymało ceftazydym (N = 11) lub piperacylinę/tazobaktam (N = 4) w ramieniu LEVAQUIN®, a 16 z 17 (94,1%) otrzymało aminoglikozyd w ramieniu porównawczym. Ogólnie rzecz biorąc, u pacjentów ocenianych klinicznie i mikrobiologicznie, wankomycynę dodano do schematu leczenia 37 z 93 (39,8%) pacjentów w ramieniu LEVAQUIN® i 28 z 94 (29,8%) pacjentów w ramieniu porównawczym z podejrzeniem S oporności na metycylinę. infekcja złocista.
Wskaźniki sukcesu klinicznego u pacjentów ocenianych klinicznie i mikrobiologicznie podczas wizyty po terapii (pierwszorzędowy punkt końcowy badania oceniany w dniach 3–15 po zakończeniu terapii) wynosiły 58,1% dla LEVAQUIN® i 60,6% dla leku porównawczego. 95% CI dla różnicy wskaźników odpowiedzi (LEVAQUIN® minus komparator) wyniósł [-17,2, 12,0]. Wskaźniki eradykacji mikrobiologicznej podczas wizyty po terapii wynosiły 66,7% dla LEVAQUIN® i 60,6% dla produktu porównawczego. 95% CI dla różnicy wskaźników eradykacji (LEVAQUIN® minus komparator) wyniósł [-8,3; 20,3]. Skuteczność kliniczna i wskaźniki eradykacji mikrobiologicznej według patogenów są wyszczególnione w Tabeli 9.
Pozaszpitalne zapalenie płuc
7-14-dniowy schemat leczenia
Dorośli pacjenci hospitalizowani i ambulatoryjny z rozpoznaniem pozaszpitalnego bakteryjnego zapalenia płuc byli oceniani w 2 głównych badaniach klinicznych. W pierwszym badaniu 590 pacjentów zostało włączonych do prospektywnego, wieloośrodkowego, odślepionego, randomizowanego badania porównującego LEVAQUIN® 500 mg raz na dobę doustnie lub dożylnie przez 7 do 14 dni z ceftriaksonem 1 do 2 gramów dożylnie raz lub w równych dawkach podzielonych dwa razy na dobę następnie aksetyl cefuroksymu 500 mg doustnie dwa razy na dobę przez 7 do 14 dni. Pacjenci przydzieleni do leczenia w schemacie kontrolnym mogli otrzymywać erytromycynę (lub doksycyklinę w przypadku nietolerancji erytromycyny), jeśli podejrzewano lub udowodniono zakażenie wywołane atypowymi patogenami. Oceny kliniczne i mikrobiologiczne przeprowadzono podczas leczenia, 5 do 7 dni po terapii i 3 do 4 tygodni po terapii. Sukces kliniczny (wyleczenie plus poprawa) z LEVAQUIN® 5 do 7 dni po terapii, główna zmienna skuteczności w tym badaniu, był lepszy (95%) w porównaniu z grupą kontrolną (83%). 95% CI dla różnicy wskaźników odpowiedzi (LEVAQUIN® minus komparator) wyniósł [-6, 19]. Do drugiego badania włączono 264 pacjentów do prospektywnego, wieloośrodkowego, nieporównawczego badania z 500 mg LEVAQUIN® podawanym doustnie lub dożylnie raz dziennie przez 7 do 14 dni. Sukces kliniczny dla pacjentów ocenianych klinicznie wyniósł 93%. W obu badaniach wskaźnik sukcesu klinicznego u pacjentów z atypowym zapaleniem płuc wywołanym przez Chlamydophila pneumoniae, Mycoplasma pneumoniae i Legionella pneumophila wynosił odpowiednio 96%, 96% i 70%. Wskaźniki eradykacji mikrobiologicznej w obu badaniach przedstawiono w Tabeli 10.
Pozaszpitalne zapalenie płuc spowodowane wielolekoopornym Streptococcus Pneumoniae
LEVAQUIN® był skuteczny w leczeniu pozaszpitalnego zapalenia płuc wywołanego przez wielolekooporny Streptococcus pneumoniae (MDRSP). Izolaty MDRSP są izolatami opornymi na dwa lub więcej z następujących środków przeciwbakteryjnych: penicylinę (MIC ≥2 µg/ml), cefalosporyny II generacji (np. cefuroksym, makrolidy, tetracykliny i trimetoprym/sulfametoksazol). Spośród 40 pacjentów ocenianych mikrobiologicznie z izolatami MDRSP, 38 pacjentów (95,0%) osiągnęło kliniczny i bakteriologiczny sukces po leczeniu. Wskaźniki powodzenia klinicznego i bakteryjnego przedstawiono w tabeli 11.
Nie wszystkie izolaty były oporne na wszystkie testowane klasy antybiotyków. Wskaźniki powodzenia i eradykacji podsumowano w Tabeli 12.
Pozaszpitalne zapalenie płuc
5-dniowy schemat leczenia
celu oceny bezpieczeństwa i skuteczności większej dawki i krótszego leczenia LEVAQUIN ® , 528 ambulatoryjnych i hospitalizowanych dorosłych z klinicznie i radiologicznie potwierdzonym łagodnym lub ciężkim pozaszpitalnym zapaleniem płuc zostało poddanych ocenie w podwójnie zaślepionym, randomizowanym, prospektywnym, wieloośrodkowym badaniu porównującym LEVAQUIN ® 750 mg dożylnie lub doustnie codziennie przez pięć dni lub LEVAQUIN® 500 mg dożylnie lub doustnie codziennie przez 10 dni.
Wskaźniki sukcesu klinicznego (wyleczenie plus poprawa) w klinicznie ocenianej populacji wynosiły 90,9% w grupie LEVAQUIN® 750 mg i 91,1% w grupie LEVAQUIN® 500 mg. 95% CI dla różnicy wskaźników odpowiedzi (LEVAQUIN® 750 minus LEVAQUIN® 500) wynosił [-5,9, 5,4]. W klinicznie ocenianej populacji (31-38 dni po włączeniu) zapalenie płuc obserwowano u 7 ze 151 pacjentów w grupie LEVAQUIN® 750 mg i 2 ze 147 pacjentów w grupie LEVAQUIN® 500 mg. Biorąc pod uwagę obserwowane małe liczby, istotność tego odkrycia nie może być określona statystycznie. Skuteczność mikrobiologiczna 5-dniowego schematu została udokumentowana w przypadku zakażeń wymienionych w Tabeli 13.
Ostre bakteryjne zapalenie zatok
5-dniowe i 10-14-dniowe schematy leczenia
LEVAQUIN® jest zatwierdzony do leczenia ostrego bakteryjnego zapalenia zatok (ABS) przy użyciu 750 mg doustnie przez 5 dni lub 500 mg doustnie raz dziennie przez 10-14 dni. W celu oceny bezpieczeństwa i skuteczności wysokiej dawki krótkotrwałego leczenia LEVAQUIN®, 780 dorosłych pacjentów ambulatoryjnych z klinicznie i radiologicznie klinicznie stwierdzonym ostrym bakteryjnym zapaleniem zatok oceniano w podwójnie zaślepionym, randomizowanym, prospektywnym, wieloośrodkowym badaniu porównującym LEVAQUIN® 750 mg podawany doustnie raz na dobę przez pięć dni do LEVAQUIN® 500 mg doustnie raz na dobę przez 10 dni.
Wskaźniki powodzenia klinicznego (definiowane jako całkowite lub częściowe ustąpienie objawów podmiotowych i przedmiotowych ABS przed leczeniem do takiego stopnia, że dalsze leczenie antybiotykami uznano za konieczne) w populacji ocenianej mikrobiologicznie wyniosło 91,4% (139/152) w przypadku LEVAQUIN® Grupa 750 mg i 88,6% (132/149) w grupie LEVAQUIN® 500 mg na wizycie testu wyleczenia (TOC) (95% CI [-4,2, 10,0] dla LEVAQUIN® 750 mg minus LEVAQUIN® 500 mg) .
Wskaźniki powodzenia klinicznego według patogenu w populacji ocenianej mikrobiologicznie, u której próbki pobrane przez nakłucie antralne w momencie włączenia do badania wykazywały porównywalne wyniki dla schematów pięciodniowych i dziesięciodniowych podczas wizyty testowej 22 dni po leczeniu (patrz Tabela 14). .
Skomplikowane infekcje skóry i struktury skóry
Trzystu dziewięćdziesięciu dziewięciu pacjentów zostało włączonych do otwartego, randomizowanego, porównawczego badania dotyczącego powikłanych infekcji skóry i struktury skóry. Pacjenci zostali losowo przydzieleni do grupy otrzymującej albo LEVAQUIN® 750 mg raz na dobę (IV, a następnie doustnie) lub zatwierdzony lek porównawczy przez medianę 10 ± 4,7 dni. Zgodnie z oczekiwaniami w przypadku skomplikowanych infekcji skóry i struktury skóry, zabiegi chirurgiczne przeprowadzono w grupie LEVAQUIN® i porównawczej. Zabieg chirurgiczny (nacięcie i drenaż lub oczyszczenie rany) przeprowadzono u 45% pacjentów leczonych LEVAQUIN® i 44% pacjentów leczonych preparatem porównawczym, na krótko przed lub w trakcie leczenia antybiotykami i stanowił integralną część terapii w tym wskazaniu.
Wśród osób, które można było ocenić klinicznie 2–5 dni po zakończeniu przyjmowania badanego leku, ogólne wskaźniki powodzenia (poprawa lub wyleczenie) wyniosły 116/138 (84,1%) dla pacjentów leczonych LEVAQUIN® i 106/132 (80,3%) dla pacjentów leczonych z komparatorem.
Wskaźniki powodzenia różniły się w zależności od rodzaju diagnozy, od 68% u pacjentów z zakażonymi owrzodzeniami do 90% u pacjentów z zakażonymi ranami i ropniami. Wskaźniki te były równoważne z tymi obserwowanymi w przypadku leków porównawczych.
Przewlekłe bakteryjne zapalenie gruczołu krokowego
Dorośli pacjenci z klinicznym rozpoznaniem zapalenia gruczołu krokowego i wynikami posiewu mikrobiologicznego z próbki moczu pobranej po masażu gruczołu krokowego (VB3) lub próbek wydzielenia gruczołu krokowego (EPS) uzyskanych za pomocą procedury Mearesa-Stameya zostali włączeni do wieloośrodkowego, randomizowanego, podwójnie ślepego badania porównującego doustnie LEVAQUIN® 500 mg raz na dobę przez łącznie 28 dni do doustnej cyprofloksacyny 500 mg dwa razy na dobę przez łącznie 28 dni. Pierwszorzędowym punktem końcowym skuteczności była skuteczność mikrobiologiczna u pacjentów poddawanych ocenie mikrobiologicznej. Łącznie 136 i 125 pacjentów poddawanych ocenie mikrobiologicznej zostało włączonych odpowiednio do grup LEVAQUIN® i ciprofloksacyny. Wskaźnik eradykacji mikrobiologicznej przez zakażenie pacjenta w 5–18 dniach po zakończeniu leczenia wyniósł 75,0% w grupie LEVAQUIN® i 76,8% w grupie cyprofloksacyny (95% CI [-12,58, 8,98] dla LEVAQUIN® minus cyprofloksacyna). Ogólne wskaźniki eradykacji patogenów będących przedmiotem zainteresowania przedstawiono w Tabeli 15.
Wskaźniki eradykacji S. epidermidis wykryte z innymi współpatogenami są zgodne ze wskaźnikami obserwowanymi w czystych izolatach.
Wskaźniki sukcesu klinicznego (wyleczenie + poprawa bez konieczności dalszej antybiotykoterapii) w populacji ocenianej mikrobiologicznie 5–18 dni po zakończeniu leczenia wynosiły 75,0% dla pacjentów leczonych LEVAQUIN® i 72,8% dla pacjentów leczonych cyprofloksacyną (95% CI [- 8,87, 13,27] dla LEVAQUIN® bez cyprofloksacyny). Odsetek powodzenia klinicznego (24–45 dni po zakończeniu leczenia) wyniósł 66,7% dla pacjentów leczonych LEVAQUIN® i 76,9% dla pacjentów leczonych ciprofloksacyną (95% CI [-23,40; 2,89] dla LEVAQUIN® minus cyprofloksacyna).
Powikłane infekcje dróg moczowych i ostre odmiedniczkowe zapalenie nerek
5-dniowy schemat leczenia
Aby ocenić bezpieczeństwo i skuteczność większej dawki i krótszego leczenia LEVAQUIN® , 1109 pacjentów z cUTI i AP zostało włączonych do randomizowanego, podwójnie zaślepionego, wieloośrodkowego badania klinicznego przeprowadzonego w USA od listopada 2004 do kwietnia 2006 roku porównującego LEVAQUIN® 750 mg dożylnie lub doustnie raz na dobę przez 5 dni (546 pacjentów) z cyprofloksacyną 400 mg dożylnie lub 500 mg doustnie dwa razy na dobę przez 10 dni (563 pacjentów). Wykluczono pacjentów z AP powikłanym współistniejącymi chorobami nerek lub stanami, takimi jak całkowita niedrożność, operacja, przeszczep, współistniejąca infekcja lub wada wrodzona. Skuteczność mierzono przez eradykację bakteriologiczną wyjściowego drobnoustroju podczas wizyty po terapii u pacjentów z patogenem zidentyfikowanym na początku leczenia. Wizyta po terapii (test wyleczenia) miała miejsce 10 do 14 dni po ostatniej aktywnej dawce LEVAQUIN® i 5 do 9 dni po ostatniej dawce aktywnej cyprofloksacyny.
Ogólne wskaźniki wyleczeń bakteriologicznych dla LEVAQUIN® i kontroli podczas wizyty test-of-cure (TOC) dla grupy wszystkich pacjentów z udokumentowanym patogenem na początku badania (zmodyfikowany zamiar leczenia lub mITT) oraz grupy pacjentów w populacji mITT którzy ściśle przestrzegali protokołu (ocena mikrobiologiczna) podsumowano w Tabeli 16.
Wskaźniki eradykacji mikrobiologicznej w populacji ocenianej mikrobiologicznie w TOC dla poszczególnych patogenów odzyskanych od pacjentów randomizowanych do leczenia LEVAQUIN® przedstawiono w Tabeli 17.
Powikłane infekcje dróg moczowych i ostre odmiedniczkowe zapalenie nerek
10-dniowy schemat leczenia
celu oceny bezpieczeństwa i skuteczności dawki 250 mg, 10-dniowy schemat leczenia LEVAQUIN® , 567 pacjentów z niepowikłanym ZUM, łagodnym do umiarkowanego CUTI oraz łagodnym do umiarkowanego AP włączono do randomizowanego, podwójnie zaślepionego, wieloośrodkowego badanie kliniczne przeprowadzone w USA od czerwca 1993 do stycznia 1995 porównujące LEVAQUIN® 250 mg doustnie raz dziennie przez 10 dni (285 pacjentów) z cyprofloksacyną 500 mg doustnie dwa razy dziennie przez 10 dni (282 pacjentów). Pacjenci z opornym patogenem, nawracającym ZUM, kobiety w wieku powyżej 55 lat oraz z założonym na stałe cewnikiem byli początkowo wykluczeni, przed zmianą protokołu, która nastąpiła po 30% rekrutacji. Skuteczność mikrobiologiczną mierzono przez eradykację bakteriologiczną wyjściowego drobnoustroju(ów) 1–12 dni po leczeniu u pacjentów z patogenem zidentyfikowanym na początku leczenia.
Ogólne wskaźniki wyleczeń bakteriologicznych dla LEVAQUIN® i kontroli podczas wizyty test-of-cure (TOC) dla grupy wszystkich pacjentów z udokumentowanym patogenem na początku badania (zmodyfikowany zamiar leczenia lub mITT) oraz grupy pacjentów w populacji mITT którzy ściśle przestrzegali protokołu (ocena mikrobiologiczna) podsumowano w Tabeli 18.
Wąglik wziewny (po ekspozycji)
Skuteczność LEVAQUIN® w tym wskazaniu opiera się na stężeniach w osoczu osiąganych u ludzi, co jest zastępczym punktem końcowym, który może przewidywać korzyści kliniczne. LEVAQUIN® nie był testowany na ludziach pod kątem zapobiegania wąglikowi inhalacyjnemu po ekspozycji. Średnie stężenia LEVAQUIN® w osoczu związane ze statystycznie istotną poprawą przeżycia w porównaniu z placebo w modelu wąglika wziewnego małpy rezus są osiągane lub przekraczane u dorosłych i dzieci, otrzymujących zalecane doustne i dożylne schematy dawkowania [patrz WSKAZANIA oraz DAWKOWANIE I SPOSÓB PODAWANIA ].
Farmakokinetykę lewofloksacyny oceniano u pacjentów dorosłych i dzieci. Średnie (± SD) maksymalne stężenie w osoczu w stanie stacjonarnym u dorosłych ludzi otrzymujących 500 mg doustnie lub dożylnie raz na dobę wynosi odpowiednio 5,7 ± 1,4 i 6,4 ± 0,8 µg/ml; a odpowiadająca całkowita ekspozycja w osoczu (AUC ) wynosi odpowiednio 47,5 ± 6,7 i 54,6 ± 11,1 mcg.h/ml. Obliczono, że przewidywane parametry farmakokinetyczne w stanie stacjonarnym u dzieci w wieku od 6 miesięcy do 17 lat otrzymujących 8 mg/kg doustnie co 12 godzin (nie więcej niż 250 mg na dawkę) są porównywalne z obserwowanymi u dorosłych otrzymujących 500 mg doustnie raz dziennie [patrz FARMAKOLOGIA KLINICZNA ].
LEVAQUIN® Tabletki można podawać wyłącznie pacjentom pediatrycznym z wąglikiem wziewnym (po ekspozycji) lub dżumie, którzy ważą 30 kg lub więcej ze względu na ograniczenia dostępnych mocy [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
osób dorosłych bezpieczeństwo LEVAQUIN® podczas leczenia trwającego do 28 dni jest dobrze scharakteryzowane. Jednak informacje dotyczące przedłużonego stosowania w dawce 500 mg dziennie do 60 dni są ograniczone. Przedłużoną terapię LEVAQUIN® u dorosłych należy stosować tylko wtedy, gdy korzyści przewyższają ryzyko.
U dzieci i młodzieży nie badano bezpieczeństwa stosowania lewofloksacyny w leczeniu trwającym dłużej niż 14 dni. W badaniach klinicznych, w których leczenie trwało do 14 dni, obserwowano zwiększoną częstość występowania działań niepożądanych ze strony układu mięśniowo-szkieletowego (bóle stawów, zapalenie stawów, tendinopatia, zaburzenia chodu) w porównaniu z grupą kontrolną. Długoterminowe dane dotyczące bezpieczeństwa, w tym wpływu na chrząstkę, po podaniu lewofloksacyny pacjentom pediatrycznym są ograniczone [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
Przeprowadzono kontrolowane placebo badanie na małpach rezus narażonych na wziewną średnią dawkę 49 LD50 (~2,7 × 106) zarodników (zakres 17 – 118 LD50) B. anthracis (szczep Ames). Minimalne stężenie hamujące (MIC) lewofloksacyny dla szczepu wąglika zastosowanego w tym badaniu wynosiło 0,125 µg/ml. U badanych zwierząt średnie stężenia lewofloksacyny w osoczu osiągane przy spodziewanym Tmax (1 godzina po podaniu) do stanu stacjonarnego po podaniu doustnym wahały się od 2,79 do 4,87 µg/ml. Stężenia minimalne w stanie stacjonarnym 24 godziny po podaniu mieściły się w zakresie od 0,107 do 0,164 µg/ml. Średnia (SD) wartość AUC0-24 w stanie stacjonarnym wynosiła 33,4 ± 3,2 µg.h/ml (zakres od 30,4 do 36,0 µg.h/ml). Śmiertelność z powodu wąglika u zwierząt, które otrzymały 30-dniowy schemat doustnego podawania LEVAQUIN® począwszy od 24 godzin po ekspozycji, była znacznie niższa (1/10), w porównaniu z grupą placebo (9/10) [P = 0,0011, dwustronny Fisher 39; dokładny test]. Jedno zwierzę leczone lewofloksacyną, które zmarło z powodu wąglika, zrobiło to po 30-dniowym okresie podawania leku.
Plaga
Badania skuteczności LEVAQUIN® nie mogły być prowadzone u ludzi z dżumą płucną ze względów etycznych i wykonalności. Dlatego zatwierdzenie tego wskazania oparto na badaniu skuteczności przeprowadzonym na zwierzętach.
Średnie stężenia LEVAQUIN® w osoczu związane ze statystycznie istotną poprawą przeżycia w porównaniu z placebo w modelu dżumy płucnej u afrykańskich małp zielonych są osiągane lub przekraczane u dorosłych i dzieci, otrzymujących zalecane doustne i dożylne schematy dawkowania [patrz WSKAZANIA oraz DAWKOWANIE I SPOSÓB PODAWANIA ].
Farmakokinetykę lewofloksacyny oceniano u pacjentów dorosłych i dzieci. Średnie (± SD) maksymalne stężenie w osoczu w stanie stacjonarnym u dorosłych ludzi otrzymujących 500 mg doustnie lub dożylnie raz na dobę wynosi odpowiednio 5,7 ± 1,4 i 6,4 ± 0,8 µg/ml; a odpowiadająca całkowita ekspozycja w osoczu (AUC0-24) wynosi odpowiednio 47,5 ± 6,7 i 54,6 ± 11,1 µg.h/ml. Obliczono, że przewidywane parametry farmakokinetyczne w stanie stacjonarnym u dzieci w wieku od 6 miesięcy do 17 lat otrzymujących 8 mg/kg doustnie co 12 godzin (nie więcej niż 250 mg na dawkę) są porównywalne z obserwowanymi u dorosłych otrzymujących 500 mg doustnie raz dziennie [patrz FARMAKOLOGIA KLINICZNA ]. LEVAQUIN® Tabletki można podawać wyłącznie pacjentom pediatrycznym z wąglikiem wziewnym (po ekspozycji) lub dżumie, którzy ważą 30 kg lub więcej ze względu na ograniczenia dostępnych mocy [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Przeprowadzono kontrolowane placebo badanie na afrykańskich małpach zielonych narażonych na wziewną średnią dawkę 65 LD (zakres od 3 do 145 LD50) Yersinia pestis (szczep CO92). Minimalne stężenie hamujące (MIC) lewofloksacyny dla szczepu Y. pestis zastosowanego w tym badaniu wynosiło 0,03 µg/ml. Średnie stężenia lewofloksacyny w osoczu osiągane pod koniec pojedynczej 30-minutowej infuzji wahały się od 2,84 do 3,50 µg/ml u afrykańskich małp zielonych. Stężenia minimalne 24 godziny po podaniu mieściły się w zakresie od
INFORMACJA O PACJENCIE
LEVAQUIN® (Zostaw ah kwin) (lewofloksacyna) tabletki
Jakie są najważniejsze informacje, które powinienem wiedzieć o LEVAQUIN 500mg?
LEVAQUIN 500 mg, antybiotyk fluorochinolonowy, może powodować poważne skutki uboczne. Niektóre z tych poważnych działań niepożądanych mogą wystąpić w tym samym czasie i mogą prowadzić do śmierci.
Jeśli u pacjenta wystąpi którekolwiek z poniższych ciężkich działań niepożądanych podczas stosowania leku LEVAQUIN 500 mg, należy natychmiast przerwać przyjmowanie leku LEVAQUIN i natychmiast uzyskać pomoc medyczną.
- Problemy ze ścięgnami mogą wystąpić u osób w każdym wieku, które przyjmują LEVAQUIN. Ścięgna to twarde sznury tkanki, które łączą mięśnie z kośćmi. Niektóre problemy ze ścięgnami obejmują:
- ból
- obrzęk
- łzy i obrzęk ścięgien, w tym tylnej części kostki (Achillesa), barku, dłoni lub innych miejsc ścięgien.
- Ryzyko wystąpienia problemów ze ścięgnami podczas przyjmowania leku LEVAQUIN jest większe, jeśli:
- ukończyły 60 rok życia
- przeszła przeszczep nerki, serca lub płuc.
- Problemy ze ścięgnami mogą wystąpić u osób, które nie mają powyższych czynników ryzyka podczas przyjmowania leku LEVAQUIN.
- Inne powody, które mogą zwiększać ryzyko problemów ze ścięgnami, mogą obejmować:
- aktywność fizyczna lub ćwiczenia
- niewydolność nerek
- problemy ze ścięgnami w przeszłości, takie jak u osób z reumatoidalnym zapaleniem stawów (RZS)
- Należy natychmiast przerwać przyjmowanie leku LEVAQUIN i natychmiast uzyskać pomoc medyczną przy pierwszych objawach bólu ścięgna, obrzęku lub stanu zapalnego. Unikaj ćwiczeń i używania dotkniętego obszaru.
- Najczęstszym obszarem bólu i obrzęku jest ścięgno Achillesa z tyłu kostki. Może się to zdarzyć również w przypadku innych ścięgien. Do leczenia infekcji może być potrzebny inny antybiotyk, który nie jest fluorochinolonem.
- Zerwanie ścięgna może nastąpić podczas lub po zakończeniu przyjmowania leku LEVAQUIN. Zerwanie ścięgien może nastąpić w ciągu kilku godzin lub dni po przyjęciu leku LEVAQUIN i może wystąpić nawet kilka miesięcy po zakończeniu przyjmowania fluorochinolonów.
- Należy natychmiast przerwać przyjmowanie leku LEVAQUIN 750 mg i natychmiast uzyskać pomoc medyczną, jeśli wystąpi którykolwiek z następujących objawów zerwania ścięgna:
- usłyszeć lub poczuć trzask lub trzask w okolicy ścięgna
- zasinienie zaraz po urazie w okolicy ścięgna
- niezdolny do poruszania się dotkniętym obszarem lub znoszenia ciężaru
- ból
- palenie
- mrowienie
- drętwienie
- słabość
Uszkodzenie nerwu może być trwałe.
- drgawki
- słyszeć głosy, widzieć lub wyczuwać rzeczy, których nie ma (omamy)
- czuć się niespokojnie
- drżenia
- odczuwać niepokój lub zdenerwowanie
- dezorientacja
- depresja
- problemy ze snem
- koszmary
- czuć oszołomienie lub zawroty głowy
- czuć się bardziej podejrzliwie (paranoja)
- myśli lub czyny samobójcze
- bóle głowy, które nie ustępują, z niewyraźnym widzeniem lub bez
Co to jest LEVAQUIN?
LEVAQUIN 500 mg jest antybiotykiem fluorochinolonowym stosowanym u osób dorosłych w wieku 18 lat lub starszych w leczeniu niektórych zakażeń wywołanych przez niektóre drobnoustroje zwane bakteriami. Te infekcje bakteryjne obejmują:
- szpitalne zapalenie płuc
- pozaszpitalne zapalenie płuc
- infekcje skóry, powikłane i nieskomplikowane
- przewlekła infekcja prostaty
- zarazki wąglika wziewnego
- plaga
- infekcje dróg moczowych, powikłane i niepowikłane
- ostra infekcja nerek (odmiedniczkowe zapalenie nerek)
- ostra infekcja zatok
- ostre pogorszenie lub przewlekłe zapalenie oskrzeli
Badania preparatu LEVAQUIN do stosowania w leczeniu dżumy i wąglika przeprowadzono wyłącznie na zwierzętach, ponieważ dżumy i wąglika nie można było badać u ludzi.
Leku LEVAQUIN nie należy stosować u pacjentów z niepowikłanymi zakażeniami dróg moczowych, ostrym bakteryjnym zaostrzeniem przewlekłego zapalenia oskrzeli lub ostrym bakteryjnym zapaleniem zatok, jeśli dostępne są inne opcje leczenia.
LEVAQUIN 750 mg tabletki jest również stosowany w leczeniu dzieci, które ważą co najmniej 66 funtów (lub co najmniej 30 kilogramów) i które mogły wdychać zarazki wąglika, mieć dżumę lub były narażone na kontakt z zarazkami. Nie wiadomo, czy LEVAQUIN jest bezpieczny i skuteczny u dzieci w wieku poniżej 6 miesięcy.
Bezpieczeństwo i skuteczność u dzieci leczonych LEVAQUIN® przez ponad 14 dni nie jest znane.
Kto nie powinien zażywać LEVAQUIN 750 mg?
Nie należy przyjmować leku LEVAQUIN: jeśli u pacjenta kiedykolwiek wystąpiła ciężka reakcja alergiczna na antybiotyk znany jako fluorochinolon lub jeśli pacjent ma uczulenie na lewofloksacynę lub którykolwiek ze składników leku LEVAQUIN. Pełny wykaz składników leku LEVAQUIN znajduje się na końcu tej ulotki.
Przed przyjęciem leku LEVAQUIN należy poinformować lekarza o wszystkich swoich schorzeniach, w tym o:
- mieć problemy ze ścięgnami; LEVAQUIN 250mg nie powinien być stosowany u osób, które w przeszłości miały problemy ze ścięgnami.
- masz problem, który powoduje osłabienie mięśni (myasthenia gravis); Leku LEVAQUIN nie należy stosować u osób, u których rozpoznano miastenię ciężką.
- mają problemy z ośrodkowym układem nerwowym, takie jak drgawki (padaczka).
- mieć problemy z nerwami; Leku LEVAQUIN 250 mg nie należy stosować u pacjentów z zaburzeniami nerwowymi zwanymi neuropatią obwodową w wywiadzie.
- masz lub ktokolwiek z Twojej rodziny ma nieregularne bicie serca, zwłaszcza stan zwany „wydłużeniem odstępu QT”.
- mają niski poziom potasu we krwi (hipokaliemia).
- mieć problemy z kośćmi.
- mają problemy ze stawami, w tym reumatoidalne zapalenie stawów (RZS).
- mają problemy z nerkami. Jeśli nerki nie pracują prawidłowo, może być konieczne zastosowanie mniejszej dawki leku LEVAQUIN.
- masz problemy z wątrobą.
- mieć cukrzycę lub problemy z niskim poziomem cukru we krwi (hipoglikemia).
- są w ciąży lub planują zajść w ciążę. Nie wiadomo, czy LEVAQUIN 750 mg zaszkodzi nienarodzonemu dziecku.
- karmisz piersią lub planujesz karmić piersią. Nie wiadomo, czy LEVAQUIN przenika do mleka matki. Ty i Twój lekarz powinniście zdecydować, czy będziecie przyjmować lek LEVAQUIN 250 mg, czy karmić piersią. Nie powinieneś robić obu.
Poinformuj swojego lekarza o wszystkich przyjmowanych lekach, w tym leki na receptę i bez recepty, witaminy i suplementy ziołowe.
LEVAQUIN i inne leki mogą wzajemnie na siebie oddziaływać, powodując działania niepożądane.
Szczególnie powiedz swojemu lekarzowi, jeśli bierzesz:
- lek steroidowy.
- lek przeciwpsychotyczny.
- trójpierścieniowy lek przeciwdepresyjny.
- pigułka na wodę (diuretyk).
- niektóre leki mogą uniemożliwić prawidłowe działanie leku LEVAQUIN 750 mg. Lek LEVAQUIN® należy przyjmować 2 godziny przed lub 2 godziny po przyjęciu tych leków lub suplementów:
- środek zobojętniający kwas, multiwitaminy lub inne leki lub suplementy zawierające magnez, glin, żelazo lub cynk
- sukralfat (Carafate® )
- didanozyna (Videx®, Videx® EC)
- rozcieńczalnik krwi (warfaryna, Coumadin, Jantoven).
- doustny lek przeciwcukrzycowy lub insulina.
- NLPZ (niesteroidowy lek przeciwzapalny). Wiele popularnych leków przeciwbólowych to NLPZ. Przyjmowanie NLPZ podczas przyjmowania leku LEVAQUIN 250 mg lub innych fluorochinolonów może zwiększać ryzyko wystąpienia objawów ze strony ośrodkowego układu nerwowego i drgawek.
- teofilina (Theo-24®, Elixophyllin®, Theochron®, Uniphyl®, Theolair®).
- lek kontrolujący tętno lub rytm serca (leki przeciwarytmiczne).
Zapytaj swojego lekarza, jeśli nie masz pewności, czy którykolwiek z twoich leków jest wymieniony powyżej. Poznaj leki, które przyjmujesz. Zachowaj listę swoich leków i pokaż ją swojemu lekarzowi i farmaceucie, gdy otrzymasz nowy lek.
Jak powinienem przyjmować LEVAQUIN 500mg?
- Lek LEVAQUIN należy przyjmować zgodnie z zaleceniami lekarza.
- Lek LEVAQUIN 750 mg należy przyjmować mniej więcej o tej samej porze każdego dnia.
- Pij dużo płynów podczas przyjmowania leku LEVAQUIN.
- Lek LEVAQUIN można przyjmować z posiłkiem lub bez posiłku.
- W przypadku pominięcia dawki leku LEVAQUIN 500 mg należy ją przyjąć, gdy tylko sobie o tym przypomni. Nie należy przyjmować więcej niż 1 dawkę w ciągu 1 dnia.
- Nie należy pomijać żadnych dawek leku LEVAQUIN 750 mg ani przerywać jego przyjmowania, nawet jeśli poczujesz się lepiej, aż do zakończenia przepisanego leczenia, chyba że:
- masz problemy ze ścięgnami. Widzieć "Jakie są najważniejsze informacje, które powinienem wiedzieć o LEVAQUIN 500mg?".
- masz problem z nerwami. Widzieć „Jakie są możliwe skutki uboczne LEVAQUIN?”.
- masz problem z ośrodkowym układem nerwowym. Widzieć „Jakie są możliwe skutki uboczne LEVAQUIN 750mg?”.
- masz poważną reakcję alergiczną. Widzieć „Jakie są możliwe skutki uboczne LEVAQUIN 250mg?”.
- Twój lekarz poinformuje Cię o zaprzestaniu przyjmowania leku LEVAQUIN.
Przyjmowanie wszystkich dawek leku LEVAQUIN 500 mg pomoże upewnić się, że wszystkie bakterie zostaną zabite. Przyjmowanie wszystkich dawek LEVAQUIN 250 mg pomoże zmniejszyć ryzyko, że bakterie staną się oporne na LEVAQUIN. Jeśli zakażenie nie ustąpi podczas przyjmowania leku LEVAQUIN 750 mg, może to oznaczać, że bakterie powodujące zakażenie mogą być oporne na lek LEVAQUIN. Jeśli infekcja nie ustępuje, zadzwoń do swojego lekarza. Jeśli infekcja nie ustąpi, LEVAQUIN i inne podobne antybiotyki mogą nie działać w przyszłości.
- Jeśli zażyjesz zbyt dużo LEVAQUIN, skontaktuj się z lekarzem lub natychmiast uzyskaj pomoc medyczną.
Czego powinienem unikać podczas przyjmowania LEVAQUIN 500mg?
- LEVAQUIN może wywołać zawroty głowy i oszołomienie. Nie rób prowadzić pojazdów, obsługiwać maszyny lub wykonywać inne czynności wymagające sprawności umysłowej lub koordynacji do czasu poznania wpływu leku LEVAQUIN na pacjenta.
- Unikaj lamp słonecznych, solarium i staraj się ograniczać czas przebywania na słońcu. LEVAQUIN 750 mg może sprawić, że Twoja skóra stanie się wrażliwa na słońce (światłoczułość) oraz światło lamp słonecznych i łóżek opalających. Mogą wystąpić poważne oparzenia słoneczne, pęcherze lub obrzęk skóry. Jeśli wystąpi którykolwiek z tych objawów podczas przyjmowania leku LEVAQUIN, należy natychmiast skontaktować się z lekarzem. Powinieneś używać kremu przeciwsłonecznego i nosić czapkę i ubrania zakrywające skórę, jeśli musisz przebywać w słońcu.
Jakie są możliwe skutki uboczne LEVAQUIN 750mg?
LEVAQUIN 750mg może powodować poważne skutki uboczne, w tym:
- Widzieć "Jakie są najważniejsze informacje, które powinienem wiedzieć o LEVAQUIN 250mg?"
- Poważne reakcje alergiczne.
Reakcje alergiczne mogą wystąpić u osób przyjmujących fluorochinolony, w tym LEVAQUIN 500 mg, nawet po 1 dawce. Należy przerwać przyjmowanie leku LEVAQUIN 500 mg i natychmiast uzyskać pomoc medyczną w nagłych wypadkach, jeśli wystąpi którykolwiek z następujących objawów ciężkiej reakcji alergicznej:
- pokrzywka
- problemy z oddychaniem lub połykaniem
- obrzęk ust, języka, twarzy
- ucisk w gardle, chrypka
- szybkie bicie serca
- mdleć
- wysypka na skórze
Wysypka skórna może wystąpić u osób przyjmujących LEVAQUIN 500 mg, nawet po 1 dawce. Należy przerwać przyjmowanie leku LEVAQUIN 250 mg przy pierwszych oznakach wysypki skórnej i natychmiast skontaktować się z lekarzem. Wysypka skórna może być oznaką poważniejszej reakcji na LEVAQUIN.
- Uszkodzenie wątroby (hepatotoksyczność): Hepatotoksyczność może wystąpić u osób przyjmujących LEVAQUIN®. Zadzwoń do swojego lekarza natychmiast, jeśli masz niewyjaśnione objawy, takie jak:
- nudności lub wymioty
- ból brzucha
- gorączka
- słabość
- ból lub tkliwość brzucha
- swędzący
- niezwykłe zmęczenie
- utrata apetytu
- jasne wypróżnienia
- ciemny kolor moczu
- zażółcenie skóry lub białek oczu
Należy przerwać przyjmowanie leku LEVAQUIN 750 mg i natychmiast poinformować lekarza, jeśli u pacjenta występuje zażółcenie skóry lub białych części oczu lub ciemne zabarwienie moczu. Mogą to być objawy ciężkiej reakcji na LEVAQUIN (choroba wątroby).
- Zakażenie jelit (rzekomobłoniaste zapalenie jelita grubego) Rzekomobłoniaste zapalenie jelita grubego może wystąpić w przypadku wielu antybiotyków, w tym LEVAQUIN. Natychmiast skontaktuj się z lekarzem, jeśli wystąpi wodnista biegunka, biegunka, która nie ustępuje lub krwawe stolce. Możesz mieć skurcze żołądka i gorączkę. Rzekomobłoniaste zapalenie jelita grubego może wystąpić 2 lub więcej miesięcy po odstawieniu antybiotyku.
- Poważne zmiany rytmu serca (wydłużenie odstępu QT i torsades depointes) Poinformuj natychmiast swojego lekarza, jeśli zauważysz zmianę rytmu serca (szybkie lub nieregularne bicie serca) lub jeśli zemdlejesz. LEVAQUIN 250 mg może powodować rzadkie problemy z sercem znane jako wydłużenie odstępu QT. Ten stan może powodować nieprawidłowe bicie serca i może być bardzo niebezpieczny. Szanse na to są większe u ludzi:
- którzy są starsi?
- z wywiadem rodzinnym wydłużonego odstępu QT
- z niskim poziomem potasu we krwi (hipokaliemia)
- którzy przyjmują pewne leki kontrolujące rytm serca (leki przeciwarytmiczne)
- Wspólne problemy Może wystąpić zwiększone ryzyko problemów ze stawami i tkankami wokół stawów u dzieci. Należy poinformować lekarza dziecka, jeśli dziecko ma jakiekolwiek problemy ze stawami podczas lub po leczeniu lekiem LEVAQUIN.
- Zmiany poziomu cukru we krwi Osoby przyjmujące LEVAQUIN i inne leki fluorochinolonowe z doustnymi lekami przeciwcukrzycowymi lub insuliną mogą mieć niski poziom cukru we krwi (hipoglikemia) i wysoki poziom cukru we krwi (hiperglikemia). Postępuj zgodnie z instrukcjami lekarza, jak często sprawdzać poziom cukru we krwi. Jeśli masz cukrzycę i masz niski poziom cukru we krwi podczas przyjmowania leku LEVAQUIN, przerwij przyjmowanie leku LEVAQUIN 500 mg i natychmiast skontaktuj się z lekarzem. Może być konieczna zmiana antybiotyku.
- Wrażliwość na światło słoneczne (światłoczułość) Widzieć „Czego powinienem unikać podczas przyjmowania leku LEVAQUIN?” Najczęstsze skutki uboczne LEVAQUIN 250mg to:
- mdłości
- ból głowy
- biegunka
- bezsenność
- zaparcie
- zawroty głowy
U dzieci w wieku 6 miesięcy i starszych, które przyjmują lek LEVAQUIN w leczeniu wąglika lub dżumy, często występują również wymioty.
LEVAQUIN może powodować fałszywie dodatnie wyniki badań przesiewowych moczu na obecność opiatów, gdy testy są wykonywane za pomocą niektórych dostępnych na rynku zestawów. Wynik dodatni należy potwierdzić bardziej szczegółowym testem. To nie wszystkie możliwe działania niepożądane leku LEVAQUIN.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Jak przechowywać lek LEVAQUIN 250mg?
- Przechowywać LEVAQUIN 500mg w temperaturze pokojowej pomiędzy 59°F do 86°F (15°C do 30°C).
- Przechowywać LEVAQUIN 500 mg w szczelnie zamkniętym pojemniku.
Ogólne informacje o bezpiecznym i skutecznym stosowaniu LEVAQUIN.
Leki są czasami przepisywane do celów innych niż wymienione w Przewodniku po lekach. Nie należy stosować leku LEVAQUIN w stanie, na który nie jest przepisany. Nie należy podawać leku LEVAQUIN 500 mg innym osobom, nawet jeśli mają takie same objawy jak ty. Może im to zaszkodzić. Ten przewodnik po lekach podsumowuje najważniejsze informacje o LEVAQUIN. Jeśli chcesz uzyskać więcej informacji na temat LEVAQUIN 750 mg, porozmawiaj ze swoim lekarzem. Możesz poprosić swojego lekarza lub farmaceutę o informacje o LEVAQUIN 500 mg, które są przeznaczone dla pracowników służby zdrowia.
Jakie są składniki LEVAQUIN 500mg?
Składnik czynny: lewofloksacyna
Nieaktywne składniki : krospowidon, hypromeloza, magnezu stearynian, celuloza mikrokrystaliczna, glikol polietylenowy, polisorbat 80, dwutlenek tytanu.
Tabletki LEVAQUIN 250 mg zawierają również syntetyczny czerwony tlenek żelaza.
Tabletki LEVAQUIN 500 mg zawierają również syntetyczny czerwony tlenek żelaza i syntetyczny żółty tlenek żelaza.
Ten przewodnik po lekach został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków
