Vantin 200mg, 100mg Cefpodoxime Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Vantin 100mg i jak się go stosuje?
Vantin 100mg to lek na receptę stosowany w leczeniu objawów różnych infekcji bakteryjnych, takich jak zapalenie oskrzeli, zapalenie płuc, zapalenie zatok, zapalenie gardła, zapalenie migdałków, infekcje dróg moczowych, infekcje skóry i rzeżączka. Vantin 200mg może być stosowany samodzielnie lub z innymi lekami.
Vantin należy do klasy leków o nazwie Caphalosporins, trzeciej generacji.
Nie wiadomo, czy Vantin jest bezpieczny i skuteczny u dzieci w wieku poniżej 2 miesięcy.
Jakie są możliwe skutki uboczne Vantin 200mg?
Vantin może powodować poważne skutki uboczne, w tym:
- pokrzywka,
- trudności w oddychaniu,
- obrzęk twarzy, warg, języka lub gardła,
- gorączka,
- ból gardła,
- płonący w twoich oczach,
- ból skóry,
- czerwona lub fioletowa wysypka skórna, która rozprzestrzenia się i powoduje powstawanie pęcherzy i łuszczenie,
- silny ból brzucha,
- biegunka wodnista lub krwawa,
- obrzęk gruczołów,
- ból stawu,
- ogólne złe samopoczucie,
- bicie serca,
- fruwające w piersi,
- duszność i
- konfiskata
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Vantinu to:
- swędzenie lub upławy pochwy,
- wysypka pieluszkowa u niemowlęcia stosującego ten lek,
- mdłości,
- wymioty,
- biegunka,
- ból brzucha i
- ból głowy
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Vantinu. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
Aby ograniczyć rozwój bakterii opornych na leki i utrzymać skuteczność VANTIN 100 mg i innych leków przeciwbakteryjnych, VANTIN 100 mg należy stosować wyłącznie w leczeniu lub zapobieganiu zakażeniom, co do których udowodniono lub z dużym podejrzeniem, że są wywołane przez bakterie.
OPIS
Cefpodoksym proksetyl jest podawanym doustnie półsyntetycznym antybiotykiem z klasy cefalosporyn o rozszerzonym spektrum działania. Nazwa chemiczna to (RS)-1(izopropoksykarbonyloksy)etylo(+)-(6R,7R)-7-[2-(2-amino-4-tiazolilo)-2-{(Z)metoksyimino}acetamido]-3 -metoksymetylo-8-okso-5-tia-1-azabicyklo[4.2.0]okt-2-eno-2-karboksylan. Jego wzór empiryczny to C21H27N5O9S2, a jego wzór strukturalny przedstawiono poniżej:
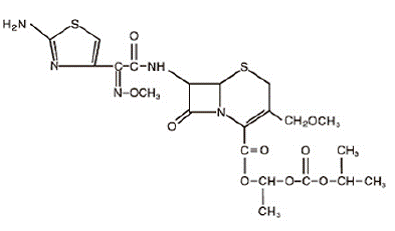
Masa cząsteczkowa proksetylu cefpodoksymu wynosi 557,6.
Proksetyl cefpodoksymu jest prolekiem; jego aktywnym metabolitem jest cefpodoksym. Wszystkie dawki proksetylu cefpodoksymu we wkładce wyrażono jako aktywne ugrupowanie cefpodoksymu. Lek jest dostarczany zarówno w postaci tabletek powlekanych, jak i aromatyzowanych granulek do sporządzania zawiesiny doustnej.
Tabletki VANTIN zawierają proksetyl cefpodoksymu odpowiadający 100 mg lub 200 mg aktywności cefpodoksymu oraz następujące składniki nieaktywne: wapniowa karboksymetyloceluloza, wosk karnauba, FD&C Yellow nr 6, hydroksypropyloceluloza, hypromeloza, laktoza uwodniona, stearynian magnezu, glikol propylenowy, laurylosiarczan sodu i dwutlenek tytanu. Ponadto tabletki powlekane 100 mg zawierają D&C Yellow No. 10, a tabletki powlekane 200 mg zawierają FD&C Red No. 40.
Każde 5 ml zawiesiny doustnej VANTIN zawiera proksetyl cefpodoksymu odpowiadający 50 mg lub 100 mg aktywności cefpodoksymu po utworzeniu oraz następujące składniki nieaktywne: sztuczne aromaty, butylohydroksyanizol (BHA), sól sodowa karboksymetylocelulozy, celuloza mikrokrystaliczna, karagen, kwas cytrynowy, koloidalny dwutlenek krzemu, kroskarmeloza sodowa, hydroksypropyloceluloza, laktoza, maltodekstryna, naturalne aromaty, alginian glikolu propylenowego, cytrynian sodu, benzoesan sodu, skrobia, sacharoza i olej roślinny.
WSKAZANIA
Cefpodoksym proksetylu jest wskazany w leczeniu pacjentów z łagodnymi lub umiarkowanymi zakażeniami wywołanymi przez wrażliwe szczepy wskazanych drobnoustrojów w stanach wymienionych poniżej.
Zalecane dawki, czas trwania terapii i odpowiednie populacje pacjentów różnią się w zależności od tych infekcji. Szczegółowe zalecenia można znaleźć w DAWKOWANIE I PODAWANIE. Ostre zapalenie ucha środkowego wywołane przez Streptococcus pneumoniae (z wyłączeniem szczepów opornych na penicylinę), Streptococcus pyogenes, Haemophilus influenzae (w tym szczepy wytwarzające beta-laktamazę) lub Moraxella (Branhamella) catarrhalis (w tym szczepy wytwarzające beta-laktamazę).
Zapalenie gardła i/lub migdałków wywołane przez Streptococcus pyogenes.
NOTATKA: Wykazano, że tylko penicylina podawana domięśniowo jest skuteczna w profilaktyce gorączki reumatycznej. Proksetyl cefpodoksymu jest ogólnie skuteczny w eradykacji paciorkowców z jamy ustnej i gardła. Nie są jednak dostępne dane określające skuteczność proksetylu cefpodoksymu w profilaktyce późniejszej gorączki reumatycznej.
Pozaszpitalne zapalenie płuc wywołane przez S. pneumoniae lub H. Influenzae (w tym szczepy wytwarzające beta-laktamazy).
Ostre bakteryjne zaostrzenie przewlekłego zapalenia oskrzeli wywołane przez S. pneumoniae, H. influenzae (tylko szczepy nie wytwarzające betalaktamaz) lub M. catarrhalis. Obecnie dane są niewystarczające do ustalenia skuteczności u pacjentów z ostrymi bakteryjnymi zaostrzeniami przewlekłego zapalenia oskrzeli wywołanymi przez szczepy H. influenzae wytwarzające beta-laktamazę.
Ostra, nieskomplikowana rzeżączka cewki moczowej i szyjki macicy wywołane przez Neisseria gonorrhoeae (w tym szczepy wytwarzające penicylinazy).
Ostre, niepowikłane infekcje odbytu u kobiet z powodu Neisseria gonorrhoeae (w tym szczepów wytwarzających penicylinazę).
NOTATKA: Nie ustalono skuteczności cefpodoksymu w leczeniu pacjentów płci męskiej z zakażeniami odbytnicy wywołanymi przez N. gonorrhoeae. Dane nie potwierdzają stosowania proksetylu cefpodoksymu w leczeniu zakażeń gardła wywołanych przez N. gonorrhoeae u mężczyzn lub kobiet.
Nieskomplikowane infekcje skóry i struktury skóry wywołane przez Staphylococcus aureus (w tym szczepy wytwarzające penicylinazę) lub Streptococcus pyogenes. Ropnie należy drenować chirurgicznie, zgodnie ze wskazaniami klinicznymi.
NOTATKA: W badaniach klinicznych skuteczne leczenie niepowikłanych zakażeń skóry i struktur skóry było zależne od dawki. Skuteczna dawka terapeutyczna w przypadku infekcji skóry była wyższa niż stosowana w innych zalecanych wskazaniach. (Widzieć DAWKOWANIE I SPOSÓB PODAWANIA .)
Ostre zapalenie zatok szczękowych wywołane przez Haemophilus influenzae (w tym szczepy wytwarzające beta-laktamazę), Streptococcus pneumoniae i Moraxella catarrhalis.
Nieskomplikowane infekcje dróg moczowych (zapalenie pęcherza moczowego) wywołane przez Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis lub Staphylococcus saprophyticus.
NOTATKA: Rozważając zastosowanie proksetylu cefpodoksymu w leczeniu zapalenia pęcherza moczowego, należy porównać niższe wskaźniki eradykacji bakterii cefpodoksymu proksetylu ze zwiększonymi wskaźnikami eradykacji i różnymi profilami bezpieczeństwa niektórych innych klas zatwierdzonych leków. (Widzieć Studia kliniczne Sekcja.)
Należy pobrać odpowiednie próbki do badania bakteriologicznego w celu wyizolowania i zidentyfikowania drobnoustrojów sprawczych oraz określenia ich wrażliwości na cefpodoksym. Terapię można rozpocząć w oczekiwaniu na wyniki tych badań. Gdy wyniki te staną się dostępne, należy odpowiednio dostosować terapię przeciwdrobnoustrojową.
celu ograniczenia rozwoju bakterii lekoopornych i utrzymania skuteczności preparatu VANTIN 100 mg i innych leków przeciwbakteryjnych, VANTIN 200 mg należy stosować wyłącznie w leczeniu lub zapobieganiu zakażeniom, co do których udowodniono lub z dużym podejrzeniem, że są powodowane przez wrażliwe bakterie. Gdy dostępne są informacje dotyczące hodowli i wrażliwości, należy je uwzględnić przy wyborze lub modyfikacji terapii przeciwbakteryjnej. W przypadku braku takich danych, lokalna epidemiologia i wzorce podatności mogą przyczynić się do empirycznego doboru terapii.
DAWKOWANIE I SPOSÓB PODAWANIA
(Widzieć WSKAZANIA I ZASTOSOWANIE dla wskazanych patogenów.)
Tabletki powlekane
Tabletki VANTIN należy podawać doustnie z pokarmem w celu zwiększenia wchłaniania. (Widzieć FARMAKOLOGIA KLINICZNA .)
Zalecane dawki, czas trwania leczenia i odpowiednia populacja pacjentów są opisane w poniższej tabeli:
Dorośli i młodzież (w wieku 12 lat i starsi)
Granulki do zawiesiny doustnej
Zawiesinę doustną VANTIN można podawać niezależnie od posiłków. Zalecane dawki, czas trwania leczenia i odpowiednie populacje pacjentów są opisane w poniższej tabeli:
Dorośli i młodzież (w wieku 12 lat i starsi)
Niemowlęta i pacjenci pediatryczni (w wieku od 2 miesięcy do 12 lat)
Pacjenci z zaburzeniami czynności nerek
U pacjentów z ciężkimi zaburzeniami czynności nerek (klirens kreatyniny
Gdy dostępny jest tylko poziom kreatyniny w surowicy, do oszacowania klirensu kreatyniny (ml/min) można użyć następującego wzoru (w oparciu o płeć, wagę i wiek pacjenta). Aby to oszacowanie było prawidłowe, poziom kreatyniny w surowicy powinien odpowiadać ustalonemu stanowi czynności nerek.
Mężczyźni (ml/min): Waga (kg) x (140 - wiek)/ 72 x kreatynina w surowicy (mg/100 ml)
Kobiety (ml/min) : 0,85 x powyżej wartości
Pacjenci z marskością wątroby
Farmakokinetyka cefpodoksymu u pacjentów z marskością wątroby (z wodobrzuszem lub bez) jest podobna jak u zdrowych osób. W tej populacji dostosowanie dawki nie jest konieczne.
Przygotowanie zawieszenia
Wskazówki konstytucyjne dotyczące zawieszenia ustnego
Po wymieszaniu zawiesinę należy przechowywać w lodówce w temperaturze od 2° do 8°C (36° do 46°F). Wstrząśnij porządnie przed użyciem. Przechowywać pojemnik szczelnie zamknięty. Mieszankę można stosować przez 14 dni. Wyrzucić niewykorzystaną porcję po 14 dniach.
JAK DOSTARCZONE
Tabletki VANTIN są dostępne w następujących mocach (odpowiednik cefpodoksymu), kolorach i rozmiarach:
100 mg (jasnopomarańczowy, eliptyczny, wytłoczony U3617)
Butelki 20 NDC 0009-3617-01 Butelki 100 NDC 0009-3617-02 Opakowania jednostkowe po 100 NDC 0009-3617-03
200 mg (koral czerwony, eliptyczny, wytłoczony U3618)
Butelki 20 NDC 0009-3618-01 Butelki 100 NDC 0009-3618-02
200 mg (koral czerwony, eliptyczny, wytłoczony U3618)
Opakowania jednostkowe po 100 NDC 0009-3618-03
Przechowuj tabletki w kontrolowanej temperaturze pokojowej od 20 do 25 ° C (68 do 77 ° F) [patrz USP ].
Po każdym otwarciu założyć zatyczkę. Chronić opakowania jednostkowe przed nadmierną wilgocią.
VANTIN 200 mg zawiesina doustna zapewnia ekwiwalent 50 mg lub 100 mg cefpodoksymu na 5 ml zawiesiny (jeśli jest sporządzony zgodnie z zaleceniami) i jest dostępny w smaku cytrynowo-kremowym w następujących rozmiarach:
50 mg/5 ml
100 ml zawiesiny NDC 0009-3531-01 75-ml zawiesina NDC 0009-3531-02 50 ml zawiesina NDC 0009-3531-03
100 mg/5 ml
100 ml zawiesiny NDC 0009-3615-01 75-ml zawiesina NDC 0009-3615-02 50 ml zawiesina NDC 0009-3615-03
Przechowywać nie zawieszone granulki w kontrolowanej temperaturze pokojowej 20 ° do 25 ° C (68 ° do 77 ° F) [patrz USP ].
Wskazówki dotyczące mieszania znajdują się na etykiecie. Po wymieszaniu zawiesinę należy przechowywać w lodówce w temperaturze od 2° do 8°C (36° do 46°F). Wstrząśnij porządnie przed użyciem. Przechowywać pojemnik szczelnie zamknięty. Mieszankę można stosować przez 14 dni. Wyrzucić niewykorzystaną porcję po 14 dniach.
Dystrybutor: Pharmacia & Upjohn Company, oddział firmy Pfizer Inc., NY, NY 10017. Aktualizacja: sierpień 2016
SKUTKI UBOCZNE
Badania kliniczne
Tabletki powlekane (wielodawkowe)
W badaniach klinicznych przy użyciu wielokrotne dawki tabletek powlekanych cefpodoksymu proksetylu, 4696 pacjentów było leczonych zalecanymi dawkami cefpodoksymu (100 do 400 mg co 12 godzin). Nie było żadnych zgonów ani trwałej niepełnosprawności związanej z toksycznością leków. Stu dwudziestu dziewięciu (2,7%) pacjentów przerwało leczenie z powodu zdarzeń niepożądanych, które przypuszczalnie lub prawdopodobnie miały związek z toksycznością leku. Dziewięćdziesiąt trzy (52%) ze 178 pacjentów, którzy przerwali terapię (bez względu na to, czy myślano o terapii lekowej, czy nie), zrobiło to z powodu zaburzeń żołądkowo-jelitowych, nudności, wymiotów lub biegunki. Odsetek pacjentów leczonych cefpodoksymem proksetylem, którzy przerwali stosowanie badanego leku z powodu działań niepożądanych, był istotnie większy przy dawce 800 mg na dobę niż przy dawce 400 mg na dobę lub 200 mg na dobę. Zdarzenia niepożądane uważane za prawdopodobnie lub prawdopodobnie związane z cefpodoksymem w badaniach klinicznych po podaniu wielokrotnym (n=4696 pacjentów leczonych cefpodoksymem):
Częstość występowania większa niż 1%
Biegunka 7,0%
Biegunka lub luźne stolce były zależne od dawki: zmniejszyły się z 10,4% pacjentów otrzymujących 800 mg dziennie do 5,7% dla pacjentów otrzymujących 200 mg dziennie. Spośród pacjentów z biegunką 10% miało drobnoustrój lub toksynę C. difficile w kale. (Widzieć OSTRZEŻENIA .)
Nudności 3,3% Grzybice pochwy 1,0% Zakażenia sromu i pochwy 1,3% Ból brzucha 1,2% Ból głowy 1,0%
Częstość występowania poniżej 1%
Według układu ciała w porządku malejącym
Studia kliniczne
Zdarzenia niepożądane, które prawdopodobnie lub prawdopodobnie są związane z proksetylem cefpodoksymu, które wystąpiły u mniej niż 1% pacjentów (N=4696)
Ciało - zakażenia grzybicze, wzdęcie brzucha, złe samopoczucie, zmęczenie, astenia, gorączka, ból w klatce piersiowej, ból pleców, dreszcze, ból uogólniony, nieprawidłowe wyniki badań mikrobiologicznych, drożdżyca, ropień, reakcja alergiczna, obrzęk twarzy, zakażenia bakteryjne, zakażenia pasożytnicze, obrzęk miejscowy, ból miejscowy .
Układ sercowo-naczyniowy - zastoinowa niewydolność serca, migrena, kołatanie serca, rozszerzenie naczyń krwionośnych, krwiak, nadciśnienie, niedociśnienie.
Trawienny - wymioty, niestrawność, suchość w ustach, wzdęcia, zmniejszony apetyt, zaparcia, drożdżyca jamy ustnej, jadłowstręt, odbijanie się, zapalenie żołądka, owrzodzenie jamy ustnej, zaburzenia żołądkowo-jelitowe, zaburzenia odbytnicy, zaburzenia języka, zaburzenia zębów, zwiększone pragnienie, zmiany w jamie ustnej, parcie, suchość gardła, ból zęba .
Hemiczny i limfatyczny - niedokrwistość.
Metaboliczne i odżywcze - odwodnienie, dna moczanowa, obrzęki obwodowe, wzrost masy ciała.
mięśniowo-szkieletowy - bóle mięśniowe.
Nerwowy - zawroty głowy, bezsenność, senność, lęk, drżenie, nerwowość, zawał mózgu, zmiany w snach, zaburzenia koncentracji, splątanie, koszmary senne, parestezje, zawroty głowy.
Układ oddechowy - astma, kaszel, krwawienie z nosa, nieżyt nosa, świszczący oddech, zapalenie oskrzeli, duszność, wysięk opłucnowy, zapalenie płuc, zapalenie zatok.
Skóra - pokrzywka, wysypka, świąd w miejscu bez aplikacji, obfite pocenie się, wysypka plamkowo-grudkowa, grzybicze zapalenie skóry, łuszczenie, suchość skóry w miejscu aplikacji, wypadanie włosów, wysypka pęcherzykowo-pęcherzowa, oparzenie słoneczne.
Zmysły specjalne - zmiany smaku, podrażnienie oczu, utrata smaku, szum w uszach.
Układ moczowo-płciowy - krwiomocz, infekcje dróg moczowych, krwotok maciczny, bolesne oddawanie moczu, częste oddawanie moczu, nokturia, zakażenie prącia, białkomocz, ból pochwy.
Granulki do zawiesiny doustnej (wielodawkowe)
badaniach klinicznych, w których stosowano wielokrotne dawki cefpodoksymu proksetylu w postaci granulatu do sporządzania zawiesiny doustnej, 2128 pacjentów pediatrycznych (93% z nich było w wieku poniżej 12 lat) było leczonych zalecanymi dawkami cefpodoksymu (10 mg/kg mc./dobę co 24 godziny lub Q 12 godzin do maksymalnej równoważnej dawki dla dorosłych). U żadnego z pacjentów w tych badaniach nie było zgonów ani trwałej niepełnosprawności. Dwudziestu czterech pacjentów (1,1%) przerwało leczenie z powodu zdarzeń niepożądanych, które przypuszczalnie lub prawdopodobnie miały związek z badanym lekiem. Przede wszystkim przerwania te dotyczyły zaburzeń żołądkowo-jelitowych, zwykle biegunki, wymiotów lub wysypki.
Zdarzenia niepożądane uważane za prawdopodobnie lub prawdopodobnie związane lub o nieznanym związku z proksetylem cefpodoksymu w postaci zawiesiny doustnej w badaniach klinicznych z wielokrotnymi dawkami (N=2128 pacjentów leczonych cefpodoksymem):
Częstość występowania większa niż 1%
Biegunka 6,0% Częstość występowania biegunki u niemowląt i małych dzieci (w wieku od 1 miesiąca do 2 lat) wyniosła 12,8%. Wysypka pieluszkowa/Grzybica wysypka skórna 2,0% (w tym drożdżyca) Częstość występowania pieluszkowej wysypki u niemowląt i małych dzieci wynosiła 8,5%. Inne wysypki skórne 1,8% Wymioty 2,3%
Częstość występowania poniżej 1%
Ciało: Miejscowy ból brzucha, skurcze brzucha, ból głowy, monilia, uogólniony ból brzucha, astenia, gorączka, infekcja grzybicza.
Trawienny: Nudności, monilia, anoreksja, suchość w ustach, zapalenie jamy ustnej, rzekomobłoniaste zapalenie okrężnicy.
Hemiczny i limfatyczny: Małopłytkowość, dodatni bezpośredni test Coombsa, eozynofilia, leukocytoza, leukopenia, wydłużony czas częściowej tromboplastyny, plamica małopłytkowa.
Metaboliczne i odżywcze: Zwiększony SGPT.
Układ mięśniowo-szkieletowy: Bóle mięśni.
Nerwowy: Halucynacje, hiperkinezja, nerwowość, senność.
Oddechowy: Krwawienie z nosa, nieżyt nosa.

Skóra: Monilioza skóry, pokrzywka, grzybicze zapalenie skóry, trądzik, złuszczające zapalenie skóry, wysypka plamkowo-grudkowa.
Zmysły specjalne: Perwersja smaku.
Tabletki powlekane (pojedyncza dawka)
W badaniach klinicznych z użyciem pojedyncza dawka tabletek powlekanych cefpodoksymu proksetylu, 509 pacjentów leczono zalecaną dawką cefpodoksymu (200 mg). W badaniach tych nie stwierdzono zgonów ani trwałej niepełnosprawności związanej z toksycznością leków.
Zdarzenia niepożądane uważane za potencjalnie lub prawdopodobnie związane z cefpodoksymem w badaniach klinicznych z pojedynczą dawką przeprowadzonych w Stanach Zjednoczonych to:
Częstość występowania większa niż 1%
Nudności 1,4% Biegunka 1,2%
Częstość występowania poniżej 1%
Centralny układ nerwowy: zawroty głowy, ból głowy, omdlenia. Dermatologiczne: wysypka. Narządy płciowe: zapalenie pochwy. Przewód pokarmowy: Ból brzucha. Psychiatryczny: niepokój.
Zmiany laboratoryjne
Istotne zmiany laboratoryjne, które zgłoszono u dorosłych i dzieci w badaniach klinicznych proksetylu cefpodoksymu, niezależnie od związku z lekiem, to:
Wątrobiany: Przejściowy wzrost AST (SGOT), ALT (SGPT), GGT, fosfatazy alkalicznej, bilirubiny i LDH.
Hematologiczny: Eozynofilia, leukocytoza, limfocytoza, granulocytoza, bazofilia, monocytoza, trombocytoza, obniżony poziom hemoglobiny, obniżony hematokryt, leukopenia, neutropenia, limfocytopenia, trombocytopenia, trombocytemia, dodatni wynik testu Coombsa oraz wydłużenie PT i PTT.
Chemia surowicy: Hiperglikemia, hipoglikemia, hipoalbuminemia, hipoproteinemia, hiperkaliemia i hiponatremia.
Nerkowy: Zwiększa BUN i kreatyninę.
Większość z tych nieprawidłowości była przemijająca i nieistotna klinicznie.
Doświadczenie po marketingu
Zgłaszano następujące ciężkie działania niepożądane: reakcje alergiczne, w tym zespół Stevensa-Johnsona, toksyczne martwicze oddzielanie się naskórka, rumień wielopostaciowy i reakcje przypominające chorobę posurowiczą, rzekomobłoniaste zapalenie jelita grubego, krwawa biegunka z bólem brzucha, wrzodziejące zapalenie jelita grubego, krwotok odbytniczy z niedociśnieniem, wstrząs anafilaktyczny, ostry uszkodzenie wątroby, ekspozycja w macicy z poronieniem, plamicowe zapalenie nerek, nacieki płucne z eozynofilią i zapalenie skóry powiek.
Jeden zgon przypisano rzekomobłoniastemu zapaleniu jelita grubego i rozsianemu wykrzepianiu wewnątrznaczyniowemu.
Oznakowanie klasy cefalosporyn
Poza wymienionymi powyżej działaniami niepożądanymi, które obserwowano u pacjentów leczonych proksetylem cefpodoksymu, zgłaszano następujące działania niepożądane i zmienione wyniki badań laboratoryjnych dla antybiotyków z grupy cefalosporyn:
Działania niepożądane i nieprawidłowe testy laboratoryjne: Zaburzenia czynności nerek, nefropatia toksyczna, zaburzenia czynności wątroby, w tym cholestaza, niedokrwistość aplastyczna, niedokrwistość hemolityczna, reakcja przypominająca chorobę posurowiczą, krwotok, agranulocytoza i pancytopenia.
Kilka cefalosporyn powiązano z wywoływaniem drgawek, szczególnie u pacjentów z zaburzeniami czynności nerek, gdy nie zmniejszono dawki. (Widzieć DAWKOWANIE I SPOSÓB PODAWANIA oraz PRZEDAWKOWANIE .) Jeśli wystąpią drgawki związane z farmakoterapią, lek należy odstawić. Leczenie przeciwdrgawkowe można zastosować, jeśli jest to klinicznie wskazane.
INTERAKCJE Z LEKAMI
Leki zobojętniające sok żołądkowy
Jednoczesne podawanie dużych dawek leków zobojętniających (wodorowęglan sodu i wodorotlenek glinu) lub H2-blokerów zmniejsza maksymalne stężenia w osoczu odpowiednio o 24% do 42%, a stopień wchłaniania o 27% do 32%. Jednoczesne przyjmowanie leków nie wpływa na szybkość wchłaniania. Doustne leki przeciwcholinergiczne (np. propantelina) opóźniają maksymalne stężenia w osoczu (wzrost Tmax o 47%), ale nie wpływają na stopień wchłaniania (AUC).
Probenecyd
Podobnie jak w przypadku innych antybiotyków beta-laktamowych, probenecyd hamował wydalanie cefpodoksymu przez nerki i powodowało zwiększenie AUC o około 31% i zwiększenie maksymalnego stężenia cefpodoksymu w osoczu o 20%.
Leki nefrotoksyczne
Chociaż nie stwierdzono nefrotoksyczności podczas podawania samego cefpodoksymu proksetyl, zaleca się ścisłe monitorowanie czynności nerek, gdy cefpodoksym proksetyl jest podawany jednocześnie ze związkami o znanym potencjale nefrotoksycznym.
Interakcje leków/testów laboratoryjnych
Wiadomo, że cefalosporyny, w tym proksetyl cefpodoksymu, czasami wywołują dodatni bezpośredni test Coombsa.
OSTRZEŻENIA
PRZED WPROWADZENIEM TERAPII CEFPODOKSYMEM PROXETIL NALEŻY UWAŻNIE WYKONAĆ DOCHODZENIE W CELU OKREŚLENIA, CZY PACJENT WYSTĄPIŁ WCZEŚNIEJSZE REAKCJE NADWRAŻLIWOŚCI NA CEFPODOKSYM, INNE CEFALOSPORYNY, PENICILNY LUB INNE DRU. W PRZYPADKU PODAWANIA CEFPODOKSYMU PACJENTOM WRAŻLIWYM NA PENICYLINĘ NALEŻY ZACHOWAĆ OSTROŻNOŚĆ, PONIEWAŻ NADWRAŻLIWOŚĆ KRZYŻOWA WŚRÓD ANTYBIOTYKÓW BETA-LAKTAMOWYCH JEST WYRAŹNIE UDOKUMENTOWANA I MOŻE WYSTĄPIĆ DO 10% PACJENTÓW Z CHOROBĄ. W PRZYPADKU REAKCJI ALERGICZNEJ NA PROXETIL CEFPODOKSYMU NALEŻY ZAPRZESTAĆ STOSOWANIA LEKÓW. POWAŻNE Ostre REAKCJE NADWRAŻLIWOŚCI MOGĄ WYMAGAĆ LECZENIA EPINEFRYNĄ I INNYCH ŚRODKÓW NAGŁYCH, W TLENU, PŁYNÓW DOŻYLNYCH, DOŻYLNYCH PRZECIWHISTAMIENI I DRÓG ODDECHOWYCH, ZGODNIE Z WSKAZANIAMI KLINICZNYMI.
Biegunkę związaną z Clostridium difficile (CDAD) zgłaszano po zastosowaniu prawie wszystkich środków przeciwbakteryjnych, w tym VANTIN, a jej nasilenie może wahać się od łagodnej biegunki do zapalenia okrężnicy zakończonego zgonem. Leczenie środkami przeciwbakteryjnymi zmienia normalną florę okrężnicy, prowadząc do przerostu C. difficile.
C. difficile wytwarza toksyny A i B, które przyczyniają się do rozwoju CDAD. Szczepy C. difficile wytwarzające hipertoksyny powodują zwiększoną zachorowalność i śmiertelność, ponieważ zakażenia te mogą być oporne na leczenie przeciwbakteryjne i mogą wymagać kolektomii. CDAD należy rozważyć u wszystkich pacjentów, u których po zastosowaniu antybiotyków wystąpi biegunka. Konieczna jest staranna historia choroby, ponieważ donoszono, że CDAD występuje w ciągu dwóch miesięcy po podaniu leków przeciwbakteryjnych.
przypadku podejrzenia lub potwierdzenia CDAD, może być konieczne przerwanie trwającego stosowania antybiotyków, które nie są skierowane przeciwko C. difficile. W zależności od wskazań klinicznych należy wdrożyć odpowiednią gospodarkę wodno-elektrolitową, suplementację białka, antybiotykoterapię C. difficile oraz ocenę chirurgiczną.
Podjęto wspólne wysiłki w celu monitorowania obecności C. difficile u pacjentów z biegunką leczonych cefpodoksymem ze względu na zwiększoną częstość występowania biegunki związanej z C. difficile we wczesnych badaniach klinicznych u zdrowych osób. Obecność drobnoustrojów lub toksyn C. difficile stwierdzono u 10% dorosłych pacjentów z biegunką leczonych cefpodoksymem; jednak u tych pacjentów nie postawiono specyficznego rozpoznania rzekomobłoniastego zapalenia jelita grubego.
Po wprowadzeniu do obrotu poza Stanami Zjednoczonymi otrzymano zgłoszenia rzekomobłoniastego zapalenia jelita grubego związanego ze stosowaniem proksetylu cefpodoksymu.
ŚRODKI OSTROŻNOŚCI
Ogólny
U pacjentów z przemijającym lub utrzymującym się zmniejszeniem wydalania moczu z powodu niewydolności nerek, całkowita dobowa dawka cefpodoksymu proksetylu powinna być zmniejszona, ponieważ u takich osób może wystąpić wysokie i długotrwałe stężenie antybiotyków w surowicy po zastosowaniu zwykłych dawek. Cefpodoksym, podobnie jak inne cefalosporyny, należy podawać ostrożnie pacjentom otrzymującym jednocześnie silne leki moczopędne. (Widzieć DAWKOWANIE I SPOSÓB PODAWANIA .)
Podobnie jak w przypadku innych antybiotyków, długotrwałe stosowanie proksetylu cefpodoksymu może spowodować przerost drobnoustrojów niewrażliwych. Niezbędna jest powtórna ocena stanu pacjenta. Jeśli podczas leczenia wystąpi nadkażenie, należy podjąć odpowiednie środki.
Przepisywanie VANTIN w przypadku braku potwierdzonego lub silnie podejrzewanego zakażenia bakteryjnego lub wskazania profilaktycznego prawdopodobnie nie przyniesie korzyści pacjentowi i zwiększa ryzyko rozwoju bakterii lekoopornych.
rakotwórczość, mutageneza, upośledzenie płodności
Nie przeprowadzono długoterminowych badań nad karcynogenezą u zwierząt proksetylu cefpodoksymu. Wszystkie badania mutagenezy cefpodoksymu, w tym test Amesa z aktywacją metaboliczną i bez aktywacji metabolicznej, test aberracji chromosomowych, test nieplanowej syntezy DNA, rekombinacja mitotyczna i konwersja genów, test postępującej mutacji genów oraz test mikrojądrowy in vivo, dały wynik negatywny. Nie stwierdzono niekorzystnego wpływu na płodność lub reprodukcję, gdy szczurom podano doustnie dawkę 100 mg/kg/dobę lub mniej (2-krotność dawki dla ludzi w przeliczeniu na mg/m²).
Ciąża
Efekty teratogenne
Proksetyl cefpodoksymu nie wykazywał działania teratogennego ani embriobójczego, gdy był podawany szczurom w trakcie organogenezy w dawkach do 100 mg/kg/dobę (dwukrotność dawki dla ludzi w przeliczeniu na mg/m²) lub królikom w dawkach do 30 mg/kg/dobę (1 -2 razy większa od dawki dla człowieka w przeliczeniu na mg/m²).
Nie ma jednak odpowiednich i dobrze kontrolowanych badań dotyczących stosowania proksetylu cefpodoksymu u kobiet w ciąży. Ponieważ badania reprodukcji na zwierzętach nie zawsze pozwalają przewidzieć reakcję człowieka, lek ten powinien być stosowany w czasie ciąży tylko wtedy, gdy jest to bezwzględnie konieczne.
Praca i dostawa
Proksetylu cefpodoksymu nie badano pod kątem stosowania podczas porodu i porodu. Leczenie należy podawać tylko wtedy, gdy jest to bezwzględnie konieczne.
Matki karmiące
Cefpodoksym przenika do mleka ludzkiego. W badaniu z udziałem 3 kobiet w okresie laktacji stężenia cefpodoksymu w mleku ludzkim wynosiły 0%, 2% i 6% jednoczesnego stężenia w surowicy po 4 godzinach po podaniu doustnym 200 mg proksetylu cefpodoksymu. Po 6 godzinach od podania stężenia wynosiły 0%, 9% i 16% równoczesnych stężeń w surowicy. Ze względu na możliwość wystąpienia poważnych reakcji u niemowląt karmionych piersią, należy podjąć decyzję, czy przerwać karmienie piersią, czy odstawić lek, biorąc pod uwagę znaczenie leku dla matki.
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność u niemowląt w wieku poniżej 2 miesięcy nie zostały ustalone.
Zastosowanie geriatryczne
Spośród 3338 pacjentów w badaniach klinicznych z zastosowaniem wielokrotnych dawek cefpodoksymu proksetylu w postaci tabletek powlekanych, 521 (16%) miało 65 lat i więcej, a 214 (6%) miało 75 lat i więcej. Nie zaobserwowano ogólnych różnic w skuteczności lub bezpieczeństwie pomiędzy pacjentami w podeszłym wieku i młodszymi. U zdrowych osób w podeszłym wieku z prawidłową czynnością nerek okres półtrwania cefpodoksymu w osoczu wynosił średnio 4,2 godziny, a odzysk moczu średnio 21% po podaniu dawki 400 mg co 12 godzin przez 15 dni. Inne parametry farmakokinetyczne pozostały niezmienione w stosunku do obserwowanych u zdrowych młodszych osób.
Dostosowanie dawki u pacjentów w podeszłym wieku z prawidłową czynnością nerek nie jest konieczne.
PRZEDAWKOWAĆ
W badaniach ostrej toksyczności na gryzoniach pojedyncza dawka doustna 5 g/kg nie wywołała działań niepożądanych.
W przypadku poważnej reakcji toksycznej spowodowanej przedawkowaniem, hemodializa lub dializa otrzewnowa mogą pomóc w usunięciu cefpodoksymu z organizmu, zwłaszcza jeśli czynność nerek jest zaburzona.
Objawy toksyczne po przedawkowaniu antybiotyków beta-laktamowych mogą obejmować nudności, wymioty, zaburzenia w nadbrzuszu i biegunkę.
PRZECIWWSKAZANIA
Proksetyl cefpodoksymu jest przeciwwskazany u pacjentów ze stwierdzoną alergią na cefpodoksym lub antybiotyki z grupy cefalosporyn.
FARMAKOLOGIA KLINICZNA
Wchłanianie i wydalanie
Proksetyl cefpodoksymu jest prolekiem wchłanianym z przewodu pokarmowego i deestryfikowanym do aktywnego metabolitu cefpodoksymu. Po podaniu doustnym 100 mg proksetylu cefpodoksymu pacjentom na czczo około 50% podanej dawki cefpodoksymu zostało wchłonięte ogólnoustrojowo. W zalecanym zakresie dawkowania (100 do 400 mg) około 29 do 33% podanej dawki cefpodoksymu było wydalane w postaci niezmienionej z moczem w ciągu 12 godzin. Metabolizm cefpodoksymu in vivo jest minimalny.
Skutki jedzenia
Stopień wchłaniania (średnia wartość AUC) i średnie maksymalne stężenie w osoczu wzrastały, gdy tabletki powlekane podawano z pokarmem. Po podaniu dawki tabletki 200 mg z posiłkiem, AUC było o 21 do 33% wyższe niż w warunkach na czczo, a maksymalne stężenie w osoczu wynosiło średnio 3,1 μg/ml u osób po posiłku w porównaniu z 2,6 μg/ml u osób na czczo. Czas do osiągnięcia maksymalnego stężenia nie różnił się istotnie między osobami po posiłku i na czczo.
Gdy dawka 200 mg zawiesiny była przyjmowana z posiłkiem, stopień wchłaniania (średnia wartość AUC) i średnie maksymalne stężenie w osoczu u osób po posiłku nie różniły się istotnie od osób na czczo, ale szybkość wchłaniania była wolniejsza z posiłkiem (wzrost o 48%). w Tmax).
Farmakokinetyka tabletek powlekanych cefpodoksymu proksetylu
zalecanym zakresie dawkowania (100 do 400 mg) szybkość i stopień wchłaniania cefpodoksymu wykazywały zależność od dawki; Cmax i AUC znormalizowane względem dawki zmniejszały się nawet o 32% wraz ze wzrostem dawki. W zalecanym zakresie dawkowania Tmax wynosił około 2 do 3 godzin, a T½ wahał się od 2,09 do 2,84 godziny. Średnie Cmax wynosiło 1,4 µg/ml dla dawki 100 mg, 2,3 µg/ml dla dawki 200 mg i 3,9 µg/ml dla dawki 400 mg. U pacjentów z prawidłową czynnością nerek nie stwierdzono kumulacji ani istotnych zmian innych parametrów farmakokinetycznych po wielokrotnych dawkach doustnych do 400 mg co 12 godzin.
POZIOMY CEFPODOKSYMU W OSOCZU (mcg/ml) U DOROSŁYCH NACZONYCH PO PODANIEM TABLETKI POWLEKANEJ (pojedyncza dawka)
Farmakokinetyka zawiesiny proksetylu cefpodoksymu
osób dorosłych dawka 100 mg zawiesiny doustnej powodowała średnie maksymalne stężenie cefpodoksymu wynoszące około 1,5 µg/ml (zakres: 1,1 do 2,1 µg/ml), co jest równoważne ze stężeniem odnotowanym po podaniu tabletki 100 mg. Czas do osiągnięcia maksymalnego stężenia w osoczu i pole pod krzywą zależności stężenia w osoczu od czasu (AUC) dla zawiesiny doustnej były również równoważne wartościom uzyskanym po podaniu tabletek powlekanych u dorosłych po podaniu doustnym dawki 100 mg.
Farmakokinetykę cefpodoksymu badano u 29 pacjentów w wieku od 1 do 17 lat. Każdy pacjent otrzymał pojedynczą doustną dawkę 5 mg/kg zawiesiny doustnej cefpodoksymu. Próbki osocza i moczu pobierano przez 12 godzin po podaniu. Poziomy w osoczu zgłoszone w tym badaniu są następujące:
POZIOMY CEFPODOKSYMU W OSOCZU (mcg/ml) U PACJENTÓW NA CZCZO (od 1 do 17 lat) PO PODANIE W ZAWIESIENIU
Dystrybucja
Wiązanie cefpodoksymu z białkami wynosi od 22 do 33% w surowicy i od 21 do 29% w osoczu.
Pęcherz skóry
Po wielokrotnym podawaniu co 12 godzin przez 5 dni 200 mg lub 400 mg proksetylu cefpodoksymu średnie maksymalne stężenie cefpodoksymu w płynie z pęcherzy skórnych wynosiło średnio odpowiednio 1,6 i 2,8 µg/ml. Poziomy cefpodoksymu w płynie z pęcherzy skórnych po 12 godzinach od podania wynosiły średnio 0,2 i 0,4 µg/ml odpowiednio dla schematów dawek wielokrotnych 200 mg i 400 mg.
Tkanka migdałowa
Po podaniu pojedynczej doustnej tabletki powlekanej 100 mg cefpodoksymu proksetylu średnie maksymalne stężenie cefpodoksymu w tkance migdałków wynosiło średnio 0,24 µg/g po 4 godzinach od podania i 0,09 µg/g po 7 godzinach od podania. Równowagę pomiędzy osoczem a tkanką migdałków osiągnięto w ciągu 4 godzin od podania. Nie zgłoszono wykrycia cefpodoksymu w tkance migdałków 12 godzin po podaniu. Wyniki te wykazały, że stężenia cefpodoksymu przekraczały MIC90 dla S. pyogenes przez co najmniej 7 godzin po podaniu 100 mg proksetylu cefpodoksymu.
Tkanka płucna
Po podaniu pojedynczej doustnej tabletki powlekanej cefpodoksymu proksetylu 200 mg, średnie maksymalne stężenie cefpodoksymu w tkance płuc wynosiło średnio 0,63 µg/g po 3 godzinach od podania, 0,52 µg/g po 6 godzinach od podania i 0,19 µg/g 12 godzin po podaniu. Wyniki tego badania wskazują, że cefpodoksym przenika do tkanki płucnej i utrzymuje stężenie leku przez co najmniej 12 godzin po podaniu na poziomach przekraczających MIC90 dla S. pneumoniae i H. influenzae.
CSF
Nie są dostępne odpowiednie dane dotyczące poziomów cefpodoksymu w płynie mózgowo-rdzeniowym.
Skutki zmniejszonej czynności nerek
Eliminacja cefpodoksymu jest zmniejszona u pacjentów z umiarkowanymi do ciężkich zaburzeniami czynności nerek (klirens kreatyniny ŚRODKI OSTROŻNOŚCI oraz DAWKOWANIE I SPOSÓB PODAWANIA .) U osób z łagodnymi zaburzeniami czynności nerek (50 do 80 ml/min klirensu kreatyniny) średni okres półtrwania cefpodoksymu w osoczu wynosił 3,5 godziny. U pacjentów z umiarkowanym (klirens kreatyniny 30 do 49 ml/min) lub ciężkim zaburzeniem czynności nerek (klirens kreatyniny 5 do 29 ml/min) okres półtrwania zwiększył się odpowiednio do 5,9 i 9,8 godziny. Około 23% podanej dawki zostało usunięte z organizmu podczas standardowej 3-godzinnej procedury hemodializy.
Wpływ niewydolności wątroby (marskość)
Wchłanianie było nieco zmniejszone, a eliminacja niezmieniona u pacjentów z marskością wątroby. Średnie T½ i klirens nerkowy cefpodoksymu u pacjentów z marskością wątroby były podobne do tych uzyskanych w badaniach z udziałem zdrowych osób. Wodobrzusze nie wydawały się wpływać na wartości u pacjentów z marskością wątroby. W tej populacji pacjentów nie zaleca się dostosowywania dawki.
Farmakokinetyka u osób w podeszłym wieku
Osoby w podeszłym wieku nie wymagają dostosowania dawkowania, chyba że mają zaburzoną czynność nerek. (Widzieć ŚRODKI OSTROŻNOŚCI .) U zdrowych osób w podeszłym wieku okres półtrwania cefpodoksymu w osoczu wynosił średnio 4,2 godziny (w porównaniu z 3,3 u młodszych osób), a odzysk moczu średnio 21% po podaniu dawki 400 mg co 12 godzin. Inne parametry farmakokinetyczne (Cmax, AUC i Tmax) pozostały niezmienione w stosunku do obserwowanych u zdrowych młodych osób.
Mikrobiologia
Mechanizm akcji
Cefpodoksym jest środkiem bakteriobójczym, który działa poprzez hamowanie syntezy ściany komórkowej bakterii. Cefpodoksym wykazuje aktywność w obecności niektórych beta-laktamaz, zarówno penicylinaz, jak i cefalosporynaz, bakterii Gram-ujemnych i Gram-dodatnich.
Mechanizm oporu
Oporność na cefpodoksym wynika głównie z hydrolizy przez beta-laktamazę, zmiany białek wiążących penicylinę (PBP) i zmniejszonej przepuszczalności.
Wykazano, że cefpodoksym działa na większość izolatów następujących bakterii, zarówno in vitro, jak i w zakażeniach klinicznych, jak opisano w części Wskazania i zastosowanie (1):
Bakterie Gram-dodatnie
Staphylococcus aureus (szczepy wrażliwe na metycylinę, w tym wytwarzające penicylinazy) Staphylococcus saprophyticus Streptococcus pneumoniae (z wyjątkiem izolatów opornych na penicylinę) Streptococcus pyogenes
Bakterie Gram-ujemne
Escherichia coli Klebsiella pneumoniae Proteus mirabilis Haemophilus influenzae (w tym izolaty wytwarzające beta-laktamazę) Moraxella catarrhalis Neisseria gonorrhoeae (w tym izolaty wytwarzające penicylinazę)
Dostępne są następujące dane in vitro, ale ich znaczenie kliniczne nie jest znane. Co najmniej 90 procent następujących mikroorganizmów wykazuje in vitro minimalne stężenie hamujące (MIC) mniejsze lub równe wartości granicznej wrażliwości dla cefpodoksymu. Jednak skuteczność cefpodoksymu w leczeniu zakażeń klinicznych wywoływanych przez te drobnoustroje nie została ustalona w odpowiednich i dobrze kontrolowanych badaniach klinicznych.
Bakterie Gram-dodatnie
Streptococcus agalactiae Streptococcus spp. (Grupy C, F, G)
Bakterie Gram-ujemne
Citrobacter diversus Klebsiella oxytoca Proteus vulgaris Providencia rettgeri Haemophilus parainfluenzae
Beztlenowe bakterie Gram-dodatnie
Peptostreptococcus magnus
Metody badania wrażliwości
Jeśli to możliwe, laboratorium mikrobiologii klinicznej powinno przekazywać lekarzowi wyniki badań wrażliwości in vitro na leki przeciwdrobnoustrojowe stosowane w szpitalach stacjonarnych w formie raportów okresowych opisujących profil wrażliwości patogenów szpitalnych i pozaszpitalnych. Raporty te powinny pomóc lekarzowi w wyborze leku przeciwbakteryjnego do leczenia.
Techniki rozcieńczania
Do określenia minimalnych stężeń hamujących (MIC) środków przeciwdrobnoustrojowych stosuje się metody ilościowe. Te wartości MIC zapewniają oszacowanie wrażliwości bakterii na związki przeciwdrobnoustrojowe. Wartości MIC należy określić przy użyciu znormalizowanej metody badawczej. Wartości MIC należy interpretować zgodnie z kryteriami podanymi w Tabeli 1.
Techniki dyfuzji
Metody ilościowe, które wymagają pomiaru średnic stref, zapewniają również powtarzalne szacunki podatności bakterii na związki przeciwdrobnoustrojowe. Wielkość strefy pozwala oszacować podatność bakterii na związki przeciwdrobnoustrojowe. Wielkość strefy należy określić przy użyciu znormalizowanej metody badawczej. W tej procedurze wykorzystuje się papierowe krążki nasączone 10 µg cefpodoksymu w celu zbadania wrażliwości drobnoustrojów na cefpodoksym. Kryteria interpretacji dyfuzji krążkowej przedstawiono w tabeli 1.
Raport dotyczący podatnych wskazuje, że środek przeciwdrobnoustrojowy prawdopodobnie hamuje wzrost patogenu, jeśli związek przeciwdrobnoustrojowy osiąga stężenie w miejscu zakażenia niezbędne do zahamowania wzrostu patogenu. Raport o poziomie pośrednim wskazuje, że wynik należy uznać za niejednoznaczny, a jeśli drobnoustrój nie jest w pełni wrażliwy na alternatywne, klinicznie możliwe do zastosowania leki, badanie należy powtórzyć. Ta kategoria implikuje możliwość zastosowania klinicznego w miejscach ciała, w których lek jest stężony fizjologicznie lub w sytuacjach, w których można stosować duże dawki leku. Ta kategoria zapewnia również strefę buforową, która zapobiega powodowaniu poważnych rozbieżności w interpretacji przez małe, niekontrolowane czynniki techniczne. Raport o odporności wskazuje, że środek przeciwdrobnoustrojowy prawdopodobnie nie będzie hamował wzrostu patogenu, jeśli związek przeciwdrobnoustrojowy osiągnie stężenia zwykle osiągalne w miejscu zakażenia; należy wybrać inną terapię.
Kontrola jakości
Znormalizowane procedury badania wrażliwości wymagają stosowania laboratoryjnych kontroli w celu monitorowania i zapewnienia dokładności i precyzji materiałów eksploatacyjnych i odczynników stosowanych w teście, a także technik osoby wykonującej badanie1,2,3. Standardowy proszek cefpodoksymu powinien zapewniać następujący zakres wartości MIC przedstawiony w Tabeli 2. W przypadku techniki dyfuzyjnej z użyciem krążka 10 mcg należy spełnić kryteria z Tabeli 2.
Badania kliniczne
Zapalenie pęcherza
W dwóch podwójnie zaślepionych, randomizowanych badaniach porównawczych 2:1 przeprowadzonych u dorosłych w Stanach Zjednoczonych, cefpodoksym proksetyl porównywano z innymi antybiotykami beta-laktamowymi. W tych badaniach uzyskano następujące wskaźniki eradykacji bakterii po 5 do 9 dniach po terapii:
badaniach tych wskaźniki wyleczeń klinicznych i eradykacji bakterii dla proksetylu cefpodoksymu były porównywalne z lekami porównawczymi; jednak wskaźniki wyleczeń klinicznych i eradykacji bakteriologicznej były niższe niż obserwowane w przypadku niektórych innych klas zatwierdzonych leków na zapalenie pęcherza moczowego.
Badania nad ostrym zapaleniem ucha środkowego
W kontrolowanych badaniach ostrego zapalenia ucha środkowego przeprowadzonych w Stanach Zjednoczonych, w których stwierdzono znaczny odsetek drobnoustrojów wytwarzających betalaktamazę, proksetyl cefpodoksymu porównywano z cefiksymem. W tych badaniach, stosując bardzo ścisłe kryteria oceny oraz kryteria odpowiedzi mikrobiologicznej i klinicznej w okresie obserwacji 4 do 21 dni po terapii, uzyskano następujące przypuszczalne wyniki w zakresie eradykacji bakterii/sukcesu klinicznego (wyleczenie i poprawa).
BIBLIOGRAFIA
1. Instytut Norm Klinicznych i Laboratoryjnych (CLSI). Metody rozcieńczeń Testy wrażliwości drobnoustrojów na bakterie, które rosną w warunkach tlenowych; Zatwierdzony standard — wydanie dziewiąte. Dokument CLSI M07-A9, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pensylwania 19087, USA, 2012.
2. Instytut Norm Klinicznych i Laboratoryjnych (CLSI). Normy wydajności dla badań wrażliwości na środki przeciwdrobnoustrojowe; Dwudziesty Trzeci Suplement Informacyjny, dokument CLSI M100-S23. Dokument CLSI M100-S23, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pensylwania 19087, USA, 2013.
3. Instytut Norm Klinicznych i Laboratoryjnych (CLSI). Normy wydajności dla testów podatności na dyfuzję przeciwdrobnoustrojową; Approved Standard — jedenasta edycja dokumentu CLSI M02-A11, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pensylwania 19087, USA, 2012.
INFORMACJA O PACJENCIE
Pacjentów należy pouczyć, że leki przeciwbakteryjne, w tym VANTIN, należy stosować wyłącznie w leczeniu zakażeń bakteryjnych. Nie leczą infekcji wirusowych (np. przeziębienia). Kiedy VANTIN jest przepisywany w celu leczenia infekcji bakteryjnej, pacjentom należy poinformować, że chociaż często czuje się lepiej na początku leczenia, lek należy przyjmować dokładnie zgodnie z zaleceniami. Pomijanie dawek lub nieukończenie pełnego cyklu leczenia może (1) zmniejszyć skuteczność natychmiastowego leczenia i (2) zwiększyć prawdopodobieństwo, że bakterie rozwiną oporność i nie będą mogły być wyleczone za pomocą VANTIN lub innych leków przeciwbakteryjnych w przyszłości.
Biegunka jest częstym problemem powodowanym przez antybiotyki, który zwykle kończy się wraz z odstawieniem antybiotyku. Czasami po rozpoczęciu leczenia antybiotykami u pacjentów mogą pojawić się wodniste i krwawe stolce (ze skurczami żołądka i gorączką lub bez), nawet po dwóch lub więcej miesiącach od przyjęcia ostatniej dawki antybiotyku. W takim przypadku pacjenci powinni jak najszybciej skontaktować się z lekarzem.
