Zyvox 600mg Linezolid Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Zyvox 600mg i jak się go stosuje?
Zyvox to lek na receptę stosowany w leczeniu objawów infekcji bakteryjnych, takich jak zapalenie płuc, infekcje skóry i infekcje oporne na inne antybiotyki. Zyvox 600 mg może być stosowany samodzielnie lub z innymi lekami.
Zyvox należy do klasy leków o nazwie Antybiotyki, Inne; Oksazolidynony.
Nie wiadomo, czy Zyvox jest bezpieczny i skuteczny u dzieci.
Jakie są możliwe skutki uboczne leku Zyvox?
Zyvox może powodować poważne działania niepożądane, w tym:
- pokrzywka,
- trudności w oddychaniu,
- obrzęk twarzy lub gardła,
- ciężka reakcja skórna,
- gorączka,
- ból gardła,
- płonące oczy,
- ból skóry,
- czerwona lub fioletowa wysypka skórna z powstawaniem pęcherzy i łuszczeniem się,
- Problemy ze wzrokiem,
- zmiany w Twojej wizji,
- silny ból brzucha,
- biegunka wodnista lub krwawa,
- drgawki,
- wyzysk,
- uczucie niepokoju lub drżenia,
- podniecenie,
- halucynacje,
- gorączka,
- dreszcze,
- szybkie tętno,
- sztywność mięśni,
- drganie,
- utrata koordynacji,
- mdłości,
- wymioty,
- biegunka,
- nietypowy ból mięśni,
- problemy z oddychaniem,
- ból brzucha,
- nieregularne tętno,
- zawroty głowy,
- uczucie zimna,
- uczucie osłabienia lub zmęczenia,
- dezorientacja,
- owrzodzenia jamy ustnej,
- owrzodzenia skóry,
- łatwe siniaki,
- nietypowe krwawienie,
- blada skóra,
- zimne dłonie i stopy,
- zawroty głowy i
- duszność
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze działania niepożądane leku Zyvox to:
- mdłości,
- wymioty,
- biegunka,
- łagodna wysypka skórna,
- niedokrwistość (niski poziom czerwonych krwinek),
- ból głowy i
- zawroty głowy
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe działania niepożądane leku Zyvox. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OPIS
ZYVOX 600 mg do wstrzykiwań dożylnych, tabletki ZYVOX i ZYVOX do sporządzania zawiesiny doustnej zawierają linezolid, który jest syntetycznym środkiem przeciwbakteryjnym z klasy oksazolidynonów. Nazwa chemiczna linezolidu to (S)-N-[[3-[3-Fluoro-4-(4morfolinylo)fenylo]-2-okso-5-oksazolidynylo]metylo]-acetamid.
Wzór empiryczny to C16H20FN3O4. Jego masa cząsteczkowa wynosi 337,35, a jego strukturę chemiczną przedstawiono poniżej:
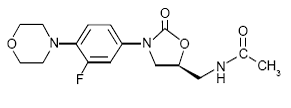
ZYVOX 600 mg IV Injection jest dostarczany w postaci gotowego do użycia sterylnego izotonicznego roztworu do infuzji dożylnej. Każdy ml zawiera 2 mg linezolidu. Nieaktywnymi składnikami są cytrynian sodu, kwas cytrynowy i dekstroza w wodnym nośniku do podawania dożylnego. Zawartość sodu (Na+) wynosi 0,38 mg/ml (5 mEq/300-ml worek i 1,7 mEq/100-ml worek).
Tabletka ZYVOX do podawania doustnego zawiera 600 mg linezolidu w postaci sprasowanej tabletki powlekanej. Składniki nieaktywne to skrobia kukurydziana, celuloza mikrokrystaliczna, hydroksypropyloceluloza, glikolan sodowy skrobi, stearynian magnezu, hypromeloza, glikol polietylenowy, dwutlenek tytanu i wosk Carnauba. Zawartość sodu (Na+) wynosi 2,92 mg na tabletkę 600 mg (0,1 mEq/tabletkę).
ZYVOX 600 mg do sporządzania zawiesiny doustnej jest dostarczany w postaci granulatu/proszku o smaku pomarańczowym do sporządzania zawiesiny do podawania doustnego. Po przygotowaniu każde 5 ml zawiera 100 mg linezolidu. Składniki nieaktywne to sacharoza, kwas cytrynowy, cytrynian sodu, celuloza mikrokrystaliczna i sól sodowa karboksymetylocelulozy, aspartam, guma ksantanowa, mannitol, benzoesan sodu, koloidalny dwutlenek krzemu, chlorek sodu i aromaty [patrz INFORMACJA O PACJENCIE ]. Zawartość sodu (Na+) wynosi 8,52 mg/5 ml (0,4 mEq/5 ml).
WSKAZANIA
Szpitalne zapalenie płuc
ZYVOX jest wskazany w leczeniu szpitalnego zapalenia płuc wywołanego przez Staphylococcus aureus (izolaty wrażliwe i oporne na metycylinę) lub Streptococcus pneumoniae [patrz Studia kliniczne ].
Pozaszpitalne zapalenie płuc
ZYVOX 600 mg jest wskazany w leczeniu pozaszpitalnego zapalenia płuc wywołanego przez Streptococcus pneumoniae, w tym przypadków ze współistniejącą bakteriemią lub Staphylococcus aureus (wyłącznie izolaty wrażliwe na metycylinę) [patrz Studia kliniczne ].
Skomplikowane infekcje skóry i struktury skóry
ZYVOX 600 mg jest wskazany w leczeniu skomplikowanych zakażeń skóry i struktury skóry, w tym zakażeń stopy cukrzycowej, bez współistniejącego zapalenia kości i szpiku, wywołanych przez Staphylococcus aureus (izolaty wrażliwe i oporne na metycylinę), Streptococcus pyogenes lub Streptococcus agalactiae. ZYVOX nie był badany w leczeniu odleżyn [patrz Studia kliniczne ].
Nieskomplikowane infekcje skóry i struktury skóry
ZYVOX 600 mg jest wskazany w leczeniu niepowikłanych zakażeń skóry i struktur skóry wywołanych przez Staphylococcus aureus (tylko izolaty wrażliwe na metycylinę) lub Streptococcus pyogenes [patrz Studia kliniczne ].
Zakażenia Enterococcus faecium oporne na wankomycynę
ZYVOX 600 mg jest wskazany w leczeniu zakażeń Enterococcus faecium opornych na wankomycynę, w tym przypadków ze współistniejącą bakteriemią [patrz Studia kliniczne ].
Ograniczenia użytkowania
- ZYVOX 600 mg nie jest wskazany do leczenia zakażeń Gram-ujemnych. Niezwykle ważne jest natychmiastowe rozpoczęcie swoistej terapii Gram-ujemnej w przypadku udokumentowania lub podejrzenia współistniejącego patogenu Gram-ujemnego [patrz OSTRZEŻENIA I ŚRODKI ].
- Bezpieczeństwo i skuteczność preparatów ZYVOX 600 mg podawanych przez okres dłuższy niż 28 dni nie były oceniane w kontrolowanych badaniach klinicznych [patrz Studia kliniczne ].
Stosowanie
Aby ograniczyć rozwój bakterii opornych na leki i utrzymać skuteczność preparatu ZYVOX 600 mg i innych leków przeciwbakteryjnych, preparat ZYVOX należy stosować wyłącznie w leczeniu lub zapobieganiu zakażeniom, co do których udowodniono, lub co do których istnieje silne podejrzenie, że są wywołane przez wrażliwe bakterie. Gdy dostępne są informacje dotyczące hodowli i wrażliwości, należy je uwzględnić przy wyborze lub modyfikacji terapii przeciwbakteryjnej. W przypadku braku takich danych, lokalna epidemiologia i wzorce podatności mogą przyczynić się do empirycznego doboru terapii.
DAWKOWANIE I SPOSÓB PODAWANIA
Ogólne dawkowanie i administracja
Zalecane dawkowanie preparatów ZYVOX 600 mg do leczenia zakażeń przedstawiono w Tabeli 1.
Zmiana dawki z podawania dożylnego na doustne nie jest konieczna.
Administracja dożylna
ZYVOX 600 mg IV Injection jest dostarczany w jednodawkowych, gotowych do użycia workach infuzyjnych. Produkty lecznicze do podawania pozajelitowego należy przed podaniem skontrolować wzrokowo pod kątem obecności cząstek stałych. Sprawdź, czy nie ma drobnych przecieków, mocno ściskając worek. W przypadku wykrycia przecieków roztwór należy wyrzucić, ponieważ może to pogorszyć sterylność. Przechowywać worki infuzyjne w opakowaniu do czasu użycia. Przechowywać w temperaturze pokojowej. Chronić przed zamarzaniem. ZYVOX 600 mg IV Iniekcja może wykazywać żółty kolor, który może nasilać się w czasie bez negatywnego wpływu na moc.
Produkt ZYVOX IV należy podawać we wlewie dożylnym trwającym od 30 do 120 minut. Nie należy używać tego worka do infuzji dożylnej w połączeniu szeregowym. Do tego roztworu nie należy wprowadzać dodatków. Jeśli ZYVOX 600 mg dożylnie ma być podawany jednocześnie z innym lekiem, każdy lek należy podawać oddzielnie, zgodnie z zalecaną dawką i drogą podania dla każdego produktu. Wyrzucić niewykorzystaną część.
Jeśli ta sama linia dożylna jest używana do sekwencyjnej infuzji kilku leków, należy ją przepłukać przed i po infuzji produktu ZYVOX IV do wstrzykiwań roztworem do infuzji zgodnym z produktem ZYVOX 600 mg IV do wstrzykiwań i dowolnym innym lekiem podawanym przez tę wspólną linię. .
Kompatybilność
Kompatybilne roztwory dożylne obejmują 0,9% chlorek sodu do wstrzykiwań USP, 5% dekstrozę do wstrzykiwań USP i zastrzyk Ringera z dodatkiem mleczanu USP.
Niezgodności
Niezgodności fizyczne wystąpiły, gdy ZYVOX 600 mg dożylnie został połączony z następującymi lekami podczas symulowanego podawania w miejscu Y: amfoterycyna B, chlorpromazyna HCl, diazepam, izotionian pentamidyny, laktobionian erytromycyny, sól sodowa fenytoiny i trimetoprym-sulfametoksazol. Dodatkowo wystąpiła niezgodność chemiczna, gdy ZYVOX IV Injection połączono z ceftriaksonem sodowym.
Konstytucja Zawieszenia Ustnego
ZYVOX do sporządzania zawiesiny doustnej jest dostarczany w postaci proszku/granulek do sporządzania zawiesiny. Delikatnie postukaj w butelkę, aby rozpuścić proszek. Dodać łącznie 123 ml wody destylowanej w dwóch porcjach. Po dodaniu pierwszej połowy energicznie wstrząśnij, aby zwilżyć cały proszek. Następnie dodaj drugą połowę wody i energicznie wstrząśnij, aby uzyskać jednolitą zawiesinę. Po przygotowaniu każde 5 ml zawiesiny zawiera 100 mg linezolidu. Przed użyciem delikatnie wymieszaj, odwracając butelkę 3 do 5 razy. Nie wstrząsaj. Przechowywać w postaci zawiesiny w temperaturze pokojowej. Zużyć w ciągu 21 dni po utworzeniu.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
ZYVOX 600 mg IV Iniekcja: 200 mg/100 ml (2 mg/ml) i 600 mg/300 ml (2 mg/ml) linezolidu w pojedynczej dawce, gotowe do użycia, elastyczne plastikowe worki infuzyjne w laminowanej folii.
Tabletka ZYVOX 600 mg:
biała tabletka powlekana w kształcie kapsułki z wytłoczonym napisem „ZYV” po jednej stronie i „600” po drugiej. ZYVOX 600 mg do sporządzania zawiesiny doustnej: suchy, biały lub prawie biały granulat/proszek o smaku pomarańczowym. Po utworzeniu zgodnie z zaleceniami, każda butelka będzie zawierać 150 ml zawiesiny zapewniającej równowartość 100 mg linezolidu na każde 5 ml.
Składowania i stosowania
Zastrzyk
ZYVOX 600 mg dożylnie Urządzenie do wstrzykiwania jest dostępne w jednodawkowych, gotowych do użycia, elastycznych plastikowych workach infuzyjnych w laminowanej folii. Worki i porty infuzyjne nie są wykonane z lateksu kauczuku naturalnego. Worki infuzyjne są dostępne w następujących wielkościach opakowań:
200 mg/100 ml (2 mg/ml) linezolid x 10 - NDC 0009-5137-04 600 mg/300 ml (2 mg/ml) linezolid x 10 - NDC 0009-5140-04
Tablety
Tabletki ZYVOX 600 mg są dostępne w następujący sposób:
600 mg (białe tabletki powlekane w kształcie kapsułki z wytłoczonym napisem „ZYV” po jednej stronie i „600” po drugiej)
20 tabletek w butelce HDPE - NDC 0009-5138-02 Opakowania jednostkowe po 30 tabletek - NDC 0009-5138-03
Zawiesina doustna
ZYVOX do doustnego zawieszenia jest dostępny w postaci suchej, białej do białawej, granulki/proszku o smaku pomarańczowym. Po utworzeniu zgodnie z zaleceniami, każda butelka będzie zawierać 150 ml zawiesiny zapewniającej równowartość 100 mg linezolidu na każde 5 ml. ZYVOX do zawiesiny doustnej jest dostarczany w następujący sposób:
100 mg/5 ml w szklanych butelkach 240 ml — NDC 0009-5136-01
Składowania i stosowania
Przechowywać w temperaturze 25°C (77°F). Chronić przed światłem. Butelki przechowywać szczelnie zamknięte w celu ochrony przed wilgocią. Zaleca się przechowywanie worków infuzyjnych w opakowaniu do czasu użycia. Worki infuzyjne chronić przed zamarzaniem.
Dystrybucja: Pharmacia & Upjohn Co Division firmy Pfizer Inc, NY, NY 10017. Aktualizacja: listopad 2021.
SKUTKI UBOCZNE
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Dorośli ludzie
Bezpieczeństwo preparatów ZYVOX 600 mg oceniono u 2046 dorosłych pacjentów włączonych do siedmiu kontrolowanych badań klinicznych fazy 3 z grupą kontrolną, których leczono przez okres do 28 dni.
Spośród pacjentów leczonych z powodu niepowikłanych zakażeń skóry i struktury skóry (uSSSI), u 25,4% pacjentów leczonych preparatem ZYVOX i 19,6% pacjentów leczonych produktem porównawczym wystąpiło co najmniej jedno zdarzenie niepożądane związane z lekiem. We wszystkich innych wskazaniach u 20,4% pacjentów leczonych preparatem ZYVOX i u 14,3% pacjentów leczonych produktem porównawczym wystąpiło co najmniej jedno zdarzenie niepożądane związane z lekiem.
W Tabeli 2 przedstawiono częstość występowania wszystkich przyczyn, związanych z leczeniem działań niepożądanych, zgłoszonych u co najmniej 1% dorosłych pacjentów w tych badaniach, według dawki produktu ZYVOX.
Spośród pacjentów leczonych z powodu uSSSI 3,5% pacjentów leczonych preparatem ZYVOX i 2,4% pacjentów leczonych lekiem porównawczym przerwało leczenie z powodu działań niepożądanych związanych z lekiem. We wszystkich innych wskazaniach przerwanie leczenia z powodu działań niepożądanych związanych z lekiem wystąpiło u 2,1% pacjentów leczonych preparatem ZYVOX i 1,7% pacjentów leczonych lekiem porównawczym. Najczęściej zgłaszanymi zdarzeniami niepożądanymi związanymi z lekiem, które doprowadziły do przerwania leczenia, były nudności, ból głowy, biegunka i wymioty.
Pacjenci pediatryczni
Bezpieczeństwo preparatów ZYVOX oceniano u 215 pacjentów pediatrycznych w wieku od urodzenia do 11 lat oraz u 248 pacjentów w wieku od 5 do 17 lat (146 z nich 248 było w wieku od 5 do 11 lat, a 102 było w wieku od 12 do 17 lat). Pacjenci ci zostali włączeni do dwóch kontrolowanych porównawczych badań klinicznych fazy 3 i byli leczeni przez okres do 28 dni. W badaniu hospitalizowanych pacjentów pediatrycznych (od urodzenia do 11 lat) z zakażeniami Gram-dodatnimi, którzy zostali zrandomizowani 2 do 1 (linezolid:wankomycyna), śmiertelność wyniosła 6,0% (13/215) w ramieniu z linezolidem i 3,0% (3/101) w ramieniu wankomycyny. Jednak biorąc pod uwagę ciężką chorobę podstawową w populacji pacjentów, nie można było ustalić związku przyczynowego.
Spośród pacjentów pediatrycznych leczonych z powodu uSSSI, 19,2% pacjentów leczonych preparatem ZYVOX i 14,1% pacjentów leczonych lekiem porównawczym doświadczyło co najmniej jednego zdarzenia niepożądanego związanego z lekiem. We wszystkich innych wskazaniach u 18,8% pacjentów leczonych preparatem ZYVOX i 34,3% pacjentów leczonych produktem porównawczym wystąpiło co najmniej jedno zdarzenie niepożądane związane z lekiem.
Tabeli 3 przedstawiono częstość występowania działań niepożądanych wynikających z jakiejkolwiek przyczyny, związanych z leczeniem, zgłoszonych u ponad 1% pacjentów pediatrycznych (i więcej niż 1 pacjenta) w każdej z leczonych grup w kontrolowanych badaniach fazy III z grupą kontrolną.
Spośród pacjentów pediatrycznych leczonych z powodu uSSSI 1,6% pacjentów leczonych preparatem ZYVOX i 2,4% pacjentów leczonych lekiem porównawczym przerwało leczenie z powodu działań niepożądanych związanych z lekiem. We wszystkich innych wskazaniach przerwanie leczenia z powodu działań niepożądanych związanych z lekiem wystąpiło u 0,9% pacjentów leczonych preparatem ZYVOX i 6,1% pacjentów leczonych lekiem porównawczym.
Nieprawidłowości laboratoryjne
Preparat ZYVOX był związany z małopłytkowością, gdy był stosowany w dawkach do 600 mg włącznie co 12 godzin przez okres do 28 dni. W kontrolowanych badaniach fazy III z grupą kontrolną odsetek dorosłych pacjentów, u których rozwinęła się istotnie mała liczba płytek krwi (definiowana jako mniej niż 75% dolnej granicy normy i (lub) wartości wyjściowej) wynosił 2,4% (zakres między badaniami: 0,3 do 10,0%) z ZYVOX 600 mg i 1,5% (zakres między badaniami: 0,4 do 7,0%) z komparatorem. W badaniu hospitalizowanych pacjentów pediatrycznych w wieku od urodzenia do 11 lat odsetek pacjentów, u których rozwinęła się istotnie niska liczba płytek krwi (definiowana jako mniej niż 75% dolnej granicy normy i (lub) wartości wyjściowej) wynosił 12,9% po podaniu produktu ZYVOX 600 mg. i 13,4% z wankomycyną. W badaniu ambulatoryjnym z udziałem dzieci w wieku od 5 do 17 lat odsetek pacjentów, u których rozwinęła się istotnie mała liczba płytek krwi, wynosił 0% w przypadku ZYVOX i 0,4% w przypadku cefadroksylu. Małopłytkowość związana ze stosowaniem preparatu ZYVOX wydaje się zależeć od czasu trwania leczenia (na ogół dłuższego niż 2 tygodnie leczenia). Liczba płytek krwi u większości pacjentów powróciła do normalnego zakresu/wyjściowej wartości w okresie obserwacji. W badaniach klinicznych III fazy u pacjentów z małopłytkowością nie zidentyfikowano żadnych powiązanych klinicznych zdarzeń niepożądanych. Krwawienia zostały zidentyfikowane u pacjentów z trombocytopenią w programie współczucia dla ZYVOX; nie można określić roli linezolidu w tych zdarzeniach [patrz OSTRZEŻENIA I ŚRODKI ].
Zmiany obserwowane w innych parametrach laboratoryjnych, bez względu na związek z lekiem, nie ujawniły istotnych różnic między preparatem ZYVOX 600 mg a lekami porównawczymi. Zmiany te na ogół nie były istotne klinicznie, nie prowadziły do przerwania terapii i były odwracalne. Częstość występowania u pacjentów dorosłych i pediatrycznych z co najmniej jedną istotnie nieprawidłową wartością parametrów hematologicznych lub biochemicznych surowicy przedstawiono w tabelach 4, 5, 6 i 7.
Doświadczenie postmarketingowe
Następujące działania niepożądane zostały zidentyfikowane po zatwierdzeniu produktu ZYVOX. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z narażeniem na lek:
- Mielosupresja (w tym niedokrwistość, leukopenia, pancytopenia i trombocytopenia) [patrz OSTRZEŻENIA I ŚRODKI ]; niedokrwistość syderoblastyczna.
- Neuropatia obwodowa i neuropatia nerwu wzrokowego czasami przechodząca w utratę wzroku [patrz OSTRZEŻENIA I ŚRODKI ].
- Kwasica mleczanowa [patrz OSTRZEŻENIA I ŚRODKI ]. Chociaż zgłoszenia te dotyczyły głównie pacjentów leczonych przez okres dłuższy niż maksymalny zalecany okres 28 dni, zdarzenia te zgłaszano również u pacjentów otrzymujących krótsze cykle leczenia.
- Zespół serotoninowy zgłaszano u pacjentów otrzymujących jednocześnie leki serotoninergiczne, w tym leki przeciwdepresyjne, takie jak selektywne inhibitory wychwytu zwrotnego serotoniny (SSRI) i opioidy oraz ZYVOX [patrz OSTRZEŻENIA I ŚRODKI ].
- Drgawki [patrz OSTRZEŻENIA I ŚRODKI ].
- Anafilaksja, obrzęk naczynioruchowy, pęcherzowe zaburzenia skóry, w tym ciężkie skórne reakcje niepożądane (SCAR), takie jak martwica toksyczno-rozpływna naskórka i zespół Stevensa-Johnsona oraz zapalenie naczyń z nadwrażliwości.
- Po zastosowaniu linezolidu zgłaszano powierzchowne przebarwienia zębów i języka. Przebarwienia zęba można było usunąć po profesjonalnym oczyszczeniu zębów (ręczne odkamienianie) w przypadkach o znanym wyniku.
- Hipoglikemia, w tym epizody objawowe [patrz OSTRZEŻENIA I ŚRODKI ].
- Hiponatremia i/lub zespół nieprawidłowego wydzielania hormonu antydiuretycznego (SIADH) [patrz OSTRZEŻENIA I ŚRODKI ].
INTERAKCJE Z LEKAMI
Inhibitory monoaminooksydazy
Linezolid jest odwracalnym, nieselektywnym inhibitorem monoaminooksydazy [patrz PRZECIWWSKAZANIA oraz FARMAKOLOGIA KLINICZNA ].
Środki adrenergiczne i serotoninergiczne
Linezolid może wchodzić w interakcje z lekami adrenergicznymi i serotoninergicznymi [patrz OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
OSTRZEŻENIA
Zawarte jako część "ŚRODKI OSTROŻNOŚCI" Sekcja
ŚRODKI OSTROŻNOŚCI
Mielosupresja
pacjentów otrzymujących linezolid zgłaszano mielosupresję (w tym niedokrwistość, leukopenię, pancytopenię i małopłytkowość). W przypadkach, gdy wynik jest znany, po odstawieniu linezolidu zmienione parametry hematologiczne wzrosły do poziomu sprzed leczenia. U pacjentów otrzymujących linezolid, szczególnie u tych, którzy otrzymują linezolid dłużej niż dwa tygodnie, z istniejącą wcześniej mielosupresją, otrzymujących jednocześnie leki powodujące zahamowanie czynności szpiku kostnego lub u pacjentów z przewlekłą infekcją, u których występuje otrzymywał wcześniej lub jednocześnie stosował leki przeciwbakteryjne. Należy rozważyć przerwanie leczenia linezolidem u pacjentów, u których doszło do rozwoju lub nasilenia mielosupresji.
Neuropatia obwodowa i wzrokowa
Neuropatie obwodowe i nerwu wzrokowego zgłaszano u pacjentów leczonych produktem ZYVOX 600 mg, głównie u pacjentów leczonych przez okres dłuższy niż maksymalny zalecany czas trwania wynoszący 28 dni. W przypadkach neuropatii nerwu wzrokowego, która rozwinęła się do utraty wzroku, pacjenci byli leczeni przez dłuższy czas, przekraczający maksymalny zalecany czas trwania. U niektórych pacjentów leczonych preparatem ZYVOX przez mniej niż 28 dni zgłaszano niewyraźne widzenie. U dzieci zgłaszano również neuropatię obwodową i nerwu wzrokowego.
Jeśli u pacjentów wystąpią objawy upośledzenia wzroku, takie jak zmiany ostrości wzroku, zmiany w widzeniu kolorów, niewyraźne widzenie lub ubytki pola widzenia, zaleca się szybką ocenę okulistyczną. Czynność wzroku należy monitorować u wszystkich pacjentów przyjmujących preparat ZYVOX przez dłuższy czas (≥ 3 miesiące) oraz u wszystkich pacjentów zgłaszających nowe objawy wzrokowe, niezależnie od długości leczenia preparatem ZYVOX. Jeśli wystąpi neuropatia obwodowa lub nerwu wzrokowego, należy rozważyć dalsze stosowanie produktu ZYVOX 600 mg u tych pacjentów z potencjalnym ryzykiem.
Zespół serotoninowy
Zgłaszano spontaniczne zgłoszenia zespołu serotoninowego, w tym przypadki śmiertelne związane ze równoczesnym podawaniem produktu ZYVOX i leków serotoninergicznych, w tym leków przeciwdepresyjnych, takich jak selektywne inhibitory wychwytu zwrotnego serotoniny (SSRI).
Linezolidu nie należy podawać pacjentom z zespołem rakowiaka i (lub) pacjentom przyjmującym którykolwiek z poniższych leków, chyba że jest to klinicznie uzasadnione i pacjenci są uważnie obserwowani pod kątem objawów przedmiotowych i (lub) objawów zespołu serotoninowego lub złośliwych reakcji neuroleptycznych podobnych do zespołu neuroleptycznego (NMS). : inhibitory wychwytu zwrotnego serotoniny, trójpierścieniowe leki przeciwdepresyjne, bupropion, buspiron, agoniści receptora serotoninowego 5-HT1 (tryptany) oraz opioidy, w tym meperydyna [patrz INTERAKCJE Z LEKAMI oraz FARMAKOLOGIA KLINICZNA ].
niektórych przypadkach pacjent już otrzymujący serotoninergiczny lek przeciwdepresyjny lub buspiron może wymagać pilnego leczenia linezolidem. Jeśli alternatywy dla linezolidu nie są dostępne, a potencjalne korzyści ze stosowania linezolidu przewyższają ryzyko wystąpienia zespołu serotoninowego lub reakcji podobnych do NMS, należy niezwłocznie przerwać stosowanie serotoninergicznego leku przeciwdepresyjnego i podać linezolid. Pacjenta należy monitorować przez dwa tygodnie (pięć tygodni w przypadku przyjmowania fluoksetyny) lub do 24 godzin po podaniu ostatniej dawki linezolidu, w zależności od tego, co nastąpi wcześniej. Objawy zespołu serotoninowego lub reakcji podobnych do NMS obejmują hipertermię, sztywność mięśni, mioklonie, niestabilność autonomiczną i zmiany stanu psychicznego obejmujące skrajne pobudzenie przechodzące w majaczenie i śpiączkę. Pacjenta należy również monitorować pod kątem objawów odstawiennych leku przeciwdepresyjnego (patrz ulotka dołączona do opakowania określonego leku (opis związanych z nim objawów odstawiennych).
Brak równowagi śmiertelności w badaniu badawczym u pacjentów z zakażeniami krwi związanymi z cewnikiem, w tym z zakażeniami w miejscu cewnika
Brak równowagi w śmiertelności zaobserwowano u pacjentów leczonych linezolidem w porównaniu z wankomycyną/dikloksacyliną/oksacyliną w otwartym badaniu z udziałem ciężko chorych pacjentów z zakażeniami wewnątrznaczyniowym związanymi z cewnikiem [78/363 (21,5%) vs. 58/363 (16,0%) ); iloraz szans 1,426, 95% CI 0,970, 2,098]. Chociaż przyczyna nie została ustalona, ta obserwowana nierównowaga wystąpiła głównie u pacjentów leczonych linezolidem, u których na początku badania nie wykryto patogenów Gram-ujemnych, mieszanych patogenów Gram-ujemnych i Gram-dodatnich lub nie stwierdzono żadnego patogenu, ale nie zaobserwowano go u pacjentów z Tylko infekcje Gram-dodatnie.
Linezolid nie jest zatwierdzony i nie powinien być stosowany w leczeniu pacjentów z zakażeniami krwi związanymi z cewnikiem lub zakażeniami w miejscu cewnika.
Linezolid nie wykazuje działania klinicznego na patogeny Gram-ujemne i nie jest wskazany w leczeniu zakażeń Gram-ujemnych. Niezwykle ważne jest natychmiastowe rozpoczęcie swoistej terapii Gram-ujemnej w przypadku udokumentowania lub podejrzenia współistniejącego patogenu Gram-ujemnego [patrz WSKAZANIA ].
Biegunka wywołana przez Clostridioides
Przy stosowaniu prawie wszystkich leków przeciwbakteryjnych, w tym ZYVOX 600 mg, zgłaszano występowanie biegunki związanej z Clostridioides difficile (CDAD), której nasilenie może wahać się od łagodnej biegunki do zapalenia okrężnicy zakończonego zgonem. Leczenie środkami przeciwbakteryjnymi zmienia normalną florę okrężnicy, prowadząc do przerostu C. difficile.
C. difficile wytwarza toksyny A i B, które przyczyniają się do rozwoju CDAD. Szczepy C. difficile wytwarzające hipertoksyny powodują zwiększoną zachorowalność i śmiertelność, ponieważ zakażenia te mogą być oporne na leczenie przeciwbakteryjne i mogą wymagać kolektomii. CDAD należy rozważyć u wszystkich pacjentów, u których po zastosowaniu leków przeciwbakteryjnych wystąpi biegunka.
Konieczna jest staranna historia choroby, ponieważ donoszono, że CDAD występuje w ciągu dwóch miesięcy po podaniu leków przeciwbakteryjnych.
W przypadku podejrzenia lub potwierdzenia CDAD, może być konieczne przerwanie stosowania leków przeciwbakteryjnych, które nie są skierowane przeciwko C. difficile. Zgodnie ze wskazaniami klinicznymi należy wdrożyć odpowiednią gospodarkę wodno-elektrolitową, suplementację białka, leczenie przeciwbakteryjne C. difficile oraz ocenę chirurgiczną.
Potencjalne interakcje powodujące podwyższenie ciśnienia krwi
Linezolidu nie należy podawać pacjentom z niekontrolowanym nadciśnieniem tętniczym, guzem chromochłonnym, tyreotoksykozą i/lub pacjentom przyjmującym którykolwiek z następujących rodzajów leków: leki sympatykomimetyczne działające bezpośrednio lub pośrednio (np. pseudoefedryna), środki wazopresyjne (np. epinefryna, norepinefryna), środki dopaminergiczne (np. dopamina, dobutamina) [patrz INTERAKCJE Z LEKAMI oraz FARMAKOLOGIA KLINICZNA ].
Kwasica mleczanowa
Podczas stosowania preparatu ZYVOX zgłaszano kwasicę mleczanową. W zgłoszonych przypadkach pacjenci doświadczali powtarzających się epizodów nudności i wymiotów. Pacjenci, u których podczas leczenia produktem ZYVOX wystąpią nawracające nudności lub wymioty, niewyjaśniona kwasica lub niski poziom wodorowęglanów, powinni zostać natychmiast zbadani przez lekarza.
Drgawki
pacjentów leczonych linezolidem zgłaszano drgawki. W niektórych z tych przypadków zgłoszono historię napadów lub czynniki ryzyka napadów.
Hipoglikemia
Po wprowadzeniu produktu do obrotu zgłaszano przypadki objawowej hipoglikemii u pacjentów z cukrzycą otrzymujących insulinę lub doustne leki hipoglikemizujące podczas leczenia linezolidem, odwracalnym, nieselektywnym inhibitorem MAO. Niektóre inhibitory MAO powiązano z epizodami hipoglikemii u pacjentów z cukrzycą otrzymujących insulinę lub leki hipoglikemizujące. Chociaż nie ustalono związku przyczynowego między linezolidem a hipoglikemią, pacjentów z cukrzycą należy ostrzec przed możliwymi reakcjami hipoglikemicznymi podczas leczenia linezolidem.
W przypadku wystąpienia hipoglikemii może być konieczne zmniejszenie dawki insuliny lub doustnego środka hipoglikemizującego lub odstawienie doustnego środka hipoglikemizującego, insuliny lub linezolidu.
Hiponatremia i/lub zespół nieprawidłowego wydzielania hormonu antydiuretycznego (SIADH)
Po wprowadzeniu do obrotu u pacjentów leczonych linezolidem obserwowano przypadki hiponatremii i (lub) zespołu nieprawidłowego wydzielania hormonu antydiuretycznego (SIADH). W zgłoszonych przypadkach objawy przedmiotowe i podmiotowe obejmowały splątanie, senność, uogólnione osłabienie, aw ciężkich przypadkach prowadziły do niewydolności oddechowej, a nawet zgonu. Należy regularnie monitorować stężenie sodu w surowicy u osób w podeszłym wieku, pacjentów przyjmujących leki moczopędne oraz u innych pacjentów z ryzykiem hiponatremii i (lub) SIADH podczas przyjmowania leku ZYVOX. W przypadku wystąpienia objawów hiponatremii i (lub) SIADH należy przerwać podawanie produktu ZYVOX 600 mg i zastosować odpowiednie środki wspomagające.
Zagrożenia u pacjentów z fenyloketonurią
Fenyloalanina może być szkodliwa dla pacjentów z fenyloketonurią (PKU). ZYVOX do doustnej zawiesiny zawiera fenyloalaninę, składnik aspartamu. Każde 5 ml zawiesiny doustnej 100 mg/5 ml zawiera 20 mg fenyloalaniny. Przed przepisaniem preparatu ZYVOX 600 mg w postaci zawiesiny doustnej pacjentowi z PKU należy rozważyć łączną dzienną ilość fenyloalaniny ze wszystkich źródeł, w tym preparatu ZYVOX w postaci zawiesiny doustnej.
Inne preparaty ZYVOX nie zawierają fenyloalaniny.
Rozwój bakterii lekoopornych
Jest mało prawdopodobne, aby przepisywanie preparatu ZYVOX w przypadku braku potwierdzonego lub silnie podejrzewanego zakażenia bakteryjnego lub wskazania profilaktycznego przyniosło korzyści pacjentowi i zwiększyło ryzyko rozwoju bakterii lekoopornych.
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Nie przeprowadzono badań na zwierzętach w ciągu całego życia w celu oceny potencjalnego działania rakotwórczego linezolidu. Ani potencjału mutagennego, ani klastogennego nie wykryto w zestawie testów obejmujących: testy na mutagenność (rewersję bakteryjną Amesa i mutację komórek CHO), test nieplanowanej syntezy DNA (UDS) in vitro, test aberracji chromosomowych in vitro w ludzkich limfocytach oraz test mikrojądrowy u myszy in vivo.
Linezolid nie wpływał na płodność ani zdolność rozrodczą dorosłych samic szczurów, którym podawano doustnie dawki do 100 mg/kg/dobę przez 14 dni przed kryciem do 7. dnia ciąży. Podawany w dawki ≥ 50 mg/kg/dobę, przy ekspozycji w przybliżeniu równej lub większej niż oczekiwany poziom ekspozycji u ludzi (porównania ekspozycji oparte są na AUC). W odwracalnym wpływie na płodność pośredniczyła zmieniona spermatogeneza. Dotknięte spermatydy zawierały nieprawidłowo uformowane i zorientowane mitochondria i były niezdolne do życia. Przerost i rozrost komórek nabłonka w najądrza obserwowano w połączeniu ze zmniejszoną płodnością. Podobnych zmian w najądrzach nie zaobserwowano u psów.
dojrzałych płciowo samców szczurów narażonych na lek jako osobniki młodociane, po leczeniu linezolidem przez większość okresu rozwoju płciowego obserwowano łagodne zmniejszenie płodności (50 mg/kg/dobę od 7. do 36. dnia życia i 100 mg/kg/dobę). od 37. do 55. dnia życia), z ekspozycjami do 1,7 razy większymi niż średnie AUC obserwowane u dzieci w wieku od 3 miesięcy do 11 lat. Zmniejszenia płodności nie obserwowano w przypadku krótszych okresów leczenia, co odpowiada ekspozycji w macicy przez wczesny okres noworodkowy (od 6. dnia ciąży do 5. dnia po urodzeniu), ekspozycji u noworodków (od 5. do 21. dnia po urodzeniu) lub ekspozycji u młodych osobników (od 22. do 35. dnia po urodzeniu). ). U szczurów leczonych od 22 do 35 dnia po urodzeniu obserwowano odwracalne zmniejszenie ruchliwości plemników i zmienioną morfologię plemników.
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
Dostępne dane z opublikowanych i postmarketingowych opisów przypadków stosowania linezolidu u kobiet w ciąży nie wykazały związanego z lekiem ryzyka wystąpienia poważnych wad wrodzonych, poronienia ani niekorzystnych skutków dla matki lub płodu. Podany w trakcie organogenezy linezolid nie powodował wad rozwojowych u myszy, szczurów ani królików przy poziomie ekspozycji matek około 6,5-krotności (myszy), równoważnej (u szczurów) lub 0,06-krotności (króliki) klinicznej ekspozycji terapeutycznej, na podstawie AUC. Jednak u myszy obserwowano śmiertelność zarodków i płodów przy 6,5-krotności szacowanej ekspozycji u ludzi. Gdy samicom szczurów podawano dawki podczas organogenezy w okresie laktacji, przeżywalność po urodzeniu młodych zmniejszała się przy dawkach w przybliżeniu równoważnych oszacowanej ekspozycji u ludzi na podstawie AUC (patrz Dane ).
Podstawowe ryzyko poważnych wad wrodzonych i poronienia we wskazanych populacjach jest nieznane. Wszystkie ciąże wiążą się z ryzykiem wady wrodzonej, utraty lub innych niekorzystnych skutków. W ogólnej populacji USA szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2-4% i 15-20%.
Dane
Dane zwierząt
U myszy toksyczne działanie na zarodek i płód obserwowano tylko po dawkach, które powodowały toksyczne działanie na matkę (objawy kliniczne i zmniejszony przyrost masy ciała). Dawka doustna 450 mg/kg/dobę podawana od 6-16 dnia ciąży (GD) (6,5-krotność szacowanego narażenia człowieka na podstawie AUC) korelowała ze zwiększoną śmiercią zarodków po implantacji, w tym całkowitą utratą miotu, zmniejszeniem masy ciała płodu i zwiększona częstość występowania zespolenia chrząstki żebrowej. W dawkach do 150 mg/kg mc./dobę nie obserwowano działań toksycznych na matkę ani zarodek i płód. Nie zaobserwowano wad rozwojowych płodu.
szczurów toksyczność dla płodów obserwowano przy 15 i 50 mg/kg/dobę podawanych doustnie od GD 6-17 (ekspozycje odpowiednio 0,22 razy w przybliżeniu równoważne oszacowanej ekspozycji u ludzi na podstawie AUC). Skutki obejmowały zmniejszenie masy ciała płodu i zmniejszenie kostnienia mostków, co często obserwuje się w związku ze zmniejszeniem masy ciała płodu. Nie zaobserwowano wad rozwojowych płodu. Toksyczność matczyną w postaci zmniejszonego przyrostu masy ciała obserwowano przy dawce 50 mg/kg/dobę.
U królików zmniejszona masa ciała płodu występowała tylko w przypadku wystąpienia toksyczności matczynej (objawy kliniczne, zmniejszony przyrost masy ciała i spożycie pokarmu) po podaniu doustnym w dawce 15 mg/kg/dobę od 6-20 GD (0,06 razy większej szacowane narażenie ludzi na podstawie AUC). Nie zaobserwowano wad rozwojowych płodu.
Gdy samicom szczurów podawano w czasie ciąży i laktacji (od 6 do 20. dnia laktacji) linezolid w dawce 50 mg/kg/dobę (w przybliżeniu równoważną oszacowanej ekspozycji u ludzi na podstawie AUC), przeżywalność młodych była zmniejszona w 1. do 4. dniu po urodzeniu. U szczeniąt płci męskiej i żeńskiej, którym dozwolono dojrzeć do wieku rozrodczego, obserwowano wzrost strat przedimplantacyjnych.
Laktacja
Podsumowanie ryzyka
Linezolid jest obecny w mleku matki. Na podstawie danych z dostępnych opublikowanych opisów przypadków dzienna dawka linezolidu, jaką niemowlę otrzymywałoby z mleka matki, wynosiłaby około 6% do 9% zalecanej dawki terapeutycznej dla niemowląt (10 mg/kg co 8 godzin). Brak informacji na temat wpływu linezolidu na niemowlę karmione piersią; jednak biegunka i wymioty były najczęstszymi działaniami niepożądanymi zgłaszanymi w badaniach klinicznych u niemowląt otrzymujących terapeutycznie linezolid [patrz DZIAŁANIA NIEPOŻĄDANE i (patrz Rozważania kliniczne). Brak informacji na temat wpływu linezolidu na produkcję mleka. Należy wziąć pod uwagę korzyści rozwojowe i zdrowotne wynikające z karmienia piersią, a także kliniczne zapotrzebowanie matki na linezolid oraz wszelkie potencjalne działania niepożądane linezolidu lub choroby matki na dziecko karmione piersią.
Rozważania kliniczne
Doradź kobietom karmiącym, aby monitorowały niemowlę karmione piersią pod kątem biegunki i wymiotów.
Kobiety i mężczyźni o potencjale rozrodczym
Bezpłodność
Mężczyźni
W oparciu o wyniki badań na szczurach, ZYVOX może odwracalnie zaburzać płodność u mężczyzn [patrz Toksykologia niekliniczna )].
Zastosowanie pediatryczne
Bezpieczeństwo i skuteczność produktu ZYVOX 600 mg w leczeniu pacjentów pediatrycznych z następującymi zakażeniami są poparte dowodami z odpowiednich i dobrze kontrolowanych badań z udziałem dorosłych, danymi farmakokinetycznymi u pacjentów pediatrycznych oraz dodatkowymi danymi z kontrolowanego badania porównawczego zakażenia u pacjentów pediatrycznych w wieku od urodzenia do 11 lat [patrz WSKAZANIA , FARMAKOLOGIA KLINICZNA oraz Studia kliniczne ]:
- szpitalne zapalenie płuc
- skomplikowane infekcje skóry i struktury skóry
- pozaszpitalne zapalenie płuc (poparte również dowodami z niekontrolowanego badania z udziałem pacjentów w wieku od 8 miesięcy do 12 lat)
- oporne na wankomycynę zakażenia Enterococcus faecium
Bezpieczeństwo i skuteczność produktu ZYVOX 600 mg w leczeniu dzieci z następującymi zakażeniami zostały ustalone w kontrolowanym badaniu porównawczym u dzieci w wieku od 5 do 17 lat [patrz Studia kliniczne ]:
- nieskomplikowane infekcje skóry i struktury skóry wywołane przez Staphylococcus aureus (tylko szczepy niewrażliwe na metycylinę) lub Streptococcus pyogenes
Dane farmakokinetyczne uzyskane u dzieci i młodzieży z przeciekiem komorowo-otrzewnowym wykazały zmienne stężenia linezolidu w płynie mózgowo-rdzeniowym (CSF) po jednorazowym i wielokrotnym podaniu linezolidu; stężenia terapeutyczne nie były konsekwentnie osiągane lub utrzymywane w płynie mózgowo-rdzeniowym. Dlatego nie zaleca się stosowania linezolidu w leczeniu empirycznym dzieci z zakażeniami ośrodkowego układu nerwowego.
Farmakokinetykę linezolidu oceniano u dzieci od urodzenia do 17 roku życia. Ogólnie rzecz biorąc, klirens linezolidu na podstawie masy ciała stopniowo zmniejsza się wraz z wiekiem dzieci. Jednak u noworodków urodzonych przedwcześnie (w wieku DAWKOWANIE I SPOSÓB PODAWANIA oraz FARMAKOLOGIA KLINICZNA ].
ograniczonym doświadczeniu klinicznym u 5 z 6 (83%) pacjentów pediatrycznych z zakażeniami wywołanymi przez patogeny Gram-dodatnie o minimalnych stężeniach hamujących (MIC) wynoszących 4 μg/ml leczonych preparatem ZYVOX 600 mg doszło do wyleczenia klinicznego. Jednak pacjenci pediatryczni wykazują większą zmienność klirensu linezolidu i ekspozycji ogólnoustrojowej (AUC) w porównaniu z dorosłymi. U pacjentów pediatrycznych z suboptymalną odpowiedzią kliniczną, szczególnie u patogenów o wartości MIC 4 μg/ml, przy ocenie odpowiedzi klinicznej należy wziąć pod uwagę niższą ekspozycję ogólnoustrojową, miejsce i nasilenie zakażenia oraz leżący u jego podstaw stan chorobowy [patrz FARMAKOLOGIA KLINICZNA oraz DAWKOWANIE I SPOSÓB PODAWANIA ].
Zastosowanie geriatryczne
Spośród 2046 pacjentów leczonych produktem ZYVOX 600 mg w kontrolowanych badaniach klinicznych fazy 3 z grupą kontrolną, 589 (29%) miało 65 lat lub więcej, a 253 (12%) 75 lat lub więcej. Nie zaobserwowano ogólnych różnic w bezpieczeństwie lub skuteczności między tymi pacjentami a młodszymi pacjentami, a inne zgłaszane doświadczenia kliniczne nie wykazały różnic w odpowiedziach między pacjentami w podeszłym wieku i młodszymi, ale nie można wykluczyć większej wrażliwości niektórych osób starszych.
PRZEDAWKOWAĆ
przypadku przedawkowania zaleca się leczenie podtrzymujące z utrzymaniem filtracji kłębuszkowej. Hemodializa może ułatwić szybszą eliminację linezolidu. W badaniu klinicznym fazy I około 30% dawki linezolidu zostało usunięte podczas 3-godzinnej hemodializy rozpoczynającej się 3 godziny po podaniu dawki linezolidu. Brak danych dotyczących usuwania linezolidu za pomocą dializy otrzewnowej lub hemoperfuzji. Klinicznymi objawami ostrej toksyczności u zwierząt były zmniejszona aktywność i ataksja u szczurów oraz wymioty i drżenie u psów leczonych odpowiednio 3000 mg/kg/dobę i 2000 mg/kg/dobę.
PRZECIWWSKAZANIA
Nadwrażliwość
Preparaty ZYVOX są przeciwwskazane do stosowania u pacjentów, u których stwierdzono nadwrażliwość na linezolid lub którykolwiek z pozostałych składników produktu.
Inhibitory monoaminooksydazy
Linezolidu nie należy stosować u pacjentów przyjmujących jakiekolwiek produkty lecznicze hamujące monoaminooksydazy A lub B (np. fenelzyna, izokarboksazyd) ani w ciągu dwóch tygodni od przyjęcia takiego produktu leczniczego.
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
ZYVOX to lek przeciwbakteryjny [patrz Mikrobiologia ].
Farmakodynamika
randomizowanym, naprzemiennym badaniu QT z kontrolą dodatnią i placebo, 40 zdrowym ochotnikom podano pojedynczą dawkę 600 mg produktu ZYVOX w jednogodzinnym wlewie dożylnym, pojedynczą dawkę 1200 mg produktu ZYVOX w jednogodzinnym wlewie dożylnym, placebo oraz pojedyncza dawka doustna kontroli pozytywnej. Zarówno przy dawkach 600 mg, jak i 1200 mg produktu ZYVOX 600 mg, nie wykryto znaczącego wpływu na odstęp QTc przy maksymalnym stężeniu w osoczu ani w jakimkolwiek innym momencie.
Farmakokinetyka
Średnie parametry farmakokinetyczne linezolidu u dorosłych po podaniu pojedynczej i wielokrotnej dawki doustnej i dożylnej podsumowano w Tabeli 8. Stężenia linezolidu w osoczu w stanie stacjonarnym po podaniu doustnym dawek 600 mg co 12 godzin przedstawiono na Rycinie 1.
Rycina 1. Stężenia linezolidu w osoczu u dorosłych w stanie stacjonarnym po podaniu doustnym co 12 godzin (średnia ± odchylenie standardowe, n=16)
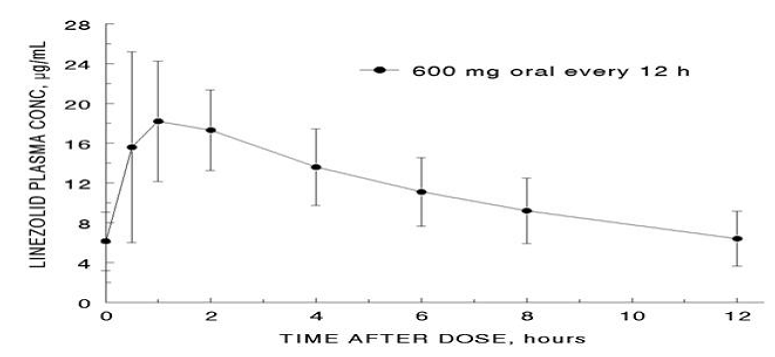
Wchłanianie
Linezolid jest w dużym stopniu wchłaniany po podaniu doustnym. Maksymalne stężenia w osoczu są osiągane po około 1 do 2 godzinach po podaniu, a bezwzględna biodostępność wynosi około 100%. Dlatego linezolid można podawać doustnie lub dożylnie bez konieczności dostosowywania dawki.
Linezolid można podawać niezależnie od pory posiłków. Czas osiągnięcia maksymalnego stężenia jest opóźniony z 1,5 godziny do 2,2 godziny, a Cmax zmniejsza się o około 17% w przypadku podawania pokarmu wysokotłuszczowego z linezolidem. Jednak całkowita ekspozycja mierzona jako AUC0-∞ jest podobna w obu warunkach.
Dystrybucja
Badania farmakokinetyczne na zwierzętach i ludziach wykazały, że linezolid łatwo przenika do dobrze perfundowanych tkanek. Wiązanie linezolidu z białkami osocza wynosi około 31% i jest niezależne od stężenia. Objętość dystrybucji linezolidu w stanie stacjonarnym u zdrowych dorosłych ochotników wynosiła średnio 40 do 50 litrów.
Stężenia linezolidu oznaczono w różnych płynach od ograniczonej liczby pacjentów w badaniach fazy 1 z udziałem ochotników po wielokrotnym podaniu linezolidu. Stosunek linezolidu w ślinie do osocza wynosił 1,2 do 1, a stosunek linezolidu w pocie do osocza wynosił 0,55 do 1.
Metabolizm
Linezolid jest metabolizowany głównie przez utlenianie pierścienia morfolinowego, w wyniku czego powstają dwa nieaktywne metabolity kwasu karboksylowego z otwartym pierścieniem: metabolit kwasu aminoetoksyoctowego (A) i metabolit hydroksyetyloglicyna (B). Zakłada się, że tworzenie metabolitu A powstaje na drodze enzymatycznej, podczas gdy metabolit B odbywa się za pośrednictwem nieenzymatycznego mechanizmu chemicznego utleniania in vitro. Badania in vitro wykazały, że linezolid jest w minimalnym stopniu metabolizowany i może być mediowany przez ludzki cytochrom P450. Jednak szlak metaboliczny linezolidu nie jest w pełni poznany.
Wydalanie
Klirens pozanerkowy stanowi około 65% całkowitego klirensu linezolidu. W stanie stacjonarnym około 30% dawki pojawia się w moczu jako linezolid, 40% jako metabolit B i 10% jako metabolit A. Średni klirens nerkowy linezolidu wynosi 40 ml/min, co sugeruje reabsorpcję netto w kanalikach nerkowych. Praktycznie żaden linezolid nie pojawia się w kale, podczas gdy około 6% dawki pojawia się w kale jako metabolit B, a 3% jako metabolit A.
Przy zwiększaniu dawek linezolidu obserwowano niewielki stopień nieliniowości klirensu, co wydaje się być spowodowane mniejszym klirensem nerkowym i nienerkowym linezolidu w wyższych stężeniach. Jednak różnica w klirensie była niewielka i nie znalazła odzwierciedlenia w pozornym okresie półtrwania w fazie eliminacji.
Określone populacje
Pacjenci geriatryczni
Farmakokinetyka linezolidu nie jest istotnie zmieniona u pacjentów w podeszłym wieku (65 lat i starszych). Dlatego dostosowanie dawki u pacjentów w podeszłym wieku nie jest konieczne.
Pacjenci pediatryczni
Farmakokinetykę linezolidu po podaniu pojedynczej dawki dożylnej badano u dzieci w wieku od urodzenia do 17 lat (w tym u wcześniaków i noworodków urodzonych o czasie), u zdrowych nastolatków w wieku od 12 do 17 lat oraz u dzieci w wieku od urodzenia do 17 lat. w wieku od 1 tygodnia do 12 lat. Parametry farmakokinetyczne linezolidu podsumowano w Tabeli 9 dla badanych populacji pediatrycznych i zdrowych osób dorosłych po podaniu pojedynczych dawek dożylnych.
Cmax i objętość dystrybucji (Vss) linezolidu są podobne niezależnie od wieku u dzieci. Klirens osoczowy linezolidu zmienia się jednak w zależności od wieku. Z wyłączeniem wcześniaków w wieku poniżej jednego tygodnia, klirens na podstawie masy ciała jest najszybszy w najmłodszych grupach wiekowych w wieku od
Podobne średnie dobowe wartości AUC obserwowano u pacjentów pediatrycznych od urodzenia do 11 roku życia, którym podawano lek co 8 godzin, w porównaniu z młodzieżą lub dorosłymi, którym podawano lek co 12 godzin. Dlatego dawka u dzieci w wieku do 11 lat powinna wynosić 10 mg/kg co 8 godzin. Pacjenci pediatryczni w wieku 12 lat i starsi powinni otrzymywać 600 mg co 12 godzin [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Płeć
Kobiety mają nieco mniejszą objętość dystrybucji linezolidu niż mężczyźni. Stężenia w osoczu są wyższe u kobiet niż u mężczyzn, co częściowo wynika z różnic w masie ciała. Po podaniu dawki 600 mg średni klirens po podaniu doustnym jest o około 38% mniejszy u kobiet niż u mężczyzn. Jednak nie ma znaczących różnic między płciami w średniej pozornej stałej szybkości eliminacji lub okresie półtrwania. W związku z tym nie oczekuje się, że ekspozycja na lek u kobiet znacząco wzrośnie powyżej poziomów, o których wiadomo, że są dobrze tolerowane. W związku z tym wydaje się, że dostosowanie dawki ze względu na płeć nie jest konieczne.
Zaburzenia czynności nerek
Farmakokinetyka leku macierzystego, linezolidu, nie zmienia się u pacjentów z jakimkolwiek stopniem niewydolności nerek; jednak dwa główne metabolity linezolidu kumulują się u pacjentów z zaburzeniami czynności nerek, przy czym ilość kumulacji wzrasta wraz z nasileniem zaburzenia czynności nerek (patrz Tabela 10). Farmakokinetykę linezolidu i jego dwóch metabolitów badano również u pacjentów ze schyłkową niewydolnością nerek (ESRD) poddawanych hemodializie. W badaniu ESRD 14 pacjentom podawano linezolid w dawce 600 mg co 12 godzin przez 14,5 dnia (patrz Tabela 11). Ponieważ podobne stężenia linezolidu w osoczu są osiągane niezależnie od czynności nerek, nie zaleca się dostosowywania dawki u pacjentów z zaburzeniami czynności nerek. Jednak biorąc pod uwagę brak informacji na temat znaczenia klinicznego akumulacji głównych metabolitów, stosowanie linezolidu u pacjentów z zaburzeniami czynności nerek należy rozważyć w kontekście potencjalnego ryzyka akumulacji tych metabolitów. Zarówno linezolid, jak i oba metabolity są eliminowane przez hemodializę. Brak dostępnych informacji dotyczących wpływu dializy otrzewnowej na farmakokinetykę linezolidu. Około 30% dawki zostało wyeliminowane podczas 3-godzinnej hemodializy rozpoczynającej się 3 godziny po podaniu dawki linezolidu; dlatego linezolid należy podawać po hemodializie.
Niewydolność wątroby
Farmakokinetyka linezolidu nie zmienia się u pacjentów (n=7) z łagodnymi do umiarkowanych zaburzeniami czynności wątroby (klasa A lub B w skali Child-Pugh). Na podstawie dostępnych informacji nie zaleca się dostosowywania dawki u pacjentów z łagodnymi lub umiarkowanymi zaburzeniami czynności wątroby. Nie oceniano farmakokinetyki linezolidu u pacjentów z ciężkimi zaburzeniami czynności wątroby.
Interakcje leków
Leki metabolizowane przez cytochrom P450
Linezolid nie jest induktorem cytochromu P450 (CYP450) u szczurów. Ponadto linezolid nie hamuje aktywności istotnych klinicznie ludzkich izoform CYP (np. 1A2, 2C9, 2C19, 2D6, 2E1, 3A4). Dlatego nie oczekuje się, aby linezolid wpływał na farmakokinetykę innych leków metabolizowanych przez te główne enzymy. Jednoczesne podawanie linezolidu nie zmienia znacząco właściwości farmakokinetycznych (S)-warfaryny, która jest w znacznym stopniu metabolizowana przez CYP2C9. Leki takie jak warfaryna i fenytoina, które są substratami CYP2C9, można podawać z linezolidem bez zmiany schematu dawkowania.
Leki przeciwbakteryjne
Aztreonam: Farmakokinetyka linezolidu lub aztreonamu nie zmienia się podczas jednoczesnego podawania.
Gentamycyna: Farmakokinetyka linezolidu lub gentamycyny nie zmienia się podczas jednoczesnego podawania.
Przeciwutleniacze
Potencjał interakcji lek-lek z linezolidem i przeciwutleniaczami, witaminą C i witaminą E, badano na zdrowych ochotnikach. Osobom podawano doustnie 600 mg linezolidu w dniu 1. i kolejną dawkę 600 mg linezolidu w dniu 8. W dniach 2-9 podawano albo witaminę C (1000 mg/dzień) albo witaminę E (800 j.m./ dzień). AUC0-∞ linezolidu zwiększyło się o 2,3% przy jednoczesnym podawaniu z witaminą C i 10,9% przy jednoczesnym podawaniu z witaminą E. Nie zaleca się dostosowywania dawki linezolidu podczas równoczesnego podawania z witaminą C lub witaminą E.
Silne induktory CYP 3A4
ryfampicyna
Wpływ ryfampiny na farmakokinetykę linezolidu oceniano w badaniu 16 zdrowych dorosłych mężczyzn. Ochotnikom podawano doustnie linezolid w dawce 600 mg dwa razy na dobę w 5 dawkach z ryfampicyną lub bez ryfampicyny w dawce 600 mg raz na dobę przez 8 dni. Jednoczesne podawanie ryfampicyny z linezolidem powodowało 21% zmniejszenie Cmax linezolidu [90% CI, 15% - 27%] i 32% zmniejszenie AUC0-12 linezolidu [90% CI, 27% - 37%]. Kliniczne znaczenie tej interakcji nie jest znane. Mechanizm tej interakcji nie jest w pełni poznany i może być związany z indukcją enzymów wątrobowych. Inne silne induktory enzymów wątrobowych (np. karbamazepina, fenytoina, fenobarbital) mogą powodować podobne lub mniejsze zmniejszenie ekspozycji na linezolid.
Hamowanie monoaminooksydazy
Linezolid jest odwracalnym, nieselektywnym inhibitorem monoaminooksydazy. Dlatego linezolid może wchodzić w interakcje z lekami adrenergicznymi i serotoninergicznymi.
Środki adrenergiczne
niektórych osób otrzymujących ZYVOX 600 mg może wystąpić odwracalne wzmocnienie odpowiedzi presyjnej na pośrednio działające środki sympatykomimetyczne, wazopresyjne lub dopaminergiczne. Konkretnie zbadano powszechnie stosowane leki, takie jak fenylopropanolamina i pseudoefedryna. Początkowe dawki środków adrenergicznych, takich jak dopamina lub epinefryna, należy zmniejszyć i dostosować, aby uzyskać pożądaną odpowiedź.
Tyramina
U zdrowych osób dorosłych otrzymujących linezolid i tyraminę w dawkach większych niż 100 mg zaobserwowano znaczną odpowiedź presyjną. Dlatego pacjenci otrzymujący linezolid powinni unikać spożywania dużych ilości pokarmów lub napojów o wysokiej zawartości tyraminy [patrz INFORMACJA O PACJENCIE ].
Pseudoefedryna HCl lub fenylopropanolamina HCl
Po podaniu linezolidu zdrowym osobom z prawidłowym ciśnieniem tętniczym obserwuje się odwracalne nasilenie reakcji presyjnej na pseudoefedrynę chlorowodorek (PSE) lub chlorowodorek fenylopropanolaminy (PPA) [patrz OSTRZEŻENIA I ŚRODKI oraz INTERAKCJE Z LEKAMI ]. Podobnego badania nie przeprowadzono u pacjentów z nadciśnieniem. W badaniach interakcji przeprowadzonych u osób z prawidłowym ciśnieniem tętniczym oceniano wpływ placebo, samego PPA lub PSE, samego linezolidu oraz połączenia linezolidu w stanie stacjonarnym (600 mg co 12 godzin przez 3 dni) z dwiema dawkami PPA (600 mg co 12 godzin przez 3 dni) na ciśnienie krwi i częstość akcji serca ( 25 mg) lub PSE (60 mg) podawane w odstępie 4 godzin. Żaden z zabiegów nie miał wpływu na tętno. Ciśnienie krwi było podwyższone w przypadku obu terapii skojarzonych. Maksymalne poziomy ciśnienia krwi były obserwowane 2 do 3 godzin po drugiej dawce PPA lub PSE i powróciły do wartości wyjściowych 2 do 3 godzin po szczycie. Poniżej przedstawiono wyniki badania PPA, pokazujące średnie (i zakres) maksymalne skurczowe ciśnienie krwi w mm Hg: placebo = 121 (103 do 158); sam linezolid = 120 (107 do 135); sam PPA = 125 (106 do 139); PPA z linezolidem = 147 (129 do 176). Wyniki badania PSE były zbliżone do wyników badania PPA. Średnie maksymalne zwiększenie skurczowego ciśnienia krwi w stosunku do wartości wyjściowej wynosiło 32 mm Hg (zakres: 20-52 mm Hg) i 38 mm Hg (zakres: 18-79 mm Hg) odpowiednio podczas jednoczesnego podawania linezolidu z pseudoefedryną lub fenylopropanolaminą.
Środki serotoninergiczne
Dekstrometorfan
Potencjalne interakcje lek-lek z dekstrometorfanem badano u zdrowych ochotników. Osobom podawano dekstrometorfan (dwie dawki 20 mg podawane w odstępie 4 godzin) z linezolidem lub bez. U zdrowych osób otrzymujących linezolid i dekstrometorfan nie obserwowano objawów zespołu serotoninowego (splątanie, majaczenie, niepokój, drżenie, rumienienie, obfite pocenie się, gorączka).
Mikrobiologia
Mechanizm akcji
Linezolid jest syntetycznym środkiem przeciwbakteryjnym z klasy oksazolidynonów, który ma zastosowanie kliniczne w leczeniu zakażeń wywołanych przez tlenowe bakterie Gram-dodatnie. Spektrum działania linezolidu in vitro obejmuje również niektóre bakterie Gram-ujemne i bakterie beztlenowe. Linezolid wiąże się z miejscem na bakteryjnym rybosomalnym RNA 23S podjednostki 50S i zapobiega tworzeniu funkcjonalnego kompleksu inicjacyjnego 70S, który jest niezbędny do rozmnażania bakterii. Wyniki badań „time kill” wykazały, że linezolid ma działanie bakteriostatyczne na enterokoki i gronkowce. Stwierdzono, że linezolid w przypadku paciorkowców ma działanie bakteriobójcze w przypadku większości izolatów.
Opór
Badania in vitro wykazały, że mutacje punktowe w 23S rRNA są związane z opornością na linezolid. Opublikowano doniesienia o tym, że Enterococcus faecium oporny na wankomycynę staje się oporny na linezolid podczas jego stosowania klinicznego. Istnieją doniesienia o rozwoju oporności Staphylococcus aureus (opornego na metycylinę) na linezolid podczas stosowania klinicznego. Oporność na linezolid w tych organizmach jest związana z mutacją punktową w 23S rRNA (podstawienie tyminy na guaninę w pozycji 2576) organizmu. Drobnoustroje oporne na oksazolidynony poprzez mutacje w genach chromosomalnych kodujących 23S rRNA lub białka rybosomalne (L3 i L4) są ogólnie oporne krzyżowo na linezolid. Zgłaszano również oporność gronkowców na linezolid, w której pośredniczy enzym metylotransferaza. W tej oporności pośredniczy gen cfr (chloramfenikol-florfenikol) zlokalizowany na plazmidzie, który można przenosić między gronkowcami.
Interakcje z innymi lekami przeciwdrobnoustrojowymi
Badania in vitro wykazały addytywność lub obojętność między linezolidem a wankomycyną, gentamycyną, ryfampicyną, imipenemem-cylastatyną, aztreonamem, ampicyliną lub streptomycyną.
Wykazano, że linezolid jest aktywny wobec większości izolatów następujących drobnoustrojów, zarówno in vitro, jak i w zakażeniach klinicznych [patrz WSKAZANIA ].
Bakterie Gram-dodatnie
Enterococcus faecium (tylko szczepy oporne na wankomycynę) Staphylococcus aureus (w tym izolaty oporne na metycylinę) Streptococcus agalactiae Streptococcus pneumoniae Streptococcus pyogenes
Dostępne są następujące dane in vitro, ale ich znaczenie kliniczne nie jest znane. Ponad 90% następujących bakterii wykazuje in vitro MIC mniejsze lub równe wartości granicznej wrażliwości na linezolid dla organizmów podobnego rodzaju. Bezpieczeństwo i skuteczność linezolidu w leczeniu zakażeń klinicznych wywoływanych przez te bakterie nie zostały ustalone w odpowiednich i dobrze kontrolowanych badaniach klinicznych.
Bakterie Gram-dodatnie
Enterococcus faecalis (w tym izolaty oporne na wankomycynę) Enterococcus faecium (izolaty wrażliwe na wankomycynę) Staphylococcus epidermidis (w tym izolaty oporne na metycylinę) Staphylococcus haemolyticus Paciorkowce z grupy Viridans
Bakterie Gram-ujemne
Pasteurella multocida
Testy podatności
Szczegółowe informacje dotyczące kryteriów interpretacyjnych testu wrażliwości i powiązanych metod badawczych oraz standardów kontroli jakości uznanych przez FDA dla tego leku można znaleźć na stronie: https://www.fda.gov/STIC.
Toksykologia i/lub farmakologia zwierząt
Narządy docelowe działania toksycznego linezolidu były podobne u młodych i dorosłych szczurów i psów. W badaniach na zwierzętach obserwowano zależną od dawki i czasu mielosupresję, o czym świadczy ubytek komórek szpiku kostnego/zmniejszona hematopoeza, zmniejszona hematopoeza pozaszpikowa w śledzionie i wątrobie oraz obniżony poziom krążących erytrocytów, leukocytów i płytek krwi. Ubytek limfoidalny wystąpił w grasicy, węzłach chłonnych i śledzionie. Ogólnie rzecz biorąc, zmiany limfoidalne wiązały się z anoreksją, utratą masy ciała i zahamowaniem przyrostu masy ciała, co mogło przyczynić się do zaobserwowanych efektów.
szczurów, którym podawano doustnie linezolid przez 6 miesięcy, obserwowano nieodwracalne, minimalne lub łagodne zwyrodnienie aksonów nerwów kulszowych przy dawce 80 mg/kg/dobę; minimalne zwyrodnienie nerwu kulszowego zaobserwowano również u 1 samca przy tym poziomie dawki podczas 3-miesięcznej częściowej sekcji zwłok. Przeprowadzono czułą ocenę morfologiczną tkanek utrwalonych przez perfuzję w celu zbadania dowodów na zwyrodnienie nerwu wzrokowego. Minimalne do umiarkowanego zwyrodnienie nerwu wzrokowego było widoczne u 2 samców szczurów po 6 miesiącach dawkowania, ale bezpośredni związek z lekiem był niejednoznaczny ze względu na ostry charakter odkrycia i jego asymetryczny rozkład. Obserwowane zwyrodnienie nerwu było mikroskopowo porównywalne do spontanicznego jednostronnego zwyrodnienia nerwu wzrokowego zgłaszanego u starzejących się szczurów i może być zaostrzeniem wspólnej zmiany tła.
Efekty te zaobserwowano przy poziomach narażenia porównywalnych do tych obserwowanych u niektórych ludzi. Efekty hematopoetyczne i limfoidalne były odwracalne, chociaż w niektórych badaniach odwrócenie było niepełne w okresie rekonwalescencji.
Studia kliniczne
Dorośli ludzie
Szpitalne zapalenie płuc
Dorośli pacjenci z klinicznie i radiologicznie udokumentowanym szpitalnym zapaleniem płuc zostali włączeni do randomizowanego, wieloośrodkowego badania z podwójnie ślepą próbą. Pacjenci byli leczeni przez 7 do 21 dni. Jedna grupa otrzymywała ZYVOX IV w zastrzyku 600 mg co 12 godzin, a druga grupa otrzymywała dożylnie 1 g wankomycyny co 12 godzin. Obie grupy otrzymywały jednocześnie aztreonam (1 do 2 g dożylnie co 8 godzin), który można było kontynuować, jeśli jest to klinicznie wskazane. Do badania włączono 203 pacjentów leczonych linezolidem i 193 pacjentów leczonych wankomycyną. Klinicznie można było ocenić stu dwudziestu dwóch (60%) pacjentów leczonych linezolidem i 103 (53%) pacjentów leczonych wankomycyną. Wskaźniki wyleczeń u pacjentów ocenianych klinicznie wynosiły 57% dla pacjentów leczonych linezolidem i 60% dla pacjentów leczonych wankomycyną. Wskaźniki wyleczeń u pacjentów z zapaleniem płuc, które można było ocenić klinicznie, wynosiły 47% dla pacjentów leczonych linezolidem i 40% dla pacjentów leczonych wankomycyną. Zmodyfikowana analiza zamiaru leczenia (MITT) 94 pacjentów leczonych linezolidem i 83 pacjentów leczonych wankomycyną obejmowała osoby, u których przed leczeniem wyizolowano patogen. Wskaźniki wyleczeń w analizie MITT wynosiły 57% u pacjentów leczonych linezolidem i 46% u pacjentów leczonych wankomycyną. Wskaźniki wyleczeń według patogenów u pacjentów poddawanych ocenie mikrobiologicznej przedstawiono w tabeli 12.
Skomplikowane infekcje skóry i struktury skóry
Dorośli pacjenci z udokumentowanymi klinicznie powikłanymi zakażeniami skóry i struktury skóry zostali włączeni do randomizowanego, wieloośrodkowego, podwójnie ślepego, podwójnie pozorowanego badania porównującego badane leki podawane dożylnie, a następnie leki podawane doustnie, łącznie przez 10 do 21 dni leczenia. Jedna grupa pacjentów otrzymywała produkt ZYVOX IV do wstrzykiwań w dawce 600 mg co 12 godzin, a następnie ZYVOX w tabletkach 600 mg w dawce 600 mg co 12 godzin; druga grupa otrzymywała oksacylinę 2 g co 6 godzin dożylnie, a następnie dikloksacylinę 500 mg co 6 godzin doustnie. Pacjenci mogą jednocześnie otrzymywać aztreonam, jeśli jest to wskazane klinicznie. Do badania włączono 400 pacjentów leczonych linezolidem i 419 pacjentów leczonych oksacyliną. Dwustu czterdziestu pięciu (61%) pacjentów leczonych linezolidem i 242 (58%) pacjentów leczonych oksacyliną było ocenianych klinicznie. Wskaźniki wyleczeń u pacjentów kwalifikujących się do oceny klinicznej wynosiły 90% u pacjentów leczonych linezolidem i 85% u pacjentów leczonych oksacyliną. Zmodyfikowana analiza intent-to-treat (MITT) 316 pacjentów leczonych linezolidem i 313 pacjentów leczonych oksacyliną obejmowała osoby spełniające wszystkie kryteria włączenia do badania. Wskaźniki wyleczeń w analizie MITT wynosiły 86% u pacjentów leczonych linezolidem i 82% u pacjentów leczonych oksacyliną. Wskaźniki wyleczeń według patogenów u pacjentów poddawanych ocenie mikrobiologicznej przedstawiono w tabeli 13.
Oddzielne badanie dostarczyło dodatkowych doświadczeń ze stosowaniem preparatu ZYVOX w leczeniu zakażeń gronkowcem złocistym opornym na metycylinę (MRSA). Było to randomizowane, otwarte badanie z udziałem hospitalizowanych dorosłych pacjentów z udokumentowaną lub podejrzewaną infekcją MRSA.
Jedna grupa pacjentów otrzymywała produkt ZYVOX IV do wstrzykiwań w dawce 600 mg co 12 godzin, a następnie tabletki ZYVOX 600 mg co 12 godzin. Druga grupa pacjentów otrzymywała dożylnie 1 g wankomycyny co 12 godzin. Obie grupy były leczone przez 7 do 28 dni i mogły otrzymywać jednocześnie aztreonam lub gentamycynę, jeśli było to klinicznie wskazane. Wskaźniki wyleczeń u pacjentów ocenianych mikrobiologicznie z zakażeniem skóry i struktury skóry MRSA wynosiły 26/33 (79%) dla pacjentów leczonych linezolidem i 24/33 (73%) dla pacjentów leczonych wankomycyną.
Zakażenia stopy cukrzycowej
Dorośli pacjenci z cukrzycą z udokumentowanymi klinicznie powikłanymi zakażeniami skóry i struktury skóry („zakażenia stopy cukrzycowej”) zostali włączeni do randomizowanego (w stosunku 2:1), wieloośrodkowego, otwartego badania, porównującego badane leki podawane dożylnie lub doustnie, łącznie 14 do 28 dni leczenia. Jedna grupa pacjentów otrzymywała ZYVOX 600 mg co 12 godzin dożylnie lub doustnie; druga grupa otrzymywała ampicylinę z sulbaktamem 1,5 do 3 g dożylnie lub amoksycylinę z klawulanianem 500 do 875 mg co 8 do 12 godzin doustnie. W krajach, w których ampicylina z sulbaktamem nie jest dostępna w obrocie, w schemacie dożylnym stosowano amoksycylinę z klawulanianem w dawce 500 mg do 2 g co 6 godzin. Pacjenci z grupy porównawczej mogli być również leczeni dożylnie wankomycyną 1 g co 12 godzin, jeśli MRSA został wyizolowany z zakażenia stopy. Pacjenci w obu grupach, u których z miejsca zakażenia wyizolowano pałeczki Gram-ujemne, mogli również otrzymywać dożylnie 1 do 2 g aztreonamu co 8-12 godzin. Wszyscy pacjenci kwalifikowali się do otrzymania odpowiednich metod leczenia wspomagającego, takich jak oczyszczenie i odciążenie, zwykle wymagane w leczeniu infekcji stopy cukrzycowej, a większość pacjentów otrzymywała takie leczenie. W populacji badanej zgodnej z zamiarem leczenia (ITT) było 241 pacjentów leczonych linezolidem i 120 pacjentów leczonych lekiem porównawczym. Dwustu dwunastu (86%) pacjentów leczonych linezolidem i 105 (85%) pacjentów leczonych lekiem porównawczym było ocenianych klinicznie. W populacji ITT wskaźniki wyleczeń wynosiły 68,5% (165/241) u pacjentów leczonych linezolidem i 64% (77/120) u pacjentów leczonych lekiem porównawczym, gdzie te z nieokreślonymi i brakującymi wynikami uznawano za niepowodzenia. Wskaźniki wyleczeń u pacjentów kwalifikujących się do oceny klinicznej (z wyłączeniem pacjentów z nieokreślonymi i brakującymi wynikami) wynosiły odpowiednio 83% (159/192) i 73% (74/101) u pacjentów leczonych linezolidem i lekiem porównawczym. Krytyczna analiza post-hoc dotyczyła 121 pacjentów leczonych linezolidem i 60 pacjentów otrzymujących lek porównawczy, u których wyizolowano patogen Gram-dodatni z miejsca zakażenia lub z krwi, którzy mieli mniej dowodów na współistniejące zapalenie kości i szpiku niż cała badana populacja i którzy nie otrzymały zabronionych środków przeciwdrobnoustrojowych. Na podstawie tej analizy wskaźniki wyleczeń wynosiły 71% (86/121) u pacjentów leczonych linezolidem i 63% (38/60) u pacjentów leczonych lekiem porównawczym. Żadna z powyższych analiz nie została dostosowana do stosowania terapii wspomagających. Wskaźniki wyleczeń według patogenów u pacjentów poddawanych ocenie mikrobiologicznej przedstawiono w tabeli 14.
Zakażenia enterokokowe oporne na wankomycynę
Dorośli pacjenci z udokumentowaną lub podejrzewaną infekcją enterokokową oporną na wankomycynę zostali włączeni do randomizowanego, wieloośrodkowego badania z podwójnie ślepą próbą, porównującego wysoką dawkę preparatu ZYVOX (600 mg) z niską dawką preparatu ZYVOX (200 mg) podawaną co 12 godzin albo dożylnie (IV) lub doustnie przez 7 do 28 dni. Pacjenci mogą jednocześnie otrzymywać aztreonam lub aminoglikozydy. 79 pacjentów przydzielono losowo do grupy otrzymującej dużą dawkę linezolidu, a 66 do grupy otrzymującej małą dawkę linezolidu. Populacja intent-to-treat (ITT) z udokumentowanym zakażeniem enterokokami opornymi na wankomycynę na początku badania składała się z 65 pacjentów w ramieniu z dużą dawką i 52 w ramieniu z małą dawką.
Wskaźniki wyleczeń dla populacji ITT z udokumentowanym wyjściowym zakażeniem enterokokami opornymi na wankomycynę przedstawiono w Tabeli 15 według źródła zakażenia. Te wskaźniki wyleczeń nie obejmują pacjentów z brakującymi lub nieokreślonymi wynikami. Wskaźnik wyleczeń był wyższy w ramieniu z dużą dawką niż w ramieniu z małą dawką, chociaż różnica nie była istotna statystycznie na poziomie 0,05.
Pacjenci pediatryczni
Zakażenia spowodowane bakteriami Gram-dodatnimi
Badanie bezpieczeństwa i skuteczności dostarczyło doświadczenia w stosowaniu produktu ZYVOX 600 mg u dzieci w leczeniu szpitalnego zapalenia płuc, powikłanych zakażeń skóry i struktury skóry oraz innych zakażeń wywołanych przez bakterie Gram-dodatnie, w tym oporny i podatny na metycylinę Staphylococcus aureus i odporne na wankomycynę Enterococcus faecium. Pacjenci pediatryczni w wieku od urodzenia do 11 lat z zakażeniami wywołanymi przez udokumentowane lub podejrzewane bakterie Gram-dodatnie zostali włączeni do randomizowanego, kontrolowanego badania porównawczego openPage. Jedna grupa pacjentów otrzymywała ZYVOX 600 mg dożylnie w dawce 10 mg/kg co 8 godzin, a następnie ZYVOX 600 mg do doustnej zawiesiny 10 mg/kg co 8 godzin. Druga grupa otrzymywała dożylnie wankomycynę w dawce 10 do 15 mg/kg co 6 do 24 godzin, w zależności od wieku i klirensu nerkowego. Pacjenci, u których stwierdzono zakażenie VRE, zostali umieszczeni w trzecim ramieniu badania i otrzymywali ZYVOX w dawce 10 mg/kg co 8 godzin dożylnie i (lub) doustnie. Wszyscy pacjenci byli leczeni łącznie przez 10 do 28 dni i mogli otrzymywać jednocześnie leki przeciwbakteryjne Gram-ujemne, jeśli było to klinicznie wskazane. W populacji zgodnej z zamiarem leczenia (ITT) było 206 pacjentów przydzielonych losowo do linezolidu i 102 pacjentów przydzielonych losowo do wankomycyny. Wskaźniki wyleczeń dla ITT, MITT i pacjentów kwalifikujących się do oceny klinicznej przedstawiono w Tabeli 16. Po zakończeniu badania, 13 dodatkowych pacjentów w wieku od 4 dni do 16 lat zostało włączonych do otwartego rozszerzenia ramienia VRE nauka. Tabela 17 przedstawia wskaźniki wyleczenia klinicznego według patogenu u pacjentów poddawanych ocenie mikrobiologicznej, w tym u pacjentów z opornym na wankomycynę Enterococcus faecium poddawanych ocenie mikrobiologicznej z rozszerzenia tego badania.
INFORMACJA O PACJENCIE
Ważne instrukcje administracyjne
Należy poinformować pacjentów, że preparat ZYVOX można przyjmować z posiłkiem lub bez posiłku.
Neuropatia obwodowa i wzrokowa
Należy doradzić pacjentom, aby poinformowali swojego lekarza, jeśli podczas przyjmowania leku ZYVOX wystąpią u nich zmiany widzenia [patrz OSTRZEŻENIA I ŚRODKI ].
Zespół serotoninowy
Należy doradzić pacjentom, aby informowali lekarza o przyjmowaniu leków serotoninergicznych, w tym inhibitorów wychwytu zwrotnego serotoniny lub innych leków przeciwdepresyjnych i opioidów [patrz OSTRZEŻENIA I ŚRODKI ].
Potencjalne interakcje powodujące podwyższenie ciśnienia krwi
- Doradź pacjentom, aby poinformowali swojego lekarza, jeśli mają historię nadciśnienia.
- Należy doradzić pacjentom, aby podczas przyjmowania leku ZYVOX unikali dużych ilości pokarmów lub napojów o wysokiej zawartości tyraminy. Pokarmy o wysokiej zawartości tyraminy obejmują te, które mogły ulec zmianie białka w wyniku starzenia, fermentacji, marynowania lub palenia w celu poprawy smaku, takie jak dojrzewające sery, fermentowane lub suszone na powietrzu mięso, kapusta kiszona, sos sojowy, piwo z beczki i czerwone wina. Zawartość tyraminy w żywności bogatej w białko może być zwiększona, jeśli jest przechowywana przez długi czas lub niewłaściwie przechowywana w lodówce.
- Poradź pacjentom, aby poinformowali swojego lekarza o przyjmowaniu leków zawierających pseudoefedrynę lub chlorowodorek fenylopropanolaminy, takich jak leki na przeziębienie i leki zmniejszające przekrwienie [patrz OSTRZEŻENIA I ŚRODKI ].
Kwasica mleczanowa
Należy doradzić pacjentom, aby poinformowali lekarza, jeśli podczas przyjmowania leku ZYVOX wystąpią powtarzające się epizody nudności lub wymiotów [patrz OSTRZEŻENIA I ŚRODKI ].
Drgawki
Doradź pacjentom, aby poinformowali swojego lekarza, jeśli mają w przeszłości napady padaczkowe lub drgawki [patrz OSTRZEŻENIA I ŚRODKI ].
Hipoglikemia
Doradź pacjentom, aby informowali swojego lekarza, jeśli mają cukrzycę. Podczas leczenia linezolidem mogą wystąpić reakcje hipoglikemiczne, takie jak pocenie się i drżenie, a także niski poziom glukozy we krwi. Jeśli takie reakcje wystąpią, pacjenci powinni skontaktować się z lekarzem lub innym pracownikiem służby zdrowia w celu odpowiedniego leczenia [patrz OSTRZEŻENIA I ŚRODKI ].
Hiponatremia i/lub SIADH
Należy doradzić pacjentom zagrożonym hiponatremią, aby poinformowali lekarza, jeśli wystąpią u nich objawy przedmiotowe i podmiotowe hiponatremii i (lub) SIADH, w tym splątanie, senność, uogólnione osłabienie i niewydolność oddechowa [patrz OSTRZEŻENIA I ŚRODKI ].
Fenyloketonuria
Należy poinformować pacjentów z fenyloketonurią (ang. PKU), że każde 5 ml preparatu ZYVOX do sporządzania zawiesiny doustnej 100 mg/5 ml zawiera 20 mg fenyloalaniny. Inne preparaty ZYVOX 600 mg nie zawierają fenyloalaniny. Fenyloalanina może być szkodliwa dla pacjentów z fenyloketonurią. W przypadku przepisania leku ZYVOX 600 mg do sporządzania zawiesiny doustnej należy skontaktować się z lekarzem lub farmaceutą [patrz OSTRZEŻENIA I ŚRODKI ].
Odporność antybakteryjna
Pacjentów należy pouczyć, że leki przeciwbakteryjne, w tym ZYVOX, należy stosować wyłącznie w leczeniu zakażeń bakteryjnych. Nie leczą infekcji wirusowych (np. przeziębienia). Kiedy ZYVOX 600 mg jest przepisywany w celu leczenia infekcji bakteryjnej, pacjentom należy poinformować, że chociaż często zdarza się, że poczują się lepiej na początku leczenia, lek należy przyjmować dokładnie zgodnie z zaleceniami. Pomijanie dawek lub nieukończenie pełnego cyklu leczenia może zmniejszyć skuteczność natychmiastowego leczenia i zwiększyć prawdopodobieństwo, że bakterie rozwiną oporność i nie będą mogły być leczone preparatem ZYVOX lub innymi lekami przeciwbakteryjnymi w przyszłości.
Biegunka
Biegunka jest częstym problemem powodowanym przez leki przeciwbakteryjne, który zwykle kończy się wraz z odstawieniem leku przeciwbakteryjnego. Czasami po rozpoczęciu leczenia lekami przeciwbakteryjnymi u pacjentów mogą pojawić się wodniste i krwawe stolce (ze skurczami żołądka i gorączką lub bez), nawet po dwóch lub więcej miesiącach od przyjęcia ostatniej dawki leku przeciwbakteryjnego. W takim przypadku pacjenci powinni jak najszybciej skontaktować się z lekarzem [patrz OSTRZEŻENIA I ŚRODKI ].
Bezpłodność
Poinformuj pacjentów płci męskiej, że ZYVOX może odwracalnie zaburzać płodność [patrz Używaj w określonych populacjach ].
Etykieta tego produktu mogła zostać zaktualizowana. Najnowsze informacje na temat przepisywania leków można znaleźć na stronie www.pfizer.com.
