Minocin 50mg, 100mg Minocycline Hydrochloride Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest zawiesina doustna Minocin i jak się ją stosuje?
Minocin (chlorowodorek minocykliny) to antybiotyk tetracyklinowy stosowany w leczeniu wielu różnych infekcji bakteryjnych, takich jak infekcje dróg moczowych, infekcje dróg oddechowych, infekcje skóry, ciężki trądzik, rzeżączka, gorączka kleszczowa, chlamydia i inne.
Jakie są skutki uboczne Minocin Oral Suspension?
Typowe działania niepożądane Minocin obejmują:
- zawroty głowy,
- uczucie zmęczenia,
- uczucie wirowania,
- ból stawów lub mięśni,
- przebarwienia skóry lub paznokci lub dziąseł,
- mdłości,
- biegunka,
- rozstrój żołądka,
- wysypka skórna lub swędzenie,
- obrzęk języka lub
- swędzenie lub wydzielina pochwy.
Należy poinformować lekarza, jeśli wystąpią poważne działania niepożądane leku Minocin 50 mg, w tym:
- skurcze żołądka,
- biegunka wodnista lub krwawa,
- Objawy grypy,
- owrzodzenia w jamie ustnej i gardle,
- słabość,
- ciemny kolor moczu,
- nietypowe krwawienie,
- fioletowe lub czerwone plamki pod skórą,
- gorączka,
- wysypka na skórze,
- siniaki,
- silne mrowienie lub drętwienie,
- słabe mięśnie,
- utrata apetytu,
- zażółcenie skóry lub oczu,
- ból w klatce piersiowej,
- nieregularny rytm serca,
- kaszel,
- świszczący oddech,
- duszność,
- dezorientacja,
- wymioty,
- obrzęk,
- przybranie na wadze,
- oddawanie moczu mniej niż zwykle lub wcale,
- ból głowy lub ból za oczami,
- dzwonienie w uszach,
- Problemy ze wzrokiem,
- ból stawów lub obrzęk z gorączką,
- obrzęk gruczołów,
- bóle mięśni,
- ogólne złe samopoczucie,
- nietypowe myśli lub zachowanie,
- drgawki (konwulsje) lub
- ciężka reakcja skórna.
Aby ograniczyć rozwój bakterii opornych na leki i utrzymać skuteczność zawiesiny doustnej MINOCIN® i innych leków przeciwbakteryjnych, zawiesinę doustną MINOCIN należy stosować wyłącznie do leczenia lub zapobiegania zakażeniom, co do których udowodniono, że są powodowane przez bakterie lub które są silnie podejrzewane.
OPIS
MINOCIN 100mg chlorowodorek minocykliny, jest półsyntetyczną pochodną tetracykliny, 4,7Bis(dimetyloamino)-1,4,4a,5,5a,6,11,12a-oktahydro-3,10,12,12a-tetrahydroksy-1,11 - monochlorowodorek diokso-2naftacenokarboksyamidu.
Jego wzór strukturalny to:
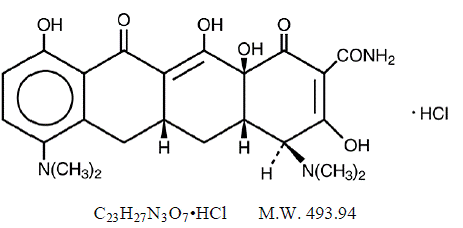 C23H27N3O7•HCl MW 493,94
C23H27N3O7•HCl MW 493,94 MINOCIN 50 mg zawiesina doustna zawiera chlorowodorek minocykliny w ilości odpowiadającej 50 mg minocykliny na 5 ml (10 mg/ml) oraz następujące składniki nieaktywne: alkohol, butyloparaben, wodorotlenek wapnia, celuloza, tetraoleinian dekaglicerylu, wersenian wapnia, guma guar, polisorbat 80 , propyloparaben, glikol propylenowy, sacharyna sodowa, siarczyn sodu (patrz OSTRZEŻENIA ) i sorbitol.
WSKAZANIA
MINOCIN 100mg zawiesina doustna jest wskazany w leczeniu następujących zakażeń wywołanych przez wrażliwe szczepy wskazanych drobnoustrojów:
Gorączka plamista Gór Skalistych, tyfus plamisty i grupa tyfusu, gorączka Q, ospa riketsjologiczna i gorączka kleszczowa wywołana przez riketsje.
Infekcje dróg oddechowych wywołane przez Mycoplasma pneumoniae.
Lymphogranuloma venereum wywołana przez Chlamydia trachomatis.
Psittacosis (ornitoza) wywołana przez Chlamydophila psittaci.
Jaglica wywołana przez Chlamydia trachomatis, chociaż czynnik zakaźny nie zawsze jest eliminowany, co ocenia się na podstawie immunofluorescencji.
Inkluzyjne zapalenie spojówek wywołane przez Chlamydia trachomatis.
Nierzeżączkowe zapalenie cewki moczowej, zakażenia szyjki macicy lub odbytnicy u dorosłych wywołane przez Ureaplasma urealyticum lub Chlamydia trachomatis.
Nawracająca gorączka spowodowana Borrelia recurrentis.
Chancroid wywołany przez Haemophilus ducreyi.
Plaga spowodowana przez Yersinia pestis.
Tularemia spowodowana Francisella tularensis.
Cholera wywołana przez Vibrio cholerae.
Zakażenia Campylobacter fetus wywołane przez Campylobacter fetus.
Bruceloza wywołana przez gatunki Brucella (w połączeniu ze streptomycyną).
Bartonelloza wywołana przez Bartonella bacilliformis.
Ziarniniak pachwinowy wywołany przez Klebsiella granulomatis.
Minocyklina jest wskazana w leczeniu zakażeń wywołanych przez następujące drobnoustroje Gram-ujemne, gdy badania bakteriologiczne wskazują na odpowiednią podatność na lek:
Escherichia coli.
Enterobacter aerogenes.
Gatunki Shigella.
Gatunki Acinetobacter.
Infekcje dróg oddechowych wywołane przez Haemophilus influenzae.
Infekcje dróg oddechowych i dróg moczowych wywoływane przez gatunki Klebsiella.
MINOCIN Oral Suspension jest wskazany w leczeniu zakażeń wywołanych przez następujące drobnoustroje Gram-dodatnie, gdy badania bakteriologiczne wskazują na odpowiednią wrażliwość na lek:
Infekcje górnych dróg oddechowych wywołane przez Streptococcus pneumoniae. Zakażenia skóry i struktury skóry wywołane przez Staphylococcus aureus (uwaga: Minocyklina nie jest lekiem z wyboru w leczeniu jakiegokolwiek rodzaju infekcji gronkowcowej).
Gdy penicylina jest przeciwwskazana, minocyklina jest lekiem alternatywnym w leczeniu następujących infekcji:
Niepowikłane zapalenie cewki moczowej u mężczyzn wywołane przez Neisseria gonorrhoeae oraz w leczeniu innych zakażeń gonokokowych.
Zakażenia u kobiet wywołane przez Neisseria gonorrhoeae.
Kiła wywołana przez podgatunek Treponema pallidum pallidum.
Fałsze wywołane przez podgatunek Treponema pallidum pertenue.
Listerioza wywołana przez Listeria monocytogenes.
Wąglik z powodu Bacillus anthracis.
Infekcja Vincenta wywołana przez Fusobacterium fusiforme.
Promienica wywołana przez Actinomyces israelii.
Zakażenia wywołane przez gatunki Clostridium.
W ostrej amebiazie jelitowej minocyklina może być użytecznym dodatkiem do środków amebicydowych.
W ciężkim trądziku minocyklina może być użyteczną terapią wspomagającą.
Minocyklina doustna jest wskazana w leczeniu bezobjawowych nosicieli Neisseria meningitidis w celu eliminacji meningokoków z nosogardzieli. W celu zachowania przydatności minocykliny w leczeniu bezobjawowych nosicieli meningokoków należy wykonać diagnostyczne procedury laboratoryjne, w tym serotypowanie i badanie lekowrażliwości, w celu ustalenia stanu nosicielstwa i prawidłowego leczenia. Zaleca się, aby profilaktyczne stosowanie minocykliny było zarezerwowane dla sytuacji, w których ryzyko meningokokowego zapalenia opon mózgowo-rdzeniowych jest wysokie.
Minocyklina doustna nie jest wskazana do leczenia infekcji meningokokowej.
Chociaż nie przeprowadzono kontrolowanych badań skuteczności klinicznej, ograniczone dane kliniczne wskazują, że doustny chlorowodorek minocykliny był z powodzeniem stosowany w leczeniu zakażeń wywołanych przez Mycobacterium marinum.
celu ograniczenia rozwoju bakterii opornych na leki i utrzymania skuteczności MINOCIN 100 mg zawiesiny doustnej i innych leków przeciwbakteryjnych, MINOCIN zawiesina doustna powinna być stosowana wyłącznie w celu leczenia lub zapobiegania zakażeniom, co do których udowodniono lub z dużym podejrzeniem, że są powodowane przez wrażliwe bakterie. Gdy dostępne są informacje dotyczące hodowli i wrażliwości, należy je uwzględnić przy wyborze lub modyfikacji terapii przeciwbakteryjnej. W przypadku braku takich danych, lokalna epidemiologia i wzorce podatności mogą przyczynić się do empirycznego doboru terapii.
DAWKOWANIE I SPOSÓB PODAWANIA
ZWYKŁE DAWKOWANIE I CZĘSTOTLIWOŚĆ PODANIA MINOCYKLINY RÓŻNI SIĘ OD INNYCH TETRACYKLIN. PRZEKROCZENIE ZALECANEJ DAWKI MOŻE SPOWODOWAĆ ZWIĘKSZONE WYSTĘPOWANIE DZIAŁAŃ UBOCZNYCH.
Terapię należy kontynuować przez co najmniej 24 do 48 godzin po ustąpieniu objawów i gorączki.
Dotychczasowe badania wykazały, że na wchłanianie doustnej zawiesiny MINOCIN nie ma znaczącego wpływu żywność i produkty mleczne.
Farmakokinetyka minocykliny u pacjentów z zaburzeniami czynności nerek (CLCR OSTRZEŻENIA ).
W leczeniu zakażeń paciorkowcami dawkę terapeutyczną tetracykliny należy podawać przez co najmniej dziesięć dni.
Dla pacjentów pediatrycznych powyżej 8 roku życia
Zazwyczaj stosowana dawka MINOCIN dla dzieci to początkowo 4 mg/kg, a następnie 2 mg/kg co 12 godzin, aby nie przekraczać zwykłej dawki dla dorosłych.
Dorośli ludzie
Zazwyczaj stosowana dawka leku MINOCIN to początkowo 200 mg, a następnie 100 mg co 12 godzin.
W leczeniu kiły zwykłą dawkę preparatu MINOCIN należy podawać przez 10 do 15 dni. Zalecana jest ścisła obserwacja, w tym badania laboratoryjne.
Pacjenci z rzeżączką wrażliwi na penicylinę mogą być leczeni MINOCIN 50 mg, podawanym początkowo w dawce 200 mg, a następnie 100 mg co 12 godzin przez minimum 4 dni, z hodowlą po terapii w ciągu 2 do 3 dni.
W leczeniu meningokokowego stanu nosicielstwa zalecana dawka wynosi 100 mg co 12 godzin przez 5 dni.
Zakażenia Mycobacterium marinum: Chociaż nie ustalono optymalnych dawek, w ograniczonej liczbie przypadków zastosowano z powodzeniem 100 mg co 12 godzin przez 6 do 8 tygodni.
Niepowikłane zakażenia cewki moczowej, szyjki macicy lub odbytnicy u dorosłych wywołane przez Chlamydia trachomatis lub Ureaplasma urealyticum: 100 mg doustnie, co 12 godzin przez co najmniej 7 dni.
W leczeniu niepowikłanego rzeżączkowego zapalenia cewki moczowej u mężczyzn zaleca się 100 mg dwa razy dziennie doustnie przez 5 dni.
JAK DOSTARCZONE
MINOCIN (chlorowodorek minocykliny) Zawiesina doustna zawiera chlorowodorek minocykliny w ilości odpowiadającej 50 mg minocykliny na łyżeczkę (5 ml). Konserwowane propyloparabenem 0,10% i butyloparabenem 0,06% alkoholem USP 5% obj./obj. O smaku kremu.
NDC 16781-473-60 - Butelka 2 fl. Oz. (60 ml)
Przechowywać w kontrolowanej temperaturze pokojowej 20° do 25°C (68° do 77°F).
NIE ZAMRAŻAĆ.
Wyprodukowano dla: Onset Dermatologics, LLC Cumberland, RI 02864. Aktualizacja: listopad 2018
SKUTKI UBOCZNE
Ze względu na praktycznie całkowite wchłanianie minocykliny podawanej doustnie, skutki uboczne w obrębie dolnego odcinka jelita, zwłaszcza biegunka, były rzadkie. Następujące działania niepożądane obserwowano u pacjentów otrzymujących tetracykliny.
Ciało jako całość: Gorączka i przebarwienia wydzieliny.
Przewód pokarmowy: Jadłowstręt, nudności, wymioty, biegunka, niestrawność, zapalenie jamy ustnej, zapalenie języka, dysfagia, niedorozwój szkliwa, zapalenie jelit, rzekomobłoniaste zapalenie okrężnicy, zapalenie trzustki, zmiany zapalne (z przerostem kanalików) w okolicy jamy ustnej i okolicy odbytowo-płciowej.
Układ moczowo-płciowy: Zapalenie sromu i pochwy.
Toksyczność wątroby: Hiperbilirubinemia, cholestaza wątrobowa, wzrost aktywności enzymów wątrobowych, śmiertelna niewydolność wątroby i żółtaczka. Zgłaszano zapalenie wątroby, w tym autoimmunologiczne zapalenie wątroby i niewydolność wątroby (patrz ŚRODKI OSTROŻNOŚCI ).

Skóra: Łysienie, rumień guzowaty, przebarwienia paznokci, świąd, martwica toksyczno-rozpływna naskórka, zapalenie naczyń, wysypka plamkowo-grudkowa i wysypka rumieniowa. Zgłaszano złuszczające zapalenie skóry. Zgłaszano naprawione wykwity polekowe, w tym zapalenie żołędzi. Zgłaszano rumień wielopostaciowy i zespół Stevensa-Johnsona. Nadwrażliwość na światło omówiono powyżej (patrz OSTRZEŻENIA ). Zgłaszano pigmentację skóry i błon śluzowych.
Oddechowy: Kaszel, duszność, skurcz oskrzeli, zaostrzenie astmy i zapalenie płuc.
Toksyczność nerek: Śródmiąższowe zapalenie nerek. Zgłoszono podwyższenie wartości BUN i są one najwyraźniej związane z dawką (patrz OSTRZEŻENIA ). Zgłaszano odwracalną ostrą niewydolność nerek.
Układ mięśniowo-szkieletowy: Bóle stawów, zapalenie stawów, przebarwienia kości, bóle mięśni, sztywność stawów i obrzęk stawów.
Reakcje nadwrażliwości: Zgłaszano pokrzywkę, obrzęk naczynioruchowy, ból wielostawowy, anafilaksję/reakcję rzekomoanafilaktyczną (w tym wstrząs i zgony), plamicę rzekomoanafilaktyczną, zapalenie mięśnia sercowego, zapalenie osierdzia, zaostrzenie tocznia rumieniowatego układowego i nacieki w płucach z eozynofilią. Zgłaszano również przemijający zespół toczniopodobny i reakcje przypominające chorobę posurowiczą.
Krew: Zgłaszano agranulocytozę, niedokrwistość hemolityczną, trombocytopenię, leukopenię, neutropenię, pancytopenię i eozynofilię.
Ośrodkowy układ nerwowy: Drgawki, zawroty głowy, niedoczulica, parestezje, sedacja i zawroty głowy. Guz rzekomy mózgu (łagodne nadciśnienie śródczaszkowe) u dorosłych i wypukłe ciemiączka u niemowląt (patrz ŚRODKI OSTROŻNOŚCI - Ogólny ). Zgłaszano również ból głowy.
Inny: Rak tarczycy był zgłaszany po wprowadzeniu do obrotu w związku z produktami minocyklinowymi. Gdy terapia minocykliną jest podawana przez dłuższy czas, należy rozważyć monitorowanie objawów raka tarczycy. Donoszono, że tetracykliny podawane przez dłuższy czas powodują brunatno-czarne, mikroskopowe przebarwienia tarczycy. Zgłaszano przypadki nieprawidłowej czynności tarczycy.
Przebarwienia zębów u dzieci poniżej 8 roku życia (patrz OSTRZEŻENIA ), a także u dorosłych.
Zgłaszano przebarwienia jamy ustnej (w tym języka, warg i dziąseł).
U pacjentów przyjmujących MINOCIN (chlorowodorek minocykliny) zgłaszano szumy uszne i osłabienie słuchu.
Zgłoszono następujące zespoły. W niektórych przypadkach dotyczących tych zespołów odnotowano zgon. Podobnie jak w przypadku innych ciężkich działań niepożądanych, w przypadku rozpoznania któregokolwiek z tych zespołów, lek należy natychmiast odstawić:
Zespół nadwrażliwości składający się z reakcji skórnej (takiej jak wysypka lub złuszczające zapalenie skóry), eozynofilii i jednego lub więcej z następujących: zapalenie wątroby, zapalenie płuc, zapalenie nerek, zapalenie mięśnia sercowego i zapalenie osierdzia. Może występować gorączka i powiększenie węzłów chłonnych.
Zespół toczniopodobny składający się z dodatniego przeciwciała przeciwjądrowego; bóle stawów, zapalenie stawów, sztywność stawów lub obrzęk stawów; oraz jedno lub więcej z następujących: gorączka, bóle mięśni, zapalenie wątroby, wysypka i zapalenie naczyń.
Zespół przypominający chorobę posurowiczą polegający na gorączce; pokrzywka lub wysypka; oraz bóle stawów, zapalenie stawów, sztywność stawów lub obrzęk stawów i powiększenie węzłów chłonnych. Może występować eozynofilia.
Aby zgłosić PODEJRZEWANE DZIAŁANIA NIEPOŻĄDANE, należy skontaktować się z Valeant Pharmaceuticals North America LLC pod numerem 1-800-321-4576 lub FDA pod numerem 1-800-FDA-1088 lub www.fda.gov/medwatch.
INTERAKCJE Z LEKAMI
Ponieważ wykazano, że tetracykliny zmniejszają aktywność protrombiny w osoczu, pacjenci leczeni antykoagulantami mogą wymagać zmniejszenia dawki leków przeciwzakrzepowych.
Ponieważ leki bakteriostatyczne mogą zakłócać bakteriobójcze działanie penicyliny, zaleca się unikanie podawania leków z grupy tetracyklin w połączeniu z penicyliną.
Wchłanianie tetracyklin jest zaburzone przez leki zobojętniające kwasy zawierające glin, wapń lub magnez oraz preparaty zawierające żelazo.
Istnieją doniesienia, że jednoczesne stosowanie tetracykliny i metoksyfluranu powoduje śmiertelną toksyczność nerkową.
Jednoczesne stosowanie tetracyklin z doustnymi środkami antykoncepcyjnymi może zmniejszyć skuteczność doustnych środków antykoncepcyjnych.
Należy unikać podawania izotretynoiny na krótko przed, w trakcie i wkrótce po terapii minocykliną. Każdy sam lek był związany z rzekomym guzem mózgu (patrz ŚRODKI OSTROŻNOŚCI ).
Zwiększone ryzyko zatrucia sporyszem, gdy alkaloidy sporyszu lub ich pochodne są podawane z tetracyklinami.
OSTRZEŻENIA
Rozwój zębów
MINOCIN Oral Suspension, podobnie jak inne antybiotyki z grupy tetracyklin, może powodować uszkodzenie płodu po podaniu kobiecie w ciąży. W przypadku stosowania jakiejkolwiek tetracykliny w okresie ciąży lub w przypadku zajścia w ciążę podczas przyjmowania tych leków, pacjentkę należy poinformować o potencjalnym zagrożeniu dla płodu. Stosowanie leków z klasy tetracyklin w okresie rozwoju zębów (ostatnia połowa ciąży, niemowlęctwa, dzieciństwa do 8 roku życia) może powodować trwałe przebarwienia zębów (żółtoszaro-brązowe).
Ta reakcja niepożądana występuje częściej podczas długotrwałego stosowania leku, ale była obserwowana po powtarzanych krótkotrwałych kursach. Zgłaszano również hipoplazję szkliwa. W związku z tym nie należy stosować tetracyklin podczas rozwoju zębów, chyba że inne leki prawdopodobnie nie będą skuteczne lub są przeciwwskazane.
Rozwój szkieletu
Wszystkie tetracykliny tworzą stabilny kompleks wapnia w każdej tkance tworzącej kości. Spadek tempa wzrostu kości strzałkowej zaobserwowano u wcześniaków, którym podawano doustnie tetracyklinę w dawkach 25 mg/kg co sześć godzin. Wykazano, że reakcja ta jest odwracalna po odstawieniu leku.
Użyj w ciąży
Wyniki badań na zwierzętach wskazują, że tetracykliny przenikają przez łożysko, znajdują się w tkankach płodu i mogą mieć toksyczny wpływ na rozwijający się płód (często związany z opóźnieniem rozwoju szkieletu). U zwierząt leczonych we wczesnym okresie ciąży odnotowano dowody embriotoksyczności. Nie ustalono bezpieczeństwa stosowania preparatu MINOCIN w czasie ciąży.
Reakcja dermatologiczna
Podczas stosowania minocykliny zgłaszano wysypkę polekową z eozynofilią i objawami ogólnoustrojowymi (DRESS), w tym przypadki śmiertelne. Jeśli ten zespół zostanie rozpoznany, lek należy natychmiast odstawić.
Działanie antyanaboliczne
Antyanaboliczne działanie tetracyklin może powodować wzrost BUN. Chociaż nie stanowi to problemu u osób z prawidłową czynnością nerek, u pacjentów ze znacznie upośledzoną funkcją wyższe poziomy tetracykliny w surowicy mogą prowadzić do azotemii, hiperfosfatemii i kwasicy. W takich warunkach zaleca się monitorowanie kreatyniny i BUN, a całkowita dawka dobowa nie powinna przekraczać 200 mg w ciągu 24 godzin (patrz DAWKOWANIE I SPOSÓB PODAWANIA ). Jeśli występuje zaburzenie czynności nerek, nawet zwykłe dawki doustne lub pozajelitowe mogą prowadzić do ogólnoustrojowej kumulacji leku i możliwej toksyczności dla wątroby.
Światłoczułość
U niektórych osób przyjmujących tetracykliny obserwowano nadwrażliwość na światło objawiającą się nadmierną reakcją na oparzenia słoneczne. Zostało to zgłoszone w przypadku minocykliny.
Skutki dla centralnego układu nerwowego
Działania niepożądane ze strony ośrodkowego układu nerwowego, w tym uczucie pustki w głowie, zawroty głowy lub zawroty głowy zgłaszano podczas terapii minocykliną. Pacjentów, u których występują te objawy, należy ostrzec przed prowadzeniem pojazdów lub używaniem niebezpiecznych maszyn podczas leczenia minocykliną. Objawy te mogą zniknąć podczas leczenia i zwykle szybko ustępują po odstawieniu leku.
Biegunka związana z Clostridium Difficile
Biegunkę związaną z Clostridium difficile (CDAD) zgłaszano po zastosowaniu prawie wszystkich środków przeciwbakteryjnych, w tym leku MINOCIN 50 mg, a jej nasilenie może wahać się od łagodnej biegunki do zapalenia okrężnicy zakończonego zgonem. Leczenie środkami przeciwbakteryjnymi zmienia normalną florę okrężnicy, prowadząc do przerostu C. difficile.
C. difficile wytwarza toksyny A i B, które przyczyniają się do rozwoju CDAD. Szczepy C. difficile wytwarzające hipertoksyny powodują zwiększoną zachorowalność i śmiertelność, ponieważ zakażenia te mogą być oporne na leczenie przeciwbakteryjne i mogą wymagać kolektomii. CDAD należy rozważyć u wszystkich pacjentów, u których po zastosowaniu antybiotyków wystąpi biegunka. Konieczna jest staranna historia choroby, ponieważ donoszono, że CDAD występuje w ciągu dwóch miesięcy po podaniu leków przeciwbakteryjnych.
W przypadku podejrzenia lub potwierdzenia CDAD, może być konieczne przerwanie trwającego stosowania antybiotyków, które nie są skierowane przeciwko C. difficile. W zależności od wskazań klinicznych należy wdrożyć odpowiednią gospodarkę wodno-elektrolitową, suplementację białka, antybiotykoterapię C. difficile oraz ocenę chirurgiczną.
Nadwrażliwość na siarczyn sodu
MINOCIN Oral Suspension zawiera siarczyn sodu, siarczyn, który może powodować reakcje typu alergicznego, w tym objawy anafilaktyczne i zagrażające życiu lub mniej ciężkie epizody astmy u niektórych podatnych osób. Ogólna częstość występowania wrażliwości na siarczyny w populacji ogólnej jest nieznana i prawdopodobnie niska. Wrażliwość na siarczyny obserwuje się częściej u osób z astmą niż u osób bez astmy.
Nadciśnienie śródczaszkowe
Nadciśnienie śródczaszkowe (IH, pseudotumor cerebri) jest związane ze stosowaniem tetracyklin, w tym MINOCIN. Objawy kliniczne IH obejmują ból głowy, niewyraźne widzenie, podwójne widzenie i utratę wzroku; papilledema można znaleźć w fundoskopii. Kobiety w wieku rozrodczym, które mają nadwagę lub przebyły IH, są bardziej narażone na rozwój IH związanego z tetracykliną. Należy unikać jednoczesnego stosowania izotretynoiny i MINOCIN, ponieważ wiadomo, że izotretynoina powoduje również guz rzekomy mózgu.
Chociaż IH zwykle ustępuje po przerwaniu leczenia, istnieje możliwość trwałej utraty wzroku. Jeśli podczas leczenia pojawią się objawy wzrokowe, konieczna jest szybka ocena okulistyczna. Ponieważ ciśnienie śródczaszkowe może pozostawać podwyższone przez kilka tygodni po odstawieniu leku, pacjentów należy monitorować do czasu ich stabilizacji.
ŚRODKI OSTROŻNOŚCI
Ogólny
Podobnie jak w przypadku innych preparatów antybiotykowych, stosowanie tego leku może spowodować przerost niewrażliwych organizmów, w tym grzybów. W przypadku wystąpienia nadkażenia należy odstawić antybiotyk i wdrożyć odpowiednie leczenie.
Hepatotoksyczność zgłaszano w przypadku minocykliny; dlatego minocyklinę należy stosować ostrożnie u pacjentów z zaburzeniami czynności wątroby oraz w połączeniu z innymi lekami hepatotoksycznymi.
Nacięcie i drenaż lub inne zabiegi chirurgiczne należy wykonywać w połączeniu z antybiotykoterapią, gdy jest to wskazane.
Jest mało prawdopodobne, aby przepisywanie doustnej zawiesiny MINOCIN w przypadku braku udowodnionego lub silnie podejrzewanego zakażenia bakteryjnego lub wskazania profilaktycznego przyniosło korzyść pacjentowi i zwiększyło ryzyko rozwoju bakterii lekoopornych.
Testy laboratoryjne
Należy przeprowadzać okresowe badania laboratoryjne układów narządów, w tym krwiotwórczych, nerkowych i wątrobowych.
Wszyscy chorzy na rzeżączkę powinni mieć w momencie rozpoznania badanie serologiczne na kiłę. Pacjenci leczeni minocykliną powinni mieć po 3 miesiącach kontrolne badanie serologiczne w kierunku kiły.
Interakcje leków/testów laboratoryjnych
Fałszywe podwyższenie poziomu katecholamin w moczu może wystąpić z powodu interferencji z testem fluorescencyjnym.
rakotwórczość, mutageneza, upośledzenie płodności
Podawanie w diecie minocykliny w długoterminowych badaniach rakotwórczości u szczurów skutkowało dowodami na wytwarzanie guza tarczycy. Stwierdzono również, że minocyklina powoduje przerost tarczycy u szczurów i psów. Ponadto, w badaniach z pokrewnym antybiotykiem, oksytetracykliną (tj. nowotwory nadnerczy i przysadki), pojawiły się dowody na działanie onkogenne u szczurów. Podobnie, chociaż nie przeprowadzono badań mutagenności minocykliny, pozytywne wyniki w testach in vitro na komórkach ssaków (tj. chłoniaka myszy i komórek płuc chomika chińskiego) odnotowano dla powiązanych antybiotyków (chlorowodorek tetracykliny i oksytetracyklina). Badania segmentu I (płodność i ogólna reprodukcja) dostarczyły dowodów na to, że minocyklina upośledza płodność u samców szczurów.
Ciąża
Podsumowanie ryzyka
Wszystkie ciąże mają podstawowe ryzyko wad wrodzonych, utraty lub innych niekorzystnych skutków, niezależnie od ekspozycji na lek. Nie ma odpowiednich i dobrze kontrolowanych badań dotyczących stosowania minocykliny u kobiet w ciąży. Minocyklina, podobnie jak inne antybiotyki z grupy tetracyklin, przenika przez łożysko i może powodować uszkodzenie płodu po podaniu kobiecie w ciąży. Po wprowadzeniu produktu do obrotu zgłaszano rzadkie spontaniczne zgłoszenia wad wrodzonych, w tym redukcji kończyn. Dostępne są tylko ograniczone informacje dotyczące tych raportów; dlatego nie można ustalić związku przyczynowego. Jeśli minocyklina jest stosowana w czasie ciąży lub jeśli pacjentka zajdzie w ciążę podczas przyjmowania tego leku, pacjentkę należy poinformować o potencjalnym zagrożeniu dla płodu.
Efekty nieteratogenne: (patrz OSTRZEŻENIA ).
Praca i dostawa
Wpływ tetracyklin na poród i poród nie jest znany.
Matki karmiące
Tetracykliny przenikają do mleka ludzkiego. Ze względu na możliwość wystąpienia poważnych działań niepożądanych wywołanych tetracyklinami u niemowląt karmionych piersią, należy podjąć decyzję, czy przerwać karmienie piersią, czy przerwać stosowanie leku, biorąc pod uwagę znaczenie leku dla matki (patrz OSTRZEŻENIA ).
Zastosowanie pediatryczne
Minocyklina nie jest zalecana do stosowania u dzieci w wieku poniżej 8 lat, chyba że oczekiwane korzyści z leczenia przewyższają ryzyko (patrz OSTRZEŻENIA ).
Zastosowanie geriatryczne
Badania kliniczne doustnej minocykliny nie obejmowały wystarczającej liczby osób w wieku 65 lat i starszych, aby ustalić, czy reagują oni inaczej niż osoby młodsze. Ogólnie rzecz biorąc, dobór dawki u pacjentów w podeszłym wieku powinien być ostrożny, zwykle zaczynając od dolnej granicy zakresu dawkowania, co odzwierciedla większą częstość pogorszenia czynności wątroby, nerek lub serca oraz współistniejących chorób lub innych leków (patrz OSTRZEŻENIA , DAWKOWANIE I SPOSÓB PODAWANIA ).
MINOCIN 50 mg zawiesina doustna zawiera 4,3 mg (0,18 mEq) sodu w 5 ml.
PRZEDAWKOWAĆ
Zdarzeniami niepożądanymi częściej obserwowanymi po przedawkowaniu są zawroty głowy, nudności i wymioty.
Nie jest znane żadne specyficzne antidotum na minocyklinę.
W przypadku przedawkowania należy odstawić leki, leczyć objawowo i zastosować środki wspomagające. Minocyklina nie jest usuwana w znaczących ilościach przez hemodializę lub dializę otrzewnową.
PRZECIWWSKAZANIA
Lek ten jest przeciwwskazany u osób, u których stwierdzono nadwrażliwość na którąkolwiek z tetracyklin lub na którykolwiek ze składników preparatu.
FARMAKOLOGIA KLINICZNA
Po podaniu pojedynczej dawki dwóch 100 mg kapsułek napełnionych proszkiem chlorowodorku minocykliny dziesięciu normalnym dorosłym ochotnikom, poziomy w surowicy wahały się od 0,74 do 4,45 mcg/ml w ciągu 1 godziny (średnio 2,24); po 12 godzinach wahały się od 0,34 do 2,36 mcg/ml (średnio 1,25). Okres półtrwania w surowicy po podaniu pojedynczej dawki 200 mg u 12 zasadniczo zdrowych ochotników wahał się od 11 do 17 godzin. U 7 chorych z dysfunkcją wątroby wahał się od 11 do 16 godzin, au 5 chorych z dysfunkcją nerek od 18 do 69 godzin. Odzysk minocykliny z moczem i kałem po podaniu 12 zdrowym ochotnikom wynosił od połowy do jednej trzeciej tego, co w przypadku innych tetracyklin.
Mikrobiologia
Mechanizm akcji
Tetracykliny są głównie bakteriostatyczne i uważa się, że wywierają działanie przeciwdrobnoustrojowe poprzez hamowanie syntezy białek. Tetracykliny, w tym minocyklina, mają podobne spektrum działania przeciwdrobnoustrojowego przeciwko szerokiej gamie organizmów Gram-dodatnich i Gram-ujemnych. Powszechna jest oporność krzyżowa tych organizmów na tetracyklinę.
Aktywność przeciwbakteryjna
Wykazano, że minocyklina jest aktywna przeciwko większości szczepów następujących mikroorganizmów, zarówno in vitro, jak i w zakażeniach klinicznych, jak opisano w WSKAZANIA Sekcja:
Bakterie Gram-dodatnie
Bacillus anthracis Listeria monocytogenes Staphylococcus aureus Streptococcus pneumoniae
Bakterie Gram-ujemne
Bartonella bacilliformis Brucella spp Klebsiella granulomatis Campylobacter fetus Francisella tularensis Haemophilus ducreyi Vibrio cholerae Yersinia pestis Acinetobacter spp Enterobacter aerogenes Escherichia coli Haemophilus influenzae Klebsiella spp Neisseria gonorrhoeae Neissgeria meningiti
Inne mikroorganizmy
Gatunek Actinomyces Borrelia recurrentis Chlamydophila psittaci Chlamydia trachomatis Gatunek Clostridium Gatunek Entamoeba Gatunek Fusobacterium nucleatum podgatunek fusiforme Mycobacterium marinum Mycoplasma pneumoniae Propionibacterium acnes Rickettsiae Podgatunek Treponema pallidum podgatunek pallidum
Testy podatności
Aby uzyskać szczegółowe informacje dotyczące kryteriów interpretacyjnych testu wrażliwości i powiązanych metod badawczych oraz standardów kontroli jakości uznanych przez FDA dla tego leku, zobacz: https://www.fda.gov/STIC.
Farmakologia i toksykologia zwierząt
Zaobserwowano, że Minocyklina HCl powoduje ciemne przebarwienie tarczycy u zwierząt doświadczalnych (szczury, świnki miniaturowe, psy i małpy). U szczurów przewlekłe leczenie chlorowodorkiem minocykliny spowodowało wole, któremu towarzyszył zwiększony wychwyt radioaktywnego jodu i dowody na wytwarzanie guza tarczycy. Stwierdzono również, że chlorowodorek minocykliny powoduje przerost tarczycy u szczurów i psów.
INFORMACJA O PACJENCIE
Biegunka jest częstym problemem powodowanym przez antybiotyki, który zwykle kończy się wraz z odstawieniem antybiotyku. Czasami po rozpoczęciu leczenia antybiotykami u pacjentów mogą pojawić się wodniste i krwawe stolce (ze skurczami żołądka i gorączką lub bez), nawet po dwóch lub więcej miesiącach od przyjęcia ostatniej dawki antybiotyku. W takim przypadku pacjenci powinni jak najszybciej skontaktować się z lekarzem.
niektórych osób przyjmujących tetracykliny obserwowano nadwrażliwość na światło objawiającą się nadmierną reakcją na oparzenia słoneczne. Pacjentów, którzy mogą być narażeni na bezpośrednie działanie promieni słonecznych lub ultrafioletowych, należy pouczyć, że taka reakcja może wystąpić po podaniu tetracyklin, a leczenie należy przerwać w przypadku wystąpienia pierwszych objawów rumienia skóry. Ta reakcja została zgłoszona podczas stosowania minocykliny.
Pacjentów, u których występują objawy ze strony ośrodkowego układu nerwowego, należy ostrzec przed prowadzeniem pojazdów lub używaniem niebezpiecznych maszyn podczas leczenia minocykliną (patrz OSTRZEŻENIA ).
Jednoczesne stosowanie tetracykliny z doustnymi środkami antykoncepcyjnymi może zmniejszać skuteczność doustnych środków antykoncepcyjnych (patrz INTERAKCJE Z LEKAMI ).
Pacjentów należy pouczyć, że leki przeciwbakteryjne, w tym MINOCIN 50 mg zawiesina doustna, powinny być stosowane wyłącznie w leczeniu zakażeń bakteryjnych. Nie leczą infekcji wirusowych (np. przeziębienia). Kiedy MINOCIN Oral Suspension jest przepisywany w celu leczenia infekcji bakteryjnej, pacjenci powinni być poinformowani, że chociaż powszechne jest samopoczucie na początku leczenia, lek należy przyjmować dokładnie zgodnie z zaleceniami. Pomijanie dawek lub nieukończenie pełnego cyklu terapii może (1) zmniejszyć skuteczność natychmiastowego leczenia i (2) zwiększyć prawdopodobieństwo, że bakterie rozwiną oporność i nie będą mogły być wyleczone za pomocą MINOCIN 50 mg zawiesiny doustnej lub innych leków przeciwbakteryjnych w przyszłości .
Niewykorzystane zapasy antybiotyków tetracyklinowych należy wyrzucić przed upływem terminu ważności.
