Benicar 10mg, 20mg, 40mg Olmesartan Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Benicar 40mg i jak się go stosuje?
Benicar to lek na receptę stosowany w leczeniu objawów wysokiego ciśnienia krwi (nadciśnienia). Benicar 10mg może być stosowany samodzielnie lub z innymi lekami.
Benicar jest blokerem receptora angiotensyny II lub ARB.
Nie wiadomo, czy Benicar jest bezpieczny i skuteczny u dzieci w wieku poniżej 6 lat.
Jakie są możliwe skutki uboczne Benicar 40mg?
Benicar może powodować poważne skutki uboczne, w tym:
- zawroty
- małe lub brak oddawania moczu
- obrzęk dłoni lub stóp
- mdłości
- słabość
- mrowienie uczucie
- ból w klatce piersiowej
- szybkie lub nieregularne bicie serca
- utrata ruchu
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Najczęstsze skutki uboczne Benicar to:
- zawroty głowy
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Benicar. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OSTRZEŻENIE
TOKSYCZNOŚĆ PŁODU
- W przypadku wykrycia ciąży należy jak najszybciej odstawić Benicar 40mg [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI]
- Leki działające bezpośrednio na układ renina-angiotens w organizmie mogą spowodować obrażenia i śmierć rozwijającego się płodu [patrz OSTRZEŻENIA I ŚRODKI OSTROŻNOŚCI]
OPIS
Medoksomil olmesartanu, prolek, jest hydrolizowany do olmesartanu podczas wchłaniania z przewodu pokarmowego. Olmesartan jest selektywnym antagonistą receptora angiotensyny II podtypu AT1.
Medoksomil olmesartanu jest opisany chemicznie jako 2,3-dihydroksy-2-butenyl 4-(1 hydroksy-1-metyloetylo)-2-propylo-1-[p-(o-1H-tetrazol-5-ilofenylo)benzylo]imidazol- 5 karboksylan, cykliczny 2,3-węglan.
Jego wzór empiryczny to C29H30N6O6, a wzór strukturalny to:
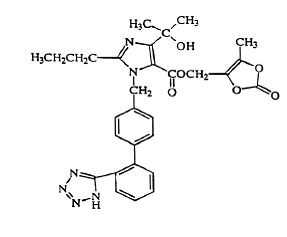
Olmesartan medoksomil jest proszkiem o barwie od białej do jasnożółtawobiałej lub krystalicznym proszkiem o masie cząsteczkowej 558,59. Jest praktycznie nierozpuszczalny w wodzie i słabo rozpuszczalny w metanolu. Benicar 20 mg jest dostępny do stosowania doustnego w postaci tabletek powlekanych zawierających 5 mg, 20 mg lub 40 mg medoksomilu olmesartanu i następujące składniki nieaktywne: hydroksypropyloceluloza, hypromeloza, laktoza jednowodna, niskopodstawiona hydroksypropyloceluloza, stearynian magnezu, celuloza mikrokrystaliczna , talk, dwutlenek tytanu i (tylko 5 mg) żółty tlenek żelaza.
WSKAZANIA
Benicar 40 mg jest wskazany w leczeniu nadciśnienia tętniczego u dorosłych i dzieci w wieku sześciu lat i starszych, w celu obniżenia ciśnienia krwi. Obniżenie ciśnienia krwi zmniejsza ryzyko śmiertelnych i niezakończonych zgonem zdarzeń sercowo-naczyniowych, głównie udarów i zawałów mięśnia sercowego. Korzyści te zaobserwowano w kontrolowanych badaniach leków przeciwnadciśnieniowych z wielu różnych klas farmakologicznych, w tym klasy, do której ten lek zasadniczo należy. Nie ma kontrolowanych badań wykazujących zmniejszenie ryzyka przy stosowaniu Benicar.
Kontrola wysokiego ciśnienia krwi powinna być częścią kompleksowego zarządzania ryzykiem sercowo-naczyniowym, w tym, w stosownych przypadkach, kontroli lipidów, leczenia cukrzycy, leczenia przeciwzakrzepowego, zaprzestania palenia, ćwiczeń i ograniczonego spożycia sodu. Wielu pacjentów będzie wymagało więcej niż jednego leku, aby osiągnąć cele dotyczące ciśnienia krwi. Aby uzyskać szczegółowe porady dotyczące celów i zarządzania, zobacz opublikowane wytyczne, takie jak wytyczne Wspólnego Narodowego Komitetu ds. Zapobiegania, Wykrywania, Oceny i Leczenia Wysokiego Ciśnienia Krwi (JNC) w ramach National High Blood Pressure Education Program.
randomizowanych kontrolowanych badaniach klinicznych wykazano, że liczne leki przeciwnadciśnieniowe z różnych klas farmakologicznych i o różnych mechanizmach działania zmniejszają chorobowość i śmiertelność sercowo-naczyniową, i można wywnioskować, że jest to obniżenie ciśnienia krwi, a nie jakaś inna właściwość farmakologiczna leki, które są w dużej mierze odpowiedzialne za te korzyści. Największą i najbardziej spójną korzyścią dla sercowo-naczyniowych punktów końcowych było zmniejszenie ryzyka udaru mózgu, ale regularnie obserwowano również zmniejszenie zawału mięśnia sercowego i śmiertelności z przyczyn sercowo-naczyniowych.
Podwyższone ciśnienie skurczowe lub rozkurczowe powoduje zwiększone ryzyko sercowo-naczyniowe, a bezwzględny wzrost ryzyka na mmHg jest większy przy wyższym ciśnieniu krwi, tak że nawet niewielkie zmniejszenie ciężkiego nadciśnienia może przynieść znaczne korzyści. Zmniejszenie względnego ryzyka wynikającego z obniżenia ciśnienia krwi jest podobne w populacjach o różnym ryzyku bezwzględnym, więc bezwzględna korzyść jest większa u pacjentów z wyższym ryzykiem niezależnie od nadciśnienia tętniczego (na przykład pacjenci z cukrzycą lub hiperlipidemią) i takich pacjentów można oczekiwać aby skorzystać z bardziej agresywnego leczenia w celu obniżenia ciśnienia krwi.
Niektóre leki przeciwnadciśnieniowe mają mniejszy wpływ na ciśnienie krwi (jako monoterapia) u pacjentów rasy czarnej, a wiele leków przeciwnadciśnieniowych ma dodatkowe zatwierdzone wskazania i działania (np. na dusznicę bolesną, niewydolność serca lub cukrzycową chorobę nerek). Te rozważania mogą kierować wyborem terapii.
Może być stosowany samodzielnie lub w połączeniu z innymi środkami przeciwnadciśnieniowymi.
DAWKOWANIE I SPOSÓB PODAWANIA
Nadciśnienie u dorosłych
Dawkowanie musi być zindywidualizowane. Zazwyczaj zalecana dawka początkowa leku Benicar 20 mg wynosi 20 mg raz na dobę w przypadku stosowania w monoterapii u pacjentów, którzy nie są zmniejszeni objętościowo. W przypadku pacjentów wymagających dalszego obniżenia ciśnienia krwi po 2 tygodniach leczenia, dawkę preparatu Benicar można zwiększyć do 40 mg. Wydaje się, że dawki powyżej 40 mg nie dają większego efektu. Dawkowanie dwa razy dziennie nie daje żadnej przewagi nad taką samą dawką całkowitą podawaną raz dziennie.
U pacjentów z możliwym zmniejszeniem objętości wewnątrznaczyniowej (np. pacjenci leczeni lekami moczopędnymi, zwłaszcza z zaburzeniami czynności nerek) należy rozpocząć podawanie leku Benicar pod ścisłym nadzorem lekarza i rozważyć zastosowanie mniejszej dawki początkowej [patrz OSTRZEŻENIA I ŚRODKI ].
Nadciśnienie u dzieci (6 lat i starsze)
Dawkowanie musi być zindywidualizowane. W przypadku dzieci, które potrafią połykać tabletki, zwykle zalecana dawka początkowa leku Benicar wynosi 10 mg raz na dobę u pacjentów o masie ciała od 20 do
Nie zaleca się stosowania leku Benicar 10 mg u dzieci w wieku poniżej 1 roku [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
Dzieciom, które nie mogą połykać tabletek, tę samą dawkę można podać w postaci zawiesiny doraźnie opisanej poniżej [patrz FARMAKOLOGIA KLINICZNA ]. Aby podać Benicar w postaci zawiesiny, należy postępować zgodnie z poniższymi instrukcjami dotyczącymi przygotowania zawiesiny.
Przygotowanie zawiesiny (dla 200 ml zawiesiny 2 mg/ml)
Dodaj 50 ml wody oczyszczonej do bursztynowej butelki z politereftalanu etylenu (PET) zawierającej dwadzieścia tabletek Benicar 20 mg i odstaw na co najmniej 5 minut. Wstrząsać pojemnikiem przez co najmniej 1 minutę i odstawić zawiesinę na co najmniej 1 minutę. Powtórz 1-minutowe wstrząsanie i 1-minutowe stanie jeszcze cztery razy. Dodaj 100 ml ORA-Sweet® i 50 ml ORA-Plus®* do zawiesiny i dobrze wytrząsaj przez co najmniej 1 minutę. Zawiesinę należy przechowywać w lodówce w temperaturze 2-8°C (36-46°F) i przechowywać do 4 tygodni. Przed każdym użyciem dobrze wstrząsnąć zawiesiną i niezwłocznie wrócić do lodówki.
JAK DOSTARCZONE
Formy dawkowania i mocne strony
- 5 mg żółte, okrągłe, powlekane tabletki bez rowka dzielącego z wytłoczonym napisem Sankyo po jednej stronie i C12 po drugiej stronie
- 20 mg białe, okrągłe, powlekane tabletki bez rowka dzielącego z wytłoczonym napisem Sankyo po jednej stronie i C14 po drugiej stronie
- 40 mg białe, owalne, powlekane tabletki bez rowka dzielącego z wytłoczonym napisem Sankyo po jednej stronie i C15 po drugiej stronie
Składowania i stosowania
Lek Benicar jest dostarczany w postaci żółtych, okrągłych tabletek powlekanych, bez rowka dzielącego, zawierających 5 mg olmesartanu medoksomilu, w postaci białych, okrągłych, powlekanych tabletek bez rowka dzielącego, zawierających 20 mg olmesartanu medoksomilu, oraz w postaci białych, owalnych , tabletki powlekane bez rowka dzielącego zawierające 40 mg olmesartanu medoksomilu. Tabletki mają wytłoczony napis Sankyo po jednej stronie i C12, C14 lub C15 po drugiej stronie odpowiednio 5, 20 i 40 mg tabletek.
Tabletki są dostarczane w następujący sposób:
Magazynowanie
Przechowywać w temperaturze 20-25°C (68-77°F) [patrz Kontrolowana temperatura pokojowa USP].
Wyprodukowano dla Daiichi Sankyo, Inc., Basking Ridge, NJ 07920. Aktualizacja: październik 2019
SKUTKI UBOCZNE
Doświadczenie w badaniach klinicznych
Ponieważ badania kliniczne prowadzone są w bardzo zróżnicowanych warunkach, częstość występowania działań niepożądanych obserwowanych w badaniach klinicznych leku nie może być bezpośrednio porównywana z częstością w badaniach klinicznych innego leku i może nie odzwierciedlać częstości obserwowanych w praktyce.
Nadciśnienie u dorosłych
Benicar oceniano pod kątem bezpieczeństwa u ponad 3825 pacjentów/osobników, w tym ponad 3275 pacjentów leczonych z powodu nadciśnienia w kontrolowanych badaniach. Doświadczenie to obejmowało około 900 pacjentów leczonych przez co najmniej 6 miesięcy i ponad 525 przez co najmniej 1 rok. Zdarzenia były na ogół łagodne, przemijające i nie miały związku z dawką Benicar.
Analiza płci, wieku i grup rasowych nie wykazała różnic między pacjentami leczonymi Benicar 40 mg i placebo. Odsetek wycofań z powodu działań niepożądanych we wszystkich badaniach z udziałem pacjentów z nadciśnieniem wynosił 2,4% (tj. 79/3278) pacjentów leczonych Benicar 40 mg i 2,7% (tj. 32/1179) pacjentów z grupy kontrolnej. W badaniach kontrolowanych placebo jedynym działaniem niepożądanym, które wystąpiło u ponad 1% pacjentów leczonych Benicar 20 mg i występowało częściej w porównaniu z placebo, były zawroty głowy (3% w porównaniu z 1%).
Obrzęk twarzy zgłoszono u pięciu pacjentów otrzymujących Benicar. W przypadku antagonistów angiotensyny II zgłaszano obrzęk naczynioruchowy.
Nadciśnienie u dzieci
Nie stwierdzono istotnych różnic między profilem działań niepożądanych u pacjentów pediatrycznych w wieku od 1 do 16 lat a profilem zgłaszanym wcześniej u pacjentów dorosłych.
Doświadczenie pomarketingowe
Po wprowadzeniu produktu do obrotu zgłoszono następujące działania niepożądane. Ponieważ reakcje te są zgłaszane dobrowolnie w populacji o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Ciało jako całość: Astenia, obrzęk naczynioruchowy, reakcje anafilaktyczne
Przewód pokarmowy: Wymioty, enteropatia przypominająca wlewki [patrz OSTRZEŻENIA I ŚRODKI ]
Zaburzenia metabolizmu i odżywiania: Hiperkaliemia
Układ mięśniowo-szkieletowy: Rabdomioliza
Układ moczowo-płciowy: Ostra niewydolność nerek, podwyższony poziom kreatyniny we krwi
Skóra i przydatki: Łysienie, świąd, pokrzywka
Dane z jednego kontrolowanego badania i badania epidemiologicznego sugerują, że duże dawki olmesartanu mogą zwiększać ryzyko sercowo-naczyniowe (CV) u pacjentów z cukrzycą, ale ogólne dane nie są rozstrzygające. W randomizowanym, kontrolowanym placebo badaniu ROADMAP z podwójnie ślepą próbą (badanie Randomized Olmesartan And Diabetes MicroAlbuminuria Prevention, n=4447) oceniano stosowanie olmesartanu w dawce 40 mg na dobę w porównaniu z placebo u pacjentów z cukrzycą typu 2, normoalbuminurią oraz w co najmniej jeden dodatkowy czynnik ryzyka choroby sercowo-naczyniowej. W badaniu osiągnięto pierwszorzędowy punkt końcowy, opóźniony początek mikroalbuminurii, ale olmesartan nie miał korzystnego wpływu na spadek współczynnika przesączania kłębuszkowego (GFR). W grupie olmesartanu w porównaniu z grupą placebo (15 olmesartanu vs. 3 placebo, HR 4,9, 95% przedział ufności) stwierdzono zwiększoną śmiertelność z przyczyn sercowo-naczyniowych (zasądzony nagły zgon sercowy, zawał serca zakończony zgonem, udar śmiertelny, zgon z powodu rewaskularyzacji) [CI ], 1,4, 17), ale ryzyko zawału serca niezakończonego zgonem było mniejsze w przypadku olmesartanu (HR 0,64, 95% CI 0,35, 1,18).
Badanie epidemiologiczne obejmowało pacjentów w wieku 65 lat i starszych z całkowitą ekspozycją > 300 000 pacjentolat. W podgrupie pacjentów z cukrzycą otrzymujących duże dawki olmesartanu (40 mg/d) przez > 6 miesięcy, wydaje się, że istnieje zwiększone ryzyko zgonu (HR 2,0; 95% CI 1,1; 3,8) w porównaniu z podobnymi pacjentami przyjmującymi inne leki. blokery receptora angiotensyny. W przeciwieństwie do tego, stosowanie dużych dawek olmesartanu u pacjentów bez cukrzycy wydawało się wiązać ze zmniejszonym ryzykiem zgonu (HR 0,46, 95% CI 0,24, 0,86) w porównaniu z podobnymi pacjentami przyjmującymi inne blokery receptora angiotensyny. Nie zaobserwowano różnic między grupami otrzymującymi niższe dawki olmesartanu w porównaniu z innymi blokerami angiotensyny lub otrzymującymi terapię przez
Ogólnie rzecz biorąc, dane te budzą obawy dotyczące możliwego zwiększonego ryzyka sercowo-naczyniowego związanego ze stosowaniem dużych dawek olmesartanu u pacjentów z cukrzycą. Istnieją jednak obawy co do wiarygodności odkrycia zwiększonego ryzyka sercowo-naczyniowego, zwłaszcza obserwacja w dużym badaniu epidemiologicznym dotycząca poprawy przeżycia u osób bez cukrzycy o wielkości podobnej do niekorzystnego wyniku u chorych na cukrzycę.
INTERAKCJE Z LEKAMI
Środki zwiększające poziom potasu w surowicy
Jednoczesne stosowanie olmesartanu z innymi lekami blokującymi układ renina-angiotensyna, diuretykami oszczędzającymi potas (np. spironolakton, triamteren, amiloryd), suplementami potasu, substytutami soli zawierającymi potas lub innymi lekami, które mogą zwiększać stężenie potasu (np. heparyna) może prowadzić do wzrostu stężenia potasu w surowicy. Jeśli równoczesne leczenie jest uważane za konieczne, zaleca się monitorowanie stężenia potasu w surowicy.
Niesteroidowe środki przeciwzapalne, w tym selektywne inhibitory cyklooksygenazy-2 (inhibitory COX-2)
pacjentów w podeszłym wieku, odwodnionych (w tym leczonych lekami moczopędnymi) lub z zaburzeniami czynności nerek, jednoczesne podawanie NLPZ, w tym selektywnych inhibitorów COX-2, z antagonistami receptora angiotensyny II, w tym medoksomilem olmesartanu, może spowodować pogorszenie czynności nerek, w tym możliwej ostrej niewydolności nerek. Efekty te są zwykle odwracalne. Okresowo monitorować czynność nerek u pacjentów otrzymujących olmesartan medoksomil i NLPZ.
Działanie przeciwnadciśnieniowe antagonistów receptora angiotensyny II, w tym medoksomilu olmesartanu, może być osłabiane przez NLPZ, w tym selektywne inhibitory COX-2.
Podwójna blokada układu renina-angiotensyna (RAS)
Podwójna blokada RAS za pomocą antagonistów receptora angiotensyny, inhibitorów ACE lub aliskirenu wiąże się ze zwiększonym ryzykiem niedociśnienia, hiperkaliemii i zmian w czynności nerek (w tym ostrej niewydolności nerek) w porównaniu z monoterapią. Większość pacjentów otrzymujących kombinację dwóch inhibitorów RAS nie uzyskuje żadnych dodatkowych korzyści w porównaniu z monoterapią. Ogólnie należy unikać łącznego stosowania inhibitorów RAS. Ściśle monitoruj ciśnienie krwi, czynność nerek i elektrolity u pacjentów przyjmujących Benicar i inne środki, które wpływają na RAS.
Nie należy podawać aliskirenu jednocześnie z lekiem Benicar u pacjentów z cukrzycą [patrz PRZECIWWSKAZANIA ]. Należy unikać stosowania aliskirenu z Benicarem 40 mg u pacjentów z zaburzeniami czynności nerek (GFR
Lit
Podczas jednoczesnego podawania litu z antagonistami receptora angiotensyny II, w tym BENICAR, zgłaszano zwiększenie stężenia litu w surowicy i toksyczność litu. Podczas jednoczesnego stosowania należy monitorować stężenie litu w surowicy.
Chlorowodorek kolesewelamu
Równoczesne podawanie substancji wiążącej kwasy żółciowe, chlorowodorek kolesewelamu, zmniejsza ekspozycję ogólnoustrojową i maksymalne stężenie olmesartanu w osoczu. Podanie olmesartanu co najmniej 4 godziny przed chlorowodorkiem kolesewelamu zmniejszyło efekt interakcji z innymi lekami. Rozważyć podanie olmesartanu co najmniej 4 godziny przed podaniem dawki chlorowodorku kolesewelamu [patrz FARMAKOLOGIA KLINICZNA ].
OSTRZEŻENIA
Zawarte jako część "ŚRODKI OSTROŻNOŚCI" Sekcja
ŚRODKI OSTROŻNOŚCI
Toksyczność płodu
Benicar 10 mg może powodować uszkodzenie płodu, gdy jest podawany kobiecie w ciąży. Stosowanie leków działających na układ renina-angiotensyna (RAS) w drugim i trzecim trymestrze ciąży zmniejsza czynność nerek płodu oraz zwiększa zachorowalność i śmierć płodu i noworodka. Powstałe małowodzie może być związane z hipoplazją płuc płodu i deformacjami szkieletu. Potencjalne działania niepożądane u noworodków obejmują hipoplazję czaszki, bezmocz, niedociśnienie, niewydolność nerek i zgon. W przypadku wykrycia ciąży należy jak najszybciej odstawić Benicar [patrz Używaj w określonych populacjach ].
Zachorowalność u niemowląt
Nie zaleca się stosowania leku Benicar u dzieci poniżej 1. roku życia. Leki działające bezpośrednio na układ renina-angiotensyna-aldosteron (RAAS) mogą mieć wpływ na rozwój niedojrzałych nerek [patrz Używaj w określonych populacjach ].
Niedociśnienie u pacjentów z niedoborem objętości lub soli
U pacjentów z aktywowanym układem renina-angiotensyna-aldosteron, takich jak pacjenci odwodnieni i (lub) z niedoborem soli (np. leczeni dużymi dawkami leków moczopędnych), po rozpoczęciu leczenia produktem Benicar można spodziewać się objawowego niedociśnienia. Rozpocznij leczenie pod ścisłym nadzorem lekarskim i rozważ rozpoczęcie od mniejszej dawki. W przypadku wystąpienia niedociśnienia należy ułożyć pacjenta na plecach i w razie potrzeby podać dożylny wlew soli fizjologicznej [patrz DAWKOWANIE I SPOSÓB PODAWANIA ]. Przejściowa odpowiedź hipotensyjna nie jest przeciwwskazaniem do dalszego leczenia, które zwykle można kontynuować bez trudności po ustabilizowaniu się ciśnienia tętniczego.
Upośledzona funkcja nerek
wyniku hamowania układu renina-angiotensyna-aldosteron, u podatnych osób leczonych produktem Benicar można spodziewać się zmian w czynności nerek. U pacjentów, których czynność nerek może zależeć od aktywności układu renina-angiotensynaaldosteron (np. pacjenci z ciężką zastoinową niewydolnością serca), leczenie inhibitorami konwertazy angiotensyny (ACE) i antagonistami receptora angiotensyny było związane ze skąpomoczem i (lub) postępującą azotemią rzadko z ostrą niewydolnością nerek i (lub) zgonem. Podobne wyniki można oczekiwać u pacjentów leczonych lekiem Benicar [patrz DAWKOWANIE I SPOSÓB PODAWANIA , INTERAKCJE Z LEKAMI , Używaj w określonych populacjach oraz FARMAKOLOGIA KLINICZNA ].
W badaniach inhibitorów ACE u pacjentów z jednostronnym lub obustronnym zwężeniem tętnicy nerkowej zgłaszano zwiększenie stężenia kreatyniny w surowicy lub azotu mocznikowego we krwi (BUN). Nie stosowano produktu Benicar przez długi czas u pacjentów z jednostronnym lub obustronnym zwężeniem tętnicy nerkowej, ale można oczekiwać podobnych wyników.
Enteropatia typu Sprue
pacjentów przyjmujących olmesartan od miesięcy do lat po rozpoczęciu leczenia zgłaszano ciężką, przewlekłą biegunkę ze znaczną utratą masy ciała. Biopsje jelitowe pacjentów często wykazywały atrofię kosmków. Jeśli u pacjenta wystąpią te objawy podczas leczenia olmesartanem, należy wykluczyć inną etiologię. Rozważ alternatywną terapię przeciwnadciśnieniową w przypadkach, gdy nie zidentyfikowano innej etiologii.
Hiperkaliemia
U pacjentów otrzymujących Benicar należy monitorować stężenie potasu w surowicy. Leki hamujące układ renina-angiotensyna mogą powodować hiperkaliemię. Czynniki ryzyka rozwoju hiperkaliemii obejmują niewydolność nerek, cukrzycę oraz jednoczesne stosowanie leków moczopędnych oszczędzających potas, suplementów potasu i/lub substytutów soli zawierających potas [patrz INTERAKCJE Z LEKAMI ].
Toksykologia niekliniczna
rakotwórczość, mutageneza, upośledzenie płodności
Medoksomil olmesartanu nie wykazywał działania rakotwórczego, gdy był podawany szczurom z dietą przez okres do 2 lat. Najwyższa badana dawka (2000 mg/kg/dzień) była, w przeliczeniu na mg/m2, około 480 razy większa od maksymalnej zalecanej dawki dla człowieka (MRHD) wynoszącej 40 mg/dzień. Dwa badania rakotwórczości przeprowadzone na myszach, 6-miesięczne badanie zgłębnikiem u myszy z nokautem p53 i 6-miesięczne badanie podawania diety u transgenicznej myszy Hras2, w dawkach do 1000 mg/kg/dobę (około 120-krotność MRHD) , nie ujawniły dowodów na działanie rakotwórcze medoksomilu olmesartanu.
Zarówno olmesartan medoksomil, jak i olmesartan uzyskały wynik ujemny w teście transformacji komórek zarodkowych chomika syryjskiego in vitro i nie wykazały toksyczności genetycznej w teście Amesa (mutagenność bakteryjna). Wykazano jednak, że obydwa indukują aberracje chromosomalne w hodowanych komórkach in vitro (płuca chomika chińskiego) i uzyskały pozytywny wynik na mutacje kinazy tymidynowej w teście chłoniaka mysiego in vitro. Medoksomil olmesartanu dał ujemny wynik in vivo pod kątem mutacji w jelicie i nerkach MutaMouse oraz klastogenności w szpiku kostnym myszy (test mikrojądrowy) przy dawkach doustnych do 2000 mg/kg (olmesartan nie był testowany).
Na płodność szczurów nie miało wpływu podawanie medoksomilu olmesartanu w dawkach tak wysokich jak 1000 mg/kg/dobę (240-krotność MRHD) w badaniu, w którym dawkowanie rozpoczęto 2 (kobiety) lub 9 (mężczyźni) tygodnie przed kryciem.
Używaj w określonych populacjach
Ciąża
Podsumowanie ryzyka
Benicar 10 mg może powodować uszkodzenie płodu, gdy jest podawany kobiecie w ciąży. Stosowanie leków działających na układ renina-angiotensyna w drugim i trzecim trymestrze ciąży zmniejsza czynność nerek płodu oraz zwiększa śmiertelność i śmiertelność płodu i noworodka. W większości badań epidemiologicznych oceniających nieprawidłowości płodu po ekspozycji na leki hipotensyjne w pierwszym trymestrze nie odróżniano leków wpływających na układ renina-angiotensyna od innych leków hipotensyjnych. W badaniach na zwierzętach dotyczących reprodukcji, leczenie produktem Benicar podczas organogenezy powodowało zwiększenie toksyczności zarodkowo-płodowej u szczurów w dawkach mniejszych niż dawki toksyczne dla matki.
W przypadku wykrycia ciąży należy jak najszybciej odstawić Benicar. Rozważ alternatywną terapię przeciwnadciśnieniową w czasie ciąży.
Szacowane ryzyko tła poważnych wad wrodzonych i poronienia dla wskazanej populacji jest nieznane. Wszystkie ciąże wiążą się z ryzykiem wady wrodzonej, utraty lub innych niekorzystnych skutków. W ogólnej populacji Stanów Zjednoczonych szacowane podstawowe ryzyko poważnych wad wrodzonych i poronienia w klinicznie rozpoznanych ciążach wynosi odpowiednio 2–4% i 15%–20%.
Rozważania kliniczne
Związane z chorobą ryzyko matki i/lub zarodka/płodu
Nadciśnienie w ciąży zwiększa ryzyko wystąpienia u matki stanu przedrzucawkowego, cukrzycy ciążowej, przedwczesnego porodu i powikłań porodowych (np. konieczności cięcia cesarskiego i krwotoku poporodowego). Nadciśnienie zwiększa ryzyko zahamowania wzrostu płodu i zgonu wewnątrzmacicznego u płodu. Kobiety w ciąży z nadciśnieniem powinny być dokładnie monitorowane i odpowiednio leczone.
Działania niepożądane u płodu/noworodka
Małowodzio u kobiet w ciąży, które stosują leki wpływające na układ renina-angiotensyna w drugim i trzecim trymestrze ciąży, może powodować: zaburzenia czynności nerek płodu prowadzące do bezmoczu i niewydolności nerek, niedorozwój płuc płodu, deformacje szkieletu, w tym niedorozwój czaszki, niedociśnienie i śmierć. U pacjentek przyjmujących Benicar 20mg w czasie ciąży należy wykonywać seryjne badania USG w celu oceny środowiska wewnątrzowodniowego. Testy płodu mogą być odpowiednie w zależności od tygodnia ciąży. Pacjenci i lekarze powinni być jednak świadomi, że małowodzie może pojawić się dopiero po nieodwracalnym uszkodzeniu płodu.
Uważnie obserwuj niemowlęta z historią ekspozycji in utero na Benicar 40 mg pod kątem niedociśnienia, skąpomoczu i hiperkaliemii. U noworodków z historią ekspozycji in utero na Benicar, jeśli wystąpi skąpomocz lub niedociśnienie, należy zastosować środki w celu utrzymania odpowiedniego ciśnienia krwi i perfuzji nerek. Transfuzje wymienne lub dializy mogą być wymagane jako sposób na odwrócenie niedociśnienia i wspomaganie czynności nerek.
Dane
Dane zwierząt
Nie zaobserwowano działania teratogennego po podaniu olmesartanu medoksomilu ciężarnym samicom szczurów w dawkach doustnych do 1000 mg/kg/dobę (240-krotność maksymalnej zalecanej dawki u ludzi (MRHD) w przeliczeniu na mg/m2) lub ciężarnym samicom królików w dawkach doustnych do 1000 mg/kg mc. 1 mg/kg/dzień (połowa MRHD na podstawie mg/m2; wyższe dawki nie mogły być ocenione pod kątem wpływu na rozwój płodu, ponieważ były śmiertelne dla łani). U szczurów zaobserwowano znaczne zmniejszenie masy urodzeniowej i przyrost masy ciała młodych po dawkach ≥1,6 mg/kg/dobę, a także opóźnienia w rozwoju kamieni milowych (opóźnione oddzielenie małżowin usznych, wyrzynanie się dolnych siekaczy, pojawienie się włosów w jamie brzusznej, opadanie jąder, i oddzielenie powiek) oraz zależne od dawki zwiększenie częstości występowania rozszerzenia miedniczek nerkowych po dawkach ≥ 8 mg/kg/dobę. Dawka, przy której nie obserwuje się działania toksycznego na rozwój szczurów, wynosi 0,3 mg/kg/dzień, około jednej dziesiątej MRHD 40 mg/dzień.
Laktacja
Podsumowanie ryzyka
Brak informacji dotyczących obecności olmesartanu w mleku ludzkim, wpływu na niemowlę karmione piersią lub wpływu na produkcję mleka. Olmesartan jest wydzielany w małym stężeniu do mleka karmiących szczurów (patrz Dane ). Ze względu na możliwość wystąpienia działań niepożądanych u karmionego niemowlęcia, należy podjąć decyzję, czy przerwać karmienie piersią, czy przerwać stosowanie leku, biorąc pod uwagę znaczenie leku dla matki.
Dane
Obecność olmesartanu w mleku zaobserwowano po jednorazowym podaniu doustnym 5 mg/kg [14C] medoksomilu olmesartanu karmiącym samicom szczurów.
Zastosowanie pediatryczne
Działanie przeciwnadciśnieniowe produktu Benicar oceniano w jednym randomizowanym, podwójnie zaślepionym badaniu klinicznym u dzieci w wieku od 1 do 16 lat [patrz Studia kliniczne ]. Farmakokinetykę preparatu Benicar oceniano u dzieci w wieku od 1 do 16 lat [patrz FARMAKOLOGIA KLINICZNA ]. Benicar 10 mg był ogólnie dobrze tolerowany przez pacjentów pediatrycznych, a profil działań niepożądanych był podobny do opisanego dla dorosłych.
Nie wykazano, aby Benicar 20 mg był skuteczny w leczeniu nadciśnienia tętniczego u dzieci w wieku
Nie zaleca się stosowania leku Benicar u dzieci w wieku poniżej 1 roku [patrz OSTRZEŻENIA I ŚRODKI ]. Układ renina-angiotensyna-aldosteron (RAAS) odgrywa kluczową rolę w rozwoju nerek. Wykazano, że blokada RAAS prowadzi do nieprawidłowego rozwoju nerek u bardzo młodych myszy. Podawanie leków działających bezpośrednio na układ reninangiotensyna-aldosteron (RAAS) może zmienić normalny rozwój nerek.
Zastosowanie geriatryczne
Spośród całkowitej liczby pacjentów z nadciśnieniem, otrzymujących Benicar w badaniach klinicznych, ponad 20% było w wieku 65 lat i starszych, a ponad 5% było w wieku 75 lat i starszych. Nie zaobserwowano ogólnych różnic w skuteczności lub bezpieczeństwie między pacjentami w podeszłym wieku i młodszymi pacjentami. Inne zgłoszone doświadczenia kliniczne nie wykazały różnic w odpowiedziach między pacjentami starszymi i młodszymi, ale nie można wykluczyć większej wrażliwości niektórych osób starszych [patrz FARMAKOLOGIA KLINICZNA ].
Niewydolność wątroby
Zwiększenie AUC0-∞ i Cmax zaobserwowano u pacjentów z umiarkowanymi zaburzeniami czynności wątroby w porównaniu z tymi w dobranej grupie kontrolnej, przy wzroście AUC o około 60%. Nie zaleca się dostosowywania dawki początkowej u pacjentów z umiarkowanymi lub znacznymi zaburzeniami czynności wątroby [patrz FARMAKOLOGIA KLINICZNA ].
Zaburzenia czynności nerek
Pacjenci z niewydolnością nerek mają podwyższone stężenie olmesartanu w surowicy w porównaniu z osobami z prawidłową czynnością nerek. Po wielokrotnym podaniu AUC było około trzykrotnie większe u pacjentów z ciężkimi zaburzeniami czynności nerek (klirens kreatyniny DAWKOWANIE I SPOSÓB PODAWANIA , OSTRZEŻENIA I ŚRODKI oraz FARMAKOLOGIA KLINICZNA ].
Czarni pacjenci
Działanie przeciwnadciśnieniowe produktu Benicar 10 mg było mniejsze u pacjentów rasy czarnej (zwykle w populacji o niskiej zawartości reniny), jak zaobserwowano w przypadku inhibitorów ACE, beta-blokerów i innych blokerów receptora angiotensyny.
PRZEDAWKOWAĆ
Dostępne są ograniczone dane dotyczące przedawkowania u ludzi. Najbardziej prawdopodobnymi objawami przedawkowania byłyby niedociśnienie i tachykardia; bradykardia może wystąpić, jeśli wystąpi stymulacja przywspółczulna (błędna). W przypadku wystąpienia objawowego niedociśnienia należy rozpocząć leczenie wspomagające. Dializowalność olmesartanu jest nieznana.
PRZECIWWSKAZANIA
Nie należy podawać aliskirenu jednocześnie z lekiem Benicar 20 mg u pacjentów z cukrzycą [patrz INTERAKCJE Z LEKAMI ].
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Angiotensyna II powstaje z angiotensyny I w reakcji katalizowanej przez enzym konwertujący angiotensynę (ACE, kininaza II). Angiotensyna II jest głównym czynnikiem presyjnym układu renina-angiotensyna, którego działanie obejmuje zwężenie naczyń krwionośnych, stymulację syntezy i uwalniania aldosteronu, stymulację serca i zwrotne wchłanianie sodu w nerkach. Olmesartan blokuje zwężające naczynia działanie angiotensyny II poprzez selektywne blokowanie wiązania angiotensyny II z receptorem AT1 w mięśniach gładkich naczyń. Jego działanie jest zatem niezależne od szlaków syntezy angiotensyny II.
Receptor AT2 znajduje się również w wielu tkankach, ale nie wiadomo, czy jest on związany z homeostazą sercowo-naczyniową. Olmesartan ma ponad 12500 razy większe powinowactwo do receptora AT1 niż do receptora AT2.
Blokada układu renina-angiotensyna za pomocą inhibitorów ACE, które hamują biosyntezę angiotensyny II z angiotensyny I, jest mechanizmem wielu leków stosowanych w leczeniu nadciśnienia tętniczego. Inhibitory ACE hamują również degradację bradykininy, reakcję również katalizowaną przez ACE. Ponieważ medoksomil olmesartanu nie hamuje ACE (kininazy II), nie wpływa na odpowiedź na bradykininę. Nie wiadomo jeszcze, czy ta różnica ma znaczenie kliniczne.
Blokada receptora angiotensyny II hamuje negatywne sprzężenie zwrotne angiotensyny II na wydzielanie reniny, ale wynikająca z tego zwiększona aktywność reninowa osocza i poziomy krążącej angiotensyny II nie przezwyciężają wpływu olmesartanu na ciśnienie krwi.
Farmakodynamika
Dawki Benicar od 2,5 mg do 40 mg hamują działanie presyjne wlewu angiotensyny I. Czas trwania efektu hamującego był zależny od dawki, przy czym dawki Benicar >40 mg dawały >90% hamowania po 24 godzinach.
Stężenie angiotensyny I i angiotensyny II w osoczu oraz aktywność reninowa osocza (PRA) wzrastają po jednorazowym i wielokrotnym podaniu preparatu Benicar 10 mg zdrowym osobom i pacjentom z nadciśnieniem. Wielokrotne podawanie do 80 mg Benicar miało minimalny wpływ na poziom aldosteronu i nie miało wpływu na stężenie potasu w surowicy.
Farmakokinetyka
Wchłanianie
Medoksomil olmesartanu jest szybko i całkowicie bioaktywowany przez hydrolizę estrów do olmesartanu podczas wchłaniania z przewodu pokarmowego.
Tabletki Benicar i preparat zawiesinowy przygotowany z tabletek Benicar są biorównoważne [patrz DAWKOWANIE I SPOSÓB PODAWANIA ].
Całkowita biodostępność olmesartanu wynosi około 26%. Po podaniu doustnym maksymalne stężenie w osoczu (Cmax) olmesartanu osiągane jest po 1 do 2 godzinach. Pokarm nie wpływa na biodostępność olmesartanu. Benicar można podawać z jedzeniem lub bez jedzenia.
Dystrybucja
Objętość dystrybucji olmesartanu wynosi około 17 l. Olmesartan silnie wiąże się z białkami osocza (99%) i nie przenika do krwinek czerwonych. Wiązanie z białkami jest stałe przy stężeniach olmesartanu w osoczu znacznie przekraczających zakres osiągany przy zalecanych dawkach.
U szczurów olmesartan słabo przekraczał barierę krew-mózg, jeśli w ogóle. Olmesartan przenikał przez barierę łożyskową u szczurów i był przenoszony na płód. Olmesartan był rozprowadzany do mleka w małych ilościach u szczurów.
Metabolizm i wydalanie
Po szybkim i całkowitym przekształceniu olmesartanu medoksomilu w olmesartan podczas wchłaniania, olmesartan praktycznie nie ulega dalszemu metabolizmowi. Całkowity klirens osoczowy olmesartanu wynosi 1,3 l/h, a klirens nerkowy 0,6 l/h. Około 35% do 50% wchłoniętej dawki jest wydalane z moczem, a pozostała część wydalana jest z kałem poprzez żółć.
Wydaje się, że olmesartan jest eliminowany dwufazowo z okresem półtrwania w końcowej fazie eliminacji wynoszącym około 13 godzin. Olmesartan wykazuje liniową farmakokinetykę po pojedynczych dawkach doustnych do 320 mg i wielokrotnych dawkach doustnych do 80 mg. Stężenia olmesartanu w stanie stacjonarnym są osiągane w ciągu 3 do 5 dni i przy dawkowaniu raz na dobę nie dochodzi do kumulacji w osoczu.
Określone populacje
Pacjenci geriatryczni
Farmakokinetykę olmesartanu badano u osób w podeszłym wieku (≥65 lat). Ogólnie maksymalne stężenia olmesartanu w osoczu były podobne u młodych osób dorosłych i osób w podeszłym wieku. U osób w podeszłym wieku po podaniu wielokrotnym zaobserwowano umiarkowaną kumulację olmesartanu; AUCss, τ było o 33% większe u pacjentów w podeszłym wieku, co odpowiada około 30% zmniejszeniu CLR [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz Używaj w określonych populacjach ].
Pacjenci pediatryczni
Farmakokinetykę olmesartanu badano u dzieci i młodzieży z nadciśnieniem w wieku od 1 do 16 lat. Klirens olmesartanu u dzieci i młodzieży był podobny do klirensu u pacjentów dorosłych po dostosowaniu do masy ciała [patrz Używaj w określonych populacjach ].
Farmakokinetyka olmesartanu nie była badana u dzieci w wieku poniżej 1 roku [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
Pacjenci płci męskiej i żeńskiej
Niewielkie różnice zaobserwowano w farmakokinetyce olmesartanu u kobiet w porównaniu z mężczyznami. AUC i Cmax były o 10-15% wyższe u kobiet niż u mężczyzn.
Pacjenci z niewydolnością wątroby
Zwiększenie wartości AUC0-∞ i Cmax zaobserwowano u pacjentów z umiarkowanymi zaburzeniami czynności wątroby w porównaniu z osobami w dobranej grupie kontrolnej, przy wzroście AUC o około 60% [patrz DAWKOWANIE I SPOSÓB PODAWANIA oraz Używaj w określonych populacjach ].
Pacjenci z niewydolnością nerek
U pacjentów z niewydolnością nerek stężenia olmesartanu w surowicy były podwyższone w porównaniu z osobami z prawidłową czynnością nerek. Po wielokrotnym podaniu AUC było około trzykrotnie większe u pacjentów z ciężkimi zaburzeniami czynności nerek (klirens kreatyniny DAWKOWANIE I SPOSÓB PODAWANIA , OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
Badania interakcji leków
Środek sekwestrujący kwasy żółciowe Coesevelam
Jednoczesne podawanie 40 mg olmesartanu medoksomilu i 3750 mg chlorowodorku kolesewelamu zdrowym ochotnikom spowodowało 28% zmniejszenie Cmax i 39% zmniejszenie AUC olmesartanu. Po podaniu olmesartanu medoksomilu 4 godziny przed kolesewelamem chlorowodorkiem zaobserwowano słabsze efekty, odpowiednio o 4% i 15% zmniejszenie Cmax i AUC [patrz INTERAKCJE Z LEKAMI ].
Inne badania
W badaniach, w których olmesartan medoksomil podawano zdrowym ochotnikom jednocześnie z digoksyną lub warfaryną, nie zgłaszano istotnych interakcji.
Biodostępność olmesartanu nie była istotnie zmieniona przez jednoczesne podawanie środków zobojętniających kwas [Al(OH)3/Mg(OH)2].
Olmesartan medoksomil nie jest metabolizowany przez układ cytochromu P450 i nie ma wpływu na enzymy P450; dlatego nie oczekuje się interakcji z lekami, które hamują, indukują lub są metabolizowane przez te enzymy.
Studia kliniczne
Nadciśnienie u dorosłych
Działanie przeciwnadciśnieniowe preparatu Benicar 10 mg wykazano w siedmiu badaniach kontrolowanych placebo przy dawkach od 2,5 mg do 80 mg przez 6 do 12 tygodni, z których każde wykazało statystycznie istotne zmniejszenie szczytowego i minimalnego ciśnienia krwi. Przebadano łącznie 2693 pacjentów (2145 Benicar; 548 placebo) z nadciśnieniem pierwotnym. Benicar 40mg raz dziennie obniżał rozkurczowe i skurczowe ciśnienie krwi. Odpowiedź była zależna od dawki, jak pokazano na poniższym wykresie. Dawka Benicar 20 mg dziennie powoduje obniżenie ciśnienia krwi w pozycji siedzącej (BP) w porównaniu z placebo o około 10/6 mmHg, a dawka 40 mg dziennie powoduje obniżenie ciśnienia krwi w pozycji siedzącej o około 12/7 mmHg w porównaniu z placebo. Benicar w dawkach 10 mg większych niż 40 mg miał niewielki dodatkowy efekt. Początek działania przeciwnadciśnieniowego wystąpił w ciągu 1 tygodnia i był w większości widoczny po 2 tygodniach.
Benicar 40 mg Reakcja na dawkę Zmniejszenie ciśnienia krwi skorygowane o placebo (mmHg) 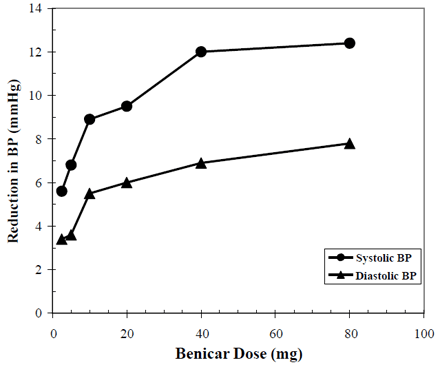
Powyższe dane pochodzą z siedmiu badań kontrolowanych placebo (2145 pacjentów Benicar, 548 pacjentów placebo). Efekt obniżania ciśnienia tętniczego utrzymywał się przez okres 24 godzin przy podawaniu Benicar raz na dobę, ze stosunkiem wartości minimalnej do szczytowej dla odpowiedzi skurczowej i rozkurczowej pomiędzy 60 a 80%.
Działanie obniżające ciśnienie krwi Benicar 40 mg z hydrochlorotiazydem lub bez hydrochlorotiazydu utrzymywało się u pacjentów leczonych przez okres do 1 roku. Nie stwierdzono tachyfilaksji podczas długotrwałego leczenia produktem Benicar ani efektu z odbicia po nagłym odstawieniu olmesartanu medoksomilu po 1 roku leczenia.
Działanie przeciwnadciśnieniowe produktu Benicar było podobne u mężczyzn i kobiet oraz u pacjentów w wieku powyżej 65 lat i młodszych. Efekt był mniejszy u pacjentów rasy czarnej (zwykle w populacji o niskiej zawartości reniny), jak zaobserwowano w przypadku inhibitorów ACE, beta-adrenolityków i innych antagonistów receptora angiotensyny. Benicar miał dodatkowe działanie obniżające ciśnienie krwi po dodaniu do hydrochlorotiazydu.
Nie ma badań z Benicarem wykazujących zmniejszenie ryzyka sercowo-naczyniowego u pacjentów z nadciśnieniem, ale przynajmniej jeden farmakologicznie podobny lek wykazał takie korzyści.
Nadciśnienie u dzieci
Działanie przeciwnadciśnieniowe produktu Benicar 40 mg w populacji pediatrycznej oceniano w randomizowanym, podwójnie zaślepionym badaniu z udziałem 302 pacjentów z nadciśnieniem w wieku od 6 do 16 lat. Badana populacja składała się z całkowicie czarnej kohorty 112 pacjentów i mieszanej rasowej kohorty 190 pacjentów, w tym 38 pacjentów rasy czarnej. Etiologia nadciśnienia była głównie nadciśnieniem pierwotnym (87% w czarnej kohorcie i 67% w mieszanej kohorcie). Pacjenci o masie ciała od 20 do
tym samym badaniu 59 pacjentów w wieku od 1 do 5 lat o masie ciała ≥5 kg otrzymywało 0,3 mg/kg Benicar 10 mg raz na dobę przez trzy tygodnie w fazie otwartej próby, a następnie zostali losowo przydzieleni do grupy otrzymującej Benicar lub placebo w podwójnie ślepej próbie. faza. Pod koniec drugiego tygodnia odstawienia średnie skurczowe/rozkurczowe ciśnienie krwi na najniższym poziomie było o 3/3 mmHg niższe w grupie randomizowanej do grupy Benicar; ta różnica w ciśnieniu krwi nie była statystycznie istotna (95% CI -2 do 7/-1 do 7).
INFORMACJA O PACJENCIE
Ciąża
Poinformuj pacjentki w wieku rozrodczym o konsekwencjach narażenia na Benicar 20mg podczas ciąży. Omów możliwości leczenia z kobietami planującymi ciążę. Powiedz pacjentkom, aby jak najszybciej zgłaszali ciążę swoim lekarzom [patrz OSTRZEŻENIA I ŚRODKI oraz Używaj w określonych populacjach ].
Laktacja
Doradzić kobietom karmiącym piersią, aby nie karmiły piersią podczas leczenia lekiem BENICAR [patrz Używaj w określonych populacjach ].
Hiperkaliemia
Poradź pacjentom, aby nie stosowali suplementów potasu lub substytutów soli zawierających potas bez konsultacji z lekarzem [patrz INTERAKCJE Z LEKAMI ].
