Vasotec 2.5mg, 5mg, 10mg Enalapril Zastosowanie, skutki uboczne i dawkowanie. Cena w aptece internetowej. Leki generyczne bez recepty.
Co to jest Vasotec i jak się go stosuje?
Vasotec to lek na receptę stosowany w leczeniu objawów wysokiego ciśnienia krwi (nadciśnienia), dysfunkcji lewej komory i zastoinowej niewydolności serca. Vasotec może być stosowany samodzielnie lub z innymi lekami.
- Vasotec należy do klasy leków zwanych inhibitorami ACE.
- Nie wiadomo, czy Vasotec jest bezpieczny i skuteczny u dzieci w wieku poniżej 1 miesiąca.
Jakie są możliwe skutki uboczne Vasotec 2,5 mg?
Vasotec 2,5 mg może powodować poważne skutki uboczne, w tym:
- zawroty,
- ból w klatce piersiowej,
- zażółcenie skóry lub oczu (żółtaczka),
- małe lub brak oddawania moczu,
- gorączka,
- dreszcze,
- ból gardła,
- mdłości,
- słabość,
- mrowienie uczucie,
- nieregularne bicie serca i
- utrata ruchu
Natychmiast uzyskaj pomoc medyczną, jeśli wystąpi którykolwiek z wymienionych powyżej objawów.
Do najczęstszych skutków ubocznych Vasotec należą:
- zawroty głowy,
- zmęczenie i
- zawroty
Poinformuj lekarza, jeśli wystąpią jakiekolwiek skutki uboczne, które Ci przeszkadzają lub które nie ustępują.
To nie wszystkie możliwe skutki uboczne Vasotecu. Aby uzyskać więcej informacji, skontaktuj się z lekarzem lub farmaceutą.
Zadzwoń do lekarza, aby uzyskać poradę medyczną na temat skutków ubocznych. Możesz zgłosić skutki uboczne do FDA pod numerem 1-800-FDA-1088.
OSTRZEŻENIE
TOKSYCZNOŚĆ PŁODU
- W przypadku wykrycia ciąży należy jak najszybciej odstawić VASOTEC®.
- Leki działające bezpośrednio na układ renina-angiotensyna mogą powodować urazy i śmierć rozwijającego się płodu. Zobacz OSTRZEŻENIA: Toksyczność dla płodu
OPIS
VASOTEC® (maleinian enalaprylu) jest solą maleinianową enalaprylu, estru etylowego długo działającego inhibitora konwertazy angiotensyny, enalaprylatu. Maleinian enalaprylu jest chemicznie opisany jako sól (Z)-2-butenodianu (S)-1[N-[1-(etoksykarbonylo)-3-fenylopropylo]-L-alanylo]-L-proliny (1:1). Jego wzór empiryczny to C20H28N2O5•C4H4O4, a wzór strukturalny to:
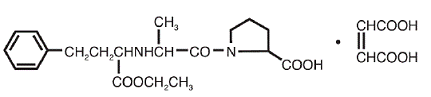
Maleinian enalaprylu jest białym lub prawie białym, krystalicznym proszkiem o masie cząsteczkowej 492,53. Jest słabo rozpuszczalny w wodzie, rozpuszczalny w etanolu i swobodnie rozpuszczalny w metanolu.
Enalapril jest prolekiem; po podaniu doustnym ulega bioaktywacji poprzez hydrolizę estru etylowego do enalaprylatu, który jest aktywnym inhibitorem konwertazy angiotensyny.
Maleinian enalaprylu jest dostarczany w postaci tabletek 2,5 mg, 5 mg, 10 mg i 20 mg do podawania doustnego. Oprócz substancji czynnej, maleinianu enalaprylu, każda tabletka zawiera następujące składniki nieaktywne: laktozę, stearynian magnezu, wodorowęglan sodu i skrobię. Tabletki 10 mg i 20 mg zawierają również tlenki żelaza.
WSKAZANIA
Nadciśnienie
VASOTEC jest wskazany w leczeniu nadciśnienia tętniczego.
VASOTEC jest skuteczny sam lub w połączeniu z innymi lekami przeciwnadciśnieniowymi, zwłaszcza diuretykami tiazydowymi. Działanie obniżające ciśnienie krwi VASOTEC 10 mg i tiazydów w przybliżeniu się sumuje.
Niewydolność serca
VASOTEC jest wskazany w leczeniu objawowej zastoinowej niewydolności serca, zwykle w połączeniu z lekami moczopędnymi i naparstnicą. U tych pacjentów VASOTEC 5 mg łagodzi objawy, zwiększa przeżywalność i zmniejsza częstość hospitalizacji (patrz FARMAKOLOGIA KLINICZNA , Niewydolność serca , Próby śmiertelności dla szczegółów i ograniczeń prób przeżycia ).
Bezobjawowa dysfunkcja lewej komory
klinicznie stabilnych bezobjawowych pacjentów z dysfunkcją lewej komory (frakcja wyrzutowa ≤ 35 procent) VASOTEC 5 mg zmniejsza tempo rozwoju jawnej niewydolności serca i zmniejsza częstość hospitalizacji z powodu niewydolności serca (patrz FARMAKOLOGIA KLINICZNA , Niewydolność serca , Próby śmiertelności dla szczegółów i ograniczeń prób przeżycia ).
Przy stosowaniu preparatu VASOTEC 2,5 mg należy wziąć pod uwagę fakt, że inny inhibitor konwertazy angiotensyny, kaptopril, powodował agranulocytozę, szczególnie u pacjentów z zaburzeniami czynności nerek lub kolagenozy naczyń krwionośnych, oraz że dostępne dane są niewystarczające, aby wykazać, że preparat VASOTEC 2,5 mg nie działa mają podobne ryzyko (patrz OSTRZEŻENIA ).
Rozważając zastosowanie preparatu VASOTEC, należy zauważyć, że w kontrolowanych badaniach klinicznych inhibitory ACE mają mniejszy wpływ na ciśnienie krwi u pacjentów rasy czarnej niż u osób innych ras. Ponadto należy zauważyć, że zgłoszono większą częstość występowania obrzęku naczynioruchowego u pacjentów rasy czarnej otrzymujących inhibitory ACE w porównaniu z osobami innych ras (patrz OSTRZEŻENIA , Obrzęk naczynioruchowy głowy i szyi ).
DAWKOWANIE I SPOSÓB PODAWANIA
Nadciśnienie
U pacjentów, którzy są obecnie leczeni lekami moczopędnymi, po podaniu początkowej dawki produktu VASOTEC może czasami wystąpić objawowe niedociśnienie. Jeśli to możliwe, lek moczopędny należy odstawić na dwa do trzech dni przed rozpoczęciem leczenia preparatem VASOTEC, aby zmniejszyć prawdopodobieństwo niedociśnienia (patrz OSTRZEŻENIA ). Jeśli ciśnienie krwi pacjenta nie jest kontrolowane za pomocą samego preparatu VASOTEC, można wznowić leczenie moczopędne.
Jeśli nie można odstawić leku moczopędnego, początkową dawkę 2,5 mg należy stosować pod nadzorem lekarza przez co najmniej dwie godziny i do czasu ustabilizowania się ciśnienia krwi przez co najmniej dodatkową godzinę (patrz OSTRZEŻENIA oraz ŚRODKI OSTROŻNOŚCI , INTERAKCJE Z LEKAMI ).
Zalecana dawka początkowa u pacjentów niestosujących leków moczopędnych wynosi 5 mg raz na dobę. Dawkowanie należy dostosować do odpowiedzi na ciśnienie krwi. Zwykle zakres dawkowania wynosi od 10 do 40 mg na dobę podawanych w pojedynczej dawce lub dwóch dawkach podzielonych. U niektórych pacjentów leczonych raz na dobę działanie przeciwnadciśnieniowe może słabnąć pod koniec przerwy w dawkowaniu. U takich pacjentów należy rozważyć zwiększenie dawki lub podawanie dwa razy na dobę. Jeśli ciśnienie krwi nie jest kontrolowane za pomocą samego VASOTEC 2,5 mg, można dodać diuretyk. Jednoczesne podawanie produktu VASOTEC 5 mg z suplementami potasu, substytutami soli potasu lub lekami moczopędnymi oszczędzającymi potas może prowadzić do zwiększenia stężenia potasu w surowicy (patrz ŚRODKI OSTROŻNOŚCI ).
Dostosowanie dawkowania u pacjentów z nadciśnieniem i zaburzeniami czynności nerek
Zazwyczaj stosowana dawka enalaprylu jest zalecana u pacjentów z klirensem kreatyniny większym niż 30 ml/min (stężenie kreatyniny w surowicy do około 3 mg/dl). U pacjentów z klirensem kreatyniny mniejszym lub równym 30 ml/min (stężenie kreatyniny w surowicy większe lub równe 3 mg/dl) pierwsza dawka wynosi 2,5 mg raz na dobę. Dawkę można zwiększać w górę, aż do uzyskania kontroli ciśnienia krwi lub maksymalnie do 40 mg na dobę.
Niewydolność serca
VASOTEC jest wskazany w leczeniu objawowej niewydolności serca, zwykle w połączeniu z lekami moczopędnymi i naparstnicą. W badaniach kontrolowanych placebo, które wykazały poprawę przeżycia, pacjenci otrzymywali dawkę tolerowaną do 40 mg, podawanych w dwóch podzielonych dawkach.
Zalecana dawka początkowa to 2,5 mg. Zalecany zakres dawkowania to 2,5 do 20 mg podawane dwa razy dziennie. Dawki należy zwiększać w górę, zgodnie z tolerancją, przez okres kilku dni lub tygodni. Maksymalna dawka dobowa podawana w badaniach klinicznych wynosiła 40 mg w dawkach podzielonych.
Po podaniu początkowej dawki preparatu VASOTEC pacjent powinien być obserwowany pod nadzorem lekarskim przez co najmniej dwie godziny i do czasu ustabilizowania się ciśnienia krwi przez co najmniej dodatkową godzinę (patrz OSTRZEŻENIA oraz INTERAKCJE Z LEKAMI ). Jeśli to możliwe, należy zmniejszyć dawkę jednocześnie stosowanego leku moczopędnego, co może zmniejszyć prawdopodobieństwo niedociśnienia. Wystąpienie niedociśnienia po podaniu początkowej dawki preparatu VASOTEC nie wyklucza późniejszego ostrożnego dostosowania dawki leku po skutecznym leczeniu niedociśnienia.
Bezobjawowa dysfunkcja lewej komory
W badaniu, w którym wykazano skuteczność, pacjenci rozpoczynali od 2,5 mg dwa razy na dobę i byli stopniowo zwiększani jako tolerowani do docelowej dawki dziennej 20 mg (w dawkach podzielonych).
Po podaniu początkowej dawki preparatu VASOTEC 10 mg pacjent powinien być obserwowany pod nadzorem lekarskim przez co najmniej dwie godziny i do czasu ustabilizowania się ciśnienia krwi przez co najmniej dodatkową godzinę (patrz OSTRZEŻENIA oraz INTERAKCJE Z LEKAMI ). Jeśli to możliwe, należy zmniejszyć dawkę jednocześnie stosowanego leku moczopędnego, co może zmniejszyć prawdopodobieństwo niedociśnienia. Wystąpienie niedociśnienia po podaniu początkowej dawki 5 mg preparatu VASOTEC nie wyklucza późniejszego ostrożnego dostosowania dawki leku po skutecznym leczeniu niedociśnienia.
Dostosowanie dawkowania u pacjentów z niewydolnością serca i niewydolnością nerek lub hiponatremią
U pacjentów z niewydolnością serca i hiponatremią (sód w surowicy poniżej 130 mEq/l) lub ze stężeniem kreatyniny w surowicy powyżej 1,6 mg/dl leczenie należy rozpocząć od dawki 2,5 mg na dobę pod ścisłym nadzorem lekarza (patrz Niewydolność serca , OSTRZEŻENIA oraz INTERAKCJE Z LEKAMI ). Dawkę można zwiększyć do 2,5 mg dwa razy na dobę, następnie do 5 mg dwa razy na dobę lub więcej w razie potrzeby, zwykle w odstępach co cztery dni lub więcej, jeśli w momencie dostosowywania dawki nie występuje nadmierne niedociśnienie lub znaczne pogorszenie czynności nerek. Maksymalna dzienna dawka to 40 mg.
Dzieci i młodzież z nadciśnieniem tętniczym
Zwykle zalecana dawka początkowa wynosi 0,08 mg/kg (do 5 mg) raz na dobę. Dawkowanie należy dostosować do odpowiedzi na ciśnienie krwi. Dawki powyżej 0,58 mg/kg (lub przekraczające 40 mg) nie były badane u dzieci i młodzieży (patrz FARMAKOLOGIA KLINICZNA , Farmakologia kliniczna u pacjentów pediatrycznych ).
VASOTEC 5 mg nie jest zalecany u noworodków i dzieci z szybkością przesączania kłębuszkowego poniżej 30 ml/min/1,73 m², ponieważ nie są dostępne żadne dane.
Przygotowanie zawiesiny (dla 200 ml zawiesiny 1,0 mg/ml)
Dodaj 50 ml Bicitra® do butelki z politereftalanu etylenu (PET) zawierającej dziesięć 20 mg tabletek VASOTEC 10 mg i wstrząsaj przez co najmniej 2 minuty. Odstawić koncentrat na 60 minut. Po upływie 60 minut wstrząsnąć koncentratem przez dodatkową minutę. Dodaj 150 ml Ora-Sweet SF™2 do koncentratu w butelce PET i wstrząśnij zawiesiną, aby rozproszyć składniki. Zawiesinę należy przechowywać w lodówce w temperaturze 2-8°C (36-46°F) i przechowywać do 30 dni. Przed każdym użyciem wstrząsnąć zawiesinę.
JAK DOSTARCZONE
Magazynowanie
Przechowywać w 25°C (77°F); wycieczki dozwolone do 15-30°C (59-86°F) [patrz Temperatura pokojowa kontrolowana przez USP ].
Przechowywać pojemnik szczelnie zamknięty.
Chronić przed wilgocią.
Dozować w szczelnym pojemniku zgodnie z USP, jeśli opakowanie produktu jest podzielone.
Wyprodukowano dla: Valeant Pharmaceuticals North America LLC Bridgewater, NJ 08807 USA. Producent: Valeant Pharmaceuticals International, Inc. Steinbach, MB R5G 1Z7 Kanada. Wersja: lipiec 2017 r.
SKUTKI UBOCZNE
VASOTEC został oceniony pod kątem bezpieczeństwa u ponad 10 000 pacjentów, w tym ponad 1000 pacjentów leczonych przez rok lub dłużej. W kontrolowanych badaniach klinicznych z udziałem 2987 pacjentów stwierdzono, że VASOTEC 10 mg jest ogólnie dobrze tolerowany. W większości niekorzystne doświadczenia miały charakter łagodny i przejściowy. W badaniach klinicznych przerwanie terapii z powodu klinicznych działań niepożądanych było wymagane u 3,3 procent pacjentów z nadciśnieniem i 5,7 procent pacjentów z niewydolnością serca. Częstość występowania działań niepożądanych nie była związana z całkowitą dawką dobową w typowych zakresach dawkowania. U pacjentów z nadciśnieniem całkowity odsetek pacjentów leczonych preparatem VASOTEC zgłaszających działania niepożądane był porównywalny z placebo.
Nadciśnienie
Poniżej przedstawiono działania niepożądane występujące u ponad jednego procenta pacjentów z nadciśnieniem leczonych preparatem VASOTEC 2,5 mg w kontrolowanych badaniach klinicznych. U pacjentów leczonych preparatem VASOTEC maksymalny czas trwania terapii wynosił trzy lata; u pacjentów otrzymujących placebo maksymalny czas trwania terapii wynosił 12 tygodni.
Niewydolność serca
Poniżej przedstawiono działania niepożądane występujące u ponad jednego procenta pacjentów z niewydolnością serca leczonych preparatem VASOTEC 5 mg. Częstości występowania odzwierciedlają doświadczenia z kontrolowanych i niekontrolowanych badań klinicznych (maksymalny czas trwania terapii wynosił około jednego roku). U pacjentów otrzymujących placebo zgłaszane częstości pochodziły z badań kontrolowanych (maksymalny czas trwania terapii wynosi 12 tygodni). Odsetek pacjentów z ciężką niewydolnością serca (klasa IV wg NYHA) wynosił 29% i 43% odpowiednio dla pacjentów leczonych VASOTEC 2,5 mg i placebo.
Inne poważne kliniczne zdarzenia niepożądane, które pojawiły się od czasu wprowadzenia leku na rynek lub zdarzenia niepożądane występujące u 0,5 do 1,0 procent pacjentów z nadciśnieniem lub niewydolnością serca w badaniach klinicznych są wymienione poniżej i dla każdej kategorii są uszeregowane według malejącego nasilenia.
Ciało jako całość
Reakcje rzekomoanafilaktyczne (patrz OSTRZEŻENIA , Reakcje rzekomoanafilaktyczne i potencjalnie powiązane ).
Układ sercowo-naczyniowy
Zatrzymanie akcji serca; zawał mięśnia sercowego lub udar naczyniowy mózgu, prawdopodobnie wtórny do nadmiernego niedociśnienia u pacjentów wysokiego ryzyka (patrz OSTRZEŻENIA , Niedociśnienie ); zator i zawał płucny; obrzęk płuc; zaburzenia rytmu obejmujące częstoskurcz przedsionkowy i bradykardię; migotanie przedsionków; kołatanie serca, zjawisko Raynauda.
Trawienny
Niedrożność jelit, zapalenie trzustki, niewydolność wątroby, zapalenie wątroby (wątrobowokomórkowe [udowodnione po ponownym podaniu] lub żółtaczka cholestatyczna) (patrz OSTRZEŻENIA , Niewydolność wątroby ), melena, anoreksja, niestrawność, zaparcia, zapalenie języka, zapalenie jamy ustnej, suchość w ustach.
Hematologiczny
Rzadkie przypadki neutropenii, małopłytkowości i zahamowania czynności szpiku kostnego.
Układ mięśniowo-szkieletowy
Skurcze mięśni.
Nerwowy/Psychiatryczny
Depresja, splątanie, ataksja, senność, bezsenność, nerwowość, neuropatia obwodowa (np. parestezje, zaburzenia czucia), zaburzenia snu.
Oddechowy
Skurcz oskrzeli, wyciek z nosa, ból gardła i chrypka, astma, infekcja górnych dróg oddechowych, nacieki w płucach, eozynofilowe zapalenie płuc.
Skóra
Złuszczające zapalenie skóry, toksyczna nekroliza naskórka, zespół Stevensa-Johnsona, pęcherzyca, półpasiec, rumień wielopostaciowy, pokrzywka, świąd, łysienie, uderzenia gorąca, obfite pocenie się, nadwrażliwość na światło.
Specjalne zmysły
Niewyraźne widzenie, zaburzenia smaku, anosmia, szum w uszach, zapalenie spojówek, suchość oczu, łzawienie.
Układ moczowo-płciowy
Niewydolność nerek, skąpomocz, zaburzenia czynności nerek (patrz ŚRODKI OSTROŻNOŚCI oraz DAWKOWANIE I SPOSÓB PODAWANIA ), ból w boku, ginekomastia, impotencja.
Różnorodny
Zgłoszono zespół objawów, który może obejmować niektóre lub wszystkie z następujących: dodatni wynik ANA, podwyższony wskaźnik sedymentacji erytrocytów, ból stawów/zapalenie stawów, bóle mięśni/zapalenie mięśni, gorączka, zapalenie błony surowiczej, zapalenie naczyń, leukocytoza, eozynofilia, nadwrażliwość na światło, wysypka i inne objawy dermatologiczne manifestacje.
Obrzęk naczynioruchowy
Obrzęk naczynioruchowy zgłaszano u pacjentów otrzymujących VASOTEC 2,5 mg, przy czym częstość występowania była częstsza u osób rasy czarnej niż u pacjentów innych ras. Obrzęk naczynioruchowy związany z obrzękiem krtani może być śmiertelny. W przypadku wystąpienia obrzęku naczynioruchowego twarzy, kończyn, warg, języka, głośni i (lub) krtani, leczenie produktem VASOTEC należy przerwać i natychmiast wdrożyć odpowiednie leczenie (patrz OSTRZEŻENIA ).
Niedociśnienie
pacjentów z nadciśnieniem niedociśnienie wystąpiło u 0,9 procenta, a omdlenia u 0,5 procenta pacjentów po podaniu dawki początkowej lub podczas przedłużonej terapii. Niedociśnienie lub omdlenia były przyczyną przerwania terapii u 0,1 procent pacjentów z nadciśnieniem. U pacjentów z niewydolnością serca niedociśnienie wystąpiło u 6,7%, a omdlenia u 2,2% pacjentów. Niedociśnienie lub omdlenia były przyczyną przerwania leczenia u 1,9% pacjentów z niewydolnością serca (patrz OSTRZEŻENIA ).
Kaszel
Widzieć ŚRODKI OSTROŻNOŚCI , Kaszel .
Pacjenci pediatryczni
Profil działań niepożądanych u pacjentów pediatrycznych wydaje się być podobny do obserwowanego u pacjentów dorosłych.
Wyniki badań laboratoryjnych klinicznych
Elektrolity w surowicy
Hiperkaliemia (patrz ŚRODKI OSTROŻNOŚCI ), hiponatremia.
Kreatynina, azot mocznikowy we krwi
kontrolowanych badaniach klinicznych niewielkie zwiększenie stężenia azotu mocznikowego we krwi i kreatyniny w surowicy, odwracalne po przerwaniu leczenia, obserwowano u około 0,2% pacjentów z nadciśnieniem pierwotnym leczonych wyłącznie preparatem VASOTEC. Zwiększenia są bardziej prawdopodobne u pacjentów przyjmujących jednocześnie leki moczopędne lub u pacjentów ze zwężeniem tętnicy nerkowej (patrz ŚRODKI OSTROŻNOŚCI ). U pacjentów z niewydolnością serca, którzy otrzymywali również leki moczopędne z naparstnicą lub bez, u około 11% pacjentów obserwowano zwiększenie stężenia azotu mocznikowego we krwi lub kreatyniny w surowicy, zwykle odwracalne po odstawieniu produktu VASOTEC 5 mg i (lub) innych jednocześnie stosowanych leków moczopędnych. Wzrost azotu mocznikowego we krwi lub kreatyniny był przyczyną przerwania leczenia u 1,2% pacjentów.
Hematologia
Niewielkie zmniejszenie stężenia hemoglobiny i hematokrytu (średnie zmniejszenie odpowiednio o około 0,3 g procent i 1,0 procent obj.) często występuje u pacjentów z nadciśnieniem lub zastoinową niewydolnością serca leczonych preparatem VASOTEC 5 mg, ale rzadko ma znaczenie kliniczne, chyba że współistnieje inna przyczyna niedokrwistości. W badaniach klinicznych mniej niż 0,1 procent pacjentów przerwało terapię z powodu anemii. Zgłaszano anemię hemolityczną, w tym przypadki hemolizy u pacjentów z niedoborem G6PD; nie można wykluczyć związku przyczynowego z enalaprylem.
Testy funkcji wątroby
Nastąpiło zwiększenie aktywności enzymów wątrobowych i (lub) stężenia bilirubiny w surowicy (patrz OSTRZEŻENIA , Niewydolność wątroby ).
Aby zgłosić PODEJRZEWANE DZIAŁANIA NIEPOŻĄDANE, należy skontaktować się z Valeant Pharmaceuticals North America LLC pod numerem 1-800-321-4576 lub FDA pod numerem 1-800-FDA-1088 lub www.fda.gov/medwatch.
INTERAKCJE Z LEKAMI
Inhibitory neprylizyny
Pacjenci przyjmujący jednocześnie inhibitory neprylizyny mogą być narażeni na zwiększone ryzyko obrzęku naczynioruchowego. (Widzieć OSTRZEŻENIA )
Podwójna blokada układu renina-angiotensyna (RAS)
Podwójna blokada RAS za pomocą antagonistów receptora angiotensyny, inhibitorów ACE lub aliskirenu wiąże się ze zwiększonym ryzykiem niedociśnienia, hiperkaliemii i zmian w czynności nerek (w tym ostrej niewydolności nerek) w porównaniu z monoterapią. Większość pacjentów otrzymujących kombinację dwóch inhibitorów RAS nie uzyskuje żadnych dodatkowych korzyści w porównaniu z monoterapią. Ogólnie należy unikać łącznego stosowania inhibitorów RAS. Ściśle monitoruj ciśnienie krwi, czynność nerek i elektrolity u pacjentów przyjmujących VASOTEC 2,5 mg i inne środki wpływające na RAS.
Nie należy podawać aliskirenu jednocześnie z preparatem VASOTEC 5 mg u pacjentów z cukrzycą. Należy unikać stosowania aliskirenu z preparatem VASOTEC u pacjentów z zaburzeniami czynności nerek (GFR
Niedociśnienie — pacjenci poddawani terapii moczopędnej
Pacjenci stosujący leki moczopędne, a zwłaszcza ci, u których niedawno wprowadzono leczenie moczopędne, mogą czasami doświadczyć nadmiernego obniżenia ciśnienia krwi po rozpoczęciu leczenia enalaprylem. Możliwość wystąpienia hipotensyjnego działania enalaprylu można zminimalizować poprzez odstawienie leku moczopędnego lub zwiększenie spożycia soli przed rozpoczęciem leczenia enalaprylem. Jeżeli konieczne jest kontynuowanie leczenia moczopędnego, należy zapewnić ścisłą kontrolę lekarską po podaniu dawki początkowej przez co najmniej dwie godziny i do czasu ustabilizowania się ciśnienia krwi przez co najmniej dodatkową godzinę (patrz OSTRZEŻENIA oraz DAWKOWANIE I SPOSÓB PODAWANIA ).
Czynniki powodujące uwolnienie Renin
Działanie przeciwnadciśnieniowe preparatu VASOTEC 10 mg jest wzmacniane przez środki przeciwnadciśnieniowe, które powodują uwalnianie reniny (np. leki moczopędne).
Niesteroidowe środki przeciwzapalne, w tym selektywne inhibitory cyklooksygenazy-2 (inhibitory COX-2)
pacjentów w podeszłym wieku, odwodnionych (w tym leczonych lekami moczopędnymi) lub z zaburzeniami czynności nerek, jednoczesne podawanie NLPZ, w tym selektywnych inhibitorów COX-2, z inhibitorami ACE, w tym enalaprylem, może spowodować pogorszenie czynności nerek, w tym możliwa ostra niewydolność nerek. Efekty te są zwykle odwracalne. Okresowo monitorować czynność nerek u pacjentów otrzymujących enalapryl i NLPZ.
W klinicznym badaniu farmakologicznym pacjentom z nadciśnieniem otrzymującym preparat VASOTEC podawano indometacynę lub sulindak. W tym badaniu nie było dowodów na osłabienie hipotensyjnego działania preparatu VASOTEC. Jednak doniesienia sugerują, że NLPZ mogą zmniejszać przeciwnadciśnieniowe działanie inhibitorów ACE.
Inne czynniki sercowo-naczyniowe
Preparat VASOTEC 10 mg stosowano jednocześnie z lekami blokującymi receptory beta-adrenergiczne, metylodopą, azotanami, lekami blokującymi wapń, hydralazyną, prazosyną i digoksyną, nie wykazując klinicznie istotnych działań niepożądanych.
Środki zwiększające poziom potasu w surowicy
VASOTEC łagodzi utratę potasu spowodowaną przez diuretyki tiazydowe. Leki moczopędne oszczędzające potas (np. spironolakton, triamteren lub amiloryd), suplementy potasu lub substytuty soli zawierające potas mogą prowadzić do znacznego zwiększenia stężenia potasu w surowicy. Dlatego, jeśli jednoczesne stosowanie tych leków jest wskazane z powodu wykazanej hipokaliemii, należy je stosować ostrożnie i często monitorować stężenie potasu w surowicy. Leki oszczędzające potas zasadniczo nie powinny być stosowane u pacjentów z niewydolnością serca otrzymujących preparat VASOTEC.
Lit
Toksyczność litu zgłaszano u pacjentów otrzymujących lit jednocześnie z lekami, które powodują eliminację sodu, w tym inhibitorami ACE. U pacjentów otrzymujących jednocześnie preparat VASOTEC i lit zgłoszono kilka przypadków toksyczności litu, które ustępowały po odstawieniu obu leków. Zaleca się częste kontrolowanie stężenia litu w surowicy, jeśli enalapryl jest podawany jednocześnie z litem.
Złoto
Reakcje po podaniu azotanów (objawy obejmują zaczerwienienie twarzy, nudności, wymioty i niedociśnienie) były rzadko zgłaszane u pacjentów leczonych złotem do wstrzykiwań (aurotiojabłczan sodu) i jednocześnie leczonych inhibitorami ACE, w tym preparatem VASOTEC.
Inhibitory mTOR (ssaczego celu rapamycyny)
Pacjenci otrzymujący jednocześnie inhibitor ACE i inhibitor mTOR (np. temsyrolimus, sirolimus, ewerolimus) mogą być narażeni na zwiększone ryzyko obrzęku naczynioruchowego (patrz OSTRZEŻENIA ).
OSTRZEŻENIA
Reakcje rzekomoanafilaktyczne i prawdopodobnie powiązane
Przypuszczalnie dlatego, że inhibitory konwertazy angiotensyny wpływają na metabolizm eikozanoidów i polipeptydów, w tym endogennej bradykininy, pacjenci otrzymujący inhibitory ACE (w tym VASOTEC) mogą być narażeni na różne działania niepożądane, niektóre z nich poważne.
Obrzęk naczynioruchowy głowy i szyi
U pacjentów leczonych inhibitorami konwertazy angiotensyny, w tym produktem VASOTEC, zgłaszano obrzęk naczynioruchowy twarzy, kończyn, warg, języka, głośni i (lub) krtani. Może to nastąpić w dowolnym momencie leczenia. W takich przypadkach należy natychmiast przerwać podawanie produktu VASOTEC 2,5 mg i zastosować odpowiednie leczenie i monitorowanie do czasu całkowitego i trwałego ustąpienia objawów przedmiotowych i podmiotowych. W przypadkach, gdy obrzęk ograniczał się do twarzy i ust, stan na ogół ustępował bez leczenia, chociaż leki przeciwhistaminowe były przydatne w łagodzeniu objawów. Obrzęk naczynioruchowy związany z obrzękiem krtani może być śmiertelny. przypadku zajęcia języka, głośni lub krtani, które mogą powodować niedrożność dróg oddechowych, należy niezwłocznie zastosować odpowiednią terapię, np. podskórny roztwór adrenaliny 1:1000 (0,3 ml do 0,5 ml) i/lub środki niezbędne do zapewnienia drożności dróg oddechowych. pod warunkiem, że (Widzieć DZIAŁANIA NIEPOŻĄDANE ).
Pacjenci otrzymujący jednocześnie inhibitor ACE i inhibitor mTOR (ssaczego celu rapamycyny) (np. temsyrolimus, sirolimus, ewerolimus) lub inhibitor neprylizyny mogą być narażeni na zwiększone ryzyko obrzęku naczynioruchowego (patrz ŚRODKI OSTROŻNOŚCI ).
Obrzęk naczynioruchowy jelit
pacjentów leczonych inhibitorami ACE zgłaszano obrzęk naczynioruchowy jelit. Pacjenci ci zgłaszali się z bólem brzucha (z nudnościami lub wymiotami lub bez nich); w niektórych przypadkach nie było wcześniej obrzęku naczynioruchowego twarzy, a poziomy C-1 esterazy były prawidłowe. Obrzęk naczynioruchowy rozpoznano za pomocą takich procedur, jak tomografia komputerowa jamy brzusznej, USG lub zabieg chirurgiczny, a objawy ustąpiły po odstawieniu inhibitora ACE. Obrzęk naczynioruchowy jelit należy uwzględnić w diagnostyce różnicowej pacjentów z bólami brzucha leczonych inhibitorami ACE.
Pacjenci z obrzękiem naczynioruchowym w wywiadzie niezwiązanym z leczeniem inhibitorem ACE mogą być narażeni na zwiększone ryzyko obrzęku naczynioruchowego podczas przyjmowania inhibitora ACE (patrz także WSKAZANIA I ZASTOSOWANIE oraz PRZECIWWSKAZANIA ).
Reakcje rzekomoanafilaktyczne podczas odczulania
Dwóch pacjentów poddawanych leczeniu odczulającemu jadem owadów błonkoskrzydłych podczas leczenia inhibitorami ACE miało zagrażające życiu reakcje rzekomoanafilaktyczne. U tych samych pacjentów można było uniknąć tych reakcji, gdy tymczasowo odstawiono inhibitory ACE, ale pojawiły się one ponownie po nieumyślnym ponownym podaniu.
Reakcje rzekomoanafilaktyczne podczas ekspozycji błonowej
Reakcje rzekomoanafilaktyczne były zgłaszane u pacjentów dializowanych z użyciem błon wysokoprzepływowych i leczonych jednocześnie inhibitorem ACE. Reakcje rzekomoanafilaktyczne zgłaszano również u pacjentów poddawanych aferezie lipoprotein o małej gęstości z wchłanianiem siarczanu dekstranu.
Niedociśnienie
Nadmierne niedociśnienie występuje rzadko u pacjentów z niepowikłanym nadciśnieniem leczonych samym VASOTEC 5 mg. U pacjentów z niewydolnością serca, którym podawano produkt VASOTEC, ciśnienie tętnicze często się zmniejszało, zwłaszcza po podaniu pierwszej dawki, ale przerwanie leczenia z powodu utrzymywania się objawowego niedociśnienia zwykle nie jest konieczne, jeśli przestrzegane są zalecenia dotyczące dawkowania; należy zachować ostrożność podczas rozpoczynania leczenia (patrz DAWKOWANIE I SPOSÓB PODAWANIA ). Pacjenci z ryzykiem nadmiernego niedociśnienia, czasami związanego ze skąpomoczem i/lub postępującą azotemią oraz rzadko z ostrą niewydolnością nerek i/lub zgonem, obejmują pacjentów z następującymi stanami lub cechami: niewydolność serca, hiponatremia, terapia dużymi dawkami leków moczopędnych, niedawno intensywna diureza lub zwiększenie dawki leku moczopędnego, dializa nerek lub ciężka objętość krwi i (lub) niedobór soli o dowolnej etiologii. Wskazane może być wyeliminowanie leku moczopędnego (z wyjątkiem pacjentów z niewydolnością serca), zmniejszenie dawki leku moczopędnego lub ostrożne zwiększenie spożycia soli przed rozpoczęciem leczenia preparatem VASOTEC 10 mg u pacjentów z ryzykiem nadmiernego niedociśnienia, którzy są w stanie tolerować takie dostosowania (patrz INTERAKCJE Z LEKAMI oraz DZIAŁANIA NIEPOŻĄDANE ). U pacjentów z ryzykiem nadmiernego niedociśnienia, leczenie należy rozpoczynać pod bardzo ścisłą kontrolą lekarską i takich pacjentów należy ściśle obserwować przez pierwsze dwa tygodnie leczenia oraz za każdym razem, gdy zwiększa się dawkę enalaprylu i (lub) leku moczopędnego. Podobne rozważania mogą dotyczyć pacjentów z chorobą niedokrwienną serca lub chorobą naczyń mózgowych, u których nadmierny spadek ciśnienia tętniczego mógłby skutkować zawałem mięśnia sercowego lub udarem naczyniowo-mózgowym.
W przypadku wystąpienia nadmiernego niedociśnienia pacjenta należy ułożyć na plecach i w razie potrzeby otrzymać dożylny wlew soli fizjologicznej. Przejściowa reakcja hipotensyjna nie jest przeciwwskazaniem do dalszych dawek VASOTEC 2,5 mg, które zwykle można podać bez trudności po ustabilizowaniu się ciśnienia krwi. W przypadku wystąpienia objawowego niedociśnienia może być konieczne zmniejszenie dawki lub odstawienie produktu VASOTEC lub jednocześnie stosowanego leku moczopędnego.
Neutropenia/agranulocytoza
Wykazano, że inny inhibitor konwertazy angiotensyny, kaptopryl, powoduje agranulocytozę i zahamowanie czynności szpiku kostnego, rzadko u pacjentów bez powikłań, ale częściej u pacjentów z zaburzeniami czynności nerek, zwłaszcza jeśli mają również kolagenozy naczyń krwionośnych. Dostępne dane z badań klinicznych enalaprylu są niewystarczające, aby wykazać, że enalapryl nie powoduje agranulocytozy w podobnym tempie. Doświadczenie marketingowe ujawniło przypadki neutropenii lub agranulocytozy, w których nie można wykluczyć związku przyczynowego z enalaprylem. Należy rozważyć okresowe monitorowanie liczby białych krwinek u pacjentów z kolagenową chorobą naczyń i chorobą nerek.
Niewydolność wątroby
Rzadko, inhibitory ACE są związane z zespołem, który zaczyna się od żółtaczki cholestatycznej i rozwija się do piorunującej martwicy wątroby i (czasami) śmierci. Mechanizm tego zespołu nie jest poznany. Pacjenci otrzymujący inhibitory ACE, u których wystąpi żółtaczka lub znaczne zwiększenie aktywności enzymów wątrobowych, powinni odstawić inhibitor ACE i poddać się odpowiedniej obserwacji lekarskiej.
Toksyczność płodu
Stosowanie leków działających na układ renina-angiotensyna w drugim i trzecim trymestrze ciąży zmniejsza czynność nerek płodu oraz zwiększa śmiertelność i śmiertelność płodu i noworodka. Powstałe małowodzie może być związane z hipoplazją płuc płodu i deformacjami szkieletu. Potencjalne działania niepożądane u noworodków obejmują hipoplazję czaszki, bezmocz, niedociśnienie, niewydolność nerek i zgon. W przypadku wykrycia ciąży należy jak najszybciej odstawić VASOTEC 10 mg. Te niekorzystne skutki są zwykle związane ze stosowaniem tych leków w drugim i trzecim trymestrze ciąży. W większości badań epidemiologicznych oceniających nieprawidłowości płodu po ekspozycji na leki hipotensyjne w pierwszym trymestrze nie odróżniano leków wpływających na układ renina-angiotensyna od innych leków hipotensyjnych. Odpowiednie leczenie nadciśnienia u matki w czasie ciąży jest ważne dla optymalizacji wyników zarówno dla matki, jak i płodu.
nietypowym przypadku, gdy nie ma odpowiedniej alternatywy dla terapii lekami wpływającymi na układ reninangiotensynowy dla konkretnego pacjenta, należy uprzedzić matkę o potencjalnym ryzyku dla płodu. Wykonuj seryjne badania ultrasonograficzne w celu oceny środowiska wewnątrzowodniowego. W przypadku zaobserwowania małowodzia należy przerwać stosowanie preparatu VASOTEC, chyba że uzna się to za ratowanie życia matki. Testy płodu mogą być odpowiednie w zależności od tygodnia ciąży. Pacjenci i lekarze powinni być jednak świadomi, że małowodzie może pojawić się dopiero po nieodwracalnym uszkodzeniu płodu. Uważnie obserwuj niemowlęta z historią ekspozycji in utero na preparat VASOTEC pod kątem niedociśnienia, skąpomoczu i hiperkaliemii (patrz ŚRODKI OSTROŻNOŚCI , Zastosowanie pediatryczne ).
W badaniach na ciężarnych szczurach i królikach nie zaobserwowano działania teratogennego enalaprylu. Na podstawie powierzchni ciała, zastosowane dawki były odpowiednio 57-krotnością i 12-krotnością maksymalnej zalecanej dawki dobowej dla ludzi (MRHDD).
ŚRODKI OSTROŻNOŚCI
Ogólny
Zwężenie aorty/Kardiomiopatia przerostowa
Podobnie jak w przypadku wszystkich leków rozszerzających naczynia, enalapryl należy stosować ostrożnie u pacjentów z niedrożnością drogi odpływu lewej komory.
Upośledzona funkcja nerek
W wyniku hamowania układu renina-angiotensyna-aldosteron można spodziewać się zmian w czynności nerek u osób wrażliwych. U pacjentów z ciężką niewydolnością serca, których czynność nerek może zależeć od aktywności układu renina-angiotensyna-aldosteron, leczenie inhibitorami konwertazy angiotensyny, w tym VASOTEC, może wiązać się ze skąpomoczem i (lub) postępującą azotemią, a rzadko z ostrą niewydolnością nerek i /lub śmierć (patrz INTERAKCJE Z LEKAMI ).
W badaniach klinicznych u pacjentów z nadciśnieniem tętniczym z jednostronnym lub obustronnym zwężeniem tętnicy nerkowej, wzrost stężenia azotu mocznikowego we krwi i kreatyniny w surowicy zaobserwowano u 20% pacjentów. Wzrosty te były prawie zawsze odwracalne po odstawieniu enalaprylu i (lub) leczenia moczopędnego. U takich pacjentów w ciągu pierwszych kilku tygodni leczenia należy monitorować czynność nerek.
niektórych pacjentów z nadciśnieniem lub niewydolnością serca bez widocznej wcześniej istniejącej choroby naczyń nerkowych wystąpił wzrost stężenia mocznika we krwi i kreatyniny w surowicy, zwykle niewielki i przemijający, zwłaszcza gdy VASOTEC podawano jednocześnie z lekiem moczopędnym. Jest to bardziej prawdopodobne u pacjentów z istniejącą wcześniej niewydolnością nerek. Może być konieczne zmniejszenie dawki i/lub odstawienie leku moczopędnego i/lub VASOTEC 5 mg.
Ocena pacjentów z nadciśnieniem lub niewydolnością serca powinna zawsze obejmować ocenę czynności nerek (Widzieć DAWKOWANIE I SPOSÓB PODAWANIA ).
Hiperkaliemia
Podwyższone stężenie potasu w surowicy (powyżej 5,7 mEq/l) obserwowano u około jednego procenta pacjentów z nadciśnieniem w badaniach klinicznych. W większości przypadków były to wartości izolowane, które ustąpiły pomimo kontynuowania terapii. Hiperkaliemia była przyczyną przerwania terapii u 0,28% pacjentów z nadciśnieniem. W badaniach klinicznych dotyczących niewydolności serca hiperkaliemię zaobserwowano u 3,8% pacjentów, ale nie stanowiła ona przyczyny przerwania leczenia.
Czynniki ryzyka rozwoju hiperkaliemii obejmują niewydolność nerek, cukrzycę oraz jednoczesne stosowanie leków moczopędnych oszczędzających potas, suplementów potasu i/lub substytutów soli zawierających potas, które należy stosować ostrożnie, jeśli w ogóle, z preparatem VASOTEC (patrz INTERAKCJE Z LEKAMI ).
Kaszel
Przypuszczalnie z powodu zahamowania degradacji endogennej bradykininy, w przypadku wszystkich inhibitorów ACE zgłaszano uporczywy kaszel nieproduktywny, który zawsze ustępował po przerwaniu leczenia. W diagnostyce różnicowej kaszlu należy uwzględnić kaszel wywołany inhibitorem ACE.
Chirurgia/znieczulenie
U pacjentów poddawanych dużym zabiegom chirurgicznym lub podczas znieczulenia środkami wywołującymi niedociśnienie, enalapryl może blokować tworzenie angiotensyny II wtórnie do kompensacyjnego uwalniania reniny. Jeśli wystąpi niedociśnienie, które uważa się za spowodowane tym mechanizmem, można je skorygować poprzez zwiększenie objętości.
rakotwórczość, mutageneza, upośledzenie płodności
Nie było dowodów na działanie rakotwórcze, gdy enalapryl był podawany przez 106 tygodni samcom i samicom szczurów w dawkach do 90 mg/kg/dobę lub przez 94 tygodnie samcom i samicom myszy w dawkach do 90 i 180 mg/kg/dobę. dzień, odpowiednio. Dawki te są 26-krotnością (u szczurów i samic myszy) i 13-krotnością (u samców myszy) maksymalnej zalecanej dawki dobowej dla człowieka (MRHDD) w porównaniu z powierzchnią ciała.
Ani maleinian enalaprylu, ani aktywny dikwas nie wykazywały działania mutagennego w teście mutagennym Amesa z lub bez aktywacji metabolicznej. Enalapril wykazał również wynik ujemny w następujących badaniach genotoksyczności: test rec, test odwrotnej mutacji E. coli, wymiana chromatyd siostrzanych z hodowanymi komórkami ssaków oraz test mikrojądrowy na myszach, jak również w badaniu cytogenetycznym in vivo z użyciem szpiku kostnego myszy .
Nie stwierdzono niekorzystnego wpływu na reprodukcję samców i samic szczurów, którym podawano enalapril w dawce do 90 mg/kg/dobę (26-krotność MRHDD w porównaniu z powierzchnią ciała).
Ciąża
Matki karmiące
Enalapryl i enalaprylat wykryto w mleku kobiecym. Ze względu na możliwość wystąpienia poważnych działań niepożądanych enalaprylu u niemowląt karmionych piersią, należy podjąć decyzję, czy przerwać karmienie piersią, czy przerwać stosowanie produktu VASOTEC 2,5 mg, biorąc pod uwagę znaczenie leku dla matki.
Zastosowanie pediatryczne
Noworodki z historią kontaktu z preparatem VASOTEC w okresie życia płodowego
przypadku wystąpienia skąpomoczu lub niedociśnienia należy zwrócić uwagę na wspomaganie ciśnienia krwi i perfuzji nerek. Transfuzje wymienne lub dializy mogą być wymagane jako sposób odwrócenia niedociśnienia i/lub zastąpienia zaburzeń czynności nerek. Enalapryl, który przenika przez łożysko, został usunięty z krążenia noworodka za pomocą dializy otrzewnowej z pewnymi korzyściami klinicznymi i teoretycznie można go usunąć za pomocą transfuzji wymiennej, chociaż brak jest doświadczeń z tą drugą procedurą.
Działanie przeciwnadciśnieniowe preparatu VASOTEC zostało ustalone u dzieci z nadciśnieniem tętniczym w wieku od 1 miesiąca do 16 lat. Stosowanie preparatu VASOTEC 5 mg w tych grupach wiekowych jest poparte dowodami z odpowiednich i dobrze kontrolowanych badań dotyczących stosowania preparatu VASOTEC 2,5 mg u dzieci i dorosłych, a także opublikowanym piśmiennictwem dotyczącym pacjentów pediatrycznych (patrz FARMAKOLOGIA KLINICZNA , Farmakologia kliniczna u pacjentów pediatrycznych oraz DAWKOWANIE I SPOSÓB PODAWANIA ).
VASOTEC nie jest zalecany u noworodków i dzieci z szybkością przesączania kłębuszkowego
PRZEDAWKOWAĆ
Dostępne są ograniczone dane dotyczące przedawkowania u ludzi.
Pojedyncze doustne dawki enalaprylu powyżej 1000 mg/kg i ≥ 1775 mg/kg były związane ze śmiertelnością odpowiednio u myszy i szczurów.
Najbardziej prawdopodobnym objawem przedawkowania byłoby niedociśnienie, w przypadku którego zwykle stosuje się dożylny wlew soli fizjologicznej.
Enalaprylat może być usuwany z krążenia ogólnego za pomocą hemodializy i został usunięty z krążenia noworodka za pomocą dializy otrzewnowej (patrz OSTRZEŻENIA , Reakcje rzekomoanafilaktyczne podczas ekspozycji błonowej ).
PRZECIWWSKAZANIA
VASOTEC 2,5 mg jest przeciwwskazany u pacjentów z nadwrażliwością na ten produkt oraz u pacjentów z obrzękiem naczynioruchowym w wywiadzie związanym z wcześniejszym leczeniem inhibitorem konwertazy angiotensyny oraz u pacjentów z dziedzicznym lub idiopatycznym obrzękiem naczynioruchowym.
Nie należy podawać aliskirenu jednocześnie z preparatem VASOTEC u pacjentów z cukrzycą (patrz INTERAKCJE Z LEKAMI ).
VASOTEC 10mg jest przeciwwskazany w połączeniu z inhibitorem neprylizyny (np. sakubitryl). Nie należy podawać produktu VASOTEC w ciągu 36 godzin od zmiany na sakubitryl/walsartan, inhibitora neprylizyny lub odwrotnie (patrz OSTRZEŻENIA ).
FARMAKOLOGIA KLINICZNA
Mechanizm akcji
Po hydrolizie do enalaprylatu enalapryl hamuje enzym konwertujący angiotensynę (ACE) u ludzi i zwierząt. ACE jest dipeptydazą peptydylową, która katalizuje konwersję angiotensyny I do substancji zwężającej naczynia, angiotensyny II. Angiotensyna II stymuluje również wydzielanie aldosteronu przez korę nadnerczy. Korzystne działanie enalaprylu w nadciśnieniu i niewydolności serca wydaje się wynikać przede wszystkim z supresji układu renina-angiotensyna-aldosteron. Hamowanie ACE powoduje zmniejszenie stężenia angiotensyny II w osoczu, co prowadzi do zmniejszenia aktywności wazopresyjnej i zmniejszenia wydzielania aldosteronu. Chociaż ten ostatni spadek jest niewielki, powoduje niewielki wzrost stężenia potasu w surowicy. U pacjentów z nadciśnieniem, leczonych wyłącznie preparatem VASOTEC przez okres do 48 tygodni, zaobserwowano średnie zwiększenie stężenia potasu w surowicy o około 0,2 mEq/l. U pacjentów leczonych preparatem VASOTEC 5 mg z diuretykiem tiazydowym zasadniczo nie stwierdzono zmiany stężenia potasu w surowicy (patrz ŚRODKI OSTROŻNOŚCI ). Usunięcie negatywnego sprzężenia zwrotnego angiotensyny II na wydzielanie reniny prowadzi do zwiększonej aktywności reninowej osocza.
ACE jest identyczny z kininazą, enzymem rozkładającym bradykininę. Nie wyjaśniono, czy zwiększone poziomy bradykininy, silnego peptydu wazodepresyjnego, odgrywają rolę w działaniu terapeutycznym preparatu VASOTEC.
Chociaż uważa się, że mechanizm, dzięki któremu VASOTEC 5 mg obniża ciśnienie krwi, polega przede wszystkim na hamowaniu układu renina-angiotensyna-aldosteron, VASOTEC 10 mg ma działanie przeciwnadciśnieniowe nawet u pacjentów z nadciśnieniem niskoreninowym. Chociaż preparat VASOTEC miał działanie przeciwnadciśnieniowe we wszystkich badanych rasach, pacjenci rasy czarnej z nadciśnieniem (zwykle populacja z niskim nadciśnieniem reniny) mieli mniejszą średnią odpowiedź na monoterapię enalaprylem niż pacjenci innych ras.
Farmakokinetyka i metabolizm
Po podaniu doustnym produktu VASOTEC maksymalne stężenie enalaprylu w surowicy występuje w ciągu około godziny. Na podstawie wydalania moczu, stopień wchłaniania enalaprilu wynosi około 60%. Na wchłanianie enalaprylu nie ma wpływu obecność pokarmu w przewodzie pokarmowym. Po wchłonięciu enalapryl jest hydrolizowany do enalaprylatu, który jest silniejszym inhibitorem konwertazy angiotensyny niż enalapryl; enalaprylat jest słabo wchłaniany po podaniu doustnym. Maksymalne stężenie enalaprylatu w surowicy występuje od trzech do czterech godzin po doustnym podaniu maleinianu enalaprylu. Produkt VASOTEC jest wydalany głównie przez nerki. Około 94 procent dawki jest odzyskiwane w moczu i kale jako enalaprylat lub enalapryl. Głównymi składnikami moczu są enalaprylat, stanowiący około 40% dawki, oraz nienaruszony enalapryl. Nie ma dowodów na istnienie metabolitów enalaprylu, innych niż enalaprylat.
Profil stężenia enalaprylatu w surowicy wykazuje przedłużoną fazę końcową, najwyraźniej stanowiącą niewielką część podanej dawki, która jest związana z ACE. Związana ilość nie zwiększa się wraz z dawką, co wskazuje na możliwe do wysycenia miejsce wiązania. Efektywny okres półtrwania kumulacji enalaprylatu po wielokrotnych dawkach maleinianu enalaprylu wynosi 11 godzin. Dyspozycja enalaprylu i enalaprylatu u pacjentów z niewydolnością nerek jest podobna do tej u pacjentów z prawidłową czynnością nerek do czasu, gdy szybkość przesączania kłębuszkowego wynosi 30 ml/min lub mniej. Przy szybkości przesączania kłębuszkowego ≤ 30 ml/min, maksymalne i minimalne stężenie enalaprylatu wzrasta, czas do osiągnięcia maksymalnego stężenia i czas do stanu stacjonarnego mogą być opóźnione. Skuteczny okres półtrwania enalaprylatu po wielokrotnych dawkach maleinianu enalaprylu jest wydłużony na tym poziomie niewydolności nerek (patrz DAWKOWANIE I SPOSÓB PODAWANIA ). Enalaprylat można dializować z szybkością 62 ml/min.
Badania na psach wskazują, że enalapryl słabo, jeśli w ogóle, przenika przez barierę krew-mózg; enalaprylat nie dostaje się do mózgu. Wielokrotne dawki maleinianu enalaprylu u szczurów nie powodują akumulacji w żadnych tkankach. Mleko karmiących szczurów zawiera radioaktywność po podaniu 14C-enalaprylu maleinianu. Stwierdzono, że radioaktywność przenika przez łożysko po podaniu znakowanego leku ciężarnym chomikom.
Farmakodynamika i efekty kliniczne
Nadciśnienie
Podawanie preparatu VASOTEC pacjentom z nadciśnieniem o nasileniu od łagodnego do ciężkiego powoduje obniżenie ciśnienia krwi zarówno w pozycji leżącej, jak i stojącej, zwykle bez komponentu ortostatycznego. Objawowe niedociśnienie ortostatyczne występuje zatem rzadko, chociaż można się go spodziewać u pacjentów odwodnionych (patrz OSTRZEŻENIA ).
większości badanych pacjentów, po doustnym podaniu pojedynczej dawki enalaprylu, początek działania przeciwnadciśnieniowego obserwowano po godzinie, a szczytowe obniżenie ciśnienia krwi osiągano po czterech do sześciu godzinach.
W zalecanych dawkach działanie przeciwnadciśnieniowe utrzymywało się przez co najmniej 24 godziny. U niektórych pacjentów skutki mogą ulec zmniejszeniu pod koniec przerwy w dawkowaniu (patrz DAWKOWANIE I SPOSÓB PODAWANIA ).
U niektórych pacjentów osiągnięcie optymalnego obniżenia ciśnienia tętniczego może wymagać kilkutygodniowej terapii.
Działanie przeciwnadciśnieniowe preparatu VASOTEC utrzymywało się podczas długotrwałej terapii. Nagłe odstawienie preparatu VASOTEC 10 mg nie wiązało się z szybkim wzrostem ciśnienia krwi.
badaniach hemodynamicznych u pacjentów z nadciśnieniem pierwotnym obniżeniu ciśnienia krwi towarzyszyło zmniejszenie oporu w tętnicach obwodowych ze wzrostem pojemności minutowej serca i niewielką zmianą częstości akcji serca lub jej brakiem. Po podaniu preparatu VASOTEC następuje zwiększenie przepływu krwi przez nerki; szybkość filtracji kłębuszkowej zwykle pozostaje niezmieniona. Efekty wydają się być podobne u pacjentów z nadciśnieniem nerkowo-naczyniowym.
W przypadku jednoczesnego podawania z diuretykami tiazydowymi działanie obniżające ciśnienie krwi 5 mg preparatu VASOTEC jest w przybliżeniu addytywne.
W klinicznym badaniu farmakologicznym pacjentom z nadciśnieniem otrzymującym preparat VASOTEC podawano indometacynę lub sulindak. W tym badaniu nie było dowodów na osłabienie hipotensyjnego działania preparatu VASOTEC (patrz INTERAKCJE Z LEKAMI ).
Niewydolność serca
badaniach z udziałem pacjentów leczonych naparstnicą i lekami moczopędnymi, leczenie enalaprylem powodowało zmniejszenie ogólnoustrojowego oporu naczyniowego, ciśnienia krwi, ciśnienia zaklinowania w kapilarach płucnych i wielkości serca oraz zwiększenie pojemności minutowej serca i tolerancji wysiłku. Częstość akcji serca pozostała niezmieniona lub nieznacznie zmniejszona, a średnia frakcja wyrzutowa pozostała niezmieniona lub zwiększona. Wykazano korzystny wpływ na ciężkość niewydolności serca mierzoną według klasyfikacji New York Heart Association (NYHA) oraz na objawy duszności i zmęczenia. Efekty hemodynamiczne obserwowano po podaniu pierwszej dawki i wydawały się utrzymywać w niekontrolowanych badaniach trwających nawet cztery miesiące. W badaniach kontrolowanych placebo trwających od ośmiu tygodni do ponad roku obserwowano wpływ na tolerancję wysiłku, wielkość serca oraz nasilenie i objawy niewydolności serca.
Niewydolność serca, próby śmiertelności
wieloośrodkowym, kontrolowanym placebo badaniu klinicznym 2569 pacjentów z objawową niewydolnością serca wszystkich stopni i frakcją wyrzutową ≤ 35 procent zostało losowo przydzielonych do grupy otrzymującej placebo lub enalapril i obserwowanych przez okres do 55 miesięcy (terapia SOLVD). Stosowanie enalaprylu wiązało się z 11-procentowym zmniejszeniem śmiertelności z jakiejkolwiek przyczyny i 30-procentowym zmniejszeniem hospitalizacji z powodu niewydolności serca. Choroby wykluczające pacjentów z udziału w badaniu obejmowały ciężką stabilną dusznicę bolesną (>2 ataki dziennie), istotną hemodynamicznie niedrożność zastawek lub dróg odpływowych, niewydolność nerek (kreatynina >2,5 mg/dl), chorobę naczyń mózgowych (np. poważną chorobę tętnic szyjnych). , zaawansowana choroba płuc, nowotwory złośliwe, czynne zapalenie mięśnia sercowego i zaciskające zapalenie osierdzia. Korzyść śmiertelności związana ze stosowaniem enalaprylu nie wydaje się zależeć od obecności naparstnicy.
drugim wieloośrodkowym badaniu wykorzystano protokół SOLVD do badania pacjentów bezobjawowych lub z minimalnymi objawami. Pacjenci SOLVD-Prevention, którzy mieli frakcję wyrzutową lewej komory ≤ 35% i nie mieli objawowej niewydolności serca w wywiadzie, zostali losowo przydzieleni do grupy otrzymującej placebo (n=2117) lub enalapril (n=2111) i obserwowani przez okres do 5 lat. Większość pacjentów biorących udział w badaniu SOLVD-Prevention miała w wywiadzie chorobę niedokrwienną serca. Zawał mięśnia sercowego w wywiadzie występował u 80 procent pacjentów, obecną dusznicę bolesną u 34 procent, a nadciśnienie w wywiadzie u 37 procent. W tej populacji nie wykazano statystycznie istotnego wpływu na śmiertelność. Osoby leczone enalaprylem miały o 32% mniej pierwszych hospitalizacji z powodu niewydolności serca io 32% mniej hospitalizacji z powodu całkowitej niewydolności serca. W porównaniu z placebo u 32 procent mniej pacjentów otrzymujących enalapryl wystąpiły objawy jawnej niewydolności serca. Zmniejszono również liczbę hospitalizacji z przyczyn sercowo-naczyniowych. Wystąpiło nieznaczne zmniejszenie liczby hospitalizacji z jakiejkolwiek przyczyny w grupie leczonej enalaprylem (odpowiednio dla enalaprylu w porównaniu z placebo, 1166 w porównaniu z 1201 pierwszych hospitalizacji, 2649 w porównaniu z 2840 ogółem), chociaż badanie nie było wystarczające do poszukiwania takiego efekt.
Badanie SOLVD-Prevention nie miało na celu ustalenia, czy leczenie bezobjawowych pacjentów z niską frakcją wyrzutową byłoby lepsze pod względem zapobiegania hospitalizacji, czy bliższej obserwacji i stosowania enalaprilu przy najwcześniejszych objawach niewydolności serca. Jednak w warunkach obserwacji w badaniu SOLVD-Prevention (co 4 miesiące w klinice badawczej; w razie potrzeby osobisty lekarz), 68% pacjentów przyjmujących placebo, którzy byli hospitalizowani z powodu niewydolności serca, nie miało wcześniejszych objawów, które mogłyby sygnalizowane rozpoczęcie leczenia.
Badanie SOLVD-Prevention nie miało również na celu wykazania, czy enalapryl modyfikuje progresję podstawowej choroby serca.
W innym wieloośrodkowym, kontrolowanym placebo badaniu (CONSENSUS) ograniczonym do pacjentów z zastoinową niewydolnością serca klasy IV wg NYHA i radiograficznymi cechami kardiomegalii, stosowanie enalaprylu wiązało się z poprawą przeżycia. Wyniki przedstawiono w poniższej tabeli.
Zarówno w badaniach CONSENSUS, jak i SOLVD-Treatment pacjenci zwykle otrzymywali również naparstnicę, diuretyki lub oba.
Farmakologia kliniczna u pacjentów pediatrycznych
Przeprowadzono badanie farmakokinetyczne dawek wielokrotnych z udziałem 40 dzieci i młodzieży płci męskiej i żeńskiej z nadciśnieniem w wieku od 2 miesięcy do ≤16 lat, którym codziennie podawano doustnie 0,07-0,14 mg/kg enalaprylu maleinianu. W stanie stacjonarnym średni efektywny okres półtrwania kumulacji enalaprylatu wynosił 14 godzin, a średni odzysk całkowitego enalaprylatu i enalaprylatu w moczu w ciągu 24 godzin wynosił 68% podanej dawki. Konwersja enalaprilu do enalaprilatu mieściła się w zakresie 63-76%. Ogólne wyniki tego badania wskazują, że farmakokinetyka enalaprylu u dzieci z nadciśnieniem w wieku od 2 miesięcy do ≤16 lat jest zgodna we wszystkich badanych grupach wiekowych i zgodna z historycznymi danymi farmakokinetycznymi dotyczącymi zdrowych osób dorosłych.
badaniu klinicznym z udziałem 110 pacjentów pediatrycznych z nadciśnieniem w wieku od 6 do 16 lat pacjenci o masie ciała
W powyższych badaniach pediatrycznych maleinian enalaprylu podawano w postaci tabletek preparatu VASOTEC, a dzieciom i niemowlętom, które nie były w stanie połykać tabletek lub wymagały mniejszej dawki niż dostępna w postaci tabletek, enalapryl podawano w postaci zawiesiny (patrz DAWKOWANIE I SPOSÓB PODAWANIA , Przygotowanie zawieszenia ).
INFORMACJA O PACJENCIE
Obrzęk naczynioruchowy
Obrzęk naczynioruchowy, w tym obrzęk krtani, może wystąpić w dowolnym momencie leczenia inhibitorami konwertazy angiotensyny, w tym enalaprylem. Należy o tym poinformować i poinformować pacjentów, aby natychmiast zgłaszali wszelkie oznaki lub objawy sugerujące obrzęk naczynioruchowy (obrzęk twarzy, kończyn, oczu, warg, języka, trudności w połykaniu lub oddychaniu) i nie przyjmowali więcej leku do czasu konsultacji z lekarzem prowadzącym.
Niedociśnienie
Należy ostrzec pacjentów, aby zgłaszali zawroty głowy, zwłaszcza w ciągu pierwszych kilku dni terapii. W przypadku wystąpienia rzeczywistego omdlenia należy poinstruować pacjentów, aby odstawili lek do czasu konsultacji z lekarzem prowadzącym. Wszystkich pacjentów należy ostrzec, że nadmierne pocenie się i odwodnienie mogą prowadzić do nadmiernego spadku ciśnienia krwi z powodu zmniejszenia objętości płynów. Inne przyczyny ubytku objętości, takie jak wymioty lub biegunka, mogą również prowadzić do spadku ciśnienia krwi; pacjentom należy zalecić skonsultowanie się z lekarzem.
Hiperkaliemia
Pacjentom należy poinformować, aby nie stosowali substytutów soli zawierających potas bez konsultacji z lekarzem.
Neutropenia
Należy poinformować pacjentów, aby niezwłocznie zgłaszali wszelkie oznaki infekcji (np. ból gardła, gorączka), które mogą być oznaką neutropenii.
Ciąża
Pacjentki w wieku rozrodczym należy poinformować o konsekwencjach narażenia na VASOTEC podczas ciąży. Omów możliwości leczenia z kobietami planującymi ciążę. Pacjentki należy poprosić o jak najszybsze zgłoszenie ciąży swoim lekarzom.
UWAGA: Podobnie jak w przypadku wielu innych leków, pewne porady dla pacjentów leczonych enalaprilem są uzasadnione. Informacje te mają na celu pomóc w bezpiecznym i skutecznym stosowaniu tego leku. Nie jest to ujawnienie wszystkich możliwych działań niepożądanych lub zamierzonych.
